Versão integral disponível em digitalis.uc.pt
|
|
|
- João Henrique de Lacerda Soares
- 6 Há anos
- Visualizações:
Transcrição
1 Versão ntegral dsponível em dgtals.uc.pt
2 1 E N S I N O Versão ntegral dsponível em dgtals.uc.pt
3 2 EDIÇÃO Imprensa da Unversdade de Combra Emal: URL: Vendas onlne CONCEPÇÃO GRÁFICA Antóno Barros EXECUÇÃO GRÁFICA Edlber, Lda ISBN ISBN Dgtal DOI DEPÓSITO LEGAL /09 SETEMBRO 2009, IMPRENSA DA UNIVERSIDADE DE COIMBRA Versão ntegral dsponível em dgtals.uc.pt
4 Isabel M. A. Fonseca Ana Paula Egas 3 Fundamentos de Balanços de Energa C O I M B R A Versão ntegral dsponível em dgtals.uc.pt
5 ÍNDICE LISTA DE SÍMBOLOS...7 PREFÁCIOS INTRODUÇÃO DEFINIÇÕES FUNDAMENTAIS FORMAS DE ENERGIA MECANISMOS DE TRANSFERÊNCIA DE ENERGIA BALANÇOS DE ENERGIA EM SISTEMAS FECHADOS EQUAÇÃO GERAL DUM BALANÇO ENERGÉTICO Balanço de energa a um Sstema Aberto em Estado Estaconáro Balanço de Energa a um Sstema Fechado Introdução da Função Entalpa na Equação do Balanço Valores Absolutos e Relatvos da Entalpa DETERMINAÇÃO DE ENTALPIAS Processos a Temperatura Varável (e Pressão Constante)...30 Calor Sensível...30 Capacdade Calorífca e Capacdade Calorífca Méda Mudanças de Fase...32 Entalpas de Transção Processos de Mstura...33 Entalpas de Mstura...34 Dagrama de Entalpa-Concentração...3 Estados de Referênca dos Componentes da Mstura BALANÇOS DE ENERGIA EM SISTEMAS COM REACÇÃO QUÍMICA Entalpa de Reacção...39 Entalpa de Formação Padrão...41 Calores de Combustão Varação da Entalpa de Reacção com a Temperatura, Pressão e Fase Balanço de Energa a um Sstema onde ocorre uma Reacção Químca Balanço de Energa no Caso Geral DEFINIÇÃO DO ESTADO DE REFERÊNCIA...6
6 10. PROBLEMAS RESOLVIDOS BIBLIOGRAFIA
7 LISTA DE SÍMBOLOS C cp <cp> caudal mássco capacdade calorífca a pressão constante capacdade calorífca méda de uma substânca, a pressão constante β α H entalpa de transção H o entalpa de combustão padrão c H o entalpa de formação padrão f L G H entalpa de condensação G L H entalpa de vaporzação H calor da mstura mx H R entalpa de reacção H o entalpa de reacção padrão R Ec Ep g h H m N P Π Q r R t energa cnétca energa potencal aceleração da gravdade entalpa específca entalpa massa número de moles pressão fase de uma substânca calor transferdo do sstema velocdade de reacção velocdade de produção da espéce tempo 7
8 T u U v V W x y ν z temperatura energa nterna específca energa nterna velocdade relatva ao centro de gravdade do sstema volume específco trabalho fracção molar no líqudo fracção molar no vapor coefcente estequométrco da espéce cota de um sstema ou corrente em relação a um plano de referênca índces nferores α fase ncal β fase fnal e condções de entrada f estado fnal de um sstema componente numa mstura; composto puro ; estado de referênca para cada espéce ; estado ncal de um sstema J corrente J mx propredade relatva a uma mstura P produto (de uma reacção químca) r propredade relatva ao estado de referênca R reagente (de uma reacção químca) s condções de saída 0 estado de referênca índces superores e corrente de entrada o estado de referênca de uma propredade s corrente de saída 8
9 em que s s C representa o caudal mássco da espéce na corrente de saída e h (T,P ) a respectva entalpa nas condções de referênca (T,P ) por undade de massa. K desgna o número de espéces nessa mesma corrente. Expressão análoga a (4) se pode escrever para H e. Para cada espéce escolhe-se um estado de referênca (T,P ) e uma entalpa de referênca h (T,P ). Deste modo é possível escrever que a entalpa absoluta de cada espéce na corrente s é: h s s [ h h (T,P )] + h (T,P ) h (rel) h (T,P ) s + (46) em que h s (rel) representa a entalpa do componente na corrente s relatva ao estado de referênca (T,P ). De gual modo se desgna as equações (4) e (46) em (44), obtemos: s s { [ h (rel) + h (T,P )] C [ h (rel) + h (T,P )] } e h. Se substturmos K e e C Q (47) ou anda, s s s {[ h (rel) C h (rel)] + h (T,P )(C C )} K e e e C Q. (48) Como K (C C ) 0, (49) s e 36
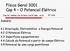
10 Fg 2. Entalpa de soluções aquosas de NaOH1 1 Gráfco adaptado da refª Versão ntegral dsponível em dgtals.uc.pt
11 então na Eq.(48) as entalpas de referênca das espéces, h (T,P ), cancelam-se obtendo-se: s s [ h (rel) C h (rel)] K e e C Q, (0) que é ndependente das entalpas de referênca de cada espéce. Portanto, na ausênca de reacções químcas a escolha do estado de referênca de cada componente da mstura não afecta o balanço de energa (vd. Problema pág. 7). 38
12 8. BALANÇOS DE ENERGIA EM SISTEMAS COM REACÇÃO QUÍMICA Num sstema onde ocorre reacção químca há formação de novos compostos e desaparecmento de outros, o que va mplcar uma lbertação ou absorção de calor. Em prncípo, a equação geral deduzda anterormente, já tem em lnha de conta as varações de entalpa que ocorrem no sstema durante a reacção. De qualquer modo, é convenente rearranjar a equação do balanço energétco de forma a explctar um termo específco que reflcta as varações de entalpa devdas à reacção químca. Vamos começar por apresentar alguns concetos que nos permtrão posterormente deduzr a equação do balanço de energa num sstema onde ocorrem reacções químcas Entalpas de Reacção Entende-se por entalpa de reacção, H R, a dferença entre a entalpa dos produtos e a entalpa dos reagentes nas seguntes crcunstâncas:. os reagentes estão na proporção estequométrca e a reacção prossegue até ao fm.. os reagentes são almentados ao reactor à temperatura T e pressão P, e os produtos formam-se também à pressão P e à temperatura T. Podemos então escrever para a entalpa de reacção: H R (T,P) ν,ph,p(t,p) ν,rh,r (T,P) (1) 39
13 em que ν representa o coefcente estequométrco da espéce e H a respectva entalpa à pressão P e temperatura T. R desgna os reagentes e P os produtos. Em prncípo, se a reacção for levada a cabo num sstema fechado a P e T constantes, de acordo com a Eq.(24), Q H s H H R, e (2) a entalpa da reacção, H R, representa o calor lbertado ou absorvdo para que a temperatura do sstema se mantenha constante. Daí a desgnação, que também é habtual de calor de reacção. Surgem frequentemente dúvdas acerca das undades de H R. O exemplo segunte é esclarecedor. Exemplo: Consdere-se a reacção 2A + B 3C, H R 0kJ / mol O sgnfcado das undades de H R é o segunte: H R 0kJ / "mol de reacção" 0kJ / 2 moles de A reagdas 0kJ /1 mole de B reagda 0kJ / 3 moles de C produzdas A desgnação mol de reacção tem de ser entendda no sentdo lato, como tendo os sgnfcados que foram ndcados anterormente. 40
14 Entalpa de Formação Padrão, o H f A reacção de formação de um composto é a reacção em que o composto é formado a partr das espéces elementares que o consttuem, na forma em que habtualmente aparecem na natureza (por exemplo, O 2 em vez de O). Assm, a entalpa dessa reacção, em condções padrão (2 ºC, 1 atm), é a entalpa de formação padrão do composto. Consdera-se que a entalpa de formação das espéces elementares é zero (Ex: O 2, N 2, H 2). Os valores das entalpas de formação padrão encontram-se tabelados para mutos compostos. Exemplo: A entalpa de formação do benzeno líqudo é a entalpa relatva à reacção de formação deste composto a 2 ºC e a 1 atm: 6C(s) + 3H C, H o kj mol 1 2 (g) 6 H 6 (l) R. Tendo em lnha de conta a le de Hess é possível demonstrar que a entalpa padrão de uma reacção se pode obter a partr das entalpas de formação dos reagentes e dos produtos pela segunte expressão, o o H o R (T, P) ν,p H f,p(t,p) ν,r H f,r(t, P ), (3) em que ν representa o coefcente estequométrco da espéce e H o f, R a respectva entalpa de formação padrão (neste caso, de um reagente). Por consegunte, a entalpa de reacção padrão relatva a uma certa reacção químca, é a dferença entre o somatóro das entalpas de formação padrão dos produtos e o somatóro das entalpas de formação padrão dos reagentes, pesadas pelos respectvos coefcentes estequometrcos. Exemplo: Determne o calor de reacção para a combustão do n-pentano a partr das entalpas de formação. 41
15 C H 12 (l) + 8O 2 (g) CO 2 (g) + 6H 2 O(l). Assm, o o H o o R H f (CO2(g)) + 6 H (H O(l)) H (C H (l)) f 2 f 12 ( 393.) + 6 ( 28.84) ( 173.0) 309 kj mol 1. Calores de Combustão, o H c Defne-se calor de combustão como sendo a entalpa da reacção de combustão de uma substânca com O 2, quando todos os reagentes e produtos se encontram a 2 ºC e 1 atm. São sempre valores negatvos. As entalpas de combustão encontram-se também tabeladas para mutos compostos. A elaboração destas tabelas obedece aos seguntes pressupostos:. todos os carbonos se transformam em CO 2(g),. todos os átomos de hdrogéno dão orgem a H 2O(l),. todos os átomos de enxofre formam SO 2(g), v. todos os átomos de ntrogéno formam N 2(g), v. os calores de combustão dos produtos de combustão (CO 2(g), H 2O(l), SO 2(g) e N 2(g)) são nulos. A entalpa de uma reacção pode ser calculada a partr do conhecmento dos calores de combustão dos reagentes e produtos de acordo com a expressão: o o o H R (T,P) ν,r Hc,R ν,p Hc,P. (4) Esta expressão também resulta da aplcação drecta da le de Hess. Exemplo: Determne a entalpa de combustão da segunte reacção a partr dos calores de combustão dos compostos que nela ntervêm: 42
16 Como a percentagem de água em E é 8.74% e a de N %, podemos agora determnar a quantdade de N 2 presente nesta corrente: n E N kmol. Fazendo um balanço ao N 2 (nerte), no reactor, resulta: C E N n n, N 2 2 pelo que o caudal de ar (C) será: n ar kmol. b) Podemos efectuar um balanço mássco global a todo o processo: m A + m C m E + m G + m H. (8) A massa das correntes C e E pode calcular-se de medato: m N2 C m O kg kg ( ) m C kg, mh O kg E mo kg m kg N 2 m E kg. 10
17 Por consegunte substtundo valores na Eq. (8) tem-se: m A m G + m H, equação com três ncógntas sendo por sso necessáro mas duas equações para resolver a questão. Podemos começar por efectuar um balanço global ao elemento carbono: m A 7 M C6 H + w C H CH 6 3 M( C) ( H CH ) 3 7 M C6 H m H w 7 C6HCHO M C6 M( C) ( H CH ) 3 + m G 7 M C6 M( C) ( H CHO) M( C) ( H COOH), + donde resulta, substtundo valores, m A 7 mh mg ou seja, m A m H m G. (86) A tercera equação pode ser obtda tendo em lnha de conta que as correntes G e H são consttudas por 80 kmol de benzaldeído e tolueno. Assm, mg mh , M( C6HCOOH) M( C6HCHO) que depos de substtur valores se transforma em, m G m H 80. (87) 106
18 A resolução do sstema de equações m A mg + mh m A mh mg mg mh 80 conduz a m m m A G H kg kg kg. A produção de ácdo benzóco é, por consegunte, kg h -1. c) O caudal de tolueno recclado pode ser obtdo fazendo um balanço ao ponto de mstura das correntes A, B e R. Assm, m A + m R m B m R ou m R 143 kg n R kmol. O caudal de tolueno recclado é 1.7 kmol h -1. d) Vamos efectuar um balanço entálpco ao reactor, consderando para temperatura de referênca 2 C e estado gasoso para todas as substâncas, 107
19 o o H B + H C + Q + r 1(- H R, 1 ) + r 2(- H R, 2 ) H E + H D T ref 2 C H B H C 0. Deste modo o balanço reduz-se a o o Q H E + H D + r 1( H R, 1 ) + r 2( H R, 2 ). Determna-se em prmero lugar as entalpas de cada reacção. Assm o H R, 1 [ (29.16)] e kcal mol -1 o H R, 2 [ (29.16)] kcal mol -1. Temos agora que determnar as velocdades de cada reacção: r1 D B n C H COOH n 6 C6HCOOH νc H COOH 6 ng kmol D B n C H CHO n 6 C6HCHO r2 νc H CHO 6 H n C H CHO kmol Vamos determnar a segur as entalpas H E e H D. Deste modo, ( n < Cp> + n < Cp> + n < Cp> )( 10 2) HE O O N N H O H O ( ) (10-2) kcal 108
20 e HD ( nc H CH < Cp> C H CH + nc H CHO< Cp> C H CHO nc H COOH< Cp> C H COOH + 6 ) ( 10 2) [( ) ] ( 10 2) kcal. 6 Podemos agora determnar Q, 3 Q kcal. 3 ( 34.09) ( 78.4) O caudal de refrgerante obtém-se da equação Q L nrefrg. Cprefrg. T onde substtundo os respectvos valores vem, nrefrg. 3 (130 10) kmol. O caudal de refrgerante necessáro é de 2.21 x 10 3 kmol h
21 BIBLIOGRAFIA 1. Reklats, G.V., Introducton to Materal and Energy Balances, 1st edton, John Wley Sons, USA, Felder, R.M., Rousseau, R.W., Elementary Prncples of Chemcal Processes, 2nd edton, John Wley & Sons, Canada, Schmdt, A.X., Lst, H.L., Materal and Energy Balances, Prentce-Hall, N.Y., Hougen, O.A., Watson, K.M., Ragatz, R.A., Prncípos dos Processos Químcos, Vol. 1, Lopes da Slva, Henley, E.J., Rosen, E.M., Materal and Energy Balance Computatons, John Wley & Sons, USA, Whtwell, J.C., Toner, R.K., Conservaton of Mass and Energy, McGraw- Hll, USA, Lews, W.K., Radash, A.H., Lews, H.C., Industral Stochometry, 2nd edton, McGraw-Hll, N.Y., Fath, W.L., Keyes, D.B., Clark, R.L., Industral Chemcals, 3rd edton, John Wley & Sons, USA,
22 9. Perry, R.H., Green, D.W., Maloney, J.O., Perry s Chemcal Engneers Handbook, 6th edton, McGraw-Hll, N.Y., Polng, B.E., Prausntz, J.M., O Connel, J.P., The Propertes of Gases and Lquds, th edton, McGraw-Hll, Murphy, R.M., Introducton to Chemcal Processes: Prncples, Analyss, Synthess, McGraw-Hll,
Problemas Propostos. Frações mássicas, volúmicas ou molares. Estequiometria.
 Elementos de Engenhara Químca I II. Frações e Estequometra (problemas resolvdos) Problemas Propostos. Frações másscas, volúmcas ou molares. Estequometra.. Em 5 moles de Benzeno (C 6 H 6 ) quanto é que
Elementos de Engenhara Químca I II. Frações e Estequometra (problemas resolvdos) Problemas Propostos. Frações másscas, volúmcas ou molares. Estequometra.. Em 5 moles de Benzeno (C 6 H 6 ) quanto é que
CQ110 : Princípios de FQ
 CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br 1 soluções eletrolítcas Qual a dferença entre uma solução 1,0 mol L -1 de glcose e outra de NaCl de mesma concentração?
CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br 1 soluções eletrolítcas Qual a dferença entre uma solução 1,0 mol L -1 de glcose e outra de NaCl de mesma concentração?
V.1. Introdução. Reações Químicas.
 V.1. Introdução. Reações Químcas. V. Balanços Materas a Processos com Reação Químca Uma equação químca acertada ornece muta normação. Por exemplo, a reação de síntese do metanol: CO (g) + 3H (g) CH 3 OH
V.1. Introdução. Reações Químcas. V. Balanços Materas a Processos com Reação Químca Uma equação químca acertada ornece muta normação. Por exemplo, a reação de síntese do metanol: CO (g) + 3H (g) CH 3 OH
8 Soluções Não Ideais
 8 Soluções Não Ideas 8.1 Convenções para o coefcente de atvdade na escala de frações molares Para a solução deal temos ln x onde é função apenas da pressão e temperatura. Fo anterormente mostrado que todas
8 Soluções Não Ideas 8.1 Convenções para o coefcente de atvdade na escala de frações molares Para a solução deal temos ln x onde é função apenas da pressão e temperatura. Fo anterormente mostrado que todas
Apêndice B Frações mássicas, molares e volúmicas. Estequiometria.
 Elementos de Engenhara Químca I Apêndce B Apêndce B Frações másscas, molares e volúmcas. Estequometra. O engenhero químco lda constantemente com msturas de compostos químcos em stuações que mporta caracterzar
Elementos de Engenhara Químca I Apêndce B Apêndce B Frações másscas, molares e volúmcas. Estequometra. O engenhero químco lda constantemente com msturas de compostos químcos em stuações que mporta caracterzar
γ = C P C V = C V + R = q = 2 γ 1 = 2 S gas = dw = W isotermico
 Q1 Um clndro feto de materal com alta condutvdade térmca e de capacdade térmca desprezível possu um êmbolo móvel de massa desprezível ncalmente fxo por um pno. O rao nterno do clndro é r = 10 cm, a altura
Q1 Um clndro feto de materal com alta condutvdade térmca e de capacdade térmca desprezível possu um êmbolo móvel de massa desprezível ncalmente fxo por um pno. O rao nterno do clndro é r = 10 cm, a altura
4 Sistemas de partículas
 4 Sstemas de partículas Nota: será feta a segunte convenção: uma letra em bold representa um vector,.e. b b Nesta secção estudaremos a generalzação das les de Newton a um sstema de váras partículas e as
4 Sstemas de partículas Nota: será feta a segunte convenção: uma letra em bold representa um vector,.e. b b Nesta secção estudaremos a generalzação das les de Newton a um sstema de váras partículas e as
Física I LEC+LET Guias de Laboratório 2ª Parte
 Físca I LEC+LET Guas de Laboratóro 2ª Parte 2002/2003 Experênca 3 Expansão lnear de sóldos. Determnação de coefcentes de expansão térmca de dferentes substâncas Resumo Grupo: Turno: ª Fera h Curso: Nome
Físca I LEC+LET Guas de Laboratóro 2ª Parte 2002/2003 Experênca 3 Expansão lnear de sóldos. Determnação de coefcentes de expansão térmca de dferentes substâncas Resumo Grupo: Turno: ª Fera h Curso: Nome
Série de exercícios 2
 Sére de exercícos -Calcule as arações em S, U e ara um rocesso que conerte mol de água líquda à 0 o C e atm em aor a 00 o C e 3 atm. Admta que a água tenha densdade e caacdade térmca constantes. Admta
Sére de exercícos -Calcule as arações em S, U e ara um rocesso que conerte mol de água líquda à 0 o C e atm em aor a 00 o C e 3 atm. Admta que a água tenha densdade e caacdade térmca constantes. Admta
% Al 48 b) Alumínio que fica em solução. Precisamos calcular o equilíbrio da alumina com Al e O no aço:
 1a Verfcação Refno dos s I EEIMVR-UFF, Setembro de 11 Prova A 1. Calcule o valor de γ no ferro, a 17 o C, com os dados fornecdos na prova. Vmos em aula que o 1% G e o γ estão relaconados através de 1%
1a Verfcação Refno dos s I EEIMVR-UFF, Setembro de 11 Prova A 1. Calcule o valor de γ no ferro, a 17 o C, com os dados fornecdos na prova. Vmos em aula que o 1% G e o γ estão relaconados através de 1%
CQ110 : Princípios de FQ
 CQ110 : Prncípos de FQ CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br Potencal químco, m potencal químco CQ110 : Prncípos de FQ Propredades termodnâmcas das soluções
CQ110 : Prncípos de FQ CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br Potencal químco, m potencal químco CQ110 : Prncípos de FQ Propredades termodnâmcas das soluções
Universidade Estadual do Sudoeste da Bahia
 Unversdade Estadual do Sudoeste da Baha Departamento de Cêncas Exatas e Naturas 5 - Rotações, Centro de Massa, Momento, Colsões, Impulso e Torque Físca I Ferrera Índce 1. Movmento Crcular Unformemente
Unversdade Estadual do Sudoeste da Baha Departamento de Cêncas Exatas e Naturas 5 - Rotações, Centro de Massa, Momento, Colsões, Impulso e Torque Físca I Ferrera Índce 1. Movmento Crcular Unformemente
COMBUSTÃO. A termodinâmica permite um estudo elementar de combustão através da termoquímica.
 COMBUSTÃO A termodnâmca permte um estudo elementar de combustão através da termoquímca. Aplcação de balanço de massa e energa (1º le) e de defenção de condções de equlíbro e sentdo de evoluções termodnâmcas
COMBUSTÃO A termodnâmca permte um estudo elementar de combustão através da termoquímca. Aplcação de balanço de massa e energa (1º le) e de defenção de condções de equlíbro e sentdo de evoluções termodnâmcas
Termodinâmica dos Sistemas Abertos Sistemas heterogêneos: Potencial Químico. Grandezas Molares.
 Termoâmca dos Sstemas Abertos Sstemas heterogêneos: Potencal Químco. Grandezas Molares. A aplcação da função Energa Lvre de Gbbs aos sstemas de um únco componente permte a construção dos Dagramas de Fases
Termoâmca dos Sstemas Abertos Sstemas heterogêneos: Potencal Químco. Grandezas Molares. A aplcação da função Energa Lvre de Gbbs aos sstemas de um únco componente permte a construção dos Dagramas de Fases
É o grau de associação entre duas ou mais variáveis. Pode ser: correlacional ou experimental.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Curso de extensão, MMQ IFUSP, fevereiro/2014. Alguns exercício básicos
 Curso de extensão, MMQ IFUSP, feverero/4 Alguns exercíco báscos I Exercícos (MMQ) Uma grandeza cujo valor verdadero x é desconhecdo, fo medda três vezes, com procedmentos expermentas dêntcos e, portanto,
Curso de extensão, MMQ IFUSP, feverero/4 Alguns exercíco báscos I Exercícos (MMQ) Uma grandeza cujo valor verdadero x é desconhecdo, fo medda três vezes, com procedmentos expermentas dêntcos e, portanto,
1º Exame de Mecânica Aplicada II
 1º Exame de Mecânca Aplcada II Este exame é consttuído por 4 perguntas e tem a duração de três horas. Justfque convenentemente todas as respostas apresentando cálculos ntermédos. Responda a cada pergunta
1º Exame de Mecânca Aplcada II Este exame é consttuído por 4 perguntas e tem a duração de três horas. Justfque convenentemente todas as respostas apresentando cálculos ntermédos. Responda a cada pergunta
Ajuste de um modelo linear aos dados:
 Propagação de erros Suponhamos que se pretende determnar uma quantdade Z, a partr da medda drecta das grandezas A, B, C,, com as quas se relacona através de Z = f(a,b,c, ). Se os erros assocados a A, B,
Propagação de erros Suponhamos que se pretende determnar uma quantdade Z, a partr da medda drecta das grandezas A, B, C,, com as quas se relacona através de Z = f(a,b,c, ). Se os erros assocados a A, B,
ANÁLISE DE ESTRUTURAS I INTRODUÇÃO AO MÉTODO DE CROSS
 DECvl ANÁLISE DE ESTRUTURAS I INTRODUÇÃO AO ÉTODO DE CROSS Orlando J. B. A. Perera 20 de ao de 206 2 . Introdução O método teratvo ntroduzdo por Hardy Cross (Analyss of Contnuous Frames by Dstrbutng Fxed-End
DECvl ANÁLISE DE ESTRUTURAS I INTRODUÇÃO AO ÉTODO DE CROSS Orlando J. B. A. Perera 20 de ao de 206 2 . Introdução O método teratvo ntroduzdo por Hardy Cross (Analyss of Contnuous Frames by Dstrbutng Fxed-End
Interpolação Segmentada
 Interpolação Segmentada Uma splne é uma função segmentada e consste na junção de váras funções defndas num ntervalo, de tal forma que as partes que estão lgadas umas às outras de uma manera contínua e
Interpolação Segmentada Uma splne é uma função segmentada e consste na junção de váras funções defndas num ntervalo, de tal forma que as partes que estão lgadas umas às outras de uma manera contínua e
Energia, calor, entalpia e variação de entalpia.
 Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Eletrotécnica AULA Nº 1 Introdução
 Eletrotécnca UL Nº Introdução INTRODUÇÃO PRODUÇÃO DE ENERGI ELÉTRIC GERDOR ESTÇÃO ELEVDOR Lnha de Transmssão ESTÇÃO IXDOR Equpamentos Elétrcos Crcuto Elétrco: camnho percorrdo por uma corrente elétrca
Eletrotécnca UL Nº Introdução INTRODUÇÃO PRODUÇÃO DE ENERGI ELÉTRIC GERDOR ESTÇÃO ELEVDOR Lnha de Transmssão ESTÇÃO IXDOR Equpamentos Elétrcos Crcuto Elétrco: camnho percorrdo por uma corrente elétrca
Leis de conservação em forma integral
 Les de conservação em forma ntegral J. L. Balño Departamento de Engenhara Mecânca Escola Poltécnca - Unversdade de São Paulo Apostla de aula Rev. 10/08/2017 Les de conservação em forma ntegral 1 / 26 Sumáro
Les de conservação em forma ntegral J. L. Balño Departamento de Engenhara Mecânca Escola Poltécnca - Unversdade de São Paulo Apostla de aula Rev. 10/08/2017 Les de conservação em forma ntegral 1 / 26 Sumáro
SC de Física I Nota Q Nota Q2 Nota Q3 NOME: DRE Teste 1
 SC de Físca I - 2017-2 Nota Q1 88888 Nota Q2 Nota Q3 NOME: DRE Teste 1 Assnatura: Questão 1 - [3,5 pontos] Uma partícula de massa m se move sobre uma calha horzontal lsa com velocdade constante de módulo
SC de Físca I - 2017-2 Nota Q1 88888 Nota Q2 Nota Q3 NOME: DRE Teste 1 Assnatura: Questão 1 - [3,5 pontos] Uma partícula de massa m se move sobre uma calha horzontal lsa com velocdade constante de módulo
Primeiro Exercício da Lista de Interpolação TOL 10 9
 Prmero Exercíco da Lsta de Interpolação TOL 9 Busque uma expressão de segundo grau e outra de tercero grau que melhor aproxmam a função x 4 no ntervalo x. Analse e dscuta seus resultados confrontado-os
Prmero Exercíco da Lsta de Interpolação TOL 9 Busque uma expressão de segundo grau e outra de tercero grau que melhor aproxmam a função x 4 no ntervalo x. Analse e dscuta seus resultados confrontado-os
Cap. 6 - Energia Potencial e Conservação da Energia Mecânica
 Unversdade Federal do Ro de Janero Insttuto de Físca Físca I IGM1 014/1 Cap. 6 - Energa Potencal e Conservação da Energa Mecânca Prof. Elvs Soares 1 Energa Potencal A energa potencal é o nome dado a forma
Unversdade Federal do Ro de Janero Insttuto de Físca Físca I IGM1 014/1 Cap. 6 - Energa Potencal e Conservação da Energa Mecânca Prof. Elvs Soares 1 Energa Potencal A energa potencal é o nome dado a forma
2 - Análise de circuitos em corrente contínua
 - Análse de crcutos em corrente contínua.-corrente eléctrca.-le de Ohm.3-Sentdos da corrente: real e convenconal.4-fontes ndependentes e fontes dependentes.5-assocação de resstêncas; Dvsores de tensão;
- Análse de crcutos em corrente contínua.-corrente eléctrca.-le de Ohm.3-Sentdos da corrente: real e convenconal.4-fontes ndependentes e fontes dependentes.5-assocação de resstêncas; Dvsores de tensão;
3. Um protão move-se numa órbita circular de raio 14 cm quando se encontra. b) Qual o valor da velocidade linear e da frequência ciclotrónica do
 Electromagnetsmo e Óptca Prmero Semestre 007 Sére. O campo magnétco numa dada regão do espaço é dado por B = 4 e x + e y (Tesla. Um electrão (q e =.6 0 9 C entra nesta regão com velocdade v = e x + 3 e
Electromagnetsmo e Óptca Prmero Semestre 007 Sére. O campo magnétco numa dada regão do espaço é dado por B = 4 e x + e y (Tesla. Um electrão (q e =.6 0 9 C entra nesta regão com velocdade v = e x + 3 e
D = POLINÔMIO INTERPOLADOR DE NEWTON 1) DIFERENÇAS DIVIDIDAS 1.1) DIFERENÇAS DIVIDIDAS ORDINÁRIAS (D) Sejam n+1 pontos de uma função y = f(x):
 POLINÔMIO INTERPOLAOR E NEWTON ) IFERENÇAS IVIIAS.) IFERENÇAS IVIIAS ORINÁRIAS () Sejam n pontos de uma função f():... n f( )... n - ferença dvdda de ordem zero: n n M - ferença dvdda de ordem um: M M
POLINÔMIO INTERPOLAOR E NEWTON ) IFERENÇAS IVIIAS.) IFERENÇAS IVIIAS ORINÁRIAS () Sejam n pontos de uma função f():... n f( )... n - ferença dvdda de ordem zero: n n M - ferença dvdda de ordem um: M M
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ 1 É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ 1 É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Gabarito para a prova de 1º Ano e 8ª serie (atual 9º Ano)
 Gabarto para a prova de 1º Ano e 8ª sere (atual 9º Ano) 1. t t c F 5 3 9 ; t c 451 3 5 9 o ; tc 33 C ΔS. a) Δ t 5 s V 4, 1 mnuto possu 6 s, portanto, dos 5 s temos: 8 mnutos (equvale a 48 s) e sobram segundos.
Gabarto para a prova de 1º Ano e 8ª sere (atual 9º Ano) 1. t t c F 5 3 9 ; t c 451 3 5 9 o ; tc 33 C ΔS. a) Δ t 5 s V 4, 1 mnuto possu 6 s, portanto, dos 5 s temos: 8 mnutos (equvale a 48 s) e sobram segundos.
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 4
 FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 4 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 4 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
UNIVERSIDADE NOVA DE LISBOA Faculdade de Economia Análise de Dados e Probabilidade 2º Semestre 2008/2009 Exame Final 1ª Época. Grupo I (4 Valores)
 UNIVERSIDADE NOVA DE LISBOA Faculdade de Economa Análse de Dados e Probabldade º Semestre 008/009 Exame Fnal ª Época Clara Costa Duarte Data: 8/05/009 Graça Slva Duração: h0 Grupo I (4 Valores) A gelatara
UNIVERSIDADE NOVA DE LISBOA Faculdade de Economa Análse de Dados e Probabldade º Semestre 008/009 Exame Fnal ª Época Clara Costa Duarte Data: 8/05/009 Graça Slva Duração: h0 Grupo I (4 Valores) A gelatara
Coeficiente de Partição
 Físco-Químca Expermental Coefcente de Partção 1. Introdução Suponha dos solventes A e B, parcalmente mscíves à temperatura T, formando as fases α (uma solução dluída de B na fase A) e β (uma solução dluída
Físco-Químca Expermental Coefcente de Partção 1. Introdução Suponha dos solventes A e B, parcalmente mscíves à temperatura T, formando as fases α (uma solução dluída de B na fase A) e β (uma solução dluída
3.6. Análise descritiva com dados agrupados Dados agrupados com variáveis discretas
 3.6. Análse descrtva com dados agrupados Em algumas stuações, os dados podem ser apresentados dretamente nas tabelas de frequêncas. Netas stuações devemos utlzar estratégas específcas para obter as meddas
3.6. Análse descrtva com dados agrupados Em algumas stuações, os dados podem ser apresentados dretamente nas tabelas de frequêncas. Netas stuações devemos utlzar estratégas específcas para obter as meddas
CORRELAÇÃO E REGRESSÃO
 CORRELAÇÃO E REGRESSÃO Constata-se, freqüentemente, a estênca de uma relação entre duas (ou mas) varáves. Se tal relação é de natureza quanttatva, a correlação é o nstrumento adequado para descobrr e medr
CORRELAÇÃO E REGRESSÃO Constata-se, freqüentemente, a estênca de uma relação entre duas (ou mas) varáves. Se tal relação é de natureza quanttatva, a correlação é o nstrumento adequado para descobrr e medr
Física Geral 3001 Cap 4 O Potencial Elétrico
 Físca Geral 3001 Cap 4 O Potencal Elétrco (Cap. 26 Hallday, Cap. 22 Sears, Cap 31 Tpler vol 2) 10 ª Aula Sumáro 4.1 Gravtação, Eletrostátca e Energa Potencal 4.2 O Potencal Elétrco 4.3 Superíces equpotencas
Físca Geral 3001 Cap 4 O Potencal Elétrco (Cap. 26 Hallday, Cap. 22 Sears, Cap 31 Tpler vol 2) 10 ª Aula Sumáro 4.1 Gravtação, Eletrostátca e Energa Potencal 4.2 O Potencal Elétrco 4.3 Superíces equpotencas
AMPLIAÇÃO DE ESCALA. Adimensionais: dq dq dqs. dt dt dt. Reynolds. Número de Potência. Número de Froude
 AMPLIAÇÃO E ESCALA Admensonas: Reynolds Re ρ N /μ Número de Potênca dq dq dqs o dqv Número de Froude Fr N / g AMPLIAÇÃO E ESCALA COMO CORRELACIONAR k L a com potênca de agtação? Os japoneses propões aquecer
AMPLIAÇÃO E ESCALA Admensonas: Reynolds Re ρ N /μ Número de Potênca dq dq dqs o dqv Número de Froude Fr N / g AMPLIAÇÃO E ESCALA COMO CORRELACIONAR k L a com potênca de agtação? Os japoneses propões aquecer
CAPÍTULO IV PROPRIEDADES GEOMÉTRICAS DA SEÇÃO TRANSVERSAL
 CPÍTULO IV PROPRIEDDES GEOMÉTRICS D SEÇÃO TRNSVERSL Propredades Geométrcas da Seção Transversal 4. Propredades Geométrcas da Seção Transversal 4.. Introdução O presente trabalho é desenvolvdo paralelamente
CPÍTULO IV PROPRIEDDES GEOMÉTRICS D SEÇÃO TRNSVERSL Propredades Geométrcas da Seção Transversal 4. Propredades Geométrcas da Seção Transversal 4.. Introdução O presente trabalho é desenvolvdo paralelamente
para i 1, 2, 3, 4, 5, 6. 0,75 i i 0 para i 1, 2, 3, 4, 5, 6
 Gabarto da Lsta de eercícos de Sstemas Algébrcos ) O modelo estaconáro do estágo de uma coluna de absorção de prato, na qual ocorre uma reação químca rreversível na fase líquda, é descrto pelas equações
Gabarto da Lsta de eercícos de Sstemas Algébrcos ) O modelo estaconáro do estágo de uma coluna de absorção de prato, na qual ocorre uma reação químca rreversível na fase líquda, é descrto pelas equações
3 Método Numérico. 3.1 Discretização da Equação Diferencial
 3 Método Numérco O presente capítulo apresenta a dscretação da equação dferencal para o campo de pressão e a ntegração numérca da expressão obtda anterormente para a Vscosdade Newtonana Equvalente possbltando
3 Método Numérco O presente capítulo apresenta a dscretação da equação dferencal para o campo de pressão e a ntegração numérca da expressão obtda anterormente para a Vscosdade Newtonana Equvalente possbltando
CAPITULO II - FORMULAÇAO MATEMATICA
 CAPITULO II - FORMULAÇAO MATEMATICA II.1. HIPOTESES BASICAS A modelagem aqu empregada está baseado nas seguntes hpóteses smplfcadoras : - Regme permanente; - Ausênca de forças de campo; - Ausênca de trabalho
CAPITULO II - FORMULAÇAO MATEMATICA II.1. HIPOTESES BASICAS A modelagem aqu empregada está baseado nas seguntes hpóteses smplfcadoras : - Regme permanente; - Ausênca de forças de campo; - Ausênca de trabalho
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 3
 FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 3 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 3 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
Mecânica. Sistemas de Partículas
 Mecânca Sstemas de Partículas Mecânca» Sstemas de Partículas Introdução A dnâmca newtonana estudada até aqu fo utlzada no entendmento e nas prevsões do movmento de objetos puntformes. Objetos dealzados,
Mecânca Sstemas de Partículas Mecânca» Sstemas de Partículas Introdução A dnâmca newtonana estudada até aqu fo utlzada no entendmento e nas prevsões do movmento de objetos puntformes. Objetos dealzados,
Trabalho e Energia. Curso de Física Básica - Mecânica J.R. Kaschny (2005)
 Trabalho e Energa Curso de Físca Básca - Mecânca J.R. Kaschny (5) Lembrando nosso epermento de queda lvre... z z 1 v t 1 z = z - v t - gt ( ) z- z v = g = t Contudo, se consderarmos obtemos: v z z 1 t
Trabalho e Energa Curso de Físca Básca - Mecânca J.R. Kaschny (5) Lembrando nosso epermento de queda lvre... z z 1 v t 1 z = z - v t - gt ( ) z- z v = g = t Contudo, se consderarmos obtemos: v z z 1 t
MODELAGEM E SIMULAÇÃO DE COLUNAS DE DESTILAÇÃO REATIVA (METÁTESE DO 2-PENTENO)
 MODELAGEM E SIMULAÇÃO DE COLUNAS DE DESTILAÇÃO REATIVA (METÁTESE DO 2-PENTENO) Vlmar Steffen, Edson Antono da Slva(Orentador/UNIOESTE), e-mal: eq.vlmar@bol.com.br. Unversdade Estadual do Oeste do Paraná/Centro
MODELAGEM E SIMULAÇÃO DE COLUNAS DE DESTILAÇÃO REATIVA (METÁTESE DO 2-PENTENO) Vlmar Steffen, Edson Antono da Slva(Orentador/UNIOESTE), e-mal: eq.vlmar@bol.com.br. Unversdade Estadual do Oeste do Paraná/Centro
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 2
 FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 2 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 2 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 1
 FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 1 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
FICHA de AVALIAÇÃO de MATEMÁTICA A 10.º Ano Versão 1 Nome Nº Turma: Data: / / Professor 10.º Ano Classfcação Apresente o seu racocíno de forma clara, ndcando todos os cálculos que tver de efetuar e todas
PÊNDULO ELÁSTICO. Fig. 1. Considere o sistema da figura 1. Quando se suspende uma massa, m, na mola, o seu comprimento aumenta de l 0
 PÊNDULO ELÁSTICO. Resuo U corpo lgado a ua ola é posto e ovento osclatóro. Deterna-se as característcas do ovento e estuda-se a conservação da energa ecânca.. Tópcos teórcos Y l 0 l Fg. F r el P r X Consdere
PÊNDULO ELÁSTICO. Resuo U corpo lgado a ua ola é posto e ovento osclatóro. Deterna-se as característcas do ovento e estuda-se a conservação da energa ecânca.. Tópcos teórcos Y l 0 l Fg. F r el P r X Consdere
Gráficos de Controle para Processos Autocorrelacionados
 Gráfcos de Controle para Processos Autocorrelaconados Gráfco de controle de Shewhart: observações ndependentes e normalmente dstrbuídas. Shewhart ao crar os gráfcos de controle não exgu que os dados fossem
Gráfcos de Controle para Processos Autocorrelaconados Gráfco de controle de Shewhart: observações ndependentes e normalmente dstrbuídas. Shewhart ao crar os gráfcos de controle não exgu que os dados fossem
Termodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem/2005 Resolução comentada Prof. Fabrício R. Sensato
 Termodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem/2005 Resolução comentada Prof. Fabrício R. Sensato 1) (1,0 ponto) a) Como é definido o fator de compressibilidade, Z, de um gás? b) Qual
Termodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem/2005 Resolução comentada Prof. Fabrício R. Sensato 1) (1,0 ponto) a) Como é definido o fator de compressibilidade, Z, de um gás? b) Qual
DETERMINAÇÃO DE VALORES LIMITE DE EMISSÃO PARA SUBSTÂNCIAS PERIGOSAS DA LISTA II DA DIRECTIVA 76/464/CEE
 DETERMINAÇÃO DE VALORES LIMITE DE EMISSÃO PARA SUBSTÂNCIAS PERIGOSAS DA LISTA II DA DIRECTIVA 76/464/CEE Anabela R. S. REBELO Lc. Químca Industral, CCDR Algarve, Rua Dr. José de Matos n.º 13, 800-503 Faro,
DETERMINAÇÃO DE VALORES LIMITE DE EMISSÃO PARA SUBSTÂNCIAS PERIGOSAS DA LISTA II DA DIRECTIVA 76/464/CEE Anabela R. S. REBELO Lc. Químca Industral, CCDR Algarve, Rua Dr. José de Matos n.º 13, 800-503 Faro,
Capítulo 24: Potencial Elétrico
 Capítulo 24: Potencal Energa Potencal Elétrca Potencal Superfíces Equpotencas Cálculo do Potencal a Partr do Campo Potencal Produzdo por uma Carga Pontual Potencal Produzdo por um Grupo de Cargas Pontuas
Capítulo 24: Potencal Energa Potencal Elétrca Potencal Superfíces Equpotencas Cálculo do Potencal a Partr do Campo Potencal Produzdo por uma Carga Pontual Potencal Produzdo por um Grupo de Cargas Pontuas
CONCEITOS INICIAIS DE ESTATÍSTICA MÓDULO 2 DISTRIBUIÇÃO DE FREQÜÊNCIA - ELEMENTOS Prof. Rogério Rodrigues
 CONCEITOS INICIAIS DE ESTATÍSTICA MÓDULO DISTRIBUIÇÃO DE FREQÜÊNCIA - ELEMENTOS Prof. Rogéro Rodrgues I) TABELA PRIMITIVA E DISTRIBUIÇÃO DE FREQÜÊNCIA : No processo de amostragem, a forma de regstro mas
CONCEITOS INICIAIS DE ESTATÍSTICA MÓDULO DISTRIBUIÇÃO DE FREQÜÊNCIA - ELEMENTOS Prof. Rogéro Rodrgues I) TABELA PRIMITIVA E DISTRIBUIÇÃO DE FREQÜÊNCIA : No processo de amostragem, a forma de regstro mas
CARGA MÓVEL. Conjunto de cargas moveis que mantêm uma posição relativa constante.
 CARGA MÓVEL Força generalsada com ntensdade, drecção e sentdo fxos, mas com uma posção varável na estrutura. COMBOIO DE CARGAS Conjunto de cargas moves que mantêm uma posção relatva constante. CARGA DISTRIBUIDA
CARGA MÓVEL Força generalsada com ntensdade, drecção e sentdo fxos, mas com uma posção varável na estrutura. COMBOIO DE CARGAS Conjunto de cargas moves que mantêm uma posção relatva constante. CARGA DISTRIBUIDA
4 Discretização e Linearização
 4 Dscretzação e Lnearzação Uma vez defndas as equações dferencas do problema, o passo segunte consste no processo de dscretzação e lnearzação das mesmas para que seja montado um sstema de equações algébrcas
4 Dscretzação e Lnearzação Uma vez defndas as equações dferencas do problema, o passo segunte consste no processo de dscretzação e lnearzação das mesmas para que seja montado um sstema de equações algébrcas
Critério de Equilíbrio
 Crtéro de Equlíbro ara um sstema echado onde exstem ases em equlíbro, o crtéro geral de equlíbro de ases mpõe que o potencal químco de cada espéce presente seja gual em todas as ases. α β π µ = µ = K=
Crtéro de Equlíbro ara um sstema echado onde exstem ases em equlíbro, o crtéro geral de equlíbro de ases mpõe que o potencal químco de cada espéce presente seja gual em todas as ases. α β π µ = µ = K=
Trocas radiativas entre superfícies: recintos fechados com meio não participativo
 Trocas radatvas entre superfíces: recntos fechados com meo não partcpatvo Concetos báscos Recnto fechado consste de ou mas superfíces que englobam uma regão do espaço (tpcamente preenchda com gás) e que
Trocas radatvas entre superfíces: recntos fechados com meo não partcpatvo Concetos báscos Recnto fechado consste de ou mas superfíces que englobam uma regão do espaço (tpcamente preenchda com gás) e que
UNIVERSIDADE ZAMBEZE. Fundamentos de Combustão Aula 2-Prática Prof. Jorge Nhambiu
 UNIVERSIDADE ZAMBEZE Fundamentos de Combustão Aula 2-Prática Aula 2. Tópicos Termodinâmica da combustão: Revisão dos conceitos da primeira lei; Propriedades das misturas; Estequiometria da combustão; Energia
UNIVERSIDADE ZAMBEZE Fundamentos de Combustão Aula 2-Prática Aula 2. Tópicos Termodinâmica da combustão: Revisão dos conceitos da primeira lei; Propriedades das misturas; Estequiometria da combustão; Energia
Análise de faltas balanceadas e não-balanceadas utilizando Z bar. 1. Análise de falta balanceada usando a matriz de impedância de barra (Z bar )
 Análse de altas balanceadas e não-balanceadas utlzando. Análse de alta balanceada usando a matrz de mpedânca de ra ( ) Aqu será eta uma análse de cálculo de curto-crcuto trásco (alta balanceada), utlzando
Análse de altas balanceadas e não-balanceadas utlzando. Análse de alta balanceada usando a matrz de mpedânca de ra ( ) Aqu será eta uma análse de cálculo de curto-crcuto trásco (alta balanceada), utlzando
2 Incerteza de medição
 2 Incerteza de medção Toda medção envolve ensaos, ajustes, condconamentos e a observação de ndcações em um nstrumento. Este conhecmento é utlzado para obter o valor de uma grandeza (mensurando) a partr
2 Incerteza de medção Toda medção envolve ensaos, ajustes, condconamentos e a observação de ndcações em um nstrumento. Este conhecmento é utlzado para obter o valor de uma grandeza (mensurando) a partr
Radiação Térmica Processos, Propriedades e Troca de Radiação entre Superfícies (Parte 2)
 Radação Térmca Processos, Propredades e Troca de Radação entre Superfíces (Parte ) Obetvo: calcular a troca por radação entre duas ou mas superfíces. Essa troca depende das geometras e orentações das superfíces,
Radação Térmca Processos, Propredades e Troca de Radação entre Superfíces (Parte ) Obetvo: calcular a troca por radação entre duas ou mas superfíces. Essa troca depende das geometras e orentações das superfíces,
2 Principio do Trabalho Virtual (PTV)
 Prncpo do Trabalho rtual (PT)..Contnuo com mcroestrutura Na teora que leva em consderação a mcroestrutura do materal, cada partícula anda é representada por um ponto P, conforme Fgura. Porém suas propredades
Prncpo do Trabalho rtual (PT)..Contnuo com mcroestrutura Na teora que leva em consderação a mcroestrutura do materal, cada partícula anda é representada por um ponto P, conforme Fgura. Porém suas propredades
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Prof. Lorí Val, Dr. UFRG Insttuto de Matemátca
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Prof. Lorí Val, Dr. UFRG Insttuto de Matemátca
QiD 6 3ª SÉRIE/PRÉ - VESTIBULAR PARTE 3 QUÍMICA
 PARA A VALIDADE DO QD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
PARA A VALIDADE DO QD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
do Semi-Árido - UFERSA
 Unversdade Federal Rural do Sem-Árdo - UFERSA Temperatura e Calor Subêna Karne de Mederos Mossoró, Outubro de 2009 Defnção: A Termodnâmca explca as prncpas propredades damatéra e a correlação entre estas
Unversdade Federal Rural do Sem-Árdo - UFERSA Temperatura e Calor Subêna Karne de Mederos Mossoró, Outubro de 2009 Defnção: A Termodnâmca explca as prncpas propredades damatéra e a correlação entre estas
( ) ( ) ( ) ( ) Algumas consequências do Primeiro Princípio. Método das misturas (utilizado para determinar calores específicos, em calorimetria)
 Método das msturas (utlzado para determnar calores especícos, em calormetra) Joseph lack (sec. XIII) ( ) ( ) ( ) ( ) W W W W ª Le aplcada a cada um dos subsstemas: No nteror de uma parede adabátca (calorímetro),
Método das msturas (utlzado para determnar calores especícos, em calormetra) Joseph lack (sec. XIII) ( ) ( ) ( ) ( ) W W W W ª Le aplcada a cada um dos subsstemas: No nteror de uma parede adabátca (calorímetro),
TERMODINÂMICA QUÍMICA. Espontaneidade e Equilíbrio
 TERMODINÂMICA QUÍMICA Espontaneidade e Equilíbrio Calculando a variação de entropia do Universo... Critério de espontaneidade: ΔS universo > 0 processo espontâneo ΔS universo = 0 equilíbrio ΔS universo
TERMODINÂMICA QUÍMICA Espontaneidade e Equilíbrio Calculando a variação de entropia do Universo... Critério de espontaneidade: ΔS universo > 0 processo espontâneo ΔS universo = 0 equilíbrio ΔS universo
D- MÉTODO DAS APROXIMAÇÕES SUCESSIVAS
 D- MÉTODO DAS APROXIMAÇÕES SUCESSIVAS O método das apromações sucessvas é um método teratvo que se basea na aplcação de uma fórmula de recorrênca que, sendo satsfetas determnadas condções de convergênca,
D- MÉTODO DAS APROXIMAÇÕES SUCESSIVAS O método das apromações sucessvas é um método teratvo que se basea na aplcação de uma fórmula de recorrênca que, sendo satsfetas determnadas condções de convergênca,
Faculdade de Engenharia Optimização. Prof. Doutor Engº Jorge Nhambiu
 1 Programação Não Lnear com Restrções Aula 9: Programação Não-Lnear - Funções de Váras Varáves com Restrções Ponto Regular; Introdução aos Multplcadores de Lagrange; Multplcadores de Lagrange e Condções
1 Programação Não Lnear com Restrções Aula 9: Programação Não-Lnear - Funções de Váras Varáves com Restrções Ponto Regular; Introdução aos Multplcadores de Lagrange; Multplcadores de Lagrange e Condções
É o grau de associação entre duas ou mais variáveis. Pode ser: correlacional. ou experimental.
 Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~vall/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal http://www.mat.ufrgs.br/~vall/ ou expermental. Numa relação
Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~vall/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal http://www.mat.ufrgs.br/~vall/ ou expermental. Numa relação
Parte 1: Exercícios Teóricos
 Cálculo Numérco SME0300 ICMC-USP Lsta 2: Sstemas Lneares Métodos Dretos Professora: Cyntha de O. Lage Ferrera Parte 1: Exercícos Teórcos 1. Consdere o sstema Ax = b, onde 1 α 3 α 1 4 ; x = 5 2 1 Para que
Cálculo Numérco SME0300 ICMC-USP Lsta 2: Sstemas Lneares Métodos Dretos Professora: Cyntha de O. Lage Ferrera Parte 1: Exercícos Teórcos 1. Consdere o sstema Ax = b, onde 1 α 3 α 1 4 ; x = 5 2 1 Para que
GABARITO ERP19. impedância total em pu. impedância linha em pu; impedância carga em pu; tensão no gerador em pu.
 GABARITO ERP9 Questão mpedânca total em pu. mpedânca lnha em pu; mpedânca carga em pu; tensão no gerador em pu. Assm, tem-se que: ( ). Mas, ou seja: : ( ).. Logo: pu. () A mpedânca da carga em pu,, tem
GABARITO ERP9 Questão mpedânca total em pu. mpedânca lnha em pu; mpedânca carga em pu; tensão no gerador em pu. Assm, tem-se que: ( ). Mas, ou seja: : ( ).. Logo: pu. () A mpedânca da carga em pu,, tem
COMBUSTÍVEIS E COMBUSTÃO
 COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenhara de Energa Dourados MS - 2013 CHAMAS DIFUSIVAS 2 INTRODUÇÃO Chamas de dfusão turbulentas tpo jato de gás são bastante comuns em aplcações ndustras. Há
COMBUSTÍVEIS E COMBUSTÃO PROF. RAMÓN SILVA Engenhara de Energa Dourados MS - 2013 CHAMAS DIFUSIVAS 2 INTRODUÇÃO Chamas de dfusão turbulentas tpo jato de gás são bastante comuns em aplcações ndustras. Há
Microeconomia I. Licenciaturas em Administração e Gestão de Empresas e em Economia
 Mcroeconoma I Lcencaturas em Admnstração e Gestão de Empresas e em Economa Ano lectvo 010-011 Teste Intermédo 1º Semestre 5 de Outubro de 010 Regente: Fernando Branco (fbranco@ucppt) Catarna Slva, Danel
Mcroeconoma I Lcencaturas em Admnstração e Gestão de Empresas e em Economa Ano lectvo 010-011 Teste Intermédo 1º Semestre 5 de Outubro de 010 Regente: Fernando Branco (fbranco@ucppt) Catarna Slva, Danel
MECÂNICA CLÁSSICA. AULA N o 7. Teorema de Liouville Fluxo no Espaço de Fases Sistemas Caóticos Lagrangeano com Potencial Vetor
 1 MECÂNICA CLÁSSICA AULA N o 7 Teorema de Louvlle Fluo no Espaço de Fases Sstemas Caótcos Lagrangeano com Potencal Vetor Voltando mas uma ve ao assunto das les admssíves na Físca, acrescentamos que, nos
1 MECÂNICA CLÁSSICA AULA N o 7 Teorema de Louvlle Fluo no Espaço de Fases Sstemas Caótcos Lagrangeano com Potencal Vetor Voltando mas uma ve ao assunto das les admssíves na Físca, acrescentamos que, nos
Modelagem de Equilíbrio de Fases Fluidas usando EDE Cúbicas
 UNIERSIDADE FEDERA DO PARANÁ SETOR DE TECNOOGIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA Modelagem de Equlíbro de Fases Fludas usando EDE Cúbcas Prof. Marcos. Corazza DEQ/UFPR
UNIERSIDADE FEDERA DO PARANÁ SETOR DE TECNOOGIA DEPARTAMENTO DE ENGENHARIA QUÍMICA PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA Modelagem de Equlíbro de Fases Fludas usando EDE Cúbcas Prof. Marcos. Corazza DEQ/UFPR
18 e 20/Abr/2016 Aulas 12 e 13. Introdução à Física Estatística Postulados Equilíbrio térmico Função de Partição; propriedades termodinâmicas
 01/Abr/2016 Aula 11 Potencas termodnâmcos Energa nterna total Entalpa Energas lvres de Helmholtz e de Gbbs Relações de Maxwell 18 e 20/Abr/2016 Aulas 12 e 13 Introdução à Físca Estatístca Postulados Equlíbro
01/Abr/2016 Aula 11 Potencas termodnâmcos Energa nterna total Entalpa Energas lvres de Helmholtz e de Gbbs Relações de Maxwell 18 e 20/Abr/2016 Aulas 12 e 13 Introdução à Físca Estatístca Postulados Equlíbro
CAPÍTULO 2 DESCRIÇÃO DE DADOS ESTATÍSTICA DESCRITIVA
 CAPÍTULO DESCRIÇÃO DE DADOS ESTATÍSTICA DESCRITIVA. A MÉDIA ARITMÉTICA OU PROMÉDIO Defnção: é gual a soma dos valores do grupo de dados dvdda pelo número de valores. X x Soma dos valores de x número de
CAPÍTULO DESCRIÇÃO DE DADOS ESTATÍSTICA DESCRITIVA. A MÉDIA ARITMÉTICA OU PROMÉDIO Defnção: é gual a soma dos valores do grupo de dados dvdda pelo número de valores. X x Soma dos valores de x número de
2ª PARTE Estudo do choque elástico e inelástico.
 2ª PARTE Estudo do choque elástco e nelástco. Introdução Consderemos dos corpos de massas m 1 e m 2, anmados de velocdades v 1 e v 2, respectvamente, movmentando-se em rota de colsão. Na colsão, os corpos
2ª PARTE Estudo do choque elástco e nelástco. Introdução Consderemos dos corpos de massas m 1 e m 2, anmados de velocdades v 1 e v 2, respectvamente, movmentando-se em rota de colsão. Na colsão, os corpos
7 - Distribuição de Freqüências
 7 - Dstrbução de Freqüêncas 7.1 Introdução Em mutas áreas há uma grande quantdade de nformações numércas que precsam ser dvulgadas de forma resumda. O método mas comum de resumr estes dados numércos consste
7 - Dstrbução de Freqüêncas 7.1 Introdução Em mutas áreas há uma grande quantdade de nformações numércas que precsam ser dvulgadas de forma resumda. O método mas comum de resumr estes dados numércos consste
Equação do Gás Ideal
 Capítulo 5 Gases Substâncias que Existem como Gases Pressão de um Gás Leis dos Gases Equação do Gás Ideal Estequiometria com Gases Lei de Dalton das Pressões Parciais Teoria Cinética Molecular dos Gases
Capítulo 5 Gases Substâncias que Existem como Gases Pressão de um Gás Leis dos Gases Equação do Gás Ideal Estequiometria com Gases Lei de Dalton das Pressões Parciais Teoria Cinética Molecular dos Gases
Observação Calor x Temperatura
 Prof. Jackson Alves Definição Parte da química que estuda a energia na forma de calor envolvido, seja nos processos químicos ou físicos. Observação Calor x Temperatura Instrumento de medição: Calorímetro
Prof. Jackson Alves Definição Parte da química que estuda a energia na forma de calor envolvido, seja nos processos químicos ou físicos. Observação Calor x Temperatura Instrumento de medição: Calorímetro
Notas Processos estocásticos. Nestor Caticha 23 de abril de 2012
 Notas Processos estocástcos Nestor Catcha 23 de abrl de 2012 notas processos estocástcos 2 O Teorema de Perron Frobenus para matrzes de Markov Consdere um processo estocástco representado por um conunto
Notas Processos estocástcos Nestor Catcha 23 de abrl de 2012 notas processos estocástcos 2 O Teorema de Perron Frobenus para matrzes de Markov Consdere um processo estocástco representado por um conunto
Covariância na Propagação de Erros
 Técncas Laboratoras de Físca Lc. Físca e Eng. omédca 007/08 Capítulo VII Covarânca e Correlação Covarânca na propagação de erros Coefcente de Correlação Lnear 35 Covarânca na Propagação de Erros Suponhamos
Técncas Laboratoras de Físca Lc. Físca e Eng. omédca 007/08 Capítulo VII Covarânca e Correlação Covarânca na propagação de erros Coefcente de Correlação Lnear 35 Covarânca na Propagação de Erros Suponhamos
8. Estudo da não-idealidade da fase líquida
 PQI 58 Fundamentos de Processos em Engenhara Químca II 009 8. Estudo da não-dealdade da fase líquda Assuntos. A le de Raoult. Defnção de atvdade 3. Convenções assmétrcas e a le de Henry 4. Exercícos 8..
PQI 58 Fundamentos de Processos em Engenhara Químca II 009 8. Estudo da não-dealdade da fase líquda Assuntos. A le de Raoult. Defnção de atvdade 3. Convenções assmétrcas e a le de Henry 4. Exercícos 8..
PROFESSOR: EQUIPE DE QUÍMICA
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA ORGÂNICA 2ª SÉRIE - ENSINO MÉDIO - PARTE 2 ============================================================================================= Termoquímica
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA ORGÂNICA 2ª SÉRIE - ENSINO MÉDIO - PARTE 2 ============================================================================================= Termoquímica
CURSO de ESTATÍSTICA Gabarito
 UNIVERSIDADE FEDERAL FLUMINENSE TRANSFERÊNCIA o semestre letvo de 010 e 1 o semestre letvo de 011 CURSO de ESTATÍSTICA Gabarto INSTRUÇÕES AO CANDIDATO Verfque se este caderno contém: PROVA DE REDAÇÃO com
UNIVERSIDADE FEDERAL FLUMINENSE TRANSFERÊNCIA o semestre letvo de 010 e 1 o semestre letvo de 011 CURSO de ESTATÍSTICA Gabarto INSTRUÇÕES AO CANDIDATO Verfque se este caderno contém: PROVA DE REDAÇÃO com
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ Em mutas stuações duas ou mas varáves estão relaconadas e surge então a necessdade de determnar a natureza deste relaconamento. A análse
Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ Em mutas stuações duas ou mas varáves estão relaconadas e surge então a necessdade de determnar a natureza deste relaconamento. A análse
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Prof. Lorí Val, Dr. UFRGS Insttuto de Matemátca
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Prof. Lorí Val, Dr. UFRGS Insttuto de Matemátca
Capítulo 2. APROXIMAÇÕES NUMÉRICAS 1D EM MALHAS UNIFORMES
 Capítulo. Aproxmações numércas 1D em malhas unformes 9 Capítulo. AROXIMAÇÕS NUMÉRICAS 1D M MALHAS UNIFORMS O prncípo fundamental do método das dferenças fntas (MDF é aproxmar através de expressões algébrcas
Capítulo. Aproxmações numércas 1D em malhas unformes 9 Capítulo. AROXIMAÇÕS NUMÉRICAS 1D M MALHAS UNIFORMS O prncípo fundamental do método das dferenças fntas (MDF é aproxmar através de expressões algébrcas
Exemplo V.1.: O clorometano pode ser obtido através da reação de cloração do metano: CH 3Cl (g) + HCl (g)
 As equações de balanço materal (as equações M), conforme ntroduzdas no capítulo anteror, são apenas aplcáves a processos de separação ou mstura. Na presença de reação(ões) químca(s), e para os compostos
As equações de balanço materal (as equações M), conforme ntroduzdas no capítulo anteror, são apenas aplcáves a processos de separação ou mstura. Na presença de reação(ões) químca(s), e para os compostos
Mecânica e Ondas 1º Ano -2º Semestre 2º Exame 06/07/2017 8:00h
 Lcencatura em Engenhara Geológca e de Mnas Lcencatura em Matemátca Aplcada e Computação Mestrado Integrado em Engenhara Bomédca Mecânca e Ondas 1º Ano -º Semestre º Exame 06/07/017 8:00h Duração do exame:
Lcencatura em Engenhara Geológca e de Mnas Lcencatura em Matemátca Aplcada e Computação Mestrado Integrado em Engenhara Bomédca Mecânca e Ondas 1º Ano -º Semestre º Exame 06/07/017 8:00h Duração do exame:
TERMODINÂMICA QUÍMICA
 TERMODIÂMICA QUÍMICA Fabano A.. Fernandes Sandro M. zzo Deovaldo Moraes Jr. a Edção 006 SUMÁRIO. ITRODUÇÃO À TERMODIÂMICA.. Introdução.. Defnção e Importânca.3. aráves Termodnâmcas.3.. Temperatura.3..
TERMODIÂMICA QUÍMICA Fabano A.. Fernandes Sandro M. zzo Deovaldo Moraes Jr. a Edção 006 SUMÁRIO. ITRODUÇÃO À TERMODIÂMICA.. Introdução.. Defnção e Importânca.3. aráves Termodnâmcas.3.. Temperatura.3..
EXPANSÃO TÉRMICA DOS LÍQUIDOS
 Físca II Protocolos das Aulas Prátcas 01 DF - Unversdade do Algarve EXPANSÃO ÉRMICA DOS ÍQUIDOS 1 Resumo Estuda-se a expansão térmca da água destlada e do glcerol utlzando um pcnómetro. Ao aquecer-se,
Físca II Protocolos das Aulas Prátcas 01 DF - Unversdade do Algarve EXPANSÃO ÉRMICA DOS ÍQUIDOS 1 Resumo Estuda-se a expansão térmca da água destlada e do glcerol utlzando um pcnómetro. Ao aquecer-se,
Aula 10: Corrente elétrica
 Unversdade Federal do Paraná Setor de Cêncas Exatas Departamento de Físca Físca III Prof. Dr. Rcardo Luz Vana Referêncas bblográfcas: H. 28-2, 28-3, 28-4, 28-5 S. 26-2, 26-3, 26-4 T. 22-1, 22-2 Aula 10:
Unversdade Federal do Paraná Setor de Cêncas Exatas Departamento de Físca Físca III Prof. Dr. Rcardo Luz Vana Referêncas bblográfcas: H. 28-2, 28-3, 28-4, 28-5 S. 26-2, 26-3, 26-4 T. 22-1, 22-2 Aula 10:
