Cinética Química. a b c p q r. As concentrações dos reagentes são funções do tempo:
|
|
|
- Stefany Cordeiro Lage
- 5 Há anos
- Visualizações:
Transcrição
1 Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes de velocidade:,,... As concentrações dos reagentes são funções do tempo: [A]= f ([A],[B],...,,,...,,,..., t ) 2 2 [B]= f ([A],[B],...,,,...,,,..., t ) 2 2 [C]= f ([A],[B],...,,,...,,,..., t )
2 Ordem e molecularidade Molecularidade de uma reacção: número de moléculas (ou átomos) envolvidas num passo reaccional elementar. Raramente superior a 2. (Porquê?) Ordem: Número de termos de concentração dos quais depende a velocidade de reacção. As constantes de velocidade têm dimensões que dependem da ordem da reacção aa + bb + cc zz P v = a b c z [A] [B] [C]...[Z] Equação de velocidade Ordem = a + b + c z
3 Passos elementares A ordem de uma reacção não é, em geral, igual à sua molecularidade, pois muitas reacções podem ser decompostas numa série de passos elementares com diferentes molecularidades O passo limitante poderá determinar a ordem global da reacção. Reacção global A + B + C P (ordem 3) Passos elementares A + B X X + C P (ordem 2) (ordem 2)
4 Ordem Reacção Equação
5 Efeito da ordem de reacção Decomposição de [A] Velocidade em função de [A] Concentração Velocidade Tempo Concentração do reagente v = [A]n d [A] = [A] n
6 Convenções de Notação Reagentes e produtos: A,B,C,D...,P,Q,R,S Concentrações iniciais: [A],[B],[C],[D]...,[P],[Q],[R],[S] Constantes de velocidade:,,,,,... (reacção directa) , 2, 3, 4, 5,... (reacção inversa) Constantes de equilíbrio: eq S d I,,,,,... K K K K K
7 Soluções das equações cinéticas Em geral as funções de evolução das concentrações no tempo podem ser obtidas como solução de um sistema de equações diferenciais de primeira ordem. Exemplo: 2 A B C d d d [A] [B] [C] = 2 2 [A] Concentração = [A] [B] = [B] Solução Condições iniciais: [A],[B],[C] Tempo
8 Mecanismo Equação diferencial Solução 2 A B C d [A] d [B] d [C] = 2 2 [A] = [A] [B] = [B] [C]= f ([A],[B],[C],,, t ) v C = etc... df 2
9 Soluções das equações cinéticas As equações diferenciais da cinética podem ser resolvidas por vários processos, dependendo do grau de complexidade dos sistemas: Solução analítica: quando os sistemas são suficientemente simples para darem origem a sistemas de equações diferenciais com solução exacta. (Ex.:passos elementares de primeira e segunda ordem) Solução aproximada: quando o sistema é descrito por um sistema de equações diferenciais sem solução analítica, mas este último é resolvido por um método numérico aproximado, usando um computador. (Ex.: mecanismos enzimáticos complexos, vias metabólicas) Solução simplificada: O sistema pode ter ou não uma solução analítica, mas assumimos serem válidas determinadas condições simplificadoras que tornam possível chegar a uma solução para o sistema através da resolução de uma equação mais simples. (Ex.:mecanismo de Henri-Michaelis-Menten para um enzima mono-substrato)
10 Hipóteses simplificadores em cinética Equílibrio rápido: quando a interconversão de um conjunto de componentes do sistema reaccional se dá suficientemente depressa para se poder assumir ter sido atingido um quasi-equilíbrio, antes de haver fluxo de reacção apreciável através das partes lentas do sistema. Estado estacionário: quando um ou mais componentes do sistema podem ser considerados como tendo a sua concentração constante num determinado período de tempo em que o sistema é estudado Aproximação de velocidade inicial: quando o ensaio experimental é feito de forma a estimar a velocidade no instante t=, permitindo simplificar a análise do sistema (ex: se houver apenas reagentes, a reacção pode ser tomada como irreversível, porque não houve ainda tempo para a reacção inversa se dar em extensão apreciável, e o efeito de acumulação de produtos e subprodutos pode ser desprezado). Passo limitante: a velocidade de reacção ao longo de uma via reaccional não pode ser mais rápida que o seu passo mais lento
11 Cinética vs. Termodinâmica A cinética descreve a evolução temporal das concentrações dos reagentes e produtos, enquanto a termodinâmica descreve os estados de equilíbrio acessíveis ao sistema Termodinâmica: K G = RT K eq A+B C+D, ln eq Cinética: = = A+B C+D, v [A][B] v [C][D] K eq v = = v (eq) (eq)
12 Reacções de primeira ordem A P d [P] = [A] = ([A] [P]) d [P] = [A] [P] Condição inicial: [P] ln([ A ] [ P ]) = t + α α = = ln([ A ] ) O tempo de meia vida só depende da constante [A] = ln t [A] [P] [P] [A] ( e t ) = t / 2 Tempo de meia vida: = ln 2
13 Reacção de primeira ordem, irreversível A P t [ P ] = [ A ] ( e )
14 Reacção de primeira ordem, irreversível A P t [ P ] = [ A ] ( e )
15 Reacção de primeira ordem (linearização) A P ln[ P ] = ln[a] t
16 Reacção de primeira ordem, irreversível Efeito da variação dos parâmetros [A] e sobre a evolução das concentrações de reagentes e produtos na reacção de primeira ordem irreversível.
17 Reacções de segunda ordem A+B P+Q d [P] = [A][B] = ([A] [P])([B] [P]) d [P] = ( [A] [P] )( [B] [P] ) Multiplicando ambos os termos por ([B] [A] ) : d [P] d [P] [A] [P] [B] [P] ( ) ( ) ( [B] [A] ) = ln([a] [P]) + ln([b] [P]) = ([B] [A] )t + α
18 Condição inicial: t=, [P] = α = ln([a] /[B] ) [A] ([B] [P]) [B] ([A] [P]) = e ([ B ] [ A ] ) t Quando [B] >>[A], a estequiometria implica também que [B] >>[P] e a expressão acima reduz-se a [B] [P] = [A] ( e t ) Esta expressão representa a evolução de uma cinética de primeira ordem em que = [B]. designa-se por constante aparente de primeira ordem.
19 Reacção reversível de primeira ordem A P d [A] = [P] [A] Condição inicial: [A] = [A] [P] = [P] Solução analítica: [A] = [A] [P] = + exp[ ( + ) t ] + [A] { exp[ ( + ) t ]} + [P] [A] = = [A] [P] K eq = = [A] + [A] +
20 Reacção reversível de primeira ordem [P] = A P [A] = = = 2
21 Reacções consecutivas 2 A B C Solução analítica: d [A] d [B] d [C] = 2 2 [A] Condições iniciais: = [A] [B] = [B] [B] = [C] = [A] + [B] + [C] = [A] [A] = [A] exp( t ) [B] = [A] exp( t ) exp( t 2 ) 2 [C] = [A] + ( 2 exp( t ) exp( t 2 )) 2
22 Reacções consecutivas 2 A B C 2 = =.5
23 t SS -tempo para atingir o estado estacionário B SS [B] no estado estacionário
Copyright McGraw-Interamericana de España. Autorização necessária para reprodução ou utilização. Cinética Química
 Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
CQ110 : Princípios de FQ. Imagens de Rorschach
 Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Cinética Química - NOx
 Cinética Química - NOx April 1st st 2017 Mecanismo Global de Formação de NOx Objetivo: a partir do Mecanismo de Zeldovich, formular um mecanismo global do tipo: N 2 + O 2 2NO (1) representado como d[no]
Cinética Química - NOx April 1st st 2017 Mecanismo Global de Formação de NOx Objetivo: a partir do Mecanismo de Zeldovich, formular um mecanismo global do tipo: N 2 + O 2 2NO (1) representado como d[no]
Noções de Cinética Química
 QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
Cinética. Módulo I - Físico Química Avançada. Profa. Kisla P. F. Siqueira
 Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições
 Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
Equilíbrio Químico. Considerando as duas reações (direta e inversa) como processos elementares, podemos escrever:
 Em um sistema fechado, um estado de equilíbrio entre reagentes e produtos sempre tende a ser atingido. Trata-se de um equilíbrio dinâmico entre duas reações reversíveis: uma direta e outra inversa. No
Em um sistema fechado, um estado de equilíbrio entre reagentes e produtos sempre tende a ser atingido. Trata-se de um equilíbrio dinâmico entre duas reações reversíveis: uma direta e outra inversa. No
Equilíbrio Químico. É uma reação reversível na qual a velocidade da reação direta é igual à velocidade da reação inversa.
 Equilíbrio Químico É uma reação reversível na qual a velocidade da reação direta é igual à velocidade da reação inversa. CLASSIFICAÇÃO DAS REAÇÕES Uma reação química diz-se completa quando leva ao esgotamento
Equilíbrio Químico É uma reação reversível na qual a velocidade da reação direta é igual à velocidade da reação inversa. CLASSIFICAÇÃO DAS REAÇÕES Uma reação química diz-se completa quando leva ao esgotamento
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS
 CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS A VELOCIDADE DE UMA REAÇÃO: É UMA MEDIDA DE QUÃO RÁPIDO UM REAGENTE É CONSUMIDO OU UM PRODUTO É FORMADO 1) Na reação de A +
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS A VELOCIDADE DE UMA REAÇÃO: É UMA MEDIDA DE QUÃO RÁPIDO UM REAGENTE É CONSUMIDO OU UM PRODUTO É FORMADO 1) Na reação de A +
Cinética Química. Prof. Alex Fabiano C. Campos
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN Campus Mossoró. Equilíbrio Químico. Albino O.
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN Campus Mossoró Equilíbrio Químico Albino O. Nunes SUMÁRIO OBJETIVOS; INTRODUÇÃO; DEFINIÇÃO; CONCEITOS BÁSICOS DE EQUILÍBRIO;
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN Campus Mossoró Equilíbrio Químico Albino O. Nunes SUMÁRIO OBJETIVOS; INTRODUÇÃO; DEFINIÇÃO; CONCEITOS BÁSICOS DE EQUILÍBRIO;
Cinética Química. Mestrado integrado em Engenharia Biológica. Disciplina Química II, 2º semestre 2009/10. Professsora Ana Margarida Martins
 Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica Estado
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica Estado
A equação de Henri-Michaelis-Menten
 A equação de Henri-Michaelis-Menten Michaelis e Menten (93) refina a abordage de Henri e propõe u odelo uito seelhante: S cat E + A EA E + P passo lento considerando o prieiro passo suficienteente rápido
A equação de Henri-Michaelis-Menten Michaelis e Menten (93) refina a abordage de Henri e propõe u odelo uito seelhante: S cat E + A EA E + P passo lento considerando o prieiro passo suficienteente rápido
Físico-química Farmácia 2014/02
 Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Cinética Tempo necessário
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Cinética Tempo necessário
Cinética de reacções. enzimáticas mono-substrato
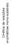 Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES
 CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES REAÇÃO GLOBAL: MOSTRA APENAS A MODIFICAÇÃO GLOBAL VELOCIDADE
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES REAÇÃO GLOBAL: MOSTRA APENAS A MODIFICAÇÃO GLOBAL VELOCIDADE
Departamento de Física e Química Química Básica Rodrigo Vieira Rodrigues
 Departamento de Física e Química Química Básica Rodrigo Vieira Rodrigues Equilíbrio Químico Todas as reações tendem alcançar o equilíbrio químico Quando as velocidades das reações directa e inversa forem
Departamento de Física e Química Química Básica Rodrigo Vieira Rodrigues Equilíbrio Químico Todas as reações tendem alcançar o equilíbrio químico Quando as velocidades das reações directa e inversa forem
Cinética Química. c) A opção (C) está correta. B 3+ e B 4+ não aparecem na reação global, portanto, são intermediários da reação.
 Capítulo 6 Cinética Química 1. (ITA) Considere o seguinte mecanismo de reação genérica: A 4+ + B 2+ A 3+ + B 3+ (etapa lenta) A 4+ + B 3+ A 3+ + B 4+ (etapa rápida) C + + B 4+ C 3+ + B 2+ (etapa rápida)
Capítulo 6 Cinética Química 1. (ITA) Considere o seguinte mecanismo de reação genérica: A 4+ + B 2+ A 3+ + B 3+ (etapa lenta) A 4+ + B 3+ A 3+ + B 4+ (etapa rápida) C + + B 4+ C 3+ + B 2+ (etapa rápida)
Polimerização Passo-a-Passo ou por Condensação
 Reacção entre grupos funcionais; duas moléculas com grupos funcionais que reagem entre si, formando como produto uma molécula mais longa. 05-11-2006 Maria da Conceição Paiva 1 05-11-2006 Maria da Conceição
Reacção entre grupos funcionais; duas moléculas com grupos funcionais que reagem entre si, formando como produto uma molécula mais longa. 05-11-2006 Maria da Conceição Paiva 1 05-11-2006 Maria da Conceição
Cinética Química. Cinética Química...? É o estudo da velocidade das reações químicas e dos fatores que as influenciam.
 Cinética Química...? Universidade Federal de Campina Grande Centro de Ciência e Tecnologia groalimentar Profª Roberlucia Candeia Disciplina: Química geral É o estudo da velocidade das reações químicas
Cinética Química...? Universidade Federal de Campina Grande Centro de Ciência e Tecnologia groalimentar Profª Roberlucia Candeia Disciplina: Química geral É o estudo da velocidade das reações químicas
Universidade Federal do ABC. Disciplina: Transformações Químicas. Equilíbrio Químico. Hueder Paulo M. de Oliveira. Santo André - SP 2018.
 Universidade Federal do ABC Disciplina: Transformações Químicas Equilíbrio Químico Hueder Paulo M. de Oliveira Santo André - SP 2018.1 EQUILÍBRIO QUÍMICO Transformação Química: É o processo de mudança
Universidade Federal do ABC Disciplina: Transformações Químicas Equilíbrio Químico Hueder Paulo M. de Oliveira Santo André - SP 2018.1 EQUILÍBRIO QUÍMICO Transformação Química: É o processo de mudança
Entropia. Energia de Gibbs e Equilíbrio
 Entropia Energia de Gibbs e Equilíbrio Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins TRANSFORMAÇÕES ESPONTÂNEAS Uma reacção diz-se
Entropia Energia de Gibbs e Equilíbrio Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins TRANSFORMAÇÕES ESPONTÂNEAS Uma reacção diz-se
LCE0182 Química Analítica Quantitativa. Equilíbrio Químico. Wanessa Melchert Mattos
 LCE0182 Química Analítica Quantitativa Equilíbrio Químico Wanessa Melchert Mattos Equilíbrio Químico Estalactites: CaCO 3 (s) + CO 2 (aq) + H 2 O (l) Ca 2+ (aq) + 2 HCO 3- (aq) Estalagmites: Ca 2+ (aq)
LCE0182 Química Analítica Quantitativa Equilíbrio Químico Wanessa Melchert Mattos Equilíbrio Químico Estalactites: CaCO 3 (s) + CO 2 (aq) + H 2 O (l) Ca 2+ (aq) + 2 HCO 3- (aq) Estalagmites: Ca 2+ (aq)
Cinética Parte A. Introdução à Química II. Prof. Edson Nossol
 Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
cas AULA 5 es Quími rmaçõ o sfo Tr C0307
 BC0307 Transfo ormaçõe es Químicas AULA 5 - Combustíveis (Termodinâmica x Cinética); - Por que uma reação ocorre? - Qual a velocidade d da reação? - Cinética: leis de velocidade, ordem de reação e sua
BC0307 Transfo ormaçõe es Químicas AULA 5 - Combustíveis (Termodinâmica x Cinética); - Por que uma reação ocorre? - Qual a velocidade d da reação? - Cinética: leis de velocidade, ordem de reação e sua
Pi Principais i i Tópicos Abordados dd
 BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
Físico-Química Experimental Exp. 10. Cinética Química
 Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016
 CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
Cinética Química 17/04/17. V m h. Prof. Xuxu. Velocidade das reações químicas. Velocidade das reações químicas. Velocidade Média. Hora da saída: 11:45
 Seja Bem-indo a Goiânia elocidade Média Cinética Química Hora da saída: 11:45 Δd 40km m 40 km Δt 1h h Distância Hidrolândia: 40 km Seja Bem-indo a Hidrolândia Prof. Xuxu Hora da chegada: 12:45 elocidade
Seja Bem-indo a Goiânia elocidade Média Cinética Química Hora da saída: 11:45 Δd 40km m 40 km Δt 1h h Distância Hidrolândia: 40 km Seja Bem-indo a Hidrolândia Prof. Xuxu Hora da chegada: 12:45 elocidade
QUI109 QUÍMICA GERAL (Ciências Biológicas) 9ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 9ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO COVALENTE HIBRIDIZAÇÃO DE ORBITAIS sp 2 Orientação dos orbitais
QUI109 QUÍMICA GERAL (Ciências Biológicas) 9ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO COVALENTE HIBRIDIZAÇÃO DE ORBITAIS sp 2 Orientação dos orbitais
2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados;
 CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
Aula 3 REAÇÕES ELEMENTARES. META Estudar as reações elementares e suas peculiaridades
 REAÇÕES ELEMENTARES Camilo Andrea Angelucci Aula META Estudar as reações elementares e suas peculiaridades OBJETIVOS Ao fi nal desta aula, o aluno deverá: reações Elementares molecularidade de uma reação
REAÇÕES ELEMENTARES Camilo Andrea Angelucci Aula META Estudar as reações elementares e suas peculiaridades OBJETIVOS Ao fi nal desta aula, o aluno deverá: reações Elementares molecularidade de uma reação
PQI 3221 Cinética Química e Processos Ambientais
 PQI 3221 inética Química e Processos Ambientais Aula 14 Balanços de massa em processos com reações químicas. inética química. Ordem de reação Prof. Antonio arlos S.. Teixeira entro de Engenharia de Sistemas
PQI 3221 inética Química e Processos Ambientais Aula 14 Balanços de massa em processos com reações químicas. inética química. Ordem de reação Prof. Antonio arlos S.. Teixeira entro de Engenharia de Sistemas
Reações químicas aplicas ao processamento de materiais cerâmicos
 Reações químicas aplicas ao processamento de materiais cerâmicos Em vários casos, no processo de fabricação de peças cerâmicas, as reações entre os diferentes constituintes dos corpos cerâmicos são interrompidas
Reações químicas aplicas ao processamento de materiais cerâmicos Em vários casos, no processo de fabricação de peças cerâmicas, as reações entre os diferentes constituintes dos corpos cerâmicos são interrompidas
Química Aplicada EQUILÍBRIO QUÍMICO
 Química Aplicada EQUILÍBRIO QUÍMICO Equilíbrio Químico Todas as reações tendem alcançar o equilíbrio químico Quando as velocidades das reações direta e inversa forem iguais e as concentrações dos reagentes
Química Aplicada EQUILÍBRIO QUÍMICO Equilíbrio Químico Todas as reações tendem alcançar o equilíbrio químico Quando as velocidades das reações direta e inversa forem iguais e as concentrações dos reagentes
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127. Cinética Química
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
Enzimas que ultrapassam o limite difusivo
 Enzimas que ultrapassam o limite difusio Em certas condições é possíel obserar eficiências catalíticas superiores ao limite difusional do substrato e enzima. 1 - Canalização de substratos: Enzima 1 Enzima
Enzimas que ultrapassam o limite difusio Em certas condições é possíel obserar eficiências catalíticas superiores ao limite difusional do substrato e enzima. 1 - Canalização de substratos: Enzima 1 Enzima
BCL 0307 Transformações Químicas
 BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
Cinética química. Vamos começar por ver como se define a velocidade de uma reacção química. Para uma reacção do tipo
 5. Cinética química. Vimos num capítulo anterior como a termodinâmica nos permite prever se uma dada transformação se dá ou não espontaneamente em determinadas condições de temperatura, pressão, etc. É
5. Cinética química. Vimos num capítulo anterior como a termodinâmica nos permite prever se uma dada transformação se dá ou não espontaneamente em determinadas condições de temperatura, pressão, etc. É
Polimerização por condensação ou polimerização passo-a-passo
 Polimerização por condensação ou polimerização passo-a-passo Ciência de Polímeros I 1º semestre 2007/2008 30-09-2007 Maria da Conceição Paiva 1 Reacção de monómeros homofuncionais: Reacção de monómeros
Polimerização por condensação ou polimerização passo-a-passo Ciência de Polímeros I 1º semestre 2007/2008 30-09-2007 Maria da Conceição Paiva 1 Reacção de monómeros homofuncionais: Reacção de monómeros
Atividade a Distância 4 CINÉTICA
 Atividade a Distância 4 CINÉTICA Na parte 1 da Aula 3 vimos a definição de velocidade inicial e como deve ser medida. Agora, vamos ver como ela varia se mudarmos a concentração dos reagentes. Estamos acostumados
Atividade a Distância 4 CINÉTICA Na parte 1 da Aula 3 vimos a definição de velocidade inicial e como deve ser medida. Agora, vamos ver como ela varia se mudarmos a concentração dos reagentes. Estamos acostumados
PQI 2321 Tópicos de Química para Engenharia Ambiental I
 PQI 2321 Tópicos de Química para Engenharia Ambiental I Aulas 14 e 15 Balanços de massa em processos com reações químicas. Cinética química. Ordem de reação Prof. Antonio Carlos S. C. Teixeira Centro de
PQI 2321 Tópicos de Química para Engenharia Ambiental I Aulas 14 e 15 Balanços de massa em processos com reações químicas. Cinética química. Ordem de reação Prof. Antonio Carlos S. C. Teixeira Centro de
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
Equilíbrio Químico. Controlo da Produção Industrial de Amoníaco
 Equilíbrio Químico Controlo da Produção Industrial de Amoníaco Reações completas Combustão do carvão C (s) + O 2 (g) CO 2 (g) Reações completas Reação do Ácido clorídrico com o Magnésio 2 HCl (aq) + Mg
Equilíbrio Químico Controlo da Produção Industrial de Amoníaco Reações completas Combustão do carvão C (s) + O 2 (g) CO 2 (g) Reações completas Reação do Ácido clorídrico com o Magnésio 2 HCl (aq) + Mg
CINÉTICA QUÍMICA. Obs.: a variação da quantidade deverá ser sempre um valor positivo, então ela deverá ser em módulo. 1.
 CINÉTICA QUÍMICA 1. Introdução O Conhecimento e o estudo da velocidade das reações, além de ser muito importante em termos industriais, também está relacionado ao nosso dia-adia, verificamos que há algumas
CINÉTICA QUÍMICA 1. Introdução O Conhecimento e o estudo da velocidade das reações, além de ser muito importante em termos industriais, também está relacionado ao nosso dia-adia, verificamos que há algumas
LCE-108 Química Inorgânica e Analítica. Equilíbrio Químico. Wanessa Melchert Mattos
 LCE-108 Química Inorgânica e Analítica Equilíbrio Químico Wanessa Melchert Mattos Equilíbrio Químico Estalactites: CaCO 3 (s) + CO 2 (aq) + H 2 O (l) Ca 2+ (aq) + 2 HCO 3- (aq) Estalagmites: Ca 2+ (aq)
LCE-108 Química Inorgânica e Analítica Equilíbrio Químico Wanessa Melchert Mattos Equilíbrio Químico Estalactites: CaCO 3 (s) + CO 2 (aq) + H 2 O (l) Ca 2+ (aq) + 2 HCO 3- (aq) Estalagmites: Ca 2+ (aq)
Capítulo by Pearson Education
 QUÍMICA A Ciência Central 9ª Edição Cinética química David P. White Fatores que afetam a velocidade de reações A cinética é o estudo da velocidade na qual as reações químicas ocorrem. Existem quatro fatores
QUÍMICA A Ciência Central 9ª Edição Cinética química David P. White Fatores que afetam a velocidade de reações A cinética é o estudo da velocidade na qual as reações químicas ocorrem. Existem quatro fatores
Fabio Rodrigo da Costa Dias. 2. Velocidade média e instantânea das Reações Químicas
 Cinética Química Fabio Rodrigo da Costa Dias 1. Introdução Cinética química é a área da química responsável pelo estudo das velocidades das reações químicas, bem como dos fatores que influenciam nessas
Cinética Química Fabio Rodrigo da Costa Dias 1. Introdução Cinética química é a área da química responsável pelo estudo das velocidades das reações químicas, bem como dos fatores que influenciam nessas
Equilíbrio Químico (2)
 Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Cinética Química. R Δ[ R] vmédia. A fórmula acima calcula a velocidade média de desaparecimento de um reagente (
![Cinética Química. R Δ[ R] vmédia. A fórmula acima calcula a velocidade média de desaparecimento de um reagente ( Cinética Química. R Δ[ R] vmédia. A fórmula acima calcula a velocidade média de desaparecimento de um reagente (](/thumbs/72/67725684.jpg) Cinética Química André Silva Franco A cinética química estuda a velocidade das reações e todos os fatores envolvidos diretamente ou indiretamente na velocidade. m geral, mede-se a velocidade de uma reação
Cinética Química André Silva Franco A cinética química estuda a velocidade das reações e todos os fatores envolvidos diretamente ou indiretamente na velocidade. m geral, mede-se a velocidade de uma reação
3.2.2 Métodos de relaxação Métodos de competição Métodos de elevada resolução temporal ORDENS E CONSTANTES DE
 ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
Engenharia das Reacções - Exercícios -
 Engenharia das Reacções - Exercícios - 1 Estudou-se a reacção de recombinação de átomos de iodo na presença de árgon: 2 I (g) + Ar (g) I 2 (g) + Ar (g) As velocidade iniciais de formação de I 2 são apresentadas
Engenharia das Reacções - Exercícios - 1 Estudou-se a reacção de recombinação de átomos de iodo na presença de árgon: 2 I (g) + Ar (g) I 2 (g) + Ar (g) As velocidade iniciais de formação de I 2 são apresentadas
META Estudar o comportamento de reações químicas que envolvem mais de uma etapa.
 EQUÇÕES CINÉTICS COMPOSTS Camilo ndrea ngelucci ula MET Estudar o comportamento de reações químicas que envolvem mais de uma etapa. OBJETIVOS o fi nal desta aula, o aluno deverá: compreender e determinar
EQUÇÕES CINÉTICS COMPOSTS Camilo ndrea ngelucci ula MET Estudar o comportamento de reações químicas que envolvem mais de uma etapa. OBJETIVOS o fi nal desta aula, o aluno deverá: compreender e determinar
QUÍMICA Cinética Química Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª.
 QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Velocidade de uma reaç Velocidade média de uma A de uma reaç é definida como a variaç variação da ão de produtos ou de DeterminaDetermina-se medindo a
 Aplicada à Engenharia Civil tica Quí tica Quí Profa. Geisamanda Pedrini Brandão Athayde tica Quí O conhecimento e o estudo da das reações são muito importantes em termos industriais, e também estão relacionados
Aplicada à Engenharia Civil tica Quí tica Quí Profa. Geisamanda Pedrini Brandão Athayde tica Quí O conhecimento e o estudo da das reações são muito importantes em termos industriais, e também estão relacionados
Hidrólise da ureia pela urease
 Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
ELETROQUÍMICA. Prof a. Dr a. Carla Dalmolin
 ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CINÉTICA E MECANISMOS DAS REAÇÕES ELETROQUÍMICAS Eletrodo Transferência de Elétrons O + e R 5. Transferência de elétrons k c O 1. Difusão k d,o k a O Para uma
ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CINÉTICA E MECANISMOS DAS REAÇÕES ELETROQUÍMICAS Eletrodo Transferência de Elétrons O + e R 5. Transferência de elétrons k c O 1. Difusão k d,o k a O Para uma
ATIVIDADES SOBRE LEIS DE VELOCIDADE CINÉTICA
 ATIVIDADES SOBRE LEIS DE VELOCIDADE CINÉTICA Camilo Andrea Angelucci META Compreender os conceitos relacionados as leis de velocidade e seus modelos matematicos. compreender as aplicações conjuntas dessas
ATIVIDADES SOBRE LEIS DE VELOCIDADE CINÉTICA Camilo Andrea Angelucci META Compreender os conceitos relacionados as leis de velocidade e seus modelos matematicos. compreender as aplicações conjuntas dessas
Transformações da Matéria
 EQUILÍBRIO QUÍMICO Transformações da Matéria Físicas Químicas Nucleares Mudanças dos Estados de Agregação Reações Químicas Reações Nucleares Sólido Líquido Gás Térmica Fotoquímica Eletroquímica Fusão Fissão
EQUILÍBRIO QUÍMICO Transformações da Matéria Físicas Químicas Nucleares Mudanças dos Estados de Agregação Reações Químicas Reações Nucleares Sólido Líquido Gás Térmica Fotoquímica Eletroquímica Fusão Fissão
[ A][ B] [ A] [ B] v {[A] }= Vmáx
![[ A][ B] [ A] [ B] v {[A] }= Vmáx [ A][ B] [ A] [ B] v {[A] }= Vmáx](/thumbs/75/72105322.jpg) Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Aula 14 Cinética Química
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 14 Cinética Química Dr. Tiago P. Camargo Velocidades de reação... 85 % das espécies dependem da luz solar Apenas
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 14 Cinética Química Dr. Tiago P. Camargo Velocidades de reação... 85 % das espécies dependem da luz solar Apenas
Cinética Química. a temperatura na qual a reação ocorre e a presença de um catalisador.
 Cinética Química Cinética é o estudo da velocidade com a qual as reações químicas ocorrem. Existem quatro fatores importantes que afetam as velocidades das reações: o estado físico do reagente, as concentrações
Cinética Química Cinética é o estudo da velocidade com a qual as reações químicas ocorrem. Existem quatro fatores importantes que afetam as velocidades das reações: o estado físico do reagente, as concentrações
Equilíbrio Profº Jaison
 Equilíbrio Profº Jaison Equilíbrio Químico Todas as reacções tendem alcançar o equilíbrio químico Quando as velocidades das reacções directa e inversa forem iguais e as concentrações dos reagentes e dos
Equilíbrio Profº Jaison Equilíbrio Químico Todas as reacções tendem alcançar o equilíbrio químico Quando as velocidades das reacções directa e inversa forem iguais e as concentrações dos reagentes e dos
BC0307 Transformações Químicas. Cinética química
 Cinética química 1 É possível que ocorra uma determinada reação? Essa reação é espontânea? Termodinâmica Quão rápida é esta reação? Qual o mecanismo desta transformação química? Cinética 2 Modelo de colisão
Cinética química 1 É possível que ocorra uma determinada reação? Essa reação é espontânea? Termodinâmica Quão rápida é esta reação? Qual o mecanismo desta transformação química? Cinética 2 Modelo de colisão
Química Geral e Inorgânica. QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin. Cinética Química
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Cinética Química Cinética Química É a área da química que está preocupada com a velocidade das reações químicas.
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Cinética Química Cinética Química É a área da química que está preocupada com a velocidade das reações químicas.
1. Escreva as expressões da velocidade de reacção para as seguintes reacções em função do desaparecimento dos reagentes e da formação dos produtos:
 EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 8. Cinética Química Ficha de exercícios 1. Escreva as expressões da velocidade de reacção para as seguintes reacções em função do desaparecimento dos reagentes
EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 8. Cinética Química Ficha de exercícios 1. Escreva as expressões da velocidade de reacção para as seguintes reacções em função do desaparecimento dos reagentes
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade.
 MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
 CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
Cinética das reações orgânicas
 inética das reações orgânicas inética de reações simples Determinação do tempo de semi-vida Ana Paula Francisco QFII 2016-2017 inética Segundo as guidelines para o estudo da Estabilidade Quando forem detetados
inética das reações orgânicas inética de reações simples Determinação do tempo de semi-vida Ana Paula Francisco QFII 2016-2017 inética Segundo as guidelines para o estudo da Estabilidade Quando forem detetados
Equilíbrios químicos homogêneos
 Equilíbrios químicos homogêneos O que é um equilíbrio químico? Algumas (muitas) reações químicas são ditas reversíveis, isto é: tanto os reagentes transformam-se em produtos como os produtos em reagentes.
Equilíbrios químicos homogêneos O que é um equilíbrio químico? Algumas (muitas) reações químicas são ditas reversíveis, isto é: tanto os reagentes transformam-se em produtos como os produtos em reagentes.
Exercícios sobre Equilíbrio químico
 Exercícios sobre Equilíbrio químico 01 - (Ueg GO) Baseado na charge e em seus conhecimentos sobre Química, responda ao que se pede. a) Caso o cientista tivesse misturado quantidades adequadas de ácido
Exercícios sobre Equilíbrio químico 01 - (Ueg GO) Baseado na charge e em seus conhecimentos sobre Química, responda ao que se pede. a) Caso o cientista tivesse misturado quantidades adequadas de ácido
RC1- A reação abaixo foi feta num reator batelada, obtendo-se os dados da tabela abaixo: 2 N 2 O 4 + O 2
 33 - Exercícios resolvidos -cinética - reação abaixo foi feta num reator batelada, obtendo-se os dados da tabela abaixo: N O 5 N O + O Ela pode ser de primeira ou segunda ordem alcule a energia de ativação
33 - Exercícios resolvidos -cinética - reação abaixo foi feta num reator batelada, obtendo-se os dados da tabela abaixo: N O 5 N O + O Ela pode ser de primeira ou segunda ordem alcule a energia de ativação
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015)
 Instituto de Ciências Biomédicas de Abel Salazar - ICBAS-UP Departamento de Química José Augusto Pereira Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015)
Instituto de Ciências Biomédicas de Abel Salazar - ICBAS-UP Departamento de Química José Augusto Pereira Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015)
Energia de Gibbs. T e P ctes. = ΔS sistema - ΔH sistema / T 0 = 0 reversível > 0 espontâneo Multiplica por ( -T )
 Energia de Gibbs ΔS total = ΔS sistema + ΔS viz T e P ctes = ΔS sistema + ΔH viz / T = ΔS sistema - ΔH sistema / T 0 = 0 reversível > 0 espontâneo Multiplica por ( -T ) -TΔS total = ΔH sistema - TΔS sistema
Energia de Gibbs ΔS total = ΔS sistema + ΔS viz T e P ctes = ΔS sistema + ΔH viz / T = ΔS sistema - ΔH sistema / T 0 = 0 reversível > 0 espontâneo Multiplica por ( -T ) -TΔS total = ΔH sistema - TΔS sistema
Velocidade de reação. Química Geral. Prof. Edson Nossol
 Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIDADE 1 QUÍMICA E INDÚSTRIA: Equilíbrios e Desequilíbrios
 Extensão da reacção UNIDADE 1 QUÍMICA E INDÚSTRIA: Equilíbrios e Desequilíbrios Reversibilidade da reacção Equilíbrio Químico Principio de Le Châtelier 1.4. Produção Industrial de Amoníaco Relação entre
Extensão da reacção UNIDADE 1 QUÍMICA E INDÚSTRIA: Equilíbrios e Desequilíbrios Reversibilidade da reacção Equilíbrio Químico Principio de Le Châtelier 1.4. Produção Industrial de Amoníaco Relação entre
Polarização e cinética de eletrodo
 Polarização e cinética de eletrodo RESUMO DA POLARIZAÇÃO O eletrodo sai da condição de equilíbrio pela passagem de corrente pelo circuito externo; A cinética da reação interfacial é mais lenta que o fluxo
Polarização e cinética de eletrodo RESUMO DA POLARIZAÇÃO O eletrodo sai da condição de equilíbrio pela passagem de corrente pelo circuito externo; A cinética da reação interfacial é mais lenta que o fluxo
ocorridas na concentração dos participantes das reações em função do tempo:
 CINÉTICA QUÍMICA Fala Gás Nobre! Preparado para reagir? Então vamos para mais um resumo de química! Você já parou pra pensar, que a velocidade com que as reações químicas acontecem, podem estar relacionadas
CINÉTICA QUÍMICA Fala Gás Nobre! Preparado para reagir? Então vamos para mais um resumo de química! Você já parou pra pensar, que a velocidade com que as reações químicas acontecem, podem estar relacionadas
Exemplo 2: A baixas temperaturas a lei de velocidade da reação A + B C + D é r A =
 Determine a energia de ativação desta reação. Exemplo 1: Para a reação SO 2 + 1 2 O 2 SO 3, se a velocidade de formação de SO 3 é de 2 mol m -3 s -1, então as velocidades de desaparecimento de SO 2, de
Determine a energia de ativação desta reação. Exemplo 1: Para a reação SO 2 + 1 2 O 2 SO 3, se a velocidade de formação de SO 3 é de 2 mol m -3 s -1, então as velocidades de desaparecimento de SO 2, de
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Equilíbrio Químico. Aulas 6. Equilíbrio Químico: Reações reversíveis. Equação de equilíbrio. Princípio de Le Chatelier
 Aulas 6 Equilíbrio Químico: Reações reversíveis Equação de equilíbrio. Princípio de Le Chatelier Reações Químicas REACÇÕES QUÍMICAS podem ser Irreversíveis Reversíveis CH 4 (g) + O 2 (g) CO 2 (g) + H 2
Aulas 6 Equilíbrio Químico: Reações reversíveis Equação de equilíbrio. Princípio de Le Chatelier Reações Químicas REACÇÕES QUÍMICAS podem ser Irreversíveis Reversíveis CH 4 (g) + O 2 (g) CO 2 (g) + H 2
Concentração dos reagentes Quanto maior a concentração dos reagentes, maior a velocidade da reação.
 Setor 3306 Aula 20 Lei da velocidade das reações Complemento. As reações químicas podem ocorrer nas mais diferentes velocidades. Existem reações tão lentas que levam milhares de anos para ocorrer, como
Setor 3306 Aula 20 Lei da velocidade das reações Complemento. As reações químicas podem ocorrer nas mais diferentes velocidades. Existem reações tão lentas que levam milhares de anos para ocorrer, como
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC
 IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
Faculdade de Educação, Ciências e Letras dos Inhamuns FECLIN Coordenação de Química Disciplina Química Geral II Professor: NOTA DE AULA
 Faculdade de Educação, Ciências e Letras dos Inhamuns FECLIN Coordenação de Química Disciplina Química Geral II Professor: NOTA DE AULA CINETICA QUÍMICA Velocidade média de uma reação Ex.1. Um balão contendo
Faculdade de Educação, Ciências e Letras dos Inhamuns FECLIN Coordenação de Química Disciplina Química Geral II Professor: NOTA DE AULA CINETICA QUÍMICA Velocidade média de uma reação Ex.1. Um balão contendo
Química Geral e Experimental II: Cinética Química. Prof. Fabrício Ronil Sensato
 Química Geral e Experimental II: Cinética Química Prof. Fabrício Ronil Sensato Resolução comentada de exercícios selecionados. Versão v2_2005 2 1) Para a reação em fase gasosa N 2 + 3H 2 2NH 3, 2) A decomposição,
Química Geral e Experimental II: Cinética Química Prof. Fabrício Ronil Sensato Resolução comentada de exercícios selecionados. Versão v2_2005 2 1) Para a reação em fase gasosa N 2 + 3H 2 2NH 3, 2) A decomposição,
Determinar a constante de velocidade, k, a energia de. Se a reação de saponificação for de segunda ordem a
 LABORATÓRIO DE FÍSICO-QUÍMICA SAPONIFICAÇÃO DO ACETATO DE ETILA: MÉTODO CONDUTIMÉTRICO OBJETIVO Determinar a constante de velocidade, k, a energia de ativação,e a, para a reação de saponificação do acetato
LABORATÓRIO DE FÍSICO-QUÍMICA SAPONIFICAÇÃO DO ACETATO DE ETILA: MÉTODO CONDUTIMÉTRICO OBJETIVO Determinar a constante de velocidade, k, a energia de ativação,e a, para a reação de saponificação do acetato
CINÉTICA QUÍMICA Conceito de velocidade de reação
 CINÉTICA QUÍMICA 1 1. Conceito de velocidade de reação Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições e quais os mecanismos de desenvolvimento
CINÉTICA QUÍMICA 1 1. Conceito de velocidade de reação Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições e quais os mecanismos de desenvolvimento
São moléculas catalíticas protéicas (exceto algumas que são RNA) - Prefixo que designa a reação: lactato desidrogenase, catalase
 1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
Química II 2º Exame B 30 de Junho de ª Parte
 Química II 2º Exame B 30 de Junho de 2018 Nome nº MEQ MEBiol Sala Duração: 3h 1: 2: 3: 4: 5: 6: 7: 8: 9: 10: SubTotal: Responda às perguntas 1 a 6 na folha do enunciado No fim do enunciado encontra todos
Química II 2º Exame B 30 de Junho de 2018 Nome nº MEQ MEBiol Sala Duração: 3h 1: 2: 3: 4: 5: 6: 7: 8: 9: 10: SubTotal: Responda às perguntas 1 a 6 na folha do enunciado No fim do enunciado encontra todos
VELOCIDADES DE REAÇÕES QUÍMICAS (I)
 VELOCIDADES DE REAÇÕES QUÍMICAS (I) INFORMAÇÃO A velocidade de uma reação química depende da rapidez com que um reagente é consumido, isto é, a taxa de consumo, ou alternativamente, como sendo a rapidez
VELOCIDADES DE REAÇÕES QUÍMICAS (I) INFORMAÇÃO A velocidade de uma reação química depende da rapidez com que um reagente é consumido, isto é, a taxa de consumo, ou alternativamente, como sendo a rapidez
