Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015)
|
|
|
- Geraldo Câmara Gonçalves
- 6 Há anos
- Visualizações:
Transcrição
1 Instituto de Ciências Biomédicas de Abel Salazar - ICBAS-UP Departamento de Química José Augusto Pereira Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015) Todas as enzimas são proteínas e são portanto lábeis, podendo ser inactivadas e desnaturadas. Distinguem-se das outras proteínas pelas propriedades catalisadoras, isto é, pela possibilidade que têm de aumentar milhares de vezes a velocidade de reacções químicas que, na ausência de um catalisador, seriam extremamente lentas. A velocidade de uma reacção catalisada enzimaticamente depende de muitos factores e o conhecimento da cinética de uma reacção é importante para a caracterização da respectiva enzima porque oferece pistas sobre o seu comportamento in vivo e permite prever o seu mecanismo de acção. A mais simples reacção enzimática pode ser representada da seguinte forma: em que E é a enzima livre, S é o substrato da reacção, P é o produto e ES é o complexo enzimasubstrato. Pode demonstrar-se que, quando [S]>>[P] (início da reacção) e quando [ES] é constante (estado estacionário), a equação da velocidade inicial da reacção, v 0, é dada pela expressão conhecida como equação cinética de Michaelis-Menten: v 0 = v max [S] / (K M + [S]) (1) em que K M é a constante de Michaelis-Menten, K M = (k 1 + k 2 ) / k 1 (2) e v max é a sua velocidade máxima que depende da constante de velocidade k 2 : v max = k 2 [E] total (3) Esta velocidade máxima é atingida quando a proporção [S]/[E] atinge valores suficientemente grandes para saturar a enzima, ou seja, para fazer com que todas as moléculas de enzima se encontrem ligadas ao substrato ([ES] = [E] total ). Os parâmetros K M e k 2 são característicos de cada reacção enzimática e de cada enzima. Se representarmos graficamente a velocidade de uma reacção catalisada enzimatica- 1
2 mente em função da concentração do substrato obtém-se um gráfico como o esquematizado na Figura 1. v v max v max /2 K m [S] Figura 1- Representação gráfica da velocidade de uma reacção enzimática em função da concentração de substrato (Equação 1). A saturação da enzima com elevadas concentrações de substrato conduz à independência da velocidade da reacção relativamente à concentração de substrato. O valor de K M coincide com o da concentração de substrato para a qual a velocidade da reacção é exactamente metade da velocidade máxima. Quando se faz o estudo experimental de uma enzima é difícil averiguar se os dados experimentais obedecem ou não à equação de Michaelis-Menten, isto é, se a relação entre a velocidade da reacção e a concentração é definida ou não pela equação da hipérbole rectangular. Para além disso, para se conhecer o valor de K M seria necessário conhecer o valor da velocidade máxima, o que nem sempre é fácil. Lineweaver e Burk propuseram que se utilizassem nos gráficos os valores inversos daqueles que aparecem na equação de Michaelis- Menten, ou seja: 1/v = 1/v max + (K M /v max )(1/[S]) (4) Se se representar graficamente 1/v em função de 1/[S], e a cinética da enzima for de Michaelis-Menten, então obtém-se uma recta cujo declive é K M /v max e cuja ordenada na origem é 1/v max, sendo 1/K M a abcissa do ponto da recta cuja ordenada é nula (Figura 2). Esta representação da equação de Michaelis-Menten é de utilização prática porque permite fazer um ajuste da função teórica aos dados experimentais através de uma simples regressão linear. 2
3 1/v declive = K m /v max 1/v max -1/K m 1/[S] Figura 2 - Representação gráfica de Lineweaver-Burk da equação de Michaelis-Menten (Equação 4). Medidas de actividade enzimática A actividade enzimática é definida pelo consumo de uma certa quantidade de substrato, ou a produção de uma certa quantidade de produto, por unidade de tempo: actividade enzimática = -d[s]/dt = d[p]/dt (5) De acordo com as unidades usadas para a actividade enzimática e para o tempo podem definir-se as seguintes unidades de actividade enzimática: Unidade Internacional: 1 U.I. = 1 mmol de substrato/minuto a 25 ºC Katal: 1 Kat = 1 mol de substrato/seg a 37ºC Estas unidades podem definir a actividade de uma determinada enzima sem haver necessidade de a isolar, pois nelas não se refere a concentração da própria enzima. Como a purificação de qualquer enzima é, normalmente, difícil, as medidas de actividade enzimática já referidas servem para definir precisamente o grau de purificação da enzima nas várias etapas do processo de isolamento. Ao dividir o valor da actividade enzimática encontrada numa solução pelo número de miligramas de proteína nela existente, define-se um novo conceito: a actividade específica. A medida da actividade específica é máxima quando a enzima se encontra pura. Cinética da invertase Reacção A invertase é uma enzima que catalisa a hidrólise da sacarose segundo a reacção: sacarose + H 2 O D-glucose + D-frutose (1) Esta é uma reacção praticamente completa, dita irreversível em que os produtos da reacção são D-glucose e D-frutose em quantidades equimoleculares. É de notar que a hidrólise da sacarose acontece por mecanismos não catalíticos. Embora a velocidade desses mecanismos seja negligenciável, a temperaturas próximas da ambiente, às quais decorrem as expe- 3
4 riências de reacção enzimática, isso já não é verdade a 100 ºC. A hidrólise da sacarose a altas temperatruras é por isso relevante para o método de doseamento dos produtos da reacção 1 tal como explicado a seguir. Doseamento Para determinar a evolução de uma reacção é necessário medir as quantidades de reagentes gastos, ou de produtos formados, em vários intervalos de tempo. Neste trabalho prático é usado um método espectrofotométrico de doseamento específico para os produtos glucose e frutose que se baseia na sua oxidação quantitativa, a 100 ºC, pelo DNS (ácido 3,5 dinitro-salicílico), originando uma solução corada cuja absorvância a 540 nm é proporcional à soma das concentrações de glucose e frutose. A relação entre concentração e absorvância, Equação 6, é determinada previamente por regressão linear, usando um método igual ao deste protocolo, mas com soluções padrão de glucose, ou frutose, com concentrações no intervalo 0 < c < 0,010 M, para os quais se obtêm absorvâncias no intervalo 0 < Abs 540 < 0,8: A 540 = ε 540 ([glucose] + [frutose]) L + oo (6) onde A 540 é a absorvância medida a 540 nm, ε 540 é a absortividade molar (M 1 cm 1 ) directamente estimada pelo declive da regressão, uma vez que L é 1 cm de espessura da solução, e oo é a ordenada na origem também estimada pela regressão para concentração zero de monossacarídeos. Uma vez que ε 540 e oo dependem da temperatura, é importante anotar a temperatura a que foram determinados este parâmetros. É de notar que as soluções para tempo zero usadas como brancos no protocolo cinético contêm sacarose. Isto é necessário devido à presença de grande excesso de sacarose nas amostras cinéticas a dosear, que se poderá hidrolisar quando a solução com DNS for aquecida a 100 ºC. Desta forma, a glucose e a frutose que se poderá formar não-enzimaticamente neste passo do trabalho aparecerá tanto nas amostras como nos brancos e é descontada automaticamente nas leituras de absorvância das amostras, sendo doseados apenas os monossacarídeos provenientes da reacção enzimática. A invertase A enzima invertase é obtida com eficácia da levedura Saccharomyces cerevisiae que produz uma forma intracelular mais leve (~135 kda) e outra extracelular mais pesada contendo uma porção importante de carboidratos (glicoproteína, 270 kda). A invertase possui um ph isoelétrico de cerca de 4 e exibe um máximo de actividade catalítica a ph próximo de 4,5. Por esta razão as soluções de enzima e de sacarose contêm NaH 2 PO 4 0,1 M. Em princípio, a espécie anfiprótica H 2 PO 4 estabelece um ph de (pka1 +pk a2 )/2 = ( )/2 = 4.7 em água pura. No entanto, devido ao ácido carbónico dissolvido em água, e uma vez que a espécie H 2 PO 4 não constitui um tampão, o ph real é normalmente entre 4.4 e 4.5. Como a concentração de enzima é de ordem nanomolar (10 9 M) nas soluções reaccionais deste tra- 4
5 Figura 3 - Evolução com o tempo das concentrações durante uma reacção enzimática com cinética de Michaelis- Menten. balho, e como os compostos da reacção 1 não possuem propriedades ácido-base e a reacção 1 não envolve H +, é esperado que o ph não varie durante a reacção e que portanto a actividade da enzima se mantenha constante. Determinação das velocidades iniciais, v 0 Para determinar a velocidade inicial (v 0 ) da reacção de hidrólise é necessário adicionar a uma solução de sacarose uma certa quantidade da enzima invertase, em concentrações tais que não não saturem a enzima. Desta solução são então retiradas alíquotas aos tempos 0, 1, 2, 3, 4 e 5 minutos às quais é adicionada solução de DNS. Esta solução pára a reacção, por inactivação da enzima, e permite dosear os produtos formados para cada um desses tempos. O declive da regressão linear aplicada aos dados ([glucose], tempo) é a velocidade média da reacção nos seus primeiros 5 minutos, velocidade essa que se considera constante e uma boa aproximação da velocidade inicial (Figura 3). Para mostrar que assim é considera-se a expressão da cinética de Michaelis-Menten que descreve a variação da concentração de produto com o tempo, isto é, o integral da Equação 1: t v max = [P] + K M ln(1+ [P]/([S] 0 [P])) (7) onde [S] 0 é a concentração de substrato (sacarose) no tempo zero e [P] é a concentração de produto (glucose, por exemplo) no tempo t. A Figura 3 mostra como a variação de [P] não é linear com o tempo. No entanto, no início da reacção, verifica-se que [S] >> [P] o que, dado que ln(1+x) x, se x << 1, permite eliminar o logaritmo da equação 7 para obter uma forma válida para os primeiros instantes da reacção: t v max [P] + K M [P]/([S] 0 [P]) (8) Reorganizando os termos em ordem a [P], esta equação pode ser expressa na forma [P] t v max [S] 0 / (K M + [S] 0 ) (9) 5
6 o que mostra haver, no início da reacção, uma relação linear entre [P] e o tempo, dependendo apenas da constante v max [S] 0 / (K M + [S] 0 ). Não é coincidência que esta constante tenha a forma da Equação 1 pois diferenciando a Equação 9 obtém-se [P] t v max [S] 0 / (K M + [S] 0 ) <=> [P]/ t v max [S] 0 / (K M + [S] 0 ) = v 0 (10) A equação 10 mostra que a velocidade instantânea inicial (em rigor quando t = 0) é aproximadamente constante durante o intervalo t se [P] << [S], ou seja, a velocidade média durante os primeiros instantes de uma reacção que se inicia só com sacarose e enzima é uma boa aproximação da velocidade inicial e será tanto melhor quanto menor puder ser t. Determinação de K M e k 2 da invertase De posse de valores para v 0 em função de [S] 0 é possível por regressão não linear da equação 1, ou regressão linear da equação 4, obter os parâmetros da enzima K M e v max. A regressão não linear é de preferir por proporcionar uma estimativa directa das incertezas associadas aos parâmetros. Sabendo v max e a concentração de enzima usada é possível calcular a constante k 2 através da equação 3. Variação de k 2 com a temperatura Os dados de k 2 em função da temperatura permitem estimar os valores de entalpia e de entropia de activação aparentes do passo [ES] -> E + P por regressão não linear da equação de Eyring, correspondente à teoria do estado de transição: k 2 = (k B T/h) exp( G /(RT)) = (k B T/h) exp( H /(RT)) exp( S /R) (11) ou por regressão linear da sua forma logarítmica ln(k 2 /T) = ( H /(RT)) + ( S /R) + ln(k B /h) (12) onde k B é a constante de Boltzman, h é a constante de Planck, T é a temperatura em Kelvin, R é a constante dos gases ideais e H, S e G são, respectivamente, variação de entalpia, variação de entropia e variação de energia de Gibbs padrão de activação. Tal como referido na sub-secção anterior, também neste caso a regressão não linear é de preferir por proporcionar uma estimativa directa das incertezas associadas aos parâmetros. Protocolo laboratorial Material Tubos de ensaio Pipetas automáticas Vortex Banho-maria 6
7 Cronómetro Pipeta de 10 cm 3 Espectrofotómetro Agitadores magnéticos Placa de aquecimento Gobelés Gelo Suportes para tubos de ensaio Reagentes Solução de NaH 2 PO 4 0,1 M Solução de invertase (Sigma-Aldrich I4504, MM = 270 x 10 3 g/mol, 1,00 g dm 3 em NaH 2 PO 4 0,1 M) Reagente de DNS (contendo ácido dinitrosalicílico a 10 g dm 3, isto é, 0,044 mol dm 3 ) Água desionizada Soluções de sacarose 0,010, 0,025, 0,050 e 0,080 M em NaH 2 PO 4 0,1 M Técnica 1. Identificar cada um dos gobelés de 50 cm 3 das soluções de sacarose com as letras A, B, C e D. Manter os gobelés num banho de água a temperatura constante. Informe-se junto do docente sobre a temperatura a estabilizar (usar gelo e água quente conforme necessário). 2. Para cada solução de sacarose, utilizar seis tubos de ensaio que deve codificar de 0x a 5x, em que x é a letra de código dessa solução de sacarose, A, B, C ou D. 3. Pipetar, com pipeta automática, 1 cm 3 do reagente DNS para todos os tubos de ensaio referidos em Retirar, com pipeta automática, 1 cm 3 de cada uma das soluções de sacarose para cada um dos tubos zero ( brancos ). 5 - Pipetar, com pipeta automática, 1 cm 3 da solução da enzima e adicioná-la ao gobelé que contém a solução de sacarose 0,010 M, desencadeando simultaneamente o cronómetro e agitando com uma vareta de vidro durante alguns segundos para homogeneizar a mistura. 6 - Uns segundos antes do minuto 1, recolher, com pipeta automática, uma amostra de 1 cm 3 da solução contida no gobelé. Exactamente ao minuto 1 despejar a amostra directamente para o fundo do tubo de ensaio 1 referente a esta concentração de sacarose. Agitar o tubo de ensaio no vortex e voltar a colocá-lo no suporte. 7 - Repetir a operação descrita em 6 para os minutos 2, 3, 4 e Terminados estes ensaios, colocar os tubos de ensaio em banho-maria fervente durante exactamente 8 minutos. É importante que a água esteja em ebulição quando 7 os tubos forem colocados no banho.
Engenharia Biomédica. Relatório Cinética da Enzima Invertase
 Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
Cinética Química. a b c p q r. As concentrações dos reagentes são funções do tempo:
 Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
Cinética de reacções. enzimáticas mono-substrato
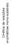 Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Catálise Enzimática. Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química.
 Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Copyright McGraw-Interamericana de España. Autorização necessária para reprodução ou utilização. Cinética Química
 Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
CQ110 : Princípios de FQ. Imagens de Rorschach
 Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA.
 ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE
 NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE O que se pretende Determinar a concentração desconhecida de uma solução aquosa de um ácido forte por titulação com uma base forte através de dois métodos. Num dos
NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE O que se pretende Determinar a concentração desconhecida de uma solução aquosa de um ácido forte por titulação com uma base forte através de dois métodos. Num dos
Estabilidade Enzimática
 Estabilidade Enzimática Biocatálise e Biorremediação 17 de Março de 2016 David Cruz Nº 47030 Matteo Melosini Nº 48286 Vânia Silva Nº 48242 Índice Objectivos... 2 Resumo... 2 Resultados... 3 Meio não aquoso
Estabilidade Enzimática Biocatálise e Biorremediação 17 de Março de 2016 David Cruz Nº 47030 Matteo Melosini Nº 48286 Vânia Silva Nº 48242 Índice Objectivos... 2 Resumo... 2 Resultados... 3 Meio não aquoso
COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae
 COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae Lauri Alves JUNIOR¹, André Luis Fachini de SOUZA², Vanessa Neves HÖPNER² ¹Acadêmico do curso
COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae Lauri Alves JUNIOR¹, André Luis Fachini de SOUZA², Vanessa Neves HÖPNER² ¹Acadêmico do curso
Bioquímica e Biologia Molecular. Cinética da Enzima Invertase
 Bioquímica e Biologia Molecular Cinética da Enzima Invertase 20 de Outubro de 2005 Realizado Por: Pedro Miguel Guerreiro Brito da Cruz nº54196 Nuno Miguel Barroso Monteiro nº54208 João Pedro da Silva Gonçalves
Bioquímica e Biologia Molecular Cinética da Enzima Invertase 20 de Outubro de 2005 Realizado Por: Pedro Miguel Guerreiro Brito da Cruz nº54196 Nuno Miguel Barroso Monteiro nº54208 João Pedro da Silva Gonçalves
BIOQUÍMICA EXPERIMENTAL
 Departamento de Bioquímica Instituto de Química USP Apostila de protocolos Parte A BIOQUÍMICA EXPERIMENTAL QBQ 036N 05 Professores Carlos T. Hotta Ronaldo B. Quaggio Esta apostila foi desenvolvida originalmente
Departamento de Bioquímica Instituto de Química USP Apostila de protocolos Parte A BIOQUÍMICA EXPERIMENTAL QBQ 036N 05 Professores Carlos T. Hotta Ronaldo B. Quaggio Esta apostila foi desenvolvida originalmente
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Problemas sobre o doseamento da actividade de enzimas
 Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
DETERMINAÇÃO DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTOS DE CÉLULAS DE LEVEDURA. Glucose + 2Pi + 2ADP + 2NAD! 2CH COCOO " 2ATP " 2NADH " 2 H
 DETERMINAÇÃ DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTS DE CÉLULAS DE LEVEDURA 1. Introdução A glicólise é um caminho metabólico quase universal no qual a glucose é convertida em piruvato com síntese
DETERMINAÇÃ DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTS DE CÉLULAS DE LEVEDURA 1. Introdução A glicólise é um caminho metabólico quase universal no qual a glucose é convertida em piruvato com síntese
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
Nesta actividade laboratorial não existe nenhum factor que leve a alguma
 REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre o carbonato de cálcio do giz e o ácido acético do vinagre medindo o tempo de formação de um determinado volume de gás dióxido
REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre o carbonato de cálcio do giz e o ácido acético do vinagre medindo o tempo de formação de um determinado volume de gás dióxido
MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO
 MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO 1. Objectivo Neste trabalho, ir-se-á observar a degradação do glicogénio ao longo tempo: i) em meio ácido e à temperatura de 100ºC (degradação química); ii) em
MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO 1. Objectivo Neste trabalho, ir-se-á observar a degradação do glicogénio ao longo tempo: i) em meio ácido e à temperatura de 100ºC (degradação química); ii) em
Aspectos práticos do estudo da cinética enzimática
 Aspectos práticos do estudo da cinética enzimática Tipos de ensaios de cinéticos Ensaios contínuos: o progresso da reacção é monitorizado continuamente, de forma automatizada Ensaios descontínuos: são
Aspectos práticos do estudo da cinética enzimática Tipos de ensaios de cinéticos Ensaios contínuos: o progresso da reacção é monitorizado continuamente, de forma automatizada Ensaios descontínuos: são
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008. Disciplina de BIOQUÍMICA I Curso de MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Teoria da Prática: Transporte de Glicídios
 Teoria da Prática: Transporte de Glicídios INTRODUÇÃO Os estudos dos fatores que afetam a síntese enzimática nos microrganismos levaram à hipótese de que há duas classes de enzimas: as constitutivas e
Teoria da Prática: Transporte de Glicídios INTRODUÇÃO Os estudos dos fatores que afetam a síntese enzimática nos microrganismos levaram à hipótese de que há duas classes de enzimas: as constitutivas e
Cinética Química. Prof. Alex Fabiano C. Campos
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
[ A][ B] [ A] [ B] v {[A] }= Vmáx
![[ A][ B] [ A] [ B] v {[A] }= Vmáx [ A][ B] [ A] [ B] v {[A] }= Vmáx](/thumbs/75/72105322.jpg) Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
ESTUDO DA FOTOSSÍNTESE COM ALGAS IMOBILIZADAS
 ESCOLA SECUNDÁRIA /3 GARCIA DE ORTA Utilização e organização dos laboratórios escolares Oficina de Formação ESTUDO DA FOTOSSÍNTESE COM ALGAS IMOBILIZADAS ANA LUÍSA SANTOS ÍNDICE pág. ÍNDICE 2 GUIÃO FORNECIDO
ESCOLA SECUNDÁRIA /3 GARCIA DE ORTA Utilização e organização dos laboratórios escolares Oficina de Formação ESTUDO DA FOTOSSÍNTESE COM ALGAS IMOBILIZADAS ANA LUÍSA SANTOS ÍNDICE pág. ÍNDICE 2 GUIÃO FORNECIDO
Com base nos dados acima, responda as questões propostas (cuidado com as unidades):
 Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Engenharia das Reacções - Exercícios -
 Engenharia das Reacções - Exercícios - 1 Estudou-se a reacção de recombinação de átomos de iodo na presença de árgon: 2 I (g) + Ar (g) I 2 (g) + Ar (g) As velocidade iniciais de formação de I 2 são apresentadas
Engenharia das Reacções - Exercícios - 1 Estudou-se a reacção de recombinação de átomos de iodo na presença de árgon: 2 I (g) + Ar (g) I 2 (g) + Ar (g) As velocidade iniciais de formação de I 2 são apresentadas
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO.
 DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
Nome.. nº Sala... Responder às perguntas 1, 2, 3, 4 na folha do enunciado
 Química II 1º Exame A 30 de Maio de 2014 Mestrado Integrado Eng. Química Mestrado Integrado Eng. Biológica Nome.. nº Sala... 1: 2: 3: 4: 5: 6: Total: Responder às perguntas 1, 2, 3, 4 na folha do enunciado
Química II 1º Exame A 30 de Maio de 2014 Mestrado Integrado Eng. Química Mestrado Integrado Eng. Biológica Nome.. nº Sala... 1: 2: 3: 4: 5: 6: Total: Responder às perguntas 1, 2, 3, 4 na folha do enunciado
Estudo da cinética Química
 Estudo da cinética Química Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 14 /04/99 Introdução A realização deste trabalho tem como objectivo principal o estudo da cinética de uma reacção segundo
Estudo da cinética Química Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 14 /04/99 Introdução A realização deste trabalho tem como objectivo principal o estudo da cinética de uma reacção segundo
II - ELECTROFORESE DE AMINOÁCIDOS
 II - ELECTROFORESE DE AMINOÁCIDOS Introdução Muitas moléculas biológicas apresentam carga eléctrica cujo valor e sinal depende das suas características e também do ph e da composição do meio em que se
II - ELECTROFORESE DE AMINOÁCIDOS Introdução Muitas moléculas biológicas apresentam carga eléctrica cujo valor e sinal depende das suas características e também do ph e da composição do meio em que se
Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
 CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
Físico-Química Experimental Exp. 10. Cinética Química
 Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
R E L A T Ó R I O D A A C T I V I D A D E L A B O R A T O R I A L
 1 R E L A T Ó R I O D A A C T I V I D A D E L A B O R A T O R I A L ACTIVIDADE LABORATORIAL 1.3 Efeitos da temperatura e da concentração na progressão global de uma reacção de equilíbrio com iões de cobalto
1 R E L A T Ó R I O D A A C T I V I D A D E L A B O R A T O R I A L ACTIVIDADE LABORATORIAL 1.3 Efeitos da temperatura e da concentração na progressão global de uma reacção de equilíbrio com iões de cobalto
DETERMINAÇÃO DO TEOR DE FENÓLICOS TOTAIS (FOLIN-CIOCALTEU) - ESPECTROFOTOMETRIA
 DETERMINAÇÃO DO TEOR DE FENÓLICOS TOTAIS (FOLIN-CIOCALTEU) - ESPECTROFOTOMETRIA MATERIAIS Reagentes Carbonato de sódio P.A. (PM= 106) Reagente Folin Ciocalteu Padrão de ácido gálico anidro (PM= 170,2)
DETERMINAÇÃO DO TEOR DE FENÓLICOS TOTAIS (FOLIN-CIOCALTEU) - ESPECTROFOTOMETRIA MATERIAIS Reagentes Carbonato de sódio P.A. (PM= 106) Reagente Folin Ciocalteu Padrão de ácido gálico anidro (PM= 170,2)
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA
 PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Prática 10 Determinação da constante de equilíbrio entre íons Fe 3+ e SCN -
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra MICROBIOLOGIA António Veríssimo Paula Morais Medição do crescimento de E. coli Fundamento A verificação do desenvolvimento das populações de E. coli
Departamento de Zoologia da Universidade de Coimbra MICROBIOLOGIA António Veríssimo Paula Morais Medição do crescimento de E. coli Fundamento A verificação do desenvolvimento das populações de E. coli
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação
 Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
QBQ 0316 Bioquímica Experimental. Carlos Hotta. Análise de dados (P1 e P2)
 QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
TITULAÇÃO ÁCIDO-BASE
 ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases no laboratório. Realizar tecnicamente uma titulação. Seleccionar
ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases no laboratório. Realizar tecnicamente uma titulação. Seleccionar
V - SEPARAÇÃO DE DUAS ENZIMAS POR CROMATOGRAFIA DE PERMUTA IÓNICA
 V - SEPARAÇÃO DE DUAS ENZIMAS POR CROMATOGRAFIA DE PERMUTA IÓNICA INTRODUÇÃO Cromatografia de permuta iónica A cromatografia é um conjunto de técnicas para a separação de compostos existentes numa mistura.
V - SEPARAÇÃO DE DUAS ENZIMAS POR CROMATOGRAFIA DE PERMUTA IÓNICA INTRODUÇÃO Cromatografia de permuta iónica A cromatografia é um conjunto de técnicas para a separação de compostos existentes numa mistura.
Atividade Laboratorial: Fatores que afetam a atividade enzimática. Biologia 12º ano. Nome: Data: / /
 Atividade Laboratorial: Fatores que afetam a atividade enzimática Biologia 12º ano Nome: Data: / / OBJETIVOS: Compreender o significado biológico das enzimas Conhecer o efeito de diversos fatores (concentração
Atividade Laboratorial: Fatores que afetam a atividade enzimática Biologia 12º ano Nome: Data: / / OBJETIVOS: Compreender o significado biológico das enzimas Conhecer o efeito de diversos fatores (concentração
Equações-chave FUNDAMENTOS. Seção A. Seção E. Seção F. Seção G. mv 2. E c E P. mgh. Energia total energia cinética energia potencial, ou E E c.
 Equações-chave FUNDAMENTOS Seção A 3 A energia cinética de uma partícula de massa m relaciona-se com sua velocidade v, por: E c mv 2 4 Um corpo de massa m que está a uma altura h da Terra tem energia potencial
Equações-chave FUNDAMENTOS Seção A 3 A energia cinética de uma partícula de massa m relaciona-se com sua velocidade v, por: E c mv 2 4 Um corpo de massa m que está a uma altura h da Terra tem energia potencial
CINÉTICA QUÍMICA. Obs.: a variação da quantidade deverá ser sempre um valor positivo, então ela deverá ser em módulo. 1.
 CINÉTICA QUÍMICA 1. Introdução O Conhecimento e o estudo da velocidade das reações, além de ser muito importante em termos industriais, também está relacionado ao nosso dia-adia, verificamos que há algumas
CINÉTICA QUÍMICA 1. Introdução O Conhecimento e o estudo da velocidade das reações, além de ser muito importante em termos industriais, também está relacionado ao nosso dia-adia, verificamos que há algumas
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Físico-química Farmácia 2014/02
 Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Química II 1º Exame B 4 de Junho de ª Parte
 Química II 1º Exame B 4 de Junho de 2018 Nome nº MEQ MEBiol Sala Duração: 3h 1: 2: 3: 4: 5: 6: 7: 8: 9: 10: Total: Responda às perguntas 1B a 5B na folha do enunciado Responda às perguntas 6B a 16B em
Química II 1º Exame B 4 de Junho de 2018 Nome nº MEQ MEBiol Sala Duração: 3h 1: 2: 3: 4: 5: 6: 7: 8: 9: 10: Total: Responda às perguntas 1B a 5B na folha do enunciado Responda às perguntas 6B a 16B em
Instituto de Ciências Biomédicas de Abel Salazar - UP. Mestrado Integrado em Bioengenharia
 Instituto de Ciências Biomédicas de Abel Salazar - UP Mestrado Integrado em Bioengenharia Ter ermodinâmica - 2014 / 2015 José Augusto Pereira INTRODUÇÃO À CALORIMETRIA ALORIMETRIA. Determinação da entalpia
Instituto de Ciências Biomédicas de Abel Salazar - UP Mestrado Integrado em Bioengenharia Ter ermodinâmica - 2014 / 2015 José Augusto Pereira INTRODUÇÃO À CALORIMETRIA ALORIMETRIA. Determinação da entalpia
Universidade Federal de Sergipe Departamento de Química Química Analítica Experimental Prof. Marcelo da Rosa Alexandre Alunos:
 Alunos: DETERMINAÇÃO DA ACIDEZ TOTAL EM BEBIDAS 1. Padronizar a solução de NaOH 0,1 mol.l -1 com biftalato de potássio (P.M. KHC8H4O4 = 204). Lembre-se de calcular a massa de biftalato de potássio para
Alunos: DETERMINAÇÃO DA ACIDEZ TOTAL EM BEBIDAS 1. Padronizar a solução de NaOH 0,1 mol.l -1 com biftalato de potássio (P.M. KHC8H4O4 = 204). Lembre-se de calcular a massa de biftalato de potássio para
Cinética das reações orgânicas
 inética das reações orgânicas inética de reações simples Determinação do tempo de semi-vida Ana Paula Francisco QFII 2016-2017 inética Segundo as guidelines para o estudo da Estabilidade Quando forem detetados
inética das reações orgânicas inética de reações simples Determinação do tempo de semi-vida Ana Paula Francisco QFII 2016-2017 inética Segundo as guidelines para o estudo da Estabilidade Quando forem detetados
Enzimas e Actividade enzimática
 Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
QUÍMICA GERAL EXPERIMENTAL 2º SEMESTRE DE 2016 EXPERIMENTO VIRTUAL DE CINÉTICA QUÍMICA
 QUÍMICA GERAL EXPERIMENTAL 2º SEMESTRE DE 2016 EXPERIMENTO VIRTUAL DE CINÉTICA QUÍMICA Acesse a página da Internet http://salvadorhurtado.wikispaces.com/file/view/cinequim.swf e siga as orientações para
QUÍMICA GERAL EXPERIMENTAL 2º SEMESTRE DE 2016 EXPERIMENTO VIRTUAL DE CINÉTICA QUÍMICA Acesse a página da Internet http://salvadorhurtado.wikispaces.com/file/view/cinequim.swf e siga as orientações para
Química II - 1º Exame A 5 de Junho de ª Parte
 Química II - 1º Exame A 5 de Junho de 2017 Nome nº MEQ MEBiol Sala 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. Duração do exame: 3h TOTAL. Responda às perguntas 1 a 6 na folha do enunciado
Química II - 1º Exame A 5 de Junho de 2017 Nome nº MEQ MEBiol Sala 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. Duração do exame: 3h TOTAL. Responda às perguntas 1 a 6 na folha do enunciado
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
A acção da catalase como função da temperatura
 A acção da catalase como função da temperatura Barroso, F. - Escola Secundária de Fernão Mendes Pinto Farinha, R. - Colégio Militar Sobreira, A. - Escola Básica 2,3/S Michel Giacometti INTRODUÇÃO A presente
A acção da catalase como função da temperatura Barroso, F. - Escola Secundária de Fernão Mendes Pinto Farinha, R. - Colégio Militar Sobreira, A. - Escola Básica 2,3/S Michel Giacometti INTRODUÇÃO A presente
ENZIMAS. Universidade Agrícola Uppsala - Suécia Julho W.J.Melo
 ENZIMAS Universidade Agrícola Uppsala Suécia Julho 2003 Cinética Enzimática EFEITO DA CONCENTRAÇÃO DO SUBSTRATO!Como avaliar?!realizase experimento com as seguintes características: #A varios tubos de
ENZIMAS Universidade Agrícola Uppsala Suécia Julho 2003 Cinética Enzimática EFEITO DA CONCENTRAÇÃO DO SUBSTRATO!Como avaliar?!realizase experimento com as seguintes características: #A varios tubos de
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE. Versão professor. Algumas notas prévias
 ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão professor O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão professor O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
EXAME DE CAPACIDADE IQ/USP 1 o SEMESTRE / 2010 PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA. Nome do Candidato: CADERNO DE QUESTÕES
 Uso SPG EXAME DE CAPACIDADE IQ/USP 1 o SEMESTRE / 2010 PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA Nome do Candidato: CADERNO DE QUESTÕES Instruções: Escreva seu nome de forma legível Das 10 (dez) questões
Uso SPG EXAME DE CAPACIDADE IQ/USP 1 o SEMESTRE / 2010 PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA Nome do Candidato: CADERNO DE QUESTÕES Instruções: Escreva seu nome de forma legível Das 10 (dez) questões
Determinação da Entalpia de uma Reacção
 INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático n.º 6 Determinação da Entalpia de uma Reacção
INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático n.º 6 Determinação da Entalpia de uma Reacção
Equilíbrio Químico (2)
 Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
PRÁTICA: EQUILÍBRIO QUÍMICO EM SOLUÇÕES. CH3COOCH2CH3 + H2O CH3COOH + CH3CH2OH (1) Acetato de etila água ácido acético etanol
 PRÁTICA: EQUILÍBRIO QUÍMICO EM SOLUÇÕES 1. Introdução Uma investigação experimental detalhada mostra que a maioria das reações químicas não avança até a realização completa, isto é, quantidades mensuráveis
PRÁTICA: EQUILÍBRIO QUÍMICO EM SOLUÇÕES 1. Introdução Uma investigação experimental detalhada mostra que a maioria das reações químicas não avança até a realização completa, isto é, quantidades mensuráveis
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO. Ano de Escolaridade : 11
 Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.2 Chuva normal e chuva ácida A classificação em chuva
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.2 Chuva normal e chuva ácida A classificação em chuva
3.2.2 Métodos de relaxação Métodos de competição Métodos de elevada resolução temporal ORDENS E CONSTANTES DE
 ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
Solução aquosa de tiossulfato de sódio 0,100 moldm. Ácido clorídrico concentrado: R: ; S: /37/ Realizar na hotte. Usar luvas.
 REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre ácido clorídrico e o tiossulfato de sódio a diferentes concentrações, através do tempo que demora a formar-se uma determinada
REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre ácido clorídrico e o tiossulfato de sódio a diferentes concentrações, através do tempo que demora a formar-se uma determinada
Físico-Química I. Profa. Dra. Carla Dalmolin. Misturas Simples. Termodinâmica das Misturas Propriedades das Soluções Atividade
 Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
QBQ 0316 Bioquímica Experimental. Carlos Hotta. Apresentação da disciplina
 QBQ 0316 Bioquímica Experimental Carlos Hotta Apresentação da disciplina 06/08/2014 Objetivos Abordar de forma prática conceitos que são apresentados de forma teórica em outras disciplinas Exercitar a
QBQ 0316 Bioquímica Experimental Carlos Hotta Apresentação da disciplina 06/08/2014 Objetivos Abordar de forma prática conceitos que são apresentados de forma teórica em outras disciplinas Exercitar a
Suporte universal Tubo de borracha comprido Bureta de 25 ml Pipeta volumétrica de 5mL Gobelé de 500 ml Kitasato de 25 ml Rolha Material e reagentes.
 REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre o ácido clorídrico e o magnésio a partir do volume de hidrogénio molecular libertado em função do tempo. Verificar que a
REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre o ácido clorídrico e o magnésio a partir do volume de hidrogénio molecular libertado em função do tempo. Verificar que a
Cinética de Reações Químicas
 Experiência 4: Cinética de Reações Químicas 1. Introdução A Cinética Química é a área da química que está relacionada com as velocidades das reações. A velocidade de uma reação química representa a variação
Experiência 4: Cinética de Reações Químicas 1. Introdução A Cinética Química é a área da química que está relacionada com as velocidades das reações. A velocidade de uma reação química representa a variação
Química II - 1º Exame B 5 de Junho de ª Parte
 Química II - 1º Exame B 5 de Junho de 2017 Nome nº MEQ MEBiol Sala 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. Duração do exame: 3h TOTAL. Responda às perguntas 1 a 6 na folha do enunciado
Química II - 1º Exame B 5 de Junho de 2017 Nome nº MEQ MEBiol Sala 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. Duração do exame: 3h TOTAL. Responda às perguntas 1 a 6 na folha do enunciado
CQ 033 FÍSICO QUÍMICA EXPERIMENTAL D
 UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE CIÊNCIAS EXATAS DEPARTAMENTO DE QUÍMICA CQ 033 FÍSICO QUÍMICA EXPERIMENTAL D REVISÃO PARA A 2ª PROVA PRÁTICA 06 - Entalpia de formação do NH 4 Cl(s) 1- formação
UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE CIÊNCIAS EXATAS DEPARTAMENTO DE QUÍMICA CQ 033 FÍSICO QUÍMICA EXPERIMENTAL D REVISÃO PARA A 2ª PROVA PRÁTICA 06 - Entalpia de formação do NH 4 Cl(s) 1- formação
LABORATÓRIO NP EN DETERMINAÇÃO DO TEMPO DE PRESA E DA EXPANSIBILIDADE DO CIMENTO.
 UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO DETERMINAÇÃO DO TEMPO DE PRESA E DA EXPANSIBILIDADE DO CIMENTO. DOCENTE: Engº Elson Almeida 2006
UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO DETERMINAÇÃO DO TEMPO DE PRESA E DA EXPANSIBILIDADE DO CIMENTO. DOCENTE: Engº Elson Almeida 2006
UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO
 UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO DETERMINAÇÃO DO TEMPO DE PRESA E DA EXPANSIBILIDADE DO CIMENTO. DOCENTE: Engº Elson Almeida 2006
UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO DETERMINAÇÃO DO TEMPO DE PRESA E DA EXPANSIBILIDADE DO CIMENTO. DOCENTE: Engº Elson Almeida 2006
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Metabolismo e Endocrinologia
 Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Neste caso, diz-se que a reação é de primeira ordem, e a equação pode ser resolvida conforme segue abaixo:
 1. Introdução Cinética Química A termodinâmica indica a direção e a extensão de uma transformação química, porém não indica como, nem a que velocidade, uma reação acontece. A velocidade de uma reação deve
1. Introdução Cinética Química A termodinâmica indica a direção e a extensão de uma transformação química, porém não indica como, nem a que velocidade, uma reação acontece. A velocidade de uma reação deve
Cinética das reacções enzimáticas
 Cinética das reacções enzimáticas Pioneiros da cinética enzimática: 1913 - L. Michaelis e M.L. Menten 1925 - Briggs e Haldane Leonor Michaelis Maud L. Menten v o = V max [S] K m + [S] Equação de Michaelis-Menten
Cinética das reacções enzimáticas Pioneiros da cinética enzimática: 1913 - L. Michaelis e M.L. Menten 1925 - Briggs e Haldane Leonor Michaelis Maud L. Menten v o = V max [S] K m + [S] Equação de Michaelis-Menten
2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados;
 CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
Hidrólise da ureia pela urease
 Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Termodinâmica. Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos. QUÍMICA GERAL Fundamentos
 Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos 1 Calor e Trabalho Calor e trabalho são formas relacionadas de energia Calor pode ser convertido em trabalho
Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos 1 Calor e Trabalho Calor e trabalho são formas relacionadas de energia Calor pode ser convertido em trabalho
Termodinâmica em Bioquímica
 Instituto de Química de São Carlos IQSC Universidade de São Paulo Termodinâmica em Bioquímica Disciplina: Bioquímica I Docente: Profa. Dra. Fernanda Canduri Sugestão de leitura: Cap. 1 do Lehninger A vida
Instituto de Química de São Carlos IQSC Universidade de São Paulo Termodinâmica em Bioquímica Disciplina: Bioquímica I Docente: Profa. Dra. Fernanda Canduri Sugestão de leitura: Cap. 1 do Lehninger A vida
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS
 BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE
 ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
Avenida Lourival Alfredo, 176, Poeira, Marechal Deodoro, Alagoas, Brasil,
 5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO. Ano de Escolaridade : 11
 Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.5 Solubilidade: solutos e solventes Apesar da água
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.5 Solubilidade: solutos e solventes Apesar da água
Noções de Cinética Química
 QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
Profª Eleonora Slide de aula. Revisão: Termodinâmica e Bioenergética
 Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
ACÇÃO DE FORMAÇÃO GUIÃO DE ACTIVIDADE PRÁTICA. (Versão Professor)
 Escola Secundária Marques de Castilho ÁGUEDA ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES GUIÃO DE ACTIVIDADE PRÁTICA FUNCIONAMENTO DE UM SISTEMA TAMPÃO (Versão Professor) Formando: Henrique
Escola Secundária Marques de Castilho ÁGUEDA ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES GUIÃO DE ACTIVIDADE PRÁTICA FUNCIONAMENTO DE UM SISTEMA TAMPÃO (Versão Professor) Formando: Henrique
METAIS COMO CATALIZADORES METAIS AMBIENTE E VIDA
 METAIS COMO CATALIZADORES METAIS AMBIENTE E VIDA Se somarmos as duas equações, a equação global é O bromo não se consome na reacção, sendo regenerado indefinidamente 2 Decomposição do peróxido de hidrogénio
METAIS COMO CATALIZADORES METAIS AMBIENTE E VIDA Se somarmos as duas equações, a equação global é O bromo não se consome na reacção, sendo regenerado indefinidamente 2 Decomposição do peróxido de hidrogénio
m = n M ρ = m V V = n V m Agrupamento de Escolas de Alcácer do Sal Escola Secundária de Alcácer do Sal
 Agrupamento de Escolas de Alcácer do Sal Escola Secundária de Alcácer do Sal Ano Letivo 2017/2018 Física e Química A 10º ano Teste de Avaliação 6A 11/06/2018 Duração: 90 minutos Tabela de Constantes 23
Agrupamento de Escolas de Alcácer do Sal Escola Secundária de Alcácer do Sal Ano Letivo 2017/2018 Física e Química A 10º ano Teste de Avaliação 6A 11/06/2018 Duração: 90 minutos Tabela de Constantes 23
1. Escreva as expressões da velocidade de reacção para as seguintes reacções em função do desaparecimento dos reagentes e da formação dos produtos:
 EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 8. Cinética Química Ficha de exercícios 1. Escreva as expressões da velocidade de reacção para as seguintes reacções em função do desaparecimento dos reagentes
EB: QUÍMICA GERAL/ EQB: QUÍMICA GERAL I Capítulo 8. Cinética Química Ficha de exercícios 1. Escreva as expressões da velocidade de reacção para as seguintes reacções em função do desaparecimento dos reagentes
ACTIVIDADE LABORATORIAL - QUÍMICA 12º ANO. Produção de BIODIESEL a partir de óleo alimentar usado
 ACTIVIDADE LABORATORIAL - QUÍMICA 12º ANO Produção de BIODIESEL a partir de óleo alimentar usado 1. Objectivo: Reutilizar os óleos vegetais rejeitados 2. O que se pretende: 2.1 Seleccionar material adequado
ACTIVIDADE LABORATORIAL - QUÍMICA 12º ANO Produção de BIODIESEL a partir de óleo alimentar usado 1. Objectivo: Reutilizar os óleos vegetais rejeitados 2. O que se pretende: 2.1 Seleccionar material adequado
é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições
 Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
QBQ 0316 Bioquímica Experimental. Carlos Hotta. Apresentação da disciplina
 QBQ 0316 Bioquímica Experimental Carlos Hotta Apresentação da disciplina 12/08/2016 Objetivos Abordar de forma prática conceitos que são apresentados de forma teórica em outras disciplinas Exercitar a
QBQ 0316 Bioquímica Experimental Carlos Hotta Apresentação da disciplina 12/08/2016 Objetivos Abordar de forma prática conceitos que são apresentados de forma teórica em outras disciplinas Exercitar a
Instituto de Ciências Biomédicas de Abel Salazar - UP
 Instituto de Ciências Biomédicas de Abel Salazar - UP Mestrado Integrado em Medicina e Mestrado Integrado em Medicina Veteriária Química Biológica II - 2012 / 2013 José Augusto Pereira PLARIMETRIA DE SLUÇÕES
Instituto de Ciências Biomédicas de Abel Salazar - UP Mestrado Integrado em Medicina e Mestrado Integrado em Medicina Veteriária Química Biológica II - 2012 / 2013 José Augusto Pereira PLARIMETRIA DE SLUÇÕES
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
MF-431.R-1 - MÉTODO TURBIDIMÉTRICO PARA DETERMINAÇÃO DE SULFATO
 MF-431.R-1 - MÉTODO TURBIDIMÉTRICO PARA DETERMINAÇÃO DE SULFATO Notas: Revisão aprovada pela Deliberação CECA nº 0102, de 04 de setembro de 1980. Publicada no DOERJ de 18 de setembro de 1980. 1. OBJETIVO
MF-431.R-1 - MÉTODO TURBIDIMÉTRICO PARA DETERMINAÇÃO DE SULFATO Notas: Revisão aprovada pela Deliberação CECA nº 0102, de 04 de setembro de 1980. Publicada no DOERJ de 18 de setembro de 1980. 1. OBJETIVO
