Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
|
|
|
- Maria Fernanda Vilanova Caminha
- 6 Há anos
- Visualizações:
Transcrição
1 CINÉTICA ENZIMÁTICA
2 Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências das condições de trabalho, como concentrações de ativadores, inibidores, reagentes, temperatura, ph; c) Correlacionar por modelos empíricos, ou matemáticos as velocidades das transformações com alguns fatores que afetam a velocidade; d) Colaborar na otimização do processo considerado; e) Estabelecer critérios para o controle do processo; f) Projetar reatores mais adequados
3 Cinética Enzimática
4 A cinética enzimática é o estudo do mecanismo pelo qual as enzimas ligam aos substratos e os transformam em produtos. São utilizados dados sobre a velocidade de reação de enzimas através de ensaios enzimáticos. Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
5 MedidadaVelocidade O primeiro problema que se apresenta ao estudar a cinética da reação é a medida de sua velocidade em condições experimentais conhecidas; Suponhamos que seja possível medir a concentração de substrato ou do produto durante o desenvolvimento da reação no seu início. Essas medidas conduzirão a curvas do tipo representada abaixo:
6 MedidadaVelocidade Observa-se que as velocidade de consumo de substrato e de formação de produto variam com o tempo; Mesmo mantendo a temperatura e ph constante, a concentração de enzima também pode diminuir, levando em conta alguns produtos que podem tornar-se inibidores da ação catatílica da enzima Portanto, o único instante em que as condições experimentais são conhecidas é no instante inicial; Por esse motivo a velocidade de reação enzimática deve ser calculada sempre que possível no instante t o
7 MedidadaVelocidade Em muitos casos as reações enzimáticas podem ser medidas no tempo inicial; Porém em alguns casos isto não é possível, neste caso, a velocidade de reação é medida por um velocidade média de consumo ou de produção de substâncias, ou pela variedade de uma propriedade do sistema, como textura, viscosidade, absorbância, etc.
8 MedidadaVelocidade A velocidade é mais elevada no início e vai decrescendo com o tempo. Isto acontece essencialmente porque: P v o S E reação mais lenta P (i) com o aumento de [P], começa a dar-se também a reação inversa, P S (ii) [S] vai decrescendo ao longo do tempo de reação, o que também diminui a velocidade da reação direta S P. reação inicial (mais elevada) (iii) se a reação for muito prolongada, começa a haver desnaturação da molécula enzimática. Tempo (t) Para evitar estes problemas, utiliza-se sempre a velocidade inicial (v o ), uma vez que se estará então a contabilizar apenas S P, com [S] conhecida e [P] = 0:
9 InfluênciadaConcentraçãode A- Concentração de Enzima Enzima Traçando um gráfico com as velocidades obtidas nestas experiências, em função das concentrações de enzima, verificamos que a variação é linear [E]
10 InfluênciadaConcentraçãode B- Concentração de substrato substrato A relação entre a concentração de substrato e as velocidades iniciais obtidas é hiperbólica. V 0 [S]
11 InfluênciadaConcentraçãode substrato Vitor Henri (903): E liga-se ao S para formar ES passo obrigatório; Leonor Michaelis e Maud Menten (93) E combina-se reversivelmente com S ES k E + S ES k 2 ES se rompe E e P k 3 ES E + P
12 InfluênciadaConcentraçãode substrato Qualquer instante da reação: E e ES; [S] = velocidade da reação [S]; V máx = todas as moléculas de E estiverem na forma ES enzima saturada ; [S]: estado pré-estacionário ES; Estado estacionário [ES] = cte; V 0 estado estacionário.
13 Equação Michaelis-Menten Curva: possui a mesma forma para a maioria das enzimas; Expressa pela Equação de Michaelis e Menten; Hipótese: limitante quebra de ES E + P.
14 Equação Michaelis-Menten Equação da velocidade para uma reação catalisada enzimaticamente e com um único substrato; Relação quantitativa entre a V 0, a V máx e a [S] inicial relacionadas através de K m. V 0 = V K máx m + [ S] [ S]
15 Equação Michaelis-Menten Relação numérica: V 0 é metade de V máx ; V0 = V máx 2 k m = afinidade pelo substrato; K m afinidade V máx é proporcional à [E].
16 Significado de K m e V máx Equação Michaelis e Menten = dependência hiperbólica; Mecanismos de reação diferentes catalisam reações com 6 ou 8 passos; Significado e magnitude de V máx e K m varia; K m : depende de aspectos específicos do mecanismo de reação.
17 Significado de K m e V máx k2 + K m = KK 3 << K 2 afinidade da enzima; K 3 >> K 2 ; K 3 e K 2 são comparáveis a K m função complexa; V máx : número de passos da reação e identidade dos passos limitantes. k k 3
18 Significado de K m e V máx K K 2 K 3 E + S ES EP E + P K - K -2 Enzima na saturação: EP e V máx = k 3.x=k.e K cat = velocidade limitante de qualquer reação enzimas saturadas; K cat e K m = ambiente celular, concentração do substrato e química da reação.
19 Lei de Michaelise Menten O modelo cinético de Michaelis e Menten é um dos mais aceitos cujo o objetivo basico é explicar a influência da concentração iniciais de enzima e de substrato na velocidade inicial de reação enzimática; As hipóses básicas do modelo são: a) O substrato e a enzima reagem reversivelmente entre sí, formando um composto intermediário, denominado complexo enzima-substrato; b) O complexo formado ou se decompõe, ou reage com outra substancia regenerando a enzima e formando os produtos da reação Consideremos o caso mais simples possível: a) A formação do composto enzima-substrato se dá na proporção de mol de substrato para mol da enzima, produzindo mol do complexo; b) O complexo formado se decompõem sem reagir com outras substâncias existente no sistema
20 Equaçãode Michaelis-MentenMenten Comportamento é explicado pela formação do complexo enzima-substrato ES. A enzima liga-se ao substrato reversivelmente formando o complexo ES Reação rápida k E + S ES k 2 2. O complexo ES dissocia-se em enzima livre e produto da reação Reação mais lenta k 3 ES E + P.A reação 2, mais lenta, limita a velocidade global da reação..a velocidade é proporcional à concentração do complexo ES..A cada momento a enzima existe na forma livre e no complexo ES..A velocidade máxima (V máx ) da reação ocorre quando todas as enzimas estão associadas as moléculas de substrato.
21 Dedução da Equação Michaelis-Menten Pressuposto: não há transformação de produto em substrato Reações de formação e dissociação do complexo ES: k E + S ES P + E k 3 e-x s-x k 2 x V k 2 Onde: [E] e [S] são as concentrações da enzima e do substrato livres. K : constante de velocidade de formação do complexo; K 2 : constante de velocidade de dissociação do complexo; K 3 : constante de decomposição do complexo formando produto V: velocidade de formação do produto s: molaridade inicial do substrato e: molaridade inicial da enzima x : molaridade do complexo no instante t
22 Dedução da Equação Michaelis-Menten dx dt = k ( e x)( s x) k2. x k3. x x k 2 Admitindo que a concentração de substrato é muito maior que a da enzima, podemos desprezar x, em relação a s: dx dt = k e x) s k2. x k ( 3 Considerando que a reação ocorra inicialmente num tempo muito curto, micro-segundos, a concentração do complexo pode ser dita constante, então: dx = 0 hipotese de Briggs e Haldane) dt. x Separando x, que vai definir a velocidade do complexo em formar produto, temos: Dividindo tudo por k e usando a constante de Michaelis, k. e. s + k + k = x = : k k 2 + k3 + k. s 3. s k. e. s Vem: k2 + k m = x = k k e. s m + k 3 s
23 Dedução da Equação Michaelis-Menten Agora é possível calcular a Velocidade de formação de produto, Correlacionando v = k. 3 x = k3. e k O máximo valor da velocidade será alcançado quando toda enzima estiver na forma de complexo, isto é, x=e, então a velocidade máxima será: s m + s Equação de Michaelis e Mentem: S : maior afinidade Permite, após determinação experimental das variações de v em função de [S], obter o valor de V max e calcular KM S 2 : menor afinidade... K M é uma medida da afinidade da enzima para o substrato (= /K M ) (K M elevado afinidade baixa) K M K M2
24 Linearização da Equação Michaelis-Menten Devido às dificuldades de cálculo de K M através da equação de Michaelis - Menten, procurou-se obter uma representação linear da relação entre V 0 e S que pudesse ser traduzida por uma reta.
25 B- Concentração de substrato: determinação dos parâmetros cinéticos (Km e V max ) Exemplo velocidades iniciais de reação da fosfatase ácida a várias concentrações de glicerol, [S].
26 EXEMPLOS DE APLICAÇÃO
27 EXEMPLOS DE APLICAÇÃO
28 INFLUENCIA DA PRESENÇA DE INIBIDOR Inibidor: substância que provoca diminuição da velocidade de reação; Inibidor irreversível: quando bloqueia parcial ou totalmente a enzima; Inibidor reversível: quando reagem reversívelmente com a enzima; O inibidor, pode ser um substrato ou um produto; Exemplo: a) a invertase que catalisa a sacarose, quando presente em altas concentrações inibe a enzima; b) a alfa amilase que catalisa o amido em dextrina e maltose pode ser inibida em determinada fase pelo produto; c) A inibição pode ser competitiva, não competitiva e incompetitiva
29 INFLUENCIA DO EXCESSO DE SUBSTRATO k E + S ES k 2 k 3 ES + S ES2 (Complexo não reativo) k 4 k 5 ES E + P V V Vmax V = VmaxS S 2 k m + S + k i onde ki é a constante de inibição; S Para encontrar as constantes faz-se a inversão segundo Lineweaver-Burk
30 INFLUENCIA DO EXCESSO DE SUBSTRATO V = Vmax + k m Vmax. S + VmaxK i X S ª Hipótese: para valores de S<<ki a equação se reduz em, V = Vmax + k m. Vmax S /V K m /v max -/k m /S
31 INFLUENCIA DO EXCESSO DE SUBSTRATO V = Vmax + k m Vmax. S X + VmaxK i S 2ª Hipótese: para valores de S>>k m a equação se reduz em, V = Vmax + VmaxKi S /V /V max /v max K i S Os valores de V max determinados em ambos os gráficos devem ser próximos.
32 INIBIÇÃO COMPETITIVA Inibidor competitivo concorre com o S pelo sitio ativo da E livre. I análogo não metabolizável, derivado de um S verdadeiro, S substituto da E ou um P da reação. I compostos com estrutura molecular lembra S afinidade da enzima pelo substrato [substrato] necessária para obter a mesma [ES] Km aparente da enzima
33 INIBIÇÃO COMPETITIVA Indicando por I a fórmula molecular do inibidor e com i, sua molaridade inicial, o modelo Michaelis e Menten pode ser representado pelas seguintes equações químicas: k E + S ES P + E e-x-y s-x k 2 x v i k 3 k 4 k 6 E + I EI P + E e-x-y i-y k 5 y Onde : v i Velocidade de formação de produto, obviamente menor que v, da equação sem inibição
34 Na prática, s>>x e i>>y: dx dt = dy dt k = INIBIÇÃO COMPETITIVA ( e x y) s ( k2 k3 + k ( e x y) i ( k5 k6 4 + k E + S ES v i P + E e-x-y s-x k x k 2 k 3 s ). x ) y k 4 k 6 E + I EI P + E e-x-y i-y k 5 y Onde : Vale destacar que a reação entre a enzima e o inibidor pode não correr, formando o P,consequentemente, k 6 =0 Fazendo dx/dt=dy/dt=0 (hipotese de Briggs e Haldane)
35 x = k e. s i ( + k INIBIÇÃO COMPETITIVA m ) + i s k + k fazendok m = k 2 + k3 k5, e ki = k 4 6 A velocidade, v será dada pela equação: i v i = k3. x = k3. e = V k m s i ( + k i ) + s
36 INIBIÇÃO COMPETIVA Linearizando pelo método Lineawer-Burk: v i = V + k m ( + V i k i ). s
37 INIBIÇÃO COMPETITIVA Linearizando pelo método Lineawer-Burk: Equação de Michaelis e Menten [ S] V = V máx K + [ I ] [ S] K Lineweaver-Burk V = V máx + m K m + V [ I ] máx K I I + [ S]
38 INIBIÇÃO COMPETITIVA v i Dividindo por Obtém-se a relação entre a velocidade de reação sem inibidor e com inibidor. s v = V v k k + s m m = +. i s = V. v k k s i i i ( m + ) km( + ) + s k i v vi Verifica-se que é possível trabalhar com concentrações de substratos relativamente altas (matematicamente, s ) a influência do inibidor pode tornar-se desprezível. v i V V 0 I = + K I K m ( [ ]) [ I ] K + S m [S] = influência do [I] desprezível.
39 INIBIÇÃO COMPETITIVA Esta tendência pode ser observado no exemplo númerico representado na Figura abaixo, onde V=6,0 mg/l; km=2,50 mg/l e ki=,60mg/l Exemplos de inibição competitiva: inibição da glicose na invertase, durante v hidrólise da sacarose; i Inibição pela alfa dextrina na alfaamilase durante a hidrólise do amido
40 INIBIÇÃO COMPETITIVA v i - sem inibidor 2- com inibidor na concentração [I] 3- com inibidor na concentração [I2] > [I]
41 INIBIÇÃO NÃO COMPETITIVA K I E + S K S ES E + P + + I I EI + S K I K 2 [ E][ I] K = = [ ES ][ I] [ EI ] [ EIS ] K S S EIS Michaelis-Menten v I = K m ( + Vmax [ S] [ I] ) + [ S]( + K I [ I] ) K I v i Lineweaver-Burk v = K V m max ( + [ I] ) K [ S] I + V max ( + [ I] ) K I
42 INIBIÇÃO NÃO COMPETITIVA Equação da velocidade: V = V máx K m + K [ S] [ I ] [ S] I + + [ I ] K I Lineweaver-Burk V K [ ] = m I + [ I ] + [ ] + Vmáx K I S Vmáx K I
43 INIBIÇÃO NÃO COMPETITIVA - sem inibidor 2- com inibidor na concentração [I] 3- com inibidor na concentração [I2] > [I]
44 INIBIÇÃO INCOMPETITIVA Inibidor incompetitivo se liga reversivelmente, em um sítio próprio, ao complexo ES. I não tem semelhança estrutural com o S I favorece a formação do ES Km e Vmax da enzima
45 INIBIÇÃO INCOMPETITIVA E + S K S ES K 2 E + P + I EIS K = [ ES ][ [ EIS I ] ] K I V max [ S ] Michaelis-Menten v I = [ I ] + K i K m + [ I ] + K I [ S ] Lineweaver-Burk v = K V m max [ S ] + V max ( + [ I ] K I )
46 INIBIÇÃO INCOMPETITIVA V = + V K + I máx [ I ] m [ ] K K I I + [ S] [ S] V K = m [ I + ] [ ] + Vmáx S Vmáx K I
47 INIBIÇÃO INCOMPETITIVA - sem inibidor. 2- com inibidor na concentração [I] 3- com inibidor na concentração [I2] > [I]
48 INIBIÇÃO IRREVERSÍVEL Combinam-se com um grupo funcional destruição; União covalente inibidor e enzima. V máx e K m =
49 INIBIÇÃO IRREVERSÍVEL Equação de Michaelis e Menten: V I ( V k [ EI ) = ] máx 3 K m [ S] + [ S]
50 INIBIÇÃO IRREVERSÍVEL Lineweaver-Burk: V I = V máx K 3 + K [ EI] V K [ EI] [ S] máx m 3
51 C- Efeito do ph INFLUÊNCIA DO PH Os ph extremos modificam irremediavelmente a estrutura das enzimas, quer devido a desnaturação, quer devido a alterações na ligação entre apoenzima e coenzima As enzimas podem apresentar dois tipos de curva de atividade em função do ph
52 C- Efeito do ph INFLUÊNCIA DO PH possível efeito duma alteração de ph ao nível do centro ativo de um enzima: A. ph óptimo B. ph inferior ao óptimo (maior [H+])
53 C- Efeito do ph INFLUÊNCIA DO PH Nem todas as enzimas têm o mesmo ph. Por exemplo, a pepsina, que hidrolisa proteínas a péptidos no estômago, extremamente ácido, e a tripsina, que hidrolisa péptidos a aminoácidos nas condições alcalinas do duodeno, têm óptimos de ph adaptados ao seu ambiente Em laboratório, quando estudamos a atividade de um enzima, temos que ter o cuidado de incluir um sistema tampão no meio de ensaio, de modo a estabilizar o ph;
54 INFLUÊNCIA DO PH ph 5 e 8 = não afeta a atividade; Declínio entre ph 6,8-8 e 6,8-5 = forma iônica não adequada; 5 > ph > 8 = inativação irreversível.
55 INFLUÊNCIA DA TEMPERATURA T velocidade de reação = energia cinética; T muito elevadas = desnaturação da enzima Rompidas as pontes de hidrogênio alterações estruturas = nova conformação; T desnaturação pouco acima da T ótima.
56 INFLUÊNCIA DA TEMPERATURA Enzimas PM cadeia polipeptídica e pontes dissulfeto = estáveis ao calor; Efeito da T = ph, força iônica e a presença ou ausência de ligantes; Substratos protegem a enzima da desnaturação.
57 INFLUÊNCIA DA TEMPERATURA K é função da T Lei de Arrhenius A influência da temperatura na constante de velocidade k, obedece a lei Arrhenius k = k 0 e α RT
58 INFLUÊNCIA DA TEMPERATURA Enzimas são termolábeis reação enzimática = inativação términa = k ' 0 β RT Efeito da T na velocidade das reações coeficiente de temperatura e Velocidade quando a T 0ºC. k ' 2,3 R T2 T logq0 = 0 O Q 0 (coeficiente de temperatura) representa o fator pelo qual a velocidade das reações enzimáticas (ou de outro processo biológico) vem multiplicada em consequência de um acréscimo de temperatura de 0 C. O Q 0 das reações enzimáticas situa-se entre e 2. E a
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
2 APLICAÇÕES INDUSTRIAIS Tabela 1: Enzimas aplicadas na indústria APLICAÇÃO ENZIMA
 CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
Engenharia Bioquímica
 Engenharia Bioquímica Cinética Enzimática Mestrando: Mateus Vinícius Casagrande da Silva Professor Doutor João Batista de Almeida e Silva Conceitos e revisão sobre Enzimas O que são enzimas? Definições
Engenharia Bioquímica Cinética Enzimática Mestrando: Mateus Vinícius Casagrande da Silva Professor Doutor João Batista de Almeida e Silva Conceitos e revisão sobre Enzimas O que são enzimas? Definições
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13
 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
CQ110 : Princípios de FQ. Imagens de Rorschach
 Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Catálise Enzimática. Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química.
 Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sítio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sítio ou centro ativo S + E
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
São moléculas catalíticas protéicas (exceto algumas que são RNA) - Prefixo que designa a reação: lactato desidrogenase, catalase
 1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 581-
 Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Cinética das reacções enzimáticas
 Cinética das reacções enzimáticas Pioneiros da cinética enzimática: 1913 - L. Michaelis e M.L. Menten 1925 - Briggs e Haldane Leonor Michaelis Maud L. Menten v o = V max [S] K m + [S] Equação de Michaelis-Menten
Cinética das reacções enzimáticas Pioneiros da cinética enzimática: 1913 - L. Michaelis e M.L. Menten 1925 - Briggs e Haldane Leonor Michaelis Maud L. Menten v o = V max [S] K m + [S] Equação de Michaelis-Menten
Cinética de reacções. enzimáticas mono-substrato
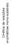 Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Enzimas e Actividade enzimática
 Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Proteínas II. (Enzimas) Bioquímica Prof. Dr. Marcelo Soares
 Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Professora: Erika Liz. C i n é t i c a. E n z i m á t i c a
 rofessora: Erika Liz C i n é t i c a E n z i m á t i c a Elementos da Enzimologia Reações Químicas Termodinâmica estuda a viabilidade e a reversibilidade das reações, a partir da análise do conteúdo energético
rofessora: Erika Liz C i n é t i c a E n z i m á t i c a Elementos da Enzimologia Reações Químicas Termodinâmica estuda a viabilidade e a reversibilidade das reações, a partir da análise do conteúdo energético
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula!
 Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
QBQ 0102 Educação Física. Carlos Hotta. Enzimas 17/03/15
 QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
Prof. Marcelo Langer. Curso de Biologia. Aula 38 Citologia
 Prof. Marcelo Langer Curso de Biologia Aula 38 Citologia ENZIMAS Apenas alguns grupos de moléculas de RNA que apresentam função biocatalisadora, todas as enzimas são proteínas. FUNÇÕES DAS ENZIMAS: Proteínas
Prof. Marcelo Langer Curso de Biologia Aula 38 Citologia ENZIMAS Apenas alguns grupos de moléculas de RNA que apresentam função biocatalisadora, todas as enzimas são proteínas. FUNÇÕES DAS ENZIMAS: Proteínas
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias.
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
Enzimas. Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
Cinética enzimática. Cinética enzimática. Cinética enzimática 20/03/2012. Classificação sistemática das enzimas
 Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Diagrama mostrando a Anidrase carbónica II. A esfera cinza é um ion de zinco que funciona como cofator no sítio ativo.
 CINÉTICA ENZIMÁTICA Diagrama mostrando a Anidrase carbónica II. A esfera cinza é um ion de zinco que funciona como cofator no sítio ativo. CINÉTICA ENZIMÁTICA CINÉTICA ENZIMÁTICA ENZIMAS Amilases (hidrolase)
CINÉTICA ENZIMÁTICA Diagrama mostrando a Anidrase carbónica II. A esfera cinza é um ion de zinco que funciona como cofator no sítio ativo. CINÉTICA ENZIMÁTICA CINÉTICA ENZIMÁTICA ENZIMAS Amilases (hidrolase)
Enzimas. Bianca Zingales IQ - USP
 Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Hidrólise da ureia pela urease
 Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global.
 ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
ENZIMAS. Dra. Flávia Cristina Goulart. Bioquímica
 ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
Aula 12: Enzimas Introdução e Cinética
 Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Aula 2: Estrutura e Função de Proteínas
 Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS. Enzimas. Prof. Me. Cássio Resende de Morais
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
Atividade a Distância 4 CINÉTICA
 Atividade a Distância 4 CINÉTICA Na parte 1 da Aula 3 vimos a definição de velocidade inicial e como deve ser medida. Agora, vamos ver como ela varia se mudarmos a concentração dos reagentes. Estamos acostumados
Atividade a Distância 4 CINÉTICA Na parte 1 da Aula 3 vimos a definição de velocidade inicial e como deve ser medida. Agora, vamos ver como ela varia se mudarmos a concentração dos reagentes. Estamos acostumados
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores
 Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
QBQ 0316 Bioquímica Experimental. Carlos Hotta. Análise de dados (P1 e P2)
 QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
ENZIMAS ENZIMAS ENZIMAS ENZIMAS ENZIMAS 31/03/2018. PROFº STUART - 1 TEORIA DA CATÁLISE A + B DEFINIÇÃO
 DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
ENZIMAS ENZIMAS ENZIMAS 19/02/17 DEFINIÇÃO CLASSIFICAÇÃO ESTRUTURAL. ativa. inativa
 DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
[ A][ B] [ A] [ B] v {[A] }= Vmáx
![[ A][ B] [ A] [ B] v {[A] }= Vmáx [ A][ B] [ A] [ B] v {[A] }= Vmáx](/thumbs/75/72105322.jpg) Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas.
 São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
Cinética Química. Prof. Alex Fabiano C. Campos
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
Introdução ao bloco II Enfermagem. Monica Montero Lomeli Sylvia Alquéres
 Introdução ao bloco II Enfermagem Monica Montero Lomeli Sylvia Alquéres Programação de aulas 16/set 21/set 23/set 28/set 30/set 05/out 07/out 12/out 14/out Apresentação do bloco + Enzimas I (cinéeca) Enzimas
Introdução ao bloco II Enfermagem Monica Montero Lomeli Sylvia Alquéres Programação de aulas 16/set 21/set 23/set 28/set 30/set 05/out 07/out 12/out 14/out Apresentação do bloco + Enzimas I (cinéeca) Enzimas
Engenharia Biomédica. Relatório Cinética da Enzima Invertase
 Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
Cinética Química. a b c p q r. As concentrações dos reagentes são funções do tempo:
 Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
Enzimas - Sítio catalítico
 Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
E Z N I Z MAS INT N RO R D O U D Ç U Ã Ç O
 ENZIMAS INTRODUÇÃO A manutenção da vida celular depende da contínua ocorrência de um conjunto de reações, que devem atender 2 exigências fundamentais: 1 a As reações devem ocorrer em velocidades adequadas
ENZIMAS INTRODUÇÃO A manutenção da vida celular depende da contínua ocorrência de um conjunto de reações, que devem atender 2 exigências fundamentais: 1 a As reações devem ocorrer em velocidades adequadas
1- Microrganismos e indústria alimentar 1.1 Fermentação e actividade enzimática
 Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
BCL 0307 Transformações Químicas
 BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008. Disciplina de BIOQUÍMICA I Curso de MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Mecanismos de catálise enzimática
 Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
ENZIMAS. Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica. Prof.: Me.
 Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
OBJETIVOS BIBLIOGRAFIA ENZIMAS E INIBIDORES ENZIMÁTICOS
 OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
PQI-2321 Tópicos de Química para Engenharia Ambiental I
 PQI-2321 Tópicos de Química para Engenharia Ambiental I Aula 20 Prof. Moisés Teles moises.teles@usp.br Departamento de Engenharia Química da Escola Politécnica da UP Motivação: Microorganismos e Engenharia
PQI-2321 Tópicos de Química para Engenharia Ambiental I Aula 20 Prof. Moisés Teles moises.teles@usp.br Departamento de Engenharia Química da Escola Politécnica da UP Motivação: Microorganismos e Engenharia
BIOENERGÉTICA INTRODUÇÃO
 INTRODUÇÃO BIOENERGÉTICA Hoje, mais do que nunca, estamos conscientes de que a energia, a capacidade de produzir trabalho, é vital para a nossa civilização moderna. Nas suas diversas formas (elétrica,
INTRODUÇÃO BIOENERGÉTICA Hoje, mais do que nunca, estamos conscientes de que a energia, a capacidade de produzir trabalho, é vital para a nossa civilização moderna. Nas suas diversas formas (elétrica,
Mecanismos de catálise enzimática
 Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
Físico-química Farmácia 2014/02
 Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Inibidores Enzimáticos
 Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
Aula de Bioquímica I. Tema: Cinética Enzimática. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Cinética Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Cinética Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
BIOLOGIA. Moléculas, células e tecidos. A química da vida Parte 5. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos A química da vida Parte 5 Professor: Alex Santos Tópicos em abordagem: Enzimas: I Conceitos fundamentais II Propriedades das enzimas III Nomenclatura de enzimas IV
BIOLOGIA Moléculas, células e tecidos A química da vida Parte 5 Professor: Alex Santos Tópicos em abordagem: Enzimas: I Conceitos fundamentais II Propriedades das enzimas III Nomenclatura de enzimas IV
ENZIMAS. Universidade Agrícola Uppsala - Suécia Julho W.J.Melo
 ENZIMAS Universidade Agrícola Uppsala Suécia Julho 2003 Cinética Enzimática EFEITO DA CONCENTRAÇÃO DO SUBSTRATO!Como avaliar?!realizase experimento com as seguintes características: #A varios tubos de
ENZIMAS Universidade Agrícola Uppsala Suécia Julho 2003 Cinética Enzimática EFEITO DA CONCENTRAÇÃO DO SUBSTRATO!Como avaliar?!realizase experimento com as seguintes características: #A varios tubos de
COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae
 COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae Lauri Alves JUNIOR¹, André Luis Fachini de SOUZA², Vanessa Neves HÖPNER² ¹Acadêmico do curso
COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae Lauri Alves JUNIOR¹, André Luis Fachini de SOUZA², Vanessa Neves HÖPNER² ¹Acadêmico do curso
Produção de alimentos e sustentabilidade
 Bio12 Unidade 4 e sustentabilidade Como produzir maiores quantidades de alimentos para resolver os problemas de alimentação? Capítulo 1.1. Fermentação e atividade enzimática Que fatores condicionam a atividade
Bio12 Unidade 4 e sustentabilidade Como produzir maiores quantidades de alimentos para resolver os problemas de alimentação? Capítulo 1.1. Fermentação e atividade enzimática Que fatores condicionam a atividade
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC
 IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
Avenida Lourival Alfredo, 176, Poeira, Marechal Deodoro, Alagoas, Brasil,
 5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
ESTABILIDADE DE ENZIMAS
 ESTABILIDADE DE ENZIMAS Estabilidade Enzimática X Atividade Enzimática Atividade Enzimática: É dada pela medição da velocidade inicial da reação sob uma faixa de condições determinadas. Establidade Enzimática:
ESTABILIDADE DE ENZIMAS Estabilidade Enzimática X Atividade Enzimática Atividade Enzimática: É dada pela medição da velocidade inicial da reação sob uma faixa de condições determinadas. Establidade Enzimática:
Cinética Química. c) A opção (C) está correta. B 3+ e B 4+ não aparecem na reação global, portanto, são intermediários da reação.
 Capítulo 6 Cinética Química 1. (ITA) Considere o seguinte mecanismo de reação genérica: A 4+ + B 2+ A 3+ + B 3+ (etapa lenta) A 4+ + B 3+ A 3+ + B 4+ (etapa rápida) C + + B 4+ C 3+ + B 2+ (etapa rápida)
Capítulo 6 Cinética Química 1. (ITA) Considere o seguinte mecanismo de reação genérica: A 4+ + B 2+ A 3+ + B 3+ (etapa lenta) A 4+ + B 3+ A 3+ + B 4+ (etapa rápida) C + + B 4+ C 3+ + B 2+ (etapa rápida)
Metabolismo e Endocrinologia
 Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Equipe de Biologia. Biologia
 Aluno (a): Série: 3ª Turma: TUTORIAL 4B Ensino Médio Equipe de Biologia Data: Biologia ENZIMAS CONCEITOS GERAIS E FUNÇÕES As enzimas são proteínas especializadas na catálise de reações biológicas. Elas
Aluno (a): Série: 3ª Turma: TUTORIAL 4B Ensino Médio Equipe de Biologia Data: Biologia ENZIMAS CONCEITOS GERAIS E FUNÇÕES As enzimas são proteínas especializadas na catálise de reações biológicas. Elas
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa
 Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
Enzimas Alostéricas e com Múltiplos Sítios Ativos
 Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação
 Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
ENZIMAS CINÉTICA ENZIMÁTICA. Classificação. Natureza da reação catalisada. Disponibilidade comercial IMPORTÂNCIA INDUSTRIAL OBJETIVOS
 OBJETIO Medir as elocidades de transforação CINÉTICA ENZIMÁTICA Aaliar a influência de condições de reação (conc. de reagentes, enzias, teperatura, ph, etc..) nas elocidades de reação Correlacionar atraés
OBJETIO Medir as elocidades de transforação CINÉTICA ENZIMÁTICA Aaliar a influência de condições de reação (conc. de reagentes, enzias, teperatura, ph, etc..) nas elocidades de reação Correlacionar atraés
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2016_2017_1º Teste
 BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2016_2017_1º Teste 24/11/2016 (Duração: 1h,30 m) Nome do Aluno: Nº: Curso: Cada uma das questões tem a cotação de 0,5 valores. Nas questões de escolha múltipla será
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2016_2017_1º Teste 24/11/2016 (Duração: 1h,30 m) Nome do Aluno: Nº: Curso: Cada uma das questões tem a cotação de 0,5 valores. Nas questões de escolha múltipla será
Biologia Molecular (Parte I)
 Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Tabela 1: Aumento de velocidade de reação proporcionado por certas enzimas Enzima Velocidade da reação não catalisada
 Bioquímica Metabólica Noturno Prof. Roberto K. Salinas 2. Cinética enzimática Enzimas são catalisadores em sistemas biológicos. As características mais notáveis das enzimas são o seu poder catalítico e
Bioquímica Metabólica Noturno Prof. Roberto K. Salinas 2. Cinética enzimática Enzimas são catalisadores em sistemas biológicos. As características mais notáveis das enzimas são o seu poder catalítico e
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
Equilíbrio Químico. É uma reação reversível na qual a velocidade da reação direta é igual à velocidade da reação inversa.
 Equilíbrio Químico É uma reação reversível na qual a velocidade da reação direta é igual à velocidade da reação inversa. CLASSIFICAÇÃO DAS REAÇÕES Uma reação química diz-se completa quando leva ao esgotamento
Equilíbrio Químico É uma reação reversível na qual a velocidade da reação direta é igual à velocidade da reação inversa. CLASSIFICAÇÃO DAS REAÇÕES Uma reação química diz-se completa quando leva ao esgotamento
Cinética Química 17/04/17. V m h. Prof. Xuxu. Velocidade das reações químicas. Velocidade das reações químicas. Velocidade Média. Hora da saída: 11:45
 Seja Bem-indo a Goiânia elocidade Média Cinética Química Hora da saída: 11:45 Δd 40km m 40 km Δt 1h h Distância Hidrolândia: 40 km Seja Bem-indo a Hidrolândia Prof. Xuxu Hora da chegada: 12:45 elocidade
Seja Bem-indo a Goiânia elocidade Média Cinética Química Hora da saída: 11:45 Δd 40km m 40 km Δt 1h h Distância Hidrolândia: 40 km Seja Bem-indo a Hidrolândia Prof. Xuxu Hora da chegada: 12:45 elocidade
A B A B. Espontaneidade vs. Velocidade de Reações. Enzimas como Catalisadores. Velocidade das reações depende da Energia de Ativação
 Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
EQUILÍBRIOS: QUÍMICO E IÔNICO Profº Jaison Mattei
 EQUILÍBRIOS: QUÍMICO E IÔNICO Profº Jaison Mattei Reações completas ou irreversíveis São reações nas quais os reagentes são totalmente convertidos em produtos, não havendo sobra de reagente, ao final da
EQUILÍBRIOS: QUÍMICO E IÔNICO Profº Jaison Mattei Reações completas ou irreversíveis São reações nas quais os reagentes são totalmente convertidos em produtos, não havendo sobra de reagente, ao final da
Físico-Química Experimental Exp. 10. Cinética Química
 Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Caracterização de Disciplina
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DE PELOTAS PRÓ-REITORIA DE GRADUAÇÃO CURSO DE BACHARELADO EM ZOOTECNIA Caracterização de Disciplina Disciplina Bioquímica Caráter da Disciplina Obrigatório Pré-Requisito
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DE PELOTAS PRÓ-REITORIA DE GRADUAÇÃO CURSO DE BACHARELADO EM ZOOTECNIA Caracterização de Disciplina Disciplina Bioquímica Caráter da Disciplina Obrigatório Pré-Requisito
Aplicações de Enzimas e Biocatálise
 Aplicações de Enzimas e Biocatálise Estabilidade enzimática Raúl J. Barros 2012 Uma preparação enzimática geralmente perde atividade ao longo do tempo, à medida que as moléculas proteicas que a constituem
Aplicações de Enzimas e Biocatálise Estabilidade enzimática Raúl J. Barros 2012 Uma preparação enzimática geralmente perde atividade ao longo do tempo, à medida que as moléculas proteicas que a constituem
Enzimas são polímeros biológicos que catalisam as reações químicas que tornam a vida possível como a conhecemos.
 ENZIMAS Enzimas são polímeros biológicos que catalisam as reações químicas que tornam a vida possível como a conhecemos. A presença e a manutenção dum conjunto completo e balanceado de enzimas é essencial
ENZIMAS Enzimas são polímeros biológicos que catalisam as reações químicas que tornam a vida possível como a conhecemos. A presença e a manutenção dum conjunto completo e balanceado de enzimas é essencial
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia - UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia - UFPel Introdução Don't waste clean thinking on dirty enzymes!!! Efraim Racker (1913-1991) Introdução Desta
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia - UFPel Introdução Don't waste clean thinking on dirty enzymes!!! Efraim Racker (1913-1991) Introdução Desta
é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições
 Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética das reações orgânicas
 inética das reações orgânicas inética de reações simples Determinação do tempo de semi-vida Ana Paula Francisco QFII 2016-2017 inética Segundo as guidelines para o estudo da Estabilidade Quando forem detetados
inética das reações orgânicas inética de reações simples Determinação do tempo de semi-vida Ana Paula Francisco QFII 2016-2017 inética Segundo as guidelines para o estudo da Estabilidade Quando forem detetados
Com base nos dados acima, responda as questões propostas (cuidado com as unidades):
 Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Pi Principais i i Tópicos Abordados dd
 BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
Resposta: B Comentário: Resposta: A Comentário: Item A: verdadeiro Item B: falso Item C: falso Item D: falso Item E: falso Resposta: C Comentário
 1. Comentário: Enzimas são proteínas catalíticas, aumentando a velocidade de uma reação química específica através da diminuição de sua energia de ativação. Como as demais proteínas, são orgânicas e biodegradáveis,
1. Comentário: Enzimas são proteínas catalíticas, aumentando a velocidade de uma reação química específica através da diminuição de sua energia de ativação. Como as demais proteínas, são orgânicas e biodegradáveis,
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
Biologia 12 Fermentação e actividade enzimática
 Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
