SFI 5800 Espectroscopia Física. Simetria e Teoria de Grupos
|
|
|
- Washington Caetano Fontes
- 7 Há anos
- Visualizações:
Transcrição
1 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Simetria e Teoria de Grupos Prof. Dr. José Pedro Donoso
2 Simetria molecular e Teoria de Grupos A aplicação de argumentos de simetria a átomos e moléculas começou nos anos 20 e 30, e teve origen na Teoria de Grupos desenvolvida pelos matemáticos no século XIX. Ela constitui uma ferramenta essencial para compreender as propriedades de sistemas atômicos e moleculares. Depois de descrever as propriedades de simetria das moléculas analisaremos o efeito das transformações de simetria sobre os estados (vibracionais e eletrônicos) e veremos que é possível deduzir regras de seleção que governam as transições espectroscópicas. Transições espectroscópicas permtidas e proibidas podem ser identificadas pelos criterios de simetria para que o momento de transição entre os estados inicial e final não seja nulo (regra de seleção)
3 Elementos de simetria Uma operação que deixa a aparência de um corpo inalterada depois de efetuada é uma operação de simetria As operações de simetria típicas são as rotações, as reflexões e as inversões. Para cada operação de simetria há um elemento de simetria correspondente, que é um ponto, uma linha (eixo de simetria) ou um plano, em relação ao qual se faz a operação de simetria Molecular Physics and Elements of Quantum Chemistry. Haken & Wolf
4 Operação de simetria σ A figura mostra o efeito das operações de simetria σ 1, σ 2 e σ 3 (reflexões num plano) num arranjo molecular de simetria triangular
5 A figura mostra o efeito da uma operação C 3 (rotação) seguida de uma operação de simetria σ 2 (reflexão num plano) Molecular Physics and Elements of Quantum Chemistry. Haken & Wolf
6 Rotação em torno de um eixo de simetria Modern Spectroscopy. J.M. Hollas
7 Modern Spectroscopy. J.M. Hollas
8 Espectroscopia Molecular. J.C. Teixeira Dias
9
10
11 Modern Spectroscopy J.M. Hollas
12 Elementos de simetria no CH 4 e no SF 6 Modern Spectroscopy. J.M. Hollas
13 Simetria molecular Físico Química. Atkins & de Paula
14 Tabela de multiplicação do Grupo C 3v Os elementos são obtidos pelo produto dos elementos de simetria. Este produto envolve a aplicação sucessiva das operações. De esta forma é possivel construir uma tabela de multiplicação. O conjunto completo das operações formam um grupo.
15 Exemplo: operações de simetria na molécula de água A molécula de água tem dois planos de simetria. Ambos são verticais (contem o eixo principal) e são simbolizados por σ. O grupo de simetria da molécula tem o elemento identidade (E) e um eixo de simetria C 2 correspondente a uma operação de uma rotação de (2π/2). Por ter planos de simetria verticais, ela pertence ao Grupo C 2v constituido pelos seguintes elementos: C 2 v = { E, C,2 σ } 2 v A ordem do grupo, ou seja o número de seus elementos, é h = 4
16 Exemplo de Grupo pontual H 2 C CH 2 Operações de simetria: C 2, σ, I Grupo pontual: D 2h D 2h = {E, C 2 (x), C 2 (y), C 2 (z), I, σ(x,y), σ(x,z), σ(y,z)} Molecular Physics and Elements of Quantum Chemistry. Haken & Wolf
17 Um Grupo pontual é um grupo de operações de simetria que deixa pelo menos um ponto inalterado. Para classificar as moléculas pelas respectivas simetrias, relacionamos os elementos de simetria que elas possuem e reunimos num grupo todas as moléculas que epresentam esses elementos. Exemplo: Grupo C n : uma molécula pertence a este grupo se tiver um eixo n-ário
18
19 Simetria molecular e grupo pontual Inorganic Chemistry. Shriver & Atkins
20 Inorganic Chemistry. Shriver & Atkins
21 Mais exemplo de grupos pontuais
22 Symmetry and Spectroscopy. Harris & Bertolucci
23 Diagrama para determinação do grupo pontual de simetria de uma molécula A identificação começa pelo reconhecimento dos grupos especiais de elevada simetria (lineares, tetraédricas, octaédricas) A seguir se reconhece se possui ou não algum eixo de simetria. Por ultimo se verifica se a molécula possui um eixo S 2n. Caso não satisfaça, se verifica se ela admite eixos binários perpendiculares. No caso afirmativo ela pertenecerá aos grupos D n, D nh ou D nv. Caso contrario ela pertenecerá aos grupos C n, C nh ou C nv Espectroscopia molecular Jose C. Teixeira Dias
24 Tabelas de caracteres Para dar expressão matemática às operações de simetria é necessário considerar a sua aplicação a vetores e funções. Consideremos a representação matricial das operações de simetria na molécula de água na base de vetores (x, y) E 1 = = = 0 ' C σ ( ) ( yz) = v xz 0 1 σ v A soma dos elementos da diagonal de uma matriz constitui o caracter da matriz (χ) O carater de uma representação é o conjunto dos carateres das matrizes que compõem essa representação. A notação matricial têm grande utilidade na Teoria de Grupos porque é possível decompor uma representação numa soma direta das representações constituidas pelas submatrizes correspondentes. Uma representação indecomponível em outras de menores dimensões se chama representação irredutível.
25 Estrutura das tabelas de caracteres Símbolo do grupo Espécies de simetria operações de simetria Funções base Cada linha corresponde a uma dada representação (espécie). Na espectroscopia vibracional vamos associar cada modo normal de vibração a uma destas espécies, de acordo com suas propriedades de simetria frente as operações do grupo. Na espectroscopia eletrônica se faz o mesmo com os orbitais moleculares. Na mecânica quântica analisamos as propriedades de simetria das funções de onda e dos operadores, e os associamos a especies de simetria de grupo correspondente. Considerando como transforma o operador de uma transição, por exemplo, poderemos identificar quais transições são permitidas e proibidas.
26 Estrutura das tabelas de caracteres Símbolo do grupo Espécies de simetria operações de simetria Funções base Caracteres As representações (espécies) unidimensionais são rotuladas por A e B; as bi-dimensionais por E (não confundir com E : operação identidade) e as tri-dimensionais por T ou F. Na espectroscopia eletrônica usam-se os símbolos Σ, Π,, Φ correspondentes ao numero quântico de momento angular.
27 Símbolo do grupo Espécies de simetria operações de simetria Funções base Caracteres As funções de base resumem as propriedades das tranformação da espécie. Elas podem ser lineares (x, y, z; funções de traslação T x, T y e T z ) ou quadráticas (x 2, y 2, z 2, xy,xz, yz). R x, R y e R z indicam rotações em torno de eixos de simetria.
28 Caracteres χ 1 - Espécies unidimensionais que são simetricas em relação ao eixo de simetria são rotuladas A (carater χ(c n ) = +1). Caso contrario são rotuladas B (χ(c n ) = -1). 2 - Os sub-indices 1 ou 2 referem-se a simetria em relação aos eixos C n ou S n. No grupo C 2v estes sub-índices indicam a simetria em relação ao plano σ(xz). 3 - A simetria em relação ao centro de simetria é indicada pelos sub-índices g (gerade) e u (ungerade) 4 Os carateres da operação identidade (E) revelam a degenerescência da espécie.
29 Símbolo do grupo Espécies de simetria operações de simetria Funções base Caracteres χ 1- As espécies do grupo C 2v são A 1, A 2, B 1 e B 2. A espécie A 1 transforma como z. As espécies B 1 e B 2 transformam como x e y, respectivamente. 2 - A função de base z na linha da espécie A 1 indica que a coordenada z não muda de sinal quando são aplicadas todas as operações de simetria: E, C 2, σ v (xz), σ v (yz) Os carateres, então: χ(e) = +1, χ(c 2 ) = +1, χ(σ v ) = +1 e χ(σ ) = A função de base x na linha da espécie B 1 indica que a coordenada x muda de sinal se é aplicada uma rotação C 2 ou uma reflexão σ (yz): χ(c 2 ) = -1 e χ(σ ) = -1
30 Tabelas de caracteres do grupo C 3v utilizado para descrever a molécula NH 3 As colunas da Tabela identificam as operações de simetria. Os números que multiplicam cada operação sào os números de membros de cada classe. Vemos que as duas rotações C 3 (de 120 o ) pertencem à mesma classe. As três reflexões σ v (uma para cada um dos três planos verticais de simetria) também pertencem à mesma classe.
31 Tabelas de caracteres do grupo C v utilizado para descrever moléculas lineares
32 Exemplo da análise das propriedades de simetria de um orbital atômico Symmetry and Spectroscopy. Harris & Bertolucci
33 Regras de seleção e momentos de transição A interação entre uma molécula e a componente elétrica (oscilante) da radiação eletromagnética, para a absorção ou emissão de um foton de frequência ν, só ocorre se a molécula tiver um dipolo elétrico oscilando na frequência do campo. Na mecânica quântica, isto se expressa em termos do momento de dipolo da transição, M fi M fi = ψ f ˆ µ ψ i = ψ f ˆ µψ dτ i µˆ é o operador momento de dipolo elétrico (na espectroscopia infravermelha e eletrônica) ou o operador polarizabilidade (na espectroscopia Raman) A teoria de perturbações dependente do tempo estabelece que a probabilidade de transição é proporcional a M fi 2. Somente se o momento de transição for diferente de zero a transição contribuirá para o espectro.
34 Espectroscopia infravermelha A regra de seleção para a absorção de radiação por uma vibração molecular é a de que o momento de dipolo elétrico da molécula varie quando os átomos forem deslocados ums em relação aos outros. As vibrações desse tipo são ditas ativas no infravermelho A base da regra é a da geração de um campo eletromagnético oscilante devido à vibração de um dipolo variável, e vice-versa. A regra não impõe a existência de um dipolo permanente, mas somente a variação do momento de dipolo. Algumas vibrações não afetam o momento de dipolo da molécula (por exemplo, a vibração de estiramento de uma molécula diatômica homonuclear), e são chamadas de inativas no infravermelho.
35 Modos normais ativos no infravermelho A probabilidade de transição da molécula de um estado vibracional inicial (função de onda Ψ i ) para um estado final (função de onda Ψ f ) depende do operador momento de dipolo elétrico, de componentes ex, ey e ez. Dizemos então que o operador transforma como as coordenadas x, y, z M x fi = e ψ f xψ dτ i As funções de onda vibracionais tem a simetria dos polinómio de Hermite, ou seja a simetria de uma coordenada. O operador dipolo elétrico transforman como os produtos cartesianos x, y, z. Se a espécie de simetria de um modo normal de vibração tem a espécie de simetria de uma coordenada (x, y, z) esta vibração será ativa no infravermelho. Por tanto, para saber se um dado modo normal é ativo no infravermelho basta observar na tabela de carateres se sua espécie de simetria tem alguma coordenada como função base.
36 Espectroscopia Raman A regra de seleção para a espectroscopia Raman de uma vibração é a de que a polarizabilidade da molécula deve mudar durante a vibração. Moléculas diatômicas Como as moléculas diatômicas homonucleares e heteronucleares se expandem e se contraem durante a vibração, a polarizabilidade da molécula se altera e as vibrações são ativas no Raman. Moléculas poliatômicas Os modos normais de vibração são ativos no Raman se forem acompanhados por mudança na polarizabilidade. Em geral, é necessário o uso da Teoria de Grupos para prever se um modo é ativo no infravermelho ou no Raman. Se a molécula tiver um centro de simetria (i), nenhum modo de vibração pode ser simultaneamente ativo no infravermelho e na espectroscopia Raman.
37 Modos normais ativos no Raman A polarizabilidade α mede a deformação da molécula num campo elétrico E. O momento da transição, M fi é dada por: M fi = v f α ( x) v E i O operador tensorial da polarizabilidade têm seis componentes: α xx, α yy, α zz, α xy, α xz e α yz. Estas componentes transforman como os produtos cartesianos quadráticos (x 2, y 2, z 2, xy, etc.). A Teoria de Grupos proporciona uma regra explícita para analisar a atividade Raman de um modo normal de vibração: se a espécie de simetria de um modo normal tem a espécie de simetria de uma forma quadrática (x 2, y 2, z 2, xy, etc.) essa vibração será Raman ativa. Por tanto, para saber se um dado modo normal de vibração é Raman ativo basta observar na tabela de carateres se sua espécie de simetria tem uma função base de forma quadrática.
38 Simetria dos modos de vibração da molécula de água Número de modos normais de vibração: (3N - 6) = 3 Simetria dos três modos normais (no Grupo C 2v ): E C 2 σ(xz) σ(yz) ν = A 1 ν = A 1 ν = B 2 O modo normal de vibração ν 1 transforma como a espécie A 1 em C 2v, ν 2 também transforma como A 1, e ν 3 transformam como B 2
39 Como a espécie A 1 tem uma coordenada (z) como função base, os modos de vibração ν 1 e ν 2 são ativos no infravermelho. E como B 2 também tem uma coordenada como função base (y) ν 3 também é ativo no infravermelho. Consultando a tabela de carateres de C 2v verificamos que todos os três modos normais da H 2 O também são ativos na espectroscopia Raman (as espécie A 1 e B 2 tem produtos quadráticos como funções base).
40 Modos normais de vibração na molécula de água Banda (cm -1 ) Intensidade very strong medium strong vs m weak Identificação ν 2 (A 1 ) 2ν 2 ν 1 (A 1 ) ν 3 (B 2 ) ν 2 + ν 3 2ν 2 + ν 3 A banda em 5332 cm -1 resulta da combinação ν 2 + ν 3 Espectroscopicamente ν 2 + ν 3 = = cm -1 Verifica-se que A 1 B 2 = B 2, espécie ativa no infravermelho: E C 2 σ(xz) σ(yz) Physical Chemistry Alberty & Silbey A B A 1 B
41 Modos normais de vibração da molécula CH 4 Grupo: T d Graus de liberdade: 3N = 15 Modos normais de vibração: 3N 6 = 9 Operações de simetria: Sob E, nenhuma coordenada se altera, χ(e) = 15 Sob C 3, nenhuma coordenada fica imutável, χ = 0 Sob C 2, as componentes x e y trocam de sinal Sob S 4, a coordenada z do étomo central é invertido, de modo que χ(s 4 ) = -1 Sob σ d, y é invertido
42 Caracteres da representação total: E 8C 3 3C 2 6S 4 6σ d Γ tot A 1 +E+T 1 +3T 2 Translações: Γ tras = T 2 Rotações: Γ rot = T 1 vibrações Γ v = Γ tot - Γ tras - Γ rot = A 1 + E + 2T 2 Consultando a tabela de Carateres verificamos que somente os modos T 2 são ativos no IR. O modo simetrico de respiração A 1 é inativo no IR. Os modos A 1, E e T 2 são todos ativos no Raman. (Ref: Fisico Quimica, Atkins & de Paula)
43 Molécula trans-n 2 F 2 estrutura planar não linear Caracteres da representação total: Γ tot E C 2 i σ h A g +2B g +2A u +4B u Translações e rotações: Γ = A g + 2B g + 2A u + 2B u vibrações Γ v = Γ tot - Γ tras - Γ rot = 3A g + A u + 2B u Consultando a tabela de Carateres verificamos que os modos A u e B u são ativos no Infravermelho. O modo A g é ativo na espectroscopia Raman. Chemical Applications of Group Theory, Cotton
44 Os deslocamentos observados nas bandas ν 4 e ν 1 na amostra deuterada (CDCl 3 ) em relação a CHCl 3 permite identificar estes modos como C-H bending e C-H stretching, respectivamente.
45 Teoria de Grupos Aplicada, Nussbaum
46 CHCl 3 (cloroformio) Grupo de simetria: C 3v Modos normais de vibração: 3N 6 = os seis modos normais de vibração são ativos no infravermelho e na espectroscopia Raman 2 - As bandas ν 1, ν 2 e ν 3 em 3033, 667 e 364 cm -1 correspondem as vibrações totalmente simétricas da espécie A 1, e são Raman polarizadas 3 - As bandas ν 4, ν 5 e ν 6 em 1205, 760 e 260 cm -1 pertencem a espécie E Physical Methods for Chemists, Drago Teoria de Grupos Aplicada, Nussbaum
47 BF 3 (molecula plana) Grupo de simetria: D 3h Modos normais de vibração: 3N 6 = 6
48 BF 3 (molecula plana) Grupo de simetria: D 3h Correspondência modos normal e representação (espécie): A 1 ν 1 A 2 ν 2 E ν 3 e ν 4 Infravermelho : ν 2, ν 3, ν 4 ativas Raman : ν 1, ν 3, ν 4 ativas
49 Modos normais de vibração ativos em IR e Raman Infrared and Raman Spectroscopy, Schrader (ed.)
50 Atividade IR e Raman dos modos normais de vibração Numero de bandas Raman ativas (n R ), Raman polarizadas (n P ), bandas IR ativas (n I ) e bandas coincidentes IR e Raman (n C ). Banda inativa: ia Raman Spectroscopy, Szymanski
51 Bibliografia 1 - Atkins & de Paula, Físico Química. 2 - Haken & Wolf, Molecular Physics and Elements of Quantum Chemistry. 3 - Harris & Bertolucci, Symmetry and Spectroscopy. 4 Nussbaum, Teoria de Grupos Aplicada. 5 Cotton, Chemical Applications of Group Theory. 6 Sala, Fundamentos da espectroscopia Raman e Infravermelha 7 Teixeira Dias, Espectroscopia molecular. 8 Schrader (editor) Infrared and Raman Spectroscopy. Tabelas de Caracteres:
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 14/03/2017 Bibliografia Simetria de moléculas e cristais. Gelson
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 14/03/2017 Bibliografia Simetria de moléculas e cristais. Gelson
Simetria Molecular e Teoria de Grupo. Prof. Fernando R. Xavier
 Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2017 Uma idéia intuitiva... 2 Por que estudar simetria e teoria de grupo? A química estuda íons, moléculas e suas transformações; A química
Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2017 Uma idéia intuitiva... 2 Por que estudar simetria e teoria de grupo? A química estuda íons, moléculas e suas transformações; A química
Espectroscopia Infravermelha: Moléculas
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC Espectroscopia Infravermelha: Moléculas Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha Infravermelho próximo.800 4.000 cm -
Universidade de São Paulo Instituto de Física de São Carlos - IFSC Espectroscopia Infravermelha: Moléculas Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha Infravermelho próximo.800 4.000 cm -
SFI 5800 Espectroscopia Física. Espectroscopia eletrônica: moléculas
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia eletrônica: moléculas Prof. Dr. José Pedro Donoso Espectroscopia Eletrônica 1 - Moléculas
Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia eletrônica: moléculas Prof. Dr. José Pedro Donoso Espectroscopia Eletrônica 1 - Moléculas
Simetria Molecular e Teoria de Grupo. Prof. Fernando R. Xavier
 Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2013 Uma idéia intuitiva... Simetria molecular Por que estudar simetria e teoria de grupo? A química moléculas e suas transformações;
Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2013 Uma idéia intuitiva... Simetria molecular Por que estudar simetria e teoria de grupo? A química moléculas e suas transformações;
Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I ESPECTROSCOPIA VIBRACIONAL. Prof. Dr. João Batista Marques Novo
 Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I ESPECTROSCOPIA VIBRACIONAL Determinação das simetrias dos modos normais de vibração Prof. Dr. João
Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I ESPECTROSCOPIA VIBRACIONAL Determinação das simetrias dos modos normais de vibração Prof. Dr. João
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química
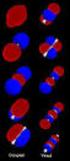 Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Simetria molecular e teoria de grupos
 Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA FUNDAMENTAL I
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA FUNDAMENTAL I Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br Sala GQI 308, Ramal 2170
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA FUNDAMENTAL I Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br Sala GQI 308, Ramal 2170
SFI 5800 Espectroscopia Física. Espectroscopia de Microondas
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia de Microondas Prof. Dr. José Pedro Donoso Espectroscopia de microondas Gama de frequência:
Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia de Microondas Prof. Dr. José Pedro Donoso Espectroscopia de microondas Gama de frequência:
Simetria molecular e teoria de grupos
 Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS
 Quim Nova, Vol 3, No 6, S1-S, 2012 ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II: UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr, Juliana dos Santos de Souza, Paula Homem-de-Mello,
Quim Nova, Vol 3, No 6, S1-S, 2012 ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II: UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr, Juliana dos Santos de Souza, Paula Homem-de-Mello,
Caracterização da disciplina. Turma: Turno: Quadrimestre: Ano: turma: Docente(s) responsável(is): Hueder Paulo Moisés de Oliveira
 Caracterização da disciplina Código da NHT4007.14 Nome da Espectroscopia disciplina: disciplina: Créditos (T-P- I): (4-2-6) Carga horária: 72 horas Aula prática: Câmpus: SA Código da Turma: Turno: Quadrimestre:
Caracterização da disciplina Código da NHT4007.14 Nome da Espectroscopia disciplina: disciplina: Créditos (T-P- I): (4-2-6) Carga horária: 72 horas Aula prática: Câmpus: SA Código da Turma: Turno: Quadrimestre:
Simetria e Teoria de Grupo. Profa. Célia Machado Ronconi
 Simetria e Teoria de Grupo Profa. Célia Machado Ronconi cmronconi@id.uff.br 1 Sabemos intuitivamente quando algo é simétrico. 2 Hemoglobina Cadeia polipeptídica Hemoglobina Grupo hemo contendo Fe 3 Simetria
Simetria e Teoria de Grupo Profa. Célia Machado Ronconi cmronconi@id.uff.br 1 Sabemos intuitivamente quando algo é simétrico. 2 Hemoglobina Cadeia polipeptídica Hemoglobina Grupo hemo contendo Fe 3 Simetria
Instituto de Física de São Carlos - USP Lista 1 1-Espectroscopia atómica : revisão não 2 - Regiões espectrais
 Instituto de Física de São Carlos - USP SFI 5800 Espectroscopia Física SCM 5770 Caracterização de Materiais por Técnicas de Espectroscopia Prof. Dr. José Pedro Donoso (010) Lista 1 1-Espectroscopia atómica
Instituto de Física de São Carlos - USP SFI 5800 Espectroscopia Física SCM 5770 Caracterização de Materiais por Técnicas de Espectroscopia Prof. Dr. José Pedro Donoso (010) Lista 1 1-Espectroscopia atómica
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 21/03/2017 Espectroscopia no infravermelho ACIK, M., LEE, G.,
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 21/03/2017 Espectroscopia no infravermelho ACIK, M., LEE, G.,
Bibliografia. Universidade de São Paulo Instituto de Física de São Carlos - IFSC
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física SCM5770 - Caracterização de Materiais por Técnicas de Espectroscopia Bibliografia Prof. Dr. José Pedro
Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física SCM5770 - Caracterização de Materiais por Técnicas de Espectroscopia Bibliografia Prof. Dr. José Pedro
ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS
 Quim. Nova, Vol. 35, No. 6, 12641270, 2012 Educação ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr., Juliana dos Santos de
Quim. Nova, Vol. 35, No. 6, 12641270, 2012 Educação ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr., Juliana dos Santos de
Caracterização da disciplina. Turma: Turno: Diurno/Noturno Quadrimestre: 3 Ano:2018 turma: Docente(s)
 Caracterização da disciplina Código da NHT4007- Nome da Espectroscopia disciplina: 15 disciplina: Créditos (T- P-I): (4-2-6) Carga horária: 72 horas Aula prática: Câmpus: SA Código da Turma: Turno: Diurno/Noturno
Caracterização da disciplina Código da NHT4007- Nome da Espectroscopia disciplina: 15 disciplina: Créditos (T- P-I): (4-2-6) Carga horária: 72 horas Aula prática: Câmpus: SA Código da Turma: Turno: Diurno/Noturno
Espectroscopia Vibracional
 Espectroscopia Vibracional Infravermelho (IV) Difusão de Raman (R) Vibrações moleculares Transições vibracionais Região do Infravermelho 12820 4000 400 Número de onda (cm -1 ) 33 IVP IVM IVL IVP IV próximo;
Espectroscopia Vibracional Infravermelho (IV) Difusão de Raman (R) Vibrações moleculares Transições vibracionais Região do Infravermelho 12820 4000 400 Número de onda (cm -1 ) 33 IVP IVM IVL IVP IV próximo;
Questão 01 - Em qual região do espectro você encontraria uma banda C=C?
 Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Diretoria de Graduação e Educação Profissional Departamento Acadêmico de Química e Biologia Segunda Lista de Exercícios
Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Diretoria de Graduação e Educação Profissional Departamento Acadêmico de Química e Biologia Segunda Lista de Exercícios
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos.
 Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Espectroscopia no infravermelho ACIK, M., LEE, G., MATTEVI, C., CHHOWALLA,
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Espectroscopia no infravermelho ACIK, M., LEE, G., MATTEVI, C., CHHOWALLA,
Teoria do Campo Ligante. Prof. Fernando R. Xavier
 Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2017 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregada ainda
Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2017 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregada ainda
Molécula de água. σ v : σ v ': 0 1. (h 1 +h 2 ) (h 1 +h 2 ) (h 1 +h 2 ) (h 1 +h 2 ) (h 1 +h 2 ) (h 1 h 2 ) (h 1 h 2 ) (h 1 h 2 ) (h 1 h 2 ) (h 1 h 2 )
 Orientação da molécula: H 2 Elementos de simetria: C 2 = z σ v = plano z σ v ' = plano z Aplicação das operações de simetria sobre os orbitais do átomo de O: 2p z (O) 2p z (O) 2p z (O) 2p z (O) 2p z (O)
Orientação da molécula: H 2 Elementos de simetria: C 2 = z σ v = plano z σ v ' = plano z Aplicação das operações de simetria sobre os orbitais do átomo de O: 2p z (O) 2p z (O) 2p z (O) 2p z (O) 2p z (O)
Física para Ciências Biológicas Lista de Exercícios 5 - CASA Data: 22/05/2014
 Física para Ciências Biológicas - 2014 Lista de Exercícios 5 - CASA Data: 22/05/2014 1. Abaixo representamos a energia de interação dos átomos de K e Cl em função da distância interatômica. A energia de
Física para Ciências Biológicas - 2014 Lista de Exercícios 5 - CASA Data: 22/05/2014 1. Abaixo representamos a energia de interação dos átomos de K e Cl em função da distância interatômica. A energia de
Molécula de água C 2 : ( σ v : σ v ': ( 0 1 1
 CQ832 - moléculas poliatômicas Prof. Dr. Flávio M. Matsumoto 1 Orientação da molécula: z O H 2 Elementos de simetria: H 1 C 2 = z σ v = plano z σ v ' = plano z Molécula de água Aplicação das operações
CQ832 - moléculas poliatômicas Prof. Dr. Flávio M. Matsumoto 1 Orientação da molécula: z O H 2 Elementos de simetria: H 1 C 2 = z σ v = plano z σ v ' = plano z Molécula de água Aplicação das operações
Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I. Prof. Dr. João Batista Marques Novo
 Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS I a PARTE: TEORIA DE GRUPOS Prof. Dr. João Batista Marques Novo ÍNDICE Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS
Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS I a PARTE: TEORIA DE GRUPOS Prof. Dr. João Batista Marques Novo ÍNDICE Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS
Molécula de água. σ v : σ v ': ( 0 1
 QUIM7031 - moléculas poliatômicas Prof Dr Flávio M Matsumoto - 1 Molécula de água Orientação da molécula z O H 2 H 1 Aplicação das operações de simetria, em notação matricial E: 0 1( h 1 h 2 = ( h 1 h
QUIM7031 - moléculas poliatômicas Prof Dr Flávio M Matsumoto - 1 Molécula de água Orientação da molécula z O H 2 H 1 Aplicação das operações de simetria, em notação matricial E: 0 1( h 1 h 2 = ( h 1 h
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 24 Prof. Dr. Anselmo E de Oliveira
Físico-Química Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 24 Prof. Dr. Anselmo E de Oliveira
Teoria do Campo Ligante. Prof. Fernando R. Xavier
 Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2014 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregrada ainda
Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2014 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregrada ainda
Problemas de Química-Física 20015/2016
 Problemas de Química-Física 0015/016 Capítulo 5 - Espectroscopia Rotacional, Vibracional, Rotovibracional e Electrónica 1 O espectro rotacional da molécula 1 C 3 S tem as seguintes riscas (em MHz): Risca
Problemas de Química-Física 0015/016 Capítulo 5 - Espectroscopia Rotacional, Vibracional, Rotovibracional e Electrónica 1 O espectro rotacional da molécula 1 C 3 S tem as seguintes riscas (em MHz): Risca
Raios atômicos Física Moderna 2 Aula 6
 Raios atômicos 1 2 8 8 18 18 32 2 Energias de ionização 3 Espectros de R-X A organização da tabela periódica reflete a distribuição dos e - nas camadas mais externas dos átomos. No entanto, é importante
Raios atômicos 1 2 8 8 18 18 32 2 Energias de ionização 3 Espectros de R-X A organização da tabela periódica reflete a distribuição dos e - nas camadas mais externas dos átomos. No entanto, é importante
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
3 Espectroscopia Molecular
 3 Espectroscopia Molecular 3.1. Aspectos gerais Todos os espectros se devem às transições entre estados de energia. A espectroscopia molecular fornece o valor da variação da energia interna quando uma
3 Espectroscopia Molecular 3.1. Aspectos gerais Todos os espectros se devem às transições entre estados de energia. A espectroscopia molecular fornece o valor da variação da energia interna quando uma
SFI 5800 Espectroscopia Física Espectroscopia Infravermelha: sólidos
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia Infravermelha: sólidos Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha : sólidos
Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia Infravermelha: sólidos Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha : sólidos
Teoria de Grupos e Simetria Cristalina
 Teoria de Grupos e Simetria Cristalina Teorema de Bloch Tiago de Campos Resumo Neste texto serão apresentados conceitos fundamentais para o entendimento de estruturas cristalinas bem como suas simetrias.
Teoria de Grupos e Simetria Cristalina Teorema de Bloch Tiago de Campos Resumo Neste texto serão apresentados conceitos fundamentais para o entendimento de estruturas cristalinas bem como suas simetrias.
Espectroscopia no IV
 Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Geometria Molecular e polaridade de ligações
 Geometria Molecular e polaridade de ligações Prof. Éderson Química Geometria Molecular Geometria molecular O arranjo tri-dimensional dos átomos em uma molécula, ou seja, é a orientação espacial das moléculas,
Geometria Molecular e polaridade de ligações Prof. Éderson Química Geometria Molecular Geometria molecular O arranjo tri-dimensional dos átomos em uma molécula, ou seja, é a orientação espacial das moléculas,
SFI 5800 Espectroscopia Física. Espectroscopia Fotoeletrônica: UPS, XPS (ESCA) e Auger
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia Fotoeletrônica: UPS, XPS (ESCA) e Auger Prof. Dr. José Pedro Donoso Espectroscopia Fotoeletrônica
Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Espectroscopia Fotoeletrônica: UPS, XPS (ESCA) e Auger Prof. Dr. José Pedro Donoso Espectroscopia Fotoeletrônica
Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA. Eliana Midori Sussuchi Danilo Oliveira Santos
 Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA META Aplicar os conceitos de mecânica quântica aos orbitais atômicos; Descrever a distribuição dos elétrons nos átomos. OBJETIVOS Ao final desta aula,
Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA META Aplicar os conceitos de mecânica quântica aos orbitais atômicos; Descrever a distribuição dos elétrons nos átomos. OBJETIVOS Ao final desta aula,
Interações do CS 2 com solventes moleculares
 UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química JENNIFER DAYANA ROZENDO DE LIMA Interações do CS 2 com solventes moleculares Versão original corrigida da dissertação
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química JENNIFER DAYANA ROZENDO DE LIMA Interações do CS 2 com solventes moleculares Versão original corrigida da dissertação
Interações Atômicas e Moleculares
 Interações Atômicas e Moleculares Código da disciplina: BCK0104-15 (antes: BC0104) TPI: 3-0-4. Carga Horária: 36hs. Coordenador: Prof. Dr. Alexsandre F. Lago Ementa resumida: Fundamentos de mecânica-quântica
Interações Atômicas e Moleculares Código da disciplina: BCK0104-15 (antes: BC0104) TPI: 3-0-4. Carga Horária: 36hs. Coordenador: Prof. Dr. Alexsandre F. Lago Ementa resumida: Fundamentos de mecânica-quântica
Problemas de Duas Partículas
 Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Interações Atômicas e Moleculares
 Interações Atômicas e Moleculares 6. O Princípio Variacional Prof. Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/iam.html Na aula anterior, tratando de moléculas
Interações Atômicas e Moleculares 6. O Princípio Variacional Prof. Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/iam.html Na aula anterior, tratando de moléculas
2.1.2 Ligação covalente
 2.1.2 Ligação covalente Adaptado pelo Prof. Luís Perna Ligações covalentes Quando a partilha de eletrões é significativa e localizada entre átomos denomina-se de ligação covalente. Nem todos os átomos
2.1.2 Ligação covalente Adaptado pelo Prof. Luís Perna Ligações covalentes Quando a partilha de eletrões é significativa e localizada entre átomos denomina-se de ligação covalente. Nem todos os átomos
Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares
 Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares 1) Construa os orbitais moleculares para H 2 O e NO 2 baseado nos SALCs de
Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares 1) Construa os orbitais moleculares para H 2 O e NO 2 baseado nos SALCs de
Universidade Federal de Viçosa Centro de Ciências Exatas e Tecnológicas Departamento de Matemática
 1 Universidade Federal de Viçosa Centro de Ciências Exatas e Tecnológicas Departamento de Matemática 3 a Lista - MAT 137 - Introdução à Álgebra Linear 2017/II 1. Sejam u = ( 4 3) v = (2 5) e w = (a b).
1 Universidade Federal de Viçosa Centro de Ciências Exatas e Tecnológicas Departamento de Matemática 3 a Lista - MAT 137 - Introdução à Álgebra Linear 2017/II 1. Sejam u = ( 4 3) v = (2 5) e w = (a b).
Instituto de Física USP. Física V - Aula 18. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 18 Professora: Mazé Bechara Aula 28 Discussão da 1ª prova e Apresentação do Tópico III 1. Soluções das questões da prova com comentários. Critérios de correção.
Instituto de Física USP Física V - Aula 18 Professora: Mazé Bechara Aula 28 Discussão da 1ª prova e Apresentação do Tópico III 1. Soluções das questões da prova com comentários. Critérios de correção.
(x 1, y 1 ) (x 2, y 2 ) = (x 1 x 2, y 1 y 2 ); e α (x, y) = (x α, y α ), α R.
 INSTITUTO DE MATEMÁTICA E ESTATÍSTICA UNIVERSIDADE DE SÃO PAULO MAT-2457 Álgebra Linear para Engenharia I Terceira Lista de Exercícios - Professor: Equipe da Disciplina EXERCÍCIOS 1. Considere as retas
INSTITUTO DE MATEMÁTICA E ESTATÍSTICA UNIVERSIDADE DE SÃO PAULO MAT-2457 Álgebra Linear para Engenharia I Terceira Lista de Exercícios - Professor: Equipe da Disciplina EXERCÍCIOS 1. Considere as retas
Mais um exemplo e as dificuldades inerentes a uma teoria "incompleta"
 Mais um exemplo e as dificuldades inerentes a uma teoria "incompleta" Pense: Qual seria a estrutura de Lewis para a molécula de H 2 SO 3? Qual deve ser a geometria desta molécula com base no modelo da
Mais um exemplo e as dificuldades inerentes a uma teoria "incompleta" Pense: Qual seria a estrutura de Lewis para a molécula de H 2 SO 3? Qual deve ser a geometria desta molécula com base no modelo da
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II ONDAS. Prof.
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II ONDAS Prof. Bruno Farias Ondas Uma onda surge quando um sistema é deslocado de sua posição
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II ONDAS Prof. Bruno Farias Ondas Uma onda surge quando um sistema é deslocado de sua posição
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química
 UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química QUÍMICA DE COORDENAÇÃO AVANÇADA QFL5825 ECTOR AGUILAR VITORINO Número USP: 7774685 São Paulo 26/9/2 QFL-5825 Química
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química QUÍMICA DE COORDENAÇÃO AVANÇADA QFL5825 ECTOR AGUILAR VITORINO Número USP: 7774685 São Paulo 26/9/2 QFL-5825 Química
Espectroscopia no Infravermelho (IR)
 Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA CURSO DE BACHARELADO EM QUÍMICA TECNOLÓGICA
 UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA CURSO DE BACHARELADO EM QUÍMICA TECNOLÓGICA GUSTAVO JULIANI COSTA AUTOMATIZAÇÃO DO USO DE SIMETRIA NO PROGRAMA PLACZEK,
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA CURSO DE BACHARELADO EM QUÍMICA TECNOLÓGICA GUSTAVO JULIANI COSTA AUTOMATIZAÇÃO DO USO DE SIMETRIA NO PROGRAMA PLACZEK,
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
Oswaldo Sala Departamento de Química Fundamental, Universidade de São Paulo, CP 26077, São Paulo - SP
 Quim. Nova, Vol. 31, No. 4, 914-920, 2008 - UMA MOLÉCULA DIDÁTICA Educação Oswaldo Sala Departamento de Química Fundamental, Universidade de São Paulo, CP 26077, 05513-970 São Paulo - SP Recebido em 14/6/07;
Quim. Nova, Vol. 31, No. 4, 914-920, 2008 - UMA MOLÉCULA DIDÁTICA Educação Oswaldo Sala Departamento de Química Fundamental, Universidade de São Paulo, CP 26077, 05513-970 São Paulo - SP Recebido em 14/6/07;
ASPECTOS GERAIS. Prof. Harley P. Martins filho
 /6/08 ASPECTOS GERAIS Prof. Harley P. Martins filho Aspectos Gerais Espectroscopia por emissão: Abaixamento de energia de um sistema de um nível permitido para outro, com emissão da energia perdida na
/6/08 ASPECTOS GERAIS Prof. Harley P. Martins filho Aspectos Gerais Espectroscopia por emissão: Abaixamento de energia de um sistema de um nível permitido para outro, com emissão da energia perdida na
Resumo dos pontos importantes
 Resumo dos pontos importantes Equação básica da espectroscopia de RMN. γ X o ν X = B (1 σ X ) π Espectros de RMN e deslocamentos químicos. v X ν ref 6 δ ( ppm) = 10 ν ref 2 δ ( Hz) = δ ( ppm) ν 10 = 6
Resumo dos pontos importantes Equação básica da espectroscopia de RMN. γ X o ν X = B (1 σ X ) π Espectros de RMN e deslocamentos químicos. v X ν ref 6 δ ( ppm) = 10 ν ref 2 δ ( Hz) = δ ( ppm) ν 10 = 6
Universidade Federal de Sergipe. Inorgânica Avançada
 Universidade Federal de Sergipe Departamento de Pós-Graduação em Química Inorgânica Avançada Deyvisson da Mota Santos Química de Coordenação A TOM Aplicada a Complexos Teoria do Campo Cristalino A TCC,
Universidade Federal de Sergipe Departamento de Pós-Graduação em Química Inorgânica Avançada Deyvisson da Mota Santos Química de Coordenação A TOM Aplicada a Complexos Teoria do Campo Cristalino A TCC,
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. FÍSICA PARA CIÊNCIAS BIOLÓGIAS.
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. FÍSICA PARA CIÊNCIAS BIOLÓGIAS. ASPECTOS FÍSICO-QUÍMICOS DA ABSORÇÃO DE ENERGIA SOLAR NA FOTOSSÍNTESE. Professor: Thomas Braun. Graduando: Carlos Santos Costa.
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. FÍSICA PARA CIÊNCIAS BIOLÓGIAS. ASPECTOS FÍSICO-QUÍMICOS DA ABSORÇÃO DE ENERGIA SOLAR NA FOTOSSÍNTESE. Professor: Thomas Braun. Graduando: Carlos Santos Costa.
Simetrias na Mecânica Quântica
 Simetrias na Mecânica Quântica Prof. 26 de maio de 2010 Definição de Simetria na Mecânica Quântica G(a) elemento de um grupo G de transformações contínuas, ˆT(G(a)) operador unitário. G(a) M.Q. ˆT(G(a)),
Simetrias na Mecânica Quântica Prof. 26 de maio de 2010 Definição de Simetria na Mecânica Quântica G(a) elemento de um grupo G de transformações contínuas, ˆT(G(a)) operador unitário. G(a) M.Q. ˆT(G(a)),
Click to edit Master title style
 Teoria das orbitais moleculares (TOM) Contrariamente à TEV, esta teoria assume que os electrões que fazem a ligação não estão de facto localizados em determinada ligação mas pertencem à molécula como um
Teoria das orbitais moleculares (TOM) Contrariamente à TEV, esta teoria assume que os electrões que fazem a ligação não estão de facto localizados em determinada ligação mas pertencem à molécula como um
1. Considere a seguinte matriz dos vértices dum triângulo D = 0 2 3
 INSTITUTO SUPERIOR TÉCNICO - DEPARTAMENTO DE MATEMÁTICA 7 a LISTA DE PROBLEMAS E EXERCÍCIOS DE ÁLGEBRA LINEAR LEIC-Taguspark, LERCI, LEGI, LEE 1 o semestre 2006/07 - aulas práticas de 2006-12-04 e 2006-12-06
INSTITUTO SUPERIOR TÉCNICO - DEPARTAMENTO DE MATEMÁTICA 7 a LISTA DE PROBLEMAS E EXERCÍCIOS DE ÁLGEBRA LINEAR LEIC-Taguspark, LERCI, LEGI, LEE 1 o semestre 2006/07 - aulas práticas de 2006-12-04 e 2006-12-06
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Como Entender a Física Quântica em 8 Passos! Passos
 Como Entender a Física Quântica em 8 Passos! A física quântica (também chamada de teoria quântica ou mecânica quântica) é um ramo da física que permite uma descrição do comportamento e interação da matéria
Como Entender a Física Quântica em 8 Passos! A física quântica (também chamada de teoria quântica ou mecânica quântica) é um ramo da física que permite uma descrição do comportamento e interação da matéria
Espectro Vibracional do Iodo na Região do Visível: Uma Alternativa ao Uso da Espectroscopia RAMAN
 Artigo Espectro Vibracional do Iodo na Região do Visível: Uma Alternativa ao Uso da Espectroscopia RAMAN Santos, V. P.* Rev. Virtual Quim., 04, 6 (4), 898-90. Data de publicação na Web: 0 de maio de 04
Artigo Espectro Vibracional do Iodo na Região do Visível: Uma Alternativa ao Uso da Espectroscopia RAMAN Santos, V. P.* Rev. Virtual Quim., 04, 6 (4), 898-90. Data de publicação na Web: 0 de maio de 04
Métodos de RMN no estado sólido
 Métodos de RMN no estado sólido Jair C. C. Freitas Programa de Pós-graduação em Física UFES Programa de Pós-graduação em Química - UFES Sumário Interações de spin nuclear: Hamiltoniano de spin nuclear.
Métodos de RMN no estado sólido Jair C. C. Freitas Programa de Pós-graduação em Física UFES Programa de Pós-graduação em Química - UFES Sumário Interações de spin nuclear: Hamiltoniano de spin nuclear.
Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO
 Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos
Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos
Átomo de Hélio. Tiago Santiago. 2 de novembro de Resumo
 Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
ESPECTROSCOPIA DE RESSONANCIA MAGNÉTICA NUCLEAR
 ESPECTROSCOPIA DE RESSONANCIA MAGNÉTICA NUCLEAR Histórico 1924: W. Pauli descreveu a base teórica da RMN; 1946: Bloch (Stanford) e Purcell (Harvard) demonstraram a teoria de absorção de radiação eletromagnética
ESPECTROSCOPIA DE RESSONANCIA MAGNÉTICA NUCLEAR Histórico 1924: W. Pauli descreveu a base teórica da RMN; 1946: Bloch (Stanford) e Purcell (Harvard) demonstraram a teoria de absorção de radiação eletromagnética
Ligações Químicas - II. Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
 Ligações Químicas - II Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares 1 Revisão: Estruturas de Lewis G.N. Lewis (~1916) Representação das ligações químicas Compartilhamento
Ligações Químicas - II Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares 1 Revisão: Estruturas de Lewis G.N. Lewis (~1916) Representação das ligações químicas Compartilhamento
Análise de alimentos II Introdução aos Métodos Espectrométricos
 Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
SFI 5800 Espectroscopia Física. Infravermelho distante (FIR)
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Infravermelho distante (FIR) Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha Infravermelho perto
Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Infravermelho distante (FIR) Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha Infravermelho perto
P4 de Álgebra Linear I de junho de 2005 Gabarito
 P4 de Álgebra Linear I 25.1 15 de junho de 25 Gabarito 1) Considere os pontos A = (1,, 1), B = (2, 2, 4), e C = (1, 2, 3). (1.a) Determine o ponto médio M do segmento AB. (1.b) Determine a equação cartesiana
P4 de Álgebra Linear I 25.1 15 de junho de 25 Gabarito 1) Considere os pontos A = (1,, 1), B = (2, 2, 4), e C = (1, 2, 3). (1.a) Determine o ponto médio M do segmento AB. (1.b) Determine a equação cartesiana
Teoria dos Orbitais Moleculares. Prof. Fernando R. Xavier
 Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
SEMINÁRIO As simetrias dos orbitais: Construção dos orbitais moleculares, exemplos e aplicações
 UNIVERSIDADE FEDERAL DE SERGIPE CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIAS DEPARTAMENTO DE QUÍMICA NPGQ SEMINÁRIO As simetrias dos orbitais: Construção dos orbitais moleculares, exemplos e aplicações Isaac
UNIVERSIDADE FEDERAL DE SERGIPE CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIAS DEPARTAMENTO DE QUÍMICA NPGQ SEMINÁRIO As simetrias dos orbitais: Construção dos orbitais moleculares, exemplos e aplicações Isaac
Conceitos de vetores. Decomposição de vetores
 Conceitos de vetores. Decomposição de vetores 1. Introdução De forma prática, o conceito de vetor pode ser bem assimilado com auxílio da representação matemática de grandezas físicas. Figura 1.1 Grandezas
Conceitos de vetores. Decomposição de vetores 1. Introdução De forma prática, o conceito de vetor pode ser bem assimilado com auxílio da representação matemática de grandezas físicas. Figura 1.1 Grandezas
6. Verifique detalhadamente que os seguintes conjuntos são espaços vetoriais(com a soma e produto por escalar usuais):
 a Lista. Sejam u = ( 4 ) v = ( 5) e w = (a b). Encontre a e b tais que (a)w = u + v (b)w = 5v (c)u + w = u v. Represente os vetores acima no plano cartesiano.. Sejam u = (4 ) v = ( 4) e w = (a b c). Encontre
a Lista. Sejam u = ( 4 ) v = ( 5) e w = (a b). Encontre a e b tais que (a)w = u + v (b)w = 5v (c)u + w = u v. Represente os vetores acima no plano cartesiano.. Sejam u = (4 ) v = ( 4) e w = (a b c). Encontre
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Dr. Tiago P. Camargo. Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia
 Dr. Tiago P. Camargo Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Teoria de ligação de Valência - TLV Como fica a hibridização do oxygênio em O 2? Falhas na TLV
Dr. Tiago P. Camargo Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Teoria de ligação de Valência - TLV Como fica a hibridização do oxygênio em O 2? Falhas na TLV
Teorias de Ligação. Teoria da Ligação de Valência. Ligações s e p Hibridização de orbitais Ligações dos hidrocarbonetos
 Teorias de Ligação Ligações s e p Hibridização de orbitais Ligações dos hidrocarbonetos Orbitais e Teorias de Ligação Estruturas de Lewis Elétrons localizados? Elétrons de valência responsáveis pelas ligações
Teorias de Ligação Ligações s e p Hibridização de orbitais Ligações dos hidrocarbonetos Orbitais e Teorias de Ligação Estruturas de Lewis Elétrons localizados? Elétrons de valência responsáveis pelas ligações
Cinemática da partícula fluida
 Cinemática da partícula fluida J. L. Baliño Escola Politécnica - Universidade de São Paulo Apostila de aula 2017, v.1 Cinemática da partícula fluida 1 / 16 Sumário 1 Descrição do movimento 2 Cinemática
Cinemática da partícula fluida J. L. Baliño Escola Politécnica - Universidade de São Paulo Apostila de aula 2017, v.1 Cinemática da partícula fluida 1 / 16 Sumário 1 Descrição do movimento 2 Cinemática
Teoria da Ligação Covalente. Teoria da Ligação de Valência (TLV)
 Teoria da Ligação Covalente Teoria da Ligação de Valência (TLV) Teoria da Ligação Covalente Teorias de Lewis e VSEPR identificam: - Pares de elétrons ligados - Pares de elétrons isolados - Forma molecular
Teoria da Ligação Covalente Teoria da Ligação de Valência (TLV) Teoria da Ligação Covalente Teorias de Lewis e VSEPR identificam: - Pares de elétrons ligados - Pares de elétrons isolados - Forma molecular
Material Teórico - Módulo: Vetores em R 2 e R 3. Produto Vetorial. Terceiro Ano - Médio
 Material Teórico - Módulo: Vetores em R 2 e R 3 Produto Vetorial Terceiro Ano - Médio Autor: Prof. Angelo Papa Neto Revisor: Prof. Antonio Caminha M. Neto Nesta aula, estudaremos uma operação definida
Material Teórico - Módulo: Vetores em R 2 e R 3 Produto Vetorial Terceiro Ano - Médio Autor: Prof. Angelo Papa Neto Revisor: Prof. Antonio Caminha M. Neto Nesta aula, estudaremos uma operação definida
MINISTÉRIO DA EDUCAÇÃO E DO DESPORTO UNIVERSIDADE FEDERAL DE VIÇOSA DEPARTAMENTO DE MATEMÁTICA
 MINISTÉRIO DA EDUCAÇÃO E DO DESPORTO UNIVERSIDADE FEDERAL DE VIÇOSA DEPARTAMENTO DE MATEMÁTICA 1 a LISTA DE EXERCÍCIOS DE MAT 17 1. Suponha que uma força de 1 newtons é aplicada em um objeto ao longo do
MINISTÉRIO DA EDUCAÇÃO E DO DESPORTO UNIVERSIDADE FEDERAL DE VIÇOSA DEPARTAMENTO DE MATEMÁTICA 1 a LISTA DE EXERCÍCIOS DE MAT 17 1. Suponha que uma força de 1 newtons é aplicada em um objeto ao longo do
Química Inorgânica Avançada
 Química Inorgânica Avançada Prof. Dr. Antônio Reinaldo Cestari Discente: Érika Barbosa SÃO CRISTÓVÃO-SE 04 DE NOVEMBRO DE 2014 1 Espectros eletrônicos de complexos. 2 A espectroscopia eletrônica, decorre
Química Inorgânica Avançada Prof. Dr. Antônio Reinaldo Cestari Discente: Érika Barbosa SÃO CRISTÓVÃO-SE 04 DE NOVEMBRO DE 2014 1 Espectros eletrônicos de complexos. 2 A espectroscopia eletrônica, decorre
Estrutura atômica. Modelo quântico do átomo
 Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
(2008/2009) Espaços vectoriais. Matemática 1º Ano - 1º Semestre 2008/2009. Mafalda Johannsen
 Espaços vectoriais Matemática 1º Ano 1º Semestre 2008/2009 Capítulos Características de um Espaço Vectorial Dimensão do Espaço Subespaço Vectorial Combinação Linear de Vectores Representação de Vectores
Espaços vectoriais Matemática 1º Ano 1º Semestre 2008/2009 Capítulos Características de um Espaço Vectorial Dimensão do Espaço Subespaço Vectorial Combinação Linear de Vectores Representação de Vectores
Aula 7 TEORIA DO ORBITAL MOLECULAR. Eliana Midori Sussuchi Danilo Oliveira Santos
 Aula 7 TEORIA DO ORBITAL MOLECULAR META Discutir os fundamentos da ligação covalente sob a óptica da Teoria do Orbital Molecular (TOM). OBJETIVOS Ao final desta aula, o aluno deverá: Definir os princípios
Aula 7 TEORIA DO ORBITAL MOLECULAR META Discutir os fundamentos da ligação covalente sob a óptica da Teoria do Orbital Molecular (TOM). OBJETIVOS Ao final desta aula, o aluno deverá: Definir os princípios
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
Capítulo Equações da reta no espaço. Sejam A e B dois pontos distintos no espaço e seja r a reta que os contém. Então, P r existe t R tal que
 Capítulo 11 1. Equações da reta no espaço Sejam A e B dois pontos distintos no espaço e seja r a reta que os contém. Então, P r existe t R tal que AP = t AB Fig. 1: Reta r passando por A e B. Como o ponto
Capítulo 11 1. Equações da reta no espaço Sejam A e B dois pontos distintos no espaço e seja r a reta que os contém. Então, P r existe t R tal que AP = t AB Fig. 1: Reta r passando por A e B. Como o ponto
A Dualidade Onda-Partícula
 A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
n, l, m l, ms (1) quando estes quatro números quânticos são dados, o estado físico do sistema (no caso, um elétron) é então especificado.
 Introdução. Consideramos nos textos anteriores sistemas quantum mecânicos que possuem vários níveis de energia mas somente um elétron orbital, ou seja, consideramos até o presente momento átomos hidrogenóides.
Introdução. Consideramos nos textos anteriores sistemas quantum mecânicos que possuem vários níveis de energia mas somente um elétron orbital, ou seja, consideramos até o presente momento átomos hidrogenóides.
Aula Orientação do espaço. Observação 1
 Aula 14 Nesta aula vamos definir dois novos produtos entre vetores do espaço, o produto vetorial e o produto misto. Para isso, primeiro vamos apresentar o conceito de orientação. 1. Orientação do espaço
Aula 14 Nesta aula vamos definir dois novos produtos entre vetores do espaço, o produto vetorial e o produto misto. Para isso, primeiro vamos apresentar o conceito de orientação. 1. Orientação do espaço
Notas de Aula Disciplina Matemática Tópico 03 Licenciatura em Matemática Osasco -2010
 1. Funções : Definição Considere dois sub-conjuntos A e B do conjunto dos números reais. Uma função f: A B é uma regra que define uma relação entre os elementos de A e B, de tal forma que a cada elemento
1. Funções : Definição Considere dois sub-conjuntos A e B do conjunto dos números reais. Uma função f: A B é uma regra que define uma relação entre os elementos de A e B, de tal forma que a cada elemento
Estruturas de Lewis. Ligação química partilha de pares de electrões. 5 B 2He. 3 Li. Átomos em moléculas última camada completamente preenchida
 Estruturas de Lewis Átomos em moléculas última camada completamente preenchida Ligação química partilha de pares de electrões Grupo 2 3 4 5 6 7 8 Nº e - s 2 3 4 5 6 7 8 H 4 Be 0 6 C 7 N 8 O 9 F Ne 3 Li
Estruturas de Lewis Átomos em moléculas última camada completamente preenchida Ligação química partilha de pares de electrões Grupo 2 3 4 5 6 7 8 Nº e - s 2 3 4 5 6 7 8 H 4 Be 0 6 C 7 N 8 O 9 F Ne 3 Li
