UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA FUNDAMENTAL I
|
|
|
- João Gabriel Borja Porto
- 6 Há anos
- Visualizações:
Transcrição
1 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA FUNDAMENTAL I Prof. Fabio da Silva Miranda miranda@vm.uff.br Sala GQI 308, Ramal
2 2
3 3
4 4
5 A simetria controla as ligações e consequentemente as propriedades físicas e espectroscópicas das moléculas. Considerações da simetria são essenciais para construção dos orbitais moleculares, análise das vibrações moleculares e obtenção de informações a respeito das estruturas moleculares e eletrônicas a partir de dados espectroscópicos. Sempre é possível encontrar algum elemento de simetria em moléculas, associamos operações de simetria a estes elementos de simetria. 5
6 Operação de simetria é uma operação (ação) geométrica conduzida em uma molécula levando a uma situação de indistinguibilidade (sem mudanças), isto é, não é possível distinguir o objeto antes e depois da operação de simetria (não ocorrem mudanças). Cada operação de simetria está associada a um elemento de simetria. O grupo de ponto de uma molécula é identificado pelos elementos de simetria e comparando esses elementos de simetria com os elementos que definem cada grupo. As propriedades de simetria de um sistema estão relacionadas com o conceito de grupo matemático. 6
7 Identidade (E) é o próprio objeto como um todo. Todo objeto possui pelo menos o elemento identidade. Ou seja, C 1 = rotação de 360 (2p) Rotação (C n ) eixo de rotação de ordem n. Rotação será 360 /n ou 2p/n Reflexão (s) planos de simetria s h perpendicular ao C n s v paralelo ao eixo que contém C n s d contém C n e bisseta o ângulo entre dois eixos C 2 perpendiculares ao C n Inversão (i) centro de inversão ao centro de simetria Rotação-reflexão (S n ) também chamado de rotação imprópria. O eixo roto-reflexão S n = C n s h, é uma rotação de ordem n seguida de uma reflexão perpendicular ao eixo em torno do qual foi executada a rotação 7
8 Operações de simetria e elementos de simetria 8
9 Eixo de rotação C 3 9
10 10
11 11
12 12
13 13
14 14
15 Deve-se tomar cuidado ao se realizar as operações C n e i para não haver confusão. 15
16 S 4 na moléculas de metano 16
17 S 4 na moléculas de metano 17
18 18
19 19
20 20
21 Exercício: Ache o erro na aplicação do S 4 na molécula de aleno 21
22 Resposta! Aplicação do S 4 na molécula de aleno 22
23 Exercício: encontre os elementos de simetria nas formas eclipsada e estrelada do etano. Eclipsada Estrelada Exercício: Esboce o eixo S 4 no íon amônio. Quantos desses eixo o íon possui? 23
24 Exemplo: Alguns dos elementos de simetria de uma molécula quadrado planar como XeF 4 24
25 25
26 26
27 27
28 Tetraedro (T d ) Icosaedro (I h ) (c) Octaedro (O h ) 28
29 C s C i T d O h Tetraedro Cubo 29
30 O h I h Octaedro dodecaedro I h R 3 icosaedro esfera 30
31 31
32 32
33 Grupo de ponto Classes (cada coluna representa uma classe) Funções quadráticas Funções de um eixo Operações de simetria C 2V E C 2 s v s v Funções cúbicas A z, s x 2, y 2, z 2 z 3, x(z 2 y 2 ) A R z xy xyz B x, R y xz xz 2, x(x 2 3y 2 ) B y, R x yz yz 2, y(3x 2 y 2 ) Representações Irredutíveis ou espécies de simetria Caracteres Propriedades irredutíveis vetoriais (Cada linha corresponde a uma representação irredutível) 33
34 Análises sistemáticas das propriedades espectroscópicas de moléculas podem ser realizadas usando tabelas de caracteres para o respectivo grupo de ponto; Cada grupo de ponto possui uma tabela de caracteres. Os grupos de ponto e as operações de simetria são nomeados pela notação de Schöenflies (ex: C 2v ); As espécies de simetria contidas num grupo de ponto são nomeados utilizando os símbolos de Mulliken (ex: A 1 ); 34
35 A tabela de caracteres mostra todos os elementos de simetria de um grupo de ponto, juntamente com a sua descrição: objetos ou funções matemáticas são transformados através da operação de simetria correspondente; A tabela de caracteres é completa: todos os possíveis objetos ou funções matemáticas relacionados a uma molécula (pertencente a um grupo de ponto particular) devem ser transformados como uma linha da tabela de caracteres desse grupo. 35
36 Arthur Moritz Schönflies ( ) Matemático alemão 36
37 László Tisza ( ) Físico Hungáro que publicou tabelas de caracteres pela primeira vez em
38 Robert Sanderson Mulliken ( ) Físico-químico americano que em 1933 publicou tabelas de caracteres em inglês pela primeira vez. Prêmio Nobel de química em
39 Hans Albrecht Bethe ( ) Físico americano-alemão que utilizou teoria de grupo em seu trabalho sobre teoria do campo ligante. Prêmio Nobel de física em
40 As entradas na parte principal da tabela são chamados de caracteres, c (chi). Cada caractere mostra como um objeto, átomo, vetor ou função matemática (como um orbital atômico) é afetada pela operação de simetria correspondente do grupo, como mostrado na tabela abaixo: Caractere Significância 1 O objeto permanece inalterado -1 O objeto muda de sinal 0 O objeto faz uma mudança mais complexa, como mudar de posição espacial Por exemplo: A rotação do orbital p z ao redor do eixo z não causará mudanças (consequentemente o caractere será 1); A reflexão do orbital p z no plano xy resulta em mudança de sinal (caractere -1) 40
41 Resumo dos componentes de uma tabela de caracteres 41
42 Rótulos usados em operações com tabelas de caracteres R Qualquer operação de simetria, tal como C 2 ou s v (xz) Γ Espécie de simetria (rótulo da representação irredutível) c Caractere de uma operação R em Γ i e j Designação de representações diferentes, tais como: A 1 ou A 2 42
43 A Classe de uma operação é um grupo especifico de operações de simetria do mesmo tipo geométrico. Rotações ao redor de um eixo formam uma classe, reflexões em um espelho formam outra classe e assim por diante. O número de membros de cada classe é mostrado no topo da coluna, por exemplo: 2C 3 denota que existe dois membros da classe de rotação com eixo C 3 ; 2S 43 denota que existe dois membros S 4 operados com rotação C 4 três vezes seguida, resultando em uma rotação com 270º; Cada linha corresponde a uma representação irredutível do grupo. É o tipo de simetria fundamental no grupo. A primeira linha corresponde a espécie de maior simetria. 43
44 Vetores de translação x, y, z ou T x, T y, T z Transformação das coordenadas (x, y, z) Componentes do momentos de dipolo (x, y, z) relevantes para a atividade infravermelho Orbitais p Vetores de rotação R x, R y, R z Rotações ao redor dos eixos (x, y, z) Vetores combinados (quadráticos) xy, xz, yz, (x 2, y 2, z 2 ) Funções quadráticas de relevância para a atividade Raman Orbitais d Vetores combinados (cúbicos) xyz, x 3, y 3, z 3, x(z 2 y 2 ), y(z 2 x 2 ), z(x 2 y 2 ), xz 2, yz 2, x(x 2 3y 2 ), y(3x 2 y 2 ) Orbitais f 44
45 Principais características da tabela de caracteres 1 O número total de operações simetria é denominado de ordem do grupo (h). Para determinar a ordem do grupo basta somar o número de operações nas classes (linha do topo da tabela de caracteres) C 2V = {E, C 2, s v, s v } ordem h = 4 C 3V = {E, C 3, C 32, s v, s v, s v } ordem h = 6 D 3h = {E, 2C 3, 3C 2, s h, 2S 3, 3s d } ordem h = 12 45
46 2 Operações de simetria são agrupadas em classes. Todas as operações de simetria em uma classe tem caracteres idênticos para suas matrizes de transformação e são agrupados na mesma coluna na tabela de caracteres. Cada operação de simetria é uma classe separada, portanto temos 4 colunas na tabela de caracteres do grupo C 2v : E, C 2, s v e s v '. 3 O número de representações irredutíveis (espécies de simetria) é igual ao número de classes. Isto significa que a tabela de caracteres deve conter o mesmo número de linhas e colunas, gerando uma matriz quadrada. No caso do grupo C 2v, são 4 classes e 4 representações irredutíveis. 46
47 4 A soma dos quadrados das dimensões (caracteres pertencentes a classe identidade, E) de cada representação irredutível é igual a ordem do grupo: = χ i (E) 2 Exemplo: ordem do grupo C 2v, h = = 4 ordem do grupo D 3h, h = = 12 i 5 Para qualquer representação irredutível, a soma dos quadrados dos caracteres multiplicado pelo número de operações na classe é igual a ordem do grupo: = χ i (R) 2 R Exemplo: A 2 no grupo C 2v : h = (1 x 1) 2 + (1 x 1) 2 + (1 x (-1)) 2 + (1 x (-1)) 2 = 4 47
48 6 O produto de duas representações irredutíveis deve obedecer a relação ortonormal (d ij ). A soma dos produtos dos caracteres, multiplicados para cada classe, para qualquer representação irredutível deve resultar em 0 ou 1. δ ij = 1 R χ i (R)χ j (R) = 0 quando i j 1 quando i = j Exemplo: No grupo C 2v as espécies de simetria B 1 e B 2 são ortogonais: (1 x 1 x 1) + (1 x (-1) x (-1)) + (1 x 1 x (-1)) + (1 x (-1) x 1) = 0 E C 2 s v (xz) s v '(yz) 7 A representação totalmente simétrica, com caractere igual a 1 para todas as operações está inclusa em todos os grupos. O grupo C 2v tem a espécie A 1 em que todos os caracteres são igual a 1. 48
49 Notação de Bethe: Γ 1, Γ 2, Γ 3, Γ 4... Notação mais utilizada em física do estado sólido Notação de Mulliken: A, B, E, T( F) A,B são notações restritas para representações unidimensionais, isto é c(e) =1 A indica simetria do eixo principal, isto é, c(c n ) = 1 B indica anti-simetria em relação ao eixo principal, isto é, c(c n ) = -1 E restrita para representações bidimensionais, isto é c(e) = 2 T( F) restrita para representações tridimensionais, isto é c(e) = 3 G restrita a quatro dimensões, isto é c(e) = 4 H restrita a cinco dimensões, isto é c(e) = 5 49
50 S + unidimensional, simetria com relação a s v ou C 2, ou seja, c(e) = 1, c(s v ) ou c(c 2 ) = 1 S - unidimensional, anti-simetria com relação a s v ou C 2, ou seja, c(e) = 1, c(s v ) ou c(c 2 ) = -1 P duas dimensões, isto é c(e) = 2 D duas dimensões, isto é c(e) = 2 F duas dimensões, isto é c(e) = 2 Letras minúsculas (a, b, e, t, s, p,...) são usadas para a simetria de orbitais individuais; letras maiúsculas (A, B, E, T, S, P,...) são usadas para a simetria de estados. 50
51 Índices em A e B 1, 2 e 3 1 simetria com relação ao C 2 C n (ou s v ), isto é c(c 2 ) ou c(s v ) = 1 2 anti-simetria com relação ao C 2 C n (ou s v ), isto é c(c 2 ) ou c(s v ) = -1 3 usado quando temos 3 operações equivalentes nas direções x,y,z. Exemplo: o grupo D 2h que tem 3 eixos C 2 equivalentes, onde 1 está para z, 2 para y e 3 para x. Superescritos (ou potências) ( ) ex: A, E, indicam simetria com relação ao s h, isto é c(s h ) = 1 ( ) ex: A, E, indicam anti-simetria com relação ao s h, isto é c(s h ) = -1 51
52 Subscritos g e u g = gerade = par, simetria com relação ao centro de inversão, isto é c(i) =1 u = ungerade = ímpar, anti-simetria com relação ao centro de inversão, isto é c(i) = -1 Para as representações E e T, os subscritos numéricos 1, 2,..., também são empregados da mesma maneira. Entretanto, nem sempre indicam simetria relativo ao C 2 ou s v. 52
53 Exemplo: Analisando os orbitais da molécula de amônia é possível observar que o orbital N-2p z é o único com simetria A 1 (totalmente simétrico), enquanto que ambos orbitais N-2p x e N-2p y pertencem a representação de simetria E, possuem as mesmas características de simetria, ou seja, são chamado de degenerados, devendo serem tratados juntos. 53
54 Definição Conjunto de elementos que obedecem a 4 regas básicas 1. O produto entre dois elementos de um grupo também pertencem ao grupo 2. O produto é associativo, que significa que as operações podem ser agrupadas conforme desejado ou necessário desde que não se altere a ordem das operações: A (B C) = (A B) C Embora a multiplicação seja associativa não é necessário que comute: A C C A O grupo em que as multiplicações são comutativas é chamado de grupo Abeliano em homenagem ao matemático norueguês Niels Henrik Abel. 54
55 Niels Henrik Abel ( ) Matemático norueguês considerado um dos mais notáveis matemáticos do século XIX 55
56 3. Existe o elemento (operador) identidade (E) que comuta com todos os outros membros do grupo deixando-os inalterados. O termo comuta significa que a ordem da multiplicação não importa: EA = AE = A, EB = BE = B Existe o elemento inverso ou recíproco (R) para cada operador. O produto de um operador e o seu inverso resulta no operador identidade. Qualquer operador e o seu inverso devem comutar: AA -1 = A -1 A = E, BB -1 = B -1 B = E 56
57 Subgrupos um subgrupo é apenas um grupo dentro de um grupo maior. Existem também grupos que não contém subgrupos. As ordens dos subgrupos deve ser um fator da ordem do grupo principal. Ou seja, a ordem de qualquer subgrupo g de um grupo de ordem h deve ser um divisor de h. h/g = k onde k é um inteiro 57
58 Transformação por similaridade é definida pela aplicação sucessiva de três operações Z, X e Z -1, onde X e Z são qualquer operação: Z -1 X Z = Y 58
59 As seguintes regras valem se a representação irredutível não tiver o número 3 A x B = B 1 x 1 = 1 g x g = g ( ) x ( ) = ( ) A x A = A 1 x 2 = 2 g x u = u ( ) x ( ) = ( ) B x B = A 2 x 2 = 1 u x u = g ( ) x ( ) = ( ) A 1 g ( ) B 2 u ( ) Exemplos: A 1 x B 2 = B 2 A 2 x B 1 = B 2 A 2 x B 1 = B 2 A 2g x B 2u = B 1u B 2 x B 2 = A 1 A 1u x A 2g = A 2u 59
60 O produto direto Ґ ij de duas representações irredutíveis Ґ i e Ґ j : Γ i Γ j = Γ ij (também escrito comoγ i Γ j ) Ґ ij tem as seguintes propriedades: 1) A dimensão de Ґ ij é o produto das dimensões de Ґ i e Ґ j. Por exemplo: 60
61 C 3V E 2C 3 3s v A A E A 1 x A 1 A 1 x A 2 A 1 x E E x E 61
62 E: C n : cos 2π n sen 2π n 0 sen 2π n cos 2π n (C 2 ) Z σ xy : , σ xz : , σ yz : i:
63 Uma molécula não pode ser polar se pertencer a qualquer grupo de ponto que inclua um centro de inversão. Dessa maneira não serão polares, qualquer molécula pertencente aos grupos: D e derivações, grupos cúbicos (T, O), grupo icosaédrico (I) e suas modificações. Uma molécula polar tem que ter um momento de dipolo permanente. Uma molécula não poderá ser polar se tiver centro de inversão. A inversão implica que a molécula tem distribuição de carga em todas as direções (pontos opostos ao centro). 63
64 Resumindo: - Uma molécula não será polar se tiver centro de inversão - Uma molécula não pode ter um momento de dipolo elétrico perpendicular a qualquer plano - Uma molécula não pode ter um momento de dipolo de elétrico perpendicular a qualquer eixo de rotação 64
65 Exercício: A molécula de rutenoceno é um prisma pentagonal com os átomos de Ru dentro de um sanduíche (entre os dois anéis ciclopentadienil, C 5 H 5 2- ). Essa molécula pode ser polar? Exercício: A conformação do ferroceno (estrelada ou antiprismática pentagonal) é 4 kj.mol -1 mais estável do que a prismática pentagonal. Essa molécula é polar? 65
66 Momentos de Dipolo Região pobre em elétrons H Região rica em elétrons F m = Q x r Q é a carga d+ d- r é a distância entre as cargas 1 D = 3.36 x C m 66
67 Comportamento de moléculas polares na ausência e presença de campo elétrico 67
68 Quais moléculas apresentam um momento de dipolo? H 2 O, CO 2, SO 2, and CH 4 O S Momento de dipolo Molécula polar Momento de dipolo Molécula polar H O C O H C H Sem momento de dipolo Molécula apolar H Sem momento de dipolo Molécula apolar 68
69 BF 3 tem momento de dipolo? 69
70 CH 2 Cl 2 tem momento de dipolo? 70
71 71
72 Estas moléculas possuem ligações polares, e tem momento de dipolo diferente de zero 72
73 Formaldeído tem ligações polares e é uma molécula polar direction O of dipole moment H C H Formaldehyde m = 2.33 D 73
74 Estas moléculas possuem ligações polares, entretanto tem momento de dipolo zero F Cl O C O Carbon dioxide m = 0 D F B F Boron trifluoride m = 0 D Cl Cl C Cl Carbon tetrachloride m = 0 D 74
75 75
76 Química em ação: forno de microondas 76
77 Uma molécula não pode ser quiral se possuir um eixo de rotação imprópria (S n ). Uma molécula quiral é uma molécula que não é sobreponível sobre sua imagem especular. As imagens especulares das moléculas quirais são chamados de enantiômeros. Moléculas quirais possuem atividade óptica porque rotacionam o plano da luz polarizada. Grupo de ponto C 1 Possui geometria tetraédrica mas não simetria tetraédrica T d. Portanto quiral Possui um eixo S 4 Portanto não é quiral 77
78 78
79 79
80 Exercício: Diga se o complexo [Mn(acac) 3 ] (Onde acac é a abreviação para o ligante acetilacetonato (CH 3 COCHCOCH 3- ) mostrado abaixo é quiral? Exercício: A conformação do H 2 O 2 mostrada abaixo é quiral? A molécula tem rotação livre ao redor da ligação O-O, comente a possibilidade de observar atividade óptica nesta molécula. 80
81 81
82 Se uma molécula possuir centro de inversão (i) nenhum de seus modos vibracionais poderá ser ativo simultaneamente no Raman e infravermelho (um modo poderá ser inativo em ambos) Um modo vibracional é ativo no infravermelho se tiver a mesma simetria do componente de vetor do campo elétrico Um modo vibracional é ativo no Raman se tiver a mesma simetria do componente de polarizabilidade molecular 82
83 A frequência de vibração é dada por: ν = 1 2π K μ ou ν = 1 2πc K μ Absorção de radiação no infravermelho ocorre quando a vibração resulta em mudança no dipolo de momento elétrico Uma transição Raman ocorre quando a polarizabilidade de uma molécula muda durante a vibração 83
84 Espectros do XeF4
85 Comparação das técnicas de espectroscopia Infravermelho e Raman 85
86 Parâmetros Infravermelho Raman Fenômeno espectroscópico Absorção da luz: hn IR = DE vib Espalhamento inelástico da luz: hn 0 - hn sc = DE vib Transições permitida Du = +1, +2, +3,... Du = ±1, ±2, ±3,... (transições para Du = +2, +3,... São menos distintas do que no IR) Excitação Radiação IR policromática Radiação monocromática (n 0 ) na região do UV-visível e NIR Origem molecular Momento de dipolo m = qr Momento de dipolo induzido: P = ae Requerimento para atividade vibracional Mudança do momento de dipolo durante a vibração: ( m/ Q k ) 0 0 Mudança na polarizabilidade durante a vibração: ( a/ Q k ) 0 0 Intensidade da banda I IR ( m/ Q k ) 0 I R ( a/ Q k ) 0 Frequência da Absoluto: n vib = n IR Relativo a frequência de excitação: n vib medida = n 0 - n sc 86
87 Parâmetros Infravermelho Raman Leitura do sinal Gráfico Característica espectral dominante Comparativo: Transmitância (T = I A /I R ) ou absorbância (A = -log T) Linear em % T ou logaritmo em A vs. número de onda (cm -1 ) Vibrações destroem a simetria molecular: modos de estiramento antissimétrico e deformações Absoluto: potência radiante ou intensidade da radiação espalhada Linear: Intensidade Raman vs. número de onda (cm -1 ) Vibrações preservam a simetria molecular: modos de estiramento simétrico Molécula inativa Diatômicas homonucleares Nenhuma Moléculas centrosimétricas Meio Somente são ativos modos de simetria u Água absorve fortemente e é um solvente ruim para estudos IR Somente são ativos modos de simetria g Água é um espalhador fraco e é um bom solvente para estudos Raman 87
88 Previsão do números modos vibracionais no espectro vibracional Γ 3N molécula = Γ 3N + Γ Trans + Γ Rot Molécula linear: 3N 5 Molécula Não-linear: 3N 6 N número de átomos na molécula f(r) fator da operação f C φ = cos φ f S φ = cos φ Para operação própria (C f ) Para operação imprópria (S n, i e s) Por exemplo: f(s 1 ) = f(s) = f(c 1. s) = 1 f(s 2 ) = f(i) = f(c 2. s) = -3 88
89 Normalmente, na aplicação de teoria de grupo para resolver problemas relacionados a estrutura e dinâmica molecular envolve calcular a representação redutível do fenômeno de interesse, tal como vibração molecular e então decompor em seus componentes irredutíveis. A representação redutível será sempre a soma das representações irredutíveis. Embora a decomposição possa ser acompanhada por dedução, para a maioria dos casos a redução é feita através da fórmula: n k = 1 R n g χ ij (R)χ k (R) Nessa expressão n k é o número de vezes que uma representação irredutível aparece na representação que está sendo reduzida, h é a ordem do grupo, n g é o número de operações na classe, c ij (R) caractere da representação redutível e c k (R) caractere da representação irredutível. 89
90 Para encontrar o número de vezes (n Γ ) que uma representação irredutível está contida em uma representação redutível, aplica-se a seguinte fórmula: n k = 1 n g χ ij (R)χ k (R) R n k é o número de vezes que a representação irredutível está contida na representação redutível h ordem do grupo n g número de operações na classe g, número de membros da classe R c ij (R) caractere da representação redutível c k (R) caractere da representação irredutível R uma operação do grupo ou classe 90
91 Uma representação mais simples da fórmula de redução de caracteres: a i = 1 R (χ R χ R i C R ) a i é o número de vezes que a representação irredutível está contida na representação redutível h ordem do grupo R uma operação do grupo (classe) C R número de operações na classe, número de membros da classe R c R caractere da representação redutível c R caractere da representação irredutível 91
92 Previsão do números modos vibracionais no espectro vibracional Γ 3N graus de liberdade Γ Trans translacional Γ Rot rotacional Γ(N 0 ) componentes inalterados após operação de simetria da classe 92
93 93
94 C 2V E C 2 s v (xz) s v (yz) A z, s x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz Γ(N 0 ) f(r) ou Γ x,y,z Γ 3N = Γ x,y,z x Γ(N 0 ) Γ (A 1 ) = Γ (A 2 ) = Γ (B 1 ) = Γ (B 2 ) = 94
95 C 2V E C 2 s v (xz) s v (yz) A z, s x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz Γ(N 0 ) f(r) = Γ x,y,z Γ 3N = Γ x,y,z x Γ(N 0 ) Γ 3N (A 1 ) = ¼ x [(9 x 1) + (-1 x 1) + (1 x 1) + (3 x 1)] = 3A 1 Γ 3N (A 2 ) = ¼ x [(9 x 1 ) + ( - 1 x 1) + (1 x (-1)) + (3 x (-1))] = 1A2 Γ3N (B1) = ¼ x [(9 x 1 ) + ( - 1 x (-1)) + (1 x 1) + (3 x (-1))] = 2B 1 Γ 3N (B 2 ) = ¼ x [(9 x 1) + (-1 x (-1)) + (1 x (-1)) + (3 x 1)] = 3B 2 95
96 Todos os movimentos Translação (x, y, z) Rotação (R x, R y, R z ) Vibrações 3A 1 A 1 2A 1 1A 2 A 2 3B 1 B 1 B 1 B 1 2B 2 B 2 B 2 96
97 Água molécula não-linear: 3N 6 modos vibracionais (3 x 3) 6 = 3 modos ativos t Translação; r rotação; v - vibração 97
98 98
99 D 4h E 2C 4 C 2 2C 2 2C 2 i 2S 4 s h 2s v s d A 1g x 2 + y 2, z 2 A 2g R z B 1g x 2 y 2 B 2g xy E g (R x, R y ) (xz, yz) A 1u A 2u z B 1u B 2u E u (x, y) Γ N0 f(r) Γ 3N 99
100 D 4h E 2C 4 C 2 2C 2 2C 2 i 2S 4 s h 2s v s d A 1g x 2 + y 2, z 2 A 2g R z B 1g x 2 y 2 B 2g xy E g (R x, R y ) (xz, yz) A 1u A 2u z B 1u B 2u E u (x, y) Γ N f(r) Γ 3N
101 D 4h E 2C 4 C 2 2C 2 2C 2 i 2S 4 s h 2s v s d A 1g x 2 + y 2, z 2 A 2g R z B 1g x 2 y 2 B 2g xy E g (R x, R y ) (xz, yz) A 1u A 2u z B 1u B 2u E u (x, y) Γ N f(r) Γ 3N Γ= A 1g + A 2g + B 1g + B 2g + E g + 2 A 2u + B 2u + 3 E u Translacional: A 2u + E u Rotacional: A 2g + E g Vibracional Raman: A 1g + B 1g + B 2g ; Infravermelho: A 2u + 2 E u ; Inativo: B 2u 101
102 102
103 103
104 104
105 Exercício: Existem quatro modos vibracionais para a molécula triatômica linear CO 2 (ver esquema abaixo). Quais desses modos são ativos no IR e no Raman? Exercício: O modo de deformação angular do N 2 O (óxido nitroso) é ativo no IR. Esse modo pode ser ativo no Raman? 105
106 Exercício: Identifique as espécies de simetria dos deslocamentos vibracionais. O isômero trans tem simetria D 2h. Mostre que a espécie de simetria do estiramento anti-simétrico Pd Cl é B 2u. Confirme que a espécie de simetria do modo de estiramento totalmente simétrico do Pd Cl no isômero trans é A g. Encontre as espécies de simetria dos modos ativos no infravermelho e Raman de ambos os isômeros. 106
107 107
108 108
109 109
110 Exercício: Faça a previsão dos modos vibracionais ativos no infravermelho e Raman para os isômeros cis e trans do composto [Fe(CO) 4 Cl 2 ], ilustrados abaixo. Encontre as espécies de simetria dos modos ativos. Seria possível distinguir um composto dos outro através da espectroscopia vibracional? 110
111 D 4h E 2C 4 C 2 2C 2 2C 2 i 2S 4 s h 2s v s d A 1g x 2 + y 2, z 2 A 2g R z B 1g x 2 y 2 B 2g xy E g (R x, R y ) (xz, yz) A 1u A 2u z B 1u B 2u E u (x, y) Γ N0 f(r) Γ 3N 111
112 D 4h E 2C 4 C 2 2C 2 2C 2 i 2S 4 s h 2s v s d A 1g x 2 + y 2, z 2 A 2g R z B 1g x 2 y 2 B 2g xy E g (R x, R y ) (xz, yz) A 1u A 2u z B 1u B 2u E u (x, y) Γ N f(r) Γ 3N Γ= 3A 1g + 2A 2g + 2B 1g + 2B 2g + 3E g + 4A 2u + 2B 2u + 6E u Translacional: A 2u + E u ; Rotacional: A 2g + E g Vibracional Raman: 3A 1g + 2B 1g + 2B 2g + 2Eg Infravermelho: 3A 2u + 5E u ; Inativo: 1A 2g + 2B 2u
113 C 2V E C 2 s v (xz) s v (yz) A z, s x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz Γ(N 0 ) f(r) Γ 3N 113
114 C 2V E C 2 s v (xz) s v (yz) A z, s x 2, y 2, z 2 A R z xy B x, R y xz B y, R x yz Γ(N 0 ) f(r) Γ 3N Γ= 11A 1 + 5A 2 + 9B 1 + 8B 2 Translacional: A 1 + B 1 + B 2 Rotacional: A 2 + B 1 + B 2 Somente Raman: 4A 2 Infravermelho e Raman coincidindo: 10A 1 + 7B 1 + 6B 2 114
115 Exercício: Um dos primeiros compostos do tipo metal carbonil sintetizados foi a molécula tetraédrica (T d ) Ni(CO) 4. Os modos vibracionais da molécula que surgem movimentos de estiramento dos grupos CO são quatro combinações dos vetores de deslocamento dos COs. Quais modos são ativos no IR e no Raman? O próximo slide mostra os vetores dos deslocamento dos grupos CO na molécula de Ni(CO) 4. Exercício: Mostre que os quatro deslocamentos CO no cátion [Pt(CO) 4 ] 2+ de geometria quadrado planar transformam-se como A 1g + B 1g + E u. Quantas bandas são esperadas no espectro IR e Raman do cátion [Pt(CO) 4 ] 2+? 115
116 116
117 117
118 118
119 Bishop, D. M.; Group Theory and Chemistry, Dover, 1992 de Oliveira, G. M.; Simetria de Moléculas e Cristais: Fundamentos da Espectroscopia Vibracional, Bookman, 2009 Huheey, J. E.; Keiter, E. A.; Keiter, R. L.; Inorganic Chemistry: Principles of Structure and Reactivity, 4th Ed.; Harper & Row, New York, 1993 Atkins, P. W., Overton, T. L.; Rourke, J. P.; Weller, M. T.; Armstrong, F. A.; Inorganic Chemistry, W. H. Freeman, New York, 5th Ed., 2010 Douglas, B.; McDaniel, D. H.; Alexander, J. J.; Concepts and Models of Inorganic Chemistry, New York, John Wiley, 3th Ed., 1993 Nakamoto, K. Infrared and Raman Spectra of Inorganic and Coordination Compounds, Part A: Theory and Applications in Inorganic Chemistry, 6th. Ed, Wiley, 2010 Ogden, J. S.; Introduction to Molecular Symmetry, Oxford Chemistry Primers, 2001 Miessler, G. L.; Tarr, D. A.; Inorganic Chemistry, 4th Ed., Pearson,
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 14/03/2017 Bibliografia Simetria de moléculas e cristais. Gelson
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 14/03/2017 Bibliografia Simetria de moléculas e cristais. Gelson
Simetria Molecular e Teoria de Grupo. Prof. Fernando R. Xavier
 Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2017 Uma idéia intuitiva... 2 Por que estudar simetria e teoria de grupo? A química estuda íons, moléculas e suas transformações; A química
Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2017 Uma idéia intuitiva... 2 Por que estudar simetria e teoria de grupo? A química estuda íons, moléculas e suas transformações; A química
SFI 5800 Espectroscopia Física. Simetria e Teoria de Grupos
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Simetria e Teoria de Grupos Prof. Dr. José Pedro Donoso Simetria molecular e Teoria de Grupos A aplicação
Universidade de São Paulo Instituto de Física de São Carlos - IFSC SFI 5800 Espectroscopia Física Simetria e Teoria de Grupos Prof. Dr. José Pedro Donoso Simetria molecular e Teoria de Grupos A aplicação
Simetria e Teoria de Grupo. Profa. Célia Machado Ronconi
 Simetria e Teoria de Grupo Profa. Célia Machado Ronconi cmronconi@id.uff.br 1 Sabemos intuitivamente quando algo é simétrico. 2 Hemoglobina Cadeia polipeptídica Hemoglobina Grupo hemo contendo Fe 3 Simetria
Simetria e Teoria de Grupo Profa. Célia Machado Ronconi cmronconi@id.uff.br 1 Sabemos intuitivamente quando algo é simétrico. 2 Hemoglobina Cadeia polipeptídica Hemoglobina Grupo hemo contendo Fe 3 Simetria
Simetria molecular e teoria de grupos
 Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares
 Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares 1) Construa os orbitais moleculares para H 2 O e NO 2 baseado nos SALCs de
Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares 1) Construa os orbitais moleculares para H 2 O e NO 2 baseado nos SALCs de
Simetria Molecular e Teoria de Grupo. Prof. Fernando R. Xavier
 Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2013 Uma idéia intuitiva... Simetria molecular Por que estudar simetria e teoria de grupo? A química moléculas e suas transformações;
Simetria Molecular e Teoria de Grupo Prof. Fernando R. Xavier UDESC 2013 Uma idéia intuitiva... Simetria molecular Por que estudar simetria e teoria de grupo? A química moléculas e suas transformações;
ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS
 Quim Nova, Vol 3, No 6, S1-S, 2012 ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II: UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr, Juliana dos Santos de Souza, Paula Homem-de-Mello,
Quim Nova, Vol 3, No 6, S1-S, 2012 ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II: UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr, Juliana dos Santos de Souza, Paula Homem-de-Mello,
Simetria molecular e teoria de grupos
 Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
Simetria molecular e teoria de grupos As propriedades de simetria das moléculas e como elas podem ser usadas para prever espectros vibracionais, hibridização, atividade óptica, etc. Grupo Pontual As moléculas
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química
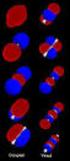 Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 21/03/2017 Espectroscopia no infravermelho ACIK, M., LEE, G.,
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 21/03/2017 Espectroscopia no infravermelho ACIK, M., LEE, G.,
Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I. Prof. Dr. João Batista Marques Novo
 Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS I a PARTE: TEORIA DE GRUPOS Prof. Dr. João Batista Marques Novo ÍNDICE Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS
Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS I a PARTE: TEORIA DE GRUPOS Prof. Dr. João Batista Marques Novo ÍNDICE Disciplina CQ8 MÉTODOS ESPECTROSCÓPICOS
Geometria Molecular e polaridade de ligações
 Geometria Molecular e polaridade de ligações Prof. Éderson Química Geometria Molecular Geometria molecular O arranjo tri-dimensional dos átomos em uma molécula, ou seja, é a orientação espacial das moléculas,
Geometria Molecular e polaridade de ligações Prof. Éderson Química Geometria Molecular Geometria molecular O arranjo tri-dimensional dos átomos em uma molécula, ou seja, é a orientação espacial das moléculas,
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Espectroscopia no infravermelho ACIK, M., LEE, G., MATTEVI, C., CHHOWALLA,
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Espectroscopia no infravermelho ACIK, M., LEE, G., MATTEVI, C., CHHOWALLA,
Molécula de água. σ v : σ v ': ( 0 1
 QUIM7031 - moléculas poliatômicas Prof Dr Flávio M Matsumoto - 1 Molécula de água Orientação da molécula z O H 2 H 1 Aplicação das operações de simetria, em notação matricial E: 0 1( h 1 h 2 = ( h 1 h
QUIM7031 - moléculas poliatômicas Prof Dr Flávio M Matsumoto - 1 Molécula de água Orientação da molécula z O H 2 H 1 Aplicação das operações de simetria, em notação matricial E: 0 1( h 1 h 2 = ( h 1 h
Cristalografia para não-cristalógrafos
 Cristalografia para não-cristalógrafos Interpretando a Estrutura Cristalina dos Materiais MC-7 01, 02 e 03 de Agosto de 2018 (14:00-16:00h) Leonardo H. R. Dos Santos Departamento de Química UFMG leonardohrs@ufmg.br
Cristalografia para não-cristalógrafos Interpretando a Estrutura Cristalina dos Materiais MC-7 01, 02 e 03 de Agosto de 2018 (14:00-16:00h) Leonardo H. R. Dos Santos Departamento de Química UFMG leonardohrs@ufmg.br
Química Inorgânica Avançada
 Disciplina: Química Inorgânica Avançada (obrigatória) Créditos: 04 Carga Horária: 60 horas Docente: Antonio Reinaldo Cestari arcestari@gmail.com Sala 23, DQI-UFS Ementa: Química de Coordenação. Definições,
Disciplina: Química Inorgânica Avançada (obrigatória) Créditos: 04 Carga Horária: 60 horas Docente: Antonio Reinaldo Cestari arcestari@gmail.com Sala 23, DQI-UFS Ementa: Química de Coordenação. Definições,
Questão 01 - Em qual região do espectro você encontraria uma banda C=C?
 Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Diretoria de Graduação e Educação Profissional Departamento Acadêmico de Química e Biologia Segunda Lista de Exercícios
Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Diretoria de Graduação e Educação Profissional Departamento Acadêmico de Química e Biologia Segunda Lista de Exercícios
Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel
 Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Física para Ciências Biológicas Lista de Exercícios 5 - CASA Data: 22/05/2014
 Física para Ciências Biológicas - 2014 Lista de Exercícios 5 - CASA Data: 22/05/2014 1. Abaixo representamos a energia de interação dos átomos de K e Cl em função da distância interatômica. A energia de
Física para Ciências Biológicas - 2014 Lista de Exercícios 5 - CASA Data: 22/05/2014 1. Abaixo representamos a energia de interação dos átomos de K e Cl em função da distância interatômica. A energia de
Molécula de água C 2 : ( σ v : σ v ': ( 0 1 1
 CQ832 - moléculas poliatômicas Prof. Dr. Flávio M. Matsumoto 1 Orientação da molécula: z O H 2 Elementos de simetria: H 1 C 2 = z σ v = plano z σ v ' = plano z Molécula de água Aplicação das operações
CQ832 - moléculas poliatômicas Prof. Dr. Flávio M. Matsumoto 1 Orientação da molécula: z O H 2 Elementos de simetria: H 1 C 2 = z σ v = plano z σ v ' = plano z Molécula de água Aplicação das operações
Espectroscopia Infravermelha: Moléculas
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC Espectroscopia Infravermelha: Moléculas Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha Infravermelho próximo.800 4.000 cm -
Universidade de São Paulo Instituto de Física de São Carlos - IFSC Espectroscopia Infravermelha: Moléculas Prof. Dr. José Pedro Donoso Espectroscopia Infravermelha Infravermelho próximo.800 4.000 cm -
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos.
 Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
INSTITUTO DE QUÍMICA da UFRJ DEPARTAMENTO DE QUÍMICA INORGÂNICA. Programa de Disciplina. Química Inorgânica EQ. Nome: Código: IQG 244 CARACTERÍSTICAS
 Programa de Disciplina Nome: Química Inorgânica EQ Código: IQG 244 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina:
Programa de Disciplina Nome: Química Inorgânica EQ Código: IQG 244 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina:
Molécula de água. σ v : σ v ': 0 1. (h 1 +h 2 ) (h 1 +h 2 ) (h 1 +h 2 ) (h 1 +h 2 ) (h 1 +h 2 ) (h 1 h 2 ) (h 1 h 2 ) (h 1 h 2 ) (h 1 h 2 ) (h 1 h 2 )
 Orientação da molécula: H 2 Elementos de simetria: C 2 = z σ v = plano z σ v ' = plano z Aplicação das operações de simetria sobre os orbitais do átomo de O: 2p z (O) 2p z (O) 2p z (O) 2p z (O) 2p z (O)
Orientação da molécula: H 2 Elementos de simetria: C 2 = z σ v = plano z σ v ' = plano z Aplicação das operações de simetria sobre os orbitais do átomo de O: 2p z (O) 2p z (O) 2p z (O) 2p z (O) 2p z (O)
Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I ESPECTROSCOPIA VIBRACIONAL. Prof. Dr. João Batista Marques Novo
 Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I ESPECTROSCOPIA VIBRACIONAL Determinação das simetrias dos modos normais de vibração Prof. Dr. João
Programa de Pós-Graduação em Química Departamento de Química Disciplina CQ830 MÉTODOS ESPECTROSCÓPICOS I ESPECTROSCOPIA VIBRACIONAL Determinação das simetrias dos modos normais de vibração Prof. Dr. João
ORDEM. Periocidade. SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico de átomos, moléculas ou iões, formando uma estrutura cristalina regular
 Capítulo I ESTRUTURA CRISTALINA DE SÓLIDOS ORDEM curto alcance médio alcance longo alcance Periocidade unidimensional bidimensional tridimensional SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico
Capítulo I ESTRUTURA CRISTALINA DE SÓLIDOS ORDEM curto alcance médio alcance longo alcance Periocidade unidimensional bidimensional tridimensional SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico
Teoria do Campo Ligante. Prof. Fernando R. Xavier
 Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2017 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregada ainda
Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2017 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregada ainda
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química
 UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química QUÍMICA DE COORDENAÇÃO AVANÇADA QFL5825 ECTOR AGUILAR VITORINO Número USP: 7774685 São Paulo 26/9/2 QFL-5825 Química
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA Programa de Pós-Graduação em Química QUÍMICA DE COORDENAÇÃO AVANÇADA QFL5825 ECTOR AGUILAR VITORINO Número USP: 7774685 São Paulo 26/9/2 QFL-5825 Química
Por que o CuCl 2, ácido acético, e etanol dissolvem em água?
 Por que o CuCl 2, ácido acético, e etanol dissolvem em água? 1 Eletronegatividade (EN) 2 1811 - O conceito de EN foi introduzido por J. J. Berzelius que o definiu como sendo a capacidade que um átomo tem
Por que o CuCl 2, ácido acético, e etanol dissolvem em água? 1 Eletronegatividade (EN) 2 1811 - O conceito de EN foi introduzido por J. J. Berzelius que o definiu como sendo a capacidade que um átomo tem
ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS
 Quim. Nova, Vol. 35, No. 6, 12641270, 2012 Educação ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr., Juliana dos Santos de
Quim. Nova, Vol. 35, No. 6, 12641270, 2012 Educação ANÁLISE VIBRACIONAL DE COMPOSTOS DE COORDENAÇÃO DE NIQUEL(II): UMA ABORDAGEM AO ENSINO DOS GRUPOS PONTUAIS Sergio Kogikoski Jr., Juliana dos Santos de
Programa Analítico de Disciplina QUI320 Química Inorgânica II
 0 Programa Analítico de Disciplina Departamento de Química - Centro de Ciências Exatas e Tecnológicas Número de créditos: 6 Teóricas Práticas Total Duração em semanas: Carga horária semanal 4 6 Períodos
0 Programa Analítico de Disciplina Departamento de Química - Centro de Ciências Exatas e Tecnológicas Número de créditos: 6 Teóricas Práticas Total Duração em semanas: Carga horária semanal 4 6 Períodos
Lista de Exercícios de Cálculo 3 Primeira Semana
 Lista de Exercícios de Cálculo 3 Primeira Semana Parte A 1. Se v é um vetor no plano que está no primeiro quadrante, faz um ângulo de π/3 com o eixo x positivo e tem módulo v = 4, determine suas componentes.
Lista de Exercícios de Cálculo 3 Primeira Semana Parte A 1. Se v é um vetor no plano que está no primeiro quadrante, faz um ângulo de π/3 com o eixo x positivo e tem módulo v = 4, determine suas componentes.
3 Espectroscopia Molecular
 3 Espectroscopia Molecular 3.1. Aspectos gerais Todos os espectros se devem às transições entre estados de energia. A espectroscopia molecular fornece o valor da variação da energia interna quando uma
3 Espectroscopia Molecular 3.1. Aspectos gerais Todos os espectros se devem às transições entre estados de energia. A espectroscopia molecular fornece o valor da variação da energia interna quando uma
QB70D:// Química (Turmas S15/S16) Ligações Químicas
 QB70D:// Química (Turmas S15/S16) Ligações Químicas Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Estrutura de Lewis É muito importante saber desenhar estruturas de Lewis para moléculas
QB70D:// Química (Turmas S15/S16) Ligações Químicas Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Estrutura de Lewis É muito importante saber desenhar estruturas de Lewis para moléculas
QUÍMICA ORGÂNICA LIGAÇÕES QUÍMICAS GEOMETRIA MOLECULAR HIBRIDIZAÇÃO
 QUÍMICA ORGÂNICA LIGAÇÕES QUÍMICAS GEOMETRIA MOLECULAR IBRIDIZAÇÃO 1 Geometria molecular O arranjo tri-dimensional dos átomos em uma molécula geometria molecular A teoria da repulsão dos pares de elétrons
QUÍMICA ORGÂNICA LIGAÇÕES QUÍMICAS GEOMETRIA MOLECULAR IBRIDIZAÇÃO 1 Geometria molecular O arranjo tri-dimensional dos átomos em uma molécula geometria molecular A teoria da repulsão dos pares de elétrons
Espectroscopia Vibracional
 Espectroscopia Vibracional Infravermelho (IV) Difusão de Raman (R) Vibrações moleculares Transições vibracionais Região do Infravermelho 12820 4000 400 Número de onda (cm -1 ) 33 IVP IVM IVL IVP IV próximo;
Espectroscopia Vibracional Infravermelho (IV) Difusão de Raman (R) Vibrações moleculares Transições vibracionais Região do Infravermelho 12820 4000 400 Número de onda (cm -1 ) 33 IVP IVM IVL IVP IV próximo;
Geometria Molecular e Forças Intermoleculares
 Geometria Molecular e Forças Intermoleculares GEOMETRIA MOLECULAR DEPENDE: Disposição espacial dos núcleos dos átomos. Repulsão dos pares eletrônicos das ligações ou pares livres dos átomos. Obs. Toda
Geometria Molecular e Forças Intermoleculares GEOMETRIA MOLECULAR DEPENDE: Disposição espacial dos núcleos dos átomos. Repulsão dos pares eletrônicos das ligações ou pares livres dos átomos. Obs. Toda
Teoria do Campo Ligante. Prof. Fernando R. Xavier
 Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2014 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregrada ainda
Teoria do Campo Ligante Prof. Fernando R. Xavier UDESC 2014 Até então... A TCC apresenta um modelo conceitual simples para o fenômeno de formação de compostos de coordenação que pode ser empregrada ainda
Teoria de Grupos e Simetria Cristalina
 Teoria de Grupos e Simetria Cristalina Teorema de Bloch Tiago de Campos Resumo Neste texto serão apresentados conceitos fundamentais para o entendimento de estruturas cristalinas bem como suas simetrias.
Teoria de Grupos e Simetria Cristalina Teorema de Bloch Tiago de Campos Resumo Neste texto serão apresentados conceitos fundamentais para o entendimento de estruturas cristalinas bem como suas simetrias.
Aula Orientação do espaço. Observação 1
 Aula 14 Nesta aula vamos definir dois novos produtos entre vetores do espaço, o produto vetorial e o produto misto. Para isso, primeiro vamos apresentar o conceito de orientação. 1. Orientação do espaço
Aula 14 Nesta aula vamos definir dois novos produtos entre vetores do espaço, o produto vetorial e o produto misto. Para isso, primeiro vamos apresentar o conceito de orientação. 1. Orientação do espaço
Valence shell electron pair repulsion (VSEPR)
 Ligação química II geometria molecular Ligação química II geometria molecular Teoria da repulsão electrónica dos pares de e - da camada de valência Valence shell electron pair repulsion (VSEPR) Prediz
Ligação química II geometria molecular Ligação química II geometria molecular Teoria da repulsão electrónica dos pares de e - da camada de valência Valence shell electron pair repulsion (VSEPR) Prediz
Caracterização da disciplina. Turma: Turno: Quadrimestre: Ano: turma: Docente(s) responsável(is): Hueder Paulo Moisés de Oliveira
 Caracterização da disciplina Código da NHT4007.14 Nome da Espectroscopia disciplina: disciplina: Créditos (T-P- I): (4-2-6) Carga horária: 72 horas Aula prática: Câmpus: SA Código da Turma: Turno: Quadrimestre:
Caracterização da disciplina Código da NHT4007.14 Nome da Espectroscopia disciplina: disciplina: Créditos (T-P- I): (4-2-6) Carga horária: 72 horas Aula prática: Câmpus: SA Código da Turma: Turno: Quadrimestre:
Geometria Molecular. A forma geométrica de uma molécula é determinada pelo arranjo dos pares eletrônicos em torno dos átomos.
 Geometria Molecular A forma geométrica de uma molécula é determinada pelo arranjo dos pares eletrônicos em torno dos átomos. O método pelo qual se estabelece a orientação mais estável dos pares eletrônicos
Geometria Molecular A forma geométrica de uma molécula é determinada pelo arranjo dos pares eletrônicos em torno dos átomos. O método pelo qual se estabelece a orientação mais estável dos pares eletrônicos
Problemas de Duas Partículas
 Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
A Dualidade Onda-Partícula
 A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
Espectroscopia no IV
 Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
QUI109 QUÍMICA GERAL (Ciências Biológicas) 8ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 8ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) A LIGAÇÃO COVALENTE É BASEADA NO COMPARTILHAMENTO DE ELÉTRONS Ex.
QUI109 QUÍMICA GERAL (Ciências Biológicas) 8ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) A LIGAÇÃO COVALENTE É BASEADA NO COMPARTILHAMENTO DE ELÉTRONS Ex.
Ligação Química. - Os elétrons mais fracamente ligados ao átomo podem tomar parte na formação de ligações químicas.
 Ligação Química É necessário compreender (prever) as ligações químicas, se quisermos entender as propriedades químicas e físicas de elementos e compostos. - Os elétrons mais fracamente ligados ao átomo
Ligação Química É necessário compreender (prever) as ligações químicas, se quisermos entender as propriedades químicas e físicas de elementos e compostos. - Os elétrons mais fracamente ligados ao átomo
Química Orgânica. Compostos orgânicos contêm carbono. O carbono não ganha nem cede elétrons
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 1 Estrutura Eletrônica e Ligação Química Ácidos e Bases Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Química Orgânica
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 1 Estrutura Eletrônica e Ligação Química Ácidos e Bases Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Química Orgânica
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
QB70C:// Química (Turmas S71/S72) Ligação Química
 QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
Espectroscopia no Infravermelho (IR)
 Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
18/04/ Formas das moléculas. 6. Formas das moléculas. 6. Formas das moléculas. 6. Formas das moléculas
 As estruturas de Lewis mostram como os átomos estão unidos nas moléculas e nos íons poliatômicos. Entretando, elas não mostram a geometria tridimensional Átomos centrais rodeados por pares ligados apenas
As estruturas de Lewis mostram como os átomos estão unidos nas moléculas e nos íons poliatômicos. Entretando, elas não mostram a geometria tridimensional Átomos centrais rodeados por pares ligados apenas
CURSO FARMÁCIA SEMESTRE
 QUÍMICA ORGÂNICA I INTRODUÇÃO À QUÍMICA ORGÂNICA (Parte I) CURSO FARMÁCIA SEMESTRE 2016/2 Professoras: Alceni Augusta Werle Tânia Márcia Sacramento Melo Tabela Periódica/Revisão Representação esquemática
QUÍMICA ORGÂNICA I INTRODUÇÃO À QUÍMICA ORGÂNICA (Parte I) CURSO FARMÁCIA SEMESTRE 2016/2 Professoras: Alceni Augusta Werle Tânia Márcia Sacramento Melo Tabela Periódica/Revisão Representação esquemática
Biologia Estrutural. Espaço Recíproco e a Esfera de Ewald. Prof. Dr. Walter Filgueira de Azevedo Jr. wfdaj.sites.uol.com.br
 Biologia Estrutural Espaço Recíproco e a Esfera de Ewald Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Índices de Miller Índices de Direções Espaço Recíproco Esfera de Ewald Esfera Limite Número de
Biologia Estrutural Espaço Recíproco e a Esfera de Ewald Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Índices de Miller Índices de Direções Espaço Recíproco Esfera de Ewald Esfera Limite Número de
Ligações químicas. 1. Ligações Iônicas vs. Ligações covalentes 2. Modelo RPECV ou VSEPR 3. Teoria da Ligação de Valência.
 Ligações químicas 1. Ligações Iônicas vs. Ligações covalentes 2. Modelo RPECV ou VSEPR 3. Teoria da Ligação de Valência. Iônica X Covalente As ligações iônicas e covalentes são dois modelos extremos de
Ligações químicas 1. Ligações Iônicas vs. Ligações covalentes 2. Modelo RPECV ou VSEPR 3. Teoria da Ligação de Valência. Iônica X Covalente As ligações iônicas e covalentes são dois modelos extremos de
Conceitos de vetores. Decomposição de vetores
 Conceitos de vetores. Decomposição de vetores 1. Introdução De forma prática, o conceito de vetor pode ser bem assimilado com auxílio da representação matemática de grandezas físicas. Figura 1.1 Grandezas
Conceitos de vetores. Decomposição de vetores 1. Introdução De forma prática, o conceito de vetor pode ser bem assimilado com auxílio da representação matemática de grandezas físicas. Figura 1.1 Grandezas
Introdução à Física do Estado Sólido
 Introdução à Física do Estado Sólido Escritório: Edifício Alessandro Volta, Bloco C, sala 210. Fone: 3091-7041 (celular:98346-3882) e-mail: lassali@if.usp.br IFUSP 2º Semestre/2018 Introdução à Física
Introdução à Física do Estado Sólido Escritório: Edifício Alessandro Volta, Bloco C, sala 210. Fone: 3091-7041 (celular:98346-3882) e-mail: lassali@if.usp.br IFUSP 2º Semestre/2018 Introdução à Física
Aula 10 B Compostos de Coordenação Teorias de ligação Propriedades espectrais e magnéticas
 Aula 10 B Compostos de Coordenação Teorias de ligação Propriedades espectrais e magnéticas QFL 2129 Química Inorgânica 2017 Ana Maria da Costa Ferreira Alfred Werner Estrutura eletrônica dos compostos
Aula 10 B Compostos de Coordenação Teorias de ligação Propriedades espectrais e magnéticas QFL 2129 Química Inorgânica 2017 Ana Maria da Costa Ferreira Alfred Werner Estrutura eletrônica dos compostos
Aula15 COMPOSTOS ORGANOMETÁLICOS PARTE II. Anne Souza
 Aula15 COMPOSTOS ORGANOMETÁLICOS PARTE II META Apresentar a estrutura e métodos de síntese de alguns compostos organometálicos; Apresentar algumas aplicações dos compostos organometálicos; OBJETIVOS Ao
Aula15 COMPOSTOS ORGANOMETÁLICOS PARTE II META Apresentar a estrutura e métodos de síntese de alguns compostos organometálicos; Apresentar algumas aplicações dos compostos organometálicos; OBJETIVOS Ao
Teoria dos Orbitais Moleculares. Prof. Fernando R. Xavier
 Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008.
 UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
Análise de alimentos II Introdução aos Métodos Espectrométricos
 Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Universidade Tecnológica Federal do Paraná Campus Curitiba Departamento Acadêmico de Química e Biologia - DAQBI. Teoria VSEPR
 Universidade Tecnológica Federal do Paraná Campus Curitiba Departamento Acadêmico de Química e Biologia - DAQBI Teoria VSEPR O modelo Valence Shell Electron Pair Repulsion (VSEPR) ou Repulsão Eletrônica
Universidade Tecnológica Federal do Paraná Campus Curitiba Departamento Acadêmico de Química e Biologia - DAQBI Teoria VSEPR O modelo Valence Shell Electron Pair Repulsion (VSEPR) ou Repulsão Eletrônica
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA CONCEITOS BÁSICOS DE ESPECTROSCOPIA
 QFL5947-1onceitos Básicos de Espectroscopia 2011-2 UNIVERIDADE DE Ã PAUL INTITUT DE QUÍMIA Programa de Pós-Graduação em Química NEIT BÁI DE EPETRPIA QFL5947-1 3 a Prova de I.V.-Raman-2011 ETR AGUILAR VITRIN
QFL5947-1onceitos Básicos de Espectroscopia 2011-2 UNIVERIDADE DE Ã PAUL INTITUT DE QUÍMIA Programa de Pós-Graduação em Química NEIT BÁI DE EPETRPIA QFL5947-1 3 a Prova de I.V.-Raman-2011 ETR AGUILAR VITRIN
Bioquímica Inorgânica. 1º exame 18 de Junho de 2014
 Nº Nome Bioquímica Inorgânica 1º exame 18 de Junho de 2014 Duração: 3h00. Leia todo o enunciado antes de começar a responder. Justifique as respostas. RESPONDA APENAS NOS ESPAÇOS ASSINALADOS. I (1,5) Alguns
Nº Nome Bioquímica Inorgânica 1º exame 18 de Junho de 2014 Duração: 3h00. Leia todo o enunciado antes de começar a responder. Justifique as respostas. RESPONDA APENAS NOS ESPAÇOS ASSINALADOS. I (1,5) Alguns
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia. Dr. Tiago P. Camargo
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Dr. Tiago P. Camargo Forma das moléculas Correlação da geometria com propriedades físico-químicas Instável Instável
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Dr. Tiago P. Camargo Forma das moléculas Correlação da geometria com propriedades físico-químicas Instável Instável
aula6 Projeções Planas 2017/2 IC / UFF
 http://computacaografica.ic.uff.br/conteudocap2.html aula6 P p O Projeções Planas 2017/2 IC / UFF Relembrando Transformações De corpo rígido (semelhança). Distância entre 2 pontos quaisquer é inalterada.
http://computacaografica.ic.uff.br/conteudocap2.html aula6 P p O Projeções Planas 2017/2 IC / UFF Relembrando Transformações De corpo rígido (semelhança). Distância entre 2 pontos quaisquer é inalterada.
Problemas de Química-Física 20015/2016
 Problemas de Química-Física 0015/016 Capítulo 5 - Espectroscopia Rotacional, Vibracional, Rotovibracional e Electrónica 1 O espectro rotacional da molécula 1 C 3 S tem as seguintes riscas (em MHz): Risca
Problemas de Química-Física 0015/016 Capítulo 5 - Espectroscopia Rotacional, Vibracional, Rotovibracional e Electrónica 1 O espectro rotacional da molécula 1 C 3 S tem as seguintes riscas (em MHz): Risca
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Síntese de compostos carbonílicos São conhecidos vários caminhos para preparação destes compostos: Reação direta
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Síntese de compostos carbonílicos São conhecidos vários caminhos para preparação destes compostos: Reação direta
Estrutura da Matéria Prof.ª Fanny Nascimento Costa
 Estrutura da Matéria Prof.ª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 10 Hibridização Teoria da ligação de valência Formas Espaciais Moleculares As estruturas de Lewis fornecem a conectividade
Estrutura da Matéria Prof.ª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 10 Hibridização Teoria da ligação de valência Formas Espaciais Moleculares As estruturas de Lewis fornecem a conectividade
Modelagem Cinemática de Robôs Industriais. Prof. Assoc. Mário Luiz Tronco
 Modelagem Cinemática de Robôs Industriais Prof. Assoc. Mário Luiz Tronco Transformação direta de coordenadas 1 2... N Variáveis de junta Variáveis cartesianas Transformação inversa de coordenadas Transformação
Modelagem Cinemática de Robôs Industriais Prof. Assoc. Mário Luiz Tronco Transformação direta de coordenadas 1 2... N Variáveis de junta Variáveis cartesianas Transformação inversa de coordenadas Transformação
Análise de Alimentos II Espectroscopia de Absorção Molecular
 Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Esse é um exemplo do fenômeno denominado isomeria. O estudo da isomeria será dividido em duas partes: plana e espacial (estereoisomeria).
 ISOMERIA O QUE É ISOMERIA? Quando se substitui um átomo de hidrogênio do etano por um átomo de cloro, pode-se obter somente uma substância, pois, qualquer que seja o hidrogênio substituído, a estrutura
ISOMERIA O QUE É ISOMERIA? Quando se substitui um átomo de hidrogênio do etano por um átomo de cloro, pode-se obter somente uma substância, pois, qualquer que seja o hidrogênio substituído, a estrutura
Os orbitais 2p (3 orb p = px + py + pz ) estão na segunda camada energética, portanto mais afastados que o orbital esférico 2s, logo mais energético.
 1 - Introdução Os elementos mais importantes para a química orgânica são C, H, N e O. Estes elementos estão nos dois primeiros períodos da tabela periódica e os seus elétrons estão distribuídos próximos
1 - Introdução Os elementos mais importantes para a química orgânica são C, H, N e O. Estes elementos estão nos dois primeiros períodos da tabela periódica e os seus elétrons estão distribuídos próximos
Aula 2. Organic Chemistry. Espectroscopia UV-VIS e Infravermelho. 4 th Edition Paula Yurkanis Bruice
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 2 Espectroscopia UV-VIS e Infravermelho Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Radiação Eletromagnética E
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 2 Espectroscopia UV-VIS e Infravermelho Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Radiação Eletromagnética E
Pró-Reitoria de Graduação. Plano de Ensino 1º Quadrimestre de Caracterização da disciplina Código da NHT Nome da Química de Coordenação
 Caracterização da disciplina Código da NHT4052.15 Nome da Química de Coordenação disciplina: disciplina: Créditos (T-P- (4-4-8) Carga 96 horas Aula prática: Câmpus: SA I): horária: Código da Turma: Turno:
Caracterização da disciplina Código da NHT4052.15 Nome da Química de Coordenação disciplina: disciplina: Créditos (T-P- (4-4-8) Carga 96 horas Aula prática: Câmpus: SA I): horária: Código da Turma: Turno:
Universidade de Aveiro Departamento de Electrónica, Telecomunicações e Informática. Transformações 2D
 Universidade de Aveiro Departamento de Electrónica, Telecomunicações e Informática Transformações 2D Computação Visual Beatriz Sousa Santos, Joaquim Madeira Transformações 2D Posicionar, orientar e escalar
Universidade de Aveiro Departamento de Electrónica, Telecomunicações e Informática Transformações 2D Computação Visual Beatriz Sousa Santos, Joaquim Madeira Transformações 2D Posicionar, orientar e escalar
Geometria molecular :
 CIÊNCIAS DA NATUREZA - QUÍMICA Prof. Adriana Strelow 1º Ano - 2017 Geometria molecular : Forma como os átomos estão espacialmente dispostos em uma molécula. A geometria de uma molécula depende do número
CIÊNCIAS DA NATUREZA - QUÍMICA Prof. Adriana Strelow 1º Ano - 2017 Geometria molecular : Forma como os átomos estão espacialmente dispostos em uma molécula. A geometria de uma molécula depende do número
SEMINÁRIO As simetrias dos orbitais: Construção dos orbitais moleculares, exemplos e aplicações
 UNIVERSIDADE FEDERAL DE SERGIPE CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIAS DEPARTAMENTO DE QUÍMICA NPGQ SEMINÁRIO As simetrias dos orbitais: Construção dos orbitais moleculares, exemplos e aplicações Isaac
UNIVERSIDADE FEDERAL DE SERGIPE CENTRO DE CIÊNCIAS EXATAS E TECNOLOGIAS DEPARTAMENTO DE QUÍMICA NPGQ SEMINÁRIO As simetrias dos orbitais: Construção dos orbitais moleculares, exemplos e aplicações Isaac
Polaridade das moléculas
 Ligação covalente apolar Ligação covalente em que os eletrões ligantes são igualmente partilhados pelos átomos unidos. A ligação covalente numa molécula diatómica homonuclear, isto é, formada por dois
Ligação covalente apolar Ligação covalente em que os eletrões ligantes são igualmente partilhados pelos átomos unidos. A ligação covalente numa molécula diatómica homonuclear, isto é, formada por dois
Algumas EXCEÇÕES à TEORIA DO OCTETO. H Be H. H Be H. O berílio ficou estável com 4 elétrons na camada de valência
 Algumas EXCEÇÕES à TEORIA DO OCTETO H Be H H Be H O berílio ficou estável com 4 elétrons na camada de valência Algumas EXCEÇÕES à TEORIA DO OCTETO B B O boro ficou estável com 6 elétrons na camada de valência
Algumas EXCEÇÕES à TEORIA DO OCTETO H Be H H Be H O berílio ficou estável com 4 elétrons na camada de valência Algumas EXCEÇÕES à TEORIA DO OCTETO B B O boro ficou estável com 6 elétrons na camada de valência
Respostas Esperadas Prova do PPG/IQ-PS
 Respostas Esperadas Prova do PPG/IQ-PS 2018-2 Q1) Para cada uma das espécies abaixo: i) desenhe a estrutura de Lewis atribuindo as cargas formais de cada átomo; ii) indique a forma geométrica; iii) indique
Respostas Esperadas Prova do PPG/IQ-PS 2018-2 Q1) Para cada uma das espécies abaixo: i) desenhe a estrutura de Lewis atribuindo as cargas formais de cada átomo; ii) indique a forma geométrica; iii) indique
Polaridade molecular
 Polaridade molecular Relembrando: Eletronegatividade Nuvem eletrônica Relembrando: Eletronegatividade É a capacidade (ou tendência) do átomo em atrair elétrons para si Nuvem eletrônica Relembrando: Eletronegatividade
Polaridade molecular Relembrando: Eletronegatividade Nuvem eletrônica Relembrando: Eletronegatividade É a capacidade (ou tendência) do átomo em atrair elétrons para si Nuvem eletrônica Relembrando: Eletronegatividade
FCAV/ UNESP. DISCIPLINA: Química Orgânica. ASSUNTO: Isomeria
 FCAV/ UNESP DISCIPLINA: Química Orgânica ASSUNTO: Isomeria Prof a. Dr a. Luciana Maria Saran 1 1. ISÔMEROS Isômeros: dois ou mais compostos diferentes que apresentam a mesma fórmula molecular. Isomeria
FCAV/ UNESP DISCIPLINA: Química Orgânica ASSUNTO: Isomeria Prof a. Dr a. Luciana Maria Saran 1 1. ISÔMEROS Isômeros: dois ou mais compostos diferentes que apresentam a mesma fórmula molecular. Isomeria
INSTITUTO DE QUÍMICA da UFRJ DEPARTAMENTO DE QUÍMICA INORGÂNICA
 Programa de Disciplina Nome: Química Inorgânica I Código: IQG 354 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4
Programa de Disciplina Nome: Química Inorgânica I Código: IQG 354 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4
Teoria da Ligação Covalente. Teoria da Ligação de Valência (TLV)
 Teoria da Ligação Covalente Teoria da Ligação de Valência (TLV) Teoria da Ligação Covalente Teorias de Lewis e VSEPR identificam: - Pares de elétrons ligados - Pares de elétrons isolados - Forma molecular
Teoria da Ligação Covalente Teoria da Ligação de Valência (TLV) Teoria da Ligação Covalente Teorias de Lewis e VSEPR identificam: - Pares de elétrons ligados - Pares de elétrons isolados - Forma molecular
Complexos: Estrutura
 Complexos: estrutura 1 Complexos: Estrutura Teoria do Campo Ligante (ou Campo Cristalino) Campo octaédrico Campo esférico α 4 =6Dq 2 / 3 α 4 =4Dq Dq= Ze2 r 4 6 a 5 r 4 =r 4 médio doselétrons d a=distância
Complexos: estrutura 1 Complexos: Estrutura Teoria do Campo Ligante (ou Campo Cristalino) Campo octaédrico Campo esférico α 4 =6Dq 2 / 3 α 4 =4Dq Dq= Ze2 r 4 6 a 5 r 4 =r 4 médio doselétrons d a=distância
Chemistry 140 Fall 2002
 Ligações Químicas: Parte II Conteúdo O Que se Espera de uma Teoria de Ligação Introdução ao método da Ligação de Valência Hibridização de Orbitais Atômicos Ligações Covalentes Múltiplas Teoria de Orbitais
Ligações Químicas: Parte II Conteúdo O Que se Espera de uma Teoria de Ligação Introdução ao método da Ligação de Valência Hibridização de Orbitais Atômicos Ligações Covalentes Múltiplas Teoria de Orbitais
CURSO DE CIÊNCIAS BIOLÓGICAS DISCIPLINA: Química Geral. ASSUNTO: Formas e Polaridade das Moléculas. Prof a. Dr a. Luciana M. Saran
 CURSO DE CIÊNCIAS BIOLÓGICAS DISCIPLINA: Química Geral ASSUNTO: Formas e Polaridade das Moléculas Prof a. Dr a. Luciana M. Saran 1 I. INTRODUÇÃO Qual a importância de conhecermos as formas das moléculas?
CURSO DE CIÊNCIAS BIOLÓGICAS DISCIPLINA: Química Geral ASSUNTO: Formas e Polaridade das Moléculas Prof a. Dr a. Luciana M. Saran 1 I. INTRODUÇÃO Qual a importância de conhecermos as formas das moléculas?
ROBÓTICA TRANSFORMAÇÕES MATRICIAIS. Prof a. Dra. GIOVANA TRIPOLONI TANGERINO Tecnologia em Automação Industrial
 SP CAMPUS PIRACICABA ROBÓTICA Prof a. Dra. GIOVANA TRIPOLONI TANGERINO Tecnologia em Automação Industrial TRANSFORMAÇÕES MATRICIAIS https://giovanatangerino.wordpress.com giovanatangerino@ifsp.edu.br giovanatt@gmail.com
SP CAMPUS PIRACICABA ROBÓTICA Prof a. Dra. GIOVANA TRIPOLONI TANGERINO Tecnologia em Automação Industrial TRANSFORMAÇÕES MATRICIAIS https://giovanatangerino.wordpress.com giovanatangerino@ifsp.edu.br giovanatt@gmail.com
Experimento 3A: A QUÍMICA DOS COMPOSTOS DE COORDENAÇÃO E A ESPECTROSCOPIA
 Universidade Federal do Paraná Departamento de Química Disciplina: Química Inorgânica e Experimental CQ071 Curso: Licenciatura e Bacharelado em Química Professor: Shirley Nakagaki Experimento 3A: A QUÍMICA
Universidade Federal do Paraná Departamento de Química Disciplina: Química Inorgânica e Experimental CQ071 Curso: Licenciatura e Bacharelado em Química Professor: Shirley Nakagaki Experimento 3A: A QUÍMICA
Teorias de Ligação. Teoria da Ligação de Valência. Ligações s e p Hibridização de orbitais Ligações dos hidrocarbonetos
 Teorias de Ligação Ligações s e p Hibridização de orbitais Ligações dos hidrocarbonetos Orbitais e Teorias de Ligação Estruturas de Lewis Elétrons localizados? Elétrons de valência responsáveis pelas ligações
Teorias de Ligação Ligações s e p Hibridização de orbitais Ligações dos hidrocarbonetos Orbitais e Teorias de Ligação Estruturas de Lewis Elétrons localizados? Elétrons de valência responsáveis pelas ligações
2.1 Princípios gerais da ligação química. Ligações químicas
 2.1 Princípios gerais da ligação química Ligações químicas A associação de átomos formando moléculas, ou em agregados de maiores dimensões como, por exemplo, nos metais, é possível pelo estabelecimento
2.1 Princípios gerais da ligação química Ligações químicas A associação de átomos formando moléculas, ou em agregados de maiores dimensões como, por exemplo, nos metais, é possível pelo estabelecimento
Estrutura Molecular, Ligações Químicas e Propriedades dos Compostos Orgânicos
 Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Profa. Roberlucia A. Candeia Disciplina: Química Orgânica Estrutura Molecular, Ligações Químicas e Propriedades dos
Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Profa. Roberlucia A. Candeia Disciplina: Química Orgânica Estrutura Molecular, Ligações Químicas e Propriedades dos
Álgebra Linear I - Aula Bases Ortonormais e Matrizes Ortogonais
 Álgebra Linear I - Aula 19 1. Bases Ortonormais e Matrizes Ortogonais. 2. Matrizes ortogonais 2 2. 3. Rotações em R 3. Roteiro 1 Bases Ortonormais e Matrizes Ortogonais 1.1 Bases ortogonais Lembre que
Álgebra Linear I - Aula 19 1. Bases Ortonormais e Matrizes Ortogonais. 2. Matrizes ortogonais 2 2. 3. Rotações em R 3. Roteiro 1 Bases Ortonormais e Matrizes Ortogonais 1.1 Bases ortogonais Lembre que
