INSTITUTO DE QUÍMICA da UFRJ DEPARTAMENTO DE QUÍMICA INORGÂNICA. Programa de Disciplina. Química Inorgânica EQ. Nome: Código: IQG 244 CARACTERÍSTICAS
|
|
|
- Wagner Galvão Coelho
- 6 Há anos
- Visualizações:
Transcrição
1 Programa de Disciplina Nome: Química Inorgânica EQ Código: IQG 244 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4 OBRIGATÓRIA 4 (TEÓRICA) Pré-Requisito para a Disciplina: QUÍMICA EXPERIMENTAL EQ (IQG 231) Cursos para os quais a Disciplina é Indicada: ENGENHARIA DE BIOPROCESSOS, ENGENHARIA DE ALIMENTOS, ENGENHARIA QUÍMICA, QUÍMICA INDUSTRIAL. 1 / 5
2 PROGRAMA ANALÍTICO 1 SIMETRIA. (CARGA HORÁRIA RECOMENDADA 8 HORAS) 1.1 Operações de Simetria. 1.2 Elementos de Simetria. 1.3 Grupos de Pontos. 1.4 Determinação do Grupo de Pontos de uma Molécula ou Íon. 1.5 Representação Matricial das Operações de Simetria. 1.6 Tabelas de Caracteres. 1.7 Produto Direto. 1.8 Representações Redutíveis e Irredutíveis. 2 ESTRUTURA E PROPRIEDADES ATÔMICAS. (CARGA HORÁRIA RECOMENDADA 6 HORAS) 2.1 Orbitais Hidrogenóides. 2.2 Funções de Onda Radiais e Funções Probabilidade Radial para Vários Valores de n e l diferentes. 2.3 Funções de Onda Angulares. 2.4 Forma dos Orbitais s, p, d e f. 2.5 Configuração Eletrônica dos Elementos. 2.6 Princípio de Exclusão de PAULI. 2.7 Regra de HUND da Multiplicidade Máxima. 2.8 Estados Atômicos. 2.9 Termos Espectrais Acoplamento Spin-Órbita Blindagem 2.12 Regras de SLATER Raio Iônico e Covalente Potencial de Ionização Afinidade ao Életron. 2 / 5
3 3 ELETRONEGATIVIDADE. (CARGA HORÁRIA RECOMENDADA 4 HORAS) 3.1 Escala de PAULING. 3.2 Outras Escalas de Eletronegatividade. 3.3 Eletronegatividade de Grupo. 3.4 Princípio da Equalização da Eletronegatividade. 3.5 Medida Experimental da Distribuição de Cargas em Moléculas. 3.6 Momentos Dipolares. 4 LIGAÇÃO QUÍMICA. (CARGA HORÁRIA RECOMENDADA 8 HORAS) 4.1 Orbitais Moleculares de Moléculas Diatômicas Homonucleares. 4.2 Orbitais Moleculares de Moléculas Diatômicas Heteronucleares. 4.3 Orbitais Moleculares de Moléculas e Íons Polinucleares. 4.4 Espectroscopia Fotoeletrônica e a Ordem Energética dos Orbitais Moleculares. 4.5 Diagramas de Correlação. 4.6 Teoria de Grupo e a Classificação dos Orbitais Moleculares. 5 ESTADO SÓLIDO. (CARGA HORÁRIA RECOMENDADA 10 HORAS) 5.1 Periodicidade de Sólidos. 5.2 Células Unitárias e Redes de BRAVAIS. 5.3 Classificação das Ligações em Sólidos. 5.4 Energia da Rede Cristalina e o Ciclo BORN-HABER. 5.5 Efeitos dos Raios Iônicos sobre a Estabilidade das Estruturas. 5.6 Propriedades de Sólidos Condutores e Semi-Condutores. 6 FORÇAS E INTERAÇÕES INTERMOLECULARES. (CARGA HORÁRIA RECOMENDADA 6 HORAS) 6.1 Raio de VAN DER WAALS, Iônico e Covalente e as Distâncias Internucleares. 6.2 Forças Químicas: Ligação Covalente, Iônica, Íon-Dipolo, Dipolo-Dipolo, Dipolo- Dipolo Induzido, Forças de Dispersão ou de LONDON, Forças Repulsivas. 6.3 Ligação Hidrogênio. 6.4 Hidratos e Clatratos. 6.5 Efeito das Forças Químicas sobre os Pontos de Fusão e Ebulição e sobre a Solubilidade. 3 / 5
4 7 QUÍMICA ÁCIDO-BASE. (CARGA HORÁRIA RECOMENDADA 10 HORAS) 7.1 Ácidos e Bases Duros e Moles. 7.2 Simbiose. 7.3 Ácidos de LEWIS de Alguns Elementos Representativos: Haletos de Boro e Alumínio, Complexos de Silício e Estanho, Ácidos dos Grupos do Nitrogênio e do Oxigênio, Ácidos Halogenados. 7.4 Reações Ácido-Base Heterogêneas: Acidez das Superfícies da Alumina, Aluminossilicatos e Sílica. 7.5 Solventes Não Aquosos. 7.6 Efeito Nivelador e Diferenciador. 7.7 Superácidos. 7.8 Equação de DRAGO. 7.9 Orbitais de Fronteira e as Reações Ácido-Base Orbitais Moleculares e o Conceito de Dureza e Moleza. 8 OXIRREDUÇÃO. (CARGA HORÁRIA RECOMENDADA 8 HORAS) 8.1 Extração dos Elementos. 8.2 Diagramas de ELLINGHAM. 8.3 Processos Envolvendo Reduções: Extração Pirometalúrgica, Hidrometalúrgica e Eletrolítica. 8.4 Processos Envolvendo Oxidações. 8.5 Fatores Cinéticos. 8.6 Estabilidade em Água. 8.7 Desproporcionação e Oxidação pelo Oxigênio Atmosférico. 8.8 Diagramas de LATIMER e FROST. 8.9 Efeito do ph Diagramas de POURBAIX Efeito da Complexação sobre o Potencial Tendências Periódicas sobre a Estabilidade dos Estados de Oxidação dos Metais do Bloco p, d e f. 4 / 5
5 LIVROS RECOMENDADOS. 1 Principles of Structure and Reactivity ; HUHEEY J. E.; KEITER E. A.; KEITER R. L.; 1993, 4 th. Edition; HarperCollins College Publishers. 2 Chemical Applications of Group Theory ; COTTON, F. A.; 1990, 3 rd. Edition; John Wiley & Sons, Inc.. 3 Shriver & Atkins Inorganic Chemistry ; ATKINS P. W., OVERTON, T.; ROURKE, J.; WELLER, M.; ARMSTRONG, F.; 2006, 4 th Edition; Oxford University Press. 4 Shriver & Atkins Química Inorgânica ; ATKINS P. W., OVERTON, T.; ROURKE, J.; WELLER, M.; ARMSTRONG, F.; 2008, 4a Edição; Artmed Editora S.A. 5 Inorganic Chemistry ; KOTZ J. C., PURCEL K. F.; 1977 (reimpresso em 1987); Holt-Saunders International Edition.. 6 Concepts and Models of Inorganic Chemistry ; DOUGLAS B., McDANIEL D. H., ALEXANDER J. J.; 1994, 2 rd. Edition; John Wiley & Sons, Inc.. 7 Química Inorgânica ; HOUSECROFT, C.E.; SHARPE, A. G.; 2012, 4a Edição; LTC Livros Técnicos e Científicos Editora Ltda. 5 / 5
Programa de Disciplina CARACTERÍSTICAS OBRIGATÓRIA 4 (TEÓRICA) NENHUM
 Programa de Disciplina Nome: Química Geral I Código: IQG 114 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4 OBRIGATÓRIA
Programa de Disciplina Nome: Química Geral I Código: IQG 114 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4 OBRIGATÓRIA
Programa Analítico de Disciplina QUI120 Química Inorgânica I
 0 Programa Analítico de Disciplina Departamento de Química - Centro de Ciências Exatas e Tecnológicas Número de créditos: 5 Teóricas Práticas Total Duração em semanas: 15 Carga horária semanal 3 2 5 Períodos
0 Programa Analítico de Disciplina Departamento de Química - Centro de Ciências Exatas e Tecnológicas Número de créditos: 5 Teóricas Práticas Total Duração em semanas: 15 Carga horária semanal 3 2 5 Períodos
Interações Atômicas e Moleculares
 Interações Atômicas e Moleculares Código da disciplina: BCK0104-15 (antes: BC0104) TPI: 3-0-4. Carga Horária: 36hs. Coordenador: Prof. Dr. Alexsandre F. Lago Ementa resumida: Fundamentos de mecânica-quântica
Interações Atômicas e Moleculares Código da disciplina: BCK0104-15 (antes: BC0104) TPI: 3-0-4. Carga Horária: 36hs. Coordenador: Prof. Dr. Alexsandre F. Lago Ementa resumida: Fundamentos de mecânica-quântica
Sumário. 1 Introdução: matéria e medidas 1. 2 Átomos, moléculas e íons Estequiometria: cálculos com fórmulas e equações químicas 67
 Prefácio 1 Introdução: matéria e medidas 1 1.1 O estudo da química 1 1.2 Classificações da matéria 3 1.3 Propriedades da matéria 8 1.4 Unidades de medida 12 1.5 Incerteza na medida 18 1.6 Análise dimensional
Prefácio 1 Introdução: matéria e medidas 1 1.1 O estudo da química 1 1.2 Classificações da matéria 3 1.3 Propriedades da matéria 8 1.4 Unidades de medida 12 1.5 Incerteza na medida 18 1.6 Análise dimensional
PROPRIEDADES PERIÓDIOCAS
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I PROPRIEDADES PERIÓDIOCAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br Sala GQI 308,
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I PROPRIEDADES PERIÓDIOCAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br Sala GQI 308,
Ligações Químicas - I
 Ligações Químicas - I Orbitais atômicos e números quânticos A tabela periódica; propriedades Ligações químicas A ligação iônica Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
Ligações Químicas - I Orbitais atômicos e números quânticos A tabela periódica; propriedades Ligações químicas A ligação iônica Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
Ministério da Educação Universidade Federal do Paraná Setor Palotina
 Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 7 Ligação Iônica Prof. Isac G. Rosset Prof. Isac G. Rosset - UFPR - Palotina - Ciências Exatas 13 1 Ligações fortes: Ligações fracas:
Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 7 Ligação Iônica Prof. Isac G. Rosset Prof. Isac G. Rosset - UFPR - Palotina - Ciências Exatas 13 1 Ligações fortes: Ligações fracas:
ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento;
 1.1 CONCEITOS FUNDAMENTAIS ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento; Elétrons e prótons são eletricamente carregados: 1,60 x 10-19 C; Elétrons:
1.1 CONCEITOS FUNDAMENTAIS ÁTOMO: núcleo muito pequeno composto por prótons e nêutrons, que é circundado por elétrons em movimento; Elétrons e prótons são eletricamente carregados: 1,60 x 10-19 C; Elétrons:
UNIVERSIDADE FEDERAL DE SANTA CATARINA CENTRO DE CIÊNCIAS FÍSICAS E MATEMÁTICAS DEPARTAMENTO DE QUÍMICA
 UNIVERSIDADE FEDERAL DE SANTA CATARINA CENTRO DE CIÊNCIAS FÍSICAS E MATEMÁTICAS DEPARTAMENTO DE QUÍMICA Campus Universitário -Trindade - 88040-900 - Florianópolis - SC - Brasil Fone: (048) 3721-6852 Disciplina:
UNIVERSIDADE FEDERAL DE SANTA CATARINA CENTRO DE CIÊNCIAS FÍSICAS E MATEMÁTICAS DEPARTAMENTO DE QUÍMICA Campus Universitário -Trindade - 88040-900 - Florianópolis - SC - Brasil Fone: (048) 3721-6852 Disciplina:
LICENCIATURA EM QUÍMICA QUÍMICA
 Programa de Disciplina Nome: Química Geral II IQ Código: IQG 120 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4
Programa de Disciplina Nome: Química Geral II IQ Código: IQG 120 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4
CURSO: FARMÁCIA INFORMAÇÕES BÁSICAS
 Turno: Integral Currículo 2014 Período 1º Período Tipo Obrigatória Teórica 72 horas CURSO: FARMÁCIA INFORMAÇÕES BÁSICAS Unidade curricular Química Fundamental Carga Horária Prática ----- Habilitação /
Turno: Integral Currículo 2014 Período 1º Período Tipo Obrigatória Teórica 72 horas CURSO: FARMÁCIA INFORMAÇÕES BÁSICAS Unidade curricular Química Fundamental Carga Horária Prática ----- Habilitação /
2.2.1 Efeito Hall e Magnetoresistência Condutividade Elétrica AC Corrente Elétrica em um Campo Magnético
 Conteúdo 1 Revisão de Física Moderna 1 1.1 Equação de Schrödinger; Autoestados e Valores Esperados.. 1 1.2 O Poço de Potencial Innito:Quantização da Energia.............................. 7 1.3 O Oscilador
Conteúdo 1 Revisão de Física Moderna 1 1.1 Equação de Schrödinger; Autoestados e Valores Esperados.. 1 1.2 O Poço de Potencial Innito:Quantização da Energia.............................. 7 1.3 O Oscilador
Estrutura dos Materiais. e Engenharia dos Materiais Prof. Douglas Gouvêa
 Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
CAPÍTULO 1 Quantidades e Unidades 1. CAPÍTULO 2 Massa Atômica e Molecular; Massa Molar 16. CAPÍTULO 3 O Cálculo de Fórmulas e de Composições 26
 Sumário CAPÍTULO 1 Quantidades e Unidades 1 Introdução 1 Os sistemas de medida 1 O Sistema Internacional de Unidades (SI) 1 A temperatura 2 Outras escalas de temperatura 3 O uso e o mau uso das unidades
Sumário CAPÍTULO 1 Quantidades e Unidades 1 Introdução 1 Os sistemas de medida 1 O Sistema Internacional de Unidades (SI) 1 A temperatura 2 Outras escalas de temperatura 3 O uso e o mau uso das unidades
Princípios fisico-químicos laboratoriais. Aula 08 Profº Ricardo Dalla Zanna
 Princípios fisico-químicos laboratoriais Aula 08 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 3 Química orgânica o Seção 3.1 Ligação e estrutura molecular o Seção 3.2 Funções orgânicas - Hidrocarbonetos
Princípios fisico-químicos laboratoriais Aula 08 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 3 Química orgânica o Seção 3.1 Ligação e estrutura molecular o Seção 3.2 Funções orgânicas - Hidrocarbonetos
O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS.
 Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
LIGAÇÕES QUÍMICAS. Prof. Marcel Piovezan. Curso Superior de Tecnologia em Processos Químicos
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES LIGAÇÕES QUÍMICAS Prof. Marcel Piovezan marcel.piovezan@ifsc.edu.br
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES LIGAÇÕES QUÍMICAS Prof. Marcel Piovezan marcel.piovezan@ifsc.edu.br
Química Inorgânica Avançada
 Disciplina: Química Inorgânica Avançada (obrigatória) Créditos: 04 Carga Horária: 60 horas Docente: Antonio Reinaldo Cestari arcestari@gmail.com Sala 23, DQI-UFS Ementa: Química de Coordenação. Definições,
Disciplina: Química Inorgânica Avançada (obrigatória) Créditos: 04 Carga Horária: 60 horas Docente: Antonio Reinaldo Cestari arcestari@gmail.com Sala 23, DQI-UFS Ementa: Química de Coordenação. Definições,
Propriedades da tabela periódica
 Propriedades da tabela periódica Química Geral Prof. Edson Nossol Uberlândia, 30/09/2016 calcogênioos halogênios Metais alcalinos Metais alcalinos terrosos Gases nobres Metais de transição Dimitris Mendeliev
Propriedades da tabela periódica Química Geral Prof. Edson Nossol Uberlândia, 30/09/2016 calcogênioos halogênios Metais alcalinos Metais alcalinos terrosos Gases nobres Metais de transição Dimitris Mendeliev
Estrutura da Matéria Profª Fanny Nascimento Costa
 Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
Sumário. Unidade II Propriedades dos materiais 40. Introdução ao estudo da Química 14. Unidade I. Capítulo 2 Unidades de medida...
 Sumário Unidade I Capítulo 1 Introdução ao estudo da Química 14 Química: objeto de estudo e aplicações... 16 1. Química: a ciência que estuda a matéria... 17 Matéria... 17 Características da matéria...
Sumário Unidade I Capítulo 1 Introdução ao estudo da Química 14 Química: objeto de estudo e aplicações... 16 1. Química: a ciência que estuda a matéria... 17 Matéria... 17 Características da matéria...
UNIVERSIDADE PRESBITERIANA MACKENZIE Decanato Acadêmico
 Unidade Universitária: Escola de Engenharia Curso: QUÍMICA Núcleo Temático: Matemática, Física e Química Básica Disciplina: Química Fundamental Código da Disciplina: 060.1104.7 Professor(es): ANA CRISTINA
Unidade Universitária: Escola de Engenharia Curso: QUÍMICA Núcleo Temático: Matemática, Física e Química Básica Disciplina: Química Fundamental Código da Disciplina: 060.1104.7 Professor(es): ANA CRISTINA
QB70C:// Química (Turmas S71/S72) Ligação Química
 QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
Equações-chave FUNDAMENTOS. Seção A. Seção E. Seção F. Seção G. mv 2. E c E P. mgh. Energia total energia cinética energia potencial, ou E E c.
 Equações-chave FUNDAMENTOS Seção A 3 A energia cinética de uma partícula de massa m relaciona-se com sua velocidade v, por: E c mv 2 4 Um corpo de massa m que está a uma altura h da Terra tem energia potencial
Equações-chave FUNDAMENTOS Seção A 3 A energia cinética de uma partícula de massa m relaciona-se com sua velocidade v, por: E c mv 2 4 Um corpo de massa m que está a uma altura h da Terra tem energia potencial
Universidade Federal de Sergipe Departamento de Química. Disciplina de Química I. Prof. Dr. Adriano Bof de Oliveira. São Cristóvão, 2011
 Universidade Federal de Sergipe Departamento de Química Disciplina de Química I Prof. Dr. Adriano Bof de Oliveira São Cristóvão, 2011 Avaliações Datas: 21 e 29 de julho Locais: Didática 4 Turma M1 Sala
Universidade Federal de Sergipe Departamento de Química Disciplina de Química I Prof. Dr. Adriano Bof de Oliveira São Cristóvão, 2011 Avaliações Datas: 21 e 29 de julho Locais: Didática 4 Turma M1 Sala
PLANO DE ENSINO ENGENHARIA DE BIOPROCESSOS INFORMAÇÕES BÁSICAS. Unidade curricular. Carga Horária Prática - Grau acadêmico / Habilitação
 PLANO DE ENSINO ENGENHARIA DE BIOPROCESSOS Turno: Integral Currículo: 2010 INFORMAÇÕES BÁSICAS Unidade curricular Departamento Química Geral DQBIO Período 2017/2 Teórica 54h Carga Horária Prática Total
PLANO DE ENSINO ENGENHARIA DE BIOPROCESSOS Turno: Integral Currículo: 2010 INFORMAÇÕES BÁSICAS Unidade curricular Departamento Química Geral DQBIO Período 2017/2 Teórica 54h Carga Horária Prática Total
Curso Preparatório para o Ingresso no Ensino Superior (Pré-Vestibular)
 Curso Preparatório para o Ingresso no Ensino Superior (Pré-Vestibular) Os conteúdos conceituais de Química estão distribuídos em 5 frentes. Química Extensivo A)Meio ambiente; estrutura atômica; Classificação
Curso Preparatório para o Ingresso no Ensino Superior (Pré-Vestibular) Os conteúdos conceituais de Química estão distribuídos em 5 frentes. Química Extensivo A)Meio ambiente; estrutura atômica; Classificação
Como classificar os elementos. Classificação periódica dos elementos químicos. As tríades de Döbereiner. Lei das oitavas 06/09/2017
 Como classificar os elementos Classificação periódica dos elementos químicos 1650: prata, arsênio, ouro, carbono, cobre, ferro, mercúrio, chumbo, enxofre, antimônio e estanho; Hemnning Brand: tentando
Como classificar os elementos Classificação periódica dos elementos químicos 1650: prata, arsênio, ouro, carbono, cobre, ferro, mercúrio, chumbo, enxofre, antimônio e estanho; Hemnning Brand: tentando
FORÇAS INTERMOLECULARES
 FORÇAS INTERMOLECULARES São as forças que mantêm os sólidos e líquidos unidos. A ligação covalente que mantém uma molécula unida é uma força intramolecular. A atração entre moléculas é uma força intermolecular.
FORÇAS INTERMOLECULARES São as forças que mantêm os sólidos e líquidos unidos. A ligação covalente que mantém uma molécula unida é uma força intramolecular. A atração entre moléculas é uma força intermolecular.
Disciplina de Didáctica da Química I
 Disciplina de Didáctica da Química I Texto de Apoio Estrutura dos átomos no ensino básico e secundário Visão crítica / síntese dos tópicos de química nos ensinos básico e secundário A - ESTRUTURA DOS ÁTOMOS
Disciplina de Didáctica da Química I Texto de Apoio Estrutura dos átomos no ensino básico e secundário Visão crítica / síntese dos tópicos de química nos ensinos básico e secundário A - ESTRUTURA DOS ÁTOMOS
LUAULA. Professor: Eduardo Ulisses
 LUAULA Professor: Eduardo Ulisses Sobre as ligações químicas, analise as afirmativas. I. Nas estruturas de Lewis, a ligação covalente resulta do compartilhamento de um par de elétrons entre dois átomos.
LUAULA Professor: Eduardo Ulisses Sobre as ligações químicas, analise as afirmativas. I. Nas estruturas de Lewis, a ligação covalente resulta do compartilhamento de um par de elétrons entre dois átomos.
N P P N. Ciências de Materiais I Prof. Nilson C. Cruz. Aula 2 Ligação Química. Átomos. Diferença entre materiais = Diferença entre arranjos atômicos e
 Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais
 Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
QUIMICA ORGÂNICA BÁSICA
 QUIMICA ORGÂNICA BÁSICA Estrutura Molecular Conceitos Básicos 1 A estrutura do átomo Distribuição de elétrons Mecânica Quântica Camadas e Orbitais atômicos Configuração eletrônica Construção Diagrama Princípio
QUIMICA ORGÂNICA BÁSICA Estrutura Molecular Conceitos Básicos 1 A estrutura do átomo Distribuição de elétrons Mecânica Quântica Camadas e Orbitais atômicos Configuração eletrônica Construção Diagrama Princípio
PROGRAMA DE DISCIPLINA
 PROGRAMA DE DISCIPLINA Disciplina: Química Inorgânica I Código da Disciplina: NDC 132 Curso: Engenharia Civil Semestre de oferta da disciplina: 2 Faculdade responsável: Núcleo de Disciplinas Comuns (NDC)
PROGRAMA DE DISCIPLINA Disciplina: Química Inorgânica I Código da Disciplina: NDC 132 Curso: Engenharia Civil Semestre de oferta da disciplina: 2 Faculdade responsável: Núcleo de Disciplinas Comuns (NDC)
MATRIZ DE CONTEÚDOS E DE PROCEDIMENTOS
 Elementos químicos e sua organização Agrupamento de Escolas General Humberto Delgado Sede na Escola Secundária/3 José Cardoso Pires Santo António dos Cavaleiros 10º Ano Planificação Anual 201-2016 Física
Elementos químicos e sua organização Agrupamento de Escolas General Humberto Delgado Sede na Escola Secundária/3 José Cardoso Pires Santo António dos Cavaleiros 10º Ano Planificação Anual 201-2016 Física
ESCOLA SECUNDÁRIA PINHAL DO REI FICHA FORMATIVA 2ºTESTE
 Ano Letivo 2016/2017 ESCOLA SECUNDÁRIA PINHAL DO REI FICHA FORMATIVA 2ºTESTE Física e Química A 10ºAno 1. A energia dos eletrões nos átomos inclui: (A) apenas o efeito das atrações entre os eletrões e
Ano Letivo 2016/2017 ESCOLA SECUNDÁRIA PINHAL DO REI FICHA FORMATIVA 2ºTESTE Física e Química A 10ºAno 1. A energia dos eletrões nos átomos inclui: (A) apenas o efeito das atrações entre os eletrões e
Propriedades Físicas e Químicas dos Compostos Orgânicos
 Aumenta Propriedades das Moléculas Orgânicas Propriedades Físicas e Químicas dos Compostos Orgânicos A partir das ligações químicas que unem os átomos de suas moléculas, e das forças que agem entre elas
Aumenta Propriedades das Moléculas Orgânicas Propriedades Físicas e Químicas dos Compostos Orgânicos A partir das ligações químicas que unem os átomos de suas moléculas, e das forças que agem entre elas
DISTRIBUIÇÃO DA CARGA HORÁRIA TEÓRICA PRÁTICA OUTRAS NÚMERO MÁXIMO DE ALUNOS POR TURMA AULAS TEÓRICAS AULAS PRÁTICAS OUTRAS 30
 Dasta UNIDADE UNIVERSITÁRIA: Instituto de Química CURSO: LICENCIATURA EM QUÍMICA DEPARTAMENTO RESPONSÁVEL: QUÍMICA GERAL E INORGÂNICA IDENTIFICAÇÃO: CÓDIGO NOME DA DISCIPLINA OU ESTÁGIO SERIAÇÃO IDEAL
Dasta UNIDADE UNIVERSITÁRIA: Instituto de Química CURSO: LICENCIATURA EM QUÍMICA DEPARTAMENTO RESPONSÁVEL: QUÍMICA GERAL E INORGÂNICA IDENTIFICAÇÃO: CÓDIGO NOME DA DISCIPLINA OU ESTÁGIO SERIAÇÃO IDEAL
Aula 5: Propriedades e Ligação Química
 Aula 5: Propriedades e Ligação Química Relacionar o tipo de ligação química com as propriedades dos materiais Um entendimento de muitas propriedades físicas dos materiais é previsto através do conhecimento
Aula 5: Propriedades e Ligação Química Relacionar o tipo de ligação química com as propriedades dos materiais Um entendimento de muitas propriedades físicas dos materiais é previsto através do conhecimento
Estrutura Atômica e Ligações Químicas. Conceitos
 Estrutura Atômica e Ligações Químicas Conceitos Estrutura esquemática do átomo de sódio 2003 Brooks/Cole Publishing / Thomson Learning A dualidade da matéria (partícula/onda) Louis de Broglie: λ h m.v
Estrutura Atômica e Ligações Químicas Conceitos Estrutura esquemática do átomo de sódio 2003 Brooks/Cole Publishing / Thomson Learning A dualidade da matéria (partícula/onda) Louis de Broglie: λ h m.v
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
Programa Analítico de Disciplina QUI102 Química Fundamental
 Catálogo de Graduação 016 da UFV 0 Programa Analítico de Disciplina QUI10 Química Fundamental Departamento de Química - Centro de Ciências Exatas e Tecnológicas Número de créditos: 7 Teóricas Práticas
Catálogo de Graduação 016 da UFV 0 Programa Analítico de Disciplina QUI10 Química Fundamental Departamento de Química - Centro de Ciências Exatas e Tecnológicas Número de créditos: 7 Teóricas Práticas
CURSO DE ENGENHARIA CIVIL Autorizado pela Portaria MEC nº 276, de 30 de março de 2015
 CURSO DE ENGENHARIA CIVIL Autorizado pela Portaria MEC nº 276, de 30 de março de 2015 Componente Curricular: QUÍMICA GERAL E EXPERIMENTAL Código: Pré-requisito: ------ Período Letivo: 2016.2 Professor:
CURSO DE ENGENHARIA CIVIL Autorizado pela Portaria MEC nº 276, de 30 de março de 2015 Componente Curricular: QUÍMICA GERAL E EXPERIMENTAL Código: Pré-requisito: ------ Período Letivo: 2016.2 Professor:
TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS. Prof. Cristiano Torres Miranda Disciplina: Química Geral QM83A Turma Q33
 TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS Prof. Cristiano Torres Miranda Disciplina: Química Geral QM83A Turma Q33 Johann Wolfgang Döbereiner John Alexander Reina Newlands Tríades Döbereiner Lei das Oitavas
TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS Prof. Cristiano Torres Miranda Disciplina: Química Geral QM83A Turma Q33 Johann Wolfgang Döbereiner John Alexander Reina Newlands Tríades Döbereiner Lei das Oitavas
Estrutura atômica e ligação interatômica. Profa. Daniela Becker
 Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
Ligação iônica e suas propriedades
 Ligação iônica e suas propriedades Química Geral Prof. Edson Nossol Uberlândia, 17/03/2016 Ligação química: é a força atrativa que mantém dois ou mais átomos unidos. c Cl = 3,0 c Br = 2,8 Ligação covalente:
Ligação iônica e suas propriedades Química Geral Prof. Edson Nossol Uberlândia, 17/03/2016 Ligação química: é a força atrativa que mantém dois ou mais átomos unidos. c Cl = 3,0 c Br = 2,8 Ligação covalente:
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1
 PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
Aulão de Química. Química Geral Professor: Eduardo Ulisses
 Aulão de Química Química Geral Professor: Eduardo Ulisses Substâncias e Misturas Substância é qualquer parte da matéria que possui propriedades constantes. As substâncias podem ser classificadas como sendo
Aulão de Química Química Geral Professor: Eduardo Ulisses Substâncias e Misturas Substância é qualquer parte da matéria que possui propriedades constantes. As substâncias podem ser classificadas como sendo
DISCIPLINA DE QUÍMICA
 DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
Teoria dos Orbitais Moleculares. Prof. Fernando R. Xavier
 Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
INSTITUTO DE QUÍMICA - USP QFL QUÍMICA GERAL FARMÁCIA & BIOQUÍMICA
 INSTITUTO DE QUÍMICA - USP QFL-0137 - QUÍMICA GERAL - 2017 FARMÁCIA & BIOQUÍMICA OBJETIVOS: Introduzir conceitos fundamentais de Química, com ênfase na correlação entre a estrutura da matéria e suas propriedades
INSTITUTO DE QUÍMICA - USP QFL-0137 - QUÍMICA GERAL - 2017 FARMÁCIA & BIOQUÍMICA OBJETIVOS: Introduzir conceitos fundamentais de Química, com ênfase na correlação entre a estrutura da matéria e suas propriedades
Ligação iônica e suas propriedades
 Ligação iônica e suas propriedades Química Geral Prof. Edson Nossol Uberlândia, 26/05/2017 Ligação química: é a força atrativa que mantém dois ou mais átomos unidos. c Cl = 3,0 c Br = 2,8 Ligação covalente:
Ligação iônica e suas propriedades Química Geral Prof. Edson Nossol Uberlândia, 26/05/2017 Ligação química: é a força atrativa que mantém dois ou mais átomos unidos. c Cl = 3,0 c Br = 2,8 Ligação covalente:
Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais
 Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligação Covalente. O íon molecular H 2
 O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados por um único elétron O que acontece à medida que os núcleos se aproximam? 4 O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados
O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados por um único elétron O que acontece à medida que os núcleos se aproximam? 4 O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados
Princípios da Mecânica ondulatória. Funções de onda atômicas são somadas para obter funções de onda moleculares
 Princípios da Mecânica ondulatória Funções de onda atômicas são somadas para obter funções de onda moleculares Se as funções de onda resultantes se reforçam mutuamente, é formado um tipo de orbital chamado
Princípios da Mecânica ondulatória Funções de onda atômicas são somadas para obter funções de onda moleculares Se as funções de onda resultantes se reforçam mutuamente, é formado um tipo de orbital chamado
 Ligações Químicas Por que os átomos formam ligações químicas? Distância de equilíbrio Comprimento da ligação H-H r o = 74 pm distância internuclear Uma ligação química entre dois átomos é formada se
Ligações Químicas Por que os átomos formam ligações químicas? Distância de equilíbrio Comprimento da ligação H-H r o = 74 pm distância internuclear Uma ligação química entre dois átomos é formada se
1 Resolução CEPE N 2615
 _II n Universidade Federal de Ouro Preto 1 Resolução CEPE N 2615 Aprova aplicação de prova específica no processo de transferência para o Curso de Química Industrial. O Conselho de Ensino, Pesquisa e Extensão
_II n Universidade Federal de Ouro Preto 1 Resolução CEPE N 2615 Aprova aplicação de prova específica no processo de transferência para o Curso de Química Industrial. O Conselho de Ensino, Pesquisa e Extensão
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química
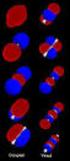 Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Visualizando os Orbitais Moleculares de Moléculas Pequenas e Complexos. Uma aplicação de simetria em química Roberto B. Faria faria@iq.ufrj.br www.iq.ufrj.br/~faria Universidade Federal do Rio de Janeiro
Química Bio-inorgânica - roteiro de aulas
 Química Bio-inorgânica - roteiro de aulas 2014 - Prof. André Ferraz Pense: Como esta um metal em um sistema vivo? Para entender a questão dos "metais em sistemas biológicos" precisamos entender: 1. Ligação
Química Bio-inorgânica - roteiro de aulas 2014 - Prof. André Ferraz Pense: Como esta um metal em um sistema vivo? Para entender a questão dos "metais em sistemas biológicos" precisamos entender: 1. Ligação
Forças Intermoleculares
 Forças Intermoleculares Você já se perguntou por que a água forma gotas ou como os insetos conseguem caminhar sobre a água? Gota d'água caindo sobre a superfície da água. Inseto pousado sobre a superfície
Forças Intermoleculares Você já se perguntou por que a água forma gotas ou como os insetos conseguem caminhar sobre a água? Gota d'água caindo sobre a superfície da água. Inseto pousado sobre a superfície
QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO QUÍMICA É A FORÇA QUE MANTÉM ÁTOMOS E/OU ÍONS UNIDOS NAS
QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO QUÍMICA É A FORÇA QUE MANTÉM ÁTOMOS E/OU ÍONS UNIDOS NAS
Configurações eletrônicas e a tabela periódica. Os grupos 1 e 2 têm elétrons nos orbitais s. Os grupos 13 ao 18 têm elétrons nos orbitais p
 TABELA PERIÓDICA 32 18 Configurações eletrônicas e a tabela periódica A tabela periódica pode ser utilizada como um guia para as configurações eletrônicas. O número do período é o valor de n. Os grupos
TABELA PERIÓDICA 32 18 Configurações eletrônicas e a tabela periódica A tabela periódica pode ser utilizada como um guia para as configurações eletrônicas. O número do período é o valor de n. Os grupos
Sumário 7 Moléculas Poliatómicas 1
 Sumário 7 Moléculas Poliatómicas 1 Be 2, B 3, 4, N 3 e 2 O idretos dos Elementos do 2º Período da T. P. Teoria do Enlace de Valência - ibridação de orbitais atómicas onceito de Orbital íbrida ibridações
Sumário 7 Moléculas Poliatómicas 1 Be 2, B 3, 4, N 3 e 2 O idretos dos Elementos do 2º Período da T. P. Teoria do Enlace de Valência - ibridação de orbitais atómicas onceito de Orbital íbrida ibridações
LIGAÇÕES INTERATÔMICAS X LIGAÇÕES INTERMOLECULARES
 Prof. Edson Cruz LIGAÇÕES INTERATÔMICAS X LIGAÇÕES INTERMOLECULARES Já estudamos que qualquer tipo de matéria é formado por átomos. Vimos também que cada agrupamento de átomos, combinados em uma determinada
Prof. Edson Cruz LIGAÇÕES INTERATÔMICAS X LIGAÇÕES INTERMOLECULARES Já estudamos que qualquer tipo de matéria é formado por átomos. Vimos também que cada agrupamento de átomos, combinados em uma determinada
CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS
 CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO ESTABILIZAÇÃO DO AMETAL LIGAÇÃO IÔNICA
CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO ESTABILIZAÇÃO DO AMETAL LIGAÇÃO IÔNICA
CURSO ENGENHARIA DE PRODUÇÃO Autorizado pela Portaria nº de 25/08/10 D.O.U de 27/08/10 Componente Curricular: Química Geral e Experimental
 CURSO ENGENHARIA DE PRODUÇÃO Autorizado pela Portaria nº 1.150 de 25/08/10 D.O.U de 27/08/10 Componente Curricular: Química Geral e Experimental Código: ENGP -170 Pré-requisito: --------------- Período
CURSO ENGENHARIA DE PRODUÇÃO Autorizado pela Portaria nº 1.150 de 25/08/10 D.O.U de 27/08/10 Componente Curricular: Química Geral e Experimental Código: ENGP -170 Pré-requisito: --------------- Período
Forma e estrutura das moléculas Atkins e Jones, Princípios de Química, cap. 3, p (5 a edição)
 Forma e estrutura das moléculas Atkins e Jones, Princípios de Química, cap. 3, p. 93-131 (5 a edição) Relembre: Estrutura de Lewis e a regra do octeto - Antiga (introduzida por GN Lewis em 1916), mas útil
Forma e estrutura das moléculas Atkins e Jones, Princípios de Química, cap. 3, p. 93-131 (5 a edição) Relembre: Estrutura de Lewis e a regra do octeto - Antiga (introduzida por GN Lewis em 1916), mas útil
Qui. Semana. Allan Rodrigues Xandão (Gabriel Pereira)
 Semana 6 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Semana 6 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Ligação Iônica. Ligação Metálica. Ligações Química. Ligação Covalente. Polaridade. Geometria. Ligações Intermoleculares
 Ligação Iônica Ligação Metálica Ligações Química Ligação Covalente Polaridade Geometria Ligações Intermoleculares Teoria do octeto Os átomos se estabilizam com 8 elétrons na última camada. (Porém existem
Ligação Iônica Ligação Metálica Ligações Química Ligação Covalente Polaridade Geometria Ligações Intermoleculares Teoria do octeto Os átomos se estabilizam com 8 elétrons na última camada. (Porém existem
Estrutura Atômica. Prof. Dr. Carlos Roberto Grandini. Bauru 2006
 Estrutura Atômica Prof. Dr. Carlos Roberto Grandini Bauru 2006 O que é nanotecnologia? Nanotecnologia pode ser considerada como um conjunto de atividades ao nível de átomos e moléculas que tem aplicação
Estrutura Atômica Prof. Dr. Carlos Roberto Grandini Bauru 2006 O que é nanotecnologia? Nanotecnologia pode ser considerada como um conjunto de atividades ao nível de átomos e moléculas que tem aplicação
CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS
 CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS ELETRONEGATIVIDADE CARÁTER AMETÁLICO CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO
CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS ELETRONEGATIVIDADE CARÁTER AMETÁLICO CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO
DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª Série
 DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª Série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª Série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
Ligações Químicas. Iônicas. Metálicas. Covalentes. Átomo: constituinte da menor parte de qualquer matéria;
 Ligações Químicas Átomo: constituinte da menor parte de qualquer matéria; -capacidade de se combinarem uns com os outros, lhes permite a formação de uma grande variedade de substâncias; Ligações Químicas
Ligações Químicas Átomo: constituinte da menor parte de qualquer matéria; -capacidade de se combinarem uns com os outros, lhes permite a formação de uma grande variedade de substâncias; Ligações Químicas
TEORIA DAS ORBITAIS MOLECULARES
 TORIA DAS ORBITAIS MOLCULARS Na teoria das orbitais moleculares (TOM), os eletrões ocupam precisamente orbitais definidas, chamadas orbitais moleculares (OM), que se estendem por toda a molécula. Na TOM,
TORIA DAS ORBITAIS MOLCULARS Na teoria das orbitais moleculares (TOM), os eletrões ocupam precisamente orbitais definidas, chamadas orbitais moleculares (OM), que se estendem por toda a molécula. Na TOM,
Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D.
 01 Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D. 02 A energia de ionização cresce para direita da tabela periódica, portanto
01 Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D. 02 A energia de ionização cresce para direita da tabela periódica, portanto
Ligações Químicas. Profº Jaison Mattei
 Ligações Químicas Profº Jaison Mattei LIGAÇÃO IÔNICA Ocorre geralmente entre METAIS e AMETAIS com de eletronegatividade > 1,7. Não Esqueça!!! Eletropositivos Metais: Ametais: Perdem elétrons Viram Cátions(+)
Ligações Químicas Profº Jaison Mattei LIGAÇÃO IÔNICA Ocorre geralmente entre METAIS e AMETAIS com de eletronegatividade > 1,7. Não Esqueça!!! Eletropositivos Metais: Ametais: Perdem elétrons Viram Cátions(+)
Estrutura atômica e ligação interatômica
 Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1 Estrutura atômica e ligação interatômica 1º semestre / 2016 Estrutura atômica e ligação
Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1 Estrutura atômica e ligação interatômica 1º semestre / 2016 Estrutura atômica e ligação
estrutura atômica e ligações
 Aula 02 estrutura atômica e ligações ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone introdução conceitos elementares a estrutura dos átomos a estrutura
Aula 02 estrutura atômica e ligações ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone introdução conceitos elementares a estrutura dos átomos a estrutura
05 - (UEL PR/1994) Localize na tabela periódica o elemento químico de número atômico 20 e escolha a(s)
 01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS
 PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
Módulo II: A visão clássica da ligação covalente
 Módulo II: A visão clássica da ligação covalente Aula 3: Eletronegatividade de Pauling e o caráter iônico das ligações químicas 4. Eletronegatividade de Pauling e o caráter iônico das ligações covalentes
Módulo II: A visão clássica da ligação covalente Aula 3: Eletronegatividade de Pauling e o caráter iônico das ligações químicas 4. Eletronegatividade de Pauling e o caráter iônico das ligações covalentes
Ligações Químicas - II. Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
 Ligações Químicas - II Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares 1 Revisão: Estruturas de Lewis G.N. Lewis (~1916) Representação das ligações químicas Compartilhamento
Ligações Químicas - II Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares 1 Revisão: Estruturas de Lewis G.N. Lewis (~1916) Representação das ligações químicas Compartilhamento
3. Misturas, Substâncias Simples e Compostas e Processos de Separação de Misturas.
 Conteúdo 1. Elementos, modelos atômicos e representações: modelos atômicos de Dalton, Tomson, Rutherford-Bohr. Elemento químico. Número atômico e número de massa. Prótons, elétrons e nêutrons. Distribuição
Conteúdo 1. Elementos, modelos atômicos e representações: modelos atômicos de Dalton, Tomson, Rutherford-Bohr. Elemento químico. Número atômico e número de massa. Prótons, elétrons e nêutrons. Distribuição
Tabela Periódica e Propriedades Periódicas dos Elementos. periódico permite fazer previsões gerais sobre seu comportamento químico e físico.
 Tabela Periódica e Propriedades Periódicas dos Elementos Agrupar os elementos num quadro Agrupar os elementos num quadro periódico permite fazer previsões gerais sobre seu comportamento químico e físico.
Tabela Periódica e Propriedades Periódicas dos Elementos Agrupar os elementos num quadro Agrupar os elementos num quadro periódico permite fazer previsões gerais sobre seu comportamento químico e físico.
Estrutura Molecular, Ligações Químicas e Propriedades dos Compostos Orgânicos
 Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Profa. Roberlucia A. Candeia Disciplina: Química Orgânica Estrutura Molecular, Ligações Químicas e Propriedades dos
Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Profa. Roberlucia A. Candeia Disciplina: Química Orgânica Estrutura Molecular, Ligações Químicas e Propriedades dos
Universidade Federal do Tocantins
 Universidade Federal do Tocantins Estrutura eletrônica dos átomos e periodicidade química Prof. Dr. Edenilson dos Santos Niculau enicolau@uft.edu.br www.profedenilsonniculau.wordpress.com Sumário 2 PERIODICIDADE
Universidade Federal do Tocantins Estrutura eletrônica dos átomos e periodicidade química Prof. Dr. Edenilson dos Santos Niculau enicolau@uft.edu.br www.profedenilsonniculau.wordpress.com Sumário 2 PERIODICIDADE
Químicas. Profa. Ms. Loraine Cristina do Valle Jacobs DAQBI.
 Ligações Químicas Profa. Ms. Loraine Cristina do Valle Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs LIGAÇÕES IÔNICAS LIGAÇÕES IÔNICAS IMPORTANTE : alguns metais,
Ligações Químicas Profa. Ms. Loraine Cristina do Valle Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs LIGAÇÕES IÔNICAS LIGAÇÕES IÔNICAS IMPORTANTE : alguns metais,
Introdução à Nanotecnologia
 Introdução à Nanotecnologia Ele 1060 Aula 4 2010-01 Fundamentos Aula Anterior Classificação dos Materiais; Átomos; Elétrons nos Átomos. Ligação Atômica no Sólidos Para compreender as propriedades físicas
Introdução à Nanotecnologia Ele 1060 Aula 4 2010-01 Fundamentos Aula Anterior Classificação dos Materiais; Átomos; Elétrons nos Átomos. Ligação Atômica no Sólidos Para compreender as propriedades físicas
FUNDAÇÃO UNIVERSIDADE FEDERAL DE RONDÔNIA. Licenciatura em Química. 7 0 SEMESTRE Carga Horária : Objetivos
 FUNDAÇÃO UNIVERSIDADE FEDERAL DE RONDÔNIA Unidade FILOSOFIA 60 Apresentar as principais idéias filosóficas e os filósofos mais importantes da história do pensamento humano, entendendo o homem como produtor
FUNDAÇÃO UNIVERSIDADE FEDERAL DE RONDÔNIA Unidade FILOSOFIA 60 Apresentar as principais idéias filosóficas e os filósofos mais importantes da história do pensamento humano, entendendo o homem como produtor
Ligação Covalente: compartilhamento de elétrons entre os átomos.
 Aula 14 10/jun Marcelo Ligação Covalente: compartilhamento de elétrons entre os átomos. Formação de compostos moleculares Ocorre entre átomos de não-metais (baixa diferença de eletronegatividade) Acima,
Aula 14 10/jun Marcelo Ligação Covalente: compartilhamento de elétrons entre os átomos. Formação de compostos moleculares Ocorre entre átomos de não-metais (baixa diferença de eletronegatividade) Acima,
Ligações Químicas. Profª Drª Cristiane de Abreu Dias
 Ligações Químicas Profª Drª Cristiane de Abreu Dias Quais São as Ideias Importantes? A ideia central deste assunto é que os átomos ligam-se uns aos outros se energia é liberada no processo. O abaixamento
Ligações Químicas Profª Drª Cristiane de Abreu Dias Quais São as Ideias Importantes? A ideia central deste assunto é que os átomos ligam-se uns aos outros se energia é liberada no processo. O abaixamento
8.1 Química Realidade e Contexto: Antônio Lembo (1999)
 8 ANEXOS Nesta seção são colocados os anexos que foram julgados pertinentes para complementar o entendimento de questões relativas à análise dos livros. A seguir apresentamos um espelho dos temas que compõem
8 ANEXOS Nesta seção são colocados os anexos que foram julgados pertinentes para complementar o entendimento de questões relativas à análise dos livros. A seguir apresentamos um espelho dos temas que compõem
ESCOLA SECUNDÁRIA PINHAL DO REI FICHA FORMATIVA 2ºTESTE
 Ano Letivo 2016/2017 ESOLA SEUNDÁRIA PINAL DO REI FIA FORMATIVA 2ºTESTE Física e Química A 10ºAno 1. A energia dos eletrões nos átomos inclui: (A) apenas o efeito das atrações entre os eletrões e o núcleo.
Ano Letivo 2016/2017 ESOLA SEUNDÁRIA PINAL DO REI FIA FORMATIVA 2ºTESTE Física e Química A 10ºAno 1. A energia dos eletrões nos átomos inclui: (A) apenas o efeito das atrações entre os eletrões e o núcleo.
A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos...
 Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
QUÍMICA GERAL Ligações Químicas. slide- 1 LIGAÇÕES QUÍMICAS. Profª. Camila Amorim
 slide- 1 LIGAÇÕES QUÍMICAS Cap. 8 J.B. Russel 1 LIGAÇÕES QUÍMICAS slide- 2 Definição: forças que unem átomos formando moléculas, agrupamentos de átomos ou sólidos iônicos; Forças de interação mais fortes;
slide- 1 LIGAÇÕES QUÍMICAS Cap. 8 J.B. Russel 1 LIGAÇÕES QUÍMICAS slide- 2 Definição: forças que unem átomos formando moléculas, agrupamentos de átomos ou sólidos iônicos; Forças de interação mais fortes;
ÁGUA, SOLUBILIDADE E PH
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
Estrutura atômica & Classificação periódica
 Estrutura atômica & Classificação periódica Aula de química (20/08) Gabriel e Leonardo Estrutura atômica Modelos Atômicos Modelos Atômicos - Dalton Os átomos são esferas rígidas, indivisíveis e indestrutíveis
Estrutura atômica & Classificação periódica Aula de química (20/08) Gabriel e Leonardo Estrutura atômica Modelos Atômicos Modelos Atômicos - Dalton Os átomos são esferas rígidas, indivisíveis e indestrutíveis
INSTITUTO DE QUÍMICA da UFRJ DEPARTAMENTO DE QUÍMICA INORGÂNICA. Programa de Disciplina. Química Geral EQ. Nome: Código: IQG 115 CARACTERÍSTICAS
 Programa de Disciplina Nome: Química Geral EQ Código: IQG 115 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4 Pré-Requisito
Programa de Disciplina Nome: Química Geral EQ Código: IQG 115 Categoria: Carga Horária Semanal: CARACTERÍSTICAS Número de Semanas Previstas para a Disciplina: 15 Número de Créditos da Disciplina: 4 Pré-Requisito
