QFL-5922 Espectrometria de Massa Parte 2 Luiz Henrique Catalani
|
|
|
- Alessandra Arruda Câmara
- 7 Há anos
- Visualizações:
Transcrição
1 QFL-5922 Espectrometria de Massa Parte 2 Luiz Henrique Catalani Aula 2 Análise do espectro de massas Fragmentação
2 McLafferty & Turecek, Interpretation of Mass Spectra, 4th Ed., R. Martin Smith, Understanding Mass Spectra, 4th Ed., NIST s Chemistry (National Institute of Standards and Technology)
3 Massa molecular nominal: a massa molecular mais próxima de um número inteiro Cada valor m/z é a massa molecular nominal de um determinado fragmento O pico com o maior valor de m/z representa o íon molecular (M) Picos com valores m/z menores, chamados picos de fragmentação, representam fragmentos carregados positivamente da molécula
4 O pico do íon molecular tem número IMPAR de elétrons; sua fragmentação pode gerar fragmentos com número IMPAR de elétrons (OE. ) ou com de número PAR de elétrons (EE ) O pico base é o pico de maior intensidade, pois tem a maior abundância Ligações mais fracas quebram preferencialmente Ligações que se quebram para formar fragmentos mais estáveis têm preferência
5 The Molecular Ion Most valuable info of the mass spectrum Molecular mass Elemental composition Fragments must be consistent with it Not always stable with EI Be careful about over-interpretation of peak of highest m/z! Use soft-ionization such as CI in parallel MS Definition: m/z of the molecular ion is the peak that contains the most abundant isotope of all the elements involved (by convention) Won t always be most abundant peak
6 Requirements for the Molecular Ion Necessary but not sufficient conditions It must be the ion of highest mass (isotope caveat) It must be an odd-electron ion It must be capable of yielding the most important ions in the high-mass region by loss of logical neutral species If candidate fails either test, it cannot be the MI If candidate passes all tests, it may or may not be the MI
7 Odd-Electron Ions For EI, a molecule becomes ionized by loosing one electron It must have an unpaired electron (so it s a radical)
8 Even Electron Ions Even-electron ions: All electrons on the outer shell are fully paired Generally more stable Often the more abundant fragment ions CH 4 CH 3 H In CI, even electron ions such as MH are formed, resulting in lower fragmentation
9 O pico base m/z = 43 no espectro de massa do pentano indica a preferência de fragmentação em C-2 do que em C-3 Carbocátions podem sofrer fragmentações adicionais
10 O 2-metilbutano tem a mesma massa molecular do que o pentano, mas o pico em m/z = 57 (M 15) é mais intenso
11 Isotopos na Espectroscopia de Massa
12 Isotopos na Espectroscopia de Massa picos atribuídos à isótopos ajudam na identificação estrutural do composto picos M2: contribuição do 18 O ou de dois átomos pesados na mesma molécula um pico grande M2 sugere um composto contendo cloro ou bromo: um cloro se M2 é 1/3 da altura de M; um bromo, se M2 é da mesma altura que M para calcular as massas molares de fragmentos e moléculas, a massa atômica de um isótopo único deve ser usada
13 Isotopos na Espectroscopia de Massa
14 Isotopos na Espectroscopia de Massa
15 Abundância de picos isotópicos é dada por: AaBbCc. %(M1) = a %(A1) b %(B1) c %(C1).. %(M2) = a %(A2) b %(B2) c %(C2).. Isótopos de baixa abundância: C, H, N, O (M1) = 1,1 n o C 0,36 n o de N (M2) = (1,1 n o C)/200 0,2 n o de O Isótopos de alta abundância: S, Si, Cl, Br (a b) n expandido a = % leve, b = %pesado, n = n o de átomos presente
16 Regra do Nitrogênio: - Composto onde M é par deve conter número par de átomos de N, ou nenhum - Composto onde M é impar deve conter número impar de átomos de N - Causa: valência é impar e massa é par
17 N-Rule applies to all ions An odd-electron ion will be at an even mass number if it contains an even number of nitrogen atoms An even-electron ion containing an even number of nitrogen atoms will appear at an odd mass number
18 Cálculo do número de anéis e duplas ligações (rpdb): - Para C x H y N z O n rpdb = x ½ y ½ z 1 - Causa: valência dos átomos (para íons rpdb pode terminar em 0,5) - caso geral A x B y C z D n onde A = C, Si B = H, F, Cl, Br, I C = N, P D = O, S (não conta duplas ligações de elementos de estados de valência superior)
19 More on Odd- & Even-Electron Ions If you can establish the elemental composition of the ion, the rings plus double-bonds rule will show whether the ion is odd or even-electron: Even: integer 1/2 RPDB Odd: integer RPDB
20 Espectrometria de massa de alta resolução
21 Espectrometria de massa de alta resolução Espectrômetros de massa de baixa resolução medem valores de m/ z ao número inteiro mais próximo (massa molecular) Espectrômetros de massa de alta resolução medem valores de m/z com três ou quatro casas decimais A alta precisão do cálculo de massa molecular permite a determinação exata da fórmula do fragmento Exemplo Pode-se escolher a fórmula molecular de fragmento com peso molecular de 32 usando MS de alta resolução =
22 Equações de Fragmentação O íon M. É formado pela perda de um dos seus elétrons mais lábeis Se elétrons não-ligantes ou elétrons pi estão presentes, um destes elétrons é perdido por impacto de elétrons para formar M. Elétrons lábeis não-ligantes de nitrogênio e oxigênio, e elétrons pi de duplas ligações são preferencialmente perdidos Em moléculas com somente ligações C-C e C-H, a localização do elétron solitário não pode ser prevista e a fórmula é escrita entre parênteses para refletir isto
23 Mecanismos de Reações de Fragmentação a) clivagem em uma ligação C-C (sigma cleavage, s): b) clivagem em uma ligação C-Heteroátomo (inductive cleavage, i): c) iniciação radicalar vizinha (alpha cleavage, a):
24 Mecanismos de Reações de Fragmentação d) rearranjos e extrusão (rearrangement, rh e rd): e) Retro-Diels-Alder (rearrangement, rrda): f) Rearranjo McLafferty (rearrangement, rmcl):
25 FRAGMENTAÇÃO DOS HIDROCARBONETOS ALCANOS Sinal do Íon Molecular Cadeias Lineares: normalmente aparece (baixa intensidade) Cadeias Ramificadas: menor ocorrência (às vezes ausente) Clivagem Favorecida Formação de Carbocátion estável R CH 3 R CH 3
26 Octano CH 3 (CH 2 ) 6 CH 3 M (114) CH 3 CH 2 CH 2 m/z 43 CH 3 CH 2 CH 2 CH 2 m/z 57 CH 3 CH 2 m/z 29 CH 3 CH 2 CH 2 CH 2 CH 2 m/z 71 CH 3 CH 2 CH 2 CH 2 CH 2 CH 2 m/z M (114)
27 2,2,4-trimetilpentano CH 3 CH 3 C CH 2 CH 3 M (114) CH CH 3 CH 3 57 CH 3 CH 3 C CH 3 m/z 57
28 FRAGMENTAÇÃO DOS HIDROCARBONETOS ALCENOS Sinal do Íon Molecular Normalmente observado Clivagem Favorecida alílica R. CH 2 CH CH 2 R CH 2 CH CH 2 CH 2 CH CH 2 m/z 41
29 FRAGMENTAÇÃO DOS HIDROCARBONETOS ALCENOS Alcenos cíclicos Sofrem Retro Diels-Alder Íon radicalar Neutro
30 1-buteno CH 3 CH 2 CH CH 2 M (56) CH 2 CH CH 2 m/z M (56)
31 Limoneno CH 3 C CH 3 CH 2 M (136) CH 3 H 2 C C H 68 m/z 68 C CH 3 CH 2 M (136)
32 FRAGMENTAÇÃO DOS HIDROCARBONETOS ALCINOS Tipos de Clivagem. H C C R H C C R H C C CH 2 R R. H C C CH 2 H C C CH 2 Íon propargil m/z 39
33 1-pentino C C CH 2 CH 2 CH 3 m/z 67 H C C CH 2 CH 2 CH 3 H C C CH 2 M (68) 39 m/z M (68)
34 FRAGMENTAÇÃO DOS HIDROCARBONETOS AROMÁTICOS Sinal do Íon Molecular Intenso Tipos de Clivagem Anel com cadeia lateral alquila CH 2 R R. CH 2 CH 2 Íon benzílico Íon tropílio m/z 91
35 FRAGMENTAÇÃO DOS HIDROCARBONETOS AROMÁTICOS Fragmentações do íon tropílio m/z 39 Tipos de Clivagem m/z 91 m/z 65 Cadeia lateral alquila com 3 ou C Rearranjo de McLafferty CH 2 H H CH2 CH R m/z 92 CH 2 H H H CH 2 R
36 Isopropil benzeno CH 3 C H CH 3.CH 3 CH 3 C H CH 3 M (120) 105 m/z 105 M (120)
37 Propil benzeno CH 2 CH 2 CH 3 M (120) m/z H H m/z 92 CH 2 92 M (120)
38 FRAGMENTAÇÃO DOS ÁLCOOIS Sinal do Íon Molecular Baixa Intensidade (1 ários e 2 ários ) Ausente (3 ários ) Tipos de Clivagem Quebra da ligação C-C vizinha ao Oxigênio R R' C. R''... OH R''. R' R C OH R' R C OH Saída primeiro do substituinte maior
39 FRAGMENTAÇÃO DOS ÁLCOOIS Tipos de Clivagem Desidratação CH 2 CH 2 OH CH 2 CH 2 OH 2 H H 2 O CH 2 CH 2 RCH (CH 2 )n H H O CHR'. RCH (CH 2 )n H 2 O CHR' H 2 O. RCH (CH 2 )n OU (CH 2 )n CHR' RCH CHR'
40 FRAGMENTAÇÃO DOS ÁLCOOIS Tipos de Clivagem Perda simultânea de H 2 O e alceno ( de 4C) H 2 C. OH H CH 2 CHR H 2 O H 2 C CH 2 CHR M (alceno H 2 O)
41 1-butanol HO CH 2 CH 2 CH 2 CH 3 M (74) CH 2 OH m/z 31 CH 2 CH 2 CH 2 CH 2 m/z M (74)
42 2-butanol CH 3 CH CH 2 CH 3 OH 45 CH 3 CH OH m/z 45 M (74)
43 2-metil-2-propanol CH 3 CH 3 C OH CH 3 CH 3 C OH CH 3 m/z 59 59
44 Álcool benzílico CH 2 OH -H. OH -CO H H -H 2 M 108 m/z 107 m/z 79 m/z M
45 FRAGMENTAÇÃO DOS FENÓIS Sinal do Íon Molecular Intenso (é o pico base) Clivagens OH H H. -CO -H. C 5 H 5 m/z 66 m/z 65
46 Fenol OH H H. -CO -H. m/z 94 m/z 66 C 5 H 5 m/z
47 FRAGMENTAÇÃO DOS ÉTERES Sinal do Íon Molecular Baixa Intensidade Tipos de Clivagem RCH 2 CH 2 CH O.. CH 2 CH 3 CH 3. - RCH 2 CH 2. CH O.. CH 2 CH 3 CH 3 CH 3 CH O.. CH 2 H CH 2 - CH 2 CH 2 CH 3 CH OH.. m/z 45
48 Éter diisopropílico CH 3 CH 3 CH 3 CH 3 CH O CHCH 3 CH 3 CH O CHCH 3 m/z 87 CH 3 CH OH M 102 m/z
49 FRAGMENTAÇÃO DOS ALDEÍDOS Sinal do Íon Molecular Normalmente observado Tipos de Clivagem Clivagem α R C O H R C O. H R CHO H C O. R Clivagem β R CH 2 CHO R CH 2 CH O.
50 Butanal O CH 3 CH 2 CH 2 C H M (72) CH 3 CH 2 CH 2 C O m/z 71 H C O CH m/z 29 2 CH OH m/z M (72) 29 71
51 FRAGMENTAÇÃO DAS CETONAS Pico do Íon Molecular Intenso Tipos de Clivagem Cetonas alifáticas R R' C Ȯ.. -R... R' C O R' C O Rearranjo de McLafferty R. O. C H CHR 3 CH CHR 2 R' _. H O R 3 C H C H R 2 R C. CH R' R. O. C H CH R'
52 CETONAS CÍCLICAS O H H O C. CH 2 O C CH 2. C 2 H 4 m/z 98 m/z 98 m/z 70. CH 2 CH 2 CH 2 m/z 42 CO
53 CETONAS CÍCLICAS H H O C. CH 2 H. O C CH 3 O C. CH C 3 H 7 CH 2 m/z 98 m/z 98 m/z 55 H. O C CH 3 C O CH 3. m/z 98 m/z 83
54 CETONAS AROMÁTICAS Rearranjo de McLafferty. O. C H CHR 3 CH CHR 2 R 3 CH CHR 2. O C. CH R' R' H. O. C CH R'
55 2-octanona O CH 3 C (CH 2 ) 5 CH 3 M= CH 3 C O m/z 43 OH CH 3 C CH 2 m/z
56 Cicloexanona O m/z 98 O C CH 2 m/z 70.. CH 2 CH 2 CH 2 42 m/z O C CH CH 2 m/z 55 C O m/z
57 Estabilidade Relativa de Carbocátions
58 Estabilidade Relativa de Radicais
59 FRAGMENTAÇÃO DOS ÁCIDOS CARBOXÍLICOS ÁCIDOS ALIFÁTICOS Sinal do Íon Molecular Normalmente observado Ácidos de baixo peso molecular Clivagem α a C=O Picos intensos R O C OH R. (M -COOH) COOH COOH R. (m/z 45) R O C OH R CO. (M -OH)
60 Ácidos de cadeia longa Rearranjo de McLafferty. O H CHR 3 HO C CH CHR 2. H H O O R 3 CH CHR 2. HO C HO C CH CH R 1 R 1 R 1
61 ÁCIDOS AROMÁTICOS Sinal do Íon Molecular Intenso. Perda de OH (M - 17). Perda de COOH (M - 45). O Perda de água C OH H H 2 O CH 2 Efeito orto C O. CH 2 C O. CH 2
62 Ácido butírico O CH 3 CH 2 CH 2 C OH M (88) O H C HO CH 2 m/z M (88)
63 FRAGMENTAÇÃO DOS ÉSTERES ÉSTERES ALIFÁTICOS Sinal do Íon Molecular Clivagem mais característica Normalmente observado Rearranjo de McLafferty Íons resultantes da quebra da ligação α em relação ao grupo C=O O R C OR' R e O C OR' O R C OR' R C O OR' e
64 FRAGMENTAÇÃO DOS ÉSTERES ÉSTERES BENZÍLICOS E FENÍLICOS Acetato de benzila e de fenila Eliminam uma molécula neutra de ceteno Pico resultante é o pico base O CH 2. O C CH 2 C O H CH 2 CH 2 O m/z 108 H
65 Butirato de metila O CH 3 CH 2 CH 2 C OCH 3 M (102) CH 3 CH 2 CH 2 CO m/z 71 CH 3 O C O m/z CH 3 CH 2 CH 2 m/z 43 O H CH 3 O C CH 2 m/z M (102)
66 Benzoato de metila O C O C OCH3 m/z 105 m/z 77 M (136) M (136)
67 FRAGMENTAÇÃO DAS AMINAS Sinal do Íon Molecular monoamina alifática ÍMPAR Clivagem C-C próxima ao átomo de N R 1 R.. R2 R 2 C N R 3 R 4 R 1 R C N R 3 R 4 R C N R 3 R 1 R 4 Aminas de cadeia longa Fragmentos cíclicos R CH 2 (CH 2 )n NH 2 R CH 2 (CH 2 )n NH 2 n=3,4
68 AMINAS ALIFÁTICAS CÍCLICAS Sinal do Íon Molecular Intenso N N. H CH 3 CH 3 CH 3 N CH m/z 42. CH 2 CH 2 CH. 2 m/z 84 N CH 3. CH 2 N CH 3 m/z 57 CH 2 CH 2 CH 2 CH 2 N CH 2 m/z 42. CH 3
69 AMINAS AROMÁTICAS Sinal do Íon Molecular Intenso NH 2 -H. NH m/z 93 m/z 92 H H HCN m/z 66
70 Etilamina CH 3 CH 2 NH 2 M (45) CH 2 NH 2 m/z M (45)
71 Dietilamina CH 2 CH 3 NH CH 2 CH 3 M (73) CH 2 N CH 2 CH 3 H m/z CH 2 NH 2 m/z 30 M (73)
72 Trietilamina CH 2 CH 3 N CH 2 CH 3 CH 2 CH 3 M (101) CH 2 N CH 2 CH 3 CH 2 CH 3 m/z CH 2 NH 2 m/z 30 CH 2 N CH 2 CH 3 H m/z M (101)
73 FRAGMENTAÇÃO DAS AMIDAS Sinal do Íon Molecular Normalmente observado Amidas primárias Sinal intenso em m/z 44 R C NH2 - R O C NH 2 O O C NH 2 m/z 44 Pico base em amidas primárias maiores que propionamida resulta do Rearranjo de McLafferty H 2 N O C H CHR C CH 2 CH 2 CHR H 2 N O C H CH 2 H 2 m/z 59
74 FRAGMENTAÇÃO DAS AMIDAS Clivagem entre os C γ e δ ao átomo de N ciclização H 2 C H 2 C R CH 2 C. NH 2 O -R. H 2 C H 2 C C H 2 C NH 2 O m/z 86 Amidas secundárias Quebra do grupo N-alquila na posição β R O C NH CH 2 R' CH 2 R' R O C NH CH 2 C H H RHC C O NH 2 CH 2 m/z 30
75 AMIDAS AROMÁTICAS O C NH 2 NH 2. C O m/z 121 m/z 105 CO m/z 77
76 Acetamida O CH 3 C NH 2 M(59) O C NH 2 m/z M(59) CH 3 CO m/z 43
77 Butanamida CH 3 CH 2 CH 2 M(87) O C NH 2 O H H 2 N C CH 2 m/z O C NH 2 H 2 C m/z 44 H 2 C C H 2 C NH 2 O m/z M(87) 86
78 FRAGMENTAÇÃO DAS NITRILAS Sinal do Íon Molecular Fraco ou ausente (exceto a acetonitrila e a propionitrila) Clivagens Eliminação de um hidrogênio α Μ. 1 (útil na diagnose) RCH C N H. H. RCH C N RCH C N
79 FRAGMENTAÇÃO DAS NITRILAS Nitrilas Lineares de 4 a 9 C Rearranjo de McLafferty. N H CHR CH 2 CHR. N H. N H C C H2 CH 2 C CH2 C CH2 m/z 41
80 Hexanonitrila CH 3 CH 2 CH 2 CH 2 CH 2 CN CH 3 (CH 2 ) 3 CH C N m/z 96 N C H M(97) CH 2 41 m/z M(97)
81 FRAGMENTAÇÃO DOS NITRO COMPOSTOS COMPOSTOS NITRO-ALIFÁTICOS Sinal do Íon Molecular (NÚMERO ÍMPAR) Fraco ou ausente Presença de um grupo nitro Indicada por um sinal em m/z 30 ( )e um em m/z 46( ) NO NO 2 Os sinais principais são atribuídos aos fragmentos hidrocarbônicos
82 FRAGMENTAÇÃO DOS NITRO COMPOSTOS COMPOSTOS NITRO-AROMÁTICOS Sinal do Íon Molecular (NÚMERO ÍMPAR) Intenso O NO 2 NO CO m/z 93 m/z 65 NO 2 NO 2 C 4 H 3 HC CH m/z 77 m/z 51
83 1-nitropropano CH 3 CH 2 CH 2 NO 2 M(89) NO m/z 30 NO 2 m/z 46 C 3 H 7 m/z
84 Nitrobenzeno NO 2 O C 4 H 3 M(123) m/z 93 m/z 65 m/z 77 m/z M(123) 65 93
85 FRAGMENTAÇÃO DOS NITRITOS ALIFÁTICOS Sinal do Íon Molecular (NÚMERO ÍMPAR) Fraco ou ausente O sinal em m/z 30 ( NO ) é sempre intenso Pico base Clivagem da ligação C-C próxima ao grupo ONO R. R CH 2 ONO CH 2 ONO A ausência de um pico em m/z 46 distingui os nitritos dos nitro compostos m/z 60
86 Nitrito de metila CH 3 ONO M(61) NO m/z 30 CH 2 ONO m/z 60 CH 3 m/z M(61)
87 FRAGMENTAÇÃO DOS NITRATOS ALIFÁTICOS Sinal do Íon Molecular (NÚMERO ÍMPAR) Fraco ou ausente Clivagem da ligação C-C próxima ao grupo ONO 2 Pico base R CH O NO 2 R' R. CH O NO 2 R' O sinal em m/z 46 ( NO 2 ) é proeminente
88 Nitrato de etila CH 3 CH 2 O NO 2 M(91) NO 2 m/z CH 3 CH 2 m/z 29 H 2 C O NO 2 m/z M(91)
89 FRAGMENTAÇÃO DOS COMPOSTOS SULFURADOS A contribuição do isótopo 34 S para o sinal em M 2 e para os sinais correspondentes aos fragmentos mais duas unidades Facilita a identificação dos compostos contendo enxofre
90 Isotopos na Espectroscopia de Massa
91 FRAGMENTAÇÃO DOS COMPOSTOS SULFURADOS MERCAPTANS ALIFÁTICOS (TIÓIS) Sinal do Íon Molecular Forte o bastante para que o pico M2 possa ser medido Clivagem da ligação C-C próxima ao grupo SH R CH 2 SH. R CH 2 SH CH2 SH m/z 47
92 MERCAPTANS ALIFÁTICOS (TIÓIS) Tióis primários perdem uma molécula neutra de H 2 S H 2 C H 2 C H.. S H CHR CH 2 M CHR H 2 S (alceno H 2 S) CH 2
93 Etanotiol CH 3 CH 2 SH M( 62) CH 2 m/z 47 SH CH 3 CH 2 m/z M( 62) 47 M2
94 FRAGMENTAÇÃO DOS COMPOSTOS SULFURADOS SULFETOS ALIFÁTICOS Sinal do Íon Molecular Forte o bastante para que o pico M2 possa ser medido Clivagem da ligação C-C vizinha do S CH 3 CH 3 CH S CH 2 CH 3 CH 3 CH 3 CH S CH 2 H CH 2 CH 2 CH 2 CH 3 CH SH CH 3 CH SH m/z 61
95 Sulfeto de di-pentila CH 3 (CH 2 ) 4 S (CH 2 )CH 3 M( 174) 70 C 5 H 11 S CH 2 C 5 H 11 SH m/z 117 m/z 104 C 5 H 11 S m/z 103 CH 2 C 5 H 10 m/z 70 SH m/z 47 H S H 2 C CH 2 m/z M( 174)
96 FRAGMENTAÇÃO DOS COMPOSTOS HALOGENADOS COMPOSTO COM UM ÁTOMO DE CLORO Terá um pico M2 com 1/3 da intensidade do íon molecular (presença do isótopo 37 Cl) COMPOSTO COM UM ÁTOMO DE BROMO Terá um pico M2 com igual intensidade do íon molecular (presença do isótopo 81 Br)
97 FRAGMENTAÇÃO DOS COMPOSTOS HALOGENADOS CLORETOS E BROMETOS ALIFÁTICOS Sinal do Íon Molecular R CH 2 Cl R. CH 2 Só observado nos compostos de baixo peso molecular Cl CH 2 Cl m/z 49 e m/z 51 R. R CH 2 Br CH 2 Br CH 2 Br m/z 93 e m/z 95
98 IODETOS ALIFÁTICOS Sinal do Íon Molecular É o mais forte dentre todos os halogenetos Os iodetos quebram da mesma forma que os cloretos e brometos FLUORETOS ALIFÁTICOS Sinal do Íon Molecular É o mais fraco dentre todos os halogenetos A quebra da ligação C-C α,β é menos importante do que nos demais mono-halogenetos, porém a quebra de uma ligação C-H no Cα é mais importante
99 Standard Interpretation Procedure 1) Study all available information (spectroscopic, chemical, sample history). Give explicit directions for obtaining spectrum (better yet, do it yourself). a) Verify the m/z assignments. Use calibrants if needed. 2) Using isotopic abundances (where possible) deduce the elemental composition of each peak in the spectrum; calculate rings plus double bonds. 3) Test molecular ion identity; must be the highest mass peak in spectrum, odd-electron ion, and give logical neutral losses. Check with CI or other soft ionization. 4) Mark important ions: odd-electron and those of highest abundance, highest mass, and/or highest in a group of peaks. 99
100 Standard Interpretation Procedure 5) Study general appearance of the spectrum: molecular stability, labile bonds, etc. 6) Postulate and rank possible sub-structural assignments for: a) Important low-mass ion series b) Important primary neutral fragments from M. indicated by high-mass ions (loss of largest alkyl favored) plus those secondary fragmentations indicated by MS/MS spectra. c) Important characteristic ions. 7) Postulate molecular structures; test against a reference spectrum, against spectra of similar compounds, or against spectra predicted from mechanisms of ion decompositions 100
Espectrometria de massas
 Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
Algumas considerações iniciais. Interpretação de espectros de massas
 Interpretação de espectros de massas 1. A maioria dos espectros de massas não são de interpretação fácil sem informações adicionais, tais como análise elementar, RMN, etc. 2. Os padrões de fragmentação
Interpretação de espectros de massas 1. A maioria dos espectros de massas não são de interpretação fácil sem informações adicionais, tais como análise elementar, RMN, etc. 2. Os padrões de fragmentação
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução
 Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons)
 Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons) Clivagem α: fragmentação iniciada pelo sítio radicalar em acetona Fragmentações do íon molecular podem
Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons) Clivagem α: fragmentação iniciada pelo sítio radicalar em acetona Fragmentações do íon molecular podem
Resumo de Mecanismos de fragmentação
 Resumo de Mecanismos de fragmentação Clivagem s. Clivagem a: iniciada pelo sítio radicalar. Clivagem i: iniciada pela carga do íon. Fragmentações subseqüentes por transferência 1,2 ou 1,4 de H. Rearranjo
Resumo de Mecanismos de fragmentação Clivagem s. Clivagem a: iniciada pelo sítio radicalar. Clivagem i: iniciada pela carga do íon. Fragmentações subseqüentes por transferência 1,2 ou 1,4 de H. Rearranjo
Estratégias para interpretação de espectros de massas
 Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
Mary Santiago Silva 05/05/2010
 Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
HIDROCARBONETOS FUNÇÕES ORGÂNICAS
 HIDROCARBONETOS FUNÇÕES ORGÂNICAS FUNÇÕES ORGÂNICAS O átomo de carbono: Apresenta capacidade singular de compartilhar elétrons com outros átomos de carbono formando ligações carbono-carbono estáveis. Permite
HIDROCARBONETOS FUNÇÕES ORGÂNICAS FUNÇÕES ORGÂNICAS O átomo de carbono: Apresenta capacidade singular de compartilhar elétrons com outros átomos de carbono formando ligações carbono-carbono estáveis. Permite
QUÍMICA ORGÂNICA PARTE1 PROFESSOR: JOÃO RODRIGO ESCALARI QUINTILIANO
 QUÍMICA ORGÂNICA PARTE1 PROFESSOR: JOÃO RODRIGO ESCALARI QUINTILIANO 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono
QUÍMICA ORGÂNICA PARTE1 PROFESSOR: JOÃO RODRIGO ESCALARI QUINTILIANO 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono
Introdução à Química Orgânica. Ana Clara Vasconcelos Helber Cardoso Heloísa Miranda Edirley Maruzo Costa Michelle Rodrigues Thaís Andrade
 Introdução à Química Orgânica Ana Clara Vasconcelos Helber Cardoso Heloísa Miranda Edirley Maruzo Costa Michelle Rodrigues Thaís Andrade Química Orgânica é o ramo da Química que estuda os compostos de
Introdução à Química Orgânica Ana Clara Vasconcelos Helber Cardoso Heloísa Miranda Edirley Maruzo Costa Michelle Rodrigues Thaís Andrade Química Orgânica é o ramo da Química que estuda os compostos de
LISTA DAS FUNÇÕES ORGÂNICAS
 Orgânica Na pré-história, o ser humano se limitava a usar materiais que encontrava na natureza, sem provocar neles grandes modificações. A descoberta do fogo trouxe ao ser humano a primeira maneira efetiva
Orgânica Na pré-história, o ser humano se limitava a usar materiais que encontrava na natureza, sem provocar neles grandes modificações. A descoberta do fogo trouxe ao ser humano a primeira maneira efetiva
Química 2 aula 1 COMENTÁRIOS ATIVIDADES PARA SALA COMENTÁRIOS ATIVIDADES PROPOSTAS. 4. Seja a estrutura do β-caroteno abaixo:
 Química aula. Seja a estrutura do β-caroteno abaixo: MENTÁRIS ATIVIDADES PARA SALA. π π Veja que a estrutura só apresenta ligações do tipo simples e dupla. Logo, as hibridações são do tipo sp e sp.. No
Química aula. Seja a estrutura do β-caroteno abaixo: MENTÁRIS ATIVIDADES PARA SALA. π π Veja que a estrutura só apresenta ligações do tipo simples e dupla. Logo, as hibridações são do tipo sp e sp.. No
AULA 21 NOMENCLATURA DE COMPOSTOS ORGÂNICOS E HIDROCARBONETOS
 AULA 21 NOMENCLATURA DE COMPOSTOS ORGÂNICOS E HIDROCARBONETOS NOMENCLATURA OFICIAL DOS COMPOSTOS ORGÂNICOS De acordo com a União Internacional de Química Pura e Aplicada (I.U.P.AC.), o nome de um composto
AULA 21 NOMENCLATURA DE COMPOSTOS ORGÂNICOS E HIDROCARBONETOS NOMENCLATURA OFICIAL DOS COMPOSTOS ORGÂNICOS De acordo com a União Internacional de Química Pura e Aplicada (I.U.P.AC.), o nome de um composto
TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS
 TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS 1) 3.600-2.700 cm -1 A absorção nesta região é associada às vibrações de deformação axial nos átomos de hidrogênio ligados a carbono,
TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS 1) 3.600-2.700 cm -1 A absorção nesta região é associada às vibrações de deformação axial nos átomos de hidrogênio ligados a carbono,
Química E Extensivo V. 4
 Química E Extensivo V. 4 Exercícios 01) D 02) A Exemplo de obtenção de benzoato de sódio: O O COH + NaHCO 3(aq) + CO Na + HO l + CO 2 () 2(g) Ácido benzoico + bicarbonato de sódio Benzoato de sódio 03)
Química E Extensivo V. 4 Exercícios 01) D 02) A Exemplo de obtenção de benzoato de sódio: O O COH + NaHCO 3(aq) + CO Na + HO l + CO 2 () 2(g) Ácido benzoico + bicarbonato de sódio Benzoato de sódio 03)
QUÍMICA ORGÂNICA parte 1
 QUÍMICA ORGÂNICA parte 1 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono primário Ligado diretamente, no máximo, a
QUÍMICA ORGÂNICA parte 1 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono primário Ligado diretamente, no máximo, a
QUÍMICA Prof. Alison Cosme Souza Gomes. Funções Orgânicas Resumo UERJ
 QUÍMICA Prof. Alison Cosme Souza Gomes Funções Orgânicas Resumo UERJ A Química Orgânica é a parte da química que estuda os diversos compostos de carbonos existentes. São compostos com sua base nos átomos
QUÍMICA Prof. Alison Cosme Souza Gomes Funções Orgânicas Resumo UERJ A Química Orgânica é a parte da química que estuda os diversos compostos de carbonos existentes. São compostos com sua base nos átomos
SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS
 SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS ÁLCOOL São compostos orgânicos que apresentam o grupo funcional hidroxila ( OH) ligado a carbono saturado. ÁLCOOL Classificação Quanto ao número
SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS ÁLCOOL São compostos orgânicos que apresentam o grupo funcional hidroxila ( OH) ligado a carbono saturado. ÁLCOOL Classificação Quanto ao número
Estratégias para interpretação de espectros de massas
 Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
Química Orgânica. Química orgânica: Estrutura das moléculas. Grupos funcionais. Estereoquímica. Reatividade..
 Química Orgânica X Química orgânica: Estrutura das moléculas. Grupos funcionais. Estereoquímica. Reatividade.. Química Orgânica Os compostos orgânicos são as substâncias químicas que contêm carbono e hidrogénio,
Química Orgânica X Química orgânica: Estrutura das moléculas. Grupos funcionais. Estereoquímica. Reatividade.. Química Orgânica Os compostos orgânicos são as substâncias químicas que contêm carbono e hidrogénio,
Espectroscopia no IV
 Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Estrutura de moléculas orgânicas e biológicas
 Hidrocarbonetos Os hidrocarbonetos são compostos orgânicos formados exclusivamente por átomos de carbono e hidrogénio, ligados por ligações covalentes simples (C H e C C), duplas (C = C) ou triplas (C
Hidrocarbonetos Os hidrocarbonetos são compostos orgânicos formados exclusivamente por átomos de carbono e hidrogénio, ligados por ligações covalentes simples (C H e C C), duplas (C = C) ou triplas (C
Região do Espectro Eletromagnético
 Região do Espectro Eletromagnético Região do Espectro Eletromagnético Raios X UV / V Infravermelho Microonda Radiofrequência Transição Quebra de ligação Eletrônica Vibracional Rotacional Spin nuclear (RMN),
Região do Espectro Eletromagnético Região do Espectro Eletromagnético Raios X UV / V Infravermelho Microonda Radiofrequência Transição Quebra de ligação Eletrônica Vibracional Rotacional Spin nuclear (RMN),
Gabaritos Resolvidos Energia Química Semiextensivo V3 Frente D
 01) B Composto A: éter Composto B: fenol Composto C: álcool Fórmula molecular dos 3 compostos: C 7 H 8 O Compostos de mesma fórmula molecular e função química diferente isomeria de função. 02) B I. Álcool
01) B Composto A: éter Composto B: fenol Composto C: álcool Fórmula molecular dos 3 compostos: C 7 H 8 O Compostos de mesma fórmula molecular e função química diferente isomeria de função. 02) B I. Álcool
6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS
 131 6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS Quando a ligação pi estiver entre dois carbonos, formando alcenos, a reação será de adição eletrofílica. Substratos que apresentam a ligação pi formada entre
131 6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS Quando a ligação pi estiver entre dois carbonos, formando alcenos, a reação será de adição eletrofílica. Substratos que apresentam a ligação pi formada entre
Aula 7. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Reações de Eliminação de Haletos de Alquila. Reações de Álcoois e Éteres
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 7 Reações de Eliminação de Haletos de Alquila Reações de Álcoois e Éteres Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 7 Reações de Eliminação de Haletos de Alquila Reações de Álcoois e Éteres Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice
O DIAMANTE POSSUI HIBRIDIZAÇÃO
 QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
BC 0307 Transformações Químicas
 BC 0307 Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 BC 0307 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares
BC 0307 Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 BC 0307 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares
AULA 17. Reações Orgânicas. Prof Taynara Oliveira
 AULA 17 Reações Orgânicas Prof Taynara Oliveira Para que ocorra uma reação química, é necessário que as ligações existentes entre os átomos de uma molécula se rompam e esses átomos se rearranjem, formando
AULA 17 Reações Orgânicas Prof Taynara Oliveira Para que ocorra uma reação química, é necessário que as ligações existentes entre os átomos de uma molécula se rompam e esses átomos se rearranjem, formando
INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO QUESTÕES. Escolha 12 exercícios dos mostrados abaixo e responda-os.
 3º EM Química A Wesley Av. Dissertativa 19/10/16 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta
3º EM Química A Wesley Av. Dissertativa 19/10/16 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta
Absorções de grupos funcionais na região do Infravermelho
 Intensidade Deformação/Observação Grupo requência cm -1 Alcanos 2840-3000 C-H axial -CH 3 2970-2950 C-H axial assimétrica ( as ) -CH 3 2880-2860 C-H axial simétrica ( s ) -CH 3 1735 C-H angular simétrica
Intensidade Deformação/Observação Grupo requência cm -1 Alcanos 2840-3000 C-H axial -CH 3 2970-2950 C-H axial assimétrica ( as ) -CH 3 2880-2860 C-H axial simétrica ( s ) -CH 3 1735 C-H angular simétrica
NORMAL: RAMIFICADA: H H H C C
 C4 OBS.: C Carbono primário: Se o átomo de carbono estiver ligado a um átomo de carbono. Carbono secundário: se um átomo de carbono estiver ligado a dois átomos de carbono. Carbono terciário: se estiver
C4 OBS.: C Carbono primário: Se o átomo de carbono estiver ligado a um átomo de carbono. Carbono secundário: se um átomo de carbono estiver ligado a dois átomos de carbono. Carbono terciário: se estiver
Profº André Montillo
 Profº André Montillo www.montillo.com.br Definição: É o ramo da química que estuda os composto formados pelo arbono. São os compostos encontrados nos organismos vivos e representam 60% da massa do organismo:
Profº André Montillo www.montillo.com.br Definição: É o ramo da química que estuda os composto formados pelo arbono. São os compostos encontrados nos organismos vivos e representam 60% da massa do organismo:
ANDERSON ORZARI RIBEIRO
 Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares CAPÍTULO 3
Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares CAPÍTULO 3
Solução Comentada Prova de Química
 34. A histamina, estrutura mostrada abaixo, é uma substância orgânica que provoca inchaço e coceira, e que é liberada pelas células de defesa, quando somos picados por insetos. N NH 2 N H Se quisermos
34. A histamina, estrutura mostrada abaixo, é uma substância orgânica que provoca inchaço e coceira, e que é liberada pelas células de defesa, quando somos picados por insetos. N NH 2 N H Se quisermos
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 12 TURMA INTENSIVA
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 12 TURMA INTENSIVA 01. Para os compostos Os grupos CH 3 (A) e OH (D) aumentam a reatividade pois deixam o ciclo mais rico em elétrons, sendo que D é ainda mais reativo
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 12 TURMA INTENSIVA 01. Para os compostos Os grupos CH 3 (A) e OH (D) aumentam a reatividade pois deixam o ciclo mais rico em elétrons, sendo que D é ainda mais reativo
Gabaritos Resolvidos Energia Química Semiextensivo V4 Frente E
 01) D A preferência de substituição obedece a ordem: C terciário C secundário C primário. A halogenação de um alcano se dá por substituição de um átomo de hidrogênio por um halogênio, resultando em um
01) D A preferência de substituição obedece a ordem: C terciário C secundário C primário. A halogenação de um alcano se dá por substituição de um átomo de hidrogênio por um halogênio, resultando em um
Carbonos Hidrogênios Oxigênios C 2 H 6 O
 Prof. Edson Cruz ISOMERIA Carbonos Hidrogênios Oxigênios H H H C C O H H C O C H H H H H H H C 2 H 6 O C 2 H 6 O Os compostos H 3 C CH 2 OH e H 3 C O CH 3 são ISÔMEROS. ISÔMEROS são compostos diferentes
Prof. Edson Cruz ISOMERIA Carbonos Hidrogênios Oxigênios H H H C C O H H C O C H H H H H H H C 2 H 6 O C 2 H 6 O Os compostos H 3 C CH 2 OH e H 3 C O CH 3 são ISÔMEROS. ISÔMEROS são compostos diferentes
FCAV/UNESP. DISCIPLINA: Química Orgânica. ASSUNTO: Introdução à Química Orgânica
 FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Introdução à Química Orgânica QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos orgânicos.
FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Introdução à Química Orgânica QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos orgânicos.
LISTA DE EXERCÍCIOS 2º ANO
 Dentre os compostos apresentados, os dois que proporcionam melhor qualidade para os óleos de cozinha são os ácidos linolênico (três duplas entre carbonos) e linoleico (duas duplas entre carbonos). Carbono
Dentre os compostos apresentados, os dois que proporcionam melhor qualidade para os óleos de cozinha são os ácidos linolênico (três duplas entre carbonos) e linoleico (duas duplas entre carbonos). Carbono
Química Orgânica. Profª Drª Cristiane de Abreu Dias
 Química Orgânica Profª Drª Cristiane de Abreu Dias Composição dos Compostos Orgânicos Características Gerais dos Compostos Orgânicos Capacidade de formar Cadeias Representação usual das Cadeias Carbônicas
Química Orgânica Profª Drª Cristiane de Abreu Dias Composição dos Compostos Orgânicos Características Gerais dos Compostos Orgânicos Capacidade de formar Cadeias Representação usual das Cadeias Carbônicas
Análise Estrutural. José Carlos Marques Departamento de Química Universidade da Madeira
 Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
FCAV/UNESP. DISCIPLINA: Química Orgânica. ASSUNTO: Introdução à Química Orgânica
 FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Introdução à Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Introdução à Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
Química E Intensivo V. 1
 GABARIT Química E Intensivo V. Exercícios 0 adeia carbônica normal é a cadeia não ramificada. Nesse tipo de cadeia, existirão apenas carbonos primários e secundários. 0 99 Na cadeia carbônica saturada,
GABARIT Química E Intensivo V. Exercícios 0 adeia carbônica normal é a cadeia não ramificada. Nesse tipo de cadeia, existirão apenas carbonos primários e secundários. 0 99 Na cadeia carbônica saturada,
Química D Intensivo V. 1
 Química D Intensivo V. 1 Exercícios 01) A 07) B Na síntese de Wöhler, o cianato de amônio (inorgânico) foi transformado em ureia (orgânica). 02) 63 01. Certa. 02. Certa. 04. Certa. 08. Certa. 16. Certa.
Química D Intensivo V. 1 Exercícios 01) A 07) B Na síntese de Wöhler, o cianato de amônio (inorgânico) foi transformado em ureia (orgânica). 02) 63 01. Certa. 02. Certa. 04. Certa. 08. Certa. 16. Certa.
Isomeria h Quantas vezes caiu no ENEM. Complexidade. Tempo de estudo a dedicar. Videoaulas para estudar. Exercícios por resolver
 TEMAS VESTIBULARES Q1 Isomeria Quantas vezes caiu no ENEM Complexidade Tempo de estudo a dedicar Videoaulas para estudar Exercícios por resolver 8 3 8h 10 20 Isomeria 05 out EXERCÍCIOS DE AULA 1. A isomerização
TEMAS VESTIBULARES Q1 Isomeria Quantas vezes caiu no ENEM Complexidade Tempo de estudo a dedicar Videoaulas para estudar Exercícios por resolver 8 3 8h 10 20 Isomeria 05 out EXERCÍCIOS DE AULA 1. A isomerização
Professor Armando J. De Azevedo
 Professor Armando J. De Azevedo Química Professor Armando J. De Azevedo WWW.quimicarmando.com REAÇÃO DE ADIÇÃO As reações de adição são aquelas onde um átomo proveniente de uma substância orgânica ou inorgânica
Professor Armando J. De Azevedo Química Professor Armando J. De Azevedo WWW.quimicarmando.com REAÇÃO DE ADIÇÃO As reações de adição são aquelas onde um átomo proveniente de uma substância orgânica ou inorgânica
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS
 PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
Estrutura e reatividade de grupos de compostos
 Estrutura e reatividade de grupos de compostos 1. Alcanos 2. Alcenos 3. Alcinos 4. 5. Aldeídos e Cetonas 6. 7. Fenóis 8. Ácidos carboxilicos 9. Aminas Reatividade Polarização da ligação C-O ou da ligação
Estrutura e reatividade de grupos de compostos 1. Alcanos 2. Alcenos 3. Alcinos 4. 5. Aldeídos e Cetonas 6. 7. Fenóis 8. Ácidos carboxilicos 9. Aminas Reatividade Polarização da ligação C-O ou da ligação
Química Geral I Aula 3
 Química Geral I Aula 3 Curso de Química Licenciatura 2016-1 Prof. Udo Eckard Sinks Moléculas, Compostos e Fórmulas: Modelos Moleculares, Compostos Iônicos, Compostos moleculares, Fórmulas, Compostos e
Química Geral I Aula 3 Curso de Química Licenciatura 2016-1 Prof. Udo Eckard Sinks Moléculas, Compostos e Fórmulas: Modelos Moleculares, Compostos Iônicos, Compostos moleculares, Fórmulas, Compostos e
Exercícios de Introdução a Química Orgânica e Hidrocarbonetos
 Exercícios de Introdução a Orgânica e Hidrocarbonetos 1. A sibutramina (representada a seguir) é um fármaco controlado pela Agência Nacional de Vigilância Sanitária que tem por finalidade agir como moderador
Exercícios de Introdução a Orgânica e Hidrocarbonetos 1. A sibutramina (representada a seguir) é um fármaco controlado pela Agência Nacional de Vigilância Sanitária que tem por finalidade agir como moderador
Pré UFSC Química. Química Orgânica. Alcinos. Funções Orgânicas. Alcadienos. Hidrocarbonetos. Alcanos. Cicloalcanos. Alcenos.
 Química Orgânica Estuda as propriedades e composição dos compostos que apresentam o carbono como principal elemento químico. Alcinos São hidrocarbonetos acíclicos contendo uma única ligação tripla entre
Química Orgânica Estuda as propriedades e composição dos compostos que apresentam o carbono como principal elemento químico. Alcinos São hidrocarbonetos acíclicos contendo uma única ligação tripla entre
AMINAS,AMIDAS E OUTRAS FUNÇÕES ORGÂNICAS. Karla Gomes Diamantina-MG
 AMINAS,AMIDAS E OUTRAS FUNÇÕES ORGÂNICAS Karla Gomes Diamantina-MG AMINAS Compostos derivados da amônia, NH 3, pela substituição de um átomo de H (ou mais) por grupos carbônicos, em que o nitrogênio se
AMINAS,AMIDAS E OUTRAS FUNÇÕES ORGÂNICAS Karla Gomes Diamantina-MG AMINAS Compostos derivados da amônia, NH 3, pela substituição de um átomo de H (ou mais) por grupos carbônicos, em que o nitrogênio se
Química E Extensivo V. 8
 Química E Extensivo V. 8 Resolva Aula 9 Aula 0 9.01) E [ ] alceno ácido acético e ácido propanóico enérgica 0.01) ácido acético ácido propanóico U penteno- Aula 1 1.01) Método ofmann :N Rx x R Ṅ (primária)
Química E Extensivo V. 8 Resolva Aula 9 Aula 0 9.01) E [ ] alceno ácido acético e ácido propanóico enérgica 0.01) ácido acético ácido propanóico U penteno- Aula 1 1.01) Método ofmann :N Rx x R Ṅ (primária)
Química E Extensivo V. 3
 Química E Extensivo V. 3 01) Alternativa correta: A Exercícios O clorofórmio, nome usual do Triclorometano fórmula CHCl 3. É um polialeto, pois possui 3 átomos de Cloro. 02) Respostas: Pentaclorofenol
Química E Extensivo V. 3 01) Alternativa correta: A Exercícios O clorofórmio, nome usual do Triclorometano fórmula CHCl 3. É um polialeto, pois possui 3 átomos de Cloro. 02) Respostas: Pentaclorofenol
7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR
 163 7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR Para que uma reação orgânica ocorra, é necessário que haja rompimento nas ligações químicas envolvidas na estrutura das moléculas do substrato e do
163 7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR Para que uma reação orgânica ocorra, é necessário que haja rompimento nas ligações químicas envolvidas na estrutura das moléculas do substrato e do
Reações em Aromáticos
 Reações em Aromáticos 01 (Unicamp-SP) Um dos átomos de hidrogênio do anel benzênico pode ser substituído por CH3, OH, Cℓ ou COOH. a) Escreva as fórmulas e os nomes dos derivados benzênicos obtidos por
Reações em Aromáticos 01 (Unicamp-SP) Um dos átomos de hidrogênio do anel benzênico pode ser substituído por CH3, OH, Cℓ ou COOH. a) Escreva as fórmulas e os nomes dos derivados benzênicos obtidos por
CLASSIFICAÇÃO DAS CADEIAS CARBÔNICAS
 QUÍMICA ORGÂNICA 1 Profª Márcia Ribeiro Representação dos Compostos Orgânicos Os compostos orgânicos podem ser representados por diferentes fórmulas: Fórmula Estrutural Plana Fórmula Estrutural Condensada
QUÍMICA ORGÂNICA 1 Profª Márcia Ribeiro Representação dos Compostos Orgânicos Os compostos orgânicos podem ser representados por diferentes fórmulas: Fórmula Estrutural Plana Fórmula Estrutural Condensada
Química E Extensivo V. 4
 Química E Extensivo V. 4 Resolva Aula 1 Aula 14 1.01) a) 14.01) a) metanoato de sódio formato de sódio b) b) etanoato de sódio acetato de sódio propanoato de sódio propionato de sódio butanoato de sódio
Química E Extensivo V. 4 Resolva Aula 1 Aula 14 1.01) a) 14.01) a) metanoato de sódio formato de sódio b) b) etanoato de sódio acetato de sódio propanoato de sódio propionato de sódio butanoato de sódio
Definição: São compostos derivados dos hidrocarbonetos pela substituição de um ou mais hidrogênios por igual número de halogênios (F, Cl, Br e I)
 QUÍMICA ORGÂNICA Definição: São compostos derivados dos hidrocarbonetos pela substituição de um ou mais hidrogênios por igual número de halogênios (F, Cl, Br e I) Exemplos: Algumas Propriedades Físicas
QUÍMICA ORGÂNICA Definição: São compostos derivados dos hidrocarbonetos pela substituição de um ou mais hidrogênios por igual número de halogênios (F, Cl, Br e I) Exemplos: Algumas Propriedades Físicas
Química: Reações Orgânicas
 Química: Reações Orgânicas 1. (Ufrgs 2015) Dois hidrocarbonetos I e II reagem com bromo, conforme mostrado abaixo. C H Br C H Br HBr x y 2 x y 1 I CzHn Br2 C2HnBr 2 II É correto afirmar que I e II são,
Química: Reações Orgânicas 1. (Ufrgs 2015) Dois hidrocarbonetos I e II reagem com bromo, conforme mostrado abaixo. C H Br C H Br HBr x y 2 x y 1 I CzHn Br2 C2HnBr 2 II É correto afirmar que I e II são,
QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES)
 QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES) REAÇÕES DE SUBSTITUIÇÃO São assim denominadas porque um hidrogênio da molécula orgânica é substituído por um átomo de halogênio, por um grupo nitro (NO 2 ) ou um grupo
QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES) REAÇÕES DE SUBSTITUIÇÃO São assim denominadas porque um hidrogênio da molécula orgânica é substituído por um átomo de halogênio, por um grupo nitro (NO 2 ) ou um grupo
Funções orgânicas oxigenadas e nitrogenadas.
 Funções orgânicas oxigenadas e nitrogenadas Funções que possuem ou derivam do grupo funcional hidroxila ( OH) Ex: a) Etanol Álcool b) Prop 2 en 1 ol Ex:... estiver ligado a um carbono saturado...... estiver
Funções orgânicas oxigenadas e nitrogenadas Funções que possuem ou derivam do grupo funcional hidroxila ( OH) Ex: a) Etanol Álcool b) Prop 2 en 1 ol Ex:... estiver ligado a um carbono saturado...... estiver
QFL 2340 Estrutura e Propriedade de Compostos Orgânicos Lista 08: Reações Orgânicas. Parte I: Noções Gerais e Adição Nucleofílica
 QFL 2340 Estrutura e Propriedade de Compostos Orgânicos - 2013 Lista 08: Reações Orgânicas Parte I: Noções Gerais e Adição Nucleofílica 1. Cada uma das moléculas abaixo são eletrofílicas, identifique o
QFL 2340 Estrutura e Propriedade de Compostos Orgânicos - 2013 Lista 08: Reações Orgânicas Parte I: Noções Gerais e Adição Nucleofílica 1. Cada uma das moléculas abaixo são eletrofílicas, identifique o
Química E Extensivo V. 8
 Química E Extensivo V. 8 Exercícios 01) E 02) 05 03) B a) O ataque ao H 2 C = CH 2 é feito pelo H + (regente que precisa de elétrons). Assim, ocorrerá adição eletrófila pois, o H + encontrará os elétons
Química E Extensivo V. 8 Exercícios 01) E 02) 05 03) B a) O ataque ao H 2 C = CH 2 é feito pelo H + (regente que precisa de elétrons). Assim, ocorrerá adição eletrófila pois, o H + encontrará os elétons
REAÇÕES ORGÂNICAS. Prof: WELLINGTON DIAS
 REAÇÕES ORGÂNICAS Prof: WELLINGTON DIAS REAÇÕES ORGÂNICAS 1. REAÇÕES DE SUBSTITUIÇÃO. 1.1. ALCANOS: Por serem apolares sofrem cisão homolítica e a reação ocorre por meio de radicais livres. EXEMPLO: Halogenação
REAÇÕES ORGÂNICAS Prof: WELLINGTON DIAS REAÇÕES ORGÂNICAS 1. REAÇÕES DE SUBSTITUIÇÃO. 1.1. ALCANOS: Por serem apolares sofrem cisão homolítica e a reação ocorre por meio de radicais livres. EXEMPLO: Halogenação
Introdução à Química Orgânica
 Introdução à Química Orgânica O que é Química Orgânica? Acreditava-se, antigamente, que a química orgânica estudava os compostos extraídos de organismos vivos,na qual esses compostos orgânicos precisariam
Introdução à Química Orgânica O que é Química Orgânica? Acreditava-se, antigamente, que a química orgânica estudava os compostos extraídos de organismos vivos,na qual esses compostos orgânicos precisariam
Disciplina: Química C
 Disciplina: Química C EXTENSIVO E TERCEIRÃO VOLUME 10 AULA 28 FRENTE: C PÁGINA: 2 EXERCÍCIO: 28.01 a) A redução de um aldeído leva a formação de um álcool primário: (etanal) (etanol) b) Como o grupo funcional
Disciplina: Química C EXTENSIVO E TERCEIRÃO VOLUME 10 AULA 28 FRENTE: C PÁGINA: 2 EXERCÍCIO: 28.01 a) A redução de um aldeído leva a formação de um álcool primário: (etanal) (etanol) b) Como o grupo funcional
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da
 Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
1164 BIOLOGIA ESTRUTURAL Aula 1 Prof. Dr. Valmir Fadel
 H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
Compostos de carbono
 Compostos de carbono aroma de banana canela ácido fórmico O que são? Como podemos classificá-los? Compostos de carbono Como podemos obtê-los? Porque são importantes? Respostas às questões Podem ser constituídos
Compostos de carbono aroma de banana canela ácido fórmico O que são? Como podemos classificá-los? Compostos de carbono Como podemos obtê-los? Porque são importantes? Respostas às questões Podem ser constituídos
IDENTIFICAÇÃO DE UMA ESTRUTURA MOLECULAR A PARTIR
 Licenciatura em Ciências da Saúde Métodos Instrumentais de Análise IDENTIFICAÇÃO DE UMA ESTRUTURA MOLECULAR A PARTIR DE GRÁFICOS DE ESPECTROMETRIA DE MASSA, RESSONÂNCIA MAGNÉTICA NUCLEAR E INFRAVERMELHOS
Licenciatura em Ciências da Saúde Métodos Instrumentais de Análise IDENTIFICAÇÃO DE UMA ESTRUTURA MOLECULAR A PARTIR DE GRÁFICOS DE ESPECTROMETRIA DE MASSA, RESSONÂNCIA MAGNÉTICA NUCLEAR E INFRAVERMELHOS
Tarefa 09 Professor Negri. 01. Quanto à classificação e nomenclatura da estrutura abaixo, assinale a alternativa CORRETA:
 Tarefa 09 Professor Negri 01. Quanto à classificação e nomenclatura da estrutura abaixo, assinale a alternativa ORRETA: a) hidrocarboneto de cadeia aberta, alcano, metano b) hidrocarboneto de cadeia aberta,
Tarefa 09 Professor Negri 01. Quanto à classificação e nomenclatura da estrutura abaixo, assinale a alternativa ORRETA: a) hidrocarboneto de cadeia aberta, alcano, metano b) hidrocarboneto de cadeia aberta,
Interpretação de Espectros de Infravermelho
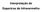 Interpretação de Espectros de Infravermelho Frequências aproximadas de Absorção no Infravermelho correspondentes aos movimentos de Stretching de ligações X-H (cm -1 ) B-H 2400 C-H 3000 N-H 3400 O-H 3600
Interpretação de Espectros de Infravermelho Frequências aproximadas de Absorção no Infravermelho correspondentes aos movimentos de Stretching de ligações X-H (cm -1 ) B-H 2400 C-H 3000 N-H 3400 O-H 3600
QFL 2340 Estrutura e Propriedade de Compostos Orgânicos Lista 09: Reações Orgânicas. Parte I: Noções Gerais e Adição Nucleofílica
 QFL 2340 Estrutura e Propriedade de Compostos Orgânicos - 2014 Lista 09: Reações Orgânicas Parte I: Noções Gerais e Adição Nucleofílica 1. Cada uma das moléculas abaixo são eletrofílicas, identifique o
QFL 2340 Estrutura e Propriedade de Compostos Orgânicos - 2014 Lista 09: Reações Orgânicas Parte I: Noções Gerais e Adição Nucleofílica 1. Cada uma das moléculas abaixo são eletrofílicas, identifique o
H 2 C OCH 3 H 2 C OH EXERCÍCIOS DE CLASSE
 EXERCÍCIOS DE CLASSE 1- De um modo geral, o ponto de ebulição dos compostos orgânicos cresce com o aumento do peso molecular, o que não acontece com os compostos do quadro abaixo: COMPOSTO PESO MOLECULAR
EXERCÍCIOS DE CLASSE 1- De um modo geral, o ponto de ebulição dos compostos orgânicos cresce com o aumento do peso molecular, o que não acontece com os compostos do quadro abaixo: COMPOSTO PESO MOLECULAR
DISCIPLINA: Química Fisiológica ASSUNTO: Fundamentos de Química Orgânica
 Universidade Estadual Paulista UNESP Faculdade de Ciências Agrárias e Veterinárias - FCAV DISCIPLINA: Química Fisiológica ASSUNTO: Fundamentos de Química Orgânica 1 1ª Semana 21/02/2019: Composição e estrutura
Universidade Estadual Paulista UNESP Faculdade de Ciências Agrárias e Veterinárias - FCAV DISCIPLINA: Química Fisiológica ASSUNTO: Fundamentos de Química Orgânica 1 1ª Semana 21/02/2019: Composição e estrutura
1.1. Tipos de ligações químicas. Tipos de ligações químicas
 1.1. Tipos de ligações químicas Tipos de ligações químicas LIGAÇÃO QUÍMICA Tipos de ligações químicas As ligações covalentes, iónicas e metálicas caraterizam-se por uma partilha significativa de eletrões
1.1. Tipos de ligações químicas Tipos de ligações químicas LIGAÇÃO QUÍMICA Tipos de ligações químicas As ligações covalentes, iónicas e metálicas caraterizam-se por uma partilha significativa de eletrões
PPGQTA. Prof. MGM D Oca
 PPGQTA Prof. Compostos Carbonílicos O grupo carbonila é um dos mais importantes grupos funcionais e está envolvido em muitas reações. Reações envolvendo grupos carbonila também são particularmente importantes
PPGQTA Prof. Compostos Carbonílicos O grupo carbonila é um dos mais importantes grupos funcionais e está envolvido em muitas reações. Reações envolvendo grupos carbonila também são particularmente importantes
Análise Estrutural. José Carlos Marques Departamento de Química Universidade da Madeira
 Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
Reações de Oxidação e Substituição. Karla Gomes Diamantina-MG
 Reações de Oxidação e Substituição Karla Gomes Diamantina-MG Reações de oxidação Envolvem aumento no estado de oxidação (Nox) dos átomos presentes em uma molécula. De forma geral: Substância orgânica (redutora)
Reações de Oxidação e Substituição Karla Gomes Diamantina-MG Reações de oxidação Envolvem aumento no estado de oxidação (Nox) dos átomos presentes em uma molécula. De forma geral: Substância orgânica (redutora)
Funções Orgânicas e Suas Nomenclaturas. Hidrocarbonetos
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA ORGÂNICA 2ª SÉRIE - ENSINO MÉDIO - PARTE 2 ============================================================================================= Funções
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA ORGÂNICA 2ª SÉRIE - ENSINO MÉDIO - PARTE 2 ============================================================================================= Funções
ESTUDANTE: Química Orgânica Básica
 ESTUDANTE: Química Orgânica Básica Professor André Calaça QUÍMICA ORGÂNICA O carbono é um elemento que está sempre presente no nosso cotidiano. Ele pode ser encontrado no ar na forma de moléculas de gás
ESTUDANTE: Química Orgânica Básica Professor André Calaça QUÍMICA ORGÂNICA O carbono é um elemento que está sempre presente no nosso cotidiano. Ele pode ser encontrado no ar na forma de moléculas de gás
Química E Extensivo V. 5
 Química E Extensivo V. 5 Exercícios 01) a) b) 02) F V V F a) Errada. Existem séries homólogas em qualquer função. b) Certa. Na série homóloga, cada membro tem um CH 2 a mais. Massa molecular: 14µ. c) Certa.
Química E Extensivo V. 5 Exercícios 01) a) b) 02) F V V F a) Errada. Existem séries homólogas em qualquer função. b) Certa. Na série homóloga, cada membro tem um CH 2 a mais. Massa molecular: 14µ. c) Certa.
Espectroscopia no Infravermelho (IR)
 Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
CH 3 CH 2 CH 2 CH 3 Butano
 1. Isomeria Moléculas que têm a mesma fórmula molecular, mas não são idênticas, são chamadas isômeros. s isômeros dividem se em duas classes: isômeros constitucionais e Estereoisômeros. 1.1 Isômeros constitucionais
1. Isomeria Moléculas que têm a mesma fórmula molecular, mas não são idênticas, são chamadas isômeros. s isômeros dividem se em duas classes: isômeros constitucionais e Estereoisômeros. 1.1 Isômeros constitucionais
Química II. Módulo 9. Questões de Aplicação. OH b) O c) C C C C C C C C C C. 1. a) 3,4,4-trimetil-2-pentanol C OH
 Química II Módulo 9 Questões de Aplicação 1. a) 3,4,4-trimetil-2-pentanol 5 4 3 2 1 b) 3-etil-4-metil-1-hidróxi-benzeno 8 7 6 5 4 3 2 1 i) 1-hidróxi-4-metil-benzeno ou p- hidróxi-metil-benzeno 2. a) Fenóxi-Benzeno
Química II Módulo 9 Questões de Aplicação 1. a) 3,4,4-trimetil-2-pentanol 5 4 3 2 1 b) 3-etil-4-metil-1-hidróxi-benzeno 8 7 6 5 4 3 2 1 i) 1-hidróxi-4-metil-benzeno ou p- hidróxi-metil-benzeno 2. a) Fenóxi-Benzeno
1.1. REAÇÃO DE SUBSTITUIÇÃO CARACTERÍSTICA DE COMPOSTOS SATURADOS ( ALCANOS E HALETOS ORGÂNICOS) C A + B X C B + A X
 1.1. REAÇÃO DE SUBSTITUIÇÃO CARACTERÍSTICA DE COMPOSTOS SATURADOS ( ALCANOS E HALETOS ORGÂNICOS) C A + B X C B + A X 1.1.1. SUBSTITUIÇÃO EM ALCANOS ( APOLARES SOFREM CISÃO HOMOLÍTICA) SUBSTITUIÇÃO POR
1.1. REAÇÃO DE SUBSTITUIÇÃO CARACTERÍSTICA DE COMPOSTOS SATURADOS ( ALCANOS E HALETOS ORGÂNICOS) C A + B X C B + A X 1.1.1. SUBSTITUIÇÃO EM ALCANOS ( APOLARES SOFREM CISÃO HOMOLÍTICA) SUBSTITUIÇÃO POR
Estrutura e reactividade de grupos de compostos
 Estrutura e reactividade de grupos de compostos 1. Alcanos 2. Alcenos 3. Alcinos 4. Álcoois 5. Aldeídos e Cetonas 6. Aromáticos 7. Fenóis 8. Ácidos carboxilicos 9. Aminas Fenóis Tal como para os álcoois
Estrutura e reactividade de grupos de compostos 1. Alcanos 2. Alcenos 3. Alcinos 4. Álcoois 5. Aldeídos e Cetonas 6. Aromáticos 7. Fenóis 8. Ácidos carboxilicos 9. Aminas Fenóis Tal como para os álcoois
Química D Extensivo V. 4
 Química D Extensivo V. 4 Exercícios 01) D 04) B I. II. III. 02) D Nas aminas terciárias, o nitrôgênio se liga a 3 carbonos. Isso ocorre nos dois compostos. 05) A O odor de peixe é provocado principalmente
Química D Extensivo V. 4 Exercícios 01) D 04) B I. II. III. 02) D Nas aminas terciárias, o nitrôgênio se liga a 3 carbonos. Isso ocorre nos dois compostos. 05) A O odor de peixe é provocado principalmente
Química D Semiextensivo V. 3
 GABARIT Química D Semiextensivo V 3 Exercícios 01) B 02) B 03) E omposto A: éter omposto B: fenol omposto : álcool Fórmula molecular dos três compostos: 7 8 éter fenol 2 álcool ompostos de mesma fórmula
GABARIT Química D Semiextensivo V 3 Exercícios 01) B 02) B 03) E omposto A: éter omposto B: fenol omposto : álcool Fórmula molecular dos três compostos: 7 8 éter fenol 2 álcool ompostos de mesma fórmula
Química COMPOSTOS DE CARBONO
 COMPOSTOS DE CARBONO COMPOSTOS DE CARBONO Compostos Orgânicos / Compostos de Carbono CO 2 COMPOSTOS DE CARBONO Inorgânicos Eram os que se obtinham de minerais Orgânicos Eram os que se obtinham de organismos
COMPOSTOS DE CARBONO COMPOSTOS DE CARBONO Compostos Orgânicos / Compostos de Carbono CO 2 COMPOSTOS DE CARBONO Inorgânicos Eram os que se obtinham de minerais Orgânicos Eram os que se obtinham de organismos
Abuso Sexual nas escolas Não dá para aceitar
 Abuso Sexual nas escolas Não dá para aceitar Por uma escola livre do SIDA República de Moçambique Química Ministério da Educação Exame Extraordinário 12ª Classe / 2013 Conselho Nacional de Exames, Certificação
Abuso Sexual nas escolas Não dá para aceitar Por uma escola livre do SIDA República de Moçambique Química Ministério da Educação Exame Extraordinário 12ª Classe / 2013 Conselho Nacional de Exames, Certificação
Índice. reações de S N 2. reações de S N 1. comparação entre S N 2 e S N 1. concorrência entre S N e eliminação
 Química Orgânica Substituição substituição nucleofílica alifática 1 Índice reações de S N 2 reações de S N 1 comparação entre S N 2 e S N 1 concorrência entre S N e eliminação Literatura recomendada Clayden,
Química Orgânica Substituição substituição nucleofílica alifática 1 Índice reações de S N 2 reações de S N 1 comparação entre S N 2 e S N 1 concorrência entre S N e eliminação Literatura recomendada Clayden,
Quí. Monitor: Victor Pontes
 Professor: Allan e Xandão Monitor: Victor Pontes Isomeria plana: função, posição, cadeia, metameria e tautomeria 12 set RESUMO Isomeria É o fenômeno quando dois ou mais compostos apresentam a mesma fórmula
Professor: Allan e Xandão Monitor: Victor Pontes Isomeria plana: função, posição, cadeia, metameria e tautomeria 12 set RESUMO Isomeria É o fenômeno quando dois ou mais compostos apresentam a mesma fórmula
Química 12.º Ano Unidade 2 Combustíveis, Energia e Ambiente Carlos Alberto da Silva Ribeiro de Melo
 Química 12.º Ano Unidade 2 Combustíveis, Energia e Ambiente Carlos Alberto da Silva Ribeiro de Melo Lição n.º 54 Sumário: Continuação da aula anterior. Hidrocarbonetos: grupos funcionais. Isomeria. COMPETÊNCIAS
Química 12.º Ano Unidade 2 Combustíveis, Energia e Ambiente Carlos Alberto da Silva Ribeiro de Melo Lição n.º 54 Sumário: Continuação da aula anterior. Hidrocarbonetos: grupos funcionais. Isomeria. COMPETÊNCIAS
Estrutura de moléculas orgânicas e biológicas
 Estrutura de moléculas orgânicas e biológicas Adaptado pelo Prof. Luís Perna 1 Compostos orgânicos Os compostos orgânicos formam um grupo enorme de substâncias que inclui a maioria daquelas que contêm
Estrutura de moléculas orgânicas e biológicas Adaptado pelo Prof. Luís Perna 1 Compostos orgânicos Os compostos orgânicos formam um grupo enorme de substâncias que inclui a maioria daquelas que contêm
CADEIAS CARBÔNICAS. 4. (G1 - cftsc) Qual a fórmula molecular do 2-metil-1-buteno? a) C 5 H 12. b) C 5 H 10. c) C 4 H 8. d) C 10 H 10. e) C 10 H 5.
 1. (Pucpr) Um tema de discussão atual tem sido o uso de sementes transgênicas voltado aos supostos aumento da produção de alimentos e diminuição do uso de pesticidas, tais como o carbofurano (I), o tralometrin
1. (Pucpr) Um tema de discussão atual tem sido o uso de sementes transgênicas voltado aos supostos aumento da produção de alimentos e diminuição do uso de pesticidas, tais como o carbofurano (I), o tralometrin
