Índice : 1-Objetivos Introdução Materiais utilizados Procedimento Resultados e análise dos resultados 09
|
|
|
- Victoria Weber
- 5 Há anos
- Visualizações:
Transcrição
1 Índice : -Objetivos 0 -Introdução 03 3-Materiais utilizados 05 4-Procedimento 06 5-Resultados e análise dos resultados 09 6-Discussão e conclusão 6 7-Bibliografia 8
2 -Objetivos O aproveitamento de linguagens de computação (C, Fortran, Basic, etc...) em ciências exatas tem permitido o desenvolvimento de aplicativos singulares em pesquisa e desenvolvimento de softwares em química. A programação de um aplicativo para cálculo é muitas vezes necessária e interessante devido à falta de programas específicos, como para o cálculo de constantes de velocidades de reações unimoleculares em fase gasosa. Este projeto visa a programação de um aplicativo para cálculo de constantes de velocidade, com base na teoria RRKM, usando a linguagem de programação C para uso em microcomputadores, aproveitando o conhecimento obtido do curso de computação e de cinética química adquirido durante a graduação no Instituto de Química da USP.
3 -Introdução O esquema de reação usado na teoria RRKM compreende as reações. e. : A + M k ( E * E * E *) A* (E*E*+E*) + M. A* (E*) k a ( E *) A + k produtos. onde a constante de velocidade de energização k é avaliada como função da energia por um tratamento mecânico-estatistico-quântico e a constante de velocidade de deenergização k é considerada independente da energia. Aplicando a teoria de transição do estado canônico (CTST) para o calculo de k a (E*), a reação. é escrita em termos de dois passos, onde A* é a molécula energizada (chamada também de molécula ativa) e A + é a transição de estado ( chamada também de complexo ativado). A molécula energizada A* é basicamente uma molécula A mas é caracterizada por possuir uma energia não fixada maior que um valor crítico E 0. A transição de estado A + é uma espécie intermediária entre reagentes e produtos e é caracterizada por possuir uma configuração correspondente ao topo da barreira de energia entre reagentes e produtos. Na teoria RRKM assim como na CTST (os estados de transição estão efetivamente em equilíbrio com as moléculas reagentes) a conversão de A* em produtos é considerada em termos do movimento translacional na coordenada de reação. A transição de estado é uma molécula cuja extensão da coordenada de reação encontrase em uma faixa arbitrariamente pequena no topo da barreira. Haverá usualmente mais de um estado quântico de A + que pode ser formada de um dado A*, por causa das diferente possíveis distribuições da energia entre a coordenada de reação e os graus de liberdade rotacional e vibracional da transição de estado. Assim a constante 3
4 de velocidade k a (E*) será avaliada como a soma de um conjunto de contribuições de vários estado de transição possíveis. A energia vibracional do ponto zero e a energia translacional são fixadas, porém a energia vibracional (a partir do ponto zero de energia) está sujeita a rápida redistribuição estatística, e a energia rotacional também pode contribuir para reação. Se um grau de liberdade rotacional mantém-se no mesmo estado quântico durante a reação o modo é chamado de adiabático. A teoria RRKM assume que todos os graus de liberdade não-adiabáticos da molécula são ativos e contribuem para a energia não fixa para a reação. A terminologia para energias de uma reação unimolecular é mostrada na figura : Figura : ilustração da terminologia das energias para uma reação unimolecular : A energia E* compreende ambas energias vibracional e rotacional (.3). A energia não fixa de um dado estado de transição é dada por (.4). A energia x está associada com o movimento translacional de A + na coordenada de reação (.5): E* E* vr = E* v + E* r.3 E + = E* - E 0.4 E + = E + vr + x = E + v + E + r + x.5 Whiten-Rabnovitch criaram um tratamento semi-clássico para a obtenção da soma de estados vibracionais-rotacionais e a densidade de estados vibracionais- 4
5 rotacionais. Além desse método também pode ser feita a contagem direta de estados vibracionais-rotacionais. Com estes resultados e com os parâmetros da molécula em estudo, podem ser feitos os cálculos para a determinação de k uni (constante de velocidade unimolecular). 3-Materiais utilizados Computador pessoal XT processador 486 DX4 00 MHz, memória RAM 5 Mb, HD,5 Gb Computador pessoal com processador Intel 00 MHz, memória RAM 36 Mb, HD,064Gb Compilador para linguagem C.5 da Microsoft (mesmo programa utilizado na graduação na matéria de mac5) Compilador para linguagem C++ da Borland International 5
6 4-Procedimento O programa foi elaborado com base no método analítico criado por Whiten- Rabnovitch. Nas equações analíticas de Whiten-Rabnovitch é feito um tratamento semi-clássico que incorpora a soma de estados vibracionais e rotacionais. A equação analítica obtida é mostrada a seguir : Q s r r W ( E ) ( E ae ) vr vr z r ( kt ) ( s r ) hv i 4. A densidade de estados vibracionais-rotacionais é obtida por diferenciação da equação 4.: s r Q ( E ae ) dw r vr z ( E ) vr r r de ( kt ) ( s r ) hv i 4. onde: W(E vr ) é o número de estados vibracionais rotacionais (sem unidades). (E vr ) é a densidade de estados vibracionais (em unidades de energia por mol). Q r é a função de partição rotacional E vr é a energia da molécula envolvendo os estados vibracionais e rotacionais. a é um fator empírico com valor entre 0 e. 6
7 E z é a energia do ponto zero de energia e corresponde a hv s é o número de freqüências vibracionais da molécula. r é o número de graus de liberdade rotacionais da molécula. k é a constante de Boltzmann T é a temperatura em que a reação ocorre, em Kelvin (n) é a função gama do valor n : (n) = (n - )(n ) = (n )(n ) =... = (n )(n ) () = (n )! hv é a produtória de h ( h aqui representa N A hc =,96*0-3 kj cm mol - onde h é a constante de Plank, N A é o número de Avogadro e c a velocidade da luz) vezes cada freqüência vibracional da molécula. R é o parâmetro modificado da dispersão da freqüência que pode ser calculado a partir da equação 4.3: s r s v R 4.3 s s v Sendo v a média dos quadrados das frequências da molécula e v o quadrado da média das frequências da molécula. Conhecendo-se o valor de R é possível calcular o valor de a através da equação 4.4 : a w( E ) R Sendo w(e )dado por : 4.4 (0, (,0 E,0) E 8,0) w (5,00 E,73 ( E ) w exp(,49 ( E ) 0,5 0, 5 ) 3,5) 4.5 7
8 Onde E = E vr / E z. dw/de é obtido por diferenciação da equação 4.5 : (0, (,0 E,0) E 8,0) dw / de (5,00,365 ( E ) dw / de (0,60478 ( E ) ,5 ) w ) w 4.6 O programa foi preparado de modo a fazer cada cálculo separadamente dado um valor de E vr. O programa também visa calcular a constante de velocidade unimolecular, portanto foram utilizadas as seguintes equações : k uni LQ hq Q exp( E 0 / RT ) E i max i W ( E vr k a ) exp( E c / RT ( E *) / Z M ) 4.7 Onde : k ( E*) a Q L W ( E vr ) / h ( E*) 4.8 Q E* = E 0 + E E ) ( i E onde i = 0,,, Onde : k uni é a constante de velocidade unimolecular, que é dada em s - se as energias E 0, E + e E + forem expressas em kjmol -. h neste caso é dado por N A h = 3,9903*0-3 kjmol - s (N A é o número de Avogadro e h a constante de Plank). R é a constante dos gases, cujo valor é 0, kjmol - K - L é um fator estatístico ou degenerecência do caminho da reação Q, Q +, Q são funções de partição rotacionais e vibracionais. 8
9 k [M] é substituído na equação 4.7 por c Z[M] onde c é a eficiência de desativação colisional, e Z é dado pela equação 4.,ou pode ser diretamente pedido pelo programa : Z 8RT d N 4. A / Onde Z é dado em m 3 mol - s -, quando o diâmetro de colisão d é expresso em metros e a massa reduzida em kgmol -. O teste do programa desenvolvido foi feito utilizando-se o estudo da isomerização do,-dicloro-ciclopropano para,3-cicloropropeno conforme a reação mostrada abaixo : Figura : reação de isomerização do,-ciclopropano a,3-ciclopropeno : A reação é de primeira ordem e não é afetada pela presença de radicais livres inibidores, e é um reação unimolecular. O fator estatístico para a transição de estado é 4, Q + /Q é igual a, e foi assumido que não há rotações ativas (r = 0) 5-Resultados e análise dos resultados Algoritmo e os Parâmetros Moleculares Quando o programa elaborado é iniciado, gera as seguintes mensagens na tela (as mensagens geradas pelo programa estão sublinhadas) : The RRKM Program version.0 9
10 - calculo de WE+vr e/ou PE*vr - Calculo de k uni Digite a opção e em seguir enter Caso se escolha a opção : Calcular WE+vr? -se sim -se não Se a escolha for : Temperatura : Valor de r : Valor de s : Valor das energias em kcal=, kj=, kev=3 Valor de E+vr: Valor de Ez : Valor de Qr : Número de freqüências do complexo ativado : Valor da freqüência do complexo ativado (em cm-) : (repetido quantas vezes for o número de freqüências) Se a escolha foi : Calcular PE*vr? -se sim -se não Se a escolha for : Temperatura : Valor de r : Valor de s : Valor das energias em Kcal=, KJ=, KeV=3 Valor de E*vr: 0
11 Valor de Ez : Valor de Eo : Valor de Qr : Número de freqüências da molecula reagente : Valor da freqüência da molécula reagente (em cm-): A saída gerada pelo programa após feitos os cálculos é: Se foi escolhido calcular WE+vr : O valor de WE+vr = Se foi escolhido calcular PE*vr : O valor de PE*vr = Se a opção escolhida foi : Temperatura : Valor de r para o complexo ativado: Valor de r para para a molécula reagente : Valor de s para o complexo ativado: Valor de s para a molécula reagente : Valor de L : Valor do diâmetro de colisão : Valor da masssa reduzida : Valor da eficiencia de destivação colisional : Valor da pressão (em torr) : Numero de colisão (Z em torr -s-): Valor das energias em Kcal=, KJ=, KeV=3 Valor de E+max:
12 Valor de AE : Valor de Ez : Valor de Qr : Valor de Q : Valor de Q+ : Valor de Q : Número de freqüências do complexo ativado : Valor da freqüência do complexo ativado (em cm-) : Número de freqüências da molecula reagente : Valor da freqüência da molécula reagente (em cm-): A saída gerada pelo programa é : O valor de WE+vr = (sem unidades) (quantas vezes for feito o cálculo para cada acréscimo de E) O valor de PE*vr = (em kj mol - ) (quantas vezes for feito o cálculo para cada acréscimo de E) valor de Kuni = (em s - ) O teste do programa foi feito utilizando os dados para a molécula do, diclorociclopropano. Para efetivar o cálculo da constante de velocidade unimolecualar em função da pressão, são necessários os parâmetros da molécula A e do estado de transição A +. Os parâmetros de A são as vibrações e rotações internas, os momentos de inércia e o diâmetro de colisão. Os mesmos parâmetros, exceto o diâmetro de colisão, são também necessários para a espécie A +. Os parâmetros básicos utilizados no cálculo foram retirados da bibliografia e são dados na tabela :
13 Tabela : parâmetros básicos : L = 4 Q + = Q =Q R = d = 0,65 nm = M A / = 55,5 kg mol - Freqüências de vibração da molécula reagente e do estado de transição dados na tabela E z = 6,8 kj mol - r = 0 Integração até E + max = 70 kj mol - em acréscimos de E + = 0,0 kj mol - Temperatura 697,6K E 0 = 3,86 kj mol - Q =5.84 Q + = 568,3 Tabela : freqüências vibracionais do, dicloro-propano e um transição de estado postulado : Vibrações da molécula reagente Vibrações correspondentesdo estado de transição Freqüência / cm - Freqüência / cm - e degenerescência 306, , , 490 9, 38 64, (4) 346 (4) 068 (4) 445 (5) 6,8 (3) 037, , 85, , 443, , 300, 7 s = s + = 0 3
14 7-Bibliografia -Holbrook, Kenneth A. ; Piling, Michael J. ; Robertson, Struan H. ; Unimolecular Reactions, Second Edition ; John Wiley & Sons, 996, pag 3 a 44. -Gottfried, Biron S. ; Programando em C ; Makron Books do Brasil Editora Ltda ; São Paulo ; 993 ; pag a
Esta etapa foi desenvolvida na teoria RRK
 Aplicações da Teoria de Reações Unimoleculares Teoria RRK (Rice, Ramsperger e Kassel) Considerando os graus de liberdade internos da molécula, que inicialmente eram negligenciados por Lindemann é necessário
Aplicações da Teoria de Reações Unimoleculares Teoria RRK (Rice, Ramsperger e Kassel) Considerando os graus de liberdade internos da molécula, que inicialmente eram negligenciados por Lindemann é necessário
Objetivo : obter por cálculo teórico a constante de velocidade k 1
 Aplicações da Teoria de Reações Unimoleculares Mecanismo unimolecular: - dado uma reação elementar de primeira ordem k 1 CD Produtos Objetivo : obter por cálculo teórico a constante de velocidade k 1 ocorrem,
Aplicações da Teoria de Reações Unimoleculares Mecanismo unimolecular: - dado uma reação elementar de primeira ordem k 1 CD Produtos Objetivo : obter por cálculo teórico a constante de velocidade k 1 ocorrem,
APLICAÇÃO DO FORMALISMO DA TEORIA RRKM
 APLICAÇÃO DO FORMALISMO DA TEORIA RRKM Efeito isotópico, hidrogênio-deutério, na cinética das reações unimoleculares: - substituição isotópica, ex.: composto deuterado isomerisa lentamente a pressões altas;
APLICAÇÃO DO FORMALISMO DA TEORIA RRKM Efeito isotópico, hidrogênio-deutério, na cinética das reações unimoleculares: - substituição isotópica, ex.: composto deuterado isomerisa lentamente a pressões altas;
APLICAÇÃO DO FORMALISMO DA TEORIA RRKM NA DISSOCIAÇÃO UNIMOLECULAR DO ÉTER DIMETÍLICO. Em particular, para o éter dimetílico (decomposição térmica):
 APLICAÇÃO DO FORMALISMO DA TEORIA RRKM NA DISSOCIAÇÃO UNIMOLECULAR DO ÉTER DIMETÍLICO - Os éteres (metílico e etílico) têm sido estudados como combustíveis alternativos ou aditivos de combustíveis. (Robbins,
APLICAÇÃO DO FORMALISMO DA TEORIA RRKM NA DISSOCIAÇÃO UNIMOLECULAR DO ÉTER DIMETÍLICO - Os éteres (metílico e etílico) têm sido estudados como combustíveis alternativos ou aditivos de combustíveis. (Robbins,
QFL1343 FÍSICO- QUÍMICA III 2019
 QFL1343 FÍSICO- QUÍMICA III 2019 Química I n t e g r a l 2 a lista de exercícios 1. O programa localizado em http://www.stolaf.edu/people/hansonr/imt/intro/boltz/ permite obter a distribuição de energia
QFL1343 FÍSICO- QUÍMICA III 2019 Química I n t e g r a l 2 a lista de exercícios 1. O programa localizado em http://www.stolaf.edu/people/hansonr/imt/intro/boltz/ permite obter a distribuição de energia
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia. Aula Interlúdio molecular
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula Interlúdio molecular Energia Interna somatório de energias (cinética + potencial) Energia cinética relacionada
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula Interlúdio molecular Energia Interna somatório de energias (cinética + potencial) Energia cinética relacionada
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade.
 MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
As bases da Dinâmica Molecular - 8
 As bases da Dinâmica Molecular - 8 Alexandre Diehl Departamento de Física - UFPel Hipóteses fundamentais da teoria cinética Qualquer porção pequena do gás contém um número N enorme de moléculas. Número
As bases da Dinâmica Molecular - 8 Alexandre Diehl Departamento de Física - UFPel Hipóteses fundamentais da teoria cinética Qualquer porção pequena do gás contém um número N enorme de moléculas. Número
Complexos Ativados - Intermediários e Energia de Ativação
 Complexos Ativados - Intermediários e Energia de Ativação Referências: LEVENSPIEL, Octave. Chemical Reaction Engineering. Third Edition, United States of America, John Wiley & Sons, c1999. (Ou outras edições)
Complexos Ativados - Intermediários e Energia de Ativação Referências: LEVENSPIEL, Octave. Chemical Reaction Engineering. Third Edition, United States of America, John Wiley & Sons, c1999. (Ou outras edições)
Estudo Teórico das Propriedades Cinéticas da Reação NF+F = N+F 2
 SIMPOETS, CEFET-GO, 121-130, 2008 Estudo Teórico das Propriedades Cinéticas da Reação NF+F = N+F 2 Danielle Maria Fernandes Do Prado 1 Graduanda de Licenciatura em Química daniellemarfe@hotmail.com Simone
SIMPOETS, CEFET-GO, 121-130, 2008 Estudo Teórico das Propriedades Cinéticas da Reação NF+F = N+F 2 Danielle Maria Fernandes Do Prado 1 Graduanda de Licenciatura em Química daniellemarfe@hotmail.com Simone
Fundamentos da Termodinâmica
 1 Fundamentos da Termodinâmica Objetivos: Definição de sistema e vizinhança Compreender o trabalho P-V Compreender processos reversíveis e irreversíveis Definir a primeira Lei da termodinâmica Cálculo
1 Fundamentos da Termodinâmica Objetivos: Definição de sistema e vizinhança Compreender o trabalho P-V Compreender processos reversíveis e irreversíveis Definir a primeira Lei da termodinâmica Cálculo
QFL1343 FÍSICO- QUÍMICA III 2018
 QFL1343 FÍSICO- QUÍMICA III 2018 Química Noturno 1 a lista de exercícios 1. Para o gás carbônico, a 25,0 o C, calcule a) a velocidade mais provável das moléculas; b) a velocidade média das moléculas; c)
QFL1343 FÍSICO- QUÍMICA III 2018 Química Noturno 1 a lista de exercícios 1. Para o gás carbônico, a 25,0 o C, calcule a) a velocidade mais provável das moléculas; b) a velocidade média das moléculas; c)
TEORIA DO ESTADO ESTACIONÁRIO E SIMULAÇÃO COMPUTACIONAL.
 EXERCÍCIOS SOBRE: TEORIA DA COLISÃO, TEORIA DO ESTADO ESTACIONÁRIO E SIMULAÇÃO COMPUTACIONAL. Glauber Silva Godoi META Desenvolver no aluno a capacidade de extrair os parâmetros cinéticos de uma reação
EXERCÍCIOS SOBRE: TEORIA DA COLISÃO, TEORIA DO ESTADO ESTACIONÁRIO E SIMULAÇÃO COMPUTACIONAL. Glauber Silva Godoi META Desenvolver no aluno a capacidade de extrair os parâmetros cinéticos de uma reação
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação
 Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
1 Termodinâmica: Modelos e Leis 1. 2 Princípio da Conservação da Energia: A 1.ª Lei da Termodinâmica 13
 Prefácio Lista de Símbolos xiii xvii 1 Termodinâmica: Modelos e Leis 1 1.1 Introdução 1 1.2 Modelo do Gás Perfeito 3 1.3 Mistura de Gases Perfeitos: Lei de Dalton 6 1.4 Leis da Termodinâmica 7 1.5 Expansão
Prefácio Lista de Símbolos xiii xvii 1 Termodinâmica: Modelos e Leis 1 1.1 Introdução 1 1.2 Modelo do Gás Perfeito 3 1.3 Mistura de Gases Perfeitos: Lei de Dalton 6 1.4 Leis da Termodinâmica 7 1.5 Expansão
Velocidade de reação. Química Geral. Prof. Edson Nossol
 Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
Cinética Parte A. Introdução à Química II. Prof. Edson Nossol
 Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
Noções de Cinética Química
 QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
FIS-14 Prova 02 Novembro/2013
 FIS-14 Prova 02 Novembro/2013 Nome: Nota: Duração máxima da prova: 240 min. Responda às questões de forma clara, completa e concisa dentro do espaço previsto. Uma parte da pontuação de cada questão será
FIS-14 Prova 02 Novembro/2013 Nome: Nota: Duração máxima da prova: 240 min. Responda às questões de forma clara, completa e concisa dentro do espaço previsto. Uma parte da pontuação de cada questão será
é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições
 Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a. o resultado do movimento dos átomos e moléculas.
 TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
Universidade Estadual do Sudoeste da Bahia
 Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
24/Abr/2014 Aula /Abr/2014 Aula 15
 /Abr/014 Aula 15 Ondas de matéria; comprimento de onda de de Broglie. Quantização do momento angular no modelo de Bohr. Difracção e interferência. Função de onda; representação matemática do pacote de
/Abr/014 Aula 15 Ondas de matéria; comprimento de onda de de Broglie. Quantização do momento angular no modelo de Bohr. Difracção e interferência. Função de onda; representação matemática do pacote de
Físico-química Farmácia 2014/02
 Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Capítulo 11 - Teoria Cinética dos Gases. O número de Avogrado é número de moléculas contido em 1 mol de qualquer substãncia
 Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
Instituto de Física USP. Física V - Aula 18. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 18 Professora: Mazé Bechara Aula 28 Discussão da 1ª prova e Apresentação do Tópico III 1. Soluções das questões da prova com comentários. Critérios de correção.
Instituto de Física USP Física V - Aula 18 Professora: Mazé Bechara Aula 28 Discussão da 1ª prova e Apresentação do Tópico III 1. Soluções das questões da prova com comentários. Critérios de correção.
Ciência e Tecnologia de Filmes Finos. Aula Cinética dos Gases (Cap.2/Smith) (detalhes)
 Ciência e Tecnologia de Filmes Finos Aula 02-2009 Cinética dos Gases (Cap.2/Smith) (detalhes) Cinética de Gases - como os gases participam dos processos de crescimento de filmes? - quais as propriedades
Ciência e Tecnologia de Filmes Finos Aula 02-2009 Cinética dos Gases (Cap.2/Smith) (detalhes) Cinética de Gases - como os gases participam dos processos de crescimento de filmes? - quais as propriedades
As bases da Dinâmica Molecular - 9
 As bases da Dinâmica Molecular - 9 Alexandre Diehl Departamento de Física - UFPel Termostato de Berendsen [J. Chem. Phys. 81, 3684 (1984)] Não simula o sistema em contato com um banho térmico (temperatura
As bases da Dinâmica Molecular - 9 Alexandre Diehl Departamento de Física - UFPel Termostato de Berendsen [J. Chem. Phys. 81, 3684 (1984)] Não simula o sistema em contato com um banho térmico (temperatura
GASES. https://www.youtube.com/watch?v=wtmmvs3uiv0. David P. White. QUÍMICA: A Ciência Central 9ª Edição Capítulo by Pearson Education
 GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
Instituto de Física USP Física V - Aula 04
 Instituto de Física USP Física V - Aula 04 Professora: Mazé Bechara Aula 04 Mecânica estatística clássica. Estimativa dos do calor específico molar a volume constante em gases mono e poliatômicos e nos
Instituto de Física USP Física V - Aula 04 Professora: Mazé Bechara Aula 04 Mecânica estatística clássica. Estimativa dos do calor específico molar a volume constante em gases mono e poliatômicos e nos
QFL1343 FÍSICO- QUÍMICA III 2019
 QFL1343 FÍSICO- QUÍMICA III 2019 Química I n t e g r a l 1 a lista de exercícios 1. Para a amônia, a 25,0 o C, calcule a) a velocidade mais provável das moléculas; b) a velocidade média das moléculas;
QFL1343 FÍSICO- QUÍMICA III 2019 Química I n t e g r a l 1 a lista de exercícios 1. Para a amônia, a 25,0 o C, calcule a) a velocidade mais provável das moléculas; b) a velocidade média das moléculas;
rádio molécula transições rotacionais E = B J (J+1) Δ J = ± 1 B : relacionado ao momento de inércia da 4-1
 Bloco 4 Processos radiativos no MI Linhas espectrais no MI: teoria Referências Maciel Cap. 3 formulário e teoria Spitzer, Physical Processes in the ISM Cap. 2 e 3 explicação e teoria de forma mais aprofundada
Bloco 4 Processos radiativos no MI Linhas espectrais no MI: teoria Referências Maciel Cap. 3 formulário e teoria Spitzer, Physical Processes in the ISM Cap. 2 e 3 explicação e teoria de forma mais aprofundada
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
Energia Interna 𝐸(= 𝐸𝑡𝑒𝑟𝑚) de gases ideais
 P3 Energia Interna E(= E term ) de gases ideais Em geral, E = K micro e U micro U(r) r Em um gás IDEAL a energia é puramente INTRA-molecular Em um gás NÃO IDEAL há ainda a energia potencial de INTERAÇÃO
P3 Energia Interna E(= E term ) de gases ideais Em geral, E = K micro e U micro U(r) r Em um gás IDEAL a energia é puramente INTRA-molecular Em um gás NÃO IDEAL há ainda a energia potencial de INTERAÇÃO
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS
 BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
ASPECTOS GERAIS. Prof. Harley P. Martins filho
 /6/08 ASPECTOS GERAIS Prof. Harley P. Martins filho Aspectos Gerais Espectroscopia por emissão: Abaixamento de energia de um sistema de um nível permitido para outro, com emissão da energia perdida na
/6/08 ASPECTOS GERAIS Prof. Harley P. Martins filho Aspectos Gerais Espectroscopia por emissão: Abaixamento de energia de um sistema de um nível permitido para outro, com emissão da energia perdida na
Avaliação para Seleção de Mestrado em Agroquímica I. Número ou código do(a) candidato(a): INSTRUÇÕES
 Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2012-I Número ou código do(a) candidato(a): INSTRUÇÕES
Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2012-I Número ou código do(a) candidato(a): INSTRUÇÕES
Universidade Federal da Paraíba. Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química
 Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 2019.2) DATA:
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Programa de Pós-graduação em Química PROVA DE SELEÇÃO PARA INGRESSO NO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA (PERÍODO 2019.2) DATA:
INTEGRAÇÃO NUMÉRICA DA EQUAÇÃO DE SCHRÖDINGER DE PENDENTE DO TEMPO
 INTEGRAÇÃO NUMÉRICA DA EQUAÇÃO DE SCHRÖDINGER DE PENDENTE DO TEMPO RESUMO Christopher Rodrigues Vieira 1 ;Nilo Mauricio Sotomayo Choque 2 ; 1 Aluno do Curso de Licenciatura em Física; Campus de Araguaína;
INTEGRAÇÃO NUMÉRICA DA EQUAÇÃO DE SCHRÖDINGER DE PENDENTE DO TEMPO RESUMO Christopher Rodrigues Vieira 1 ;Nilo Mauricio Sotomayo Choque 2 ; 1 Aluno do Curso de Licenciatura em Física; Campus de Araguaína;
Prefácio. Lista de Símbolos. Modelo do Gás Perfeito 2 Mistura de Gases Perfeitos. Lei de Dalton 4 Problemas 6
 Índice Geral Prefácio xv Lista de Símbolos xvii 1 Modelo do Gás Perfeito 1 Modelo do Gás Perfeito 2 Mistura de Gases Perfeitos. Lei de Dalton 4 Problemas 6 2 Princípio da Conservação da Energia. A 1.ª
Índice Geral Prefácio xv Lista de Símbolos xvii 1 Modelo do Gás Perfeito 1 Modelo do Gás Perfeito 2 Mistura de Gases Perfeitos. Lei de Dalton 4 Problemas 6 2 Princípio da Conservação da Energia. A 1.ª
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS
 CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS A VELOCIDADE DE UMA REAÇÃO: É UMA MEDIDA DE QUÃO RÁPIDO UM REAGENTE É CONSUMIDO OU UM PRODUTO É FORMADO 1) Na reação de A +
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS A VELOCIDADE DE UMA REAÇÃO: É UMA MEDIDA DE QUÃO RÁPIDO UM REAGENTE É CONSUMIDO OU UM PRODUTO É FORMADO 1) Na reação de A +
Formalismo microcanônico ( ensemble microcanônico) Formalismo canônico ( ensemble canônico)
 Formalismo microcanônico ( ensemble microcanônico) sist(j) estado j f j = Ω j Ω Formalismo canônico ( ensemble canônico) reservatório de temperatura tot res sistema f j = Ω res+sist(j) Ω tot sist(j) Física
Formalismo microcanônico ( ensemble microcanônico) sist(j) estado j f j = Ω j Ω Formalismo canônico ( ensemble canônico) reservatório de temperatura tot res sistema f j = Ω res+sist(j) Ω tot sist(j) Física
BCL 0307 Transformações Químicas
 BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
Instituto de Física USP. Física Moderna I. Aula 4. Professora: Mazé Bechara
 Instituto de Física USP Física Moderna I Aula 4 Professora: Mazé Bechara Aula 04 Modelos de estrutura da matéria e a mecânica estatística clássica 1. Uma teoria para a dinâmica de um sistema de muitas
Instituto de Física USP Física Moderna I Aula 4 Professora: Mazé Bechara Aula 04 Modelos de estrutura da matéria e a mecânica estatística clássica 1. Uma teoria para a dinâmica de um sistema de muitas
As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana.
 Estudo dos gases Gás Ideal As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana. As moléculas não exercem força uma sobre as outras, exceto quando
Estudo dos gases Gás Ideal As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana. As moléculas não exercem força uma sobre as outras, exceto quando
Terceira série de exercícios Mecânica Estatística - IFUSP - 13/9/ ensemble canônico -
 Terceira série de exercícios Mecânica Estatística - IFUSP - 3/9/00 - ensemble canônico - We consider especially ensembles of systems in which the index (or logarithm) of probability of phase is a linear
Terceira série de exercícios Mecânica Estatística - IFUSP - 3/9/00 - ensemble canônico - We consider especially ensembles of systems in which the index (or logarithm) of probability of phase is a linear
Cinética Química. Cinética Química...? É o estudo da velocidade das reações químicas e dos fatores que as influenciam.
 Cinética Química...? Universidade Federal de Campina Grande Centro de Ciência e Tecnologia groalimentar Profª Roberlucia Candeia Disciplina: Química geral É o estudo da velocidade das reações químicas
Cinética Química...? Universidade Federal de Campina Grande Centro de Ciência e Tecnologia groalimentar Profª Roberlucia Candeia Disciplina: Química geral É o estudo da velocidade das reações químicas
3.2.2 Métodos de relaxação Métodos de competição Métodos de elevada resolução temporal ORDENS E CONSTANTES DE
 ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
Mecânica Estatística - Exercícios do EUF Professor: Gabriel T. Landi
 Mecânica Estatística - Exercícios do EUF Professor: Gabriel T. Landi (2016-2) Sólido cristalino Num modelo para um sólido cristalino podemos supor que os N átomos sejam equivalentes a 3N osciladores harmônicos
Mecânica Estatística - Exercícios do EUF Professor: Gabriel T. Landi (2016-2) Sólido cristalino Num modelo para um sólido cristalino podemos supor que os N átomos sejam equivalentes a 3N osciladores harmônicos
Físico-Química de Alimentos
 Físico-Química de Alimentos Docentes: Prof. Dr. Odinei Hess Gonçalves e Prof. Dr. Evandro Bona Ementa: Definição termodinâmica de atividade de água. Atividade de água e estabilidade de alimentos. Isotermas
Físico-Química de Alimentos Docentes: Prof. Dr. Odinei Hess Gonçalves e Prof. Dr. Evandro Bona Ementa: Definição termodinâmica de atividade de água. Atividade de água e estabilidade de alimentos. Isotermas
Faculdade de Educação, Ciências e Letras dos Inhamuns FECLIN Coordenação de Química Disciplina Química Geral II Professor: NOTA DE AULA
 Faculdade de Educação, Ciências e Letras dos Inhamuns FECLIN Coordenação de Química Disciplina Química Geral II Professor: NOTA DE AULA CINETICA QUÍMICA Velocidade média de uma reação Ex.1. Um balão contendo
Faculdade de Educação, Ciências e Letras dos Inhamuns FECLIN Coordenação de Química Disciplina Química Geral II Professor: NOTA DE AULA CINETICA QUÍMICA Velocidade média de uma reação Ex.1. Um balão contendo
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
Estudo Físico-Químico dos Gases
 19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
Instituto de Física USP. Física Moderna I. Aula 03. Professora: Mazé Bechara
 Instituto de Física USP Física Moderna I Aula 03 Professora: Mazé Bechara Aula 03 AVISOS. Na página da disciplina há uma programação aula a aula até a ª prova em de abril.. Alguns dos alunos matriculados
Instituto de Física USP Física Moderna I Aula 03 Professora: Mazé Bechara Aula 03 AVISOS. Na página da disciplina há uma programação aula a aula até a ª prova em de abril.. Alguns dos alunos matriculados
Medição. Os conceitos fundamentais da física são as grandezas que usamos para expressar as suas leis. Ex.: massa, comprimento, força, velocidade...
 Universidade Federal Rural do Semi Árido UFERSA Pro Reitoria de Graduação PROGRAD Disciplina: Mecânica Clássica Professora: Subênia Medeiros Medição Os conceitos fundamentais da física são as grandezas
Universidade Federal Rural do Semi Árido UFERSA Pro Reitoria de Graduação PROGRAD Disciplina: Mecânica Clássica Professora: Subênia Medeiros Medição Os conceitos fundamentais da física são as grandezas
Cinética. Módulo I - Físico Química Avançada. Profa. Kisla P. F. Siqueira
 Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
Aula 02 : EM-524. Capítulo 2 : Definições e Conceitos Termodinâmicos
 Aula 02 : EM-524 Capítulo 2 : Definições e Conceitos Termodinâmicos 1. Termodinâmica Clássica; 2. Sistema Termodinâmico; 3. Propriedades Termodinâmicas; 4. As propriedades termodinâmicas pressão, volume
Aula 02 : EM-524 Capítulo 2 : Definições e Conceitos Termodinâmicos 1. Termodinâmica Clássica; 2. Sistema Termodinâmico; 3. Propriedades Termodinâmicas; 4. As propriedades termodinâmicas pressão, volume
Partícula na Caixa. Química Quântica Prof a. Dr a. Carla Dalmolin
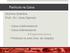 Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
Agrupamento de Escolas de Alcácer do Sal Escola Secundária de Alcácer do Sal
 Agrupamento de Escolas de Alcácer do Sal Escola Secundária de Alcácer do Sal Ano Letivo 2017/2018 Física e Química A 10º ano Teste de Avaliação 3 A 15/02/2018 Duração: 90 minutos Página 1 de 6 Teste 3A
Agrupamento de Escolas de Alcácer do Sal Escola Secundária de Alcácer do Sal Ano Letivo 2017/2018 Física e Química A 10º ano Teste de Avaliação 3 A 15/02/2018 Duração: 90 minutos Página 1 de 6 Teste 3A
Disciplina: FGE5748 Simulação Computacional de Líquidos Moleculares 1
 Disciplina: FGE5748 Simulação Computacional de Líquidos Moleculares 1 A matéria é composta por átomos e moléculas Geralmente, fazemos simplificações e desenvolvemos modelos O estudo teórico não permite
Disciplina: FGE5748 Simulação Computacional de Líquidos Moleculares 1 A matéria é composta por átomos e moléculas Geralmente, fazemos simplificações e desenvolvemos modelos O estudo teórico não permite
ESTUDO DA REAÇÃO PH 2 + NH 2
 ESTUDO DA REAÇÃO PH 2 + NH 2 Aluna: Érica Silva da Costa Orientador: André S. Pimentel Apresentação Este projeto foi planejado para em sua primeira etapa se realizar a pesquisa bibliográfica, o treinamento
ESTUDO DA REAÇÃO PH 2 + NH 2 Aluna: Érica Silva da Costa Orientador: André S. Pimentel Apresentação Este projeto foi planejado para em sua primeira etapa se realizar a pesquisa bibliográfica, o treinamento
Computadores podem ser úteis em problemas que envolvem: Grande número de dados. Grande número de cálculos. Complexidade. Precisão.
 O uso do computador Computadores podem ser úteis em problemas que envolvem: Grande número de dados. Grande número de cálculos. Complexidade. Precisão. Exemplos: Modelos meteorológicos. Cálculo estrutural.
O uso do computador Computadores podem ser úteis em problemas que envolvem: Grande número de dados. Grande número de cálculos. Complexidade. Precisão. Exemplos: Modelos meteorológicos. Cálculo estrutural.
Química Geral e Inorgânica. QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin. Cinética Química
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Cinética Química Cinética Química É a área da química que está preocupada com a velocidade das reações químicas.
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Cinética Química Cinética Química É a área da química que está preocupada com a velocidade das reações químicas.
O que é um transição de fase?
 Transição de Fase O que é um transição de fase? Fases são estados macroscópicos específicos da Matéria em equilíbrio termodinâmico. Exemplo: estado sólido, líquido ou gasoso. Transição de fase é uma transformação
Transição de Fase O que é um transição de fase? Fases são estados macroscópicos específicos da Matéria em equilíbrio termodinâmico. Exemplo: estado sólido, líquido ou gasoso. Transição de fase é uma transformação
Conceitos Fundamentais
 Conceitos Fundamentais Introdução. Equilíbrio térmico. Temperatura. Medidas de temperatura. Introdução Escopo da Termodinâmica: A termodinâmica diz respeito ao estudo das propriedades macroscópicas dos
Conceitos Fundamentais Introdução. Equilíbrio térmico. Temperatura. Medidas de temperatura. Introdução Escopo da Termodinâmica: A termodinâmica diz respeito ao estudo das propriedades macroscópicas dos
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127. Cinética Química
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
Física. B) Determine a distância x entre o ponto em que o bloco foi posicionado e a extremidade em que a reação é maior.
 Física 01. Uma haste de comprimento L e massa m uniformemente distribuída repousa sobre dois apoios localizados em suas extremidades. Um bloco de massa m uniformemente distribuída encontra-se sobre a barra
Física 01. Uma haste de comprimento L e massa m uniformemente distribuída repousa sobre dois apoios localizados em suas extremidades. Um bloco de massa m uniformemente distribuída encontra-se sobre a barra
2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados;
 CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
Universidade Federal do Pampa UNIPAMPA. Teoria Cinética do Gases
 Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Desintegração Nuclear. Paulo R. Costa
 Desintegração Nuclear Paulo R. Costa Sumário Introdução Massas atômicas e nucleares Razões para a desintegração nuclear Decaimento nuclear Introdução Unidades e SI Introdução Comprimento metro Tempo segundo
Desintegração Nuclear Paulo R. Costa Sumário Introdução Massas atômicas e nucleares Razões para a desintegração nuclear Decaimento nuclear Introdução Unidades e SI Introdução Comprimento metro Tempo segundo
Cinética Química. Mestrado integrado em Engenharia Biológica. Disciplina Química II, 2º semestre 2009/10. Professsora Ana Margarida Martins
 Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
Física do Calor Licenciatura: 4ª Aula (19/08/2015)
 Física do Calor Licenciatura: 4ª ula (19/08/015) Prof. lvaro annucci imos, na última aula: Definição de massa molecular, que corresponde à massa de 1 mol da substância: M M m N Nos processos que envolvem
Física do Calor Licenciatura: 4ª ula (19/08/015) Prof. lvaro annucci imos, na última aula: Definição de massa molecular, que corresponde à massa de 1 mol da substância: M M m N Nos processos que envolvem
Laboratório de Física I TEORIA DE ERROS Prof. Dr. Anderson André Felix Técnico do Lab.: Vinicius Valente
 Laboratório de Física I TEORIA DE ERROS Prof. Dr. Anderson André Felix Técnico do Lab.: Vinicius Valente aa.felix@unesp.br vinicius.valente@unesp.br www.iq.unesp.br/laboratoriodefisica Número 1 Grandeza
Laboratório de Física I TEORIA DE ERROS Prof. Dr. Anderson André Felix Técnico do Lab.: Vinicius Valente aa.felix@unesp.br vinicius.valente@unesp.br www.iq.unesp.br/laboratoriodefisica Número 1 Grandeza
PROGRAMAÇÃO de COMPUTADORES: LINGUAGEM FORTRAN 90/95
 PROGRAMAÇÃO de COMPUTADORES: LINGUAGEM FORTRAN 90/95 Exercícios de revisão Lista 01: a) Monte um mapa conceitual indicando as relações entre os seguintes conceitos, no contexto do assunto visto em aula:
PROGRAMAÇÃO de COMPUTADORES: LINGUAGEM FORTRAN 90/95 Exercícios de revisão Lista 01: a) Monte um mapa conceitual indicando as relações entre os seguintes conceitos, no contexto do assunto visto em aula:
Problemas de Química-Física 20015/2016
 Problemas de Química-Física 0015/016 Capítulo 5 - Espectroscopia Rotacional, Vibracional, Rotovibracional e Electrónica 1 O espectro rotacional da molécula 1 C 3 S tem as seguintes riscas (em MHz): Risca
Problemas de Química-Física 0015/016 Capítulo 5 - Espectroscopia Rotacional, Vibracional, Rotovibracional e Electrónica 1 O espectro rotacional da molécula 1 C 3 S tem as seguintes riscas (em MHz): Risca
Notas de aula - Profa. Zélia Aulas 07,08,09 e 10. Capítulo 3 Relações formais e sistemas amostrais (exemplares)
 Notas de aula - Profa. Zélia Aulas 07,08,09 e 10 Livro texto: Thermodynamics and an Introduction to Thermostatistics (2nd edition) H. B. Callen. Capítulo 3 Relações formais e sistemas amostrais (exemplares)
Notas de aula - Profa. Zélia Aulas 07,08,09 e 10 Livro texto: Thermodynamics and an Introduction to Thermostatistics (2nd edition) H. B. Callen. Capítulo 3 Relações formais e sistemas amostrais (exemplares)
Capítulo 21 Temperatura
 Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
Aula 8 DINÂMICA DAS REAÇÕES MOLECULARES: TEORIA DA COLISÃO. META Apresentar ao aluno os conceitos da Teoria da Colisão.
 DINÂMICA DAS REAÇÕES MOLECULARES: TEORIA DA COLISÃO Glauber Silva Godoi META Apresentar ao aluno os conceitos da Teoria da Colisão. OBJETIVOS Ao fi nal desta aula, o aluno deverá: Conhecer os fatores que
DINÂMICA DAS REAÇÕES MOLECULARES: TEORIA DA COLISÃO Glauber Silva Godoi META Apresentar ao aluno os conceitos da Teoria da Colisão. OBJETIVOS Ao fi nal desta aula, o aluno deverá: Conhecer os fatores que
Apresentar os conceitos fundamentais da termodinâmica estatística e como aplicá-los as propriedades termodinâmicas vista até então.
 Introdução À Termodinâmica Estatística Aula 15 Meta Apresentar os conceitos fundamentais da termodinâmica estatística e como aplicá-los as propriedades termodinâmicas vista até então. Objetivos Ao final
Introdução À Termodinâmica Estatística Aula 15 Meta Apresentar os conceitos fundamentais da termodinâmica estatística e como aplicá-los as propriedades termodinâmicas vista até então. Objetivos Ao final
6/Mar/2013 Aula 7 Entropia Variação da entropia em processos reversíveis Entropia e os gases ideais
 6/Mar/01 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
6/Mar/01 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 6 MECÂNICA QUÂNTICA DE SCHRÖDINGER Edição de janeiro de 2010 CAPÍTULO 6 MECÂNICA QUÂNTICA DE SCHRÖDINGER ÍNDICE 6.1- Introdução 6.2- Equação
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 6 MECÂNICA QUÂNTICA DE SCHRÖDINGER Edição de janeiro de 2010 CAPÍTULO 6 MECÂNICA QUÂNTICA DE SCHRÖDINGER ÍNDICE 6.1- Introdução 6.2- Equação
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
UFABC - BC Prof. Germán Lugones. AULA 9 Teoria Cinética dos Gases III
 UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES
 CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES REAÇÃO GLOBAL: MOSTRA APENAS A MODIFICAÇÃO GLOBAL VELOCIDADE
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES REAÇÃO GLOBAL: MOSTRA APENAS A MODIFICAÇÃO GLOBAL VELOCIDADE
DISCIPLINAS ELETIVAS GRUPO 1 Mínimo de 840 horas
 DISCIPLINAS TIVAS GRUPO 1 Mínimo de 0 horas (disciplinas obrigatórias de algum dos cursos de segundo ciclo lotadas no Instituto de Ciências Exatas ou na Faculdade de Engenharia, exceto estágios e trabalhos
DISCIPLINAS TIVAS GRUPO 1 Mínimo de 0 horas (disciplinas obrigatórias de algum dos cursos de segundo ciclo lotadas no Instituto de Ciências Exatas ou na Faculdade de Engenharia, exceto estágios e trabalhos
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica
 Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
A teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE QUÍMICA PROGRAMA DE PÓS GRADUAÇÃO EM QUÍMICA. Exame de Seleção para o Mestrado em Química-2011.
 UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE QUÍMICA PROGRAMA DE PÓS GRADUAÇÃO EM QUÍMICA Exame de Seleção para o Mestrado em Química-2011.2 PROVA DE QUÍMICA CÓDIGO do CANDIDATO: INSTRUÇÕES: Confira o caderno
UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE QUÍMICA PROGRAMA DE PÓS GRADUAÇÃO EM QUÍMICA Exame de Seleção para o Mestrado em Química-2011.2 PROVA DE QUÍMICA CÓDIGO do CANDIDATO: INSTRUÇÕES: Confira o caderno
Físico-Química I. Profa. Dra. Carla Dalmolin. Gases. Gás perfeito (equações de estado e lei dos gases) Gases reais
 Físico-Química I Profa. Dra. Carla Dalmolin Gases Gás perfeito (equações de estado e lei dos gases) Gases reais Gás Estado mais simples da matéria Uma forma da matéria que ocupa o volume total de qualquer
Físico-Química I Profa. Dra. Carla Dalmolin Gases Gás perfeito (equações de estado e lei dos gases) Gases reais Gás Estado mais simples da matéria Uma forma da matéria que ocupa o volume total de qualquer
Física II FEP 112 ( ) 1º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Calor Específico Molar, Transformações Adiabáticas e Expansão Livre
 Calor Específico Molar, Transformações Adiabáticas e Expansão Livre Revisando Deduzimos que a temperatura determina a energia cinética média (via a velocidade média). O modelo de gás ideal não considera
Calor Específico Molar, Transformações Adiabáticas e Expansão Livre Revisando Deduzimos que a temperatura determina a energia cinética média (via a velocidade média). O modelo de gás ideal não considera
CQ110 : Princípios de FQ. Imagens de Rorschach
 Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Instituto de Física USP. Física V - Aula 03. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 03 Professora: Mazé Bechara Aula 03 AVISOS 1. Página da disciplina: se organize e use os mecanismos de apoio para o seu bom aproveitamento e desenvolvimento nos
Instituto de Física USP Física V - Aula 03 Professora: Mazé Bechara Aula 03 AVISOS 1. Página da disciplina: se organize e use os mecanismos de apoio para o seu bom aproveitamento e desenvolvimento nos
Q RT. Lista de Exercícios 9. Comportamento Mecânico dos Materiais - Parte II
 1 Lista de Exercícios 9 Comportamento Mecânico dos Materiais - Parte II 2014 1. Suponha que você é o responsável pelo projeto de uma turbina a gás funcionando a 800 o C. As palhetas do rotor serão construídas
1 Lista de Exercícios 9 Comportamento Mecânico dos Materiais - Parte II 2014 1. Suponha que você é o responsável pelo projeto de uma turbina a gás funcionando a 800 o C. As palhetas do rotor serão construídas
Combustíveis Energia e Ambiente. Combustíveis gasosos, líquidos e sólidos: compreender as diferenças
 Combustíveis gasosos, líquidos e sólidos: compreender as diferenças 1 Estados físicos de hidrocarbonetos em função do número de carbonos da cadeia Os gases combustíveis podem ser agrupados em famílias,
Combustíveis gasosos, líquidos e sólidos: compreender as diferenças 1 Estados físicos de hidrocarbonetos em função do número de carbonos da cadeia Os gases combustíveis podem ser agrupados em famílias,
