Proteínas funcionais: hemoglobina e mioglobina
|
|
|
- Maria do Mar Bicalho Palmeira
- 6 Há anos
- Visualizações:
Transcrição
1 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008 9ª aula teórica Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H. Freeman & Company, 2006, Cap 7. - Lehninger Principles of Biochemistry (D.L. Nelson & M. M. Cox) 4ª Ed., W. H.Freeman & Company, 2004, Cap Out-07 Objectivos 1. Explicar as diferenças estruturais entre hemoglobina e mioglobina. 2. Descrever como se estabelece e quais as características da ligação do oxigénio à mioglobina e à hemoglobina. 3. Avaliar a importância do Fe do grupo heme na ligação ao oxigénio. 4. Interpretar as curvas de ligação da hemoglobina e da mioglobina ao oxigénio. 5. Analisar a regulação da ligação do oxigénio ao grupo heme por H + e CO 2 (efeito de Bohr), e pelo 2,3- bifosfoglicerato. 1
2 Porque necessitamos de oxigénio? Todos os tecidos do nosso organismo necessitam de um aporte de oxigénio adequado para a respiração celular. CÉLULA O 2 N MITOCÔNDRIA H 2 O Mioglobina (Mb) e Hemoglobina (Hb) ligam O 2, facilitando a sua cedência aos tecidos. Mioglobina - armazena O 2 no músculo Hemoglobina transporta O 2 no sangue 2
3 Aula nº 9 1. Quais as diferenças estruturais entre Mb e Hb? 2. Como se estabelece a ligação do O 2 à Mb e Hb? 3. Quais as características da ligação do O 2 àmb e Hb? 1. Quais as diferenças estruturais entre Mb e Hb? 2. Como se estabelece a ligação do O 2 à Mb e Hb? 3. Quais as características da ligação do O 2 àmb e Hb? 3
4 Estruturas da Mioglobina (Mb) e Hemoglobina (Hb) Mathews, 2004 Mioglobina - armazena O 2 no músculo Hemoglobina transporta O 2 no sangue (GV) Mioglobina (Mb) (Jonh Kendrew, 1950) * Uma única cadeia (estrutura terciária) * 75% da cadeia - conformação em α-hélice 8 segmentos helicoidais - A... H *4 α-hélices terminam em prolina * Interior - resíduos apolares: Leu, Val, Phe, Met - excepção: His F8 e E7 (AA polares) 4
5 Hemoglobina (Hb) Hb A Hemoglobina (Hb) (Max Perutz, 1950) * Tetrâmero: 2 pares de cadeias polipeptídicas, α, β (~Mb), γ e/ou δ, ligadas por ligações não covalentes. * Hb adulto A - α 2 β 2 (~ 97%) A 2 - α 2 δ 2 (2-3%) F - α 2 γ 2 (< 1%) * Cada cadeia está ligada covalentemente a um grupo heme (~ Mb). * Cada cadeia α contacta com as β, mas não entre si. * Cadeia α tem 141 resíduos AA; β, γ e δ têm 146 AA. 5
6 Hemoglobina Síntese das cadeias da hemoglobina humana ao longo do desenvolvimento: Hb Gower1 (ζ 2 ε 2 ) Hb Gower2 (α 2 ε 2 ) Hb Portland (ζ 2 γ 2 ) Hb fetal (α 2 γ 2 ) Hb A (α 2 β 2 ) Hb A 2 (α 2 δ 2 ) Hemoglobina - Existem resíduos de AA invariáveis com importantes funções (Ex: His, Tyr) - AA no interior variam, mas sem alteração da polaridade - manutenção do interior hidrofóbico * Estabilização da estrututura tridimensional - AA na superfície variam muito 6
7 1. Quais as diferenças estruturais entre Mb e Hb? 2. Como se estabelece a ligação do O 2 àmb e Hb? 3. Quais as características da ligação do O 2 àmb e Hb? A Hemoglobina (Hb) e a Mioglobina (Mb) ligam O 2 (2 hemoproteínas) Importância da presença do grupo HEME: - Parte orgânica - Protoporfirina IX + - Um átomo Ferro (Fe 2+ ) Liga O 2 7
8 Protoporfirina IX - 4 anéis pirrólicos ligados por pontes meteno - A que se ligam: - 4 grupos metilo - 2 grupos vinilo - 2 cadeias laterais de propionato Estrutura das Porfirinas: Geometria de coordenação do ferro na OxiMb e OxiHb His distal (E7) - Exterior - AA polares e não polares; Interior - AA apolares, excepção His. - O heme está numa fenda da molécula. - O ferro está directamente ligado à histidina proximal (F8), fora do plano hémico (5ª posição coordenação) -O O 2 liga-se na 6ª posição coordenação do Fe 2+, de forma angular. His proximal (F8) 8
9 Ligação do CO e O 2 ao ferro (Fe 2+ ) do grupo hémico A ligação linear do CO ao grupo heme é evitada pela histidina distal Permite uma ligação angular Enfraquece a ligação do CO e do O 2 à Mb e Hb Afinidade (relativamente ao O 2 ) 20,000x 200x Mb e Hb: formas Oxi-, Desoxi- e Ferri- A conformação das 3 formas da Mb são muito semelhantes, excepto na 6ª posição de coordenação. A função do grupo prostético é modulada pelo seu ambiente polipeptídico: A Histidina distal (E7) impede a oxidação do ferro (heme) Mathews, 2004 Formas da Mb 6 ª pos.coord. Estado de oxidação do ferro Desoximioglobina Vazia +2 Oximioglobina O 2 +2 Ferrimioglobina H 2 O +3 9
10 Ligação do oxigénio ao heme Durante a oxigenação, o ferro move-se para o plano do heme O movimento do ferro é transmitido a outras subunidades da Hb pela histidina proximal (F8). Fe Fe Fe Mioglobina (alteração molecular após ligação do O 2 ) 10
11 Hemoglobina Alteração da estrutura quaternária da hemoglobina durante a oxigenação (transição T R) Desoxihemoglobina (T) + O 2 Oxihemoglobina (R) Desoxihemoglobina (T) Oxihemoglobina (R) Transição T R: Estabelecem-se novas lig. hidrogénio entre β 2 e α 1 e entre β 1 e α 2 11
12 Ligações iónicas (pontes salinas) estabilizam a forma T da desoxihemoglobina Forma T (desoxi - pontes salinas) Forma R (oxi - quebra pontes salinas) Figura: Lig. iónica entre His e Asp da subunidade β; Lig. iónica entre Lys (subunidade α) e -COO - da His. Ligação do oxigénio à hemoglobina Durante a oxigenação, um par de subunidades α-β roda cerca de 15 graus Stryer, 5ª Ed Desoxihemoglobina (T) + O 2 Oxihemoglobina (R) 12
13 Hemoglobina uma proteína que respira From Wikipedia, the free encyclopedia 1. Quais as diferenças estruturais entre Mb e Hb? 2. Como se estabelece a ligação do O 2 à Mb e Hb? 3. Quais as características da ligação do O 2 à Mb e Hb? 13
14 A Mb tem uma grande afinidade pelo O 2 (hipérbole). A ligação do O 2 à Hb é cooperativa (sigmóide). Mioglobina e Hemoglobina ligação do O 2 : - A ligação da Hb ao O 2 é cooperativa Curva de dissociação do O 2 da Hb é sigmoide A Hb é um transportador eficiente de O 2!! - A ligação da Mb ao O 2 não é cooperativa hipérbole sigmoide Curva de dissociação do O 2 da Mb é hiperbólica 14
15 Gráficos de Hill da ligação de Oxigénio à Mioglobina e Hemoglobina Ligação Cooperativa n>1 θ = (po 2 ) n (p50) n + (po 2 ) n Equação de Hill θ = fracção de saturação ou ocupação locais de ligação ( 0-1) Mb: n= 1 Hb: n= 2,8 n= nº Hill Se n=1 (hipérbole) não existe cooperatividade Se n>1 cooperatividade positiva Se n<1 cooperatividade negativa n=1 Ligação das moléculas de O 2 à Mb é independente n>1 Ligação cooperativa de O 2 à Hb e depende das alterações da po 2 cooperatividade positiva Capacidade de ligação/libertação de O 2 Mioglobina vs Hemoglobina θ = (po 2 ) n (p50) n + (po 2 ) n Qual destas proteínas possui maior capacidade de ligar/libertar O 2? Exercício: po 2 cap. Alv.= 100 torr θ cap. alv.= 0.98 po 2 cap. Musc.= 20 torr θ cap. musc.= 0.32 Δ= 0.66 se p50= 26 torr e n= 2.8 mas se n= 1 θ cap. alv.= 0.79 θ cap. musc.= 0.43 Δ= 0.36 A Hb facilita a libertação de 1.83x mais O 2 do que a Mb! 15
16 Hemoglobina - A Hb transporta O 2, H + e CO 2 - A Hb é uma proteína alostérica A afinidade pelo O 2 é regulada por ph CO 2 BPG < afinidade pelo O 2 > libertação de O 2 para tecidos BPG = biphosphoglicerate Hemoglobina Se ph e pco 2 Afinidade da Hb pelo O 2 (estabilização da forma T, tensa ) ph Facilita a libertação de O 2 nos tecidos CO 2 liga-se na forma de carbamato ao terminal-n de cada cadeia polipeptídica Carbaminohemoglobina pco 2 16
17 Curvas de saturação da mioglobina e hemoglobina efeito do ph Hemoglobina Efeito de Bohr O 2 Hb + H + + CO 2 Tecido muscular (Bohr) Hb H + Tecido pulmonar (Haldane) O 2 CO 2 O 2 17
18 Hemoglobina Transporte de O 2 e CO 2 nos glóbulos vermelhos Tecidos Pulmões Hemoglobina e o 2,3-bifosfoglicerato (BPG) - O BPG a afinidade da Hb pelo O 2 Estabilização da estrutura quaternária na forma desoxi (T) - Liga-se às cadeias β (AA+) (Lys E1, Lys F6 e His H21) - O BPG liga-se menos à Hb F > afinidade da Hb F pelo O 2 (HbF: H21 é uma serina e não histidina) Transferência de O 2 da circulação materna para a Hb fetal 18
19 Ligação de 2,3-bifosfoglicerato (BPG) à desoxihemoglobina (T) As cargas negativas (-) do BPG interagem com cargas positivas (+) das 2 subunidades β Curvas de saturação da mioglobina e hemoglobina efeito do CO 2 e BPG 19
20 Mioglobina e Hemoglobina 1. A mioglobina (Mb) é uma proteína monomérica. A Hemoglobina (Hb) é um tetrâmero. 2. Cada cadeia polipeptídica liga um grupo prostético Heme (protoporfirina + ferro) 3. O oxigénio liga-se à 6ª posição de coordenação do ferro (Fe 2+ ) no heme. 4. A histidina F8 (proximal) ocupa a 5ª posição de coordenação. A histidina E7 (distal) induz um ângulo (~120º) na ligação do O 2 ao Fe 2+ no plano do heme. 5. Durante a oxigenação, o ferro move-se para o plano do heme. 6. A alteração estrutural resultante da oxigenação induz a alteração da estrutura quaternária da Hb. 7. O oxigénio liga-se de forma cooperativa à Hb (a curva de dissociação do O 2 é sigmóide) maior eficiência no transporte de O O CO 2 liga-se na forma de carbamato à Hb (carbaminohb). 9. A afinidade da Hb pelo O 2 é regulada por: ph, CO 2 e BPG. 10. O BPG liga-se menos à Hb F > afinidade da Hb F pelo O 2. Porque é tóxico o monóxido de carbono? - O heme possui uma maior afinidade pelo CO do que pelo O 2. - A histidina 64 (E7) dificulta (~10x) a ligação de CO ao heme (angulação imposta pela His). - CO é tóxico porque impossibilita o transporte de O 2 pela Hb ou o seu armazenamento pela Mb. A Hb (GV) liga CO com alta afinidade. Como o CO não é utilizado pelas células e não existe O 2, ocorre hipóxia, morte celular e do próprio organismo. 20
As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos
 Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
PROTEÍNAS GLOBULARES E
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
accad.osu.edu/~vberezin/ibp/progress.htm Interações - e - mantém tetrâmero Hemoglobina é formada por cadeias e A G B D
 accad.osu.edu/~vberezin/ibp/progress.htm Hemoglobina é formada por cadeias e Interações - e - mantém tetrâmero 2 2 A G H B E D F C 1 Mioglobina e Hemoglobina O grupo heme Heme é um grupo prostético. Proteína
accad.osu.edu/~vberezin/ibp/progress.htm Hemoglobina é formada por cadeias e Interações - e - mantém tetrâmero 2 2 A G H B E D F C 1 Mioglobina e Hemoglobina O grupo heme Heme é um grupo prostético. Proteína
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
Proteínas. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Proteínas Estrutura Tridimensional de proteína Conformação Estabilidade de proteínas Ligação peptídica Estrutura Secundária
Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Proteínas Estrutura Tridimensional de proteína Conformação Estabilidade de proteínas Ligação peptídica Estrutura Secundária
Função de Proteínas: Mioglobina e Hemoglobina
 Aula de Bioquímica Avançada Tema: Função de Proteínas: Mioglobina e Hemoglobina Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade
Aula de Bioquímica Avançada Tema: Função de Proteínas: Mioglobina e Hemoglobina Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade
Introdução à Bioquímica. Função das Proteínas
 Introdução à Bioquímica Função das Proteínas Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto.. SP. Tópicos! Mioglobina! Hemoglobina! Miosina
Introdução à Bioquímica Função das Proteínas Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto.. SP. Tópicos! Mioglobina! Hemoglobina! Miosina
Hemoglobina. Prof. Archangelo Fernandes Profa Alessandra Barone
 Hemoglobina Prof. Archangelo Fernandes Profa Alessandra Barone www.profbio.com.br Hemoglobina (Hb) Molécula formada por quadro cadeias polipeptídicas globínicas associadas a 4 anéis porfirínicos heme.
Hemoglobina Prof. Archangelo Fernandes Profa Alessandra Barone www.profbio.com.br Hemoglobina (Hb) Molécula formada por quadro cadeias polipeptídicas globínicas associadas a 4 anéis porfirínicos heme.
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades e funções de proteínas: Mioglobina / Hemoglobina
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades e funções de proteínas: Mioglobina / Hemoglobina
Metais no Organismo Humano
 Metais no Organismo Humano Relativamente à necessidade biológica podem classificar-se Metais Essenciais: Metais Tóxicos: sódio, potássio, cálcio, magnésio, ferro, crómio, zinco, cobalto, manganês e níquel.
Metais no Organismo Humano Relativamente à necessidade biológica podem classificar-se Metais Essenciais: Metais Tóxicos: sódio, potássio, cálcio, magnésio, ferro, crómio, zinco, cobalto, manganês e níquel.
Aula 2: Estrutura e Função de Proteínas
 Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
resumo da aula anterior: Estrutura e função de proteinas
 QBQ 2451 Introdução à Bioquímica 2013 Maria Teresa Machini Laboratório de Química de Peptídeos Bloco 8 Superior sala 0854 mtmachini@iq.usp.br resumo da aula anterior: Estrutura e função de proteinas IDENTIFICAÇÃO
QBQ 2451 Introdução à Bioquímica 2013 Maria Teresa Machini Laboratório de Química de Peptídeos Bloco 8 Superior sala 0854 mtmachini@iq.usp.br resumo da aula anterior: Estrutura e função de proteinas IDENTIFICAÇÃO
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO. Profa. Dra. Celene Fernandes Bernardes
 TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Todas essas forças são usadas para a manutenção da estrutura tridimensional das proteínas - conformação A conformação de uma proteína é fundamental para a função que ela exerce
ESTRUTURA DAS PROTEÍNAS Todas essas forças são usadas para a manutenção da estrutura tridimensional das proteínas - conformação A conformação de uma proteína é fundamental para a função que ela exerce
ESTRUTURAS TRIDIMENSIONAIS E FUNÇÕES BIOLÓGICAS DAS PROTEÍNAS GLOBULARES
 ESTRUTURAS TRIDIMENSIONAIS E FUNÇÕES BIOLÓGICAS DAS PROTEÍNAS GLOBULARES Aula 6 META Identificar as estruturas tridimensionais das proteínas globulares, relacionando-as com as funções biológicas que essas
ESTRUTURAS TRIDIMENSIONAIS E FUNÇÕES BIOLÓGICAS DAS PROTEÍNAS GLOBULARES Aula 6 META Identificar as estruturas tridimensionais das proteínas globulares, relacionando-as com as funções biológicas que essas
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
SO9 TOXICIDADE DO MONÓXIDO DE CARBONO
 9 de Novembro de 2011 Turma 2 Grupo 6 SO9 TOXICIDADE DO MONÓXIDO DE CARBONO Beatriz Teixeira Pinto Daniel Melo Pinto Verena Almeida Pires Dina Rodriguez Pita Ana Cristina Vitorino Diana Murteira Maria
9 de Novembro de 2011 Turma 2 Grupo 6 SO9 TOXICIDADE DO MONÓXIDO DE CARBONO Beatriz Teixeira Pinto Daniel Melo Pinto Verena Almeida Pires Dina Rodriguez Pita Ana Cristina Vitorino Diana Murteira Maria
PROTEÍNAS. Um polipeptídeo de dimensão macromolecular ou um conjunto de polipeptídeos associados entre si constituem proteínas.
 PROTEÍNAS PROTEÍNAS DEFINIÇÃO Compostos nitrogenados orgânicos complexos, presentes em todas as células vivas, formados fundamentalmente por C, H, O e N. Contêm ainda S, P, Cu, etc.. Os compostos nitrogenados
PROTEÍNAS PROTEÍNAS DEFINIÇÃO Compostos nitrogenados orgânicos complexos, presentes em todas as células vivas, formados fundamentalmente por C, H, O e N. Contêm ainda S, P, Cu, etc.. Os compostos nitrogenados
Proteínas. Proteínas são polímeros de aminoácidos
 Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
A função das proteínas fibrosas como elementos estruturais de células e tecidos depende de interações entre cadeias polipeptídicas idênticas.
 A função das proteínas quase sempre depende da interação com outras moléculas A função das proteínas fibrosas como elementos estruturais de células e tecidos depende de interações entre cadeias polipeptídicas
A função das proteínas quase sempre depende da interação com outras moléculas A função das proteínas fibrosas como elementos estruturais de células e tecidos depende de interações entre cadeias polipeptídicas
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
LIGAÇÃO PEPTÍDICA. ligação peptídica DIPEPTÍDEO AMINOÁCIDOS
 PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
Sistema Respiratório. Superior. Língua. Inferior
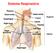 Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III
 Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Aminoácidos peptídeos e proteínas
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Casos clínicos. Seção II
 Casos clínicos Seção II CASO 1 Menina afro-americana de 15 anos vai à emergência com queixa de dor bilateral na coxa e no quadril. A dor está presente há um dia e é cada vez mais intensa em termos de
Casos clínicos Seção II CASO 1 Menina afro-americana de 15 anos vai à emergência com queixa de dor bilateral na coxa e no quadril. A dor está presente há um dia e é cada vez mais intensa em termos de
Proteínas. Profa. Alana Cecília
 Proteínas Profa. Alana Cecília Proteínas Aminoácidos ligados formam uma cadeia proteica (polipeptídica). As unidades de repetição são planos de amida que contêm ligações peptídicas. Esses planos de amida
Proteínas Profa. Alana Cecília Proteínas Aminoácidos ligados formam uma cadeia proteica (polipeptídica). As unidades de repetição são planos de amida que contêm ligações peptídicas. Esses planos de amida
Faculdade Anhanguera Curso de Graduação em Educação Física
 Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Os gases respiratórios não exercem pressão parcial quando estão combinados com os pigmentos respiratórios, nem quando estão quimicamente modificados.
 A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios (movimento por fluxo). Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas.
A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios (movimento por fluxo). Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas.
AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES
 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
Ciclo Respiratório Normal. Como Respiramos? Prova de Função Pulmonar. Que diz a espirometria? Espirômetro. Sensível ao volume.
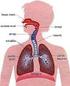 Ciclo Respiratório Normal Como Respiramos? Prova de Função Pulmonar Que diz a espirometria? Espirômetro Sensível ao volume Sensível ao fluxo 1 FEV1 / FVC % Visão Geral da Hematose O índice espirométrico
Ciclo Respiratório Normal Como Respiramos? Prova de Função Pulmonar Que diz a espirometria? Espirômetro Sensível ao volume Sensível ao fluxo 1 FEV1 / FVC % Visão Geral da Hematose O índice espirométrico
Os gases respiratórios não exercem pressão parcial quando estão combinados com os pigmentos respiratórios, nem quando estão quimicamente modificados.
 A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios (movimento por fluxo). Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas.
A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios (movimento por fluxo). Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas.
29/08/2015 QUÍMICA DE PROTEÍNAS. Medicina Veterinária IBGM - IBS. Medicina Veterinária IBGM - IBS
 QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
Universidade de São Paulo QFL0343: Reações de Compostos Orgânicos II e Biomoléculas Grupo 2: Peptídeos e Proteínas - Estrutura de Proteínas
 Universidade de São Paulo QFL0343: Reações de Compostos Orgânicos II e Biomoléculas - 2016 Grupo 2: Peptídeos e Proteínas - Estrutura de Proteínas Alex Monteiro Magalhães (8020779) Karina Brandt (8566483)
Universidade de São Paulo QFL0343: Reações de Compostos Orgânicos II e Biomoléculas - 2016 Grupo 2: Peptídeos e Proteínas - Estrutura de Proteínas Alex Monteiro Magalhães (8020779) Karina Brandt (8566483)
O QUE É UMA PROTEÍNA?
 PROTEÍNAS O QUE É UMA PROTEÍNA? Macromoléculas que agem em processos biológicos como: Mediação por catálise proteica, transporte de outras moléculas, controle de condições intra/extra celulares e transporte
PROTEÍNAS O QUE É UMA PROTEÍNA? Macromoléculas que agem em processos biológicos como: Mediação por catálise proteica, transporte de outras moléculas, controle de condições intra/extra celulares e transporte
O grupo responsável pelo transporte de O 2 é uma porfirina lidada à cadeia proteica com um átomo de Fe 2+ quelado
 Transporte de Oxigênio Shriver & Atikins, cap. 26 Mioglobina é uma proteína de baixa massa molar (17 kda) presente nos tecidos musculares de mamíferos que apresenta a função de transportar O 2 O grupo
Transporte de Oxigênio Shriver & Atikins, cap. 26 Mioglobina é uma proteína de baixa massa molar (17 kda) presente nos tecidos musculares de mamíferos que apresenta a função de transportar O 2 O grupo
Aminoácidos. Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP.
 Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Composição e Estrutura Molecular dos Sistemas Biológicos
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
BIOQUÍMICA PARA ODONTO
 BIOQUÍMICA PARA ODONTO Aula 3: Autoria: Ligação peptídica Proteínas globulares: estrutura primária, secundária e terciária Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade
BIOQUÍMICA PARA ODONTO Aula 3: Autoria: Ligação peptídica Proteínas globulares: estrutura primária, secundária e terciária Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade
Proteínas são organizadas em níveis. Na aula passada... Cadeia polipetídica na conformação estendida
 Na aula passada... Proteínas são organizadas em níveis Proteínas adotam forma tridimensional característica sua forma nativa Uma cadeia polipetídica com uma certa sequência de aminoácidos sempre se dobra
Na aula passada... Proteínas são organizadas em níveis Proteínas adotam forma tridimensional característica sua forma nativa Uma cadeia polipetídica com uma certa sequência de aminoácidos sempre se dobra
TRANSPORTE DE GASES NO SANGUE. Departamento de Bioquímica e Biologia Molecular Setor de Ciências Biológicas
 TRANSPORTE DE GASES NO SANGUE Departamento de Bioquímica e Biologia Molecular Setor de Ciências Biológicas ANATOMIA DO SISTEMA RESPIRATÓRIO ESTRUTURA DAS VIAS AÉREAS ESQUERDO WEST 2002 VASOS ALVEOLARES
TRANSPORTE DE GASES NO SANGUE Departamento de Bioquímica e Biologia Molecular Setor de Ciências Biológicas ANATOMIA DO SISTEMA RESPIRATÓRIO ESTRUTURA DAS VIAS AÉREAS ESQUERDO WEST 2002 VASOS ALVEOLARES
Função de Proteínas: Mioglobina e Hemoglobina
 Aula de Bioquímica I Tema: Função de Proteínas: Mioglobina e Hemoglobina Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São
Aula de Bioquímica I Tema: Função de Proteínas: Mioglobina e Hemoglobina Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Você deve desenhar o aminoácido com o grupo amino protonado (pka > 7) e o grupo carboxílico desprotonado (pka <7).
 QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
LIGAÇÕES QUÍMICAS REVISÃO
 LIGAÇÕES QUÍMICAS REVISÃO Ligações químicas e forças atrativas 1- Ligações covalentes Ligação química entre dois átomos na qual elétrons são compartilhados Ligação Forte Energia de ligação é a energia
LIGAÇÕES QUÍMICAS REVISÃO Ligações químicas e forças atrativas 1- Ligações covalentes Ligação química entre dois átomos na qual elétrons são compartilhados Ligação Forte Energia de ligação é a energia
FISIOLOGIA DO EXERCÍCIO
 FISIOLOGIA DO EXERCÍCIO 1 Ventilação e metabolismo energético Equivalente ventilatório de oxigênio: Relação entre volume de ar ventilado (VaV) e a quantidade de oxigênio consumida pelos tecidos (VO2) indica
FISIOLOGIA DO EXERCÍCIO 1 Ventilação e metabolismo energético Equivalente ventilatório de oxigênio: Relação entre volume de ar ventilado (VaV) e a quantidade de oxigênio consumida pelos tecidos (VO2) indica
Interações de van der Waals. Interações de van der Waals. Interações de van der Waals.
 Interações de van der Waals aandrico@if.sc.usp.br Também conhecidas como forças de dispersão de London, caracterizam-se pelo momento de dipolo induzido e ocorrem entre todos os átomos. Apesar de moléculas
Interações de van der Waals aandrico@if.sc.usp.br Também conhecidas como forças de dispersão de London, caracterizam-se pelo momento de dipolo induzido e ocorrem entre todos os átomos. Apesar de moléculas
Aminoácidos, Péptidos e Proteínas
 Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 7ª AULA PRÁTICA
 Disciplina de BOQUÍMCA do Ciclo Básico de MEDCNA Universidade dos Açores 1º Ano ENSNO PRÁTCO 7ª AULA PRÁTCA 1. PRNCÍPOS GERAS DE ESPECTROFOTOMETRA DE ABSORÇÃO - Lei de Beer-Lambert - Espectro de absorção
Disciplina de BOQUÍMCA do Ciclo Básico de MEDCNA Universidade dos Açores 1º Ano ENSNO PRÁTCO 7ª AULA PRÁTCA 1. PRNCÍPOS GERAS DE ESPECTROFOTOMETRA DE ABSORÇÃO - Lei de Beer-Lambert - Espectro de absorção
Função de Proteínas: Mioglobina e Hemoglobina
 Aula de Bioquímica I Tema: Função de Proteínas: Mioglobina e Hemoglobina Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São
Aula de Bioquímica I Tema: Função de Proteínas: Mioglobina e Hemoglobina Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
água 47 mmhg Hg) 37 o C Temperatura ( o C)
 Difusão e Transporte dos Gases Propriedade dos Gases Lei dos gases A pressão dos gases é determinada pelo impacto constante das moléculas em movimento contra uma superfície. Os gases dissolvidos na água
Difusão e Transporte dos Gases Propriedade dos Gases Lei dos gases A pressão dos gases é determinada pelo impacto constante das moléculas em movimento contra uma superfície. Os gases dissolvidos na água
BIOENGENHARIA I UFPB CT DEQ Prof. Sharline Florentino de Melo Santos
 BIOENGENHARIA I UFPB CT DEQ Prof. Sharline Florentino de Melo Santos As proteínas são compostos orgânicos de alto peso molecular formadas pelo encadeamento de aminoácidos. Representam cerca do 50 a 80%
BIOENGENHARIA I UFPB CT DEQ Prof. Sharline Florentino de Melo Santos As proteínas são compostos orgânicos de alto peso molecular formadas pelo encadeamento de aminoácidos. Representam cerca do 50 a 80%
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
Componentes Químicos das Células
 Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Sangue!!! TRANSPORTE DE GASES NOS FLUÍDOS CORPORAIS. O que é sangue? Qual(is) a(s) sua(s) função(ões)? 03/04/2017 PERGUNTAS INICIAIS FUNÇÕES DO SANGUE
 TRANSPORTE DE GASES NOS FLUÍDOS CORPORAIS Sangue!!! PERGUNTAS INICIAIS O que é sangue? Qual(is) a(s) sua(s) função(ões)? FUNÇÕES DO SANGUE Transporte: Nutrientes Metabólitos Gases Hormônios Calor (regulação
TRANSPORTE DE GASES NOS FLUÍDOS CORPORAIS Sangue!!! PERGUNTAS INICIAIS O que é sangue? Qual(is) a(s) sua(s) função(ões)? FUNÇÕES DO SANGUE Transporte: Nutrientes Metabólitos Gases Hormônios Calor (regulação
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
Bioinformática Estrutural Aula 1
 Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Aula 5 Estrutura e função de proteínas
 Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
8ª aula teórica Proteínas estruturais: colagénio, queratina e elastina. Bibliografia
 BIOQUÍMICA I 2010/2011 Ensino teórico - 1º ano Mestrado Integrado em Medicina 8ª aula teórica Proteínas estruturais: colagénio, queratina e elastina 12-10-2010 Bibliografia Biochemistry with clinical correlations,
BIOQUÍMICA I 2010/2011 Ensino teórico - 1º ano Mestrado Integrado em Medicina 8ª aula teórica Proteínas estruturais: colagénio, queratina e elastina 12-10-2010 Bibliografia Biochemistry with clinical correlations,
Lista de Exercícios de Bioquímica
 Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
META Introduzir o estudo das proteínas, compreendendo algumas de suas principais funções biológicas e de suas classificações.
 INTRODUÇÃO AO ESTUDO DAS PROTEÍNAS Aula 4 META Introduzir o estudo das proteínas, compreendendo algumas de suas principais funções biológicas e de suas classificações. OBJETIVOS Ao final desta aula, o
INTRODUÇÃO AO ESTUDO DAS PROTEÍNAS Aula 4 META Introduzir o estudo das proteínas, compreendendo algumas de suas principais funções biológicas e de suas classificações. OBJETIVOS Ao final desta aula, o
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
XI SEMINÁRIO. Tema: HEMOGLOBINAS NORMAIS E ANORMAIS DREPANOCITOSE. Subtemas: Hemoglobinas normais e hemoglobinopatias Clínica da drepanocitose
 XI SEMINÁRIO Tema: HEMOGLOBINAS NORMAIS E ANORMAIS DREPANOCITOSE Subtemas: Hemoglobinas normais e hemoglobinopatias Clínica da drepanocitose Intervenientes Docente convidado Dra. Filomena Pereira (Assistente
XI SEMINÁRIO Tema: HEMOGLOBINAS NORMAIS E ANORMAIS DREPANOCITOSE Subtemas: Hemoglobinas normais e hemoglobinopatias Clínica da drepanocitose Intervenientes Docente convidado Dra. Filomena Pereira (Assistente
Profª Eleonora Slide de aula
 Proteínas Profª Eleonora Slide de aula Estruturas conformacionais Proteínas São resultantes das forças de ligação entre os diferentes segmentos da cadeia polipeptídica e freqüentemente envolvem grupamentos
Proteínas Profª Eleonora Slide de aula Estruturas conformacionais Proteínas São resultantes das forças de ligação entre os diferentes segmentos da cadeia polipeptídica e freqüentemente envolvem grupamentos
Macromolécula mais abundante nas células
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
III SEMINÁRIO. Tema: PATOLOGIA MOLECULAR DA HEMOGLOBINA. Subtemas:
 III SEMINÁRIO Tema: PATOLOGIA MOLECULAR DA HEMOGLOBINA Subtemas: Estrutura da hemoglobina e transporte de oxigénio Síntese de hemoglobina durante o desenvolvimento fetal Generalidades sobre as hemoglobinas
III SEMINÁRIO Tema: PATOLOGIA MOLECULAR DA HEMOGLOBINA Subtemas: Estrutura da hemoglobina e transporte de oxigénio Síntese de hemoglobina durante o desenvolvimento fetal Generalidades sobre as hemoglobinas
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
INTRODUÇÃO Á BIOQUÍMICA
 INTRODUÇÃO Á BIOQUÍMICA BIOQUÍMICA ENFERMAGEM FIO Faculdades Integradas de Ourinhos. Prof. Esp. Roberto Venerando Fundação Educacional Miguel Mofarrej. FIO robertovenerando@fio.edu.br 1 - Introdução à
INTRODUÇÃO Á BIOQUÍMICA BIOQUÍMICA ENFERMAGEM FIO Faculdades Integradas de Ourinhos. Prof. Esp. Roberto Venerando Fundação Educacional Miguel Mofarrej. FIO robertovenerando@fio.edu.br 1 - Introdução à
Exame normal módulo de Bioquímica 11 Fev 08
 Licenciatura em Enfermagem Biofísica e Bioquímica 1º Ano - 1º Semestre 2007/2008 Exame normal módulo de Bioquímica 11 Fev 08 Duração = 2 horas Cotação máxima = 13,5 valores (A cotação de cada pergunta
Licenciatura em Enfermagem Biofísica e Bioquímica 1º Ano - 1º Semestre 2007/2008 Exame normal módulo de Bioquímica 11 Fev 08 Duração = 2 horas Cotação máxima = 13,5 valores (A cotação de cada pergunta
Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro:
 TROCAS GASOSAS E CONTROLE DO TRANSPORTE DE GASES Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro: 1. Trocas gasosas 1.1. Locais
TROCAS GASOSAS E CONTROLE DO TRANSPORTE DE GASES Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro: 1. Trocas gasosas 1.1. Locais
Aula 1. Referência. Bancos de Dados. Linguagem x Informação. Introdução a Bioquímica: Biomoléculas. Introdução ao Curso: Aminoácidos.
 Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica Metabólica
 Bioquímica Metabólica Notas de aula Roberto K. Salinas roberto@iq.usp.br Instituto de Química - USP versão 12/08/2016 1. Aminoácidos 1. Desenhe a estrutura da metionina. Indique qual carbono é quiral.
Bioquímica Metabólica Notas de aula Roberto K. Salinas roberto@iq.usp.br Instituto de Química - USP versão 12/08/2016 1. Aminoácidos 1. Desenhe a estrutura da metionina. Indique qual carbono é quiral.
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas.
 São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Enzimas Alostéricas e com Múltiplos Sítios Ativos
 Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs
 Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa
 OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
Aminoácidos FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
1. Respiração Orgânica x Respiração Celular
 Respiração 1. Respiração Orgânica x Respiração Celular 2. Respiração Direta x Respiração Indireta O 2 CO 2 O 2 CO 2 superfície respiratória tecidos Problema Limita o tamanho Ex: poríferos, cnidários, platelmintos,
Respiração 1. Respiração Orgânica x Respiração Celular 2. Respiração Direta x Respiração Indireta O 2 CO 2 O 2 CO 2 superfície respiratória tecidos Problema Limita o tamanho Ex: poríferos, cnidários, platelmintos,
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA. * Catabolismo do Heme e produção de Bilirrubina
 DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA A bilirrubina refere-se à concentração de bilirrubina (Brb) no sangue. A bilirrubina é um produto do catabolismo do
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA A bilirrubina refere-se à concentração de bilirrubina (Brb) no sangue. A bilirrubina é um produto do catabolismo do
Biologia e Geologia 10º ano. Natércia Charruadas 2011
 Biologia e Geologia 10º ano Natércia Charruadas 2011 Todos os seres vivos, logo todas as células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por um
Biologia e Geologia 10º ano Natércia Charruadas 2011 Todos os seres vivos, logo todas as células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por um
Lípidos e proteínas como componentes das membranas biológicas
 BIOQUÍMICA I 2010/2011 Ensino teórico - 1º ano Mestrado Integrado em Medicina 5ª Aula teórica Lípidos e proteínas como componentes das membranas biológicas 28/09/2010 Bibliografia Stryer, Biochemistry,
BIOQUÍMICA I 2010/2011 Ensino teórico - 1º ano Mestrado Integrado em Medicina 5ª Aula teórica Lípidos e proteínas como componentes das membranas biológicas 28/09/2010 Bibliografia Stryer, Biochemistry,
Proteínas FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Proteínas Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Peptídeos São cadeias de aminoácidos; São percursores
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Proteínas Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Peptídeos São cadeias de aminoácidos; São percursores
Proteínas - I. (Estrutura) Bioquímica Prof. Dr. Marcelo Soares
 Proteínas - I (Estrutura) Proteínas São polímeros compostos por combinações entre os 20 aminoácidos-padrão Apresentam tamanho que vai desde 50 até 4000 aminoácidos, variando também nas proporções entre
Proteínas - I (Estrutura) Proteínas São polímeros compostos por combinações entre os 20 aminoácidos-padrão Apresentam tamanho que vai desde 50 até 4000 aminoácidos, variando também nas proporções entre
ph do sangue arterial = 7.4
 Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Prof. Marcelo Langer. Curso de Biologia. Aula Genética
 Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia
 A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia elétrica Micrografia eletrônica de uma mitocôndria
A mitocôndria oxida combustíveis para gerar energia, em analogia ao processo pelo qual as usinas de força utilizam os combustíveis para gerar energia elétrica Micrografia eletrônica de uma mitocôndria
Ciência que estuda a química da vida (características dos seres vivos)
 Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
