Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 7ª AULA PRÁTICA
|
|
|
- Ricardo Francisco Freire Pacheco
- 7 Há anos
- Visualizações:
Transcrição
1 Disciplina de BOQUÍMCA do Ciclo Básico de MEDCNA Universidade dos Açores 1º Ano ENSNO PRÁTCO 7ª AULA PRÁTCA 1. PRNCÍPOS GERAS DE ESPECTROFOTOMETRA DE ABSORÇÃO - Lei de Beer-Lambert - Espectro de absorção (Hemoglobina oxigenada e desoxigenada) - Utilização do espectrofotómetro 2. ANÁLSE DO ESPECTRO DE ABSORÇÃO DA HEMOGLOBNA REDUZDA E OXDADA
2 1. PRNCÍPOS GERAS DE ESPECTROFOTOMETRA DE ABSORÇÃO A absorção de luz por uma substância em solução pode ser utilizada para determinar a sua concentração, uma vez que, para soluções diluídas, existe uma relação linear entre a concentração da substância e a quantidade de luz absorvida. Além disso, cada substância absorve mais fortemente uns comprimentos de onda do que outros. A absorção de luz característica de cada substância, que representa o seu Espectro de Absorção, pode ser utilizada para caracterizar e identificar uma ou mais substâncias numa mistura. Na Figura 1 exemplificam-se os espectros de absorção da hemoglobina na forma oxigenada (oxihemoglobina) e desoxigenada (desoxihemoglobina). Coeficiente de extinção molar (cm -1 M -1 ) Oxihemoglobina Desoxihemoglobina Comprimento de onda λ (nm) Fig. 1- Espectros de absorção da oxihemoglobina e desoxihemoglobina. O espectro da hemoglobina modifica-se acentuadamente, quando a hemoglobina liga O 2, como se observa pelos máximos de absorção característicos de cada espectro. 1
3 Leis da absorção aplicáveis à determinação da concentração de substâncias em solução (Lei de Beer-Lambert) Quando um feixe de luz passa através de uma solução, parte da luz é absorvida pelos componentes da solução. A relação matemática entre a concentração de uma substância em solução e a absorção, é dada pela lei de Beer-Lambert. Consideremos um tubo de espessura (l) contendo uma solução, e um feixe de luz monocromática ( ) que a atravessa: l A lei de Lambert pode expressar-se por: log K 1 x l em que: = intensidade original do feixe de luz = intensidade do feixe de luz depois de atravessar a solução l = espessura da solução, expressa em centímetros K 1 = constante de proporcionalidade que depende das características de absorção da substância, da temperatura e do comprimento de onda utilizado A lei de Beer pode expressar-se por: log K 2 x C em que: e têm o mesmo significado. C = concentração da substância em solução, expressa em moles por litro (ou molar) K 2 = constante de proporcionalidade 2
4 Combinando as duas expressões obtém-se a equação fundamental da absorção da luz, conhecida como lei de Beer-Lambert: 1og = k x l x C em que: k = coeficiente de extinção molar, normalmente referido por ε e log = Abs (absorvância) Assim, a expressão da lei de Beer-Lambert pode tomar a seguinte forma: Abs = ε x l x C Chama-se coeficiente de extinção molar de uma substância, ε, ao valor da absorvância de uma substância de concentração 1 M, medida num tubo com uma espessura de 1cm. O coeficiente de extinção molar é específico da substância, para um dado comprimento de onda, e tem normalmente um valor grande quando a luz de um dado comprimento de onda é absorvida eficientemente pela substância. A lei de Beer-Lambert pode, portanto, ser utilizada para determinar o coeficiente de extinção molar de substâncias em solução e para determinar a concentração de uma ou mais substâncias em solução. Deve notar-se que as leis da absorção indicadas só se aplicam à luz monocromática (de um comprimento de onda particular) e não podem ser aplicadas a bandas, ainda que estreitas, de diferentes comprimentos de onda. A lei de Beer-Lambert é válida somente para soluções relativamente diluídas, uma vez que acima de certas concentrações a relação entre a absorvância e a concentração deixa de ser linear, como se exemplifica na Figura 2. Para que seja possível utilizar a relação entre a densidade óptica de soluções de concentração conhecida e a concentração (curva padrão) para extrapolar concentrações de amostras de concentração desconhecida a partir da sua absorvância, é necessário que o meio usado na preparação dos padrões seja o mesmo usado na preparação das amostras e que se desconte sempre a leitura da absorvância do solvente sem substância adicionada, a todas as leituras das amostras. 3
5 Abs 0,6 0,5 0,4 Lei de Beer-Lambert não aplicável 0,3 Lei de Beer-Lambert aplicável 0,2 0,1 0 2,5 5,0 7,5 10,0 Concentração (mg/ml) Fig. 2- Relação entre a absorvância e a concentração de uma substância em solução. Esta curva padrão só deve ser utilizada para calcular a concentração de uma dada solução a partir da absorvância medida na região linear (linha a tracejado). No exemplo indicado, a uma absorvância de 0,2, corresponde uma concentração de 2,5 mg/ml. Funcionamento de um espectrofotómetro Há diversos tipos de espectrofotómetro. Consistem essencialmente num prisma de difracção, que funciona como monocromador e de um sistema eléctrico de detecção, amplificação e medição. Assim, a luz, proveniente de uma lâmpada, passa através de um monocromador que a separa nos vários comprimentos de onda (λ); apenas um feixe de luz (de um λ específico) atravessa uma pequena fenda e incide na amostra. Esta absorve uma parte da luz e a que não é absorvida é transmitida através da amostra e vai ser detectada por um detector; o sinal eléctrico gerado é amplificado no amplificador e é enviado para o voltímetro (calibrado em unidades de absorvância) que lê a quantidade de luz que passou através da amostra. O voltímetro pode ligar-se a um registador, onde se pode obter um registo permanente da absorvância da amostra em função do tempo. O aparelho que vamos utilizar tem a capacidade de medir valores de absorvância numa gama de comprimentos de onda determinados (por exemplo, de 400 a 500 nm, dando-nos os valores de absorvância de 1 em 1 nm) e inclui um registador. Antes de medir a absorvância a cada comprimento de onda acerta-se o zero do aparelho (Abs=0), com uma célula contendo água ou o solvente do ensaio em causa. 4
6 2. DETERMNAÇÃO DOS ESPECTROS DE ABSORÇÃO DE DFERENTES FORMAS DE HEMOGLOBNA A análise por difracção de raios X da desoxihemoglobina mostra que a estrutura terciária das quatro subunidades é idêntica à observada na oxihemoglobina Porém, existe uma alteração significativa na estrutura quaternária, isto é, no modo pelo qual as cadeias estão orientadas em relação umas às outras. Na desoxigenação, as cadeias α sofrem uma rotação de cerca de 9º e as cadeias β de cerca de 7º, seguindo eixos diferentes, o que origina uma alteração nos pontos de contacto entre as quatro subunidades e a formação de novas ligações iónicas entre elas. A ligação das quatro moléculas de oxigénio, cada uma apresentando um diâmetro relativamente pequeno, pode ocasionar uma profunda alteração na estrutura quaternária da hemoglobina. O modo pelo qual a molécula de hemoglobina liga o oxigénio tem uma importância fundamental na sua função, como transportador de oxigénio na hemácia, dos pulmões para os tecidos periféricos, pobres em oxigénio. A hemoglobina constitui cerca de 90% da proteína total das hemácias, encontrandose concentrada no citoplasma. Devido à capacidade da hemoglobina em ligar oxigénio, o sangue total pode absorver cerca de 21 ml de oxigénio gasoso por 100 ml de sangue, enquanto que o plasma sanguíneo absorve apenas cerca de 0,3 ml de oxigénio. A curva sigmoidal de ligação do oxigénio pela hemoglobina significa que esta possui uma afinidade relativamente baixa para a ligação da primeira ou segunda moléculas de oxigénio; porém, uma vez que estas estejam ligadas, a ligação das moléculas subsequentes de oxigénio é bastante favorecida. É de salientar que a ligação da hemoglobina ao oxigénio requer que o ião ferro do grupo hémico se encontre na forma reduzida (Fe 2+ ). De maneira inversa, a perda de uma molécula de oxigénio pela molécula de hemoglobina, totalmente oxigenada, ocasiona a dissociação do oxigénio mais rapidamente quando a pressão parcial de oxigénio é reduzida. A interacção hemoglobina/oxigénio é também afectada pelo ph. Quanto maior fôr o ph da solução de hemoglobina, a uma determinada pressão parcial de oxigénio, maior é a percentagem de saturação com o oxigénio. Este efeito, reversível, ocorre, porque a hemoglobina oxigenada ioniza-se, libertando um protão por cada oxigénio ligado, de acordo com a equação HHb + + O 2 HbO 2 + H +, 5
7 na qual HHb +, é uma subunidade protonada da molécula de desoxihemoglobina. Uma vez que essa reacção é reversível, o aumento na concentração de H +, ocasionará o deslocamento do equilíbrio para a esquerda, no sentido da menor saturação, enquanto que uma diminuição da concentração hidrogeniónica ( [H + ] ph) ocasionará o deslocamento do equilíbrio para a direita, no sentido do aumento da saturação. O efeito do ph no equilíbrio oxigénio/hemoglobina é denominado Efeito de Bohr. A pressão parcial do oxigénio e o ph, são os dois factores mais importantes que regulam a função da hemoglobina no transporte do oxigénio. Nos pulmões, onde a pressão parcial do oxigénio é elevada (cerca de 100 mmhg) e o ph é também relativamente alto, a hemoglobina tende a atingir quase o máximo de saturação com o oxigénio (cerca de 96%). No interior dos tecidos periféricos, onde a tensão do oxigénio é baixa (cerca de 45 mmhg) e o ph também é baixo (devido à elevada concentração do CO 2, formado como produto final do metabolismo energético), a hemoglobina liga-se ao oxigénio com menos intensidade e irá, assim, ceder parte do seu oxigénio às células. Ao nível dos tecidos, a hemoglobina apresenta cerca de 65% saturação pelo O 2. Assim, a hemoglobina recicla entre 65 e 96% de saturação com o oxigénio, na sua função como transportadora do oxigénio. A determinação dos espectros de absorção das diferentes formas de hemoglobina tem como objectivo ilustrar como o espectro de absorção serve para caracterizar substâncias de acordo com as suas propriedades de absorção da luz. Os espectros da hemoglobina oxigenada e desoxigenada são diferentes (Fig. 1), o que impossibilita uma determinação precisa da concentração de hemoglobina total numa solução que contém as duas formas (oxigenada e desoxigenada) em proporções desconhecidas. Uma possibilidade de resolver o problema é converter toda a hemoglobina na forma desoxigenada, medindo a sua concentração nesta forma. O problema prático é que uma solução de hemoglobina desoxigenada pelo ditionito de sódio não é estável, porque a reacção é reversível e a hemoglobina vai-se oxigenando lentamente. No entanto, a hemoglobina pode ser convertida irreversívelmente em cianometa-hemoglobina, através da adição de um reagente apropriado, o reagente de Drabkins, usado correntemente na determinação clínica da concentração de hemoglobina no sangue. 6
8 PROTOCOLO 1. dentifique dois tubos de ensaio, um para a determinação do espectro da hemoglobina reduzida (Hb-Fe 2+ ) e outro para o espectro da hemoglobina oxidada (Hb-Fe 3+ ). 2. Meça para o tubo Hb-Fe 2+ 5 ml de água destilada e para o tubo Hb-Fe 3+ Medir 5 ml de HCl 0,1 N. 3. Pique um dedo com uma lanceta hematológica esterilizada e coloque uma gota de sangue em cada um dos tubos. Agite bem e espere alguns segundos para permitir a hemólise dos glóbulos vermelhos e obter uma soluções límpidas de hemoglobina.. Determinação do espectro de absorção da Hemoglobina reduzida (Fe 2+ ) 1. Com uma cuvette contendo água destilada, faça a linha de base no espectrofotómetro entre 480 e 620 nm. Em seguida, trace o espectro o espectro de absorção da solução de hemoglobina, na mesma gama de comprimentos de onda. 2. Assinalar os picos de absorção máxima do espectro traçado e compare com as curvas teóricas para os dois tipos de Hb-Fe 2+.. Determinação do espectro de absorção da Hemoglobina oxidada (Fe 3+ ) NOTA: Na solução diluída de HCl, os glóbulos vermelhos hemolisam e o Fe 2+ passa a Fe 3+, isto é, oxida, o que confere ao grupo heme da hemoglobina diferentes características de absorção de luz. 1. Repita o que foi feito para a hemoglobina reduzida (ponto 1 do nº), ou seja, trace o espectro entre 480 e 620 nm. 2. Assinalar os picos de absorção máxima característicos desta forma de hemoglobina. Análise dos resultados: - Discuta os resultados obtidos de acordo com a estrutura da hemoglobina e as características da ligação do oxigénio ao grupo hémico. 1
Adsorção de Azul de Metileno em Fibras de Algodão
 Adsorção de Azul de Metileno em Fibras de Algodão 1. Introdução A adsorção está intimamente ligada à tensão superficial das soluções e a intensidade desse fenômeno depende da temperatura, da natureza e
Adsorção de Azul de Metileno em Fibras de Algodão 1. Introdução A adsorção está intimamente ligada à tensão superficial das soluções e a intensidade desse fenômeno depende da temperatura, da natureza e
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Prática 10 Determinação da constante de equilíbrio entre íons Fe 3+ e SCN -
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
ESTUDO DA ESTABILIDADE E PROPRIEDADES DE COMPOSTOS DE COORDENAÇÃO
 versão Fev 2007 TRABALHO 2 ESTUDO DA ESTABILIDADE E PROPRIEDADES DE COMPOSTOS DE COORDENAÇÃO 1. OBJECTIVOS 1) Determinação da estequiometria e do coeficiente de extinção molar do complexo [Ni- EDTA] 2-
versão Fev 2007 TRABALHO 2 ESTUDO DA ESTABILIDADE E PROPRIEDADES DE COMPOSTOS DE COORDENAÇÃO 1. OBJECTIVOS 1) Determinação da estequiometria e do coeficiente de extinção molar do complexo [Ni- EDTA] 2-
Doseamento do Fe 2+ por espectroscopia de absorção
 Práticas Laboratoriais de Diagnóstico e Teoria do Restauro I (Ciências da Arte e do Património) Doseamento do Fe 2+ por espectroscopia de absorção Objectivo Determinar a concentração do ferro(ii) numa
Práticas Laboratoriais de Diagnóstico e Teoria do Restauro I (Ciências da Arte e do Património) Doseamento do Fe 2+ por espectroscopia de absorção Objectivo Determinar a concentração do ferro(ii) numa
EXPERIMENTO 3 ADSORÇÃO Determinação da Isoterma de adsorção do azul de metileno em fibra de algodão
 EXPERIMETO 3 ADSORÇÃO Determinação da Isoterma de adsorção do azul de metileno em fibra de algodão Adsorção é o acúmulo de uma substância numa interface, que é a superfície ou região limítrofe entre duas
EXPERIMETO 3 ADSORÇÃO Determinação da Isoterma de adsorção do azul de metileno em fibra de algodão Adsorção é o acúmulo de uma substância numa interface, que é a superfície ou região limítrofe entre duas
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
Espectrofotometria UV-Vis. Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva
 Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Relembrando... Conceitos Comprimento de onda (λ): distância entre dois pontos na mesma
Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Relembrando... Conceitos Comprimento de onda (λ): distância entre dois pontos na mesma
As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos
 Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA
 Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA Introdução: Método aplicado na determinação de compostos inorgânicos e orgânicos, como por
Análise Instrumental ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA ESPECTROSCOPIA NA LUZ VISÍVEL E ULTRAVIOLETA Introdução: Método aplicado na determinação de compostos inorgânicos e orgânicos, como por
Centro Universitário Anchieta Análise Química Instrumental 2016/1 Semestre - Prof.Ms. Vanderlei I. Paula Lista 3A Nome: RA
 Centro Universitário Anchieta Análise Química Instrumental 2016/1 Semestre - Prof.Ms. Vanderlei I. Paula Lista 3A Nome: RA 1) Qual é a relação entre *(a) absorbância e transmitância? (b) absortividade
Centro Universitário Anchieta Análise Química Instrumental 2016/1 Semestre - Prof.Ms. Vanderlei I. Paula Lista 3A Nome: RA 1) Qual é a relação entre *(a) absorbância e transmitância? (b) absortividade
Determinação dos espectros de absorção de diferentes formas de Hemoglobina
 Faculdade de Medicina da Universidade de Coimbra Bioquímica I 1º Ano Medicina Determinação dos espectros de absorção de diferentes formas de Hemoglobina T U R M A 6 A N O L E C T I V O 2 0 1 0 / 2 0 1
Faculdade de Medicina da Universidade de Coimbra Bioquímica I 1º Ano Medicina Determinação dos espectros de absorção de diferentes formas de Hemoglobina T U R M A 6 A N O L E C T I V O 2 0 1 0 / 2 0 1
Metodologia Analítica
 Metodologia Analítica Espectrofotometria UV-vis Prof. Renato Camargo Matos http://www.ufjf.br/nupis Prática Otimização de um Método Espectrofotométrico para Quantificação de Ferro Objetivo Estudar as propriedades
Metodologia Analítica Espectrofotometria UV-vis Prof. Renato Camargo Matos http://www.ufjf.br/nupis Prática Otimização de um Método Espectrofotométrico para Quantificação de Ferro Objetivo Estudar as propriedades
Determinação espectrofotométrica do pka do indicador vermelho de metilo
 Determinação espectrofotométrica do pka do indicador vermelho de metilo Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 28 /05/99 Objectivos Nesta actividade experimental temos como objectivo a determinação
Determinação espectrofotométrica do pka do indicador vermelho de metilo Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 28 /05/99 Objectivos Nesta actividade experimental temos como objectivo a determinação
DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE
 ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
Laboratório de Análise Instrumental
 Laboratório de Análise Instrumental Prof. Renato Camargo Matos Profa. Maria Auxiliadora Costa Matos http://www.ufjf.br/nupis DIA/MÊS ASSUNTO 06/03 Apresentação do curso 13/03 PRÁTICA 1: Determinação de
Laboratório de Análise Instrumental Prof. Renato Camargo Matos Profa. Maria Auxiliadora Costa Matos http://www.ufjf.br/nupis DIA/MÊS ASSUNTO 06/03 Apresentação do curso 13/03 PRÁTICA 1: Determinação de
Química Analítica Ambiental II
 Química Analítica Ambiental II Prof. Morun Bernardino Neto, DSc ESPECTROFOTOMETRIA II INSTRUMENTOS E APLICAÇÕES BREVE REVISÃO O gráfico abaixo mostra o espectro de absorção de um protetor solar que absorve
Química Analítica Ambiental II Prof. Morun Bernardino Neto, DSc ESPECTROFOTOMETRIA II INSTRUMENTOS E APLICAÇÕES BREVE REVISÃO O gráfico abaixo mostra o espectro de absorção de um protetor solar que absorve
Laboratório de Análise Instrumental
 Laboratório de Análise Instrumental Prof. Renato Camargo Matos Tutora: Aparecida Maria http://www.ufjf.br/nupis Caderno de Laboratório 1. Título 2. Introdução 3. Objetivo 4. Parte Experimental 4.1. Reagentes
Laboratório de Análise Instrumental Prof. Renato Camargo Matos Tutora: Aparecida Maria http://www.ufjf.br/nupis Caderno de Laboratório 1. Título 2. Introdução 3. Objetivo 4. Parte Experimental 4.1. Reagentes
UNIVERSIDADE PAULISTA. A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética e a matéria.
 DISCIPLINA: MÉTODOS INSTRUMENTAIS DE ANÁLISE TÓPICO 4: Espectrofotometria de Absorção Molecular UV/Visível A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética
DISCIPLINA: MÉTODOS INSTRUMENTAIS DE ANÁLISE TÓPICO 4: Espectrofotometria de Absorção Molecular UV/Visível A espectrofotometria é uma técnica de análise baseadas na interação entre a radiação eletromagnética
3. Metais Ambiente e Vida. A Cor nos Complexos Dulce Campos
 A Cor nos Complexos 1 A Cor nos Complexos Porquê uma solução apresenta cor? 2 A Cor nos Complexos 3 A Cor nos Complexos Porquê os complexos apresentam cor? [Ar] 3d 1 4 A Cor nos Complexos Espectro de Absorção
A Cor nos Complexos 1 A Cor nos Complexos Porquê uma solução apresenta cor? 2 A Cor nos Complexos 3 A Cor nos Complexos Porquê os complexos apresentam cor? [Ar] 3d 1 4 A Cor nos Complexos Espectro de Absorção
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 2º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Disciplina: Bioquímica Clínica Curso: Análises Clínicas 2º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 2º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
QUI346 ESPECTROFOTOMETRIA
 QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença entre as
QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença entre as
Espectros de Absorção
 Espectros de Absorção Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 21 /4/99 Introdução Este trabalho prático trabalhos consistiu no estudo, análise e interpretação do espectro de absorção de espécies
Espectros de Absorção Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 21 /4/99 Introdução Este trabalho prático trabalhos consistiu no estudo, análise e interpretação do espectro de absorção de espécies
Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro:
 TROCAS GASOSAS E CONTROLE DO TRANSPORTE DE GASES Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro: 1. Trocas gasosas 1.1. Locais
TROCAS GASOSAS E CONTROLE DO TRANSPORTE DE GASES Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro: 1. Trocas gasosas 1.1. Locais
Proteínas funcionais: hemoglobina e mioglobina
 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 9ª aula teórica 18 Outubro 2010 Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H.
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 9ª aula teórica 18 Outubro 2010 Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H.
Eng. Biomédica Lista de Exercícios Comprimento de onda (nm) Frequência ( verde
 Eng. Biomédica 01 Lista de Exercícios 01 1) Complete a Tabela de Frequências e comprimentos de onda Cor Comprimento de onda (nm) Frequência (10 1 Hz) vermelho 780 6 laranja amarelo 48-503 503-50 verde
Eng. Biomédica 01 Lista de Exercícios 01 1) Complete a Tabela de Frequências e comprimentos de onda Cor Comprimento de onda (nm) Frequência (10 1 Hz) vermelho 780 6 laranja amarelo 48-503 503-50 verde
UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE CIÊNCIAS EXATAS DEPARTAMENTO DE QUÍMICA CURSO DE QUÍMICA
 UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE CIÊNCIAS EXATAS DEPARTAMENTO DE QUÍMICA CURSO DE QUÍMICA LABORATÓRIO DE QUÍMICA ANALÍTICA INSTRUMENTAL II CQ122 Prática 1 Profa. Iara Messerschmidt Prof. Claudio
UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE CIÊNCIAS EXATAS DEPARTAMENTO DE QUÍMICA CURSO DE QUÍMICA LABORATÓRIO DE QUÍMICA ANALÍTICA INSTRUMENTAL II CQ122 Prática 1 Profa. Iara Messerschmidt Prof. Claudio
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO. Profa. Dra. Celene Fernandes Bernardes
 TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
ANÁLISE QUÍMICA INSTRUMENTAL. Métodos espectrais e opticos
 ANÁLISE QUÍMICA INSTRUMENTAL Métodos espectrais e opticos 6 Ed. Cap. 6 Pg.147-151 6 Ed. Cap. 1 Pg.1-28 6 Ed. Cap. 24 Pg.669-690 07/03/2018 2 Espectro eletromagnético Fonte: www.cena.usp.br/ irradiacao/espectro.htm
ANÁLISE QUÍMICA INSTRUMENTAL Métodos espectrais e opticos 6 Ed. Cap. 6 Pg.147-151 6 Ed. Cap. 1 Pg.1-28 6 Ed. Cap. 24 Pg.669-690 07/03/2018 2 Espectro eletromagnético Fonte: www.cena.usp.br/ irradiacao/espectro.htm
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA. * Catabolismo do Heme e produção de Bilirrubina
 DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA A bilirrubina refere-se à concentração de bilirrubina (Brb) no sangue. A bilirrubina é um produto do catabolismo do
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA A bilirrubina refere-se à concentração de bilirrubina (Brb) no sangue. A bilirrubina é um produto do catabolismo do
Química. APL 1.5 A cor e a composição quantitativa de soluções com iões metálicos
 Química APL 1.5 A cor e a composição quantitativa de soluções com iões metálicos Luísa Neves, 12ºCT 26 de janeiro de 2015 Índice Introdução...2 Material e Reagentes...3 Procedimento..4 Perigos específicos
Química APL 1.5 A cor e a composição quantitativa de soluções com iões metálicos Luísa Neves, 12ºCT 26 de janeiro de 2015 Índice Introdução...2 Material e Reagentes...3 Procedimento..4 Perigos específicos
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
accad.osu.edu/~vberezin/ibp/progress.htm Interações - e - mantém tetrâmero Hemoglobina é formada por cadeias e A G B D
 accad.osu.edu/~vberezin/ibp/progress.htm Hemoglobina é formada por cadeias e Interações - e - mantém tetrâmero 2 2 A G H B E D F C 1 Mioglobina e Hemoglobina O grupo heme Heme é um grupo prostético. Proteína
accad.osu.edu/~vberezin/ibp/progress.htm Hemoglobina é formada por cadeias e Interações - e - mantém tetrâmero 2 2 A G H B E D F C 1 Mioglobina e Hemoglobina O grupo heme Heme é um grupo prostético. Proteína
8.2. Na extremidade de uma corda suficientemente longa é imposta uma perturbação com frequência f = 5 Hz que provoca uma onda de amplitude
 Constantes Velocidade do som no ar: v som = 344 m /s Velocidade da luz no vácuo c = 3 10 8 m/s 8.1. Considere uma corda de comprimento L e densidade linear µ = m/l, onde m é a massa da corda. Partindo
Constantes Velocidade do som no ar: v som = 344 m /s Velocidade da luz no vácuo c = 3 10 8 m/s 8.1. Considere uma corda de comprimento L e densidade linear µ = m/l, onde m é a massa da corda. Partindo
Experiência 10: Estudo do equilíbrio cromato-dicromato
 1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015/1 Experiência 10: Estudo do equilíbrio cromato-dicromato 1. Equilíbrio químico Muitas reações químicas são reversíveis,
1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015/1 Experiência 10: Estudo do equilíbrio cromato-dicromato 1. Equilíbrio químico Muitas reações químicas são reversíveis,
Lista de Exercício 1ª TVC Química Analítica V Teoria
 Lista de Exercício 1ª TVC Química Analítica V Teoria Capítulo 7 Tratamento e Avaliação Estatística de Dados 7-3. Discuta como a dimensão do intervalo de confiança da média é influenciada pelos seguintes
Lista de Exercício 1ª TVC Química Analítica V Teoria Capítulo 7 Tratamento e Avaliação Estatística de Dados 7-3. Discuta como a dimensão do intervalo de confiança da média é influenciada pelos seguintes
Luís H. Melo de Carvalho Química Analítica II Luís H. Melo de Carvalho Química Analítica II
 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 1 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 2 Luís H. Melo de Carvalho 3 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 4 Luís H. Melo de Carvalho
Luís H. Melo de Carvalho Luís H. Melo de Carvalho 1 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 2 Luís H. Melo de Carvalho 3 Luís H. Melo de Carvalho Luís H. Melo de Carvalho 4 Luís H. Melo de Carvalho
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr.
 Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr. Fernando Ananias NOME: RA: ATIVIDADE PRÁTICA 1 A- ESPECTROFOTOMETRIA Espectroscopia
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr. Fernando Ananias NOME: RA: ATIVIDADE PRÁTICA 1 A- ESPECTROFOTOMETRIA Espectroscopia
Desenvolvimento de um método
 Desenvolvimento de um método -Espectro: registro de um espectro na região de interesse seleção do comprimento de onda -Fixação de comprimento de onda: monitoramento da absorbância no comprimento de onda
Desenvolvimento de um método -Espectro: registro de um espectro na região de interesse seleção do comprimento de onda -Fixação de comprimento de onda: monitoramento da absorbância no comprimento de onda
Ba 2+ (aq) + CrO 4. 2 (aq)
 Experiência 9: ESTUDO DO EQUILÍBRIO CROMATO-DICROMATO 1. Objetivos Ao final desta atividade experimental espera-se que o aluno seja capaz de: - A partir da equação química de um sistema em equilíbrio escrever
Experiência 9: ESTUDO DO EQUILÍBRIO CROMATO-DICROMATO 1. Objetivos Ao final desta atividade experimental espera-se que o aluno seja capaz de: - A partir da equação química de um sistema em equilíbrio escrever
UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química. CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012
 UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012 A Química Analítica A divisão tradicional em química analítica
UNIVERSIDADE FEDERAL DO PARANÁ Departamento de Química CQ122 Química Analítica Instrumental II Prof. Claudio Antonio Tonegutti Aula 01 09/11/2012 A Química Analítica A divisão tradicional em química analítica
DEPARTAMENTO DE QUÍMICA UFJF QUI102 Metodologia Analítica
 DEPARTAMENTO DE QUÍMICA UFJF QUI102 Metodologia Analítica OTIMIZAÇÃO DE UM MÉTODO ESPECTROFOTOMÉTRICO PARA QUANTIFICAÇÃO DE FERRO Data do experimento: Grupo: Objetivo: Estudar as propriedades colorimétricas
DEPARTAMENTO DE QUÍMICA UFJF QUI102 Metodologia Analítica OTIMIZAÇÃO DE UM MÉTODO ESPECTROFOTOMÉTRICO PARA QUANTIFICAÇÃO DE FERRO Data do experimento: Grupo: Objetivo: Estudar as propriedades colorimétricas
1. RESUMO 2. INTRODUÇÃO
 1. RESUMO O oxímetro de pulso é um aparelho capaz de medir a oxigenação do sangue e a frequência cardíaca, utilizado em aplicações médicas. Este trabalho tem como fundamento estudar o funcionamento de
1. RESUMO O oxímetro de pulso é um aparelho capaz de medir a oxigenação do sangue e a frequência cardíaca, utilizado em aplicações médicas. Este trabalho tem como fundamento estudar o funcionamento de
38 th International Chemistry Olympiad Gyeongsan - Coréia
 38 th Olimpíada Internacional de Química EXAME PRÁTICO 38 th International Chemistry Olympiad Gyeongsan - Coréia Experimento 1 - Cromatografia em fase reversa: Análise Espectrofotométrica Separação cromatográfica
38 th Olimpíada Internacional de Química EXAME PRÁTICO 38 th International Chemistry Olympiad Gyeongsan - Coréia Experimento 1 - Cromatografia em fase reversa: Análise Espectrofotométrica Separação cromatográfica
Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017
 1 ESPECTROFOTOMETRIA DE UV-VIS Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017 2 CONCEITOS PRINCIPAIS O que é Espectroscopia e Espectrometria? IUPAC, Compendium
1 ESPECTROFOTOMETRIA DE UV-VIS Mestrando: Jefferson Willian Martins Prof. Dr. Júlio César José da Silva Juiz de Fora, 2/2017 2 CONCEITOS PRINCIPAIS O que é Espectroscopia e Espectrometria? IUPAC, Compendium
Espectroscopia Óptica Instrumentação e aplicações UV/VIS. CQ122 Química Analítica Instrumental II 1º sem Prof. Claudio Antonio Tonegutti
 Espectroscopia Óptica Instrumentação e aplicações UV/VIS CQ122 Química Analítica Instrumental II 1º sem. 2017 Prof. Claudio Antonio Tonegutti Lei de Beer A = b c A = absorbância = absortividade molar (L
Espectroscopia Óptica Instrumentação e aplicações UV/VIS CQ122 Química Analítica Instrumental II 1º sem. 2017 Prof. Claudio Antonio Tonegutti Lei de Beer A = b c A = absorbância = absortividade molar (L
Lista de Exercício 1ª TVC Química Analítica V Teoria (1º Sem 2015)
 Lista de Exercício 1ª TVC Química Analítica V Teoria (1º Sem 2015) Capítulo 7 (Skoog) Tratamento e Avaliação Estatística de Dados 7-3. Discuta como a dimensão do intervalo de confiança da média é influenciada
Lista de Exercício 1ª TVC Química Analítica V Teoria (1º Sem 2015) Capítulo 7 (Skoog) Tratamento e Avaliação Estatística de Dados 7-3. Discuta como a dimensão do intervalo de confiança da média é influenciada
Espectrofotometria UV-Vis. Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva
 Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Juiz de Fora, 1/2018 1 Terminologia Espectroscopia: Parte da ciência que estuda o fenômeno
Espectrofotometria UV-Vis Química Analítica V Mestranda: Joseane Maria de Almeida Prof. Dr. Júlio César José da Silva Juiz de Fora, 1/2018 1 Terminologia Espectroscopia: Parte da ciência que estuda o fenômeno
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DE ESPECTROSCOPIA MOLECULAR UV-VISÍVEL. Prof a. Dr a. Luciana Maria Saran
 FCVA/ UNESP JABOTICABAL FUNDAMENTOS DE ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DE ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
TRABALHO Nº 1 DETERMINAÇÃO DO COMPRIMENTO DE ONDA DE UMA RADIAÇÃO DUPLA FENDA DE YOUNG
 TRABALHO Nº 1 DETERMINAÇÃO DO COMPRIMENTO DE ONDA DE UMA RADIAÇÃO DUPLA FENDA DE YOUNG Pretende-se realizar a experiência clássica de Thomas Young e utilizar o padrão de interferência de duas fontes pontuais
TRABALHO Nº 1 DETERMINAÇÃO DO COMPRIMENTO DE ONDA DE UMA RADIAÇÃO DUPLA FENDA DE YOUNG Pretende-se realizar a experiência clássica de Thomas Young e utilizar o padrão de interferência de duas fontes pontuais
Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC.
 Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC. Capítulo 24 (Skoog) Introdução aos Métodos Espectroquímicos 24-1. Por que uma solução de Cu(NH3)4 2+
Lista de Exercício 2ª TVC Química Analítica V Teoria (1º Sem 2016). Obs.: Entregar antes da 2ª TVC. Capítulo 24 (Skoog) Introdução aos Métodos Espectroquímicos 24-1. Por que uma solução de Cu(NH3)4 2+
Proteínas funcionais: hemoglobina e mioglobina
 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008 9ª aula teórica Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H. Freeman & Company,
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008 9ª aula teórica Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H. Freeman & Company,
08 Colorímetro Uma visão quantitativa da lei de Beer-Lambert
 08 Colorímetro Uma visão quantitativa da lei de Beer-Lambert 1 INTRODUÇÃO Uma questão essencial para os químicos e outros profissionais de áreas correlatas é a determinação da relação existente entre a
08 Colorímetro Uma visão quantitativa da lei de Beer-Lambert 1 INTRODUÇÃO Uma questão essencial para os químicos e outros profissionais de áreas correlatas é a determinação da relação existente entre a
CQ122 Química Analítica Instrumental II. Turma B 2º semestre 2012 Prof. Claudio Antonio Tonegutti. 1ª Avaliação Teórica 21/12/2012 GABARITO
 CQ122 Química Analítica Instrumental II Turma B 2º semestre 2012 Prof. Claudio Antonio Tonegutti 1ª Avaliação Teórica 21/12/2012 GABARITO 1) A figura abaixo apresenta o espectro eletromagnético com as
CQ122 Química Analítica Instrumental II Turma B 2º semestre 2012 Prof. Claudio Antonio Tonegutti 1ª Avaliação Teórica 21/12/2012 GABARITO 1) A figura abaixo apresenta o espectro eletromagnético com as
K P 10. Concentração. Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema
 Concentração Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema F = emissão de fluorescência P o = potência do feixe incidente
Concentração Potência a emissão de fluorescência (F) é proporcional à potência radiante do feixe de excitação que é absorvido pelo sistema F = emissão de fluorescência P o = potência do feixe incidente
CQ 033 FÍSICO QUÍMICA EXPERIMENTAL D
 UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE CIÊNCIAS EXATAS DEPARTAMENTO DE QUÍMICA CQ 033 FÍSICO QUÍMICA EXPERIMENTAL D REVISÃO PARA A 2ª PROVA PRÁTICA 06 - Entalpia de formação do NH 4 Cl(s) 1- formação
UNIVERSIDADE FEDERAL DO PARANÁ SETOR DE CIÊNCIAS EXATAS DEPARTAMENTO DE QUÍMICA CQ 033 FÍSICO QUÍMICA EXPERIMENTAL D REVISÃO PARA A 2ª PROVA PRÁTICA 06 - Entalpia de formação do NH 4 Cl(s) 1- formação
TÉCNICAS LABORATORIAIS EM QUÍMICA E BIOQUÍMICA Espetrofotometria de absorção atómica
 TÉCNICAS LABORATORIAIS EM QUÍMICA E BIOQUÍMICA Espetrofotometria de absorção atómica Determinação de elementos minerais em rações para animais Miguel Mourato (Coordenador) Inês Leitão Mestrado em Engenharia
TÉCNICAS LABORATORIAIS EM QUÍMICA E BIOQUÍMICA Espetrofotometria de absorção atómica Determinação de elementos minerais em rações para animais Miguel Mourato (Coordenador) Inês Leitão Mestrado em Engenharia
Energia, calor, entalpia e variação de entalpia.
 Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Espectrofotometria UV-VIS PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA
 Espectrofotometria UV-VIS QUÍMICA ANALÍTICA V ESTAGIÁRIA A DOCÊNCIA: FERNANDA CERQUEIRA M. FERREIRA PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA 1 Conceitos Básicos Espectroscopia: É o estudo de sistemas físicos
Espectrofotometria UV-VIS QUÍMICA ANALÍTICA V ESTAGIÁRIA A DOCÊNCIA: FERNANDA CERQUEIRA M. FERREIRA PROF. DR. JÚLIO CÉSAR JOSÉ DA SILVA 1 Conceitos Básicos Espectroscopia: É o estudo de sistemas físicos
Converta os seguintes dados de transmitâncias para as respectivas absorbâncias: (a) 22,7% (b) 0,567 (c) 31,5% (d) 7,93% (e) 0,103 (f ) 58,2%
 Lista de Exercício 2ª TVC Química Analítica V Teoria (2º Sem 2017). Obs.: 1) A lista deve ser entregue antes da 2ª TVC (24/10). 2) O exercícios devem ser feitos a mão Capítulo 24 (Skoog) Introdução aos
Lista de Exercício 2ª TVC Química Analítica V Teoria (2º Sem 2017). Obs.: 1) A lista deve ser entregue antes da 2ª TVC (24/10). 2) O exercícios devem ser feitos a mão Capítulo 24 (Skoog) Introdução aos
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Disciplina: Bioquímica Clínica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
Disciplina: Bioquímica Clínica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação
Sistema Respiratório. Superior. Língua. Inferior
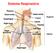 Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO
 MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO 1. Objectivo Neste trabalho, ir-se-á observar a degradação do glicogénio ao longo tempo: i) em meio ácido e à temperatura de 100ºC (degradação química); ii) em
MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO 1. Objectivo Neste trabalho, ir-se-á observar a degradação do glicogénio ao longo tempo: i) em meio ácido e à temperatura de 100ºC (degradação química); ii) em
Problemas sobre o doseamento da actividade de enzimas
 Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
QUI346 ESPECTROFOTOMETRIA
 QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO 07/10/2013 Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença
QUI346 ESPECTROFOTOMETRIA ABSORÇÃO FOTOQUÍMICA 3ª Parte (cont.) A QUANTIFICAÇÃO 07/10/2013 Mauricio X. Coutrim QUANTIFICAÇÃO: BRANCO O BRANCO NA DETERMINAÇÃO A radiação absorvida não é a simples diferença
Curso de Química e Física dos Materiais I Ciências da Arte e do Património. Espectroscopia do visível ano 2015/16
 Curso de Química e Física dos Materiais I Ciências da Arte e do Património Espectroscopia do visível ano 2015/16 Objetivos Pretende-se proceder à identificação de alguns elementos químicos a partir do
Curso de Química e Física dos Materiais I Ciências da Arte e do Património Espectroscopia do visível ano 2015/16 Objetivos Pretende-se proceder à identificação de alguns elementos químicos a partir do
Radiação de corpo negro, f.e.m. termoelétrica, dependência da resistência com a temperatura.
 1 Roteiro elaborado com base na documentação que acompanha o conjunto por: Máximo F. da Silveira Instituto de Física - UFRJ Tópicos Relacionados Radiação de corpo negro, f.e.m. termoelétrica, dependência
1 Roteiro elaborado com base na documentação que acompanha o conjunto por: Máximo F. da Silveira Instituto de Física - UFRJ Tópicos Relacionados Radiação de corpo negro, f.e.m. termoelétrica, dependência
N 2 O 4(g) 2NO 2(g) incolor castanho
 Equilíbrios Químicos Conceito de equilíbrio químico Primeira experiência N 2 O 4(g) 2NO 2(g) incolor castanho Análise microscópica N 2 O 4(g) 2NO 2(g) incolor castanho Pela reação: 1 mol de N 2 O 4 2 mols
Equilíbrios Químicos Conceito de equilíbrio químico Primeira experiência N 2 O 4(g) 2NO 2(g) incolor castanho Análise microscópica N 2 O 4(g) 2NO 2(g) incolor castanho Pela reação: 1 mol de N 2 O 4 2 mols
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN Campus Mossoró. Equilíbrio Químico. Albino O.
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN Campus Mossoró Equilíbrio Químico Albino O. Nunes SUMÁRIO OBJETIVOS; INTRODUÇÃO; DEFINIÇÃO; CONCEITOS BÁSICOS DE EQUILÍBRIO;
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN Campus Mossoró Equilíbrio Químico Albino O. Nunes SUMÁRIO OBJETIVOS; INTRODUÇÃO; DEFINIÇÃO; CONCEITOS BÁSICOS DE EQUILÍBRIO;
ESPECTROFOTOMETRIA UV-VISÍVEL. Departamento de Engenharia Química DEQUI ESCOLA DE ENGENHARIA DE LORENA EEL/USP
 ESPECTROFOTOMETRIA UV-VISÍVEL Departamento de Engenharia Química DEQUI ESCOLA DE ENGENHARIA DE LORENA EEL/USP Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação eletromagnética
ESPECTROFOTOMETRIA UV-VISÍVEL Departamento de Engenharia Química DEQUI ESCOLA DE ENGENHARIA DE LORENA EEL/USP Fundamentos da Espectrofotometria Uma maneira boa de cutucar moléculas, é com radiação eletromagnética
Espectrofotometria. centrifugação. electroforese. cromatografia. Métodos (p.ex:) radioisótopos. espectroscopia (espectrofotometria)
 Espectrofotometria Estudos de metabolismo Métodos de separação, purificação e análise Métodos de separação e análise: - procura de métodos que permitam distinguir o composto que nos interessa de outros
Espectrofotometria Estudos de metabolismo Métodos de separação, purificação e análise Métodos de separação e análise: - procura de métodos que permitam distinguir o composto que nos interessa de outros
História antiga da química de proteínas é a da Hb Hb cristalina atlas fotográfico com cristais de 109 espécies. Urease 1926.
 História antiga da química de proteínas é a da Hb. 1849 Hb cristalina. 1909 atlas fotográfico com cristais de 109 espécies. Urease 1926. Uma das primeiras proteínas a ter a massa molecular determinada,
História antiga da química de proteínas é a da Hb. 1849 Hb cristalina. 1909 atlas fotográfico com cristais de 109 espécies. Urease 1926. Uma das primeiras proteínas a ter a massa molecular determinada,
ESPECTROFLUORIMETRIA MOLECULAR (FL) Ficha técnica do equipamento Espectrofluorímetro Shimadzu RF-5301PC
 ESPECTROFLUORIMETRIA MOLECULAR (FL) Ficha técnica do equipamento Espectrofluorímetro Shimadzu RF-5301PC Fonte de excitação: Lâmpada de arco de Xe, 150 W; Seletores de comprimento de onda: Monocromadores
ESPECTROFLUORIMETRIA MOLECULAR (FL) Ficha técnica do equipamento Espectrofluorímetro Shimadzu RF-5301PC Fonte de excitação: Lâmpada de arco de Xe, 150 W; Seletores de comprimento de onda: Monocromadores
Sangue!!! TRANSPORTE DE GASES NOS FLUÍDOS CORPORAIS. O que é sangue? Qual(is) a(s) sua(s) função(ões)? 03/04/2017 PERGUNTAS INICIAIS FUNÇÕES DO SANGUE
 TRANSPORTE DE GASES NOS FLUÍDOS CORPORAIS Sangue!!! PERGUNTAS INICIAIS O que é sangue? Qual(is) a(s) sua(s) função(ões)? FUNÇÕES DO SANGUE Transporte: Nutrientes Metabólitos Gases Hormônios Calor (regulação
TRANSPORTE DE GASES NOS FLUÍDOS CORPORAIS Sangue!!! PERGUNTAS INICIAIS O que é sangue? Qual(is) a(s) sua(s) função(ões)? FUNÇÕES DO SANGUE Transporte: Nutrientes Metabólitos Gases Hormônios Calor (regulação
Ciclo Respiratório Normal. Como Respiramos? Prova de Função Pulmonar. Que diz a espirometria? Espirômetro. Sensível ao volume.
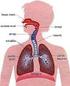 Ciclo Respiratório Normal Como Respiramos? Prova de Função Pulmonar Que diz a espirometria? Espirômetro Sensível ao volume Sensível ao fluxo 1 FEV1 / FVC % Visão Geral da Hematose O índice espirométrico
Ciclo Respiratório Normal Como Respiramos? Prova de Função Pulmonar Que diz a espirometria? Espirômetro Sensível ao volume Sensível ao fluxo 1 FEV1 / FVC % Visão Geral da Hematose O índice espirométrico
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DA ESPECTROSCOPIA MOLECULAR UV-VISÍVEL. Prof a. Dr a. Luciana Maria Saran
 FCVA/ UNESP JABOTICABAL FUNDAMENTOS DA ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
FCVA/ UNESP JABOTICABAL FUNDAMENTOS DA ESPECTROSCOPIA MOLECULAR UV-VISÍVEL Prof a. Dr a. Luciana Maria Saran 1. Introdução Espectroscopia é qualquer processo que utiliza a luz para medir as concentrações
Introdução aos métodos espectrométricos. Propriedades da radiação eletromagnética
 Introdução aos métodos espectrométricos A espectrometria compreende um grupo de métodos analíticos baseados nas propriedades dos átomos e moléculas de absorver ou emitir energia eletromagnética em uma
Introdução aos métodos espectrométricos A espectrometria compreende um grupo de métodos analíticos baseados nas propriedades dos átomos e moléculas de absorver ou emitir energia eletromagnética em uma
FUNÇÃO PROTÉICA. Bioquímica da Respiração. Transporte de O 2
 FUNÇÃO PROTÉICA Bioquímica da Respiração Transporte de O 2 1 DEFININDO CONCEITOS Ligante Ligação reversível de uma molécula à proteína. (Ex: enzima-substrato). Sítio de ligação Ligante se liga ao sítio
FUNÇÃO PROTÉICA Bioquímica da Respiração Transporte de O 2 1 DEFININDO CONCEITOS Ligante Ligação reversível de uma molécula à proteína. (Ex: enzima-substrato). Sítio de ligação Ligante se liga ao sítio
Hemoglobina. Prof. Archangelo Fernandes Profa Alessandra Barone
 Hemoglobina Prof. Archangelo Fernandes Profa Alessandra Barone www.profbio.com.br Hemoglobina (Hb) Molécula formada por quadro cadeias polipeptídicas globínicas associadas a 4 anéis porfirínicos heme.
Hemoglobina Prof. Archangelo Fernandes Profa Alessandra Barone www.profbio.com.br Hemoglobina (Hb) Molécula formada por quadro cadeias polipeptídicas globínicas associadas a 4 anéis porfirínicos heme.
Metais no Organismo Humano
 Metais no Organismo Humano Relativamente à necessidade biológica podem classificar-se Metais Essenciais: Metais Tóxicos: sódio, potássio, cálcio, magnésio, ferro, crómio, zinco, cobalto, manganês e níquel.
Metais no Organismo Humano Relativamente à necessidade biológica podem classificar-se Metais Essenciais: Metais Tóxicos: sódio, potássio, cálcio, magnésio, ferro, crómio, zinco, cobalto, manganês e níquel.
ia p sco ctro e sp E
 Espectroscopia Onda electromagnética A onda electromagnética resulta da associação de um campo eléctrico alternado com um campo magnético(em planos perpendiculares) a componente eléctrica é responsável
Espectroscopia Onda electromagnética A onda electromagnética resulta da associação de um campo eléctrico alternado com um campo magnético(em planos perpendiculares) a componente eléctrica é responsável
Espectrometria de emissão atômica
 Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE QUÍMICA PROGRAMA DE PÓS GRADUAÇÃO EM QUÍMICA
 UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE QUÍMICA PROGRAMA DE PÓS GRADUAÇÃO EM QUÍMICA SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DA UFBA 2017.2 AVALIAÇÃO ESCRITA DE QUÍMICA CÓDIGO DO CANDIDATO:
UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE QUÍMICA PROGRAMA DE PÓS GRADUAÇÃO EM QUÍMICA SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DA UFBA 2017.2 AVALIAÇÃO ESCRITA DE QUÍMICA CÓDIGO DO CANDIDATO:
PROTEÍNAS GLOBULARES E
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
Espectrofotometria Molecular UV-VIS
 Controlo Controlo da Qualidade Qualidade e Segurança e Segurança Química Alimentar dos Alimentos II Espectrofotometria Molecular UV-VIS 1 Controlo Controlo da Qualidade Qualidade e Segurança e Segurança
Controlo Controlo da Qualidade Qualidade e Segurança e Segurança Química Alimentar dos Alimentos II Espectrofotometria Molecular UV-VIS 1 Controlo Controlo da Qualidade Qualidade e Segurança e Segurança
Unidade Curricular: Física Aplicada
 FFUP Física Aplicada 206/207 Mestrado Integrado em Ciências Farmacêuticas Unidade Curricular: Física Aplicada Aulas Laboratoriais Trabalho laboratorial n.º 7 Estudo da condução elétrica: aplicação à determinação
FFUP Física Aplicada 206/207 Mestrado Integrado em Ciências Farmacêuticas Unidade Curricular: Física Aplicada Aulas Laboratoriais Trabalho laboratorial n.º 7 Estudo da condução elétrica: aplicação à determinação
Concentração de soluções e diluição
 Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
muda de marrom para azula (medida pela absorvância da luz em um comprimento de onda de 595 nm) é proporcional à concentração de proteína presente.
 ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS E APOSTILAS CITADOS ABAIXO. 1 Na determinação de uma proteína pelo método de Bradford, a cor de um corante muda de marrom para
ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS E APOSTILAS CITADOS ABAIXO. 1 Na determinação de uma proteína pelo método de Bradford, a cor de um corante muda de marrom para
Proposta de Resolução do Exame Nacional de Física e Química A 11.º ano, 2017, 2.ª Fase, versão 1
 Proposta de Resolução do Exame Nacional de Física e Química A, 2.ª Fase, 2017 Proposta de Resolução do Exame Nacional de Física e Química A 11.º ano, 2017, 2.ª Fase, versão 1 Exame Final Nacional do Ensino
Proposta de Resolução do Exame Nacional de Física e Química A, 2.ª Fase, 2017 Proposta de Resolução do Exame Nacional de Física e Química A 11.º ano, 2017, 2.ª Fase, versão 1 Exame Final Nacional do Ensino
Química Aplicada EQUILÍBRIO QUÍMICO
 Química Aplicada EQUILÍBRIO QUÍMICO Equilíbrio Químico Todas as reações tendem alcançar o equilíbrio químico Quando as velocidades das reações direta e inversa forem iguais e as concentrações dos reagentes
Química Aplicada EQUILÍBRIO QUÍMICO Equilíbrio Químico Todas as reações tendem alcançar o equilíbrio químico Quando as velocidades das reações direta e inversa forem iguais e as concentrações dos reagentes
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008. Disciplina de BIOQUÍMICA I Curso de MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Nanopartículas de Prata e. Curva de Calibração da Curcumina
 RELATÓRIODEAULAPRÁTICA Disciplina:NanotecnologiaFarmacêutica NanopartículasdePratae CurvadeCalibraçãodaCurcumina Grupo 4 Erick Nunes Garcia Fernanda Buzatto Gabriela do Amaral Gleicy Romão Manuela Pereira
RELATÓRIODEAULAPRÁTICA Disciplina:NanotecnologiaFarmacêutica NanopartículasdePratae CurvadeCalibraçãodaCurcumina Grupo 4 Erick Nunes Garcia Fernanda Buzatto Gabriela do Amaral Gleicy Romão Manuela Pereira
PROVA PARA INGRESSO NO MESTRADO. Programa de Pós Graduação em Química 14/06/2017 NOME
 PROVA PARA INGRESSO NO MESTRADO Programa de Pós Graduação em Química 14/06/2017 NOME Instruções para a prova: Coloque seu nome nesta folha antes de continuar; Marcar com um X, no quadro abaixo, as questões
PROVA PARA INGRESSO NO MESTRADO Programa de Pós Graduação em Química 14/06/2017 NOME Instruções para a prova: Coloque seu nome nesta folha antes de continuar; Marcar com um X, no quadro abaixo, as questões
Os gases respiratórios não exercem pressão parcial quando estão combinados com os pigmentos respiratórios, nem quando estão quimicamente modificados.
 A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios (movimento por fluxo). Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas.
A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios (movimento por fluxo). Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas.
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação
EFEITO FOTO-ELÉCTRICO DETERMINAÇÃO DA CONSTANTE DE PLANCK
 EFEITO FOTO-ELÉCTRICO DETERMINAÇÃO DA CONSTANTE DE PLANCK Objectivo: O objectivo desta experiência é o estudo do efeito fotoeléctrico de um metal, e a determinação da constante de Planck. Introdução :
EFEITO FOTO-ELÉCTRICO DETERMINAÇÃO DA CONSTANTE DE PLANCK Objectivo: O objectivo desta experiência é o estudo do efeito fotoeléctrico de um metal, e a determinação da constante de Planck. Introdução :
