ESTUDO TEÓRICO COMPUTACIONAL DA INTERAÇÃO DE ÁTOMOS COM FULERENOS
|
|
|
- Valentina Ramalho Fragoso
- 7 Há anos
- Visualizações:
Transcrição
1 TESE DE MESTRADO Centro Braslero de Pesqusas Físcas ESTUDO TEÓRICO COMPUTACIOAL DA ITERAÇÃO DE ÁTOMOS COM FULEREOS Octavo Danel Rodríguez Salmón Orentador: Prof. Dr. Carlton Antony Taft CBPF Ro de Janero Outubro 005
2 ABSTRACT Theoretcal sem-emprcal, ab-nto Hartree-Fock and densty functonal methods are used to study the dopng of C 60 molecules wth the atoms A = Be, B, Mg, Al, Zn, Ga, Ge, Sn, Sb for dfferent values of total charges m of the clusters [A+C 60 ] m and [A+C 60 ] m, m=-,0,. We have nvestgated the effects of cluster geometry on the nteracton energes, stablty, HOMO-LUMO, potental energy surfaces and charge dstrbuton. The reducton, odaton and poston of the dopng atom n the clusters can yeld changes of ther physcal-chemcal propertes. The potental energy barrers to penetrate or leave the C 60 tend to ncrease wth the atomc number of the dopng atom. For the regon n the vcnty of 5.5 Å from the center of the C 60 there s charge transfer between the dopng atoms and the fullerenes, reducton of the HOMO-LUMO and more stablzed total energes. Our results from computatonal smulaton suggest that through control of the HOMO-LUMO there s possblty to desgn doped clusters of fullerenes wth electrc propertes of technologcal nterest.
3 Resumo Métodos teórcos sem-empírcos, Ab-Into Hartree-Fock e Funconal da Densdade são utlzados para estudar a dopagem de moléculas C 60 como os átomos A=Be, B, Mg, Al, Zn, Ga, Ge, Sn, Sb, para dferentes valores de cargas totas m dos aglomerados [A+C 60 ] m e [A+C 60 ] m,m=-,0,. Investgamos os efetos das geometras dos aglomerados nas energas de nteração, establdades, HOMO-LUMO, dstrbução de cargas e superfíces de energa potencal. A redução, odação e posconamento do átomo dopante A nos aglomerados, pode resultar em mudanças nas propredades físco-químcas dos sstemas nvestgados. Uma barrera de energa potencal para penetrar ou sar do C 60 é observada em todas as confgurações em torno de 3.5 Å. a regão em torno de 5.5 Å do centro do C 60, observa-se transferêncas de cargas entre os átomos dopantes e os fulerenos, redução do HOMO-LUMO e energas totas mas establzadas. ossos resultados de smulação computaconal sugerem que através do controle do HOMO-LUMO há possbldade do desenho de aglomerados dopados de fulerenos com propredades elétrcas de nteresse tecnológco.
4 Agradecmentos Meus agradecmentos : Ao Prof. Dr. Carlton Antony Taft, pela orentação, colaboração e pela auda na preparação no teto da tese. À mnha esposa Jéssca, pelo estímulo e apoo moral. Ao Cásso Amador pelas correções ortogáfcas Ao Sra. Myram e Sr. Rcardo, secretáros de pós-graduação do CBPF, pelo apoo e auda em soluções dos problemas admnstratvos. À Coordenação de Aperfeçoamento de Pessoal de ível Superor CAPES, pelo apoo fnancero desse trabalho. À Vcente Atoche e Adolfo Poma, pelas dscussões centífcas. Ao únco Deus o Pa, crador do unverso
5 Índce.Introdução.... Métodos Teórcos Apromação de Born-Oppenhemer...5. O método monolelectrônco A Apromação de Hartree O Método de Hartree-Fock Equações de Hartree-Fock para camadas fechadas As equações Hartree-Fock Roothaan Hartree Fock ão Restrto....8 O Modelo de Thomas Ferm Os Teoremas de Hohenberg Kohn A Teora de Kohn-Sham Apromações Sem-empírcas Referêncas Bblográfcas Fulerenos...43 Referêncas bblográfcas Metodologas...53 Referêncas bblográfcas Resultados e dscusões...59 Referêncas bblográfcas Conclusões...8 Apêndce I...83 Apêndce II...85
6 . Introdução Há mas de.500 anos, alguns flósofos gregos se perguntavam se a mensa varedade de materas que nos cerca não pode ser reduzda a componentes mas smples. A própra palavra átomo vem daquele tempo e sgnfca "ndvsível". Entre os gregos e a nossa época, muto se aprendeu sobre o unverso. Há apenas cerca de cem anos, os centstas obtveram evdêncas fortes de que a velha hpótese atômca, formulada há mas de dos mlênos, corresponde à realdade da natureza. O problema é que átomos são muto pequenos, medem menos de um centésmo de blonésmo de metro. Anda antes dos centstas desenvolverem nstrumentos para ver e manpular átomos ndvduas, alguns poneros mas ousados se colocavam a pergunta: o que acontecera se pudéssemos construr novos materas, átomo a átomo, manpulando-os dretamente? Um desses poneros fo um dos maores físcos do século XX: Rchard Feynman. A déa de Feynman é que não precsamos acetar os materas com que a natureza nos fornece como os úncos possíves no unverso. O nteresse por materas de Carbono estmulou mutas pesqusas e trabalhos em síntese e nvestgação teórca de novas fases de Carbono. O Carbono caraterísa-se por su habldade de lgar-se com outros átomos de Carbono e com os demas elementos da Tabela Peródca, crando as mas varadas combnações através de hbrdzações dos tpos sp 3, sp e sp. O grafte e o damante são as formas bem conhecdas de carbono com propredades físcas dferentes. A recente descoberta de fulerenos mult-camadas, nanopartículas contendo outras espéces químcas, rodeadas de espéces dstntas, e dos nanotubos de carbono estmulou, especalmente em escala nanométrca, grande nteresse por materas à base de carbono. A molécula de fulereno, C 60, é deal para construr condutores orgâncos. A molécula é estável, rca em sua estrutura eletrônca e vbraconal. Os orbtas moleculares não saturados podem formar bandas
7 eletrôncas no estado sóldo. O tamanho da molécula é apromadamente esférco, deando muto espaço para outros consttuntes orgâncos e norgâncos. ão é surpresa, portanto, o ntenso esforço para estudar novos materas a partr da descoberta de síntese de volume de C 60. Os materas à base do carbono têm dversas aplcações devdo a suas propredades elétrcas, magnétcas, químcas e mecâncas. Algumas dessas aplcações são para produção de eletrodos, resstores, equpamento de solda, bateras elétrcas, combustível, produção de aço, moderador de fssão nuclear, lubrfcantes, revestmento de dscos rígdos, transstores, retfcadores, heterounções de dodo e dspostvos fotovoltacos, processo de catálse, crescmento de flmes fnos, síntese de damantes, fortalecmento de plástcos, resstênca de cerâmcas, establdade de polímeros, transporte eletrônco, supercondutvdade, nanorobótca, nanofbras e tecdos ntelgentes. Uma década após o descobrmento, o conhecmento adqurdo nesta área fulerenos e nanotubos ndca que o C 60 e seus dervados podem ser usados em mportantes aplcações centfcas consttundo uma das mas promssoras áreas de pesqusa deste mlêno. A nanotecnologa ano é um prefo que vem do grego antgo e sgnfca "anão". é um conunto de técncas, baseadas na Físca, na Químca, na Bologa, na Engenhara de Materas e na Computação, que vsam estender a capacdade humana de manpular a matéra até os lmtes do átomo. As aplcações possíves ncluem: aumentar espetacularmente a capacdade de armazenamento e processamento de dados dos computadores; crar novos mecansmos para a produção de medcamentos, mas seguros e menos preudcas ao pacente dos que os dsponíves hoe; crar materas mas leves e mas resstentes do que metas e plástcos, para prédos, automóves, avões; e muto mas novações em desenvolvmento ou que anda não foram sequer magnadas. A economa de energa, proteção ao meo ambente, menor uso de matéras prmas escassas, são possbldades muto concretas dos desenvolvmentos em nanotecnologa que
8 estão ocorrendo hoe e podem ser antevstos. Essa convergênca á está levando ao surgmento de novos processos ndustras e de novos produtos, sto é, ao surgmento de novas ndústras e de novos mercados. A nteração de átomos com C 60 e a redução, odação e dopagem de fulerenos tem ntroduzdo mportantes possbldades de aplcações centífcas e tecnológcas em comparação com outros materas. Há necessdade de estudar como as espéces nteragem com o sóldo C 60 e o C 60 lvre. Devdo às lmtações e dfculdades epermentas é de fundamental mportânca a utlzação de métodos teórcos e de smulação computaconal para a determnação de propredades com potencal de aplcação tecnológca. ossa contrbução se nsere na determnação de propredades eletrôncas, establdade, gaps de energa, transferênca de cargas, odação, redução e efetos da dopagem de fulerenos. o captulo apresentamos a metodologa dos métodos de químca quântca computaconal para estudo de moléculas e sóldos através da smulação computaconal. Dscutmos o método Hartree-Fock-Roothaan, modelos semempírcos assm como Funconal da Densdade. Estudamos a dopagem, redução e odação de confgurações de uma e duas moléculas de C 60 dopados com átomos. Foram utlzados métodos semempírcos, ab-nto e funconal da densdade funconal para estudar as confgurações em função das dstâncas dos átomos dopantes do centro dos fulerenos e as cargas totas dos aglomerados.. Analsamos através de tabelas e gráfcos b e trdmensonas as establdades, cargas e HOMO-LUMO. Tanto para o caso de uma ou duas moléculas de fulerenos observamos para todos os átomos dopantes mudanças nas establdades das dversas confgurações assm como transferênca de cargas para o C 60. As mudanças no 3
9 HOMO-LUMO destes sstemas sugerem a possbldade de desenhar materas com dversas propredades elétrcas. Cada confguração fo detalhadamente nvestgada e ao fnal analsamos e apresentamos os resultados obtdos ao longo do trabalho. 4
10 . MÉTODOS TEÓRICOS. Apromação de Born-Oppenhemer A fm de poder resolver a equação de Schrödnger para sstemas maores de que um átomo com um elétron, váras apromações necesstam ser fetas. Cada uma destas apromações contrbuem com suas própras mprecsões ao resultado fnal, que devem ser eplcadas ao relatar seus resultados. Uma das apromações mas mportantes usadas é a apromação de Born-Oppenhemer []. Esta é a prmera de dversas apromações que podem ser fetas ao tentar resolver a equação de Schrödnger para sstemas mas compleos. Ela separa o movmento nuclear do movmento dos elétrons baseado no fato de que a massa nuclear é muto maor do que a massa do elétron e que assm os núcleos podem ser consderados como partículas fas. Os elétrons reagem nstantaneamente às mudanças na posção dos núcleos. A equação abao mostra o Hamltonano completo para um sstema molecular: H = T elet nucl nucl elet elet nucl r + T R + V R, r + V r + V R. Onde T elet é a energa cnétca dos elétrons, T nucl é a energa cnétca dos núcleos, V nucl-elet é o potencal total de nteração dos núcleos com os elétrons, V elet é a energa potencal repulsva elétron-elétron, V nucl é o potencal de nteração entre os núcleos, R representa o conunto das coordenadas dos núcleos e r representa o conunto das coordenadas dos elétrons. A equação para o Hamltonano "eletrônco" um que despreza o termo cnétco da energa para os núcleos é dada por : 5
11 H elec = elet Z elet elet nucl nucl Z nz p. R r r r R + + elet nucl k< n p< n R p n Para os elétrons num campo de núcleos fos têm-se: H elet ψ elet, r R E elet ψ elet, r R =.3 E elet. Ao resolver esta equação para a função de onda eletrônca ψ elet obtém-se. O método mono-eletrônco Dentro da apromação de Born-Oppenhemer, a equação de Schrödnger ndependente do tempo para um sstema de nteração eletrônca [] é dada por : Hψ Z k ψ + ψ = r R r r = = k k Eψ.5 Uma das maneras mas comuns de tratar o problema de mutos férmons é supor que cada elétron pode ser consderado ndependente, como estvesse se movendo em um potencal médo U r, que modela os efetos de todas as outras partículas no sstema. As equações monoeletrôncas são dadas por: ψ r U r r r + ψ = ε ψ.6 onde ψ r é a função de onda monoeletrônca e ε são os multplcadores de Lagrange que surgem do fato que as funções de onda monoeletrôncas estão normalzadas. r depende das nterações entre os elétrons e U conseqüentemente das funções de onda monoeletrôncas. Já que ncalmente 6
12 U r ou ψ r não são conhecdas, é necessáro resolver a equação.6 autoconsstentemente..3 A Apromação de Hartree U r esta apromação [3-5] parte-se das equações monoeletrôncas.6. é escolhdo de modo a se tentar modelar os termos da nteração nesta equação. Os íons contrbuem com um potencal : U on Zα r = r R α α.7 Todos os elétrons restantes no sstema contrbuem também ao potencal que pode ser apromado pela nteração eletrostátca escrta em função da densdade do elétron ρ r como: U H dr r = [ ρ r ρ r ].8 r r onde o potencal da nteração com o própro elétron fo removdo. Para calcular o potencal de Hartree é necessáro saber a dstrbução eletrônca da carga do sstema. Se os elétrons forem supostos ndependentes entre s, constró-se ρ r dretamente das auto funções do elétron ρ r = ψ r.9 Onde a soma sobre nclu todos os estados ocupados. Usando esta densdade de carga, o potencal monoeletrônco é : 7
13 U r = U on r + r r r ote-se que r dr ψ.0 U depende de todos os orbtas restantes ψ e assm a r solução da eq..6 deve ser um resultado auto consstente. A escolha de na equação.0 pode ser dervada também usando o prncípo varaconal. Para usar este prncípo, começamos com a equação.5. Os elétrons são supostos ndependentes, e que as funções de onda de elétrons são o produto de funções de onda monoeletrôncas: Ψ =ψ r ψ r ψ r... ψ r. 3 3 U pode ser substtuído na eq..6 para encontrar o valor esperado de Ψ H Ψ = * r [ + U r ] ψ r dr ψ. Introduzndo um multplcador de Lagrange ε para o caso em que as funções de onda monoeletrôncas esteam normalzadas, e mnmzando a equação acma com respeto às funções de onda, tem-se que : δ H ε ψ dr = 0.3 conduz a um conunto de equações : ψ r + U on r ψ r + ψ r dr = ε ψ r.4 r r Estas são conhecdas como as equações de Hartree [6]. 8
14 .4 O método de Hartree-Fock A base do formalsmo do método de Hartree-Fock consste em apromar a função de onda total do sstema por um produto antssmetrzado de funções monoeletrôncas chamado determnante de Slater. Esta função satsfaz o prncípo de eclusão de Paul e é antssmetrzada com relação à troca de coordenadas espacas e de spn de dos elétrons [7]. O determnante de Slater para um sstema de elétrons tem a segunte forma: φ =! ψ r ψ r ψ r ψ r ψ r ψ r ψ r ψ r ψ r p ˆ = Ppψ r ψ r... ψ r! p.5 A determnante acma se aplca a sstemas de camadas fechadas orbtas duplamente ocupados. o caso de camadas parcalmente cheas ou sea, número ímpar de elétrons, a função de onda total é geralmente descrta como uma combnação lnear de funções de determnantes. é a constante de! normalzação, obtda supondo que os spn-orbtas ψ seam ortonormas; Pˆ p é um operador que permuta dos elétrons. Uma vez que a nteração magnétca spn-orbtal é desprezível em relação à nteração Coulombana, é possível escrever o spn-orbtal ψ da segunte forma: ψ = θ r ξ σ.6 9
15 onde θ r somente depende das coordenadas espacas e σ é função do spn. O método de Hartree-Fock [8] consste essencalmente em varar os spnorbtas ψ de modo a mnmzar a energa total, com a restrção de ortonormaldade dos spn-orbtas, ou sea: ξ ψ ψ ψ d d = δ < ψ >= *.7.5 Equações de Hartree-Fock para átomos de camadas fechadas Uma estrutura de camada fechada é aquela que se refere a uma função φ que é consttuída de camadas eletrôncas totalmente ocupadas. A Hamltonana para um átomo com elétrons e carga nuclear Z pode ser escrta: Hˆ = = hˆ + Lˆ pares,.8 onde hˆ Z = é um operador monoeletrônco relaconado com a energa r cnétca do elétron e o potencal entre o núcleo de carga Z e um elétron dstante r do núcleo. Lˆ = é um operador beletrônco relaconado com a energa de r repulsão Coulombana entre os elétrons e, separados por uma dstânca r. Foram fetas as seguntes apromações na Hamltonana. A prmera é que somente as nterações eletrostátcas foram consderadas; acoplamento spn-órbta, spn nuclear-spn eletrônco, etc., foram supostos mas fracos, podendo ser tratados posterormente como perturbações. A segunda é que as partículas envolvdas são consderadas como não relatvístcas. O valor esperado da Hamltonana calculada com a função φ é dado por: 0
16 = = φ φ Hˆ E > + < = =... ˆ ˆ ˆ... ˆ, p p pares p p p P L h P ψ ψ ψ ψ ψ ψ.9 Segue-se que: = = d h E * ˆ ψ ψ = < + d d r r ψ ψ.0 = < d d r r * * ' ψ ψ ψ ψ O prmero termo representa a energa méda do elétron de coordenadas no spn-orbtal ψ movendo-se no campo dos núcleos. O segundo termo é chamado ntegral Coulombana, por analoga com a nteração eletrostátca clássca, pos pode ser nterpretada como a energa potencal da nteração entre as dstrbuções de carga e ψ ψ. O últmo termo é chamado ntegral ou termo de troca, e não tem análogo clássco; seu aparecmento é provenente da natureza antssmétrca da função de onda de város elétrons, relaconada com o prncípo de eclusão de Paul. Devdo à ortogonaldade das funções de spn, este termo é dferente de zero somente quando, ψ ψ forem autofunções correspondentes ao mesmo auto-valor do operador de spn S z. Introduzndo a δ de Krönecker e assumndo que as funções espacas e de spn podem ser separadas, usando a equação.6, obtemos a segunte epressão para o termo de troca.
17 = = δ ψ ψ r ψ ψ d d * * m m S S. Usando a segunte notação: h J * = ˆ =< ˆ ψ hψ d ψ h ψ > * * = J ψ ψ ψ ψ dd r = K * * = K = ψ ψ ψ ψ dd r =< ψ ψ ψ ψ > r. Podemos escrever a energa total: = = E = h + J K δ.3 = m, m S S É convenente defnr o operador Coulombano: * ˆ ψ ψ d J ψ = ψ r =< ψ ψ > ψ.4 r e de troca ˆ ψ ψ d K =< ψ ψ > ψ r * ψ = ψ r.5 onde os operadores J, K e h são hermtanos. Usando as defnções acma, as ntegras Coulombana e de troca podem ser escrtas como:
18 3 * * ˆ ˆ d J d J J ψ ψ ψ ψ = = > < = > =< ˆ ˆ J J ψ ψ ψ ψ * * ˆ ˆ d K d K K ψ ψ ψ ψ = = > < = > =< ˆ ˆ K K ψ ψ ψ ψ.6 otamos que: J = J, K = K e J = K por defnção. Lembrando que nos átomos de camadas fechadas cada spn-orbtal ocorrerá duas vezes, um com m S = +/ e outro com m S = -/. A epressão da energa total de um sstema para elétrons é: = = + = K J h E,.7 sendo agora o número de funções espacas φ duplamente ocupados. Os elementos de matrz h, J e K podem ser calculados com estas funções espacas. Devemos agora mnmzar a energa total, e através da aplcação do prncípo varaconal encontrar o melhor conunto de orbtas } { C φ, para formar uma função φ que descreve um sstema de camadas fechadas, sueta à condção de ortonormaldade dos orbtas. β φ α φ β φ α φ β φ α φ β φ α φ β φ α φ β φ α φ β φ α φ β φ α φ φ! =.8
19 Onde a função de spn ξ σ corresponde a m S = +/ e β corresponde a m S = -/. Consderamos agora o funconal J = h + J K λ < φ φ > δ =, =,.9 onde ntroduzmos os multplcadores de Lagrange λ, para garantr a condção de ortonormaldade dos orbtas. Vamos mpor que δ J = 0 para pequenas varações δφ destes orbtas. A varação de prmera ordem de J será: δj = < δφ hˆ φ > + < φ hˆ δφ > + + < δφ ˆ ˆ > + < ˆ ˆ J K φ φ J K δφ >, + ˆ ˆ ˆ ˆ < δφ J K φ > + < φ J K δφ >,, λ < δφ φ > + λ < φ δφ >= 0.30 Onde a prmera e a segunda somatóras duplas são smétrcas nos seus índces, e consderando que que : hˆ, Jˆ ekˆ são Hermtanos pode ser mostrado [6] λ < φ δφ >= λ < δφ φ >,, *.3 Assm, temos: δ J = [ < δφ hˆ + Jˆ Kˆ φ > λ < δφ φ > ] + = 4
20 = + [ < δφ hˆ + Jˆ Kˆ φ > * + * λ < δφ φ > ] = 0.3 Para satsfazer à anulação de δ J equação.30 para uma varação arbtrára δ { φ k } deve-se obter a anulação smultânea dos dos termos do segundo membro de.3 o que mpõe a realzação smultânea das condções: [ hˆ + Jˆ Kˆ ] φ >= λ φ >.33 = = = = [ hˆ + Jˆ Kˆ ] < φ = λ < φ.34 Tomando o compleo conugado da equação.34 e subtrando da equação.33 obtemos = * λ λ φ >= 0.35 como os orbtas { φ } são lnearmente ndependentes, segue-se que: * λ = λ.36 Ou sea, os multplcadores de Lagrange são os elementos de uma matrz hermtana, portanto o conunto de equações.33 e.34 são equvalentes. Estas condções fornecem as equações conhecdas como equações de Hartree-Fock e foram propostas smultaneamente por Fock [7] e por Slater [6] e mas tarde por Roothaan [9] que as generalzou para o caso de moléculas. 5
21 As equações de Hartree-Fock equação.33 podem ser escrtas na forma matrcal,tomando a segunte forma: F ˆ[ φ ] = [ φ][ λ].37 onde F ˆ = hˆ + Jˆ Kˆ.38 = é um operador monoeletrônco, chamado operador de Hartree-Fock, e [φ] e [λ] são defndos por: φ = φ φ... ] e [ φ λ λ λ =.39 λ λ λ λ λ λ λ Para um sstema de camadas fechadas é possível elmnar os multplcadores de Lagrange não dagonas sem mudar a forma da equação.37, fazendo apenas uma transformação untára: + [ U ] [ λ ][ U ] = [ ε ].40 onde [ε] é uma matrz dagonal e U e uma matrz untára. Multplcando ambos membros da equação.37 à dreta por [U] e usando a equação.40, obtemos: ˆ ' ' F [ φ ] = [ φ] [ ε ].4 ' onde [ φ ] = [ φ][ U ] 6
22 Entretanto, o operador F é defndo em termos dos orbtas orgnas { φ } e não em termos dos orbtas transformados { φ ' }. o entanto, é possível provar que o operador F é nvarante sob a transformação untára consderada. Como H não depende dos { φ }, precsamos apenas consderar os operadores J e K. Consderando prmero o operador Coulombano: ˆ ' ' * J φ = φk U k φ U r = = k = d φ = = * φ k φ d δ kφ = = r = k, k Jˆ φ k.4 Uma operação semelhante pode ser feta para operadores de troca para obter um resultado equvalente, que nos permte escrever a segunte equação: ˆ' ˆ ' ˆ ˆ = J K J K.43 A vantagem da transformação untára é que tendo-se a matrz dagonal [ε] as equações de Hartree-Fock tomam agora a forma de equações de auto-valores, sto é: ' F φ = ε φ.44 ' ' ' As equações..44 são váldas para o caso de camadas fechadas, onde os { ε } são formalmente auto-valores do operador Hartree-Fock assocados aos orbtas { φ }. As equações.44 são resolvdas por um processo teratvo. Em cada etapa um conunto{φ é usado para calcular F, que va gerar um novo } 7
23 conunto { } + φ, até que, dentro da apromação deseada, as funções obtdas gerem o própro potencal e as funções seam auto-consstentes..6 As Equações de Hartree-Fock-Roothan O método de Hartree-Fock tornou-se muto popular, entre outras cosas, pela qualdade dos resultados produzdos ao ser aplcado em cálculo de propredades químcas e moleculares. Entretanto, hava outro problema etremamente mportante para ser soluconado: qual devera ser a forma matemátca das funções orbtas?. Enquanto que para cálculos atômcos as equações de Hartree- Fock podam ser resolvdas numercamente, para as moléculas este mesmo procedmento demonstrava ser computaconalmente nadequado. Uma solução que se tornou amplamente dfundda e que é aplcada para cálculos de propredades eletrôncas de város sstemas, fo proposto por Roothaan [9]. Roothaan sugeru que as funções que fossem usadas para representar orbtas moleculares poderam ser obtdas em termos das funções que representam os orbtas atômcos. Se consderarmos que os orbtas atômcos de sstemas multeletrôncos são funções apromadas de funções matemátcas, e que estas funções permtram cálculos computaconalmente precsos de propredades atômcas e moleculares, podera ser utlzada a mesma déa para resolver as equações de Hartree-Fock. Este método era conhecdo como o método de combnação lnear de orbtas atômcos LCAO, na sgla em nglês que sgnfca Lnear combnaton of atomc orbtals. A sugestão de Roothaan não fo a cração da LCAO, mas sm sua aplcação nas equações de hartree-fock. Em geral, pode-se dzer que os orbtas atômcos ou moleculares podem ser obtdos de forma auto-consstente como combnações lneares de determnadas funções matemátcas ou funções de base. Antes de buscar eplorar os tpos de funções de base, é convenente confrmar quas são as mplcações matemátcas nas equações de Hartree-Fock 8
24 na utlzação de LCAO. Este é um tratamento compleo e será abordado de manera superfcal através de um sstema no qual os elétrons se encontram todos emparelhados e a esta restrção se denomna em nglês Restrcted Hartree-Fock RHF e que, por conseqüênca, em cada orbtal atômco ou molecular se encontram os elétrons. Incalmente deve-se consderar que um orbtal atômco ou molecular φ pode ser descrto através da epansão lnear: M = C k k = φ χ.45 k onde C k corresponde aos coefcentes de combnação lnear que representarão os orbtas como msturas de M funções de base χ k prevamente escolhdas. Cada orbtal atômco ou molecular terá seu própro conunto de coefcentes que mostrará propredades característcas desse orbtal. Substtundo a eq..45 na equação de Hartree-Fock se obtém: Fˆ φ φ M k = M = ε Fˆ C = ε C.46 k χ k k = k χ k Os úncos parâmetros conhecdos nesta equação são as funções χ k e o operador ncal de Fock. A solução desta equação mplca determnar os valores dos coefcentes de combnação lnear de todos os coefcentes de combnação lnear de todos os orbtas ocupados e as energas respectvamente. Consderando-se que se tem um conunto de M funções do tpo χ, se nca o processo de solução multplcando-se a equação anteror por cada uma das funções χ e se ntegra sobre todo o espaço de varáves. Isto crará um conunto k de M equações do tpo: k χl M χ χl M χ Fˆ C dτ = ε C dτ.47 k = k k k = k k 9
25 M k = C Esta equação pode ser epressa como: χ χ χ χ k l k k l k M Fˆ dτ = ε C dτ.48 k = Empregando uma notação smplfcada para as ntegras: M M Ck f lk = k = k = Onde χl k S ε C.49 lk S = χ dτ.50 lk k é um elemento de matrz chamada matrz de sobreposção. E f = Fˆ χ dτ.5 lk χ l k A equação.49 é ordenada da segunte forma: f S Ck lk ε lk = 0.5 Uma solução trval, mas não deseada para esta equação, sera consderar que todos os coefcentes de combnação lnear fossem guas a zero. Isto satsfaz a eq..5, mas não proporcona nenhum resultado de nteresse físco. Esta equação pode ser representada em uma forma matrcal como: f f f M ε S ε S : : k k ε S k M f f f M ε S ε S : : k k ε S k M f f f M M MM ε S ε S : : k k ε S k M M MM c c : : c k k Mk = 0.53 A equação.5 pode ser escrta também de um modo computaconalmente mas convenente, como: 0
26 ˆ f. C = ε Sˆ. C.54 ou, se todas as equações de todos os orbtas moleculares fossem agrupados em uma únca equação, se tem: ˆ. = ε...55 f Cˆ Sˆ Cˆ Esta equação apresenta característcas que permtem a aplcação de técncas numércas efcentes para determnar os coefcentes de combnação lnear e as energas dos orbtas moleculares. Esta equação é denomnada de equação secular. Para obter soluções não trvas se deve cumprr que det ˆ ˆ = 0 f ε. S.56: Um aspecto de suma mportânca corresponde às possíves soluções obtdas através da equação.55. Como pode ser observado, as dmensões das matrzes representadas pela equação.55 são de ordem M M, o que corresponde a obter um número de soluções orbtas e energas de orbtas maor do que o necessáro. O número de orbtas duplamente ocupados, n, é sempre menor, ou, em raras ocasões, gual, ao número de funções de base M. A escolha das soluções deseadas se faz através dos orbtas que apresentam menor energa. Isto se faz, através da solução da equação.55, ao se obter m dferentes orbtas moleculares. Os orbtas se organzam em ordem crescente de energa e se escolhem os n orbtas de menor energa. Através da especfcação dos orbtas ocupados pode-se determnar a energa eletrônca total do sstema e também o valor de qualquer outra propredade de nteresse. Os orbtas desocupados ou vrtuas e as respectvas energas obtdas através da solução da equação.54 não são caracterzados corretamente. A
27 defnção de operador de Fock leva em conta a dstrbução eletrônca e por consegunte todos os orbtas ocupados. Mas precsamente, a nteração de cada um dos elétrons em um determnado orbtal em relação ao campo médo de todos os outros orbtas ocupados. Desta manera, os orbtas vrtuas são obtdos epermentando-se a nteração de um elétron nesse orbtal com todos os orbtas ocupados. Consequentemente, os orbtas vrtuas apresentam uma característca mas próma dos orbtas de um íon negatvo em um estado ectado, que de um sstema neutro. Os elementos da matrz fˆ são representados eplctamente da segunte forma: f = lk χ Fˆ χ dτ = h + P kl k l.57 l k lk onde P = CuCu.58 u é um elemento da matrz defnda como matrz densdade. A notação ab cd é usada para representar as ntegras do tpo: ab cd = χa χb χc χd dτdτ.59 r r.7 Hartree-Fock ão Restrngdo UHF as seções anterores estudamos o método de Hartree-Fock restrngdo a camadas cerradas, denomnado Hartree-Fock Restrngdo Restrcted Hartree Fock, ou RHF, em nglês. Ou sea, estudamos sstemas com átomos cuos
28 elétrons têm número par e no estado fundamental os orbtas são restrngdos a estar duplamente ocupados com spns antparalelos. Chamamos elétrons α aos elétrons cuo autovalor do operador Ŝ z é ½ e β para -½. Apresentamos uma lustração desta stuação na segunte forma: Orbtal 4 Orbtal 3 Orbtal Orbtal Tal como mostra a lustração anteror, os orbtas espacas estão duplamente ocupados. Devdo ao prncípo de eclusão de Paul o mesmo orbtal espacal não podera conter dos elétrons com spns paralelos. Para que os elétrons ocupem o mesmo orbtal espacal devem se dferencar em sua proeção de spn. Entretanto, quando o número total de elétrons é ímpar camadas abertas, pensar em orbtas duplamente ocupados não sera convenente. Como eemplo dsto temos o átomo de Líto L, que tem três elétrons []. Poderíamos pensar que no estado fundamental dos elétrons estão ocupando o mesmo orbtal espacal de energa mas baa s e o tercero estara desemparelhado no orbtal segunte s. Para tanto a função de onda eletrônca do sstema sera: ˆ Ψ = A φ s α, φs β, φs 3 α3.60 Onde o operador  é um operador antssmetrzador. esta confguração o elétron α no orbtal s tem uma nteração de ntercâmbo K s,s com o elétron α na s. O elétron β tem uma nteração de ntercâmbo nula com ambos elétrons devdo a que somente este nteração de 3
29 ntercâmbo de elétrons com spns paralelos. Para tanto não sera aproprado consderar que o elétron β tenha a mesma função espacal que o elétron α em s. Então deveríamos consderar o elétron β com uma função espacal dferente ou lgeramente dferente, chamada φ. Desta manera a função de onda no estado s' fundamental sera: ˆ Ψ = A φ s α, φs ' β, φs 3 α3.6 Isto podera ser lustrado como se segue: s s s L Para sstemas com número de elétrons ímpar o método de Hartree-Fock não restrto fo consderado pela prmera vez por J.A. Pople e R.K. esbet [0]. Para aplcar o método de Hartree-Fock a radcas ou a estados ectado representados por um únco determnante de Slater eles procederam da segunte manera. Se α α consdera um sstema com M elétrons α com orbtas ortonormas φ... φm e β β elétrons β com orbtas espacas ortonormas φ... φ. ão há nenhuma razão a pror de que alguns de seus orbtas seam dêntcos a outros. A função de onda do sstema antssmetrzada é: Ψ = α α β β { φ α... φ α M φ M + β M +... φ M + M + } p Pˆ M β > M +! p 4
30 .6 A energa eletrônca correspondente é: α+ β α+ βα + β α α β β = h + J + E K.63 onde os termos h, J e K estão defndos na.6. Se agora escrevemos os orbtas moleculares φ como uma combnação lnear de orbtas atômcos χ r : φ = Crχr.64 r Então os coefcentes C r são determnados autoconsstentemente por aplcar o prncípo varaconal na.7. Se demonstra que estes coefcentes satsfazem as equações escrtas na forma matrcal: α α α α β β β β F ˆ. C = ε Sˆ. C, Fˆ. C = ε Sˆ. C.65 Onde α β C, C são vetores coluna especfcando os coefcentes dos orbtas α φ e β φ e respectvamente. As matrzes α Fˆ e β Fˆ são. α α β β Fˆ = hˆ + Jˆ Kˆ ; Fˆ = hˆ + Jˆ Kˆ.66 e os elementos rs de S, h, J e K α são: Sˆ rs = χr χsdτ.67 5
31 hˆ = χ hˆ rs r χsdτ.68 α β Jˆ rs = Ptu + Ptu χr χt χs χu dτdτ.69 r t, u Kˆ α α rs = Ptu χr χt χu χs dτdτ r t.70 α β α β P tu = CtCu, Ptu = CtCu,.7 Consderar os elétrons α e β em dferentes orbtas espacas para camadas abertas melhora os cálculos da nteração hperfna []. A desvantagem é a contamnação de spn []. A contamnação de spn sgnfca que a função de onda eletrônca não é autofunção do operador Ŝ. Isto ocorre por se lmtar a função de onda a somente um determnante de Slater, sto sendo necessáro para smplfcação dos cálculos..8 O Modelo de Thomas Ferm A teora de Thomas-Ferm [3-4] marca uma mudança na apromação de Hartree e Hartree-Fock. Este fo o prmero método proposto usando a densdade eletrônca como varável fundamental em lugar da função de onda. este modelo a energa total no estado fundamental é um funconal da densdade eletrônca ρ r, composta de três termos: 6
32 E TF ρ r ρ r' [ ρ r] = T[ ρ r] + ρ r Vet r dτ + dτdτ ' r r'.7 O prmero termo é a energa cnétca de um gás homogêneo de elétrons que não nteragem entre s e é obtdo por ntegração da densdade de energa cnétca de um gás homogêneo de elétrons t0[ ρ r], ou sea T [ ρ r] = t0 [ ρ r] dτ. Para determnar eplctamente t [ ρ ] calculamos a méda da energa cnétca 0 r k do elétron lvre consderando, m = no estado fundamental tomando em = e conta que a dstrbução de Ferm é constante neste caso: k F k 3 t0 [ρ r] = D k d k.73 0 sendo τ D k = k a densdade de estados e τ o volume que ocupa o elétron, π de onde tramos que = 3π ρ r 3. Integrando temos a segunte epressão k F para a densdade de energa cnétca: t [ r] 3π ρ r ρ =.74 0 Para tanto o funconal de energa cnétca fca epresso como T[ ρ r] = CTF ρ r dτ onde C = 3π 3 TF. 0 O segundo termo da equação.7 é a energa potencal eletrostátca de atração devdo aos núcleos, sendo V et o potencal de Coulomb que tem a segunte forma: 7
33 V et Z r =.75 m = r R Fnalmente o tercero termo representa a nteração entre os elétrons, apromada pela repulsão clássca de Coulomb entre os elétrons. É conhecdo como energa de Hartree. Para obter a densdade do estado fundamental é necessáro mnmzar a energa dada em.7, sueta à restrção que mplca a conservação do número total de partículas. Matematcamente sto é epresso como: δ { E TF [ ρ r] µ ρ r dτ } = 0.76 onde µ é o parâmetro de Lagrange correspondente. Isto nos conduz à segunte equação: 3 5 ρ r' CTF ρ r + Vet r + ' = 0 3 dτ µ.77 r r' Chamando = ρ r' ν nt r dτ r r' ' ao potencal devdo aos elétrons, então a equação de Posson correspondente é ν r = 4πρ r..78 nt Substtundo na equação.77 temos a equação de Thomas-Ferm: 7 3 ν nt r = [ µ Vet r ν nt r].79 3π 8
34 Este modelo não pode predzer enlaces entre átomos devdo a que a energa que resulta dos átomos solados é menor que a da molécula composta pelos mesmos. A densdade eletrônca não é fnta na orgem do núcleo r - >0, sendo que tem uma assíntota, e para r-> não deca eponencalmente, mas sm como r -6. Ao aumentar o número atômco Z, o átomo se encolhe como Z -/3. estas defcêncas são devdas a que neste modelo não se consdera a correlação que este entre os elétrons, o qual mplca ntroduzr correções aos termos da energa total [5]. Pouco depos da ntrodução do método de Thomas-Ferm, Drac desenvolveu uma apromação para a nteração de ntercâmbo entre os elétrons de um gás homogêneo. A epressão que resulta é smples e é uma funconal local da densdade: 4 E X [ ρ r] = ρ r dτ.80 4 π função ρ se Matematcamente uma função F se defne como funconal local de uma 3 F[ ρ ] = f ρ r d r, onde f é uma função de ρ. A relação.80 é usualmente escrta em termos da densdade de energa de troca: LDA E X [ ρ r] = ρ r ε X [ ρ r ] dτ.8 sendo: ε X [ ρ r] = ρ r.8 4 π A abrevação LDA sgnfca Apromação de Densdade Local, em nglês Local Densty Apromaton. 9
35 O termo de troca de Drac fo ncorporado à teora de Thomas-Ferm por meo de ntroduzr.8 em.79, o qual conduz ao modelo chamado de Thomas-Ferm-Drac. Este modelo não representa um progresso sgnfcatvo por motvo do termo de energa cnétca que é aplcável somente para um gás homogêneo de elétrons lvres [5]. Antes de contnuar com os modelos que melhoram a apromação dos termos da energa total como função da densdade, vamos tratar com os teoremas de Hohenberg-Kohn [6] que demonstram formalmente que a energa do estado fundamental de um sstema de elétrons é uma função da densdade eletrônca..9 Os Teoremas de Hohenberg e Kohn Este teorema não dz que a energa de um sstema de elétrons é uma funconal de sua densdade eletrônca. Em prmero lugar veremos que se temos dos estados não degenerados de dos sstemas de elétrons cuos potencas eternos dferem em mas de uma constante, seus funconas devem ser dstntas. Temos um conunto de elétrons descrto por um operador Hamltonano Ĥ, com um potencal eterno V et r e outro sstema com o mesmo número de elétrons descrto por outro operador Hamltonano Ĥ ' cuo potencal eterno ' V et r dfere de V et r em mas de uma constante, ou sea, Hˆ ' ' ' Hˆ = [ V r V r ] cte.83 = et et 30
36 Seam Ψ 0 e ' Ψ 0, respectvamente, os funconas que descrevem os estados fundamentas de Ĥ e Ĥ '. O prncípo varaconal mplca que, para qualquer função de onda Ψ, vale: Ψ H ˆ Ψ > < Ψ Hˆ Ψ > = E.84 < 0 0 < Ψ H ˆ ' Ψ > < Ψ' Hˆ ' Ψ' > = ' E onde E e E são, respectvamente, as energas dos estados fundamentas de Ĥ e Ĥ '. Ao serem não degenerados, as gualdades só valem quando Ψ = Ψ0, e se ' Ψ = Ψ 0 na prmera e segunda desgualdade respectvamente. Schrödnger As funções de onda Ψ 0 e ' Ψ 0 cumprem suas respectvas equações de H ˆΨ = EΨ H ˆ ' Ψ Ψ.87 ' 0 = E' ' 0 Ψ 0 e onde se deduzra que ' Ψ 0 não podem ser guas, porque se fossem sera cumprdo que, de ' ' ' [ Vet r Vet r ]} Ψ0 = E' Ψ0 + { = = ' EΨ = Hˆ ' ' 0 Ψ0 = { Hˆ ' + [ Vet r Vet r ]}.88 e que 3
37 = ' et [ V r V r ] = E E'.89 et Contraramente a nossa suposção ncal, os potencas eternos dferram somente em uma constante. O fato de que Ψ 0 e Ψ 0 ' seam necessaramente dstntas nos permte escrever as segunte desgualdades estrtas estrtas no sentdo que a gualdade nunca pode acontecer. ' ' E < < Ψ Hˆ Ψ > E ' < Ψ Hˆ ' Ψ >.9 < 0 0 Cabe perguntar agora se suas respectvas densdades eletrôncas podem ser guas. A resposta é negatva e é dada pelo prmero Teorema de Hohenberg- Kohn. A demonstração segue a segur. Em prmero lugar substtuímos o operador Ĥ na desgualdade.90 por H ˆ ' ' [ V r V r ] e Ĥ ' o operador na desgualdade.9 por = = et et H ˆ ' + [ V r V r ]. et et E << Ψ ' Hˆ ' ' ' ' ' 0 Ψ0 >=< Ψ0 Hˆ ' Ψ0 > < Ψ0 [ Vet r Vet r ] = Ψ >.9 ' 0 ' 0 Hˆ ' Ψ0 >=< Ψ0 Hˆ Ψ0 > < Ψ0 [ Vet r Vet r ] = E' << Ψ Ψ >
38 Agora substtuímos a equação para o valor médo operador potencal eterno em ambas desgualdades E ' ' [ V r < E V r] ρ' r dτ et et.94 E' ' et et < E [ V r V r] ρ r dτ.95 Fnalmente, procedemos pela redução ao absurdo, supondo que as duas densdades são guas ρ = ρ, e somamos as duas desgualdades anterores, com o qual obtemos: E + E' < E + E'.96 o qual é uma contradção. Para tanto, salvo uma constante adtva, o potencal eterno fca determnado pela densdade eletrônca do estado fundamental. Isto mplca que não pode haver dos sstemas no estado fundamental. Aqu o termo dferente sgnfca que dfere em mas de uma constante. A forma habtual de epressar o anteror é dzer que para estados fundamentas, a energa é um funconal da densdade eletrônca E E[ ρ ] =< Ψ Hˆ Ψ >.97 = 0 0 A segur defnmos o funconal da densdade F [ρ] como a soma da energa cnétca e de repulsão beletrônca do estado fundamental de um sstema com densdade ρ, ou sea, F[ ρ] = E[ ρ] Vet r ρ r dτ.98 33
39 O prncípo varaconal da função de onda do estado fundamental nos dz que, para o estado fundamental cumpre que: ' Ψ 0 de qualquer sstema com Hamltonano Ĥ ', se ' ' < Ψ0 H ˆ Ψ0 > < Ψ ˆ 0 H Ψ0 >.99 A gualdade se cumpre uncamente quando Ψ 0 = Ψ0, ou sea, quando H ˆ ' = Hˆ. Agora podemos substtur o operador H por H ' [ V o que obtemos: ' = ' et r V et r ], com ' < Ψ ˆ ' ' ' Ψ > [ ] ' < Ψ ˆ 0 H 0 Vet r Vet r ρ r dτ 0 H Ψ0 >,.00 e, recordando que a energa é um funconal da densdade, temos ' E[ ρ'] [ Vet r Vet r] ρ' r dτ E[ ρ].0 Fnalmente, utlzando a defnção F [ρ], obtemos: F[ ρ'] = Vet r ρ' r dτ E[ ρ].0 esta desgualdade é conhecda como o segundo teorema de Hohenberg-Kohn e estabelece que o mínmo do funconal F[ ρ] + Vet r ρ r dτ se obtém quando ρ é a densdade do estado fundamental assocada ao potencal eterno. 34
40 Os teoremas de Hohenberg-Kohn só garantem que a energa do estado fundamental é um funconal da densdade eletrônca, mas não podem determnar a forma eplícta de sua dependênca com respeto à densdade. Como á fo menconado, o modelo de Thomas-Ferm-Drac tem como prncpal problema a apromação do termo de energa cnétca, que não consdera a não homogenedade do sstema e a correção eletrônca..0 A Teora de Kohn-Sham Obter uma epressão para a energa cnétca em função da densdade é um problema complcado. A apromação de densdade local de Thomas-Ferm não é satsfatóra. A solução proposta por Kohn e Sham [7] para atacar o problema é transladar o sstema dos elétrons para um de partículas que não nteragem e que estão suetas a um potencal efetvo ν eff, onde os termos de nteração podem ser ncluídos neste. A densdade eletrônca neste sstema de referênca pode ser epressa por meo dos funconas de onda de cada spn-orbtal ρ r = ψ.03 = r E a energa cnétca por T = ψ ψ dτ.04 Como conseqüênca dos teoremas de Hohenberg-Kohn podemos epressar cada um dos termos da energa eletrônca total como função da densdade. E [ ρ] = T[ ρ] + E [ ρ] + E [ ρ] + E [ ρ].05 et coulomb XC 35
41 O prmero termo é a funconal de energa cnétca, o segundo é o termo correspondente à energa devda ao potencal eterno que é da forma V et r ρ r dτ, o tercero é a energa de nteração Coulombana que é ρ r ρ r' dτdτ '. O quarto termo é a energa devda à nteração de troca e a da r r' correlação eletrônca. Em vrtude do segundo teorema de Hohenberg-Kohn, a energa total é mnmzada pela densdade eletrônca do estado fundamental, então o prncípo varaconal pode ser utlzado. A energa total dada em.05 pode ser mnmzada, sueta à restrção de ortonormaldade dos spns-orbtas. Epressando sto matematcamente, temos δ [ ] * E ρ ε ψ δψ = dτ = 0,=.06 onde ε são os multplcadores de Lagrange correspondentes. A mnmzação.06 nos conduz às equações de Kohn-Sham para cada spn-orbtal: + ν eff r ψ r = εψ r.07 onde ν eff ρ r' r = Vet r + dτ ' + ν XC r.08 r r' O potencal ν é devdo à energa de troca e correlação e se epressa como XC 36
42 ν =.09 ρ XC E XC Para consegur uma melhora na precsão dos cálculos em obter uma parametrzação de E XC em função da densdade, que pode descrever o melhor possível a nteração de troca e a correlação do sstema. Os autovalores ε carecem de sgnfcado físco e sua nterpretação é todava matéra de debate. É mportante menconar que a energa total eletrônca não é a soma dos autovalores obtdos em.07. A epressão para a energa total é dada por E total ρ r ρ r' [ ρ ] = ε dτdτ ' + EXC[ ρ] Vet r ' ρ r' dτ '.0 r r' = A equação.07 se resolve autoconsstentemente por meo de ntroduzr uma densdade ncal. O segunte dagrama de fluo mostra como se chega à autoconsstênca. 37
43 Fgura. Cclo de autoconsstênca. A energa de troca e correlação pode ser dvdda separando a parte que corresponde ao ntercâmbo e à correlação: E [ ρ] = E [ ρ] + E [ ρ]. XC X C Uma apromação local para E X fo obtda por Drac, mostrada na relação.80. Devdo a que na medante apromação de hartree-fock se obtém eatamente a nteração de troca, podemos obter eatamente a energa de correlação E C medante o conhecdo por métodos epermentas da energa total do sstema de elétrons. Isto é E C total eacta total HF = E E. onde total E HF é a energa total obtda pelo método de Hartree-Fock. 38
44 Geralmente a dependênca do térmno de troca e correlação E XC não só depende da densdade eletrônca ρ, sno também do gradente ρ. Só para gases homogêneos este uma dependênca local de ρ. Lee, Yang e Parr [8], fzeram austes da energa de correlação com termos locales e não locales. Esta apromação se chama LYP. Este uma funconal híbrda que mstura termos de ntercambo de Hartree-Fock, termos de ntercambo parametrzados por Becke e agrega os fetos por LYP, resultando em uma parametrzação chamada B3LYP [9]. Esta funconal melhora os austes de LYP.. Apromações Sem-empírcas Cálculos de Hartree-Fock-Roothaan requerem muto tempo computaconal além das dfculdades assocadas ao cálculo das ntegras pq rs. os métodos sem-empírcos todo o formalsmo autoconsstente da teora de orbtas moleculares usando a epansão no orbtas atômcos é mantdo, e procura-se resolver as dfculdades nerentes no método com a ntrodução de parâmetros. A apromação ZDO Zero Dfferental Overlap [0] consste em mpor que χ p r χ r d µ 0, para p q, o qual mplca S pq µ = χ p rµ χ q rµ dϑ = δ pq e a equação de Hartree-Fock- Roothaan tornase : µ q µ ϑ FpqCq = ε C p.3 q A apromação de ZDO apresenta o nconvenente de não ser nvarante para uma rotação do sstema de coordenadas. Para resolver este problema fo ntroduzdo o método CDO Complete dfferental overlap [0], no qual as ntegras de dos elétrons são substtuídos por parâmetros γ AB que dependem 39
45 da natureza dos átomos A e B e da dstânca nternuclear. Quando os orbtas atômcos estão no mesmo átomo, o parâmetro é γ AA representa a repulsão méda elétron-elétron no átomo A. Também fo ntroduzdo um parâmetro V AB para nterações elétron-caroço, assm como parâmetros de lgação, e o ntegral de ressonânca β AB responsável pelo abaamento da energa devdo ao compartlhamento de elétrons no campo eletrostátco de dos átomos. O método DO eglect of datomc dfferental Overlap [] é uma varante do método CDO com uma forma menos apromada, neste método a dferencal de sobreposção às ntegras de dos elétrons é elmnada somente para orbtas atômcos centrados em dferentes átomos. o método IDO, µ µ dϑ χ µ χ envolvendo dferentes orbtas atômcos são consderados q r apenas para as ntegras de um centro. a apromação MDO modfed neglect of datomc orbtal as contrbuções de elétrons dos mesmos átomos são obtdas de valores epermentas dos átomos solados. As ntegras de dos centros são consderadas como parâmetros austáves do método calculados para as moléculas cua geometra, calor de formação, potencal de onzação e momento dpolar são epermentalmente conhecdos. O método AM Austn model fo desenhado para elmnar os problemas do MDO, que tenda a sobreestmar as repulsões entre átomos separados por dstâncas apromadamente guas à soma do rao de Van der Waals. O PM3 está também baseado no MDO o nome derva do fato de ser a tercera parametrzação de MDO. O Hamltonano contêm essencalmente os mesmos elementos que AM, mas os parâmetros para o modelo PM3 foram dervados usando procedmento de parametrzação automátca. Referêncas M. Born and R. Oppenhemer. Zur Quantentheore der Molekeln. 40
46 Ann. Phys.Lepzg 840, Aschcroft and. Mermn.Sold State Physcs.Holt-Saunders, D.R. Hartree,Proc. Cam.Phl.Soc D.R. Hartree, Proc. Cam. Phl. Soc D.R. Hartree, Proc. Cam. Phl. Soc D.R. Hartree, the Calculaton of Atomc Structure, John Wley & Sons, ew York V. Fock, Z. Physk, 6,6930 8J. C. Slater. ote on Hartree s method. Phys. Rev. 05,.p C.C.J. Roothaan, Rev. Mod. Phys., 3, J. A. Pople, R. K. esbet, J. Chem. Phys G. W. Pratt, Jr. Phys. Rev. 0, R. K. esbet. 8, Thomas,L.H. the calculaton of atomc felds. Proc. Cam. Phl. Soc. 3, p , E. A. Ferm, Statstcal method for the determnaton of some atomc propertes and the applcaton of ths method to the theory of the perodc 48, p.73-79, 98. 4
47 5 S. Lundqvst,. H. March, Theory of the nhomogeneus electron gas, Physcs of Solds and Lquds. ew York, Plenum, p. 6 P. Honenberg, W. Kohn, Inhomogeneus electron gas, Phys. Rev., 36, p.b864, W. Kohn and L.J. Sham, Phys. Rev., 40, A C. Lee, W. Yang, and R. G. Parr, Phys. Rev. B 37, A. D. Becke, J. Chem. Phys. 98, R. G. Parr. A method for estmatng electronc repulson ntegrals over LCAO mos n comple unsaturated. J. Chem. Phys, 0,p ,95. J. A. Pople, Appromate self-consstent molecular-orbtal theory. 6. IDO calculated equlbrum geometres. J. Chem. Phys., 43, p.9-3, 95. 4
48 3. Fulerenos Em 996 fo outorgado a H. W. Kroto, R. F.Curl e R. E. Smalley o prêmo obel de químca pela descoberta dos fulerenos. Eles relataram a descoberta de mas uma forma alotrópca de carbono: o buckmnsterfulereno C 60, uma molécula em forma de bola de futebol. Graftes classfcados en duas formas, α e β e damante são duas das formas alotrópcas bem conhecdas do carbono, das quas a grafte α heagonal é a mas estável a temperaturas e pressões normas. Essas formas alotrópcas dferem no ambente de coordenação dos átomos de carbono ou na seqüênca de empacotamento de camadas na rede crstalna e determnam mportantes dferenças nas propredades físcas e químcas. As graftes α e β, ambas formadas por redes heagonas planares de átomos de carbono dferem somente no arrano das camadas. o damante cada átomo está rodeado tetraedrcamente por quatro vznhos eqüdstantes, resultando em uma célula untára cúbca. A lonsdaleta é uma forma muto rara de damante heagonal, nela apesar de cada carbono ser tetraédrco o arrano dos tetraedros é tal que a estrutura é heagonal em vez de cúbca. Os fulerenos são formados quando carbono vaporzado se condensa em uma atmosfera de gás nerte Hélo; a vaporzação de carbono pode ser feto com lasers ou com arcos voltacos usando eletrodos de grafte. Os átomos de carbono vaporzados são msturados ao Hélo que se combnam para formar agregados moleculares que podem reunr alguns poucos átomos ou até centenas deles.os Fulerenos são alótropos moleculares de carbono estndo numa enorme gama. O numero de átomos de carbono de uma molécula fulerênca pode varar de 60 a mlhares, formando heágonos e eatamente pentágonos. A medda que o número de heágonos fca maor que 0 caso do C 60, a establdade da molécula 43
49 dmnu, pos os pentágonos ocupam posções cada vez com mas tensão e portanto mas suscetíves a ataques químcos. Embora sea um poledro de 0 faces heagonas e pentagonas, o C 60 pode ser vsualzado como consttuído de pentágonos gualmente dstrbuídos pela superfíce de uma esfera, cada um conectado a seus cnco vznhos por uma lgação-ponte. Essas pontes geram os 0 heágonos.um modelo de molécula de C 60 poder ser faclmente construído a partr de papel marcado heagonalmente, e com buracos apropradamente dstrbuídos. À medda que os heágonos forem sendo sobrepostos a estrutura poledral do C 60, uma bola de futebol surge naturalmente. Os fulerenos dssolvdos em solventes aproprados, formam soluções colordas C 60, magenta; C 70, vnho; C 76, amarelo/verde. O C 60 tem propredades eletroquímcas nteressantes, permtndo a transferênca reversível de elétrons. As moléculas quase esfércas de C 60 empacotam-se num arrano compacto do tpo cúbco. Esse arrano tem lacunas tetraédrcas e octaédrcas entre as moléculas, nas quas átomos e moléculas pequenas podem se ntercalar. Epermentos a pressões altíssmas levaram à formação de damante. Em atmosfera de gás nerte pode-se obter C 60 crstalna, com moléculas equvalentes nos sítos. Os centros das moléculas de C 60 fazem uma rede de FCC Face Centrada Cúbca com uma dstânca de vznhos mas prómos C 60 -C 60 que corresponde ao dâmetro da molécula. À temperatura ambente o tamanho da cela untára é de 4.7 Å e o vznho mas prómo é de 0.0 Å. Os anotubos são fulerenos com outra estrutura. Em meados de 99, no laboratóro de pesqusas báscas da EC, no Japão, o crstalógrafo S.Ima fez uma pequena, mas crucal modfcação no método de síntese; em vez de dear que os eletrodos de grafte entrassem em contato, deou-os separados enquanto descargas elétrcas fascavam entre eles. Houve a formação de um depósto sobre o eletrodo negatvo catodo. A análse desse depósto ao mcroscópo 44
50 eletrônco revelou a estênca do que hoe se denomna nanotubos: tubos clíndrcos de dâmetros nanométrcos, empacotados um dentro do outro, com as etremdades fechadas por hemsféros fulerêncos. Cada tubo habtualmente consste de 0 a 0 camadas de átomos de carbono, seu dâmetro eterno vara de 8 nm a 5 nm e o seu comprmento de dezenas de nanômetros até dversos mcrometros. Mutas propredades de C 60 têm sdo nvestgadas epermental e teorcamente, como a estrutura eletrônca, estados vbraconas, reatvdade químca com átomos e moléculas. Epermentos de colsão de altas energas podem nserr átomos na estrutura dos fulerenos. C 60 contendo metas também podem ser obtdos pelo laser e vaporzação de compostos metal-grafte numa atmosfera de gás nerte. Há dferentes possbldades de dopagem,.e. dopagem endohedral onde o dopante está dentro do fulereno dopante subttuconal, onde o dopante esta ncluído na camada do fulereno e dopagem heoedral onde o dopante está fora ou entre os fulerenos. O C 60 puro forma crstas moleculares dspostos na forma FCC Face Centrada Cúbca lgadas por forças van der Waals..C 60 pode formar compostos do tpo M C 60, com város metas alcalnos doadores de elétrons.. A maor parte das pesqusas dos sóldos baseados nos fulerenos foram fetas no C 60. esta molécula o núcleo do carbono esta em uma esfera de rao de apromadamente 7.0 Å de dâmetro cua função de onda eletrônca se estende para dentro e para fora em torno de.5 Å. O dâmetro da molécula é de apromadamente 0 Å, e possu uma cavdade nterna de apromadamente 4.0 Å de dâmetro Ver fgura 3.. Os átomos estão posconados nos 60 vértces de um cosaedro truncado com pentágonos e 0 heágonos.as duas dferentes dstâncas C-C no C e.46 Å ndcam que os elétrons π não estão deslocados unformemente sobre todas as lgações. Para comparação a lgação sp 3 no damante é de apromadamente.35 Å. As 30 lgações curtas estão nos 45
51 bordes compartlhadas pelos heágonos, a dstânca das lgações nas bordas compartlhadas pelo heágono e pelo pentágono são mas longos. O C 60 tem 40 elétrons de valênca, mas cada átomo de carbono têm três lgações sgma com os vznhos, usando um total de 80 elétrons para este propósto. A energa destes elétrons está embao da superfíce de Ferm, establzam a estrutura mas não contrbuem para a condução. Os 60 elétrons restantes estão dstrbuídos em torno da molécula em orbtas que se orgnam dos orbtas carbono-carbono menos lgado. Esses orbtas são smlares aos elétrons π do plano de grafene com duas dferenças mportantes. Prmero as três lgações em torno do átomo de carbono no C 60 ou qualquer outro fulereno não fazem um plano. Enquanto no grafene os elétrons tem probabldades guas de estarem embao ou acma dos planos, nos fulerenos os elétrons π tendem a passar mas tempo fora da bola que dentro. Em segundo lugar, no C 60 as lgações C-C não são unformes, os elétrons π não são verdaderamente deslocados em torno dos anés de ses membros mas dstrbuídos sobre 30 orbtas eletrôncos que se estendem para fora da molécula de C 60. Uma densdade eletrônca mas baa pertence aos outros 60 orbtas conectando pares de carbonos com maores lgações. A sobreposção entre estes orbtas em moléculas adacentes determnará as propredades da banda de condução eletrônca dos sóldos dopados. Sóldos formados com fulerenos em combnação com outros elementos tem resultado em materas com mportantes propredades tecnológcas como condutvdade e supercondutvdade em C 60 dopado com metas alcalnos. o prncpo da década de noventa os prmeros dopantes alcalnos que mostraram superconductvdade são o potásso [7] e o rubído [8]. O prmero com uma temperatura crítca de 8 K e o rubído com 8 K. Isto é uma motvação para nvestgar a dopagem de fulerenos e encontrar as condções ótmas para reduzr a dferença entre o nível de energa mas alto ocupado HOMO pelos elétrons do sstema e o prmero nível de energa desocupado LUMO Fgura 3.3. Esta 46
52 dferença de energa HOMO-LUMO, que também é conhecda como Gap, é a que determna as propredades de conductvdade do sstema. Outra mportante motvação no estudo da dopagem de fulerenos, como o C 60, é o poder de armazenar átomos em seu nteror ver fgura 3., sem perturbar a confguração eletrônca do estado fundamental do átomo dopante. Isto mplca que um passo prévo à ntrodução do átomo dopante no fulereno dopagem endohedral é vencer a barrera de potencal em sua superfce. Estudos epermentas com dopagem de Hélo, trogêno e Fósforo [0] mostraram que estes átomos mantnham as propredades de seu estado fundamental dentro da cavdade do C 60, sto valendo para o Hélo até a temperatura de 00K, e entre 400K e 600K para o Potásso e Fósforo. 47
53 Fgura 3.. a fgura superor se mostra a dopagem Endohedral, onde o átomo dopante fca dentro do buraco do fulereno. a fgura nferor se mostra a dopagem Heohedral, onde o átomo dopante fca fora do fulereno. 48
54 Fgura 3. Ilustração que mostra a nuvem eletrônca do C 60 de 3.0 Å de espessura. A dstânca do centro aos núcleos dos carbonos é de 3.5 Å. O buraco é de.0 Å de rao. 49
55 LUMO HOMO HOMO LUMO íves de energa Fgura 3.3. Se mostram os níves de energía do sstema molecular. o estado fundamental, o elétron de maor energa ocupará o nível denomnado HOMO Hghest ocuped molecular orbtal. O prmero nível não ocupado no estado fundamental, se denomna LUMO Lowest unocuped molecular orbtal. A redução da dferença HOMO-LUMO é nteresse para se obter maor conductvdade. 50
56 Referêncas bblográfcas F. R. Curl, R. E. Smalley, Scentfc Amercan, 54 October 99. H. W. Kroto, J. R. Heath, S.C O Bren, R. F. Curl, R. E. Smalley, ature 38, R. C Haddon, A. F. Hebard, M. J. Rossensky, D. W. Murphy, S. J. Duclos, K. B. Lyons, B. Mllel, J. M. Rosamla, R. M. Flemng, A. R. Kortan, S. H. Glarum, A. V. Makha, A. J. Muller, R. H. Eck, S. M. Zahurak, R. Tycko, G.Dabbagh, F. A.Thel, ature 350, P. W. Stephens, Physcs and Chemstry of Fullerens Sngapore: World Scentfc M. S. Dresselhaus, G. Dresselhaus, P. C. Eklund, Scence of Fullerenes and carbon anotubes : Ther Propertes and Applcatons, Cambrdge Unversty Press Karl M. Kadsh and Rodney S, Ruoff, Fullerens: Chemstry, Physcs and technology, Wlley-Interscence A. F. Hebard, M. J. Rossensky, R. C. Haddon, D. W. Murphy, S. H. Glarum, T. T. M. Palstra, A. P. Ramrez, A. R. Kortan. ature 350,
57 8 M. J. Rossensky, A. P. Ramrez, S. H. Glarum, D. W. Murphy, R. C. Haddon, A. F. Hebard, T. T. M. Palstra, A. R. Kortan, S. M. Zahurak, A. V. Makha. Phys. Rev. Lett. 66, M. Saunders, H. A. Jmenez-Vazquez, R. J. Cross, and R. J. Poreda, Scence 59, M. Wablnger, K. Lps, W. Harnet, and A. Wednger. Phys. Rev. B
58 4. Metodologas este trabalho se estudaram dos sstemas de dopagem para o fulereno C 60. O prmero consstu em dopar o C 60 somente com um átomo. A nomenclatura empregada para este sstema é [A+C 60 ] m, onde A é o tpo de átomo dopante e m é um número ntero que corresponde à carga total do sstema. Por eemplo, se o sstema é neutro então m tem o valor zero. Se netamos um elétron no sstema o valor de m sera de. O segundo sstema consstu em dopar dos fulerenos com um átomo. A nomenclatura empregada para este caso é [A+C 60 ] m. Se estudaram nove átomos dopantes: Be, B, Mg, Al, Zn, Ga, Sn e Sb. Se utlzou o programa Gaussan [] para realzar os cálculos dos parâmetros físcos estudados, tas como energa total do sstema, valores de HOMO-LUMO e a dstrbução de carga eletrônca no átomo dopante. O prmero conunto de dados que o programa requere são as coordenadas dos núcleos dos átomos do C 60. Se utlzou dados das coordenadas obtdas epermentalmente da geometra do estado fundamental. Tac como se menconou no capítulo anteror, o rao do C 60 é apromadamente 3,5 Å, que é a dstânca do centro do C 60 a um núcleo de carbono. O passo segunte é ngressar como dado a posção do átomo dopante. o caso do sstema [A+C 60 ] m, a orgem das coordenadas é o centro do C 60. Para o sstema [A+C 60 ] m, a orgem é o centro de um dos C 60. Se realzaram cálculos para dferentes posções do átomo dopante A. Isto mplca que para cada posção se determnou a energa total, o valor de HOMO- LUMO e a dstrbução de carga do átomo dopante, de acordo com o método escolhdo, que é o Hartree-Fock restrngdo RHF e não restrngdo UHF, Densdade Funconal e PM3, e de acordo com a carga total escolhda do sstema. Para o sstema [A+C 60 ] m se escolheram város valores da posção do átomo A, desde 5,0 Å com respeto ao centro do fulereno, até chegar ao centro deste ver fgura 4.. Para construr os gráfcos de energa total e HOMO-LUMO em função da posção do átomo dopante A, se escolheu ncrementos de 0,5 Å para 53
59 tentar uma melhor contnudade nas curvas. Para o sstema [A+C 60 ] m se aplcou o mesmo crtéro, somente com a dferença que a posção ncal do átomo A fo escolhda no ponto médo 7,5 Å do segmento que une os centros dos dos C 60, tomando como referênca o centro do C 60 do lado esquerdo ver fgura 4.. Fgura 4.. Sstema [A+C 60 ] m. Se mostram dferentes posções do átomo dopante. O rao do C 60 é de 3,5 Å. O centro do fulereno fo tomado como orgem das coordenadas. A dstânca mas longe do átomo A com respeto ao centro do C 60 se escolheu como sendo 5 Å. Fgura 4.. Sstema [A+C 60 ] m. Se mostram as dferentes posções do átomo dopante A. O centro do C 60 do lado esquerdo de tomou como orgem das coordenadas. O ponto médo do segmento que une os centros é de 7,5 Å. Cada fulereno é dêntco. o sstema [A+C 60 ] m se destacam quatro posções do átomo dopante A, as quas têm uma nomenclatura partcular que mostraremos a segur: 54
60 C A: sto representa o átomo A, a uma dstânca de 5,0 Å do centro fulereno. esta confguração a nteração entre o átomo dopante e o C 60 é desprezível. C 60.A: sto representa o átomo A, a uma dstânca de 5,5 Å do centro do fulereno. A nteração é aprecável. 3 C 60 A: sto representa o átomo A, a uma dstânca de 3,5 Å do centro do fulereno. esta confguração, o átomo dopante está na superfíce do C C sto representa o átomo A, no centro do C 60. Para construr as tabelas que mostram os resultados se tomou como valor de referênca a energa total na confguração C A. Também os resultados de HOMO-LUMO tveram como referênca esse ponto. Isto sgnfca que a energa total quando o átomo dopante está a 5,0 Å do fulereno tem zero como valor relatvo. E m = 0 A... C ] 4. [ 60 E m = E m E m 4. [ A. C60 ] [ A. C60 ] [ A... C60 ] E m = E m E m 4.3 [ AC60 ] [ AC60 ] [ A... C60 ] E m = E m E m 4.4 [ A@ C60 ] [ A@ C60 ] [ A... C60 ] o sstema [A+C 60 ] m também se destacam quatro posções do átomo dopante A, as quas têm uma nomenclatura partcular que mostraremos a segur: C 60 A C 60 : sto representa o átomo A, a uma dstânca de 7,5 Å do centro do fulereno do lado esquerdo. 55
61 C 60.A C 60 : sto representa o átomo A, a uma dstânca de 5,5 Å do centro do fulereno do lado esquerdo. 3 C 60 A C 60 : sto representa o átomo A, a uma dstânca de 3,5 Å do centro do fulereno. esta confguração o átomo dopante está na superfíce do C C 60 : sto representa o átomo A, no centro do C 60 do lado esquerdo. o caso do sstema [A+C 60 ] m as tabelas que mostram os resultados tveram como referênca a confguração C 60...A...C 60, tanto para os valores da energa total quanto para os de HOMO-LUMO. Isto sgnfca que a energa total tem valor relatvo zero quando o átomo dopante está a 7,5 Å do centro do fulereno. Temos então que: E m = 0 C... A... C ] 4.5 [ E m = E m E m 4.6 [ C60 A... C60 ] [ C60 A... C60 ] [ C60... A... C60 ] E m = E m E m 4.7 [ C60 A... C60 ] [ C60 A... C60 ] [ C60... A... C60 ] E = E E 4.8 n n m [ C60@ A... C60] [ C60@ A... C60] [ C60... A... C60] Quando se utlzou o método de Hartree-Fock fo necessáro tomar em consderação a multplcdade total do sstema. A multplcdade é um dado a ser colocado no programa. Isto sgnfca que quando o número total de elétrons do sstema é par, no estado fundamental todas as camadas eletrôncas estão duplamente ocupadas camadas fechadas e o número quântco do spn total S é zero. Então se dz que a multplcdade se determna pela fórmula S+, onde S é o número quântco de spn que toma dversos valores, desde 0, /,, 3/,... Para tanto, o método de Hartree-Fock Restrngdo RHF é o convenente a usar se estamos no caso de camadas fechadas, e no caso de camadas abertas, o 56
62 método de Hartree-Fock não restrngdo UHF, onde o número total de elétrons é ímpar. Por eemplo Por eemplo, se nosso sstema está no estado fundamental, é neutro e sua carga total m=0, e tem um número de elétrons par multplcdade=, usaríamos o método restrngdo RHF, mas se netarmos um elétron no sstema redução m=-, ou etrarmos um odação m=, não sera todas as camadas que estaram duplamente ocupadas, então a multplcdade sera e deveríamos usar o método não restrngdo UHF. Os métodos de funconal densdade DFT e PM3 foram usados somente em camadas fechadas. A dstrbução de carga fo calculada na apromação de Mullken. o Apêndce I se eplca como se obtém esta apromação. A escolha desta apromação ocorre em vrtude de sua smplcdade. O tpo de bases utlzadas para se apromar os orbtas atômcos foram as de Huznaga e 6-3G*. o Apêndce II se eplca como elas estão defndas. o caso de 6-3G*, sua escolha é devdo a sua alta precsão para austar o orbtal atômco s em sua promdade com o núcleo. As desvantagens são o maor custo computaconal que mplca e que não está parametrzada para todos os átomos. Uma vantagem é a rápda convergênca nos cálculos autoconsstentes. Sua desvantagem é a menor precsão em comparação a 6-3G*. Os gráfcos bdmensonas foram fetos utlzando o programa GUPLOT 3.0. Os gráfcos trdmensonas de Energa Total, e de HOMO-LUMO, versus carga versus dstânca, foram fetos usando o GUPLOT e um programa que escrevemos em lnguagem C. Os valores de Energa Total, e de HOMO-LUMO, foram calculados em ncrementos de dstânca de 0.5 Å entre o átomo dopante e o centro dos fulerenos para dferentes valores de carga total. Os dados de entrada para o GUPLOT foram calculados por meo do nosso programa em C usando nterpolação cúbca []. Esta nterpolação teve que ser feta nos eos Z - X e Z - Y, onde o eo Z representa Energa total ou HOMO-LUMO, o eo X para a carga e Y para dstânca. 57
63 Referêncas bblográfcas M. J. Frsh et all,gaussan 03, Gaussan, Inc., Pttsburgh, PA, 003. R. L. Burden, J. D. Fares. Análss umérco, Grupo Edtoral Iberoamérca,Méco,
64 5. RESULTADOS E DISCUSÔES A Interação dos átomos A=Be,B,Mg,Al,Zn,Ga,Ge,Sn,Sb em aglomerados com confgurações [A+C 60 ] m e [A+C 60 ] m, carga total m=-,0,, foram calculados usando os métodos sem-empírcos PM3, Ab-Into UHF,RHF e Densdade Funconal B3LYP/6-3G* resultando em tabelas e gráfcas que descrevem as establdades, transferêncas de cargas, HOMO-LUMO, dos aglomerados para dferentes posções do átomo A relatvo ao centro de uma das duas moléculas de C 60. as tabelas 5., 5. e 5.3 mostramos as varações das energas totas, calor de formação PM3 dos aglomerados com referênca a dstânca 7.5 Å e 5.0 Å do átomo dopante dstante do centro do fulereno usando os métodos semempírco, ab-nto e densdade funconal. A metodologa para descrever as varações nas dversas regões foram descrtas no captulo IV, através das equações 4. a 4.8. Tabela 5. Varação da Energa Total ev do [A+C 60 ] m DFT A m En. Tot. En. Tot. En. Tot. En. Tot. C 60...A 5.0 Å C 60.A 5.5 Å C 60 A 3.5 Å C 0.0 Å Be B Al Ge Ga Mg Zn Tabela 5. Varação da Energa Total ev do [A+C 60 ] m e Calor de Formação Kcal 0 3 em parêntess PM3 A m En. Tot. En. Tot. En. Tot. En. Tot. C 60...A...C Å C 60...A.C Å C 60...A.C Å C 60...A@C Å Be B Al Zn
65 Tabela 5.3 Varação da Energa Total ev do [A+C 60 ] m A m En.Tot En.Tot En.Tot C 60...A...C 60 C 60...A.C 60 C 60...A.C 60 Ab-Into En.Tot C 60 A@C Å 5.5Å 3.5Å 0.0Å Be UHF B RHF Mg UHF Al RHF Zn UHF Ga UHF Sn UHF Sb RHF Be RHF B UHF Mg RHF Al UHF Zn RHF Ga RHF Sn RHF Sb UHF Be UHF B RHF Mg UHF Al RHF Zn UHF Ga UHF Sn UHF Sb RHF Destacam-se nas tabelas ,quatro stuações envolvendo as dstâncas em relação ao centro de C 60. O átomo A dstante, 7.5 Å e 5 Å; nteragendo com C 60, 5.5 Å ; 3 perto do rado do C 60, 3.5 Å; 4 no centro do C 60, 0.0 Å. As varações das energas foram determnadas usando como parâmetro de comparação as energas do sstema à 7.5 Å e 5.0 Å do centro de um dos C
66 Os cálculos das varações das energas totas e calores de formação ndcam maor establdade para os sstemas com carga total 0 e - e nas confgurações com dstâncas C 60...A.C 60 e A.C Å assm como C A@C 60 e A@C Å. As confgurações C 60...AC 60 e AC Å ndcam aumento postvo das varações de energa total dos aglomerados. As barreras de energa potencal em torno de 3.5 Å tendem a aumentar com o número atômco do átomo dopante A no Hartree-Fock e PM3. as fguras Fg mostramos as energas totas versus dstânca entre os centros dos fulerenos e os átomos dopantes A = Be, B, Mg, Al, Zn, Ga, Sn, Sb calculados usando os métodos ab-nto UHF e RHF no [A+C 60 ] m. Os cálculos foram fetos em função do movmento dos átomos em dreção ao centro de um dos dos C 60 para sstemas com carga total m= 0,,-. a 6
67 b c Fg 5. Cálculos Ab-Into da Energa Total ev0, versus Dstânca Å, para dferentes valores da Carga Total m= -,0, u.a. no aglomerado que modela a nteração de a Be, b B, c Mg, com dos C 60. 6
68 a d b Fg 5. Cálculos Ab-Into da Energa Total ev0, versus Dstânca Å, para dferentes valores da Carga Total m= -,0, u.a. no aglomerado que modela a nteração de a Al, b Zn, com dos C
69 a b Fg 5.3 Cálculos Ab-Into da Energa Total ev0, versus Dstânca Å, para dferentes valores da Carga Total m= -,0, u.a. no aglomerado que modela a nteração de a Ga, b Sn, com dos C
70 FIG. 5.4 Cálculos Ab-Into da Energa Total ev0, versus Dstânca Å, para dferentes valores da Carga Total m = 0, u.a. no aglomerado que modela a nteração de Sb com dos C 60. Os aglomerados estão, em geral, mas establzados para carga total m=0, -. Observa-se barreras de energa potencal em torno de 3.5 Å e energas mas baas ou establzadas em torno de 5.5 Å. as fguras 5.5 a,b,c mostramos as gráfcas b-dmensonas de energa total versus dstânca entre os átomos dopantes e os centros de um dos dos fulerenos para carga total m=0, usando o método de Funconal da Densdade. a 65
71 b c Fg 5.5 Cálculos com Densdade Funconal da Energa Total ev0, versus Dstânca Å, para Carga Total m = 0, no aglomerado que modela a nteração de a Be,b Zn,c Mg,com dos C
72 Como no caso dos cálculos ab-nto observamos também nos cálculos DFT barreras de energa potencal em torno de 3.5 Å e regões de energa baas ou establzadas em torno de 5.5 Å. Mostramos em 5.6 a,b, 5.7 a,b, 5.8 a,b, 5.9 as gráfcas trdmensonas de energa versus carga versus dstânca dos cálculos ab-nto para m=0,,-. Fg 5.6 Cálculos Ab-Into da Energa Total, En. Tot., ev0 versus Dstânca Å, versus Carga Total m= -,0, u.a. no aglomerado que modela a nteração de Be com dos C 60 67
73 a b Fg 5.7 Cálculos Ab-Into da Energa Total, En.Tot, ev0 versus Dstânca Å, versus Carga Total m=-,0, u.a. no aglomerado que modela a nteração de a B e b Mg com dos C
74 a b Fg 5.8 Cálculos Ab-Into da Energa Total, En.Tot, ev 0 versus Dstânca Å, versus Carga Total m=-,0, u.a. no aglomerado que modela a nteração de a Al, b Zn com dos C
75 Fg 5.9 Cálculos Ab-Into da Energa Total, En.Tot, ev 0 versus Dstânca Å, versus Carga Total m=-,0, u.a. no aglomerado que modela a nteração de Sn com dos C 60. Para todas as confgurações [A+C 60 ] m, m=-,0,, A=Be, B, Mg, Al, Zn, Ga, Sn e Sb observamos dos cálculos ab-into nas fguras trdmensonas 5.6, 5.7, 5.8, 5.9 da energa total versus dstânca,versus carga que há um potencal de barrera para penetrar no C 60 em torno de 3.5 Å assm como regões de energas baas ou establzadas em torno de 5.5 Å. as Tabelas 5.4 e 5.5 mostramos os valores de HOMO LUMO nas prncpas regões 7.5, 5.0 Å, 5.5 Å, 3.5 Å e 0.0 Å calculados com os métodos ab-nto e Funconal de Densdade. 70
76 Tabela 5.4 HOMO LUMO H-L do [A +C 60 ] m ev ab-nto A m H-L H-L H-L H-L C 60...A...C 60 C 60...A.C 60 C 60...AC 60 C 60 A@C Å 5.5 Å 3.5 Å 0.0 Å Be UHF B RHF Mg UHF Al RHF Zn UHF Ga UHF Sn UHF Sb RHF Be RHF B UHF Mg RHF Al UHF Zn RHF Ga RHF Sn RHF Sb UHF Be UHF B RHF Mg UHF Al RHF Zn UHF Ga UHF Sn UHF Sb RHF A tabela 5.4 mostra que o HOMO-LUMO tende á aumentar nas regões de barreras de energa de potencal em torno de 3.5 Å e a dmnur nas regões de energas baas ou establzadas em torno de 5.5 Å. Esta tendênca se mantém para dferentes cargas totas dos sstema [A+C 60 ] m, m=-,0,. 7
77 Tabela 5.5 HOMO LUMO, H-L ev para varas dstancas DFT A m H-L H-L H-L H-L C 60...A C 60.A C 60.A C 5.0 Å 5.5 Å 3.5 Å 0.0 Å Be B Al Ge Ga Mg Zn A tabela 5.5 do DFT também ndca que o HOMO-LUMO tende a dmnur na regão de energas baas ou establzadas. as Fguras 5.0 a,b,c mostramos as gráfcas b-dmensonas de HOMO- LUMO vs dstanca m=0, DFT, na confguração [A+C 60 ] m para dopagens com Be, Zn e Mg. a 7
78 b c Fg 5.0 Cálculos DFT do HOMO LUMO, H L, ev 0 versus Dstânca Å, carga total m=0 no aglomerado que modela a nteração de a Zn, b Mg e c Be com dos C 60 Observa-se uma tendênca de redução do HOMO-LUMO na regão de energas mas baas. as fguras 5. até 5.3 mostramos as fguras trdmensonas de HOMO LUMO vs dstânca vs carga m=-,0,, cálculos ab-nto, na confguração [A+C 60 ] m para A = Be, B, Mg, Al, Zn, Ga, Sn e Sb. 73
79 a b Fg 5. Cálculos Ab-Into do HOMO LUMO, H L, ev 0 versus Dstânca Å, versus Carga Total m=-,0, u.a. no aglomerado que modela a nteração de a Mg, b Al com dos C
80 a Fg 5. Cálculos Ab-Into do HOMO LUMO, H L, ev 0 versus Dstânca Å, versus Carga Total m=-,0, u.a. no aglomerado que modela a nteração de a Zn, b Ga, com dos C
81 Fg 5.3 Cálculos Ab-Into do HOMO LUMO H L ev 0 versus Dstânca Å, versus Carga Total m=-,0, u.a. no aglomerado que modela a nteração de Sn com dos C 60 Os gráfcos trdmensonas de HOMO-LUMO também mostram que o GAP tende a aumentar nas regões de mámos de energa e dmnur nas regões de energas mas baas ou establzadas, tanto para redução como odação do sstema. Apresentamos na tabela 5.6 valores de carga do átomo dopante nas regões de maor nteresse usando o DFT e a metodologa descrta nas equações Tabela 5.6 Carga u.a do A no [A+C 60 ] m DFT A m C 60...A C 60.A C 60 A C 5.0 Å 5.5 Å 3.5 Å 0.0 Å Be B Al Ge Ga Mg Zn
82 Observa-se que as prncpas transferêncas de carga dos dopantes A para os fulerenos acontecem na regão de nteração em torno de 5.5 Å. Pode haver transferênca também de carga do fulereno para os átomos dopantes A na regão em torno de 3.5 Å. A fgura 5.4 mostra o buraco do fulereno o qual têm um rao de.0 Å. Isto sugere que se ntroduzmos um átomo de um rao consderavelmente menor que.0 Å, a nuvem eletrônca não terá nteração como a nuvem eletrônca do fulereno. Então a transferênca de carga será desprezível. A tabela 5.7 mostra esta tendênca. O átomo de rao menor deste conunto Tabela 5.7 de átomos dopantes é o ntrogêno, o qual não mostra epermentalmente transferênca de carga. O fósforo como rao atômco pouco maor que o ntrogêno, também não ndca epermentalmente transferênca de carga. ossos cálculos em DFT na apromação de Mullken mostram que para os átomos B e Be, cuos raos atômcos estão entre os do ntrogêno e o fósforo, apresentam uma transferênca de carga que tende a zero. O Ga e o Al cuos raos atômcos são maores mostram transferênca de carga. O átomo de La, que tem o maor rao atômco mostra epermentalmente uma transferênca de tda a carga de valênca. 77
83 Tabela 5.7 Carga u.a do A no [A+C 60 ] m em função do rao atômco Átomo dopantea Carga do A em Rao atômco Å A@C 60 u.a EXP [] B DFT Be DFT P EXP [] Ge DFT Zn DFT Ga DFT Al DFT Mg DFT La EXP []
84 C 60 R=.00 Å Fgura 5.4. A fgura mostra o buraco do fulereno C 60 de Å do rao rodeado da nove eletrônca. Resumndo, a análse das tabelas e fguras b e trdmensonas vs dstânca vs carga para as confgurações [A+C 60 ] m e [A+C 60 ] m, m= -,0,, ndcam que a redução m= - tende a abaar as energas totas dos sstemas e a dmnur o potencal de barrera para penetrar no C 60. Em geral, os sstemas estão mas establzados na regão em torno de 5.5 Å. Todos os sstemas nvestgados ndcam barreras de energa potencal em torno de 3.5 Å. Os valores de HOMO- LUMO tendem aumentar na regão do mámo de energa, e a dmnur na regão de energas mas baas ou establzadas. Em geral, estas regões tendem à concdr com as regões de transferênca de carga. À medda que o átomo dopante se aproma do centro do C 60, há uma tendênca do átomo A, de doar cargas para o fulereno, tornando os dopantes mas eletropostvos. O HOMO- LUMO muda com a posção dos átomos dopantes, redução, odação, establdade e transferêncas de cargas, sugerndo a possbldade de mudar as propredades fsco-químocas destes sstemas. Em partcular, as mudanças nas propredades dependentes dos Gaps de energa, como as elétrcas, são de consderável nteresse tecnológco devdo a dependênca da condutvdade como o Gap. Observa-se também quando o átomo dopante está dentro do buraco do 79
O íon lantanídeo no acoplamento Russell-Saunders e a classificação de seus estados segundo os subgrupos do grupo GL(4
 O íon lantanídeo no acoplamento Russell-aunders e a classfcação de seus estados segundo os subgrupos do grupo G(4 ) O hamltonano, H, dos íons lantanídeos contém uma parte que corresponde ao campo central,
O íon lantanídeo no acoplamento Russell-aunders e a classfcação de seus estados segundo os subgrupos do grupo G(4 ) O hamltonano, H, dos íons lantanídeos contém uma parte que corresponde ao campo central,
Palavras Chaves: Linear Combination of Atomic Orbitals, LCAO, Molecular Orbitals, MO, Atomic Orbitals, AO.
 Dego da Slva Manoel Insttuto de Físca de São Carlos, Unversdade de São Paulo, São Carlos-SP, Brasl Resumo Neste trabalho abordamos a descrção dos Orbtas Moleculares (MO), obtdos va Combnação Lnear dos
Dego da Slva Manoel Insttuto de Físca de São Carlos, Unversdade de São Paulo, São Carlos-SP, Brasl Resumo Neste trabalho abordamos a descrção dos Orbtas Moleculares (MO), obtdos va Combnação Lnear dos
Parênteses termodinâmico
 Parênteses termodnâmco Lembrando de 1 dos lmtes de valdade da dstrbução de Maxwell-Boltzmann: λ
Parênteses termodnâmco Lembrando de 1 dos lmtes de valdade da dstrbução de Maxwell-Boltzmann: λ
2 Análise de Campos Modais em Guias de Onda Arbitrários
 Análse de Campos Modas em Guas de Onda Arbtráros Neste capítulo serão analsados os campos modas em guas de onda de seção arbtrára. A seção transversal do gua é apromada por um polígono conveo descrto por
Análse de Campos Modas em Guas de Onda Arbtráros Neste capítulo serão analsados os campos modas em guas de onda de seção arbtrára. A seção transversal do gua é apromada por um polígono conveo descrto por
4 Autovetores e autovalores de um operador hermiteano
 T (ψ) j = ψ j ˆT ψ = k ψ j ˆT φ k S k = k,l ψ j φ l T (φ) S k = k,l φ l ψ j T (φ) S k = k,l SljT (φ) S k. Após todos esses passos vemos que T (ψ) j = k,l S jl T (φ) S k ou, em termos matrcas T (ψ) = S
T (ψ) j = ψ j ˆT ψ = k ψ j ˆT φ k S k = k,l ψ j φ l T (φ) S k = k,l φ l ψ j T (φ) S k = k,l SljT (φ) S k. Após todos esses passos vemos que T (ψ) j = k,l S jl T (φ) S k ou, em termos matrcas T (ψ) = S
Estudo de Solubilidade por Método Monte Carlo Para a Molécula do Fulereno
 Fundação Unversdade Federal do Amapá Pro - Retora de Ensno de Graduação Coordenação do Curso de Físca Estudo de Solubldade por Método Monte Carlo Para a Molécula do Fulereno Acadêmco: Robert Sarava Matos
Fundação Unversdade Federal do Amapá Pro - Retora de Ensno de Graduação Coordenação do Curso de Físca Estudo de Solubldade por Método Monte Carlo Para a Molécula do Fulereno Acadêmco: Robert Sarava Matos
Notas Processos estocásticos. Nestor Caticha 23 de abril de 2012
 Notas Processos estocástcos Nestor Catcha 23 de abrl de 2012 notas processos estocástcos 2 O Teorema de Perron Frobenus para matrzes de Markov Consdere um processo estocástco representado por um conunto
Notas Processos estocástcos Nestor Catcha 23 de abrl de 2012 notas processos estocástcos 2 O Teorema de Perron Frobenus para matrzes de Markov Consdere um processo estocástco representado por um conunto
Algarismos Significativos Propagação de Erros ou Desvios
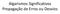 Algarsmos Sgnfcatvos Propagação de Erros ou Desvos L1 = 1,35 cm; L = 1,3 cm; L3 = 1,30 cm L4 = 1,4 cm; L5 = 1,7 cm. Qual destas meddas está correta? Qual apresenta algarsmos com sgnfcado? O nstrumento
Algarsmos Sgnfcatvos Propagação de Erros ou Desvos L1 = 1,35 cm; L = 1,3 cm; L3 = 1,30 cm L4 = 1,4 cm; L5 = 1,7 cm. Qual destas meddas está correta? Qual apresenta algarsmos com sgnfcado? O nstrumento
Método de Hartree-Fock
 Método de Hartree-Fock CARLOS MACIEL DE OLIVEIRA BASTOS Insttuto de Físca de São Carlos - Unversdade de São Paulo 17 de ovembro de 2015 1 Introdução Os prmeros trabalhos sobre como tratar mutos elétrons
Método de Hartree-Fock CARLOS MACIEL DE OLIVEIRA BASTOS Insttuto de Físca de São Carlos - Unversdade de São Paulo 17 de ovembro de 2015 1 Introdução Os prmeros trabalhos sobre como tratar mutos elétrons
Flambagem. Cálculo da carga crítica via MDF
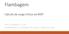 Flambagem Cálculo da carga crítca va MDF ROF. ALEXANDRE A. CURY DEARTAMENTO DE MECÂNICA ALICADA E COMUTACIONAL Flambagem - Cálculo da carga crítca va MDF Nas aulas anterores, vmos como avalar a carga crítca
Flambagem Cálculo da carga crítca va MDF ROF. ALEXANDRE A. CURY DEARTAMENTO DE MECÂNICA ALICADA E COMUTACIONAL Flambagem - Cálculo da carga crítca va MDF Nas aulas anterores, vmos como avalar a carga crítca
Faculdade de Engenharia Optimização. Prof. Doutor Engº Jorge Nhambiu
 1 Programação Não Lnear com Restrções Aula 9: Programação Não-Lnear - Funções de Váras Varáves com Restrções Ponto Regular; Introdução aos Multplcadores de Lagrange; Multplcadores de Lagrange e Condções
1 Programação Não Lnear com Restrções Aula 9: Programação Não-Lnear - Funções de Váras Varáves com Restrções Ponto Regular; Introdução aos Multplcadores de Lagrange; Multplcadores de Lagrange e Condções
Figura 8.1: Distribuição uniforme de pontos em uma malha uni-dimensional. A notação empregada neste capítulo para avaliação da derivada de uma
 Capítulo 8 Dferencação Numérca Quase todos os métodos numércos utlzados atualmente para obtenção de soluções de equações erencas ordnáras e parcas utlzam algum tpo de aproxmação para as dervadas contínuas
Capítulo 8 Dferencação Numérca Quase todos os métodos numércos utlzados atualmente para obtenção de soluções de equações erencas ordnáras e parcas utlzam algum tpo de aproxmação para as dervadas contínuas
2 Principio do Trabalho Virtual (PTV)
 Prncpo do Trabalho rtual (PT)..Contnuo com mcroestrutura Na teora que leva em consderação a mcroestrutura do materal, cada partícula anda é representada por um ponto P, conforme Fgura. Porém suas propredades
Prncpo do Trabalho rtual (PT)..Contnuo com mcroestrutura Na teora que leva em consderação a mcroestrutura do materal, cada partícula anda é representada por um ponto P, conforme Fgura. Porém suas propredades
4 Discretização e Linearização
 4 Dscretzação e Lnearzação Uma vez defndas as equações dferencas do problema, o passo segunte consste no processo de dscretzação e lnearzação das mesmas para que seja montado um sstema de equações algébrcas
4 Dscretzação e Lnearzação Uma vez defndas as equações dferencas do problema, o passo segunte consste no processo de dscretzação e lnearzação das mesmas para que seja montado um sstema de equações algébrcas
Radiação Térmica Processos, Propriedades e Troca de Radiação entre Superfícies (Parte 2)
 Radação Térmca Processos, Propredades e Troca de Radação entre Superfíces (Parte ) Obetvo: calcular a troca por radação entre duas ou mas superfíces. Essa troca depende das geometras e orentações das superfíces,
Radação Térmca Processos, Propredades e Troca de Radação entre Superfíces (Parte ) Obetvo: calcular a troca por radação entre duas ou mas superfíces. Essa troca depende das geometras e orentações das superfíces,
Ajuste de um modelo linear aos dados:
 Propagação de erros Suponhamos que se pretende determnar uma quantdade Z, a partr da medda drecta das grandezas A, B, C,, com as quas se relacona através de Z = f(a,b,c, ). Se os erros assocados a A, B,
Propagação de erros Suponhamos que se pretende determnar uma quantdade Z, a partr da medda drecta das grandezas A, B, C,, com as quas se relacona através de Z = f(a,b,c, ). Se os erros assocados a A, B,
2 Incerteza de medição
 2 Incerteza de medção Toda medção envolve ensaos, ajustes, condconamentos e a observação de ndcações em um nstrumento. Este conhecmento é utlzado para obter o valor de uma grandeza (mensurando) a partr
2 Incerteza de medção Toda medção envolve ensaos, ajustes, condconamentos e a observação de ndcações em um nstrumento. Este conhecmento é utlzado para obter o valor de uma grandeza (mensurando) a partr
3 Metodologia de Avaliação da Relação entre o Custo Operacional e o Preço do Óleo
 3 Metodologa de Avalação da Relação entre o Custo Operaconal e o Preço do Óleo Este capítulo tem como objetvo apresentar a metodologa que será empregada nesta pesqusa para avalar a dependênca entre duas
3 Metodologa de Avalação da Relação entre o Custo Operaconal e o Preço do Óleo Este capítulo tem como objetvo apresentar a metodologa que será empregada nesta pesqusa para avalar a dependênca entre duas
UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE FÍSICA PROGRAMA DE PÓS-GRADUAÇÃO EM FÍSICA
 UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE FÍSICA PROGRAMA DE PÓS-GRADUAÇÃO EM FÍSICA ANDRÉIA DOS SANTOS SIMÕES Espalhamento Elástco Elétron-Molécula: um Estudo usando o Método Interação de Confguração
UNIVERSIDADE FEDERAL DA BAHIA INSTITUTO DE FÍSICA PROGRAMA DE PÓS-GRADUAÇÃO EM FÍSICA ANDRÉIA DOS SANTOS SIMÕES Espalhamento Elástco Elétron-Molécula: um Estudo usando o Método Interação de Confguração
0.5 setgray0 0.5 setgray1. Mecânica dos Fluidos Computacional. Aula 7. Leandro Franco de Souza. Leandro Franco de Souza p.
 Leandro Franco de Souza lefraso@cmc.usp.br p. 1/1 0.5 setgray0 0.5 setgray1 Mecânca dos Fludos Computaconal Aula 7 Leandro Franco de Souza Leandro Franco de Souza lefraso@cmc.usp.br p. 2/1 Equações Dferencas
Leandro Franco de Souza lefraso@cmc.usp.br p. 1/1 0.5 setgray0 0.5 setgray1 Mecânca dos Fludos Computaconal Aula 7 Leandro Franco de Souza Leandro Franco de Souza lefraso@cmc.usp.br p. 2/1 Equações Dferencas
Palavras-Chave: Métodos Interativos da Potência e Inverso, Sistemas Lineares, Autovetores e Autovalores.
 MSc leandre Estáco Féo ssocação Educaconal Dom Bosco - Faculdade de Engenhara de Resende Caa Postal 8.698/87 - CEP 75-97 - Resende - RJ Brasl Professor e Doutorando de Engenhara aefeo@yahoo.com.br Resumo
MSc leandre Estáco Féo ssocação Educaconal Dom Bosco - Faculdade de Engenhara de Resende Caa Postal 8.698/87 - CEP 75-97 - Resende - RJ Brasl Professor e Doutorando de Engenhara aefeo@yahoo.com.br Resumo
CORRELAÇÃO E REGRESSÃO
 CORRELAÇÃO E REGRESSÃO Constata-se, freqüentemente, a estênca de uma relação entre duas (ou mas) varáves. Se tal relação é de natureza quanttatva, a correlação é o nstrumento adequado para descobrr e medr
CORRELAÇÃO E REGRESSÃO Constata-se, freqüentemente, a estênca de uma relação entre duas (ou mas) varáves. Se tal relação é de natureza quanttatva, a correlação é o nstrumento adequado para descobrr e medr
Eletrotécnica AULA Nº 1 Introdução
 Eletrotécnca UL Nº Introdução INTRODUÇÃO PRODUÇÃO DE ENERGI ELÉTRIC GERDOR ESTÇÃO ELEVDOR Lnha de Transmssão ESTÇÃO IXDOR Equpamentos Elétrcos Crcuto Elétrco: camnho percorrdo por uma corrente elétrca
Eletrotécnca UL Nº Introdução INTRODUÇÃO PRODUÇÃO DE ENERGI ELÉTRIC GERDOR ESTÇÃO ELEVDOR Lnha de Transmssão ESTÇÃO IXDOR Equpamentos Elétrcos Crcuto Elétrco: camnho percorrdo por uma corrente elétrca
É o grau de associação entre duas ou mais variáveis. Pode ser: correlacional ou experimental.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Os modelos de regressão paramétricos vistos anteriormente exigem que se suponha uma distribuição estatística para o tempo de sobrevivência.
 MODELO DE REGRESSÃO DE COX Os modelos de regressão paramétrcos vstos anterormente exgem que se suponha uma dstrbução estatístca para o tempo de sobrevvênca. Contudo esta suposção, caso não sea adequada,
MODELO DE REGRESSÃO DE COX Os modelos de regressão paramétrcos vstos anterormente exgem que se suponha uma dstrbução estatístca para o tempo de sobrevvênca. Contudo esta suposção, caso não sea adequada,
Regressão Múltipla. Parte I: Modelo Geral e Estimação
 Regressão Múltpla Parte I: Modelo Geral e Estmação Regressão lnear múltpla Exemplos: Num estudo sobre a produtvdade de trabalhadores ( em aeronave, navos) o pesqusador deseja controlar o número desses
Regressão Múltpla Parte I: Modelo Geral e Estmação Regressão lnear múltpla Exemplos: Num estudo sobre a produtvdade de trabalhadores ( em aeronave, navos) o pesqusador deseja controlar o número desses
3 Método Numérico. 3.1 Discretização da Equação Diferencial
 3 Método Numérco O presente capítulo apresenta a dscretação da equação dferencal para o campo de pressão e a ntegração numérca da expressão obtda anterormente para a Vscosdade Newtonana Equvalente possbltando
3 Método Numérco O presente capítulo apresenta a dscretação da equação dferencal para o campo de pressão e a ntegração numérca da expressão obtda anterormente para a Vscosdade Newtonana Equvalente possbltando
ESTUDO DA TEORIA DO FUNCIONAL DA DENSIDADE APLICADO ÀS SIMULAÇÕES DE PROPRIEDADES ELETRÔNICAS E ESTRUTURAIS DE SEMICONDUTORES
 Anas do XVI Encontro de Incação Centífca e Pós-Graduação do ITA XVI ENCITA / 2010 Insttuto Tecnológco de Aeronáutca, São José dos Campos, SP, Brasl, 20 de outubro de 2010 ESTUDO DA TEORIA DO FUNCIONAL
Anas do XVI Encontro de Incação Centífca e Pós-Graduação do ITA XVI ENCITA / 2010 Insttuto Tecnológco de Aeronáutca, São José dos Campos, SP, Brasl, 20 de outubro de 2010 ESTUDO DA TEORIA DO FUNCIONAL
Covariância na Propagação de Erros
 Técncas Laboratoras de Físca Lc. Físca e Eng. omédca 007/08 Capítulo VII Covarânca e Correlação Covarânca na propagação de erros Coefcente de Correlação Lnear 35 Covarânca na Propagação de Erros Suponhamos
Técncas Laboratoras de Físca Lc. Físca e Eng. omédca 007/08 Capítulo VII Covarânca e Correlação Covarânca na propagação de erros Coefcente de Correlação Lnear 35 Covarânca na Propagação de Erros Suponhamos
Estatística II Antonio Roque Aula 18. Regressão Linear
 Estatístca II Antono Roque Aula 18 Regressão Lnear Quando se consderam duas varáves aleatóras ao mesmo tempo, X e Y, as técncas estatístcas aplcadas são as de regressão e correlação. As duas técncas estão
Estatístca II Antono Roque Aula 18 Regressão Lnear Quando se consderam duas varáves aleatóras ao mesmo tempo, X e Y, as técncas estatístcas aplcadas são as de regressão e correlação. As duas técncas estão
CQ110 : Princípios de FQ
 CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br 1 soluções eletrolítcas Qual a dferença entre uma solução 1,0 mol L -1 de glcose e outra de NaCl de mesma concentração?
CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br 1 soluções eletrolítcas Qual a dferença entre uma solução 1,0 mol L -1 de glcose e outra de NaCl de mesma concentração?
Interpolação Segmentada
 Interpolação Segmentada Uma splne é uma função segmentada e consste na junção de váras funções defndas num ntervalo, de tal forma que as partes que estão lgadas umas às outras de uma manera contínua e
Interpolação Segmentada Uma splne é uma função segmentada e consste na junção de váras funções defndas num ntervalo, de tal forma que as partes que estão lgadas umas às outras de uma manera contínua e
INTRODUÇÃO À ASTROFÍSICA
 Introdução à Astrofísca INTRODUÇÃO À ASTROFÍSICA LIÇÃO 7: A MECÂNICA CELESTE Lção 6 A Mecânca Celeste O que vmos até agora fo um panorama da hstóra da astronoma. Porém, esse curso não pretende ser de dvulgação
Introdução à Astrofísca INTRODUÇÃO À ASTROFÍSICA LIÇÃO 7: A MECÂNICA CELESTE Lção 6 A Mecânca Celeste O que vmos até agora fo um panorama da hstóra da astronoma. Porém, esse curso não pretende ser de dvulgação
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Prof. Lorí Val, Dr. UFRG Insttuto de Matemátca
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Prof. Lorí Val, Dr. UFRG Insttuto de Matemátca
8 Soluções Não Ideais
 8 Soluções Não Ideas 8.1 Convenções para o coefcente de atvdade na escala de frações molares Para a solução deal temos ln x onde é função apenas da pressão e temperatura. Fo anterormente mostrado que todas
8 Soluções Não Ideas 8.1 Convenções para o coefcente de atvdade na escala de frações molares Para a solução deal temos ln x onde é função apenas da pressão e temperatura. Fo anterormente mostrado que todas
Cálculo Numérico BCC760 Interpolação Polinomial
 Cálculo Numérco BCC76 Interpolação Polnomal Departamento de Computação Págna da dscplna http://www.decom.ufop.br/bcc76/ 1 Interpolação Polnomal Conteúdo 1. Introdução 2. Objetvo 3. Estênca e uncdade 4.
Cálculo Numérco BCC76 Interpolação Polnomal Departamento de Computação Págna da dscplna http://www.decom.ufop.br/bcc76/ 1 Interpolação Polnomal Conteúdo 1. Introdução 2. Objetvo 3. Estênca e uncdade 4.
Física Moderna II - FNC376
 Unversdade de São Paulo Insttuto de Físca Físca Moderna II - FNC376 Profa. Márca de Almeda Rzzutto 1o. Semestre de 008 FNC0376 - Fsca Moderna 1 Revsão A organzação da tabela peródca reflete a dstrbução
Unversdade de São Paulo Insttuto de Físca Físca Moderna II - FNC376 Profa. Márca de Almeda Rzzutto 1o. Semestre de 008 FNC0376 - Fsca Moderna 1 Revsão A organzação da tabela peródca reflete a dstrbução
Cap. 6 - Energia Potencial e Conservação da Energia Mecânica
 Unversdade Federal do Ro de Janero Insttuto de Físca Físca I IGM1 014/1 Cap. 6 - Energa Potencal e Conservação da Energa Mecânca Prof. Elvs Soares 1 Energa Potencal A energa potencal é o nome dado a forma
Unversdade Federal do Ro de Janero Insttuto de Físca Físca I IGM1 014/1 Cap. 6 - Energa Potencal e Conservação da Energa Mecânca Prof. Elvs Soares 1 Energa Potencal A energa potencal é o nome dado a forma
MECÂNICA CLÁSSICA. AULA N o 7. Teorema de Liouville Fluxo no Espaço de Fases Sistemas Caóticos Lagrangeano com Potencial Vetor
 1 MECÂNICA CLÁSSICA AULA N o 7 Teorema de Louvlle Fluo no Espaço de Fases Sstemas Caótcos Lagrangeano com Potencal Vetor Voltando mas uma ve ao assunto das les admssíves na Físca, acrescentamos que, nos
1 MECÂNICA CLÁSSICA AULA N o 7 Teorema de Louvlle Fluo no Espaço de Fases Sstemas Caótcos Lagrangeano com Potencal Vetor Voltando mas uma ve ao assunto das les admssíves na Físca, acrescentamos que, nos
Implementação Bayesiana
 Implementação Bayesana Defnção 1 O perfl de estratégas s.) = s 1.),..., s I.)) é um equlíbro Nash-Bayesano do mecansmo Γ = S 1,..., S I, g.)) se, para todo e todo θ Θ, u gs θ ), s θ )), θ ) θ Eθ u gŝ,
Implementação Bayesana Defnção 1 O perfl de estratégas s.) = s 1.),..., s I.)) é um equlíbro Nash-Bayesano do mecansmo Γ = S 1,..., S I, g.)) se, para todo e todo θ Θ, u gs θ ), s θ )), θ ) θ Eθ u gŝ,
Experiência V (aulas 08 e 09) Curvas características
 Experênca (aulas 08 e 09) Curvas característcas 1. Objetvos 2. Introdução 3. Procedmento expermental 4. Análse de dados 5. Referêncas 1. Objetvos Como no expermento anteror, remos estudar a adequação de
Experênca (aulas 08 e 09) Curvas característcas 1. Objetvos 2. Introdução 3. Procedmento expermental 4. Análse de dados 5. Referêncas 1. Objetvos Como no expermento anteror, remos estudar a adequação de
3 A técnica de computação intensiva Bootstrap
 A técnca de computação ntensva ootstrap O termo ootstrap tem orgem na expressão de língua nglesa lft oneself by pullng hs/her bootstrap, ou seja, alguém levantar-se puxando seu própro cadarço de bota.
A técnca de computação ntensva ootstrap O termo ootstrap tem orgem na expressão de língua nglesa lft oneself by pullng hs/her bootstrap, ou seja, alguém levantar-se puxando seu própro cadarço de bota.
Capítulo 2. APROXIMAÇÕES NUMÉRICAS 1D EM MALHAS UNIFORMES
 Capítulo. Aproxmações numércas 1D em malhas unformes 9 Capítulo. AROXIMAÇÕS NUMÉRICAS 1D M MALHAS UNIFORMS O prncípo fundamental do método das dferenças fntas (MDF é aproxmar através de expressões algébrcas
Capítulo. Aproxmações numércas 1D em malhas unformes 9 Capítulo. AROXIMAÇÕS NUMÉRICAS 1D M MALHAS UNIFORMS O prncípo fundamental do método das dferenças fntas (MDF é aproxmar através de expressões algébrcas
ANÁLISE DINÂMICA DE SISTEMAS CONTÍNUOS
 ANÁISE DINÂMICA DE SISTEMAS CONTÍNUOS INTRODUÇÃO Sstemas dscretos e sstemas contínuos representam modelos matemátcos dstntos de sstemas fsícos semelhantes, com característcas dnâmcas semelhantes Os sstemas
ANÁISE DINÂMICA DE SISTEMAS CONTÍNUOS INTRODUÇÃO Sstemas dscretos e sstemas contínuos representam modelos matemátcos dstntos de sstemas fsícos semelhantes, com característcas dnâmcas semelhantes Os sstemas
Atividade em Soluções Eletrolíticas
 Modelo de solução eletrolítca segundo Debye-Hückel. - A le lmte de Debye-Hückel (LLDH) tem o lmte que está em: I 0,01. log z.z A I 1/ valêncas do íons + e do eletrólto I 1 [ z b / b ] constante que depende
Modelo de solução eletrolítca segundo Debye-Hückel. - A le lmte de Debye-Hückel (LLDH) tem o lmte que está em: I 0,01. log z.z A I 1/ valêncas do íons + e do eletrólto I 1 [ z b / b ] constante que depende
Associação entre duas variáveis quantitativas
 Exemplo O departamento de RH de uma empresa deseja avalar a efcáca dos testes aplcados para a seleção de funconáros. Para tanto, fo sorteada uma amostra aleatóra de 50 funconáros que fazem parte da empresa
Exemplo O departamento de RH de uma empresa deseja avalar a efcáca dos testes aplcados para a seleção de funconáros. Para tanto, fo sorteada uma amostra aleatóra de 50 funconáros que fazem parte da empresa
CAPÍTULO VI Introdução ao Método de Elementos Finitos (MEF)
 PMR 40 - Mecânca Computaconal CAPÍTULO VI Introdução ao Método de Elementos Fntos (MEF). Formulação Teórca - MEF em uma dmensão Consderemos a equação abao que representa a dstrbução de temperatura na barra
PMR 40 - Mecânca Computaconal CAPÍTULO VI Introdução ao Método de Elementos Fntos (MEF). Formulação Teórca - MEF em uma dmensão Consderemos a equação abao que representa a dstrbução de temperatura na barra
CURSO A DISTÂNCIA DE GEOESTATÍSTICA
 CURSO A DISTÂNCIA DE GEOESTATÍSTICA Aula 6: Estaconardade e Semvarânca: Estaconardade de a. ordem, Hpótese ntríseca, Hpótese de krgagem unversal, Crtéros para escolha, Verfcação, Representatvdade espacal,
CURSO A DISTÂNCIA DE GEOESTATÍSTICA Aula 6: Estaconardade e Semvarânca: Estaconardade de a. ordem, Hpótese ntríseca, Hpótese de krgagem unversal, Crtéros para escolha, Verfcação, Representatvdade espacal,
Capítulo 24: Potencial Elétrico
 Capítulo 24: Potencal Energa Potencal Elétrca Potencal Superfíces Equpotencas Cálculo do Potencal a Partr do Campo Potencal Produzdo por uma Carga Pontual Potencal Produzdo por um Grupo de Cargas Pontuas
Capítulo 24: Potencal Energa Potencal Elétrca Potencal Superfíces Equpotencas Cálculo do Potencal a Partr do Campo Potencal Produzdo por uma Carga Pontual Potencal Produzdo por um Grupo de Cargas Pontuas
O problema da superdispersão na análise de dados de contagens
 O problema da superdspersão na análse de dados de contagens 1 Uma das restrções mpostas pelas dstrbuções bnomal e Posson, aplcadas usualmente na análse de dados dscretos, é que o parâmetro de dspersão
O problema da superdspersão na análse de dados de contagens 1 Uma das restrções mpostas pelas dstrbuções bnomal e Posson, aplcadas usualmente na análse de dados dscretos, é que o parâmetro de dspersão
R X. X(s) Y Y(s) Variáveis aleatórias discretas bidimensionais
 30 Varáves aleatóras bdmensonas Sea ε uma experênca aleatóra e S um espaço amostral assocado a essa experênca. Seam X X(s) e Y Y(s) duas funções cada uma assocando um número real a cada resultado s S.
30 Varáves aleatóras bdmensonas Sea ε uma experênca aleatóra e S um espaço amostral assocado a essa experênca. Seam X X(s) e Y Y(s) duas funções cada uma assocando um número real a cada resultado s S.
O problema da superdispersão na análise de dados de contagens
 O problema da superdspersão na análse de dados de contagens 1 Uma das restrções mpostas pelas dstrbuções bnomal e Posson, aplcadas usualmente na análse de dados dscretos, é que o parâmetro de dspersão
O problema da superdspersão na análse de dados de contagens 1 Uma das restrções mpostas pelas dstrbuções bnomal e Posson, aplcadas usualmente na análse de dados dscretos, é que o parâmetro de dspersão
Equações de Bloch. Richard H. Chaviguri November 27, 2017
 INSTITUTO DE FÍSICA DE SÃO CARLOS-USP Equações de Bloch Rchard H. Chavgur November 7, 017 1 INTRODUÇÃO O estudo da nteração radação-matéra abrange dversos processos tas como: absorçao, ndução tanto espontânea
INSTITUTO DE FÍSICA DE SÃO CARLOS-USP Equações de Bloch Rchard H. Chavgur November 7, 017 1 INTRODUÇÃO O estudo da nteração radação-matéra abrange dversos processos tas como: absorçao, ndução tanto espontânea
MODELOS DE REGRESSÃO PARAMÉTRICOS
 MODELOS DE REGRESSÃO PARAMÉTRICOS Às vezes é de nteresse nclur na análse, característcas dos ndvíduos que podem estar relaconadas com o tempo de vda. Estudo de nsufcênca renal: verfcar qual o efeto da
MODELOS DE REGRESSÃO PARAMÉTRICOS Às vezes é de nteresse nclur na análse, característcas dos ndvíduos que podem estar relaconadas com o tempo de vda. Estudo de nsufcênca renal: verfcar qual o efeto da
5 Métodos de cálculo do limite de retenção em função da ruína e do capital inicial
 5 Métodos de cálculo do lmte de retenção em função da ruína e do captal ncal Nesta dssertação serão utlzados dos métodos comparatvos de cálculo de lmte de retenção, onde ambos consderam a necessdade de
5 Métodos de cálculo do lmte de retenção em função da ruína e do captal ncal Nesta dssertação serão utlzados dos métodos comparatvos de cálculo de lmte de retenção, onde ambos consderam a necessdade de
Programa do Curso. Sistemas Inteligentes Aplicados. Análise e Seleção de Variáveis. Análise e Seleção de Variáveis. Carlos Hall
 Sstemas Intelgentes Aplcados Carlos Hall Programa do Curso Lmpeza/Integração de Dados Transformação de Dados Dscretzação de Varáves Contínuas Transformação de Varáves Dscretas em Contínuas Transformação
Sstemas Intelgentes Aplcados Carlos Hall Programa do Curso Lmpeza/Integração de Dados Transformação de Dados Dscretzação de Varáves Contínuas Transformação de Varáves Dscretas em Contínuas Transformação
Dinâmica do Movimento de Rotação
 Dnâmca do Movmento de Rotação - ntrodução Neste Capítulo vamos defnr uma nova grandeza físca, o torque, que descreve a ação gratóra ou o efeto de rotação de uma força. Verfcaremos que o torque efetvo que
Dnâmca do Movmento de Rotação - ntrodução Neste Capítulo vamos defnr uma nova grandeza físca, o torque, que descreve a ação gratóra ou o efeto de rotação de uma força. Verfcaremos que o torque efetvo que
Departamento de Informática. Modelagem Analítica do Desempenho de Sistemas de Computação. Modelagem Analítica. Disciplina: Variável Aleatória
 Departamento de Informátca Dscplna: do Desempenho de Sstemas de Computação Varável leatóra Prof. Sérgo Colcher colcher@nf.puc-ro.br Varável leatóra eal O espaço de amostras Ω fo defndo como o conjunto
Departamento de Informátca Dscplna: do Desempenho de Sstemas de Computação Varável leatóra Prof. Sérgo Colcher colcher@nf.puc-ro.br Varável leatóra eal O espaço de amostras Ω fo defndo como o conjunto
5 Relação entre Análise Limite e Programação Linear 5.1. Modelo Matemático para Análise Limite
 5 Relação entre Análse Lmte e Programação Lnear 5.. Modelo Matemátco para Análse Lmte Como fo explcado anterormente, a análse lmte oferece a facldade para o cálculo da carga de ruptura pelo fato de utlzar
5 Relação entre Análse Lmte e Programação Lnear 5.. Modelo Matemátco para Análse Lmte Como fo explcado anterormente, a análse lmte oferece a facldade para o cálculo da carga de ruptura pelo fato de utlzar
2003/2004. então o momento total das forças exercidas sobre o sistema é dado por. F ij = r i F (e)
 Resolução da Frequênca de Mecânca Clássca I/Mecânca Clássca 2003/2004 I Consdere um sstema de N partículas de massas m, =,..., N. a Demonstre que, se a força nterna exercda sobre a partícula pela partícula
Resolução da Frequênca de Mecânca Clássca I/Mecânca Clássca 2003/2004 I Consdere um sstema de N partículas de massas m, =,..., N. a Demonstre que, se a força nterna exercda sobre a partícula pela partícula
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ 1 É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ 1 É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Ao se calcular a média, moda e mediana, temos: Quanto mais os dados variam, menos representativa é a média.
 Estatístca Dscplna de Estatístca 0/ Curso de Admnstração em Gestão Públca Profª. Me. Valéra Espíndola Lessa e-mal: lessavalera@gmal.com Meddas de Dspersão Indcam se os dados estão, ou não, prómos uns dos
Estatístca Dscplna de Estatístca 0/ Curso de Admnstração em Gestão Públca Profª. Me. Valéra Espíndola Lessa e-mal: lessavalera@gmal.com Meddas de Dspersão Indcam se os dados estão, ou não, prómos uns dos
APLICAÇÃO DO MÉTODO DAS DIFERENÇAS FINITAS PARA SOLUÇÃO DAS EQUAÇÕES DE LAPLACE E POISSON PARA LINHAS DE MICROFITAS ACOPLADAS
 APLICAÇÃO DO MÉTODO DAS DIFERENÇAS FINITAS PARA SOLUÇÃO DAS EQUAÇÕES DE LAPLACE E POISSON PARA LINHAS DE MICROFITAS ACOPLADAS Raann Pablo de Alencar AZEEDO; Ícaro Bezerra de Queroz ARAÚJO; Elel Pogg dos
APLICAÇÃO DO MÉTODO DAS DIFERENÇAS FINITAS PARA SOLUÇÃO DAS EQUAÇÕES DE LAPLACE E POISSON PARA LINHAS DE MICROFITAS ACOPLADAS Raann Pablo de Alencar AZEEDO; Ícaro Bezerra de Queroz ARAÚJO; Elel Pogg dos
3 Animação de fluidos com SPH
 3 Anmação de fludos com SPH O SPH (Smoothed Partcle Hydrodynamcs) é um método Lagrangeano baseado em partículas, proposto orgnalmente para smulação de problemas astrofíscos por Gngold e Monaghan (1977)
3 Anmação de fludos com SPH O SPH (Smoothed Partcle Hydrodynamcs) é um método Lagrangeano baseado em partículas, proposto orgnalmente para smulação de problemas astrofíscos por Gngold e Monaghan (1977)
Curso de extensão, MMQ IFUSP, fevereiro/2014. Alguns exercício básicos
 Curso de extensão, MMQ IFUSP, feverero/4 Alguns exercíco báscos I Exercícos (MMQ) Uma grandeza cujo valor verdadero x é desconhecdo, fo medda três vezes, com procedmentos expermentas dêntcos e, portanto,
Curso de extensão, MMQ IFUSP, feverero/4 Alguns exercíco báscos I Exercícos (MMQ) Uma grandeza cujo valor verdadero x é desconhecdo, fo medda três vezes, com procedmentos expermentas dêntcos e, portanto,
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ Em mutas stuações duas ou mas varáves estão relaconadas e surge então a necessdade de determnar a natureza deste relaconamento. A análse
Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ Em mutas stuações duas ou mas varáves estão relaconadas e surge então a necessdade de determnar a natureza deste relaconamento. A análse
Método do limite superior
 Introdução O método do lmte superor é uma alternata analítca apromada aos métodos completos (e: método das lnhas de escorregamento) que possu um domíno de aplcabldade muto asto e que permte obter alores
Introdução O método do lmte superor é uma alternata analítca apromada aos métodos completos (e: método das lnhas de escorregamento) que possu um domíno de aplcabldade muto asto e que permte obter alores
Dados ajustáveis a uma linha recta
 Capítulo VI juste dos Mínmos Quadrados Dados ajustáves a uma lnha recta Determnação das constantes e B Incerteza nas meddas de Incerteza na determnação de e B juste dos mínmos quadrados a outras curvas:
Capítulo VI juste dos Mínmos Quadrados Dados ajustáves a uma lnha recta Determnação das constantes e B Incerteza nas meddas de Incerteza na determnação de e B juste dos mínmos quadrados a outras curvas:
2 Agregação Dinâmica de Modelos de Turbinas e Reguladores de Velocidade: Teoria
 Agregação Dnâmca de Modelos de urbnas e Reguladores de elocdade: eora. Introdução O objetvo da agregação dnâmca de turbnas e reguladores de velocdade é a obtenção dos parâmetros do modelo equvalente, dados
Agregação Dnâmca de Modelos de urbnas e Reguladores de elocdade: eora. Introdução O objetvo da agregação dnâmca de turbnas e reguladores de velocdade é a obtenção dos parâmetros do modelo equvalente, dados
2010 The McGraw-Hill Companies, Inc. All rights reserved. Prof.: Anastácio Pinto Gonçalves Filho
 rof.: nastáco nto Gonçalves lho Introdução Nem sempre é possível tratar um corpo como uma únca partícula. Em geral, o tamanho do corpo e os pontos de aplcação específcos de cada uma das forças que nele
rof.: nastáco nto Gonçalves lho Introdução Nem sempre é possível tratar um corpo como uma únca partícula. Em geral, o tamanho do corpo e os pontos de aplcação específcos de cada uma das forças que nele
Faculdade de Engenharia Optimização. Prof. Doutor Engº Jorge Nhambiu
 Programação Lnear (PL) Aula : Dualdade. Defnção do Problema Dual. Defnção do problema dual. O que é dualdade em Programação Lnear? Dualdade sgnfca a exstênca de um outro problema de PL, assocado a cada
Programação Lnear (PL) Aula : Dualdade. Defnção do Problema Dual. Defnção do problema dual. O que é dualdade em Programação Lnear? Dualdade sgnfca a exstênca de um outro problema de PL, assocado a cada
Trabalho e Energia. Curso de Física Básica - Mecânica J.R. Kaschny (2005)
 Trabalho e Energa Curso de Físca Básca - Mecânca J.R. Kaschny (5) Lembrando nosso epermento de queda lvre... z z 1 v t 1 z = z - v t - gt ( ) z- z v = g = t Contudo, se consderarmos obtemos: v z z 1 t
Trabalho e Energa Curso de Físca Básca - Mecânca J.R. Kaschny (5) Lembrando nosso epermento de queda lvre... z z 1 v t 1 z = z - v t - gt ( ) z- z v = g = t Contudo, se consderarmos obtemos: v z z 1 t
UNIDADE IV DELINEAMENTO INTEIRAMENTE CASUALIZADO (DIC)
 UNDADE V DELNEAMENTO NTERAMENTE CASUALZADO (DC) CUABÁ, MT 015/ PROF.: RÔMULO MÔRA romulomora.webnode.com 1. NTRODUÇÃO Este delneamento apresenta como característca prncpal a necessdade de homogenedade
UNDADE V DELNEAMENTO NTERAMENTE CASUALZADO (DC) CUABÁ, MT 015/ PROF.: RÔMULO MÔRA romulomora.webnode.com 1. NTRODUÇÃO Este delneamento apresenta como característca prncpal a necessdade de homogenedade
Estatística Quântica Gás de Fermi
 Unversdade de São Paulo Monografa Estatístca Quântca Gás de Ferm André Hernandes Alves Malavaz SFI5814 - Físca Atômca e Molecular, 17- de novembro de 17 Monografa Físca Atômca e Molecular Estatístca Quântca
Unversdade de São Paulo Monografa Estatístca Quântca Gás de Ferm André Hernandes Alves Malavaz SFI5814 - Físca Atômca e Molecular, 17- de novembro de 17 Monografa Físca Atômca e Molecular Estatístca Quântca
Procedimento Recursivo do Método dos Elementos de Contorno Aplicado em Problemas de Poisson
 Trabalho apresentado no III CMAC - SE, Vtóra-ES, 015. Proceedng Seres of the Brazlan Socety of Computatonal and Appled Mathematcs Procedmento Recursvo do Método dos Elementos de Contorno Aplcado em Problemas
Trabalho apresentado no III CMAC - SE, Vtóra-ES, 015. Proceedng Seres of the Brazlan Socety of Computatonal and Appled Mathematcs Procedmento Recursvo do Método dos Elementos de Contorno Aplcado em Problemas
4.1 Modelagem dos Resultados Considerando Sazonalização
 30 4 METODOLOGIA 4.1 Modelagem dos Resultados Consderando Sazonalzação A sazonalzação da quantdade de energa assegurada versus a quantdade contratada unforme, em contratos de fornecmento de energa elétrca,
30 4 METODOLOGIA 4.1 Modelagem dos Resultados Consderando Sazonalzação A sazonalzação da quantdade de energa assegurada versus a quantdade contratada unforme, em contratos de fornecmento de energa elétrca,
A de nição do operador derivada, em coordenadas cartesianas ortogonais é dada por. + r i^e i i ; i =
 1 Segunda aula Lucana Eban luc.eban@gmal.com Sumáro: 1. Operador Dferencal; 2. Grandente de uma função escalar; 3. Dvergente de um vetor; 4. Rotaconal de um vetor; 5. Laplacano; 6. Algumas dentdades; 7.
1 Segunda aula Lucana Eban luc.eban@gmal.com Sumáro: 1. Operador Dferencal; 2. Grandente de uma função escalar; 3. Dvergente de um vetor; 4. Rotaconal de um vetor; 5. Laplacano; 6. Algumas dentdades; 7.
CAPÍTULO 2 DESCRIÇÃO DE DADOS ESTATÍSTICA DESCRITIVA
 CAPÍTULO DESCRIÇÃO DE DADOS ESTATÍSTICA DESCRITIVA. A MÉDIA ARITMÉTICA OU PROMÉDIO Defnção: é gual a soma dos valores do grupo de dados dvdda pelo número de valores. X x Soma dos valores de x número de
CAPÍTULO DESCRIÇÃO DE DADOS ESTATÍSTICA DESCRITIVA. A MÉDIA ARITMÉTICA OU PROMÉDIO Defnção: é gual a soma dos valores do grupo de dados dvdda pelo número de valores. X x Soma dos valores de x número de
ANÁLISE DAS TENSÕES TÉRMICAS EM MATERIAIS CERÂMICOS. Palavras-chave: Tensões térmicas, Propriedades variáveis, Condução de calor, GITT
 ANÁLISE DAS TENSÕES TÉRMICAS EM MATERIAIS CERÂMICOS Dnz, L.S. Santos, C.A.C. Lma, J.A. Unversdade Federal da Paraíba Laboratóro de Energa Solar LES/DTM/CT/UFPB 5859-9 - João Pessoa - PB, Brasl e-mal: cabral@les.ufpb.br
ANÁLISE DAS TENSÕES TÉRMICAS EM MATERIAIS CERÂMICOS Dnz, L.S. Santos, C.A.C. Lma, J.A. Unversdade Federal da Paraíba Laboratóro de Energa Solar LES/DTM/CT/UFPB 5859-9 - João Pessoa - PB, Brasl e-mal: cabral@les.ufpb.br
D- MÉTODO DAS APROXIMAÇÕES SUCESSIVAS
 D- MÉTODO DAS APROXIMAÇÕES SUCESSIVAS O método das apromações sucessvas é um método teratvo que se basea na aplcação de uma fórmula de recorrênca que, sendo satsfetas determnadas condções de convergênca,
D- MÉTODO DAS APROXIMAÇÕES SUCESSIVAS O método das apromações sucessvas é um método teratvo que se basea na aplcação de uma fórmula de recorrênca que, sendo satsfetas determnadas condções de convergênca,
Ao se calcular a média, moda e mediana, temos: Quanto mais os dados variam, menos representativa é a média.
 Estatístca Dscplna de Estatístca 0/ Curso Superor de tecnólogo em Gestão Ambental Profª. Me. Valéra Espíndola Lessa e-mal: lessavalera@gmal.com Meddas de Dspersão Indcam se os dados estão, ou não, prómos
Estatístca Dscplna de Estatístca 0/ Curso Superor de tecnólogo em Gestão Ambental Profª. Me. Valéra Espíndola Lessa e-mal: lessavalera@gmal.com Meddas de Dspersão Indcam se os dados estão, ou não, prómos
Representação e Descrição de Regiões
 Depos de uma magem ter sdo segmentada em regões é necessáro representar e descrever cada regão para posteror processamento A escolha da representação de uma regão envolve a escolha dos elementos que são
Depos de uma magem ter sdo segmentada em regões é necessáro representar e descrever cada regão para posteror processamento A escolha da representação de uma regão envolve a escolha dos elementos que são
7 - Distribuição de Freqüências
 7 - Dstrbução de Freqüêncas 7.1 Introdução Em mutas áreas há uma grande quantdade de nformações numércas que precsam ser dvulgadas de forma resumda. O método mas comum de resumr estes dados numércos consste
7 - Dstrbução de Freqüêncas 7.1 Introdução Em mutas áreas há uma grande quantdade de nformações numércas que precsam ser dvulgadas de forma resumda. O método mas comum de resumr estes dados numércos consste
Cap. 11 Correlação e Regressão
 Estatístca para Cursos de Engenhara e Informátca Pedro Alberto Barbetta / Marcelo Menezes Res / Antono Cezar Borna São Paulo: Atlas, 2004 Cap. 11 Correlação e Regressão APOIO: Fundação de Apoo à Pesqusa
Estatístca para Cursos de Engenhara e Informátca Pedro Alberto Barbetta / Marcelo Menezes Res / Antono Cezar Borna São Paulo: Atlas, 2004 Cap. 11 Correlação e Regressão APOIO: Fundação de Apoo à Pesqusa
INTRODUÇÃO À CALIBRAÇÃO MULTIVARIADA
 INTRODUÇÃO À CALIBRAÇÃO MULTIVARIADA APLICAÇÃO NO CONTROLE DE QUALIDADE DE FÁRMACOS Prof. Dr. Marcelo Martns de Sena MÓDULO 04 Undade Unverstára de Cêncas Eatas e Tecnológcas UnUCET Anápols 1 MÓDULO 04
INTRODUÇÃO À CALIBRAÇÃO MULTIVARIADA APLICAÇÃO NO CONTROLE DE QUALIDADE DE FÁRMACOS Prof. Dr. Marcelo Martns de Sena MÓDULO 04 Undade Unverstára de Cêncas Eatas e Tecnológcas UnUCET Anápols 1 MÓDULO 04
4 Sistemas de partículas
 4 Sstemas de partículas Nota: será feta a segunte convenção: uma letra em bold representa um vector,.e. b b Nesta secção estudaremos a generalzação das les de Newton a um sstema de váras partículas e as
4 Sstemas de partículas Nota: será feta a segunte convenção: uma letra em bold representa um vector,.e. b b Nesta secção estudaremos a generalzação das les de Newton a um sstema de váras partículas e as
Deformações na Notação Indicial
 SEÇÃO DE ENSINO DE ENGENHARIA DE FORTIFICAÇÃO E CONSTRUÇÃO Pós-gradação em Engenhara de Transportes Deformações na Notação Indcal MAJ MONIZ DE ARAGÃO Campo de deslocamentos; Componentes de deformação;
SEÇÃO DE ENSINO DE ENGENHARIA DE FORTIFICAÇÃO E CONSTRUÇÃO Pós-gradação em Engenhara de Transportes Deformações na Notação Indcal MAJ MONIZ DE ARAGÃO Campo de deslocamentos; Componentes de deformação;
Gráficos de Controle para Processos Autocorrelacionados
 Gráfcos de Controle para Processos Autocorrelaconados Gráfco de controle de Shewhart: observações ndependentes e normalmente dstrbuídas. Shewhart ao crar os gráfcos de controle não exgu que os dados fossem
Gráfcos de Controle para Processos Autocorrelaconados Gráfco de controle de Shewhart: observações ndependentes e normalmente dstrbuídas. Shewhart ao crar os gráfcos de controle não exgu que os dados fossem
Teoria Elementar da Probabilidade
 10 Teora Elementar da Probabldade MODELOS MATEMÁTICOS DETERMINÍSTICOS PROBABILÍSTICOS PROCESSO (FENÓMENO) ALEATÓRIO - Quando o acaso nterfere na ocorrênca de um ou mas dos resultados nos quas tal processo
10 Teora Elementar da Probabldade MODELOS MATEMÁTICOS DETERMINÍSTICOS PROBABILÍSTICOS PROCESSO (FENÓMENO) ALEATÓRIO - Quando o acaso nterfere na ocorrênca de um ou mas dos resultados nos quas tal processo
Ajuste dos Mínimos Quadrados
 TLF 00/ Cap. IX juste dos mínmos quadrados Capítulo IX juste dos Mínmos Quadrados 9.. juste de uma lnha recta a dados epermentas 9 9.. Determnação dos parâmetros da recta, e B (Incertezas apenas em e guas
TLF 00/ Cap. IX juste dos mínmos quadrados Capítulo IX juste dos Mínmos Quadrados 9.. juste de uma lnha recta a dados epermentas 9 9.. Determnação dos parâmetros da recta, e B (Incertezas apenas em e guas
EXERCÍCIO: VIA EXPRESSA CONTROLADA
 EXERCÍCIO: VIA EXPRESSA CONTROLADA Engenhara de Tráfego Consdere o segmento de va expressa esquematzado abaxo, que apresenta problemas de congestonamento no pco, e os dados a segur apresentados: Trechos
EXERCÍCIO: VIA EXPRESSA CONTROLADA Engenhara de Tráfego Consdere o segmento de va expressa esquematzado abaxo, que apresenta problemas de congestonamento no pco, e os dados a segur apresentados: Trechos
Problemas Propostos. Frações mássicas, volúmicas ou molares. Estequiometria.
 Elementos de Engenhara Químca I II. Frações e Estequometra (problemas resolvdos) Problemas Propostos. Frações másscas, volúmcas ou molares. Estequometra.. Em 5 moles de Benzeno (C 6 H 6 ) quanto é que
Elementos de Engenhara Químca I II. Frações e Estequometra (problemas resolvdos) Problemas Propostos. Frações másscas, volúmcas ou molares. Estequometra.. Em 5 moles de Benzeno (C 6 H 6 ) quanto é que
Sempre que surgir uma dúvida quanto à utilização de um instrumento ou componente, o aluno deverá consultar o professor para esclarecimentos.
 Nesse prátca, estudaremos a potênca dsspada numa resstênca de carga, em função da resstênca nterna da fonte que a almenta. Veremos o Teorema da Máxma Transferênca de Potênca, que dz que a potênca transferda
Nesse prátca, estudaremos a potênca dsspada numa resstênca de carga, em função da resstênca nterna da fonte que a almenta. Veremos o Teorema da Máxma Transferênca de Potênca, que dz que a potênca transferda
18 e 20/Abr/2016 Aulas 12 e 13. Introdução à Física Estatística Postulados Equilíbrio térmico Função de Partição; propriedades termodinâmicas
 01/Abr/2016 Aula 11 Potencas termodnâmcos Energa nterna total Entalpa Energas lvres de Helmholtz e de Gbbs Relações de Maxwell 18 e 20/Abr/2016 Aulas 12 e 13 Introdução à Físca Estatístca Postulados Equlíbro
01/Abr/2016 Aula 11 Potencas termodnâmcos Energa nterna total Entalpa Energas lvres de Helmholtz e de Gbbs Relações de Maxwell 18 e 20/Abr/2016 Aulas 12 e 13 Introdução à Físca Estatístca Postulados Equlíbro
NOTA II TABELAS E GRÁFICOS
 Depto de Físca/UFMG Laboratóro de Fundamentos de Físca NOTA II TABELAS E GRÁFICOS II.1 - TABELAS A manera mas adequada na apresentação de uma sére de meddas de um certo epermento é através de tabelas.
Depto de Físca/UFMG Laboratóro de Fundamentos de Físca NOTA II TABELAS E GRÁFICOS II.1 - TABELAS A manera mas adequada na apresentação de uma sére de meddas de um certo epermento é através de tabelas.
ESTUDO DA MÁQUINA SIMÉTRICA TRIFÁSICA
 CAPÍTUO ETUDO DA ÁQUINA IÉTICA TIFÁICA. INTODUÇÃO A máquna de ndução trfásca com rotor bobnado é smétrca. Apresenta estruturas magnétcas clíndrcas tanto no rotor quanto no estator. Os enrolamentos, tanto
CAPÍTUO ETUDO DA ÁQUINA IÉTICA TIFÁICA. INTODUÇÃO A máquna de ndução trfásca com rotor bobnado é smétrca. Apresenta estruturas magnétcas clíndrcas tanto no rotor quanto no estator. Os enrolamentos, tanto
Sistemas Reticulados
 9//6 EF6 EF6 Estruturas na rqutetura I I - Sstemas Retculados Estruturas na rqutetura I Sstemas Retculados E-US FU-US Estruturas Hperestátcas Sstemas Retculados & ão-lneardade do omportamento Estrutural
9//6 EF6 EF6 Estruturas na rqutetura I I - Sstemas Retculados Estruturas na rqutetura I Sstemas Retculados E-US FU-US Estruturas Hperestátcas Sstemas Retculados & ão-lneardade do omportamento Estrutural
