UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL INSTITUTO DE QUÍMICA JOEL MARCIONÍLIO GONÇALVES GALVÃO
|
|
|
- Jónatas Oliveira de Sintra
- 6 Há anos
- Visualizações:
Transcrição
1 1 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL INSTITUTO DE QUÍMICA JOEL MARCIONÍLIO GONÇALVES GALVÃO SÍNTESE DE QUINAZOLINAS GRAXAS DERIVADAS DE COMPOSTOS DE BIGINELLI Porto Alegre, 2013
2 2 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL INSTITUTO DE QUÍMICA JOEL MARCIONÍLIO GONÇALVES GALVÃO SÍNTESE DE QUINAZOLINAS GRAXAS DERIVADAS DE COMPOSTOS DE BIGINELLI Trabalho de conclusão de curso apresentado junto à atividade de ensino Trabalho de Conclusão de Curso QUI do curso de química, como requisito parcial para obtenção de grau de Bacharel em Química. Prof. Dr. Dennis Russowsky Orientador Porto Alegre, 2013
3 Ao meu filho Gabriel. Não há título que compense o tempo que tivemos que ficar afastados. 3
4 4 Moro em minha própria casa, Jamais imitei ninguém E rio de todos os mestres Que nunca riram de si. (Friedrich Nietzschie)
5 5 RESUMO Algumas moléculas com núcleo pirimidínico apresentam atividade antineoplásica, devido à afinidade desse núcleo com o sítio de ligação do ATP nas proteínas quinases. Este trabalho teve como objetivo a criação de um novo tipo de moléculas híbridas, com um núcleo quinazolina ligado a uma cadeia graxa. O propósito é aumentar a solubilidade lipídica dessas moléculas para explorar sua atividade em tecidos que os medicamentos atuais não conseguem alcançar. A reação foi feita em quatro etapas, partindo de um composto de Biginelli, através de metodologias descritas na literatura. Na primeira etapa foi feito a síntese dos compostos de Biginelli; em seguida esses compostos foram oxidados com persulfato de potássio; o produto oxidado foi tratado com POCl3 para formar 2-cloro pirimidinas; na última etapa, foi feita a substituição do cloro por uma amina graxa. A etapa de oxidação foi aperfeiçoada, resultando em melhores rendimentos que os obtidos através do protocolo descrito na literatura. A caracterização por RMN- 1 H e RMN- 13 C indicam que molécula alvo foi obtida. O produto será encaminhado para testes biológicos. Biginelli. Palavras-chave: Quinazolinas graxas, Pirimidinas, Antineoplástico, Derivados de
6 6 LISTA DE FIGURAS Figura 1- Inibidores de quinazolinas...10 Figura 2 - Estrutura do ATP...10 Figura 3 - DHPMs utilizadas como material de partida...16 Figura 4 - Espectro RMN- 1 H do composto 1a (Solvente: DMSO)...21 Figura 5 - Espectro RMN- 13 C do composto 1a (Solvente: DMSO)...22 Figura 6 - Espectro RMN- 1 H do composto 1b (Solvente: DMSO)...23 Figura 7 - Espectro RMN- 13 C do composto 1b (Solvente: DMSO)...24 Figura 8 - Espectro RMN- 1 H do composto 2a (Solvente: CDCl3)...26 Figura 9 - Espectro RMN- 13 C do composto 2a (Solvente: CDCl3)...27 Figura 10 - Espectro RMN- 1 H do composto 2b (Solvente CDCl3)...28 Figura 11 - Espectro RMN- 13 C do composto 2b (Solvente CDCl3)...28 Figura 12 - Espectro RMN- 1 H do composto 3a (Solvente CDCl3)...30 Figura 13 - Espectro RMN- 13 C do composto 3a (Solvente CDCl3)...31 Figura 14 - Espectro RMN- 1 H do composto 3b (Solvente: CDCl3 )...31 Figura 15 - Espectro RMN- 13 C do composto 3b (Solvente: CDCl3)...32 Figura 16 - Espectro RMN- 1 H da pirimidinona graxa (Solvente: CDCl3)...34 Figura 17 - Espectro RMN- 13 C da pirimidinona graxa (Solvente CDCl3)...35
7 7 LISTA DE ESQUEMAS Esquema 1 - Reação Multicomponente de Hantzsch...11 Esquema 2 - Reação de Behrend entre uréia e acetoacetato de etila...12 Esquema 3 - Reação de Shiff entre uréia e 2-hidroxibenzaldeído...12 Esquema 4 - Reação Multicomponente de Biginelli...12 Esquema 5 - Etapas envolvidas na conversão de di-hidropirimidin-2-ona em derivados 2- cloro pirimidinas...13 Esquema 6 Etapas envolvidas na síntese das pirimidinonas...14 Esquema 7 - Proposta de mecanismo para a síntese das DHPMs...20 Esquema 8 - Proposta de mecanismo para a oxidação das DHPMs com persulfato de potássio...25 Esquema 9 - Proposta de mecanismo para a etapa de halogenação com POCl Esquema 10 - Substituição nucleofílica do cloro pela amina...33
8 8 SUMÁRIO 1. INTRODUÇÃO REAÇÃO DE BIGINELLI OBJETIVO OBJETIVOS ESPECÍFICOS METODOLOGIA PARTE EXPERIMENTAL Procedimento geral para a síntese das 3,4-diidropirimidin-2(1H)- onas Procedimento geral para a oxidação das DHPMs Procedimento geral para a oxidação das DHPMs Procedimento geral para a substituição do cloro por uma Amina RESULTADOS E DISCUSSÃO SÍNTESE DAS DHPM S OXIDAÇÃO DAS DHPM S HALOGENAÇÃO DAS DHPMS SUBSTITUIÇÃO POR UMA AMINA GRAXA CONCLUSÕES REFERÊNCIAS...37
9 9 1. INTRODUÇÃO O termo neoplasia é utilizado para designar as formas não controladas de crescimento celular. As principais diferenças entre células neoplásicas e células normais são a perda do controle da proliferação e da divisão celular; incapacidade de diferenciação ou especialização; alterações na forma e número dos cromossomos; capacidade de invadir o tecido vizinho e perda das propriedades adesivas da membrana plasmática, que permite o reconhecimento entre as células e a inibição por contato do movimento e crescimento celular. As neoplasias podem ser classificadas, de acordo com o comportamento biológico, como benignas, limítrofes ou malignas. As neoplasias são mais conhecidas como tumores e as neoplasias malignas são comumente chamadas de câncer. Segundo a Organização Mundial de Saúde (OMS), o câncer é uma das principais causas de morte no mundo; sendo responsável por 13% dos óbitos no ano 2008, cerca de 7,8 milhões de pessoas. A OMS estima 17 milhões de mortes por câncer no ano Os principais tipos de tratamento de câncer são cirurgia, radioterapia e quimioterapia. Geralmente esses métodos são utilizados em conjunto, a cirurgia e a radioterapia são eficazes para o tratamento de tumores localizados e o tratamento com quimioterápicos é o importante para tumores espalhados. Dentre os principais tipos de quimioterápicos, destaca-se uma classe de moléculas denominadas quinasolinas, que atuam na inibição de uma família de proteínas conhecidas como proteínas quinases (Silva, et al. 2009). As proteínas quinases são enzimas que catalisam a transferência de um grupo fosforila de ATP (Adenosine triphosphate) para outras proteínas. As quinases estão envolvidas em processos de transdução de sinais onde a transferência do grupo fosforila resulta em estímulos extracelulares e intracelulares, que transmitem informações para o controle da atividade das proteínas; o processo descontrolado de crescimento celular é resultado de algum desequilíbrio na transdução de sinais, quando uma anomalia favorece alguma via de sinalização. A desregulação ou superexpressão da proteína quinase afeta o processo de comunicação celular, podendo resultar no desenvolvimento e manutenção de tumores (Fabbe, et al. 2002). Todas as proteínas quinases possuem um sítio para ligação com uma molécula de ATP; as quinasolinas se ligam a esse sítio, inibindo a atividade dessas
10 10 proteínas (Silva, et al. 2009). A figura 1 apresenta uma série de compostos que apresentam atividade inibitória da proteína quinase. Os compostos apresentados possuem um centro pirimidínico ou quinazolínico que mimetizam o grupo adenina do ATP, figura 2. É, principalmente, através desse sítio que essas moléculas se ligam às proteínas quinases. Figura 1- Inibidores de quinazolinas. Fonte: Silva, Barbara et. al., (2009).
11 11 Figura 2: Estrutura do ATP. 1.1 REAÇÃO DE BIGINELLI Em 1882, o químico alemão Arthur Hantzsch relatou uma maneira simples de preparar di-hidropiridinas (DHP s) (Tron, et al. 2011). O protocolo descrito por Hantzsch consiste em uma reação multicomponente (RMC) one-pot entre um aldeído, dois equivalentes de um composto dicarbonílico e amônia ou sais de amônio (Esquema 1). Esquema 1: Reação Multicomponente de Hantzsch. Uma década depois da descoberta de Hantzsch, o químico italiano Pietro Biginelli desenvolveu uma RMC one-pot que permite a síntese, em uma única etapa, de aza-análogos das DHP s de Hantzsch (Tron et al. 2011). Esses compostos são conhecidos atualmente como compostos de Biginelli ou di-hidropirimidinonas (DHPMs). Biginelli tinha experiência com a RMC de Hantzsch e conhecia as reações entre uréia e acetoacetato de etila (Esquema 2) e entre uréia e 2-hidroxibenzaldeído (Esquema 3) relatadas por Behrend e Schiff respectivamente (Tron et al. 2011).
12 12 Percebendo a possibilidade de uma nova RMC, ele dissolveu quantidades equivalentes de acetoacetato de etila e benzaldeído em uma solução etanólica de uréia com quantidades catalíticas de ácido clorídrico. O resultado dessa reação é a ciclocondensação dos três materiais de partida (Esquema 4). Esquema 2: Reação de Behrend entre uréia e acetoacetato de etila. Esquema 3: Reação de Shiff entre uréia e 2-hidroxibenzaldeído. Esquema 4: Reação Multicomponente de Biginelli (Florença, 1893). A reação de Biginelli permaneceu inexplorada durante décadas após sua descoberta. Atualmente se conhece uma série de DHPMs com propriedades farmacológicas importantes, a saber: atividade antiploriferativa, antiviral, antitumoral, anti-inflamatória, antifúngica, antibacteriana, antituberculose, entre outras (Sandhu, et al. 2012). Variando a estrutura dos substratos empregados, é possível obter uma infinidade de DHPMs (Figura 2). O grupo aldeído é o que permite o maior número de variações; normalmente a reação é feita com aldeídos aromáticos. O grupo acetoacetato de etila pode ser substituído por outros tipos de β-cetoésteres,
13 13 acetoamidas, β-ceto-tioésteres, β-dicetonas, entre outros. A uréia pode ser trocada por uréias substituídas, tiouréias e guanidinas (Sandhu, et al. 2012). Recentemente, vários tipos de catalisadores foram desenvolvidos, resultando em melhores rendimentos e menor tempo de reação. A reação pode ser feita com catalisadores do tipo ácido de Lewis, ácido de Bronsted, líquidos iônicos, biocatalisadores e organocatalisadores (Sandhu, et al. 2012)..
14 14 2. OBJETIVOS O objetivo desse trabalho foi a construção de pirimidinonas graxas a partir de uma série de três reações seletivas envolvendo o núcleo di-hidridropirimidin-2-ona de compostos de Biginelli. 2.1 OBJETIVOS ESPECÍFICOS Singh et al. (2011) desenvolveram um método de conversão DHPMs em pirimidinonas através de uma sequência de três reações. O esquema 5 apresenta as etapas envolvidas na transformação. Na primeira etapa, a di-hidropirimidin-2-ona é oxidada com clorocromato de piridínio (PCC); o produto resultante é tratado com oxicloreto de fósforo POCl3, produzindo 2-cloro pirimidinonas; na última etapa, o cloro é substituído por uma amina em uma reação de substituição nucleofílica bimolecular. Esquema 5: Etapas envolvidas na conversão de di-hidropirimidin-2-ona em derivados 2- cloro pirimidinas. Etapa 1: Oxidação da DHPM. Etapa 2: Formação do composto 2-cloro pirimidina.
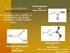
15 15 Etapa 3: Substituição nucleofílica. Memarian e Farhadi (2008) relataram uma forma de oxidar DHPMs através de uma reação radicalar regiosseletiva com persulfato de potássio K2S2O8, que é um reagente mais acessível e de menor custo que o PCC. Neste trabalho, pretende-se preparar pirimidinonas-graxas derivadas de compostos de Biginelli. O objetivo é fazer a ligação de uma amina graxa no núcleo pirimidina, com o intuito de aumentar a solubilidade lipídica dessa classe de moléculas para explorar a sua atividade em outros tecidos do corpo. O esquema 6 apresenta as reações envolvidas na síntese da pirimidinona-graxa. A oxidação é feita com persulfato de potássio e a amina utilizada na substituição é a dodecilamina. Esquema 6 Etapas envolvidas na síntese das pirimidinonas. A síntese foi feita partindo da 5-etoxicarbonil-6-metil-4-fenil-3,4-diidropirimidin- 2(1H)-ona (1a) e da 5-etoxicarbonil-6-propil-4-fenil-3,4-diidropirimidin-2(1H)-ona (1b), apresentados na figura 3.
16 Figura 3 - DHPMs utilizadas como material de partida. 16
17 17 3. METODOLOGIA 3.1 PARTE EXPERIMENTAL A caracterização dos produtos obtidos foi feita a partir de espectroscopia de ressonância magnética nuclear (RMN- 1 H) e espectroscopia de ressonância magnética de carbono 13 (RMN- 13 C). Os espectros foram obtidos em espectrômetros Varian Inova 300 e Varian VNMRs Procedimento geral para a síntese das 3,4-diidropirimidin-2(1H)-onas Para a síntese dos produtos 1a, foram adicionados, em um balão de 50 ml, 10 ml de etanol, 12 mmol de uréia, 2 mmol do catalisador cloreto de manganês, 8 mmol do aldeído e 8 mmol do β-cetoéster. A mistura reacional ficou mantida em refluxo e o progresso da reação foi acompanhado por cromatografia em camada delgada (CCD), utilizando-se placas de SiO2 para monitorar o consumo do aldeído (eluente, acetato de etila:hexano, 8:2). Os produtos foram lavados com água seguida de etanol gelado e recristalizados em etanol. O mesmo procedimento foi utilizado na síntese do composto 1b, utilizando acetonitrila como solvente em vez de etanol. O produto foi lavado com acetonitrila gelada e recristalizado em acetonitrila. 5-etoxicarbonil-6-metil-4-fenil-3,4-diidropirimidin-2(1H)-ona (1a): Sólido branco; Rendimento: 68%; 1 H (300 MHz, DMSO): δ 1.10 (t, 3H, J = 7.0 Hz, - CH3), 2.26 (s, 3H, - CH3), 3.99 (q, 2H, J = 7.1 Hz, -CO2CH2-), 5.16 (s, 1H, CH-N), 7.25 (m, 3H, Ar-H), 7.33 (m, 2H, Ar-H), 7.74 (s, -NH), 9.20 (s, -NH). 13 C NMR (75 MHz, DMSO): δ 14.54, 18.24, 54.44, 59.65, 99.74, , , , , , etoxicarbonil-6-propil-4-fenil-3,4-diidropirimidin-2(1H)-ona (1b): Sólido branco; Rendimento: 56 %; 1 H (300 MHz, CDCl3): δ 0.92 (t, 3H, J = 7.3, Hz, - CH3), 1.10 (t, 3H, J = 7.2, -CH3), 1.57 (sexteto, 2H, J = 7.5, Hz, -CH2-), 2.64 (t, 2H, -CH2-), 4.00 (q, 2H, - CH2-O), 5.16 (d, 1H, CH-NH), 7.25 (m, 3H, Ar-H), 7.32 (m, 2H, Ar-H), 7.74 (s, 1H, NH), 9.17 (s, 1H, NH). 13 C NMR (75 MHz, CDCl 3 ): δ 14.13, 18.48, 22.11, 32.80, 54.43, 59.69, 99.54, , , , ,
18 Procedimento geral para a oxidação das DHPMs Em um balão de 100 ml, foram adicionados 2 mmols da DHPM e 4 mmols de persulfato de potássio. Em seguida, foi adicionado 45 ml de acetonitrila e 9 ml de água. A temperatura da mistura foi mantida entre 71 e 73 C e o progresso da reação foi monitorado por CCD, utilizando-se placas com SiO2 para verificar o consumo da DHPM (eluente, acetato de etila:hexano, 8:2). A mistura, ainda quente, foi filtrada e a mistura de solventes foi evaporada em evaporador rotativo. O produto foi extraído do bruto com diclorometano. Repetiu-se o processo de adição de pequenas porções de diclorometano seguido de evaporação do mesmo até o produto se converter de uma goma para um sólido. No final, produto foi lavado com uma mistura de hexano e acetato de etila (4:1). 5-etoxicarbonil-6-metil-4-fenil-3,4-pirimidin-2(1H)-ona (2a): Sólido amarelo; Rendimento: 81 %; 1 H (300 MHz, CDCl3): δ 0.90 (t, 3H, J = 7.2 Hz, - CH3), 2.59 (s, 3H, -CH3), 4.02 (q, 2H, J = 7.2 Hz, -CO2CH2-), 7.43 (m, 3H, Ar-H), 7.57 (m, 2H, Ar- H), 9.91 (s, -NH). 13 C NMR (75 MHz, CDCl 3 ): δ 13.41, 19.34, 61.69, , , , , , , , , etoxicarbonil-6-propil-4-fenil-3,4-pirimidin-2(1H)-ona (2b): Sólido amarelo; Rendimento: 87 %; 1 H (300 MHz, CDCl3): δ 0.92 (t, 3H, J = 7.2 Hz, - CH3), 1.02 (t, 3H, -CH3), 1.80 (m, 2H, J = 7.2 Hz, -CH2-), 2.84 (t, 2H, -CH2-), 4.04 (q, 2H, -CH2-CO2-), 7.45 (m, Ar-H), 7.58 (m, Ar-H). 13 C NMR (75 MHz, CDCl 3 ): δ 13.41, 13.75, 22.57, 34.44, 53.44, 61.73, , , , , , , Procedimento geral para a halogenação da pirimidinona Foram adicionados 2 mmols da DHPM e 2 ml de POCl3 em um balão de 25 ml. A mistura ficou em refluxo e o progresso da reação foi monitorado por CCD, utilizandose como eluente uma mistura de hexano e acetato de etila (4:1). A mistura final foi destilada para remover o excesso de POCl3. O produto foi extraído do bruto com hexano. 2-Cloro-5-etoxicarbonil-6-metil-4-fenil-3,4-pirimidina (3a): Líquido viscoso marrom; Rendimento: 45 %; 1 H (300 MHz, CDCl 3 ): δ 1.09 (t, 3H, J = 7.2 Hz, - CH3), 2.65 (s, 3H, -CH3), 4.23 (q, 2H, J = 7.2 Hz, -CO2CH2-), 7.49 (m, 3H, Ar-H), 7.67 (m, 2H,
19 19 Ar-H). 13 C NMR (75 MHz, CDCl 3 ): δ 13.55, 22.44, 62.21, , , , , , , , , cloro-5-etoxicarbonil-6-propil-4-fenil-3,4-pirimidina (3b): Líquido viscoso marrom; Rendimento: 41 %; 1H (300 MHz, CDCl3): δ 1.01 (t, 3H, J = 7.2 Hz, -CH3), 1.06 (3H, J=, -CH3),1.81 (sexteto, 2H, -CH2-), 2.82 (q, 2H, J = 7.2 Hz, -CO2CH2-), 4.20 (m, 3H, Ar-H), 7.47 (m, 2H, Ar- H), 7.65 (m, Ar-H). 13 C NMR (75 MHz, CDCl 3 ): δ 13.55, 13.91, 22.41, 37.43, 62.20, , , , , , , , , , Procedimento geral para a substituição do cloro por uma amina Adicionou-se 0,4 mmol do composto 1c em um balão contendo 5 ml de etanol anidro e 0,8 mmol de dodecilamina. A mistura ficou mantida em refluxo durante 14 horas. O etanol foi evaporado a pressão reduzida e a mistura foi filtrada em uma coluna de sílica. Pirimidinona Graxa (3b): Líquido viscoso marrom; Rendimento: 98%. 13 C NMR (75 MHz, CDCl 3 ): δ 13.41, 13.75, 22.57, 34.44, 53.44, 61.73, , , , , , ,
20 20 4. RESULTADOS E DISCUSSÃO 4.1 SÍNTESE DAS DHPM S O esquema 7 apresenta uma proposta de mecanismo para a reação. Primeiro ocorre a adição de um dos nitrogênios da uréia ao aldeído para formar o intermediário 1, que sofre desidratação por catálise ácida na etapa seguinte para formar o intermediário imínio. A enolização do β-cetoéster é facilitada pelo ácido de Lewis e o enol resultante se adiciona ao intermediário imínio. O intermediário 3 sofre adição intramolecular, catalisada pelo ácido de Lewis, do nitrogênio do grupo uréia ao carbono da carbonila. A desidratação da estrutura cíclica formada resulta na DHPM. Esquema 7 - Proposta de mecanismo para a síntese das DHPMs. O espectro RMN-1H do composto 1a está apresentado na figura 4. O tripleto centrado em 1,10 ppm está dentro da faixa esperada para hidrogênios metílicos e correspondem aos hidrogênios metílicos do grupo éster, numerados como grupo 1. O singleto em 2,26 ppm corresponde aos hidrogênios metílicos do grupo 3, que são mais desblindados por estarem próximos a um carbono sp 2. O quarteto centrado em
21 21 3,99 ppm é referente aos hidrogênios do grupo 2, que são desblindados pelo oxigênio adjacente. O sinal em 5,17 ppm corresponde ao hidrogênio do grupo 6, que é desblindado pelo efeito de anisotropia do anel, por um nitrogênio, e um carbono sp 2 adjacentes. O multipleto entre 7,2 e 7,5 ppm pertencem aos hidrogênios do grupo benzila, que são fortemente desblindados pelo efeito de anisotropia magnética. Os sinais em 7,74 e 9,20 ppm estão na faixa esperada para hidrogênios ligados a um átomo de nitrogênio em amidas e são gerados pelos hidrogênios dos grupos 4 e 5. Figura 4 - Espectro RMN-H do composto 1a (Solvente: DMSO). A figura 5 apresenta o espectro RMN- 13 C do composto 1a. Os sinais em 14,54 ppm e 18,25 ppm estão na dentro da faixa de deslocamento químico esperada para carbonos metílicos, e pertencem aos carbonos 1 e 6, respectivamente. O carbono 6 está ligado a um carbono sp 2 e, portanto, é um pouco mais desblindado que o carbono 1. O sinal em 54,44 ppm correspondente ao carbono 8, desblindado pelo nitrogênio. Em 59,65 ppm, observa-se o sinal correspondente ao carbono 2, que é desblindado pelo oxigênio. O sinal em 99,74 ppm é referente ao carbono 4 e está dentro da faixa esperada para carbonos sp 2. Em e 128,85 ppm, encontramse dois picos intensos dos quatro carbonos orto e meta, que são duplicados por simetria. O sinal do hidrogênio para, de maior intensidade, aparece em ppm, o sinal referente ao carbono 9 aparece em ppm. O sinal em ppm
22 22 pertence ao carbono 5; esse valor está dentro da faixa esperada para compostos carbonílicos α,β-insaturados. Os sinais dos carbonos 7 e 3 aparecem dentro da faixa de deslocamento químico do grupo C=O em ésteres e amidas. O carbono 7 aparece em 152,61 ppm e o carbono 3 em 165,80 ppm. Figura 5 - Espectro RMN- 13 C do composto 1a (Solvente: DMSO). A figura 6 apresenta o espectro RMN-1H do composto 1b. Comparando com o espectro do composto 1a, verifica-se a ausência do singleto referente aos hidrogênios metílicos do grupo 3 e a presença de três novos sinais referentes a hidrogênios do grupo propila. O tripleto centrado em 0,92 ppm corresponde aos hidrogênios metílicos do grupo 5; o sexteto centrado em 1,57 ppm está dentro da faixa esperada para hidrogênios metilênicos e correspondem aos hidrogênios do grupo 4; o tripleto centrado em 2,65 ppm é referente aos hidrogênios metilênicos do grupo 3, levemente desblindados pelo carbono sp 2 e pelo carbono sp 3 adjacentes.
23 23 Figura 6 - Espectro RMN-H do composto 1b (Solvente: DMSO). O espectro de RMN-13C do composto 1b (figura 7) é semelhante ao do composto 1a. Os picos dos carbonos 1 e 8 aparecem em e ppm. Os sinais em e pertencem aos carbonos metilênicos 7 e 6, respectivamente. O carbono 6 é mais desblindado porque está ligado a um carbono sp 2. Os outros picos são análogos aos do composto 1a.
24 24 Figura 7 - Espectro RMN- 13 C do composto 1b (Solvente: DMSO). 4.2 OXIDAÇÃO DAS DHPMs A oxidação com persulfato é uma reação radicalar regiosseletiva. O hidrogênio derivado do grupo aldeído é abstraído preferencialmente pelo radical, em detrimento dos outros grupos. Essa regiosseletividade é uma consequência do efeito de estabilização por ressonância do radical pelo grupo fenila. O esquema 8 apresenta uma proposta de mecanismo para essa reação. Conforme apresentado no esquema 8, a reação começa com a cisão homolítica do persulfato por aquecimento. O radical sulfato abstrai um hidrogênio de uma molécula de água para formar um radical hidroxila. Em seguida, um radical hidroxila ou um radical sulfato abstrai o hidrogênio derivado do aldeído na DHPM. A interação entre o par de elétrons do nitrogênio e o orbital p semipreenchido do carbono radical enfraquece a ligação N-H. O hidrogênio dessa ligação é abstraído na etapa seguinte, dando origem a uma ligação dupla C=N. Embora a participação de moléculas de água no mecanismo da reação seja muito provável, a adição água é necessária apenas para a solubilização do persulfato.
25 25 Esquema 8 - Proposta de mecanismo para a oxidação das DHPMs com persulfato de potássio. Memarian e Farhadi (2008) relataram que o composto 1b pode ser obtido com um rendimento de 93% por oxidação do composto 1a com persulfato de potássio. Eles utilizaram uma mistura 10:2 de acetonitrila e água como solvente e mantiveram o sistema em refluxo por 80 minutos. No entanto, as tentativas de oxidação das DHPMs seguindo esse protocolo resultaram em rendimentos muito baixos e uma mistura de produtos de difícil separação. Na tentativa de minimizar reações laterais, algumas mudanças foram feitas no protocolo de Memarian. Para isso, minimizou-se a temperatura e o tempo da reação. A reação foi feita com o composto 1a para diferentes temperaturas e o progresso da reação foi monitorado por CCD, pelo consumo da DHPM. A cronometragem teve início quando a mistura atingiu a temperatura desejada. Nenhuma reação foi observada para temperaturas menores que 70 C durante 30 minutos. Obteve-se um rendimento de 81% quando a reação foi feita a 73 C em 13 minutos. A reação é mais rápida para temperaturas maiores que 75 C, mas resulta em rendimentos
26 26 menores. O aumento do tempo de aquecimento também provoca redução no rendimento, mesmo quando a temperatura é mantida entre 72 e 73 C. O espectro RMN-1H do composto 2a está apresentado na figura 8. A ausência de sinal em 5.17 ppm evidencia a ocorrência de oxidação. Um dos sinais do tipo NH também desaparece, o sinal da outra ligação N-H aparece em 9.91 ppm. As absorções de hidrogênios ligados a nitrogênio de grupos amida são muito variáveis e dependem da posição desse grupo na molécula, da temperatura e do solvente utilizado (Pavia, 2010). Figura 8 - Espectro RMN-H do composto 2a (Solvente: CDCl3). O espectro RMN-13C está apresentado na figura 9. O sinal do carbono se desloca para uma frequência mais alta; carbonos de ligações C=N aparecem próximos a carbonos de carbonilas. A formação de uma ligação dupla conjugada ao anel modifica o padrão dos picos dos carbonos aromáticos. Os carbonos do grupo éster não são muito afetados pela formação de uma ligação dupla, os picos desses carbonos permanecem praticamente inalterados.
27 27 Figura 9 - Espectro RMN-13C do composto 2a (Solvente: CDCl3). A figura 10 apresenta o espectro RMN- 1 H do composto 2b. A oxidação é confirmada pelo desaparecimento do sinal em 5.17 ppm. O sinal em 5.30 ppm é de cloreto de metileno, utilizado como solvente na extração. O espectro RMN- 13 C (figura 11) sofre as mesmas modificações do espectro do composto 2a. Todos os carbonos que podem ser afetados pela formação da ligação dupla foram deslocados para outra posição. Os picos dos carbonos do grupo propila e do grupo éster não se deslocaram significativamente.
28 28 Figura 10 - Espectro RMN-H do composto 2b (Solvente CDCl3). Figura 11 - Espectro RMN-13C do composto 2b (Solvente CDCl3).
29 HALOGENAÇÃO DAS PIRIMIDINONAS Uma proposta de mecanismo para a reação de halogenação é apresentada no esquema 9. A reação começa com uma adição do oxigênio da carbonila ao oxicloreto de fósforo seguido de uma substituição nucleofílica por um grupo cloreto para formar pirimidina halogenada. Esquema 9 - Proposta de mecanismo para a etapa de halogenação com POCl3. Comparando o espectro RMN- 1 H do composto 3a (figura 12) com o do composto 1a, observa-se que o singleto dos hidrogênios metílicos do grupo 3 é deslocado de 2.59 para 2.65 ppm. Esse deslocamento pode indicar a formação de um anel pirimidínico, que exerce um pequeno efeito de desblindagem por anisotropia nesses hidrogênios. O espectro não apresenta sinal do tipo N-H e, a partir da integração dos picos, observa-se que a molécula apresenta 13 hidrogênios em vez de 14, confirmando a ocorrência da reação.
30 30 Figura 12 - Espectro RMN- 1 H do composto 3a (Solvente: CDCl 3 ). A partir do espectro RMN- 13 C do composto 3a (figura 13), observa-se que os picos referentes aos carbonos 4, 5, 7 e 8 se deslocam em relação aos picos correspondentes no espectro do composto 1a. Esses carbonos são os mais afetados pela formação de um anel aromático. O sinal do carbono 6 se desloca de 19.34, no composto 2a, para 22.4 ppm; com a formação de um anel aromático, esse carbono se torna mais desblindado. Os sinais dos carbonos do grupo benzila sofrem um rearranjo no padrão dos picos. Esses carbonos são afetados pelo efeito de conjugação dos dois anéis.
31 31 Figura 13 - Espectro RMN-13C do composto 3a (Solvente CDCl3). A figura 14 apresenta o espectro RMN- 1 H do composto 3b. O espectro apresenta os sinais esperados para a estrutura desse composto. Não são observados picos referentes a hidrogênios do tipo N-H e as integrais dos picos indicam a presença de 17 hidrogênios na molécula, evidenciando a ocorrência de halogenação. Figura 14 - Espectro RMN-H do composto 3b (Solvente: CDCl3 ).
32 32 No espectro RMN- 13 C do composto 3b, também se observa um rearranjo dos picos dos carbonos benzílicos e dos carbonos envolvidos no núcleo pirimidina, em relação ao espectro do composto 1b. O sinal do carbono 6 se desloca de para ppm, em relação ao do composto 2b,devido à pequena desblindagem exercida pelo anel. Figura 15 - Espectro RMN- 13 C do composto 3b (Solvente: CDCl3). 4.4 SUBSTITUIÇÃO A última etapa desta sequência de reações é uma reação de substituição nucleofílica bimolecular SN 2 do cloro por uma amina (Esquema 10).
33 33 Esquema 10: Substituição nucleofílica do cloro pela amina. A figura 16 apresenta o espectro RMN- 1 H do produto final. O produto passou apenas por uma etapa de pré-purificação, alguns sinais do produto podem estar sobrepostos com sinais de impurezas. Os hidrogênios do grupo 1 deveriam gerar um tripleto em próximo a 0.9 ppm; no entanto, o espectro apresenta um multipleto nessa região. O sinal referente ao grupo metila provavelmente está sobreposto a esse multipleto. O sinal intenso em 1.23 ppm pertence aos hidrogênios 2 a 9 da cadeia carbônica. O grupo 9 sofre um pequeno efeito de desblindagem a longa distância pelo nitrogênio e aparece em 1.55 ppm. Observa-se o hidrogênio metílico do grupo 11 como um singleto em 2.46 ppm. Os hidrogênios do grupo 10 são desblindados pelo nitrogênio e aparecem em 3.43 ppm. O hidrogênio metilênico do grupo éster, desblindado pelo oxigênio, aparece como um quarteto em 4.02 ppm. Os hidrogênios benzílicos aparecem entre 7.37 e 7.52 ppm.
34 34 Figura 16 Espectro RMN- 1 H da pirimidina graxa (Solvente: CDCl 3 ). O espectro RMN- 13 C do produto final está apresentado na figura 17. Os picos em e são gerados pelos carbonos metílicos 1 e 18. O sinal em ppm é gerado pelo carbono 2, o sinal mais intenso, em 29,59 ppm corresponde aos carbonos mais internos da cadeia e o sinal em ppm é gerado pelo carbono 9. O sinal do carbono 10, desblindado pelo nitrogênio, aparece em ppm, o sinal em ppm corresponde ao carbono 17, desblindado pelo oxigênio. Na região acima de 110 ppm, observa-se os sinais do grupo benzila seguido dos sinais dos carbonos do anel pirimidínico e do carbono 16, que são análogos aos do espectro do composto 3a.
35 Figura 17 Espectro RMN- 13 C da pirimidinona graxa (solvente CDCl 3 ). 35
36 36 5. CONCLUSÕES As etapas de oxidação com persulfato de potássio e substituição com a amina graxa forneceram rendimentos satisfatórios. A etapa de halogenação leva a rendimentos muito baixos e ainda precisa ser melhorada. A oxidação da DHPM foi a etapa mais complicada; com este trabalho, essa etapa foi superada, podendo ser feita de forma simples em um curto intervalo de tempo. Como perspectiva, deseja-se testar essas reações para outras DHPM s e verificar a atividade Biológica dessas moléculas.
37 37 6. REFERÊNCIAS Fabbe, D. et al. Protein kinases as targets for anticancer agents: from inhibitors to useful drugs. Pharmacology & Therapeutics, v 93, p 78-79, KAPPE, O. C. Recent advances in the Biginelli dihydropyrimidine synthesis: New tricks from an old dog. Accounts of Chemical Research, Áustria, v. 33, p , Kappe, O. C. 100 Years of the Biginelli dihydropyrimidine synthesis, SYNTHESIS,Tetrahedron, Áustria, v. 49, n. 32, p , Kappe, O. C. 4-Aryldihydropyrimidines via the Biginelli Condensation: Aza-Analogs of Nifedipine-Type Calcium Channel Modulators. Molecules, Áustria, n. 3, p. 1-9, Memarian H.R., Farhadi A. Potassium peroxydisulfate as an efficient oxidizing agent for conversion of ethyl 3,4-dihydropyrimidin-2(1H)-one-5-carboxylates to their corresponding ethyl pyrimidin-2(1h)-one-5-carboxylates. Jounal of the Iranian Chemical Society, Iran, vol. 6, n. 3, p , Pavia, Donald L.; Lampman Gary M.; George S. Kriz; Vyvyan James R. Introdução à espectroscopia. 4. ed. São Paulo: Learning, Sandhu J. S. et al. Past, present and future of the Biginelli reaction: a critical perspective. Arkivoc, p , Silva, B. V. et al. Proteínas quinases: características estruturais e inibidores químicos. Quimimica Nova, v. 32, n. 2, p , Singh K. et al. An Efficacious Protocol for the Oxidation of 3,4-Dihydropyrimidin-2(1H)-ones using Pyridinium Chlorochromate as Catalyst. Australian Journal of Chemistry, índia, n. 61, p , Singh K. et al. Facile transformation of Biginelli pyrimidin-2(1h)-ones to pyrimidines. In vitro evaluation as inhibitors of Mycobacterium tuberculosis and modulators of cytostatic activity. European Journal of Medicinal Chemistry, n. 46, p , Tron G. C. et al. Pietro Biginelli: The Man Behind the Reaction. European journal of organic chemistry. p , World Health Organization. Câncer. Disponível em: < Acesso em: 13 de junho Zhang J. et al. Targeting cancer with small molecule kinase inhibitors. Nature Reviews, v.9, 2009.
Obtenção de 3,4-dihidropirimidinonas via reação de Biginelli sob catálise com um ácido de Lewis
 btenção de 3,4-dihidropirimidinonas via reação de Biginelli sob catálise com um ácido de Lewis Karina Micaelle de liveira 1* (IC), Luciana Machado Ramos 1 (PQ). * email: karinamicaelle@gmail.com 1 Universidade
btenção de 3,4-dihidropirimidinonas via reação de Biginelli sob catálise com um ácido de Lewis Karina Micaelle de liveira 1* (IC), Luciana Machado Ramos 1 (PQ). * email: karinamicaelle@gmail.com 1 Universidade
2017 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia
 217 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Classificação Tipos de reação e classes de
217 Obtenção da amida do ácido cinâmico através da reação do cloreto do ácido cinâmico com amônia O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Classificação Tipos de reação e classes de
MATERIAL SUPLEMENTAR. Benzamidoxima
 MATERIAL SUPLEMENTAR Benzamidoxima Em um erlenmeyer de 125 ml, adicionou-se 2,0 g de cloridrato de hidroxilamina (29,1 mmol), 2,4 g de carbonato de sódio (29,1 mmol) e 25 ml de água destilada a temperatura
MATERIAL SUPLEMENTAR Benzamidoxima Em um erlenmeyer de 125 ml, adicionou-se 2,0 g de cloridrato de hidroxilamina (29,1 mmol), 2,4 g de carbonato de sódio (29,1 mmol) e 25 ml de água destilada a temperatura
4001 Transesterificação do óleo de mamona em ricinoleato de metila
 4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
4002 Síntese de benzil a partir da benzoína
 4002 Síntese de benzil a partir da benzoína H + 1 / 2 2 VCl 3 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212,3) 173,3 (210,2) Classificação Tipos de reações e classes de substâncias oxidação álcool, cetona,
4002 Síntese de benzil a partir da benzoína H + 1 / 2 2 VCl 3 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212,3) 173,3 (210,2) Classificação Tipos de reações e classes de substâncias oxidação álcool, cetona,
3016 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4
 6 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4 CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Classificação
6 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4 CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Classificação
4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico
 NP 4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202,2) (23,0) (46,1) (156,2) Classificação Tipos
NP 4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202,2) (23,0) (46,1) (156,2) Classificação Tipos
Aplicação de tiazolidina-2,4-diona na síntese de arilidenos via condensação de Knoevenagel
 Aplicação de tiazolidina-2,4-diona na síntese de arilidenos via condensação de Knoevenagel Ana Caroline lopes Leal¹* (IC, PIVIC-UEG), Luciana Machado Ramos¹ (PQ) 1 UEG-CCET, Anápolis-Goiás, Brasil 1 Unidade
Aplicação de tiazolidina-2,4-diona na síntese de arilidenos via condensação de Knoevenagel Ana Caroline lopes Leal¹* (IC, PIVIC-UEG), Luciana Machado Ramos¹ (PQ) 1 UEG-CCET, Anápolis-Goiás, Brasil 1 Unidade
Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos
 UNIVERSIDADE DE SÃO PAULO USP FARMÁCIA BIOQUÍMICA 015N Reatividade de Compostos Orgânicos II Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos Beatriz In Soon Chang (9328183) João Gabriel
UNIVERSIDADE DE SÃO PAULO USP FARMÁCIA BIOQUÍMICA 015N Reatividade de Compostos Orgânicos II Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos Beatriz In Soon Chang (9328183) João Gabriel
Aula 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Espectroscopia de RMN
 Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
3003 Síntese de 2-cloro-ciclohexanol a partir de ciclohexeno
 3003 Síntese de 2-cloro-ciclohexanol a partir de ciclohexeno _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7
3003 Síntese de 2-cloro-ciclohexanol a partir de ciclohexeno _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7
PPGQTA. Prof. MGM D Oca
 PPGQTA Prof. Compostos Carbonílicos O grupo carbonila é um dos mais importantes grupos funcionais e está envolvido em muitas reações. Reações envolvendo grupos carbonila também são particularmente importantes
PPGQTA Prof. Compostos Carbonílicos O grupo carbonila é um dos mais importantes grupos funcionais e está envolvido em muitas reações. Reações envolvendo grupos carbonila também são particularmente importantes
Ressonância Magnética Nuclear
 Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
1011 Síntese do 1,4-di-terc-butil benzeno a partir do terc-butil benzeno e cloreto de terc-butila.
 1011 Síntese do 1,4-di-terc-butil benzeno a partir do terc-butil benzeno e cloreto de terc-butila. + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Classificação Tipos de Reações e
1011 Síntese do 1,4-di-terc-butil benzeno a partir do terc-butil benzeno e cloreto de terc-butila. + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Classificação Tipos de Reações e
Compostos Carbonílicos I (Ácidos carboxílicos e seus derivados) Aula 2
 Universidade Federal de Ouro Preto Compostos Carbonílicos I (Ácidos carboxílicos e seus derivados) Aula 2 Flaviane Francisco Hilário 1 1 Haletos de acila 1.1 - Preparação 2 O objetivo é converter o grupo
Universidade Federal de Ouro Preto Compostos Carbonílicos I (Ácidos carboxílicos e seus derivados) Aula 2 Flaviane Francisco Hilário 1 1 Haletos de acila 1.1 - Preparação 2 O objetivo é converter o grupo
3001 Hidroboração/oxidação de 1-octeno a 1-octanol
 3001 Hidroboração/oxidação de 1-octeno a 1-octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Referência Bibliográfica A.S. Bhanu
3001 Hidroboração/oxidação de 1-octeno a 1-octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Referência Bibliográfica A.S. Bhanu
4004 Síntese de γ-decalactona a partir de 1-octeno e éster etílico do ácido iodoacético
 NP 4004 Síntese de γ-decalactona a partir de 1-octeno e éster etílico do ácido iodoacético + I CH 2 CH 3 Cu + CH 3 CH 2 I C 8 H 16 C 4 H 7 I 2 C 10 H 18 2 (112,2) (214,0) (63,6) (170,3) C 2 H 5 I (156,0)
NP 4004 Síntese de γ-decalactona a partir de 1-octeno e éster etílico do ácido iodoacético + I CH 2 CH 3 Cu + CH 3 CH 2 I C 8 H 16 C 4 H 7 I 2 C 10 H 18 2 (112,2) (214,0) (63,6) (170,3) C 2 H 5 I (156,0)
O DIAMANTE POSSUI HIBRIDIZAÇÃO
 QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
5007 Reação do anidrido ftálico com resorcinol para obtenção de fluoresceína
 57 Reação do anidrido ftálico com resorcinol para obtenção de fluoresceína CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificação Tipos de reações e classes das substâncias
57 Reação do anidrido ftálico com resorcinol para obtenção de fluoresceína CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificação Tipos de reações e classes das substâncias
4013 Síntese de benzalacetofenona a partir de benzaldeído e acetofenona
 NP 4013 Síntese de benzalacetofenona a partir de benzaldeído e acetofenona KSF/ + + H 2 C 8 H 8 C 7 H 6 C 15 H 12 (120.2) (106.1) (208.3) Classificação Tipos de reações e classes das substâncias reação
NP 4013 Síntese de benzalacetofenona a partir de benzaldeído e acetofenona KSF/ + + H 2 C 8 H 8 C 7 H 6 C 15 H 12 (120.2) (106.1) (208.3) Classificação Tipos de reações e classes das substâncias reação
2029 Reação do trifenilfosfano com o éster metílico do ácido bromoacético originando brometo de (carbometoximetil) trifenilfosfônio
 229 Reação do trifenilfosfano com o éster metílico do ácido bromoacético originando brometo de (carbometoximetil) trifenilfosfônio CH 3 Br + P P Br C 3 H 5 Br 2 C 18 H 15 P (153,) (262,3) CH 3 C 21 H 2
229 Reação do trifenilfosfano com o éster metílico do ácido bromoacético originando brometo de (carbometoximetil) trifenilfosfônio CH 3 Br + P P Br C 3 H 5 Br 2 C 18 H 15 P (153,) (262,3) CH 3 C 21 H 2
4016 Síntese de (±)-2,2'-dihidroxi-1,1'-binaftil (1,1'-bi-2-naftol)
 4016 Síntese de (±)-2,2'-dihidroxi-1,1'-binaftil (1,1'-bi-2-naftol) FeCl 3. 6 H2 O C 10 H 7 C 20 H 14 O 2 (144,2) (270,3) (286,3) Classificação Tipos de reação e classes de substâncias acoplamento oxidativo
4016 Síntese de (±)-2,2'-dihidroxi-1,1'-binaftil (1,1'-bi-2-naftol) FeCl 3. 6 H2 O C 10 H 7 C 20 H 14 O 2 (144,2) (270,3) (286,3) Classificação Tipos de reação e classes de substâncias acoplamento oxidativo
3002 Adição de bromo ao ácido fumárico para formação de ácido meso-dibromo-succínico
 32 Adição de bromo ao ácido fumárico para formação de ácido meso-dibromo-succínico H HOOC COOH H Br 2 HOOC H Br Br H COOH C 4 H 4 O 4 (116.1) (159.8) C 4 H 4 Br 2 O 4 (275.9) Referência Bibliográfica A.
32 Adição de bromo ao ácido fumárico para formação de ácido meso-dibromo-succínico H HOOC COOH H Br 2 HOOC H Br Br H COOH C 4 H 4 O 4 (116.1) (159.8) C 4 H 4 Br 2 O 4 (275.9) Referência Bibliográfica A.
Métodos Físicos de Análise - RESSONÂNCIA MAGNÉTICA NUCLEAR. Métodos Físicos de Análise. Métodos Físicos de Análise
 - RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos Fiocruz Docente do Programa
- RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos Fiocruz Docente do Programa
3033 Síntese do ácido acetilenodicarboxílico a partir de ácido meso dibromosuccínico
 3033 Síntese do ácido acetilenodicarboxílico a partir de ácido meso dibromosuccínico HOOC H Br Br H COOH KOH HOOC COOH C 4 H 4 Br 2 O 4 C 4 H 2 O 4 (275.9) (56.1) (114.1) Classificação Tipos de reação
3033 Síntese do ácido acetilenodicarboxílico a partir de ácido meso dibromosuccínico HOOC H Br Br H COOH KOH HOOC COOH C 4 H 4 Br 2 O 4 C 4 H 2 O 4 (275.9) (56.1) (114.1) Classificação Tipos de reação
2030 Reação do brometo de (carbometoximetil) trifenilfosfônio com benzaldeído
 23 Reação do brometo de (carbometoximetil) trifenilfosfônio com benzaldeído H P Br + H NaH + H H H CH 3 + PPh 3 + NaBr CH 3 C 2 H 2 Br 2 P C 7 H 6 (45,3) (6,) (4,) C H 2 (62,2) CH 3 C 8 H 5 P (278,3) NaBr
23 Reação do brometo de (carbometoximetil) trifenilfosfônio com benzaldeído H P Br + H NaH + H H H CH 3 + PPh 3 + NaBr CH 3 C 2 H 2 Br 2 P C 7 H 6 (45,3) (6,) (4,) C H 2 (62,2) CH 3 C 8 H 5 P (278,3) NaBr
Química Orgânica Experimental I BAC CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS
 Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
6. Substituição Nucleofílica Acílica via Adição/Eliminação
 6. Substituição Nucleofílica Acílica via Adição/Eliminação 6.1. Ácidos carboxílicos e derivados: nomenclatura. 6.2. Acidez de ácidos carboxílicos 6.3. Reações de derivados de ácido carboxílicos: reatividade.
6. Substituição Nucleofílica Acílica via Adição/Eliminação 6.1. Ácidos carboxílicos e derivados: nomenclatura. 6.2. Acidez de ácidos carboxílicos 6.3. Reações de derivados de ácido carboxílicos: reatividade.
Química Orgânica. Aula 5 - Propriedades da Carbonila - Adição Nucleofílica em substâncias Carboniladas - Equilíbrio Ceto-Enólico - Adição aldólica
 Química Orgânica Aula 5 - Propriedades da Carbonila - Adição Nucleofílica em substâncias Carboniladas - Equilíbrio Ceto-Enólico - Adição aldólica Prof. Davyson Moreira (davysonmoreira@hotmail.com) 1 Orbitais
Química Orgânica Aula 5 - Propriedades da Carbonila - Adição Nucleofílica em substâncias Carboniladas - Equilíbrio Ceto-Enólico - Adição aldólica Prof. Davyson Moreira (davysonmoreira@hotmail.com) 1 Orbitais
Química Orgânica. Aula 5. Prof. Davyson Moreira
 Química Orgânica Aula 5 - Propriedades da Carbonila - Adição Nucleofílica em substâncias Carboniladas - Equilíbrio Ceto-Enólico - Adição aldólica Prof. Davyson Moreira (davysonmoreira@hotmail.com) 1 Orbitais
Química Orgânica Aula 5 - Propriedades da Carbonila - Adição Nucleofílica em substâncias Carboniladas - Equilíbrio Ceto-Enólico - Adição aldólica Prof. Davyson Moreira (davysonmoreira@hotmail.com) 1 Orbitais
2004 Redução diastereosseletiva de benzoina com boro-hidreto de sódio a 1,2-difenil-1,2-etanodiol
 24 Redução diastereosseletiva de benzoina com boro-hidreto de sódio a 1,2-difenil-1,2-etanodiol OH O NaBH 4 H HO OH meso H + H OH H OH racemic C 14 H 12 O 2 (212.3) (37.8) C 14 H 14 O 2 (214.3) Referência
24 Redução diastereosseletiva de benzoina com boro-hidreto de sódio a 1,2-difenil-1,2-etanodiol OH O NaBH 4 H HO OH meso H + H OH H OH racemic C 14 H 12 O 2 (212.3) (37.8) C 14 H 14 O 2 (214.3) Referência
4009 Síntese de ácido adípico a partir do ciclohexeno
 4009 Síntese de ácido adípico a partir do ciclohexeno C 6 H 10 (82,2) + tungstato de sódio dihidratado 4 H 2 H + 2 H + 4 H 2 + Aliquat 336. Na 2 W 4 2 H 2 (329,9) C 6 H 10 4 (34,0) C 25 H 54 ClN (404,2)
4009 Síntese de ácido adípico a partir do ciclohexeno C 6 H 10 (82,2) + tungstato de sódio dihidratado 4 H 2 H + 2 H + 4 H 2 + Aliquat 336. Na 2 W 4 2 H 2 (329,9) C 6 H 10 4 (34,0) C 25 H 54 ClN (404,2)
6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS
 131 6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS Quando a ligação pi estiver entre dois carbonos, formando alcenos, a reação será de adição eletrofílica. Substratos que apresentam a ligação pi formada entre
131 6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS Quando a ligação pi estiver entre dois carbonos, formando alcenos, a reação será de adição eletrofílica. Substratos que apresentam a ligação pi formada entre
4024 Síntese enantioseletiva do éster etílico do ácido (1R,2S)-cishidroxiciclopentano-carboxílico
 4024 Síntese enantioseletiva do éster etílico do ácido (1R,2S)-cishidroxiciclopentano-carboxílico H levedura C 8 H 12 3 C 8 H 14 3 (156,2) (158,2) Classificação Tipos de reação e classes de substâncias
4024 Síntese enantioseletiva do éster etílico do ácido (1R,2S)-cishidroxiciclopentano-carboxílico H levedura C 8 H 12 3 C 8 H 14 3 (156,2) (158,2) Classificação Tipos de reação e classes de substâncias
3005 Síntese de 7,7-diclorobiciclo [4.1.0] heptano (7,7- dicloronorcarano) a partir de ciclohexeno
![3005 Síntese de 7,7-diclorobiciclo [4.1.0] heptano (7,7- dicloronorcarano) a partir de ciclohexeno 3005 Síntese de 7,7-diclorobiciclo [4.1.0] heptano (7,7- dicloronorcarano) a partir de ciclohexeno](/thumbs/61/45682965.jpg) 00 Síntese de,-diclorobiciclo [..0] heptano (,- dicloronorcarano) a partir de ciclohexeno + CHCl NaOH tri-n-propylamine CCl + HCl C H 0 (8.) (9.) NaOH C 9 H N C H 0 Cl (0.0) (.) (.) (.) Classificação Tipos
00 Síntese de,-diclorobiciclo [..0] heptano (,- dicloronorcarano) a partir de ciclohexeno + CHCl NaOH tri-n-propylamine CCl + HCl C H 0 (8.) (9.) NaOH C 9 H N C H 0 Cl (0.0) (.) (.) (.) Classificação Tipos
Gabaritos Resolvidos Energia Química Semiextensivo V4 Frente E
 01) D A preferência de substituição obedece a ordem: C terciário C secundário C primário. A halogenação de um alcano se dá por substituição de um átomo de hidrogênio por um halogênio, resultando em um
01) D A preferência de substituição obedece a ordem: C terciário C secundário C primário. A halogenação de um alcano se dá por substituição de um átomo de hidrogênio por um halogênio, resultando em um
5009 Síntese de ftalocianina de cobre
 P 59 Síntese de ftalocianina de cobre 4 H 2 + 8 H 2 + CuCl (H 4 ) 6 Mo 7 24. 4 H 2-8 H 3-8 C 2-4 H 2 - HCl Cu C 8 H 4 3 CH 4 2 CuCl H 24 Mo 7 6 24. 4 H2 C 32 H 16 8 Cu (148,1) (6,1) (99,) (1235,9) (576,1)
P 59 Síntese de ftalocianina de cobre 4 H 2 + 8 H 2 + CuCl (H 4 ) 6 Mo 7 24. 4 H 2-8 H 3-8 C 2-4 H 2 - HCl Cu C 8 H 4 3 CH 4 2 CuCl H 24 Mo 7 6 24. 4 H2 C 32 H 16 8 Cu (148,1) (6,1) (99,) (1235,9) (576,1)
4010 Síntese de p-metoxiacetofenona a partir do anisol
 4010 Síntese de p-metoxiacetofenona a partir do anisol O C 3 + O O C 3 O C 3 Zeolith O C 3 + C 3 COO O C 3 C 7 8 O (108,1) C 4 6 O 3 (102,1) C 9 10 O 2 (150,2) C 2 4 O 2 (60,1) Classificação Tipos de reação
4010 Síntese de p-metoxiacetofenona a partir do anisol O C 3 + O O C 3 O C 3 Zeolith O C 3 + C 3 COO O C 3 C 7 8 O (108,1) C 4 6 O 3 (102,1) C 9 10 O 2 (150,2) C 2 4 O 2 (60,1) Classificação Tipos de reação
1024 Eliminação de água do 4-hidroxi-4-metil-2-pentanona
 1024 Eliminação de água do 4-hidroxi-4-metil-2-pentanona C H I 2 CH 3 CH 3 H 3 C CH 3 - H 2 H 3 + H 3 C CH 3 H 2 C CH 3 C 6 H 12 I 2 C 6 H 10 (116.2) (253.8) (98.2) Classificação Tipo de reação e classes
1024 Eliminação de água do 4-hidroxi-4-metil-2-pentanona C H I 2 CH 3 CH 3 H 3 C CH 3 - H 2 H 3 + H 3 C CH 3 H 2 C CH 3 C 6 H 12 I 2 C 6 H 10 (116.2) (253.8) (98.2) Classificação Tipo de reação e classes
4025 Síntese de 2-iodopropano a partir do 2-propanol
 4025 Síntese de 2-iodopropano a partir do 2-propanol OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60,1) (253,8) (31,0) C 3 H 7 I (170,0) (82,0) Classificação Tipos de reação e classes de substâncias
4025 Síntese de 2-iodopropano a partir do 2-propanol OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60,1) (253,8) (31,0) C 3 H 7 I (170,0) (82,0) Classificação Tipos de reação e classes de substâncias
3012 Síntese do adamantilideno (adamantanilideno) adamantano a partir de adamantanona
 Síntese do adamantilideno (adamantanilideno) adamantano a partir de adamantanona O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Referência Bibliográfica D. Lenoir, Synthesis, 99, -9 Classificação Tipos
Síntese do adamantilideno (adamantanilideno) adamantano a partir de adamantanona O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Referência Bibliográfica D. Lenoir, Synthesis, 99, -9 Classificação Tipos
QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES)
 QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES) REAÇÕES DE SUBSTITUIÇÃO São assim denominadas porque um hidrogênio da molécula orgânica é substituído por um átomo de halogênio, por um grupo nitro (NO 2 ) ou um grupo
QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES) REAÇÕES DE SUBSTITUIÇÃO São assim denominadas porque um hidrogênio da molécula orgânica é substituído por um átomo de halogênio, por um grupo nitro (NO 2 ) ou um grupo
LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira
 LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA QUÍMICA ORGÂNICA I Introdução a química orgânica: teoria estrutural e o átomo de carbono
LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA QUÍMICA ORGÂNICA I Introdução a química orgânica: teoria estrutural e o átomo de carbono
7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR
 163 7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR Para que uma reação orgânica ocorra, é necessário que haja rompimento nas ligações químicas envolvidas na estrutura das moléculas do substrato e do
163 7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR Para que uma reação orgânica ocorra, é necessário que haja rompimento nas ligações químicas envolvidas na estrutura das moléculas do substrato e do
5026 Oxidação do antraceno à antraquinona
 506 xidação do antraceno à antraquinona KMn /Al C H 0 KMn C H 8 (78.) (58.0) (08.) Referência Bibliográfica Nüchter, M., ndruschka, B., Trotzki, R., J. Prakt. Chem. 000,, No. 7 Classificação Tipos de Reações
506 xidação do antraceno à antraquinona KMn /Al C H 0 KMn C H 8 (78.) (58.0) (08.) Referência Bibliográfica Nüchter, M., ndruschka, B., Trotzki, R., J. Prakt. Chem. 000,, No. 7 Classificação Tipos de Reações
TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS
 TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS 1) 3.600-2.700 cm -1 A absorção nesta região é associada às vibrações de deformação axial nos átomos de hidrogênio ligados a carbono,
TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS 1) 3.600-2.700 cm -1 A absorção nesta região é associada às vibrações de deformação axial nos átomos de hidrogênio ligados a carbono,
Química D Intensivo V. 1
 Química D Intensivo V. 1 Exercícios 01) A 07) B Na síntese de Wöhler, o cianato de amônio (inorgânico) foi transformado em ureia (orgânica). 02) 63 01. Certa. 02. Certa. 04. Certa. 08. Certa. 16. Certa.
Química D Intensivo V. 1 Exercícios 01) A 07) B Na síntese de Wöhler, o cianato de amônio (inorgânico) foi transformado em ureia (orgânica). 02) 63 01. Certa. 02. Certa. 04. Certa. 08. Certa. 16. Certa.
Química E Extensivo V. 4
 Química E Extensivo V. 4 Exercícios 01) D 02) A Exemplo de obtenção de benzoato de sódio: O O COH + NaHCO 3(aq) + CO Na + HO l + CO 2 () 2(g) Ácido benzoico + bicarbonato de sódio Benzoato de sódio 03)
Química E Extensivo V. 4 Exercícios 01) D 02) A Exemplo de obtenção de benzoato de sódio: O O COH + NaHCO 3(aq) + CO Na + HO l + CO 2 () 2(g) Ácido benzoico + bicarbonato de sódio Benzoato de sódio 03)
ESTUDO DA INFLUÊNCIA DA TEMPERATURA SOBRE OS ESPECTROS DE RMN DE
 ESTUD DA INFLUÊNCIA DA TEMPERATURA SBRE S ESPECTRS DE RMN DE 1 H E DE 13 C DE LACTNAS Anderson Barros Archanjo, André Kulitz Marins, Patrícia Fontes Pinheiro, Vagner Tebaldi de Queiroz, Adilson Vidal Costa
ESTUD DA INFLUÊNCIA DA TEMPERATURA SBRE S ESPECTRS DE RMN DE 1 H E DE 13 C DE LACTNAS Anderson Barros Archanjo, André Kulitz Marins, Patrícia Fontes Pinheiro, Vagner Tebaldi de Queiroz, Adilson Vidal Costa
Gabarito-R Profº Jaqueline Química. a) Dados: Solubilidade do KOH em etanol a 25 C
 1: a) Dados: Solubilidade do KOH em etanol a 25 C 40 g em 100 ml. Adicionou-se 1,5 g de KOH a 35 ml de etanol, agitando-se continuamente a mistura. 100 ml (etanol) 40 g (KOH) 35 ml (etanol) mkoh mkoh 14
1: a) Dados: Solubilidade do KOH em etanol a 25 C 40 g em 100 ml. Adicionou-se 1,5 g de KOH a 35 ml de etanol, agitando-se continuamente a mistura. 100 ml (etanol) 40 g (KOH) 35 ml (etanol) mkoh mkoh 14
Química. Questão 17 A gasolina é uma mistura de hidrocarbonetos diversos que apresenta, dentre outros, os seguintes componentes:
 Questão 16 Uma molécula de água, isolada, não apresenta certas propriedades físicas - como ponto de fusão e de ebulição - que dependem de interações entre moléculas. Em 1998, um grupo de pesquisadores
Questão 16 Uma molécula de água, isolada, não apresenta certas propriedades físicas - como ponto de fusão e de ebulição - que dependem de interações entre moléculas. Em 1998, um grupo de pesquisadores
LISTA DAS FUNÇÕES ORGÂNICAS
 Orgânica Na pré-história, o ser humano se limitava a usar materiais que encontrava na natureza, sem provocar neles grandes modificações. A descoberta do fogo trouxe ao ser humano a primeira maneira efetiva
Orgânica Na pré-história, o ser humano se limitava a usar materiais que encontrava na natureza, sem provocar neles grandes modificações. A descoberta do fogo trouxe ao ser humano a primeira maneira efetiva
2008 Esterificação do ácido propiônico com 1-butanol via catálise ácida para a obtenção do éster propanoato de butila
 28 Esterificação do ácido propiônico com 1-butanol via catálise ácida para a obtenção do éster propanoato de butila Classificação Tipos de reações e classes de substâncias Reação de carbonila de ácidos
28 Esterificação do ácido propiônico com 1-butanol via catálise ácida para a obtenção do éster propanoato de butila Classificação Tipos de reações e classes de substâncias Reação de carbonila de ácidos
EXPERIÊNCIA 07 OXIDAÇÃO DO CICLOEXANOL: SÍNTESE DA CICLOEXANONA
 EXPERIÊNCIA 07 XIDAÇÃ D CICLEXANL: SÍNTESE DA CICLEXANNA 1- INTRDUÇÃ produto formado a partir da oxidação de álcoois depende do agente oxidante empregado e da natureza do álcool de partida (álcool primário,
EXPERIÊNCIA 07 XIDAÇÃ D CICLEXANL: SÍNTESE DA CICLEXANNA 1- INTRDUÇÃ produto formado a partir da oxidação de álcoois depende do agente oxidante empregado e da natureza do álcool de partida (álcool primário,
Reações em Aromáticos
 Reações em Aromáticos 01 (Unicamp-SP) Um dos átomos de hidrogênio do anel benzênico pode ser substituído por CH3, OH, Cℓ ou COOH. a) Escreva as fórmulas e os nomes dos derivados benzênicos obtidos por
Reações em Aromáticos 01 (Unicamp-SP) Um dos átomos de hidrogênio do anel benzênico pode ser substituído por CH3, OH, Cℓ ou COOH. a) Escreva as fórmulas e os nomes dos derivados benzênicos obtidos por
Compostos Carbonílicos α,β-insaturados: Adição Conjugada (Adição de Michael)
 Compostos Carbonílicos α,β-insaturados: Adição Conjugada (Adição de Michael) T1 11 e 15: Clayden, p. 227 40. T13 14: March, p. 260 3. T16 18 : Bruice, p. 869 71. T19 23 : Clayden, p. 748 55. T24 26 : Clayden,
Compostos Carbonílicos α,β-insaturados: Adição Conjugada (Adição de Michael) T1 11 e 15: Clayden, p. 227 40. T13 14: March, p. 260 3. T16 18 : Bruice, p. 869 71. T19 23 : Clayden, p. 748 55. T24 26 : Clayden,
GABARITO ÁREA DE CONCENTRAÇÃO FARMACOQUÍMICA
 GABARIT ÁREA DE CNCENTRAÇÃ FARMACQUÍMICA 1. Um farmacêutico desenvolveu uma rota sintética para desenvolvimento de um novo fármaco com ação anti-inflamatória. Durante o planejamento de síntese foi possível
GABARIT ÁREA DE CNCENTRAÇÃ FARMACQUÍMICA 1. Um farmacêutico desenvolveu uma rota sintética para desenvolvimento de um novo fármaco com ação anti-inflamatória. Durante o planejamento de síntese foi possível
3009 Síntese de ácido-trans-5-norborneno-2-3-dicarboxílico a partir de ácido fumárico e ciclopentadieno
 3009 Síntese de ácido-trans-5-norborneno-2-3-dicarboxílico a partir de ácido fumárico e ciclopentadieno 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1)
3009 Síntese de ácido-trans-5-norborneno-2-3-dicarboxílico a partir de ácido fumárico e ciclopentadieno 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1)
Prof a. Dr a. Patrícia Bulegon Brondani. Cromatografia de Camada Delgada (CCD)
 Cromatografia de Camada Delgada (CCD) A cromatografia de camada delgada é um exemplo de cromatografia de adsorção. Esta técnica consiste de uma fase estacionária fixada em uma placa (de vidro ou alumínio)
Cromatografia de Camada Delgada (CCD) A cromatografia de camada delgada é um exemplo de cromatografia de adsorção. Esta técnica consiste de uma fase estacionária fixada em uma placa (de vidro ou alumínio)
Substituição Nucleofílica em Ácidos Carboxílicos e Derivados
 Substituição Nucleofílica em Ácidos Carboxílicos e Derivados Estrutura, Nomenclatura, ocorrência natural, aplicação, propriedades físicas,preparação e reatividade. 2- Estrutura dos ácidos carboxílicos
Substituição Nucleofílica em Ácidos Carboxílicos e Derivados Estrutura, Nomenclatura, ocorrência natural, aplicação, propriedades físicas,preparação e reatividade. 2- Estrutura dos ácidos carboxílicos
Ciência que estuda a química da vida
 Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física que regem
Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física que regem
Espectroscopia no IV
 Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Compostos heterocíclicos: estrutura, síntese e reatividade. Aula 6
 Universidade Federal de Ouro Preto Compostos heterocíclicos: estrutura, síntese e reatividade Aula 6 Flaviane Francisco Hilário 1 1 - Estrutura Um heterociclo é um anel que contém um heteroátomo (, O,
Universidade Federal de Ouro Preto Compostos heterocíclicos: estrutura, síntese e reatividade Aula 6 Flaviane Francisco Hilário 1 1 - Estrutura Um heterociclo é um anel que contém um heteroátomo (, O,
Ciência que estuda a química da vida
 Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física e conferindo
Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física e conferindo
QFL (a) Aqui se trata de mero uso de fórmula e uso da constante magnetogírica do próton. 2πν
 QFL-2144-2013 Roteiro da 1 a Lista de exercícios de RMN 1.) A maioria dos espectrômetros de RMN utilizados para estudos em Química utiliza campos magnéticos fixos tais que a freqüência de ressonância de
QFL-2144-2013 Roteiro da 1 a Lista de exercícios de RMN 1.) A maioria dos espectrômetros de RMN utilizados para estudos em Química utiliza campos magnéticos fixos tais que a freqüência de ressonância de
QFL-2349 Reatividade de Compostos Orgânicos II 2016 Exercícios 04 Compostos Aromáticos
 QFL-2349 Reatividade de ompostos rgânicos II 2016 Exercícios 04 ompostos Aromáticos 1. Quais dos compostos abaixo podem ser considerados aromáticos, segundo a regra de Hückel? (a) (b) (c) (d) 2- (e) (f)
QFL-2349 Reatividade de ompostos rgânicos II 2016 Exercícios 04 ompostos Aromáticos 1. Quais dos compostos abaixo podem ser considerados aromáticos, segundo a regra de Hückel? (a) (b) (c) (d) 2- (e) (f)
Material Suplementar. Quim. Nova, Vol. 38, No. 6, S1-S9, 2015
 Quim. Nova, Vol. 38, No. 6, S1-S9, 2015 DESENVLVIMENT DE FÁRMACS PR HIBRIDAÇÃ MLECULAR: UMA AULA PRÁTICA DE QUÍMICA MEDICINAL USAND CMPRIMIDS DE PARACETAML E SULFADIAZINA E A FERRAMENTA VIRTUAL SciFinder
Quim. Nova, Vol. 38, No. 6, S1-S9, 2015 DESENVLVIMENT DE FÁRMACS PR HIBRIDAÇÃ MLECULAR: UMA AULA PRÁTICA DE QUÍMICA MEDICINAL USAND CMPRIMIDS DE PARACETAML E SULFADIAZINA E A FERRAMENTA VIRTUAL SciFinder
Reações de Oxidação e Substituição. Karla Gomes Diamantina-MG
 Reações de Oxidação e Substituição Karla Gomes Diamantina-MG Reações de oxidação Envolvem aumento no estado de oxidação (Nox) dos átomos presentes em uma molécula. De forma geral: Substância orgânica (redutora)
Reações de Oxidação e Substituição Karla Gomes Diamantina-MG Reações de oxidação Envolvem aumento no estado de oxidação (Nox) dos átomos presentes em uma molécula. De forma geral: Substância orgânica (redutora)
UFSC. Resposta: = 40. Comentário
 Resposta: 08 + 32 = 40 01. Incorreta. O butano não possui isomeria óptica, pois não possui carbono assimétrico. 02. Incorreta. Ao serem liberados para a atmosfera os gases sofrem expansão de volume. 04.
Resposta: 08 + 32 = 40 01. Incorreta. O butano não possui isomeria óptica, pois não possui carbono assimétrico. 02. Incorreta. Ao serem liberados para a atmosfera os gases sofrem expansão de volume. 04.
HNT 205 Produção e Composição de Alimentos, 2016/Noturno GABARITO Lista Lipideos
 1. O que são lipídeos? Qual sua importância nutricional? Quais os alimentos ricos em lipídeos? Lipídeos são substancias de origem biológica, solúveis em solventes orgânicos e pouco solúveis em água. São
1. O que são lipídeos? Qual sua importância nutricional? Quais os alimentos ricos em lipídeos? Lipídeos são substancias de origem biológica, solúveis em solventes orgânicos e pouco solúveis em água. São
Resposta: D Resolução comentada: Ci x Vi = Cf x Vf Ci = 0,5 mol/l Cf = 0,15 mol/l Vf = 250 ml Vi = 0,5 x Vi = 0,15 x 250 Vi = 75 ml.
 Unesp 1-Em 2013 comemora-se o centenário do modelo atômico proposto pelo físico dinamarquês Niels Bohr para o átomo de hidrogênio, o qual incorporou o conceito de quantização da energia, possibilitando
Unesp 1-Em 2013 comemora-se o centenário do modelo atômico proposto pelo físico dinamarquês Niels Bohr para o átomo de hidrogênio, o qual incorporou o conceito de quantização da energia, possibilitando
Espectrometria de massas
 Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
AULA 17. Reações Orgânicas. Prof Taynara Oliveira
 AULA 17 Reações Orgânicas Prof Taynara Oliveira Para que ocorra uma reação química, é necessário que as ligações existentes entre os átomos de uma molécula se rompam e esses átomos se rearranjem, formando
AULA 17 Reações Orgânicas Prof Taynara Oliveira Para que ocorra uma reação química, é necessário que as ligações existentes entre os átomos de uma molécula se rompam e esses átomos se rearranjem, formando
Química Orgânica Aplicada a Engenharia Geológica
 Química Orgânica Aplicada a Engenharia Geológica Aula 10 Estudo dos alcoóis Prof. Dr. Leandro Vinícius Alves Gurgel 1. Introdução Os alcoóis são compostos que possuem um ou mais grupos hidroxila ligados
Química Orgânica Aplicada a Engenharia Geológica Aula 10 Estudo dos alcoóis Prof. Dr. Leandro Vinícius Alves Gurgel 1. Introdução Os alcoóis são compostos que possuem um ou mais grupos hidroxila ligados
Enzimas. As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica.
 Enzimas As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica. Diferem dos catalisadores comuns em vários aspectos Velocidades de reações catalisadas por
Enzimas As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica. Diferem dos catalisadores comuns em vários aspectos Velocidades de reações catalisadas por
Química Orgânica Ambiental
 Química Orgânica Ambiental Aula 8 Estudo dos compostos aromáticos Prof. Dr. Leandro Vinícius Alves Gurgel 1. Introdução O Estudo do Benzeno Durante o século XIX foram isolados uma série de compostos que
Química Orgânica Ambiental Aula 8 Estudo dos compostos aromáticos Prof. Dr. Leandro Vinícius Alves Gurgel 1. Introdução O Estudo do Benzeno Durante o século XIX foram isolados uma série de compostos que
3015 Síntese de iodociclohexano a partir de ciclohexano e iodofórmio
 5 Síntese de iodociclohexano a partir de ciclohexano e iodofórmio + CHI NaOH I C 6 H (8.) CHI (9.7) (.) C 6 H I (.) Referências Bibliográficas P. R. Schreiner, O. Lauenstein, E. D. Butova, and A. A. Fokin,
5 Síntese de iodociclohexano a partir de ciclohexano e iodofórmio + CHI NaOH I C 6 H (8.) CHI (9.7) (.) C 6 H I (.) Referências Bibliográficas P. R. Schreiner, O. Lauenstein, E. D. Butova, and A. A. Fokin,
HIDROCARBONETOS FUNÇÕES ORGÂNICAS
 HIDROCARBONETOS FUNÇÕES ORGÂNICAS FUNÇÕES ORGÂNICAS O átomo de carbono: Apresenta capacidade singular de compartilhar elétrons com outros átomos de carbono formando ligações carbono-carbono estáveis. Permite
HIDROCARBONETOS FUNÇÕES ORGÂNICAS FUNÇÕES ORGÂNICAS O átomo de carbono: Apresenta capacidade singular de compartilhar elétrons com outros átomos de carbono formando ligações carbono-carbono estáveis. Permite
Química Orgânica. Aula 7. Prof. Davyson Moreira
 Química Orgânica Aula 7 - Reações em Aromáticos: Substituição Nucleofílica SNAr - Reações de Álcoois: Eliminação - Reações de Alcenos: Adição - Exercícios Prof. Davyson Moreira (davysonmoreira@hotmail.com)
Química Orgânica Aula 7 - Reações em Aromáticos: Substituição Nucleofílica SNAr - Reações de Álcoois: Eliminação - Reações de Alcenos: Adição - Exercícios Prof. Davyson Moreira (davysonmoreira@hotmail.com)
1001 Nitração do tolueno para 4-nitrotolueno, 2-nitrotolueno e 2,4-dinitrotolueno
 1001 Nitração do tolueno para 4-nitrotolueno, 2-nitrotolueno e 2,4-dinitrotolueno CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + produtos adicionais NO 2 NO 2 C 7 H 8 (92,1) HNO 3 (63,0) H 2 SO 4
1001 Nitração do tolueno para 4-nitrotolueno, 2-nitrotolueno e 2,4-dinitrotolueno CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + produtos adicionais NO 2 NO 2 C 7 H 8 (92,1) HNO 3 (63,0) H 2 SO 4
III PARTE EXPERIMENTAL. III.1 Sínteses. III.1.1 Síntese da porfirina de base livre (TMPP) 16
 III Parte experimental 30 III PARTE EXPERIMENTAL III.1 Sínteses III.1.1 Síntese da porfirina de base livre (TMPP) 16 Método 1: Inicialmente, a síntese da meso-tetrakis(4-metóxifenil)porfirina (TMPP) 16
III Parte experimental 30 III PARTE EXPERIMENTAL III.1 Sínteses III.1.1 Síntese da porfirina de base livre (TMPP) 16 Método 1: Inicialmente, a síntese da meso-tetrakis(4-metóxifenil)porfirina (TMPP) 16
Química Orgânica. Substância cíclica Substância planar Sistema completamente conjugado 4n + 2 π elétrons (Regra de Huckel) 27/04/2012
 Química Orgânica Aula 7 - Reações em Aromáticos: Substituição Nucleofílica SNAr - Reações de Álcoois: Eliminação - Reações de Alcenos: Adição - Exercícios Prof. Davyson Moreira (davysonmoreira@hotmail.com)
Química Orgânica Aula 7 - Reações em Aromáticos: Substituição Nucleofílica SNAr - Reações de Álcoois: Eliminação - Reações de Alcenos: Adição - Exercícios Prof. Davyson Moreira (davysonmoreira@hotmail.com)
AVALIAÇÃO DE CATALISADORES PARA A PREPARAÇÃO DE BIODIESEL UTILIZANDO ÁLCOOL NÃO-CONVENCIONAL.
 AVALIAÇÃO DE CATALISADORES PARA A PREPARAÇÃO DE BIODIESEL UTILIZANDO ÁLCOOL NÃO-CONVENCIONAL. Maria Cláudia Rodrigues Brandão 1 ; Juliana Kelly Dionísio de Souza 2, Wandson Lukas do Nascimento Amorim 3
AVALIAÇÃO DE CATALISADORES PARA A PREPARAÇÃO DE BIODIESEL UTILIZANDO ÁLCOOL NÃO-CONVENCIONAL. Maria Cláudia Rodrigues Brandão 1 ; Juliana Kelly Dionísio de Souza 2, Wandson Lukas do Nascimento Amorim 3
ANÁLISE INSTRUMENTAL RESSONÂNCIA MAGNÉTICA NUCLEAR EXERCÍCIOS/RESPOSTAS 2º SEMESTRE 2018
 ANÁLISE INSTRUMENTAL RESSONÂNCIA MAGNÉTICA NUCLEAR EXERCÍCIOS/RESPOSTAS 2º SEMESTRE 2018 Profa. Dra. Jayne Carlos de Souza Barboza Prof. Dr. Antônio Aarão Serra 1 1 o EXERCÍCIO: DETERMINE A ESTRUTURA DO
ANÁLISE INSTRUMENTAL RESSONÂNCIA MAGNÉTICA NUCLEAR EXERCÍCIOS/RESPOSTAS 2º SEMESTRE 2018 Profa. Dra. Jayne Carlos de Souza Barboza Prof. Dr. Antônio Aarão Serra 1 1 o EXERCÍCIO: DETERMINE A ESTRUTURA DO
Síntese e Purificação de Chalconas.
 Síntese e Purificação de Chalconas. Erick de Oliveira Lemes¹ (PG)*, Renata Awad¹ (PG), Jaqueline Evangelista de Queiroz¹ (PG), Hérika Danielle Almeida Vidal¹ (PG), Ingrid Vieira Machado¹ (PG), Gilberto
Síntese e Purificação de Chalconas. Erick de Oliveira Lemes¹ (PG)*, Renata Awad¹ (PG), Jaqueline Evangelista de Queiroz¹ (PG), Hérika Danielle Almeida Vidal¹ (PG), Ingrid Vieira Machado¹ (PG), Gilberto
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da
 Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
Estudo Visando a Síntese de Cromenonas
 Estudo Visando a Síntese de Cromenonas Brenda liveira Magalhães (IC), Maísa Borges Costa * (PQ) Câmpus Anápolis e Ciências Exatas e Tecnológicas Henrique Santillo Universidade Estadual de Goiás (CCET/UEG)
Estudo Visando a Síntese de Cromenonas Brenda liveira Magalhães (IC), Maísa Borges Costa * (PQ) Câmpus Anápolis e Ciências Exatas e Tecnológicas Henrique Santillo Universidade Estadual de Goiás (CCET/UEG)
SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS
 SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS ÁLCOOL São compostos orgânicos que apresentam o grupo funcional hidroxila ( OH) ligado a carbono saturado. ÁLCOOL Classificação Quanto ao número
SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS ÁLCOOL São compostos orgânicos que apresentam o grupo funcional hidroxila ( OH) ligado a carbono saturado. ÁLCOOL Classificação Quanto ao número
2023 Redução da D-(+)-cânfora com hidreto de lítio e alumínio para uma mistura isomérica de (+)-borneol e ( )-isoborneol
 223 Redução da D-(+)-cânfora com hidreto de lítio e alumínio para uma mistura isomérica de (+)-borneol e ( )-isoborneol Classificação Tipos de reações e classes de substâncias Reação de carbonila de cetonas,
223 Redução da D-(+)-cânfora com hidreto de lítio e alumínio para uma mistura isomérica de (+)-borneol e ( )-isoborneol Classificação Tipos de reações e classes de substâncias Reação de carbonila de cetonas,
FUVEST 2015 (Questões 1 a 6)
 (Questões 1 a 6) Provas de Vestibular 1. O metabissulfito de potássio (K 2 S2O 5 ) e o dióxido de enxofre (SO 2 ) são amplamente utilizados na conservação de alimentos como sucos de frutas, retardando
(Questões 1 a 6) Provas de Vestibular 1. O metabissulfito de potássio (K 2 S2O 5 ) e o dióxido de enxofre (SO 2 ) são amplamente utilizados na conservação de alimentos como sucos de frutas, retardando
Ciência que estuda a química da vida (características dos seres vivos)
 Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
Tópicos em destaque. O que é um orbital atômico? É a provável distribuição espacial dos elétrons ao redor do núcleo.
 Tópicos em destaque Por que alguns átomos se ligam e outros não? egra do octeto. s átomos procuram maior estabilidade formando ligação com outros átomos. s átomos estáveis (gases nobres) não se ligam.
Tópicos em destaque Por que alguns átomos se ligam e outros não? egra do octeto. s átomos procuram maior estabilidade formando ligação com outros átomos. s átomos estáveis (gases nobres) não se ligam.
Solução Comentada Prova de Química
 34. A histamina, estrutura mostrada abaixo, é uma substância orgânica que provoca inchaço e coceira, e que é liberada pelas células de defesa, quando somos picados por insetos. N NH 2 N H Se quisermos
34. A histamina, estrutura mostrada abaixo, é uma substância orgânica que provoca inchaço e coceira, e que é liberada pelas células de defesa, quando somos picados por insetos. N NH 2 N H Se quisermos
Estrutura de moléculas orgânicas e biológicas
 Hidrocarbonetos Os hidrocarbonetos são compostos orgânicos formados exclusivamente por átomos de carbono e hidrogénio, ligados por ligações covalentes simples (C H e C C), duplas (C = C) ou triplas (C
Hidrocarbonetos Os hidrocarbonetos são compostos orgânicos formados exclusivamente por átomos de carbono e hidrogénio, ligados por ligações covalentes simples (C H e C C), duplas (C = C) ou triplas (C
Funções Oxigenadas. Fórmula Geral: R OH. Nomenclatura:
 Funções xigenadas Álcoois São compostos orgânicos que apresentam um ou mais radicais hidroxila (-) ligados à átomos de carbono saturados. ibridização sp³. R Etan-1,2-diol 1 2 como combustível, nas indústrias
Funções xigenadas Álcoois São compostos orgânicos que apresentam um ou mais radicais hidroxila (-) ligados à átomos de carbono saturados. ibridização sp³. R Etan-1,2-diol 1 2 como combustível, nas indústrias
