Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de
|
|
|
- Wilson Castelhano Fidalgo
- 6 Há anos
- Visualizações:
Transcrição
1 Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de elétrons resultando na formação de M seguida de fragmentação induzida por excesso de energia interna do íon molecular; (c) ionização química: método mais suave de ionização resultante de uma reação, em fase gasosa, entre íons e moléculas neutras; (d) outros métodos mais recentes. Analisar m/z é preciso: Cenas dos próximos capítulos!!
2 MALDI Analito depositado numa matriz orgânica, que possui absorção intensa no do laser ( = 337 nm para laser de N 2 ); Dessorção por um laser pulsado (ns) de alta intensidade; Matrizes típicas: ácido 2,5-dihidroxibenzóico; ácido 3,5-dimetóxi-4- hidroxicinámico; ácido 5-clorosalicílico; Espectro resultante inclui íons (MH), e outros com prótons adicionais, retirados da matriz.
3
4 Relative Abundance Espectro de um anticorpo monoclonal MALDI TOF spectrum of IgG MH (M2H) (M3H) Mass (m/z)
5 Espectro (MALDI) de poli-metil metacrilato <M> = 7100 Da
6 Espectro de complexo de Pt obtido por ionização MALDI
7 Polysulfated-Derived Oligosaccharides Positive-ion (a) and negative-ion (b) MALDI mass spectra of CS-D tetra with pmg.
8 Aplicações de MALDI Identificação de proteínas de elevada massa molecular ( > Da). Espectros apresentam proteínas grandes com íons [MH], [M2H] 2, e [M3H] 3. Proteínas pequenas apresentam espectros apenas com [MH]. Alta sensibilidade. Espectros de polímeros sintéticos. Imagem por espectrometria de massas!!
9 IMS allows for distinction of different molecular species of β-amyloid plaques in an Alzheimer's disease model. Seeley E H, and Caprioli R M PNAS 2008;105: by National Academy of Sciences
10 Métodos de ionização a pressão atmosférica APCI: ionização química a pressão atmosférica. APPI: ionização química por fotoionização. ESI: electrospray DESI: electrospray por dessorção DART: (direct analysis in real time).
11 APCI (atmospheric pressure chemical ionization)
12 Formação de íons em APCI (atmospheric pressure chemical ionization)
13 Tipo de amostras Aplicações de APCI Substancias de polaridade e massa molecular mediana: PAH, PCB, ácidos graxos, esteroides, ftalatos,... Substancias sem sítios ácidos ou básicos. Substancias contendo heteroátomos: uréias, carbamatos,.. Substancias a serem evitadas: substancias instáveis a temperaturas mais altas, massa molecular elevada,...
14 Exemplos de espectros obtidos por APCI no modo positivo e no modo negativo
15 Positive APCI spectra of n-octane in synthetic air at 30 C, Vcone 1 V and at different n-octane concentrations of (a) 6 ppm, (b) 30 ppm, (c) 65 ppm, (d) 90 ppm, and (e) 150 ppm
16 APPI (atmospheric pressure photoionization)
17
18 Espectro de massas obtido no modo negativo por APPI
19 Espectro de massas de íons positivos obtido por APPI de petróleo venezuelano (cortesia do líder imortal HC)
20 Comparação entre métodos de ionização: exemplo da cafeína
21 Comparação entre métodos de ionização: exemplo da budesonida (anti-inflamatório)
22 Extraindo íons da solução...
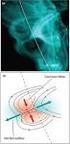
23 ESI electronspray ionization Pressão atmosférica Regiões de vácuo Capilar borossilicato Solução ~10-5 M Cone de Taylor fissão íons solvatados íons sem solvente ver 1-10 kv N 2 para dessolvatação
24 CRM (charge residue) vs. IDM (ion desorption) IDM - Íons desorvidos da superfície da gotícula CRM - Íons perdem solventes até dessolvatarem completamente
25 Procedimento típico em ionização electrospray Substancia dissolvida numa mistura, p.ex. agua-metanol, é injetada diretamente, ou por HPLC, ou por eletroforese capilar. Íons são formados a partir das gotas a pressão atmosférica e formam um jato por expansão livre. O mecanismo exato ainda é objeto de especulações. Amostragem ocorre através de um skimmer, e introduzidos no alto vácuo do espectrômetro. Íons provenientes de macromoléculas possuem freqüentemente um numero elevado de cargas. Espectros de massa medem a relação m/z e portanto íons com carga múltipla podem ser detectados mesmos com instrumentos menos sofisticados. A medida de distribuição de cargas não é sempre trivial. O número de cargas pode depender do ph, da presença de sais, desnaturação da proteína, quebra de ligações S-S, etc.
26 Solução NaBF 4 em metanol/água
27 Fe(CN) 6 4- e Fe(CN) 6 3-
28 Fe(CN) 6 4- e Fe(CN) 6 3-
29 ESI de macromoléculas
30 Espectro de massas pela técnica de electrospray de uma enzima: espectro indica as cargas dos íons e M = Da
31 MH n n M=? n=?
32 Variação do espectro de massa por electrospray, em função do ph, da mioglobina
33 Múltiplas cargas carga m s m r
34 Múltiplas cargas r =14 MH M = Da m s m r
35 Determinação do número de cargas e de M em espectros contendo íons com cargas múltiplas a) Em espectros electrospray, a massa de um íon m 1 com carga z 1 pode ser equacionada em termos da massa da molécula (M) e da massa do próton (m p ) m 1 z 1 = M z 1 m p b) Escolhendo outro pico no espectro, separado por (j-1) picos em ordem crescente de m/z, podemos equacionar a massa m 2 como m 2 (z 1 j) = M (z 1 j) m p c) Resolvendo as duas equações, z 1 M j( m ( m z ( m m 1 m 1 p ) m ) p )
36 DESI (desorption electrospray ionization)
37 DESI (desorption electrospray ionization)
38 Métodos muito recentes DESI Espectro de massas obtido por DESI de traços de urina em papel
39 DART (direct analysis in real time)
40 Ionização DART: distinguindo entre a amostra autentica e o genérico
41
42 polaridade Comparação dos métodos de ionização n-hexano CH 2 Cl 2 metanol H 2 O
Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de
 Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de elétrons resultando na formação de M seguida de fragmentação
Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de elétrons resultando na formação de M seguida de fragmentação
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS INTRODUÇÃO A ESPECTROMETRIA DE MASSAS. Aplicações
 INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Pioneiros da espectrometria de massas Espectrometria de massas: técnica analítica que separa e mede a relação massa:carga (m/z) de íons, em fase gasosa, produzidos
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Pioneiros da espectrometria de massas Espectrometria de massas: técnica analítica que separa e mede a relação massa:carga (m/z) de íons, em fase gasosa, produzidos
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS
 INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Espectrometria de massas: técnica que separa e mede, em fase gasosa, a relação m/z (massa/carga) de íons produzidos por algum método de ionização. Qual o princípio
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Espectrometria de massas: técnica que separa e mede, em fase gasosa, a relação m/z (massa/carga) de íons produzidos por algum método de ionização. Qual o princípio
3 Espectrometria de Massa
 3 Espectrometria de Massa 3.1 Princípios A espectrometria de massa determina as razões massa/carga de íons emitidos quando uma amostra é excitada por algum agente ionizante. Os agentes ionizantes podem
3 Espectrometria de Massa 3.1 Princípios A espectrometria de massa determina as razões massa/carga de íons emitidos quando uma amostra é excitada por algum agente ionizante. Os agentes ionizantes podem
ESPECTROMETRIA DE MASSAS
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DISCIPLINA: INORGÂNICA AVANÇADA II ESPECTROMETRIA DE MASSAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DISCIPLINA: INORGÂNICA AVANÇADA II ESPECTROMETRIA DE MASSAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
Espectrometria de massas Princípios básicos Teoria DESENVOLVENDO UMA CIÊNCIA MELHOR AGILENT E VOCÊ
 Espectrometria de massas Princípios básicos Teoria DESENVOLVENDO UMA CIÊNCIA MELHOR AGILENT E VOCÊ 1 A Agilent Technologies tem um compromisso com a comunidade educacional e está disposta a conceder acesso
Espectrometria de massas Princípios básicos Teoria DESENVOLVENDO UMA CIÊNCIA MELHOR AGILENT E VOCÊ 1 A Agilent Technologies tem um compromisso com a comunidade educacional e está disposta a conceder acesso
Estratégias para interpretação de espectros de massas
 Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
API Atmospheric Pressure Ionization
 API Atmospheric Pressure Ionization 6.000 V APCI H. Kambara 1982 Ionização Química a Pressão Atmosférica (APCI) Probe de APCI Gás de Desolvatação Cone de amostra Agulha para descarga corona Ionização
API Atmospheric Pressure Ionization 6.000 V APCI H. Kambara 1982 Ionização Química a Pressão Atmosférica (APCI) Probe de APCI Gás de Desolvatação Cone de amostra Agulha para descarga corona Ionização
Algumas considerações iniciais. Interpretação de espectros de massas
 Interpretação de espectros de massas 1. A maioria dos espectros de massas não são de interpretação fácil sem informações adicionais, tais como análise elementar, RMN, etc. 2. Os padrões de fragmentação
Interpretação de espectros de massas 1. A maioria dos espectros de massas não são de interpretação fácil sem informações adicionais, tais como análise elementar, RMN, etc. 2. Os padrões de fragmentação
ESPECTROMETRIA DE MASSAS MALDI-TOF
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DISCIPLINA: INORGÂNICA AVANÇADA II ESPECTROMETRIA DE MASSAS MALDI-TOF Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DISCIPLINA: INORGÂNICA AVANÇADA II ESPECTROMETRIA DE MASSAS MALDI-TOF Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
Análise proteômica e metabolômica por espectrometria de massas Analisadores de massas
 Análise proteômica e metabolômica por espectrometria de massas Analisadores de massas Prof. Alexandre K. Tashima Departamento de Bioquímica EPM/UNIFESP Bibliografia Mass Spectrometry, a Textbook. Ju rgen
Análise proteômica e metabolômica por espectrometria de massas Analisadores de massas Prof. Alexandre K. Tashima Departamento de Bioquímica EPM/UNIFESP Bibliografia Mass Spectrometry, a Textbook. Ju rgen
A base da espectrometria de massas
 A base da espectrometria de massas The father of MS and the first mass spectrometrist to win the Nobel Prize. Pure species and mixtures JJ Thomson's 'Plum Pudding Model' of the atom, a sphere of positive
A base da espectrometria de massas The father of MS and the first mass spectrometrist to win the Nobel Prize. Pure species and mixtures JJ Thomson's 'Plum Pudding Model' of the atom, a sphere of positive
Disciplina de Química Geral Profa. Marcia Margarete Meier
 Soluções 1 Propriedades gerais das soluções Os materiais são feitos geralmente de misturas de substâncias mais simples. Ex.: ar, sangue, água do mar, ligas metálicas, perfumes, etc As composições precisam
Soluções 1 Propriedades gerais das soluções Os materiais são feitos geralmente de misturas de substâncias mais simples. Ex.: ar, sangue, água do mar, ligas metálicas, perfumes, etc As composições precisam
QFL-5922. Espectrometria de Massa. Luiz Henrique Catalani
 QFL-5922 Espectrometria de Massa Luiz Henrique Catalani Data Tópicos 30/03 Espectrometria de massas Técnicas básicas 06/04 Espectrometria de massas Teoria de fragmentação 13/04 Espectrometria de massas
QFL-5922 Espectrometria de Massa Luiz Henrique Catalani Data Tópicos 30/03 Espectrometria de massas Técnicas básicas 06/04 Espectrometria de massas Teoria de fragmentação 13/04 Espectrometria de massas
Espectrometria de emissão atômica
 Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
Espectrometria de emissão atômica Técnica analítica que se baseia na emissão de radiação eletromagnética das regiões visível e ultravioleta do espectro eletromagnético por átomos neutros ou átomos ionizados
Espectrometria de Massas (MS)
 Universidade de São Paulo Instituto de Química de São Carlos Departamento de Química e Física Molecular Disciplina: SQM0418 - Análise Instrumental II Espectrometria de Massas (MS) Álvaro José dos Santos
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Química e Física Molecular Disciplina: SQM0418 - Análise Instrumental II Espectrometria de Massas (MS) Álvaro José dos Santos
Técnicas Modernas em Espectrometria de Massas
 XXVI SEMANA DA QUÍMICA III JORNADA DE PÓS-GRADUAÇÃO EM QUÍMICA Técnicas Modernas em Espectrometria de Massas Prof. Luiz Alberto (Beto) luizmoraes@ffclrp.usp.br Objetivo O principal objetivo deste curso
XXVI SEMANA DA QUÍMICA III JORNADA DE PÓS-GRADUAÇÃO EM QUÍMICA Técnicas Modernas em Espectrometria de Massas Prof. Luiz Alberto (Beto) luizmoraes@ffclrp.usp.br Objetivo O principal objetivo deste curso
Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons)
 Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons) Clivagem α: fragmentação iniciada pelo sítio radicalar em acetona Fragmentações do íon molecular podem
Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons) Clivagem α: fragmentação iniciada pelo sítio radicalar em acetona Fragmentações do íon molecular podem
QO423 Espectrometria d e de M assas Massas
 QO423 Espectrometria de Massas Oqueéamassadeumátomo? um M = 5 1 H (1p, 1e) = 1.0079 2 H (1p, 1n, 1e) = 2.0141 4 He (2p, 2n, 2e) = 4.0026 4 He/ 2 H = 1.98!! Como é um átomo? Como o núcleo não explode?!!
QO423 Espectrometria de Massas Oqueéamassadeumátomo? um M = 5 1 H (1p, 1e) = 1.0079 2 H (1p, 1n, 1e) = 2.0141 4 He (2p, 2n, 2e) = 4.0026 4 He/ 2 H = 1.98!! Como é um átomo? Como o núcleo não explode?!!
t RESOLUÇÃO COMECE DO BÁSICO
 t RESOLUÇÃO COMECE DO BÁSICO - o processo I sugere a evaporação (transformação física) dos componentes do medicamento. - a decomposição das substâncias (transformação química) que constituem o princípio
t RESOLUÇÃO COMECE DO BÁSICO - o processo I sugere a evaporação (transformação física) dos componentes do medicamento. - a decomposição das substâncias (transformação química) que constituem o princípio
Prof. Luiz F. Silva Jr - IQ-USP
 ü Leitura Recomendada: Organic Chemistry, J. Clayden, N. Greeves, S. Warren, P. Wothers, Oxford, Oxford, 2001, cap. 8. ü Compreender aspectos de acidez e basicidade é essencial em Química Orgânica: i)
ü Leitura Recomendada: Organic Chemistry, J. Clayden, N. Greeves, S. Warren, P. Wothers, Oxford, Oxford, 2001, cap. 8. ü Compreender aspectos de acidez e basicidade é essencial em Química Orgânica: i)
UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI
 UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI Questão 1 Em uma análise química desejava-se determinar o teor percentual de zinco em 96,57g de uma amostra
UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI Questão 1 Em uma análise química desejava-se determinar o teor percentual de zinco em 96,57g de uma amostra
Mary Santiago Silva 16/04/2010
 Espectrometria de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Técnica analítica, utilizada para identificar e quantificar compostos conhecidos e elucidar a estrutura
Espectrometria de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Técnica analítica, utilizada para identificar e quantificar compostos conhecidos e elucidar a estrutura
Espectrometria de Massas: Estudo Dirigido
 1 Disciplina: Química Orgânica III / 2009.2 Ministrante: Prof. Dr. Sidney Lima 1). O que é um EM e qual a utilidade da EM? Espectrometria de Massas: Estudo Dirigido R = Nos permite determinar a massa molecular
1 Disciplina: Química Orgânica III / 2009.2 Ministrante: Prof. Dr. Sidney Lima 1). O que é um EM e qual a utilidade da EM? Espectrometria de Massas: Estudo Dirigido R = Nos permite determinar a massa molecular
Gabarito das Questões
 II OLIMPÍADA BAIANA DE QUÍMICA 19 DE MAIO DE 2007 Gabarito das Questões Para cada questão de 1 a 5, marque com um X a alternativa correta e justifique porque as outras duas estão erradas. QUESTÃO 1 a)
II OLIMPÍADA BAIANA DE QUÍMICA 19 DE MAIO DE 2007 Gabarito das Questões Para cada questão de 1 a 5, marque com um X a alternativa correta e justifique porque as outras duas estão erradas. QUESTÃO 1 a)
Aula de Bioquímica I. Tema: Água. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Água Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Água Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Ligações químicas. Forças de ligações secundárias
 Ligações químicas Forças de ligações secundárias 1 Introdução Forças intermoleculares. Genericamente - são responsáveis pela possibilidade de liquefação e solidificação das moléculas. São de fraca intensidade
Ligações químicas Forças de ligações secundárias 1 Introdução Forças intermoleculares. Genericamente - são responsáveis pela possibilidade de liquefação e solidificação das moléculas. São de fraca intensidade
1% de ácido acético em água ultrapura
 QUESTÃO 1 Os diuréticos são utilizados para controlar a pressão alta. Eles estimulam os rins a produzir mais urina, eliminando fluidos e minerais do corpo e diminuindo a pressão. Atletas podem utilizar
QUESTÃO 1 Os diuréticos são utilizados para controlar a pressão alta. Eles estimulam os rins a produzir mais urina, eliminando fluidos e minerais do corpo e diminuindo a pressão. Atletas podem utilizar
Introdução à Bioquímica
 Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
LUAULA. Professor: Eduardo Ulisses
 LUAULA Professor: Eduardo Ulisses Sobre as ligações químicas, analise as afirmativas. I. Nas estruturas de Lewis, a ligação covalente resulta do compartilhamento de um par de elétrons entre dois átomos.
LUAULA Professor: Eduardo Ulisses Sobre as ligações químicas, analise as afirmativas. I. Nas estruturas de Lewis, a ligação covalente resulta do compartilhamento de um par de elétrons entre dois átomos.
Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos
 UNIVERSIDADE DE SÃO PAULO USP FARMÁCIA BIOQUÍMICA 015N Reatividade de Compostos Orgânicos II Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos Beatriz In Soon Chang (9328183) João Gabriel
UNIVERSIDADE DE SÃO PAULO USP FARMÁCIA BIOQUÍMICA 015N Reatividade de Compostos Orgânicos II Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos Beatriz In Soon Chang (9328183) João Gabriel
1º Questão: Escreva a distribuição eletrônica dos elementos abaixo e determine o número de valência de cada elemento: a) Fe (26):.
 FOLHA DE EXERCÍCIOS CURSO: Otimizado ASS.: Exercícios de Conteúdo DISCIPLINA: Fundamentos de Química e Bioquímica NOME: TURMA: 1SAU 1º Questão: Escreva a distribuição eletrônica dos elementos abaixo e
FOLHA DE EXERCÍCIOS CURSO: Otimizado ASS.: Exercícios de Conteúdo DISCIPLINA: Fundamentos de Química e Bioquímica NOME: TURMA: 1SAU 1º Questão: Escreva a distribuição eletrônica dos elementos abaixo e
Aplicações do paper spray ionization : uma possível interface entre a microfluídica e a espectrometria de massas. Boniek G. Vaz. boniek@ufg.
 Aplicações do paper spray ionization : uma possível interface entre a microfluídica e a espectrometria de massas Boniek G. Vaz boniek@ufg.br ESPECTROMETRIA DE MASSAS (MS) Ionização + Geração de Íons (moléculas
Aplicações do paper spray ionization : uma possível interface entre a microfluídica e a espectrometria de massas Boniek G. Vaz boniek@ufg.br ESPECTROMETRIA DE MASSAS (MS) Ionização + Geração de Íons (moléculas
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução
 Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
Estrutura covalente de proteínas estrutura tridimensional. Proteina: estrutura covalente com muitas restrições conformacionais
 Estrutura covalente de proteínas estrutura tridimensional Proteina: estrutura covalente com muitas restrições conformacionais M. Teresa Machini IQ/USP Análise de sequência de aminoácidos Conteúdo de aminoácidos
Estrutura covalente de proteínas estrutura tridimensional Proteina: estrutura covalente com muitas restrições conformacionais M. Teresa Machini IQ/USP Análise de sequência de aminoácidos Conteúdo de aminoácidos
Química. Xandão (Renan Micha) Soluções
 Soluções Soluções 1. (FUVEST) Sabe-se que os metais ferro (Fe 0 ), magnésio (Mg 0 ) e estanho (Sn 0 ) reagem com soluções de ácidos minerais, liberando gás hidrogênio e formando íons divalentes em solução.
Soluções Soluções 1. (FUVEST) Sabe-se que os metais ferro (Fe 0 ), magnésio (Mg 0 ) e estanho (Sn 0 ) reagem com soluções de ácidos minerais, liberando gás hidrogênio e formando íons divalentes em solução.
A base da espectrometria de massas
 A base da espectrometria de massas The father of MS and the first mass spectrometrist to win the Nobel Prize. Pure species and mixtures JJ Thomson's 'Plum Pudding Model' of the atom, a sphere of positive
A base da espectrometria de massas The father of MS and the first mass spectrometrist to win the Nobel Prize. Pure species and mixtures JJ Thomson's 'Plum Pudding Model' of the atom, a sphere of positive
Profº André Montillo
 Profº André Montillo www.montillo.com.br Dispersão Definição: É colocar uma substância dentro de outra substância, onde a primeira substância se caracteriza por ser uma partícula, ou seja, a substância
Profº André Montillo www.montillo.com.br Dispersão Definição: É colocar uma substância dentro de outra substância, onde a primeira substância se caracteriza por ser uma partícula, ou seja, a substância
Resolução de Questões de Provas Específicas de Química (Aula 7)
 Resolução de Questões de Provas Específicas de Química (Aula 7) Resolução de Questões de Provas Específicas (Aula 7) 1. (UECE) A tabela periódica já era objeto das preocupações dos antigos químicos a partir
Resolução de Questões de Provas Específicas de Química (Aula 7) Resolução de Questões de Provas Específicas (Aula 7) 1. (UECE) A tabela periódica já era objeto das preocupações dos antigos químicos a partir
a) Escreva os nomes das substâncias presentes nos frascos A, B e C. A B C
 PROVA DE QUÍMICA 2ª ETAPA do VESTIBULAR 2006 (cada questão desta prova vale até cinco pontos) Questão 01 Foram encontrados, em um laboratório, três frascos A, B e C, contendo soluções incolores e sem rótulos.
PROVA DE QUÍMICA 2ª ETAPA do VESTIBULAR 2006 (cada questão desta prova vale até cinco pontos) Questão 01 Foram encontrados, em um laboratório, três frascos A, B e C, contendo soluções incolores e sem rótulos.
- SOLUÇÃO = SOLUTO + SOLVENTE. COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura.
 Soluções - MISTURA HOMOGÊNEA - SOLUÇÃO = SOLUTO + SOLVENTE menor quantidade maior quantidade COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura. Cs = g de soluto
Soluções - MISTURA HOMOGÊNEA - SOLUÇÃO = SOLUTO + SOLVENTE menor quantidade maior quantidade COEFICIENTE DE SOLUBILIDADE ( Cs) Grandeza que depende da natureza do soluto e da temperatura. Cs = g de soluto
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
COMENTÁRIO DA PROVA DE QUÍMICA
 COMENTÁRIO DA PROVA DE QUÍMICA Os responsáveis pelo vestibular da UFPR determinam uma lista de conteúdos considerados por eles relevantes e, supõe-se, importantes para que seus futuros alunos tenham bom
COMENTÁRIO DA PROVA DE QUÍMICA Os responsáveis pelo vestibular da UFPR determinam uma lista de conteúdos considerados por eles relevantes e, supõe-se, importantes para que seus futuros alunos tenham bom
QUESTÃO 1. Atenção: Caso seja necessário simbolizar a presença de espaços entre os elementos da equação, utilize o símbolo f.
 QUESTÃO 1 Uma das funções disponíveis no programa Microsoft Excel é denominada de Média, que retorna à média (aritmética) dos argumentos que podem ser números ou nomes, matrizes ou referências que contém
QUESTÃO 1 Uma das funções disponíveis no programa Microsoft Excel é denominada de Média, que retorna à média (aritmética) dos argumentos que podem ser números ou nomes, matrizes ou referências que contém
Espectrometria de Ressonância Magnética Nuclear
 Espectrometria de Ressonância Magnética Nuclear 2002 - Prof. Hamilton M. Viana 1 Introdução Semelhante ao IR, Ação do campo magnético Absorção de radiação eletromagnética Espectro freqüências x intensidades
Espectrometria de Ressonância Magnética Nuclear 2002 - Prof. Hamilton M. Viana 1 Introdução Semelhante ao IR, Ação do campo magnético Absorção de radiação eletromagnética Espectro freqüências x intensidades
Identificação funções inorgânicas, ionização e dissociação, número de oxidação
 Identificação funções inorgânicas, ionização e dissociação, número de oxidação Várias teorias tentaram explicar o fato de algumas soluções conduzirem energia elétrica e outra não 1903 Arrhenius experiências
Identificação funções inorgânicas, ionização e dissociação, número de oxidação Várias teorias tentaram explicar o fato de algumas soluções conduzirem energia elétrica e outra não 1903 Arrhenius experiências
Aula 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Espectroscopia de RMN
 Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
GASES NOBRES CQ133 FSN
 GASES NOBRES CQ133 FSN GASES NOBRES CQ133 FSN CONFIGURAÇÃO ELETRÔNICA He 1s 2 ; Ne, Ar, Kr, Xe, Rn ns 2 p 6 confere a estabilidade química dos elementos; os gases nobres apresentam uma afinidade eletrônica
GASES NOBRES CQ133 FSN GASES NOBRES CQ133 FSN CONFIGURAÇÃO ELETRÔNICA He 1s 2 ; Ne, Ar, Kr, Xe, Rn ns 2 p 6 confere a estabilidade química dos elementos; os gases nobres apresentam uma afinidade eletrônica
PROVA DE QUÍMICA TABELA PERIÓDICA DOS ELEMENTOS
 PROVA DE QUÍMICA TABELA PERIÓDICA DOS ELEMENTOS FONTE: Tabela Periódica da IUPAC/versão 2005(adaptada). Acesso: http://www.iupac.org/reports/periodic_table/ 25 QUESTÃO 3 Analise este quadro, em que se
PROVA DE QUÍMICA TABELA PERIÓDICA DOS ELEMENTOS FONTE: Tabela Periódica da IUPAC/versão 2005(adaptada). Acesso: http://www.iupac.org/reports/periodic_table/ 25 QUESTÃO 3 Analise este quadro, em que se
DISCIPLINA DE QUÍMICA
 DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
1.5. Ácidos e Bases (Bibliografia Principal: Brown, 2nd) Primeira Definição: Arrhenius (1884)
 1.5. Ácidos e Bases (Bibliografia Principal: Brown, 2nd) i) Reações orgânicas são catalisadas por: a) ácidos doadores de prótons (Ex: H 3 O + ) b) ácidos de Lewis (Ex: AlCl 3 ) ii) Muitas reações em química
1.5. Ácidos e Bases (Bibliografia Principal: Brown, 2nd) i) Reações orgânicas são catalisadas por: a) ácidos doadores de prótons (Ex: H 3 O + ) b) ácidos de Lewis (Ex: AlCl 3 ) ii) Muitas reações em química
CPV seu pé direito também na Medicina
 seu pé direito também na Medicina UNIFESP 17/dezembro/2010 QUÍMICA 06. Ligas metálicas são comuns no cotidiano e muito utilizadas nas indústrias automobilística, aeronáutica, eletrônica e na construção
seu pé direito também na Medicina UNIFESP 17/dezembro/2010 QUÍMICA 06. Ligas metálicas são comuns no cotidiano e muito utilizadas nas indústrias automobilística, aeronáutica, eletrônica e na construção
Assunto: Ligações Químicas. 1) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 Aluno: Série: 1º ano Assunto: Ligações Químicas 1) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais
Aluno: Série: 1º ano Assunto: Ligações Químicas 1) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais
Sumário. 1 Introdução: matéria e medidas 1. 2 Átomos, moléculas e íons Estequiometria: cálculos com fórmulas e equações químicas 67
 Prefácio 1 Introdução: matéria e medidas 1 1.1 O estudo da química 1 1.2 Classificações da matéria 3 1.3 Propriedades da matéria 8 1.4 Unidades de medida 12 1.5 Incerteza na medida 18 1.6 Análise dimensional
Prefácio 1 Introdução: matéria e medidas 1 1.1 O estudo da química 1 1.2 Classificações da matéria 3 1.3 Propriedades da matéria 8 1.4 Unidades de medida 12 1.5 Incerteza na medida 18 1.6 Análise dimensional
2005 by Pearson Education. Capítulo 04
 QUÍMICA A Ciência Central 9ª Edição Capítulo 4 Reações em soluções aquosas e estequiometria de soluções David P. White Propriedades gerais das soluções aquosas Propriedades eletrolíticas As soluções aquosas
QUÍMICA A Ciência Central 9ª Edição Capítulo 4 Reações em soluções aquosas e estequiometria de soluções David P. White Propriedades gerais das soluções aquosas Propriedades eletrolíticas As soluções aquosas
RESPOSTAS ESPERADAS QUÍMICA
 Questão 1 Sim, a analogia está correta. Por se tratar de mudança de estado físico, a temperatura do sistema água permanece constante durante o processo de solidificação, assim como ocorre para o caso das
Questão 1 Sim, a analogia está correta. Por se tratar de mudança de estado físico, a temperatura do sistema água permanece constante durante o processo de solidificação, assim como ocorre para o caso das
Revisão Específicas. Química Monitores: Luciana Lima e Rafael França 02-08/11/2015. Material de Apoio para Monitoria
 Revisão Específicas 1. As conchas marinhas não se dissolvem apreciavelmente na água do mar, por serem compostas, na sua maioria, de carbonato de cálcio, um sal insolúvel cujo produto de solubilidade é
Revisão Específicas 1. As conchas marinhas não se dissolvem apreciavelmente na água do mar, por serem compostas, na sua maioria, de carbonato de cálcio, um sal insolúvel cujo produto de solubilidade é
ÁGUA, SOLUBILIDADE E PH
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
Aulão de Química. Química Geral Professor: Eduardo Ulisses
 Aulão de Química Química Geral Professor: Eduardo Ulisses Substâncias e Misturas Substância é qualquer parte da matéria que possui propriedades constantes. As substâncias podem ser classificadas como sendo
Aulão de Química Química Geral Professor: Eduardo Ulisses Substâncias e Misturas Substância é qualquer parte da matéria que possui propriedades constantes. As substâncias podem ser classificadas como sendo
Disciplina: Química A
 Disciplina: Química A EXTENSIVO E TERCEIRÃO PÁGINA: 6 EXERCÍCIO: 28.01 O álcool apresenta interações por ligações de hidrogênio, enquanto o hidrocarboneto interage por forças de dipolo induzido, dessa
Disciplina: Química A EXTENSIVO E TERCEIRÃO PÁGINA: 6 EXERCÍCIO: 28.01 O álcool apresenta interações por ligações de hidrogênio, enquanto o hidrocarboneto interage por forças de dipolo induzido, dessa
Ligações Químicas. Iônicas. Metálicas. Covalentes. Átomo: constituinte da menor parte de qualquer matéria;
 Ligações Químicas Átomo: constituinte da menor parte de qualquer matéria; -capacidade de se combinarem uns com os outros, lhes permite a formação de uma grande variedade de substâncias; Ligações Químicas
Ligações Químicas Átomo: constituinte da menor parte de qualquer matéria; -capacidade de se combinarem uns com os outros, lhes permite a formação de uma grande variedade de substâncias; Ligações Químicas
FORÇAS INTERMOLECULARES QUÍMICA GERAL
 FORÇAS INTERMOLECULARES QUÍMICA GERAL FORÇAS INTERMOLECULARES As forças intermoleculares, forças que existem entre as moléculas, contribuem em grande parte com as propriedades físicas apresentadas pelos
FORÇAS INTERMOLECULARES QUÍMICA GERAL FORÇAS INTERMOLECULARES As forças intermoleculares, forças que existem entre as moléculas, contribuem em grande parte com as propriedades físicas apresentadas pelos
INTERAÇÕES INTERMOLECULARES
 INTERAÇÕES INTERMOLECULARES Serão abordados: as forças íon-dipolo, dipolo-dipolo, dispersão de London e ligação de hidrogênio e a relação entre propriedade física e interação intermolecular. As partículas
INTERAÇÕES INTERMOLECULARES Serão abordados: as forças íon-dipolo, dipolo-dipolo, dispersão de London e ligação de hidrogênio e a relação entre propriedade física e interação intermolecular. As partículas
UNIDADE: DATA: 03 / 12 / 2015 III ETAPA AVALIAÇÃO ESPECIAL DE INTRODUÇÃO À QUÍMICA 9.º ANO/EF
 SOCIEDADE MINEIRA DE CULTURA Mantenedora da PUC Minas e do COLÉGIO SANTA MARIA UNIDADE: DATA: 03 / 2 / 205 III ETAPA AVALIAÇÃO ESPECIAL DE INTRODUÇÃO À QUÍMICA 9.º ANO/EF ALUNO(A): N.º: TURMA: PROFESSOR(A):
SOCIEDADE MINEIRA DE CULTURA Mantenedora da PUC Minas e do COLÉGIO SANTA MARIA UNIDADE: DATA: 03 / 2 / 205 III ETAPA AVALIAÇÃO ESPECIAL DE INTRODUÇÃO À QUÍMICA 9.º ANO/EF ALUNO(A): N.º: TURMA: PROFESSOR(A):
29/2/2008. Interações intermoleculares
 Química 2 ano Forças Intermoleculares Décio Helena Fev/08 O tipo de interação existente entre as moléculas e/ou íons definem algumas propriedades importantes das substâncias, como o estado físico, temperaturas
Química 2 ano Forças Intermoleculares Décio Helena Fev/08 O tipo de interação existente entre as moléculas e/ou íons definem algumas propriedades importantes das substâncias, como o estado físico, temperaturas
7ª LISTA - EXERCÍCIOS DE PROVAS Equilíbrio ácido-base. 2,10 x 10-4
 Pg. 1/8 1 a Questão A tabela abaixo apresenta os valores das constantes de basicidade, K b, a 25 C, para diferentes espécies em solução aquosa. Espécies K b CH 3 C - 5,60 x 10-10 CN - 2,50 x 10-5 C 3 2-2,10
Pg. 1/8 1 a Questão A tabela abaixo apresenta os valores das constantes de basicidade, K b, a 25 C, para diferentes espécies em solução aquosa. Espécies K b CH 3 C - 5,60 x 10-10 CN - 2,50 x 10-5 C 3 2-2,10
PREVENÇÃO, PREPARAÇÃO E RESPOSTA À EMERGÊNCIAS E DESASTRES QUÍMICOS
 Curso de Auto-aprendizagem PREVENÇÃO, PREPARAÇÃO E RESPOSTA À EMERGÊNCIAS E DESASTRES QUÍMICOS Equipamentos portáteis de detecção Químico Agnaldo R. de Vasconcellos CETESB Sustância não identificada Mantenha
Curso de Auto-aprendizagem PREVENÇÃO, PREPARAÇÃO E RESPOSTA À EMERGÊNCIAS E DESASTRES QUÍMICOS Equipamentos portáteis de detecção Químico Agnaldo R. de Vasconcellos CETESB Sustância não identificada Mantenha
Ligações intermoleculares
 Comparações entre ligações e interações químicas Ligação covalente : Interação intramolecular Ligação de hidrogênio: Interação intermolecular Forças íon-dipolo Existem entre um íon e a carga parcial em
Comparações entre ligações e interações químicas Ligação covalente : Interação intramolecular Ligação de hidrogênio: Interação intermolecular Forças íon-dipolo Existem entre um íon e a carga parcial em
Seu pé direito nas melhores faculdades
 Seu pé direito nas melhores faculdades FUVEST 2 a Fase 11/janeiro/2011 QUÍMICA 01. s componentes principais dos óleos vegetais são os triglicerídeos, que possuem a seguinte fórmula genérica: Nessa fórmula,
Seu pé direito nas melhores faculdades FUVEST 2 a Fase 11/janeiro/2011 QUÍMICA 01. s componentes principais dos óleos vegetais são os triglicerídeos, que possuem a seguinte fórmula genérica: Nessa fórmula,
Fundamentos de Química Profa. Janete Yariwake
 2. Introdução: Conceitos e cálculos fundamentais (Estequiometria; Concentrações) 1 Lei das proporções definidas (Lei de Proust) Em uma substância química, os elementos estão sempre presentes em proporções
2. Introdução: Conceitos e cálculos fundamentais (Estequiometria; Concentrações) 1 Lei das proporções definidas (Lei de Proust) Em uma substância química, os elementos estão sempre presentes em proporções
4001 Transesterificação do óleo de mamona em ricinoleato de metila
 4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
4001 Transesterificação do óleo de mamona em ricinoleato de metila Classificação Tipos de reações e classes de substâncias. Reação do grupo carbonila de derivados do ácido carboxílico, trans-esterificação,
QUÍMICA COMENTÁRIO DA PROVA DE QUÍMICA
 COMENTÁRIO DA PROVA DE QUÍMICA Reiterando o que destacamos na 1ª fase, sabemos que para manter a lisura da prova, ela deve passar pelo menor número de mãos possível. Porém, uma avaliação final técnica
COMENTÁRIO DA PROVA DE QUÍMICA Reiterando o que destacamos na 1ª fase, sabemos que para manter a lisura da prova, ela deve passar pelo menor número de mãos possível. Porém, uma avaliação final técnica
LCE0182 Química Analítica Quantitativa. Informações Gerais. Wanessa Melchert Mattos.
 LCE0182 Química Analítica Quantitativa Informações Gerais Wanessa Melchert Mattos wanemelc@usp.br Aprovação Para que o aluno possa ser aprovado exige-se média mínima de 5,0 em notas e 70% de frequência
LCE0182 Química Analítica Quantitativa Informações Gerais Wanessa Melchert Mattos wanemelc@usp.br Aprovação Para que o aluno possa ser aprovado exige-se média mínima de 5,0 em notas e 70% de frequência
Agronomia Química Analítica Prof. Dr. Gustavo Rocha de Castro. As medidas baseadas na luz (radiação eletromagnética) são muito empregadas
 ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
Cromatografia Líquida
 Analítica V Aula 11: 05-03-13 Cromatografia Líquida PRÓXIMA AULA TEÓRICA (Eletroforese Capilar): 12-03-13, às 08:15h, como Prof. Marcone Prof. Rafael Sousa Departamento de Química - ICE rafael.arromba@ufjf.edu.br
Analítica V Aula 11: 05-03-13 Cromatografia Líquida PRÓXIMA AULA TEÓRICA (Eletroforese Capilar): 12-03-13, às 08:15h, como Prof. Marcone Prof. Rafael Sousa Departamento de Química - ICE rafael.arromba@ufjf.edu.br
RELAÇÕES DE MASSA E MOL
 RELAÇÃO DE MASSA E MOL A relação entre massa e quantidade Em uma gota de água de 0,05 ml há 1,67 sextilhão (1,67 x 10 21 ) de moléculas de água. A relação entre massa e quantidade A unidade de massa atômica
RELAÇÃO DE MASSA E MOL A relação entre massa e quantidade Em uma gota de água de 0,05 ml há 1,67 sextilhão (1,67 x 10 21 ) de moléculas de água. A relação entre massa e quantidade A unidade de massa atômica
Equações-chave FUNDAMENTOS. Seção A. Seção E. Seção F. Seção G. mv 2. E c E P. mgh. Energia total energia cinética energia potencial, ou E E c.
 Equações-chave FUNDAMENTOS Seção A 3 A energia cinética de uma partícula de massa m relaciona-se com sua velocidade v, por: E c mv 2 4 Um corpo de massa m que está a uma altura h da Terra tem energia potencial
Equações-chave FUNDAMENTOS Seção A 3 A energia cinética de uma partícula de massa m relaciona-se com sua velocidade v, por: E c mv 2 4 Um corpo de massa m que está a uma altura h da Terra tem energia potencial
Fonte de plasma - DCP
 Fonte de plasma - DCP Dois anodos de grafite e um catodo de tungstênio, em forma de Y invertido Plasma é formado, colocando-se momentaneamente os eletrodos em contato Ocorre ionização, gerando corrente
Fonte de plasma - DCP Dois anodos de grafite e um catodo de tungstênio, em forma de Y invertido Plasma é formado, colocando-se momentaneamente os eletrodos em contato Ocorre ionização, gerando corrente
Introdução à LC/MS. Introdução
 Introdução à LC/MS Introdução n LC provém a separação, em fase líquida, de misturas complexas, porém dificilmente fornece a identificação positiva de componentes individuais. n MS é uma técnica que auxilia
Introdução à LC/MS Introdução n LC provém a separação, em fase líquida, de misturas complexas, porém dificilmente fornece a identificação positiva de componentes individuais. n MS é uma técnica que auxilia
FORÇAS INTERMOLECULARES
 FORÇAS INTERMOLECULARES São as forças que mantêm os sólidos e líquidos unidos. A ligação covalente que mantém uma molécula unida é uma força intramolecular. A atração entre moléculas é uma força intermolecular.
FORÇAS INTERMOLECULARES São as forças que mantêm os sólidos e líquidos unidos. A ligação covalente que mantém uma molécula unida é uma força intramolecular. A atração entre moléculas é uma força intermolecular.
Energia, calor, entalpia e variação de entalpia.
 Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Química Orgânica I. Formas de representação de moléculas orgânicas e interações intermoleculares Aula 3
 Química rgânica I Formas de representação de moléculas orgânicas e interações intermoleculares Aula 3 Profa. Alceni Augusta Werle ProfaTânia Márcia Sacramento Melo 2- Formas de representação de moléculas
Química rgânica I Formas de representação de moléculas orgânicas e interações intermoleculares Aula 3 Profa. Alceni Augusta Werle ProfaTânia Márcia Sacramento Melo 2- Formas de representação de moléculas
Radiação e Ionização. Proteção e higiene das Radiações I Profª: Marina de Carvalho CETEA
 Radiação e Ionização Proteção e higiene das Radiações I Profª: Marina de Carvalho CETEA Introdução O que é onda? Perturbação em um meio que se propaga transportando energia sem que haja transporte de matéria.
Radiação e Ionização Proteção e higiene das Radiações I Profª: Marina de Carvalho CETEA Introdução O que é onda? Perturbação em um meio que se propaga transportando energia sem que haja transporte de matéria.
O processo de dissolução
 SOLUBILIDADE Sabemos que um soluto altera as propriedades do solvente. Solução sólida: silício dopado com fósforo eletrônica. indústria Sal sobre o gelo abaixa o ponto e congelamento se a temperatura é
SOLUBILIDADE Sabemos que um soluto altera as propriedades do solvente. Solução sólida: silício dopado com fósforo eletrônica. indústria Sal sobre o gelo abaixa o ponto e congelamento se a temperatura é
QUI109 QUÍMICA GERAL (Ciências Biológicas) 4ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 4ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) REAÇÃO EM SOLUÇÃO AQUOSA São reações envolvendo compostos iônicos
QUI109 QUÍMICA GERAL (Ciências Biológicas) 4ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) REAÇÃO EM SOLUÇÃO AQUOSA São reações envolvendo compostos iônicos
Lauro de Sena Laurentino - SEAPQ - LAFIQ - DEQUA - Bio-Manguinhos Cláudio Dutra de Figueira - SEPFI LAFIQ DEQUA - Bio-Manguinhos
 Desenvolvimento e Validação do método de determinação de Fósforo no Polissacarídeo Meningocócico A (PSA) e no Polirribosil Ribitol Fosfato (PRRP) POR ICP-OES Lauro de Sena Laurentino - SEAPQ - LAFIQ -
Desenvolvimento e Validação do método de determinação de Fósforo no Polissacarídeo Meningocócico A (PSA) e no Polirribosil Ribitol Fosfato (PRRP) POR ICP-OES Lauro de Sena Laurentino - SEAPQ - LAFIQ -
A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos...
 Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
Forças Intermoleculares
 Forças Intermoleculares Você já se perguntou por que a água forma gotas ou como os insetos conseguem caminhar sobre a água? Gota d'água caindo sobre a superfície da água. Inseto pousado sobre a superfície
Forças Intermoleculares Você já se perguntou por que a água forma gotas ou como os insetos conseguem caminhar sobre a água? Gota d'água caindo sobre a superfície da água. Inseto pousado sobre a superfície
Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula.
 Aula 01 Composição química de uma célula O que é uma célula? Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula. Toda célula possui a capacidade de crescer,
Aula 01 Composição química de uma célula O que é uma célula? Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula. Toda célula possui a capacidade de crescer,
Fundamentos de Química Profa. Janete Yariwake
 Bloco 2. Soluções. Equilíbrio químico em solução aquosa 2.1 Ácidos e bases 1 Bibliografia - Exercícios selecionados Exercícios retirados dos seguintes livros-texto: J.E. Brady, G.E. Humiston. Química Geral,
Bloco 2. Soluções. Equilíbrio químico em solução aquosa 2.1 Ácidos e bases 1 Bibliografia - Exercícios selecionados Exercícios retirados dos seguintes livros-texto: J.E. Brady, G.E. Humiston. Química Geral,
DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente
 FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
ESPECTROMETRIA DE MASSA ACOPLADA À CROMATOGRAFIA LÍQUIDA E GASOSA: SUA APLICAÇÃO NAS CIÊNCIAS FORENSES
 ESPECTROMETRIA DE MASSA ACOPLADA À CROMATOGRAFIA LÍQUIDA E GASOSA: SUA APLICAÇÃO NAS CIÊNCIAS FORENSES Rafael Christofoli Cavalcanti Bacharel e licenciado em Ciências Biológicas pela Universidade de Brasília
ESPECTROMETRIA DE MASSA ACOPLADA À CROMATOGRAFIA LÍQUIDA E GASOSA: SUA APLICAÇÃO NAS CIÊNCIAS FORENSES Rafael Christofoli Cavalcanti Bacharel e licenciado em Ciências Biológicas pela Universidade de Brasília
02- Quais das propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida?
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016
 CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
Gabarito Química Grupo J. 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor. Considerando-se as substâncias I, II e III mostradas abaixo,
 VESTIB LAR Gabarito Química Grupo J 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor Considerando-se as substâncias I, II e III mostradas abaixo, I) 2-clorobutano II) hidroxi benzeno III) tolueno a) Escreva
VESTIB LAR Gabarito Química Grupo J 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor Considerando-se as substâncias I, II e III mostradas abaixo, I) 2-clorobutano II) hidroxi benzeno III) tolueno a) Escreva
RESOLUÇÃO DA LISTA COMPLEMENTAR INTERAÇÕES INTERMOLECULARES E SUA ASSOCIAÇÃO COM PROPRIEDADES FÍSICAS DAS SUBSTÂNCIAS
 RESOLUÇÃO DA LISTA COMPLEMENTAR INTERAÇÕES INTERMOLECULARES E SUA ASSOCIAÇÃO COM PROPRIEDADES FÍSICAS DAS SUBSTÂNCIAS 1 E Molécula A: apesar de essa molécula apresentar somente ligações polares (entre
RESOLUÇÃO DA LISTA COMPLEMENTAR INTERAÇÕES INTERMOLECULARES E SUA ASSOCIAÇÃO COM PROPRIEDADES FÍSICAS DAS SUBSTÂNCIAS 1 E Molécula A: apesar de essa molécula apresentar somente ligações polares (entre
Acidez e Basicidade de Compostos Orgânicos
 Acidez e Basicidade de Compostos Orgânicos 1. Teorias sobre ácidos e bases Teoria de Arrhenius (1884) Substâncias neutras dissolvidas em água formam espécies carregadas ou íons através de dissociação iônica
Acidez e Basicidade de Compostos Orgânicos 1. Teorias sobre ácidos e bases Teoria de Arrhenius (1884) Substâncias neutras dissolvidas em água formam espécies carregadas ou íons através de dissociação iônica
Reações ácido-base. Ácidos. Ácido = substâncias que se ionizam para formar H + em solução (por exemplo, HCl, HNO 3, CH 3 CO 2 H - vinagre).
 Ácidos Ácido = substâncias que se ionizam para formar H + em solução (por exemplo, HCl, HNO 3, CH 3 CO 2 H - vinagre). H + é conhecido como próton Ácidos com um próton ácido são chamados monopróticos (por
Ácidos Ácido = substâncias que se ionizam para formar H + em solução (por exemplo, HCl, HNO 3, CH 3 CO 2 H - vinagre). H + é conhecido como próton Ácidos com um próton ácido são chamados monopróticos (por
MUDANÇA DE ESTADO ROMPIMENTO DE FORÇAS INTERMOLECULARES
 MUDANÇA DE ESTADO ROMPIMENTO DE FORÇAS INTERMOLECULARES DEFORMAÇÃO DA NUVEM ELETRÔNICA EFEITO COLISÃO = CHOQUE ///// EFEITO INDUÇÃO = VARIAÇÃO ELÉTRICA DIPOLO INDUZIDO FORÇAS DE LONDON ///// DIPOLO INSTANTÂNEO
MUDANÇA DE ESTADO ROMPIMENTO DE FORÇAS INTERMOLECULARES DEFORMAÇÃO DA NUVEM ELETRÔNICA EFEITO COLISÃO = CHOQUE ///// EFEITO INDUÇÃO = VARIAÇÃO ELÉTRICA DIPOLO INDUZIDO FORÇAS DE LONDON ///// DIPOLO INSTANTÂNEO
PROCESSO DE SELEÇÃO 2016/2 ANTES DE RESPONDER ÀS QUESTÕES DESTA PROVA, LEIA ATENTAMENTE ESTAS INSTRUÇÕES:
 Código do candidato PROCESSO DE SELEÇÃO 2016/2 ANTES DE RESPONDER ÀS QUESTÕES DESTA PROVA, LEIA ATENTAMENTE ESTAS INSTRUÇÕES: Escreva o seu código de identificação em todas as folhas de resposta e também
Código do candidato PROCESSO DE SELEÇÃO 2016/2 ANTES DE RESPONDER ÀS QUESTÕES DESTA PROVA, LEIA ATENTAMENTE ESTAS INSTRUÇÕES: Escreva o seu código de identificação em todas as folhas de resposta e também
