A base da espectrometria de massas
|
|
|
- Cíntia Cruz Dias
- 7 Há anos
- Visualizações:
Transcrição
1 A base da espectrometria de massas
2 The father of MS and the first mass spectrometrist to win the Nobel Prize. Pure species and mixtures JJ Thomson's 'Plum Pudding Model' of the atom, a sphere of positive charge containing electrons
3 Mass spectra and isotopes The Nobel Prize in Chemistry 1922 "for his discovery, by means of his mass spectrograph, of isotopes, in a large number of non-radioactive elements, and for his enunciation of the wholenumber rule" Francis William Aston At the end of 1909 he accepted the invitation of Sir J.J.Thomson to work as his assistant at the Cavendish Laboratory, Cambridge, on studies of positive rays. It was during this period that he obtained definite evidence for the existence of two isotopes of the inert gas neon.
4 EI : Ionização por elétrons (Dempster e Nier)
5 Princípio Geral de EI Moléculas neutras, na fase gasosa (dessorção térmica), a uma pressão típica de 10-5 torr, são bombardeadas por elétrons, com energia típica de 70 ev. Ocorre principalmente a retirada ou captura de um eléctron formando íons M +. ou M -.. Íons positivos são em geral predominantes (~100 vezes mais). M -. se tornam importantes para moléculas com alta EA. M + e - (70 ev) M +. (~ 5 ev) + 2e - (65 ev) ē F 1 F 2 M M + F 3 F 4
6
7 Princípios Gerais Processo unimolecular. Os íons formados são rapidamente extraídos da fonte de ionização pelo eletrodo de repulsão ("repeller ). Íons moleculares são formados com excesso de energia interna e se fragmentam total ou parcialmente. EI é bastante popular: produz tanto o íon molecular (massa) como também fragmentos (estrutura); espectros reprodutíveis; bibliotecas de espectros de EI a 70 ev; estável; fácil de operar; alta sensibilidade. Aplica-se a moléculas de média e baixa polaridade e baixo peso molecular (~500u), voláteis e termo-estáveis: moléculas orgânicas relativamente pequenas.
8 Princípios Gerais Quando o íon molecular não é observado (devido a dissociação excessiva), é inútil diminuir a energia dos elétrons. Uma em cada moléculas que entram na fonte de EI é ionizada. EI ocorre em ~10-16 s. Ocorre sem mudanças nas distâncias internucleares (Frank-Condon).
9 Esquema Geral
10 A diminuição da energia dos elétrons provoca uma queda brusca nas intensidades absolutas de todos os íons, mas um aumento na intensidade relativa do íon molecular.
11 Espectros Típicos de EI a 70 ev 2-Hydroxy-1,2-diphenyl-ethanone
12 OH (mainlib) 1-Octanol (mainlib) 1-Octene (mainlib) 2-Octene
13 Alguns espectros de EI apresentam dissociação excessiva, outros pouca dissociação. M +. = massa e isótopos F + = estrutura
14 Espectro de Massas: Ionização por Elétrons (EI)
15 Isômeros C 3 H 6 O
16 M-1 Perda de hidrogênio radicalar M -. H M-15 Perda de metil radicalar M -. CH 3 M-29 Perda de etil radicalar M -. C 2 H 5 M-31 Perda de metoxi radicalar M -. OCH 3 M-43 Perda de propil radicalar M -. C 3 H 7 M-45 Perda de etoxi radicalar M -. OC 2 H 5 M-57 Perda de butil radicalar M -. C 4 H 9 M-2 Perda de hidrogênio M H 2 M-18 Perda de água M H 2 O M-28 Perda de CO ou etileno M-CO ou M- C 2 H 4 M-30 Perda de formaldeido M- CH 2 O M-32 Perda de metanol M-CH 3 OH M-44 Perda de CO 2 M-CO 2 M-60 Perda de ácido acético M-CH 3 CO 2 H
17 OH Íon Molecular (mainlib) 1-Octanol (mainlib) 1-Octene
18 Chemical Ionization CI Munson and Field
19 Princípios Gerais Ionização por reação química (ex: protonação : MH + ). A exotermicidade da reação controla a extensão dos processos dissociativos. Gases ionizantes típicos: metano, isobutano, amônia. Como em EI, aplica-se a moléculas de média e baixa polaridade e baixo peso molecular (~500u), voláteis e termo-estáveis: "moléculas orgânicas". Uma aplicação típica de CI ocorre para substâncias que não apresentam o íon molecular por EI. Adutos formados entre M e o íon reagente podem ser observados (Ex. M-NH 4+ ). Estes adutos podem diferenciar isômeros. CI é uma técnica branda de ionização, por provocar pouca ou nenhuma fragmentação da molécula ionizada.
20 CI IONIZAÇÃO QUÍMICA
21 Ionização Química (CI).
22 Controle da Exotermicidade da Reação: Extensão de Fragmentação Reação Íon/molécula CH 4 + e - 70 ev + CH 4 + CH + 4 CH 3 + H + + CH 4 CH 2 + H 2 + CH 4 + CH 4 CH CH 3 + CH 3 + CH 4 C 2 H H 2 + CH 2 + CH 4 C 2 H H 2 + C 2 H CH 4 C 3 H e - + e - 50 ev térmica H 2 H
23
24 Ionização Química (CI). Ionização Química Positiva: Metano: CH 4 + e -----> CH e > CH 3+ + H. CH CH > CH 5+ + CH. 3 CH CH > C 2 H 5+ + H 2 + H. Isobutano: i-c 4 H 10 + e -----> i-c 4 H e i-c 4 H i-c 4 H > i-c 4 H 9+ + C 4 H 9 +H 2 Amônia: NH 3 + e -----> NH e NH NH > NH 4+ + NH. 2 NH 4+ + NH >N 2 H + 7
25
26 Reserpina EI 70 ev Reserpina CH 4 CI
27 MS?
28 APCI Atmospheric Pressure Chemical Ionization APPI Atmospheric Pressure Photo-Ionization
29 SIMS IONIZAÇÃO POR ÍONS SECUNDÁRIOS 1970 Benninghoven ion guns (LMIG) Ga+ and In+ Csþ ions give higher yield SF5 +, Bi + n, Au + n
30 FAB IONIZAÇÃO POR BOMBARDEAMENTO DE ÁTOMOS ACELERADOS (liquid SIMS)
31 Formação de átomos acelerados Xe + e - IONIZAÇÃO ÁTOMO LENTO Xe + ACELERAÇÃO Xe + ÍON LENTO Xe + ÍON LENTO Xe + + Xe ÍON RÁPIDO ÁTOMO LENTO ÍON RÁPIDO TROCA DE ENERGIA Xe + + Xe ÍON LENTO ÁTOMO RÁPIDO
32 Índice de popularidade - FAB
33 Matrizes
34
35 Efeito da Matriz
36
37 Sistema CF-FAB (continuous-flow FAB)
38 The Nobel Prize in Chemistry 2002 "for the development of methods for identification and structure analyses of biological macromolecules" Yamashita, M.; Fenn, J.B., J. Phys. Chem. 88 (1984) Whitehouse, C.M.; Dreyer, R.N.; Yamashita, M.; Fenn, J.B., Anal. Chem. 57 (1985) 675. Fenn, J.B.; Mann, M.; Meng, C.K.; Wong, S.F.; Whitehouse, C.M., Science 246 (1989) 64. "Electrospray Ionization for Mass Spectrometry of Large Biomolecules,
39 Popularidade do Electrospray
40 Príncipio Geral Uma solução acidificada ou basificada da amostra (ou neutra de um sal) é submetida a um spray eletrolítico sob pressão atmosférica. Um fino spray (aerosol) se forma (cone de taylor) na presença de um alto campo elétrico (+4000V ou 4000V). O contra-íon é oxidado ou reduzido e formam-se gôtas com excesso de carga (positiva ou negativa). O solvente das gôtas evapora com redução de volume, e as gôtas se subdividem. Eventualmente, devido a alta repulsão entre os íons de mesma carga, ou se formam gôtas contendo apenas um íon (modelo CRM) ou íons são expelidos das gôtas para a fase gasosa (modelo IEM de evaporação de íons).
41 O C OH HCl H 3 N + Cl - O C OH V H 3 N + O C OH ESI Positivo NH 2 NaOH H 2 N O C O - Na V H 2 N O C O - ESI Negativo
42
43
44 Enganando as moléculas neutras com curvas Z-spray (Micromass)
45
46 Fonte Z-spray ESI+, Full Scan Extracted at m/z 256 Total Run Time > 25 Hr More than 500 mg salt n = 1 n = Time
47 Fonte de ESI: Ionização sob pressão atmosférica! MS
48 Proteínas Positive ESI-MS m/z spectrum of the protein hen egg white lysozyme
49 Ionização a Pressão Atmosférica (API). Eletrospray (ESI)/Pequenas moléculas Possibilidade de formação de íons com múltiplas cargas
50 Espectros de ESI-MS típicos : Pequenas Moléculas
51 Espectros de ESI-MS típicos : Pequenas Moléculas
52
53 n=(m1-1)/(m2 M1) n=( )/( ) = 14,1 M = n(m1 1) 14 ( )= 15822,8
54
55 MALDI vs ESI
56 Popularidade do Electrospray
57 MS?
58 MALDI Matrix-Assisted Laser Desorption Ionization The Nobel Prize in Chemistry 2002 "for the development of methods for identification and structure analyses of biological macromolecules" (Karas & Hillenkamp )
59 Popularidade do MALDI
60 MALDI fazendo um elefante voar!
61 MALDI fazendo um elefante voar!
62 MALDI- IONIZAÇÃO/DISSORÇÃO A LASER ASSISTIDA POR MATRIZ
63
64 MALDI- IONIZAÇÃO/DISSORÇÃO A LASER ASSISTIDA POR MATRIZ
65 Matrizes (1) α-cyano-4-hydroxycinnamic acid : CCA (2) 3,5-dimethoxy-4-hydroxycinnamic acid (sinapinic acid) : SA (3) 2,5-dihydroxybenzoic acid. Razão matriz-amostra: 100:1 a 5000:1
66 Prepara-se solução da amostra e matriz (pequenas moléculas orgânicas). O solvente é evaporado resultando em uma solução sólido-sólido que é depositada sobre a superfície da sonda. Esta solução é então irradiada com laser. Ocorre aquecimento localizado e seletivo. A matriz absorve fortemente a radiação do laser. Ocorre a evaporação rápida da matriz e a molécula ionizada (ex: MH + ) é então liberada para a fase gasosa, e acelerada em direção ao analisador de massas pelo alto potencial ( V) aplicado à sonda.
67
68
69
70
71 Espectros e Aplicações
72 MALDI de polímeros
73 Conceitos Importantes
74 Notação dos Espectro de Massas 100 Ion Abundance (%) m/z Eixo y: Abundância % Eixo x: Relação massa/carga (m/z) Informações Estruturais Informação da Massa do Compostos
75 Algumas definições importantes Isóbaros São moléculas com diferentes elementos e mesma de massa molecular. Ex.: [C 5 H 6 O 4 ] + ; [C 6 H 10 O 3 ] +, [C 9 H 22 ] + = 130 Da Isótopos São núcleos associados ao mesmo elemento da tabela periódica (mesmo número atômico) mas com diferentes números de nêutrons. Ex: Hidrogênio, Deutério e Trítio
76 Espectro de Massas: ISÓTOPOS Elemento Carbono Hidrogênio Nitrogêio Oxigênio Enxoger Cloro Bromo Isótopo Abund. Relativa Isótopo Abund. Relativa Isótopo Abund. Relativa 12 C C H H N N O O O S S S Cl Cl Br Br 98
77 Espectro de Massas: abundância isotópica Pico monoisotópico Pico do Carbono 13
78 Espectro de Massas Ion Abundance (%) Espectro de dissociação/fragmentação Fragmentos Precursor Íon molecular m/z
79 100 C 7 H 6 O C 60.87% H 4.38% O 34.75% 120 OH 92 O 50 O (mainlib) Benzoic acid, 2-hydroxy-, methyl ester
80 Espectro de Massas: abundância isotópica 25% Para se estimar o número de carbonos em uma molécula: dividir a intensidade de A+1 por 1.1 (abundância do Carbono 13 na natureza). 25 / 1.1 = 23,7 ~ 23 átomos de carbono na molécula
81 Espectro de Massas: abundância isotópica Br - CH 3 15 uma 79 Br-CH 3 =94 81 Br-CH 3 =96 Informações: Relação m/z Presença dos isótopos Diferença de massa entre os sinais
82 Espectro de Massas: abundância isotópica Cloro Peso atômico = 35,453 Mistura de Cloro 35 (75,77%) e Cloro 37 (24,23%) e12 % CH 3 Cl mass
83 Padrão isotópico: Cloro 35 (75,77%) e Cloro 37 (24,23%) % CH 3 Cl % 86.0 CH 2 Cl mass mass % CHCl 3 % CCl mass mass
84 Padrões isotópicos complexos 100 % e12 Composto contendo 1 átomo de Rutênio mass e12 % Composto contendo 2 átomo de Rutênio mass Evidência do número de elementos presentes na molécula
85 Medida de Massa Molecular Ex: M = 249 C 20 H 9 + C 19 H 7 N+ C 13 H 19 N 3 O 2 + Sistemas de Baixa resolução Ex: M = 249 C 20 H C 19 H 7 N C 13 H 19 N 3 O Sistemas de Alta resolução
86 Massa Massa nominal Massa de um íon de uma determinada fórmula empírica calculada através do isótopo mais abundante. Ex : M=249 C 20 H 9+ or C 19 H 7 N + or C 13 H 19 N 3 O 2 + Massa exata Massa de um íon da uma determinada fórmula empírica calculada através da massa exata do isótopo mais abaundante da cada elemento. Ex : M=249 C 20 H C 19 H 7 N C 13 H 19 N 3 O Faixa de massas - Limite superior e inferior de m/z observáveis por um dado analisador de massas.
87 Resolução Medida da habilidade de um analisador de massas de separar íons adjacentes. C 20 H 9 + C 19 H 7 N+ C 13 H 19 N 3 O 2 + C 20 H 9 + C 19 H 7 N+ C 13 H 19 N 3 O compostos diferentes Mesma massa nominal Baixa Resolução 3 compostos diferentes 3 massas exatas diferentes alta resolução
88
89 Massa Exata [C 18 H 15 P] + m/z Massa exata (ppm)=10 6 (M cal. M obs )/M obs
90 Caminhos de Fragmentação
91
92 Possibilidades de EI
93 Regra do Nitrogênio Contém Números ímpares de nitrogênio: Íon molecular [M]+. terá massa ímpar!! Contém Números pares de átomos de Nitrogênio ou não contém átomos de nitrogênio: Íon molecular [M]+. terá massa par!!
94 Regras do elétron impar Regras do elétron par
95 Fragmentação direcionada pelo elétron Fragmentação direcionada pela carga
96 Rearranjos
A base da espectrometria de massas
 A base da espectrometria de massas The father of MS and the first mass spectrometrist to win the Nobel Prize. Pure species and mixtures JJ Thomson's 'Plum Pudding Model' of the atom, a sphere of positive
A base da espectrometria de massas The father of MS and the first mass spectrometrist to win the Nobel Prize. Pure species and mixtures JJ Thomson's 'Plum Pudding Model' of the atom, a sphere of positive
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS
 INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Espectrometria de massas: técnica que separa e mede, em fase gasosa, a relação m/z (massa/carga) de íons produzidos por algum método de ionização. Qual o princípio
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Espectrometria de massas: técnica que separa e mede, em fase gasosa, a relação m/z (massa/carga) de íons produzidos por algum método de ionização. Qual o princípio
Aplicações e características da EM
 Aplicações e características da EM Algumas aplicações da EM: (a) determinação de massa molecular com elevada exatidão, inclusive de biomoléculas e materiais poliméricos; (b) identificação de substancias,
Aplicações e características da EM Algumas aplicações da EM: (a) determinação de massa molecular com elevada exatidão, inclusive de biomoléculas e materiais poliméricos; (b) identificação de substancias,
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS INTRODUÇÃO A ESPECTROMETRIA DE MASSAS. Aplicações
 INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Pioneiros da espectrometria de massas Espectrometria de massas: técnica analítica que separa e mede a relação massa:carga (m/z) de íons, em fase gasosa, produzidos
INTRODUÇÃO A ESPECTROMETRIA DE MASSAS Pioneiros da espectrometria de massas Espectrometria de massas: técnica analítica que separa e mede a relação massa:carga (m/z) de íons, em fase gasosa, produzidos
Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de
 Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de elétrons resultando na formação de M seguida de fragmentação
Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de elétrons resultando na formação de M seguida de fragmentação
Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de
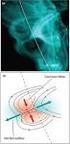 Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de elétrons resultando na formação de M seguida de fragmentação
Aspectos fundamentais de EM Ionizar é preciso: (a) ionização da amostra direta ou indiretamente; (b) método tradicional: ionização por impacto de elétrons resultando na formação de M seguida de fragmentação
QO423 Espectrometria d e de M assas Massas
 QO423 Espectrometria de Massas Oqueéamassadeumátomo? um M = 5 1 H (1p, 1e) = 1.0079 2 H (1p, 1n, 1e) = 2.0141 4 He (2p, 2n, 2e) = 4.0026 4 He/ 2 H = 1.98!! Como é um átomo? Como o núcleo não explode?!!
QO423 Espectrometria de Massas Oqueéamassadeumátomo? um M = 5 1 H (1p, 1e) = 1.0079 2 H (1p, 1n, 1e) = 2.0141 4 He (2p, 2n, 2e) = 4.0026 4 He/ 2 H = 1.98!! Como é um átomo? Como o núcleo não explode?!!
n LC provém a separação, em fase líquida, de misturas complexas, porém dificilmente fornece a identificação positiva de componentes individuais.
 Introdução à LC/MS Introdução n LC provém a separação, em fase líquida, de misturas complexas, porém dificilmente fornece a identificação positiva de componentes individuais. n MS é uma técnica que auxilia
Introdução à LC/MS Introdução n LC provém a separação, em fase líquida, de misturas complexas, porém dificilmente fornece a identificação positiva de componentes individuais. n MS é uma técnica que auxilia
Espectrometria de Massas
 Introdução Mede as massas e abundâncias dos íons na fase gasosa. É bastante sensível e fornece informações qualitativas e quantitativas. É possível distinguir substâncias diferentes, que apresentam o mesmo
Introdução Mede as massas e abundâncias dos íons na fase gasosa. É bastante sensível e fornece informações qualitativas e quantitativas. É possível distinguir substâncias diferentes, que apresentam o mesmo
Como funciona a espectrometria de massas acoplada à cromatografia?
 Espectrometria de Massas: Introdução Sistemas de vácuo Fontes de Ionização Analisadores de massa Resolução e Exatidão de Massa Detectores MS/MS Álvaro José dos Santos Neto O que é a espectrometria de massas?
Espectrometria de Massas: Introdução Sistemas de vácuo Fontes de Ionização Analisadores de massa Resolução e Exatidão de Massa Detectores MS/MS Álvaro José dos Santos Neto O que é a espectrometria de massas?
Análise proteômica e metabolômica por espectrometria de massas Analisadores de massas
 Análise proteômica e metabolômica por espectrometria de massas Analisadores de massas Prof. Alexandre K. Tashima Departamento de Bioquímica EPM/UNIFESP Bibliografia Mass Spectrometry, a Textbook. Ju rgen
Análise proteômica e metabolômica por espectrometria de massas Analisadores de massas Prof. Alexandre K. Tashima Departamento de Bioquímica EPM/UNIFESP Bibliografia Mass Spectrometry, a Textbook. Ju rgen
ESPECTROMETRIA DE MASSAS
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DISCIPLINA: INORGÂNICA AVANÇADA II ESPECTROMETRIA DE MASSAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA DISCIPLINA: INORGÂNICA AVANÇADA II ESPECTROMETRIA DE MASSAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
Espectrometria de Massas
 Componentes de um Espectrômetro de Massas Alto vácuo (10 5 a 10 8 mbar Inlet Fonte de Íons Analisador Detector CG HPLC Bomba Seringa EI CI MALDI ESI APCI Quadrupolo TOF Ion Trap FT-ICR Setor Magnético
Componentes de um Espectrômetro de Massas Alto vácuo (10 5 a 10 8 mbar Inlet Fonte de Íons Analisador Detector CG HPLC Bomba Seringa EI CI MALDI ESI APCI Quadrupolo TOF Ion Trap FT-ICR Setor Magnético
3 Espectrometria de Massa
 3 Espectrometria de Massa 3.1 Princípios A espectrometria de massa determina as razões massa/carga de íons emitidos quando uma amostra é excitada por algum agente ionizante. Os agentes ionizantes podem
3 Espectrometria de Massa 3.1 Princípios A espectrometria de massa determina as razões massa/carga de íons emitidos quando uma amostra é excitada por algum agente ionizante. Os agentes ionizantes podem
Química. 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30
 Química 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30 02. Para que um átomo de número atômico 55 e número de massa 137 seja eletricamente neutro, ele deverá ter, necessariamente:
Química 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30 02. Para que um átomo de número atômico 55 e número de massa 137 seja eletricamente neutro, ele deverá ter, necessariamente:
Estratégias para interpretação de espectros de massas
 Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
Estratégias para interpretação de espectros de massas Composição elementar dos íons a partir de medidas exatas de massas. Resolução em espectrometria de massas. Padrões isotópicos. Etapas na identificação
Algumas considerações iniciais. Interpretação de espectros de massas
 Interpretação de espectros de massas 1. A maioria dos espectros de massas não são de interpretação fácil sem informações adicionais, tais como análise elementar, RMN, etc. 2. Os padrões de fragmentação
Interpretação de espectros de massas 1. A maioria dos espectros de massas não são de interpretação fácil sem informações adicionais, tais como análise elementar, RMN, etc. 2. Os padrões de fragmentação
Espectrometria de Massas: Estudo Dirigido
 1 Disciplina: Química Orgânica III / 2009.2 Ministrante: Prof. Dr. Sidney Lima 1). O que é um EM e qual a utilidade da EM? Espectrometria de Massas: Estudo Dirigido R = Nos permite determinar a massa molecular
1 Disciplina: Química Orgânica III / 2009.2 Ministrante: Prof. Dr. Sidney Lima 1). O que é um EM e qual a utilidade da EM? Espectrometria de Massas: Estudo Dirigido R = Nos permite determinar a massa molecular
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008.
 UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
Estudo de Fragmentação
 Estudo de Fragmentação EI - fragmentação de alta energia (carga e radical) ESI fragmentação direcionado pela carga CID: Baixa tensão de Cone Cone de extração 5V Cone de amostra 3V Hexapolo CID: Baixa
Estudo de Fragmentação EI - fragmentação de alta energia (carga e radical) ESI fragmentação direcionado pela carga CID: Baixa tensão de Cone Cone de extração 5V Cone de amostra 3V Hexapolo CID: Baixa
Resumo de Mecanismos de fragmentação
 Resumo de Mecanismos de fragmentação Clivagem s. Clivagem a: iniciada pelo sítio radicalar. Clivagem i: iniciada pela carga do íon. Fragmentações subseqüentes por transferência 1,2 ou 1,4 de H. Rearranjo
Resumo de Mecanismos de fragmentação Clivagem s. Clivagem a: iniciada pelo sítio radicalar. Clivagem i: iniciada pela carga do íon. Fragmentações subseqüentes por transferência 1,2 ou 1,4 de H. Rearranjo
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução
 Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
Espectrometria de massas
 Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
LISTA DE EXERCÍCIO PARA A PROVA MENSAL
 Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Técnicas Modernas em Espectrometria de Massas
 XXVI SEMANA DA QUÍMICA III JORNADA DE PÓS-GRADUAÇÃO EM QUÍMICA Técnicas Modernas em Espectrometria de Massas Prof. Luiz Alberto (Beto) luizmoraes@ffclrp.usp.br Objetivo O principal objetivo deste curso
XXVI SEMANA DA QUÍMICA III JORNADA DE PÓS-GRADUAÇÃO EM QUÍMICA Técnicas Modernas em Espectrometria de Massas Prof. Luiz Alberto (Beto) luizmoraes@ffclrp.usp.br Objetivo O principal objetivo deste curso
FUVEST 1984 Primeira fase e Segunda fase
 FUVEST 1984 Primeira fase e Segunda fase Professora Sonia 9. A melhor maneira de separar os três componentes de uma mistura de areia com solução aquosa de sal é: CONHECIMENTOS GERAIS 5. O peso atômico
FUVEST 1984 Primeira fase e Segunda fase Professora Sonia 9. A melhor maneira de separar os três componentes de uma mistura de areia com solução aquosa de sal é: CONHECIMENTOS GERAIS 5. O peso atômico
Espectrometria de massa & análise de biomoléculas
 Espectrometria de massa & análise de biomoléculas Curso de Inverno 16/07/2012 Sayuri Miyamoto Tópicos I. Breve Introdução II. Espectrômetros de Massa III. Aplicações em Análise de Biomoléculas 1 Os primeiros
Espectrometria de massa & análise de biomoléculas Curso de Inverno 16/07/2012 Sayuri Miyamoto Tópicos I. Breve Introdução II. Espectrômetros de Massa III. Aplicações em Análise de Biomoléculas 1 Os primeiros
Acoplamento LC-ESI-MS. Electrospray - ESI. ESI (com assistência pneumática) old term: Ionspray 01/06/2017. Cromatografia líquidaespectrometria LC-MS
 Acoplamento LC-ESI-MS Cromatografia líquidaespectrometria de massas: LC-MS Melhor opção para análise de fármacos Álvaro José dos Santos Neto Mais compatível com baixas vazões Electrospray - ESI Mecanismos
Acoplamento LC-ESI-MS Cromatografia líquidaespectrometria de massas: LC-MS Melhor opção para análise de fármacos Álvaro José dos Santos Neto Mais compatível com baixas vazões Electrospray - ESI Mecanismos
UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI
 UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI Questão 1 Em uma análise química desejava-se determinar o teor percentual de zinco em 96,57g de uma amostra
UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE CIÊNCIAS OLIMPÍADA BRASILEIRA DE QUÍMICA 2004 FASE VI Questão 1 Em uma análise química desejava-se determinar o teor percentual de zinco em 96,57g de uma amostra
Espectrometria de massas Princípios básicos Teoria DESENVOLVENDO UMA CIÊNCIA MELHOR AGILENT E VOCÊ
 Espectrometria de massas Princípios básicos Teoria DESENVOLVENDO UMA CIÊNCIA MELHOR AGILENT E VOCÊ 1 A Agilent Technologies tem um compromisso com a comunidade educacional e está disposta a conceder acesso
Espectrometria de massas Princípios básicos Teoria DESENVOLVENDO UMA CIÊNCIA MELHOR AGILENT E VOCÊ 1 A Agilent Technologies tem um compromisso com a comunidade educacional e está disposta a conceder acesso
FNC376N: Lista de junho de A energia de dissociação às vezes é expressa em quilocalorias por mol (kcal/mol). No SI se utiliza kj/mol.
 FNC376N: Lista 7 23 de junho de 2004 9-1 Ligação iônica 9-1. A energia de dissociação às vezes é expressa em quilocalorias por mol (kcal/mol). No SI se utiliza kj/mol. a) Determine a relação entre ev/molécula
FNC376N: Lista 7 23 de junho de 2004 9-1 Ligação iônica 9-1. A energia de dissociação às vezes é expressa em quilocalorias por mol (kcal/mol). No SI se utiliza kj/mol. a) Determine a relação entre ev/molécula
Espectrometria de Massas (MS)
 Universidade de São Paulo Instituto de Química de São Carlos Departamento de Química e Física Molecular Disciplina: SQM0418 - Análise Instrumental II Espectrometria de Massas (MS) Álvaro José dos Santos
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Química e Física Molecular Disciplina: SQM0418 - Análise Instrumental II Espectrometria de Massas (MS) Álvaro José dos Santos
Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons)
 Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons) Clivagem α: fragmentação iniciada pelo sítio radicalar em acetona Fragmentações do íon molecular podem
Mecanismos mais comuns de fragmentação observados em espectros de massas (ionização por elétrons) Clivagem α: fragmentação iniciada pelo sítio radicalar em acetona Fragmentações do íon molecular podem
Física e Química A 10.º ano
 Massa e tamanho dos átomos 1. Seleciona a opção que completa corretamente a frase. O ião Y 2+ formou-se por a) perda de dois protões. b) ganho de dois eletrões. c) ganho de dois protões. d) perda de dois
Massa e tamanho dos átomos 1. Seleciona a opção que completa corretamente a frase. O ião Y 2+ formou-se por a) perda de dois protões. b) ganho de dois eletrões. c) ganho de dois protões. d) perda de dois
2 NH 3 (g) + CO 2 (g)
 PROCESSO SELETIVO 2007 1 O DIA GABARITO 4 7 QUÍMICA QUESTÕES DE 16 A 30 16. O equilíbrio de ionização da água pura é dado pela equação abaixo, cuja constante do produto iônico é 2,5x10-14, a 37 o C. H
PROCESSO SELETIVO 2007 1 O DIA GABARITO 4 7 QUÍMICA QUESTÕES DE 16 A 30 16. O equilíbrio de ionização da água pura é dado pela equação abaixo, cuja constante do produto iônico é 2,5x10-14, a 37 o C. H
16. Em soluções aquosas o ânion dicromato está em equilíbrio dinâmico com o ânion cromato, segundo a reação representada por:
 PROCESSO SELETIVO 2007 1 O DIA GABARITO 2 7 QUÍMICA QUESTÕES DE 16 A 30 16. Em soluções aquosas o ânion dicromato está em equilíbrio dinâmico com o ânion cromato, segundo a reação representada por: Cr
PROCESSO SELETIVO 2007 1 O DIA GABARITO 2 7 QUÍMICA QUESTÕES DE 16 A 30 16. Em soluções aquosas o ânion dicromato está em equilíbrio dinâmico com o ânion cromato, segundo a reação representada por: Cr
2 KClO 3 2 KCl + 3 O 2
 PROCESSO SELETIVO 2007 1 O DIA GABARITO 1 7 QUÍMICA QUESTÕES DE 16 A 30 16. O ânion cloreto (Cl - ), o argônio (Ar) e o cátion potássio (K + ) têm em comum o mesmo número: a) de prótons. b) de elétrons.
PROCESSO SELETIVO 2007 1 O DIA GABARITO 1 7 QUÍMICA QUESTÕES DE 16 A 30 16. O ânion cloreto (Cl - ), o argônio (Ar) e o cátion potássio (K + ) têm em comum o mesmo número: a) de prótons. b) de elétrons.
IME º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 IME - 2003 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Uma fonte de vanádio é o mineral vanadinita, cuja fórmula é Pb 5 (VO 4 ) 3 Cl. DETERMINE: A) A porcentagem em massa de vanádio
IME - 2003 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Uma fonte de vanádio é o mineral vanadinita, cuja fórmula é Pb 5 (VO 4 ) 3 Cl. DETERMINE: A) A porcentagem em massa de vanádio
XIII Olimpíada Baiana de Química Exame 2018
 GABARITO Questões discursivas Data da aplicação da prova: 04/08/2018 Data da publicação do gabarito: 05/10/2018 Questão 01 (Peso 3) Uma fita de magnésio com dimensão de 2,0 cm foi aquecida em uma chama
GABARITO Questões discursivas Data da aplicação da prova: 04/08/2018 Data da publicação do gabarito: 05/10/2018 Questão 01 (Peso 3) Uma fita de magnésio com dimensão de 2,0 cm foi aquecida em uma chama
Em nosso planeta o hidrogênio é encontrado na forma combinada, na água, nos oceanos, nos rios, nos minerais e até nos seres vivos.
 Aula: 02 Temática: Hidrogênio Na última aula você aprendeu sobre os gases nobres. Nessa aula continuaremos nos gases, mas não nos nobres, falaremos então sobre o gás de grande abundância no universo: o
Aula: 02 Temática: Hidrogênio Na última aula você aprendeu sobre os gases nobres. Nessa aula continuaremos nos gases, mas não nos nobres, falaremos então sobre o gás de grande abundância no universo: o
44. Com relação aos compostos representados abaixo, é INCORRETO afirmar que: N(CH 2 CH 3 ) 3 CH 3 CO 2 H ClCH 2 CO 2 H I II III
 22 GABARITO 1 1º DIA 2º Processo Seletivo/2004 44. Com relação aos compostos representados abaixo, é INCORRETO afirmar que: N(CH 2 CH 3 ) 3 CH 3 CO 2 H ClCH 2 CO 2 H I II III a) o composto III é um ácido
22 GABARITO 1 1º DIA 2º Processo Seletivo/2004 44. Com relação aos compostos representados abaixo, é INCORRETO afirmar que: N(CH 2 CH 3 ) 3 CH 3 CO 2 H ClCH 2 CO 2 H I II III a) o composto III é um ácido
FUVEST 1981 Primeira fase e Segunda fase
 FUVEST 1981 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 5. Nas condições ambientes, pastilhas de hidróxido de sódio, expostas ao ar durante várias horas, transformam-se em um líquido claro. Este
FUVEST 1981 Primeira fase e Segunda fase CONHECIMENTOS GERAIS 5. Nas condições ambientes, pastilhas de hidróxido de sódio, expostas ao ar durante várias horas, transformam-se em um líquido claro. Este
LISTA 02 - TEORIA ATÔMICA MOLECULAR
 LISTA 02 - TEORIA ATÔMICA MOLECULAR 1º ano QUÍMICA PROF. PEDRO 2º Bimestre Questão 01) A massa de uma molécula de ácido acético, CH 3 COOH, é: a) 1,0. 10-21 g b) 1,0. 10-22 g c) 1,0. 10-23 g d) 1,0. 10-24
LISTA 02 - TEORIA ATÔMICA MOLECULAR 1º ano QUÍMICA PROF. PEDRO 2º Bimestre Questão 01) A massa de uma molécula de ácido acético, CH 3 COOH, é: a) 1,0. 10-21 g b) 1,0. 10-22 g c) 1,0. 10-23 g d) 1,0. 10-24
Geometria Molecular e Forças Intermoleculares
 Geometria Molecular e Forças Intermoleculares GEOMETRIA MOLECULAR DEPENDE: Disposição espacial dos núcleos dos átomos. Repulsão dos pares eletrônicos das ligações ou pares livres dos átomos. Obs. Toda
Geometria Molecular e Forças Intermoleculares GEOMETRIA MOLECULAR DEPENDE: Disposição espacial dos núcleos dos átomos. Repulsão dos pares eletrônicos das ligações ou pares livres dos átomos. Obs. Toda
Mary Santiago Silva 16/04/2010
 Espectrometria de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Técnica analítica, utilizada para identificar e quantificar compostos conhecidos e elucidar a estrutura
Espectrometria de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Técnica analítica, utilizada para identificar e quantificar compostos conhecidos e elucidar a estrutura
 MATERIAIS «Nós somos química e o resto do Universo também» Os conhecimentos de Química são essenciais para a compreensão dos fenômenos naturais, desde a microscópica divisão celular à astronômica explosão
MATERIAIS «Nós somos química e o resto do Universo também» Os conhecimentos de Química são essenciais para a compreensão dos fenômenos naturais, desde a microscópica divisão celular à astronômica explosão
LIGAÇÃO COVALENTE: PRINCÍPIOS/ESTRUTURAS DE LEWIS. QFL-4010 Prof. Gianluca C. Azzellini
 LIGAÇÃO COVALENTE: PRINCÍPIOS/ESTRUTURAS DE LEWIS LIGAÇÃO QUÍMICA Principais Tipos de Ligação Química Iônica Covalente Metálica Gilbert N. Lewis LIGAÇÃO COVALENTE: Compartilhamento de elétrons entre dois
LIGAÇÃO COVALENTE: PRINCÍPIOS/ESTRUTURAS DE LEWIS LIGAÇÃO QUÍMICA Principais Tipos de Ligação Química Iônica Covalente Metálica Gilbert N. Lewis LIGAÇÃO COVALENTE: Compartilhamento de elétrons entre dois
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
Massa Atômica e Molecular, Mol
 Capítulo Massa Atômica e Molecular, Mol Leia o texto seguinte, referente ao espectrógrafo de massa, e a seguir resolva os exercícios de a 6. É um aparelho capaz de fornecer a composição isotópica qualitativa
Capítulo Massa Atômica e Molecular, Mol Leia o texto seguinte, referente ao espectrógrafo de massa, e a seguir resolva os exercícios de a 6. É um aparelho capaz de fornecer a composição isotópica qualitativa
Uma fonte de vanádio é o mineral vanadinita, cuja fórmula é Pb 5 (VO 4 ) 3 Cl. Determine: a) a porcentagem em massa de vanádio nesse mineral;
 1 a QUESTÃO Valor 1,0 Uma fonte de vanádio é o mineral vanadinita, cuja fórmula é Pb 5 (VO 4 ) 3 Cl. Determine: a) a porcentagem em massa de vanádio nesse mineral; b) a massa em gramas de vanádio numa
1 a QUESTÃO Valor 1,0 Uma fonte de vanádio é o mineral vanadinita, cuja fórmula é Pb 5 (VO 4 ) 3 Cl. Determine: a) a porcentagem em massa de vanádio nesse mineral; b) a massa em gramas de vanádio numa
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 4
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considerando que, a uma certa temperatura,
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considerando que, a uma certa temperatura,
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 3
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Assinale a alternativa correta.
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Assinale a alternativa correta.
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 1
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Em um reator, colocam-se 1,0 mol
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Em um reator, colocam-se 1,0 mol
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 2
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Os números de oxidação dos átomos
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Os números de oxidação dos átomos
HIDROGÊNIO CQ133 FSN
 HIDROGÊNIO CQ133 FSN GASES NOBRES CQ133 FSN HIDROGÊNIO o hidrogênio é o elemento mais abundante do universo com 92% seguido do hélio (7%) e os demais elementos (1%); é quarto elemento mais abundante na
HIDROGÊNIO CQ133 FSN GASES NOBRES CQ133 FSN HIDROGÊNIO o hidrogênio é o elemento mais abundante do universo com 92% seguido do hélio (7%) e os demais elementos (1%); é quarto elemento mais abundante na
3º Trimestre Sala de estudos Química Data: 03/12/18 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº
 3º Trimestre Sala de estudos Química Data: 03/12/18 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº Conteúdo: FAMERP/UNIFESP (REVISÃO) Questão 01 - (FAMERP SP/2018) A tabela indica a abundância aproximada
3º Trimestre Sala de estudos Química Data: 03/12/18 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº Conteúdo: FAMERP/UNIFESP (REVISÃO) Questão 01 - (FAMERP SP/2018) A tabela indica a abundância aproximada
Colégio São Paulo-Teresópolis/RJ. Projeto Sabadão. Química. Raquel Berco
 Colégio São Paulo-Teresópolis/RJ Projeto Sabadão Química Raquel Berco Ligações químicas: são constituídas de elétrons. Devemos respeitar a regra do octeto. Regra do Octeto : todo elemento tende a se estabilizar
Colégio São Paulo-Teresópolis/RJ Projeto Sabadão Química Raquel Berco Ligações químicas: são constituídas de elétrons. Devemos respeitar a regra do octeto. Regra do Octeto : todo elemento tende a se estabilizar
Estabilidade dos Átomos
 Ligações Químicas Estabilidade dos Átomos Os gases nobres são os únicos encontrados na natureza na forma monoatômica, ou seja, não se ligam se, apresentam na forma de átomos. Os gases nobres, com exceção
Ligações Químicas Estabilidade dos Átomos Os gases nobres são os únicos encontrados na natureza na forma monoatômica, ou seja, não se ligam se, apresentam na forma de átomos. Os gases nobres, com exceção
1º Questão: Escreva a distribuição eletrônica dos elementos abaixo e determine o número de valência de cada elemento: a) Fe (26):.
 FOLHA DE EXERCÍCIOS CURSO: Otimizado ASS.: Exercícios de Conteúdo DISCIPLINA: Fundamentos de Química e Bioquímica NOME: TURMA: 1SAU 1º Questão: Escreva a distribuição eletrônica dos elementos abaixo e
FOLHA DE EXERCÍCIOS CURSO: Otimizado ASS.: Exercícios de Conteúdo DISCIPLINA: Fundamentos de Química e Bioquímica NOME: TURMA: 1SAU 1º Questão: Escreva a distribuição eletrônica dos elementos abaixo e
A estrutura atômica do hidrogênio, a mais simples de todos os elementos químicos, apresenta um próton no núcleo, e um elétron, na camada externa.
 O ELEMENTO HIDROGÊNIO INTRODUÇÃO Embora na terra ocupe o nono lugar entre os elementos em termos de ocorrência, correspondendo a 0,9% da massa do planeta, é o mais abundante no universo, pois apresenta
O ELEMENTO HIDROGÊNIO INTRODUÇÃO Embora na terra ocupe o nono lugar entre os elementos em termos de ocorrência, correspondendo a 0,9% da massa do planeta, é o mais abundante no universo, pois apresenta
Ligações Químicas. No hidrônio, quantos pares de elétrons pertencem, no total, tanto ao hidrogênio quanto ao oxigênio? a) 1 b) 2 c) 3 d) 4 e) 6
 Aluno(a): Prof.: Éderson Ligações Químicas Questão 1) Abaixo temos as fórmulas de Lewis para átomos de cinco elementos químicos. Fórmulas eletrônicas de Lewis para alguns elementos Podemos afirmar que
Aluno(a): Prof.: Éderson Ligações Químicas Questão 1) Abaixo temos as fórmulas de Lewis para átomos de cinco elementos químicos. Fórmulas eletrônicas de Lewis para alguns elementos Podemos afirmar que
Fundamentos de Química. PROFª LORAINE JACOBS
 Fundamentos de Química PROFª LORAINE JACOBS lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Matéria e Energia Matéria e Energia Matéria Essência Tem existência física real Tem
Fundamentos de Química PROFª LORAINE JACOBS lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Matéria e Energia Matéria e Energia Matéria Essência Tem existência física real Tem
Unidade I Átomos, Moléculas e íons
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC QUÍMICA GERAL I - QGE1001 Unidade I Átomos, Moléculas e íons Profª Drª Karine P. Naidek 1 2 Estrutura
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC QUÍMICA GERAL I - QGE1001 Unidade I Átomos, Moléculas e íons Profª Drª Karine P. Naidek 1 2 Estrutura
QB70D:// Química (Turmas S15/S16) Ligações Químicas
 QB70D:// Química (Turmas S15/S16) Ligações Químicas Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Estrutura de Lewis É muito importante saber desenhar estruturas de Lewis para moléculas
QB70D:// Química (Turmas S15/S16) Ligações Químicas Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Estrutura de Lewis É muito importante saber desenhar estruturas de Lewis para moléculas
Exercícios Sobre Massa atômica e molecular
 Exercícios Sobre Massa atômica e molecular Dado: 01. As massas moleculares do álcool etílico (C 2H 5OH) e do ácido acético (C 2H 4O 2) são respectivamente: a) 60 u e 46 u b) 66 u e 40 u c) 46 u e 66 u
Exercícios Sobre Massa atômica e molecular Dado: 01. As massas moleculares do álcool etílico (C 2H 5OH) e do ácido acético (C 2H 4O 2) são respectivamente: a) 60 u e 46 u b) 66 u e 40 u c) 46 u e 66 u
2) Um átomo T apresenta menos 2 prótons que um átomo Q. Com base nessa informação, assinale a opção falsa.
 1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
PROPRIEDADES DOS ELEMENTOS
 PROPRIEDADES DOS ELEMENTOS Classificação dos Elementos : Hidrogênio 1 elemento : Metais 93 elementos : Ametais 11 elementos : Semimetais 7 elementos : Gases nobres 6 elementos Estrutura da Tabela Periódica
PROPRIEDADES DOS ELEMENTOS Classificação dos Elementos : Hidrogênio 1 elemento : Metais 93 elementos : Ametais 11 elementos : Semimetais 7 elementos : Gases nobres 6 elementos Estrutura da Tabela Periódica
FORÇAS INTERMOLECULARES
 FORÇAS INTERMOLECULARES São as forças que mantêm os sólidos e líquidos unidos. A ligação covalente que mantém uma molécula unida é uma força intramolecular. A atração entre moléculas é uma força intermolecular.
FORÇAS INTERMOLECULARES São as forças que mantêm os sólidos e líquidos unidos. A ligação covalente que mantém uma molécula unida é uma força intramolecular. A atração entre moléculas é uma força intermolecular.
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS
 PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
Estrutura atômica e ligação interatômica. Profa. Daniela Becker
 Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica
 Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Disciplina: Química Professor: Rubens Barreto. III Unidade
 Disciplina: Química Professor: Rubens Barreto III Unidade Ligações Químicas Ligações iônicas Tipos de Ligações Ligações covalentes Ligações metálicas Os gases nobres e a regra do octeto Todas as substâncias
Disciplina: Química Professor: Rubens Barreto III Unidade Ligações Químicas Ligações iônicas Tipos de Ligações Ligações covalentes Ligações metálicas Os gases nobres e a regra do octeto Todas as substâncias
Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel
 Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Fundamentos de Química Profa. Janete Yariwake
 2. Introdução: Conceitos e cálculos fundamentais (Estequiometria; Concentrações) 1 Lei das proporções definidas (Lei de Proust) Em uma substância química, os elementos estão sempre presentes em proporções
2. Introdução: Conceitos e cálculos fundamentais (Estequiometria; Concentrações) 1 Lei das proporções definidas (Lei de Proust) Em uma substância química, os elementos estão sempre presentes em proporções
Cálculos Químicos. Mol, massa molar, Constante de Avogadro
 Cálculos Químicos Mol, massa molar, Constante de Avogadro Medidas massa (Kg SI) 1 Kg 1000 g Grama 1 g Massa átomo? Unidade? Massa atômica Unidade de massa atômica 1 u massa de 1/12 do átomo de carbono
Cálculos Químicos Mol, massa molar, Constante de Avogadro Medidas massa (Kg SI) 1 Kg 1000 g Grama 1 g Massa átomo? Unidade? Massa atômica Unidade de massa atômica 1 u massa de 1/12 do átomo de carbono
Química 4 Módulo 5. Módulo 6 COMENTÁRIOS ATIVIDADES PARA SALA COMENTÁRIOS ATIVIDADES PROPOSTAS CLASSIFICAÇÃO PERIÓDICA CLASSIFICAÇÃO DOS ELEMENTOS
 Química 4 Módulo 5 CLSSIFICÇÃO PERIÓDIC Elementos de um mesmo grupo ou família apresentam o mesmo número de elétrons na última camada Em 93, o inglês Henry G J Moseley (884-95 estabeleceu o conceito de
Química 4 Módulo 5 CLSSIFICÇÃO PERIÓDIC Elementos de um mesmo grupo ou família apresentam o mesmo número de elétrons na última camada Em 93, o inglês Henry G J Moseley (884-95 estabeleceu o conceito de
RELAÇÕES DE MASSA E MOL
 RELAÇÃO DE MASSA E MOL A relação entre massa e quantidade Em uma gota de água de 0,05 ml há 1,67 sextilhão (1,67 x 10 21 ) de moléculas de água. A relação entre massa e quantidade A unidade de massa atômica
RELAÇÃO DE MASSA E MOL A relação entre massa e quantidade Em uma gota de água de 0,05 ml há 1,67 sextilhão (1,67 x 10 21 ) de moléculas de água. A relação entre massa e quantidade A unidade de massa atômica
UFSC. Resposta: = 40. Comentário
 Resposta: 08 + 32 = 40 01. Incorreta. O butano não possui isomeria óptica, pois não possui carbono assimétrico. 02. Incorreta. Ao serem liberados para a atmosfera os gases sofrem expansão de volume. 04.
Resposta: 08 + 32 = 40 01. Incorreta. O butano não possui isomeria óptica, pois não possui carbono assimétrico. 02. Incorreta. Ao serem liberados para a atmosfera os gases sofrem expansão de volume. 04.
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 4
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considerando os compostos I e II,
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considerando os compostos I e II,
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 1
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Três átomos cujos números atômicos
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Três átomos cujos números atômicos
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 3
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Observe os dados a seguir: 2Mg
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Observe os dados a seguir: 2Mg
QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. Prova 3 Química QUESTÕES OBJETIVAS GABARITO 2
 Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considerando a equação química
Prova 3 QUESTÕES OBJETIVAS QUESTÕES APLICADAS A TODOS OS CANDIDATOS QUE REALIZARAM A PROVA ESPECÍFICA DE QUÍMICA. UEM Comissão Central do Vestibular Unificado QUÍMICA 01 Considerando a equação química
EXERCÍCIOS DE APLICAÇÃO
 GRANDEZAS QUÍMICAS EXERCÍCIOS DE APLICAÇÃO 01 (ETF-SP) A massa atômica de um elemento químico é dada pela média ponderada dos isótopos. Por exemplo, a massa do oxigênio que aparece na tabela é 15,99, isto
GRANDEZAS QUÍMICAS EXERCÍCIOS DE APLICAÇÃO 01 (ETF-SP) A massa atômica de um elemento químico é dada pela média ponderada dos isótopos. Por exemplo, a massa do oxigênio que aparece na tabela é 15,99, isto
QB70C:// Química (Turmas S71/S72) Ligação Química
 QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente
 FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO QUÍMICA É A FORÇA QUE MANTÉM ÁTOMOS E/OU ÍONS UNIDOS NAS
QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO QUÍMICA É A FORÇA QUE MANTÉM ÁTOMOS E/OU ÍONS UNIDOS NAS
Disciplina de Química Geral Profa. Marcia Margarete Meier
 Soluções 1 Propriedades gerais das soluções Os materiais são feitos geralmente de misturas de substâncias mais simples. Ex.: ar, sangue, água do mar, ligas metálicas, perfumes, etc As composições precisam
Soluções 1 Propriedades gerais das soluções Os materiais são feitos geralmente de misturas de substâncias mais simples. Ex.: ar, sangue, água do mar, ligas metálicas, perfumes, etc As composições precisam
com o oxigênio, formando o trióxido de enxofre (SO 3 ), e deste com a água, resultando no H 2
 11 Em 2004 iniciou-se, no Brasil, a exploração de uma importante jazida de minério de cobre. Nestes minérios, o metal é normalmente encontrado na forma de sulfetos, como o CuS, e para sua obtenção o minério
11 Em 2004 iniciou-se, no Brasil, a exploração de uma importante jazida de minério de cobre. Nestes minérios, o metal é normalmente encontrado na forma de sulfetos, como o CuS, e para sua obtenção o minério
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
Espectrometria de Massas QP422. Prof. Dr. Fábio Cesar Gozzo fabio@iqm.unicamp.br
 Espectrometria de Massas QP422 Prof. Dr. Fábio Cesar Gozzo fabio@iqm.unicamp.br Introdução Espectrometria de massas (MS, do inglês Mass Spectrometry) é o estudo da matéria através da formação de íons em
Espectrometria de Massas QP422 Prof. Dr. Fábio Cesar Gozzo fabio@iqm.unicamp.br Introdução Espectrometria de massas (MS, do inglês Mass Spectrometry) é o estudo da matéria através da formação de íons em
Resolução de Questões de Provas Específicas de Química (Aula 7)
 Resolução de Questões de Provas Específicas de Química (Aula 7) Resolução de Questões de Provas Específicas (Aula 7) 1. (UECE) A tabela periódica já era objeto das preocupações dos antigos químicos a partir
Resolução de Questões de Provas Específicas de Química (Aula 7) Resolução de Questões de Provas Específicas (Aula 7) 1. (UECE) A tabela periódica já era objeto das preocupações dos antigos químicos a partir
Massa atômica, molecular e molar mol
 Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama. Disciplina: Química Volume: 1 Série: 7 Massa atômica, molecular e molar mol 1. D I. Verdadeira II. Verdadeira 12 6C (6 prótons + 6 nêutrons).
Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama. Disciplina: Química Volume: 1 Série: 7 Massa atômica, molecular e molar mol 1. D I. Verdadeira II. Verdadeira 12 6C (6 prótons + 6 nêutrons).
Atividade extra. Questão 1 Cecierj Questão 2 Adaptado de UFRJ. Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Veja a seguir as distribuições eletrônicas para o magnésio e o oxigênio: Mg: K = 2 L = 8 M = 2 12 O: K = 2 L = 6 8 Explique como o composto MgO é formado e indique
Atividade extra Questão 1 Cecierj - 2013 Veja a seguir as distribuições eletrônicas para o magnésio e o oxigênio: Mg: K = 2 L = 8 M = 2 12 O: K = 2 L = 6 8 Explique como o composto MgO é formado e indique
1 a Questão: Valor : 1,0 FOLHA DE DADOS. I ) Entalpias de Formação (H o f ) H 2. O (líquida) = - 68,3 kcal / mol. CO 2 (gasoso) = - 94,1 kcal / mol
 PROVA DE QUÍMICA DO VESTIBULAR 96/97 DO INSTITUTO MILITAR DE ENGENHARIA (04/12/96) FOLHA DE DADOS I ) Entalpias de Formação (H o f ) H 2 O (líquida) = - 68,3 kcal / mol CO 2 (gasoso) = - 94,1 kcal / mol
PROVA DE QUÍMICA DO VESTIBULAR 96/97 DO INSTITUTO MILITAR DE ENGENHARIA (04/12/96) FOLHA DE DADOS I ) Entalpias de Formação (H o f ) H 2 O (líquida) = - 68,3 kcal / mol CO 2 (gasoso) = - 94,1 kcal / mol
ATIVIDADES RECUPERAÇÃO PARALELA
 ATIVIDADES RECUPERAÇÃO PARALELA Nome: Nº Ano: 7º Data: 14/11/2012 Bimestre: 4 Professor: Vanildo Disciplina: Química Orientações para estudo: Esta atividade deverá ser entregue no dia da avaliação de recuperação,
ATIVIDADES RECUPERAÇÃO PARALELA Nome: Nº Ano: 7º Data: 14/11/2012 Bimestre: 4 Professor: Vanildo Disciplina: Química Orientações para estudo: Esta atividade deverá ser entregue no dia da avaliação de recuperação,
ESTEQUIOMETRIA - 3C13 - Profª
 ESTEQUIOMETRIA - 3C13 - Profª Estequiometria é a parte da Química que estuda as proporções dos elementos que se combinam ou que reagem. MASSA ATÔMICA (u) É a massa do átomo medida em unidades de massa
ESTEQUIOMETRIA - 3C13 - Profª Estequiometria é a parte da Química que estuda as proporções dos elementos que se combinam ou que reagem. MASSA ATÔMICA (u) É a massa do átomo medida em unidades de massa
1º SIMULADO DISCURSIVO IME QUÍMICA
 QUÍMICA Questão 1 A partir do modelo da Repulsão por Pares Eletrônicos da Camada de Valência (RPECV), identifique as geometrias moleculares das espécies químicas abaixo e, com base nelas, classifique cada
QUÍMICA Questão 1 A partir do modelo da Repulsão por Pares Eletrônicos da Camada de Valência (RPECV), identifique as geometrias moleculares das espécies químicas abaixo e, com base nelas, classifique cada
LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1 Ano
 LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1 Ano Professor: Cassio Pacheco Disciplina: Química 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H2, P4, H2O, O2 b) Cl2, CO2, H2,
LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1 Ano Professor: Cassio Pacheco Disciplina: Química 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H2, P4, H2O, O2 b) Cl2, CO2, H2,
INTRODUÇÃO À QUÍMICA
 INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
