Elétron. Nêutron. Próton COLÉGIO E CURSO
|
|
|
- Luciano Bennert Antas
- 6 Há anos
- Visualizações:
Transcrição
1 FERA COLÉGIO E CURSO (83) Educar: arte de tecer um futuro de boas escolhas Título: Química elementar Data: / /2016 COLÉGIO E CURSO Série: 3ª série do ensino médio Turma: Aluna(o): Nº: 01 - (ITA SP) Neste ano comemora-se o centenário da descoberta do elétron Qual dos pesquisadores abaixo foi o principal responsável pela determinação de sua carga elétrica? a) R A Milikan b) E R Rutherford c) M Faraday d) JJ Thomson e) C Coulomb 02 - (ITA SP) Um átomo de hidrogênio com o elétron inicialmente no estado fundamental é excitado para um estado com número quântico principal (n) igual a 3 Em correlação a este fato qual das opções abaixo é a CORRETA? a) Este estado excitado é o primeiro estado excitado permitido para o átomo de hidrogênio b) A distância média do elétron ao núcleo será menor no estado excitado do que no estado fundamental c) Será necessário fornecer mais energia para ionizar o átomo a partir deste estado excitado do que para ionizá-lo a partir do estado fundamental d) A energia necessária para excitar um elétron do estado com n = 3 para um estado n = 5 é a mesma para excitá-lo do estado com n = 1 para um estado com n = 3 e) O comprimento de onda da radiação emitida quando este elétron retornar para o estado fundamental será igual ao comprimento de onda da radiação absorvida para ele ir do estado fundamental para o estado excitado 03 - (UFES) A configuração eletrônica do átomo de ferro em ordem crescente de energia é 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Na formação do íon Fe 2+, o átomo neutro perde 2 elétrons A configuração eletrônica do íon formado é : a) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 b) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 4 c) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 5 d) 1s 2 2s 2 2p 6 3s 2 3p 4 4s 1 3d 6 e) 1s 2 2s 2 2p 6 3s 2 3p 4 4s 2 3d (UCS RS) No organismo humano, alguns dos elementos químicos existem na forma de íons Esses íons desempenham um papel fundamental em vários processos vitais, participando de reações químicas Os íons Na + e Mg 2+, por exemplo, estão, respectivamente, envolvidos no equilíbrio eletrolítico e no funcionamento dos nervos Em relação aos íons 23 Na + e 24 Mg 2+, é correto afirmar que são a) isótopos e isoeletrônicos b) isoeletrônicos e isótonos c) isótonos e isóbaros d) isóbaros e isótopos e) isoeletrônicos e isóbaros 05 - (UERJ) A figura abaixo foi proposta por um ilustrador para representar um átomo de lítio (Li) no estado fundamental, segundo o modelo de Rutherford-Bohr Elétron Nêutron Próton Constatamos que a figura está incorreta em relação ao número de: a) nêutrons no núcleo b) partículas no núcleo c) elétrons por camada d) partículas na eletrosfera 06 - (UFG GO) O esquema a seguir representa de modo simplificado o experimento de J J Thomson Um feixe de partículas sai do cátodo, passa através de um orifício no ânodo e sofre a influência das placas metálicas A e B De acordo com esse esquema, o feixe se aproxima de A quando a) as placas A e B forem negativas b) a placa A for negativa e a B, positiva c) a placa A for positiva e a B negativa d) as placas A e B forem positivas e) as placas A e B forem neutras 07 - (UFG GO) O movimento de um elétron entre dois núcleos atômicos pode ser representado por uma onda, conforme o gráfico abaixo A função que representa esse gráfico é: _ wwwcolegiogeopatoscombr hedilbertoalves@gmailcom 1
2 a) sen 2 (x) b) cos 2 (x) + sen(x) c) cos(x) + sen 2 (x) d) sen(x) e) cos(x) 08 - (UFPE) A água contendo isótopos 2 H é denominada água pesada, porque a molécula 2 H 2 16 O quando comparada com a molécula 1 H 2 16 O possui: a) maior número de nêutrons b) maior número de prótons c) maior número de elétrons d) menor número de elétrons e) menor número de prótons 09 - (UERJ) Um sistema é formado por partículas que apresentam a composição atômica: 10 prótons, 10 elétrons e 11 nêutrons Ao sistema foram adicionadas novas partículas O sistema resultante será quimicamente puro se as partículas adicionadas apresentarem a seguinte composição atômica: a) 21 prótons, 10 elétrons e 11 nêutrons b) 20 prótons, 20 elétrons e 22 nêutrons c) 10 prótons, 10 elétrons e 12 nêutrons d) 11 prótons, 11 elétrons e 12 nêutrons e) 11 prótons, 11 elétrons e 11 nêutrons 10 - (UFOP MG) Um átomo constituído por prótons, 82 nêutrons e elétrons apresenta número atômico e número de massa, respectivamente, iguais a: a) e 1 b) 82 e 110 c) 54 e d) e 136 e) 54 e (UFOP MG) A tabela abaixo apresenta estruturas de Lewis para alguns elementos (Os pontos representam elétrons de valência) Na Mg F Ṅ C Xe Estão CORRETAMENTE representadas as seguintes estruturas: a) Mg, F, C b) Na, Mg, F c) Na, N, C d) Mg, N, Xe e) F, C, Xe 12 - (UEPB) A representação gráfica abaixo mostra três níveis de energia de um determinado átomo: Nível 3 - n 3 E3 E 2 Nível 2 - n 2 Nível 1 - n 1 wwwcolegiogeopatoscombr wwwquimicasolucionadacombr 2 Energia E 1 I Um elétron precisa receber energia (E) correspondente a E 2 - E 1 para saltar do nível 1 para o nível 2 II O salto quântico referido acima (I) libera energia na III forma de ondas eletromagnéticas O salto quântico n 1 para n 3 é menos energético que o salto n 1 para n 2 Está(ão) correta(s) somente a(s) afirmativa(s) a) III b) II c) I d) I e II e) I e III 13 - (UNIMEP SP) No íon 32 16S 2- encontramos: a) 48 nêutrons b) 32 prótons c) 16 prótons d) número de massa 16 e) 32 elétrons 14 - (UNIMEP SP) Qual dos seguintes conjuntos de números quânticos (citados na ordem n, l, m, S) é impossível para um elétron num átomo? a) 4, 2, 0, + 1/2 b) 3, 3, -2, - 1/2 c) 2, 1, -1, + 1/2 d) 4, 3, 0, -1/2 e) 3, 2, / (ITA SP) Em 1803, John Dalton propôs um modelo de teoria atômica Considere que sobre a base conceitual desse modelo sejam feitas as seguintes afirmações: I O átomo apresentará a configuração de uma esfera rígida II Os átomos caracterizam os elementos químicos e somente os átomos de um mesmo elemento são idênticos em todos os aspectos III As transformações químicas consistem de combinação, separação e/ou rearranjo de átomos IV Compostos químicos são formados de átomos de dois ou mais elementos unidos em uma razão fixa Qual das opções abaixo se referem a todas as afirmações CORRETAS? a) I e IV b) II e III c) II e IV d) II, III e IV e) I, II, III e IV 16 - (FATEC SP) Se 26 Fe e 27 Co são espécies de elementos diferentes que possuem o mesmo número de massa, uma
3 característica que os distingue sempre é o número de a) elétrons na elétrosfera b) elétrons no núcleo c) nêutrons na eletrosfera d) prótons no núcleo e) nêutrons no núcleo 17 - (UNIFICADO RJ) Quando um átomo de bromo ( 35 Br 80 ) recebe um elétron, 80 transforma-se no íon 35 Br -, que possui, na sua estrutura, prótons, elétrons e nêutrons, respectivamente em número de: a) b) c) d) e) (UNIFICADO RJ) As torcidas vêm colorindo cada vez mais os estádios de futebol com fogos de artifício Sabemos que as cores desses fogos são devidas à presença de certos elementos químicos Um dos mais usados para obter a cor vermelha é o estrôncio (Z = ), que, na forma do íon Sr +2, tem a seguinte configuração eletrônica: a) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 b) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 c) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 5p 2 d) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 4d 2 e) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 4 5s (UEM PR) Assinale o que for correto a) A passagem da água sólida para a água líquida é uma transformação química b) Substâncias simples são aquelas formadas por diversos elementos químicos, ou seja, por diferentes tipos de átomos c) Alotropia é o fenômeno em que o mesmo elemento químico constitui substâncias compostas diferentes d) Um mol de O 2 (g) equivale a 6,02x10 23 átomos de oxigênio e) Átomos com diferentes números de prótons mas que possuem o mesmo número de massa são chamados de isóbaros 20 - (PUC MG) Qual das seguintes espécies NÃO é isoeletrônica com o neônio? a) Cl b) Na + c) O 2 d) Mg (UNIRIO RJ) A distribuição espacial dos elétrons que ocupam orbitais s e p, respectivamente, segue a geometria de: a) dois halteres b) dois cubos c) duas esferas d) um halter e um cubo e) uma esfera e um halter 22 - (UESPI) Considere as espécies químicas monoatômicas apresentadas na tabela a seguir: Espéciequímica monoatômica Número deprótons Número denêutrons Número deelétrons wwwcolegiogeopatoscombr wwwquimicasolucionadacombr 3 1 Com relação às espécies químicas monoatômicas apresentadas acima, pode-se afirmar que: a) 1 e 2 não são isótopos b) 2 é eletricamente neutro c) 3 é um ânion d) 5 é um cátion e) 3 e 4 são de um mesmo elemento químico 23 - (UFMG) Observações experimentais podem contribuir para a formulação ou adoção de um modelo teórico, se esse as prevê ou as explica Por outro lado, observações experimentais imprevistas ou inexplicáveis por um modelo teórico podem contribuir para sua rejeição Em todas as alternativas, a associação observaçãomodelo atômico, está correta, EXCETO em: OBSERVAÇÃO EXPERIMENTAL I Conservação da massa em reações químicas II Proporções entre as massas de reagentes e produtos III Espectros atômicos descontínuos IV Trajetória de partículas alfa que colidem com uma lâmina metálica V Emissão de elétrons em tubos de raios catódicos IMPLICAÇÃO EM TERMOS DE MODELO ATÔMICO a) Adoção do modelo de Dalton b) Adoção do modelo de Dalton c) Adoção do modelo de Rutherford d) Adoção do modelo de Rutherford e) Rejeição do modelo de Dalton 24 - (GF RJ) Considere as informações abaixo, a respeito de um átomo genérico X: Z=3x + 4 A=8x N=16 De acordo com o conceito de estrutura atômica, o valor de X é: a) 1 b) 2 c) 3 d) 4 e) (GF RJ) A respeito da estrutura do átomo, considere as seguintes afirmações: I O número quântico principal (n) é um número inteiro que identifica os níveis ou camadas de elétrons II Um orbital está associado ao movimento de rotação de um elétron e é identificado pelo número quântico "spin" III Os subníveis energéticos são identificados pelo número quântico secundário (l), que assume os valores 0, 1, 2 e 3 IV Os elétrons descrevem movimento de rotação chamado "spin", que é identificado pelo número quântico de "spin" (s), com valores de -l até +l São corretas as afirmações: a) somente I e II b) somente I e III c) somente I e IV
4 d) somente II e III e) somente II e IV d) 5 e) (GF RJ) O elemento Cálcio (Z = 20) encontra-se no grupo 2A da tabela periódica e forma o íon Ca 2+ A configuração eletrônica deste íon é: a) 1s 2 2s 2 2p 6 3s 2 3p 6 b) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2 c) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 d) 1s 2 2s 2 2p 6 3s 2 3p 6 4d 2 e) 1s 2 2s 2 2p 6 3s 2 3p 6 4s (UNESP SP) O íon possui: 39 19X + a) 19 prótons b) 19 nêutrons c) 39 elétrons d) número de massa igual a 20 e) número atômico igual a (UEL PR) Os átomos isótopos 2x+6 X 54 e 3x-4Y têm número atômico: a) 26 b) 27 c) 28 d) 54 e) 34 - (UFPI) Assinale a afirmativa correta em relação aos átomos neutros : 8 O 16 e 8 O 17 a) são isóbaros b) 8O 17 tem um elétron a mais que 8 O 16 c) O 17 tem um próton a mais que 8 O 16 d) são isótopos e) um mol de 8 O 17 contém mais átomos que um mol de 8O (UNIFICADO RJ) Assinale a opção que contraria a Regra de Hund: 29 - (UNIFICADO RJ) A configuração eletrônica do íon Ca 2+ (Z = 20) é: a) 1s 2 2s 2 2p 6 3s 2 3p 4 b) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 c) 1s 2 2s 2 2p 6 3s 2 3p 6 d) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2 e) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d (UNIFICADO RJ) Considere os elementos abaixo e assinale a opção correta: 19K 40 ; 8 O 16 ; 18 Ar 40 ; 8 O 17 ; 17 Cl 37 ; 8 O 18 ; 20 Ca 40 a) I e III são isótopos; II, IV e VI são isóbaros b) III e VII são isóbaros; V e VII são isótonos c) II, IV e VI são isótopos; III e VII são isótonos d) II e III são isótonos, IV e VI são isóbaros e) II e IV são isótonos; V e VII são isóbaros 31 - (UEL PR) Dentre os seguintes números atômicos, o que corresponde ao elemento químico com 2 elétrons no subnível 4d é: a) 22 b) 28 c) 30 d) 40 e) (UEL PR) Quantos elétrons de valência existem na configuração do elemento químico de número atômico 52? a) 2 b) 3 c) (UFPI) Qual a afirmativa correta: a) o número máximo de elétrons f no segundo nível de energia é 14 b) um elétrons 2s está num nível de energia mais alto do que um 2p c) o quarto nível de energia (n = 4) poderá ter o nível máximo 18 elétrons d) os orbitais 2px, 2py e 2pz estão no mesmo nível de energia e) a estrutura eletrônica fundamental do átomo do potássio (z = 19) é 1s 2 2s 2 2p 6 2d 8 3s (UDESC SC) Em um átomo com 12 elétrons e 16 nêutrons, seu número de massa atômica e seu número atômico são respectivamente: a) 27 e 12 b) 12 e 28 c) 28 e 11 d) 28 e 12 e) 11 e (UFV MG) Observe a tabela abaixo: Elemento X Y Atômico 13 D Prótons A 15 Elétrons B 15 Nêutrons C 16 Massa 27 E Os valores corretos de A, B, C, D e E são, respectivamente: a) 13, 13, 14, 15, 31 b) 13, 14, 15, 16, 31 c) 14, 14, 13, 16, 30 d) 12, 12, 15, 30, 31 e) 15, 15, 12, 30, 31 - (PUC MG) Íons são formados, a partir de átomos neutros, por: a) perda de nêutrons b) ganho ou perda de prótons c) perda ou ganho de energia d) ganho de nêutrons e) ganho ou perda de elétrons 39 - (PUC MG) Isótopos de hidrogênio formam com o isótopo 16 do wwwcolegiogeopatoscombr wwwquimicasolucionadacombr 4
5 oxigênio moléculas H 2 O e D 2 O Todas as afirmações a seguir são corretas, EXCETO: a) O total de elétrons na molécula H 2 O é 10 b) O total de prótons na molécula D 2 O é 10 c) O total de nêutrons na molécula H 2 O é 10 d) O total de elétrons na molécula D 2 O é 10 e) O total de nêutrons na molécula D 2 O é (ITA SP) Um átomo de hidrogênio com o elétron inicialmente no estado fundamental é excitado para um estado com número quântico principal (n) igual a 3 Em correlação a este fato qual das opções abaixo é a CORRETA? a) Este estado excitado é o primeiro estado excitado permitido para o átomo de hidrogênio b) A distância média do elétron ao núcleo será menor no estado excitado do que no estado fundamental c) Será necessário fornecer mais energia para ionizar o átomo a partir deste estado excitado do que para ionizá-lo a partir do estado fundamental d) A energia necessária para excitar um elétron do estado com n = 3 para um estado n = 5 é a mesma para excitá-lo do estado com n = 1 para um estado com n = 3 e) O comprimento de onda da radiação emitida quando este elétron retornar para o estado fundamental será igual ao comprimento de onda da radiação absorvida para ele ir do estado fundamental para o estado excitado 41 - (ITA SP) São feitas as seguintes afirmações a respeito das contribuições do pesquisador francês A L Lavoisier ( ) para o desenvolvimento da ciência: I Desenvolvimento de um dos primeiros tipos de calorímetros II Participação na comissão responsável pela criação do sistema métrico de medidas III Proposta de que todos os ácidos deveriam conter pelo menos um átomo de oxigênio IV Escolha do nome oxigênio para o componente do ar atmosférico indispensável para a respiração humana V Comprovação experimental da conservação de massa em transformações químicas realizadas em sistemas fechados Qual das opções abaixo contém a(s) afirmação(ões) CORRETA(S)? a) I, II, III, IV e V b) Apenas I, II e IV c) Apenas II e III d) Apenas IV e V e) Apenas V 42 - (PUC RJ) Os átomos 81 Tl 203 e 81 Tl 205 são : a) isóbaros b) isômeros c) isótopos d) isólogos e) idênticos 43 - (PUC RJ) A configuração eletrônica do átomo de carbono 6 C 12 é: a) 1s 2 2s 2px 2py 2pz b) 1s 2 2s 2 2px 1 2py 1 c) 1s 2 2s 2 2px 2 d) 1s 2 2s 2 2px 2 2py 2 2pz 2 3s 2 e) 1s 2 2s 2 3s (UNIUBE MG) Dos íons, abaixo, aquele(s) que possui(em) o seu último elétron representado em 2p 6, de acordo com o diagrama de Pauling, é(são): I 11Na + II 19K + III 20Ca 2+ IV 9 F Assinale a afirmativa correta: a) II, III e IV b) I e IV c) I e III d) II e III 45 - (UNIFOR CE) Considerando os resultados da experiência de Rutherford, que investigou a deflexão de partículas alfa em lâminas metálicas muito finas, pode-se afirmar que: I Eles seriam os mesmos, se tivessem sido utilizadas lâminas metálicas espessas wwwcolegiogeopatoscombr wwwquimicasolucionadacombr 5 II A eletrosfera praticamente não impõe resistência ao movimento das partículas alfa III O fato de apenas uma pequena porção das partículas alfa terem sofrido grandes desvios indica que o núcleo é maciço e constitui a menor parte do átomo É correto o que se afirma SOMENTE em a) I b) II c) III d) I e II e) II e III 46 - (ULBRA RS) Para adquirir configuração eletrônica de gás nobre, o átomo de número atômico 34 deve: a) ganhar 2 elétrons b) ganhar 3 elétrons c) perder 1 elétron d) perder 2 elétrons e) perder 3 elétrons 47 - (UFRGS RS) Comparando-se a posição dos elementos neônio (Ne) e fósforo (P) a partir de suas posições na classificação periódica, pode-se concluir que: a) ambos apresentam praticamente o mesmo potencial de ionização b) o Ne apresenta menor número de elétrons no último nível de energia c) o P apresenta elétrons distribuídos em um maior número de níveis energéticos d) o P apresenta menor número de elétrons celibatários (desemparelhados) e) o Ne apresenta uma maior tendência a formação de ânions 48 - (VUNESP SP) Para o elemento de número atômico 28, a configuração eletrônica é: a) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 b) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 2 4s 2 4p 6 c) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 4p 6 5s 2 d) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 8 e) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d (INTEGRADO RJ) Os implantes dentários estão mais seguros no Brasil e já atendem às normas internacionais de qualidade O grande salto de qualidade aconteceu no processo de confecção dos parafusos e pinos de titânio que compões
6 as próteses Feitas com ligas de titânio, essas prótese são usadas para fixar coroas dentárias, aparelhos ortodônticos e dentaduras nos ossos da mandíbula e do maxilar Considerando que o número atômico do Titânio é 22, sua configuração eletrônica será: a) 1s 2 2s 2 2p 6 3s 2 3p 3 b) 1s 2 2s 2 2p 6 3s 2 3p 5 c) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 d) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 2 e) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p (PUC MT) O bromo, único halogênio que nas condições ambiente se encontra no estado líquido, formado por átomos representados por 35 Br 80, apresenta: a) 25 elétrons na camada de valência b) 2 elétrons na camada de valência c) 7 elétrons na camada de valência d) 35 partículas nucleares e) 45 partículas nucleares GABARITO: 1) Gab: A 2) Gab: E 3) Gab: A 4) Gab: B 5) Gab: C 6) Gab: C 7) Gab: D 8) Gab: A 9) Gab: C 10) Gab: A 11) D 12) Gab: C 13) Gab: C 14) Gab: B 15) Gab: E 16) Gab: D 17) Gab: B 18) Gab: A 19) Gab: E 20) Gab: A 21) Gab: E 22) Gab: E 23) Gab: C 24) Gab: D 25) Gab: E 26) Gab: A 27) Gab: A 28) Gab: E 29) Gab: C 30) Gab: B 31) Gab: D 32) Gab: E 33) Gab: A 34) Gab: D 35) Gab: D 36) Gab: D 37) Gab: A ) Gab: E 39) Gab: C 40) Gab: E 41) Gab: A 42) GAB: C 43) GAB: B 44) Gab: B 45) Gab: E 46) Gab: A 47) Gab: C 48) Gab: D 49) Gab: D 50) Gab: C wwwcolegiogeopatoscombr wwwquimicasolucionadacombr 6
OPÇÃO CONCURSO. e) 11 prótons, 11 elétrons e 11 nêutrons.
 1) Somando-se todas as partículas (prótons, nêutrons e elétrons) de um átomo de 28 Ni 59 com as do átomo de 80 Hg 201, o total de partículas será: a) 281. b) 158. c) 368. d) 108. e) 360. 2) O átomo de
1) Somando-se todas as partículas (prótons, nêutrons e elétrons) de um átomo de 28 Ni 59 com as do átomo de 80 Hg 201, o total de partículas será: a) 281. b) 158. c) 368. d) 108. e) 360. 2) O átomo de
SÉRIE: 1 Ano. ALUNO (a): NOTA: LISTA DE EXERCÍCIOS P1 (2 BIMESTRE)
 GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS P1 (2 BIMESTRE) 1. X é isótopo de 20 41 Ca e isótono de 19
GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS P1 (2 BIMESTRE) 1. X é isótopo de 20 41 Ca e isótono de 19
Exercícios de atomística
 DISCIPLINA PROFESSOR QUÍMICA REVISADA DATA (rubrica) ARMANDO 2017 NOME Nº ANO TURMA ENSINO 1º MÉDIO Exercícios de atomística 1. (ITA) Em 1808, John Dalton propôs um modelo de teoria atômica. Considere
DISCIPLINA PROFESSOR QUÍMICA REVISADA DATA (rubrica) ARMANDO 2017 NOME Nº ANO TURMA ENSINO 1º MÉDIO Exercícios de atomística 1. (ITA) Em 1808, John Dalton propôs um modelo de teoria atômica. Considere
GOIÂNIA, / / Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: LISTA DE EXERCÍCIOS P2 (1 BIMESTRE)
 GOIÂNIA, / / 2016 PROFESSOR: Taynara Oliveira DISCIPLINA: Química Geral SÉRIE: 1 Anos ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
GOIÂNIA, / / 2016 PROFESSOR: Taynara Oliveira DISCIPLINA: Química Geral SÉRIE: 1 Anos ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
Tarefa 23 Professor Gustavo
 Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito)
 SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
SÉRIE: 1 Ano. ALUNO (a): NOTA: LISTA DE EXERCÍCIOS RECUPERAÇÃO SEMESTRAL
 GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS RECUPERAÇÃO SEMESTRAL 01. X é isótopo de 20 41 Ca e isótono
GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS RECUPERAÇÃO SEMESTRAL 01. X é isótopo de 20 41 Ca e isótono
1. O modelo atômico de Rutherford é também conhecido como modelo planetário do átomo.
 2º Trimestre_8AB_2014_REVISÃO_Química_Prof.ª Caroline Oliveira Nome: Turma: 8 Data: / /2014. 1- Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford
2º Trimestre_8AB_2014_REVISÃO_Química_Prof.ª Caroline Oliveira Nome: Turma: 8 Data: / /2014. 1- Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford
Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio. Números Quânticos e Diagrama de Pauling;
 Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio Números Quânticos e Diagrama de Pauling; Número quântico principal (n): indica o nível de energia do elétron no átomo.
Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio Números Quânticos e Diagrama de Pauling; Número quântico principal (n): indica o nível de energia do elétron no átomo.
1º Trimestre Sala de Estudos-Química Data: 13/03/17 Ensino Médio 1º ano classe: A_B_C Profª Danusa Nome: nº
 º Trimestre Sala de Estudos-Química Data: 3/03/7 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Estrutura atômica e Configuração Eletrônica Questão 0 - (PUC- RS) Ao se deixar cair sal
º Trimestre Sala de Estudos-Química Data: 3/03/7 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Estrutura atômica e Configuração Eletrônica Questão 0 - (PUC- RS) Ao se deixar cair sal
QUÍMICA 1 ANO - PROGRESSÃO 2015
 QUÍMICA 1 ANO - PROGRESSÃO 2015 1. Esta questão apresenta três afirmativas, que podem estar corretas ou incorretas. Responda-a, obedecendo ao seguinte código: I) Fe, AI, C, Na são conjunto de elementos
QUÍMICA 1 ANO - PROGRESSÃO 2015 1. Esta questão apresenta três afirmativas, que podem estar corretas ou incorretas. Responda-a, obedecendo ao seguinte código: I) Fe, AI, C, Na são conjunto de elementos
CONCEITOS FUNDAMENTAIS
 CONCEITOS FUNDAMENTAIS EXERCÍCIOS DE APLICAÇÃO 01 (UNIRIO-RJ) O átomo X é isóbaro do 40 Ca e isótopo do 36 Ar. Assinale o número de nêutrons do átomo X. Dados: Número atômicos: Ar = 18; Ca = 20 a) 4 b)
CONCEITOS FUNDAMENTAIS EXERCÍCIOS DE APLICAÇÃO 01 (UNIRIO-RJ) O átomo X é isóbaro do 40 Ca e isótopo do 36 Ar. Assinale o número de nêutrons do átomo X. Dados: Número atômicos: Ar = 18; Ca = 20 a) 4 b)
04) (FGV-SP) As figuras representam alguns experimentos de raios catódicos realizados no início do século passado, no estudo da estrutura atômica.
 01) (FMTM-MG) De acordo com o modelo atômico proposto por Rutherford, os átomos são constituídos por um núcleo de carga elétrica positiva, que concentra quase toda a massa do átomo, onde estão os prótons,
01) (FMTM-MG) De acordo com o modelo atômico proposto por Rutherford, os átomos são constituídos por um núcleo de carga elétrica positiva, que concentra quase toda a massa do átomo, onde estão os prótons,
ATOMÍSTICA PROF. ADRIANO ALVES
 ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON
 LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e)
LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e)
Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular
 Colégio Drummond Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular MATERIAL DE QUÍMICA PROF.: CARLINHOS CURSINHO 2+ efeito estufa é o monóxido de carbono CO2, este é liberado principalmente
Colégio Drummond Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular MATERIAL DE QUÍMICA PROF.: CARLINHOS CURSINHO 2+ efeito estufa é o monóxido de carbono CO2, este é liberado principalmente
Coluna II ( ) Rutherford ( ) Thomson ( ) Hund ( ) Bohr ( ) Heisenberg
 Lista de Química P2 1 Ano Professora: Núbia de Andrade Aluno: 01 - (UFPR) Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford é também conhecido como
Lista de Química P2 1 Ano Professora: Núbia de Andrade Aluno: 01 - (UFPR) Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford é também conhecido como
05 - (UEL PR/1994) Localize na tabela periódica o elemento químico de número atômico 20 e escolha a(s)
 01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
ESTRUTURA ATÔMICA. Modelos Atômicos
 ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
TEORIAS ATÔMICAS. Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807)
 TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
Química. 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30
 Química 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30 02. Para que um átomo de número atômico 55 e número de massa 137 seja eletricamente neutro, ele deverá ter, necessariamente:
Química 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30 02. Para que um átomo de número atômico 55 e número de massa 137 seja eletricamente neutro, ele deverá ter, necessariamente:
Lista de exercícios Aulas 03 e 04. 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em:
 Lista de exercícios Aulas 03 e 04 Prof. Fernanda Dias 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em: a) a formação dos materiais dá-se através de diferentes associações entre
Lista de exercícios Aulas 03 e 04 Prof. Fernanda Dias 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em: a) a formação dos materiais dá-se através de diferentes associações entre
QUÍMICA GERAL I PROF. PRISCILA BONFIM GONÇALVES
 Exercícios 1. Sobre os modelos atômicos, assinale o que for incorreto. 01) O modelo que suscitou a ideia do átomo constituído de duas regiões distintas foi proposto pelo químico francês John Dalton, no
Exercícios 1. Sobre os modelos atômicos, assinale o que for incorreto. 01) O modelo que suscitou a ideia do átomo constituído de duas regiões distintas foi proposto pelo químico francês John Dalton, no
Resoluções. Estrutura atômica
 Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 1 Estrutura atômica 1. A A composição metafísica presente no poema remete aos modelos atômicos propostos
Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 1 Estrutura atômica 1. A A composição metafísica presente no poema remete aos modelos atômicos propostos
Curso Semi-extensivo LISTA EXERCÍCIOS - 05 Disciplina: Química Professor: Eduar Fernando Rosso
 Curso Semi-extensivo LISTA EXERCÍCIOS - 05 Disciplina: Química Professor: Eduar Fernando Rosso ESTRUTURA ATÔMICA 01 (Ufpr 017) As propriedades das substâncias químicas podem ser previstas a partir das
Curso Semi-extensivo LISTA EXERCÍCIOS - 05 Disciplina: Química Professor: Eduar Fernando Rosso ESTRUTURA ATÔMICA 01 (Ufpr 017) As propriedades das substâncias químicas podem ser previstas a partir das
Química A Extensivo V. 2
 Química A Extensivo V. 2 01) Alternativa correta: B Exercícios a) Errada ao mudar de órbita, o elétrons emite ou absorve energia igual a diferença de energia entre as órbitas; b) Certa; c) Errada de acordo
Química A Extensivo V. 2 01) Alternativa correta: B Exercícios a) Errada ao mudar de órbita, o elétrons emite ou absorve energia igual a diferença de energia entre as órbitas; b) Certa; c) Errada de acordo
Ciências da Natureza e Matemática
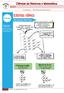 1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 1. Cada átomo possui um certo número de elétrons, que é igual ao valor de seu número atômico (Z). Os elétrons se encontram distribuídos nos
1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 1. Cada átomo possui um certo número de elétrons, que é igual ao valor de seu número atômico (Z). Os elétrons se encontram distribuídos nos
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica
 Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
T.C de Química 1 o ano Prof. Alan Ibiapina
 T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
ESTRUTURA ATÔMICA (PARTE 1)
 ESTRUTURA ATÔMICA (PARTE 1) 1.01. A experiência de Rutherford permitiu: a) a descoberta do próton; b) a descoberta do nêutron; c) a descoberta do elétron; d) caracterizar que, na maior parte do átomo,
ESTRUTURA ATÔMICA (PARTE 1) 1.01. A experiência de Rutherford permitiu: a) a descoberta do próton; b) a descoberta do nêutron; c) a descoberta do elétron; d) caracterizar que, na maior parte do átomo,
Estrutura atômica & Classificação periódica
 Estrutura atômica & Classificação periódica Aula de química (20/08) Gabriel e Leonardo Estrutura atômica Modelos Atômicos Modelos Atômicos - Dalton Os átomos são esferas rígidas, indivisíveis e indestrutíveis
Estrutura atômica & Classificação periódica Aula de química (20/08) Gabriel e Leonardo Estrutura atômica Modelos Atômicos Modelos Atômicos - Dalton Os átomos são esferas rígidas, indivisíveis e indestrutíveis
LISTA DE EXERCÍCIO PARA A PROVA MENSAL
 Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1
 PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
Sendo o cálcio pertencente ao grupo dos alcalinos terrosos e possuindo número atômico Z = 20, a configuração eletrônica do seu cátion bivalente é:
 1- (U.F.Uberlândia-MG\Pales) Dalton, Thomson, Rutherford e Bohr são cientistas que contribuíram, significativamente, para o desenvolvimento da teoria atômica. Em relação a estrutura atômica, assinale com(v)
1- (U.F.Uberlândia-MG\Pales) Dalton, Thomson, Rutherford e Bohr são cientistas que contribuíram, significativamente, para o desenvolvimento da teoria atômica. Em relação a estrutura atômica, assinale com(v)
Exercícios Sobre DistribuiÇão eletrônica
 Exercícios Sobre DistribuiÇão eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z= 55) b) Tl (Z= 81) 02. Faça a distribuição eletrônica nas camadas, para os átomos:
Exercícios Sobre DistribuiÇão eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z= 55) b) Tl (Z= 81) 02. Faça a distribuição eletrônica nas camadas, para os átomos:
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB
 AULA DE RECUPERAÇÃO PROF. NEIF NAGIB CONCEITOS SOBRE O ÁTOMO Número Atômico (Z): quantidades de prótons. Z = p = e Número de Massa (A): a soma das partículas que constitui o átomo. A = Z + N REPRESENTAÇÃO
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB CONCEITOS SOBRE O ÁTOMO Número Atômico (Z): quantidades de prótons. Z = p = e Número de Massa (A): a soma das partículas que constitui o átomo. A = Z + N REPRESENTAÇÃO
1ª Série do ensino médio _ TD 10 _ 10 de maio de 2006
 1ª Série do ensino médio _ TD 10 _ 10 de maio de 2006 16. Verifique os elementos do segundo período da Classificação Periódica. À medida que cresce o número atômico desses elementos: (a) sua eletronegatividade
1ª Série do ensino médio _ TD 10 _ 10 de maio de 2006 16. Verifique os elementos do segundo período da Classificação Periódica. À medida que cresce o número atômico desses elementos: (a) sua eletronegatividade
estrutura atômica e ligações
 Aula 02 estrutura atômica e ligações ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone introdução conceitos elementares a estrutura dos átomos a estrutura
Aula 02 estrutura atômica e ligações ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone introdução conceitos elementares a estrutura dos átomos a estrutura
QUÍMICA GERAL Cap. 01. Prof. Kristian Sales Vieira
 QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
QUÍMICA GERAL PROF. PAULO VALIM
 QUÍMICA GERAL PROF. PAULO VALIM 4 TABELA PERIÓDICA Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
QUÍMICA GERAL PROF. PAULO VALIM 4 TABELA PERIÓDICA Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
2- (UEL-PR) Assinale a opção que apresenta as massas moleculares dos seguintes compostos: C 6 H 12 O 6 ; Ca 3 (PO 4 ) 2 e Ca(OH) 2, respectivamente:
 QUÍMICA 1- A magnetita, um minério do qual se extrai ferro possui fórmula molecular Fe 3 O x e sua massa molecular é 232u. Determine o valor de x e escreva a fórmula molecular correta da magnetita. 2-
QUÍMICA 1- A magnetita, um minério do qual se extrai ferro possui fórmula molecular Fe 3 O x e sua massa molecular é 232u. Determine o valor de x e escreva a fórmula molecular correta da magnetita. 2-
1) Delineie os elementos-chave da teoria atômica de Dalton. Quais deles não são consistentes com a visão moderna do átomo?
 Disciplina: Química Geral I QM81B. 1ª Lista de Exercícios: Modelos Atômicos, Estrutura Atômica, Tabela Periódica e Propriedades Periódicas. Prof. Dr. Cristiano Torres Miranda. Nome: Modelos atômicos 1)
Disciplina: Química Geral I QM81B. 1ª Lista de Exercícios: Modelos Atômicos, Estrutura Atômica, Tabela Periódica e Propriedades Periódicas. Prof. Dr. Cristiano Torres Miranda. Nome: Modelos atômicos 1)
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
Átomo. Modelos atômicos e propriedades
 Átomo Modelos atômicos e propriedades O ÁTOMO CONCEITO: Aprox. 500 AC Demócrito e outros filósofos gregos desenvolveram o conceito de átomo A matéria poderia ser dividida progressivamente até chegar à
Átomo Modelos atômicos e propriedades O ÁTOMO CONCEITO: Aprox. 500 AC Demócrito e outros filósofos gregos desenvolveram o conceito de átomo A matéria poderia ser dividida progressivamente até chegar à
ESTRUTURA ATÔMICA. As partículas do átomo
 QUÍMICA M.2 ESTRUTURA ATÔMICA As partículas do átomo Multimídia 1803 - Dalton (Inglês) A partir de experimentos com gases. Dalton propõe uma hipótese atômica. Segundo ele, os átomos são: Indivisíveis Maciços
QUÍMICA M.2 ESTRUTURA ATÔMICA As partículas do átomo Multimídia 1803 - Dalton (Inglês) A partir de experimentos com gases. Dalton propõe uma hipótese atômica. Segundo ele, os átomos são: Indivisíveis Maciços
Qímica Estrutura At mica
 Q ímica Estrutura At mica MODELOS ATÔMICOS Modelo dos Filósofos Gregos: Leucipo (500 a.c.) e Demócrito (460 a.c.) Indestrutível, indivisível e maciço. Modelo baseado apenas na intuição e na lógica. Aristóteles
Q ímica Estrutura At mica MODELOS ATÔMICOS Modelo dos Filósofos Gregos: Leucipo (500 a.c.) e Demócrito (460 a.c.) Indestrutível, indivisível e maciço. Modelo baseado apenas na intuição e na lógica. Aristóteles
Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida
 Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida Índice Substâncias e Misturas...1 Evolução do Modelo Atômico...3 Tabela Periódica...4 Exercícios...5 Gabarito...7
Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida Índice Substâncias e Misturas...1 Evolução do Modelo Atômico...3 Tabela Periódica...4 Exercícios...5 Gabarito...7
Química Geral -Aula 2 Átomo e estrutura atômica. *Mas afinal, de que são feitas as coisas?
 Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
QUÍMICA A Ciênca Central 9ª Edição
 QUÍMICA A Ciênca Central 9ª Edição Capítulo 2 átomos, moléculas e íons David P. White Teoria atômica da matéria John Dalton (1803 1807): Cada elemento é composto de átomos. Todos os átomos de um elemento
QUÍMICA A Ciênca Central 9ª Edição Capítulo 2 átomos, moléculas e íons David P. White Teoria atômica da matéria John Dalton (1803 1807): Cada elemento é composto de átomos. Todos os átomos de um elemento
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
Avaliação da unidade II Pontuação: 7,5 pontos
 Avaliação da unidade II Pontuação: 7,5 pontos 2 QUESTÃO 01 (Ufg) Leia o poema apresentado a seguir. 3 Pudim de passas Campo de futebol Bolinhas se chocando Os planetas do sistema solar Átomos Às vezes
Avaliação da unidade II Pontuação: 7,5 pontos 2 QUESTÃO 01 (Ufg) Leia o poema apresentado a seguir. 3 Pudim de passas Campo de futebol Bolinhas se chocando Os planetas do sistema solar Átomos Às vezes
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
QUÍMICA PROFº JAISON MATTEI
 QUÍMICA PROFº JAISON MATTEI 1. O modelo atômico de Dalton, concebendo o átomo como uma bolinha maciça e indivisível, fez a Química progredir muito no século XIX. Mas o conhecimento sobre estrutura atômica
QUÍMICA PROFº JAISON MATTEI 1. O modelo atômico de Dalton, concebendo o átomo como uma bolinha maciça e indivisível, fez a Química progredir muito no século XIX. Mas o conhecimento sobre estrutura atômica
DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente
 FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
LOGO. Modelos Atômicos. Profa. Núria Galacini
 LOGO Modelos Atômicos Profa. Núria Galacini Demócrito: no século IV a.c. afirmava que a matéria era composta de partículas indivisíveis, o átomo. John Dalton: em 1808 formulou uma definição acerca dos
LOGO Modelos Atômicos Profa. Núria Galacini Demócrito: no século IV a.c. afirmava que a matéria era composta de partículas indivisíveis, o átomo. John Dalton: em 1808 formulou uma definição acerca dos
LISTA D QUÍMICA- TONI - ATITUDE
 LISTA D QUÍMICA- TONI - ATITUDE www.sosprofessor.xpg.com.br 1 (FESP) Considere os elementos A, B, C e D. As distribuições eletrônicas dos elementos são respectivamente: 1s² 3s¹, 1s². 3p 4, 1s². 30p 5 e
LISTA D QUÍMICA- TONI - ATITUDE www.sosprofessor.xpg.com.br 1 (FESP) Considere os elementos A, B, C e D. As distribuições eletrônicas dos elementos são respectivamente: 1s² 3s¹, 1s². 3p 4, 1s². 30p 5 e
Química A Extensivo V. 2
 Química A Extensivo V. 2 Exercícios 01) B 02) A a) Errada. Ao mudar de órbita, os elétrons emite ou absorve energia igual à diferença de energia entre as órbitas. b) Certa. c) Errada. De acordo com a teoria
Química A Extensivo V. 2 Exercícios 01) B 02) A a) Errada. Ao mudar de órbita, os elétrons emite ou absorve energia igual à diferença de energia entre as órbitas. b) Certa. c) Errada. De acordo com a teoria
2) Um átomo T apresenta menos 2 prótons que um átomo Q. Com base nessa informação, assinale a opção falsa.
 1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
SOLUÇÃO ALUNO PRATIQUE EM CASA
 SOLUÇÃO AR1. [E] [F] X é um metal e possui 1 elétron na camada de valência, pois a primeira energia de ionização (50kJ mol) é baixa comparada com a segunda (7.97kJ mol) e com a terceira (11.810 kj mol).
SOLUÇÃO AR1. [E] [F] X é um metal e possui 1 elétron na camada de valência, pois a primeira energia de ionização (50kJ mol) é baixa comparada com a segunda (7.97kJ mol) e com a terceira (11.810 kj mol).
NOVOS AVANÇOS NA TEORIA ATÔMICA
 Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da aula: Modelo Atômico de Bohr e Distribuição Eletrônica O desenvolvimento da teoria atômica NOVOS AVANÇOS NA TEORIA ATÔMICA - Ao longo
Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da aula: Modelo Atômico de Bohr e Distribuição Eletrônica O desenvolvimento da teoria atômica NOVOS AVANÇOS NA TEORIA ATÔMICA - Ao longo
ATOMÍSTICA. Teoria de Thomson (1898) Todo átomo é formado por uma matéria positiva, na qual se encontrariam os elétrons distribuídos ao acaso.
 1. MODLOS ATÔMICOS Teoria de Dalton (1803): Toda matéria é constituída por átomos; Átomos de um mesmo elemento químico possuem propriedades químicas e físicas iguais; Todo átomo corresponde a uma esfera
1. MODLOS ATÔMICOS Teoria de Dalton (1803): Toda matéria é constituída por átomos; Átomos de um mesmo elemento químico possuem propriedades químicas e físicas iguais; Todo átomo corresponde a uma esfera
- Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil.
 - Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil www.profkemil.ning.com EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade sobre do que era constituída a matéria parecia
- Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil www.profkemil.ning.com EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade sobre do que era constituída a matéria parecia
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Exercícios de Química
 Exercícios de Química Atomística e Tabela periódica 1)Os metais alcalino-terrosos, como o estrôncio, têm a tendência de perder elétrons para a formação de sais com os elementos do grupo 17. Considerando
Exercícios de Química Atomística e Tabela periódica 1)Os metais alcalino-terrosos, como o estrôncio, têm a tendência de perder elétrons para a formação de sais com os elementos do grupo 17. Considerando
O que é um modelo atômico?
 O que é um modelo atômico? É uma tentativa de ilustrar o átomo. Sendo o átomo a menor estrutura da matéria, se entendermos o átomo, entenderemos melhor o mundo. Importância - explicar os fenômenos, entender
O que é um modelo atômico? É uma tentativa de ilustrar o átomo. Sendo o átomo a menor estrutura da matéria, se entendermos o átomo, entenderemos melhor o mundo. Importância - explicar os fenômenos, entender
TESTES. estrutura atômica. química a apostila 01
 TESTES 01.(UNIFOR-CE) Os átomos: I. diferem de elemento para elemento; II. são as unidades envolvidas nas transformações químicas; III. são indivisíveis;. IV. consistem de unidades com um núcleo e uma
TESTES 01.(UNIFOR-CE) Os átomos: I. diferem de elemento para elemento; II. são as unidades envolvidas nas transformações químicas; III. são indivisíveis;. IV. consistem de unidades com um núcleo e uma
ESTRUTURA ATÔMICA. Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14
 ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
Química A Semiextensivo V. 1
 Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
Exercícios sobre distribuição eletrônica
 Exercícios sobre distribuição eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z = 55) b) T (Z = 81) 0. Faça a distribuição eletrônica nas camadas, para os átomos:
Exercícios sobre distribuição eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z = 55) b) T (Z = 81) 0. Faça a distribuição eletrônica nas camadas, para os átomos:
Modelos atômicos. Curso de Química. Prof. Rui Medeiros. quimicadorui.com.br
 Modelos atômicos Curso de Química Prof. Rui Medeiros quimicadorui.com.br Módulo Extra - 2017 2 CURSO DE QUÍMICA PROFESSOR RUI MEDEIROS MÓDULO EXTRA - 2017 Modelos atômicos ü A representação esquemática
Modelos atômicos Curso de Química Prof. Rui Medeiros quimicadorui.com.br Módulo Extra - 2017 2 CURSO DE QUÍMICA PROFESSOR RUI MEDEIROS MÓDULO EXTRA - 2017 Modelos atômicos ü A representação esquemática
Lista de exercícios Parte 2 Ligações Químicas
 Lista de exercícios Parte 2 Ligações Químicas Disciplina: Química Aplicada 01) (ACAFE) O grupo de átomos que é encontrado de forma estáveis na natureza e não precisam ganhar ou perder elétrons são os:
Lista de exercícios Parte 2 Ligações Químicas Disciplina: Química Aplicada 01) (ACAFE) O grupo de átomos que é encontrado de forma estáveis na natureza e não precisam ganhar ou perder elétrons são os:
1. ESTRUTURA DO ÁTOMO
 Química Profª SIMONE MORGADO Aula 2 Estrutura do átomo, nº atômico, nº de massa e isoátomos. 1. ESTRUTURA DO ÁTOMO Como nós já vimos a Química é essa ciência que busca compreender os mistérios da matéria,
Química Profª SIMONE MORGADO Aula 2 Estrutura do átomo, nº atômico, nº de massa e isoátomos. 1. ESTRUTURA DO ÁTOMO Como nós já vimos a Química é essa ciência que busca compreender os mistérios da matéria,
Colégio Notre Dame de Campinas Congregação de Santa Cruz PLANTÕES DE FÉRIAS QUÍMICA. Nome: Nº: Série: 1º ANO Profª BIANCA RIBEIRO Data: JULHO 2016
 PLANTÕES DE FÉRIAS QUÍMICA Nome: Nº: Série: 1º ANO Profª BIANCA RIBEIRO Data: JULHO 2016 Roteiro de Estudos Primeiramente, revise em seu caderno alguns conceitos importantes da estrutura do átomo, como:
PLANTÕES DE FÉRIAS QUÍMICA Nome: Nº: Série: 1º ANO Profª BIANCA RIBEIRO Data: JULHO 2016 Roteiro de Estudos Primeiramente, revise em seu caderno alguns conceitos importantes da estrutura do átomo, como:
- ATOMÍSTICA Folha 03 João Roberto Mazzei
 01- (UFRJ 2005) Um professor decidiu decorar seu laboratório com um "relógio de Química" no qual, no lugar das horas, estivessem alguns elementos, dispostos de acordo com seus respectivos números atômicos,
01- (UFRJ 2005) Um professor decidiu decorar seu laboratório com um "relógio de Química" no qual, no lugar das horas, estivessem alguns elementos, dispostos de acordo com seus respectivos números atômicos,
OLIMPÍADA PIAUIENSE DE QUÍMICA Modalidade EF
 OLIMPÍADA PIAUIENSE DE QUÍMICA - 2013 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
OLIMPÍADA PIAUIENSE DE QUÍMICA - 2013 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
5) (PUC MG/2006) - O modelo atômico de Rutherford NÃO inclui especificamente: a) nêutrons. b) núcleo. c) próton. d) elétron. Ver resposta!
 Exercícios de Química Setor A Professora- Juliana 1) (Puc - RS) - O átomo, na visão de Thomson, é constituído de a) níveis e subníveis de energia. b) cargas positivas e negativas. c) núcleo e eletrosfera.
Exercícios de Química Setor A Professora- Juliana 1) (Puc - RS) - O átomo, na visão de Thomson, é constituído de a) níveis e subníveis de energia. b) cargas positivas e negativas. c) núcleo e eletrosfera.
Colégio FAAT Ensino Fundamental e Médio
 Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 2º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Constituição da matéria Elementos químicos e a representação atômica
Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 2º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Constituição da matéria Elementos químicos e a representação atômica
Atomística Tabela Periódica Teresópolis, 10 de março de 2018
 Projeto Sabadão Química Prof. Marcos Paulo Atomística Tabela Periódica Teresópolis, 10 de março de 2018 Modelos Atômicos 4ª questão) Associe as afirmações a seus respectivos responsáveis: I- O átomo não
Projeto Sabadão Química Prof. Marcos Paulo Atomística Tabela Periódica Teresópolis, 10 de março de 2018 Modelos Atômicos 4ª questão) Associe as afirmações a seus respectivos responsáveis: I- O átomo não
Lista de exercícios 01) 02) 03) 04)
 Lista de exercícios 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e) Eletroafinidade. 02) Na tabela
Lista de exercícios 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e) Eletroafinidade. 02) Na tabela
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA
 Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
ESTRUTURA ATÔMICA. 4. (UEM-PR) Assinale o que for correto. 5. (UFPE) Entre as seguintes espécies nucleares
 ESTRUTURA ATÔMICA 1. (UEM-PR) Assinale o que for correto. 01. A configuração eletrônica s p 6 s p 6 4s pode representar um átomo no estado fundamental cujo número atômico é 0. 0. O átomo de manganês, 5
ESTRUTURA ATÔMICA 1. (UEM-PR) Assinale o que for correto. 01. A configuração eletrônica s p 6 s p 6 4s pode representar um átomo no estado fundamental cujo número atômico é 0. 0. O átomo de manganês, 5
Aulas 1 e 2. Atomística
 Aulas 1 e 2 Atomística Modelos Atômicos Dalton - 1808 Primeiro cientista a desenvolver uma teoria atômica, segundo a qual a matéria se compõe de partículas indestrutíveis chamadas átomos. Modelos Atômicos
Aulas 1 e 2 Atomística Modelos Atômicos Dalton - 1808 Primeiro cientista a desenvolver uma teoria atômica, segundo a qual a matéria se compõe de partículas indestrutíveis chamadas átomos. Modelos Atômicos
APOSTILA DE QUÍMICA 2º BIMESTRE
 Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
Estrutura Atômica II
 Estrutura Atômica II Modelo nuclear do átomo: Constituído de partículas subatômicas: Prótons, Nêutrons e elétrons Os prótons e nêutrons formam o núcleo minúsculo e denso que compreende quase toda a massa
Estrutura Atômica II Modelo nuclear do átomo: Constituído de partículas subatômicas: Prótons, Nêutrons e elétrons Os prótons e nêutrons formam o núcleo minúsculo e denso que compreende quase toda a massa
RESUMO SOBRE MODELOS ATÔMICOS.
 SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: 9 anos TURMA(S):
SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR NADER ALVES DOS SANTOS SÉRIE/ANO: 9 anos TURMA(S):
A (g) + energia A + (g) + e -
 Atividade de química Escola: Aluno(a): Série/turma: Nº Nota: Professor: Abedias Disciplina: Química Data: 1(UCDB-MT) Os elementos x A, x+1 B e x+2 C pertencem a um mesmo período da tabela periódica. Se
Atividade de química Escola: Aluno(a): Série/turma: Nº Nota: Professor: Abedias Disciplina: Química Data: 1(UCDB-MT) Os elementos x A, x+1 B e x+2 C pertencem a um mesmo período da tabela periódica. Se
DISTRIBUIÇÃO ELETRÔNICA PARA ÍONS
 DISTRIBUIÇÃO ELETRÔNICA PARA ÍONS EXERCÍCIOS DE APLICAÇÃO 01 (UEL-PR) Considere as configurações eletrônicas nos níveis 3 e 4 dos átomos: I. 3s 1 II. 3s 2 3p 4 III. 3s 2 3p 6 4s 2 IV. 3s 2 3p 6 3d 5 4s
DISTRIBUIÇÃO ELETRÔNICA PARA ÍONS EXERCÍCIOS DE APLICAÇÃO 01 (UEL-PR) Considere as configurações eletrônicas nos níveis 3 e 4 dos átomos: I. 3s 1 II. 3s 2 3p 4 III. 3s 2 3p 6 4s 2 IV. 3s 2 3p 6 3d 5 4s
PROPRIEDADES DA MATÉRIA
 Química Revisão Aula 2 1 os anos Décio ago/09 Nome: N o : Turma: PROPRIEDADES DA MATÉRIA Objetivo O objetivo dessa ficha é revisar alguns dos tópicos trabalhados no 1º semestre. As dúvidas devem ser encaminhadas
Química Revisão Aula 2 1 os anos Décio ago/09 Nome: N o : Turma: PROPRIEDADES DA MATÉRIA Objetivo O objetivo dessa ficha é revisar alguns dos tópicos trabalhados no 1º semestre. As dúvidas devem ser encaminhadas
Estrutura da matéria. Estrutura atômica
 Estrutura da matéria 1. Considere a tabela de pontos de fusão e pontos de ebulição da substância a seguir. Substância P.F P.E Cloro - 101,0-34.6 Flúor - 219,6-188,1 Bromo - 7,2 58,8 Mercúrio - 38,8 356,6
Estrutura da matéria 1. Considere a tabela de pontos de fusão e pontos de ebulição da substância a seguir. Substância P.F P.E Cloro - 101,0-34.6 Flúor - 219,6-188,1 Bromo - 7,2 58,8 Mercúrio - 38,8 356,6
Qui. Semana. Allan Rodrigues Xandão Victor Pontes
 Semana 3 Allan Rodrigues Xandão Victor Pontes Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Semana 3 Allan Rodrigues Xandão Victor Pontes Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Estrutura Atômica. Descrever a estrutura do átomo e definir seus termos fundamentais;
 Estrutura Atômica Objetivos Descrever a estrutura do átomo e definir seus termos fundamentais; Estudar a evolução histórica do modelo atômico para conhecer os fundamentos da Tabela Periódica Átomos e Elementos
Estrutura Atômica Objetivos Descrever a estrutura do átomo e definir seus termos fundamentais; Estudar a evolução histórica do modelo atômico para conhecer os fundamentos da Tabela Periódica Átomos e Elementos
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
J.J. Thomson N. Bohr E. Schrödinger. J. Dalton E. Rutherford. Demócrito e Leucipo. A. Sommerfeld. Evolução histórica
 J.J. Thomson N. Bohr E. Schrödinger Demócrito e Leucipo J. Dalton E. Rutherford Evolução histórica A. Sommerfeld Demócrito e Leucipo (modelo filosofal) Do que a matéria é constituída? A matéria é descontínua.
J.J. Thomson N. Bohr E. Schrödinger Demócrito e Leucipo J. Dalton E. Rutherford Evolução histórica A. Sommerfeld Demócrito e Leucipo (modelo filosofal) Do que a matéria é constituída? A matéria é descontínua.
PROVA DE QUÍMICA 3 o TRIMESTRE DE 2015
 PROVA DE QUÍMICA 3 o TRIMESTRE DE 2015 PROF. MARCOS NOME Nº 9º ANO A prova deve ser feita com caneta azul ou preta. É terminantemente proibido o uso de corretor. Respostas com corretor serão anuladas.
PROVA DE QUÍMICA 3 o TRIMESTRE DE 2015 PROF. MARCOS NOME Nº 9º ANO A prova deve ser feita com caneta azul ou preta. É terminantemente proibido o uso de corretor. Respostas com corretor serão anuladas.
Qui. Semana. Allan Rodrigues Xandão (Renan Micha)
 Semana 4 Allan Rodrigues Xandão (Renan Micha) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Semana 4 Allan Rodrigues Xandão (Renan Micha) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Estrutura Atômica. Atomística.
 Estrutura Atômica Atomística. Democrito e Leucipo (450 a. C) Átomo Dalton (séc. XIX) Bola de Bilhar Thomson (séc. XIX) Pudim de passas Rutherford (séc. XX) sistema solar Átomos núcleo prótons (+1) eletrosfera
Estrutura Atômica Atomística. Democrito e Leucipo (450 a. C) Átomo Dalton (séc. XIX) Bola de Bilhar Thomson (séc. XIX) Pudim de passas Rutherford (séc. XX) sistema solar Átomos núcleo prótons (+1) eletrosfera
QUÍMICA ÁTOMOS. Professor: Rafael Odorico
 QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO CAMPUS VALENÇA SÉRIE: 1º ANO DISCIPLINA: QUÍMICA PROFESSOR: JOSÉ TIAGO PEREIRA BARBOSA
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO CAMPUS VALENÇA SÉRIE: 1º ANO DISCIPLINA: QUÍMICA PROFESSOR: JOSÉ TIAGO PEREIRA BARBOSA Lista de Exercícios Ligações Químicas Teoria do Octeto
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO CAMPUS VALENÇA SÉRIE: 1º ANO DISCIPLINA: QUÍMICA PROFESSOR: JOSÉ TIAGO PEREIRA BARBOSA Lista de Exercícios Ligações Químicas Teoria do Octeto
ATOMÍSTICA MODELOS ATÔMICOS. MODELO ATÔMICO DE DALTON: o átomo é constituído de uma pequena esfera maciça indivisível e indestrutível.
 ATOMÍSTICA MODELOS ATÔMICOS MODELO ATÔMICO DE DALTON: o átomo é constituído de uma pequena esfera maciça indivisível e indestrutível. O Átomo é constituído de uma região central chamada de núcleo onde
ATOMÍSTICA MODELOS ATÔMICOS MODELO ATÔMICO DE DALTON: o átomo é constituído de uma pequena esfera maciça indivisível e indestrutível. O Átomo é constituído de uma região central chamada de núcleo onde
