NOVOS AVANÇOS NA TEORIA ATÔMICA
|
|
|
- Bianca Mirandela Cesário
- 6 Há anos
- Visualizações:
Transcrição
1 Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da aula: Modelo Atômico de Bohr e Distribuição Eletrônica O desenvolvimento da teoria atômica NOVOS AVANÇOS NA TEORIA ATÔMICA - Ao longo da história da química, diversos cientistas contribuíram para o melhor entendimento sobre a constituição da matéria e diferentes modelos sobre a estrutura do átomo surgiram. Os três modelos de maior relevância foram os modelos de Dalton, Thomson e Rutherford. - Modelo de Dalton: átomo é uma esfera maciça, indivisível e indestrutível. - Modelo de Thomson: átomo é uma massa de carga positiva contendo elétrons (partículas de carga negativa) espalhados. Como um todo, o átomo é eletricamente neutro. - Modelo de Rutherford: átomo é composto por núcleo, onde se encontram os prótons (partículas de carga positiva) e nêutrons (partículas de carga neutra), e eletrosfera, onde estão localizados os elétrons. O Modelo Atômico de Bohr - Depois de Rutherford ter proposto seu modelo, os cientistas direcionaram seus estudos para a distribuição dos elétrons na elestrofera. Em 1913, Niels Bohr ( ) propôs um novo modelo atômico, relacionando a distribuição dos elétrons na eletrosfera com sua quantidade de energia. - Esse modelo baseia-se nos seguintes postulados: 1. Os elétrons descrevem órbitas circulares ao redor do núcleo. 2. Cada uma dessas órbitas tem energia constante (órbita estacionária). Os elétrons que estão situados em órbitas mais afastadas do núcleo apresentarão maior quantidade de energia. 3. Quando um elétron absorve certa quantidade de energia, salta para uma órbita mais energética. Quando ele retorna à sua órbita original, libera a mesma quantidade de energia, na forma de onda eletromagnética (luz). - Estudos posteriores mostraram que as órbitas eletrônicas de todos os átomos conhecidos se agrupam em sete camadas eletrônicas, denominadas K, L, M, N, O, P, Q. Em cada camada, os elétrons possuem uma quantidade fixa de energia; por esse motivo, as camadas são também denominadas níveis de energia. Além disso, cada camada comporta um número máximo de elétrons, conforme é mostrado no esquema a seguir:
2 - O trabalho de Bohr despertou o interesse de vários cientistas. Um deles, Sommerfield, percebeu, em 1916, que os níveis de energia estariam divididos em regiões ainda menores, por ele denominadas subníveis de energia. - O número de cada nível indica a quantidade de subníveis nele existentes. Por exemplo, o nível 1 apresenta um subnível, o nível 2 apresenta dois subníveis, e assim por diante. - Esses subníveis são representados pelas letras s, p, d, f, g, h, - Estudos específicos para determinar a energia dos subníveis mostraram que: - existe uma ordem crescente de energia nos subníveis; s < p < d < f - os elétrons de um mesmo subnível contêm a mesma quantidade de energia; - os elétrons se distribuem pela eletrosfera ocupando o subnível de menor energia disponível. - O número de camadas, de níveis e de subníveis ocupados pelos elétrons dos átomos de um elemento depende do número de elétrons desses átomos. Camada Nível Subnível Número de elétrons K 1 s s 2 = 2 L 2 s p s 2 p 6 = 8 M 3 s p d s 2 p 6 d 10 = 18 N 4 s p d f s 2 p 6 d 10 f 14 = 32 O 5 s p d f s 2 p 6 d 10 f 14 = 32 P 6 s p d s 2 p 6 d 10 = 18 Q 7 s s 2 = 2 - A criação de uma representação gráfica para os subníveis facilitou a visualização da sua ordem crescente de energia. Essa representação é conhecida como diagrama de Linus Pauling. - Consideremos, como exemplo, a distribuição dos 26 elétrons de um átomo de ferro (Z = 26). Aplicando o diagrama de Pauling, temos:
3 - Para indicar, de modo abreviado, essa distribuição eletrônica, escrevemos: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Exemplos de distribuição eletrônica - Como exemplos, podemos dar a configuração eletrônica para os átomos dos elementos químicos em ordem crescente de número atômico, conforme são representados na tabela periódica. - Começando pelo hidrogênio (H), que possui Z = 1. Como o átomo é neutro, o número atômico (que é o número de prótons totais que compõem o núcleo de um átomo) é igual ao número de elétrons. Logo, um elétron deverá ser distribuído: 1H 1s 1 - Seguindo a ordem crescente de número atômico, tem-se: Elemento Distribuição eletrônica 2He 1s 2 3Li 1s 2 2s 1 4Be 1s 2 2s 2 5B 1s 2 2s 2 2p 1 6C 1s 2 2s 2 2p 2 7N 1s 2 2s 2 2p 3 8O 1s 2 2s 2 2p 4 9F 1s 2 2s 2 2p 5 10Ne 1s 2 2s 2 2p 6 12Mg 1s 2 2s 2 2p 6 3s 2 13Al 1s 2 2s 2 2p 6 3s 2 3p 1 18Ar 1s 2 2s 2 2p 6 3s 2 3p 6 19K 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 20Ca 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 21Sc 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1 27Co 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 7
4 - Duas importantes informações que podem ser obtidas a partir da distribuição eletrônica dos elétrons de um determinado átomo são qual é a camada de valência e o subnível mais energético, que nos ajudam a entender, por exemplo, a localização exata de um elemento químico na tabela periódica, bem como algumas de suas propriedades. Camada ou nível de valência: é a camada mais afastada do núcleo (a mais externa) Subnível mais energético: último subnível a ser preenchido na distribuição eletrônica Exemplos Para o 12 Mg, cuja configuração eletrônica é 1s 2 2s 2 2p 6 3s 2, os doze elétrons foram distribuídos até a terceira camada ou nível energético, logo, diz-se que a camada de valência é a camada M. O último subnível a receber elétrons foi o 3s, logo, esse é classificado como o subnível mais energético. Para o 27 Co, com configuração eletrônica 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 7, a distribuição eletrônica foi até o quarto nível energético (camada N), logo, essa é camada de valência. O subnível mais energético é o 3d, pois esse foi o último subnível a ser preenchido por elétrons na distribuição eletrônica. Subníveis em ordem energética e em ordem geométrica - No exemplo da distribuição do átomo de ferro, perceba que quando escrevemos a sequência de subníveis segundo as diagonais do diagrama, escrevemos exatamente na ordem crescente de energia: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6. Essa é a chamada ordem energética. - A outra forma de representar a distribuição eletrônica por subníveis de energia é a ordem geométrica. Nela, após fazer a distribuição conforme a ordem energética, agrupamos os subníveis de cada nível. No caso átomo neutro de ferro, a ordem geométrica fica assim: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2.
5 Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da lista de exercícios: Modelo Atômico de Bohr e Distribuição Eletrônica 1) Faça a distribuição eletrônica para os elétrons dos seguintes átomos: a) cloro: 17 Cl b) alumínio: 13 Al c) molibdênio: 42 Mo d) rubídio: 37 Rb e) índio: 49 In f) urânio: 92 U g) silício: 14 Si h) bromo: 35 Br 2) A última camada de um átomo possui configuração eletrônica 3s 2 3p 6. Determine o número atômico do elemento a que pertence esse átomo. 3) (VUNESP) Dê a configuração eletrônica para o elemento químico cujo número atômico é 24. Indique qual é a camada de valência e o subnível mais energético. 4) (FEI-SP) Um átomo que possui configuração eletrônica 1s 2 2s 2 2p 6 3s 2 3p 5 apresenta na camada mais externa: a) 5 elétrons b) 7 elétrons c) 3 elétrons d) 1 elétron e) 11 elétrons 5) Que palavra você deve colocar no lugar de * para que a afirmação seja correta? Um átomo, ao perder elétrons, converte-se num *; ao receber elétrons, torna-se um *. 6) Para os íons abaixo, determine o número de prótons, de elétrons e classifique-os em cátions e ânions: a) 35 Br - b) 16 S 2- c) 38 Sr 2+ d) 19 K + e) 24 Cr 3+ f) 8 O 2-7) (VUNESP) Um átomo tem número de massa 31 e 16 nêutrons. Qual é o número de elétrons da sua camada de valência? a) 2 b) 4 c) 5 d) 3 e) 8 8) (FEI-SP) Um cátion metálico trivalente possui 76 elétrons e 118 nêutrons. O átomo do elemento químico, do qual se originou, tem número atômico e número de massa, respectivamente: a) 76 e 194. b) 76 e 197. c) 79 e 200. d) 79 e 194. e) 79 e ) O quadro abaixo representa algumas características de modelos atômicos. Com base nos dados apresentados, relacione as características aos respectivos cientistas: Tipo A B C Característica A matéria é formada por átomos indivisíveis. Núcleos positivos, pequenos e densos. Carga negativa dispersa pelo átomo positivo. a) A = Dalton; B = Thomson; C = Rutherford. b) A = Dalton; B = Rutherford; C = Thomson. c) A = Thomson; B = Rutherford; C = Bohr. d) A = Rutherford; B = Thomson; C = Bohr. e) A = Thomson; B = Bohr; C = Rutherford. 10) São dadas as seguintes informações relativas aos átomos A, B e C. I) A possui o mesmo número de massa de B e mesmo número de nêutrons que C. II) B tem número atômico 56, número de massa 137 e é isótopo de C. III) O número de massa de C é 138. Qual o número atômico de A? 11) Dadas as espécies químicas : I = 48 Cd 112 II = 27 Co 60 III = 48 Cd 114 IV = 29 Cu 60 a) Quais representam átomos com igual número de massa? b) Quais representam átomos isótopos? c) Determine o número de nêutrons em cada espécie. d) Dê a configuração eletrônica para cada um dos átomos dos quatro elementos químicos. 12) (UNISA-SP) Em qual das sequências a seguir, estão representados um elemento, uma substância simples e uma substância composta, respectivamente? a) H 2, Cl 2, O 2 b) H 2, Ne, H 2 O c) N, HI, He d) H 2 O, O 2, H 2 e) Cl, N 2, HI. 13) Qual o número atômico de um átomo, sabendo que o subnível de maior energia da sua distribuição eletrônica no estado fundamental é 4p 2? 14) (EEP-SP) Um átomo que possui configuração 1s 2 2s 2 2p 6 3s 2 3p 5 apresenta quantos elétrons na camada mais externa?
6 15) (UFOP-MG) Um átomo tem número de massa 30 e 16 nêutrons. Qual é o número de elétrons no seu subnível mais energético? 16) (UEL-PR) Um estudante apresentou a seguinte distribuição eletrônica para o átomo de bromo: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 9 4s 2 4p 6. Houve incorreção no número de elétrons dos subníveis: a) 3d e 4p b) 3d e 4s c) 4s e 4p d) 3d e) 4p 17) (UNIP-SP) O átomo 3x+2 A 7x tem 38 nêutrons. O número de elétrons existente na camada de valência desse átomo é: a) 1 b) 2 c) 3 d) 4 e) 5 18) Numa bancada de laboratório temos cinco frascos fechados com rolha comum que contém, separadamente, os líquidos seguintes: Frasco Substância Ponto de fusão Ponto de ebulição (ºC) (ºC) 1 Anilina Benzeno Etanol Pentano Ácido acético Num dia de muito calor, em determinado instante, ouve-se no laboratório, um estampido produzido pelo arremesso da rolha de um dos frascos para o teto. De qual dos frascos foi arremessada a rolha? 19) (IFSP) Separação de misturas é uma operação muito comum no setor de petróleo e combustíveis. Diversos métodos são aplicados para atender a essa necessidade. Sabendo-se que a água e o álcool são miscíveis e o óleo imiscível nestes e que o álcool tem o menor e o óleo o maior ponto de ebulição, o método adequado para separar essas três substâncias é: a) decantação e filtração. b) filtração e fusão fracionada. c) decantação e centrifugação. d) filtração simples e evaporação. e) decantação e destilação fracionada 20) O titânio (Z = 22) é muito utilizado atualmente, quando se deseja um material de difícil oxidação. Sobre esse elemento, são feitas as seguintes proposições: I) Possui 12 elétrons na camada M. II) Apresenta 4 camadas eletrônicas. III) Apresenta 8 elétrons no subnível s. IV) O seu subnível mais energético é o subnível 4s. São corretas: a) II, III e IV b) II e IV c) III e IV d) II e III e) todas Avaliação Diagnóstica Leia um trecho do texto Os elementos e a manutenção da vida e responda as questões abaixo: Para facilitar o estudo da constituição da Terra, os geólogos costumam dividi-la em três camadas: núcleo, manto e crosta terrestre. O núcleo é a camada mais profunda, e acredita-se ser formada por óxidos de níquel e ferro, provavelmente fundidos. O manto localiza-se entre o núcleo e a crosta. Supõe-se que seja formado pelos elementos químicos oxigênio (O), silício (Si) e alumínio (Al). A crosta terrestre é a camada mais externa, cuja profundidade é estimada em 40 km. Os 12 elementos que constituem 99,7% da crosta terrestre são (em ordem decrescente de abundância): O, Si, Al, Fe, Ca, Mg, Na, K, Ti, H, P e Mn. a) De acordo com o trecho, o núcleo da Terra é formado, majoritariamente, por óxido de ferro, cuja fórmula é Fe 2 O 3, e óxido de níquel, com fórmula NiO. Analisando as fórmulas, essas duas substâncias podem ser classificadas como simples ou compostas? Por que? b) Analisando a fórmula do óxido de ferro (Fe 2 O 3 ), quantos átomos e quantos elementos químicos estão envolvidos na formação dessa substância? c) De acordo com o texto, qual é o estado físico dos óxidos de ferro e níquel no núcleo da Terra? d) Sabendo que átomos de oxigênio, sódio e manganês possuem número atômico de 8, 11 e 25, respectivamente, dê a configuração eletrônica para os átomos de cada um desses três elementos. Identifique também qual é a camada de valência e o subnível mais energético para cada caso. Gabarito 1) a) Cl: 1s 2 2s 2 2p 6 3s 2 3p 5 ; b) Al: 1s 2 2s 2 2p 6 3s 2 3p 1 ; c) Mo: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 4 ; d) Rb: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 1 ; e) In: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 1 ; f) U: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6 7s 2 5f 4 ; g) Si: 1s 2 2s 2 2p 6 3s 2 3p 2 ; h) Br: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 5. 2) Z = 18. 3) camada de valência: N (4º nível), subnível mais energético 4d. 4) b). 5) cátion/ânion. 6) a) ânion, 35 prótons, 36 elétrons; b) ânion, 16 prótons, 18 elétrons; c) cátion, 38 prótons, 36 elétrons; d) cátion, 19 prótons, 18 elétrons; e) cátion, 24 prótons, 21 elétrons; f) ânion, 8 prótons, 10 elétrons. 7) c). 8) e). 9) b). 10) Z = ) a) nenhum b) I e III c) Cd = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 ; Co = 1s² 2s² 2p 6 3s² 3p 6 4s² 3d 7, Cu = 1s² 2s² 2p 6 3s² 3p 6 4s² 3d 9. 12) e). 13) Z = ) 7 elétrons. 15) 2 elétrons. 16) e). 17) d). 18) pentano. 19) e). 20) d)
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA
 Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito)
 SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica
 Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
QUÍMICA 1 ANO - PROGRESSÃO 2015
 QUÍMICA 1 ANO - PROGRESSÃO 2015 1. Esta questão apresenta três afirmativas, que podem estar corretas ou incorretas. Responda-a, obedecendo ao seguinte código: I) Fe, AI, C, Na são conjunto de elementos
QUÍMICA 1 ANO - PROGRESSÃO 2015 1. Esta questão apresenta três afirmativas, que podem estar corretas ou incorretas. Responda-a, obedecendo ao seguinte código: I) Fe, AI, C, Na são conjunto de elementos
Química A Semiextensivo V. 1
 Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular
 Colégio Drummond Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular MATERIAL DE QUÍMICA PROF.: CARLINHOS CURSINHO 2+ efeito estufa é o monóxido de carbono CO2, este é liberado principalmente
Colégio Drummond Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular MATERIAL DE QUÍMICA PROF.: CARLINHOS CURSINHO 2+ efeito estufa é o monóxido de carbono CO2, este é liberado principalmente
Ciências da Natureza e Matemática
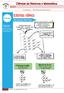 1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 1. Cada átomo possui um certo número de elétrons, que é igual ao valor de seu número atômico (Z). Os elétrons se encontram distribuídos nos
1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 1. Cada átomo possui um certo número de elétrons, que é igual ao valor de seu número atômico (Z). Os elétrons se encontram distribuídos nos
QUÍMICA ÁTOMOS. Professor: Rafael Odorico
 QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
Exercícios de atomística
 DISCIPLINA PROFESSOR QUÍMICA REVISADA DATA (rubrica) ARMANDO 2017 NOME Nº ANO TURMA ENSINO 1º MÉDIO Exercícios de atomística 1. (ITA) Em 1808, John Dalton propôs um modelo de teoria atômica. Considere
DISCIPLINA PROFESSOR QUÍMICA REVISADA DATA (rubrica) ARMANDO 2017 NOME Nº ANO TURMA ENSINO 1º MÉDIO Exercícios de atomística 1. (ITA) Em 1808, John Dalton propôs um modelo de teoria atômica. Considere
Química A Extensivo V. 2
 Química A Extensivo V. 2 Exercícios 01) B 02) A a) Errada. Ao mudar de órbita, os elétrons emite ou absorve energia igual à diferença de energia entre as órbitas. b) Certa. c) Errada. De acordo com a teoria
Química A Extensivo V. 2 Exercícios 01) B 02) A a) Errada. Ao mudar de órbita, os elétrons emite ou absorve energia igual à diferença de energia entre as órbitas. b) Certa. c) Errada. De acordo com a teoria
APOSTILA DE QUÍMICA 2º BIMESTRE
 Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
PROVA DE QUÍMICA 3 o TRIMESTRE DE 2015
 PROVA DE QUÍMICA 3 o TRIMESTRE DE 2015 PROF. MARCOS NOME Nº 9º ANO A prova deve ser feita com caneta azul ou preta. É terminantemente proibido o uso de corretor. Respostas com corretor serão anuladas.
PROVA DE QUÍMICA 3 o TRIMESTRE DE 2015 PROF. MARCOS NOME Nº 9º ANO A prova deve ser feita com caneta azul ou preta. É terminantemente proibido o uso de corretor. Respostas com corretor serão anuladas.
LOGO. Modelos Atômicos. Profa. Núria Galacini
 LOGO Modelos Atômicos Profa. Núria Galacini Demócrito: no século IV a.c. afirmava que a matéria era composta de partículas indivisíveis, o átomo. John Dalton: em 1808 formulou uma definição acerca dos
LOGO Modelos Atômicos Profa. Núria Galacini Demócrito: no século IV a.c. afirmava que a matéria era composta de partículas indivisíveis, o átomo. John Dalton: em 1808 formulou uma definição acerca dos
1. O modelo atômico de Rutherford é também conhecido como modelo planetário do átomo.
 2º Trimestre_8AB_2014_REVISÃO_Química_Prof.ª Caroline Oliveira Nome: Turma: 8 Data: / /2014. 1- Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford
2º Trimestre_8AB_2014_REVISÃO_Química_Prof.ª Caroline Oliveira Nome: Turma: 8 Data: / /2014. 1- Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA 2016
 ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 2,0 ) I. Introdução Neste ano, seu total de pontos foi inferior a 60,0 e, portanto
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 2,0 ) I. Introdução Neste ano, seu total de pontos foi inferior a 60,0 e, portanto
- Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil.
 - Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil www.profkemil.ning.com EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade sobre do que era constituída a matéria parecia
- Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil www.profkemil.ning.com EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade sobre do que era constituída a matéria parecia
Estrutura Atômica. Atomística.
 Estrutura Atômica Atomística. Democrito e Leucipo (450 a. C) Átomo Dalton (séc. XIX) Bola de Bilhar Thomson (séc. XIX) Pudim de passas Rutherford (séc. XX) sistema solar Átomos núcleo prótons (+1) eletrosfera
Estrutura Atômica Atomística. Democrito e Leucipo (450 a. C) Átomo Dalton (séc. XIX) Bola de Bilhar Thomson (séc. XIX) Pudim de passas Rutherford (séc. XX) sistema solar Átomos núcleo prótons (+1) eletrosfera
DISTRIBUIÇÃO ELETRÔNICA
 DISTRIBUIÇÃO ELETRÔNICA Profª. Regina Modesto Raszl Um problema para os químicos era construir uma teoria consistente que explicasse como os elétrons se distribuíam ao redor dos átomos, dando-lhes as características
DISTRIBUIÇÃO ELETRÔNICA Profª. Regina Modesto Raszl Um problema para os químicos era construir uma teoria consistente que explicasse como os elétrons se distribuíam ao redor dos átomos, dando-lhes as características
2) Um átomo T apresenta menos 2 prótons que um átomo Q. Com base nessa informação, assinale a opção falsa.
 1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
Química A Extensivo V. 2
 Química A Extensivo V. 2 01) Alternativa correta: B Exercícios a) Errada ao mudar de órbita, o elétrons emite ou absorve energia igual a diferença de energia entre as órbitas; b) Certa; c) Errada de acordo
Química A Extensivo V. 2 01) Alternativa correta: B Exercícios a) Errada ao mudar de órbita, o elétrons emite ou absorve energia igual a diferença de energia entre as órbitas; b) Certa; c) Errada de acordo
LISTA DE EXERCÍCIO PARA A PROVA MENSAL
 Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Estrutura Atômica II
 Estrutura Atômica II Modelo nuclear do átomo: Constituído de partículas subatômicas: Prótons, Nêutrons e elétrons Os prótons e nêutrons formam o núcleo minúsculo e denso que compreende quase toda a massa
Estrutura Atômica II Modelo nuclear do átomo: Constituído de partículas subatômicas: Prótons, Nêutrons e elétrons Os prótons e nêutrons formam o núcleo minúsculo e denso que compreende quase toda a massa
Átomo. Modelos atômicos e propriedades
 Átomo Modelos atômicos e propriedades O ÁTOMO CONCEITO: Aprox. 500 AC Demócrito e outros filósofos gregos desenvolveram o conceito de átomo A matéria poderia ser dividida progressivamente até chegar à
Átomo Modelos atômicos e propriedades O ÁTOMO CONCEITO: Aprox. 500 AC Demócrito e outros filósofos gregos desenvolveram o conceito de átomo A matéria poderia ser dividida progressivamente até chegar à
AULA 1: EXERCÍCIOS DE FIXAÇÃO QUÍMICA AULA 1: EXERCÍCIOS DE FIXAÇÃO ELEMENTOS QUÍMICOS, TABELA PERIÓDICA, PROPRIEDADES PERIÓDICAS.
 QUÍMICA AULA 1: EXERCÍCIOS DE FIXAÇÃO ELEMENTOS QUÍMICOS, TABELA PERIÓDICA, PROPRIEDADES PERIÓDICAS. Professora Priscila Miranda E-mail: miranda.educacao@gmail.com WhatsApp: +5511976100005 Turmas de Agosto
QUÍMICA AULA 1: EXERCÍCIOS DE FIXAÇÃO ELEMENTOS QUÍMICOS, TABELA PERIÓDICA, PROPRIEDADES PERIÓDICAS. Professora Priscila Miranda E-mail: miranda.educacao@gmail.com WhatsApp: +5511976100005 Turmas de Agosto
esféricas maciças e indivisíveis.
 a) A-I, B-II, C-III b) A-II, B-III, C-I c) A-III, B-I, C-II d) A-III, B-II, C-I e) A-II, B-I, C-III LISTA DE EXERCÍCIOS DE QUÍMICA 1º Ano do Ensino Médio Professor: Anderson Paschôa É preciso estudar todos
a) A-I, B-II, C-III b) A-II, B-III, C-I c) A-III, B-I, C-II d) A-III, B-II, C-I e) A-II, B-I, C-III LISTA DE EXERCÍCIOS DE QUÍMICA 1º Ano do Ensino Médio Professor: Anderson Paschôa É preciso estudar todos
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB
 AULA DE RECUPERAÇÃO PROF. NEIF NAGIB CONCEITOS SOBRE O ÁTOMO Número Atômico (Z): quantidades de prótons. Z = p = e Número de Massa (A): a soma das partículas que constitui o átomo. A = Z + N REPRESENTAÇÃO
AULA DE RECUPERAÇÃO PROF. NEIF NAGIB CONCEITOS SOBRE O ÁTOMO Número Atômico (Z): quantidades de prótons. Z = p = e Número de Massa (A): a soma das partículas que constitui o átomo. A = Z + N REPRESENTAÇÃO
Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica
 Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um
Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um
Temática: Distribuição eletrônica
 Temática: Distribuição eletrônica Nesta aula, você verá que em átomos com poucos elétrons, todos os orbitais da mesma camada têm a mesma energia, entretanto as energias dos orbitais dos átomos com muitos
Temática: Distribuição eletrônica Nesta aula, você verá que em átomos com poucos elétrons, todos os orbitais da mesma camada têm a mesma energia, entretanto as energias dos orbitais dos átomos com muitos
Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio. Números Quânticos e Diagrama de Pauling;
 Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio Números Quânticos e Diagrama de Pauling; Número quântico principal (n): indica o nível de energia do elétron no átomo.
Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 1º ano Ensino Médio Números Quânticos e Diagrama de Pauling; Número quântico principal (n): indica o nível de energia do elétron no átomo.
C i ê n c i a s d a N a t u r e z a e s u a s T e c n o l o g i a s Q U Í M I C A N O M E: N º T U R M A : D A T A :
 C i ê n c i a s d a N a t u r e z a e s u a s T e c n o l o g i a s Q U Í M I C A P r o f ª M á r c i a R i b e i r o N O M E: N º T U R M A : D A T A : C a m a d a s e l e t r ô n i c a s Os átomos são
C i ê n c i a s d a N a t u r e z a e s u a s T e c n o l o g i a s Q U Í M I C A P r o f ª M á r c i a R i b e i r o N O M E: N º T U R M A : D A T A : C a m a d a s e l e t r ô n i c a s Os átomos são
Lista de exercícios Aulas 03 e 04. 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em:
 Lista de exercícios Aulas 03 e 04 Prof. Fernanda Dias 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em: a) a formação dos materiais dá-se através de diferentes associações entre
Lista de exercícios Aulas 03 e 04 Prof. Fernanda Dias 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em: a) a formação dos materiais dá-se através de diferentes associações entre
Aula 08 - Níveis e subníveis eletrônicos e a Distribuição Eletrônica
 Aula 08 - Níveis e subníveis eletrônicos e a Distribuição Eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um átomo
Aula 08 - Níveis e subníveis eletrônicos e a Distribuição Eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um átomo
LIGAÇÕES QUÍMICAS Parte 2
 Disciplina: Química Prof.: Guilherme Turma: IU 08/06/2017 Tema da aula: Ligação covalente Relembrando a ligação iônica LIGAÇÕES QUÍMICAS Parte 2 - A ligação iônica ocorre entre íons positivos (os cátions)
Disciplina: Química Prof.: Guilherme Turma: IU 08/06/2017 Tema da aula: Ligação covalente Relembrando a ligação iônica LIGAÇÕES QUÍMICAS Parte 2 - A ligação iônica ocorre entre íons positivos (os cátions)
Tarefa 23 Professor Gustavo
 Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
05 - (UEL PR/1994) Localize na tabela periódica o elemento químico de número atômico 20 e escolha a(s)
 01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
Exercícios Sobre DistribuiÇão eletrônica
 Exercícios Sobre DistribuiÇão eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z= 55) b) Tl (Z= 81) 02. Faça a distribuição eletrônica nas camadas, para os átomos:
Exercícios Sobre DistribuiÇão eletrônica Dado: 01. Faça a distribuição eletrônica nas camadas para os átomos: a) Cs (Z= 55) b) Tl (Z= 81) 02. Faça a distribuição eletrônica nas camadas, para os átomos:
11Na 12Mg 15P 16S 17Cl 19K 20Ca. 24Cr 25Mn 26Fe 27Co 29Cu .../.../... TRO TEC CVI TURMA M V N
 CINAT COORDENADORIA DE QUÍMICA Química I (Inorgânica) 1º semestre 2015 Prof. Éder C. Assunto: Reavaliação 1ª Etapa. DATA CURSO.../.../... TRO TEC CVI Lista: 1h TURMA M V N Z 1 6 7 8 11 12 15 16 17 19 20
CINAT COORDENADORIA DE QUÍMICA Química I (Inorgânica) 1º semestre 2015 Prof. Éder C. Assunto: Reavaliação 1ª Etapa. DATA CURSO.../.../... TRO TEC CVI Lista: 1h TURMA M V N Z 1 6 7 8 11 12 15 16 17 19 20
BIMESTRAL QUÍMICA - 1ºBIMESTRE
 BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
Química. 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30
 Química 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30 02. Para que um átomo de número atômico 55 e número de massa 137 seja eletricamente neutro, ele deverá ter, necessariamente:
Química 01. Quantos prótons há na espécie química (A) 2 (D) 32 (B) 28 (E) 60 (C) 30 02. Para que um átomo de número atômico 55 e número de massa 137 seja eletricamente neutro, ele deverá ter, necessariamente:
Aula 4 24/03/2016. Atomística Parte 2
 Aula 4 24/03/2016 Atomística Parte 2 - Todo elemento químico possui um número atômico, representado pela letra Z, característico. Esse número atômico indica a quantidade de prótons existentes no núcleo
Aula 4 24/03/2016 Atomística Parte 2 - Todo elemento químico possui um número atômico, representado pela letra Z, característico. Esse número atômico indica a quantidade de prótons existentes no núcleo
T.C de Química 1 o ano Prof. Alan Ibiapina
 T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
QUÍMICA PROFº JAISON MATTEI
 QUÍMICA PROFº JAISON MATTEI 1. O modelo atômico de Dalton, concebendo o átomo como uma bolinha maciça e indivisível, fez a Química progredir muito no século XIX. Mas o conhecimento sobre estrutura atômica
QUÍMICA PROFº JAISON MATTEI 1. O modelo atômico de Dalton, concebendo o átomo como uma bolinha maciça e indivisível, fez a Química progredir muito no século XIX. Mas o conhecimento sobre estrutura atômica
Química. Aula 04 Profº Ricardo Dalla Zanna
 Química Aula 04 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Átomos e Elementos o Seção 2.1 Evolução do modelo atômico e classificação periódica dos elementos o Seção 2.2 Leis ponderais o
Química Aula 04 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Átomos e Elementos o Seção 2.1 Evolução do modelo atômico e classificação periódica dos elementos o Seção 2.2 Leis ponderais o
Aulas 1 e 2. Atomística
 Aulas 1 e 2 Atomística Modelos Atômicos Dalton - 1808 Primeiro cientista a desenvolver uma teoria atômica, segundo a qual a matéria se compõe de partículas indestrutíveis chamadas átomos. Modelos Atômicos
Aulas 1 e 2 Atomística Modelos Atômicos Dalton - 1808 Primeiro cientista a desenvolver uma teoria atômica, segundo a qual a matéria se compõe de partículas indestrutíveis chamadas átomos. Modelos Atômicos
CIÊNCIAS DA NATUREZA - QUÍMICA Prof. Adriana Strelow 1º Ano
 CIÊNCIAS DA NATUREZA - QUÍMICA Prof. Adriana Strelow 1º Ano - 2016 TABELA PERIÓDICA ATUAL: Os elementos estão ordenados em ordem crescente de número atômico. O critério utilizado para classificar os elementos
CIÊNCIAS DA NATUREZA - QUÍMICA Prof. Adriana Strelow 1º Ano - 2016 TABELA PERIÓDICA ATUAL: Os elementos estão ordenados em ordem crescente de número atômico. O critério utilizado para classificar os elementos
Terceira aula de química
 Terceira aula de química Nome: Laísa 24/04/2017 O modelo atômico de Thomson Foi proposta em 1898 pelo físico inglês Joseph John Thomson. Ele derrubou a teoria da indivisibilidade do átomo proposta por
Terceira aula de química Nome: Laísa 24/04/2017 O modelo atômico de Thomson Foi proposta em 1898 pelo físico inglês Joseph John Thomson. Ele derrubou a teoria da indivisibilidade do átomo proposta por
Resoluções. Estrutura atômica
 Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 1 Estrutura atômica 1. A A composição metafísica presente no poema remete aos modelos atômicos propostos
Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 1 Estrutura atômica 1. A A composição metafísica presente no poema remete aos modelos atômicos propostos
K L M N O P Q 7 NÍVEIS DE ENERGIA n =
 Química / profª SIMONE MORGADO Aula 3 Configuração Eletrônica 1. A ELETROSFERA Nossa caminhada hoje é pela eletrosfera, uma região bastante importante, pois nas reações químicas os elétrons são as partículas
Química / profª SIMONE MORGADO Aula 3 Configuração Eletrônica 1. A ELETROSFERA Nossa caminhada hoje é pela eletrosfera, uma região bastante importante, pois nas reações químicas os elétrons são as partículas
ATOMÍSTICA. Teoria de Thomson (1898) Todo átomo é formado por uma matéria positiva, na qual se encontrariam os elétrons distribuídos ao acaso.
 1. MODLOS ATÔMICOS Teoria de Dalton (1803): Toda matéria é constituída por átomos; Átomos de um mesmo elemento químico possuem propriedades químicas e físicas iguais; Todo átomo corresponde a uma esfera
1. MODLOS ATÔMICOS Teoria de Dalton (1803): Toda matéria é constituída por átomos; Átomos de um mesmo elemento químico possuem propriedades químicas e físicas iguais; Todo átomo corresponde a uma esfera
- ATOMÍSTICA Folha 03 João Roberto Mazzei
 01- (UFRJ 2005) Um professor decidiu decorar seu laboratório com um "relógio de Química" no qual, no lugar das horas, estivessem alguns elementos, dispostos de acordo com seus respectivos números atômicos,
01- (UFRJ 2005) Um professor decidiu decorar seu laboratório com um "relógio de Química" no qual, no lugar das horas, estivessem alguns elementos, dispostos de acordo com seus respectivos números atômicos,
Química Geral -Aula 2 Átomo e estrutura atômica. *Mas afinal, de que são feitas as coisas?
 Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
Sendo o cálcio pertencente ao grupo dos alcalinos terrosos e possuindo número atômico Z = 20, a configuração eletrônica do seu cátion bivalente é:
 1- (U.F.Uberlândia-MG\Pales) Dalton, Thomson, Rutherford e Bohr são cientistas que contribuíram, significativamente, para o desenvolvimento da teoria atômica. Em relação a estrutura atômica, assinale com(v)
1- (U.F.Uberlândia-MG\Pales) Dalton, Thomson, Rutherford e Bohr são cientistas que contribuíram, significativamente, para o desenvolvimento da teoria atômica. Em relação a estrutura atômica, assinale com(v)
OLIMPÍADA PIAUIENSE DE QUÍMICA Modalidade EF
 OLIMPÍADA PIAUIENSE DE QUÍMICA - 2013 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
OLIMPÍADA PIAUIENSE DE QUÍMICA - 2013 Modalidade EF INSTRUÇÕES 1 Esta prova contém oito questões no total, sendo duas questões abertas e seis questões de múltipla escolha. 2 Antes de iniciar a prova, confira
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 2 o SEMESTRE DE 2016
 ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 2 o SEMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 2,0 ) I. Introdução Neste semestre, seu total de pontos foi inferior
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 2 o SEMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 2,0 ) I. Introdução Neste semestre, seu total de pontos foi inferior
OPÇÃO CONCURSO. e) 11 prótons, 11 elétrons e 11 nêutrons.
 1) Somando-se todas as partículas (prótons, nêutrons e elétrons) de um átomo de 28 Ni 59 com as do átomo de 80 Hg 201, o total de partículas será: a) 281. b) 158. c) 368. d) 108. e) 360. 2) O átomo de
1) Somando-se todas as partículas (prótons, nêutrons e elétrons) de um átomo de 28 Ni 59 com as do átomo de 80 Hg 201, o total de partículas será: a) 281. b) 158. c) 368. d) 108. e) 360. 2) O átomo de
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
QUÍMICA. Transformações Químicas. Teoria Atômica Modelo Atômico de Dalton, Thomson, Rutherford, Rutherford-Bohr Parte 2. Prof a.
 QUÍMICA Transformações Químicas Teoria Atômica Modelo Atômico de Dalton, Thomson, Parte 2 Prof a. Giselle Blois Problemas com o átomo de Rutherford: Teoria Atômica: Modelo Atômico de Dalton, Thomson, -
QUÍMICA Transformações Químicas Teoria Atômica Modelo Atômico de Dalton, Thomson, Parte 2 Prof a. Giselle Blois Problemas com o átomo de Rutherford: Teoria Atômica: Modelo Atômico de Dalton, Thomson, -
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
1. ESTRUTURA DO ÁTOMO
 Química Profª SIMONE MORGADO Aula 2 Estrutura do átomo, nº atômico, nº de massa e isoátomos. 1. ESTRUTURA DO ÁTOMO Como nós já vimos a Química é essa ciência que busca compreender os mistérios da matéria,
Química Profª SIMONE MORGADO Aula 2 Estrutura do átomo, nº atômico, nº de massa e isoátomos. 1. ESTRUTURA DO ÁTOMO Como nós já vimos a Química é essa ciência que busca compreender os mistérios da matéria,
LOGO. Tabela Periódica. Profa. Samara Garcia
 LOGO Tabela Periódica Profa. Samara Garcia Antes da Tabela Periódica O trabalho de Böhr despertou o interesse de vários cientistas para o estudo dos espectros descontínuos. Um deles, Sommerfeld, percebeu,
LOGO Tabela Periódica Profa. Samara Garcia Antes da Tabela Periódica O trabalho de Böhr despertou o interesse de vários cientistas para o estudo dos espectros descontínuos. Um deles, Sommerfeld, percebeu,
QUÍMICA GERAL Cap. 01. Prof. Kristian Sales Vieira
 QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! CIÊNCIAS - UNIDADE 3 ÁTOMOS E LIGAÇÕES QUÍMICAS
 Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
1º Trimestre Sala de Estudos-Química Data: 13/03/17 Ensino Médio 1º ano classe: A_B_C Profª Danusa Nome: nº
 º Trimestre Sala de Estudos-Química Data: 3/03/7 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Estrutura atômica e Configuração Eletrônica Questão 0 - (PUC- RS) Ao se deixar cair sal
º Trimestre Sala de Estudos-Química Data: 3/03/7 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Estrutura atômica e Configuração Eletrônica Questão 0 - (PUC- RS) Ao se deixar cair sal
DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente
 FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
Distribuição dos elétrons
 Distribuição dos elétrons Camadas Eletrônicas ou Níveis de Energia A coroa ou eletrosfera está dividida em 7 níveis ou camadas designadas por K, L, M, N, O, P, Q ou pelos números: n = 1, 2, 3, 4, 5, 6,
Distribuição dos elétrons Camadas Eletrônicas ou Níveis de Energia A coroa ou eletrosfera está dividida em 7 níveis ou camadas designadas por K, L, M, N, O, P, Q ou pelos números: n = 1, 2, 3, 4, 5, 6,
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
QUI109 QUÍMICA GERAL (Ciências Biológicas) 6ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) MODELO ATÔMICO J. Dalton a matéria é formada por átomos / as inúmeras
Química. Resolução das atividades complementares. Q34 Distribuição de íons
 Resolução das atividades complementares 3 Química Q34 istribuição de íons p. 11 1 orneça a configuração eletrônica 2 segundo o diagrama de Linus Pauling 2 dos íons a seguir no estado fundamental em ordem
Resolução das atividades complementares 3 Química Q34 istribuição de íons p. 11 1 orneça a configuração eletrônica 2 segundo o diagrama de Linus Pauling 2 dos íons a seguir no estado fundamental em ordem
Qui. Semana. Allan Rodrigues Xandão (Renan Micha)
 Semana 4 Allan Rodrigues Xandão (Renan Micha) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Semana 4 Allan Rodrigues Xandão (Renan Micha) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
1) Delineie os elementos-chave da teoria atômica de Dalton. Quais deles não são consistentes com a visão moderna do átomo?
 Disciplina: Química Geral I QM81B. 1ª Lista de Exercícios: Modelos Atômicos, Estrutura Atômica, Tabela Periódica e Propriedades Periódicas. Prof. Dr. Cristiano Torres Miranda. Nome: Modelos atômicos 1)
Disciplina: Química Geral I QM81B. 1ª Lista de Exercícios: Modelos Atômicos, Estrutura Atômica, Tabela Periódica e Propriedades Periódicas. Prof. Dr. Cristiano Torres Miranda. Nome: Modelos atômicos 1)
Roteiro de Estudos 2 trimestre Disciplina: Química 9ºs Anos Professor: Ricardo Augusto Marques da Costa
 Roteiro de Estudos 2 trimestre - 2017 Disciplina: Química 9ºs Anos Professor: Ricardo Augusto Marques da Costa O que devo saber: Constituição da matéria: Teoria atômica de Dalton. Representação dos elementos
Roteiro de Estudos 2 trimestre - 2017 Disciplina: Química 9ºs Anos Professor: Ricardo Augusto Marques da Costa O que devo saber: Constituição da matéria: Teoria atômica de Dalton. Representação dos elementos
3º EM. Química A Jaque / Lailson Aval. Mensal 06/03/13. Para efeitos de consulta, se necessário, utilize a tabela periódica abaixo:
 3º EM Química A Jaque / Lailson Aval. Mensal 06/03/13 Para efeitos de consulta, se necessário, utilize a tabela periódica abaixo: 1. (1,0) Tendo por base o modelo atômico atual, assinale (V) para verdadeiro
3º EM Química A Jaque / Lailson Aval. Mensal 06/03/13 Para efeitos de consulta, se necessário, utilize a tabela periódica abaixo: 1. (1,0) Tendo por base o modelo atômico atual, assinale (V) para verdadeiro
ESTRUTURA ATÔMICA. Modelos Atômicos
 ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
2- (UEL-PR) Assinale a opção que apresenta as massas moleculares dos seguintes compostos: C 6 H 12 O 6 ; Ca 3 (PO 4 ) 2 e Ca(OH) 2, respectivamente:
 QUÍMICA 1- A magnetita, um minério do qual se extrai ferro possui fórmula molecular Fe 3 O x e sua massa molecular é 232u. Determine o valor de x e escreva a fórmula molecular correta da magnetita. 2-
QUÍMICA 1- A magnetita, um minério do qual se extrai ferro possui fórmula molecular Fe 3 O x e sua massa molecular é 232u. Determine o valor de x e escreva a fórmula molecular correta da magnetita. 2-
Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida
 Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida Índice Substâncias e Misturas...1 Evolução do Modelo Atômico...3 Tabela Periódica...4 Exercícios...5 Gabarito...7
Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida Índice Substâncias e Misturas...1 Evolução do Modelo Atômico...3 Tabela Periódica...4 Exercícios...5 Gabarito...7
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO CAMPUS VALENÇA SÉRIE: 1º ANO DISCIPLINA: QUÍMICA PROFESSOR: JOSÉ TIAGO PEREIRA BARBOSA
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO CAMPUS VALENÇA SÉRIE: 1º ANO DISCIPLINA: QUÍMICA PROFESSOR: JOSÉ TIAGO PEREIRA BARBOSA Lista de Exercícios Distribuição Eletrônica Diagrama de
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO CAMPUS VALENÇA SÉRIE: 1º ANO DISCIPLINA: QUÍMICA PROFESSOR: JOSÉ TIAGO PEREIRA BARBOSA Lista de Exercícios Distribuição Eletrônica Diagrama de
Química Geral Aula 2 Notação científica / atomística
 Química Geral Aula 2 Notação científica / atomística Revisão Sistema internacional de unidades (SI) 2 O que é o SI? É um sistema de unidades de medida concebido em torno de sete unidades básicas: Visa
Química Geral Aula 2 Notação científica / atomística Revisão Sistema internacional de unidades (SI) 2 O que é o SI? É um sistema de unidades de medida concebido em torno de sete unidades básicas: Visa
Questão 1) Questão 2)
 QUÍMICA CARLÃO Questão 1) Muitos produtos tecnológicos da atualidade são resultados de experimentos que trouxeram grandes resultados para o desenvolvimento da Química. Um destes experimentos foi o da ampola
QUÍMICA CARLÃO Questão 1) Muitos produtos tecnológicos da atualidade são resultados de experimentos que trouxeram grandes resultados para o desenvolvimento da Química. Um destes experimentos foi o da ampola
ATIVIDADE DE QUÍMICA REVISÃO 9º ANO. Distribuição Eletrônica de Linus Pauling
 ATIVIDADE DE QUÍMICA REVISÃO 9º ANO Distribuição Eletrônica de Linus Pauling Em anos anteriores ao rearranjo que Linus Pauling fez para distribuir eletronicamente os elementos, os Cientistas Bohr e Sommerfield
ATIVIDADE DE QUÍMICA REVISÃO 9º ANO Distribuição Eletrônica de Linus Pauling Em anos anteriores ao rearranjo que Linus Pauling fez para distribuir eletronicamente os elementos, os Cientistas Bohr e Sommerfield
PLANO DE ESTUDO TRIMESTRE: 1º
 C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 03 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 27/04/2018 DISCIPLINA: Química ANO/SÉRIE: 9º ANO
C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 03 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 27/04/2018 DISCIPLINA: Química ANO/SÉRIE: 9º ANO
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1
 PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
PROPRIEDADES E COMPOSIÇÃO DA MATÉRIA Aula 1 Matéria: é qualquer coisa que tem massa e ocupa espaço. Átomo: é a menor partícula possível de um elemento químico. É formado por núcleo e eletrosfera. É constituído
O ÁTOMO pág. 66. Átomo: do grego, indivisível.
 O ÁTOMO pág. 66 Átomo: do grego, indivisível. Núcleo: Prótons + Nêutrons Eletrosfera: Elétrons Número atômico (Z): nº de prótons no núcleo Número de massa (A): nº de prótons + nêutrons Prótons: carga positiva
O ÁTOMO pág. 66 Átomo: do grego, indivisível. Núcleo: Prótons + Nêutrons Eletrosfera: Elétrons Número atômico (Z): nº de prótons no núcleo Número de massa (A): nº de prótons + nêutrons Prótons: carga positiva
LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON
 LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e)
LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e)
2) Um átomo T apresenta menos 2 prótons que um átomo Q. Com base nessa informação, assinale a opção falsa.
 1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
OLIMPÍADA PIAUIENSE DE QUÍMICA 2016 Modalidade EF - 12/11/2016. Código: Nome: Escola: Endereço: Telefone: Destaque aqui...
 Identificação Modalidade EF Código: Nome: Escola: Endereço: Telefone: Destaque aqui... CÓDIGO DO ALUNO (escreva aqui seu código) GABARITO Assinale a letra correspondente à resposta correta de cada uma
Identificação Modalidade EF Código: Nome: Escola: Endereço: Telefone: Destaque aqui... CÓDIGO DO ALUNO (escreva aqui seu código) GABARITO Assinale a letra correspondente à resposta correta de cada uma
COLÉGIO NOSSA SENHORA DO MONTE CALVÁRIO CIÊNCIAS
 COLÉGIO NOSSA SENHORA DO MONTE CALVÁRIO CIÊNCIAS SEGMENTO: ENSINO FUNDAMENTAL II ANO: 9º TÍTULO: ATIVIDADE DE REVISÃO PARA AVALIAÇÃO MENSAL II PROFESSORA: ALESSANDRA ARCA DATA: 20/ 04/ 2016 1. Classifique
COLÉGIO NOSSA SENHORA DO MONTE CALVÁRIO CIÊNCIAS SEGMENTO: ENSINO FUNDAMENTAL II ANO: 9º TÍTULO: ATIVIDADE DE REVISÃO PARA AVALIAÇÃO MENSAL II PROFESSORA: ALESSANDRA ARCA DATA: 20/ 04/ 2016 1. Classifique
1 0 Ano ENSINO MÉDIO QUÍMICA
 1 0 Ano ENSINO MÉDIO QUÍMICA MODELOS ATÔMICOS A QUÍMICA Uma ciência é definida como um conjunto organizado de conhecimentos sobre um assunto definido. A química é uma ciência e acumula conhecimentos há
1 0 Ano ENSINO MÉDIO QUÍMICA MODELOS ATÔMICOS A QUÍMICA Uma ciência é definida como um conjunto organizado de conhecimentos sobre um assunto definido. A química é uma ciência e acumula conhecimentos há
SÉRIE: 1 Ano. ALUNO (a): NOTA: LISTA DE EXERCÍCIOS RECUPERAÇÃO SEMESTRAL
 GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS RECUPERAÇÃO SEMESTRAL 01. X é isótopo de 20 41 Ca e isótono
GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS RECUPERAÇÃO SEMESTRAL 01. X é isótopo de 20 41 Ca e isótono
SÉRIE: 1 Ano. ALUNO (a): NOTA: LISTA DE EXERCÍCIOS P1 (2 BIMESTRE)
 GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS P1 (2 BIMESTRE) 1. X é isótopo de 20 41 Ca e isótono de 19
GOIÂNIA, / / 2015 PROFESSOR: Taynara Oliveira DISCIPLINA: Química SÉRIE: 1 Ano ALUNO (a): NOTA: No Anhanguera você é + Enem LISTA DE EXERCÍCIOS P1 (2 BIMESTRE) 1. X é isótopo de 20 41 Ca e isótono de 19
Resoluções das atividades
 Resoluções das atividades Sumário apítulo 6 Modelo atômico segundo a Mecânica ndulatória...1 apítulo 7 lassificação periódica dos elementos...4 apítulo 8 Ligações químicas I...8 apítulo 9 Ligações químicas
Resoluções das atividades Sumário apítulo 6 Modelo atômico segundo a Mecânica ndulatória...1 apítulo 7 lassificação periódica dos elementos...4 apítulo 8 Ligações químicas I...8 apítulo 9 Ligações químicas
Princípios fisico-químicos laboratoriais. Aula 01 Profº Ricardo Dalla Zanna
 Princípios fisico-químicos laboratoriais Aula 01 Profº Ricardo Dalla Zanna Quintas Disciplina 1ª aula Princípios físico-químicos laboratoriais 2ª aula Princípios físico-químicos laboratoriais Intervalo
Princípios fisico-químicos laboratoriais Aula 01 Profº Ricardo Dalla Zanna Quintas Disciplina 1ª aula Princípios físico-químicos laboratoriais 2ª aula Princípios físico-químicos laboratoriais Intervalo
QUÍMICA A Ciênca Central 9ª Edição
 QUÍMICA A Ciênca Central 9ª Edição Capítulo 2 átomos, moléculas e íons David P. White Teoria atômica da matéria John Dalton (1803 1807): Cada elemento é composto de átomos. Todos os átomos de um elemento
QUÍMICA A Ciênca Central 9ª Edição Capítulo 2 átomos, moléculas e íons David P. White Teoria atômica da matéria John Dalton (1803 1807): Cada elemento é composto de átomos. Todos os átomos de um elemento
Colégio Notre Dame de Campinas Congregação de Santa Cruz PLANTÕES DE FÉRIAS QUÍMICA. Nome: Nº: Série: 1º ANO Profª BIANCA RIBEIRO Data: JULHO 2016
 PLANTÕES DE FÉRIAS QUÍMICA Nome: Nº: Série: 1º ANO Profª BIANCA RIBEIRO Data: JULHO 2016 Roteiro de Estudos Primeiramente, revise em seu caderno alguns conceitos importantes da estrutura do átomo, como:
PLANTÕES DE FÉRIAS QUÍMICA Nome: Nº: Série: 1º ANO Profª BIANCA RIBEIRO Data: JULHO 2016 Roteiro de Estudos Primeiramente, revise em seu caderno alguns conceitos importantes da estrutura do átomo, como:
Lista de exercícios de recuperação semestral Aluno (a):
 Lista de exercícios de recuperação semestral Aluno (a): Turma: 9º Ano Professora: Taynara (Ensino fundamental) Disciplina: Química Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
Lista de exercícios de recuperação semestral Aluno (a): Turma: 9º Ano Professora: Taynara (Ensino fundamental) Disciplina: Química Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
Estrutura da matéria. Estrutura atômica
 Estrutura da matéria 1. Considere a tabela de pontos de fusão e pontos de ebulição da substância a seguir. Substância P.F P.E Cloro - 101,0-34.6 Flúor - 219,6-188,1 Bromo - 7,2 58,8 Mercúrio - 38,8 356,6
Estrutura da matéria 1. Considere a tabela de pontos de fusão e pontos de ebulição da substância a seguir. Substância P.F P.E Cloro - 101,0-34.6 Flúor - 219,6-188,1 Bromo - 7,2 58,8 Mercúrio - 38,8 356,6
Linha do Tempo. 400 a.c. Radioatividade. Demócrito. Dalton. Thomson. Rutherford Rutherford-Bohr Rutherford-Bohr (Chadwick)
 Linha do Tempo 400 a.c. 1808 1897 1911 1913 1932 Demócrito Dalton Radioatividade Thomson Rutherford Rutherford-Bohr Rutherford-Bohr (Chadwick) Evolução dos Modelos Atômicos Teoria dos quatro elementos
Linha do Tempo 400 a.c. 1808 1897 1911 1913 1932 Demócrito Dalton Radioatividade Thomson Rutherford Rutherford-Bohr Rutherford-Bohr (Chadwick) Evolução dos Modelos Atômicos Teoria dos quatro elementos
exercícios Sobre a imagem e intensidade das forças intermoleculares,
 Química Marcus Vinícius exercícios 1. (Idecan/CBMMG/CFO/2016) A intensidade das forças intermoleculares em diferentes substâncias varia em uma grande faixa, mas essas forças são muito mais fracas que as
Química Marcus Vinícius exercícios 1. (Idecan/CBMMG/CFO/2016) A intensidade das forças intermoleculares em diferentes substâncias varia em uma grande faixa, mas essas forças são muito mais fracas que as
Atividade extra. Questão 1 Adaptado de CFTMG Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Adaptado de CFTMG - 2007 Em fogos de artifício, observam-se as colorações, quando se adicionam sais de diferentes metais às misturas explosivas. As cores produzidas resultam de
Atividade extra Questão 1 Adaptado de CFTMG - 2007 Em fogos de artifício, observam-se as colorações, quando se adicionam sais de diferentes metais às misturas explosivas. As cores produzidas resultam de
QUÍMICA GERAL PROF. PAULO VALIM
 QUÍMICA GERAL PROF. PAULO VALIM 4 TABELA PERIÓDICA Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
QUÍMICA GERAL PROF. PAULO VALIM 4 TABELA PERIÓDICA Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
TEORIA ATÔMICA. Química Geral
 TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
