ATOMÍSTICA & ISOTOPIA
|
|
|
- Bruno Henriques Castelo
- 8 Há anos
- Visualizações:
Transcrição
1 ATOMÍSTICA & ISOTOPIA MÓDULO 1 TRANSFORMAÇÕES QUÍMICAS
2 EXERCÍCIOS ATOMÍSTICA & ISOTOPIA 1. (IFSP/2013) O número de elétrons da camada de valência do átomo de cálcio (Z = 20), no estado fundamental, é a) 1. b) 2. c) 6. d) 8. e) (FM Petrópolis RJ/2013) O chumbo é um metal pesado que pode contaminar o ar, o solo, os rios e alimentos. A absorção de quantidades pequenas de chumbo por longos períodos pode levar a uma toxicidade crônica, que se manifesta de várias formas, especialmente afetando o sistema nervoso, sendo as crianças as principais vítimas. Sendo o número atômico (Z) do chumbo igual a 82, o íon plumboso (Pb +2 ) possui os elétrons mais energéticos no subnível a) 6p 2 b) 6s 2 c) 6p 4 d) 5d 10 e) 4f (UCS RS/2012) Os dias dos carros com luzes azuis estão contados, pois, desde 1º de janeiro de 2009, as lâmpadas de xenônio (Xe), não podem mais ser instaladas em faróis convencionais. Mesmo que as lâmpadas azuis possibilitem três vezes mais luminosidade do que as convencionais, elas não se adaptam adequadamente aos refletores feitos para o uso com lâmpadas convencionais, podendo causar ofuscamento à visão dos motoristas que trafegam em sentido contrário e possibilitando, assim, a ocorrência de acidentes. Quantos elétrons o gás xenônio apresenta na camada de valência? a) 2. b) 6. c) 8. d) 10. e) (ESCS DF/2012) Os pesquisadores alertam que os metais dos quais as panelas são feitas podem causar intoxicações, anemia, distúrbios gástricos e até expor os usuários a substâncias cancerígenas. Pesquisas mostram que o excesso de alumínio no corpo pode induzir a estados de demência, panelas deste metal devem ser utilizadas para cozimentos rápidos. O cobre em excesso pode originar leucemia e câncer do intestino, embora sua falta possa levar a doenças respiratórias, as panelas deste metal devem ser revestidas com uma camada protetora de titânio. Até mesmo revestimentos de níquel ou de material antiaderente apresentam riscos para saúde. De um modo geral, as panelas de ferro fundido são as melhores para a saúde, pois liberam o nutriente na comida e ajudam a suprir as necessidades do organismo, mas não são boas para quem tem colesterol alto. As panelas de INOX são bastante seguras, porque o material não se oxida e não libera o metal na comida, dizem alguns pesquisadores. (Adaptado de O Globo, 14/10/2011) Dos metais de transição citados no texto, o que mais facilmente forma cátions é o: a) alumínio. b) cobre. c) ferro. d) níquel. e) titânio.
3 5. (PUC-RJ/2012) Os átomos de um elemento químico possuem a seguinte distribuição de elétrons em subníveis e níveis, em torno do núcleo: 8. (IFSP/2013) Considere a tabela abaixo, que fornece características de cinco átomos (I, II, III, IV e V). 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 3 A localização do elemento (período e grupo) na tabela periódica é: a) terceiro período, grupo 9 ou 8B. b) quarto período, grupo 13 ou 13A. c) quarto período, grupo 10 ou 7B. d) quinto período, grupo 13 ou 3A. e) quinto período, grupo 15 ou 5A. 6. (FCM MG/2012) Observe as duas configurações eletrônicas abaixo: I. 1s 2 2s 2 2p 6 3s 1 II. 1s 2 2s 2 2p 6 6s 1 Assinale a alternativa INCORRETA: a) a configuração I representa o átomo de sódio em seu estado fundamental. b) as configurações I e II representam átomos de elementos químicos diferentes. C) é necessário fornecer energia para obter a configuração II, a partir da configuração I. d) é necessário fornecer menos energia para remover um elétron da configuração II do que da I. 7. (FAVIP PE/2012) O cálcio é o elemento da rigidez e da construção: é o cátion dos ossos do nosso esqueleto, das conchas dos moluscos, do concreto, da argamassa e da pedra calcária das nossas construções. Sabendo que o átomo de cálcio tem número atômico 20 e número de massa 40, é correto afirmar que o cátion Ca 2+ tem: a) 18 prótons. b) 18 nêutrons. c) 20 elétrons. d) configuração eletrônica igual à do íon K + (Z = 19). e) configuração eletrônica 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2. São isótopos entre si os átomos a) I e II. b) II e III. c) I, II e III. d) III e IV. e) IV e V. 9. (MACK SP/2013) Sabendo-se que dois elementos químicos e são isóbaros, é correto afirmar que o número de nêutrons de A e o número atômico de B são, respectivamente, a) 15 e 32. b) 32 e 16. c) 15 e 17. d) 20 e 18. e) 17 e (UEPG PR/2013) Considerando os elementos químicos representados por 19 A 42, 19 B 40 e 21 C 42, assinale o que for correto. 01. Os elementos A e B são isótopos. 02. Os elementos A e C são isóbaros. 04. Os elementos B e C são isótonos. 08. O elemento A é o que possui maior número de nêutrons no núcleo.
4 11. (UERJ/2013) A descoberta dos isótopos foi de grande importância para o conhecimento da estrutura atômica da matéria. Sabe-se, hoje, que os isótopos 54 Fe e 56 Fe têm, respectivamente, 28 e 30 nêutrons. A razão entre as cargas elétricas dos núcleos dos isótopos 54 Fe e 56 Fe é igual a: a) 0,5. b) 1,0. c)1,5. d) 2, (FGV SP/2012) A tabela seguinte apresenta dados referentes às espécies K, K +, Ca 2+ e S (UDESC SC/2012) Assinale a alternativa correta. Os isótopos são átomos: a) de um mesmo elemento químico, apresentam propriedades químicas praticamente idênticas, mas têm um número diferente de nêutrons no seu núcleo. b) que têm o mesmo número de prótons e um número diferente de nêutrons no seu núcleo, apresentando propriedades químicas totalmente distintas. c) de um mesmo elemento químico, apresentam propriedades químicas idênticas, mas têm um número diferente de prótons no seu núcleo. d) de elementos químicos diferentes, com o mesmo número de nêutrons no seu núcleo e apresentam propriedades químicas semelhantes. Em relação a essas espécies, são feitas as seguintes afirmações: I. K + e Ca 2+ são isótonos; II. K e Ca 2+ são isóbaros; III. K + tem mais prótons que K; IV. K + e S 2 têm o mesmo número de elétrons. É correto apenas o que se afirma em a) I e II. b) I e III. c) I e IV. d) II e III. e) II e IV. 13. (UEM PR/2012) Considerando os elementos químicos Mendelévio, Férmio e Einstênio, conforme abaixo, assinale o que for correto. e) de elementos químicos diferentes, apresentam propriedades químicas distintas, mas têm o mesmo número de nêutrons no seu núcleo. 15. (IME RJ/2013) Os trabalhos de Joseph John Thomson e Ernest Rutherford resultaram em importantes contribuições na história da evolução dos modelos atômicos e no estudo de fenômenos relacionados à matéria. Das alternativas abaixo, aquela que apresenta corretamente o autor e uma de suas contribuições é: a) Thomson Concluiu que o átomo e suas partículas formam um modelo semelhante ao sistema solar. b) Thomson Constatou a indivisibilidade do átomo. 01. O íon Md 1+ é isótopo do elemento Fm. 02. O elemento Es é isótono do elemento Md. 04. O íon Es 2 possui 101 elétrons. 08. O elemento Fm é isóbaro do íon Es O elemento Md possui massa maior do que o elemento Fm devido ao maior número de nêutrons do Md. c) Rutherford Pela primeira vez, constatou a natureza elétrica da matéria. d) Thomson A partir de experimentos com raios catódicos, comprovou a existência de partículas subatômicas. e) Rutherford Reconheceu a existência das partículas nucleares sem carga elétrica, denominadas nêutrons.
5 16. (UFG GO/2013) Em um determinado momento histórico, o modelo atômico vigente e que explicava parte da constituição da matéria considerava que o átomo era composto de um núcleo com carga positiva. Ao redor deste, haviam partículas negativas uniformemente distribuídas. A experiência investigativa que levou à proposição desse modelo foi aquela na qual a) realizou-se uma série de descargas elétricas em tubos de gases rarefeitos. b) determinou-se as leis ponderais das combinações químicas. c) analisou-se espectros atômicos com emissão de luz com cores características para cada elemento. d) caracterizou-se estudos sobre radioatividade e dispersão e reflexão de partículas alfa. e) providenciou-se a resolução de uma equação para determinação dos níveis de energia da camada eletrônica. 17. (ITA SP/2013) Um átomo A com n elétrons, após (n 1) sucessivas ionizações, foi novamente ionizado de acordo com a equação: A (n 1)+ A n+ + 1e Sabendo o valor experimental da energia de ionização deste processo, pode-se conhecer o átomo A utilizando o modelo proposto por a) E. Rutherford. b) J. Dalton. c) J. Thomson. d) N. Bohr. e) R. Mulliken. 18. (UFGD MS/2013) Até algum tempo atrás, adolescentes colecionavam figurinhas que brilhavam no escuro. Essas figuras apresentam em sua composição uma substância chamada sulfeto de zinco (ZnS). Este fenômeno ocorre porque alguns elétrons que compõe os átomos desta substância absorvem energia luminosa e saltam para níveis de energia mais externos. No escuro, estes elétrons retornam aos seus níveis de origem liberando energia luminosa e fazendo a figurinha brilhar. Este fenômeno pode ser explicado considerando o modelo atômico proposto por a) Thomson. b) Dalton. c) Lavoisier. d) Bohr. e) Linus Pauling. 19. (UFRN/2013) O Diodo Emissor de Luz (LED) é um dispositivo eletrônico capaz de emitir luz visível e tem sido utilizado nas mais variadas aplicações. A mais recente é sua utilização na iluminação de ambientes devido ao seu baixo consumo de energia e à sua grande durabilidade. Atualmente, dispomos de tecnologia capaz de produzir tais dispositivos para emissão de luz em diversas cores, como, por exemplo, a cor vermelha de comprimento de onda, λv, igual a 629 nm, e a cor azul, de comprimento de onda, λa, igual a 469 nm. A energia, E, dos fótons emitidos por cada um dos LEDs é determinada a partir da equação de Einstein E = hf onde h é a constante de Planck, e f é a frequência do fóton emitido. Sabendo ainda que c = λf, onde c é a velocidade da luz no vácuo e λ, o comprimento de onda do fóton, é correto afirmar que a) o fóton correspondente à cor vermelha tem menos energia que o fóton correspondente à cor azul, pois sua frequência é menor que a do fóton de cor azul. b) o fóton correspondente à cor vermelha tem mais energia que o fóton correspondente à cor azul, pois sua frequência é maior que a do fóton de cor azul. c) o fóton correspondente à cor azul tem menos energia que o fóton correspondente à cor vermelha, pois seu comprimento de onda é maior que o do fóton de cor vermelha. d) o fóton correspondente à cor vermelha tem mais energia que o fóton correspondente à cor azul, pois seu comprimento de onda é menor que a do fóton de cor azul.
6 20. (PUC RS/2012) Leia o texto a seguir. A aceitação histórica da ideia de que a matéria é composta de átomos foi lenta e gradual. Na Grécia antiga, Leucipo e Demócrito são lembrados por terem introduzido o conceito de átomo, mas suas propostas foram rejeitadas por outros filósofos e caíram no esquecimento. No final do século XVIII e início do século XIX, quando as ideias de Lavoisier ganhavam aceitação generalizada, surgiu a primeira teoria atômica moderna, proposta por. Essa teoria postulava que os elementos eram constituídos de um único tipo de átomo, enquanto que as substâncias compostas eram combinações de diferentes átomos segundo proporções determinadas. Quase cem anos depois, estudos com raios catódicos levaram J. J. Thomson à descoberta do, uma partícula de massa muito pequena e carga elétrica, presente em todos os materiais conhecidos. Alguns anos depois, por meio de experimentos em que uma fina folha de ouro foi bombardeada com partículas alfa, Rutherford chegou à conclusão de que o átomo possui em seu centro um pequeno, porém de massa considerável. As palavras que preenchem as lacunas correta e res pectivamente estão reunidas em a) Dalton elétron negativa núcleo b) Bohr cátion positiva elétron c) Dalton nêutron neutra próton d) Bohr fóton negativa ânion e) Dalton próton positiva núcleo GABARITO: 1B; 2D; 3C; 4E; 5E; 6B; 7D; 8A; 9E; 10(15); 11B; 12C; 13(04); 14A; 15D; 16D; 17D; 18D; 19A; 20A.
LISTA DE EXERCÍCIO DE QUÍMICA II BIMESTRE
 LISTA DE EXERCÍCIO DE QUÍMICA II BIMESTRE - O átomo constituído de prótons, 2 nêutrons e elétrons apresenta, respectivamente, número atômico e número de massa iguais a : a) e b) 2 e c) 23 e d) e 2 e) e
LISTA DE EXERCÍCIO DE QUÍMICA II BIMESTRE - O átomo constituído de prótons, 2 nêutrons e elétrons apresenta, respectivamente, número atômico e número de massa iguais a : a) e b) 2 e c) 23 e d) e 2 e) e
1. O modelo atômico de Rutherford é também conhecido como modelo planetário do átomo.
 2º Trimestre_8AB_2014_REVISÃO_Química_Prof.ª Caroline Oliveira Nome: Turma: 8 Data: / /2014. 1- Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford
2º Trimestre_8AB_2014_REVISÃO_Química_Prof.ª Caroline Oliveira Nome: Turma: 8 Data: / /2014. 1- Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford
1º Trimestre Sala de Estudos-Química Data: 13/03/17 Ensino Médio 1º ano classe: A_B_C Profª Danusa Nome: nº
 º Trimestre Sala de Estudos-Química Data: 3/03/7 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Estrutura atômica e Configuração Eletrônica Questão 0 - (PUC- RS) Ao se deixar cair sal
º Trimestre Sala de Estudos-Química Data: 3/03/7 Ensino Médio º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Estrutura atômica e Configuração Eletrônica Questão 0 - (PUC- RS) Ao se deixar cair sal
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito)
 SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
QUÍMICA GERAL PROF. PAULO VALIM
 QUÍMICA GERAL PROF. PAULO VALIM 2 O ÁTOMO Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos exercícios
QUÍMICA GERAL PROF. PAULO VALIM 2 O ÁTOMO Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos exercícios
SOLUÇÃO ALUNO PRATIQUE EM CASA
 SOLUÇÃO AR1. [E] [F] X é um metal e possui 1 elétron na camada de valência, pois a primeira energia de ionização (50kJ mol) é baixa comparada com a segunda (7.97kJ mol) e com a terceira (11.810 kj mol).
SOLUÇÃO AR1. [E] [F] X é um metal e possui 1 elétron na camada de valência, pois a primeira energia de ionização (50kJ mol) é baixa comparada com a segunda (7.97kJ mol) e com a terceira (11.810 kj mol).
- Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil.
 - Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil www.profkemil.ning.com EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade sobre do que era constituída a matéria parecia
- Evolução dos modelos atômicos; - Estudo da eletrosfera; Prof. Kemil www.profkemil.ning.com EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade sobre do que era constituída a matéria parecia
Exercícios de atomística
 DISCIPLINA PROFESSOR QUÍMICA REVISADA DATA (rubrica) ARMANDO 2017 NOME Nº ANO TURMA ENSINO 1º MÉDIO Exercícios de atomística 1. (ITA) Em 1808, John Dalton propôs um modelo de teoria atômica. Considere
DISCIPLINA PROFESSOR QUÍMICA REVISADA DATA (rubrica) ARMANDO 2017 NOME Nº ANO TURMA ENSINO 1º MÉDIO Exercícios de atomística 1. (ITA) Em 1808, John Dalton propôs um modelo de teoria atômica. Considere
Sendo o cálcio pertencente ao grupo dos alcalinos terrosos e possuindo número atômico Z = 20, a configuração eletrônica do seu cátion bivalente é:
 1- (U.F.Uberlândia-MG\Pales) Dalton, Thomson, Rutherford e Bohr são cientistas que contribuíram, significativamente, para o desenvolvimento da teoria atômica. Em relação a estrutura atômica, assinale com(v)
1- (U.F.Uberlândia-MG\Pales) Dalton, Thomson, Rutherford e Bohr são cientistas que contribuíram, significativamente, para o desenvolvimento da teoria atômica. Em relação a estrutura atômica, assinale com(v)
ock shutterst / A lsk ska A Agnieszk Química a
 Química A Agnieszka Skalska / Shutterstock Química A aula. (UFJF-MG, adaptada) Associe a coluna da esquerda, que descreve os modelos atômicos, com a da direita, onde se encontram os cientistas que os propuseram.
Química A Agnieszka Skalska / Shutterstock Química A aula. (UFJF-MG, adaptada) Associe a coluna da esquerda, que descreve os modelos atômicos, com a da direita, onde se encontram os cientistas que os propuseram.
Resoluções. Estrutura atômica
 Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 1 Estrutura atômica 1. A A composição metafísica presente no poema remete aos modelos atômicos propostos
Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 1 Estrutura atômica 1. A A composição metafísica presente no poema remete aos modelos atômicos propostos
Átomo. Modelos atômicos e propriedades
 Átomo Modelos atômicos e propriedades O ÁTOMO CONCEITO: Aprox. 500 AC Demócrito e outros filósofos gregos desenvolveram o conceito de átomo A matéria poderia ser dividida progressivamente até chegar à
Átomo Modelos atômicos e propriedades O ÁTOMO CONCEITO: Aprox. 500 AC Demócrito e outros filósofos gregos desenvolveram o conceito de átomo A matéria poderia ser dividida progressivamente até chegar à
QUÍMICA GERAL I PROF. PRISCILA BONFIM GONÇALVES
 Exercícios 1. Sobre os modelos atômicos, assinale o que for incorreto. 01) O modelo que suscitou a ideia do átomo constituído de duas regiões distintas foi proposto pelo químico francês John Dalton, no
Exercícios 1. Sobre os modelos atômicos, assinale o que for incorreto. 01) O modelo que suscitou a ideia do átomo constituído de duas regiões distintas foi proposto pelo químico francês John Dalton, no
ATOMÍSTICA PROF. ADRIANO ALVES
 ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
Lista de exercícios Aulas 03 e 04. 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em:
 Lista de exercícios Aulas 03 e 04 Prof. Fernanda Dias 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em: a) a formação dos materiais dá-se através de diferentes associações entre
Lista de exercícios Aulas 03 e 04 Prof. Fernanda Dias 1) (PUC-SP) A teoria atômica de Dalton só não está claramente expressa em: a) a formação dos materiais dá-se através de diferentes associações entre
QUÍMICA - 1 o ANO MÓDULO 03 MODELOS ATÔMICOS
 QUÍMICA - 1 o ANO MÓDULO 03 MODELOS ATÔMICOS - cátodo + ânodo bomba de vácuo A - cátodo + ânodo bomba de vácuo - cátodo + ânodo campo elétrico alta voltagem cátodo - + + - + - -- - ânodo - bloco de chumbo
QUÍMICA - 1 o ANO MÓDULO 03 MODELOS ATÔMICOS - cátodo + ânodo bomba de vácuo A - cátodo + ânodo bomba de vácuo - cátodo + ânodo campo elétrico alta voltagem cátodo - + + - + - -- - ânodo - bloco de chumbo
ESTRUTURA ATÔMICA. 4. (UEM-PR) Assinale o que for correto. 5. (UFPE) Entre as seguintes espécies nucleares
 ESTRUTURA ATÔMICA 1. (UEM-PR) Assinale o que for correto. 01. A configuração eletrônica s p 6 s p 6 4s pode representar um átomo no estado fundamental cujo número atômico é 0. 0. O átomo de manganês, 5
ESTRUTURA ATÔMICA 1. (UEM-PR) Assinale o que for correto. 01. A configuração eletrônica s p 6 s p 6 4s pode representar um átomo no estado fundamental cujo número atômico é 0. 0. O átomo de manganês, 5
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica
 Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
TEORIAS ATÔMICAS. Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807)
 TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
QUESTÕES DE FÍSICA MODERNA
 QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
LOGO. Modelos Atômicos. Profa. Núria Galacini
 LOGO Modelos Atômicos Profa. Núria Galacini Demócrito: no século IV a.c. afirmava que a matéria era composta de partículas indivisíveis, o átomo. John Dalton: em 1808 formulou uma definição acerca dos
LOGO Modelos Atômicos Profa. Núria Galacini Demócrito: no século IV a.c. afirmava que a matéria era composta de partículas indivisíveis, o átomo. John Dalton: em 1808 formulou uma definição acerca dos
CONCEITOS FUNDAMENTAIS
 CONCEITOS FUNDAMENTAIS EXERCÍCIOS DE APLICAÇÃO 01 (UNIRIO-RJ) O átomo X é isóbaro do 40 Ca e isótopo do 36 Ar. Assinale o número de nêutrons do átomo X. Dados: Número atômicos: Ar = 18; Ca = 20 a) 4 b)
CONCEITOS FUNDAMENTAIS EXERCÍCIOS DE APLICAÇÃO 01 (UNIRIO-RJ) O átomo X é isóbaro do 40 Ca e isótopo do 36 Ar. Assinale o número de nêutrons do átomo X. Dados: Número atômicos: Ar = 18; Ca = 20 a) 4 b)
Exercícios: Estrutura Atômica Professora: Miriam 1ª série. E.M. Química. Aluno 1 Aluno 2 Aluno 3. Unidade de S.B.C
 Química Unidade de S.B.C 1 Exercícios: Estrutura Atômica Professora: Miriam 1ª série. E.M 1- O entendimento dos fenômenos que nos cercam continua sendo uma das grandes preocupações dos seres humanos, para
Química Unidade de S.B.C 1 Exercícios: Estrutura Atômica Professora: Miriam 1ª série. E.M 1- O entendimento dos fenômenos que nos cercam continua sendo uma das grandes preocupações dos seres humanos, para
Sendo o número atômico (Z) do chumbo igual a 82, o íon plumboso (Pb +2 ) possui os elétrons mais energéticos no subnível
 Questão 01) O chumbo é um metal pesado que pode contaminar o ar, o solo, os rios e alimentos. A absorção de quantidades pequenas de chumbo por longos períodos pode levar a uma toxicidade crônica, que se
Questão 01) O chumbo é um metal pesado que pode contaminar o ar, o solo, os rios e alimentos. A absorção de quantidades pequenas de chumbo por longos períodos pode levar a uma toxicidade crônica, que se
Química A Semiextensivo V. 1
 Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
Química A Semiextensivo V. 1 Exercícios 01) D 02) A a) Errada. A teoria de Dalton não incluía partículas ou cargas elétricas (modelo de bola de bilhar). b) Errada. Essa descrição corresponde à teoria de
APOSTILA DE QUÍMICA 2º BIMESTRE
 Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
ESTRUTURA ATÔMICA A EVOLUÇÃO DOS MODELOS ATÔMICOS
 ESTRUTURA ATÔMICA A EVOLUÇÃO DOS MODELOS ATÔMICOS Demócrito Defendeu a idéia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição
ESTRUTURA ATÔMICA A EVOLUÇÃO DOS MODELOS ATÔMICOS Demócrito Defendeu a idéia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição
ESTRUTURA ATÔMICA. Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14
 ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
O que é um modelo atômico?
 O que é um modelo atômico? É uma tentativa de ilustrar o átomo. Sendo o átomo a menor estrutura da matéria, se entendermos o átomo, entenderemos melhor o mundo. Importância - explicar os fenômenos, entender
O que é um modelo atômico? É uma tentativa de ilustrar o átomo. Sendo o átomo a menor estrutura da matéria, se entendermos o átomo, entenderemos melhor o mundo. Importância - explicar os fenômenos, entender
1º trimestre Trabalho de Recuperação Data: 28/04/17 Ensino Médio 1º ano classe: A_B_C Profª Danusa Nome: nº
 1º trimestre Trabalho de Recuperação Data: 28/04/17 Ensino Médio 1º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Atomística, Distribuição Eletrônica e Tabela Periódica *Entregar todos os exercícios
1º trimestre Trabalho de Recuperação Data: 28/04/17 Ensino Médio 1º ano classe: A_B_C Profª Danusa Nome: nº Conteúdo: Atomística, Distribuição Eletrônica e Tabela Periódica *Entregar todos os exercícios
ESTRUTURA ATÔMICA. As partículas do átomo
 QUÍMICA M.2 ESTRUTURA ATÔMICA As partículas do átomo Multimídia 1803 - Dalton (Inglês) A partir de experimentos com gases. Dalton propõe uma hipótese atômica. Segundo ele, os átomos são: Indivisíveis Maciços
QUÍMICA M.2 ESTRUTURA ATÔMICA As partículas do átomo Multimídia 1803 - Dalton (Inglês) A partir de experimentos com gases. Dalton propõe uma hipótese atômica. Segundo ele, os átomos são: Indivisíveis Maciços
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Qímica Estrutura At mica
 Q ímica Estrutura At mica MODELOS ATÔMICOS Modelo dos Filósofos Gregos: Leucipo (500 a.c.) e Demócrito (460 a.c.) Indestrutível, indivisível e maciço. Modelo baseado apenas na intuição e na lógica. Aristóteles
Q ímica Estrutura At mica MODELOS ATÔMICOS Modelo dos Filósofos Gregos: Leucipo (500 a.c.) e Demócrito (460 a.c.) Indestrutível, indivisível e maciço. Modelo baseado apenas na intuição e na lógica. Aristóteles
QUÍMICA ÁTOMOS. Professor: Rafael Odorico
 QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
QUÍMICA ÁTOMOS MODELO DE DALTON A matéria é formada por partículas extremamente pequenas chamadas átomos; Os átomos são esferas maciças e indivisíveis; Os átomos com as mesmas propriedades, constituem
Química Professor Ricardo Júnior
 Questão 01 - (UEA AM/2017) Química Professor Ricardo Júnior Frequentemente, ouve-se falar no método de datação por carbono-14 para estimar a idade de fósseis. O número 14 corresponde ao número de ---------------
Questão 01 - (UEA AM/2017) Química Professor Ricardo Júnior Frequentemente, ouve-se falar no método de datação por carbono-14 para estimar a idade de fósseis. O número 14 corresponde ao número de ---------------
DISTRIBUIÇÃO ELETRÔNICA
 DISTRIBUIÇÃO ELETRÔNICA Profª. Regina Modesto Raszl Um problema para os químicos era construir uma teoria consistente que explicasse como os elétrons se distribuíam ao redor dos átomos, dando-lhes as características
DISTRIBUIÇÃO ELETRÔNICA Profª. Regina Modesto Raszl Um problema para os químicos era construir uma teoria consistente que explicasse como os elétrons se distribuíam ao redor dos átomos, dando-lhes as características
LISTA DE ATIVIDADES TAREFÃO
 LISTA DE ATIVIDADES TAREFÃO ALUNO(a): TURMA: Valor: 0-2 pontos PROFESSOR(a): DATA: / / A lista de exercícios deste tarefão estão relacionadas aos seguintes conteúdos: Capitulo 03 Modelos atômicos e suas
LISTA DE ATIVIDADES TAREFÃO ALUNO(a): TURMA: Valor: 0-2 pontos PROFESSOR(a): DATA: / / A lista de exercícios deste tarefão estão relacionadas aos seguintes conteúdos: Capitulo 03 Modelos atômicos e suas
LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON
 LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e)
LISTA DE EXERCÍCIOS QUÍMICA 8ª SÉRIE Prof MAICON 01) Na tabela periódica os elementos estão ordenados em ordem crescente de: a) Número de massa. b) Massa atômica. c) Número atômico. d) Raio atômico. e)
Modelos atômicos. Curso de Química. Prof. Rui Medeiros. quimicadorui.com.br
 Modelos atômicos Curso de Química Prof. Rui Medeiros quimicadorui.com.br Módulo Extra - 2017 2 CURSO DE QUÍMICA PROFESSOR RUI MEDEIROS MÓDULO EXTRA - 2017 Modelos atômicos ü A representação esquemática
Modelos atômicos Curso de Química Prof. Rui Medeiros quimicadorui.com.br Módulo Extra - 2017 2 CURSO DE QUÍMICA PROFESSOR RUI MEDEIROS MÓDULO EXTRA - 2017 Modelos atômicos ü A representação esquemática
LISTA DE EXERCÍCIOS 9º ANO PRÉ-COLUNI PROF. LUCÃO QUÍMICA (Ciências da Natureza e suas Tecnologias)
 LISTA DE EXERCÍCIOS 9º ANO PRÉ-COLUNI PROF. LUCÃO QUÍMICA (Ciências da Natureza e suas Tecnologias) ESTUDO DA COMPOSIÇÃO DO ÁTOMO ATOMÍSTICA: Teorias Atômicas, Partículas Fundamentais e Relações Atômicas.
LISTA DE EXERCÍCIOS 9º ANO PRÉ-COLUNI PROF. LUCÃO QUÍMICA (Ciências da Natureza e suas Tecnologias) ESTUDO DA COMPOSIÇÃO DO ÁTOMO ATOMÍSTICA: Teorias Atômicas, Partículas Fundamentais e Relações Atômicas.
Estrutura Atômica. Atomística.
 Estrutura Atômica Atomística. Democrito e Leucipo (450 a. C) Átomo Dalton (séc. XIX) Bola de Bilhar Thomson (séc. XIX) Pudim de passas Rutherford (séc. XX) sistema solar Átomos núcleo prótons (+1) eletrosfera
Estrutura Atômica Atomística. Democrito e Leucipo (450 a. C) Átomo Dalton (séc. XIX) Bola de Bilhar Thomson (séc. XIX) Pudim de passas Rutherford (séc. XX) sistema solar Átomos núcleo prótons (+1) eletrosfera
Mg e Fe. Com base nas afirmações acima assinale a alternativa correta. a) Esses elementos são representados por 286Nh, 288Mc, 294Ts e 188
 1. (G1 - ifsul 2017) Um ânion de carga 1 possui 18 elétrons e 20 nêutrons. O átomo neutro que o originou apresenta número atômico e de massa, respectivamente, a) 17 e 37 b) 17 e 38 c) 19 e 37 d) 19 e 38
1. (G1 - ifsul 2017) Um ânion de carga 1 possui 18 elétrons e 20 nêutrons. O átomo neutro que o originou apresenta número atômico e de massa, respectivamente, a) 17 e 37 b) 17 e 38 c) 19 e 37 d) 19 e 38
LISTA DE EXERCÍCIO PARA A PROVA MENSAL
 Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Química. Aula 04 Profº Ricardo Dalla Zanna
 Química Aula 04 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Átomos e Elementos o Seção 2.1 Evolução do modelo atômico e classificação periódica dos elementos o Seção 2.2 Leis ponderais o
Química Aula 04 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Átomos e Elementos o Seção 2.1 Evolução do modelo atômico e classificação periódica dos elementos o Seção 2.2 Leis ponderais o
ATOMÍSTICA. Teoria de Thomson (1898) Todo átomo é formado por uma matéria positiva, na qual se encontrariam os elétrons distribuídos ao acaso.
 1. MODLOS ATÔMICOS Teoria de Dalton (1803): Toda matéria é constituída por átomos; Átomos de um mesmo elemento químico possuem propriedades químicas e físicas iguais; Todo átomo corresponde a uma esfera
1. MODLOS ATÔMICOS Teoria de Dalton (1803): Toda matéria é constituída por átomos; Átomos de um mesmo elemento químico possuem propriedades químicas e físicas iguais; Todo átomo corresponde a uma esfera
Principais Postulados de Dalton (1803)
 Teoria Atômica da Matéria Breve Histórico Leucipo e Demócrito ( 400 a.c.) descontinuidade da matéria (átomo). Alquimia ( 300 a.c. 1500 d.c.) civilizações árabes e gregas. Paracelsus ( 1500 d.c.) Iatroquímica.
Teoria Atômica da Matéria Breve Histórico Leucipo e Demócrito ( 400 a.c.) descontinuidade da matéria (átomo). Alquimia ( 300 a.c. 1500 d.c.) civilizações árabes e gregas. Paracelsus ( 1500 d.c.) Iatroquímica.
Exercícios de Química Estrutura Atômica
 Exercícios de Química Estrutura Atômica 5. Unifor-CE Entre os conjuntos de características abaixo, o que melhor descreve o elétron quando comparado ao próton é: 1. U. Católica-DF Os fogos de artifício
Exercícios de Química Estrutura Atômica 5. Unifor-CE Entre os conjuntos de características abaixo, o que melhor descreve o elétron quando comparado ao próton é: 1. U. Católica-DF Os fogos de artifício
1ª e 2 ª Lista de Exercícios de Química Geral - Estrutura Atômica
 1ª e 2 ª Lista de Exercícios de Química Geral - Estrutura Atômica Prof. Dr. Newton Luiz Dias Filho 1) a) Qual é a frequência de radiação que tem um comprimento de onda de 0,452 pm? b) Qual é o comprimento
1ª e 2 ª Lista de Exercícios de Química Geral - Estrutura Atômica Prof. Dr. Newton Luiz Dias Filho 1) a) Qual é a frequência de radiação que tem um comprimento de onda de 0,452 pm? b) Qual é o comprimento
Átomos, Moléculas e Íons
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Átomos, Moléculas e Íons Química Tecnológica I Prof a. Dr a. Flaviana Tavares Vieira A origem
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Átomos, Moléculas e Íons Química Tecnológica I Prof a. Dr a. Flaviana Tavares Vieira A origem
QUÍMICA GERAL PROF. PAULO VALIM
 QUÍMICA GERAL PROF. PAULO VALIM 4 TABELA PERIÓDICA Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
QUÍMICA GERAL PROF. PAULO VALIM 4 TABELA PERIÓDICA Gás Nobre para catalisar sua reação, vamos disponibilizar alguns exercícios com gabarito ao final de cada capítulo de estudo. Eles não fazem parte dos
MONITORIA_2015 DISCIPLINA: QUÍMICA AULA: EVOLUÇÃO DOS MODELOS ATÔMICOS
 MONITORIA_2015 DISCIPLINA: QUÍMICA AULA: EVOLUÇÃO DOS MODELOS ATÔMICOS LEMBRETES! Olá, galerinha!! (: Eu sou a Lygia, monitora de Química do Descomplica e tenho alguns recadinhos: Dúvidas & material da
MONITORIA_2015 DISCIPLINA: QUÍMICA AULA: EVOLUÇÃO DOS MODELOS ATÔMICOS LEMBRETES! Olá, galerinha!! (: Eu sou a Lygia, monitora de Química do Descomplica e tenho alguns recadinhos: Dúvidas & material da
10) Assinale a alternativa que indica a última distribuição eletrônica em seus respectivos orbitais atômicos do átomo
 1 CECOM TURMA 1º ANO Nº ALUNO(A): QUÍMICA / AVALIAÇÃO SIMULADA 1ºBIM / 2018 DATA / /2018 TEMA: ATOMÍSTICA Prof. Whélynton OBJETIVO: Compreender, visualizar e interpretar do ponto de vista da química (microscopicamente)
1 CECOM TURMA 1º ANO Nº ALUNO(A): QUÍMICA / AVALIAÇÃO SIMULADA 1ºBIM / 2018 DATA / /2018 TEMA: ATOMÍSTICA Prof. Whélynton OBJETIVO: Compreender, visualizar e interpretar do ponto de vista da química (microscopicamente)
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
MODELOS ATÔMICOS Profº Jaison Mattei
 MODELOS ATÔMICOS Profº Jaison Mattei Vamos falar sobre: A evolução do modelo para o átomo; Cientistas importantes para esse estudo; Dalton, Thomson, Rutherford e Bohr; Experimentos realizados para obter
MODELOS ATÔMICOS Profº Jaison Mattei Vamos falar sobre: A evolução do modelo para o átomo; Cientistas importantes para esse estudo; Dalton, Thomson, Rutherford e Bohr; Experimentos realizados para obter
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA
 Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
Em torno do núcleo do átomo temos uma região denominada ELETROSFERA A eletrosfera é dividida em 7 partes chamada CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA Do núcleo para fora estas camadas são representadas
Demócrito. Demócrito a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos.
 Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Atomística Demócrito Demócrito 460-370 a.c. Filósofo grego. A matéria é formada por partículas indivisíveis chamadas átomos. Lavoisier NADA SE PERDE NADA SE CRIA TUDO SE TRANSFORMA Dalton BASEADO NA LEI
Química Geral -Aula 2 Átomo e estrutura atômica. *Mas afinal, de que são feitas as coisas?
 Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
Química Geral -Aula 2 Átomo e estrutura atômica *Mas afinal, de que são feitas as coisas? Átomo na Grécia antiga 2 teorias (Demócrito, Leucipo e Aristóteles) Demócrito, Leucipo e Aristóteles Átomo como
ESTRUTURA ATÔMICA. Modelos Atômicos
 ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
ESTRUTURA ATÔMICA Modelos Atômicos 1.Modelo atômico de Dalton 2.Modelo atômico de Thomson 3.Modelo atômico de Rutherford 4.Modelo atômico de Rutherford-Bohr 5.Modelo atômico atual MODELOS ATÔMICOS 1808
Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica
 Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um
Aula 12- Íons, níveis e subníveis eletrônicos e a distribuição eletrônica Nas nossas aulas passadas nós vimos que cada elemento químico é caracterizado pelo seu número atômico (Z). Vimos também que um
Curso Semi-extensivo LISTA EXERCÍCIOS - 05 Disciplina: Química Professor: Eduar Fernando Rosso
 Curso Semi-extensivo LISTA EXERCÍCIOS - 05 Disciplina: Química Professor: Eduar Fernando Rosso ESTRUTURA ATÔMICA 01 (Ufpr 017) As propriedades das substâncias químicas podem ser previstas a partir das
Curso Semi-extensivo LISTA EXERCÍCIOS - 05 Disciplina: Química Professor: Eduar Fernando Rosso ESTRUTURA ATÔMICA 01 (Ufpr 017) As propriedades das substâncias químicas podem ser previstas a partir das
04) (FGV-SP) As figuras representam alguns experimentos de raios catódicos realizados no início do século passado, no estudo da estrutura atômica.
 01) (FMTM-MG) De acordo com o modelo atômico proposto por Rutherford, os átomos são constituídos por um núcleo de carga elétrica positiva, que concentra quase toda a massa do átomo, onde estão os prótons,
01) (FMTM-MG) De acordo com o modelo atômico proposto por Rutherford, os átomos são constituídos por um núcleo de carga elétrica positiva, que concentra quase toda a massa do átomo, onde estão os prótons,
Pré UFSC Química. Somatório: Somatório:
 Exercícios 1) Uma das principais partículas atômicas é o elétron. Sua descoberta foi efetuada por J. J. Thomson em uma sala do Laboratório Cavendish, na Inglaterra, ao provocar descargas de elevada voltagem
Exercícios 1) Uma das principais partículas atômicas é o elétron. Sua descoberta foi efetuada por J. J. Thomson em uma sala do Laboratório Cavendish, na Inglaterra, ao provocar descargas de elevada voltagem
5) (PUC MG/2006) - O modelo atômico de Rutherford NÃO inclui especificamente: a) nêutrons. b) núcleo. c) próton. d) elétron. Ver resposta!
 Exercícios de Química Setor A Professora- Juliana 1) (Puc - RS) - O átomo, na visão de Thomson, é constituído de a) níveis e subníveis de energia. b) cargas positivas e negativas. c) núcleo e eletrosfera.
Exercícios de Química Setor A Professora- Juliana 1) (Puc - RS) - O átomo, na visão de Thomson, é constituído de a) níveis e subníveis de energia. b) cargas positivas e negativas. c) núcleo e eletrosfera.
3º EM. Química A Jaque / Lailson Aval. Mensal 06/03/13. Para efeitos de consulta, se necessário, utilize a tabela periódica abaixo:
 3º EM Química A Jaque / Lailson Aval. Mensal 06/03/13 Para efeitos de consulta, se necessário, utilize a tabela periódica abaixo: 1. (1,0) Tendo por base o modelo atômico atual, assinale (V) para verdadeiro
3º EM Química A Jaque / Lailson Aval. Mensal 06/03/13 Para efeitos de consulta, se necessário, utilize a tabela periódica abaixo: 1. (1,0) Tendo por base o modelo atômico atual, assinale (V) para verdadeiro
1
 EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade do que era constituída a matéria parecia ser impossível de ser desvendada. Até que em 450 a.c. o filósofo grego Leucipo de Mileto afirmava
EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade do que era constituída a matéria parecia ser impossível de ser desvendada. Até que em 450 a.c. o filósofo grego Leucipo de Mileto afirmava
QUÍMICA GERAL Cap. 01. Prof. Kristian Sales Vieira
 QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
QUÍMICA GERAL Cap. 01 Prof. Kristian Sales Vieira Modelo atômico O processo de descoberta Grécia século V a.c. Empédocles Explicar a constituição da matéria ; 04 Elementos: fogo, ar, água e terra; Constante
Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular
 Colégio Drummond Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular MATERIAL DE QUÍMICA PROF.: CARLINHOS CURSINHO 2+ efeito estufa é o monóxido de carbono CO2, este é liberado principalmente
Colégio Drummond Educação Infantil, Ensino Fundamental, Médio e Pré- Vestibular MATERIAL DE QUÍMICA PROF.: CARLINHOS CURSINHO 2+ efeito estufa é o monóxido de carbono CO2, este é liberado principalmente
Coluna II ( ) Rutherford ( ) Thomson ( ) Hund ( ) Bohr ( ) Heisenberg
 Lista de Química P2 1 Ano Professora: Núbia de Andrade Aluno: 01 - (UFPR) Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford é também conhecido como
Lista de Química P2 1 Ano Professora: Núbia de Andrade Aluno: 01 - (UFPR) Considere as seguintes afirmativas sobre o modelo atômico de Rutherford: 1. O modelo atômico de Rutherford é também conhecido como
LISTA DE EXERCÍCIOS - 1.4: LEIS PONDERAIS E MODELOS ATÔMICOS. 1 São anotados os seguintes valores nas experiências I, II e III
 LISTA DE EXERCÍCIOS - 1.4: LEIS PONDERAIS E MODELOS ATÔMICOS 1 São anotados os seguintes valores nas experiências I, II e III Determine os valores de x, y, z, w e k mencionando a(s) Lei(s) empregadas nestas
LISTA DE EXERCÍCIOS - 1.4: LEIS PONDERAIS E MODELOS ATÔMICOS 1 São anotados os seguintes valores nas experiências I, II e III Determine os valores de x, y, z, w e k mencionando a(s) Lei(s) empregadas nestas
Terceira aula de química
 Terceira aula de química Nome: Laísa 24/04/2017 O modelo atômico de Thomson Foi proposta em 1898 pelo físico inglês Joseph John Thomson. Ele derrubou a teoria da indivisibilidade do átomo proposta por
Terceira aula de química Nome: Laísa 24/04/2017 O modelo atômico de Thomson Foi proposta em 1898 pelo físico inglês Joseph John Thomson. Ele derrubou a teoria da indivisibilidade do átomo proposta por
Avaliação da unidade II Pontuação: 7,5 pontos
 Avaliação da unidade II Pontuação: 7,5 pontos 2 QUESTÃO 01 (Ufg) Leia o poema apresentado a seguir. 3 Pudim de passas Campo de futebol Bolinhas se chocando Os planetas do sistema solar Átomos Às vezes
Avaliação da unidade II Pontuação: 7,5 pontos 2 QUESTÃO 01 (Ufg) Leia o poema apresentado a seguir. 3 Pudim de passas Campo de futebol Bolinhas se chocando Os planetas do sistema solar Átomos Às vezes
QUÍMICA. Transformações Químicas. Teoria Atômica Modelo Atômico de Dalton, Thomson, Rutherford, Rutherford-Bohr Parte 2. Prof a.
 QUÍMICA Transformações Químicas Teoria Atômica Modelo Atômico de Dalton, Thomson, Parte 2 Prof a. Giselle Blois Problemas com o átomo de Rutherford: Teoria Atômica: Modelo Atômico de Dalton, Thomson, -
QUÍMICA Transformações Químicas Teoria Atômica Modelo Atômico de Dalton, Thomson, Parte 2 Prof a. Giselle Blois Problemas com o átomo de Rutherford: Teoria Atômica: Modelo Atômico de Dalton, Thomson, -
Disciplina: MAF 2130 Química aplicada às engenharias
 Pontifícia Universidade Católica de Goiás Av. Universitária 1.440, Setor Universitário Goiânia-GO, CEP: 74605-010 Fone: +55 62 3946-1000 Disciplina: MAF 2130 Química aplicada às engenharias Prof. Dr. Julio
Pontifícia Universidade Católica de Goiás Av. Universitária 1.440, Setor Universitário Goiânia-GO, CEP: 74605-010 Fone: +55 62 3946-1000 Disciplina: MAF 2130 Química aplicada às engenharias Prof. Dr. Julio
Ciências Exatas UFPR Palotina
 Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 3 Teoria Atômica, Massas Atômicas e Moleculares e Íons Prof. Isac G. Rosset Ciências Exatas UFPR Palotina Prof. Isac G. Rosset
Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 3 Teoria Atômica, Massas Atômicas e Moleculares e Íons Prof. Isac G. Rosset Ciências Exatas UFPR Palotina Prof. Isac G. Rosset
Ciências da Natureza e Matemática
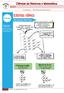 1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 1. Cada átomo possui um certo número de elétrons, que é igual ao valor de seu número atômico (Z). Os elétrons se encontram distribuídos nos
1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 1. Cada átomo possui um certo número de elétrons, que é igual ao valor de seu número atômico (Z). Os elétrons se encontram distribuídos nos
Balanceamento, Modelo Atômico, Tabela Periódica e Ligações Inter atômicas.
 Ciências da Natureza Química Flávia Alves Ramalho Trabalho de Recuperação 1 ano 1ª 10 pts 6,5 pts 05 18 1º A / B Balanceamento, Modelo Atômico, Tabela Periódica e Ligações Inter atômicas. QUESTÃO 01: Sabendo-se
Ciências da Natureza Química Flávia Alves Ramalho Trabalho de Recuperação 1 ano 1ª 10 pts 6,5 pts 05 18 1º A / B Balanceamento, Modelo Atômico, Tabela Periódica e Ligações Inter atômicas. QUESTÃO 01: Sabendo-se
Qui. Semana. Allan Rodrigues Xandão (Renan Micha)
 Semana 4 Allan Rodrigues Xandão (Renan Micha) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Semana 4 Allan Rodrigues Xandão (Renan Micha) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
ESTRUTURA ATÔMICA. Prof. Dr. Cristiano Torres Miranda Disciplina: Química Inorgânica I QM83A Turma Q33
 ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Inorgânica I QM83A Turma Q33 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Inorgânica I QM83A Turma Q33 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
Modelos atômicos. Disciplina: Química Tecnológica Professora: Lukese Rosa Menegussi
 Modelos atômicos Disciplina: Química Tecnológica Professora: Lukese Rosa Menegussi Dalton Lei de Lavoisier Conservação da massa Lei de Proust Proporções constantes Balanceamento Excesso de reagente A natureza
Modelos atômicos Disciplina: Química Tecnológica Professora: Lukese Rosa Menegussi Dalton Lei de Lavoisier Conservação da massa Lei de Proust Proporções constantes Balanceamento Excesso de reagente A natureza
Tarefa 23 Professor Gustavo
 Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
exercícios Sobre a imagem e intensidade das forças intermoleculares,
 Química Marcus Vinícius exercícios 1. (Idecan/CBMMG/CFO/2016) A intensidade das forças intermoleculares em diferentes substâncias varia em uma grande faixa, mas essas forças são muito mais fracas que as
Química Marcus Vinícius exercícios 1. (Idecan/CBMMG/CFO/2016) A intensidade das forças intermoleculares em diferentes substâncias varia em uma grande faixa, mas essas forças são muito mais fracas que as
Colégio dos Santos Anjos Avenida Iraí, 1330 Planalto Paulista A Serviço da Vida por Amor
 Colégio dos Santos Anjos Avenida Iraí, 1330 Planalto Paulista www.colegiosantosanjos.g12.br A Serviço da Vida por Amor Curso: 1º Ensino Médio Nome do (a) Aluno (a): Ano: 2013 Componente Curricular: Química
Colégio dos Santos Anjos Avenida Iraí, 1330 Planalto Paulista www.colegiosantosanjos.g12.br A Serviço da Vida por Amor Curso: 1º Ensino Médio Nome do (a) Aluno (a): Ano: 2013 Componente Curricular: Química
Os modelos Atômicos e a evolução da constituição elembentar da matéria
 Os modelos Atômicos e a evolução da constituição elembentar da matéria Ao longo do desenvolvimento da humanidade, um dos tópicos que sempre intrigaram os filósofos e os cientistas é a composição elementar
Os modelos Atômicos e a evolução da constituição elembentar da matéria Ao longo do desenvolvimento da humanidade, um dos tópicos que sempre intrigaram os filósofos e os cientistas é a composição elementar
Química Geral Aula 2 Notação científica / atomística
 Química Geral Aula 2 Notação científica / atomística Revisão Sistema internacional de unidades (SI) 2 O que é o SI? É um sistema de unidades de medida concebido em torno de sete unidades básicas: Visa
Química Geral Aula 2 Notação científica / atomística Revisão Sistema internacional de unidades (SI) 2 O que é o SI? É um sistema de unidades de medida concebido em torno de sete unidades básicas: Visa
- ATOMÍSTICA Folha 03 João Roberto Mazzei
 01- (UFRJ 2005) Um professor decidiu decorar seu laboratório com um "relógio de Química" no qual, no lugar das horas, estivessem alguns elementos, dispostos de acordo com seus respectivos números atômicos,
01- (UFRJ 2005) Um professor decidiu decorar seu laboratório com um "relógio de Química" no qual, no lugar das horas, estivessem alguns elementos, dispostos de acordo com seus respectivos números atômicos,
ESTRUTURA ATÔMICA (PARTE 1)
 ESTRUTURA ATÔMICA (PARTE 1) 1.01. A experiência de Rutherford permitiu: a) a descoberta do próton; b) a descoberta do nêutron; c) a descoberta do elétron; d) caracterizar que, na maior parte do átomo,
ESTRUTURA ATÔMICA (PARTE 1) 1.01. A experiência de Rutherford permitiu: a) a descoberta do próton; b) a descoberta do nêutron; c) a descoberta do elétron; d) caracterizar que, na maior parte do átomo,
Atomística. Matéria. Sistemas. Órgãos. Tecidos. Células. Moléculas Átomos
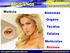 Atomística Matéria Sistemas Órgãos Tecidos Células Moléculas Átomos Atomística Tales de Mileto (640 a.c. e 2610 a.h.): Descobriu as cargas elétricas Empédocles (V a.c. e XXV a.h.) água terra fogo ar Atomística
Atomística Matéria Sistemas Órgãos Tecidos Células Moléculas Átomos Atomística Tales de Mileto (640 a.c. e 2610 a.h.): Descobriu as cargas elétricas Empédocles (V a.c. e XXV a.h.) água terra fogo ar Atomística
Estrutura Atômica. Descrever a estrutura do átomo e definir seus termos fundamentais;
 Estrutura Atômica Objetivos Descrever a estrutura do átomo e definir seus termos fundamentais; Estudar a evolução histórica do modelo atômico para conhecer os fundamentos da Tabela Periódica Átomos e Elementos
Estrutura Atômica Objetivos Descrever a estrutura do átomo e definir seus termos fundamentais; Estudar a evolução histórica do modelo atômico para conhecer os fundamentos da Tabela Periódica Átomos e Elementos
QUÍMICA MODELOS ATÔMICOS, ATOMÍSTICA, CONCEITOS FUNDAMENTAIS, SEMELHANÇA ATÔMICA
 QUÍMICA Prof. Rodrigo Rocha MODELOS ATÔMICOS, ATOMÍSTICA, CONCEITOS FUNDAMENTAIS, SEMELHANÇA ATÔMICA 1. Sobre os principais fundamentos da teoria atômica de Dalton, assinale a(s) alternativa(s) CORRETA(s).
QUÍMICA Prof. Rodrigo Rocha MODELOS ATÔMICOS, ATOMÍSTICA, CONCEITOS FUNDAMENTAIS, SEMELHANÇA ATÔMICA 1. Sobre os principais fundamentos da teoria atômica de Dalton, assinale a(s) alternativa(s) CORRETA(s).
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
Tarefas 13, 14, 15 e 16 Professor Willian
 9º ano Química Tarefas 13, 14, 15 e 16 Professor Willian 1ªsemana 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente
9º ano Química Tarefas 13, 14, 15 e 16 Professor Willian 1ªsemana 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente
PROPRIEDADES DA MATÉRIA
 Química Revisão Aula 2 1 os anos Décio ago/09 Nome: N o : Turma: PROPRIEDADES DA MATÉRIA Objetivo O objetivo dessa ficha é revisar alguns dos tópicos trabalhados no 1º semestre. As dúvidas devem ser encaminhadas
Química Revisão Aula 2 1 os anos Décio ago/09 Nome: N o : Turma: PROPRIEDADES DA MATÉRIA Objetivo O objetivo dessa ficha é revisar alguns dos tópicos trabalhados no 1º semestre. As dúvidas devem ser encaminhadas
NOVOS AVANÇOS NA TEORIA ATÔMICA
 Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da aula: Modelo Atômico de Bohr e Distribuição Eletrônica O desenvolvimento da teoria atômica NOVOS AVANÇOS NA TEORIA ATÔMICA - Ao longo
Disciplina: Química Prof.: Guilherme Turma: IU 20/ 04/2017 Tema da aula: Modelo Atômico de Bohr e Distribuição Eletrônica O desenvolvimento da teoria atômica NOVOS AVANÇOS NA TEORIA ATÔMICA - Ao longo
T.C de Química 1 o ano Prof. Alan Ibiapina
 T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
TEORIA ATÔMICA. Química Geral
 TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
TEORIA ATÔMICA Química Geral 1 Modelo Atômico de Dalton John Dalton 1766 1844: Físico, Químico e Meteorologista inglês Primeira tentativa de relacionar mudanças químicas a eventos que ocorrem ao nível
Estrutura atômica & Classificação periódica
 Estrutura atômica & Classificação periódica Aula de química (20/08) Gabriel e Leonardo Estrutura atômica Modelos Atômicos Modelos Atômicos - Dalton Os átomos são esferas rígidas, indivisíveis e indestrutíveis
Estrutura atômica & Classificação periódica Aula de química (20/08) Gabriel e Leonardo Estrutura atômica Modelos Atômicos Modelos Atômicos - Dalton Os átomos são esferas rígidas, indivisíveis e indestrutíveis
Elétron. Nêutron. Próton COLÉGIO E CURSO
 FERA COLÉGIO E CURSO (83) 34212325 Educar: arte de tecer um futuro de boas escolhas Título: Química elementar Data: / /2016 COLÉGIO E CURSO Série: 3ª série do ensino médio Turma: Aluna(o): Nº: 01 - (ITA
FERA COLÉGIO E CURSO (83) 34212325 Educar: arte de tecer um futuro de boas escolhas Título: Química elementar Data: / /2016 COLÉGIO E CURSO Série: 3ª série do ensino médio Turma: Aluna(o): Nº: 01 - (ITA
