Universidade Federal de São Carlos Centro de Ciências Exatas e de Tecnologia Departamento de Química Programa de Pós-Graduação em Química
|
|
|
- Natan Marcelo Conceição Alencar
- 8 Há anos
- Visualizações:
Transcrição
1 Universidade Federal de São Carlos Centro de Ciências Exatas e de Tecnologia Departamento de Química Programa de Pós-Graduação em Química Estudos de Separação Enantiosseletiva para uma Série de Sulfóxidos Quirais em Colunas Poliméricas. Tiago de Campos Lourenço* Dissertação apresentada ao Programa de Pós-Graduação em Química, como parte dos requisitos para a obtenção do título de Mestre em Química, área de concentração Química Orgânica Orientadora: Prof a. Dra. Quezia B. Cass *Bolsista FAPESP São Carlos SP 2010
2 Ficha catalográfica elaborada pelo DePT da Biblioteca Comunitária da UFSCar L892es Lourenço, Tiago de Campos. Estudos de separação enantiosseletiva para uma série de sulfóxidos quirais em colunas poliméricas / Tiago de Campos Lourenço. -- São Carlos : UFSCar, f. Dissertação (Mestrado) -- Universidade Federal de São Carlos, Análise cromatográfica. 2. Cromatografia quiral. 3. Coluna - cromatografia. 4. Colunas de polissacarídeos. I. Título. CDD: (20 a )
3 UNIVERSIDADE FEDERAL DE SAO CARLOS Centro de Cihcias Exatas e de Tecnologia Departamento de Quimica PROGRAMA DE P~S-GRADUACAO EM QU~MICA Curso de Mestrado Academic0 Assinaturas dos membros da banca examinadbra que avaliaram e aprovaram a defesa de dissertaro de mestrado acadomico do candiidnto Tiago de Campos Louren~o, realkzada em 12 de margo de 2010: Dr. Nelson ~@ira Claro Junior
4 Discovery consists of seeing what everybody has seen and thinking what nobody has thought. Albert Von Szent-Györgyi
5 Dedico esta dissertação à minha família meu pai, José Maria, minha mãe, Ilza e meu irmão, Felipe pelo amor incondicional e incentivo em todos os momentos.
6 À Alice, pelo amor, amizade e companheirismo.
7 Agradecimentos Agradeço, principalmente, a Prof a. Dra. Quezia B. Cass pela orientação, confiança e apoio recebido durante a realização deste trabalho. À Profª. Dra. Regina V. Oliveira e à Dra. Neila M. Cassiano pela amizade e ensinamentos durante o cotidiano. Ao corpo docente, técnico e administrativo do Departamento de Química da Universidade Federal de São Carlos pela oportunidade de realização da parte experimental desta dissertação. A todos os meus amigos do grupo de Síntese Orgânica e CLAE, em especial, a Kenia, a Marcela e a Roberta pelas sugestões durante a realização deste trabalho. Ao meu grande amigo Fernando Gonçalvez de Almeida pela amizade e conselhos. À minha prima e irmã Ana Gabriele. À família Lopes pela confiança e, principalmente, pela amizade. Aos amigos Fernando (Bombinha), Diego (Feio), Rodrigo Smirmaul (Tigrão), Rodrigo Lourenço (Jóia), Felipe Pacheco (Burga), João Volpatto, Alan Escodro e Claudia Rodrigues (Claudinha). Ao Alexandre Augusto Cruz, por sua amizade e disponibilidade para ajudar com os equipamentos. Aos meus amigos dos laboratórios vizinhos de química orgânica, por serem prestativos sempre que necessário. À FAPEPS pela bolsa concedida e pelo suporte financeiro. Ao CNPQ e CAPES pelo suporte financeiro. À todos que de alguma forma colaboraram na realização deste trabalho.
8 Lista de Figuras Introdução Figura Representação do modelo de interação de três pontos 2 Figura Reconhecimento quiral entre os (S)-enantiômeros e do metil N-(2-naftil) alaninato (1) e do N-(3,5-dinitrobenzoil)leucina n-propilamida (2) Figura Estrutura do seletor quiral (NEC-β-CD) 3 9 Figura Fases quirais derivadas de benzil e fenilcarbamatos de celulose e amilose. 1(a): tris(3,5-dimetilfenilcarbamato) de celulose, 2(a): tris(3,5- dimetilfenilcarbamato) de amilose e 2(b): tris[(s)-1-feniletilcarbamato] de amilose Figura Estrutura química da Teicoplanina Figura Estruturas químicas das CSPs do tipo Pirkle. a) 3,5-dinitro-benzoilfenilglicina, b) Naftilalanina e c) (S,S) Whelk-O 1 17 Figura Estrutura química da CSP (+)-(18-coroa-6)-2,3,11,12-ácido tetracarboxílico Figura a) Estrutura Tradicional, b) Estrutura dos enantiômeros Figura Estrutura do Esomeprazol (Nexium TM ) Resultados e Discussões Figura Série de sulfóxidos quirais avaliada 28 Figura Estrutura proposta da (R,R) P-CAP 29 Figura N,N-[(1R,2R)-1,2-difenil-1,2-etanoedil]bis-2-propenamida 30 Figura Perfil de retenção do 1º e 2º enantiômero do omeprazol no modo normal de eluição na (R,R) P-CAP 34 Figura a) Perfil de retenção do 1º e 2º enantiômero,b) Fator de resolução, do Metil naftil sulfóxido no modo normal de eluição na (R,R) P-CAP-DP 34 Figura Cromatogramas do omeprazol, (R,R) P-CAP, 250mm X 4,6mm, vazão:1ml/min, λ=302nm, 20ºC 36 Figura Cromatogramas do metil naftil sulfóxido (7), (R,R) P-CAP-DP, 250mm X 4,6mm, vazão:1ml/min, λ=240nm, 20ºC 37
9 Figura Perfil de retenção do 1º e 2º enantiômero do a) pantoprazol na (R,R) P- CAP e b) metil naftil sulfóxido na (R,R) P-CAP-DP, no modo polar orgânico 38 Figura Representação estrutural do monômero da DEAVB 40 Figura Perfil de retenção do 1º e 2º enantiômero do pantoprazol no modo normal de eluição na DEAVB 44 Figura a) Perfil de retenção do 1º e 2º enantiômero, b) Parâmetros cromatográficos, do omeprazol (10) no modo polar orgânico de eluição na DEAVB 45 Figura Gráfico ilustrativo das enantiorresoluções obtidas para a série de sulfóxidos quirais na (R,R)P-CAP e na (R,R)P-CAP-DP 49 Figura Gráfico ilustrativo das enantiorresoluções obtidas para a série de sulfóxidos quirais na DEAVB 50 Figura Gráfico ilustrativo da complementariedade de resoluções das colunas (R,R)P-CAP, (R,R)P-CAP-DP e DEAVB 50 Figura Carbamatos sintetizados 52 Figura Espectro no Infravermelho tris-3,5-dimetilfenilcarbamato de amilose 53 Figura Síntese da 3-aminopropilsílica 54 Figura Analise de distribuição dos tamanhos da partícula sílica APS 55 Figura Metodologia para a preparação das CSPs de polissacarídeos adsorvidos (CSP 1-2) 55 Figura Analise de distribuição dos tamanhos da partícula a) tris-3,5- dimetilfenilcarbamato de amilose (CSP 1) b) tris-3,5-dimetoxifenilcarbamato de amilose (CSP 2) 57 Figura Estruturas dos padrões utilizados na avaliação das colunas quirais 57 Figura Esquema da CSP de polissacarídeo imobilizado por reticulação 58 Figura Metodologia de preparo das colunas quirais de polissacarídeo imobilizado (CSP 3 e CSP 4) 58 Figura Metodologia de preparo das colunas quirais de polissacarídeo imobilizado (CSP 5 e CSP 6) 61 Figura Analise de distribuição dos tamanhos da partícula da CSP Figura Analise de distribuição dos tamanhos da partícula da tris-3,5- dimetoxifenilcarbamato de amilose (CSP 8) 66
10 Lista de Tabelas Introdução Tabela 1.1: Seletores quirais e principais interações com analitos quirais 6 Resultados e Discussões Tabela 3.1: Parâmetros cromatográficos das separações obtidas pela (R,R) P-CAP e pela (R,R) P-CAP-DP 31 Tabela 3.2: Comparação da eficiência da enantiorresolução do modafinil (12) no modo normal, polar orgânico e normal com solvente clorado de eluição na (R,R) P-CAP 39 Tabela 3.3: Parâmetros cromatográficos das separações obtidas pela DEAVB 41 Tabela 3.4: Comparação da eficiência da enantioresolução do modafinil (12) no modo normal, polar orgânico e normal com solvente clorado de eluição na DEAVB 46 Tabela 3.5: Parâmetros cromatográficos das separações obtidas no modo reverso de eluição na DEAVB 48 Tabela 3.6: Avaliação das colunas cromatográficas CSP 1, CSP 4, CSP 5 e CSP 6 Tabela 3.7: Avaliação das colunas cromatográficas CSP 1 e CSP
11 Resumo Estudos de Separação Enantiosseletividade para uma Série de Sulfóxidos Quirais em Colunas Poliméricas. Este trabalho descreve a investigação do poder de enantiorresolução de novas fases estacionária quirais (CSP) de polímero sintético preparadas a partir dos monômeros poli(trans-1,2-ciclohexanediil-bis acrilamida (P-CAP ), N,N - [(1R,2R)-1,2-difenil-1,2-etanodil]bis-2-propenamida (P-CAP-DP ) e trans-9,10- dihidro-9,10-etanoantraceno-(11s,12s)-11,12-acido dicarboxilico bis-4-vinilfenilamida (DEAVB) para uma série de dezessete sulfóxidos quirais. A série de sulfóxidos composta por aril alquil sulfóxidos, sulfóxidos benzoimidazólicos e pelos fármacos quirais modafinil, albendazol sulfóxido, omeprazol, lansoprazol, pantoprazol e rabeprazol foram eluidos no modo multimodal. O estudo sistemático da eficiência das três colunas de polímero sintético na enantiorresolução da séries de sulfóxidos quirais e a superioridade da DEAVB nas separações destes compostos nos três diferentes modos de eluição são apresentados. A P-CAP, P-CAP-DP e DEAVB também foram avaliadas pela primeira vez no modo reverso de eluição e a estabilidade destas colunas foi investigada pelo uso de solventes cromatográficos não usuais. O estudo do desenvolvimento de fases estacionárias quirais de derivados de polissacarídeos imobilizados em sílica APS foi realizado utilizando-se métodos térmicos ou fotoquímicos. O método fotoquímico foi mais eficiente e proporcionou o preparo da coluna de tris-3,5-dimetilfenilcarbamato de amilose (CSP 7). Esta coluna apresentou estabilidade frente a solventes cromatográficos não usuais, porém demonstrou baixo poder de enantiorresolução para os compostos quirais avaliados. Através do procedimento fotoquímico a CSP de tris-3,5- dimetoxifenilcarbamato de amilose (CSP 8) também foi preparada. Todavia, as condições de imobilização necessitam de maiores investigações, estes resultados estão também presentes e discutidos neste trabalho.
12 Abstract Enantiomeric Resolution of a Chiral Sulfoxide Series by LC on Synthetic Polymeric Columns with Multimodal Elution. The liquid chromatography enantiomeric separation of a series of seventeen chiral sulfoxides was systematically investigated using multimodal elution with the new synthetic polymeric stationary phases based on monomers N-(2- acryloylamino-(1r,2r)-cyclohexyl)-acrylamine (P-CAP ), N,N0-[(1R,2R)-1,2- diphenyl-1,2-ethanediyl]bis-2-propenamide (P-CAP-DP ) and trans-9,10-dihydro- 9,10-ethanoanthracene-(11S,12S)-11,12-dicarboxylic acid bis-4-vinylphenylamide (DEAVB). The sulfoxide series was composed of aryl alkyl sulfoxides, benzoimidazole sulfoxides and the drugs modafinil, albendazole sulfoxide, omeprazole, lansoprazole, pantoprazole and rabeprazole. This work examines the effectiveness of the polymeric chiral stationary phases for the separation of chiral sulfoxides and describes the superiority of DEABV for these separations in three different elution modes. The first ever reversed phase enantiomeric separations on these columns is demonstrated. Besides that, the use of non standard chromatography solvents was evaluated for the sulfoxides series on the polymeric stationary phases. The study of the development of polysaccharides chiral stationary phases (CSPs) immobilized on to aminopropilsilica was carried out using thermal or photochemical methods. The photochemical method was more effective and provided the production of a CSP based on amilose tris-3,5- dimethylphenylcarbamate (CSP 7). This column showed stability for non standards mobile phases; however, has showed low enantiorresolution power for the compounds investigated. Using the photochemical approach an amilose tris-3,5- dimetoxiphenylcarbamate (CSP 8) was also prepared. The immobilization conditions needs, however, futher investigations and these results will be also presented and discussed in this work.
13 Sumário 1- Introdução Fases Estacionárias Quirais para Cromatografia Líquida de Alta Eficiência Seletores Quirais Naturais Proteínas Ciclodextrinas Polissacarídeos Glicopeptídeos Macrocíclicos Alcalóides de Cinchona Seletores Quirais Sintéticos Tipo Pirkle Troca de Ligantes Éteres de Coroa Polimero sintético Polímero impresso molecularmente (MIP) Sulfóxidos Quirais Objetivos Resultados e Discussões Avaliação das CSPs de polímero sintético Avaliação da (R,R)P-CAP e da (R,R)P-CAP-DP Avaliação da DEAVB Síntese e preparo de CSPs de polissacarídeo imobilizado Síntese dos tris-arilcarbamatos de amilose Modificação da superfície da sílica Preparação das CSPs de polissacarídeos quirais adsorvidos (CSP 1 e CSP 2) Preparo e Avaliação das CSPs de polissacarídeos quirais imobilizados. (CSP 3 CSP 8) 57
14 4- Conclusões e Perspectivas Parte Experimental Generalidades Procedimento Experimental Condições cromatográficas para as análises das colunas de polímero sintético (R,R)P-CAP, (R,R)P-CAP-DP e DEAVB Síntese do complexo de molibdênio de n-óxido de piridina Síntese dos sulfetos pró-quirais Síntese dos Sulfóxidos quirais Síntese dos Tris-fenilcarbamatos de Amilose Preparação do suporte 3-Aminopropilsílica Preparação das CSPs de polissacarídeo adsorvido em sílica APS-Nucleosil Preparação das CSPs de polissacarídeo imobilizado em sílica APS-Nucleosil Empacotamento das Fases Estacionárias Quirais Referências Bibliográficas 83 ANEXO I - Cromatogramas Selecionados DEAVB 97 ANEXO II - Cromatogramas das CSPs de Polissacarídeos Derivados 111
15 Introdução INTRODUÇÃO Fases Estacionárias Quirais para Cromatografia Líquida de Alta Eficiência. O conceito básico de resolução quiral teve início em 1809, com o cristalógrafo Hauy 1apud, mas foi Pasteur, em 1848, que efetivamente descobriu a diferença de atividade entre dois enantiômeros, ao publicar que a enzima Penicillium glaucum consome mais rapidamente o enantiômero (+)-tartarato de amônio do que o (-)-tartarato de amônio 2apud. Pasteur também foi responsável pela primeira resolução de enantiômeros. Após observar que os cristais do racemato de amônio tartarato de sódio possuíam duas formas enantiomórficas distintas, ele separou-os manualmente, com o auxílio de uma pinça e uma lente de aumento, e demonstrou que os dois tipos diferentes de cristais rotacionavam a luz polarizada em sentidos opostos 3apud. Este experimento de Pasteur é conhecido como o marco da resolução quiral. A diferença do coeficiente de adsorção de dois enantiômeros em compostos com morfologia assimétrica mostrou ser uma importante técnica de separação desde o início do século XX. Em 1936, Nakamura et al 4 utilizaram cristais enantiomórficos de quartzo para separar pequenas quantidades de [Codg 2 (NH 3 )Cl], propondo que a morfologia assimétrica do quartzo é responsável por adsorver mais fortemente um dos enantiômeros. Henderson e Rule 5, em 1939, separaram o (±)-pfenilenebisimino cânfora utilizando lactose sólida. A mistura racêmica foi adsorvida na parte superior de um tubo contendo o adsorvente e após sucessivas lavagens com solvente, um dos enantiômeros permaneceu adsorvido no topo do tubo enquanto o outro foi encontrado na parte inferior do tubo. A primeira técnica de relativo sucesso na resolução de enantiômeros foi a cromatografia em papel, tendo sido eficiente na separação de alguns aminoácidos aromáticos 6,7. Baseado nestes trabalhos de separação em papel, Dagliesh, em 1952, propôs o modelo de interação de três pontos entre enantiômeros e o seletor quiral 6. Segundo este modelo, são necessárias três interações simultâneas entre um dos enantiômeros e o seletor quiral, sendo que pelo menos uma delas deve ser dependente da estereoquímica do analito. Além disso,
16 Introdução 2 estas interações devem ser de sítios distintos tanto no enantiômero quanto no seletor quiral 2 (Figura 1.1a). O outro enantiômero interage somente com dois sítios do seletor quiral, conforme mostrado na Figura 1.1b. Figura Representação do modelo de interação de três pontos O modelo original 6 considera que apenas as interações atrativas são responsáveis pela discriminação quiral. Atualmente, porém, é aceito que as interações repulsivas também participam do mecanismo de resolução enantiomérica. Assim, por exemplo, duas interações podem ser repulsivas se uma terceira for atrativa e forte o suficiente para promover a formação de, no mínimo, um dos complexos diastereoisoméricos transitórios enantiômero/seletor quiral 8. Se as três interações são atrativas, então o enantiômero na Figura 1a estará mais fortemente ligado ao seletor do que o enantiômero na Figura 1b. Os principais tipos de interações, responsáveis pela discriminação, entre os enantiômeros de um analito e o seletor quiral, no sentido decrescente de intensidade, são 2 : interação coulômbica, ligação de hidrogênio e interação estérica (muito forte), interação π-π e íon-dipolo (fortes), interação dipolo-dipolo (intermediária), interação dipolo-dipolo induzido (fraca) e dispersão de London (muito fraca). As interações coulômbicas e do tipo π-π podem ser atrativas ou repulsivas, a estérica é repulsiva e as demais são todas atrativas.
17 Introdução 3 O modelo de interação de três pontos é bem aceito no meio científico, principalmente para explicar a discriminação de aminoácidos em fases estacionárias quirais do tipo troca de ligantes. Entretanto, este mesmo modelo é freqüentemente questionado para explicar as separações em seletores quirais de proteínas. Devido à complexa estrutura tridimensional das proteínas, o mecanismo de discriminação quiral não é completamente conhecido, sendo considerado estéreo-específico para cada mistura enantioméricas 9,10. Pirkle e Pochapsky 11 demonstraram que para sistemas com interação π-π, a rigidez conformacional dos anéis aromáticos participa da formação do complexo diastereoisomérico e, como consequência, apenas dois grupos funcionais ligados ao centro estereogênico do analito precisam interagir com os grupos funcionais do seletor quiral. Segundo os autores, ocorrem três interações entre o seletor quiral da fase estacionária, (S)-metil N-(2-naftil)alaninato (1), e o enantiômero (S)-N-(3,5-dinitrobenzoil)leucina n-propilamida (2); uma interação π-π entre os grupos aromáticos da fase estacionária e do (S)-enantiômero do analito e duas ligações de hidrogênio com os grupos C=O (Figura 1.2). Topiol e Sabio 12 denominaram este modelo como uma interação pseudo-dois-pontos. Figura Reconhecimento quiral entre os (S)-enantiômeros e do metil N-(2- naftil)alaninato (1) e do N-(3,5-dinitrobenzoil)leucina n-propilamida (2)
18 Introdução 4 É importante salientar que o reconhecimento quiral não necessariamente resulta em uma discriminação quiral dos enantiômeros. A separação é baseada na diferença de energia livre (δδg) da formação dos dois complexos diastereoisoméricos, a qual depende da entalpia (δδh) e da entropia (T x δδs). Normalmente a contribuição da entalpia é mais efetiva, uma vez que os dois complexos diastereoisoméricos diferem no número de interações (duas ou três). Algumas vezes, porém, o que predomina é a grande diferença na entropia de formação dos dois complexos, situação que ocorre, por exemplo, quando há uma considerável diferença no número de moléculas do solvente que participam da formação dos dois complexos. Em ambos os casos, quando há predominância da entalpia ou da entropia, ocorre discriminação quiral 8. Entretanto, há uma temperatura específica onde a entalpia e a entropia se anulam. Nesta temperatura há formação dos complexos diasteroisoméricos e, portanto, reconhecimento quiral, mas não ocorre discriminação dos enantiômeros. Para que haja discriminação quiral é necessário temperaturas maiores ou menores do que esta temperatura específica 8. Os processos envolvidos na formação dos complexos diastereoisoméricos transitórios analito/fase estacionária quiral (CSP) não são simples e singulares, visto que várias interações simultâneas são requeridas para discriminar um enantiômero do outro. Nos mecanismos enantiosseletivos, muitas vezes as interações fracas podem desempenhar um papel tão decisivo quanto as interações fortes 11. Além disso, geralmente os seletores quirais possuem vários grupos que podem apresentar mais de um tipo de interação com os analito. O grupo naftil, por exemplo, muito usado nos seletores do tipo Pirkle, pode interagir estericamente ou eletronicamente (π-π) com os enantiômeros do analito. Adicionalmente, a fase móvel desempenha um papel importante na resolução enantiomérica. Mesmo assim, usualmente a escolha do seletor quiral é feita considerando as interações mais fortes entre os enantiômeros e a CSP 2. O crescente número de fases estacionárias quirais desenvolvidas e comercialmente disponíveis se, por um lado, possibilita a separação de enantiômeros de uma ampla variedade de compostos, ao mesmo tempo dificulta a escolha da fase estacionária mais apropriada para cada tipo de separação. Em vista
19 Introdução 5 disto, Wainer 13 classificou as CSPs em cinco tipos diferentes (I-V), de acordo com as interações analito/csp que levam ao reconhecimento quiral: Tipo I: A grande maioria das fases do tipo I é baseada em derivados de aminoácidos, cujos grupos funcionais atuam como sítios de interação entre o analito e a fase estacionária quiral. Os complexos diastereoisoméricos analito/csp são formados, principalmente, por meio de interações π-π, ligação de hidrogênio e interações dipolo-dipolo e estéricas. As CSPs do tipo Pirkle estão classificadas no Tipo I. Tipo II: Neste grupo estão classificadas as fases estacionárias quirais baseadas em derivados de polissacarídeos. A formação dos complexos diastereoisoméricos analito/csp ocorre, principalmente, devido a interações π-π, ligação de hidrogênio e interações dipolo-dipolo. Entretanto, a formação de complexos de inclusão contribui de forma efetiva para o mecanismo de discriminação quiral. Tipo III: O reconhecimento quiral é devido a formação de complexos de inclusão decorrente da entrada do analito na cavidade quiral da fase estacionária. Interações secundárias, tais como ligação de hidrogênio e interações estéricas, estabilizam os complexos diastereoisoméricos formados. Ciclodextrinas, polímeros impressos molecularmente (MIPs), éteres de coroa e alguns polímeros sintéticos, são fases quirais pertencentes a este grupo. Tipo IV: O mecanismo de separação dos enantiômeros é baseado na formação de complexos diastereoisoméricos ternários envolvendo um enantiômero de uma molécula quiral (L), usualmente um aminoácido; um íon de um metal de transição (M), normalmente Cu 2+ ; e os enantiômeros do analito racêmico (R e S). Os complexos formados, representados por L-M-R e L-M-S, podem ser separados se possuírem estabilidades diferentes. As CSPs baseadas em troca de ligantes são classificadas neste tipo IV. Tipo V: Quando a CSP é uma proteína, o mecanismo de reconhecimento quiral é baseado, principalmente, em interações polares e hidrofóbicas. Em outra classificação, sugerida por Berthod 2, as CSPs foram agrupadas de acordo com o tipo de seletor quiral, natural ou sintético, da fase estacionária (Tabela 1.1).
20 Introdução 6 Tabela 1.1: Seletores quirais e principais interações com analitos quirais Seletor Quiral CSPs Principais Interações Natural Sintético Proteínas Ciclodextrinas Polissacarídeos Glicopeptídeos Macrocíclicos Cinchona Tipo Pirkle Troca de Ligantes Éteres de Coroa Polímeros Sintéticos MIPs Interações hidrofóbicas e eletrostáticas Complexo de Inclusão e ligação de hidrogênio Complexo de Inclusão e interação atrativas Complexo de inclusão e interações iônicas Interações eletrostáticas Interação π-π e ligação de hidrogênio Interações coulômbicas e íon-dipolo Complexo de inclusão e íon dipolo Interação π-π, ligação de hidrogênio e interação dipolo-dipolo Específico para cada analito Seletores Quirais Naturais Proteínas As proteínas apresentam uma estrutura altamente complexa e possuem diferentes sítios que podem interagir com analitos quirais. Apesar do mecanismo de reconhecimento quiral não estar totalmente elucidado, é conhecido que as principais interações envolvidas na discriminação quiral são eletrostáticas, hidrofóbicas e ligações de hidrogênio 14. As fases quirais protéicas podem ser preparadas por dois métodos distintos. Em um deles, o seletor quiral é adsorvido no suporte da fase estacionária, usualmente sílica, enquanto no outro a proteína é quimicamente ligada ao suporte cromatográfico por meio de ligações covalentes 15. As CSP de proteínas preparadas quimicamente são as mais estáveis e, portanto, as mais utilizadas 15. As proteínas podem ser covalentemente ligadas à sílica derivada (aminopropilsílica) através dos grupos amino ou carboxílico da proteína. No primeiro procedimento são utilizados reagentes eletrófilos como espaçadores, tais quais o suberato de N,N-disuccinimidila (DSS) 16 e o
21 Introdução 7 glutaraldeído 17. Reações com reagentes nucleofílicos como, por exemplo, o 1-etil-3- (3 -dimetilaminopropil)carbodimida (EDC) promovem a imobilização da proteína por meio dos seus grupos carboxílicos 18. Diferentes proteínas têm sido utilizadas no preparo de colunas comerciais e dentre elas destacam-se a albumina sérica bovina (BSA), a albumina sérica humana (HSA), a ovomucóide e a α 1 -glicoproteína ácida 19. Estas CSPs são altamente sensíveis a variações nas condições cromatográficas, uma vez que alterações no ph da fase móvel, solventes orgânicos, aditivos e temperatura podem modificar a conformação espacial e os sítios de discriminação quiral destes seletores. Desta forma, a alteração nestes parâmetros pode afetar a retenção e a enantioseletividade dos analitos 15. Devido a sua baixa capacidade de carga, decorrente da pequena quantidade de seletor quiral que pode ser imobilizado por grama de sílica, as fases estacionárias protéicas não são utilizadas para a separação de enantiômeros em escala preparativa 20. Entretanto, as mesmas encontram grande aplicabilidade na área biomédica, principalmente em estudos de interação fármaco-proteína. Wainer e colaboradores 21 investigaram as interações de alguns benzodiazepínicos e da warfarina com os sítios ativos da HSA utilizada como fase estacionária quiral. Os resultados obtidos neste estudo confirmaram a existência de interação alostérica entre os sítios ativos dos benzodiazepínicos e da warfarina. A literatura também descreve estudos da interação carbamazepina-proteína 22 e interações de ibuprofeno/acetato de S-lorazepam, S-oxazepam hemisuccinato/r-oxazepam hemisuccinato e L-triptofano/fenitoína 23 em colunas de HSA e das interações de diversos compostos ácidos, básicos e neutros em coluna de α 1 -glicoproteína ácida Ciclodextrinas Ciclodextrinas (CDs) são polissacarídeos cíclicos constituídos por unidades de D-(+)-glicopiranose conectadas por ligações α-(1,4). As colunas de ciclodextrinas comercialmente disponíveis são as que possuem seis, sete ou oito unidades de α-d-glicose, as quais são denominadas de α-, β- e γ-ciclodextrina 25. A molécula de ciclodextrina possui uma estrutura estereoespecífica, na forma de cone truncado. A ausência de grupos hidroxila livres orientados para o
22 Introdução 8 interior da cavidade faz com que esta apresente um caráter relativamente hidrofóbico. Por outro lado, a superfície externa é hidrofílica, devido à presença de grupos hidroxila primários e secundários 25. No processo de reconhecimento quiral, os enantiômeros entram, pelo menos parcialmente, na cavidade das moléculas de ciclodextrina formando complexos diastereoisoméricos. Estes complexos de inclusão são estabilizados por interações dipolo-dipolo induzido, dispersões de London e estéricas entre os enantiômeros do analito e a fase estacionária. Interações secundárias do tipo ligações de hidrogênio, entre os grupos hidroxila da superfície externa da ciclodextrina e parte da molécula do analito que ficou para fora da cavidade, também contribuem para a estabilização dos complexos diastereoisoméricos 13,26. As colunas de CD são muito utilizadas no modo reverso de eluição, sendo que o uso de tampões tais como fosfato e acetato de trimetilamônio podem melhorar a eficiência das fases e diminuir a retenção de analitos aniônicos e catiônicos 13. A derivação das hidroxilas primárias e secundárias, presentes na parte externa, possibilitou o desenvolvimento de novas fases com diferentes funcionalidades e polaridades e, consequentemente, com diferentes tipos de interações 27. Dentre os derivados de CD, a fase naftiletilcarbamato de β-ciclodextrina (NEC-β-CD), ilustrada na Figura 1.3, merece destaque pois, além de apresentarem as tradicionais possibilidades de interações (π-π, ligação de hidrogênio e formação de complexo de inclusão), um novo centro estereogênico é adicionado à estrutura do seletor quiral. Armstrong e colaboradores 28 relataram a separação de 121 compostos racêmicos na fase estacionária quiral (S)-(1-naftiletil)carbamato de β- ciclodextrina (S-NEC-β-CD) e 74 racematos na CSP R-NEC-β-CD, usando modo normal de eluição. A NEC-β-CD também é conhecida por ser uma das primeiras CSPs utilizada em eluição multimodal 29.
23 Introdução 9 Figura Estrutura do seletor quiral (NEC-β-CD) Chang et al descreveram a atuação complementar destes seletores no modo polar orgânico em relação aos outros dois modos de eluição. O uso de fases móveis constituídas predominantemente de acetonitrila, com pequenas porcentagens de metanol, ácido acético e trietilamina possibilitou a separação enantiomérica de vários compostos quirais que não foram resolvidos no modo normal ou reverso 30. Apesar das colunas de ciclodextrinas serem utilizadas com sucesso em separações análiticas 31, devido a sua baixa capacidade de carga estas fases quirais não são usadas em cromatografia preparativa Polissacarídeos Os polissacarídeos na sua forma nativa são capazes de discriminar enantiômeros e resolver compostos quirais. Entretanto, as suas habilidades de reconhecimento quiral não são suficientes para serem utilizadas como CSP em cromatografia líquida 32. A primeira CSP derivada de polissacarídeo, o triacetato de celulose microcristalina, foi desenvolvida por Hesse e Hagel em Esta fase quiral apresentou boa habilidade de separação enantiosseletiva e foi usada para separação de muitos compostos alifáticos e aromáticos 34,35. Okamoto e colaboradores 36 solubilizaram o triacetato de celulose e o adsorveram em sílica macroporosa. Esta fase mostrou uma capacidade de reconhecimento quiral completamente distinta da fase preparada por Hesse e Hagel, sendo observada inversão na ordem de eluição de enantiômeros 37. Desde então,
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
QUÍMICA FARMACÊUTICA I
 PROTÓTIPO QUÍMICA FARMACÊUTICA I AULA 5 Primeiro tipo ou exemplar original, modelo. Diz-se do composto originalmente identificado que apresenta atividade farmacológica in vivo. Profa. Ms. Paula Cristina
PROTÓTIPO QUÍMICA FARMACÊUTICA I AULA 5 Primeiro tipo ou exemplar original, modelo. Diz-se do composto originalmente identificado que apresenta atividade farmacológica in vivo. Profa. Ms. Paula Cristina
- CROMATOGRAFIA EM CAMADA FINA (CCF)
 - CROMATOGRAFIA EM CAMADA FINA (CCF) Técnica de identificação e separação de compostos orgânicos Aplicações: - Identificação de componentes de uma mistura - Acompanhamento da evolução de uma reação - Análise
- CROMATOGRAFIA EM CAMADA FINA (CCF) Técnica de identificação e separação de compostos orgânicos Aplicações: - Identificação de componentes de uma mistura - Acompanhamento da evolução de uma reação - Análise
Forças intermoleculares, Disciplina de Química Geral Profa. Marcia Margarete Meier
 , líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
, líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
Mary Santiago Silva 05/05/2010
 Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
MÉTODOS CROMATOGRÁFICOS
 MÉTODOS CROMATOGRÁFICOS Aula 1 - Introdução a Cromatografia Profa. Daniele Adão DEFINIÇÃO Conjunto de técnicas de separação cujo princípio depende da distribuição diferenciada dos componentes de uma mistura
MÉTODOS CROMATOGRÁFICOS Aula 1 - Introdução a Cromatografia Profa. Daniele Adão DEFINIÇÃO Conjunto de técnicas de separação cujo princípio depende da distribuição diferenciada dos componentes de uma mistura
Síntese Artificial de Peptídeos
 Síntese Artificial de Peptídeos Rebeca Bayeh Seminário apresentado para a disciplina Princípios Físicos Aplicados à Fisiologia (PGF530) Prof. Dr. Adriano Mesquita Alencar Segundo semestre de 2013 Motivação
Síntese Artificial de Peptídeos Rebeca Bayeh Seminário apresentado para a disciplina Princípios Físicos Aplicados à Fisiologia (PGF530) Prof. Dr. Adriano Mesquita Alencar Segundo semestre de 2013 Motivação
Aula 6. Organic Chemistry. Reações de Substituição em Haletos de Alquila. O que é uma reação de substituição?
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 6 Reações de Substituição em Haletos de Alquila Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall O que é uma reação
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 6 Reações de Substituição em Haletos de Alquila Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall O que é uma reação
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
ANÁLISE QUÍMICA INSTRUMENTAL
 ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
LIGAÇÕES INTERATÔMICAS
 UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
Teoria Ácido-Base e Reações Químicas
 Aula ao Vivo Teoria Ácido-Base e Reações Químicas Química Allan Rodrigues 27.04.2015 Existem várias teorias sobre ácidos e bases. Dentre elas, temos a teoria do químico sueco Svante August Arrhenius, que
Aula ao Vivo Teoria Ácido-Base e Reações Químicas Química Allan Rodrigues 27.04.2015 Existem várias teorias sobre ácidos e bases. Dentre elas, temos a teoria do químico sueco Svante August Arrhenius, que
Apostila de Química Geral
 Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I. Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas.
 Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X
 DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA
 PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Aminoácidos ligam-se por ligações peptídicas = reação de condensação entre: OH do grupo carboxila de um aminoácido H do grupo amina do outro aminoácido ( liberação de uma molécula
ESTRUTURA DAS PROTEÍNAS Aminoácidos ligam-se por ligações peptídicas = reação de condensação entre: OH do grupo carboxila de um aminoácido H do grupo amina do outro aminoácido ( liberação de uma molécula
Ligações Químicas Ligação Iônica Ligação Metálica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
http://www.quimica.net/emiliano 1
 Resolução da Prova de Química Vestibular Verão UPF 2004 Professor Emiliano hemello www.quimica.net/emiliano emiliano@quimica.net Questões Resolução: B Resoluções Em 1875, rookes colocou gases muito rarefeitos
Resolução da Prova de Química Vestibular Verão UPF 2004 Professor Emiliano hemello www.quimica.net/emiliano emiliano@quimica.net Questões Resolução: B Resoluções Em 1875, rookes colocou gases muito rarefeitos
APROFUNDAMENTO DE QUIMICA ORGÂNICA LISTA 04 09/10/2014. Assunto: Estudo das Funções Orgânicas
 APROFUNDAMENTO DE QUIMICA ORGÂNICA LISTA 04 09/10/2014 Assunto: Estudo das Funções Orgânicas 01-( Medicina Jundiaí 2014 ) Considere as fórmulas estruturais de substâncias utilizadas como antibióticos:
APROFUNDAMENTO DE QUIMICA ORGÂNICA LISTA 04 09/10/2014 Assunto: Estudo das Funções Orgânicas 01-( Medicina Jundiaí 2014 ) Considere as fórmulas estruturais de substâncias utilizadas como antibióticos:
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011
 RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
QUÍMICA. Questão 31. Questão 32
 QUÍMICA Questão 3 Em 9,9 g de um sal de cálcio encontra-se 0,5 mol desse elemento. Qual a massa molar do ânion trivalente que forma esse sal? Dado: Ca 40 g/mol. (A) 39 g/mol. (B) 278 g/mol. (C) 63,3 g/mol.
QUÍMICA Questão 3 Em 9,9 g de um sal de cálcio encontra-se 0,5 mol desse elemento. Qual a massa molar do ânion trivalente que forma esse sal? Dado: Ca 40 g/mol. (A) 39 g/mol. (B) 278 g/mol. (C) 63,3 g/mol.
Quando esses temas são compreendidos, o aprendizado da química orgânica se torna muito mais fácil, diminuindo a necessidade de memorização.
 REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
Separação e Cromatografia de Proteínas
 QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro 2013 Separação e Cromatografia de Proteínas Universidade de São Paulo QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro
QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro 2013 Separação e Cromatografia de Proteínas Universidade de São Paulo QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro
- LIGAÇÕES IÔNICAS: Na (1s 2 2s 2 2p 6 3s 1 ) + Cl (1s 2 2s 2 2p 6 3s 2 3p 5 ) Na + (1s 2 2s 2 2p 6 ) + Cl - (1s 2 2s 2 2p 6 3s 2 3p 6 )
 - LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
- LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
COLÉGIO SANTA TERESINHA R. Madre Beatriz 135 centro Tel. (33) 3341-1244 www.colegiosantateresinha.com.br
 PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
01/04/2015. Métodos Instrumentais Farmacêuticos FENÔMENOS DE SUPERFÍCIE. Cromatografia. Parte 2 CROMATOGRAFIA E ELETROFORESE CROMATOGRAFIA
 Métodos Instrumentais Farmacêuticos FENÔMENOS DE SUPERFÍCIE Cromatografia CROMATOGRAFIA Plano de Aula -Princípios da separação de moléculas -Cromatografia: Classificação e mecanismos de separação -Cromatografia
Métodos Instrumentais Farmacêuticos FENÔMENOS DE SUPERFÍCIE Cromatografia CROMATOGRAFIA Plano de Aula -Princípios da separação de moléculas -Cromatografia: Classificação e mecanismos de separação -Cromatografia
Funções organometálicas:
 Funções organometálicas: 1- Para dar nome em compostos organometálicos, primeiramente coloca-se o nome do radical orgânico e em seguida o nome do metal: a) Metil sódio. b) Dimetil Zinco c) Butil lítio.
Funções organometálicas: 1- Para dar nome em compostos organometálicos, primeiramente coloca-se o nome do radical orgânico e em seguida o nome do metal: a) Metil sódio. b) Dimetil Zinco c) Butil lítio.
8. Estereoquímica. 1) Organic Chemistry Structure and Function, K. P. C. Vollhardt e N. E.
 8. Estereoquímica 8.1. Estereoisômeros e Moléculas Quirais 8.2. Atividade Óptica 8.3. Configuração Absoluta 8.4. Compostos Meso 8.5. Obtenção de Moléculas Enantiomericamente Puras 8.6. Quiralidade no Mundo
8. Estereoquímica 8.1. Estereoisômeros e Moléculas Quirais 8.2. Atividade Óptica 8.3. Configuração Absoluta 8.4. Compostos Meso 8.5. Obtenção de Moléculas Enantiomericamente Puras 8.6. Quiralidade no Mundo
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia
 Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia Aluno: Julys Pablo Atayde Fernandes Células a Combustível:
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia Aluno: Julys Pablo Atayde Fernandes Células a Combustível:
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
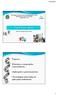
Determinação do poder rotatório específico [a] D de fármacos. Química Medicinal Farmacêutica Curso de Farmácia UFPR
![Determinação do poder rotatório específico [a] D de fármacos. Química Medicinal Farmacêutica Curso de Farmácia UFPR Determinação do poder rotatório específico [a] D de fármacos. Química Medicinal Farmacêutica Curso de Farmácia UFPR](/thumbs/28/12697601.jpg) Determinação do poder rotatório específico [a] D de fármacos Química Medicinal Farmacêutica Curso de Farmácia UFPR Substâncias opticamente ativas Quando uma luz polarizada passa através de uma solução
Determinação do poder rotatório específico [a] D de fármacos Química Medicinal Farmacêutica Curso de Farmácia UFPR Substâncias opticamente ativas Quando uma luz polarizada passa através de uma solução
 Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
Professor Carlos - Proteinas
 14085. (Fuvest 2001) Os três compostos abaixo têm uso farmacológico Considere as afirmações: I Nas moléculas dos três compostos, há ligações peptídicas. II A porcentagem em massa de oxigênio na dropropizina
14085. (Fuvest 2001) Os três compostos abaixo têm uso farmacológico Considere as afirmações: I Nas moléculas dos três compostos, há ligações peptídicas. II A porcentagem em massa de oxigênio na dropropizina
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS
 Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
QUÍMICA Exercícios de revisão resolvidos
 13. (ENEM 2014) O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo envolve a formação do hidroperóxido de cumila,
13. (ENEM 2014) O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo envolve a formação do hidroperóxido de cumila,
caso especial de micelas:= microfase/pseudofase/fase microdispersa/fase pseudo-estacionária
 Cromatografia Separação de solutos de uma solução por diferenças de coeficientes de partição Princípio: partição de um soluto entre duas fases sendo uma sólida ou estacionária e outra móvel, líquida ou
Cromatografia Separação de solutos de uma solução por diferenças de coeficientes de partição Princípio: partição de um soluto entre duas fases sendo uma sólida ou estacionária e outra móvel, líquida ou
UNIDADE 3 - COORDENAÇÃO ATÔMICA
 A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
Química. Resolução das atividades complementares. Q50 Forças intermoleculares
 Resolução das atividades complementares 4 Química Q50 Forças intermoleculares p. 15 1 (Unifor-CE) Considerando a natureza das ligações químicas intermoleculares existentes nas substâncias: Etanol C 2 H
Resolução das atividades complementares 4 Química Q50 Forças intermoleculares p. 15 1 (Unifor-CE) Considerando a natureza das ligações químicas intermoleculares existentes nas substâncias: Etanol C 2 H
COMENTÁRIO DA PROVA DE QUÍMICA EQUIPE DE QUÍMICA DO CURSO POSITIVO
 COMENTÁRIO DA PROVA DE QUÍMICA Sem sombra de dúvida, a prova deste ano está muito melhor que a dos anos anteriores. Maior abrangência com temas mais relevantes e grau de dificuldade de médio para difícil,
COMENTÁRIO DA PROVA DE QUÍMICA Sem sombra de dúvida, a prova deste ano está muito melhor que a dos anos anteriores. Maior abrangência com temas mais relevantes e grau de dificuldade de médio para difícil,
ANÁLISE DOS RESULTADOS DOS PROGRAMAS DE APOIO ÀS PMEs NO BRASIL Resumo Executivo PARA BAIXAR A AVALIAÇÃO COMPLETA: WWW.IADB.
 ANÁLISE DOS RESULTADOS DOS PROGRAMAS DE APOIO ÀS PMEs NO BRASIL Resumo Executivo PARA BAIXAR A AVALIAÇÃO COMPLETA: WWW.IADB.ORG/EVALUATION ANÁLISE DOS RESULTADOS DOS PROGRAMAS DE APOIO ÀS PMEs NO BRASIL
ANÁLISE DOS RESULTADOS DOS PROGRAMAS DE APOIO ÀS PMEs NO BRASIL Resumo Executivo PARA BAIXAR A AVALIAÇÃO COMPLETA: WWW.IADB.ORG/EVALUATION ANÁLISE DOS RESULTADOS DOS PROGRAMAS DE APOIO ÀS PMEs NO BRASIL
Hidrogênio x Hidrogênio Hidrogênio x Não metal Não metal x Não metal
 LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014
 RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
LIGAÇÕES INTERMOLECULARES
 Ligações Intermoleculares 1 LIGAÇÕES INTERMOLECULARES Introdução O que mantém as moléculas unidas nos estados líquido e sólido? Que força faz a água, contrariando a gravidade, subir por um capilar? Como
Ligações Intermoleculares 1 LIGAÇÕES INTERMOLECULARES Introdução O que mantém as moléculas unidas nos estados líquido e sólido? Que força faz a água, contrariando a gravidade, subir por um capilar? Como
PROFESSOR LOURIVAL NETO
 QUÍMICA EM 1 DIA PROFESSOR LOURIVAL NETO UBERLÂNDIA LIGAÇÕES QUÍMICAS Iônica: Ocorre devido a transferência de elétrons! Ìons mantêmse em um cristal Retículo cristalino. A força eletrostática mantém os
QUÍMICA EM 1 DIA PROFESSOR LOURIVAL NETO UBERLÂNDIA LIGAÇÕES QUÍMICAS Iônica: Ocorre devido a transferência de elétrons! Ìons mantêmse em um cristal Retículo cristalino. A força eletrostática mantém os
Escola Secundária Dr. Manuel Gomes de Almeida
 Escola Secundária Dr. Manuel Gomes de Almeida Ficha de trabalho de Biologia - 12º Ano Fermentação e actividade enzimática Nome: N º: Turma: Data: 1. A figura 1 representa um tipo de fermentação. Figura
Escola Secundária Dr. Manuel Gomes de Almeida Ficha de trabalho de Biologia - 12º Ano Fermentação e actividade enzimática Nome: N º: Turma: Data: 1. A figura 1 representa um tipo de fermentação. Figura
Química em Solventes não Aquosos. Prof. Fernando R. Xavier
 Química em Solventes não Aquosos Prof. Fernando R. Xavier UDESC 2013 Reações químicas podem acontecer em cada uma das fases ordinárias da matéria (gasosa, líquida ou sólida). Exemplos: Grande parte das
Química em Solventes não Aquosos Prof. Fernando R. Xavier UDESC 2013 Reações químicas podem acontecer em cada uma das fases ordinárias da matéria (gasosa, líquida ou sólida). Exemplos: Grande parte das
TURMA DE REVISÃO - EMESCAM 1º SEMESTRE 2012 - QUÍMICA
 TURMA DE REVISÃO - EMESCAM 1º SEMESTRE 2012 - QUÍMICA Prof. Borges EXERCÍCIOS DE AMINOÁCIDOS 1. (Fuvest) A hidrólise de um peptídeo rompe a ligação peptídica, originando aminoácidos. Quantos aminoácidos
TURMA DE REVISÃO - EMESCAM 1º SEMESTRE 2012 - QUÍMICA Prof. Borges EXERCÍCIOS DE AMINOÁCIDOS 1. (Fuvest) A hidrólise de um peptídeo rompe a ligação peptídica, originando aminoácidos. Quantos aminoácidos
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
QUIMICA ORGÂNICA BÁSICA
 QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Projeto Embuá Unidade de Aprendizagem: ENERGIA
 Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Química D Extensivo V. 3
 Química D Extensivo V. 3 Exercícios 01) Alternativa correta: A 5 4 3 2 1 CH 3 CH 2 CH CH CH 2 OH CH 3 CH 3 metil metil 02) Alternativa correta: D 8 7 6 5 4 3 2 1 CH 3 C = CH CH 2 CH 2 CH CH 2 CH 2 OH CH
Química D Extensivo V. 3 Exercícios 01) Alternativa correta: A 5 4 3 2 1 CH 3 CH 2 CH CH CH 2 OH CH 3 CH 3 metil metil 02) Alternativa correta: D 8 7 6 5 4 3 2 1 CH 3 C = CH CH 2 CH 2 CH CH 2 CH 2 OH CH
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES. Professor Cristiano
 GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
Química. Resolução das atividades complementares. Q49 Polaridade das moléculas
 Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
ENZIMAS E METABOLISMO
 ENZIMAS E METABOLISMO Metabolismo Celular é o conjunto de todas as reacções químicas celulares acompanhadas de transferência de energia. ANABOLISMO conjunto de reacções químicas que conduzem à biossíntese
ENZIMAS E METABOLISMO Metabolismo Celular é o conjunto de todas as reacções químicas celulares acompanhadas de transferência de energia. ANABOLISMO conjunto de reacções químicas que conduzem à biossíntese
QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier. Prática 09 Síntese do cloreto de pentaaminoclorocobalto(iii)
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier Prática 09 Síntese do cloreto
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier Prática 09 Síntese do cloreto
ENZIMAS. Células podem sintetizar enzimas conforme a sua necessidade.
 ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
UFU 2010/1 ABERTAS (1ª FASE = ENEM)
 UFU 2010/1 ABERTAS (1ª FASE = ENEM) 1-Leia o texto a seguir. Com o passar do tempo, objetos de prata escurecem e perdem seu brilho em decorrência da oxidação desse metalpelo seu contato com oxigênio e
UFU 2010/1 ABERTAS (1ª FASE = ENEM) 1-Leia o texto a seguir. Com o passar do tempo, objetos de prata escurecem e perdem seu brilho em decorrência da oxidação desse metalpelo seu contato com oxigênio e
INTRODUÇÃO. Capes Relatório Anual: Avaliação Continuada 2005 - Ano Base 2004 Área de Avaliação: GEOGR AFIA
 Relatório Anual: Avaliação Continuada 5 - Ano Base INTRODUÇÃO. Optou-se neste relatório por manter na introdução, os dados históricos da área de Pós-graduação em Geografia, constante no relatório do triênio
Relatório Anual: Avaliação Continuada 5 - Ano Base INTRODUÇÃO. Optou-se neste relatório por manter na introdução, os dados históricos da área de Pós-graduação em Geografia, constante no relatório do triênio
Cromatografia Gasosa. Principles of Instrumental Analysis Skoog, West, Holler, Nieman. Thomson Learning; ISBN: 0030020786. Departamento de Química
 Capítulo X-5 Cromatografia Gasosa Principles of Instrumental Analysis Skoog, West, Holler, Nieman Thomson Learning; ISBN: 0030020786 1 Na cromatografia de fase gasosa (GC) a amostra é volatizada e injectada
Capítulo X-5 Cromatografia Gasosa Principles of Instrumental Analysis Skoog, West, Holler, Nieman Thomson Learning; ISBN: 0030020786 1 Na cromatografia de fase gasosa (GC) a amostra é volatizada e injectada
Caderno de Exercícios 1 Química Série 14 Isomeria
 01 Além da fórmula molecular, também deveria constar no rótulo o nome oficial do composto, uma vez que a fórmula C 6 H 14 pode representar substâncias orgânicas completamente distintas. 1 02 Fórmula molecular:
01 Além da fórmula molecular, também deveria constar no rótulo o nome oficial do composto, uma vez que a fórmula C 6 H 14 pode representar substâncias orgânicas completamente distintas. 1 02 Fórmula molecular:
Prova Experimental Física, Química, Biologia
 Prova Experimental Física, Química, Biologia Complete os espaços: Nomes dos estudantes: Número do Grupo: País: BRAZIL Assinaturas: A proposta deste experimento é extrair DNA de trigo germinado e, posteriormente,
Prova Experimental Física, Química, Biologia Complete os espaços: Nomes dos estudantes: Número do Grupo: País: BRAZIL Assinaturas: A proposta deste experimento é extrair DNA de trigo germinado e, posteriormente,
Elementos do bloco p
 Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Estrutura Eletrônica e Ligação Aula 2. QO-427 Prof. J. Augusto
 Estrutura Eletrônica e Ligação Aula 2 QO-427 Prof. J. Augusto Química Orgânica Orgânica até meados de 1800 referia-se a compostos de fontes com vida ( fontes minerais eram inorgânicos ) Wöhler em 1828
Estrutura Eletrônica e Ligação Aula 2 QO-427 Prof. J. Augusto Química Orgânica Orgânica até meados de 1800 referia-se a compostos de fontes com vida ( fontes minerais eram inorgânicos ) Wöhler em 1828
Prof. Rogério Eletrônica Geral 1
 Prof. Rogério Eletrônica Geral 1 Apostila 2 Diodos 2 COMPONENTES SEMICONDUTORES 1-Diodos Um diodo semicondutor é uma estrutura P-N que, dentro de seus limites de tensão e de corrente, permite a passagem
Prof. Rogério Eletrônica Geral 1 Apostila 2 Diodos 2 COMPONENTES SEMICONDUTORES 1-Diodos Um diodo semicondutor é uma estrutura P-N que, dentro de seus limites de tensão e de corrente, permite a passagem
Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe!
 Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
LIGAÇÕES QUÍMICAS TEORIA CORPUSCULAR
 LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
Plano de Trabalho Docente 2014. Ensino Médio
 Plano de Trabalho Docente 2014 Ensino Médio ETEC Prof. Mário Antônio Verza Código: 164 Município: Palmital-SP Área de conhecimento: Ciências da Natureza Matemática e suas Tecnologias Componente Curricular:
Plano de Trabalho Docente 2014 Ensino Médio ETEC Prof. Mário Antônio Verza Código: 164 Município: Palmital-SP Área de conhecimento: Ciências da Natureza Matemática e suas Tecnologias Componente Curricular:
Kit para calibração de PCR pht
 Kit para calibração de PCR pht Itens fornecidos: Tampões ( concentrado) Composição ( concentrado) I0 500 mm KCl; 100 mm Tris-HCl ph 8,4; 1% Triton X-100 IB 500 mm KCl; 100 mm Tris-HCl ph 8,4; 1% Triton
Kit para calibração de PCR pht Itens fornecidos: Tampões ( concentrado) Composição ( concentrado) I0 500 mm KCl; 100 mm Tris-HCl ph 8,4; 1% Triton X-100 IB 500 mm KCl; 100 mm Tris-HCl ph 8,4; 1% Triton
Metais em água. metais tem um papel crucial em. como espécies hidroxiladas, ex.: FeOH(H 2 O)
 Metais em água Para a estabilização dos elétrons mais externos os cátions metálicos em água são ligados (coordenados) a outras espécies. Assim, os metais em soluções aquosas procuram a máxima estabilidade
Metais em água Para a estabilização dos elétrons mais externos os cátions metálicos em água são ligados (coordenados) a outras espécies. Assim, os metais em soluções aquosas procuram a máxima estabilidade
-Estrutura, composição, características. -Aplicações e processamento. -Tecnologias associadas às aplicações industriais.
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Teófilo Otoni - MG Prof a. Dr a. Flaviana Tavares Vieira Tópicos : -Estrutura, composição, características.
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Teófilo Otoni - MG Prof a. Dr a. Flaviana Tavares Vieira Tópicos : -Estrutura, composição, características.
COMPOSTOS ORGANOMETÁLICOS
 Universidade Federal de Sergipe Pró-Reitoria de Pós Graduação e Pesquisa Programa de Pós Graduação em Química Química Inorgânica Avançada COMPOSTOS ORGANOMETÁLICOS Mestranda: Tarciane Greyci dos Santos
Universidade Federal de Sergipe Pró-Reitoria de Pós Graduação e Pesquisa Programa de Pós Graduação em Química Química Inorgânica Avançada COMPOSTOS ORGANOMETÁLICOS Mestranda: Tarciane Greyci dos Santos
nome de Química do C1. De uma maneira geral é possível dividir estes produtos em três categorias:
 ,1752'8d 2 O gás natural é composto, principalmente, de metano (até 98%) e por alguns hidrocarbonetos de maior peso molecular (de C 2 a C 6 ) além dos diluentes N 2 e CO 2. Com o uso crescente de petróleo
,1752'8d 2 O gás natural é composto, principalmente, de metano (até 98%) e por alguns hidrocarbonetos de maior peso molecular (de C 2 a C 6 ) além dos diluentes N 2 e CO 2. Com o uso crescente de petróleo
Cromatografia e suas aplicações em purificação de proteínas e peptídeos. Alexandre Rosolia Assessor Técnico - HPLC
 Cromatografia e suas aplicações em purificação de proteínas e peptídeos Alexandre Rosolia Assessor Técnico - HPLC 1 - Cromatografia Líquida História e Evolução Alexandre Rosolia Assessor Técnico - HPLC
Cromatografia e suas aplicações em purificação de proteínas e peptídeos Alexandre Rosolia Assessor Técnico - HPLC 1 - Cromatografia Líquida História e Evolução Alexandre Rosolia Assessor Técnico - HPLC
Modelo Cascata ou Clássico
 Modelo Cascata ou Clássico INTRODUÇÃO O modelo clássico ou cascata, que também é conhecido por abordagem top-down, foi proposto por Royce em 1970. Até meados da década de 1980 foi o único modelo com aceitação
Modelo Cascata ou Clássico INTRODUÇÃO O modelo clássico ou cascata, que também é conhecido por abordagem top-down, foi proposto por Royce em 1970. Até meados da década de 1980 foi o único modelo com aceitação
PRODUÇÃO DE MATERIAL DIDÁTICO VOLTADO AO ENSINO DE FÍSICA E A INCLUSÃO NO ENSINO DE FÍSICA
 DEPARTAMENTO DE CIÊNCIAS EXATAS LABORATÓRIO DE ENSINO DE FÍSICA PRODUÇÃO DE MATERIAL DIDÁTICO VOLTADO AO ENSINO DE FÍSICA E A INCLUSÃO NO ENSINO DE FÍSICA Projeto Bolsa Institucional LICENCIATURAS NOTURNAS
DEPARTAMENTO DE CIÊNCIAS EXATAS LABORATÓRIO DE ENSINO DE FÍSICA PRODUÇÃO DE MATERIAL DIDÁTICO VOLTADO AO ENSINO DE FÍSICA E A INCLUSÃO NO ENSINO DE FÍSICA Projeto Bolsa Institucional LICENCIATURAS NOTURNAS
SUSPENSÕES E SOLUÇÕES
 SUSPENSÕES E SOLUÇÕES Definições SUSPENSÃO Mistura heterogênea de substâncias Ex.: sangue (suspensão de plasma e células) água e óleo; água e areia, água e açúcar SOLUÇÃO Mistura homogênea de substâncias
SUSPENSÕES E SOLUÇÕES Definições SUSPENSÃO Mistura heterogênea de substâncias Ex.: sangue (suspensão de plasma e células) água e óleo; água e areia, água e açúcar SOLUÇÃO Mistura homogênea de substâncias
Reações a altas temperaturas. Diagrama de Equilíbrio
 Reações a altas temperaturas Diagrama de Equilíbrio Propriedades de um corpo cerâmico Determinadas pelas propriedades de cada fase presente e pelo modo com que essas fases (incluindo a porosidade) estão
Reações a altas temperaturas Diagrama de Equilíbrio Propriedades de um corpo cerâmico Determinadas pelas propriedades de cada fase presente e pelo modo com que essas fases (incluindo a porosidade) estão
Avanços na transparência
 Avanços na transparência A Capes está avançando não apenas na questão dos indicadores, como vimos nas semanas anteriores, mas também na transparência do sistema. Este assunto será explicado aqui, com ênfase
Avanços na transparência A Capes está avançando não apenas na questão dos indicadores, como vimos nas semanas anteriores, mas também na transparência do sistema. Este assunto será explicado aqui, com ênfase
www.professormazzei.com ISOMERIA Folha 01 João Roberto Fortes Mazzei
 01. Dentre as alternativas a seguir, é incorreto afirmar que: a) etanol e etóxi-etano apresentam, respectivamente, isomeria funcional e de compensação. b) 2-buteno e propino apresentam, respectivamente,
01. Dentre as alternativas a seguir, é incorreto afirmar que: a) etanol e etóxi-etano apresentam, respectivamente, isomeria funcional e de compensação. b) 2-buteno e propino apresentam, respectivamente,
Sistema Elite de Ensino. Química Orgânica. Testes de identificação de compostos
 Sistema Elite de Ensino Química Orgânica Testes de identificação de compostos Roberto Rezende 14/09/2008 Introdução Este material tem por finalidade mostrar alguns métodos de identificar qual a função
Sistema Elite de Ensino Química Orgânica Testes de identificação de compostos Roberto Rezende 14/09/2008 Introdução Este material tem por finalidade mostrar alguns métodos de identificar qual a função
A) Escreva a equação que representa a semi-reação de redução e seu respectivo potencial padrão.
 QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
Recomendada. A coleção apresenta eficiência e adequação. Ciências adequados a cada faixa etária, além de
 Recomendada Por quê? A coleção apresenta eficiência e adequação metodológica, com os principais temas relacionados a Ciências adequados a cada faixa etária, além de conceitos em geral corretos. Constitui
Recomendada Por quê? A coleção apresenta eficiência e adequação metodológica, com os principais temas relacionados a Ciências adequados a cada faixa etária, além de conceitos em geral corretos. Constitui
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE
 LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
Cromatografia Líquida
 Analítica V: Aula 10 Cromatografia Líquida ATENÇÃO À SEQUENCIA DAS PRÁTICAS: Para a Prática de 08/11 cada grupo deverá trazer: - um pacote de M&M (embalagem marrom, de 104 g) - um par de luvas de procedimento
Analítica V: Aula 10 Cromatografia Líquida ATENÇÃO À SEQUENCIA DAS PRÁTICAS: Para a Prática de 08/11 cada grupo deverá trazer: - um pacote de M&M (embalagem marrom, de 104 g) - um par de luvas de procedimento
Sobre as substâncias representadas pelas estruturas I e II, é INCORRETO afirmar:
 8 GABARITO 1 1 O DIA 2 o PROCESSO SELETIVO/2005 QUÍMICA QUESTÕES DE 16 A 30 16. Devido à sua importância como catalisadores, haletos de boro (especialmente B 3 ) são produzidos na escala de toneladas por
8 GABARITO 1 1 O DIA 2 o PROCESSO SELETIVO/2005 QUÍMICA QUESTÕES DE 16 A 30 16. Devido à sua importância como catalisadores, haletos de boro (especialmente B 3 ) são produzidos na escala de toneladas por
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B
 Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
Propriedades Físicas de alguns compostos
 Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
Professor Fernando Stuchi M ETABOLISMO DE C ONSTRUÇÃO
 M ETABOLISMO DE C ONSTRUÇÃO P ROTEÍNAS P ROPRIEDADE BÁSICA São grandes moléculas (macromoléculas) constituídas por aminoácidos, através de ligações peptídicas. É o composto orgânico mais abundante no corpo
M ETABOLISMO DE C ONSTRUÇÃO P ROTEÍNAS P ROPRIEDADE BÁSICA São grandes moléculas (macromoléculas) constituídas por aminoácidos, através de ligações peptídicas. É o composto orgânico mais abundante no corpo
CINÉTICA QUÍMICA CINÉTICA QUÍMICA EQUAÇÃO DE ARRHENIUS
 CINÉTICA QUÍMICA CINÉTICA QUÍMICA EQUAÇÃO DE ARRHENIUS A DEPENDÊNCIA DA VELOCIDADE DE REAÇÃO COM A TEMPERATURA A velocidade da maioria das reações químicas aumenta à medida que a temperatura também aumenta.
CINÉTICA QUÍMICA CINÉTICA QUÍMICA EQUAÇÃO DE ARRHENIUS A DEPENDÊNCIA DA VELOCIDADE DE REAÇÃO COM A TEMPERATURA A velocidade da maioria das reações químicas aumenta à medida que a temperatura também aumenta.
Degradação de Polímeros
 Degradação de Polímeros Degradação de Polímeros e Corrosão Prof. Hamilton Viana Prof. Renato Altobelli Antunes 1. Introdução Degradação é qualquer reação química destrutiva dos polímeros. Pode ser causada
Degradação de Polímeros Degradação de Polímeros e Corrosão Prof. Hamilton Viana Prof. Renato Altobelli Antunes 1. Introdução Degradação é qualquer reação química destrutiva dos polímeros. Pode ser causada
CONCEITO CONCEITO HISTÓRIA 21/03/2013
 CONCEITO Cromatografia é um processo físico de separação, no qual os componentes a serem separados distribuem-se em duas fases: fase estacionária e fase móvel. PROFA. ALESSANDRA GUEDES SALVADOR, 2013.
CONCEITO Cromatografia é um processo físico de separação, no qual os componentes a serem separados distribuem-se em duas fases: fase estacionária e fase móvel. PROFA. ALESSANDRA GUEDES SALVADOR, 2013.
LÍQUIDOS: DETERMINAÇÃO DA VISCOSIDADE I. 1. Introdução
 LÍQUIDOS: DETERMINAÇÃO DA VISCOSIDADE I 1. Introdução No estado líquido as moléculas estão mais próximas uma das outras e entre elas existem forças atrativas. Para um líquido fluir suas moléculas devem
LÍQUIDOS: DETERMINAÇÃO DA VISCOSIDADE I 1. Introdução No estado líquido as moléculas estão mais próximas uma das outras e entre elas existem forças atrativas. Para um líquido fluir suas moléculas devem
OS EFEITOS DA POLARIDADE DAS LIGAÇÕES NAS MOLÉCULAS ORGÂNICAS DOS HALOGENETOS DE ALQUILA
 OS EFEITOS DA POLARIDADE DAS LIGAÇÕES NAS MOLÉCULAS ORGÂNICAS DOS HALOGENETOS DE ALQUILA Natalia Soares Quinete Bolsista de Inic. Científica, Eng. Química, UFF Peter Rudolf Seidl Orientador, Químico industrial,
OS EFEITOS DA POLARIDADE DAS LIGAÇÕES NAS MOLÉCULAS ORGÂNICAS DOS HALOGENETOS DE ALQUILA Natalia Soares Quinete Bolsista de Inic. Científica, Eng. Química, UFF Peter Rudolf Seidl Orientador, Químico industrial,
Ensino Médio Unidade Parque Atheneu. Professor (a): Me. DIOGO LOPES Aluno (a): Série: 3ª Data: / / 2015. LISTA DE QUÍMICA I
 Ensino Médio Unidade Parque Atheneu Professor (a): Me. DIOGO LOPES Aluno (a): Série: 3ª Data: / / 2015. LISTA DE QUÍMICA I OBS: Sua lista semanal deverá ser respondida em folha de papel almaço, copiando
Ensino Médio Unidade Parque Atheneu Professor (a): Me. DIOGO LOPES Aluno (a): Série: 3ª Data: / / 2015. LISTA DE QUÍMICA I OBS: Sua lista semanal deverá ser respondida em folha de papel almaço, copiando
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Bioquímica. Purificação de proteínas
 Bioquímica Purificação de proteínas Estratégia geral - Liberação da proteína do material biológico - Podem ser separados por fracionamento celular - Pode-se separar proteínas por características: Solubilidade
Bioquímica Purificação de proteínas Estratégia geral - Liberação da proteína do material biológico - Podem ser separados por fracionamento celular - Pode-se separar proteínas por características: Solubilidade
Osmose Reversa Conheça este processo de purificação de água
 Osmose Reversa Conheça este processo de purificação de água Antes de falarmos sobre Osmose Reversa, precisamos entender o que é Osmose. Osmose é o nome dado ao movimento da água entre meios com concentrações
Osmose Reversa Conheça este processo de purificação de água Antes de falarmos sobre Osmose Reversa, precisamos entender o que é Osmose. Osmose é o nome dado ao movimento da água entre meios com concentrações
