COMPORTAMENTO DOS GASES
|
|
|
- Ana Clara Bennert
- 5 Há anos
- Visualizações:
Transcrição
1 BC0102: ESTRUTURA DA MATÉRIA COMPORTAMENTO DOS GASES Hueder Paulo Moisés de Oliveira 1
2 Calendário Semana Aulas expositivas 1 07/06 Introdução ao curso (Informações sobre provas, conceitos); Macro ao micro; Teoria atômica. 2 11/06 Teoria atômica (continuação). 14/06 Hipótese atômica; Equações químicas; Substâncias químicas. 3 21/06 Comportamento dos gases; 2
3 Calendário Semana 4 25/06 Aulas expositivas Evidências do elétron. 28/06 Revisão de ondas; Radiatividade; Modelos atômicos. 5 05/07 Dualidade onda-partícula; Função de onda; 3
4 Calendário Semana 6 09/07 Aulas expositivas Orbitais atômicos; Spin do elétron, princípio da exclusão de Pauli e regras de seleção; 12/07 Prova /07 Átomos multi-eletrônicos; Distribuição eletrônica; Tabela periódica. 8 23/07 Ligações químicas (Parte I). 26/08 Interações Moleculares; 4
5 Calendário Semana Aulas expositivas 9 02/08 Ligações Químicas (Parte II): TLV e TOM /08 Prova 2 09/08 Prova Substitutiva 11 16/08 REC 5
6 Gases: O Ar Elementos que são gases a temperatura ambiente. Note que todos eles (menos os H) estão agrupados na tabela periódica. 6
7 Gases: Exemplos 7
8 Natureza dos Gases Muitas das propriedades físicas de diferentes gases são semelhantes entre si; Essa observação torna possível descrevê-los de maneira conjunta, em vez de tratar cada um isoladamente; Os gases são um exemplo de matéria formada por um número muito grande de moléculas; Observações: o ar é compressível: pode ser confinado em um volume menor do que o volume original. Os gases são mais compressíveis do que o sólidos e os líquidos isto sugere que há muito espaço livre entre as moléculas dos gases; Se expandem rapidamente para encher o espaço disponível. Ex: bexiga sendo esvaziada isto sugere que as moléculas se movem rapidamente. 8
9 Pressão Atmosférica A pressão (P) de uma gás é a força (F) exercida pelo gás, dividida pela área (A) sobre a qual a força se aplica : P = F A A gravidade exerce uma força sobre a atmosfera terrestre; Uma coluna de ar de 1 m 2 de seção transversal exerce uma força de 10 5 N; A pressão de uma coluna de ar de 1 m 2 é de 100 kpa. 1 Pa (pascal) = 1 Kg.m -1.s -2 1 atm = 10 5 Pa 1 bar = 10 5 Pa 760 Torr = 1 atm 9
10 Pressão Atmosférica Como medimos a pressão atmosférica? A pressão atmosférica é medida com um barômetro (com base na altura de uma coluna de mercúrio); A pressão atmosférica padrão é a pressão necessária para suportar 760 mm de Hg em uma coluna. h = 760 mm Evangelista Torricelli ( ) Barômetro 10
11 Pressão Atmosférica Como medimos a pressão atmosférica? As pressões de gases em recipientes fechados são medidas por dispositivos chamados manômetros; Um manômetro simples pode ser feito com um tubo em forma de U contendo Hg: Manômetro Se P gás < P atm então P gás + P h = P atm. Se P gás > P atm então P gás = P atm + P h. 11
12 Pressão Atmosférica Exemplo: Cálculo da pressão atmosférica a partir da altura de uma coluna de líquido. Suponha que a altura da coluna de mercúrio em um barômetro é 760 mm em 15ºC. Qual é a pressão atmosférica em pascals? Em 15ºC, a densidade do mercúrio é 13,595 g.cm -3 (que corresponde a kg.m -3 ) e a aceleração da gravidade na superfície da Terra é 9,80665 m.s -2. Resolução: 1 kg.m -1.s -2 = 1 Pa P = F A = m. g A d. h. A. g = A = d.h.g m = massa (kg) g = gravidade (m.s -2 ) h = altura (m) P = d.g.h P = (13595 kg.m -3 ) x (9,80665 m.s -2 ) x (0,760 m) P = 1,01 x 10 5 kg.m -1.s -2 = 1,01 x 10 5 Pa 12
13 Pressão Atmosférica Em termos do modelo dos gases, a pressão que um gás exerce sobre as paredes do recipiente que o contém é o resultado das colisões das moléculas com a superfície do recipiente; Quanto mais fortes as colisões das moléculas sobre a superfície, maior será a força e, consequentemente, a pressão. 13
14 Lei de Boyle para os Gases 1662: O volume de uma quantidade fixa de gás é inversamente proporcional à sua pressão. Robert Boyle ( ) 14
15 Lei de Boyle para os Gases 15
16 Lei de Boyle Isotermas Para um mesmo gás, numa mudança isotérmica: P 2 V 2 = P 1 V 1 16
17 Lei de Charles e Gay-Lussac Sabemos que balões de ar quente expandem quando são aquecidos. Lei de Charles e Gay-Lussac: A variação de volume de uma quantidade fixa de gás à pressão constante é diretamente proporcional à variação da temperatura. Jacques Charles ( ) Joseph Louis Gay-Lussac ( ) 17
18 Lei de Charles e Gay-Lussac 18
19 Lei de Charles e Gay-Lussac Um gráfico de V versus T é uma linha reta; Quando T é medida em C, a reta intercepta o eixo da temperatura em -273,15 C; Definimos o zero absoluto: 0 K = -273,15 C. T (K) = T ( o C) + 273,15 19
20 Lei de Avogadro A hipótese de Avogadro: volumes iguais de gases à mesma temperatura e pressão contêm o mesmo número de moléculas. Amedeo Avogadro ( ) 20
21 Lei de Avogadro Lei de Avogadro: O volume de gás a uma dada temperatura e pressão é diretamente proporcional à quantidade de matéria do gás. 21
22 Lei de Avogadro Princípio de Avogadro: Nas mesmas condições de temperatura e pressão, um determinado número de moléculas de gás ocupa o mesmo volume, independente de sua identidade química. V m = V n Vm = volume molar Sob as mesmas condições de temperatura e pressão: 22
23 Combinação das Leis: Equações dos Gases Ideais Lei de Boyle: Lei de Charles e Gay-Lussac: Lei de Avogadro: Podemos combiná-las em uma lei geral dos gases: A constante de proporcionalidade pode ser chamada de R (constante dos gases), então temos a equação dos gases ideais: ou 23
24 Combinação das Leis: Equações dos Gases Ideais 24
25 Combinação das Leis: Equações dos Gases Ideais O mesmo gás sob dois grupos de diferentes condições: Definimos CNTP (Condições Normais de Temperatura e Pressão): T = 0 C ou 273,15 K P = 1 atm. O volume de 1 mol de gás na CNTP é: 25
26 Combinação das Leis: Equações dos Gases Ideais Exemplo: Estequiometria das reações de gases O dióxido de carbono gerado pelos tripulantes na atmosfera artificial de submarinos e espaçonaves deve ser removido do ar, e o oxigênio recuperado. Grupos de projetistas de submarinos investigaram o uso do superóxido de potássio (KO 2 ), como purificador de ar, porque esse composto reage com o dióxido de carbono e libera oxigênio: 4KO 2(s) + 2CO 2(g) 2K 2 CO 3(s) + 3O 2(g) Calcule a massa de KO 2 que reage com 50 L de dióxido de carbono em 25ºC e 1 atm. Resolução: 1 mol CO 2 = 22,26 L x = 50 L x = 2,2462 mol CO 2 4 mol KO 2 = 2 mol CO 2 y = 2,2462 mol CO 2 y = 4,4924 mol KO 2 1 mol KO 2 = 71,10 g 4,4924 mol KO 2 = z z = 3,19 x 10² g KO 2 26
27 Lei de Dalton Mistura de Gases As moléculas de gás estão muito separadas e podemos supor que elas comportam-se independentemente. Lei de Dalton: A pressão total de uma mistura de gases é igual à soma das pressões parciais dos gases que a constituem. John Dalton ( ) P P P P total A pressão parcial de cada componente da mistura é a pressão que ele exerceria se estivesse sozinho no recipiente. 27
28 Lei de Dalton Mistura de Gases Assumindo comportamento ideal, cada gás obedece individualmente à equação dos gases: 28
29 Lei de Dalton Mistura de Gases Mistura do gás A com o gás B : 29
30 Determinação da Massa Molar de um Gás A densidade (d) tem unidades de massa por unidades de volume. Reajustando a equação dos gases ideais com M como massa molar, teremos: A massa molar de um gás pode ser determinada como se segue: 30
31 Combinação das Leis: Equações dos Gases Ideais Em pressão e temperatura fixas, quanto maior for a massa molar do gás, maior é a densidade; Quando a temperatura é constante, a densidade de um gás aumenta com a pressão. Neste caso, a pressão aumenta por adição de mais material ou por compressão (redução do volume); O aquecimento de um gás livre para se expandir sob pressão constante aumenta o volume ocupado pelo gás e, portanto, reduz sua densidade. Porque os balões de ar quente flutuam no ar? 31
32 Teoria Cinética dos Gases Teoria desenvolvida para explicar o comportamento dos gases. Suposições: 1. Os gases consistem de um grande número de moléculas em movimento aleatório constante. 2. O volume de moléculas individuais é desprezível comparado ao volume do recipiente. 3. As forças intermoleculares (forças entre moléculas de gases) são insignificantes. 4. Energia pode ser transferida entre as partículas durante as colisões, mas a ENERGIA TOTAL MÉDIA (E k ) é constante, ou seja, colisões são perfeitamente elásticas. 5. E K é proporcional à T. Podemos utilizar as equações de Newton para descrever o movimento das moléculas e entender o comportamento macroscópico dos gases! 32
33 Teoria Cinética dos Gases A ordem de grandeza da pressão é dada pela frequência e pela força da colisão das moléculas. Explica a lei de Boyle (PV = cte): À medida que o volume aumenta a temperatura constante, a velocidade cinética média do gás permanece constante. Entretanto, o volume aumenta fazendo com que as moléculas do gás tenham que viajar mais para atingirem as paredes do recipiente. Portanto, a pressão diminui. 33
34 Teoria Cinética dos Gases I. A energia cinética é a única contribuição à energia do gás; II. A energia pode ser transferida entre as moléculas; III. A energia cinética total é constante à temperatura constante; IV. A energia cinética média das moléculas é proporcional à temperatura. pv 1 2 nmu 3 massa molar das moléculas M u velocidade média quadrática das moléculas 1 2 pv constante pv nmu nrt 3 3RT c M
35 Teoria Cinética dos Gases NÍVEL MACROSCÓPICO NÍVEL SUBMICROSCÓPICO P V, n T Termodinâmica Estatística v F grandezas termodinâmicas grandezas mecânicas (flutuações, estatística) médias 35
36 Teoria Cinética dos Gases Distribuição de Maxwell-Boltzmann: distribuição das velocidades moleculares Em 1852, o físico escocês Maxwell encontrou a distribuição das velocidades moleculares de um gás. Seu resultado, conhecido como a lei da distribuição de velocidades de Maxwell-Boltzmann, é: P( v) 4 M 2 RT 3/2 Mv 2RT M = massa molar do gás, R = constante dos gases, T = temperatura do gás, v = módulo da velocidade molecular, P(v) = função distribuição de probabilidade de velocidade. v 2 e 2 James Clerk Maxwell ( ) 36
37 Teoria Cinética dos Gases Distribuição de Maxwell-Boltzmann: distribuição das velocidades moleculares O eixo y do gráfico de Maxwell-Boltzmann pode ser visto como o número de moléculas por unidade de velocidade. Então, se o gráfico está mais alto em uma dada região, significa que há mais moléculas de gás se movendo com aquelas velocidades. Observe que o gráfico não é simétrico. Há uma "cauda" mais longa na região das altas velocidades, na extremidade direita do gráfico. O gráfico continua à direita para velocidades extremamente altas, mas à esquerda o gráfico deve terminar em zero (já que uma molécula não pode ter uma velocidade menor que zero). 37
38 Teoria Cinética dos Gases Lei de Charles: Se a temperatura aumenta com volume constante, a energia cinética média das moléculas do gás aumenta. Consequentemente, há mais colisões com as paredes do recipiente e a pressão aumenta. k 38
39 Teoria Cinética dos Gases Se aquecermos o gás a uma temperatura maior, o pico do gráfico vai se deslocar para a direita (já que a velocidade molecular média vai aumentar). Conforme o gráfico se desloca para a direita, sua altura diminui para manter a mesma área total sob a curva (com o número total de moléculas constante). Da mesma forma, conforme o gás é resfriado a uma temperatura menor, o pico do gráfico é deslocado para a esquerda. Conforme o gráfico se desloca para a esquerda, sua altura aumenta para manter a mesma área sob a curva. Isso pode ser visto nas curvas abaixo, que representam a amostra de gás (com um número constante de moléculas) a temperaturas diferentes. Obs: Se mais moléculas fossem inseridas na amostra, a área total sob a curva aumentaria. Da mesma forma, se moléculas fossem retiradas da amostra, a área total sob a curva diminuiria. 39
40 Teoria Cinética dos Gases A energia cinética média é a mesma para qualquer gás a uma dada temperatura, então se m é grande, u é pequeno k A temperatura (grandeza macroscópica) está diretamente ligada à velocidade quadrática média das partículas (grandeza microscópica) ou à energia cinética média. 3RT u 2 M 40
41 Teoria Cinética dos Gases De onde vem este termo:? L v L Qual é a relação entre a pressão P, exercida pelo gás sobre as paredes da caixa e a velocidade média das moléculas? L n mol de um gás ideal em uma caixa cúbica de volume V. As paredes da caixa estão na temperatura T. 41
42 Teoria Cinética dos Gases Ignorando as colisões entre as moléculas e considerando apenas as colisões elásticas com as paredes, a variação de momento é: px = (-mv x ) (mv x ) = - 2mv x Momento atribuído à parede A 2ª Lei de Newton fornece a força experimentada pela molécula na colisão com a parede: F = m.a F = m. v x / t = (mv x ) / t Força: mudança de momento por unidade de tempo F = (variação de momento / impacto) x (nº de impactos / unidade de tempo) px / t = 2mv x / (2L/ 2mv x ) = mv x2 /L De acordo com a 2ª Lei de Newton, a taxa com a qual o momento é transferido para a parede é a força que age sobre a parede. Portanto, para determinar a força total, deve-se somar as contribuições de todas as moléculas: 42
43 Teoria Cinética dos Gases P = F x /L 2 = [(mv x12 /L) + (mv x22 /L) + (mv x32 /L) (mv xn2 /L)] / L 2 P = (m/l 3 )(v x1 2 + v x2 2 + v x v xn 2 ) sendo N (nº de moléculas) = n.n A P = (n.m.n A / L 3 )(v 2 x ) P = n. M. (v 2 x ) média /V Considerando: v 2 = v 2 x + v 2 y + v 2 z v 2 x = 1/3v 2 P = n.m.(v 2 ) média /3V v 2 média = v Vrms = rms 43
44 Lei da Efusão de Graham Considere dois gases com massas molares M 1 e M 2, a velocidade relativa de efusão é dada por: r r 1 2 u u 1 2 3RT 3RT M M1 2 M 2 M 1 Thomas Graham ( ) As moléculas escapam de seu recipiente para um espaço evacuado apenas quando batem no buraco. Consequentemente, quanto mais alta for a vqm, maior será a probabilidade de uma molécula de gás bater no buraco. 44
45 Gases reais: Desvios do Comportamento Ideal Os gases reais são formados por átomos ou moléculas sujeitos a atrações e repulsões intermoleculares. As atrações tem um alcance maior do que as repulsões. 45
46 Gases reais: Desvios do Comportamento Ideal Quando diminui a distância intermolecular, há duas consequências: O volume individual das moléculas passa a ser mais evidente; As interações intermoleculares tornam-se mais relevantes. 46
47 Gases reais: Desvios do Comportamento Ideal Da equação do gás ideal, temos PV RT = n Para 1 mol de gás, PV/RT = 1 a todas as temperaturas. A partir das suposições na teoria cinética, podemos imaginar em que situações um gás NÃO se comportará como gás ideal: as moléculas de um gás têm volume finito; as moléculas de um gás se atraem. 47
48 Gases reais: Desvios do Comportamento Ideal PV/RT versus pressão para 1 mol de vários gases a 300 K. 48
49 Gases reais: Desvios do Comportamento Ideal À medida que a temperatura aumenta, as moléculas de gás se movem mais rapidamente e se distanciam mais entre si; Altas temperaturas significam também mais energia disponível para a quebra das forças intermoleculares, portanto comportamento mais próximo da idealidade. PV/RT versus pressão para 1 mol de gás nitrogênio a três temperaturas diferentes. 49
50 Gases reais: Desvios do Comportamento Ideal O fator de compressibilidade (Z) é uma medida de força e do tipo de forças intermoleculares. Quando Z > 1 as repulsões intermoleculares são dominantes, e quando Z < 1 as atrações dominam. O valor de Z varia com a pressão: 50
51 Gases reais: Desvios do Comportamento Ideal O gás à temperatura de Boyle (T B ) apresenta comportamento ideal num intervalo maior de variação da pressão. Exemplos: 51
52 Gases reais: Desvios do Comportamento Ideal Equação de van der Waals Adicionamos dois termos à equação do gás ideal: um para corrigir o volume das moléculas e o outro para corrigir as atrações intermoleculares; Os termos de correção geram a equação de van der Waals: P = nrt V nb n2 a V 2 ou P+ 2 n a 2 V V nb = nrt Johannes Diderik van der Waals ( ) Nobel (Física): 1910 correção para o volume das moléculas correção para a atração molecular onde a (forças atrativas) e b (forças repulsivas) são constantes empíricas tabeladas. 52
53 Gases reais: Desvios do Comportamento Ideal Parâmetros tabelados da equação de van der Waals: 53
54 Fenômenos de Transporte Condutividade térmica transporte de calor Difusão transporte de moléculas Viscosidade transporte de momento Efusão Difusão Todas essas propriedades dependem da distância que a molécula irá percorrer antes de colidir com outra molécula. 54
55 Caminho livre médio A distância média percorrida antes de haver a colisão é denominada CAMINHO LIVRE MÉDIO. A figura mostra a trajetória de uma molécula típica quando ela se move através do gás. Entre colisões, a molécula se move em linha reta com velocidade constante mudando abruptamente tanto o módulo quanto o sentido da velocidade quando ela colide elasticamente com outras moléculas. 55
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
GASES. https://www.youtube.com/watch?v=wtmmvs3uiv0. David P. White. QUÍMICA: A Ciência Central 9ª Edição Capítulo by Pearson Education
 GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
Características dos gases
 Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre formam misturas
Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre formam misturas
AULA 03 GASES Cap. 4 Russel PROF. MARCELL MARIANO CORRÊA MACENO
 AULA 03 GASES Cap. 4 Russel PROF. MARCELL MARIANO CORRÊA MACENO Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
AULA 03 GASES Cap. 4 Russel PROF. MARCELL MARIANO CORRÊA MACENO Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
Estudo Físico-Químico dos Gases
 19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS. Prof. MSc. Danilo Cândido
 FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS Prof. MSc. Danilo Cândido CONCEITOS DE GASES Um gás representa a forma mais simples da matéria, de baixa densidade e que ocupa o volume total de qualquer recipiente
FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS Prof. MSc. Danilo Cândido CONCEITOS DE GASES Um gás representa a forma mais simples da matéria, de baixa densidade e que ocupa o volume total de qualquer recipiente
QUÍMICA I Gases
 QUÍMICA I 106201 Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre
QUÍMICA I 106201 Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre
Gases. Reis, Oswaldo Henrique Barolli. R375g Gases / Oswaldo Henrique Barolli. Varginha, slides : il.
 Gases Reis, Oswaldo Henrique Barolli. R375g Gases / Oswaldo Henrique Barolli. Varginha, 2015. 21 slides : il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World Wide Web 1. Dinâmica dos gases.
Gases Reis, Oswaldo Henrique Barolli. R375g Gases / Oswaldo Henrique Barolli. Varginha, 2015. 21 slides : il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World Wide Web 1. Dinâmica dos gases.
Físico-Química I. Profa. Dra. Carla Dalmolin. Gases. Gás perfeito (equações de estado e lei dos gases) Gases reais
 Físico-Química I Profa. Dra. Carla Dalmolin Gases Gás perfeito (equações de estado e lei dos gases) Gases reais Gás Estado mais simples da matéria Uma forma da matéria que ocupa o volume total de qualquer
Físico-Química I Profa. Dra. Carla Dalmolin Gases Gás perfeito (equações de estado e lei dos gases) Gases reais Gás Estado mais simples da matéria Uma forma da matéria que ocupa o volume total de qualquer
Gases UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG120. Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI
 UNIERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG10 http://www.met.reading.ac.uk/~swrmethn/balloon/ Gases Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI A Estrutura
UNIERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG10 http://www.met.reading.ac.uk/~swrmethn/balloon/ Gases Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI A Estrutura
Gases. Compostos orgânicos de baixa massa molar são gases a temperatura ambiente. CH 4 (metano gás natural), C 3 H 8
 Gases CAPÍTULO 4 AS PROPRIEDADES DOS GASES / A NATUREZA DOS GASES/ AS LEIS DOS GASES / O MOVIMENTO MOLECULAR / O MODELO CINÉTICO DOS GASES / OS GASES REAIS Introdução Gases Atmosfera 11 elementos são encontrados
Gases CAPÍTULO 4 AS PROPRIEDADES DOS GASES / A NATUREZA DOS GASES/ AS LEIS DOS GASES / O MOVIMENTO MOLECULAR / O MODELO CINÉTICO DOS GASES / OS GASES REAIS Introdução Gases Atmosfera 11 elementos são encontrados
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2. Propriedades Moleculares dos Gases
 CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
Professora : Elisângela Moraes
 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA -EEL Professora : Elisângela Moraes 02/03/2012 PROGRAMA RESUMIDO 1. Gases Ideais; 2. Gases Reais; 3. Termodinâmica; 4. Termoquímica; 5. Entropia;
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA -EEL Professora : Elisângela Moraes 02/03/2012 PROGRAMA RESUMIDO 1. Gases Ideais; 2. Gases Reais; 3. Termodinâmica; 4. Termoquímica; 5. Entropia;
Luis Eduardo C. Aleotti. Química. Aula 38 - Transformações Gasosas
 Luis Eduardo C. Aleotti Química Aula 38 - Transformações Gasosas TRANSFORMAÇÕES GASOSAS Gás e Vapor - Gás: Substância gasosa em temperatura ambiente. - Vapor: Estado gasoso de uma substância líquida ou
Luis Eduardo C. Aleotti Química Aula 38 - Transformações Gasosas TRANSFORMAÇÕES GASOSAS Gás e Vapor - Gás: Substância gasosa em temperatura ambiente. - Vapor: Estado gasoso de uma substância líquida ou
Teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
Avenida Lourival Alfredo, 176, Poeira, Marechal Deodoro, Alagoas, Brasil,
 1 ESTUDO DOS GASES 1 INTRODUÇÃO Vários processos que ocorrem na natureza e nos organismos vivos são fenômenos pertinentes aos gases, como, por exemplo: o metabolismo nos animais exige a presença de oxigênio,
1 ESTUDO DOS GASES 1 INTRODUÇÃO Vários processos que ocorrem na natureza e nos organismos vivos são fenômenos pertinentes aos gases, como, por exemplo: o metabolismo nos animais exige a presença de oxigênio,
Universidade Federal do Pampa UNIPAMPA. Teoria Cinética do Gases
 Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
A teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
Física II FEP 112 ( ) 1º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Estrutura da Matéria Prof. Fanny Nascimento Costa
 Estrutura da Matéria Prof. Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 03 Gases e suas propriedades; Conservação de massa e volume (teoria cinética). Gases Os gases são o estado mais simples
Estrutura da Matéria Prof. Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 03 Gases e suas propriedades; Conservação de massa e volume (teoria cinética). Gases Os gases são o estado mais simples
Gases ideais. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 217 Gás = conjunto de moléculas ou átomos
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 217 Gás = conjunto de moléculas ou átomos
Gases ideais. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 317 Gás = conjunto de moléculas ou átomos
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 317 Gás = conjunto de moléculas ou átomos
Combustíveis Energia e Ambiente. Combustíveis gasosos, líquidos e sólidos: compreender as diferenças
 Combustíveis gasosos, líquidos e sólidos: compreender as diferenças 1 Estados físicos de hidrocarbonetos em função do número de carbonos da cadeia Os gases combustíveis podem ser agrupados em famílias,
Combustíveis gasosos, líquidos e sólidos: compreender as diferenças 1 Estados físicos de hidrocarbonetos em função do número de carbonos da cadeia Os gases combustíveis podem ser agrupados em famílias,
UFABC Fenômenos Térmicos Prof. Germán Lugones. Aula 5: Livre caminho médio, distribuição de Maxwell-Boltzmann
 UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 5: Livre caminho médio, distribuição de Maxwell-Boltzmann Caminho Livre Médio A Figura mostra a trajetória de uma molécula típica quando ela se move através
UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 5: Livre caminho médio, distribuição de Maxwell-Boltzmann Caminho Livre Médio A Figura mostra a trajetória de uma molécula típica quando ela se move através
Teoria Cinética dos gases
 Estrutura da Matéria Unidade II: A matéria fragmentada Aula 5: Origem estatística e corpuscular da termodinâmica http://professor.ufabc.edu.br/~pieter.westera/estrutura.html Teoria Cinética dos gases Bernoulli
Estrutura da Matéria Unidade II: A matéria fragmentada Aula 5: Origem estatística e corpuscular da termodinâmica http://professor.ufabc.edu.br/~pieter.westera/estrutura.html Teoria Cinética dos gases Bernoulli
Gases. 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação?
 Capítulo 2 Gases 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação? Van der Waals verificou que o fato do gás real não se comportar como o gás ideal é
Capítulo 2 Gases 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação? Van der Waals verificou que o fato do gás real não se comportar como o gás ideal é
As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana.
 Estudo dos gases Gás Ideal As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana. As moléculas não exercem força uma sobre as outras, exceto quando
Estudo dos gases Gás Ideal As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana. As moléculas não exercem força uma sobre as outras, exceto quando
GASES. QUIMICA II a Unidade
 GASES QUIMICA II a Unidade Estado Físico de uma Substância sólido > líquido > gasoso Aumento do volume O estado de agregação da matéria varia com a distância entre as partículas que compõem a substância
GASES QUIMICA II a Unidade Estado Físico de uma Substância sólido > líquido > gasoso Aumento do volume O estado de agregação da matéria varia com a distância entre as partículas que compõem a substância
Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a. o resultado do movimento dos átomos e moléculas.
 TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal.
 Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal. Equações de Estado Não é fácil trabalhar com as tabelas termodinâmicas. A dificuldade está associada ao volume delas e a possibilidade
Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal. Equações de Estado Não é fácil trabalhar com as tabelas termodinâmicas. A dificuldade está associada ao volume delas e a possibilidade
11/08/2014. Lei de Avogadro. Equação de Clayperon. CNTP 1 atm 0 C 273K
 Disciplina de Físico Química I - Equação de Clapeyron Misturas Gases reais. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.br Lei de Avogadro 1 Lei de Avogadro Equação de Clayperon CNTP 1
Disciplina de Físico Química I - Equação de Clapeyron Misturas Gases reais. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.br Lei de Avogadro 1 Lei de Avogadro Equação de Clayperon CNTP 1
Física Geral II. Aula 1 - Teoria cinética dos gases. D. Valin 1. Universidade do Estado de Mato Grosso. Sinop-MT, April 25, 2017
 Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Soluções e Gases III. Gases
 Soluções e Gases III Gases Gases Gás é um material que preenche todo o espaço ou volume do recipiente em que se encontra, independentemente do tamanho do recipiente. Ar 78 % de N 2 21% de O 2 1% de outros
Soluções e Gases III Gases Gases Gás é um material que preenche todo o espaço ou volume do recipiente em que se encontra, independentemente do tamanho do recipiente. Ar 78 % de N 2 21% de O 2 1% de outros
UFABC - BC Prof. Germán Lugones. AULA 7 Teoria Cinética dos Gases I
 UFABC - BC0205 - Prof. Germán Lugones AULA 7 Teoria Cinética dos Gases I Teoria cinética dos gases o Um gás consiste em partículas (e.g. átomos ou moléculas) que preenchem o volume de seu recipiente e
UFABC - BC0205 - Prof. Germán Lugones AULA 7 Teoria Cinética dos Gases I Teoria cinética dos gases o Um gás consiste em partículas (e.g. átomos ou moléculas) que preenchem o volume de seu recipiente e
Capítulo 1. Propriedades dos Gases
 Capítulo 1. Propriedades dos Gases Baseado no livro: Atkins Physical Chemistry Eighth Edition Peter Atkins Julio de Paula 14-03-2007 Maria da Conceição Paiva 1 O estado físico de uma substância A equação
Capítulo 1. Propriedades dos Gases Baseado no livro: Atkins Physical Chemistry Eighth Edition Peter Atkins Julio de Paula 14-03-2007 Maria da Conceição Paiva 1 O estado físico de uma substância A equação
Moléculas em Movimento
 Físico-Química II Profa. Dra. Carla Dalmolin Moléculas em Movimento Modelo Cinético dos Gases Modelo Cinético dos Gases A única contribuição para a energia do gás vem das energias cinéticas das moléculas
Físico-Química II Profa. Dra. Carla Dalmolin Moléculas em Movimento Modelo Cinético dos Gases Modelo Cinético dos Gases A única contribuição para a energia do gás vem das energias cinéticas das moléculas
Termodinâmica 7. Alexandre Diehl. Departamento de Física - UFPel
 Termodinâmica 7 Alexandre Diehl Departamento de Física - UFPel Robert Boyle (1627-1691) Experimentos com tubo manométrico mercúrio 2 Robert Boyle (1627-1691) Experimentos com tubo manométrico 3 Robert
Termodinâmica 7 Alexandre Diehl Departamento de Física - UFPel Robert Boyle (1627-1691) Experimentos com tubo manométrico mercúrio 2 Robert Boyle (1627-1691) Experimentos com tubo manométrico 3 Robert
O ESTADO GASOSO - CARACTERÍSTICAS GERAIS
 Estado Gasoso O ESTADO GASOSO - CARACTERÍSTICAS GERAIS Os gases sempre tendem a ocupar todo o volume do recipiente que os contém (capacidade de expansão) Os gases têm massa (Volumes iguais de gases diferentes
Estado Gasoso O ESTADO GASOSO - CARACTERÍSTICAS GERAIS Os gases sempre tendem a ocupar todo o volume do recipiente que os contém (capacidade de expansão) Os gases têm massa (Volumes iguais de gases diferentes
25/Fev/2015 Aula 2. 20/Fev/2015 Aula 1
 /Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
/Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
ATMOSFERA. Volume molar; constante de Avogadro
 ATMOSFERA Volume molar; constante de Avogadro 25-01-2011 Dulce Campos 2 O ar é uma solução gasosa Enquanto solução gasosa tem comportamentos semelhantes aos das substâncias gasosas 25-01-2011 Dulce Campos
ATMOSFERA Volume molar; constante de Avogadro 25-01-2011 Dulce Campos 2 O ar é uma solução gasosa Enquanto solução gasosa tem comportamentos semelhantes aos das substâncias gasosas 25-01-2011 Dulce Campos
4. Propriedades dos gases experimentos e modelo microscópico simples para a temperatura
 PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
Apostila de Química 01 Estudo dos Gases
 Apostila de Química 01 Estudo dos Gases 1.0 Conceitos Pressão: Número de choques de suas moléculas contra as paredes do recipiente. 1atm = 760mHg = 760torr 105Pa (pascal) = 1bar. Volume 1m³ = 1000L. Temperatura:
Apostila de Química 01 Estudo dos Gases 1.0 Conceitos Pressão: Número de choques de suas moléculas contra as paredes do recipiente. 1atm = 760mHg = 760torr 105Pa (pascal) = 1bar. Volume 1m³ = 1000L. Temperatura:
baixa pressão e alta temperatura
 É um dos estados da matéria, não tem forma e volume definidos, e consiste em uma coleção de partículas cujos os movimentos são aproximadamente aleatórios. As forças de coesão entre as partículas que formam
É um dos estados da matéria, não tem forma e volume definidos, e consiste em uma coleção de partículas cujos os movimentos são aproximadamente aleatórios. As forças de coesão entre as partículas que formam
Capítulo 21 Temperatura
 Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
EXPERIÊNCIA 2 DETERMINAÇÃO DA MASSA MOLECULAR DE UM GÁS EFEITO DA PRESSÃO NO PONTO DE EBULIÇÃO
 1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Interpretar as leis que regem o comportamento dos gases ideais. Utilizar a equação da lei do gás ideal, PV = nrt Medir o volume e a
1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Interpretar as leis que regem o comportamento dos gases ideais. Utilizar a equação da lei do gás ideal, PV = nrt Medir o volume e a
Estudo dos gases. Prof. Leandro Zatta - Química Geral 1
 Estudo dos gases Prof. Leandro Zatta - Química Geral 1 Modelo molecular dos gases Há pouca matéria em um dado volume Existência de muito espaço vazio entre as moléculas individuais São tão facilmente comprimidos
Estudo dos gases Prof. Leandro Zatta - Química Geral 1 Modelo molecular dos gases Há pouca matéria em um dado volume Existência de muito espaço vazio entre as moléculas individuais São tão facilmente comprimidos
DURAÇÃO DA PROVA Manual da disciplina, livros de Química, computador, Trabalho Escrito. Conteúdos Objetivos e/ou Competências Estrutura Cotações
 ÉPOCA ESPECIAL DE EXAMES ANO LETIVO 2011/2012 MATRIZ DO EXAME DO MÓDULO QM6 Estado Físico das Substâncias e Interações Moleculares. Estado Gasoso. Química MATERIAL A UTILIZAR TIPO DE PROVA DURAÇÃO DA PROVA
ÉPOCA ESPECIAL DE EXAMES ANO LETIVO 2011/2012 MATRIZ DO EXAME DO MÓDULO QM6 Estado Físico das Substâncias e Interações Moleculares. Estado Gasoso. Química MATERIAL A UTILIZAR TIPO DE PROVA DURAÇÃO DA PROVA
Capítulo 10. 2005 by Pearson Education
 QUÍMICA A Ciência Central 9ª Edição Gases David P. White Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
QUÍMICA A Ciência Central 9ª Edição Gases David P. White Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
AS PROPRIEDADES DOS GASES. Apresentar as propriedades dos gases; explicitar as diferentes propriedades dos gases reais e dos gases perfeitos;
 AS PROPRIEDADES DOS GASES Metas Apresentar as propriedades dos gases; explicitar as diferentes propriedades dos gases reais e dos gases perfeitos; Objetivos Ao final desta aula, o aluno deverá: compreender
AS PROPRIEDADES DOS GASES Metas Apresentar as propriedades dos gases; explicitar as diferentes propriedades dos gases reais e dos gases perfeitos; Objetivos Ao final desta aula, o aluno deverá: compreender
Estequiometria. Mestranda: Daniele Potulski Disciplina: Química da madeira I
 Estequiometria Mestranda: Daniele Potulski Disciplina: Química da madeira I Estequiometria Estequiometria é o cálculo da quantidade de reagentes e produtos da reação, baseado nas leis das reações químicas.
Estequiometria Mestranda: Daniele Potulski Disciplina: Química da madeira I Estequiometria Estequiometria é o cálculo da quantidade de reagentes e produtos da reação, baseado nas leis das reações químicas.
GASES. Maira Gazzi Manfro e Giseli Menegat
 GASES Maira Gazzi Manfro e Giseli Menegat maira.manfro@caxias.ifrs.edu.br giseli.menegat@caxias.ifrs.edu.br Características dos Gases São menos densos que os sólidos e os líquidos; Sempre se misturam entre
GASES Maira Gazzi Manfro e Giseli Menegat maira.manfro@caxias.ifrs.edu.br giseli.menegat@caxias.ifrs.edu.br Características dos Gases São menos densos que os sólidos e os líquidos; Sempre se misturam entre
Física II Teoria Cinética dos Gases
 Física II Teoria Cinética dos Gases João Francisco Fuzile Rodrigues Garcia -- 8549323 Maiara Fernanda Moreno -- 8549344 Otávio Massola Sumi -- 8549452 Ex. 18.63 Explique, em termos do movimento molecular,
Física II Teoria Cinética dos Gases João Francisco Fuzile Rodrigues Garcia -- 8549323 Maiara Fernanda Moreno -- 8549344 Otávio Massola Sumi -- 8549452 Ex. 18.63 Explique, em termos do movimento molecular,
Gases. Teoria cinética
 Gases Teoria cinética Para os gases, muitas propriedades podem ser explicadas com o auxílio de um modelo microscópico muito rudimentar, criado quase um século antes da teoria atômica. Em 1738, o suíço
Gases Teoria cinética Para os gases, muitas propriedades podem ser explicadas com o auxílio de um modelo microscópico muito rudimentar, criado quase um século antes da teoria atômica. Em 1738, o suíço
Teoria Cinética dos Gases. Lucy V. C. Assali. Física II IO
 Teoria Cinética dos Gases Física II 2016 - IO Teoria Atômica da Matéria 1. Hipótese atômica na antiguidade: ideia de elementos primordiais que comporiam a matéria matéria constituída de minúsculas partículas,
Teoria Cinética dos Gases Física II 2016 - IO Teoria Atômica da Matéria 1. Hipótese atômica na antiguidade: ideia de elementos primordiais que comporiam a matéria matéria constituída de minúsculas partículas,
Estado Gasoso. Características. Expansibilidade compressibilidade. Situação de um gás. Variáveis de estado
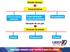 Estado Gasoso Características Forma/volume variáveis Expansibilidade compressibilidade Situação de um gás Difusibilidade Variáveis de estado Volume emperatura Pressão Mudança de estado de uma certa massa
Estado Gasoso Características Forma/volume variáveis Expansibilidade compressibilidade Situação de um gás Difusibilidade Variáveis de estado Volume emperatura Pressão Mudança de estado de uma certa massa
Tópicos da História da Física Clássica
 Tópicos da História da Física Clássica Lei dos Gases Victor O. Rivelles Instituto de Física da Universidade de São Paulo Edifício Principal, Ala Central, sala 314 e-mail: rivelles@fma.if.usp.br http://www.fma.if.usp.br/~rivelles
Tópicos da História da Física Clássica Lei dos Gases Victor O. Rivelles Instituto de Física da Universidade de São Paulo Edifício Principal, Ala Central, sala 314 e-mail: rivelles@fma.if.usp.br http://www.fma.if.usp.br/~rivelles
AULA 8 Teoria Cinética dos Gases II
 UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
ELEMENTOS QUE FORMAM GASES NAS CONDIÇÕES NORMAIS
 ELEMENTOS QUE FORMAM GASES NAS CONDIÇÕES NORMAIS Substância no estado gasoso é definida por 4 qualidades: Volume Quantidade de matéria (mol) Temperatura Pressão 1. fase gasosa Átomos He Ar (gases nobres)
ELEMENTOS QUE FORMAM GASES NAS CONDIÇÕES NORMAIS Substância no estado gasoso é definida por 4 qualidades: Volume Quantidade de matéria (mol) Temperatura Pressão 1. fase gasosa Átomos He Ar (gases nobres)
Química Prof. Giacometto
 Química Prof. Giacometto LISTA DE EXERCÍCIOS SOBRE O ESTADO GASOSO (SÓ UEM) OBS: SEMPRE QUE JULGAR NECESSÁRIO O VALOR DA MASSA ATÔMICA DE UM ELEMENTO QUÍMICO, UTILIZAR A TABELA PERIÓDICA 01) (UEM) Considerando
Química Prof. Giacometto LISTA DE EXERCÍCIOS SOBRE O ESTADO GASOSO (SÓ UEM) OBS: SEMPRE QUE JULGAR NECESSÁRIO O VALOR DA MASSA ATÔMICA DE UM ELEMENTO QUÍMICO, UTILIZAR A TABELA PERIÓDICA 01) (UEM) Considerando
Metal, Não Metal e Metaloide
 Metal, Não Metal e Metaloide 1 Metal, Não Metal e Metaloide Metal: conduz eletricidade, tem brilho, é maleável e dúctil Ex: cobre Não metal: não... Ex: Enxofre Metaloide: aparência e algumas propriedades
Metal, Não Metal e Metaloide 1 Metal, Não Metal e Metaloide Metal: conduz eletricidade, tem brilho, é maleável e dúctil Ex: cobre Não metal: não... Ex: Enxofre Metaloide: aparência e algumas propriedades
Vejamos agora alguns casos particulares dessas transformações com quantidade de gás constante.
 Setor 2306 Aula 06 Transformações Gasosas em sistemas fechados Complemento. Como vimos em aula, as transformações realizadas em sistemas fechados tem sua quantidade de gás constante. Nessa situação, a
Setor 2306 Aula 06 Transformações Gasosas em sistemas fechados Complemento. Como vimos em aula, as transformações realizadas em sistemas fechados tem sua quantidade de gás constante. Nessa situação, a
Descrição Macroscópica de um Gás ideal
 Descrição Macroscópica de um Gás ideal O gás não tem volume fixo ou uma pressão fixa O volume do gás é o volume do recipiente A pressão do gás depende do tamanho do recipiente A equação de estado relaciona
Descrição Macroscópica de um Gás ideal O gás não tem volume fixo ou uma pressão fixa O volume do gás é o volume do recipiente A pressão do gás depende do tamanho do recipiente A equação de estado relaciona
André Silva Franco ASF EOQ Escola Olímpica de Química Julho de 2011
 André Silva Franco ASF EOQ Escola Olímpica de Química Julho de 2011 Conceitos Básicos Gás é um estado da matéria; as partículas de massa m estão em movimento incessante e caótico; O tamanho das partículas
André Silva Franco ASF EOQ Escola Olímpica de Química Julho de 2011 Conceitos Básicos Gás é um estado da matéria; as partículas de massa m estão em movimento incessante e caótico; O tamanho das partículas
6/Mar/2013 Aula 7 Entropia Variação da entropia em processos reversíveis Entropia e os gases ideais
 6/Mar/01 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
6/Mar/01 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
Prática 03 Determinação do Zero Absoluto
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 03 Determinação do Zero Absoluto 1. Introdução
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 03 Determinação do Zero Absoluto 1. Introdução
Capítulo 11 - Teoria Cinética dos Gases. O número de Avogrado é número de moléculas contido em 1 mol de qualquer substãncia
 Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
Propriedades de uma substância pura
 Propriedades de uma substância pura Substância pura possui composição química invariável e homogênea, independentemente da fase em que está. Ex.: água Equilíbrio de fases em uma substância pura, as fases
Propriedades de uma substância pura Substância pura possui composição química invariável e homogênea, independentemente da fase em que está. Ex.: água Equilíbrio de fases em uma substância pura, as fases
FUNDAMENTOS FÍSICOS DO AR COMPRIMIDO
 DEFINIÇÃO: O ar é incolor, insípido e é uma mistura de diversos gases. Composição percentual do ar seco padrão: (ISO 2533). Elementos Percentual em volume Percentual em massa Nitrogênio 78,08 75,52 Oxigênio
DEFINIÇÃO: O ar é incolor, insípido e é uma mistura de diversos gases. Composição percentual do ar seco padrão: (ISO 2533). Elementos Percentual em volume Percentual em massa Nitrogênio 78,08 75,52 Oxigênio
CAPITULO 1 Propriedades dos gases. PGCEM Termodinâmica dos Materiais UDESC
 CAPITULO 1 Propriedades dos gases PGCEM Termodinâmica dos Materiais UDESC Referência Bibliográfica ATKINS, P.; Paula, J. de. Fisico-Química, Vol 1. 8ª ed., Editora LTC, Rio de Janeiro, 2006, cap 1. Ball,
CAPITULO 1 Propriedades dos gases PGCEM Termodinâmica dos Materiais UDESC Referência Bibliográfica ATKINS, P.; Paula, J. de. Fisico-Química, Vol 1. 8ª ed., Editora LTC, Rio de Janeiro, 2006, cap 1. Ball,
1,0 atm; 3,0 atm; 3,3 atm; 3,9 atm; 4,0 atm.
 1. Um tubo cilíndrico de oxigênio de um mergulhador contém 3,2 kg de O 2. Antes de mergulhar, verificou-se que a temperatura e a pressão no interior do cilindro valiam, respectivamente, 27 C e 1,5 atm.
1. Um tubo cilíndrico de oxigênio de um mergulhador contém 3,2 kg de O 2. Antes de mergulhar, verificou-se que a temperatura e a pressão no interior do cilindro valiam, respectivamente, 27 C e 1,5 atm.
Todo gás exerce uma PRESSÃO, ocupando um certo VOLUME à determinada TEMPERATURA
 Todo gás exerce uma PRESSÃO, ocupando um certo VOLUME à determinada TEMPERATURA Aos valores da pressão, do volume e da temperatura chamamos de ESTADO DE UM GÁS Assim: V 5 L T 300 K P 1 atm Os valores da
Todo gás exerce uma PRESSÃO, ocupando um certo VOLUME à determinada TEMPERATURA Aos valores da pressão, do volume e da temperatura chamamos de ESTADO DE UM GÁS Assim: V 5 L T 300 K P 1 atm Os valores da
BC0102: ESTRUTURA DA MATÉRIA HIPÓTESE ATÔMICA. Hueder Paulo Moisés de Oliveira.
 BC0102: ESTRUTURA DA MATÉRIA HIPÓTESE ATÔMICA hueder.paulo@ufabc.edu.br Hueder Paulo Moisés de Oliveira 1 Calendário Semana Aulas expositivas 1 07/06 Introdução ao curso (Informações sobre provas, conceitos);
BC0102: ESTRUTURA DA MATÉRIA HIPÓTESE ATÔMICA hueder.paulo@ufabc.edu.br Hueder Paulo Moisés de Oliveira 1 Calendário Semana Aulas expositivas 1 07/06 Introdução ao curso (Informações sobre provas, conceitos);
= 6, mol de moléculas de um gás possui aproximadamente 6, moléculas deste gás, ou seja, seiscentos e dois sextilhões de moléculas;
 TEORIA CINÉTICA DOS GASES PROF. LEANDRO NECKEL NÚMERO DE AVOGADRO Mol é a quantidade de substância de um sistema que contém tantas entidades elementares quanto são os átomos contidos em 0,012 quilograma
TEORIA CINÉTICA DOS GASES PROF. LEANDRO NECKEL NÚMERO DE AVOGADRO Mol é a quantidade de substância de um sistema que contém tantas entidades elementares quanto são os átomos contidos em 0,012 quilograma
01) (UPE-2011-Q1) Em relação à teoria cinética molecular dos gases, é CORRETO afirmar que:
 01) (UPE-2011-Q1) Em relação à teoria cinética molecular dos gases, é CORRETO afirmar que: a) a energia cinética média de um conjunto de moléculas de um gás depende, apenas e exclusivamente, das massas
01) (UPE-2011-Q1) Em relação à teoria cinética molecular dos gases, é CORRETO afirmar que: a) a energia cinética média de um conjunto de moléculas de um gás depende, apenas e exclusivamente, das massas
11/Mar/2016 Aula 7 Entropia Variação da entropia em processos reversíveis Entropia e os gases ideais
 11/Mar/016 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
11/Mar/016 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
Conceitos Básicos sobre gases
 Conceitos Básicos sobre gases ara este estudo não vamos fazer distinção entre gás e vapor, desta forma neste capítulo, o estado gasoso (gás ou vapor) será sempre referido como gás... ressão dos gases Suponha
Conceitos Básicos sobre gases ara este estudo não vamos fazer distinção entre gás e vapor, desta forma neste capítulo, o estado gasoso (gás ou vapor) será sempre referido como gás... ressão dos gases Suponha
19.2 Número de Avogadro mol número de átomos em uma amostra de 12g do carbono-12. Num mol de qualquer substância existem
 Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
Hidrostática REVISÃO ENEM O QUE É UM FLUIDO? O QUE É MASSA ESPECÍFICA? OBSERVAÇÕES
 REVISÃO ENEM Hidrostática O QUE É UM FLUIDO? Fluido é denominação genérica dada a qualquer substância que flui isto é, escoa e não apresenta forma própria, pois adquire a forma do recipiente que o contém.
REVISÃO ENEM Hidrostática O QUE É UM FLUIDO? Fluido é denominação genérica dada a qualquer substância que flui isto é, escoa e não apresenta forma própria, pois adquire a forma do recipiente que o contém.
Estrutura da Matéria Hipótese Atômica 1. Hipótese na antiquidade 2.Conceito de elementos e lei da proporções 3.Hipótese de Avogadro 4.
 Estrutura da Matéria Hipótese Atômica 1. Hipótese na antiquidade 2.Conceito de elementos e lei da proporções 3.Hipótese de Avogadro 4.Massa Atômica e molecular 5.Lei dos gases ideais 6.Lei de Van der Waals
Estrutura da Matéria Hipótese Atômica 1. Hipótese na antiquidade 2.Conceito de elementos e lei da proporções 3.Hipótese de Avogadro 4.Massa Atômica e molecular 5.Lei dos gases ideais 6.Lei de Van der Waals
Primeira Lei da Termodinâmica
 Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trabalho de expansão Trocas térmicas Entalpia Termodinâmica Estudo das transformações de
Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trabalho de expansão Trocas térmicas Entalpia Termodinâmica Estudo das transformações de
Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos
 Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos MATRIZ DE EXAME DISCIPLINA: Física e Química Módulo 5 Hidrostática e Hidrodinâmica Duração: 50 minutos Conteúdos Competências
Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos MATRIZ DE EXAME DISCIPLINA: Física e Química Módulo 5 Hidrostática e Hidrodinâmica Duração: 50 minutos Conteúdos Competências
Termodinâmica. Lucy V. C. Assali
 Termodinâmica Gases Ideais Física II 2016 - IO Propriedades dos Gases: Equação de Estado dos Gases Ideais Fluido homogêneo: caracterizado por qualquer par das três variáveis (P, V, T) uma relação funcional
Termodinâmica Gases Ideais Física II 2016 - IO Propriedades dos Gases: Equação de Estado dos Gases Ideais Fluido homogêneo: caracterizado por qualquer par das três variáveis (P, V, T) uma relação funcional
Química da atmosfera...
 Atmosfera é a camada de ar que envolve a Terra do grego atmos = vapor do latim sphaera = invólucro. Assim, a palavra atmosfera pode significar: invólucro de vapor. Química - O estudo das propriedades e
Atmosfera é a camada de ar que envolve a Terra do grego atmos = vapor do latim sphaera = invólucro. Assim, a palavra atmosfera pode significar: invólucro de vapor. Química - O estudo das propriedades e
Lei de Charles e Gay-Lussac V T. Pressão baixa. Pressão alta
 GASES Lei de Boyle V 1/P Lei de Charles e Gay-Lussac V T Pressão baixa Pressão alta Lei de Avogadro V n Equação dos gases perfeitos Lei de Boyle V 1/P Lei de Charles e Gay-Lussac Lei de Avogadro V T V
GASES Lei de Boyle V 1/P Lei de Charles e Gay-Lussac V T Pressão baixa Pressão alta Lei de Avogadro V n Equação dos gases perfeitos Lei de Boyle V 1/P Lei de Charles e Gay-Lussac Lei de Avogadro V T V
CQ 028 FÍSICO QUÍMICA GERAL
 UNIVERSIDADE FEDERAL DO ARANÁ SETOR DE CIÊNCIAS EXATAS DEARTAMENTO DE QUÍMICA CQ 028 FÍSICO QUÍMICA GERAL Aula 1.1 Apresentação do curso. Características do estado gasoso. Lei de Boyle. Lei de Gay-Lussac.
UNIVERSIDADE FEDERAL DO ARANÁ SETOR DE CIÊNCIAS EXATAS DEARTAMENTO DE QUÍMICA CQ 028 FÍSICO QUÍMICA GERAL Aula 1.1 Apresentação do curso. Características do estado gasoso. Lei de Boyle. Lei de Gay-Lussac.
Halliday Fundamentos de Física Volume 2
 Halliday Fundamentos de Física Volume 2 www.grupogen.com.br http://gen-io.grupogen.com.br O GEN Grupo Editorial Nacional reúne as editoras Guanabara Koogan, Santos, Roca, AC Farmacêutica, LTC, Forense,
Halliday Fundamentos de Física Volume 2 www.grupogen.com.br http://gen-io.grupogen.com.br O GEN Grupo Editorial Nacional reúne as editoras Guanabara Koogan, Santos, Roca, AC Farmacêutica, LTC, Forense,
Fenômenos Térmicos : primeiro conjunto de problemas
 Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
Física I 2010/2011. Aula 18. Mecânica de Fluidos I
 Física I 2010/2011 Aula 18 Mecânica de Fluidos I Sumário Capítulo 14: Fluidos 14-1 O que é um Fluido? 14-2 Densidade e Pressão 14-3 Fluidos em Repouso 14-4 A Medida da pressão 14-5 O Princípio de Pascal
Física I 2010/2011 Aula 18 Mecânica de Fluidos I Sumário Capítulo 14: Fluidos 14-1 O que é um Fluido? 14-2 Densidade e Pressão 14-3 Fluidos em Repouso 14-4 A Medida da pressão 14-5 O Princípio de Pascal
EXERCÍCIOS DE FIXAÇÃO QUÍMICA GASES I
 Aluno (a): Profº: RICARDO Série: Data: / / Disc: QUÍMICA EXERCÍCIOS DE FIXAÇÃO QUÍMICA GASES I 1. Uma Massa fixa de um gás ideal foi submetida a uma série de transformações isotérmicas e alguns dos valores
Aluno (a): Profº: RICARDO Série: Data: / / Disc: QUÍMICA EXERCÍCIOS DE FIXAÇÃO QUÍMICA GASES I 1. Uma Massa fixa de um gás ideal foi submetida a uma série de transformações isotérmicas e alguns dos valores
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 11 Estudo Geral dos Gases 1.
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 11 Estudo Geral dos Gases 1.
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica
 Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO
 REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO 1- Um aluno de química, ao investigar as propriedades de gases, colocou uma garrafa plástica (PET), contendo ar e devidamente fechada, em um freezer e observou
REVISIONAL DE QUÍMICA 1º ANO PROF. RICARDO 1- Um aluno de química, ao investigar as propriedades de gases, colocou uma garrafa plástica (PET), contendo ar e devidamente fechada, em um freezer e observou
GASES MÓDULO 1 TRANSFORMAÇÕES QUÍMICAS
 GASES MÓDULO 1 TRANSFORMAÇÕES QUÍMICAS GASES GASES IDEAIS OU PERFEITOS Um gás perfeito é um gás hipotético. Por definição, é aquele que obedece, rigorosamente, às leis de Boyle e Charles, ou seja: As moléculas
GASES MÓDULO 1 TRANSFORMAÇÕES QUÍMICAS GASES GASES IDEAIS OU PERFEITOS Um gás perfeito é um gás hipotético. Por definição, é aquele que obedece, rigorosamente, às leis de Boyle e Charles, ou seja: As moléculas
FENÔMENOS OSCILATÓRIOS E TERMODINÂMICA AULA 5 FLUIDOS
 FENÔMENOS OSCILATÓRIOS E TERMODINÂMICA AULA 5 FLUIDOS PROF.: KAIO DUTRA O que é um Fluido um fluido ao contrário de um sólido, é uma substância que pode escoar, os fluidos assumem a forma dos recipientes
FENÔMENOS OSCILATÓRIOS E TERMODINÂMICA AULA 5 FLUIDOS PROF.: KAIO DUTRA O que é um Fluido um fluido ao contrário de um sólido, é uma substância que pode escoar, os fluidos assumem a forma dos recipientes
QUÍMICA. Transformações Químicas. Sistemas Gasosos Lei, Teoria Cinética, Equação e Mistura dos Gases Princípio de Avogadro Parte 4
 QUÍMICA Transformações Químicas Sistemas Gasosos Lei, Teoria Cinética, Equação e Mistura dos Gases Parte 4 Prof a. Giselle Blois Dúvida: O ar é um gás?! Resposta: Não, o ar é uma MISTURA DE GASES. Composição:
QUÍMICA Transformações Químicas Sistemas Gasosos Lei, Teoria Cinética, Equação e Mistura dos Gases Parte 4 Prof a. Giselle Blois Dúvida: O ar é um gás?! Resposta: Não, o ar é uma MISTURA DE GASES. Composição:
