UFABC Fenômenos Térmicos Prof. Germán Lugones. Aula 5: Livre caminho médio, distribuição de Maxwell-Boltzmann
|
|
|
- Isabella Casado Figueiredo
- 5 Há anos
- Visualizações:
Transcrição
1 UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 5: Livre caminho médio, distribuição de Maxwell-Boltzmann
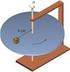
2 Caminho Livre Médio A Figura mostra a trajetória de uma molécula típica quando ela se move através do gás. Entre colisões, a molécula se move em linha reta com velocidade constante mudando abruptamente tanto o módulo quanto o sentido da velocidade quando ela colide e l a s t i c a m e n t e c o m o u t r a s moléculas. Embora a figura mostre as outras moléculas como se estivessem paradas, elas também estão se movendo.
3 Um parâmetro útil para descrever este movimento aleatório é o caminho livre médio λ das moléculas. Como o seu nome indica, λ é a distância média percorrida por uma molécula entre colisões.
4 Cálculo do Caminho Livre Médio Consideremos uma molécula que está viajando com uma velocidade constante v e que todas as demais moléculas estão em repouso. (mais tarde, vamos abrir mão desta condição). Supomos que as moléculas são esferas de diâmetro d. Uma colisão ocorrerá se os centros de duas moléculas se aproximarem dentro de uma distância d um do outro. Uma maneira equivalente de se olhar para a situação é considerar nossa molécula como tendo um raio d e todas as outras moléculas como sendo puntiformes.
5 Q u a n d o a m o l é c u l a ziguezagueia através do gás, ela varre um pequeno cilindro de área de seção t r a n s v e r s a l π d 2 e n t re colisões sucessivas. S e o b s e r v a r m o s e s t a molécula por um intervalo de tempo Δt, ela se desloca por uma distância vδt, onde v é sua velocidade. Assim, se alinharmos todos os pequenos cilindros varridos no intervalo Δt, formaremos um cilindro composto de comprimento vδt e volume (πd 2 )(vδt).
6 O número de colisões que ocorrem em um tempo Δt é então igual ao número de moléculas (puntiformes) que estão dentro deste cilindro. Como N/V é o número de moléculas por unidade de volume, o número de moléculas no cilindro é: N/V multiplicado pelo volume do cilindro, ou seja: (N/V) (π d 2 )(v Δt). Este é também o número de colisões que ocorrem no intervalo Δt. O caminho livre médio é o comprimento da trajetória (e do cilindro) dividido por este número: λ = comprimento do caminho durante Δt número de colisões em Δt = vδt πd 2.vΔt. N/V = 1 πd 2. N/V Esta equação é apenas aproximada porque está baseada na suposição de que todas as moléculas, exceto uma, estão em repouso.
7 Porém, todas as moléculas estão se movendo. Quando isto é levado em conta adequadamente, obtém-se: CAMINHO LIVRE MEDIO Exemplos: O caminho livre médio de moléculas de ar no nível do mar é cerca de 0,1 μm. Em uma altitude de 100 km, a densidade cai para níveis tão baixos que o caminho livre médio aumenta para cerca de 16 cm. A 300 km, o caminho livre médio é cerca de 20 km.
8 CAMINHO LIVRE MEDIO 1. λ varia inversamente com a densidade de moléculas. Quanto maior for N/V, maior deve ser o número de colisões e menor a distancia percorrida pelas moléculas entre duas colisões sucessivas. 2. λ varia inversamente com o tamanho das moléculas. Se as moléculas fossem puntiformes, elas nunca colidiriam e o caminho livre médio seria infinito. Alias, varia (inversamente) com o quadrado do diâmetro molecular porque a seção de choque de uma molécula determina sua área efetiva como alvo.
9 Exemplo: (a) Qual é o livre caminho médio λ de moléculas de oxigênio à temperatura T = 300 K e a uma pressão p = 1 atm? Suponha que o diâmetro das moléculas é d=290 pm e que o gás é ideal. [Obs: 1 p = 1 pico = ] Solução: O livre caminho médio é: Para um gás ideal temos PV = NkT à N/V = P/(kT), logo: O livre caminho médio é aproximadamente 380 vezes o diâmetro da molécula.
10 (b) Suponha que a velocidade média das moléculas de oxigênio é v = 450 m/s. Qual é o tempo médio t entre colisões para qualquer molécula? Qual é a frequência f das colisões? Solução: O tempo médio entre colisões é dado por: A frequência das colisões é: Uma molécula de oxigênio sofre cerca de 4 bilhões de colisões por segundo.
11 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos f o r n e c e u m a i d e i a g e r a l d a s velocidades moleculares em um gás numa dada temperatura. Mas, frequentemente, queremos mais do que isso. Por exemplo: 1. qual é a fração das moléculas que têm velocidades maiores do que V rms? 2. Qual é a fração das moléculas que têm velocidades maiores do que o dobro de Para V responder rms? tais questões, precisamos saber como os possíveis valores das velocidades estão distribuídos entre as moléculas.
12 Em 1852, o físico escocês James Clerk Maxwell resolveu pela primeira vez o problema de se encontrar a distribuição das velocidades moleculares de um gás. Seu resultado, conhecido como a lei da distribuição de velocidades de Maxwell, é: P(v) = 4π ( 3/2 M 2πRT ) v 2 e Mv2 /2RT Distribuição de Maxwell-Boltzmann M = massa molar do gás, R =constante dos gases, T = temperatura do gás v = módulo da velocidade molecular. P(v) = função distribuição de probabilidade de velocidade Para qualquer velocidade v, o produto P(v) dv (uma grandeza adimensional) é a fração das moléculas cujas velocidades estão no intervalo dv centrado em v.
13 4.0 Distribuição de velocidades para moléculas de oxigênio em dois casos: T = 300 K (temperatura ambiente) T = 80 K. P(v) (10 3 s/m) T = 80 K T = 300 K Speed (m/s)
14 O produto P(v) dv indica qual é a fração das moléculas cujas velocidades estão no intervalo dv centrado em v. Esta fração é igual à área sob a curva de uma faixa estreita de altura P(v) e espessura dv. P(v) (10 3 s/m) v avg v P Area = P(v) dv 0 v rms Speed (m/s) dv
15 - A área total sob a curva de distribuição corresponde à fração das moléculas cujos valores das velocidades estão entre zero e infinito. - Todas as moléculas se encaixam nesta categoria, de modo que o valor desta área total é um; ou seja, 0 P(v)dv = 1 - A fração fr de moléculas com velocidades entre v 1 e v 2 é dada por: fr = v 2 v 1 P(v)dv
16 Velocidade Média (vmed) Em princípio, podemos encontrar a velocidade média v méd das moléculas em um gás ponderando cada valor de v na distribuição; ou seja, multiplicamos v pela fração P(v) dv das moléculas com velocidades em um intervalo diferencial dv centrado em v. Depois adicionamos (integramos) todos estes valores de v P(v) dv. Na Eq. anterior substituímos v med = v. P(ν)dv 0 P( v) = 4π 2 M πrt 3 / 2 v 2 e Mv 2 / 2 RT Depois realizamos a integral utilizando: O resultado é: v méd = 8RT πm
17 Velocidade Quadrática Média (vrms) De forma semelhante, podemos encontrar a média dos quadrados das velocidades: Substituímos P(v) e integramos igual que antes, usando a fórmula: O resultado é: Este resultado esta de acordo com o que tínhamos obtido na aula anterior usando outro método.
18 Velocidade mais provável (vmp) A velocidade mais provável v mp é a velocidade na qual P(v) é máxima. Para calcularmos v mp fazemos dp/dv = 0 (a inclinação da curva é nula no máximo da curva) e então resolvemos para v. Fazendo isso, encontramos: 2RT v mp = M É mais provável que uma molécula tenha uma velocidade V mp do que qualquer outra velocidade, mas algumas moléculas terão velocidades muito maiores do que v mp. Essas moléculas estão na cauda de altas velocidades da curva de distribuição.
19
20 Energia Cinética Translacional Vamos considerar novamente uma molécula de um gás ideal quando ela se move no interior de uma caixa, mas agora vamos supor que sua velocidade varia quando ela colide com outras moléculas. Sua energia cinética translacional em qualquer instante é ½ mv 2. Sua energia cinética translacional média no intervalo de tempo em que a observamos é K méd =(½ mv 2 ) méd = ½ m (v 2 ) méd = ½ m v rms 2 Substituindo v rms = (3RT/M) 1/2, temos que K méd =(½ m). 3RT/M Substituindo M/m = N A e k=r/n A temos: K méd = (3/2) k T Quando medimos a temperatura de um gás, também estamos medindo a energia cinética translacional média de suas moléculas.
AULA 8 Teoria Cinética dos Gases II
 UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
UFABC - BC Prof. Germán Lugones. AULA 7 Teoria Cinética dos Gases I
 UFABC - BC0205 - Prof. Germán Lugones AULA 7 Teoria Cinética dos Gases I Teoria cinética dos gases o Um gás consiste em partículas (e.g. átomos ou moléculas) que preenchem o volume de seu recipiente e
UFABC - BC0205 - Prof. Germán Lugones AULA 7 Teoria Cinética dos Gases I Teoria cinética dos gases o Um gás consiste em partículas (e.g. átomos ou moléculas) que preenchem o volume de seu recipiente e
Teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
Física Geral II. Aula 1 - Teoria cinética dos gases. D. Valin 1. Universidade do Estado de Mato Grosso. Sinop-MT, April 25, 2017
 Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
19.2 Número de Avogadro mol número de átomos em uma amostra de 12g do carbono-12. Num mol de qualquer substância existem
 Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
A teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
Moléculas em Movimento
 Físico-Química II Profa. Dra. Carla Dalmolin Moléculas em Movimento Modelo Cinético dos Gases Modelo Cinético dos Gases A única contribuição para a energia do gás vem das energias cinéticas das moléculas
Físico-Química II Profa. Dra. Carla Dalmolin Moléculas em Movimento Modelo Cinético dos Gases Modelo Cinético dos Gases A única contribuição para a energia do gás vem das energias cinéticas das moléculas
25/Fev/2015 Aula 2. 20/Fev/2015 Aula 1
 /Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
/Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
GASES. https://www.youtube.com/watch?v=wtmmvs3uiv0. David P. White. QUÍMICA: A Ciência Central 9ª Edição Capítulo by Pearson Education
 GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a. o resultado do movimento dos átomos e moléculas.
 TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
Universidade Federal do Pampa UNIPAMPA. Teoria Cinética do Gases
 Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Capítulo 22 Propriedades Moleculares dos Gases (Teoria Cinética dos Gases)
 Capítulo Propriedades Moleculares dos Gases (Teoria Cinética dos Gases). A natureza atômica da matéria If, in some cataclysm, all of scientific knowledge were to be destroyed, and only one sentence passed
Capítulo Propriedades Moleculares dos Gases (Teoria Cinética dos Gases). A natureza atômica da matéria If, in some cataclysm, all of scientific knowledge were to be destroyed, and only one sentence passed
Física II FEP 112 ( ) 1º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
FIS-14 Mecânica I. Ronaldo Rodrigues Pela
 FIS-14 Mecânica I Ronaldo Rodrigues Pela Objetivos Visão geral: Termodinâmica e Mecânica Velocidade rms Equipartição da Energia e calor específico Origem microscópica da distribuição de Maxwell-Boltzmann
FIS-14 Mecânica I Ronaldo Rodrigues Pela Objetivos Visão geral: Termodinâmica e Mecânica Velocidade rms Equipartição da Energia e calor específico Origem microscópica da distribuição de Maxwell-Boltzmann
COMPORTAMENTO DOS GASES
 BC0102: ESTRUTURA DA MATÉRIA COMPORTAMENTO DOS GASES hueder.paulo@ufabc.edu.br Hueder Paulo Moisés de Oliveira 1 Calendário Semana Aulas expositivas 1 07/06 Introdução ao curso (Informações sobre provas,
BC0102: ESTRUTURA DA MATÉRIA COMPORTAMENTO DOS GASES hueder.paulo@ufabc.edu.br Hueder Paulo Moisés de Oliveira 1 Calendário Semana Aulas expositivas 1 07/06 Introdução ao curso (Informações sobre provas,
Física II Teoria Cinética dos Gases
 Física II Teoria Cinética dos Gases João Francisco Fuzile Rodrigues Garcia -- 8549323 Maiara Fernanda Moreno -- 8549344 Otávio Massola Sumi -- 8549452 Ex. 18.63 Explique, em termos do movimento molecular,
Física II Teoria Cinética dos Gases João Francisco Fuzile Rodrigues Garcia -- 8549323 Maiara Fernanda Moreno -- 8549344 Otávio Massola Sumi -- 8549452 Ex. 18.63 Explique, em termos do movimento molecular,
UFABC Fenômenos Térmicos Prof. Germán Lugones. Aula 7: Capacidades caloríficas de gases ideais, processos adiabáticos, equipartição da energia.
 UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 7: Capacidades caloríficas de gases ideais, processos adiabáticos, equipartição da energia. Energia interna de um gás ideal Energia interna: Do ponto
UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 7: Capacidades caloríficas de gases ideais, processos adiabáticos, equipartição da energia. Energia interna de um gás ideal Energia interna: Do ponto
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Mecânica Mecânica: estuda o estado de movimento (ou repouso) de corpos sujeitos à ação
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Mecânica Mecânica: estuda o estado de movimento (ou repouso) de corpos sujeitos à ação
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
UFABC - BC Prof. Germán Lugones. AULA 9 Teoria Cinética dos Gases III
 UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
03/Mar/2017 Aula 3. 01/Mar/2017 Aula 2
 01/Mar/2017 Aula 2 Teoria Cinética dos Gases Teoria Cinética e Equação dos Gases Ideais Gás Ideal num Campo Gravitacional Distribuição de Boltzmann; distribuição de velocidades de Maxwell e Boltzmann Velocidades
01/Mar/2017 Aula 2 Teoria Cinética dos Gases Teoria Cinética e Equação dos Gases Ideais Gás Ideal num Campo Gravitacional Distribuição de Boltzmann; distribuição de velocidades de Maxwell e Boltzmann Velocidades
~é a força normal do bloco de cima sobre o bloco de baixo É o peso do bloco de cima (baixo)
 Q1. (2,0 pontos) O coeficiente de atrito estático entre os blocos da figura vale 0,60. O coeficiente de atrito cinético entre o bloco inferior e o piso é de 0,20. A força F, aplicada ao bloco superior,
Q1. (2,0 pontos) O coeficiente de atrito estático entre os blocos da figura vale 0,60. O coeficiente de atrito cinético entre o bloco inferior e o piso é de 0,20. A força F, aplicada ao bloco superior,
Primeira Lista de Exercícios de Biofísica II. c n
 Primeira Lista de Exercícios de Biofísica II 1. Considere uma célula composta por um corpo celular ao qual está preso um longo e fino processo tubular (por exemplo, o axônio de um neurônio ou o flagelo
Primeira Lista de Exercícios de Biofísica II 1. Considere uma célula composta por um corpo celular ao qual está preso um longo e fino processo tubular (por exemplo, o axônio de um neurônio ou o flagelo
As bases da Dinâmica Molecular - 8
 As bases da Dinâmica Molecular - 8 Alexandre Diehl Departamento de Física - UFPel Hipóteses fundamentais da teoria cinética Qualquer porção pequena do gás contém um número N enorme de moléculas. Número
As bases da Dinâmica Molecular - 8 Alexandre Diehl Departamento de Física - UFPel Hipóteses fundamentais da teoria cinética Qualquer porção pequena do gás contém um número N enorme de moléculas. Número
Primeira Verificação de Aprendizagem (1 a V.A.) - 28/05/2014
 UNIVERSIDADE FEDERAL DA PARAÍBA Centro de Ciências Exatas e da Natureza Departamento de Física Disciplina: Física Geral I Prof.: Carlos Alberto Aluno(a): Matrícula: Questão 1. Responda: Primeira Verificação
UNIVERSIDADE FEDERAL DA PARAÍBA Centro de Ciências Exatas e da Natureza Departamento de Física Disciplina: Física Geral I Prof.: Carlos Alberto Aluno(a): Matrícula: Questão 1. Responda: Primeira Verificação
MOVIMENTO RETILÍNEO. Prof. Bruno Farias
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I MOVIMENTO RETILÍNEO Prof. Bruno Farias Introdução Por que estudar mecânica? Porque o mundo,
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I MOVIMENTO RETILÍNEO Prof. Bruno Farias Introdução Por que estudar mecânica? Porque o mundo,
= 6, mol de moléculas de um gás possui aproximadamente 6, moléculas deste gás, ou seja, seiscentos e dois sextilhões de moléculas;
 TEORIA CINÉTICA DOS GASES PROF. LEANDRO NECKEL NÚMERO DE AVOGADRO Mol é a quantidade de substância de um sistema que contém tantas entidades elementares quanto são os átomos contidos em 0,012 quilograma
TEORIA CINÉTICA DOS GASES PROF. LEANDRO NECKEL NÚMERO DE AVOGADRO Mol é a quantidade de substância de um sistema que contém tantas entidades elementares quanto são os átomos contidos em 0,012 quilograma
Física - 1. Dados numéricos
 Física - 1 Dados numéricos celeração da gravidade: 1 m/s Densidade da água: 1, g/cm 3 Velocidade da luz no vácuo: 3, x 1 8 m/s 1 atm = 1, x 1 5 N/m = 1 4 π o = 9, x 1 9 N.m C 1. O gráfico da velocidade
Física - 1 Dados numéricos celeração da gravidade: 1 m/s Densidade da água: 1, g/cm 3 Velocidade da luz no vácuo: 3, x 1 8 m/s 1 atm = 1, x 1 5 N/m = 1 4 π o = 9, x 1 9 N.m C 1. O gráfico da velocidade
Termodinâmica II - FMT 259
 Termodinâmica II - FMT 59 Diurno e Noturno, primeiro semestre de 1 Gabarito da lista 6 1. Considere um gás hipotético para o qual a função de distribuição de velocidades tivesse a forma indicada na gura
Termodinâmica II - FMT 59 Diurno e Noturno, primeiro semestre de 1 Gabarito da lista 6 1. Considere um gás hipotético para o qual a função de distribuição de velocidades tivesse a forma indicada na gura
Um mol é o número de átomos em uma amostra de 12 g de carbono 12.
 NOTA DE AULA 07 UNIVERSIDADE CATÓLICA DE GOIÁS DEPARTAMENTO DE MATEMÁTICA E FÍSICA Disciplina: FÍSICA GERAL E EXPERIMENTAL II (MAF 0) Coordenação: Prof. Dr. Elias Calixto Carrijo CAPÍTULO 0 A TEORIA CINÉTICA
NOTA DE AULA 07 UNIVERSIDADE CATÓLICA DE GOIÁS DEPARTAMENTO DE MATEMÁTICA E FÍSICA Disciplina: FÍSICA GERAL E EXPERIMENTAL II (MAF 0) Coordenação: Prof. Dr. Elias Calixto Carrijo CAPÍTULO 0 A TEORIA CINÉTICA
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Journal Club Teoria do funcional da densidade A energia do estado fundamental é um funcional
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Journal Club Teoria do funcional da densidade A energia do estado fundamental é um funcional
PSVS/UFES 2014 MATEMÁTICA 1ª QUESTÃO. O valor do limite 2ª QUESTÃO. O domínio da função real definida por 3ª QUESTÃO
 MATEMÁTICA 1ª QUESTÃO O valor do limite 3 x 8 lim é x 2 x 2 2ª QUESTÃO O domínio da função real definida por é 3ª QUESTÃO A imagem da função real definida por, para todo, é GRUPO 1 PROVA DE MATEMÁTICA
MATEMÁTICA 1ª QUESTÃO O valor do limite 3 x 8 lim é x 2 x 2 2ª QUESTÃO O domínio da função real definida por é 3ª QUESTÃO A imagem da função real definida por, para todo, é GRUPO 1 PROVA DE MATEMÁTICA
O modelo cinético molecular para gases e a difusão: o passeio aleatório
 O modelo cinético molecular para gases e a difusão: o passeio aleatório O modelo mecânico para a pressão que consideramos ignora as interações entre moléculas, uma molécula não vê a outra há choques apenas
O modelo cinético molecular para gases e a difusão: o passeio aleatório O modelo mecânico para a pressão que consideramos ignora as interações entre moléculas, uma molécula não vê a outra há choques apenas
Física Geral. Trabalho, Energia e Momentum Linear.
 Física Geral Trabalho, Energia e Momentum Linear. l Energia e Momentum Há muitas formas de energia como por exemplo, energia nuclear, energia elétrica, energia sonora, energia luminosa. Quando você levanta
Física Geral Trabalho, Energia e Momentum Linear. l Energia e Momentum Há muitas formas de energia como por exemplo, energia nuclear, energia elétrica, energia sonora, energia luminosa. Quando você levanta
INTRODUÇÃO À ASTROFÍSICA
 Introdução à Astrofísica INTRODUÇÃO À ASTROFÍSICA LIÇÃO 21 O EQUILÍBRIO HIDROSTÁTICO Lição 20 O Equilíbrio Hidrostático As estrelas se formam a partir de regiões densas e frias, chamadas de nebulosas.
Introdução à Astrofísica INTRODUÇÃO À ASTROFÍSICA LIÇÃO 21 O EQUILÍBRIO HIDROSTÁTICO Lição 20 O Equilíbrio Hidrostático As estrelas se formam a partir de regiões densas e frias, chamadas de nebulosas.
Interpretação Molecular da Temperatura de um Gás Ideal
 Interpretação Molecular da Temperatura de um Gás Ideal Já vimos que a pressão está relacionada com a energia cinética média das moléculas. Agora relacionaremos a temperatura à uma descrição microscópica
Interpretação Molecular da Temperatura de um Gás Ideal Já vimos que a pressão está relacionada com a energia cinética média das moléculas. Agora relacionaremos a temperatura à uma descrição microscópica
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 2 RADIAÇÃO TÉRMICA E CORPO NEGRO Edição de janeiro de 2009 CAPÍTULO 2 RADIAÇÃO TÉRMICA E CORPO NEGRO ÍNDICE 2.1- Radiação Térmica 2.2-
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 2 RADIAÇÃO TÉRMICA E CORPO NEGRO Edição de janeiro de 2009 CAPÍTULO 2 RADIAÇÃO TÉRMICA E CORPO NEGRO ÍNDICE 2.1- Radiação Térmica 2.2-
FIS-14 Prova 02 Novembro/2013
 FIS-14 Prova 02 Novembro/2013 Nome: Nota: Duração máxima da prova: 240 min. Responda às questões de forma clara, completa e concisa dentro do espaço previsto. Uma parte da pontuação de cada questão será
FIS-14 Prova 02 Novembro/2013 Nome: Nota: Duração máxima da prova: 240 min. Responda às questões de forma clara, completa e concisa dentro do espaço previsto. Uma parte da pontuação de cada questão será
Energia cinética de rotação:
 2 comenta a) Energia cinética de translação: Energia cinética de rotação: Todos os pontos que constituem o aro têm a mesma velocidade tangencial em relação ao seu centro. Por isso, sua energia cinética
2 comenta a) Energia cinética de translação: Energia cinética de rotação: Todos os pontos que constituem o aro têm a mesma velocidade tangencial em relação ao seu centro. Por isso, sua energia cinética
Física IV Relatividade. Prof. Helena Malbouisson Sala 3018A
 Física IV Relatividade Prof. Helena Malbouisson Sala 3018A uerj-fisica-ivquimica@googlegroups.com 1 Relatividade A teoria da relatividade Restrita (ou Especial) foi proposta por Albert Einstein em 1905.
Física IV Relatividade Prof. Helena Malbouisson Sala 3018A uerj-fisica-ivquimica@googlegroups.com 1 Relatividade A teoria da relatividade Restrita (ou Especial) foi proposta por Albert Einstein em 1905.
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2. Propriedades Moleculares dos Gases
 CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
Física aplicada à engenharia I
 Física aplicada à engenharia I Rotação - I 10.2 As Variáveis da Rotação Um corpo rígido é um corpo que gira com todas as partes ligadas entre si e sem mudar de forma. Um eixo fixo é um eixo de rotação
Física aplicada à engenharia I Rotação - I 10.2 As Variáveis da Rotação Um corpo rígido é um corpo que gira com todas as partes ligadas entre si e sem mudar de forma. Um eixo fixo é um eixo de rotação
INTRODUÇÃO À ASTROFÍSICA LIÇÃO 19 A DISTRIBUIÇÃO DE MAXWELL-BOLZTMANN
 Introdução à Astrofísica Lição 18 A Distribuição de Maxwell INTRODUÇÃO À ASTROFÍSICA LIÇÃO 19 A DISTRIBUIÇÃO DE MAXWELL-BOLZTMANN Um estado de um gás é especificado por suas coordenadas, de modo que representemos
Introdução à Astrofísica Lição 18 A Distribuição de Maxwell INTRODUÇÃO À ASTROFÍSICA LIÇÃO 19 A DISTRIBUIÇÃO DE MAXWELL-BOLZTMANN Um estado de um gás é especificado por suas coordenadas, de modo que representemos
EN 2010 (A)0,8 (B) 1,0 (C) 2,0 (D) 3,0 (E) 4,0
 EN 010 1. Uma pequena esfera de massa m está presa a um fio ideal de comprimento L = 0,4m, que tem sua outra extremidade presa ao teto, conforme indica a figura. No instante t = 0, quando o fio faz um
EN 010 1. Uma pequena esfera de massa m está presa a um fio ideal de comprimento L = 0,4m, que tem sua outra extremidade presa ao teto, conforme indica a figura. No instante t = 0, quando o fio faz um
2007 3ª. fase Prova para alunos do 3º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos do 3º. ano.
 007 3ª. fase Prova para alunos do 3º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos do 3º. ano. 0) A prova contém oito (8) questões e TODAS DEVEM SER RESOLVIDAS.
007 3ª. fase Prova para alunos do 3º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos do 3º. ano. 0) A prova contém oito (8) questões e TODAS DEVEM SER RESOLVIDAS.
CENTRO DE MASSA E MOMENTO LINEAR
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I CENTRO DE MASSA E MOMENTO LINEAR Prof. Bruno Farias Introdução Neste módulo vamos discutir
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I CENTRO DE MASSA E MOMENTO LINEAR Prof. Bruno Farias Introdução Neste módulo vamos discutir
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Journal Club Teoria do funcional da densidade A energia do estado fundamental é um funcional
Mecânica I (FIS-14) Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Journal Club Teoria do funcional da densidade A energia do estado fundamental é um funcional
UFABC - Física Quântica - Curso Prof. Germán Lugones. Aula 7. Exercícios
 UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 7 Exercícios 1 Ex. 1 Um laser pointer com uma potência de saída de 5,00 mw emite luz vermelha (l 650 nm). (a) Qual é o módulo do momento
UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 7 Exercícios 1 Ex. 1 Um laser pointer com uma potência de saída de 5,00 mw emite luz vermelha (l 650 nm). (a) Qual é o módulo do momento
1. Calcule a área do triângulo retângulo ABC na Figura 1, sabendo-se que n é a reta normal a f(x) = e x no ponto x o = 1. Figura 1: Exercício 1
 Lista 5: Derivada como taxa de variação e Diferencial - Cálculo Diferencial e Integral I Professora: Elisandra Bär de Figueiredo 1. Calcule a área do triângulo retângulo ABC na Figura 1, sabendo-se que
Lista 5: Derivada como taxa de variação e Diferencial - Cálculo Diferencial e Integral I Professora: Elisandra Bär de Figueiredo 1. Calcule a área do triângulo retângulo ABC na Figura 1, sabendo-se que
Matemática para Engenharia I. Lista Derivadas. 2. Calcule a derivada das funções abaixo nos pontos dados usando a definição:
 Matemática para Engenharia I Lista Derivadas. Usando que ( ) ( ) encontre a equação da reta tangente ao gráfico de f no ponto p(0,y 0 ). a) ( ) ( ) b) ( ), ( ) c) ( ), ( ) d) ( ), ( ( )) e) ( ), ( ) f)
Matemática para Engenharia I Lista Derivadas. Usando que ( ) ( ) encontre a equação da reta tangente ao gráfico de f no ponto p(0,y 0 ). a) ( ) ( ) b) ( ), ( ) c) ( ), ( ) d) ( ), ( ( )) e) ( ), ( ) f)
Física para Zootecnia
 Física para Zootecnia Rotação - I 10.2 As Variáveis da Rotação Um corpo rígido é um corpo que gira com todas as partes ligadas entre si e sem mudar de forma. Um eixo fixo é um eixo de rotação cuja posição
Física para Zootecnia Rotação - I 10.2 As Variáveis da Rotação Um corpo rígido é um corpo que gira com todas as partes ligadas entre si e sem mudar de forma. Um eixo fixo é um eixo de rotação cuja posição
1 = Pontuação: Os itens A e B valem três pontos cada; o item C vale quatro pontos.
 Física 01. Duas pessoas pegam simultaneamente escadas rolantes, paralelas, de mesmo comprimento l, em uma loja, sendo que uma delas desce e a outra sobe. escada que desce tem velocidade V = 1 m/s e a que
Física 01. Duas pessoas pegam simultaneamente escadas rolantes, paralelas, de mesmo comprimento l, em uma loja, sendo que uma delas desce e a outra sobe. escada que desce tem velocidade V = 1 m/s e a que
Princípios de Eletricidade Magnetismo
 Princípios de Eletricidade Magnetismo Corrente Elétrica e Circuitos de Corrente Contínua Professor: Cristiano Faria Corrente e Movimento de Cargas Elétricas Embora uma corrente seja um movimento de partícula
Princípios de Eletricidade Magnetismo Corrente Elétrica e Circuitos de Corrente Contínua Professor: Cristiano Faria Corrente e Movimento de Cargas Elétricas Embora uma corrente seja um movimento de partícula
Instituto Nacional de Pesquisas Espaciais
 Instituto Nacional de Pesquisas Espaciais Exame de admissão para o programa de pós-graduação em Astrofísica 16/12/2013 - Duração: 4h00 Nome: Instruções para realização do exame: a) a prova é individual,
Instituto Nacional de Pesquisas Espaciais Exame de admissão para o programa de pós-graduação em Astrofísica 16/12/2013 - Duração: 4h00 Nome: Instruções para realização do exame: a) a prova é individual,
Relatividade Especial Virtual - Uma Generalização da Relatividade Especial de Einstein
 Relatividade Especial Virtual - Uma Generalização da Relatividade Especial de Einstein Edigles Guedes e-mail: edigles.guedes@gmail.com 24 de junho de 2012. RESUMO Nós construímos a Teoria da Relatividade
Relatividade Especial Virtual - Uma Generalização da Relatividade Especial de Einstein Edigles Guedes e-mail: edigles.guedes@gmail.com 24 de junho de 2012. RESUMO Nós construímos a Teoria da Relatividade
Movimento Unidimensional
 Movimento Unidimensional Professor: Carlos Alberto Disciplina: Física Geral I Objetivos de aprendizagem Ao estudar este capítulo você aprenderá: Como descrever o movimento unidimensional em termos da velocidade
Movimento Unidimensional Professor: Carlos Alberto Disciplina: Física Geral I Objetivos de aprendizagem Ao estudar este capítulo você aprenderá: Como descrever o movimento unidimensional em termos da velocidade
4. Propriedades dos gases experimentos e modelo microscópico simples para a temperatura
 PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
MOVIMENTO EM UMA LINHA RETA
 MOVIMENTO EM UMA LINHA RETA MOVIMENTO EM UMA LINHA RETA Objetivos de aprendizagem: Descrever o movimento em uma linha reta em termos de velocidade média, velocidade instantânea, aceleração média e aceleração
MOVIMENTO EM UMA LINHA RETA MOVIMENTO EM UMA LINHA RETA Objetivos de aprendizagem: Descrever o movimento em uma linha reta em termos de velocidade média, velocidade instantânea, aceleração média e aceleração
Física. Cinemática. Professor Alexei Muller.
 Física Cinemática Professor Alexei Muller Física CINEMÁTICA Varia sucessivamente a sua posição (seu lugar) com o passar do tempo em relação a um sistema de referência. Os conceitos de repouso e de movimento
Física Cinemática Professor Alexei Muller Física CINEMÁTICA Varia sucessivamente a sua posição (seu lugar) com o passar do tempo em relação a um sistema de referência. Os conceitos de repouso e de movimento
DISCURSIVAS. Solução: (a) Com os eixos escolhidos conforme a figura, a altura instantânea da caixa a partir do instante t=0 em que começa a cair é
 DISCURSIVAS 1. Um pequeno avião monomotor, à altitude de 500m, deixa cair uma caixa. No instante em que a caixa é largada, o avião voava a 60,0m/s inclinado de 30,0 0 acima da horizontal. (a) A caixa atinge
DISCURSIVAS 1. Um pequeno avião monomotor, à altitude de 500m, deixa cair uma caixa. No instante em que a caixa é largada, o avião voava a 60,0m/s inclinado de 30,0 0 acima da horizontal. (a) A caixa atinge
As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana.
 Estudo dos gases Gás Ideal As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana. As moléculas não exercem força uma sobre as outras, exceto quando
Estudo dos gases Gás Ideal As moléculas se encontram em movimento desordenado, regido pelos princípios fundamentais da Mecânica newtoniana. As moléculas não exercem força uma sobre as outras, exceto quando
Problemas de Mecânica e Ondas 3
 Problemas de Mecânica e Ondas 3 P 3.1. ( Exercícios de Física, A. Noronha, P. Brogueira, McGraw Hill, 1994) Considere uma esfera de densidade e raio r imersa num fluido de viscosidade e massa específica
Problemas de Mecânica e Ondas 3 P 3.1. ( Exercícios de Física, A. Noronha, P. Brogueira, McGraw Hill, 1994) Considere uma esfera de densidade e raio r imersa num fluido de viscosidade e massa específica
Formalismo microcanônico ( ensemble microcanônico) Formalismo canônico ( ensemble canônico)
 Formalismo microcanônico ( ensemble microcanônico) sist(j) estado j f j = Ω j Ω Formalismo canônico ( ensemble canônico) reservatório de temperatura tot res sistema f j = Ω res+sist(j) Ω tot sist(j) Física
Formalismo microcanônico ( ensemble microcanônico) sist(j) estado j f j = Ω j Ω Formalismo canônico ( ensemble canônico) reservatório de temperatura tot res sistema f j = Ω res+sist(j) Ω tot sist(j) Física
Lista 12: Rotação de corpos rígidos
 Lista 12: Rotação de Corpos Rígidos Importante: i. Ler os enunciados com atenção. ii. Responder a questão de forma organizada, mostrando o seu raciocínio de forma coerente. iii. iv. Siga a estratégia para
Lista 12: Rotação de Corpos Rígidos Importante: i. Ler os enunciados com atenção. ii. Responder a questão de forma organizada, mostrando o seu raciocínio de forma coerente. iii. iv. Siga a estratégia para
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia. Aula Interlúdio molecular
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula Interlúdio molecular Energia Interna somatório de energias (cinética + potencial) Energia cinética relacionada
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula Interlúdio molecular Energia Interna somatório de energias (cinética + potencial) Energia cinética relacionada
UFABC - BC0205 -Fenômenos Térmicos Prof. Germán Lugones. AULA 12 Uma visão estatística da entropia
 UFABC - BC0205 -Fenômenos Térmicos Prof. Germán Lugones AULA 12 Uma visão estatística da entropia Em aulas anteriores vimos que as propriedades macroscópicas dos gases podem ser explicadas em termos do
UFABC - BC0205 -Fenômenos Térmicos Prof. Germán Lugones AULA 12 Uma visão estatística da entropia Em aulas anteriores vimos que as propriedades macroscópicas dos gases podem ser explicadas em termos do
Teoria Cinética dos gases
 Estrutura da Matéria Unidade II: A matéria fragmentada Aula 5: Origem estatística e corpuscular da termodinâmica http://professor.ufabc.edu.br/~pieter.westera/estrutura.html Teoria Cinética dos gases Bernoulli
Estrutura da Matéria Unidade II: A matéria fragmentada Aula 5: Origem estatística e corpuscular da termodinâmica http://professor.ufabc.edu.br/~pieter.westera/estrutura.html Teoria Cinética dos gases Bernoulli
FQA Ficha 9 Exercícios variados
 ESCOLA SECUNDÁRIA DE CASQUILHOS FQA Ficha 9 Exercícios variados 11.º Ano Turma A e B 10 novembro 2014 NOME Nº Turma 1. Um grupo de alunos realizou a atividade de laboratório AL-1.4 - Satélite geostacionário
ESCOLA SECUNDÁRIA DE CASQUILHOS FQA Ficha 9 Exercícios variados 11.º Ano Turma A e B 10 novembro 2014 NOME Nº Turma 1. Um grupo de alunos realizou a atividade de laboratório AL-1.4 - Satélite geostacionário
2/Mar/2016 Aula 4. 26/Fev/2016 Aula 3
 6/Fev/016 Aula 3 Calor e Primeira Lei da Termodinâmica Calor e energia térmica Capacidade calorífica e calor específico Calor latente Diagrama de fases para a água Primeira Lei da Termodinâmica Trabalho
6/Fev/016 Aula 3 Calor e Primeira Lei da Termodinâmica Calor e energia térmica Capacidade calorífica e calor específico Calor latente Diagrama de fases para a água Primeira Lei da Termodinâmica Trabalho
Exame de Ingresso. Física Aplicada Física Computacional. Segundo Semestre de 2014
 Exame de Ingresso Física Aplicada Física Computacional Segundo Semestre de 2014 Código do(a) Candidato(a): 1 2 Mecânica Figura 1: questão 1 Figura 2: questão 2 1. A Fig. 1 exibe a evolução temporal do
Exame de Ingresso Física Aplicada Física Computacional Segundo Semestre de 2014 Código do(a) Candidato(a): 1 2 Mecânica Figura 1: questão 1 Figura 2: questão 2 1. A Fig. 1 exibe a evolução temporal do
Alexandre Diehl Departamento de Física UFPel
 - 3 Alexandre Diehl Departamento de Física UFPel O que é a cinemática? Ramo da mecânica que descreve o movimento da partícula a partir do comportamento da sua posição, velocidade e aceleração, sem entrar
- 3 Alexandre Diehl Departamento de Física UFPel O que é a cinemática? Ramo da mecânica que descreve o movimento da partícula a partir do comportamento da sua posição, velocidade e aceleração, sem entrar
AULA 15 IMPULSO E QUANTIDADE DE MOVIMENTO
 AULA 15 IMPULSO E QUANTIDADE DE MOVIMENTO Profa. MSc.: Suely Silva IMPULSO E QUANTIDADE DE MOVIMENTO 1. Impulso de uma força constante Consideremos uma força constante, que atua durante um intervalo de
AULA 15 IMPULSO E QUANTIDADE DE MOVIMENTO Profa. MSc.: Suely Silva IMPULSO E QUANTIDADE DE MOVIMENTO 1. Impulso de uma força constante Consideremos uma força constante, que atua durante um intervalo de
CÁLCULO I. 1 Taxa de Variação. Objetivos da Aula. Aula n o 10: Taxa de Variação, Velocidade, Aceleração e Taxas Relacionadas. Denir taxa de variação;
 CÁLCULO I Prof. Edilson Neri Júnior Prof. André Almeida Aula n o 10: Taxa de Variação, Velocidade, Aceleração e Taxas Relacionadas Objetivos da Aula Denir taxa de variação; Usar as regras de derivação
CÁLCULO I Prof. Edilson Neri Júnior Prof. André Almeida Aula n o 10: Taxa de Variação, Velocidade, Aceleração e Taxas Relacionadas Objetivos da Aula Denir taxa de variação; Usar as regras de derivação
Aula 12 Relatividade. Física 4 Ref. Halliday Volume4. Profa. Keli F. Seidel
 Aula 12 Relatividade Física 4 Ref. Halliday Volume4 ...RELATIVIDADE RESTRITA Sumário Uma nova interpretação do momento linear Uma nova interpretação da Momento e Cinética O que muda em outros conceitos
Aula 12 Relatividade Física 4 Ref. Halliday Volume4 ...RELATIVIDADE RESTRITA Sumário Uma nova interpretação do momento linear Uma nova interpretação da Momento e Cinética O que muda em outros conceitos
Mecânica e Ondas 1º Ano -2º Semestre 2º Teste/1º Exame 21/06/ :30h. Mestrado Integrado em Engenharia Aeroespacial
 Mestrado Integrado em Engenharia Aeroespacial Mecânica e Ondas 1º Ano -º Semestre º Teste/1º Exame 1/06/014 11:30h Duração do Teste (problemas 3, 4 e 5): 1:30h Duração do Exame: :30h Leia o enunciado com
Mestrado Integrado em Engenharia Aeroespacial Mecânica e Ondas 1º Ano -º Semestre º Teste/1º Exame 1/06/014 11:30h Duração do Teste (problemas 3, 4 e 5): 1:30h Duração do Exame: :30h Leia o enunciado com
Potencial Elétrico 1
 Potencial Elétrico 1 Vamos começar com uma revisão: Quando uma força atua sobre uma partícula que se move de um ponto a até um ponto b, o trabalho W realizado pela força é dado pela integral de linha:
Potencial Elétrico 1 Vamos começar com uma revisão: Quando uma força atua sobre uma partícula que se move de um ponto a até um ponto b, o trabalho W realizado pela força é dado pela integral de linha:
Termodinâmica II - FMT 259
 Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 3 GABARITO (revisado em 22/04/0). Se as moléculas contidas em,0 g de água fossem distribuídas uniformemente sobre a superfície
Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 3 GABARITO (revisado em 22/04/0). Se as moléculas contidas em,0 g de água fossem distribuídas uniformemente sobre a superfície
Aluno(a): Nº. Professor: Fabrízio Gentil Série: 3 o ano Disciplina: Física Magnetismo e Energias. TRABALHO DE RECUPERAÇÃO 2 o SEMESTRE
 Lista de Exercícios Pré Universitário Uni-Anhanguera Aluno(a): Nº. Professor: Fabrízio Gentil Série: 3 o ano Disciplina: Física Magnetismo e Energias TRABALHO DE RECUPERAÇÃO 2 o SEMESTRE 1- Marque a alternativa
Lista de Exercícios Pré Universitário Uni-Anhanguera Aluno(a): Nº. Professor: Fabrízio Gentil Série: 3 o ano Disciplina: Física Magnetismo e Energias TRABALHO DE RECUPERAÇÃO 2 o SEMESTRE 1- Marque a alternativa
MOVIMENTO RETILÍNEO E UNIFORME
 MOVIMENTO RETILÍNEO E UNIFORME Definição: O movimento uniforme é quando a velocidade escalar é constante, o que significa afirmar que o móvel percorre sempre a mesma distância a cada unidade de tempo.
MOVIMENTO RETILÍNEO E UNIFORME Definição: O movimento uniforme é quando a velocidade escalar é constante, o que significa afirmar que o móvel percorre sempre a mesma distância a cada unidade de tempo.
Aula 20 TEORIA CINÉTICA DOS GASES. Frederico Guilherme de Carvalho Cunha. META Introduzir os conceitos relativos à Teoria Cinética dos Gases.
 Aula 20 TEORIA CINÉTICA DOS GASES META Introduzir os conceitos relativos à Teoria Cinética dos Gases. OBJETIVOS Ao final desta aula, o aluno deverá idescrever o modelo molecular do gás ideal; enunciar
Aula 20 TEORIA CINÉTICA DOS GASES META Introduzir os conceitos relativos à Teoria Cinética dos Gases. OBJETIVOS Ao final desta aula, o aluno deverá idescrever o modelo molecular do gás ideal; enunciar
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I ROTAÇÃO. Prof.
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I ROTAÇÃO Prof. Bruno Farias Introdução Neste capítulo vamos aprender: Como descrever a rotação
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA I ROTAÇÃO Prof. Bruno Farias Introdução Neste capítulo vamos aprender: Como descrever a rotação
LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO:
 LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 1 Essa prova destina-se exclusivamente a alunos do 1 o e o anos e contém vinte (0) questões. Os alunos do 1 o ano devem escolher livremente oito (8) questões para
LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 1 Essa prova destina-se exclusivamente a alunos do 1 o e o anos e contém vinte (0) questões. Os alunos do 1 o ano devem escolher livremente oito (8) questões para
2007 3ª. fase Prova para alunos 1º. e 2º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO:
 2007 3ª. fase Prova para alunos 1º. e 2º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos do 1o e 2o anos e contém vinte (20) questões. 02) Os alunos do 1o
2007 3ª. fase Prova para alunos 1º. e 2º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos do 1o e 2o anos e contém vinte (20) questões. 02) Os alunos do 1o
QUESTÕES UFBA ª FASE: DINÂMICA
 QUESTÕES UFBA 09-04 ª FASE: DINÂMICA UFBA 009 UFBA 008 UFBA 007 UFBA 006 UFBA 005 UFBA 004 GABARITO UFBA 009 UFBA 008 QUESTÃO 01 (Valor: 15 pontos) Velocidade final do conjunto Como as forças de atrito
QUESTÕES UFBA 09-04 ª FASE: DINÂMICA UFBA 009 UFBA 008 UFBA 007 UFBA 006 UFBA 005 UFBA 004 GABARITO UFBA 009 UFBA 008 QUESTÃO 01 (Valor: 15 pontos) Velocidade final do conjunto Como as forças de atrito
Aula 2 Lei de Coulomb
 Aula Lei de Coulomb Introdução Vimos na aula anterior que corpos carregados com carga sofrem interação mutua podendo ser atraídos ou repelidos entre si. Nessa aula e na próxima trataremos esses corpos
Aula Lei de Coulomb Introdução Vimos na aula anterior que corpos carregados com carga sofrem interação mutua podendo ser atraídos ou repelidos entre si. Nessa aula e na próxima trataremos esses corpos
Proposta de resolução do Exame FQ11-1ªFase
 Proposta de resolução do Exame FQ11-1ªFase Autor: Francisco Cubal 2010 1. 1.1. A lei que se encontra explicita na frase: Num sistema conservativo, a energia mecânica total permanecerá constante é: Lei
Proposta de resolução do Exame FQ11-1ªFase Autor: Francisco Cubal 2010 1. 1.1. A lei que se encontra explicita na frase: Num sistema conservativo, a energia mecânica total permanecerá constante é: Lei
Conceitos Essenciais da Cinemática 1
 Conceitos Essenciais da Cinemática 1 Física_9 EF Profa. Kelly Pascoalino Mecânica Cinemática: Estudo das características do movimento de um corpo sem se preocupar com o (s) agente (s) que o causou. Dinâmica:
Conceitos Essenciais da Cinemática 1 Física_9 EF Profa. Kelly Pascoalino Mecânica Cinemática: Estudo das características do movimento de um corpo sem se preocupar com o (s) agente (s) que o causou. Dinâmica:
Ensino Médio Unidade Parque Atheneu Professor (a): Junior Condez Aluno (a): Série: 3ª Data: / / LISTA DE FÍSICA II
 Ensino Médio Unidade Parque Atheneu Professor (a): Junior Condez Aluno (a): Série: 3ª Data: / / 2015. LISTA DE FÍSICA II 1) Duas bolas de dimensões desprezíveis se aproximam uma da outra, executando movimentos
Ensino Médio Unidade Parque Atheneu Professor (a): Junior Condez Aluno (a): Série: 3ª Data: / / 2015. LISTA DE FÍSICA II 1) Duas bolas de dimensões desprezíveis se aproximam uma da outra, executando movimentos
Física estatística. Teoria cinética dos gases MEFT, IST
 Física estatística Teoria cinética dos gases MEFT, IST Life is a series of collisions with the future; it is not the sum of what we have been, but what we yearn to be. Jose Ortega y Gasset (1883-1955)
Física estatística Teoria cinética dos gases MEFT, IST Life is a series of collisions with the future; it is not the sum of what we have been, but what we yearn to be. Jose Ortega y Gasset (1883-1955)
LISTA DE EXECÍCIOS AULA 3 FÍSICA ELETRICIDADE
 LISTA DE EXECÍCIOS AULA 3 FÍSICA ELETRICIDADE DENSIDADE DE CORRENTE E VELOCIDADE DE ARRASTE 1) A American Wire Gauge (AWG) é uma escala americana normalizada usada para padronização de fios e cabos elétricos.
LISTA DE EXECÍCIOS AULA 3 FÍSICA ELETRICIDADE DENSIDADE DE CORRENTE E VELOCIDADE DE ARRASTE 1) A American Wire Gauge (AWG) é uma escala americana normalizada usada para padronização de fios e cabos elétricos.
Física I para Engenharia FEP111 ( )
 Física I para Engenharia FEP111 (4300111) 1º Semestre de 014 Instituto de Física Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdirg@if.usp.br Fone: 3091.7104 04 e 05 de agosto Bem-vindos
Física I para Engenharia FEP111 (4300111) 1º Semestre de 014 Instituto de Física Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdirg@if.usp.br Fone: 3091.7104 04 e 05 de agosto Bem-vindos
UFABC Fenômenos Térmicos Prof. Germán Lugones. Aula 2: Hidrodinâmica
 UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 2: Hidrodinâmica Definições Escoamento laminar (ou constante). É quando cada partícula do fluido possui uma trajetória suave, de modo que as trajetórias
UFABC Fenômenos Térmicos Prof. Germán Lugones Aula 2: Hidrodinâmica Definições Escoamento laminar (ou constante). É quando cada partícula do fluido possui uma trajetória suave, de modo que as trajetórias
PROGRAD / COSEAC Padrão de Respostas Física Grupo 04
 1 a QUESTÃO: Dois blocos estão em contato sobre uma mesa horizontal. Não há atrito entre os blocos e a mesa. Uma força horizontal é aplicada a um dos blocos, como mostra a figura. a) Qual é a aceleração
1 a QUESTÃO: Dois blocos estão em contato sobre uma mesa horizontal. Não há atrito entre os blocos e a mesa. Uma força horizontal é aplicada a um dos blocos, como mostra a figura. a) Qual é a aceleração
Capítulo 11 - Teoria Cinética dos Gases. O número de Avogrado é número de moléculas contido em 1 mol de qualquer substãncia
 Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
Capítulo 11 - Teoria Cinética dos Gases Em 1811, o italiano Amedeo Avogrado enunciou 2 hipóteses: 1) As moléculas de um gás podem ser compostas por mais de um único átomo. 2) Nas mesmas condições de temperatura
Questão 01) a) km/h b) km/h c) 106 km/h d) 10,6 km/h. Questão 02)
 Questão 1) A órbita do planeta Terra, em torno do Sol, possui uma distância aproximada de 93 milhões de quilômetros. Sabendo-se que o ano possui 36 dias e horas, a velocidade média exercida pela Terra
Questão 1) A órbita do planeta Terra, em torno do Sol, possui uma distância aproximada de 93 milhões de quilômetros. Sabendo-se que o ano possui 36 dias e horas, a velocidade média exercida pela Terra
Universidade Federal do Pampa UNIPAMPA. Teoria Cinética do Gases
 Universidade Federal do ampa UNIAMA Teoria inética do Gases 7.alores específicos molares de um gás ideal A quantidade de gás ideal é medida pelo número de moles n, em vez da massa m O gás é submetido
Universidade Federal do ampa UNIAMA Teoria inética do Gases 7.alores específicos molares de um gás ideal A quantidade de gás ideal é medida pelo número de moles n, em vez da massa m O gás é submetido
