Professora : Elisângela Moraes
|
|
|
- Cláudio Carmona Bicalho
- 7 Há anos
- Visualizações:
Transcrição
1 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA -EEL Professora : Elisângela Moraes 02/03/2012
2 PROGRAMA RESUMIDO 1. Gases Ideais; 2. Gases Reais; 3. Termodinâmica; 4. Termoquímica; 5. Entropia; 6. Espontaneidade da reação.
3 AVALIAÇÃO A avaliação será feita por meio de provas escritas. A Nota Final (NF) será calculada da seguinte maneira NF = (P1 + P2)/2 EXAME: 13 de Julho de 2012
4 GASES IDEAIS a) Leide Boyle; b) Leide Charles c) Leide degay-lussac d) ALeidoGás Ideal
5 INTRODUÇÃO Gás Vapor Gás: uma substância que normalmente se encontra no estado gasoso na temperatura e pressão ambiente. Exs.:Hélio, Hidrogênio, Oxigênio, entre outros. Vapor: a forma gasosa de uma substância que normalmente é um líquido ou um sólido na temperatura e pressão ambiente. Ex.:Água
6 RAZÕES PARA INVESTIGAR OS GASES 1ª.: Alguns elementos e compostos comuns existem no estado gasoso, nas condições normais de temperatura e pressão. Além disso podem ser vaporizados, e as propriedades destes vapores são importantes. 2ª.:Nossa atmosfera gasosa proporciona meios de movimentar energia e materiais sobre toda a superfície terrestre e é a fonte de muitos produtos químicos vitais. 3ª.: Os gases são os mais simples quando a investigação é feita a nível molecular.
7 PROPRIEDADES DOS GASES Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre formam misturas homogêneas com outros gases. Os gases ocupam somente cerca de 0,1 % do volume de seus recipientes.
8 PROPRIEDADES DOS GASES Para descrever o estado gasoso são necessárias 04 (quatro) grandezas: pressão, volume, temperatura e a quantidade degás. Pressão: Força por unidade de área. Aparelho usado para medir pressão: Barômetro Unidades: a pressão medida em um barômetro de mercúrio é mmhg,,também chamada de torr; pode ser também registrada em atmosfera normal(atm) que se define por: 1atmosferapadrão=1atm=760mmHg *AUnidadedoSI(SistemaInternacional)éopascal(Pa).
9 PROPRIEDADES DOS GASES GASES IDEAIS E GASES PERFEITOS RESPEITEM AS SEGUINTES CONDIÇÕES: O gás é constituído por um número muito grande de moléculas em movimento desordenado descrito pelas Leis de Newton. O volume próprio das moléculas é desprezível frente ao volume do recipiente. As forças intermoleculares são desprezíveis, exceto nas colisões mútuas e com as paredes do recipiente. As colisões são elásticas e de duração desprezível. Os gases perfeitos obedecem a três leis bastante simples, que são a lei de Boyle, a lei de Gay-Lussac e a lei de Charles. Essas leis são formuladas segundo o comportamento de três grandezas que descrevem as propriedades dos gases: a pressão, o volume e a temperatura absoluta.
10 PROPRIEDADES DOS GASES PRESSÃO A pressão é a força atuando em um objeto por unidade de área: Pressão: A gravidade exerce uma força sobre a atmosfera terrestre. Uma coluna de ar de 1 m 2 de seção transversal exerce uma força de 10 5 N. A pressão de uma coluna de ar de 1 m 2 é de 100 kpa.
11 PRESSÃO A pressão atmosférica e o barômetro UnidadesSI:1N=1kgm/s 2 ;1Pa=1N/m 2. A pressão atmosférica é medida com um barômetro. Se um tubo é inserido em um recipiente de mercúrio aberto à atmosfera, o mercúrio subirá 760 mm no tubo. A pressão atmosférica padrão é a pressão necessária para suportar 760 mm dehgemumacoluna. Unidades: 1 atm = 760 mmhg 760 mmhg = 760 torr 760 torr = 1, Pa
12 PRESSÃO A pressão atmosférica e o barômetro As pressões de gases não abertos para a atmosfera são medidas em manômetros. Um manômetro consiste de um bulbo de gás preso a um tubo em forma de U contendo Hg: Se: Se: P gás < P atm P gás + P h = P atm P gás > P atm P gás = P atm + P h
13 PRESSÃO Se dois gases estiverem em recipientes separados tendo uma parede móvel comum, o gás comapressão mais altatenderáacomprimir o gás com pressão mais baixa. A pressão do gás que tem maior pressão diminuirá à media que ele se expande, e a do outro gás aumentará a medida em que ele é ele é comprimido. Os dois atingirão um estado em que as duas pressões são iguais e não haverá mais tendência de a parede móvel se deslocar. Esta situação corresponde ao equilíbrio mecânico.
14 VOLUME O volume de qualquer substância é o espaço ocupado por esta substância. No caso dos gases, o volume de uma dada amostra é igual ao volume do recipiente que a contém. As unidades usuais de volume são: litro (L), mililitro (ml), metro cúbico (m³)[s.i.], decímetro cúbico (dm³) e, centímetro cúbico (cm³).
15 TEMPERATURA O conceito de temperatura provém de observações que mostram ser possível uma alteração do estado físico de uma amostra. AtemperaturaT,éumapropriedadequeindicaosentidodofluxo de energia através de uma parede rígida e termicamente condutora. Se a energia passa de A para B quando dois corpos (A e B) estão em contato, dizemosqueatemperaturadeaémaiselevadodoqueadeb.
16 TEMPERATURA É conveniente fazer a distinção entre dois tipos de fronteira que podem separar dois corpos: Diatérmica: quando há condução de calor. Se uma mudança de estado é observada quando dois corpos com temperaturas diferentes são postos em contato. Adiabática: quando NÃO há condução de calor. Se não há nenhuma mudança de estado, mesmo que os dois corpos tenham temperaturas diferentes. Uma garrafa térmica é uma aproximação de um recipiente adiabático. O equilíbrio térmico é atingido quando não ocorre qualquer mudança de estado quando dois corpos A e B estão em contato através de uma parede diatérmica.
17 TEMPERATURA Imaginemos que um corpo A (por exemplo, um bloco de ferro) este já em equilíbrio térmico com um corpo B (um bloco de cobre) e que B esteja em equilíbriotérmicocomumcorpoc(umvasocomágua). Verifica-se experimentalmente que A e C também estão em equilíbrio térmico quando eles são postos em contato. Essa observação e resumida pela LEI ZERO DA TERMODINÂMICA: Se A está em equilíbrio térmico com B e se B está em equilíbrio térmico com C, então C também está em equilíbrio térmico coma. Esta lei é a base do conceito de temperatura e justifica o uso de termômetros como instrumentos de medida da temperatura.
18 TEMPERATURA Em resumo: Temperatura é a medida do grau médio de agitação térmica das partículas(moléculas) que constituem uma substância. No estudo dos gases, é utilizada a escala absoluta ou kelvin (K) e, no Brasil, a escalausualéacelsius( C). Portanto, para transformar graus Celsius (representada apenas por: T) em kelvin, temos:
19 LEI DOS GASES LEI DE BOYLE A temperatura constante, o volume ocupado por uma quantidade fixa de um gás é inversamente proporcional à sua pressão. P 1 V 1 =P 2 V 2 OU PV=K As transformações gasosas nas quais variam a pressão e o volume, mas a temperatura permanece constante, chamam-se TRANSFORMAÇÕES ISOTÉRMICAS.
20 LEI DOS GASES LEI DE BOYLE Na prática,a lei de Boyle não é obedecida com exatidão matemática. Chamamos gás ideal ou gás perfeito ao gás teórico que obedeceria à lei de Boyle com precisão matemática. Naprática,temososgasesreais. Quanto menor for a pressão e maior a temperatura do gás real,mais ele se aproxima do conceito de gás ideal ou perfeito. Podemos dizer que o gás real tende para o gás ideal à medida que a pressão tende para zero e a temperatura tende para infinito.
21 LEI DE BOYLE -EXEMPLOS Exemplo1.:Umaamostradenitrogêniogasosonabolsadeardeum carrotemapressãode745mmhgcomovolumede65l.seesta amostra foi transferida para uma bolsa de 25L, mantendo a mesma temperaturaqualapressãodogáscomonovovolume? Exemplo2.:UmaamostradeCO 2 napressãode55mmhg,ocupa umvolumede125ml.aamostraécomprimidadetalformaquea Novapressãodogásé78mmHg.Qualonovovolumequeogás ocupa?(a temperatura se manteve constante durante toda a experiência)
22 LEI DE CHARLES e GAY-LUSSAC A volume constante, a pressão de uma massa fixa de gás é diretamente proporcional à temperatura absoluta do gás. (TRANSFORMAÇÃO ISOVOLUMÉTRICA)
23 LEI DE CHARLES e GAY-LUSSAC A pressão constante, o volume de uma massa fixa de gás é diretamente proporcional à temperatura absoluta do gás. (TRANSFORMAÇÃOISOBÁRICA)
24 LEI DE CHARLES e GAY-LUSSAC À temperatura constante, uma determinada massa de gás ocupa um volume inversamente proporcional à pressão exercida sobre ele.
25 LEI DE CHARLES e GAY-LUSSAC -EXEMPLOS Exemplo1.:SuponhaquesetenhaumaamostradeCO 2 numaseringaselada.o volume degásé25,0ml àtemperatura ambiente (20ºC).Qual o volumefinal de gás,sevocêaqueceraseringasegurando-anamão,atéatemperaturade37ºc? Exemplo 2.: Um balão está cheio de hélio e tem o volume de 45,0L na temperatura ambiente (25ºC). Se o balão estiver cheio com a mesma quantidade de hélio num dia muito frio (-10ºC), qual o novo volume do balão? Considere que a pressão permaneceu constante.
26 EQUAÇÃO GERAL DOS GASES O volume de um gás é inversamente proporcional a sua pressão, a temperatura constante (Lei de Boyle) e diretamente proporcional à temperatura absoluta (K) à pressão constante (Lei de Charles). Essa equação é frequentemente chamada de LEI GERAL DOS GASES. Ela se aplica especificamente a equações onde a quantidade de gás permanece constante.
27 EQUAÇÃO GERAL DOS GASES
28 EQUAÇÃO GERAL DOS GASES -EXEMPLOS Exemplo 1.: Uma bola de gás (recipiente cilíndrico), com um volume de 22,0L contém hélio a pressão de 150atm e na temperatura de 31ºC. Quantas bolas de gás, cada uma com um volume de 5,0L, podem ser infladas num dia em que a pressãoatmosféricaéde755mmhgeatemperaturaéde22ºc? Exemplo 2.: Mesmo nos dias de hoje, a investigação das camadas superiores da atmosfera é feita através de balões equipados com instrumentos científicos. Estesbalõessãoinfladoscomgáshélio.Suponhaqueumbalão,comumvolume de4,19 x10 3 Lélançado atemperatura de22,5ºceapressão barômetrica éde 754mmHg. Qual o volume do balão quando este alcançar a altura de 32 quilômetros,ondeapressãoéde760mmhgeatemperaturaéde 33ºC?
29
GASES. https://www.youtube.com/watch?v=wtmmvs3uiv0. David P. White. QUÍMICA: A Ciência Central 9ª Edição Capítulo by Pearson Education
 GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
Características dos gases
 Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre formam misturas
Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre formam misturas
GASES. QUIMICA II a Unidade
 GASES QUIMICA II a Unidade Estado Físico de uma Substância sólido > líquido > gasoso Aumento do volume O estado de agregação da matéria varia com a distância entre as partículas que compõem a substância
GASES QUIMICA II a Unidade Estado Físico de uma Substância sólido > líquido > gasoso Aumento do volume O estado de agregação da matéria varia com a distância entre as partículas que compõem a substância
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
QUÍMICA I Gases
 QUÍMICA I 106201 Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre
QUÍMICA I 106201 Gases Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão, seu volume diminui. Os gases sempre
O ESTADO GASOSO - CARACTERÍSTICAS GERAIS
 Estado Gasoso O ESTADO GASOSO - CARACTERÍSTICAS GERAIS Os gases sempre tendem a ocupar todo o volume do recipiente que os contém (capacidade de expansão) Os gases têm massa (Volumes iguais de gases diferentes
Estado Gasoso O ESTADO GASOSO - CARACTERÍSTICAS GERAIS Os gases sempre tendem a ocupar todo o volume do recipiente que os contém (capacidade de expansão) Os gases têm massa (Volumes iguais de gases diferentes
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2. Propriedades Moleculares dos Gases
 CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
Físico-Química I. Profa. Dra. Carla Dalmolin. Gases. Gás perfeito (equações de estado e lei dos gases) Gases reais
 Físico-Química I Profa. Dra. Carla Dalmolin Gases Gás perfeito (equações de estado e lei dos gases) Gases reais Gás Estado mais simples da matéria Uma forma da matéria que ocupa o volume total de qualquer
Físico-Química I Profa. Dra. Carla Dalmolin Gases Gás perfeito (equações de estado e lei dos gases) Gases reais Gás Estado mais simples da matéria Uma forma da matéria que ocupa o volume total de qualquer
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Apostila de Química 01 Estudo dos Gases
 Apostila de Química 01 Estudo dos Gases 1.0 Conceitos Pressão: Número de choques de suas moléculas contra as paredes do recipiente. 1atm = 760mHg = 760torr 105Pa (pascal) = 1bar. Volume 1m³ = 1000L. Temperatura:
Apostila de Química 01 Estudo dos Gases 1.0 Conceitos Pressão: Número de choques de suas moléculas contra as paredes do recipiente. 1atm = 760mHg = 760torr 105Pa (pascal) = 1bar. Volume 1m³ = 1000L. Temperatura:
2.1 Breve história da termodinâmica
 2.1 Breve história da termodinâmica TERMODINÂMICA calor força, movimento No início, estudava os processos que permitiam converter calor em trabalho (força e movimento). 2.1 Breve história da termodinâmica
2.1 Breve história da termodinâmica TERMODINÂMICA calor força, movimento No início, estudava os processos que permitiam converter calor em trabalho (força e movimento). 2.1 Breve história da termodinâmica
AULA 03 GASES Cap. 4 Russel PROF. MARCELL MARIANO CORRÊA MACENO
 AULA 03 GASES Cap. 4 Russel PROF. MARCELL MARIANO CORRÊA MACENO Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
AULA 03 GASES Cap. 4 Russel PROF. MARCELL MARIANO CORRÊA MACENO Características dos gases Os gases são altamente compressíveis e ocupam o volume total de seus recipientes. Quando um gás é submetido à pressão,
Avenida Lourival Alfredo, 176, Poeira, Marechal Deodoro, Alagoas, Brasil,
 1 ESTUDO DOS GASES 1 INTRODUÇÃO Vários processos que ocorrem na natureza e nos organismos vivos são fenômenos pertinentes aos gases, como, por exemplo: o metabolismo nos animais exige a presença de oxigênio,
1 ESTUDO DOS GASES 1 INTRODUÇÃO Vários processos que ocorrem na natureza e nos organismos vivos são fenômenos pertinentes aos gases, como, por exemplo: o metabolismo nos animais exige a presença de oxigênio,
ATMOSFERA. Volume molar; constante de Avogadro
 ATMOSFERA Volume molar; constante de Avogadro 25-01-2011 Dulce Campos 2 O ar é uma solução gasosa Enquanto solução gasosa tem comportamentos semelhantes aos das substâncias gasosas 25-01-2011 Dulce Campos
ATMOSFERA Volume molar; constante de Avogadro 25-01-2011 Dulce Campos 2 O ar é uma solução gasosa Enquanto solução gasosa tem comportamentos semelhantes aos das substâncias gasosas 25-01-2011 Dulce Campos
GASES. Maira Gazzi Manfro e Giseli Menegat
 GASES Maira Gazzi Manfro e Giseli Menegat maira.manfro@caxias.ifrs.edu.br giseli.menegat@caxias.ifrs.edu.br Características dos Gases São menos densos que os sólidos e os líquidos; Sempre se misturam entre
GASES Maira Gazzi Manfro e Giseli Menegat maira.manfro@caxias.ifrs.edu.br giseli.menegat@caxias.ifrs.edu.br Características dos Gases São menos densos que os sólidos e os líquidos; Sempre se misturam entre
Luis Eduardo C. Aleotti. Química. Aula 38 - Transformações Gasosas
 Luis Eduardo C. Aleotti Química Aula 38 - Transformações Gasosas TRANSFORMAÇÕES GASOSAS Gás e Vapor - Gás: Substância gasosa em temperatura ambiente. - Vapor: Estado gasoso de uma substância líquida ou
Luis Eduardo C. Aleotti Química Aula 38 - Transformações Gasosas TRANSFORMAÇÕES GASOSAS Gás e Vapor - Gás: Substância gasosa em temperatura ambiente. - Vapor: Estado gasoso de uma substância líquida ou
Mecânica dos Fluidos 1ª parte
 Mecânica dos Fluidos 1ª parte Introdução à Mecânica dos Fluidos Prof. Luís Perna 2010/11 Noção de Fluido Fluido é toda a substância que macroscopicamente apresenta a propriedade de escoar. Essa maior ou
Mecânica dos Fluidos 1ª parte Introdução à Mecânica dos Fluidos Prof. Luís Perna 2010/11 Noção de Fluido Fluido é toda a substância que macroscopicamente apresenta a propriedade de escoar. Essa maior ou
Estudo Físico-Químico dos Gases
 19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS. Prof. MSc. Danilo Cândido
 FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS Prof. MSc. Danilo Cândido CONCEITOS DE GASES Um gás representa a forma mais simples da matéria, de baixa densidade e que ocupa o volume total de qualquer recipiente
FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS Prof. MSc. Danilo Cândido CONCEITOS DE GASES Um gás representa a forma mais simples da matéria, de baixa densidade e que ocupa o volume total de qualquer recipiente
Combustíveis Energia e Ambiente. Combustíveis gasosos, líquidos e sólidos: compreender as diferenças
 Combustíveis gasosos, líquidos e sólidos: compreender as diferenças 1 Estados físicos de hidrocarbonetos em função do número de carbonos da cadeia Os gases combustíveis podem ser agrupados em famílias,
Combustíveis gasosos, líquidos e sólidos: compreender as diferenças 1 Estados físicos de hidrocarbonetos em função do número de carbonos da cadeia Os gases combustíveis podem ser agrupados em famílias,
Equação Geral dos Gases
 Equação Geral dos Gases EXERCÍCIOS DE APLICAÇÃO 01 (EEM-SP) Uma determinada massa gasosa, confinada em um recipiente de volume igual a 6,0 L, está submetida a uma pressão de 2,5 atm e sob temperatura de
Equação Geral dos Gases EXERCÍCIOS DE APLICAÇÃO 01 (EEM-SP) Uma determinada massa gasosa, confinada em um recipiente de volume igual a 6,0 L, está submetida a uma pressão de 2,5 atm e sob temperatura de
Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal.
 Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal. Equações de Estado Não é fácil trabalhar com as tabelas termodinâmicas. A dificuldade está associada ao volume delas e a possibilidade
Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal. Equações de Estado Não é fácil trabalhar com as tabelas termodinâmicas. A dificuldade está associada ao volume delas e a possibilidade
Todo gás exerce uma PRESSÃO, ocupando um certo VOLUME à determinada TEMPERATURA
 Todo gás exerce uma PRESSÃO, ocupando um certo VOLUME à determinada TEMPERATURA Aos valores da pressão, do volume e da temperatura chamamos de ESTADO DE UM GÁS Assim: V 5 L T 300 K P 1 atm Os valores da
Todo gás exerce uma PRESSÃO, ocupando um certo VOLUME à determinada TEMPERATURA Aos valores da pressão, do volume e da temperatura chamamos de ESTADO DE UM GÁS Assim: V 5 L T 300 K P 1 atm Os valores da
Gases ideais. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 217 Gás = conjunto de moléculas ou átomos
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 217 Gás = conjunto de moléculas ou átomos
2. Conceitos e Definições
 2. Conceitos e Definições Sistema e Volume de Controle Sistema Termodinâmico: região do espaço delimitada fisicamente por superfícies geométricas arbitrárias reais ou imaginárias, que podem ser fixas ou
2. Conceitos e Definições Sistema e Volume de Controle Sistema Termodinâmico: região do espaço delimitada fisicamente por superfícies geométricas arbitrárias reais ou imaginárias, que podem ser fixas ou
3º Trimestre Sala de estudo Química Data: 26/03/19 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº
 3º Trimestre Sala de estudo Química Data: 26/03/19 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº Conteúdo: Gases (equação geral dos gases) Questão 01 - (Mackenzie SP/2018) Certa massa fixa de um
3º Trimestre Sala de estudo Química Data: 26/03/19 Ensino Médio 3º ano classe: A_B Profª Danusa Nome: nº Conteúdo: Gases (equação geral dos gases) Questão 01 - (Mackenzie SP/2018) Certa massa fixa de um
1,0 atm; 3,0 atm; 3,3 atm; 3,9 atm; 4,0 atm.
 1. Um tubo cilíndrico de oxigênio de um mergulhador contém 3,2 kg de O 2. Antes de mergulhar, verificou-se que a temperatura e a pressão no interior do cilindro valiam, respectivamente, 27 C e 1,5 atm.
1. Um tubo cilíndrico de oxigênio de um mergulhador contém 3,2 kg de O 2. Antes de mergulhar, verificou-se que a temperatura e a pressão no interior do cilindro valiam, respectivamente, 27 C e 1,5 atm.
Vejamos agora alguns casos particulares dessas transformações com quantidade de gás constante.
 Setor 2306 Aula 06 Transformações Gasosas em sistemas fechados Complemento. Como vimos em aula, as transformações realizadas em sistemas fechados tem sua quantidade de gás constante. Nessa situação, a
Setor 2306 Aula 06 Transformações Gasosas em sistemas fechados Complemento. Como vimos em aula, as transformações realizadas em sistemas fechados tem sua quantidade de gás constante. Nessa situação, a
Soluções e Gases III. Gases
 Soluções e Gases III Gases Gases Gás é um material que preenche todo o espaço ou volume do recipiente em que se encontra, independentemente do tamanho do recipiente. Ar 78 % de N 2 21% de O 2 1% de outros
Soluções e Gases III Gases Gases Gás é um material que preenche todo o espaço ou volume do recipiente em que se encontra, independentemente do tamanho do recipiente. Ar 78 % de N 2 21% de O 2 1% de outros
Gases ideais. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 317 Gás = conjunto de moléculas ou átomos
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Gases ideais Professora: Melissa Soares Caetano Disciplina QUI 317 Gás = conjunto de moléculas ou átomos
QUÍMICA Profº JAISON
 QUÍMICA Profº JAISON GASES O gás ideal As equações que utilizamos para estudar o comportamento dos gases nunca fornecem valores exatos. Na tentativa de nos aproximarmos mais do valor exato, estabelecemos
QUÍMICA Profº JAISON GASES O gás ideal As equações que utilizamos para estudar o comportamento dos gases nunca fornecem valores exatos. Na tentativa de nos aproximarmos mais do valor exato, estabelecemos
Gases. 1) Assinale a alternativa CORRETA.
 Gases 1) Assinale a alternativa CORRETA. (A) Uma determinada massa de gás ideal, ocupando um volume constante, tem sua pressão inversamente proporcional à sua temperatura absoluta. (B) Em uma transformação
Gases 1) Assinale a alternativa CORRETA. (A) Uma determinada massa de gás ideal, ocupando um volume constante, tem sua pressão inversamente proporcional à sua temperatura absoluta. (B) Em uma transformação
ESTUDO DOS GASES. Energia cinética de um gás. Prof. Patricia Caldana
 ESTUDO DOS GASES Prof. Patricia Caldana Gases são fluidos no estado gasoso, a característica que o difere dos fluidos líquidos é que, quando colocado em um recipiente, este tem a capacidade de ocupa-lo
ESTUDO DOS GASES Prof. Patricia Caldana Gases são fluidos no estado gasoso, a característica que o difere dos fluidos líquidos é que, quando colocado em um recipiente, este tem a capacidade de ocupa-lo
ELEMENTOS QUE FORMAM GASES NAS CONDIÇÕES NORMAIS
 ELEMENTOS QUE FORMAM GASES NAS CONDIÇÕES NORMAIS Substância no estado gasoso é definida por 4 qualidades: Volume Quantidade de matéria (mol) Temperatura Pressão 1. fase gasosa Átomos He Ar (gases nobres)
ELEMENTOS QUE FORMAM GASES NAS CONDIÇÕES NORMAIS Substância no estado gasoso é definida por 4 qualidades: Volume Quantidade de matéria (mol) Temperatura Pressão 1. fase gasosa Átomos He Ar (gases nobres)
2 Temperatura Empírica, Princípio de Carnot e Temperatura Termodinâmica
 2 Temperatura Empírica, Princípio de Carnot e Temperatura Termodinâmica 2.1 Temperatura empírica: medidas de temperatura Termômetro: Sistema com uma propriedade mensurável que varia com a temperatura (propriedade
2 Temperatura Empírica, Princípio de Carnot e Temperatura Termodinâmica 2.1 Temperatura empírica: medidas de temperatura Termômetro: Sistema com uma propriedade mensurável que varia com a temperatura (propriedade
Capítulo 1. Propriedades dos Gases
 Capítulo 1. Propriedades dos Gases Baseado no livro: Atkins Physical Chemistry Eighth Edition Peter Atkins Julio de Paula 14-03-2007 Maria da Conceição Paiva 1 O estado físico de uma substância A equação
Capítulo 1. Propriedades dos Gases Baseado no livro: Atkins Physical Chemistry Eighth Edition Peter Atkins Julio de Paula 14-03-2007 Maria da Conceição Paiva 1 O estado físico de uma substância A equação
Termodinâmica e Sistemas Térmicos. Prof. M.Sc. Guilherme Schünemann
 Termodinâmica e Sistemas Térmicos Prof. M.Sc. Guilherme Schünemann Introdução o que é termodinâmica Termo refere-se ao calor Dinâmica força ou movimento Atualmente é uma ciência que trata da transformação
Termodinâmica e Sistemas Térmicos Prof. M.Sc. Guilherme Schünemann Introdução o que é termodinâmica Termo refere-se ao calor Dinâmica força ou movimento Atualmente é uma ciência que trata da transformação
Aluno(a): nº: Professor: Fernanda TonettoSurmas Data: Turma: ORIENTAÇÕES DE ESTUDO REC 2º TRI PRIMEIRO ANO FSC II
 1º EM E.M. FÍSICA Aluno(a): nº: Professor: Fernanda TonettoSurmas Data: Turma: ORIENTAÇÕES DE ESTUDO REC º TRI PRIMEIRO ANO FSC II Estudar FÍSICA II LIVRO PV = nrt Dilatação dos Sólidos e dos Líquidos
1º EM E.M. FÍSICA Aluno(a): nº: Professor: Fernanda TonettoSurmas Data: Turma: ORIENTAÇÕES DE ESTUDO REC º TRI PRIMEIRO ANO FSC II Estudar FÍSICA II LIVRO PV = nrt Dilatação dos Sólidos e dos Líquidos
Aluno (a): nº: Professor: Fernanda Tonetto Surmas Data: Turma: ESTUDO DOS GASES
 1º EM E.M. FÍSICA Aluno (a): nº: Professor: Fernanda Tonetto Surmas Data: Turma: Resumão com exercícios: ESTUDO DOS GASES INTRODUÇÃO O estudo dos gases é de grande importância na compreensão de fatos que
1º EM E.M. FÍSICA Aluno (a): nº: Professor: Fernanda Tonetto Surmas Data: Turma: Resumão com exercícios: ESTUDO DOS GASES INTRODUÇÃO O estudo dos gases é de grande importância na compreensão de fatos que
Gases UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG120. Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI
 UNIERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG10 http://www.met.reading.ac.uk/~swrmethn/balloon/ Gases Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI A Estrutura
UNIERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG10 http://www.met.reading.ac.uk/~swrmethn/balloon/ Gases Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI A Estrutura
Física I 2010/2011. Aula 18. Mecânica de Fluidos I
 Física I 2010/2011 Aula 18 Mecânica de Fluidos I Sumário Capítulo 14: Fluidos 14-1 O que é um Fluido? 14-2 Densidade e Pressão 14-3 Fluidos em Repouso 14-4 A Medida da pressão 14-5 O Princípio de Pascal
Física I 2010/2011 Aula 18 Mecânica de Fluidos I Sumário Capítulo 14: Fluidos 14-1 O que é um Fluido? 14-2 Densidade e Pressão 14-3 Fluidos em Repouso 14-4 A Medida da pressão 14-5 O Princípio de Pascal
Termodinâmica 7. Alexandre Diehl. Departamento de Física - UFPel
 Termodinâmica 7 Alexandre Diehl Departamento de Física - UFPel Robert Boyle (1627-1691) Experimentos com tubo manométrico mercúrio 2 Robert Boyle (1627-1691) Experimentos com tubo manométrico 3 Robert
Termodinâmica 7 Alexandre Diehl Departamento de Física - UFPel Robert Boyle (1627-1691) Experimentos com tubo manométrico mercúrio 2 Robert Boyle (1627-1691) Experimentos com tubo manométrico 3 Robert
Profa. Dra. Ana Maria Pereira Neto
 Universidade Federal do ABC BC1309 Termodinâmica Aplicada Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Conceitos Fundamentais 1 Conceitos Fundamentais Termodinâmica:
Universidade Federal do ABC BC1309 Termodinâmica Aplicada Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Conceitos Fundamentais 1 Conceitos Fundamentais Termodinâmica:
Universidade Federal do Pampa UNIPAMPA. Teoria Cinética do Gases
 Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Física Geral e Experimental III. Exercícios Temperatura e Dilatação
 Física Geral e Experimental III Exercícios Temperatura e Dilatação 1. Em um dia quando a temperatura alcança 50ºF, qual é a temperatura em graus Celsius e Kelvins? R: 10ºC; 283 K. 2. O ouro tem um ponto
Física Geral e Experimental III Exercícios Temperatura e Dilatação 1. Em um dia quando a temperatura alcança 50ºF, qual é a temperatura em graus Celsius e Kelvins? R: 10ºC; 283 K. 2. O ouro tem um ponto
QUÍMICA - 1 o ANO MÓDULO 22 RELAÇÕES NUMÉRICAS FUNDAMENTAIS - PARTE 2
 QUÍMICA - 1 o ANO MÓDULO 22 RELAÇÕES NUMÉRICAS FUNDAMENTAIS - PARTE 2 Fixação 1) (UNESP) O volume de uma massa fixa de gás ideal, a pressão constante, é diretamente proporcional à: a) concentração do gás.
QUÍMICA - 1 o ANO MÓDULO 22 RELAÇÕES NUMÉRICAS FUNDAMENTAIS - PARTE 2 Fixação 1) (UNESP) O volume de uma massa fixa de gás ideal, a pressão constante, é diretamente proporcional à: a) concentração do gás.
Disciplina: Sistemas Térmicos
 Disciplina: Sistemas Térmicos Definição de Substância Pura Equilíbrio de Fases Líquido-Vapor de uma Substância Pura Diagrama de Temperatura versus Volume Específico Título de uma Substância com Fases Líquida
Disciplina: Sistemas Térmicos Definição de Substância Pura Equilíbrio de Fases Líquido-Vapor de uma Substância Pura Diagrama de Temperatura versus Volume Específico Título de uma Substância com Fases Líquida
Gases. 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação?
 Capítulo 2 Gases 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação? Van der Waals verificou que o fato do gás real não se comportar como o gás ideal é
Capítulo 2 Gases 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação? Van der Waals verificou que o fato do gás real não se comportar como o gás ideal é
EXERCÍCIOS DE FIXAÇÃO QUÍMICA GASES I
 Aluno (a): Profº: RICARDO Série: Data: / / Disc: QUÍMICA EXERCÍCIOS DE FIXAÇÃO QUÍMICA GASES I 1. Uma Massa fixa de um gás ideal foi submetida a uma série de transformações isotérmicas e alguns dos valores
Aluno (a): Profº: RICARDO Série: Data: / / Disc: QUÍMICA EXERCÍCIOS DE FIXAÇÃO QUÍMICA GASES I 1. Uma Massa fixa de um gás ideal foi submetida a uma série de transformações isotérmicas e alguns dos valores
Estudo dos gases. Prof. Leandro Zatta - Química Geral 1
 Estudo dos gases Prof. Leandro Zatta - Química Geral 1 Modelo molecular dos gases Há pouca matéria em um dado volume Existência de muito espaço vazio entre as moléculas individuais São tão facilmente comprimidos
Estudo dos gases Prof. Leandro Zatta - Química Geral 1 Modelo molecular dos gases Há pouca matéria em um dado volume Existência de muito espaço vazio entre as moléculas individuais São tão facilmente comprimidos
Prática 03 Determinação do Zero Absoluto
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 03 Determinação do Zero Absoluto 1. Introdução
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 03 Determinação do Zero Absoluto 1. Introdução
Transformações Gasosas
 Transformações Gasosas EXERCÍCIOS DE APLICAÇÃO 01 (FEI-SP) Certa massa de um gás perfeito sofre transformação de A para B e de B para C, conforme mostra o diagrama abaixo. Sabendo-se que a transformação
Transformações Gasosas EXERCÍCIOS DE APLICAÇÃO 01 (FEI-SP) Certa massa de um gás perfeito sofre transformação de A para B e de B para C, conforme mostra o diagrama abaixo. Sabendo-se que a transformação
Química da atmosfera...
 Atmosfera é a camada de ar que envolve a Terra do grego atmos = vapor do latim sphaera = invólucro. Assim, a palavra atmosfera pode significar: invólucro de vapor. Química - O estudo das propriedades e
Atmosfera é a camada de ar que envolve a Terra do grego atmos = vapor do latim sphaera = invólucro. Assim, a palavra atmosfera pode significar: invólucro de vapor. Química - O estudo das propriedades e
Gases. Reis, Oswaldo Henrique Barolli. R375g Gases / Oswaldo Henrique Barolli. Varginha, slides : il.
 Gases Reis, Oswaldo Henrique Barolli. R375g Gases / Oswaldo Henrique Barolli. Varginha, 2015. 21 slides : il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World Wide Web 1. Dinâmica dos gases.
Gases Reis, Oswaldo Henrique Barolli. R375g Gases / Oswaldo Henrique Barolli. Varginha, 2015. 21 slides : il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World Wide Web 1. Dinâmica dos gases.
2º ano FÍSICA Prof. Márcio Marinho DIAGRAMA DE FASES E GASES PERFEITOS
 DIAGRAMA DE FASES 1º) Uma determinada porção de uma substância passa do estado líquido para o estado sólido. A porção de sólido obtida flutua sobre a parte que ainda está líquida. Pode-se afirmar que:
DIAGRAMA DE FASES 1º) Uma determinada porção de uma substância passa do estado líquido para o estado sólido. A porção de sólido obtida flutua sobre a parte que ainda está líquida. Pode-se afirmar que:
Capítulo 21 Temperatura
 Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
Capítulo 21 Temperatura 21.1 Temperatura e equilíbrio térmico Mecânica: lida com partículas. Variáveis microscópicas: posição, velocidade, etc. Termodinâmica: lida com sistemas de muitas partículas. Variáveis
EM34F Termodinâmica A
 EM34F Termodinâmica A Prof. Dr. André Damiani Rocha arocha@utfpr.edu.br Aula 01 Parte II: Introdução 2 Aula 01 Definição de Termodinâmica A termodinâmica é a ciência da energia; O nome Termodinâmica deriva
EM34F Termodinâmica A Prof. Dr. André Damiani Rocha arocha@utfpr.edu.br Aula 01 Parte II: Introdução 2 Aula 01 Definição de Termodinâmica A termodinâmica é a ciência da energia; O nome Termodinâmica deriva
Conceitos primordiais da Termodinâmica
 Conceitos primordiais da Termodinâmica Miguel Almeida 1 Propriedades de Estado Propriedade de estado é aquela que sua variação não depende do "caminho" mas sim dos estados final e inicial. Pode ser equacionada
Conceitos primordiais da Termodinâmica Miguel Almeida 1 Propriedades de Estado Propriedade de estado é aquela que sua variação não depende do "caminho" mas sim dos estados final e inicial. Pode ser equacionada
Estudo da Física. Prof. Railander Borges
 Estudo da Física Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges ASSUNTO: GASES 1. Uma panela de pressão com
Estudo da Física Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges ASSUNTO: GASES 1. Uma panela de pressão com
Estado Gasoso. Classe: 2 2 a série. Exercícios Complementares - Recuperação Paralela PARTE A
 Ensino Médio Exercícios Complementares - Recuperação Paralela Classe: 2 2 a série QUÍMICA Estado Gasoso PARTE A 1. Explique o fato de uma bola de futebol parecer mais "cheia" durante o dia e mais murcha
Ensino Médio Exercícios Complementares - Recuperação Paralela Classe: 2 2 a série QUÍMICA Estado Gasoso PARTE A 1. Explique o fato de uma bola de futebol parecer mais "cheia" durante o dia e mais murcha
A) 2,5 B) 4 C) 5 D) 7,5 E) 10
 1-Uma massa gasosa, inicialmente num estado A, sofre duas transformações sucessivas e passa para um estado C. A partir do estado A esse gás sofre uma transformação isobárica e passa para o estado B. A
1-Uma massa gasosa, inicialmente num estado A, sofre duas transformações sucessivas e passa para um estado C. A partir do estado A esse gás sofre uma transformação isobárica e passa para o estado B. A
Disciplina: Sistemas Térmicos
 Disciplina: Sistemas Térmicos Apresentação da Termodinâmica Sistemas Termodinâmicos e Volume de Controle Estado e Propriedades de uma Substância Processos Termodinâmicos e Ciclos Conceitos e Unidades Lei
Disciplina: Sistemas Térmicos Apresentação da Termodinâmica Sistemas Termodinâmicos e Volume de Controle Estado e Propriedades de uma Substância Processos Termodinâmicos e Ciclos Conceitos e Unidades Lei
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
Lei fundamental da hidrostática
 Sumário Unidade I MECÂNICA 3- de fluidos - Lei fundamental da hidrostática ou Lei de Stevin. - Vasos comunicantes Equilíbrio de dois líquidos não miscíveis. - Relação entre as pressões de dois pontos,
Sumário Unidade I MECÂNICA 3- de fluidos - Lei fundamental da hidrostática ou Lei de Stevin. - Vasos comunicantes Equilíbrio de dois líquidos não miscíveis. - Relação entre as pressões de dois pontos,
Termodinâmica. Prof.: POMPEU
 1. DEFINIÇÃO A estuda a relação entre calor e trabalho que um sistema (por exemplo, um gás) troca com o meio exterior. 2. ENERGIA INTERNA (U) É a soma das várias formas de energia das moléculas que constituem
1. DEFINIÇÃO A estuda a relação entre calor e trabalho que um sistema (por exemplo, um gás) troca com o meio exterior. 2. ENERGIA INTERNA (U) É a soma das várias formas de energia das moléculas que constituem
Conceitos Básicos sobre gases
 Conceitos Básicos sobre gases ara este estudo não vamos fazer distinção entre gás e vapor, desta forma neste capítulo, o estado gasoso (gás ou vapor) será sempre referido como gás... ressão dos gases Suponha
Conceitos Básicos sobre gases ara este estudo não vamos fazer distinção entre gás e vapor, desta forma neste capítulo, o estado gasoso (gás ou vapor) será sempre referido como gás... ressão dos gases Suponha
EXPERIÊNCIA 2 DETERMINAÇÃO DA MASSA MOLECULAR DE UM GÁS EFEITO DA PRESSÃO NO PONTO DE EBULIÇÃO
 1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Interpretar as leis que regem o comportamento dos gases ideais. Utilizar a equação da lei do gás ideal, PV = nrt Medir o volume e a
1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Interpretar as leis que regem o comportamento dos gases ideais. Utilizar a equação da lei do gás ideal, PV = nrt Medir o volume e a
TERMODINÂMICA APLICADA
 TERMODINÂMICA APLICADA LEONARDO DE QUEIROZ MOREIRA Conceitos e definições GOIÂNIA, 29/08/2016. Objetivo Apresentar os conceitos e definições preliminares utilizadas durante o curso de termodinâmica Aplicada;
TERMODINÂMICA APLICADA LEONARDO DE QUEIROZ MOREIRA Conceitos e definições GOIÂNIA, 29/08/2016. Objetivo Apresentar os conceitos e definições preliminares utilizadas durante o curso de termodinâmica Aplicada;
Estado Gasoso. Características. Expansibilidade compressibilidade. Situação de um gás. Variáveis de estado
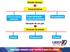 Estado Gasoso Características Forma/volume variáveis Expansibilidade compressibilidade Situação de um gás Difusibilidade Variáveis de estado Volume emperatura Pressão Mudança de estado de uma certa massa
Estado Gasoso Características Forma/volume variáveis Expansibilidade compressibilidade Situação de um gás Difusibilidade Variáveis de estado Volume emperatura Pressão Mudança de estado de uma certa massa
SISTEMAS TÉRMICOS PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução desse material sem a
 PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS INTRODUÇÃO E CONCEITOS INICIAIS ALBERTO HERNANDEZ NETO PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução
PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS INTRODUÇÃO E CONCEITOS INICIAIS ALBERTO HERNANDEZ NETO PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução
FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR
 FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR TEMPERATURA Grandeza Fundamental do S.I. Medida aproximada de agitação média de moléculas Unidade Principal: (Kelvin)
FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR TEMPERATURA Grandeza Fundamental do S.I. Medida aproximada de agitação média de moléculas Unidade Principal: (Kelvin)
4,5 cm. 3,0 cm. 3,0 cm. 4,5 cm. 3,0 cm
 1. Uma bolha de ar, com volume de 1,5 cm, forma-se no fundo de um lago, a 20 m de profundidade, e sobe até atingir a superfície. A pressão atmosférica no local tem valor de 1,0 atm e a temperatura do lago
1. Uma bolha de ar, com volume de 1,5 cm, forma-se no fundo de um lago, a 20 m de profundidade, e sobe até atingir a superfície. A pressão atmosférica no local tem valor de 1,0 atm e a temperatura do lago
01) (UPE-2011-Q1) Em relação à teoria cinética molecular dos gases, é CORRETO afirmar que:
 01) (UPE-2011-Q1) Em relação à teoria cinética molecular dos gases, é CORRETO afirmar que: a) a energia cinética média de um conjunto de moléculas de um gás depende, apenas e exclusivamente, das massas
01) (UPE-2011-Q1) Em relação à teoria cinética molecular dos gases, é CORRETO afirmar que: a) a energia cinética média de um conjunto de moléculas de um gás depende, apenas e exclusivamente, das massas
Física II FEP 112 ( ) 1º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física Geral e Experimental III. Dilatação
 Física Geral e Experimental III Dilatação 6. Em um dia quente em Las Vegas um caminhão-tanque foi carregado com 37.000 L de óleo diesel. Ele encontrou tempo frio ao chegar a Payson, Utha, onde a temperatura
Física Geral e Experimental III Dilatação 6. Em um dia quente em Las Vegas um caminhão-tanque foi carregado com 37.000 L de óleo diesel. Ele encontrou tempo frio ao chegar a Payson, Utha, onde a temperatura
Segunda Lei da Termodinâmica
 Físico-Química I Profa. Dra. Carla Dalmolin Segunda Lei da Termodinâmica Espontaneidade das reações químicas Entropia Terceira Lei da Termodinâmica Primeira Lei da Termodinâmica Estabelece que as transformações
Físico-Química I Profa. Dra. Carla Dalmolin Segunda Lei da Termodinâmica Espontaneidade das reações químicas Entropia Terceira Lei da Termodinâmica Primeira Lei da Termodinâmica Estabelece que as transformações
Fisica do Calor ( ) Prof. Adriano Mesquita Alencar Dep. Física Geral Instituto de Física da USP A01. Introdução
 Fisica do Calor (4300159) Prof. Adriano Mesquita Alencar Dep. Física Geral Instituto de Física da USP A01 Introdução Data Programa do curso agosto 9 agosto 12 agosto 16 agosto 19 agosto 23 agosto 26 Temperatura
Fisica do Calor (4300159) Prof. Adriano Mesquita Alencar Dep. Física Geral Instituto de Física da USP A01 Introdução Data Programa do curso agosto 9 agosto 12 agosto 16 agosto 19 agosto 23 agosto 26 Temperatura
Química Prof. Giacometto
 Química Prof. Giacometto LISTA DE EXERCÍCIOS SOBRE O ESTADO GASOSO (SÓ UEM) OBS: SEMPRE QUE JULGAR NECESSÁRIO O VALOR DA MASSA ATÔMICA DE UM ELEMENTO QUÍMICO, UTILIZAR A TABELA PERIÓDICA 01) (UEM) Considerando
Química Prof. Giacometto LISTA DE EXERCÍCIOS SOBRE O ESTADO GASOSO (SÓ UEM) OBS: SEMPRE QUE JULGAR NECESSÁRIO O VALOR DA MASSA ATÔMICA DE UM ELEMENTO QUÍMICO, UTILIZAR A TABELA PERIÓDICA 01) (UEM) Considerando
FUNDAMENTOS FÍSICOS DO AR COMPRIMIDO
 DEFINIÇÃO: O ar é incolor, insípido e é uma mistura de diversos gases. Composição percentual do ar seco padrão: (ISO 2533). Elementos Percentual em volume Percentual em massa Nitrogênio 78,08 75,52 Oxigênio
DEFINIÇÃO: O ar é incolor, insípido e é uma mistura de diversos gases. Composição percentual do ar seco padrão: (ISO 2533). Elementos Percentual em volume Percentual em massa Nitrogênio 78,08 75,52 Oxigênio
Escola Politécnica da Universidade de São Paulo. Termodinâmica. Conceitos Fundamentais. v. 1.0
 Termodinâmica Conceitos Fundamentais 1 v. 1.0 Sistema termodinâmico quantidade de matéria com massa e identidade fixas sobre a qual nossa atenção é dirigida. Volume de controle região do espaço sobre a
Termodinâmica Conceitos Fundamentais 1 v. 1.0 Sistema termodinâmico quantidade de matéria com massa e identidade fixas sobre a qual nossa atenção é dirigida. Volume de controle região do espaço sobre a
MÁQUINAS HIDRÁULICAS AT-087
 Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS HIDRÁULICAS AT-087 Dr. Alan Sulato de Andrade alansulato@ufpr.br DEFINIÇÃO: Um fluído consiste numa substância não sólida
Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS HIDRÁULICAS AT-087 Dr. Alan Sulato de Andrade alansulato@ufpr.br DEFINIÇÃO: Um fluído consiste numa substância não sólida
GASES MÓDULO 1 TRANSFORMAÇÕES QUÍMICAS
 GASES MÓDULO 1 TRANSFORMAÇÕES QUÍMICAS GASES GASES IDEAIS OU PERFEITOS Um gás perfeito é um gás hipotético. Por definição, é aquele que obedece, rigorosamente, às leis de Boyle e Charles, ou seja: As moléculas
GASES MÓDULO 1 TRANSFORMAÇÕES QUÍMICAS GASES GASES IDEAIS OU PERFEITOS Um gás perfeito é um gás hipotético. Por definição, é aquele que obedece, rigorosamente, às leis de Boyle e Charles, ou seja: As moléculas
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 11 Estudo Geral dos Gases 1.
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 11 Estudo Geral dos Gases 1.
Turma: 2201 Turno: Manhã Professor: Douglas Baroni
 Colégio Zaccaria TELEFAX: (0 XX 21) 3235-9400 www.zaccaria.g12.br Lista de exercícios Física II (Recuperação) 1º Período 2014 Aluno(a): N.º Turma: 2201 Turno: Manhã Professor: Douglas Baroni QUESTÃO 1
Colégio Zaccaria TELEFAX: (0 XX 21) 3235-9400 www.zaccaria.g12.br Lista de exercícios Física II (Recuperação) 1º Período 2014 Aluno(a): N.º Turma: 2201 Turno: Manhã Professor: Douglas Baroni QUESTÃO 1
Estequiometria. Mestranda: Daniele Potulski Disciplina: Química da madeira I
 Estequiometria Mestranda: Daniele Potulski Disciplina: Química da madeira I Estequiometria Estequiometria é o cálculo da quantidade de reagentes e produtos da reação, baseado nas leis das reações químicas.
Estequiometria Mestranda: Daniele Potulski Disciplina: Química da madeira I Estequiometria Estequiometria é o cálculo da quantidade de reagentes e produtos da reação, baseado nas leis das reações químicas.
Aula anterior: Esta Aula: Próxima aula:
 Aula anterior: Composição da atmosfera: do que é composta; fontes e sumidouros; como alcançou o estado atual. Breve discussão sobre pressão, densidade, temperatura. Esta Aula: Temperatura, pressão e densidade
Aula anterior: Composição da atmosfera: do que é composta; fontes e sumidouros; como alcançou o estado atual. Breve discussão sobre pressão, densidade, temperatura. Esta Aula: Temperatura, pressão e densidade
ATMOSFERA Temperatura, pressão, densidade e grandezas associadas.
 ATMOSFERA Temperatura, pressão, densidade e grandezas associadas. As camadas na atmosfera são: Troposfera. Estratosfera. Mesosfera Termosfera Exosfera As camadas na atmosfera são definidas a partir de
ATMOSFERA Temperatura, pressão, densidade e grandezas associadas. As camadas na atmosfera são: Troposfera. Estratosfera. Mesosfera Termosfera Exosfera As camadas na atmosfera são definidas a partir de
LISTA DE EXERCÍCIOS FÍSICA 2º TRIMESTRE ESTUDO DOS GASES
 LISTA DE EXERCÍCIOS FÍSICA 2º TRIMESTRE Nome: nº: Ano: 2º EM Professor: Anderson ESTUDO DOS GASES INTRODUÇÃO O estudo dos gases é de grande importância na compreensão de fatos que ocorrem no nosso cotidiano,
LISTA DE EXERCÍCIOS FÍSICA 2º TRIMESTRE Nome: nº: Ano: 2º EM Professor: Anderson ESTUDO DOS GASES INTRODUÇÃO O estudo dos gases é de grande importância na compreensão de fatos que ocorrem no nosso cotidiano,
JAMILE ROSA RAMPINELLI
 Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
Transformações Gasosas
 Transformações Gasosas Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 (FEI-SP) Certa massa de um gás perfeito sofre transformação de A para B e de B para C, conforme
Transformações Gasosas Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 (FEI-SP) Certa massa de um gás perfeito sofre transformação de A para B e de B para C, conforme
Note que, no Sistema Internacional de Unidades (SI) o calor é medido em calorias (cal) ou joules (J).
 Calor e temperatura Prof. lucasmarqui Calor e Temperatura são dois conceitos fundamentais na termologia (Termofísica) os quais, são considerados sinônimos. No entanto, o calor designa a troca de energia
Calor e temperatura Prof. lucasmarqui Calor e Temperatura são dois conceitos fundamentais na termologia (Termofísica) os quais, são considerados sinônimos. No entanto, o calor designa a troca de energia
FÍSICA TÉRMICA. Prof. Neemias Alves de Lima Instituto de Pesquisa em Ciência dos Materiais Universidade Federal do Vale do São Francisco 1
 FÍSICA TÉRMICA Prof. Neemias Alves de Lima Instituto de Pesquisa em Ciência dos Materiais Universidade Federal do Vale do São Francisco 1 Domínio da Física Térmica Como pode água aprisionada ser ejetada
FÍSICA TÉRMICA Prof. Neemias Alves de Lima Instituto de Pesquisa em Ciência dos Materiais Universidade Federal do Vale do São Francisco 1 Domínio da Física Térmica Como pode água aprisionada ser ejetada
TERMODINÂMICA E ESTÁTICA DA ATMOSFERA. Capítulo 2 Vianello & Alves Meteorologia Básica e Aplicações
 TERMODINÂMICA E ESTÁTICA DA ATMOSFERA Capítulo 2 Vianello & Alves Meteorologia Básica e Aplicações INTRODUÇÃO A atmosfera é uma imensa máquina térmica, cuja principal fonte de calor é a energia solar.
TERMODINÂMICA E ESTÁTICA DA ATMOSFERA Capítulo 2 Vianello & Alves Meteorologia Básica e Aplicações INTRODUÇÃO A atmosfera é uma imensa máquina térmica, cuja principal fonte de calor é a energia solar.
Bacharelado Engenharia Civil
 Bacharelado Engenharia Civil Disciplina: Fenômenos de Transporte 5 Período Prof.a: Msd. Érica Muniz Aula 02 Propriedades dos Fluidos Algumas propriedades são fundamentais para a análise de um fluido e
Bacharelado Engenharia Civil Disciplina: Fenômenos de Transporte 5 Período Prof.a: Msd. Érica Muniz Aula 02 Propriedades dos Fluidos Algumas propriedades são fundamentais para a análise de um fluido e
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA PARAÍBA Campus Princesa Isabel. Fluidos. Disciplina: Física Professor: Carlos Alberto
 INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA PARAÍBA Campus Princesa Isabel Fluidos Disciplina: Física Professor: Carlos Alberto Objetivos de aprendizagem Ao estudar este capítulo você aprenderá:
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA PARAÍBA Campus Princesa Isabel Fluidos Disciplina: Física Professor: Carlos Alberto Objetivos de aprendizagem Ao estudar este capítulo você aprenderá:
Capitulo-4 Calor e Temperatura
 Capitulo-4 Calor e Temperatura www.plantaofisica.blogspot.com.br 1 Resumo de aula: Termometria. 1- Temperatura Termometria é a parte da física que se preocupa unicamente em formas de se medir a temperatura
Capitulo-4 Calor e Temperatura www.plantaofisica.blogspot.com.br 1 Resumo de aula: Termometria. 1- Temperatura Termometria é a parte da física que se preocupa unicamente em formas de se medir a temperatura
