Sistemas (Homogêneo e Heterogêneo)
|
|
|
- Ronaldo Assunção Belo
- 7 Há anos
- Visualizações:
Transcrição
1 Sistemas (Homogêneo e Heterogêneo) EXERCÍCIOS DE APLICAÇÃO 01 Verifique quais os materiais homogêneos e heterogêneos: a) vidro; b) álcool 96 GL (96% de álcool e 4% de água); c) ouro 18 k; d) gás oxigênio misturado com gás nitrogênio; e) leite; f) granito; g) gelatina; h) sangue; i) ferro-gusa. 02 Indique o número de fases em cada um dos sistemas abaixo: I) água e cloreto de chumbo II (insolúvel); II) água e açúcar dissolvido; III) água e açúcar em excesso; IV)H2O(ℓ) H2O(v) ; V) H2 H2O(ℓ H2O(v) ; VI)CaO(s) + CuSO4(s) ; VII) N2(g) + CO2(g) ; VIII) água + açúcar + sal (dissolvidos); IX) água e sal em excesso X) álcool e água. Portal de Estudos em Química (PEQ) Página 1
2 03 (UFG-GO) São transformações químicas: 01) o apodrecimento de um fruto; 02) a efervescência de um comprimido de sonrisal em água; 04) o escurecimento da superfície de um metal exposta ao ar; 08) o cozimento de alimentos; 16) a fermentação da uva; 32) o derretimento de um picolé de abacaxi. 06 Em cinco recipientes encontramos misturas distintas, a saber: Soma ( ) 04 (FCC-SP) Esta questão apresenta três afirmativas que podem estar corretas ou incorretas. Responda-as, obedecendo ao seguinte código: a) Somente a afirmativa I é correta. b) Somente a afirmativa II é correta. c) Somente a afirmativa III é correta. d) Somente as afirmativas I e II são corretas. e) As afirmativas I, II e III são corretas. Em quais recipientes encontramos uma mistura homogênea? a) I, II, III e V; b) I e V; c) II, III e IV; d) II, III e V; e) II, III, IV e V. 07 (FAEE-GO) É exemplo de solução (I) sólida, (II) líquida e (III) gasosa à temperatura ambiente e à pressão normal: O conteúdo do recipiente acima representa um sistema: I) formado por substância pura. II) constituído por uma única substância. III) trifásico. 05 Imaginemos um sistema formado por gás cloro, gás metano e gás oxigênio. Não havendo nenhum tipo de reação entre eles, podemos classificar o sistema como: a) homogêneo; b) heterogêneo; c) pode ser homogêneo ou heterogêneo, conforme a proporção dos gases; d) pode ser homogêneo ou heterogêneo, conforme as condições de temperatura e pressão (sem ocorrer mudança de esta do de agregação); e) pode ser homogêno ou heterogêneo, conforme as condições de pressão dos gases. 08 (UFRN-RN) A água mineral filtrada (sem gás) é: a) uma substância pura. b) uma mistura heterogênea. c) uma mistura homogênea. d) uma substância composta. e) um elemento. 09 (FMU-SP) A água destilada é um exemplo de: a) substância simples. b) composto químico. c) mistura homogênea. d) elemento químico. e) mistura heterogênea. Portal de Estudos em Química (PEQ) Página 2
3 10 (UFES-ES) Observe a representação dos sistemas I, II e III e seus componentes. O número de fases em cada um é, respectivamente: a) 3, 2 e 4. b) 3, 3 e 4. c) 2, 2 e 4. d) 3, 2 e 5. e) 3, 3 e 6. Portal de Estudos em Química (PEQ) Página 3
4 EXERCÍCIOS PROPOSTOS 11 (FUVEST-SP) Se esses materiais forem classificados em substâncias puras e misturas, pertencerão ao grupo das substâncias puras: a) ar, gás carbônico e latão; b) iodo, ouro 18 quilates e naftaleno; c) gás carbônico, latão e iodo; d) ar, ouro 18 quilates e naftaleno; e) gás carbônico, iodo e naftaleno. 12 (Fac. Filo. do Recife-PE) Indique a alternativa falsa. a) Um sistema contendo apenas água e um pouco de açúcar forma uma mistura homogênea. b) Um sistema constituído por três pedaços de ouro puro é monofásico. c) Uma substância pura sempre constituirá um sistema monofásico. d) A água e o álcool etílico formam misturas homogêneas em quaisquer proporções. e) A água do filtro é uma mistura homogênea. 13 Assinale a alternativa correta. a) Todo sistema homogêneo é uma mistura homogênea. b) Todo sistema heterogêneo é uma mistura heterogênea. c) Todo sistema heterogêneo é monofásico. d) Todo sistema homogêneo é polifásico. e) Todo sistema heterogêneo pode ser uma mistura heterogênea ou uma substância pura em mais de um estado físico. 14 (UFV-MG) Um recipiente A contém um líquido incolor que, após aquecimento até secura, deixa um resíduo branco. Um recipiente B contém uma substância líquida azulada transparente e uma substância escura depositada. A substância líquida contida no recipiente B foi transferida para um recipiente C, que, após aquecimento, deixa um resíduo azulado. Assinale a alternativa que classifica corretamente os sistemas A, B e C, respectivamente: a) mistura homogênea, mistura heterogênea e mistura homogênea; b) mistura heterogênea, mistura heterogênea e mistura homogênea; c) solução, solução composta binária e mistura homogênea; d) mistura heterogênea, mistura heterogênea e mistura heterogênea; e) mistura homogênea, solução e mistura heterogênea. 15 Constitui um sistema heterogêno a mistura formada de: a) cubos de gelo e solução aquosa de açúcar (glicose). b) gases N 2 e CO 2. c) água e acetona. d) água e xarope de groselha. e) querosene e óleo diesel. Portal de Estudos em Química (PEQ) Página 4
5 16 (FUVEST-SP) Propriedades de algumas substâncias: 19 (UFRGS-RS) Considere as seguintes propriedades de três substâncias líquidas: A 25 C, 3,00g de iodo, 70 cm 3 de água e 50 cm 3 de CCl 4 são colocados em um funil de separação. Após agitação e repouso, qual dos esquemas abaixo deve representar a situação final? Misturando-se volumes iguais de hexano, tetracloreto de carbono e água, será obtido um sistema a) monofásico. b) bifásico, no qual a fase sobrenadante é o hexano. c) bifásico, no qual o sobrenadante é o tetracloreto de carbono. d) trifásico, no qual a fase intermediária é o tetracloreto de carbono. e) bifásico ou trifásico, dependendo da ordem de colocação das substâncias durante a preparação da mistura. 20 Um sistema fechado contendo H 2 O(gasoso); H 2 O (líquido); H 2 O (sólido), areia e pouca quantidade de açúcar apresenta quantas fases e quantos componentes? 17 (FEI-SP) Assinale a alternativa onde encontramos uma substância pura, uma mistura homogênea e um sistema heterogêneo. a) Açúcar, água doce, água do mar. b) Leite, suco de laranja, feijoada. c) Água destilada, água potável, água e gelo. d) Vinagre, vinho, álcool etílico. e) Geléia, água potável, suco de frutas. 18 (PUC-Campinas-SP) O sistema formado por etanol, água e três cubos de gelo é X e contém Y substâncias químicas. Completa-se corretamente a afirmação mencionada substituindo-se X e Y, respectivamente, por: a) bifásico - duas. b) bifásico - três. c) trifásico - duas. d) tetrafásico - três. e) pentafásico - duas. 21 (UFSM-RS) O café filtrado apresenta fase(s), contendo uma. Assinale as palavras que completam, respectivamente, as lacunas. a) uma - substância composta b) duas - mistura homogênea c) uma - mistura heterogênea d) duas - substância simples e) uma - mistura homogênea Portal de Estudos em Química (PEQ) Página 5
6 22 Uma festa de aniversário foi decorada com dois tipos de balões. Diferentes componentes gasosos foram usados para encher cada tipo de balão. As figuras observadas representam as substâncias presentes no interior de cada balão. a) Indique quantos elementos diferentes e quantas substâncias simples diferentes existem nos balões. b) Classifique o tipo de sistema de cada balão quanto à homogeneidade. 23 (ITA-SP) Num experimento, um estudante verificou ser a mesma a temperatura de fusão de várias amostras de um mesmo material no estado sólido e também que esta temperatura se manteve constante até a fusão completa. Considere que o material sólido tenha sido classificado como: I. Substância simples pura II. Substância composta pura III. Mistura homogênea eutética IV. Mistura heterogênea Então, das classificações acima, está(ão) ERRADA(S) a) apenas I e II. b) apenas II e III. c) apenas III. d) apenas III e IV. e) apenas IV. 24 (UFPR-PR) Numa proveta de 100 ml, foram colocados 25 ml de CCl 4, 25 ml de água destilada e 25 ml de tolueno (C 7 H 8 ). A seguir, foi adicionada uma pequena quantidade de iodo sólido (I 2 ) ao sistema. O aspecto final pode ser visto na figura a seguir: Pode-se dizer que o número de fases, o número de componentes e o número de elementos químicos presentes no sistema esquematizado é de: a) 3, 4 e 6. b) 1, 3 e 5. c) 1, 5 e 6. d) 3, 4 e 5. e) 2, 3 e (UNESP-SP) Uma amostra de água do rio Tietê, que apresentava partículas em suspensão, foi submetida a processos de purificação obtendo-se, ao final do tratamento, uma solução límpida e cristalina. Em relação às amostras de água antes e após o tratamento, podemos afirmar que correspondem, respectivamente, a: a) substâncias composta e simples. b) substâncias simples e composta. c) misturas homogênea e heterogênea. d) misturas heterogênea e homogênea. e) mistura heterogênea e substância simples. 26 (UFLA-MG) Considere os sistemas a seguir. Os sistemas I, II e III correspondem, respectivamente, a: a) mistura heterogênea, substância composta, mistura heterogênea. b) mistura homogênea, substância simples, mistura heterogênea. c) mistura homogênea, substância simples, mistura homogênea. d) mistura homogênea, substância composta, mistura heterogênea. Portal de Estudos em Química (PEQ) Página 6
7 27 (CFT-SC) Em um laboratório de química, em condições ambientais, foram preparadas as seguintes misturas: I) gasolina + areia II) água + gasolina III) oxigênio + nitrogênio IV) água + sal V) água + álcool Quais misturas podem ser homogêneas? a) III, IV e V, somente. b) II, III e IV, somente. c) IV e V, somente. d) I, II e IV, somente. e) I e II, somente. 28 (CFT-SC) Quando uma garrafa de água gaseificada é aberta, formam-se bolhas de dióxido de carbono. Nessa situação, o sistema água + gás forma: a) uma substância simples. b) uma mistura homogênea. c) uma solução. d) uma mistura heterogênea. e) uma substância composta. 29 (UTFPR-PR) O soro hospitalar é formado por uma solução aquosa de cloreto de sódio e glicose. Esse sistema apresenta: a) uma fase e um componente. b) três fases e um componente. c) uma fase e dois componentes. d) três fases e três componentes. e) uma fase e três componentes. d) Mistura homogênea, mistura heterogênea e mistura homogênea. e) Mistura heterogênea, substância homogênea e substância heterogênea. 31 (CFT-CE) Aplicando os conceitos fundamentais da matéria e da energia, é correto afirmar que: a) toda mistura de dois sólidos é sempre homogênea. b) uma mistura de vários gases pode ser homogênea ou heterogênea, dependendo da proporção entre os mesmos. c) toda mistura de um líquido mais um gasoso (gás) sempre é homogênea. d) as misturas água + sal e gasolina + álcool são homogêneas em quaisquer proporções. e) uma substância pura pode constituir um sistema heterogêneo, quando mudando de fase. 32 (CFT-MG) Sobre os seguintes sistemas: I - ouro II - água mineral III - água + óleo IV - ar atmosférico é correto afirmar que a) II e IV são homogêneos. b) III e IV são heterogêneos. c) I e III constituem misturas. d) I e II representam substâncias puras. 30 (UEL-PR) Um rapaz pediu sua namorada em casamento, presenteando-a com uma aliança de ouro 18 quilates. Para comemorar, sabendo que o álcool é prejudicial à saúde, eles brindaram com água gaseificada com gelo, ao ar livre. Os sistemas: ouro 18 quilates, água gaseificada com gelo e ar atmosférico, são, respectivamente: a) Substância heterogênea, mistura heterogênea e mistura homogênea. b) Mistura heterogênea, mistura homogênea e substância homogênea. c) Substância homogênea, mistura heterogênea e mistura homogênea. 33 (CFT-MG) A tabela a seguir apresenta propriedades de algumas substâncias. Analisando-se os dados fornecidos, à temperatura ambiente, a(s) substância(s) Portal de Estudos em Química (PEQ) Página 7
8 a) A é a mais volátil. b) A e D são gasosas. c) B e E formam uma mistura homogênea. d) C se separa da água por destilação simples. 34 (CFT-PR) Considere os seguintes sistemas: I) nitrogênio + oxigênio. II) 100 ml de álcool (C 2 H 6 O) em 1 litro de água. III) 1 colher de açúcar (C 12 H 22 O 11 ) em 1 litro de água. IV) 3 cubos de gelo em solução aquosa de sal. Sobre eles afirma-se corretamente que a) I é heterogêneo, formado por substâncias simples. b) II é heterogêneo, formado por substâncias compostas. c) III é homogêneo, formado por 2 fases e 1 componente. d) IV é heterogêneo, formado por 2 fases e 2 componentes. 35 (UFU-MG) Quando o preço do álcool está com "bom preço", é comum adulterarem a gasolina com adição de álcool acima dos 20 % v/v, atualmente permitidos por lei. A gasolina batizada (adulterada) cria uma série de problemas para o motor. Uma maneira de verificar a qualidade da gasolina com etanol anidro em excesso é fazer o Teste da Proveta. Este teste consiste em adicionar 50 ml de uma solução aquosa saturada com cloreto de sódio em uma proveta de 100 ml, contendo 50 ml da gasolina. Em seguida, a proveta é agitada e deixada em repouso por alguns minutos. Assinale a alternativa que representa, no Teste da Proveta, uma gasolina adulterada. (Dados: Densidade da água = 1 g cm -3 ; densidade da mistura álcool e gasolina < 1 g cm -3.) 36 (PUC-MG) Assinale a afirmativa INCORRETA. a) Todas as amostras de uma substância pura têm a mesma composição e as mesmas propriedades. b) Um exemplo de mistura homogênea é a preparada pela mistura de dois líquidos como etanol e água. c) Um exemplo de mistura heterogênea é aquela preparada pela dissolução de um sólido como o cloreto de sódio em um líquido como a água. d) Um composto é uma substância que pode ser decomposta, através de reações químicas, em substâncias mais simples. 37 (UFRRJ-RJ) Observe os dados listados na tabela a seguir: Com base nessas propriedades físicas, é possível, por exemplo, extrair o álcool que é adicionado à gasolina comercial. Este procedimento pode ser feito da seguinte maneira: a um determinado volume de gasolina adiciona-se o mesmo volume de água. A mistura é agitada, e a seguir, colocada em repouso. Forma-se, então, um sistema bifásico que pode ser separado com a ajuda de um funil de separação. Tendo como base os dados da tabela, podemos afirmar que neste procedimento ocorre(m) o(s) seguinte(s) fenômeno(s): I. Quando a gasolina (que contém álcool) é misturada à água, o álcool é extraído pela água, e o sistema resultante é bifásico: gasolina/água-álcool. II. Quando a gasolina (que contém álcool) é misturada à água, a gasolina é extraída pela água, e o sistema resultante é bifásico: álcool/água-gasolina. III. A mistura água-álcool formada é um sistema homogêneo (monofásico), com propriedades diferentes daquelas das substâncias que a compõem. Destas considerações, somente a) I é correta. b) II é correta. c) III é correta. d) II e III são corretas. e) I e III são corretas. Portal de Estudos em Química (PEQ) Página 8
9 38 (UNESP-SP) Uma das formas utilizadas na adulteração da gasolina consiste em adicionar a este combustível solventes orgânicos que formem misturas homogêneas, como o álcool combustível. Considere os seguintes sistemas, constituídos por quantidades iguais de: 1 - gás oxigênio, gás carbônico e gás argônio; 2 - água líquida, clorofórmio e sulfato de cálcio; 3 - n-heptano, benzeno e gasolina; todos nas condições normais de temperatura e pressão. a) Indique o número de fases dos sistemas 1, 2 e 3 e classifique-os como sistema homogêneo ou heterogêneo. b) Se fosse adicionado querosene ao sistema 3, quantas fases este apresentaria? Justifique sua resposta. 39 (UFRS-RS) Analise os sistemas materiais abaixo, estando ambos na temperatura ambiente. Sistema I - Mistura de 10 g de sal de cozinha, 30 g de areia fina, 20 ml de óleo e 100 ml de água. Sistema II - Mistura de 2,0 L de CO 2, 3,0 L de N 2 e 1,5 L de O 2. Sobre esses sistemas é correto afirmar que a) ambos são heterogêneos, pois apresentam mais de uma fase. b) em I, o sistema é bifásico, após forte agitação, e, em II, o sistema é monofásico. c) em I, o sistema é trifásico, após forte agitação, e, em II, o sistema é monofásico. d) ambos apresentam uma única fase, formando sistemas homogêneos. e) em I, o sistema é trifásico, independentemente da ordem de adição dos componentes, e, em II, o sistema é bifásico. 40 (PUC-RS) Responder à questão numerando corretamente a coluna que contém exemplos de sistemas, de acordo com a que apresenta a classificação dos mesmos. 1- elemento químico 2- substância simples 3- substância composta 4- mistura homogênea 5- mistura heterogênea ( ) fluoreto de sódio ( ) gás oxigênio ( ) água do mar filtrada ( ) limonada com gelo A alternativa que contém a sequência correta dos números da coluna inferior, de cima para baixo, é: a) b) c) d) e) (UFSC-SC) Observe os recipientes A, B e C e seus respectivos conteúdos. Após mistura e agitação do conteúdo dos três recipientes em um só, observa-se que apenas parte do açúcar e parte do gelo permanecem insolúveis. Assinale o número de fases e o número de componentes do sistema resultante. 01. trifásico componentes 04. bifásico componentes componentes 32. monofásico componentes Soma ( ) Portal de Estudos em Química (PEQ) Página 9
10 42 (UFSM-RS) Assinale verdadeira (V) ou falsa (F) em cada afirmação. ( ) O ouro 18 quilates é classificado como solução. ( ) O ar atmosférico com poeira constitui uma mistura homogênea. ( ) O granito é um exemplo de mistura heterogênea. ( ) O sangue constitui uma mistura homogênea. A sequência correta é a) V - F - F - V. b) V - V - F - V. c) F - V - V - F. d) V - F - V - F. e) F - V - F - F. 43 (UFU-MG) Indique a alternativa que correlaciona, corretamente, os materiais abaixo como sendo (a) mistura ou (b) substância pura. I - Bicarbonato de sódio. II - Gasolina. III - Ar atmosférico. IV - Água do mar. a) I (b); II (a); III (a); IV (b) b) I (a); II (a); III (a); IV (a) c) I (b); II (b); III (b); IV (b) d) I (b); II (a); III (a); IV (a) e) I (a); II (b); III (b); IV (a) 44 (UFES-ES) Considere os seguintes sistemas: I - nitrogênio e oxigênio; II - etanol hidratado; III - água e mercúrio. Assinale a alternativa correta. a) Os três sistemas são homogêneos. b) O sistema I é homogêneo e formado por substâncias simples. c) O sistema II é homogêneo e formado por substâncias simples e composta. d) O sistema III é heterogêneo e formado por substâncias compostas. e) O sistema III é uma solução formada por água e mercúrio. 45 (PUCCAMP-SP) As proposições a seguir foram formuladas por um estudante, após o estudo de substâncias puras e misturas. I. O leite puro não pode ser representado por fórmula molecular porque é uma mistura de várias substâncias. II. Como se trata de substância pura, o álcool anidro apresenta ponto de ebulição e densidade característicos. III. A água mineral é substância pura de composição definida. IV. O ar empoeirado é mistura heterogênea sólido + gás. V. Por ser substância pura, o café coado não pode ser submetido a processos de fracionamento de misturas. Quantas proposições estão corretas? a) 1 b) 2 c) 3 d) 4 e) 5 46 (UFF-RJ) Considere os seguintes sistemas: Os sistemas I, II e III correspondem, respectivamente, a: a) substância simples, mistura homogênea, mistura heterogênea. b) substância composta, mistura heterogênea, mistura heterogênea. c) substância composta, mistura homogênea, mistura heterogênea. d) substância simples, mistura homogênea, mistura homogênea. e) substância composta, mistura heterogênea, mistura homogênea. Portal de Estudos em Química (PEQ) Página 10
11 47 (UNESP-SP) O rótulo de uma garrafa de água mineral está reproduzido a seguir. Composição Química provável: Sulfato de cálcio 0,0038 mg/l Bicarbonato de cálcio 0,0167 mg/l Com base nestas informações, podemos classificar a água mineral como a) substância pura. b) substância simples. c) mistura heterogênea. d) mistura homogênea. e) suspensão coloidal. 48 (FUVEST-SP) Bronze, "gelo seco" e diamante são, respectivamente, exemplos de: a) mistura, substância simples e substância composta. b) mistura, substância composta e substância simples. c) substância composta, mistura e substância simples. d) substância composta, substância simples e mistura. e) substância simples, mistura e substância composta. 49 (UFBA-BA) Os diferentes tipos de matéria podem ser classificados em dois grupos: - substâncias puras; - misturas. As substâncias puras podem ser simples ou compostas... (NABUCO, p. 24) Considerando-se esse modo de classificação, pode-se afirmar: (01) O ar atmosférico é uma substância pura. (02) A água é uma substância simples. (04) O sangue é uma mistura. (08) Uma solução de açúcar é uma mistura. (16) O oxigênio e o ozônio são substâncias distintas, embora constituídas por átomos de um mesmo elemento químico. (32) A matéria que contém três tipos de molécula é uma substância composta. (64) A matéria que contém apenas um tipo de molécula é uma substância simples, mesmo que cada molécula seja formada por dois átomos diferentes. Soma ( ) 50 São dados três sistemas: A: óleo, água e gelo; B: óleo, água gaseificada e gelo; C: óleo, água e granito. O número de fases de cada sistema é respectivamente: a) 3, 4 e 5; b) 3, 3 e 5; c) 3, 3 e 3; d) 3, 4 e 3; e) 3, 4 e 4. Portal de Estudos em Química (PEQ) Página 11
12 GABARITO 01- a) vidro - homogêneo b) álcool 96 GL - homogêneo c) ouro 18 k - homogêneo d) gás oxigênio misturado com gás nitrogênio - homogêneo e) leite - heterogêneo (gotículas de gordura em suspensão num líquido) f) granito - heterogêneo (quartzo, feldspato e mica) g) gelatina - heterogêneo (todos os colóides são heterogêneos ao ultramicroscópio) h) sangue - heterogêneo (glóbulos em suspensão num líquido) i) ferro-gusa - heterogêneo (ferro-gusa é ferro com alto teor de carbono - 4%). Observando ferro-gusa ao microscópio, acharemos cristais de grafita ao lado de cristais de ferro. 02- I) 2 fases (uma sólida, pois cloreto de chumbo II é insolúvel na água, e uma líquida); II) 1 fase (açúcar é solúvel em água); III) 2 fases (uma líquida e uma sólida no fundo do recipiente ); IV)2 fases (uma líquida e uma gasosa); V) 3 fases (uma sólida, uma líquida e uma gasosa); VI)2 fases (cada sólido é uma fase); VII) 1 fase (mistura de gases forma sempre uma só fase); VIII) 1 fase (sal e açúcar são solúveis em água e não foi indicado que havia excesso de algum deles); IX) 2 fases (uma sólida no fundo e uma líquida); X) 1 fase (são miscíveis em qualquer proporção). 03- Itens corretos: C 05- A 06- D 07- B 08- C 09- B 10- E 11- E 12- C 13- E 14- A 15- A 16- B 17- C 18- A 19- E 20-4 fases e 3 componentes. H 2 O = s, l, g : 1 componente; 3 fases Areia (SiO 2 ) : 1 componente ; 1 fase Açúcar comum (C 12 H 22 O 11 ): 1 componente, dissolvido na água (líquida) Total: 4 fases e 3 componentes. 21- E 22- a) Balão I: 1 elemento e 1 substância simples. Balão II: 4 elementos e 2 substâncias simples. Total de elementos diferentes: 5 Portal de Estudos em Química (PEQ) Página 12
13 Total de substâncias simples: 3 b) Balão I: sistema homogêneo. Balão II: sistema homogêneo. 23- E 24- D 25- D 26- D 27- A 28- D 29- E 30- D 31- E 32- A 33- C 34- D 35- C 36- C 37- E 38- a) Todos os sistemas estão nas condições normais de temperatura e pressão, ou seja, 0ºC e 1 atm. Sistema 1: Temos a mistura de 3 gases (O 2, CO 2 e Ar), portanto, como nas condições normais os componentes desta mistura continuam gasosos e toda mistura gasosa é monofásica, o sistema 1 possui uma única fase e é homogêneo. Sistema 2: Temos a mistura de H 2 O(s), CH 3 Cl(l) e CaSO 4 (s), como o sulfato de cálcio é praticamente insolúvel em água e no clorofórmio e como a água é muito pouco solúvel no clorofórmio, o sistema 2 apresentará 3 fases e será heterogêneo. Sistema 3: Temos a mistura de C 7 H 16 (l), C 6 H 6 (l) e gasolina, como se trata de uma mistura miscível de três líquidos apolares o sistema formado terá uma fase e será homogêneo. b) Como o querosene é uma mistura de hidrocarbonetos apolares e todos os componentes do sistema 3 são apolares eles seriam miscíveis, logo teríamos uma única fase e o sistema seria homogêneo. 39- C 40- A = D 43- D 44- B 45- C 46- C 47- D 48- B = A Portal de Estudos em Química (PEQ) Página 13
EXERCÍCIOS SUBSTÂNCIAS E MISTURAS
 EXERCÍCIOS SUBSTÂNCIAS E MISTURAS 1- Considere o sistema e responda as questões: A) Quantos átomos estão representados? B) Quantos elementos químicos há no sistema? C) Quantas moléculas estão representadas
EXERCÍCIOS SUBSTÂNCIAS E MISTURAS 1- Considere o sistema e responda as questões: A) Quantos átomos estão representados? B) Quantos elementos químicos há no sistema? C) Quantas moléculas estão representadas
Lista de Exercício. 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada sistema?
 Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
3ªHumanas e Master - Química Prof os João Lins e Alexandre Estevão
 3ªHumanas e Master - Química Prof os João Lins e Alexandre Estevão 1) Um sistema heterogêneo, S, é constituído por uma solução colorida e um sólido branco. O sistema foi submetido ao seguinte esquema de
3ªHumanas e Master - Química Prof os João Lins e Alexandre Estevão 1) Um sistema heterogêneo, S, é constituído por uma solução colorida e um sólido branco. O sistema foi submetido ao seguinte esquema de
04) (Unicap-PE) Julgue os itens abaixo:
 01) (UNB-DF) Julgue os itens abaixo, indicando aqueles que se referem a propriedades químicas das substâncias e, aqueles que se referem a propriedades físicas das substâncias. 1) A glicose é um sólido
01) (UNB-DF) Julgue os itens abaixo, indicando aqueles que se referem a propriedades químicas das substâncias e, aqueles que se referem a propriedades físicas das substâncias. 1) A glicose é um sólido
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
9 o EF. Jeosafá de P. Lima
 9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
BIMESTRAL QUÍMICA - 1ºBIMESTRE
 BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
SUBSTÂNCIAS E MISTURAS
 SUBSTÂNCIAS E MISTURAS SUBSTÂNCIAS Uma substância química (ou apenas substância) é um material que apresenta um conjunto de propriedades bem definido e constante e tem composição fixa, independente da
SUBSTÂNCIAS E MISTURAS SUBSTÂNCIAS Uma substância química (ou apenas substância) é um material que apresenta um conjunto de propriedades bem definido e constante e tem composição fixa, independente da
Unidade São Judas Tadeu
 Unidade São Judas Tadeu Professor: Me. DIOGO LOPES Aluno (a): Ano: 9º Data: / / 2017. Lista de QUÍMICA Orientações: - A lista deverá ser respondida na própria folha impressa ou em folha de papel almaço.
Unidade São Judas Tadeu Professor: Me. DIOGO LOPES Aluno (a): Ano: 9º Data: / / 2017. Lista de QUÍMICA Orientações: - A lista deverá ser respondida na própria folha impressa ou em folha de papel almaço.
9 o EF. Jeosafá de P. Lima. Exercícios sobre separação de misturas
 9 o EF QUÍMICA Exercícios Jeosafá de P. Lima Exercícios sobre separação de misturas 1) (VUNESP-2006) A preparação de um chá utilizando os já tradicionais saquinhos envolve, em ordem de acontecimento, os
9 o EF QUÍMICA Exercícios Jeosafá de P. Lima Exercícios sobre separação de misturas 1) (VUNESP-2006) A preparação de um chá utilizando os já tradicionais saquinhos envolve, em ordem de acontecimento, os
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas:
 Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
Exercícios Aspectos Macroscópicos
 Exercícios Aspectos Macroscópicos 1. Observe atentamente os processos abaixo: I. Efervescência ocorrida ao se colocar água oxigenada sobre um ferimento. II. A imagem de uma célula é ampliada por um microscópio.
Exercícios Aspectos Macroscópicos 1. Observe atentamente os processos abaixo: I. Efervescência ocorrida ao se colocar água oxigenada sobre um ferimento. II. A imagem de uma célula é ampliada por um microscópio.
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
Hipótese de Avogadro e Volume Molar
 Hipótese de Avogadro e Volume Molar EXERCÍCIOS DE APLICAÇÃO 01 (UFES-ES) Três balões contêm H, N e O, conforme ilustrado abaixo: Considerando-se que os gases estão sob pressão de 1 atm e à mesma temperatura,
Hipótese de Avogadro e Volume Molar EXERCÍCIOS DE APLICAÇÃO 01 (UFES-ES) Três balões contêm H, N e O, conforme ilustrado abaixo: Considerando-se que os gases estão sob pressão de 1 atm e à mesma temperatura,
Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g)
 Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
Química B Extensivo V. 2
 Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
Química B Extensivo V. 2 Exercícios Sistema Componentes Fases Classificação Água + gelo 1 2 Heterogêneo Água + 3 cubos de gelo 1 2 Heterogêneo Açúcar + sal 2 2 Heterogêneo Areia + enxofre + sal 3 3 Heterogêneo
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016
 ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 1,0 ) I. Introdução Neste bimestre, sua média foi inferior a 6,0
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 1,0 ) I. Introdução Neste bimestre, sua média foi inferior a 6,0
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK
 PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
2-Nos sistemas abaixo, diga quantos átomos, elementos, moléculas e substâncias estão representados:
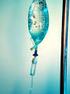 LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
Atividade extra. Questão 1 Cecierj Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Tarefa 22 Professor Gustavo
 6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA EXPERIMENTAL
 INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA EXPERIMENTAL ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA EXPERIMENTAL ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os
Tarefa 11 Professor Negri. 01. O equipamento esquematizado abaixo pode ser utilizado para separar os componentes de:
 Tarefa 11 Professor Negri 01. O equipamento esquematizado abaixo pode ser utilizado para separar os componentes de: a) um sistema homogêneo líquido/líquido. b) qualquer sistema heterogêneo. c) uma mistura
Tarefa 11 Professor Negri 01. O equipamento esquematizado abaixo pode ser utilizado para separar os componentes de: a) um sistema homogêneo líquido/líquido. b) qualquer sistema heterogêneo. c) uma mistura
Tarefa 09 à 12 Professor Willian. Com base no gráfico, assinale a alternativa que apresenta a afirmativa CORRETA.
 9º ano Química Tarefa 09 à 12 Professor Willian 01. Dois materiais sólidos, A e B, são aquecidos a uma velocidade de 10ºC.min 1. A figura a seguir representa o diagrama de aquecimento desses dois materiais.
9º ano Química Tarefa 09 à 12 Professor Willian 01. Dois materiais sólidos, A e B, são aquecidos a uma velocidade de 10ºC.min 1. A figura a seguir representa o diagrama de aquecimento desses dois materiais.
Substâncias puras e misturas; análise imediata
 Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 5 Substâncias puras e misturas; análise imediata 1. C Considerando as ilustrações, temos: I. Mistura
Segmento: Pré-vestibular Resoluções Coleção: Alfa, Beta e Gama Disciplina: Química Volume: 1 Série: 5 Substâncias puras e misturas; análise imediata 1. C Considerando as ilustrações, temos: I. Mistura
CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ
 PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A tabela
PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A tabela
02- Quais das propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida?
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Leia atentamente o texto que
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Leia atentamente o texto que
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
3. À molécula de água, H2O, pode-se adicionar o próton H +, produzindo o íon hidrônio
 1. O elemento A possui número atômico igual a 6, enquanto o elemento B possui número atômico igual a 8. A molécula que representa corretamente o composto formado por esses dois elementos é: a) AB b) BA
1. O elemento A possui número atômico igual a 6, enquanto o elemento B possui número atômico igual a 8. A molécula que representa corretamente o composto formado por esses dois elementos é: a) AB b) BA
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas:
 01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO:
 LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: Aguarde a ORDEM do fiscal para abrir este caderno de provas. Não será permitida a saída do candidato antes de esgotado o prazo mínimo de 60 minutos. Este caderno
LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: Aguarde a ORDEM do fiscal para abrir este caderno de provas. Não será permitida a saída do candidato antes de esgotado o prazo mínimo de 60 minutos. Este caderno
26/08/15 SUBSTÂNCIAS E MISTURAS. Prof. Ms. Mayanderson (Xuxu)
 SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
Separação de misturas
 Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015
 Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II
 INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais
Metas. Constituição do Mundo Material
 Materiais Metas Constituição do Mundo Material 1. Reconhecer a enorme variedade de materiais com diferentes propriedades e usos, assim como o papel da química na identificação e transformação desses materiais.
Materiais Metas Constituição do Mundo Material 1. Reconhecer a enorme variedade de materiais com diferentes propriedades e usos, assim como o papel da química na identificação e transformação desses materiais.
FICHA DE PREPARAÇÃO PARA O TESTE Nº5 FQ -7ºANO
 FICHA DE PREPARAÇÃO PARA O TESTE Nº5 FQ -7ºANO -CLASSIFICAÇÃO DOS MATERIAIS - SUBSTÃNCIAS E MISTURAS - SOLUÇÕES -TRANSFORMAÇÕES QUÍMICAS E FÍSICAS 1. A Química é a ciência que estuda as propriedades e
FICHA DE PREPARAÇÃO PARA O TESTE Nº5 FQ -7ºANO -CLASSIFICAÇÃO DOS MATERIAIS - SUBSTÃNCIAS E MISTURAS - SOLUÇÕES -TRANSFORMAÇÕES QUÍMICAS E FÍSICAS 1. A Química é a ciência que estuda as propriedades e
AULA 1 FRENTE 1. Por causa do lançamento, na atmosfera, de grande quantidade de gás carbônico, causador do efeito estufa.
 Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras A, B, C e D.
 Química Gabarito Avaliação de Sala 1B 1 os anos Décio mar/12 Nome: Nº: Turma: 1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras
Química Gabarito Avaliação de Sala 1B 1 os anos Décio mar/12 Nome: Nº: Turma: 1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras
AULA 1 FRENTE 1. Por causa do lançamento, na atmosfera, de grande quantidade de gás carbônico, causador do efeito estufa.
 Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
PROCESSOS DE SEPARAÇÃO. Prof. Ms. George Verçoza
 PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
PROMILITARES 09/08/2018 QUÍMICA. Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS
 QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
Química B Intensivo V. 1
 1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
SISTEMAS MATERIAIS. Conceitos Fundamentais, Classificação, Purificação. Reis, Oswaldo Henrique Barolli.
 SISTEMAS MATERIAIS Conceitos Fundamentais, Classificação, Purificação Reis, Oswaldo Henrique Barolli. R375s Sistemas materiais : conceitos fundamentais, classificação, purificação / Oswaldo Henrique Barolli.
SISTEMAS MATERIAIS Conceitos Fundamentais, Classificação, Purificação Reis, Oswaldo Henrique Barolli. R375s Sistemas materiais : conceitos fundamentais, classificação, purificação / Oswaldo Henrique Barolli.
RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO
 6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS
 SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS 1) Em relação às partículas atômicas, a alternativa falsa é: a) a massa do próton é igual a massa do elétron. b) a massa do elétron é menor que a massa
SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS 1) Em relação às partículas atômicas, a alternativa falsa é: a) a massa do próton é igual a massa do elétron. b) a massa do elétron é menor que a massa
Assinale a afirmativa INCORRETA.
 Atividade/Exercício: REVISÃO DE CONTEÚDO Disciplina: QUÍMICA Educador: ENDERSON BASTANI 1ª Etapa 24/ 04 /2019 Ano/Série: 1º Educando(a): Turma: Conteúdo: Sistemas - substâncias - misturas e métodos de
Atividade/Exercício: REVISÃO DE CONTEÚDO Disciplina: QUÍMICA Educador: ENDERSON BASTANI 1ª Etapa 24/ 04 /2019 Ano/Série: 1º Educando(a): Turma: Conteúdo: Sistemas - substâncias - misturas e métodos de
09) Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
PROCESSOS DE SEPARAÇÃO. Jeosafá Lima
 PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
Exercícios de Recuperação
 Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2º Período Aluno(a): Nº Turma: 1-9 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Fenômenos 1. As transformações
Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2º Período Aluno(a): Nº Turma: 1-9 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Fenômenos 1. As transformações
Gabarito Resolvido de Química (12/03/2008) A tabela abaixo apresenta dados referentes a todas as questões da prova (pressão igual a 1 atm).
 Química 1 ano Teste/Prova Rodrigo mar/08 Gabarito Resolvido de Química (12/03/2008) A tabela abaixo apresenta dados referentes a todas as questões da prova (pressão igual a 1 atm). substância densidade
Química 1 ano Teste/Prova Rodrigo mar/08 Gabarito Resolvido de Química (12/03/2008) A tabela abaixo apresenta dados referentes a todas as questões da prova (pressão igual a 1 atm). substância densidade
PROVA DE QUÍMICA 44 PROVA DE QUÍMICA
 44 QUESTÃO 46 1 Uma certa quantidade de água é colocada em um congelador, cuja temperatura é de 20 o C. Após estar formado e em equilíbrio térmico com o congelador, o gelo é transferido para outro congelador,
44 QUESTÃO 46 1 Uma certa quantidade de água é colocada em um congelador, cuja temperatura é de 20 o C. Após estar formado e em equilíbrio térmico com o congelador, o gelo é transferido para outro congelador,
Associação Catarinense das Fundações Educacionais ACAFE PARECER DOS RECURSOS
 11) Assinale a alternativa correta. A O nitrogênio principal componente do ar atmosférico é uma substância composta forma-da pelo elemento nitrogênio, 10 N. B A água pura é uma substância líquida nas condições
11) Assinale a alternativa correta. A O nitrogênio principal componente do ar atmosférico é uma substância composta forma-da pelo elemento nitrogênio, 10 N. B A água pura é uma substância líquida nas condições
DIAGRAMA DE FASES. 4) (ITA) Considere as seguintes afirmações relativas aos sistemas descritos a seguir, sob
 DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente.
 SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
1. Estados físicos da matéria Mudanças de estado Substâncias puras Misturas 4 Exercícios Densidade 6 1.
 1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
Conhecimento. Senso comum Religioso Filosófico Cientifico. Química. A matéria. propriedades. gerais funcionais específicas
 Conhecimento Senso comum Religioso Filosófico Cientifico Química A matéria propriedades gerais funcionais específicas físicas químicas organolépticas A importância da densidade Dentro da especificação
Conhecimento Senso comum Religioso Filosófico Cientifico Química A matéria propriedades gerais funcionais específicas físicas químicas organolépticas A importância da densidade Dentro da especificação
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
Química Analítica I Tratamento dos dados analíticos Soluções analíticas
 Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES. Prof a. Giselle Blois. Estudo da matéria: substâncias, misturas, processos de separação Parte 2
 QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
QUÍMICA PROF. AMANDA THOMÉ
 QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
A diversidade de materiais e a sua utilização
 Classificação dos materiais É enorme a diversidade de materiais que nos rodeia, daí a necessidade de os classificarmos. Existem, no entanto, diferentes classificações para o mesmo conjunto de materiais
Classificação dos materiais É enorme a diversidade de materiais que nos rodeia, daí a necessidade de os classificarmos. Existem, no entanto, diferentes classificações para o mesmo conjunto de materiais
1) A principal caracterís0ca de uma solução é:
 1) A principal caracterís0ca de uma solução é: a) possuir sempre um líquido com outra substância dissolvida. b) ser um sistema com mais de uma fase. c) ser homogênea ou heterogênea, dependendo das condições
1) A principal caracterís0ca de uma solução é: a) possuir sempre um líquido com outra substância dissolvida. b) ser um sistema com mais de uma fase. c) ser homogênea ou heterogênea, dependendo das condições
O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS.
 Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
LISTA DE EXERCÍCIO PARA A PROVA MENSAL
 Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Dependendo do diâmetro (Ø) das partículas que constituem o disperso, as dispersões podem ser:
 Soluções Químicas A mistura de dois ou mais materiais podem ser uma perfeita dissolução denominada mistura homogênea ou uma separação total das partes constituintes do sistema a qual chamamos mistura heterogênea.
Soluções Químicas A mistura de dois ou mais materiais podem ser uma perfeita dissolução denominada mistura homogênea ou uma separação total das partes constituintes do sistema a qual chamamos mistura heterogênea.
Lista de exercícios Aulas 01 e 02
 Lista de exercícios Aulas 01 e 02 Prof. Fernanda Dias 1) (Unicamp) Três frascos não rotulados encontram-se na prateleira de um laboratório. Um contém benzeno; outro, tetracloreto de carbono e o terceiro,
Lista de exercícios Aulas 01 e 02 Prof. Fernanda Dias 1) (Unicamp) Três frascos não rotulados encontram-se na prateleira de um laboratório. Um contém benzeno; outro, tetracloreto de carbono e o terceiro,
Resoluções das Atividades
 Resoluções das Atividades Sumário Módulo 1 Substâncias puras, misturas e sistemas Análise imediata... 1 Módulo 2 Cálculos químicos... 3 Módulo 3 úmero de oidação (o) idação e redução (redo)... 6 Módulo
Resoluções das Atividades Sumário Módulo 1 Substâncias puras, misturas e sistemas Análise imediata... 1 Módulo 2 Cálculos químicos... 3 Módulo 3 úmero de oidação (o) idação e redução (redo)... 6 Módulo
PUC Goiás MAF Coordenação de Química Lista de exercícios transformações Químicas Profa Sandra R. Longhin Goiânia. 05 de abril de 2011
 1 PUC Goiás MAF Coordenação de Química Lista de exercícios transformações Químicas Profa Sandra R. Longhin Goiânia. 05 de abril de 2011 01. A temperatura de ebulição é, entre outras, uma propriedade das
1 PUC Goiás MAF Coordenação de Química Lista de exercícios transformações Químicas Profa Sandra R. Longhin Goiânia. 05 de abril de 2011 01. A temperatura de ebulição é, entre outras, uma propriedade das
Prof.: HÚDSON SILVA. Soluções. Frente 2 Módulo 5. Coeficiente de Solubilidade.
 Prof.: HÚDSON SILVA Frente 2 Módulo 5 Soluções. Coeficiente de Solubilidade. # SOLUÇÕES É uma mistura homogênea de duas ou mais substâncias. Exemplos: Água + Açúcar, Gasolina + Álcool, CLASSIFICAÇÃO DOS
Prof.: HÚDSON SILVA Frente 2 Módulo 5 Soluções. Coeficiente de Solubilidade. # SOLUÇÕES É uma mistura homogênea de duas ou mais substâncias. Exemplos: Água + Açúcar, Gasolina + Álcool, CLASSIFICAÇÃO DOS
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma:
 TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
Conceitos importantes: a) Matéria : Tudo o que possui massa e ocupa lugar no espaço.
 SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
Separação de Misturas
 Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
Conhecimento. Senso comum Religioso Filosófico Cientifico. Química. A matéria. propriedades. gerais funcionais específicas
 Conhecimento Senso comum Religioso Filosófico Cientifico Química A matéria propriedades gerais funcionais específicas físicas químicas organolépticas Estados de agregação da matéria Estado sólido Forma
Conhecimento Senso comum Religioso Filosófico Cientifico Química A matéria propriedades gerais funcionais específicas físicas químicas organolépticas Estados de agregação da matéria Estado sólido Forma
Recuperação Paralela de Química 3ª Série 3º Bimestre
 Nome: Classe: Nº de Matrícula: Ensino Médio Série: 3ª- Bimestre: 3º- Data: 19/08/2011 Recuperação Paralela de Química 3ª Série 3º Bimestre TESTES 1. (F1) Para um químico, ao desenvolver uma análise, é
Nome: Classe: Nº de Matrícula: Ensino Médio Série: 3ª- Bimestre: 3º- Data: 19/08/2011 Recuperação Paralela de Química 3ª Série 3º Bimestre TESTES 1. (F1) Para um químico, ao desenvolver uma análise, é
Disciplina: Química Professor: Cassio Pacheco Turma: 1 Ano
 Disciplina: Química Professor: Cassio Pacheco Turma: 1 Ano Roteiro de Estudos 1- A queima da gasolina; a sublimação da naftalina; o enferrujamento do prego e o derretimento de um bloco de gelo são respectivamente,
Disciplina: Química Professor: Cassio Pacheco Turma: 1 Ano Roteiro de Estudos 1- A queima da gasolina; a sublimação da naftalina; o enferrujamento do prego e o derretimento de um bloco de gelo são respectivamente,
Átomos. Nome Símbolo Natureza Ferro Fe Fe 3 O 4 Cálcio Ca CaCO 3 Prata Ag (Argentum) Ag Oxigênio O O 2
 SOLUÇÕES ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais ou coisas que compõem o universo. A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas
SOLUÇÕES ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais ou coisas que compõem o universo. A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas
CIÊNCIAS 9º Ano Ensino Fundamental
 CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO
 Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
QUÍMICA 1ª Série Ensino Médio
 LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
Química. A matéria, suas transformações e a energia Unidade 2
 Química A matéria, suas transformações e a energia Unidade 2 Matéria (p.23) É tudo aquilo que tem massa, volume e, por isso, ocupa um lugar no espaço. Não é possível compartilhar o espaço com outra porção
Química A matéria, suas transformações e a energia Unidade 2 Matéria (p.23) É tudo aquilo que tem massa, volume e, por isso, ocupa um lugar no espaço. Não é possível compartilhar o espaço com outra porção
Processos de separação de misturas
 Disciplina: Química Prof.: Ivo Turma: IU 23/03/2017 Tema da aula: Métodos de separação de misturas Processos de separação de misturas 1) Separação de misturas heterogêneas Misturas sólido sólido Catação
Disciplina: Química Prof.: Ivo Turma: IU 23/03/2017 Tema da aula: Métodos de separação de misturas Processos de separação de misturas 1) Separação de misturas heterogêneas Misturas sólido sólido Catação
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
LISTA DE EXERCÍCIOS: TRANSFORMAÇÕES FÍSICAS E QUÍMICAS PROPRIEDADES FÍSICAS E QUÍMICAS ALGARISMOS SIGNIFICATIVOS ESTEQUIOMETRIA
 UNIVERSIDADE FEDERAL D ESTAD D RI DE JANEIR (UNIRI) INSTITUT DE BICIÊNCIAS DEP. DE CIÊNCIAS NATURAIS DISCIPLINA: QUÍMICA GERAL E INRGÂNICA 2/2015 PRFª.: CLAUDIA JRGE D NASCIMENT LISTA DE EXERCÍCIS: MATÉRIA
UNIVERSIDADE FEDERAL D ESTAD D RI DE JANEIR (UNIRI) INSTITUT DE BICIÊNCIAS DEP. DE CIÊNCIAS NATURAIS DISCIPLINA: QUÍMICA GERAL E INRGÂNICA 2/2015 PRFª.: CLAUDIA JRGE D NASCIMENT LISTA DE EXERCÍCIS: MATÉRIA
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
SUBSTÂNCIA PURA & MISTURAS
 SUBSTÂNCIA PURA & MISTURAS Química Professora: Danielle Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Sistemas Materiais Substância Pura Mistura Simples Composta Homogênea Heterogênea
SUBSTÂNCIA PURA & MISTURAS Química Professora: Danielle Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Sistemas Materiais Substância Pura Mistura Simples Composta Homogênea Heterogênea
Tabela 1: Solubilidade em água de alguns compostos presentes na água do mar a 25 ºC
 1. Enem Devido ao seu alto teor de sais, a água do mar é imprópria para o consumo humano e para a maioria dos usos da água doce. No entanto, para a indústria, a água do mar é de grande interesse, uma vez
1. Enem Devido ao seu alto teor de sais, a água do mar é imprópria para o consumo humano e para a maioria dos usos da água doce. No entanto, para a indústria, a água do mar é de grande interesse, uma vez
EXERCÍCIOS DE APLICAÇÃO
 Equilíbrio Químico EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Dada a expressão da constante de equilíbrio em termos de concentração de produtos e reagentes a equação química que pode ser representada por essa
Equilíbrio Químico EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Dada a expressão da constante de equilíbrio em termos de concentração de produtos e reagentes a equação química que pode ser representada por essa
PROVA DE QUÍMICA 2º TRIMESTRE DE 2012 PROF. MARCOS
 PROVA DE QUÍMICA 2º TRIMESTRE DE 2012 PROF. MARCOS NOME Nº 9º ANO A prova deve ser respondida a caneta azul ou preta. A compreensão do enunciado faz parte da questão, não faça perguntas ao examinador.
PROVA DE QUÍMICA 2º TRIMESTRE DE 2012 PROF. MARCOS NOME Nº 9º ANO A prova deve ser respondida a caneta azul ou preta. A compreensão do enunciado faz parte da questão, não faça perguntas ao examinador.
PLANO DE ESTUDO TRIMESTRE: 1º
 C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 02 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 14/04/2018 DISCIPLINA : Química ANO/SÉRIE: 1º ANO
C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 02 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 14/04/2018 DISCIPLINA : Química ANO/SÉRIE: 1º ANO
esféricas maciças e indivisíveis.
 a) A-I, B-II, C-III b) A-II, B-III, C-I c) A-III, B-I, C-II d) A-III, B-II, C-I e) A-II, B-I, C-III LISTA DE EXERCÍCIOS DE QUÍMICA 1º Ano do Ensino Médio Professor: Anderson Paschôa É preciso estudar todos
a) A-I, B-II, C-III b) A-II, B-III, C-I c) A-III, B-I, C-II d) A-III, B-II, C-I e) A-II, B-I, C-III LISTA DE EXERCÍCIOS DE QUÍMICA 1º Ano do Ensino Médio Professor: Anderson Paschôa É preciso estudar todos
