1 O Átomo de Hidrogênio
|
|
|
- Alexandre Camarinho Bennert
- 5 Há anos
- Visualizações:
Transcrição
1 O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica quântica, pois estabelece órbitas bem denidas para o elétron, que certamente violam o princípio de incerteza. A descrição correta deve ser obtida resolvendo-se a equação de Schoedinger para um elétron sob a ação do potencial coulombiano V (r) = e 4πɛ 0. A solução completa deve ainda incluir o spin, uma propriedade r relativística do elétron, que classicamente é equivalente a uma rotação em torno de um eixo passando por seu centro. O spin é responsável, por exemplo, pela estrutura na dos espectos atômicos, mas não será incluido nesta discussão. O tratamento que vamos descrever, assim como o modelo de Bohr, pode ser aplicado a qualquer átomo Z, com somente um elétron ligado (íon). Portanto vamos utilizar aqui a energia potencial de um elétron em um núcleo com Z prótons: V (r) = Ze2 4πɛ 0 r. Também, vamos considerar que a massa do núcleo é muito maior que a do elétron, de modo que o CM do átomo coincide com o centro de seu núcleo. Isso é equivalente a usar, nas equações, a massa reduzida do elétron, µ = M m, onde M é a massa do núcleo e m a do elétron. M+m Vimos no capítulo anterior, a equação de Schroedinger em 3 dimensões, para a partícula em uma caixa cúbica: 2 2m ( 2 x y z )Ψ(x, y, z, t) + V Ψ(x, y, z, t) = i Ψ(x, y, z, t) 2 (.) t as derivadas parciais espaciais podem ser escritas de forma compacta, denindo-se o operador Laplaciano: 2 = : x 2 y 2 z 2 2 2m 2 Ψ + V Ψ = i t Ψ Para o caso do átomo de hidrogênio, e para todo problema envolvendo um potencial central, é muito conveniente resolver o problema em um sistema de coordenadas esféricas: x = r sin θ cos ϕ y = r sin θ sin ϕ z = r cos θ pode-se vericar que o Laplaciano, em coordenadas esfericas pode ser escrito como: 2 = r 2 r (r2 r ) + r 2 sin θ θ (sin θ θ ) + r 2 sin 2 θ 2 ϕ 2
2 Figura.: Sistema de coordenas esféricas e portanto, a equação de Schroedinger para o átomo de hidrogênio, em coordenas esféricas é escrita como: 2µ r 2 r (r2 r ² )Ψ ² 2µ [ r 2 sin θ θ (sin θ θ ) + r 2 sin 2 θ 2 Ze² ]Ψ ϕ2 4πɛ 0 r Ψ = i t Ψ A parte angular dessa equação pode ser expressa em termos do operador ˆL 2, o módulo quadrado do momento angular. Classicamente, o momento angular de uma partícula é expresso como L = r p. Em coordenas cartesianas, os componentes do operador para o momento angular são então dados por: ˆL x = (yˆp z z ˆp y ) = i (y z z y ) ˆL y = (z ˆp x xˆp z ) = i (z x x z ) ˆL z = (xˆp y yˆp x ) = i (x y y x ) escrevendo-se esses componentes em termos das coordenas esféricas, temos: ˆL x = i (sin ϕ θ ˆL y = i ( cos ϕ θ ˆL z = i ϕ + cot θ cos ϕ ϕ ) + cot θ sin ϕ ϕ ) e então, ˆL 2 = ˆL.ˆL = ˆL 2 x + ˆL 2 y + ˆL 2 z, em coordenadas esfericas é escrito como: ˆL 2 = 2 [ sin θ θ (sin θ θ ) + sin 2 θ 2 ϕ 2 ] 2
3 . Separação de variáveis e a equação de Schroedinger para o átomo de hidrogênio, em termos do operador ˆL 2 é dada por: Ze2 2µ r 2 r (r2 )Ψ r 4πɛ 0 r Ψ + 2µr ˆL 2 Ψ = i 2 t Ψ ². Separação de variáveis A solução dessa equação pode ser encontrada empregando-se sucessivamente a técnica de separação de variáveis. Como o potencial não depende explicitamente do tempo, a parte temporal da função de onda será e iet/ e podemos então escrever a equação de Schroedinger independente do tempo: 2µ r 2 r (r2 r ) Ze2 ]Ψ(r, θ, ϕ) + 4πɛ 0 r 2µr ˆL 2 Ψ(r, θ, ϕ) = EΨ(r, θ, ϕ) 2 [ ² no lado esquerdo da equação o termo entre colchetes depende somente de r e o operador ˆL 2 depende somente das variáveis angulares, pode-se facilmente vericar que a solução para Ψ pode ser fatorada em dois termos: que substituido na equação resulta em: Ψ(r, θ, ϕ) = R(r).Y (θ, ϕ) Y (θ, ϕ)[ ² 2µ r 2 r (r2 r ) Ze2 R(r) ]R(r) + 4πɛ 0 r 2µr ˆL 2 Y (θ, ϕ) = ER(r)Y (θ, ϕ) 2 multiplicando-se a equação por 2µr 2 / 2 RY e deixando somente o termo em ˆL 2 no segundo membro, temos: R (r2 R r r ) + 2µr2 Ze2 (E + 2 4πɛ 0 r ) = 2 Y ˆL 2 Y portanto, como o lado esquerdo só depende de r e o direito de θ e ϕ, devem ser iguais a uma constante. Por conveniência, como será discutido posteriormente, vamos denominar a constante de separação de variáveis na forma L 2. A equação para a parte radial da função de onda será portanto r (r2 R(r) r ) + 2µr2 2 Ze2 (E + 4πɛ 0 r )R(r) = L2 R(r) e a da parte angular, substituindo a expressão para o operador ˆL 2 : sin θ θ Y (θ, ϕ) (sin θ ) 2 Y (θ, ϕ) θ sin 2 = L 2 Y (θ, ϕ) θ ϕ 2 3
4 .2 Solução da parte angular da equação A solução para a parte angular da equação pode ainda ser separada no produto Y (θ, ϕ) = Θ(θ)Φ(ϕ) Φ d dθ(θ) (sin θ sin θ dθ dθ ) Θ d 2 Φ(ϕ) sin 2 θ dϕ 2 multiplicando a equação por sin 2 θ/θ(θ)φ(ϕ), temos: sin θ Θ d dθ a solução para Φ(ϕ) é imediata: = L 2 Θ(θ)Φ(ϕ) dθ(θ) (sin θ dθ ) + L2 sin 2 θ = d 2 Φ(ϕ) = m 2 Φ dϕ 2 d 2 Φ(ϕ) dϕ 2 = m 2 Φ = Φ(ϕ) = Ce imϕ impondo-se a condição de que a função deve ser periódica, Φ(ϕ + 2π) = Φ(ϕ), resulta que m deve ser um número inteiro (0, ±, ±2,...). O termo em θ pode ser escrito como: Expandindo-se as derivadas, temos sin θ d dθ(θ) (sin θ dθ dθ ) + [L2 sin θ m 2 ]Θ = 0 sin 2 θ d2 Θ dθ 2 dθ + sin θ cos θ dθ + [L2 sin 2 θ m 2 ]Θ = 0 A solução para o termo em θ é mais complexa. Vamos reescrever essa equação, em termos da variável x = cos θ. Chamando Θ(θ) = P (cos θ) = P (x) e usando d = sin θ d dθ e d2 dθ 2 = cos θ d dx + sin2 θ d2 dx 2, temos: sin 2 θ[sin 2 θ d2 P (x) dx 2 cos θ dp (x) dx ou, dividindo a equação por sin 2 θ: sin 2 θ d2 P (x) dx 2 dp (x) ] + sin θ cos θ[ sin θ dx ] + [L2 sin 2 θ m 2 ]P (x) = 0 dp (x) dp (x) cos θ cos θ dx dx + [L2 m2 sin 2 ]P (x) = 0 θ agora, substituindo cos θ = x; sin 2 θ = x 2, temos nalmente ( x 2 ) d2 P (x) dx 2 dp (x) + 2x dx + [L2 m2 ]P (x) = 0 x2 Essa é a chamada equação associada de Legendre. Só existem soluções bem comportadas para L 2 = l(l + ), onde l é um inteiro tal que l m l. Essas soluções são os chamados polinômios associados de Legendre: dx, 4
5 .3 Solução da parte radial Pm(x) l = ( )m ( x 2 m/2 dl+m ) 2 l l! dx i+m (x2 ) l A solução completa e normalizada da parte angular é normalmente reagrupada na forma abaixo, conhecida como harmônicos esféricos: Y lm (θ, ϕ) = ( ) m (2l + )(l m )! P l 4π(l + m )! m(cos θ)e imϕ.3 Solução da parte radial Finalmente temos a equação para a parte radial da equação: ou d dr (r2 dr(r) dr ) + 2µr2 2 Ze2 (E + )R(r) = l(l + )R(r) 4πɛ 0 r d dr (r2 dr(r) dr ) + ( 2µr2 E + 2µr2 Z e 2 l(l + ))R(r) = 0 2 4πɛ 0 r denindo f(r) = rr(r), o primeiro termo da equação ca: d dr(r) (r2 ) = d d dr dr dr (r2 dr )r f(r) = d dr [r2 ( r 2 df f(r) + r dr )] = d df ( f(r) + r dr dr ) = r df 2 dr 2 a equação radial, em termos de f(r) então é escrita como: d 2 f(r) + ( 2µ dr 2 E + 2µZe2 l(l + ) )f(r) = 0 2 4πɛ 0 r r 2 denindo agora ( α 2 )2 = 2µ E (lembre-se de que como estamos tratanto de estados 2 ligados, a energia total E é negativa) e denindo a variável x = rα, e como d2 = α 2 d2 a dr 2 dx 2 equação ca ou α 2 d2 f(x) dx 2 + ( 2µZe2 α 4πɛ 0 2 x α2 l(l + ) α2 )f(x) = d 2 f(x) + ( 2µZe2 dx 2 4πɛ 0 2 αx l(l + ) )f(x) = essa equação é semelhante à conhecida como equação associada de Laguerre e suas soluções, que existem somente para determinados valores de α tais que 2µZe2 = n = 4πɛ 0 2 α j + l +, j denido à partir dos polinômios associados de Laguerre: 5
6 f j,l (x) = e x/2 x l+ G j,l (x) Pode-se vericar que ( α 2 )2 = E n = 2 2µa 2 0 n2 onde a 0 = 2 2m ee 2 é o raio de Bohr. Essas soluções podem também serem expressas em termos da função original R(r) como: R nl (r) = e Zr/na 0 ( Zr a 0 ) l G nl ( Zr a 0 ) onde os G nl ( Zr a 0 ) são os chamados polinômios associados de Laguerre e o parâmetro n se relaciona com o l e m como: n =, 2, 3,... l = 0,, 2,..., n m = l, l +,..., 0,..., l, l.3. Funções de onda e distribuições de probabilidades Portanto as funções de onda para o átomo de hidrogênio são Ψ nlm (r, θ, ϕ, t) = R nl (r)y lm (θ, ϕ)e iet/h Essas funções, excluido-se o termo em t. para valores pequenos de n, l, m são dadas por: Ψ 00 = π ( Z a 0 ) 3/2 e Zr/a 0 Ψ 200 = Ψ 20 = Ψ 2 = Ψ 2 = 4 2π ( Z ) 3/2 (2 r a 0 2a )e r/2a 0 4 2π ( Z ) 3/2 ( r )e r/2a 0 cos θ a 0 a 0 8 2π ( Z ) 3/2 ( r )e r/2a 0 sin θe iϕ a 0 a 0 8 2π ( Z ) 3/2 ( r )e r/2a 0 sin θe iϕ a 0 a 0 Por razões históricas, usa-se a nomenclatura da espectroscopia (desenvolvida no século XIX), para classicar os estados correspondentes a essas funções: s - sharp, p - principal, d - difuse, e continuando-se com as letras do alfabeto (f,g,h,...). s corresponde a l = 0, p a l = e assim por diante. 6
7 .3 Solução da parte radial n,l,m notação,0,0 s 2,0,0 2s 2,,(-,0,) 2p 3,0,0 3s 3,,(-,0,) 3p 3,2,(-2,...,2) 3d As distribuições de probabilidade de se encontrar o elétron entre r e r + dr, P nl (r)dr, são dadas por: P nl (r)dr = R nl(r)r nl (r)r 2 dr já que os harmônicos esféricos são normalizados ( Y lm Y lm sin θdθdϕ = ). P nl (r) pode ser visto na gura.2, para os primeiros valores de n e l. Figura.2: Distribuições de probabilidade P nl (r) e as correspondentes funções de onda radiais R nl (r). 7
8 Figura.3: Distribuições de probabilidade para os vários estados com n=,2,3,4. As distribuições de probabilidades em função de r, θ, ϕ, dadas por Ψ(r, θ, ϕ) 2 dv, para alguns valores de n, l, m são vistas na gura O momento angular no átomo de hidrogênio As funções de onda do átomo de hidrogênio, são obviamente autofuncões do operador hamiltoniano: ĤΨ nlm = ( ˆT + ˆV )Ψ nlm = E n Ψ nlm mas são também autofunções do operador ˆL 2 o módulo quadrado do momento angular: ˆL 2 Ψ nlm = 2 l(l + )Ψ nlm bem como do componente L z do momento angular, cujo operador é ˆL z = i ϕ : i ϕ Ψ nlm = mψ nlm Como a energia de um estado só depende de n, estados com mesmo n e l, m diferentes têm mesma energia. Diz-se que são estados degenerados. E lembrando que as transições entre estados devem obedecer a regra de seleção l = ± (conservação do momento angular, ver oscilador harmônico), o diagrama de níveis de energia e as possíveis transições entre eles são vistas na gura.4. 8
9 .3 Solução da parte radial Figura.4: Diagrama de níveis e transições no átomo de hidrog enio. Um estado atômico tem portanto E, L 2 e L z bem denidos (constantes), representados pelos números quânticos n, l e m. O momento angular total L não pode ser constante. Como L = r p, se L fosse bem denido, então r e p também o seriam, violando o princípio de incerteza. Como L = l(l + ) e L z = m são constantes, temos o correspondente à visão clássica do vetor L precessionando em torno do eixo z, como visto na gura.5. Essa precessão mostra que, para m 0, a distribuição de probabilidade da carga eletrônica está girando em torno de z, produzindo assim um campo magnético, na analogia clássica. Isso pode ser associado às propriedades mágnéticas dos materiais. Por isso, o número atômico m é também chamado número quântico magnético. Na mecânica clássica, no problema equivalente (por exemplo, planetas em torno do sol), o momento angular é Figura.5: O vetor L precessiona em torno do eixo azimutal z. 9
10 Figura.6: Direções de L para diferentes valores de L z. conservado e está sempre na direção de z, perpendicular ao plano orbital. Note no limite de grandes números quânticos, o valor máximo de m faz com que a direção de L se aproxime cada vez mais do eixo z, fazendo, nesse limite, L = L zˆk e portanto constante. 0
Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento angular bem definido
 ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
Problemas de Duas Partículas
 Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
FNC376N: Lista de março de ψ r ψ = Eψ. sin θ Y )
 FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
Equação de Schrödinger em 3D
 Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Estrutura Atômica I. Química Quântica Prof a. Dr a. Carla Dalmolin. Átomo de Hidrogênio Átomos Hidrogenóides
 Estrutura Atômica I Química Quântica Prof a. Dr a. Carla Dalmolin Átomo de Hidrogênio Átomos Hidrogenóides Aplicações da Mecânica Quântica Soluções da Equação de Schrödinger independente do tempo Partícula
Estrutura Atômica I Química Quântica Prof a. Dr a. Carla Dalmolin Átomo de Hidrogênio Átomos Hidrogenóides Aplicações da Mecânica Quântica Soluções da Equação de Schrödinger independente do tempo Partícula
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
Fundamentos de Química Quântica
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
7. A teoria quântica do átomo de Hidrogênio
 7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
Modelos Atômicos e Princípios Quânticos Parte II
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
Breve Revisão de Mecânica
 Capítulo 1 Breve Revisão de Mecânica Quântica Seguimos as secções 5.1 a 5.3 do Griffiths [1] e a secção 1.1 do meu texto de Introdução à Teoria de Campo []. É assumido como pré-requisito o conhecimento
Capítulo 1 Breve Revisão de Mecânica Quântica Seguimos as secções 5.1 a 5.3 do Griffiths [1] e a secção 1.1 do meu texto de Introdução à Teoria de Campo []. É assumido como pré-requisito o conhecimento
O spin do elétron. Vimos, na aula 2, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com 2 valores, com propriedades de momento angular.
 O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
+ E p. ψ(x) = E. ψ(x)
 Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
Estrutura Atômica - Prof. J. D. Ayala - 1 -
 Estrutura Atômica - Prof. J. D. Ayala - 1-1.1 - MODELO ATÔMICO PLANETÁRIO Supondo que o elétron tem uma massa m, desprezível em relação ao núcleo, cuja carga é Ze. Neste caso o núcleo permanecerá em repouso
Estrutura Atômica - Prof. J. D. Ayala - 1-1.1 - MODELO ATÔMICO PLANETÁRIO Supondo que o elétron tem uma massa m, desprezível em relação ao núcleo, cuja carga é Ze. Neste caso o núcleo permanecerá em repouso
SEGUNDA PROVA - F789. angular orbital. O estado da partícula, Ψ, tem componentes Ψ ± (r) =
 SEGUNDA PROVA - F789 NOME: RA:. Considere uma partícula de spin. Seja S seu spin e L seu momento angular orbital. O estado da partícula, Ψ, tem componentes Ψ ± (r) = r, ± Ψ na base r, ± de autoestados
SEGUNDA PROVA - F789 NOME: RA:. Considere uma partícula de spin. Seja S seu spin e L seu momento angular orbital. O estado da partícula, Ψ, tem componentes Ψ ± (r) = r, ± Ψ na base r, ± de autoestados
Momento Angular. 8.1 Álgebra do Momento Angular
 Capítulo 8 Momento Angular Neste capítulo vamos estudar os autovalores e autovetores do momento angular. Este problema também pode ser analisado com o uso do método de operadores, o que faremos na primeira
Capítulo 8 Momento Angular Neste capítulo vamos estudar os autovalores e autovetores do momento angular. Este problema também pode ser analisado com o uso do método de operadores, o que faremos na primeira
Lista Considere um oscilador harmonico tridimencional com o potencial, resolve a Equação de Schrödinger independente no tempo
 Lista 8. Considere um oscilador harmonico tridimencional com o potencial, V = m 2 ( ω 2 x x 2 + ω 2 yy 2 + ω 2 zz 2), onde ω x, ω y e ω z representam as frequências deste oscilador (clássico) nas direções,
Lista 8. Considere um oscilador harmonico tridimencional com o potencial, V = m 2 ( ω 2 x x 2 + ω 2 yy 2 + ω 2 zz 2), onde ω x, ω y e ω z representam as frequências deste oscilador (clássico) nas direções,
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas Equação de Schrödinger em 3D: 2 = 1 r 2 # % r $ r2 r & (+ ' 1 r 2 senθ # θ senθ & % (+ $ θ ' 1 r 2 sen 2 θ 2 φ 2 Podemos, então, escrever a eq. de Schrödinger
A eq. de Schrödinger em coordenadas esféricas Equação de Schrödinger em 3D: 2 = 1 r 2 # % r $ r2 r & (+ ' 1 r 2 senθ # θ senθ & % (+ $ θ ' 1 r 2 sen 2 θ 2 φ 2 Podemos, então, escrever a eq. de Schrödinger
Física IV Escola Politécnica PS 14 de dezembro de 2017
 Física IV - 432324 Escola Politécnica - 217 PS 14 de dezembro de 217 Questão 1 Uma espaçonave de comprimento próprio L move-se com velocidade,5 c em relação à Terra. Um meteorito, que também se move com
Física IV - 432324 Escola Politécnica - 217 PS 14 de dezembro de 217 Questão 1 Uma espaçonave de comprimento próprio L move-se com velocidade,5 c em relação à Terra. Um meteorito, que também se move com
Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui
 FÍSICA MODERNA Aula 6a: Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui Tema 5: Física dos átomos e moléculas 5.1. Átomo de hidrogénio;
FÍSICA MODERNA Aula 6a: Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui Tema 5: Física dos átomos e moléculas 5.1. Átomo de hidrogénio;
Não serão aceitas respostas sem justificativa:
 Primeira Prova de Conceitos de Mecânica Quântica -(,5) Uma partícula de massa m encontra-se no estado ψ(x,t)= A exp[ω(mx /ħ+it)], onde A e a são constantes reais e positivas. a- Normalize ψ(x,t); b- Calcule
Primeira Prova de Conceitos de Mecânica Quântica -(,5) Uma partícula de massa m encontra-se no estado ψ(x,t)= A exp[ω(mx /ħ+it)], onde A e a são constantes reais e positivas. a- Normalize ψ(x,t); b- Calcule
Física Quântica. Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio. Pieter Westera
 Física Quântica Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html A Equação
Física Quântica Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html A Equação
O ÁTOMO DE HIDROGÊNIO
 O ÁTOMO DE HIDROGÊNIO Alessandra de Souza Barbosa 04 de dezembro de 013 O átomo de hidrogênio Alessandra de Souza Barbosa CF37 - Mecânica Quântica I /36 Sistema de duas particulas um elétron e um próton;
O ÁTOMO DE HIDROGÊNIO Alessandra de Souza Barbosa 04 de dezembro de 013 O átomo de hidrogênio Alessandra de Souza Barbosa CF37 - Mecânica Quântica I /36 Sistema de duas particulas um elétron e um próton;
Rotor quântico. Quanticamente o rotor é descrito por uma função de onda, tal que: l A função de onda do estado estacionário é dada por:
 Rotor quântico Vamos tratar o caso da rotação de um corpo rígido, que corresponde a 2 massas pontuais, ligadas por uma barra rígida e sem massa. Consideremos rotação livre em torno de um eixo perpendicular
Rotor quântico Vamos tratar o caso da rotação de um corpo rígido, que corresponde a 2 massas pontuais, ligadas por uma barra rígida e sem massa. Consideremos rotação livre em torno de um eixo perpendicular
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS Edição de agosto de 2008 CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS ÍNDICE 8.1- Introdução 8.2- Problema da Força Central
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS Edição de agosto de 2008 CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS ÍNDICE 8.1- Introdução 8.2- Problema da Força Central
O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana
 Universidade Federal do Paraná Setor de Ciências Exatas Departamento de Física O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana Introdução O Hélio é, depois do Hidrogênio, o átomo mais simples
Universidade Federal do Paraná Setor de Ciências Exatas Departamento de Física O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana Introdução O Hélio é, depois do Hidrogênio, o átomo mais simples
2. No instante t = 0, o estado físico de uma partícula livre em uma dimensão é descrito pela seguinte função de onda:
 Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 03/08/2011 Nome do Candidato: Nível: Mestrado Doutorado 1. No cálculo da
Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 03/08/2011 Nome do Candidato: Nível: Mestrado Doutorado 1. No cálculo da
O Átomo de hidrogénio
 O Átomo de hidrogénio O conceito de átomo como sendo a mais pequena porção indivisível de matéria foi introduzido no ano 450 antes de Cristo mas, só em 808, Dalton propôs um modelo atómico em que os átomos
O Átomo de hidrogénio O conceito de átomo como sendo a mais pequena porção indivisível de matéria foi introduzido no ano 450 antes de Cristo mas, só em 808, Dalton propôs um modelo atómico em que os átomos
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
Aula 12. (quase) Tudo sobre os átomos. Física Geral F-428
 Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
O Método de Hartree-Fock
 O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
1) A ESTRUTURA DOS ÁTOMOS
 A ESTRUTURA DOS ÁTOMOS.. Estrutura Atômica A matéria seja no estado líquido sólido ou gasoso é constituída por átomos. Os átomos são constituídos por partículas elementares: os prótons os nêutrons e os
A ESTRUTURA DOS ÁTOMOS.. Estrutura Atômica A matéria seja no estado líquido sólido ou gasoso é constituída por átomos. Os átomos são constituídos por partículas elementares: os prótons os nêutrons e os
Mecânica Quântica. Química Quântica Prof a. Dr a. Carla Dalmolin. A Equação de Schrödinger Postulados da Mecânica Quântica
 Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin A Equação de Schrödinger Postulados da Mecânica Quântica Mecânica Clássica O movimento de uma partícula é governado pela Segunda Lei de Newton:
Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin A Equação de Schrödinger Postulados da Mecânica Quântica Mecânica Clássica O movimento de uma partícula é governado pela Segunda Lei de Newton:
Raios atômicos Física Moderna 2 Aula 6
 Raios atômicos 1 2 8 8 18 18 32 2 Energias de ionização 3 Espectros de R-X A organização da tabela periódica reflete a distribuição dos e - nas camadas mais externas dos átomos. No entanto, é importante
Raios atômicos 1 2 8 8 18 18 32 2 Energias de ionização 3 Espectros de R-X A organização da tabela periódica reflete a distribuição dos e - nas camadas mais externas dos átomos. No entanto, é importante
Física IV Escola Politécnica GABARITO DA P3 25 de novembro de 2014
 Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Física IV - FAP2204 Escola Politécnica GABARITO DA P3 8 de dezembro de 2009
 P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
Universidade de São Paulo em São Carlos Mecânica Quântica Aplicada Prova 2
 Universidade de São Paulo em São Carlos.7.04 Mecânica Quântica Aplicada Prova Nome: Questão : Método variacional (.5 pontos) Considere o oscilador harmônico descrito pelo hamiltoniano H = + m dx mω x.
Universidade de São Paulo em São Carlos.7.04 Mecânica Quântica Aplicada Prova Nome: Questão : Método variacional (.5 pontos) Considere o oscilador harmônico descrito pelo hamiltoniano H = + m dx mω x.
A Estrutura Eletrônica dos Átomos. Prof. Fernando R. Xavier
 A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
Universidade Federal do Espírito Santo Centro de Ciências Exatas Programa de Pós-Graduação em Física
 Universidade Federal do Espírito Santo Centro de Ciências Exatas Programa de Pós-Graduação em Física Av. Fernando Ferrari, 514, 29075-910. Vitória, ES - Brasil. E-mail: ppgfis.ufes@gmail.com. Telefone:
Universidade Federal do Espírito Santo Centro de Ciências Exatas Programa de Pós-Graduação em Física Av. Fernando Ferrari, 514, 29075-910. Vitória, ES - Brasil. E-mail: ppgfis.ufes@gmail.com. Telefone:
A Experiência de Stern-Gerlach e o Spin do Elétron
 UFPR 28 de Abril de 2014 Figura: Placa Comemorativa. ela foi realizada em 1922; ela investiga os possíveis valores do momento de dipolo magnético, µ, de um átomo de prata; ela explora a dinâmica do dipolo
UFPR 28 de Abril de 2014 Figura: Placa Comemorativa. ela foi realizada em 1922; ela investiga os possíveis valores do momento de dipolo magnético, µ, de um átomo de prata; ela explora a dinâmica do dipolo
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 Resultados da Teoria de Hartree As autofunções obtidas pela teoria de Hartree
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 Resultados da Teoria de Hartree As autofunções obtidas pela teoria de Hartree
Átomo de Hidrogênio 1
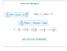 Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
h (1 cos θ) onde, m e é a massa do elétron, θ é o ângulo pelo qual a direção do fóton muda λ 1 é o comprimento de onda do fóton antes do espalhamento,
 Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 09/06/2014 Nome do Candidato: Nível: Mestrado Doutorado 1. A função de
Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 09/06/2014 Nome do Candidato: Nível: Mestrado Doutorado 1. A função de
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/2 e de Dois Níveis
 Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Universidade de São Paulo em São Carlos Mecânica Quântica Aplicada Prova 1
 Universidade de São Paulo em São Carlos 9514 Mecânica Quântica Aplicada Prova 1 Nome: Questão 1: Sistema de dois níveis (3 pontos) Considere um sistema de dois estados 1 e ortonormais H do sistema seja
Universidade de São Paulo em São Carlos 9514 Mecânica Quântica Aplicada Prova 1 Nome: Questão 1: Sistema de dois níveis (3 pontos) Considere um sistema de dois estados 1 e ortonormais H do sistema seja
Escola Politécnica FAP GABARITO DA P3 25 de novembro de 2008
 P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
Átomos multi-eletrônicos. Indistinguibilidade
 Átomos multi-eletrônicos Indistinguibilidade Princípio de exclusão, de Pauli 1. Em um átomo multi-eletrônico nunca pode haver mais de 1 e- ocupando o mesmo estado quântico.. Um sistema constituído de vários
Átomos multi-eletrônicos Indistinguibilidade Princípio de exclusão, de Pauli 1. Em um átomo multi-eletrônico nunca pode haver mais de 1 e- ocupando o mesmo estado quântico.. Um sistema constituído de vários
h mc 2 =hν mc 2 =hc/ λ
 Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Física IV Escola Politécnica GABARITO DA PS 3 de dezembro de 2013
 Física IV - 4320402 Escola Politécnica - 2013 GABARITO DA PS 3 de dezembro de 2013 Questão 1 Uma onda eletromagnética plana harmônica, de comprimento de onda λ, propaga-se no vácuo no sentido positivo
Física IV - 4320402 Escola Politécnica - 2013 GABARITO DA PS 3 de dezembro de 2013 Questão 1 Uma onda eletromagnética plana harmônica, de comprimento de onda λ, propaga-se no vácuo no sentido positivo
Universidade de São Paulo Instituto de Física. Física Moderna II. Profa. Márcia de Almeida Rizzutto 2 o Semestre de Física Moderna 2 Aula 5
 Universidade de São Paulo Instituto de Física Física Moderna II Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 19: experiência de Stern&Gerlach Proposta: Medir os valores possíveis do momento de
Universidade de São Paulo Instituto de Física Física Moderna II Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 19: experiência de Stern&Gerlach Proposta: Medir os valores possíveis do momento de
Átomo de Hélio. Tiago Santiago. 2 de novembro de Resumo
 Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Exame de Ingresso na Pós-graduação
 Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 09 de Junho de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3 (três)
Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 09 de Junho de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3 (três)
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
Física IV Escola Politécnica P3 7 de dezembro de 2017
 Física IV - 4323204 Escola Politécnica - 2017 P3 7 de dezembro de 2017 Questão 1 Uma partícula de massa m que se move em uma dimensão possui energia potencial que varia com a posição como mostra a figura.
Física IV - 4323204 Escola Politécnica - 2017 P3 7 de dezembro de 2017 Questão 1 Uma partícula de massa m que se move em uma dimensão possui energia potencial que varia com a posição como mostra a figura.
Física IV - FAP2204 Escola Politécnica GABARITO DA PS 15 de dezembro de 2009
 PS Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA PS 15 de dezembro de 2009 Questão 1 Considere os campos elétrico E = (0,E y,0) e magnético B = (0,0,B z ) onde E y (x,t) = A e a(x ct) e B z
PS Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA PS 15 de dezembro de 2009 Questão 1 Considere os campos elétrico E = (0,E y,0) e magnético B = (0,0,B z ) onde E y (x,t) = A e a(x ct) e B z
Métodos de Física Teórica II Prof. Henrique Boschi IF - UFRJ. 1º. semestre de 2010 Aula 5 Ref. Butkov, caps. 8 e 9, seções 8.8 e 9.
 Métodos de Física Teórica II Prof. Henrique Boschi IF - UFRJ 1º. semestre de 2010 Aula 5 Ref. Butkov, caps. 8 e 9, seções 8.8 e 9.1 Vibrações de uma membrana Como mencionado na aula passada, pode-se deduzir
Métodos de Física Teórica II Prof. Henrique Boschi IF - UFRJ 1º. semestre de 2010 Aula 5 Ref. Butkov, caps. 8 e 9, seções 8.8 e 9.1 Vibrações de uma membrana Como mencionado na aula passada, pode-se deduzir
EUF. Exame Unificado. Para o segundo semestre de de abril de 2017 FORMULÁRIO
 EUF Exame Unificado das Pós-graduações em Física Para o segundo semestre de 07 04-05 de abril de 07 FORMULÁRIO Não escreva nada neste formulário. Devolva-o ao final da prova. Constantes físicas Velocidade
EUF Exame Unificado das Pós-graduações em Física Para o segundo semestre de 07 04-05 de abril de 07 FORMULÁRIO Não escreva nada neste formulário. Devolva-o ao final da prova. Constantes físicas Velocidade
Eq. de Dirac com campo magnético
 Eq. de Dirac com campo magnético Rafael Cavagnoli GAME: Grupo de Médias e Altas Energias Eletromagnetismo clássico Eq. de Schrödinger Partícula carregada em campo mag. Eq. de Dirac Partícula carregada
Eq. de Dirac com campo magnético Rafael Cavagnoli GAME: Grupo de Médias e Altas Energias Eletromagnetismo clássico Eq. de Schrödinger Partícula carregada em campo mag. Eq. de Dirac Partícula carregada
UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL
 UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL LOB1021 - FÍSICA IV Prof. Dr. Durval Rodrigues Junior Departamento de Engenharia de Materiais (DEMAR) Escola de Engenharia de Lorena (EEL) Universidade
UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL LOB1021 - FÍSICA IV Prof. Dr. Durval Rodrigues Junior Departamento de Engenharia de Materiais (DEMAR) Escola de Engenharia de Lorena (EEL) Universidade
1ª AULA ONDAS E PARTÍCULAS
 1ª AULA ONDAS E PARTÍCULAS 1) Caracterização de um corpúsculo em movimento ) Caracterização de uma onda progressiva 3) Relação de De Broglie 4) Princípio de Incerteza 1 Feixe de electrões Onde há? Tubos
1ª AULA ONDAS E PARTÍCULAS 1) Caracterização de um corpúsculo em movimento ) Caracterização de uma onda progressiva 3) Relação de De Broglie 4) Princípio de Incerteza 1 Feixe de electrões Onde há? Tubos
Mecânica Quântica. Spin 1/2 e a formulação da M. Q. Parte II. A C Tort 1. Instituto Física Universidade Federal do Rio de Janeiro
 Mecânica Quântica Spin 1/ e a formulação da M. Q. Parte II A C Tort 1 1 Departmento de Física Teórica Instituto Física Universidade Federal do Rio de Janeiro 10 de Maio de 01 Mais dois postulados, agora
Mecânica Quântica Spin 1/ e a formulação da M. Q. Parte II A C Tort 1 1 Departmento de Física Teórica Instituto Física Universidade Federal do Rio de Janeiro 10 de Maio de 01 Mais dois postulados, agora
A Equação de Onda de Schröedinger. O Princípio da Incerteza de Heisenberg. λ =
 O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
Desenvolvimento. Em coordenadas esféricas:
 Desenvolvimento Para que possamos resolver a equação da onda em coordenadas esféricas, antes é necessária a dedução do operador Laplaciano nessas coordenadas, portanto temos: Em coordenadas esféricas:
Desenvolvimento Para que possamos resolver a equação da onda em coordenadas esféricas, antes é necessária a dedução do operador Laplaciano nessas coordenadas, portanto temos: Em coordenadas esféricas:
Fundamentos da Mecânica Quântica
 Fundamentos da Mecânica Quântica Vitor Oguri Departamento de Física Nuclear e Altas Energias (DFNAE) Instituto de Física Armando Dias Tavares (IFADT) Universidade do Estado do Rio de Janeiro (UERJ) Rio
Fundamentos da Mecânica Quântica Vitor Oguri Departamento de Física Nuclear e Altas Energias (DFNAE) Instituto de Física Armando Dias Tavares (IFADT) Universidade do Estado do Rio de Janeiro (UERJ) Rio
Aplicação do Método Variacional na Mecânica Quântica:
 Aplicação do Método Variacional na Mecânica Quântica: Átomo de Hélio Milena Menezes Carvalho 1 1 Instituto de Física de São Carlos, Universidade de São Paulo E-mail: glowingsea@gmail.com 1. Introdução
Aplicação do Método Variacional na Mecânica Quântica: Átomo de Hélio Milena Menezes Carvalho 1 1 Instituto de Física de São Carlos, Universidade de São Paulo E-mail: glowingsea@gmail.com 1. Introdução
MOMENTO DIPOLAR ELÉCTRICO. Resumo O objectivo deste trabalho é a resolução do problema 9 da série de exercícios n o 1 de Física Quântica da Matéria.
 MESTRADO EM ENGENHARIA FÍSICA TECNOLÓGICA - FÍSICA QUÂNTICA DA MATÉRIA Preprint typeset using LATEX style emulateapj v. 8// MOMENTO DIPOLAR ELÉCTRICO ALEXANDRE FREITAS, N o 5255 RAQUEL PINTO, N o 57 Mestrado
MESTRADO EM ENGENHARIA FÍSICA TECNOLÓGICA - FÍSICA QUÂNTICA DA MATÉRIA Preprint typeset using LATEX style emulateapj v. 8// MOMENTO DIPOLAR ELÉCTRICO ALEXANDRE FREITAS, N o 5255 RAQUEL PINTO, N o 57 Mestrado
Lista 2. As leis de Kepler e gravitação universal de Newton
 Lista 2. As leis de Kepler e gravitação universal de Newton Nestor Caticha Física Geral IFUSP Universidade de São Paulo, CP66318, CEP 05315-970, São Paulo, SP, Brazil 25 de Outubro de 2012 Resumo Esta
Lista 2. As leis de Kepler e gravitação universal de Newton Nestor Caticha Física Geral IFUSP Universidade de São Paulo, CP66318, CEP 05315-970, São Paulo, SP, Brazil 25 de Outubro de 2012 Resumo Esta
Escola Politécnica FAP GABARITO DA P2 24 de outubro de 2006
 P2 Física IV Escola Politécnica - 2006 FAP 2204 - GABARITO DA P2 24 de outubro de 2006 Questão 1 A. O comprimento de onda de corte para ejetar elétron da superfície do metal lantânio é = 3760 Å. (a) (0,5
P2 Física IV Escola Politécnica - 2006 FAP 2204 - GABARITO DA P2 24 de outubro de 2006 Questão 1 A. O comprimento de onda de corte para ejetar elétron da superfície do metal lantânio é = 3760 Å. (a) (0,5
Valores esperados. ψ (x)xψ(x)dx. ψ ψ dx. xp(x)dx P(x)dx. Vimos que: x = = ψ xψ dx. No caso geral de uma função de x: f (x) = f (x) =
 Vimos que: x = + Valores esperados ψ (x)xψ(x)dx xp(x)dx P(x)dx = ψ xψ dx ψ ψ dx No caso geral de uma função de x: f (x) = f (x) = + ψ (x) ˆf (x)ψ(x)dx Para o momento e a energia: ˆp = i x e Ê = i t. 4300375
Vimos que: x = + Valores esperados ψ (x)xψ(x)dx xp(x)dx P(x)dx = ψ xψ dx ψ ψ dx No caso geral de uma função de x: f (x) = f (x) = + ψ (x) ˆf (x)ψ(x)dx Para o momento e a energia: ˆp = i x e Ê = i t. 4300375
ESTRUTURA ELETRÔNICA DOS ÁTOMOS
 ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
UFABC - Física Quântica - Curso Prof. Germán Lugones. Aula 8. A equação de Schrödinger
 UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 8 A equação de Schrödinger 1 A equação de Schrödinger Na primeira parte do curso, introduzimos a dualidade onda-partícula. Usando as relações
UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 8 A equação de Schrödinger 1 A equação de Schrödinger Na primeira parte do curso, introduzimos a dualidade onda-partícula. Usando as relações
5.1: Aplicação da Equação de Schrödinger ao átomo de Hidrogênio
 http://www.if.ufrgs.br/~marcia/textos.html UNIDADE Aula 5 Átomo de Hidrogênio * * Tradução e adaptação livre das aulas do Professor Rick Trebino em: www.physics.gatech.edu/frog 5.1 Aplicação da Equação
http://www.if.ufrgs.br/~marcia/textos.html UNIDADE Aula 5 Átomo de Hidrogênio * * Tradução e adaptação livre das aulas do Professor Rick Trebino em: www.physics.gatech.edu/frog 5.1 Aplicação da Equação
Fundamentos da Eletrostática Aula 02 Cálculo Vetorial: derivadas
 Campo Escalar e Gradiente Fundamentos da Eletrostática Aula 02 Cálculo Vetorial: derivadas Prof. Alex G. Dias (alex.dias@ufabc.edu.br) Prof. Alysson F. Ferrari (alysson.ferrari@ufabc.edu.br) Um campo escalar
Campo Escalar e Gradiente Fundamentos da Eletrostática Aula 02 Cálculo Vetorial: derivadas Prof. Alex G. Dias (alex.dias@ufabc.edu.br) Prof. Alysson F. Ferrari (alysson.ferrari@ufabc.edu.br) Um campo escalar
Mecânica Quântica:
 Mecânica Quântica: 016-017 6 a Série 1. Considere as matrizes de Pauli, dadas por ( 0 1 0 i 1 0 σ x =, σ 1 0 y =, σ i 0 z = 0 1 ) 1.1. Demonstre que estas matrizes são Hermíticas. Determine os seus valores
Mecânica Quântica: 016-017 6 a Série 1. Considere as matrizes de Pauli, dadas por ( 0 1 0 i 1 0 σ x =, σ 1 0 y =, σ i 0 z = 0 1 ) 1.1. Demonstre que estas matrizes são Hermíticas. Determine os seus valores
NÚMEROS QUÂNTICOS. As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons.
 NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
harmônicos esféricos Os harmônicos esféricos são simultaneamente autofunções dos operadores
 A eq. de Schrödinger em 3D: Independente do tempo: Separação de variáveis: h m v Ψ + V ( r ) Ψ = h v ψ + V ( r ) ψ = m Ψ ih t Eψ ψ ( r, θ, ϕ) = R( r) Θ( θ ) Φ( ϕ) R n ( r) ; Θ ( θ ) ; Φ ( ϕ) Ylm l ( θ,
A eq. de Schrödinger em 3D: Independente do tempo: Separação de variáveis: h m v Ψ + V ( r ) Ψ = h v ψ + V ( r ) ψ = m Ψ ih t Eψ ψ ( r, θ, ϕ) = R( r) Θ( θ ) Φ( ϕ) R n ( r) ; Θ ( θ ) ; Φ ( ϕ) Ylm l ( θ,
Aula-11. (quase) Tudo sobre os átomos
 Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Processo Seletivo PPGFSC/UFSC primeiro semestre de 2015
 Processo Seletivo PPGFSC/UFSC primeiro semestre de 2015 Nome do Candidato: Instruções: A prova consta de 20 (vinte) questões, sendo que o candidato deve escolher entre as opções ou A ou B de mesma numeração,
Processo Seletivo PPGFSC/UFSC primeiro semestre de 2015 Nome do Candidato: Instruções: A prova consta de 20 (vinte) questões, sendo que o candidato deve escolher entre as opções ou A ou B de mesma numeração,
3-FUNDAMENTOS DA MECÂNICA QUÂNTICA - PARTE 2
 TE069-Física de Semicondutores 3-FUNDAMENTOS DA MECÂNICA QUÂNTICA - PARTE 2 PROF. CÉSAR AUGUSTO DARTORA - UFPR E-MAIL: CADARTORA@ELETRICA.UFPR.BR CURITIBA-PR Roteiro do Capítulo: Poço de potencial duplo:
TE069-Física de Semicondutores 3-FUNDAMENTOS DA MECÂNICA QUÂNTICA - PARTE 2 PROF. CÉSAR AUGUSTO DARTORA - UFPR E-MAIL: CADARTORA@ELETRICA.UFPR.BR CURITIBA-PR Roteiro do Capítulo: Poço de potencial duplo:
Comportamento ondulatório da matéria
 Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Física Moderna II Aula 07
 Universidade de São Paulo Instituto de Física 1 º Semestre de 015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 0 rizzutto@if.usp.br Física Moderna II Aula 07 Monitor: Gabriel M. de Souza Santos Sala
Universidade de São Paulo Instituto de Física 1 º Semestre de 015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 0 rizzutto@if.usp.br Física Moderna II Aula 07 Monitor: Gabriel M. de Souza Santos Sala
Revisão de conceitos de mecânica quântica
 Revisão de conceitos de mecânica quântica Quantização de energia A Radiação de corpo negro Estudos de Planck (1900) sobre a radiação de corpo negro, levaram a ideia de que a energia é dependente da frequência
Revisão de conceitos de mecânica quântica Quantização de energia A Radiação de corpo negro Estudos de Planck (1900) sobre a radiação de corpo negro, levaram a ideia de que a energia é dependente da frequência
FAP2293 Física para Engenharia Elétrica 4 PROVA SUB 15/12/2009 Gabarito 15 de dezembro de 2009
 IFUSP FAP93 Física para Engenharia Elétrica 4 PROVA SUB 5//9 Gabarito 5 de dezembro de 9 Questão Considere o modelo de Bohr para o átomo de hidrogênio (,5): a) Determine, usando a regra de quantização
IFUSP FAP93 Física para Engenharia Elétrica 4 PROVA SUB 5//9 Gabarito 5 de dezembro de 9 Questão Considere o modelo de Bohr para o átomo de hidrogênio (,5): a) Determine, usando a regra de quantização
Simetrias na Mecânica Quântica
 Simetrias na Mecânica Quântica Prof. 26 de maio de 2010 Definição de Simetria na Mecânica Quântica G(a) elemento de um grupo G de transformações contínuas, ˆT(G(a)) operador unitário. G(a) M.Q. ˆT(G(a)),
Simetrias na Mecânica Quântica Prof. 26 de maio de 2010 Definição de Simetria na Mecânica Quântica G(a) elemento de um grupo G de transformações contínuas, ˆT(G(a)) operador unitário. G(a) M.Q. ˆT(G(a)),
13/Maio/2016 Aula 20. Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números quânticos. 11/Maio/2016 Aula 19
 11/Maio/2016 Aula 19 Aplicações: - nanotecnologias; - microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. 13/Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números
11/Maio/2016 Aula 19 Aplicações: - nanotecnologias; - microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. 13/Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números
Aula anterior. Equação de Schrödinger a 3 dimensões. d x 2m - E -U. 2m - E -U x, y, z. x y z x py pz cin cin. E E ( x, y,z ) - 2m 2m x y z
 6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
Partícula na Caixa. Química Quântica Prof a. Dr a. Carla Dalmolin
 Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
PROPRIEDADES ONDULATÓRIAS DO ELÉTRON
 MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
Física Quântica. Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli. Pieter Westera
 Física Quântica Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html Quantização do Momento Angular
Física Quântica Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html Quantização do Momento Angular
Princípios Gerais da Mecânica Quântica
 Princípios Gerais da Mecânica Quântica Vitor Oguri Departamento de Física Nuclear e Altas Energias (DFNAE) Instituto de Física Armando Dias Tavares (IFADT) Universidade do Estado do Rio de Janeiro (UERJ)
Princípios Gerais da Mecânica Quântica Vitor Oguri Departamento de Física Nuclear e Altas Energias (DFNAE) Instituto de Física Armando Dias Tavares (IFADT) Universidade do Estado do Rio de Janeiro (UERJ)
Programa da Disciplina: Física Moderna Modalidade EAD
 Programa da Disciplina: Física Moderna Modalidade EAD Profa. Ana Paula Andrade Conteúdo: Unidade 1 Aula 1 Introdução - Aula introdutória onde discutiremos as questões centrais que levaram ao desenvolvimento
Programa da Disciplina: Física Moderna Modalidade EAD Profa. Ana Paula Andrade Conteúdo: Unidade 1 Aula 1 Introdução - Aula introdutória onde discutiremos as questões centrais que levaram ao desenvolvimento
A teoria de Hartree. r r. r r
 A teoria de Hartree Vimos, na aula 4, a proposta de Hartree: tratamento autoconsistente Ou seja, V(r) obtido a posteriori, a partir das distribuições de carga dos e -, deve concordar com o V(r) usado para
A teoria de Hartree Vimos, na aula 4, a proposta de Hartree: tratamento autoconsistente Ou seja, V(r) obtido a posteriori, a partir das distribuições de carga dos e -, deve concordar com o V(r) usado para
Figure 1: Seção transversal de um tubo
 Questão de eletromagnetismo: O Large Hadron Collider (LHC) é o maior acelerador de partículas já construido. Em um túnel circular de 27 km de extensão a aproximadamente 00 metros de profundidade, 2 feixes
Questão de eletromagnetismo: O Large Hadron Collider (LHC) é o maior acelerador de partículas já construido. Em um túnel circular de 27 km de extensão a aproximadamente 00 metros de profundidade, 2 feixes
Física Moderna II Aula 03. Marcelo G Munhoz Pelletron, sala 245, ramal 6940
 Física Moderna II Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br Schroedinger X Bohr Qual a vantagem da teoria de Schroedinger sobre a teoria de Bohr do ponto de vista da observação
Física Moderna II Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br Schroedinger X Bohr Qual a vantagem da teoria de Schroedinger sobre a teoria de Bohr do ponto de vista da observação
PGF MECÂNICA QUÂNTICA I (2010) Resolução Comentada da Lista de Problemas 5 Eduardo T. D. Matsushita
 PGF51 - MECÂNICA QUÂNTICA I (1) Resolução Coentada da Lista de Probleas 5 Eduardo T. D. Matsushita 1. Considere ua partícula de carga e no capo elétrico de ua carga puntifore de carga igual a Ze. A hailtoniana
PGF51 - MECÂNICA QUÂNTICA I (1) Resolução Coentada da Lista de Probleas 5 Eduardo T. D. Matsushita 1. Considere ua partícula de carga e no capo elétrico de ua carga puntifore de carga igual a Ze. A hailtoniana
Física IV Escola Politécnica GABARITO DA P3 27 de novembro de 2012
 Física IV - 4320402 Escola Politécnica - 2012 GABARITO DA P3 27 de novembro de 2012 Questão 1 Considere uma partícula de massa m e energia E num potencial unidimensional que é nulo na região 0 < x < d
Física IV - 4320402 Escola Politécnica - 2012 GABARITO DA P3 27 de novembro de 2012 Questão 1 Considere uma partícula de massa m e energia E num potencial unidimensional que é nulo na região 0 < x < d
