Revisão de conceitos de mecânica quântica
|
|
|
- João Guilherme Varejão
- 5 Há anos
- Visualizações:
Transcrição
1 Revisão de conceitos de mecânica quântica Quantização de energia A Radiação de corpo negro Estudos de Planck (1900) sobre a radiação de corpo negro, levaram a ideia de que a energia é dependente da frequência da radiação. E=nh ν sendo h a constante de Planck e n=1,, 3,... de forma que a energia pode assumir somente valores múltiplos inteiros do valor mínimo (energia discreta). Átomos apresentam valores de energia discretos, chamados níveis de energia. Os níveis de energia correspondem aos estados de energia possíveis. Sistemas nos quais a energia só pode assumir valores determinados, são ditos quantizados.
2 Ondas e partículas. Efeito fotoelétrico interpretado por Einstein (1905) a luz da teoria corpuscular. Um fóton e uma partícula, por exemplo um elétron, tem a eles associados uma onda. A energia E se relaciona à frequência ν pela relação: E=h ν (1) e o momento p se relaciona ao comprimento de onda λ por: hν h p= = c λ () Note que nas relações 1 e, interligam os conceitos típicos de partículas e de onda E e p=>λ,υ.
3 Ideias de quantização e o átomo de Bohr (1913) 4 me 1 E n = 8 ϵ0 h n n =1,,3,... Função de onda e equação de Schroedinger Equação de Schroedinger dependente do tempo ψ( r, t) ℏ ψ( r, t )+ V( r, t ) ψ( r, t)=i ℏ m t Sendo V a energia potencial
4 Função de onda ψ (x,y,z,t) ψ Está distribuida no espaço, para qualquer instante de tempo t. Não tem signifca físico. A probabilidade de encontrar uma partícula em um tempo e em ponto do espaço defnidos só pode ser 0 ou 1. Densidade de probabilidade ψ ψ Probabilidade de encontrar a partícula descrita pela função de onda ψ, no ponto x, y, z e no tempo t.
5 Equação de Schroedinger e o Átomo de hidrogênio Estado ligado próton-elétron, tratado como uma única partícula de massa mpme/(mp+me) sob a ação de um campo. Sendo o sistema um estado ligado, podemos assumir o potencial independente do tempo e portanto aplicar a equação de Schroedinger independente do tempo a este sistema. h ψ ψ ψ + + +[V ( r ) E] ψ m x y z ( ] Visto que mp ~1836 me, a massa do sistema se reduz a massa do elétron.
6 Átomo de hidrogênio Pode-se a assumir V como a energia potencial eletrostática entre o elétron e o próton, V (r)= e 1 4 π ϵ0 r A solução da equação de Schoredinger para o átomo de hidrogênio, fca simplifcada, quando se considera a função de onda, ψ( r, θ, ϕ)=r (r )Θ(θ)Φ(ϕ) Sendo (r, θ, ϕ), coordenadas polares.
7 Obtém-se assim três equações independentes entre si: d Φ + m l Φ (1) dϕ l m 1 d dθ sen θ + l(l+1) Θ () sen θ d θ dθ sen θ ( )[ ( [ ) ] ] l(l+1) 1 d dr m e r + +E R=0 (3) dr r dr h 4 π ϵ0 r r ( ) Exercício 1: obtenha as esquações (1), () e (3).
8 As soluções das equações (1) () e (3), levam aos números quanticos: Número quântico principal n = 1,, 3, A energia total do átomo depende de n, portanto está ligado ao nível de energia no qual o elétron está localizado. Número quântico azimutal ou orbital l = 0, 1,,, (n-1) O momento angular azimutal depende de l, portanto está ligado aos subníveis de energia do elétron. Número quântico magnético ml = 0, ± 1, ±,, ±l Ligado à energia do átomo quando este se encontra em um campo magnético externo. Sendo a função de onda do átomo, em termos dos números quânticos escrita como: Ψ =R nl Θ m Φ lm l l
9 n = 1; l =0; ml = 0 n = ; l=0, 1; ml = -1,0,+1 Portanto estados com a mesma energia total podem apresentar comportamento completamente diferentes, são ditos estados degenerados. Quantização do momento angular L L=ℏ l (l +1) ou seja, L é quantizado! Exercício : mostre que o momento angular orbital do elétron é dado por:
10 A quantização do espaço O numero quântico orbital l determina a magnitude L do momento angular L do elétron. O elétron girando em torno do núcleo pode ser visto como um anel de corrente envolvendo o próprio núcleo. Este anel de corrente produz um campo magnético Bint. Assim, um elétron atômico que possui momento angular L interage com um campo magnético externo Bext. A magnitude do número quântico magnético, ml especifca a direção de L determinando sua componente na direção do campo magnético externo Bext conhecida como quantização do espaço.
11 Considerando a direção do campo magnético paralela ao eixo z, a componente de L nesta direção será: L z =ml ℏ Com ml = 0 ± 1, ±,, ±l. Assim o número de orientações possíveis é l +1. Observe que L, nunca estará perfeitamente Alinhado com o campo, pois Lz<L. Exercício 3: Explique porque somente Uma componente do momento angular L é quantizada. Fig. 6.4, Beiser. L =. 5 valores possíveis de ml
12 Spin do elétron e princípio de exclusão de Pauli O spin do elétron, observações experimentais Mecânica quântica até aqui apresentada não é capaz de fornecer uma descrição precisa da estrutura atômica. Observáveis a serem entendidos. Estrutura fina do átomo de hidrogênio. Predição teórica: uma única linha correspondente a λ = 656,3 nm Verificação experimental: duas linhas separadas por 0,14 nm
13 Efeito Zeeman Predição teórica: átomo em um campo eletromagnético, com uma linha espectral dividida em três componentes. Observação experimental: linha espectral pode se dividir em quatro, seis ou sete ou dividindo-se em três, não corresponder à previsão teórica do efeito Zeeman normal. Fig. 7.1, Beiser. Diagrama esquemático de efeito Zeeman normal e anômalo.
14 Solução do problema! 195, Samuel Goudsmit e George Uhlenbeck Cada elétron tem um momentum angular intrínseco, chamado spin, de mesma magnitude para todos os elétrons. Imagem clássica : elétron como uma esfera carregada que gira em torno do seu eixo. Associado ao elétron, momentum angular S e momento magnético μ S Esta imagem clássica não corresponde à realidade. O elétron é uma partícula elementar e se fosse uma esfera devido a sua dimensão reduzida giraria com velocidade superior à velocidade da luz.
15 A predição do spin do elétron foi consolidada pela mecânica quântica relativística desenvolvida por Paul Dirac, em 199. A magnitude do momentum angular de spin S do elétron é dada por: 3 S = s(s+ 1)ℏ= ℏ onde s =1/ é o número quântico de spin. No exemplo a seguir mostramos uma falha da interpretação clássica do spin. Vamos então determinar a velocidade de um elétron considerando que ele seja uma esfera de raio r, que gira em torno do eixo que passa pelo seu centro com r=5, m
16 Solução. Segundo a hipótese considerada, a magnitude do momento angular de spin é igual à magnitude do momento angular devido à rotação do elétron, S = I ω O momento de inércia de uma esfera homogênea é dado por: v I= mr e sua velocidade angular ω= 5 r Logo temos: 3 ℏ = m r v = mvr (5 )( r ) 5 3 ℏ 4 v= 5 =1,67 10 c ( 4 ) mr Observe o resultado!
17 De modo similar ao momentum angular orbital, o momentum angular de spin do elétron pode ter s + 1, orientações, espaciais. Visto que o número quântico de spin do elétron é s = 1/, há duas orientações possíves, correspondentes ao spin up 1 1 m s = ms =+ e spin down Da mesma forma, a componente do momentum angular de spin de um elétron ao longo de um campo magnético na direção z é dada por: 1 S z =m s ℏ=± ℏ
18 Considerando a razão giromagnética (razão entre o momentum magnético e angular) do spin igual a S, o momento magnético de spin é: μ s = e S m A componente do momentum magnético de spin, ao longo do eixo z é dada por: eℏ μ sz =± =±μ B m onde μ é o magneton de Bohr. B Com a introdução do spin do elétron, os estados de energia de um átomo são descritos pelos números quânticos n, l, ml e ms.
19 Experimento de Stern-Gerlach (19) (quantização espacial) Posteriormente interpretado como evidência experimental do spin do elétron. Feixe de átomos de prata numa direção z, passando através de um sistema de colimadores imersos em um campo magnético variável, resultando em apenas duas componentes discretas do momento de dipolo magnético. Princípio de exclusão de Pauli. Wolfgang Pauli, 195. Dois elétrons em um átomo não podem existir num mesmo estado quântico.
20 Evidência experimental pelo estudo de espectros atômicos aonde certas combinações de números quânticos correspondentes a estados esperados não eram observadas. Exemplo: hélio, nenhuma transição observada para ou do estado fundamental no qual os spins dos elétrons têm a mesma direção. Transições observadas para spins de direções contrárias. Pauli mostrou que cada estado ausente envolve dois ou mais elétrons com números quânticos idênticos. Portanto o princípio de exclusão de Pauli permite a correta interpretação de muitas propriedades da matéria como veremos mais adiante.
21 Estrutruras atômicas e o princípio de exclusão de Pauli Funções de onda: bósons e férmions Consideremos um sistema constituido por duas partículas 1 e e autoestados α e β. Soluções possíveis da equação de Schroedinger, para este sistema, podem ser representadas por: ψ1, =ψα (1)ψβ () ψ,1 =ψα () ψβ (1) As soluções apresentadas mostram que é possível distinguir qual partícula ocupa qual estado, ou seja, as partículas são distinguíveis.
22 Porém se as partículas são quanticamente idênticas, observáveis como a densidade de probabilidade, devem permanecer inalterados quando as partículas trocam de estado. Matematicamente a densidade de probabilidade deve permanecer inalterável sob a troca de índices 1< >. A densidade de probalidade para a partícula 1 no estado α e partícula no estado β, é dada por: ψ*1, ψ1,=ψ*α (1)ψ*β () ψα (1)ψβ () enquanto que para a partícula 1 no estado β e a partícula no estado α é dada por: ψ*,1 ψ,1 =ψ*α () ψβ* (1)ψα ()ψβ (1)
23 Examinando a primeira expressão em relação a troca de índices, obtém-se: ψ*1, ψ1,=ψ*α (1)ψ*β () ψα (1)ψβ () ψ*,1 ψ,1= ψ*α ()ψ*β (1) ψα () ψβ (1) ou seja, a densidade de probabilidade é alterada pela troca de estado entre as partículas. As funções de onda que representam as trocas de estados são definidas como: Simétrica, o sinal permanece inalterado quando a partícula troca de estado, ou seja, Ψ1, = + Ψ,1 Antissimétrica, há troca de sinal quando a partícula troca de estado, ou seja, Ψ1, = Ψ,1
24 A função de onda que descreve sistemas quânticos, compostos por partículas idênticas, é dada pela combinação linear: ψ± = 1 [ψα (1) ψβ ()±ψβ (1)ψα ()] onde os sinais +/-, simétrica/antissimétrica. representam as autofunções Esta não é uma definição meramente matemática, ela representa importantes características físicas de sistemas quânticos. Observe que a função de onda antissimétrica resulta nula se as partículas encontram-se no mesmo estado, enquanto que a função de onda simétrica não impõe esta restrição.
25 Princípio de Exclusão de Pauli. Em sistemas de partículas descritas por autofunções antissimétricas, por exemplo, elétrons, a presença de uma partícula em um dado estado implica na impossibilidade de que uma segunda partícula venha a ocupar o mesmo estado quântico. Férmions São classificadas como férmions, todas as partículas que têm spin semi-inteiro e que são descritas por funções de onda antissimétricas. Portanto em um sistema de férmions partículas com mesmo números quânticos não podem ocupar o mesmo estado quântico. Os férmions obedecem à estatística de Fermi-Dirac.
26 Bósons São classificadas como bósons, todas as partículas que têm spin interio e que são descritas por funções de onda simétricas. Portanto em um sistema de bósons partículas com mesmos números quânticos podem ocupar o mesmo estado quântico. Os bósons obedecem à estatística de Bose-Einstein. As partículas que compõem a matéria ordinária, isto é, prótons, neutrons e elétrons possuem spin semi-inteiro, são férmions. Esta propriedade é independente da partícula ser elementar ou não, isto é, ter estrutura interna. Discutiremos em mais detalhes, no decorrer do curso, as propriedades das funções estatísticas e das partículas atualmente conhecidas.
27 Resumo: Férmions Obedecem ao princípio da exclusão de Pauli, autofunções anti-simétricas, spin (s) semi-inteiro. sendo n = 0,1,,... 1 s= n+ ℏ, ( ) Bósons Não obedecem ao princípio de exclusão de Pauli, autofunções simétricas, spin (s) inteiro. s =n ℏ
28 A tabela periódica Dmitri Mendeleev (1869) a busca pelo entendimento da estrutura da matéria. Organizada em colunas e linhas propriedades químicas semelhantes. de elementos com A organização da tabela periódica é explicada por meio das propriedades quânticas dos átomos e representa uma importante afirmação da mecânica quântica. Seção 7.4 livro texto Beiser.
29 As camadas e subcamadas de elétrons nos átomos As propriedades físicas de um átomo podem ser compreendidas considerando-o como um sistema organizado em camadas e subcamadas. A estrutura em camadas e subcamadas é determinada de modo que cada estado quântico particular seja ocupado somente por um elétron e que a energia energia total mínima do átomo corresponda ao seu estado mais estável. Vamos examinar como a energia de um elétron varia em função do estado quântico.
30 Em átomos multieletrônicos podemos tratar os elétrons como sujeitos a um campo elétrico devido a carga Ze decrescido da blindagem parcial dos outros elétrons que encontram-se próximos ao núcleo. Elétrons que possuem o mesmo número quântico principal, n, encontram-se em níveis de energia similares, ou seja, ocupam a mesma camada atômica (K, L, M,... correspondentes a n= 1,,3,...). A energia dos elétrons aumenta com o aumento do número quântico principal n, mas apresenta também uma dependência com o número quântico orbital, l.
31 Elétrons com l, menores encontram-se mais próximos do núcleo, portanto sofrem menos a ação da blindagem. Consequentemente eles são mais ligados ao núcleo e portanto, têm energia total mais baixa. Lembre-se que da solução da equação de Schroedinger, conclui-se que n = l +1, ou seja, l = 0,1,,3,...,n-1. Por exemplo, para n=3, l = 0,1 ou. Em cada camada a energia do elétron aumenta a medida que l cresce. Elétrons que dividem um certo valor de l, ocupam a mesma subcamada e têm energia similar.
32 Na notação representativa dos estados quânticos, cada subcamada é identificada pelo número quântico principal, n, seguido pelo número quântico orbital l e o superíndice representa o número de elétrons na subcamada. Exemplo: sódio (Na) 1s (n=1, l=0), s (n=, l =0), subcamadas com dois elétrons; p6 (n=, l=1), subcamada com 6 elétrons; 3s1 (n=3, l=0), subcamada com 1 elétron. 1s s p6 3s 1
33 O princípio de exclusão limita o número de elétrons que pode ocupar cada subcamada. Cada subcamada é caracterizada pelos números quânticos n e l, sendo que o número quântico magnético pode assumir valores de -l à +l, ou seja, ml = l, l+ 1,..., + l 1, l Por outro lado, cada elétron pode assumir um dos dois números quânticos de spin, m s=+ 1 1 ou m s= Portanto cada subcamada pode conter (l +1) elétrons.
34 O número máximo de elétons que uma camada pode conter é a igual soma do número de elétrons contidos em suas subcamadas: l=n 1 N max= (l+ 1)=[ ,...,+ n 1] = n l=0 Assim, a camada K (n=1) contém elétrons, a camada L (n=) 8 elétrons, a camada M (n=3) 18 elétrons e assim por diante. (Notação de camadas eletrônicas e tabela periódica.) Cada elétron do núcleo tem um momentum angular orbital L e um momentum angular de Spin, S que contribuem para o momentum angular total J do átomo.
35 O acoplamento spin-órbita O conceito de spin tem um importante papel no entendimento da estrutura fina observada em espetros atômicos. A dupla estrutura fina de linhas espectrais surge da interação entre o momento angular orbital e de spin de um elétron atômico, que denominamos acoplamento spin-órbita. Considere um modelo clássico simples, onde o elétron orbita em torno do núcleo. No referencial do elétron, ele sente um campo magnético devido ao movimento do núcleo e este campo magnético interage com o spin do elétron produzindo uma espécie de efeito Zeeman.
36 A energia potencial Um de um dipolo magnético, de momentum μ, em um campo magnético B, é dada por: U m= μ Bcos θ onde θ é o ângulo entre μ e B. No caso do momento magnético de spin do elétron, Logo, μ cos θ=μ SZ =±μ B U m=±μ B B Portanto dependendo da orientação espacial do spin a energia do elétron em um átomo, será maior ou menor, por uma quantidade μ B B, que a sua energia sem acoplamento.
37 Assim, cada estado quântico exceto s onde l = 0, é dividido em dois estados. Exemplo: Estime a energia magnética no estado p de um átomo de hidrogênio, usando o modelo de Bohr, cujo estado n=, corresponde ao estado p. Solução: Primeiramente precisamos calcular o campo magnético B. Para isto, consideremos o campo magnético no centro de um círculo de raio r, percorrido por uma corrente I. O campo magnético será dado por: μ0 I B= r
38 Considerando que o elétron gira em torno do núcleo de carga +e, com uma frequência f, o campo magnético será: μ 0 ef B= r O raio de Bohr, é dado por: r n=n a 0 onde a0 = 5,9 x 10-11m, o raio mais interno. A frequência f, neste movimento circular é expressa por: f= v πr
39 A velocidade do elétron, girando em um círculo de raio r, pode ser estimada igualando a força centrípeta à força elétrica: mv 1 e e = v= r 4 π ϵ0 r 4 π ϵ0 mr Substituindo convenientemente os valores obtém-se: f =8, s 1, r =, m Então, B = 0,40 T e finalmente, U m=μ B B = 3, J =, ev A diferença de energia entre os estados superior e inferior será portanto, 5 4,6 X 10 ev Compatível com o valor observado experimentalmente.
40 Momentum angular de um átomo Devido ao princípio da exclusão de Pauli, geralmente, os átomos e íons cujos elétrons distribuiem-se em camadas fechadas, têm momentum angular total e magnético, iguais a zero. Portanto o momento angular total de átomos que têm um elétron excedente às camadas fechadas, é determinado por este elétron. O momentum angular total do elétron é dado por: J=L+ S Sendo quantizado e de magnitude: J= j( j+ 1)ℏ, com j=l+ s=l± 1
41 A componente Jz de J na direção z é dada por: J z =m j ℏ, sendo m j = j, j+ 1,..., j 1, j Átomos com um único elétron, possuem apenas duas orientações, uma correspondente a J>L (j=l+s) e outra correspondente a J<L (j=l-s). A figura 7.15 do livro texto Beiser, mostra a intensidade de J para s= +1/ e s= 1/, no caso de l=1. A figura 7.16, mostra os possíveis valores de número quântico magnético mj e das componentes Jz, para o mesmo caso. Qual o efeito sobre o momento angular total no casos em que há um campo magnético externo aplicado? (Veja a figura 7.17 do livro texto Beiser).
42 Para átomos nos quais o momentum angular total é resultante da contribuição de mais de um elétron, o momentum angular orbital de todos os elétrons se acoplam produzindo o momentum resultante L. Da mesma forma os momenta angular de spin, se acoplam produzindo o momentum resultante S, ou seja: L= L i, S= Si, J=L+ S Este é o chamado acoplamento LS. As magnitudes dos momentum L, S, J e suas componentes, Lz, Sz e Jz, são expressas de modo similar ao caso de um elétron excedente, usando-se porém letras maiúsculas.
43 L= L(L+ 1)ℏ, L z =M L ℏ S= S(S+ 1)ℏ, Sz =Ms ℏ J= J(J+ 1)ℏ, J z =MJ ℏ Sendo L, S, J ML, MS e MJ, os respectivos números quânticos. L e ML, são sempre inteiros ou 0, equanto que os demais números quâticos são inteiros se o número de elétrons é par e semi-inteiros se o número de elétrons é ímpar. Exemplo: Determine os valores possíveis do número quântico, momentum angular total J, para dois elétrons com números quânticos orbitais l=1 e l=, considerando um acoplamento LS.
44 Solução: Os possíveis valores de L e S, estarão definidos nos intervalos: l 1 l à l 1+ l s 1 s à s1+ s Portanto teremos: L=1, ou 3 e S=0 ou 1 O momento angular total J estará compreendido entre L S e L+ S, portanto os valores possíveis para o momentum angular total do sistema constituído pelos dois elétrons são: J=0, 1,, 3 e 4.
45 Notação adotada, para identificar um estado de energia do átomo. Exemplo, estado fundamental do sódio: 3 S1/ O número 3, refere-se ao número quântico principal; o superíndice a multiplicidade de estados, no caso um dubleto; a letra S, ao momentum angular, no caso l=0 e o índice ½, refere-se ao momentum angular total j. Portanto neste exemplo, temos para os números quânticos: n=3, l=0, j=1/. Como mj = j, j+1,..., +j, mj = ± ½. Obs: Os núcleos atômicos também possuem momentos angular intrínseco e momentos magnéticos que contribuem para o momentos totais. Como µm nuclear ~10-3 µm elétrico, o seu espaçamento d estrutura hiperfina é muito pequena comparada à dos átomos.
46 Bibliografa: Beiser, A. Concepts of Modern Physics, New York, McGrawHill, Caruso, F. & Oguri, V., Física Quântica origens clássicas e fundamentos quânticos, Rio de Janeiro, Ed. LTC, 016. Eisberg, R. & Resnick, R., Física Quântica, Rio de Janeiro, Ed. Campus, 1979
8. Spin do elétron e átomos complexos
 8. Spin do elétron e átomos complexos Sumário Revisão: momento magnético do elétron Efeito Zeeman Spin do elétron Experiência de Stern-Gerlach O princípio da exclusão de Pauli Configuração eletrônica Tabela
8. Spin do elétron e átomos complexos Sumário Revisão: momento magnético do elétron Efeito Zeeman Spin do elétron Experiência de Stern-Gerlach O princípio da exclusão de Pauli Configuração eletrônica Tabela
Física Quântica. Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli. Pieter Westera
 Física Quântica Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html Quantização do Momento Angular
Física Quântica Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html Quantização do Momento Angular
Aula-11. (quase) Tudo sobre os átomos
 Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Aula 17 Tudo sobre os Átomos
 Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
n Camadas K L M N...
 Notação Espectroscópica para Configurações Eletrônicas em Átomos. Modelo de Partícula Independente. Podemos obter uma quantidade expressiva importante de informações sobre estados atômicos de sistemas
Notação Espectroscópica para Configurações Eletrônicas em Átomos. Modelo de Partícula Independente. Podemos obter uma quantidade expressiva importante de informações sobre estados atômicos de sistemas
A Equação de Onda de Schröedinger. O Princípio da Incerteza de Heisenberg. λ =
 O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
7. A teoria quântica do átomo de Hidrogênio
 7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
O spin do elétron. Vimos, na aula 2, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com 2 valores, com propriedades de momento angular.
 O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
Átomo de Hidrogênio 1
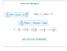 Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 10 ÁTOMOS COMPLEXOS Primeira Edição junho de 2005 CAPÍTULO 10 ÁTOMOS COMPLEXOS ÍNDICE 10-1- Introdução 10.2- Átomos com mais de um
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 10 ÁTOMOS COMPLEXOS Primeira Edição junho de 2005 CAPÍTULO 10 ÁTOMOS COMPLEXOS ÍNDICE 10-1- Introdução 10.2- Átomos com mais de um
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Aula 12. (quase) Tudo sobre os átomos. Física Geral F-428
 Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
h mc 2 =hν mc 2 =hc/ λ
 Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL
 UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL LOB1021 - FÍSICA IV Prof. Dr. Durval Rodrigues Junior Departamento de Engenharia de Materiais (DEMAR) Escola de Engenharia de Lorena (EEL) Universidade
UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL LOB1021 - FÍSICA IV Prof. Dr. Durval Rodrigues Junior Departamento de Engenharia de Materiais (DEMAR) Escola de Engenharia de Lorena (EEL) Universidade
Universidade de São Paulo Instituto de Física. Física Moderna II. Profa. Márcia de Almeida Rizzutto 2 o Semestre de Física Moderna 2 Aula 5
 Universidade de São Paulo Instituto de Física Física Moderna II Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 19: experiência de Stern&Gerlach Proposta: Medir os valores possíveis do momento de
Universidade de São Paulo Instituto de Física Física Moderna II Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 19: experiência de Stern&Gerlach Proposta: Medir os valores possíveis do momento de
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
n, l, m l, ms (1) quando estes quatro números quânticos são dados, o estado físico do sistema (no caso, um elétron) é então especificado.
 Introdução. Consideramos nos textos anteriores sistemas quantum mecânicos que possuem vários níveis de energia mas somente um elétron orbital, ou seja, consideramos até o presente momento átomos hidrogenóides.
Introdução. Consideramos nos textos anteriores sistemas quantum mecânicos que possuem vários níveis de energia mas somente um elétron orbital, ou seja, consideramos até o presente momento átomos hidrogenóides.
Átomos e Moléculas. Ligações moleculares. Energia do ion. A molécula de hidrogênio H 2
 Ligações moleculares Átomos e Moléculas Energia do ion H 2 + A molécula de hidrogênio Ligações moleculares Uma molécula é formada por um conjunto de átomos que interagem formando um sistema com energia
Ligações moleculares Átomos e Moléculas Energia do ion H 2 + A molécula de hidrogênio Ligações moleculares Uma molécula é formada por um conjunto de átomos que interagem formando um sistema com energia
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White
 QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
Introdução. O spin é uma propriedade das partículas elementares, eminentemente quântica, sem equivalente no mundo clássico.
 Ressonância de Spin Introdução O spin é uma propriedade das partículas elementares, eminentemente quântica, sem equivalente no mundo clássico. Nos próximos slides apresentaremos, brevemente, alguns aspectos
Ressonância de Spin Introdução O spin é uma propriedade das partículas elementares, eminentemente quântica, sem equivalente no mundo clássico. Nos próximos slides apresentaremos, brevemente, alguns aspectos
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
Fundamentos de Física Capítulo 39 Mais Ondas de Matéria Questões Múltipla escolha cap. 39 Fundamentos de Física Halliday Resnick Walker 1) Qual das
 Fundamentos de Física Capítulo 39 Mais Ondas de Matéria Questões Múltipla escolha cap. 39 Fundamentos de Física Halliday Resnick Walker 1) Qual das frases abaixo descreve corretamente a menor energia possível
Fundamentos de Física Capítulo 39 Mais Ondas de Matéria Questões Múltipla escolha cap. 39 Fundamentos de Física Halliday Resnick Walker 1) Qual das frases abaixo descreve corretamente a menor energia possível
TEORIAS ATÔMICAS. Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807)
 TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
Física Moderna II Aula 03. Marcelo G Munhoz Pelletron, sala 245, ramal 6940
 Física Moderna II Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br Schroedinger X Bohr Qual a vantagem da teoria de Schroedinger sobre a teoria de Bohr do ponto de vista da observação
Física Moderna II Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br Schroedinger X Bohr Qual a vantagem da teoria de Schroedinger sobre a teoria de Bohr do ponto de vista da observação
Elétrons como ondas? Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química
 OS ELÉTRONS O MODELO DA MECÂNICA QUÂNTICA E AS ENERGIAS ELETRÔNICAS Modelo atual se baseia na MECÂNICA QUÂNTICA Considera os conceitos da quantização da energia eletrônica (Bohr), fornecendo uma explicação
OS ELÉTRONS O MODELO DA MECÂNICA QUÂNTICA E AS ENERGIAS ELETRÔNICAS Modelo atual se baseia na MECÂNICA QUÂNTICA Considera os conceitos da quantização da energia eletrônica (Bohr), fornecendo uma explicação
Professor: André Luiz de Oliveira. PLANO DE ENSINO-Disponível em:
 Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas Departamento de Física PLANO DE ENSINO-Disponível em: http://www.joinville.udesc.br/portal/professores/andre 1. Identificação Curso:
Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas Departamento de Física PLANO DE ENSINO-Disponível em: http://www.joinville.udesc.br/portal/professores/andre 1. Identificação Curso:
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/2 e de Dois Níveis
 Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE FÍSICA - DFIS PLANO DE ENSINO
 DEPARTAMENTO: Física PLANO DE ENSINO DISCIPLINA: Física Moderna I CARGA HORÁRIA: 72 horas-aula SIGLA: FMO1001 Pré-requisito: FGE4001 CURSO: Licenciatura em Física SEMESTRE/ANO: 02/2014 EMENTA: História
DEPARTAMENTO: Física PLANO DE ENSINO DISCIPLINA: Física Moderna I CARGA HORÁRIA: 72 horas-aula SIGLA: FMO1001 Pré-requisito: FGE4001 CURSO: Licenciatura em Física SEMESTRE/ANO: 02/2014 EMENTA: História
Aula anterior. Equação de Schrödinger a 3 dimensões. d x 2m - E -U. 2m - E -U x, y, z. x y z x py pz cin cin. E E ( x, y,z ) - 2m 2m x y z
 6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
QFL 2144 Parte 3A: Ressonância magnética nuclear
 QFL 2144 Parte 3A: Ressonância magnética nuclear Espectroscopia de RMN: espectroscopia associada com a mudança de estado energético de núcleos atômicos na presença de um campo magnético. Elementos básicos
QFL 2144 Parte 3A: Ressonância magnética nuclear Espectroscopia de RMN: espectroscopia associada com a mudança de estado energético de núcleos atômicos na presença de um campo magnético. Elementos básicos
Revisão das observações experimentais, modelo de Bohr e Princípios da Mecânica Quântica by Pearson Education. Capítulo 06
 Revisão das observações experimentais, modelo de Bohr e Princípios da Mecânica Quântica Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com
Revisão das observações experimentais, modelo de Bohr e Princípios da Mecânica Quântica Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento angular bem definido
 ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
Capítulo 40: Tudo sobre os Átomos
 Capítulo 40: Tudo sobre os Átomos Sumário Algumas Propriedades dos Átomos O Spin do Elétron Momento Ângular e Momento Magnético O experimento destern-gerlach Resonância Magnética Princípio da Exclusão
Capítulo 40: Tudo sobre os Átomos Sumário Algumas Propriedades dos Átomos O Spin do Elétron Momento Ângular e Momento Magnético O experimento destern-gerlach Resonância Magnética Princípio da Exclusão
3) Quais são os valores possíveis do número quântico magnético de spin? a) -1,- ½,0, ½,1 b) 0 e + ½ c) 1, 0 e +1 d) 0, 1, 2, 3,...
 Fundamentos de Física Capítulo 40 Tudo sobre átomos. Questões Múltipla escolha cap. 40 Fundamentos de Física Halliday Resnick Walker 1) Qual das opções abaixo não é uma propriedade dos átomos? a) Os átomos
Fundamentos de Física Capítulo 40 Tudo sobre átomos. Questões Múltipla escolha cap. 40 Fundamentos de Física Halliday Resnick Walker 1) Qual das opções abaixo não é uma propriedade dos átomos? a) Os átomos
QUÍMICA I. Teoria atômica Capítulo 6. Aula 2
 QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
NÚMEROS QUÂNTICOS. As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons.
 NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
1) A ESTRUTURA DOS ÁTOMOS
 A ESTRUTURA DOS ÁTOMOS.. Estrutura Atômica A matéria seja no estado líquido sólido ou gasoso é constituída por átomos. Os átomos são constituídos por partículas elementares: os prótons os nêutrons e os
A ESTRUTURA DOS ÁTOMOS.. Estrutura Atômica A matéria seja no estado líquido sólido ou gasoso é constituída por átomos. Os átomos são constituídos por partículas elementares: os prótons os nêutrons e os
harmônicos esféricos Os harmônicos esféricos são simultaneamente autofunções dos operadores
 A eq. de Schrödinger em 3D: Independente do tempo: Separação de variáveis: h m v Ψ + V ( r ) Ψ = h v ψ + V ( r ) ψ = m Ψ ih t Eψ ψ ( r, θ, ϕ) = R( r) Θ( θ ) Φ( ϕ) R n ( r) ; Θ ( θ ) ; Φ ( ϕ) Ylm l ( θ,
A eq. de Schrödinger em 3D: Independente do tempo: Separação de variáveis: h m v Ψ + V ( r ) Ψ = h v ψ + V ( r ) ψ = m Ψ ih t Eψ ψ ( r, θ, ϕ) = R( r) Θ( θ ) Φ( ϕ) R n ( r) ; Θ ( θ ) ; Φ ( ϕ) Ylm l ( θ,
LCE0143 Química Geral. Estrutura Atômica. Wanessa Melchert Mattos.
 LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
Aula 17 Tudo sobre os Átomos
 Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
ÁTOMOS MULTIELETRÔNICOS. QFL-4010 Prof. Gianluca C. Azzellini
 ÁTOMOS MULTIELETRÔNICOS Número Quântico de Spin (m s ) m s = Representa o sentido de rotação do elétron no próprio eixo. m s = +1/2 e 1/2 Experimento Stern-Gerlach Vapor de átomos metálicos Números Quânticos
ÁTOMOS MULTIELETRÔNICOS Número Quântico de Spin (m s ) m s = Representa o sentido de rotação do elétron no próprio eixo. m s = +1/2 e 1/2 Experimento Stern-Gerlach Vapor de átomos metálicos Números Quânticos
Estrutura atômica. Modelo quântico do átomo
 Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
PROPRIEDADES ONDULATÓRIAS DO ELÉTRON
 MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
N P P N. Ciências de Materiais I Prof. Nilson C. Cruz. Aula 2 Ligação Química. Átomos. Diferença entre materiais = Diferença entre arranjos atômicos e
 Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Fundamentos de Química Quântica
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Aula 3 Estrutura Atômica cont
 Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Problemas de Duas Partículas
 Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
A Estrutura Eletrônica dos Átomos. Prof. Fernando R. Xavier
 A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
Tubos de Crookes e a descoberta do elétron
 Tubos de Crookes e a descoberta do elétron (A) Efeito de um obstáculo no caminho dos raios catódicos. Raios Catódicos High voltage source of high voltage shadow Resultados independem do gás usado para
Tubos de Crookes e a descoberta do elétron (A) Efeito de um obstáculo no caminho dos raios catódicos. Raios Catódicos High voltage source of high voltage shadow Resultados independem do gás usado para
FF-296: Teoria do Funcional da Densidade I. Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Problema de 2 elétrons Férmions Hartree-Fock Troca
FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Problema de 2 elétrons Férmions Hartree-Fock Troca
FF-296: Teoria do Funcional da Densidade I. Ronaldo Rodrigues Pela
 FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos O problema de 1 elétron O princípio variacional Função de onda tentativa Átomo de H unidimensional Íon H2 + unidimensional Equação
FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos O problema de 1 elétron O princípio variacional Função de onda tentativa Átomo de H unidimensional Íon H2 + unidimensional Equação
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 Tabela Periódica dos elementos 2 8 8 Alcalinos, um elétron livre na camada
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 Tabela Periódica dos elementos 2 8 8 Alcalinos, um elétron livre na camada
Atomística. Prof. Fernando R. Xavier
 Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
CF100 - Física Moderna II. 2º Semestre de 2018 Prof. Ismael André Heisler Aula 10/08/2018
 CF100 - Física Moderna II 2º Semestre de 2018 Prof. Ismael André Heisler Aula 10/08/2018 1 Átomos Multieletrônicos 2 Partículas Idênticas 3 Na física quântica, o princípio da incerteza impede a observação
CF100 - Física Moderna II 2º Semestre de 2018 Prof. Ismael André Heisler Aula 10/08/2018 1 Átomos Multieletrônicos 2 Partículas Idênticas 3 Na física quântica, o princípio da incerteza impede a observação
O átomo de Rutherford
 O átomo de Rutherford Elétrons orbitando o núcleo F Elétrica F Centrifúga Quando uma carga elétrica muda de velocidade ou direção, ela deve irradiar energia. Radiação Eletromagnética É o produto de campos
O átomo de Rutherford Elétrons orbitando o núcleo F Elétrica F Centrifúga Quando uma carga elétrica muda de velocidade ou direção, ela deve irradiar energia. Radiação Eletromagnética É o produto de campos
Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA. Eliana Midori Sussuchi Danilo Oliveira Santos
 Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA META Aplicar os conceitos de mecânica quântica aos orbitais atômicos; Descrever a distribuição dos elétrons nos átomos. OBJETIVOS Ao final desta aula,
Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA META Aplicar os conceitos de mecânica quântica aos orbitais atômicos; Descrever a distribuição dos elétrons nos átomos. OBJETIVOS Ao final desta aula,
Estrutura da Matéria Profª Fanny Nascimento Costa
 Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
Introdução à Física Atômica e Molecular
 4005 Introdução à Física Atômica e Molecular Átomos Multieletrônicos Referências: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos. P. Atkins e R. Friedman, Molecular Quantum Mechanics,
4005 Introdução à Física Atômica e Molecular Átomos Multieletrônicos Referências: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos. P. Atkins e R. Friedman, Molecular Quantum Mechanics,
-> Foi laureado com o Nobel de Física e um dos fundadores da Mecânica Quântica.
 Werner Karl Heisenberg (5 de Dezembro de 1901, Würzburg 1 de Fevereiro de 1976, Munique, Alemanha). -> foi um físico alemão. -> Foi laureado com o Nobel de Física e um dos fundadores da Mecânica Quântica.
Werner Karl Heisenberg (5 de Dezembro de 1901, Würzburg 1 de Fevereiro de 1976, Munique, Alemanha). -> foi um físico alemão. -> Foi laureado com o Nobel de Física e um dos fundadores da Mecânica Quântica.
ESTRUTURA ELETRÔNICA DOS ÁTOMOS
 ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
UNIVERSIDADE DE SÃO PAULO
 UNIVERSIDADE DE SÃO PAULO - Instituto de Química - Estrutura Atômica As propriedades ondulatórias do elétron Hermi F. Brito hefbrito@iq.usp.br QFL 1101 Química Geral I, -03-2017 Dualidade onda-partícula
UNIVERSIDADE DE SÃO PAULO - Instituto de Química - Estrutura Atômica As propriedades ondulatórias do elétron Hermi F. Brito hefbrito@iq.usp.br QFL 1101 Química Geral I, -03-2017 Dualidade onda-partícula
Física Quântica. Momentos de Dipolo Magnético e Spin. Prof. Dr. Walter F. de Azevedo Jr Dr. Walter F. de Azevedo Jr.
 2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momentos de Dipolo Magnético e Spin Prof. Dr. Walter F. de Azevedo Jr. 1 Momento de Dipolo Magnético Orbital Consideremos uma carga elétrica (e) que se
2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momentos de Dipolo Magnético e Spin Prof. Dr. Walter F. de Azevedo Jr. 1 Momento de Dipolo Magnético Orbital Consideremos uma carga elétrica (e) que se
Spin e Princípio de exclusão de Pauli
 10 AULA Spin e Princípio de exclusão de Pauli Spin e Princípio de exclusão de Pauli METAS: Introduzir o spin. Introduzir o formalismo utilizado na descrição de spin 1/2. Introduzir o Princípio de exclusão.
10 AULA Spin e Princípio de exclusão de Pauli Spin e Princípio de exclusão de Pauli METAS: Introduzir o spin. Introduzir o formalismo utilizado na descrição de spin 1/2. Introduzir o Princípio de exclusão.
Física Quântica. Momento de Dipolo Magnético. Prof. Dr. Walter F. de Azevedo Jr Dr. Walter F. de Azevedo Jr.
 2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momento de Dipolo Magnético Prof. Dr. Walter F. de Azevedo Jr. 1 Força de Lorentz Uma partícula deslocando numa região sujeita a um campo elétrico (E)
2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momento de Dipolo Magnético Prof. Dr. Walter F. de Azevedo Jr. 1 Força de Lorentz Uma partícula deslocando numa região sujeita a um campo elétrico (E)
5.1: Aplicação da Equação de Schrödinger ao átomo de Hidrogênio
 http://www.if.ufrgs.br/~marcia/textos.html UNIDADE Aula 5 Átomo de Hidrogênio * * Tradução e adaptação livre das aulas do Professor Rick Trebino em: www.physics.gatech.edu/frog 5.1 Aplicação da Equação
http://www.if.ufrgs.br/~marcia/textos.html UNIDADE Aula 5 Átomo de Hidrogênio * * Tradução e adaptação livre das aulas do Professor Rick Trebino em: www.physics.gatech.edu/frog 5.1 Aplicação da Equação
ONDAS ELETROMAGNÉTICAS ÁTOMO DE BOHR. QFL-4010 Prof. Gianluca C. Azzellini
 ONDAS ELETROMAGNÉTICAS ÁTOMO DE BOHR Ondas Eletromagnéticas ONDAS ELETROMAGNÉTICAS ASPECTOS GERAIS A= amplitude (m) λ= comprimento de onda (m) ν= frequência (Hz= s -1 ) c= velocidade da luz=,998x10 8
ONDAS ELETROMAGNÉTICAS ÁTOMO DE BOHR Ondas Eletromagnéticas ONDAS ELETROMAGNÉTICAS ASPECTOS GERAIS A= amplitude (m) λ= comprimento de onda (m) ν= frequência (Hz= s -1 ) c= velocidade da luz=,998x10 8
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 Resultados da Teoria de Hartree As autofunções obtidas pela teoria de Hartree
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 Resultados da Teoria de Hartree As autofunções obtidas pela teoria de Hartree
ESTRUTURA ATÔMICA. Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14
 ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
ESTRUTURA ATÔMICA Prof. Dr. Cristiano Torres Miranda Disciplina: Química Geral I QM81B Turmas Q13 e Q14 TEORIA ATÔMICA DA MATÉRIA Demócrito e Leucipo (discípulo) (460 370 a.c.) Aristóteles (384 a.c. 322
Escola Politécnica FAP GABARITO DA P3 25 de novembro de 2008
 P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
1 O Átomo de Hidrogênio
 O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
A Teoria de Bohr foi aceite com entusiasmo, porque pela primeira vez se conseguiu: Interpretar qualitativamente os espectros atómicos em geral;
 Sumário Das Estrelas ao átomo Unidade temática 1 Como se carateriza o modelo O modelo quântico: Números quânticos. Energia das orbitais. Princípios e regras para a distribuição dos eletrões pelas orbitais.
Sumário Das Estrelas ao átomo Unidade temática 1 Como se carateriza o modelo O modelo quântico: Números quânticos. Energia das orbitais. Princípios e regras para a distribuição dos eletrões pelas orbitais.
08/05/2013. QFL ª Parte: Ressonância magnética nuclear. Algumas aplicações de RMN
 QFL 144 3ª Parte: Ressonância nética nuclear Espectroscopia de RM: espectroscopia associada a interação, na presença de um campo nético, entre um campo eletronético de radiofrequência (RF) e núcleos atômicos.
QFL 144 3ª Parte: Ressonância nética nuclear Espectroscopia de RM: espectroscopia associada a interação, na presença de um campo nético, entre um campo eletronético de radiofrequência (RF) e núcleos atômicos.
Física Moderna II Aula 05. Marcelo G Munhoz Pelletron, sala 245, ramal 6940
 Física Moderna II Aula 05 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br 1 Átomos multi-eletrônicos A solução da equação de Schroedinger para um átomo com muitos elétrons é bastante
Física Moderna II Aula 05 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br 1 Átomos multi-eletrônicos A solução da equação de Schroedinger para um átomo com muitos elétrons é bastante
Física Moderna II Aula 07
 Universidade de São Paulo Instituto de Física 1 º Semestre de 015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 0 rizzutto@if.usp.br Física Moderna II Aula 07 Monitor: Gabriel M. de Souza Santos Sala
Universidade de São Paulo Instituto de Física 1 º Semestre de 015 Profa. Márcia de Almeida Rizzutto Oscar Sala sala 0 rizzutto@if.usp.br Física Moderna II Aula 07 Monitor: Gabriel M. de Souza Santos Sala
O Método de Hartree-Fock
 O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
Comportamento ondulatório da matéria
 Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda. Af função de onda fornece o
 Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
5. Modelo atômico de Bohr
 5. Modelo atômico de Bohr Sumário Espectros atômicos Modelo de Bohr para o átomo de hidrogênio Níveis de energia e raias espectrais Experiência de Franck-Hertz O princípio da correspondência Correção do
5. Modelo atômico de Bohr Sumário Espectros atômicos Modelo de Bohr para o átomo de hidrogênio Níveis de energia e raias espectrais Experiência de Franck-Hertz O princípio da correspondência Correção do
ATOMÍSTICA PROF. ADRIANO ALVES
 ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
Campo na matéria II. 1 Resumem da aula anterior. Aula de março de campo magnetizante
 Campo na matéria II Aula 4 3 de março de 11 1 Resumem da aula anterior A fim de explicar o magnetismo observado na matéria Ampère propões a existência de corrente internas, hoje conhecidas como correntes
Campo na matéria II Aula 4 3 de março de 11 1 Resumem da aula anterior A fim de explicar o magnetismo observado na matéria Ampère propões a existência de corrente internas, hoje conhecidas como correntes
Estrutura da Matéria BIK Prof. Fernando Carlos Giacomelli (Turma A)
 Estrutura da Matéria BIK0102-15 Prof. Fernando Carlos Giacomelli (Turma A) fernando.giacomelli@ufabc.edu.br Bloco A - Sala 613-3 Torre 3 - CCNH - Santo André Dualidade Onda-Partícula: Descrição Clássica
Estrutura da Matéria BIK0102-15 Prof. Fernando Carlos Giacomelli (Turma A) fernando.giacomelli@ufabc.edu.br Bloco A - Sala 613-3 Torre 3 - CCNH - Santo André Dualidade Onda-Partícula: Descrição Clássica
Escola Politécnica FAP GABARITO DA P2 24 de outubro de 2006
 P2 Física IV Escola Politécnica - 2006 FAP 2204 - GABARITO DA P2 24 de outubro de 2006 Questão 1 A. O comprimento de onda de corte para ejetar elétron da superfície do metal lantânio é = 3760 Å. (a) (0,5
P2 Física IV Escola Politécnica - 2006 FAP 2204 - GABARITO DA P2 24 de outubro de 2006 Questão 1 A. O comprimento de onda de corte para ejetar elétron da superfície do metal lantânio é = 3760 Å. (a) (0,5
Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui
 FÍSICA MODERNA Aula 6a: Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui Tema 5: Física dos átomos e moléculas 5.1. Átomo de hidrogénio;
FÍSICA MODERNA Aula 6a: Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui Tema 5: Física dos átomos e moléculas 5.1. Átomo de hidrogénio;
Motivação 10/29/2018. Física: compreender as propriedades dos átomos (últimos ~ 100 anos) Experimentos mais precisos :
 Cap. 40 Tudo sobre átomos Algumas propriedades dos átomos: Agrupamentos; Emissão e absorção de luz; Momento angular e magnético. Experimento de Einstein de Haas: Momento angular e magnético ORBITAL. Experimento
Cap. 40 Tudo sobre átomos Algumas propriedades dos átomos: Agrupamentos; Emissão e absorção de luz; Momento angular e magnético. Experimento de Einstein de Haas: Momento angular e magnético ORBITAL. Experimento
Estrutura dos Materiais. e Engenharia dos Materiais Prof. Douglas Gouvêa
 Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
Ligações Químicas e Estrutura dos Materiais PMT 5783 - Fundamentos de Ciência e Engenharia dos Materiais Prof. Douglas Gouvêa Objetivos Descrever a estrutura atômica e suas conseqüências no tipo de ligação
Fundamentos de Química 1ª parte
 Fundamentos de Química 1ª parte Tabela Periódica dos Elementos Metais Metalóides Não-Metais Modelo do Átomo de Bohr (1913) 1. Os e apenas podem ter valores específicos (quantizados) de energia. Fotão 2.
Fundamentos de Química 1ª parte Tabela Periódica dos Elementos Metais Metalóides Não-Metais Modelo do Átomo de Bohr (1913) 1. Os e apenas podem ter valores específicos (quantizados) de energia. Fotão 2.
Como Entender a Física Quântica em 8 Passos! Passos
 Como Entender a Física Quântica em 8 Passos! A física quântica (também chamada de teoria quântica ou mecânica quântica) é um ramo da física que permite uma descrição do comportamento e interação da matéria
Como Entender a Física Quântica em 8 Passos! A física quântica (também chamada de teoria quântica ou mecânica quântica) é um ramo da física que permite uma descrição do comportamento e interação da matéria
h (1 cos θ) onde, m e é a massa do elétron, θ é o ângulo pelo qual a direção do fóton muda λ 1 é o comprimento de onda do fóton antes do espalhamento,
 Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 09/06/2014 Nome do Candidato: Nível: Mestrado Doutorado 1. A função de
Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 09/06/2014 Nome do Candidato: Nível: Mestrado Doutorado 1. A função de
no âmbito da história da Física Moderna e suas atuais aplicaçõ
 A Ressonância ncia Magnética Nuclear no âmbito da história da Física Moderna e suas atuais aplicaçõ ções Tito J. Bonagamba LEAR / IFSC / USP Ressonância Magnética Nuclear (RMN) História Ressonância Magnética
A Ressonância ncia Magnética Nuclear no âmbito da história da Física Moderna e suas atuais aplicaçõ ções Tito J. Bonagamba LEAR / IFSC / USP Ressonância Magnética Nuclear (RMN) História Ressonância Magnética
Universidade Federal do Tocantins
 Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
Equação de Schrödinger em 3D
 Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Átomos polieletrónicos
 Átomos polieletrónicos Química Teórica e Estrutural P.J.S.B. Caridade & U. Miranda 2/12/2013 5/11/2013, Aula 8 Química Teórica & Estrutural (2013) Caridade & Ulises 1 Átomo de hidrogénio O Hamiltoniano
Átomos polieletrónicos Química Teórica e Estrutural P.J.S.B. Caridade & U. Miranda 2/12/2013 5/11/2013, Aula 8 Química Teórica & Estrutural (2013) Caridade & Ulises 1 Átomo de hidrogénio O Hamiltoniano
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 12 ESTATÍSTICA QUÂNTICA Primeira Edição junho de 2005 CAPÍTULO 12 ESTATÍSTICA QUÂNTICA ÍNDICE 12-1- Introdução 12.2- Indistinguibilidade
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 12 ESTATÍSTICA QUÂNTICA Primeira Edição junho de 2005 CAPÍTULO 12 ESTATÍSTICA QUÂNTICA ÍNDICE 12-1- Introdução 12.2- Indistinguibilidade
Instituto de Física USP. Física V - Aula 24. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 24 Professora: Mazé Bechara Aula 24 Princípio de correspondênciam Experimento de Franck e Hertz, e regra de quantização de Wilson-Sommerfeld 1. O princípio de correspondência
Instituto de Física USP Física V - Aula 24 Professora: Mazé Bechara Aula 24 Princípio de correspondênciam Experimento de Franck e Hertz, e regra de quantização de Wilson-Sommerfeld 1. O princípio de correspondência
Estrutura Atômica. Clique para editar o estilo do subtítulo mestre
 Estrutura Atômica Clique para editar o estilo do subtítulo mestre Evolução dos Modelos Atômicos 1º) Demócrito e Leucipo (400 a 500 a.c) -filósofos gregos -átomo indivisível. 2º) Modelo Atômico de Dalton
Estrutura Atômica Clique para editar o estilo do subtítulo mestre Evolução dos Modelos Atômicos 1º) Demócrito e Leucipo (400 a 500 a.c) -filósofos gregos -átomo indivisível. 2º) Modelo Atômico de Dalton
Física IV Escola Politécnica GABARITO DA P3 25 de novembro de 2014
 Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
