UNIVERSIDADE FEDERAL DE PELOTAS
|
|
|
- Isabel Farinha Brandt
- 6 Há anos
- Visualizações:
Transcrição
1 1 UNIVERSIDADE FEDERAL DE PELOTAS Programa de Pós-Graduação em Biotecnologia Dissertação Produção, caracterização e aplicação de anticorpos monoclonais contra o vírus da Bronquite Infecciosa das Galinhas Neida Lucia Conrad Pelotas, 2013
2 2 NEIDA LUCIA CONRAD Produção, caracterização e aplicação de anticorpos monoclonais contra o vírus da Bronquite Infecciosa das Galinhas Dissertação apresentada ao Programa de Pós-Graduação em Biotecnologia da Universidade Federal de Pelotas, como requisito parcial à obtenção do título de Mestre em Ciências (área do conhecimento: Imunologia). Orientadora: Ângela Nunes Moreira Co-orientador: Fabricio Rochedo Conceição Pelotas, 2013
3 3 Dados de catalogação na fonte: Ubirajara Buddin Cruz CRB-10/901 Biblioteca de Ciência & Tecnologia - UFPel
4 4 Banca examinadora: Profª. Drª. Claudia Hartleben, Universidade Federal de Pelotas Prof. Dr. Marcelo de Lima, Fundação Universidade Federal de Pelotas Dr. Paulo Augusto Esteves, Embrapa Suínos e Aves Profª. Drª. Ângela Nunes Moreira, Universidade Federal de Pelotas
5 5 Agradecimentos A Universidade Federal de Pelotas pela oportunidade de realização do curso de Pós-Graduação em Biotecnologia. A Fundação Coordenação de Aperfeicoamento de Pessoal de Nivel Superior (CAPES) pela concessão da bolsa de estudos. Aos meus pais, Ana e Valdir Conrad, pelo incalculável apoio e investimento de uma vida inteira, por vezes abdicando de suas vontades em detrimento dos meus objetivos, obrigado pelo incentivo e amor incondicional. Ao meu primeiro orientador, professor José Antônio Guimarães Aleixo, pela oportunidade de estágio, pela confiança e ensinamentos. À minha orientadora Ângela Moreira e ao Prof. Fabrício Conceição pela oportunidade, ensinamentos e amizade. Ao doutor, Marcelo Mendonça, pelos incontáveis ensinamentos e dicas, pela paciência e amizade. Aos colegas e amigos do Laboratório de Imunologia Aplicada, Carol, Clóvis, Rodrigo, Carlos, Gustavo, Marcelle, Suely, Giana e a toda família do Laboratório de Imunologia Aplicada pela convivência, pelos momentos de descontração que tornaram esta caminhada mais agradável. Aos demais colegas, professores e amigos da Biotecnologia obrigada pelo convívio, apoio e amizade. E a todos que direta ou indiretamente contribuíram de alguma forma na minha formação e/ou realização deste trabalho. Muito obrigada!
6 6 RESUMO CONRAD, NEIDA LUCIA. Produção, caracterização e aplicação de anticorpos monoclonais contra o vírus da Bronquite Infecciosa das Galinhas. 2013, 78 f. Dissertação (Mestrado) Programa de Pós Graduação em Biotecnologia.Universidade Federal de Pelotas, Pelotas. A bronquite infecciosa das galinhas (BI) é uma doença aguda, altamente contagiosa, causada por um Coronavírus que infecta principalmente células dos aparelhos respiratório e genito-urinário das galinhas. A importância econômica dessa doença decorre da diminuição na produção e qualidade interna e externa dos ovos, da redução da eclodibilidade, da diminuição da eficiência alimentar e do ganho de peso e do aumento da mortalidade e da condenação de carcaças ao abate, além dos gastos com medicamentos para debelar infecções bacterianas secundárias. A confirmação do diagnóstico de BI é baseada no isolamento viral, em conjunto com a sorologia. O uso de anticorpos monoclonais (AcMs) tem colaborado e facilitado o diagnóstico desse tipo de enfermidade, porém seu uso ainda é limitado, pois os AcMs utilizados são importados, elevando o custo de tais metodologias. Este trabalho relata a produção, caracterização e aplicação de AcMs contra o vírus da bronquite infecciosa das galinhas (VBI). Para a produção dos AcMs, camundongos Balb/c foram imunizados intraperitonealmente com o VBI clássico (M41) local ou com o variante. Foram gerados dois hibridomas secretores de AcMs anti-vbi do isotipo IgM a partir da fusão entre os linfócitos B de um camundongo imunizado com o VBI variante e células de mieloma. Foi observado, na caracterização por ELISA indireto e Western blot, que os AcMs reconhecem o VBI clássico e variante, sendo as reações com o VBI variante mais intensas. O AcM 2G4 parece ser específico para a proteína S 1. A aplicabilidade dos AcMs foi avaliada através da técnica de imuno-histoquímica em tecidos de aves inoculadas experimentalmente com o VBI clássico. Os AcMs anti-vbi apresentaram o mesmo padrão de marcação que o AcM utilizado como controle positivo, ou seja, marcaram predominantemente células inflamatórias. Este resultado pode ser explicado pelo fato de que, em casos mais severos da infecção por VBI, o antígeno pode ser localizado também em células inflamatórias. Concluiu-se que os AcMs obtidos apresentam potencial para uso no imunodiagnóstico para BI. Palavras chave: imunodiagnóstico. imuno-histoquímica. VBI clássico. VBI variante. hibridoma. Coronavírus.
7 7 ABSTRACT CONRAD, NEIDA LUCIA. Production, characterization and application of monoclonal antibodies against the virus of infectious bronchitis. 2013, 78 f. Dissertação (Mestrado) Programa de Pós-Graduação em Biotecnologia. Universidade Federal de Pelotas, Pelotas. The infectious bronchitis (IB) is an acute and highly contagious disease caused by a coronavirus that infects mainly cells of the respiratory and genitourinary of chicken. The economic importance of this disease results from decreased production, such as internal and external quality of eggs, reduced hatchability, feed efficiency and weight gain, increased mortality, condemnation of carcasses at slaughter, and also with drugs spending to suppress secondary bacterial infections. The diagnosis of IB is based on virus isolation, together with serology. The use of monoclonal antibodies (MAbs) has been collaborated to diagnosis of this type of disease, but their use are still limited because the MAbs used are imported, increasing the cost of such methodologies. This work reports the production, characterization and application of MAbs against the virus of infectious bronchitis (IBV). For the production of MAbs, Balb/c mice were immunized intraperitoneally with classic IBV (M41) or variant IBV. We generated two hybridomas secreting MAbs anti-ibv (IgM isotype) from the fusion of B-lymphocytes from a mouse immunized with the variant IBV and myeloma cells. Following the characterization by ELISA and Western blot, it was observed that MAbs recognize the IBV classic and variant, showing more intense reactions with IBV variant. The AcM 2 G4 seems to be specific for protein S1. The applicability of the MAbs was assessed using the immunohistochemistry technique on histological tissues of birds inoculated experimentally with classic IBV. These MAbs anti-ibv had the same pattern of label of the MAb used as positive control, labeling predominantly inflammatory cells. This result can be explained by the fact that in severe cases of infection with IBV, the antigen may be located also in inflammatory cells. It was concluded that the MAbs obtained have potential for use in immunodiagnostic for IB. Keywords: immunodiagnosis. immunohistochemistry. classic VBI. variant VBI hybridoma. Coronavirus.
8 8 Figura 1. Figura 2. Figura 3. Figura 4. Figura 5. Figura 6. Figura 7. Figura 8. LISTA DE FIGURAS SDS PAGE 10 % para avaliar a qualidade e pureza das amostras virais utilizadas na imunização dos camundongos para produção de AcMs anti-vbi... Western blot para avaliar a qualidade e pureza das amostras virais utilizadas na imunização dos camundongos para produção de AcMs anti-vbi utilizando soro de aves positivas para o VBI... Determinação da concentração ideal de antígeno para o ELISA indireto, utilizando 500, 250, 125 e 62,5 ng/cavidade dos VBI clássico ou variante e os soros coletados de um animal imunizado com o VBI clássico e de outro imunizado com o VBI variante, diluídos 1: Determinação da diluição ideal dos soros dos animais imunizados (diluídos em base dois de 1:100 até 1: em PBS-T) para ser utilizada como controle positivo no ELISA indireto, utilizando 250 ng dos VBI clássico ou variante como antígeno, por cavidade.... SDS PAGE 12% para a determinação do isotipo dos AcMs anti-vbi obtidos a partir da fusão celular entre os linfócitos B do camundongo imunizado com o VBI variante e células de mieloma.... Reatividade dos AcMs anti-vbi (2G4 e 5A11) frente a diferentes vírus (VBI variante e clássico M41, vírus da Bouba das aves e de Newcastle) por ELISA indireto.... Perfil eletroforético e reatividade dos AcMs anti-vbi (2G4 e 5A11) frente a diferentes vírus (VBI variante e clássico M41, vírus da Bouba das aves e de Newcastle) por Western blot.... Imuno-histoquímica utilizando os AcMs 2G4 e 5 A11 (diluídos 1:50) em tecidos de aves infectadas artificialmente via ocular com o VBI clássico (M41) e coletados 4 dias após a infecção
9 9 SUMÁRIO 1 Introdução Revisão da Literatura Materiais e Métodos Resultados e Discussão Conclusões Referências... 53
10 10 1 INTRODUÇÃO A avicultura é um dos setores mais importantes do agronegócio brasileiro e também o que mais cresceu nos últimos anos. O Brasil tem conquistado um espaço significativo na produção mundial, aumentou cerca de 1000% entre os anos de 1961 e 2003, passando de 1,4% para 10,5% da produção mundial de carne de frango (GIROTTO, 2004). Por se tratar de um amplo mercado em expansão, a avicultura vem crescendo também em âmbito de tecnologias, com o surgimento de novos fármacos e vacinas desenvolvidos com o objetivo de evitar a disseminação de enfermidades entre os animais alojados. Dentre as doenças que acometem as aves e causam grandes prejuízos econômicos aos produtores, está a bronquite infecciosa das galinhas (BI). A BI é uma doença aguda, altamente contagiosa, causada por um vírus do gênero Coronavírus que acomete a espécie Gallus gallus domesticus (KING; CAVANAGH, 1991; SANTOS et al., 2005). A BI foi descrita pela primeira vez por Shalk e Hawn (1931), na Cidade de Dakota do Norte, nos Estados Unidos, e o agente da BI foi denominado de vírus da bronquite infecciosa (VBI), por Beach e Schalm, em No Brasil, a BI foi diagnosticada pela primeira vez no ano de 1957, no Estado de Minas Gerais (HIPÓLITO; SILVA; HSIUNG, 1979). No início da década de 1960, a BI já havia sido notificada em quase todo o mundo (MUNEER et al., 1988). O genoma do VBI consiste de uma fita única de RNA de sentido positivo e contém cerca de nucleotídeos (CAVANAGH, 2007). O genoma viral é envolvido basicamente por três proteínas: a nucleoproteína (N, uma proteína fosforilada do nucleocapsídeo interno), e externamente, pelas glicoproteínas da matriz (M) e da espícula (S), sendo essa última composta por duas subunidades, S 1 e S 2. Existe ainda uma quarta proteína (E), que é associada ao envelope viral. (MARTINS, 1992; MURPHY et al.,1999; ROCHA, 2000; RESENDE, 2003, McKINLEY; HILT; JACKWOOD, 2008). O VBI infecta principalmente células dos aparelhos respiratórios e genitourinário das galinhas (KING; CAVANAGH, 1991; SANTOS; FARIA; RIBEIRO, 2005), resultando na redução do ganho de peso e da produção e qualidade dos ovos (ARIYOSHI et al., 2010). O VBI é primariamente epiteliotrópico, replicando-se nas células epiteliais, nas células secretoras de muco e nas células dos pulmões e dos
11 11 sacos aéreos. A replicação do vírus nos tecidos do trato respiratório causa sinais característicos, como dificuldades para respirar, tosse e descarga nasal. A infecção por VBI produz lesões características na traquéia, que é o órgão de eleição para sua multiplicação (KING; CAVANAGH, 1991), sendo por isso, considerada uma doença primária do aparelho respiratório (RESENDE, 2003). A BI está incluída na lista da Organização Mundial de Saúde Animal (OIE) e Organização para a Agricultura e Alimentação (FAO) como doença transmissível de notificação anual, que tem importância socioeconômica e implicações sanitárias, podendo trazer alguma repercussão a qualquer momento no comércio internacional de produtos e animais (OIE, 2008; OECD, 2011). A BI está amplamente disseminada entre as criações avícolas comerciais e é uma das enfermidades virais que mais têm causado perdas econômicas na avicultura brasileira e no mundo todo, devido à diminuição do crescimento dos animais, redução da qualidade e da produção de ovos, mortalidade, condenação ao abate e gastos com insumos, incluindo diagnóstico, vacinas e antimicrobianos, a fim de eliminar infecções bacterianas intercorrentes (CAVANAGH 2007; MENDONÇA et al., 2009) Portanto, a rápida detecção e identificação do patógeno viral são imprescindíveis para que medidas eficazes de controle sejam prontamente tomadas. Para tanto, é necessário que os métodos de diagnóstico empregados sejam sensíveis, específicos, rápidos e de baixo custo. O isolamento e a identificação do agente causal são necessários para o diagnóstico definitivo de BI. Os métodos de diagnóstico convencionais da BI são baseados no isolamento viral em ovos embrionados livres de patógenos específicos (Specific Pathogen Free, SPF) (GELB, 1989; OWEN et al., 1991) ou em culturas celulares (HOPKINS et al., 1974), seguidos da identificação antigênica dos vírus isolados. Três ou mais passagens em ovos embrionados são geralmente necessárias para o isolamento primário do VBI, o que torna tal procedimento oneroso e demorado. Além disso, somente estirpes adaptadas à passagem em ovos induzem características evidentes como nanismo e enrolamento embrionário e alguns isolados de campo do VBI não induzem lesões embrionárias específicas durante várias passagens (RAJ et al., 2004). Essa metodologia, além de ser extremamente trabalhosa, requer condições rígidas de biossegurança, em virtude da
12 12 virulência desse micro-organismo, bem como um longo tempo de análise (em média 7 a 10 dias) (GELB, 1989; OWEN et al., 1991). Na tentativa de buscar métodos mais rápidos para detecção deste patógeno, testes baseados em biologia molecular e ensaios sorológicos estão sendo aplicados. Dentre esses métodos destacam-se a Transcrição Reversa associada à Reação em Cadeia da Polimerase (RT-PCR), a análise de fragmentos genômicos gerados por enzimas de restrição (RFLP) e o seqüenciamento dos genes mais importantes desse patógeno viral (CAVANAGH; NAQI, 2003). E, entre as técnicas sorológicas, destacam-se as reações de imunofluorescência, imunodifusão em ágar gel, imunoperoxidase, inibição da hemaglutinação e os ensaios imunoenzimáticos (Enzyme-linked immunosorbent assay, ELISA) (DE WIT, 2000). O VBI também pode ser detectado diretamente em tecidos de aves infectadas por meio de técnicas de imuno-histoquímica (COLISSON et al., 1990; HANDBERG et al., 1999). A imuno-histoquímica, uma ferramenta útil para o diagnóstico da infecção por VBI, também possibilita estudos sobre a patogênese de diferentes estirpes de VBI. Através da técnica de imuno-histoquímica é possível investigar o tropismo tecidual de determinada cepa do VBI, a relação entre as lesões histopatológicas e a presença ou quantidade do vírus no tecido e acompanhar a migração do vírus durante a infecção (MONEIM et al., 2009; BENYEDA et al.,2010; BEZUIDENHOUT; MONDAL; BUCKLES, 2011). O teste de imuno-histoquímica e outros testes sorológicos utilizam anti-soros contendo anticorpos contra diferentes partes do vírus ou anticorpos monoclonais (AcMs) contra um ou mais epítopos (DE WIT, 2000). O uso de AcMs aumenta a confiabilidade destas metodologias, pois eles reconhecem um epítopo exclusivo do VBI. Além disso, AcMs apresentam outras vantagens, quando comparados com anticorpos policlonais, tais como maior especificidade, disponibilidade de quantidade ilimitada de anticorpos, uniformidade, necessidade de uma única padronização e estabilidade do hibridoma (CAMPBELL, 1991). Diversos grupos de pesquisa estão trabalhando na obtenção de AcMs, porém, devido a grande variabilidade genética entre os isolados de diferentes regiões, um anticorpo produzido contra o isolado de determinada região não apresenta a mesma sensibilidade em relação aos isolados de outras regiões (CAVANAGH; ELLIS; COOK, 1997; JONES, 2010; CHEN; WANG; CHENG, 2011). Além disso, a importação deste insumo, já que ainda não há um AcM específico
13 13 para IBV no país, torna tais metodologias dispendiosas e inacessíveis. Diante deste contexto, o objetivo deste trabalho foi produzir e caracterizar AcMs contra o VBI para sua utilização no imunodiagnóstico para esta enfermidade.
14 14 2 REVISÃO DA LITERATURA 2.1 Avicultura No cenário mundial, a carne de frango ocupa o segundo lugar no mercado de carnes (OECD, 2011). Segundo o Departamento de Agricultura dos Estados Unidos (USDA, 2012), a avicultura mundial produziu 81 milhões de toneladas de carne de frango em 2011, sendo o Brasil responsável por 16 % desta produção. No Brasil, até a década de 1960, a produção de carne de frango era realizada de forma artesanal e destinava-se apenas ao consumo próprio. A partir de meados dos anos 60, o setor passou a se desenvolver e ter importância econômica. O desenvolvimento da avicultura ocorreu através da implementação de um modelo de produção baseado em grandes produtores independentes e autônomos, em relação à indústria, e com o uso de mão de obra assalariada. Assim, iniciou-se no Estado de São Paulo, a fundamentação da avicultura nacional moderna. Nos anos 70, a avicultura brasileira teve um grande crescimento, devido à implantação do modelo de integração sudoeste catarinense, o qual introduziu um pacote tecnológico que envolveu o controle pela indústria do ciclo produtivo das aves, gerando crescimentos sucessivos da produtividade (TAVARES; RIBEIRO, 2007). As empresas passaram a controlar todo o processo produtivo (criação das matrizes, incubação dos ovos, produção da ração, o abate e a comercialização). Os pequenos e médios produtores detinham-se apenas a fase de engorda das aves, ainda sob recomendações técnicas das empresas (TAKAGI et al., 2002). Este sistema levou a uma expansão da avicultura no país, estendendo-a aos estados do Rio Grande do Sul e Paraná e, posteriormente, para Minas Gerais. A avicultura brasileira encontra-se em posição de destaque, sendo a maior exportadora de carnes de frango e a terceira maior produtora de frangos de corte (USDA, 2012). O avanço na produção de ovos é outro fator relevante, atendendo a toda demanda do mercado interno, com potencial para exportação (UBA, 2012). Entretanto, as infecções virais que acometem as aves, levam a enormes perdas econômicas na avicultura brasileira e no mundo todo, devido à diminuição do crescimento dos animais, redução da qualidade e da produção de ovos, mortalidade, condenação ao abate e gastos com insumos, incluindo diagnóstico, vacinas e antimicrobianos, a fim de eliminar infecções bacterianas intercorrentes.
15 15 Dentre os agentes com grande potencial de ocasionar as mais severas perdas, em termos de mortalidade, estão os causadores da doença de Gumboro, de Newcastle e da Bronquite Infecciosa das Galinhas (BI). E, dentre estas patologias, a BI possui maior importância econômica, em razão da sua ampla disseminação e dos enormes prejuízos que acarreta, alcançando a ordem de milhões de dólares anualmente (JONES, 2010). 2.2 Etiologia O vírus da bronquite infecciosa (VBI) pertence à família Coronaviridae, na ordem Nidovirales. A família Coronaviridae é dividida em duas subfamílias: Coronavirinae e Torovirinae). O VBI pertence à subfamília Coronavirinae e pode infectar diversas espécies animais, incluindo seres humanos, aves, bovinos, suínos, cães, gatos e roedores (PATTISON et al., 2008). Coronavirinae são divididos nos gêneros: Alphacoronavirus, Betacoronavirus e Gammacoronavirus. O VBI também é chamado de Coronavirus aviário, uma espécie do gênero Gammacoronavirus (CAVANAGH; GELB, 2008; CAVANAGH, 2007). O genoma do VBI consiste de uma fita única de RNA de sentido positivo e contém cerca de nucleotídeos (CAVANAGH, 2007). O genoma viral é envolvido basicamente por 3 proteínas: a nucleoproteína (N, uma proteína fosforilada do nucleocapsídeo interno) e externamente, pelas glicoproteínas da matriz (M) e da espícula (S), sendo essa última composta por duas subunidades, S 1 e S 2. Existe ainda uma quarta proteína (E), que é associada ao envelope viral, está presente em pequena quantidade e possui baixa massa molecular, com cerca de 100 resíduos de aminoácidos. (MARTINS, 1992; MURPHY et al., 1999; ROCHA, 2000; RESENDE, 2003, MCKINLEY; HILT; JACKWOOD, 2008). A proteína N é formada por 409 aminoácidos, com uma massa molecular de cerca de 50 KDa (MACNAUGHTON; MADGE, 1977, BOURSNELL et al., 1985). Está localizada na parte mais interna do vírion, encontrando-se diretamente associada ao RNA genômico. Esta proteína exerce um papel importante nos processos de replicação e montagem de novas partículas do VBI (COLLISON et al., 1992). Usualmente, tal proteína apresenta elevada homologia entre as diferentes cepas de VBI, sendo uma proteína bastante imunogênica e abundantemente expressa durante o processo de infecção viral (WILLIAMS; SNEED; COLLISSON, 1992).
16 16 A glicoproteína M interage com o nucleocapsídeo interno da partícula viral e possui cerca de 225 aminoácidos, sendo que desses, somente 10% estão exteriorizados no envelope viral. Essa glicoproteína apresenta variação de peso molecular (26 a 34 KDa) devido a diferentes níveis de glicosilação que a mesma sofre no Complexo de Golgi (KING; CAVANAGH, 1991, MARTINS, 1992, MURPHY et al., 1999, ROCHA, 2000). A glicoproteína S é clivada em duas subunidades: S 1 (535 aminoácidos, 92 kda) e S 2 (627 aminoácidos, 84 kda) (CAVANAGH, 1981). A função da proteína S, dentre outras, é ligar o vírus ao receptor na célula hospedeira (S 1 ) e induzir a fusão das membranas da célula e do vírus, de modo que o genoma viral possa ser libertado para dentro do citoplasma (S 2 ) (CAVANAGH, 2007). A subunidade S 2 é muito mais conservada entre os sorotipos do que a S 1 (CAVANAGH; GELB, 2008). Já foram identificados diversos sorotipos e genótipos de VBI e novas variantes continuam emergindo devido às mutações e recombinações no genoma viral (JONES, 2010). O VBI protótipo é a cepa Massachusetts M41, do sorotipo Massachusetts. O principal sítio determinante da indução de anticorpos neutralizantes contra o VBI, que define o sorotipo, reside na subunidade S 1 da proteína S (OIE, 2008), e a evolução sorotípica do vírus parece estar relacionada primariamente à sequência dessa subunidade (LIU et al., 2006). Uma mudança de apenas 2-3% da sequência de nucleotídeos no gene S 1, representando cerca de aminoácidos, podem alterar o sorotipo da estirpe (CAVANAGH, 1997). A capacidade de mutação e recombinação do VBI e a pressão de seleção exercida pelo uso prolongado de vacinas vivas contribuem para o aparecimento de uma grande variedade de sorotipos e subtipos de VBI, sendo os sorotipos Massachusetts 82828, Beaudette (cepa mutante derivada da cepa Massachusetts), Connecticut e Arkansas os mais conhecidos (DI FABIO et al., 2000). As mutações são aleatórias e ocorrem no VBI devido ao fato do vírus possuir RNA como material genético. Além disso, a ausência de fita dupla pode impedir a reparação de erros durante o processo de replicação. 2.3 Patogenia e sinais clínicos A BI ocorre sob formas clínicas e anatomopatológicas diferentes. A patogenia e os sinais clínicos decorrentes da infecção pelo VBI podem variar conforme o tropismo tecidual que a cepa possui. Entretanto, independente do tropismo, o VBI é
17 17 primariamente epiteliotrópico, replicando-se nas células epiteliais, nas células secretoras de muco e nas células dos pulmões e dos sacos aéreos. A replicação do vírus nos tecidos do trato respiratório causa sinais característicos, como dificuldades para respirar, tosse e descarga nasal (CAVANAGH, 2007). A infecção por VBI produz lesões características na traquéia, que é o órgão de eleição para sua multiplicação (KING; CAVANAGH, 1991), sendo por isso, considerada uma doença primária do aparelho respiratório (RESENDE, 2003). A mucosa da traquéia torna-se edematosa com a perda de cílios e a diminuição da atividade ciliar, e esse parâmetro tem sido usado para inferir sobre a severidade da infecção no trato respiratório (DHINAKAR; JONES, 1997, CAVANAGH; GELB, 2008, VILLARREAL et al., 2007b). Sacos aéreos e pulmões podem ou não ser atingidos (CAVANAGH; GELB, 2008, ENGSTRÖM et al., 2010). Alguns sorotipos, denominados nefropatogênicos, possuem tropismo pelos rins e causam lesões renais incluindo inchaço, palidez e dilatação dos túbulos e ureteres (CAVANAGH; GELB, 2008). A replicação do VBI nos rins foi demonstrada nos túbulos proximais, distais e coletores (CHEN et al., 1996). A severidade da infecção por estes sorotipos está relacionada com a formação e deposição de imunocomplexos, causando nefrite, nefrose, gota e uremia (WINTERFIELD; ALBASSAM, 1984). A deposição de imunocomplexos também ocorre pela infecção com outros sorotipos de VBI, podendo ser observada nos capilares dos músculos peitorais das aves, causando, nesses casos, miopatia bilateral (DHINAKAR; JONES, 1996, GOUGH; PEARSON, 1992). Certas cepas possuem a capacidade de sobreviver, tanto na presença de ph baixo, quanto na presença de enzimas digestivas e sais biliares, característica relevante para a replicação entérica. As cepas enterotrópicas de VBI podem causar diarréia aquosa nas aves infectadas (DHINAKAR; JONES, 1996). Em fêmeas, a infecção por VBI leva ao declínio da produção de ovos. Entretanto, a severidade varia de acordo com o período de postura, a virulência das cepas envolvidas e outros fatores não específicos (CAVANAGH, 2003). A produção de ovos pode aumentar após duas ou três semanas, mas atinge apenas níveis subótimos. Fêmeas infectadas com menos de duas semanas de idade podem ter danos permanentes ao desenvolvimento do trato reprodutivo (DHINAKAR; JONES, 1997). Em galos o VBI pode causar lesões no testículo e levar a infertilidade (VILLARREAL et al., 2007b).
18 18 O longo período em que o VBI pode permanecer incubado (até 50 dias) facilita que, durante este período, ocorram infecções bacterianas e virais secundárias, o que é um fator importante na patogenia do VBI (CAVANAGH, 2003). Vários patógenos respiratórios como Mycoplasma gallisepticum, M. sinoviae, Escherichia coli, Haemophilus paragallinarum, vírus da doença de Newcastle e vírus da doença de Gumboro, podem interagir sinergicamente com o VBI ou com os vírus vacinais, aumentando a severidade e duração da doença (KING; CAVANAGH, 1991, ROCHA, 2000; MATTHIJS et al., 2009). Estas infecções podem resultar em lesões nas células do oviduto, levando à redução da produção e comprometimento da qualidade interna e externa dos ovos. Além disso, estas infecções também podem causar pericardite, aerossaculite, perihepatite e peritonite (SANTOS; FARIA; RIBEIRO, 2005). Em relação à morbidade e mortalidade causada pelo VBI, todas as aves de um plantel podem ser acometidas, mas a mortalidade é variável, dependendo da estirpe viral, idade, estado imunológico do lote, fatores ambientais estressantes e infecções bacterianas secundárias. Em aves jovens a doença se manifesta com maior severidade. Com o aumento na idade, diminui a taxa de mortalidade e aumenta a ocorrência das lesões renais e do oviduto (HIPÖLITO; SILVA; HSIUNG, 1979, KING; CAVANAGH, 1991, RESENDE, 2003). 2.4 Epidemiologia O VBI está distribuído por quase todo o globo, exceto na Albânia, na Geórgia, na Groenlândia, na Letônia, na Mongólia, em St. Kitts e Nevis, em São Vicente e Granadinas, no Tajiquistão e em Trinidad e Tobago (OIE, 2008). No Brasil, há evidências de que o VBI ocorra em todo o país, pois isolados do VBI já foram identificados em São Paulo, Paraná, Rio de Janeiro, Rondônia (DI FABIO et al., 2000), Minas Gerais (ABREU et al., 2006) e no Distrito Federal (OIE). Os últimos surtos foram registrados no ano de Quatro deles ocorreram no Estado da Bahia, um no Estado de Pernambuco e um no Estado de Santa Catarina (OIE). Isto é um indicativo de que os sorotipos vacinais autorizados atualmente não conferem proteção cruzada contra os vírus circulantes no Brasil (GELB et al., 2005). Aves de todas as idades são suscetíveis a infecções por VBI. Entretanto os sinais clínicos são mais severos em aves jovens. Linhagens resistentes e sensíveis são igualmente suscetíveis à infecção inicial por VBI, no entanto, a recuperação é
19 19 mais rápida nas primeiras (CAVANAGH; NAQI, 2003; DI FÁBIO, 1993; DI FÁBIO et al., 2000). O período de incubação é de horas (CAVANAGH; GELB, 2008; ENGSTRÖM et al, 2010). Após este período, o vírus pode ser excretado via muco, secreções conjuntival e/ou nasal, por um período superior a quatro semanas. As fezes também caracterizam-se como uma via de disseminação do agente, porém, por essa via, o VBI pode ser eliminado por um período de até 20 semanas após a infecção (KING; CAVANAGH, 1991; DI FÁBIO, 1992). O VBI pode persistir por longos períodos no trato intestinal, possivelmente nas tonsilas cecais, sem causar lesões, e essa permanência é um fator importante na epidemiologia das infecções pelo VBI. Tem sido demonstrado experimentalmente, em pintos de 1 dia de idade, que a re-excreção pode ocorrer intermitentemente a partir do início da postura (COOK, 1990). Em geral, os portadores podem transmitir o vírus por até dois meses após a infecção natural, permanecendo as aves recuperadas suscetíveis à infecção por outro sorotipo (KING; CAVANAGH, 1991; DI FÁBIO, 1993; ROSSINI; MONTEIRO, 2004). A transmissão também pode ocorrer através de objetos contaminados, equipamentos e manipuladores (ENGSTRÖM et al., 2010). 2.5 Controle O controle da BI tem sido realizado através de práticas higiênico-sanitárias, juntamente com programas imunoprofiláticos realizados por meio da vacinação. Práticas básicas de manejo, como acesso limitado e controlado ao local, uso de calçados e equipamentos separados para cada lote minimizam o risco da introdução do VBI. Para prevenir infecções, deve-se realizar a limpeza do local, incluindo a remoção e descarte de todo o material orgânico do criadouro. É indicado o uso de um desinfetante adequado para reduzir a infectividade de qualquer partícula viral. Produtos contendo formaldeído, agentes que liberam cloro ou compostos de amônia quaternária são adequados. Nos locais onde há animais de diversas idades é necessário um rígido controle do movimento do pessoal e de equipamentos entre os aviários (DI FABIO, 1993). A prevenção do VBI através da imunização das aves já vem sendo praticada há mais de meio século. A vacinação é feita tanto com vacinas inativadas quanto vivas, ambas elaboradas a partir da cepa Massachussets. As vacinas vivas são
20 20 compostas de estirpes atenuadas de VBI, sendo que a atenuação é feita por meio de múltiplas e seriadas passagens em ovos embrionados de galinha. As vacinas vivas destinam-se mais ao uso em aves jovens ou em período de crescimento (frangos de corte, poedeiras e reprodutoras em fase de recria), em uma ou duas administrações, com intervalos de dias, devendo ser aplicadas preferencialmente por meio de aerossol a um grande número de aves (MENDONÇA et al., 2009, MONTASSIER et al., 2008). As vacinas vivas atenuadas conferem melhor imunidade local no trato respiratório. Entretanto, há o risco de patogenicidade residual, reversão de virulência e persistência (BIJLENGA et al., 2004; MCKINLEY; HILT; JACKWOOD., 2008). Dentre as vacinas atenuadas, citam-se a H52 e a H120, derivadas da amostra nefrotóxica Holland (H). A H120 é possivelmente a mais usada globalmente devido à sua capacidade de promover proteção cruzada contra VBIs de diferentes sorotipos (BIJLENGA et al., 2004). O uso da H52 tem declinado devido ao surgimento de vacinas inativadas altamente eficazes e seguras (BIJLENGA et al., 2004). Em regiões avícolas densamente povoadas e sem possibilidade de vazio sanitário, há o risco do uso inadequado das vacinas vivas, com oportunidade de escape de vírus entre lotes e entre granjas próximas, o que torna esse tipo de vacinação uma prática de risco, além do seu alto custo, especialmente em frangos de corte. Entretanto, em poedeiras, a relação custo benefício poderá ser favorável, além do menor risco de escape de vírus virulento na adoção da vacinação nesse tipo de plantel (MCKINLEY; HILT; JACKWOOD, 2008). As vacinas inativadas contem estirpes de VBI tratadas com agentes químicos inativantes e são acrescidas de adjuvantes (emulsões oleosas). As vacinas inativadas oleosas destinam-se mais ao uso em aves de ciclo longo de vida, como galinhas de postura e reprodutoras e devem ser aplicadas de um a dois meses antes da puberdade e recomenda-se que sejam administradas após a aplicação prévia de vacinas atenuadas (CAVANAGH; NAQI, 2003). As vacinas inativadas estão disponíveis no mercado brasileiro, exclusivamente para BI (algumas contendo mais de um sorotipo de VBI), ou associadas a vacinas contra outras doenças, como a doença de Newcastle. A vacina atenuada denominada H120 tem sido amplamente utilizada no Brasil desde Resultados parciais de testes de proteção confirmaram que a vacina H120 confere alta proteção contra o VBI do genótipo M (PEREIRA et al., 2006).
21 21 Na imunização contra o VBI, a atenção primária foi direcionada para a glicoproteína S 1, uma vez que ela contém os principais sítios antigênicos alvos de anticorpos neutralizantes desse vírus. No entanto, esta proteína está sujeita a sofrer uma enorme variabilidade na composição de aminoácidos de algumas de suas regiões, o que faz com que as variantes do VBI escapem do processo de neutralização por anticorpos contra S 1. A proteína N, por sua vez, não induz a formação de anticorpos neutralizantes, é mais conservada e parece estar envolvida na indução de respostas imunes humorais, como a ação das células T citotóxicas. Porém esta resposta ainda está sendo estudada (SEO; COLLISSON, 1997). A multiplicidade de sorotipos identificados na área representa um desafio na elaboração de um programa de vacinação eficaz. A relação genética entre os isolados brasileiros e as cepas estrangeiras, especialmente aquelas utilizadas na produção de vacinas, ainda é escassamente conhecida e são necessários mais estudos para caracterizar as mudanças causadas por mutações e/ou recombinações na proteína S 1 desses isolados. Além disso, deve-se verificar o grau de proteção dessas vacinas contra infecções causadas por cepas brasileiras (MONTASSIER et al., 2008). Apesar de diversos estudos terem demonstrado a presença de linhagens de VBI divergentes da cepa Massachusetts no Brasil (VILLARREAL, 2007a; VILLARREAL, 2007b; SANDRI et al., 2008; VILLARREAL et al., 2010) e do fato de que a vacinação com mais de uma cepa tenha demonstrado aumentar o nível de proteção para VBI (COOK et al., 1999; GANAPATHY et al., 2009), no Brasil, o Ministério da Agricultura permite o uso de vacina viva apenas da cepa Massachusetts, devido ao risco de entrada de novas variantes no país. Assim, devido a restrição da vacinação, a indústria avícola brasileira têm uma significativa desvantagem no controle da BI. 2.6 Diagnóstico A confirmação do diagnóstico do VBI é baseada no isolamento viral, sempre em conjunto com a sorologia (DI FABIO et al., 2000). Para o diagnóstico virológico da forma respiratória clássica, devem ser coletadas amostras da mucosa traqueal e dos pulmões. Para as outras formas de VBI, rins, ovidutos, tonsilas cecais do trato intestinal ou tecidos do proventriculo, dependendo da patogenia da doença, são fontes mais indicadas para o isolamento do vírus (OIE, 2008).
22 22 Os métodos de diagnóstico convencionais do VBI são baseados no isolamento viral em ovos embrionados livres de patógenos específicos (SPF) (GELB, 1989; OWEN et al., 1991) ou em culturas celulares (HOPKINS, 1974), seguidos da identificação antigênica dos vírus isolados. Três ou mais passagens em ovos embrionados são geralmente necessárias para o isolamento primário do VBI, o que torna tais procedimentos onerosos e demorados. Além disso, somente estirpes adaptadas à passagem em ovos induzem características evidentes como nanismo e enrolamento embrionário. Alguns isolados de campo do VBI não induzem lesões embrionárias específicas durante várias passagens (RAJ et al., 2004). Outra alternativa é o isolamento do VBI a partir da inoculação em anéis traqueais de embriões SPF, a qual se revelou uma técnica bastante sensível (COOK; DARBYSHIRE; PETERS, 1976), mas também muito laboriosa e demorada. Esse método pode ser associado à reação de imunofluorescência direta em culturas de órgão traqueal, permitindo a detecção mais rápida do VBI (BHATTACHARJEE; NAYLOR; JONES, 1994). Testes baseados em biologia molecular são úteis para fazer o diagnóstico direto e/ou a genotipagem do VBI. Dentre esses métodos destacam-se a Transcrição Reversa associada à Reação em Cadeia da Polimerase (RT-PCR), a análise de fragmentos genômicos gerados por enzimas de restrição (RFLP), e o seqüenciamento dos genes mais importantes desse patógeno viral (CAVANAGH; NAQI, 2003). Técnicas sorológicas também são amplamente aplicadas no diagnóstico do VBI, tais como as reações de imunofluorescência, imunodifusão em ágar gel, imunoperoxidase, inibição da hemaglutinação e os ensaios imunoenzimáticos (ELISA, Enzyme-linked immunosorbent assay) (DE WIT, 2000). Os ensaios de vírus neutralização e de inibição da hemaglutinação (IH) são técnicas amplamente utilizadas no diagnóstico e também podem ser usadas para monitorar a grande variabilidade que ocorre entre as estirpes do VBI, possibilitando a classificação das mesmas em diferentes sorotipos. A técnica de vírus neutralização geralmente é realizada em ovos embrionados, ou em anéis traqueais, mas tem como desvantagens a necessidade de adaptação do vírus ao sistema de cultivo, além de que, a infectividade do vírus é avaliada com base nas lesões que ocorrem no embrião e para isso é necessário uma grande quantidade de ovos (COWEN; HITCHNER, 1975). Ademais, deve-se considerar que são necessárias
23 23 sucessivas passagens para a adaptação do vírus à propagação em ovos embrionados. Esta etapa pode provocar alterações nas características genéticas e antigênicas no VBI (OTSUKI; TAGAWA; TSUBOKURA, 1982). O método de cultivo do VBI em anéis de traquéia de embriões de galinha não requer adaptação prévia desse vírus, porém a dificuldade reside no processo de preparação dos anéis (CHERRY; TAYLOR, 1970, DARBYSHIRE et al., 1980). A IH é uma prova sorológica qualitativa utilizada para o diagnóstico do vírus e também para a identificação sorológica. A identificação sorológica é feita por meio da IH de uma amostra viral por um soro padrão. Para realizar este teste, é necessário um tratamento prévio do vírus com a enzima fosfolipase tipo C, para a exposição das hemaglutininas (DI FABIO; ROSSINI, 2000), já que o VBI não é naturalmente hemaglutinante. Entretanto, devido às múltiplas infecções e vacinações, o soro das aves contém anticorpos que apresentam reações cruzadas, e o resultado do teste de IH não pode ser utilizado com alto grau de confiança, além de ser laborioso e de difícil padronização (DI FABIO; ROSSINI, 2000; OIE, 2008). O ELISA é utilizado para o monitoramento sorológico da resposta vacinal e para o monitoramento dos desafios de campo. No entanto, em alguns casos são observados problemas relacionados ao desenvolvimento de reações inespecíficas, baixa sensibilidade, subjetividade da análise dos resultados, além da impossibilidade de discriminação entre as diferentes estirpes do VBI (IGNJATOVIC; ASHTON, 1996; WANG et al., 2002). Entretanto, foi comprovado que os ensaios imunoenzimáticos, quando realizados com padrões apropriados, indicam, com elevada acurácia, as concentrações de anticorpos específicos anti-vbi e podem facilitar o monitoramento do estado imunitário em criações com grande número de aves (MARQUARDT; SNYDER; SCHLOTTHOBER,1981; SNYDER et al., 1983). Atualmente, kits de ELISA para o diagnóstico de VBI já estão disponíveis no mercado. Nestes kits, uma suspensão de partículas do VBI, purificada por ultracentrifugação, é usada para ser adsorvida, na primeira etapa da reação, ao suporte sólido (superfície da cavidade da microplaca). A purificação destas partículas requer, por sua vez, a propagação frequente desse vírus em sistemas de células eucarióticas, no caso específico, em ovos embrionados SPF, e torna bastante difícil e oneroso para um vírus envelopado e com elevada labilidade no que tange à conservação da estrutura nativa dos seus antígenos, especialmente as glicoproteínas das espículas de superfície (NDIFUNA et al., 1998). O VBI também
24 24 pode ser detectado diretamente em tecidos de aves infectadas por meio de técnicas de imuno-histoquímica (IHQ) ou por hibridização in situ (COLISSON et al., 1990; HANDBERG et al., 1999). A IHQ é uma ferramenta útil para o diagnóstico de infecção por VBI e também possibillita estudos sobre a patogênese de diferentes estirpes de VBI. Através da técnica de IQH é possível investigar o tropismo tecidual de determinada cepa do VBI, a relação entre as lesões histopatológicas, a presença ou quantidade do vírus no tecido e acompanhar a migração do vírus durante a infecção. Em um estudo realizado por Mahdavi et al. (2007), trinta pintos SPF com 20 dias de idade foram inoculados via intratraqueal (n = 15) ou oral (n = 15) com o VBI sorotipo 793 / B, isolado no Irã. A IQH revelou que os antígenos virais foram detectados nas células da traquéia, rins, intestino e pulmão. Os resultados deste estudo indicam que o VBI (sorotipo 793 / B), é capaz de causar lesões em diferentes tecidos, entretanto atinge mais severamente os rins. No rim, o antígeno viral foi localizado principalmente nas células epiteliais, mais proeminentemente nos túbulos renais onde também foram encontradas lesões histopatológicas. Os antígenos virais eram aparentes antes do desenvolvimento de lesões e foram detectados no citoplasma das células epiteliais por 3 dias após a infecção com VBI independente da via de infecção (MAHDAVI et al., 2007). O objetivo do estudo de Benyeda et al. (2010) foi comparar experimentalmente a patogenicidade e distribuição tecidual de diferentes cepas de VBI: a cepa emergente QX, a M41 (protótipo do VBI) e sorotipos 793 / B. Métodos histopatológicos e imuno-histoquímicos foram empregados para definir os principais locais de replicação de cada estirpe viral. Os animais foram monitorados durante 42 dias pós-infecção. Todos os frangos infectados apresentaram lesões traqueais, o que confirma a capacidade de todas as estirpes testadas de induzir doença respiratória. A replicação dos isolados no trato alimentar foi detectada, mas a infecção não causou no intestino significativas lesões. Quatro das cinco estirpes QX induziram lesões renais graves (BENYEDA et al., 2010). Os métodos de diagnóstico citados anteriormente, que visam à detecção do antígeno, utilizam anti-soros contendo anticorpos contra diferentes partes do vírus ou AcMs, contra um ou mais epítopos (DE WIT, 2000). Os AcMs possuem diversas vantagens, comparando com os anticorpos policlonais, por serem produzidos por clones híbridos derivados de células progenitoras linfoides únicas, secretando
25 25 anticorpos homogêneos. A produção e seleção dos hibridomas podem ser controladas para se obter especificidade, afinidade e funções efetoras desejadas. Além disso, esse método de produção apresenta enorme reprodutibilidade, não somente em meio de cultivo, mas também no fluido extraído das ascites, que proporciona uma quantidade ilimitada de anticorpos específicos (CAMPBELL, 1991). Os AcMs desempenham um importante papel no desenvolvimento de técnicas de diagnóstico para BI desde a década de Estudos iniciais baseavam-se na detecção de diferentes classes de anticorpos na resposta imune desenvolvida por frangos infectados e a confirmação da importância de IgM no início da resposta imune. AcMs específicos para IgM proporcionaram o desenvolvimento de um ELISA de captura específico para IgM (KARACA; NAQI; GELB, 1992). A aplicação de diferentes AcMs no diagnóstico da BI pode ser exemplificado pelo trabalho desenvolvido por Ignjatovic e McWater (1991), onde foram utilizados AcMs dirigidos contra as três principais proteínas estruturais do VBI para detectar e diferenciar as variantes do VBI encontradas na Austrália. Em um outro estudo, desenvolvido por Koch et al. (1986), foram produzidos uma série de AcMs anti-vbi e com base na sua reatividade com um painel de AcMs específicos para a proteína S, foi possível a diferenciação entre as estirpes VBI de campo, proporcionando um método muito mais rápido do que os testes de neutralização. O grupo de Chen, Wang.e Cheng (2011) desenvolveu um AcM contra a proteína S 1 que demonstrou especificidade para estirpes de VBI de Taiwan e nenhuma reatividade cruzada com a estirpe vacinal H120. Desta forma, este AcM foi utilizado em um ELISA de bloqueio para detecção do VBI em isolados locais. Os resultados demonstraram 98,0% de sensibilidade e especificidade de 97,2% (n=390). O teste detectou todos os sorotipos de VBI de Taiwan, mas não três isolados de outros sorotipos, nem soros contra a gripe aviária e outros patógenos. Este AcM tem potencial para servir como um método rápido e confiável para diagnóstico de infecções do VBI de isolados de campo em Taiwan (CHEN, WANG; CHENG, 2011). O estudo de Bezuidenhout, Mondal e Buckles (2011) utilizando os AcMs produzidos por Karaca, Naqi e Gelb (1992) comparou através da técnica de IHQ a evolução precoce de lesões do saco aéreo em aves que foram inoculadas com uma estirpe do vírus vacinal ou de uma estirpe de campo mais virulenta. Este estudo
26 26 demonstra o êxito desta técnica de imunodiagnóstico utilizando AcMs (BEZUIDENHOUT; MONDAL; BUCKLES; 2011). Diversos grupos de pesquisa estão trabalhando na obtenção de AcMs, porém, devido à grande variabilidade genética entre os isolados de diferentes regiões, um anticorpo produzido contra o isolado de determinada região não apresenta a mesma sensibilidade em relação aos isolados de outras regiões (BEZUIDENHOUT; MONDAL; BUCKLES; 2011). Além disso, a importação deste insumo, já que ainda não há um AcM específico para VBI no país, torna tais metodologias mais caras e inacessíveis.
27 27 3 MATERIAL E MÉTODOS 3.1 Vírus e anticorpos As amostras do VBI e do fluido alantóico foram preparados e gentilmente cedidos pelo Centro Nacional de Pesquisa em Suínos e Aves (CNPSA) da Empresa Brasileira de Pesquisa Agropecuária (Embrapa) de Concórdia SC. Os vírus da Bouba das Aves e de Newcastle foram obtidos a partir de vacinas comerciais gentilmente cedidas pelo Laboratório de Virologia da Faculdade de Veterinária da Universidade Federal de Pelotas. Foram utilizadas duas amostras do VBI: uma denominada VBI clássico (M41) local, constituída da cepa Massachusetts M41, obtida a partir de isolados locais, cepa padrão utilizada em vacinas para BI e responsável pelos primeiros e maiores surtos da BI, e outra denominada VBI variante, constituída de uma cepa de VBI que sofreu mutações e se diferenciou da cepa clássica (M41). Nos últimos anos esta última tornou-se prevalente nos surtos de BI na região, sendo obtida a partir de isolados locais. Para obtenção dos vírus, foram utilizados ovos livres de patógenos específicos (SPF) com 9 dias de incubação. Estes ovos foram inoculados com as amostras virais e incubados a 37ºC. Após 48h, foram colhidos o fluido alantóico (LCA) e as membranas (MCA). As MCA foram trituradas, lavadas e centrifugadas a 1400 g durante 10min por 3 vezes em solução salina fosfatada tamponada (PBS). O sobrenadante foi desprezado e o precipitado ressuspendido em uma solução contendo 10mM de Tris, 1mM de EDTA e 100mM de NaCl (Tampão TNE). O LCA foi centrifugado somente uma vez. O LCA e as MCA foram centrifugados em tubos de ultra centrífuga com um colchão de sacarose a 30% e centrifugados a g durante 3h. Os sobrenadantes foram descartados e os precipitados ressuspendidos em tampão TNE. Todo o processo de multiplicação, purificação e quantificação das amostras foi realizado na Embrapa. As concentrações das amostras do VBI clássico (M41) e VBI variante, utilizadas na imunização dos animais, corresponderam a 30mg/mL e 84mg/mL respectivamente. Foram gentilmente cedidos também, pela CNPSA-Embrapa, um painel de soros positivos (utilizados como controles positivos nos testes) e negativos para BI (utilizados como controles negativos). Como controles positivos foram utilizados também o soro do animal imunizado com o VBI variante antes da fusão celular e
28 28 uma ascite policlonal anti-vbi. Para a produção de ascite policlonal anti-vbi, três camundongos da linhagem BALB/c com 8 semanas de vida foram imunizados 6 vezes, intraperitonealmente, com 100μg da vacina contra a BI, utilizando-se adjuvante de Freund completo na primeira dose, e incompleto nas doses subsequentes. As imunizações ocorreram a intervalos de uma semana entre elas, exceto entre a primeira e a segunda imunizações, quando os animais receberam uma dose de 500μL de pristane. Aproximadamente 8 dias após a última imunização, fluido ascítico foi puncionado a partir dos camundongos, centrifugado a 1500g por 10min e estocado a 4 C. O soro pré-imune do camundongo imunizado e um soro contra as proteínas presentes na amostra de fluido alantóico, produzido através da imunização de três camundongos com o fluido alantóico de um cultivo não infectado, foram utilizados como controles negativos. Para a isotipagem dos AcMs através de SDS PAGE 12%, foram utilizados como controles dois AcMs, um anti-listeria spp. do isotipo IgM (3F8) e outro anti-internalina A (InlA) de Listeria monocytogenes do isotipo IgG (2D12). E como controle positivo na Imuno-histoquímica (IHQ) foi utilizado um AcM comercial anti-vbi específico para a proteína N de VBI. 3.2 Análise das amostras virais Para verificar a pureza das amostras, realizou-se uma análise das proteínas virais através de eletroforese em gel de poliacrilamida (SDS PAGE) a 10% e Western blot. As amostras foram preparadas adicionando-se 450μg dos vírus diluídos em 15µL de PBS, 15µL de tampão de amostra (0,92g de SDS, 2mL de glicerol, 0,3g de Tris Base, 20mL de água) e 5µL de azul de Bromofenol. As amostras foram aquecidas a 100 C por 20 min. Foram aplicados 15µl de cada amostra às cavidades de dois géis e estes foram então submetidos à eletroforese a 100V por 90min. Um dos géis foi corado com a solução de Comassie blue para a visualização das bandas correspondentes as proteínas virais. As amostras do outro gel foram transferidas para uma membrana de nitrocelulose (GE Healthcare), para a realização do Western blot utilizando-se soro de galinha positiva para BI. A transferência foi realizada por 2h a 100V, a temperatura de 4 C. As membranas foram bloqueadas por 1h com 5% de leite em pó desnatado em PBS. O soro de ave positivo para BI foi diluído 1:200 em PBS e adicionado a membrana. Após período de incubação e lavagens, foi adicionado à membrana o anticorpo secundário anti-
29 29 imunoglobulina (Ig) de galinha conjugado a peroxidase (diluído 1:6000 em PBS). A incubação de cada etapa foi realizada sob agitação, por 1h, a temperatura ambiente. Entre cada etapa a membrana foi lavada 4 vezes com PBS contendo 0,05% de Tween 20 (PBS-T). A reação antígeno-anticorpo foi revelada utilizando-se uma solução de substrato contendo tetrahidrocloreto de diaminobenzedina (DAB). 3.3 Imunização dos animais Todos os procedimentos envolvendo animais foram realizados de acordo com os princípios éticos de experimentação animal do Colégio Brasileiro de Experimentação Animal (COBEA). Para a produção dos AcMs, camundongos da linhagem Balb/c com 6 semanas de idade (2 grupos compostos de 3 animais cada) foram imunizados 10 vezes com 100µg do VBI clássico (M41) local ou do VBI variante, via intraperitoneal. Na primeira imunização, os vírus foram emulsificados com o mesmo volume de adjuvante de Freund Completo e, nas demais (duas semanas após a primeira e, semanalmente, a partir da 2ª imunização), em adjuvante de Freund Incompleto. Três dias antes da fusão celular, o camundongo selecionado recebeu uma nova dose do VBI em adjuvante incompleto, via intraperitonial, e outra dose do VBI puro, via intravenosa. 3.4 Preparo das células de mieloma Células de mieloma da linhagem celular Sp2/O foram retiradas do nitrogênio líquido, descongeladas em banho-maria a 37 C, centrifugadas em meio de Eagle modificado por Dulbecco (Dulbecco s Modified Eagle Medium, DMEM, Sigma) incompleto (MI) a 1000g por 8min, e cultivadas em frascos de cultivo celular com meio DMEM completo (MC). Após cinco dias de cultivo e sucessivas trocas de meio, as células foram expandidas para frascos de cultivo maiores até a obtenção de três frascos de 75cm². 3.5 Fusão Celular Sete dias após a décima imunização dos camundongos, o soro dos animais foi coletado por punção do plexo retro-orbital e o título de anticorpos foi determinado por ELISA indireto utilizando o VBI variante como antígeno e o fluido alantóico como controle negativo. O camundongo com maior título de anticorpos contra o VBI e
30 30 menor título contra o fluido alantóico foi selecionado para ser utilizado na fusão celular. No dia da fusão, o animal imunizado foi sacrificado e teve o baço removido em ambiente estéril. O baço foi macerado em meio de cultivo MI, centrifugado a 1000g por 8min e as células ressuspendidas em MI, sendo novamente centrifugadas. Ao final de três centrifugações para a remoção dos grumos maiores do baço, as células foram ressuspendidas em 10mL de MI. As células SP2/O cultivadas em MC foram retiradas dos frascos de cultivo e centrifugadas a 1000g por 8min. Apos três lavagens com MI, as células foram ressuspendidas em 10mL de MI e contadas em câmara de Neubauer. As células do baço foram misturadas com 4x10 7 células SP2/O e centrifugadas a 1000g por 8min, o sobrenadante foi desprezado e 1mL de uma solução de polietilenoglicol (PEG) a 50% em MI foi adicionado durante 1min. Esta suspensão foi agitada durante 1min e, em seguida, 9mL de MI foram adicionados durante 5min. As células foram centrifugadas a 1000g por 10min, ressuspendidas em 50mL de meio DMEM contendo hipoxantina (1x10-6 M), aminopterina (4x10-9 M) e timidina (1,6x10-7 M) (HAT) e 20% de soro fetal bovino e distribuídas em 5 placas de cultivo celular (0,1mL/cavidade). As placas foram incubadas a 37 C em estufa contendo 5% de CO Padronização do ELISA indireto para avaliar a soroconversão dos animais e para fazer a triagem dos hibridomas e posterior caracterização dos AcMs Para padronizar o teste, visando estabelecer a diluição ideal do antígeno e do soro a serem utilizados como controle positivo, para avaliar a soroconversão dos animais e para fazer a triagem dos hibridomas e posterior caracterização dos AcMs, inicialmente, determinou-se a concentração ideal do antígeno a ser utilizada no ELISA. Uma placa de poliestireno de 96 cavidades foi sensibilizada com 500, 250, 125 e 62,5ng/cavidade do VBI clássico ou variante, e da amostra de fluido alantóico (utilizada como controle negativo) diluídos em tampão carbonato bicarbonato (0,05M, ph 9,6). A placa foi sensibilizada com 100µL/cavidade e incubada por 16 a 18h a 4 C. Os soros coletados dos animais foram diluídos 1:100 em PBS-T, aplicados em triplicata e incubados por 1h a 37 C. Como controle positivo foi utilizada a ascite policlonal anti-vbi. O anticorpo de cabra anti-ig de camundongo conjugado a peroxidase foi diluído 1:4000 em PBS-T e adicionado a placa, e após
31 31 período de incubação de 1h e lavagem, a revelação da reação antígeno-anticorpo foi realizada com a adição de ortofenilenodiamina (OPD) diluída em tampão citratofosfato (0,2M, ph 4,0), contendo 0,01% de peróxido de hidrogênio. Após o período de incubação de 15min, no escuro, a temperatura ambiente, a leitura foi realizada em espectofotômetro a 450nm. Entre cada etapa a placa foi lavada 4 vezes com 200μL de PBS-T. Para determinar a diluição ideal dos soros dos animais imunizados para ser utilizada como controle positivo no ELISA indireto, uma placa de poliestireno de 96 cavidades foi sensibilizada com 250ng/cavidade do VBI clássico (M41) local ou variante. A mesma concentração de amostra de fluido alantóico foi utilizada como controle negativo. Os soros dos camundongos imunizados com o VBI clássico ou com o VBI variante foram diluídos em base dois de 1:100 até 1: em PBS-T. Todas as diluições dos soros foram avaliadas em triplicata. As demais etapas do ELISA foram realizadas conforme descrito anteriormente. 3.7 Triagem dos hibridomas e clonagem celular As cavidades com crescimento de células ocupando mais de 50% da superfície da cavidade foram testadas através de um ELISA indireto utilizando 250ng/cavidade do VBI variante e do fluido alantóico como antígeno. As células que demonstraram secreção de anticorpos específicos para o VBI foram selecionadas para a realização da clonagem e posteriormente reclonagem pela técnica da diluição limitante (CAMPBELL, 1991). Após a reclonagem e subsequente triagem, uma parte das células secretoras dos AcMs anti-vbi foram expandidas e congeladas em nitrogênio líquido, em uma solução contendo soro fetal com 10% de dimetilsulfóxido (DMSO), e a outra, injetada em camundongos para a produção de ascites. 3.8 Produção de ascite e purificação dos AcMs Camundongos BALB/c com 6-8 semanas de idade foram sensibilizados com 0,5mL de Pristane (2, 6, 10, 14-tetra-metil-pentadecano, Sigma), e após 10 dias, 5x10 6 células de hibridomas em MI foram inoculadas intraperitonealmente nestes animais. Quatorze dias após, os camundongos foram puncionados para retirada do fluido ascítico que foi centrifugado a 1500g por 10min. Os AcMs foram purificados em coluna de proteína A de acordo com as instruções do fabricante (Amersham, MS). Alíquotas de 1mL foram coletadas em Tris
32 32 ph 9 e dialisadas contra PBS (500 x o volume total das frações). A concentração dos anticorpos foi determinada por espectrofotometria (280nm) e o cálculo foi realizado através do coeficiente de extinção. Os anticorpos foram armazenados a -18 C. 3.9 Caracterização dos AcMs Isotipagem A isotipagem dos AcMs anti-vbi foi realizada, inicialmente, através de ELISA, onde uma placa de poliestireno de 96 cavidades foi sensibilizada com 1μg/mL dos AcMs diluídos em tampão carbonato-bicarbonato e incubada por 1h a 37 C. A placa foi lavada 4 vezes com 200μL de PBS-T, e em seguida foi adicionado 100μL dos anticorpos de cabra anti-isotipo específicos (Sigma, EUA) diluídos 1:4000 em PBS- T. Posterioremente, foram adicionados a placa 100μL de anticorpo de coelho anti- IgG de cabra conjugado a peroxidase (1:5000 em PBS-T). A revelação foi realizada com uma solução substrato-cromógeno contendo OPD. A leitura foi realizada em espectrofotômetro a 450nm. A isotipagem dos AcMs foi confirmada através de SDS PAGE 12%, utilizando como controles outros dois AcMs (anti-listeria) já caracterizados, um deles do isotipo IgM (3F8) e o outro do isotipo IgG (2D12). As amostras foram preparadas a partir de 20μL dos AcMs adicionados de 5μL de tampão de amostra com redução (2β-mercaptoetanol), e então submetidas a tratamento térmico (100 C por 10min) em termociclador. Foram aplicados 12μL de cada amostra Avaliação da capacidade dos AcMs reconhecerem a proteína na sua conformação nativa e da sua especificidade através de ELISA indireto A placa foi sensibilizada com 250ng/cavidade do VBI clássico local e variante, vírus da Bouba das Aves, vírus de Newcastle e amostra de fluido alantóico (utilizada como controle negativo) diluídos em tampão carbonato bicarbonato. Os AcMs foram diluídos 1:200 em PBS-T, e aplicados 100μL/cavidade em triplicata. Como controle positivo foi utilizado o soro do animal imunizado antes da fusão celular (1:12800). O soro pré-imune do camundongo imunizado e o soro produzido contra as proteínas presentes na amostra de fluido alantóico diluídos 1:200 foram utilizados como controles negativos. A incubação das placas foi de 1h a 37 C e entre as etapas deste ELISA, as placas foram lavadas 4 vezes com PBS-T. O anticorpo de cabra
33 33 anti-ig de camundongo conjugado a peroxidase foi diluído 1:4000 em PBS-T e adicionado a placa. Posteriormente as reações foram reveladas conforme descrito anteriormente Avaliação da capacidade dos AcMs reconhecerem a proteína na sua conformação nativa e da sua especificidade através de Western blot Quatrocentos e cinquenta microgramas de cada uma das amostras avaliadas (VBI variante, VBI clássico, vírus de Newcastle, vírus da Bouba das Aves e fluido alantóico, como controle negativo) contidas em 15µL de PBS foram adicionados de 15µL de tampão de amostra e 5µL de azul de Bromofenol. A transferência e bloqueio foram realizados conforme descrito anteriormente. Os AcMs foram diluídos 1:200 em PBS-T e adicionados às membranas. Após período de incubação e lavagem, foi adicionado à membrana anticorpo de cabra anti-ig de camundongo conjugado a peroxidase diluído 1:4000 em PBS-T. A reação antígeno-anticorpo foi revelada utilizando-se uma solução de substrato contendo DAB. Todas as reações foram realizadas a temperatura ambiente e entre cada etapa a membrana foi lavada 4 vezes por 5min com PBS-T Aplicação dos AcMs em Imuno-histoquímica (IHQ) Seis aves SPF adultas foram infectadas experimentalmente via ocular com 10 3,5 EID50 de uma amostra do VBI clássico M41. Após 2, 4 e 6 dias da infecção os animais foram sacrificados e necropsiados. Na necropsia foram coletados fragmentos da traquéia, pulmão, rins e fígado para a análise histopatológica e de IHQ. Estes fragmentos foram fixados por um período de 24 a 48 h em formol tamponado a 10%. Posteriormente os tecidos foram processados pela técnica de histopatologia de rotina. As lâminas foram coradas com Hematoxilina e Eosina para observação das lesões. Lâminas dos mesmos tecidos foram utilizadas para a técnica de IHQ para observar a reação dos AcMs produzidos com os antígenos contidos nas seções de tecido selecionadas. A reação de IHQ foi realizada com amplificação pelo Sistema HRP Dako Cytomation LSAB (Dako). Lâminas tratadas com Poly-lisina foram utilizadas para IHQ. Inicialmente as lâminas com os tecidos foram desparafinados com xilol por 10min a temperatura ambiente por duas vezes. Em seguida, os cortes foram hidratados com álcool etílico absoluto (10min), álcool 96%, 80% e 70%
34 34 respectivamente, por 5min em cada. Após, as lâminas foram incubadas em PBS-T por 4min. A recuperação antigênica foi realizada através de uma técnica de microondas. Para isso, as lâminas foram incubadas em tampão citrato (10mM, ph 6,0) aquecido a 100 C e submetidas ao tratamento no micro-ondas, na potência 7, por 5min, duas vezes, com intervalo de 5min. Após o resfriamento da solução, as lâminas foram retiradas e incubadas em uma solução de PBS contendo 3% H 2 O 2 por 5min para o bloqueio da peroxidase endógena. Posteriormente, foi realizado o bloqueio das reações inespecíficas através da adição aos cortes de uma solução de bloqueio contendo 2% de leite em pó diluído em PBS, por 10min. Os AcMs anti-vbi produzidos neste estudo e o AcM anti-vbi específico para a proteína N de VBI (controle positivo) foram diluídos em PBS (1:100) e adicionados aos cortes que foram incubados primeiramente a temperatura ambiente por 30min e após a 4 C por 18h. Como controle negativo utilizou-se PBS em substituição aos AcMs. A seguir, as lâminas foram imersas em PBS por 5min. Posteriormente, adicionou-se o anticorpo biotinilado de cabra anti-ig de camundongo e as lâminas foram incubadas a 37 C em câmara úmida por 30min. Após, adicionou-se o anticorpo conjugado com estreptavidina + peroxidase e as lâminas foram incubadas por mais 30min nas mesmas condições. Após nova etapa de lavagem, a revelação foi realizada com solução de substrato contendo aminoetil-carbazole (AEC). As lâminas foram cobertas com a solução cromógena de AEC e incubadas em câmara úmida, a temperatura ambiente por 5min. A seguir, a lavagem foi realizada em água destilada corrente por 5min. Os cortes foram contra-corados com hematoxilina de Mayer por 2min. Após a contra-coloração, os cortes foram submersos em uma cuba com água destilada por 5min. As lamínulas foram fixadas nas lâminas com uma gota de solução glicerol-gelatina a 42 C e posteriormente foram analisadas por microscopia.
35 35 4 RESULTADOS E DISCUSSÃO Para a produção dos AcMs, inicialmente três camundongos foram imunizados com o VBI clássico (M41) local e três com o VBI variante (cepa emergente na região). Antes da imunização dos animais, para avaliar a qualidade e determinar a pureza das proteínas virais, amostras dos VBIs e do fluido alantóico foram avaliadas através de SDS PAGE e Western blot com soro de aves positivas para BI (Fig. 1 e 2, respectivamente). Foi observada nas amostras de VBI, através de ambas as técnicas, a presença de uma banda de aproximadamente 50 kda, correspondente a proteína N, e de bandas sugestivas das proteínas S 1 e S 2 (92 kda e 84 kda, respectivamente). Observou-se também, através de SDS PAGE (Fig. 1), diversas bandas em comum entre as amostras virais e a amostra de fluido alantóico. Como estas bandas não correspondem ao peso molecular das proteínas do VBI e estão presentes também na amostra de fluido alantóico, sugere-se que elas sejam proteínas do fluido alantóico que não foram eliminadas durante a purificação do VBI. Embora as amostras virais não tenham apresentado o grau de pureza ideal, estas foram utilizadas para a imunização dos animais, pois os hibridomas secretores de anticorpos específicos para o VBI foram selecionados posteriormente, utilizando as amostras de VBI e de fluido alantóico como antígenos. Figura 1. SDS PAGE 10 % para avaliar a qualidade e pureza das amostras virais utilizadas na imunização dos camundongos para produção de AcMs anti-vbi 1. VBI clássico (M41) local; 2.VBI variante; 3. Amostra de fluido alantóico.
36 36 Proteína S Proteína N Figura 2. Western blot para avaliar a qualidade e pureza das amostras virais utilizadas na imunização dos camundongos para produção de AcMs anti-vbi utilizando soro de aves positivas para BI. 1. VBI clássico (M41) local; 2. VBI variante; 3. Amostra de fluido alantóico; 4. Marcador de massa molecular (Spectra Multicolor Broad Range Protein Ladder). Paralelamente ao processo de imunização dos animais, padronizou-se um ELISA indireto para estabelecer a diluição ideal do antígeno e do soro a serem utilizados como controle positivo, para verificar o processo de soroconversão dos animais imunizados e para a triagem dos hibridomas e posterior caracterização dos AcMs. Inicialmente, determinou-se a concentração ideal do antígeno a ser utilizada no ELISA. O ensaio foi realizado utilizando-se como antígeno diferentes concentrações (500, 250, 125 e 62,5ng/cavidade) das duas amostras do VBI (clássico local e variante) utilizadas na imunização dos animais, e como anticorpo, o soro de um animal imunizado com o VBI clássico local e de outro imunizado com o VBI variante (diluídos 1:100). Como controle negativo, as cavidades das placas foram sensibilizadas com as mesmas concentrações da amostra de fluido alantóico. E como controle positivo, a ascite policlonal anti-vbi produzida com a amostra vacinal para BI foi utilizada. Foi observado, através do ELISA indireto, que as absorbâncias das reações decresceram proporcionalmente à redução das concentrações dos antígenos (Fig. 3). E, como esperado, ocorreram reações entre os soros e a amostra de fluido alantóico, pois, apesar das amostras virais produzidas experimentalmente em ovos não embrionados terem sido purificadas, a fim de eliminar as proteínas presentes no fluido alantóico, uma quantidade relevante destas proteínas ainda permaneceu na amostra (Fig. 1), as quais foram, inevitavelmente, inoculadas junto com o VBI.
37 37 Devido a isso, os animais desenvolveram uma resposta imune contra proteínas presentes na amostra de fluido alantóico, ou seja, produziram anticorpos contra o VBI e essas proteínas. Assim, na triagem dos sobrenadantes dos cultivos dos hibridomas, para avaliar se os hibridomas estavam produzindo anticorpos contra o antígeno viral e se os anticorpos produzidos reconheceriam a proteína na sua forma nativa, as placas foram sensibilizadas também o fluido alantóico. Independente da concentração do antígeno utilizada na sensibilização, a diferença entre as absorbâncias das reações dos soros com os VBIs e com as amostras de fluido alantóico (controle negativo) se manteve. Figura 3. Determinação da concentração ideal de antígeno para o ELISA indireto, utilizando 500, 250, 125 e 62,5 ng/cavidade dos VBI clássico local ou variante e os soros coletados de um animal imunizado com o VBI clássico local e de outro imunizado com o VBI variante, diluídos 1:100. As mesmas concentrações de amostras de fluido alantóico foram utilizadas como controle negativo. Como controle positivo, foi utilizada a ascite anti-vbi. A. Reações entre diferentes concentrações dos antígenos e o soro de um animal imunizado com o VBI clássico. B. Reações entre diferentes concentrações dos antígenos e o soro de um animal imunizado com o VBI variante. O ponto mais elevado de cada barra representa a densidade óptica (D.O., 450 nm) média de triplicatas.
38 38 Pode-se observar também que as absorbâncias das reações utilizando ambos os soros foram muito semelhantes, sendo as melhores reações obtidas utilizando o VBI variante como antígeno, nas concentrações de 500 e 250ng/cavidade, tanto quando este reagiu com o soro do animal imunizado com o VBI clássico (Fig. 3A), quanto com o do imunizado com o VBI variante (Fig. 3B). Além disso, a diferença entre as absorbâncias destas reações e das reações dos soros com as amostras de fluido alantóico foi maior. Sendo assim, a concentração ideal do antígeno viral a ser utilizada no ELISA indireto é de 250ng/cavidade e o antígeno que apresentou as melhores reações foi o variante. O ELISA com os soros dos outros animais de cada grupo e com o controle positivo apresentaram resultados muito semelhantes (dados não demonstrados). Para determinar a diluição ideal do soro a ser utilizada como controle positivo no ELISA, para a triagem dos hibridomas e posterior caracterização dos AcMs, e para avaliar a soroconversão dos animais imunizados, ao final do processo de imunização, utilizou-se como antígeno 250ng dos VBI clássico local ou variante, e como anticorpo, o soro de um animal imunizado com a VBI clássica e de outro imunizado com o VBI variante (diluídos em base dois de 1:100 até 1: em PBS-T). Como controle negativo, cavidades das placas foram sensibilizadas com a mesma concentração da amostra de fluido alantóico e como controle positivo, foi utilizado como anticorpo primário a ascite policlonal anti-vbi. Na Fig. 4 são demonstrados os resultados do ELISA indireto para a determinação da diluição ideal do soro. Pode-se observar que as absorbâncias das reações decresceram proporcionalmente ao aumento da diluição dos soros e, novamente, as melhores reações foram obtidas utilizando o VBI variante como antígeno, tanto quando este reagiu com o soro do animal imunizado com o VBI clássico (Fig. 4A), quanto com o do imunizado com o VBI variante (Fig. 4B).
39 39 Figura 4. Determinação da diluição ideal dos soros dos animais imunizados (diluídos em base dois de 1:100 até 1: em PBS-T) para ser utilizada como controle positivo no ELISA indireto, utilizando 250 ng dos VBI clássico local ou variante como antígeno, por cavidade. A mesma concentração de amostra de fluido alantóico foi utilizada como controle negativo. Como controle positivo, foi utilizada a ascite anti-vbi. A. Reações entre os antígenos e diferentes diluições do soro de um animal imunizado com o VBI clássico; B. Reações entre os antígenos e diferentes diluições do soro de um animal imunizado com o VBI variante. Cada ponto representa a D.O (450 nm) média de triplicatas. As absorbâncias das reações dos soros com a amostra do fluido alantóico foram, muitas vezes, maiores do que as obtidas entre os soros e a amostra viral clássica. Entretanto, embora os camundongos tenham produzido anticorpos contra as proteínas presentes na amostra de fluido alantóico, quando ambos os soros avaliados foram diluídos e vezes, a diferença entre as absorbâncias das reações dos soros com o VBI variante e das reações dos soros com as amostras de fluido alantóico foi maior. Sendo assim, a diluição ideal do soro a ser utilizada no ELISA indireto é de 1: As absorbâncias das reações obtidas com a ascite policlonal anti-vbi produzida com a vacina comercial, utilizada como controle positivo, foram um pouco superiores com o VBI clássico (M41), o que pode ser explicado pelo fato da vacina ser constituída por esta cepa. O ELISA com os soros dos outros animais de cada grupo apresentaram resultados muito semelhantes (dados não demonstrados). Como os soros dos animais imunizados com o VBI variante apresentaram as melhores reações, utilizando tanto o VBI variante como antígeno, quanto o VBI clássico local, e as absorbâncias das reações dos soros destes animais com os dois VBI foram superiores as das reações dos mesmos soros com as amostras de fluido
40 40 alantóico, optou-se por produzir AcMs utilizando animais imunizados com o VBI variante. Outro fator que contribuiu para a escolha deste vírus como antígeno para a produção dos AcMs foi o aumento da incidência de cepas do VBI diferentes da clássica (M41), incluindo os genótipos brasileiros, diferentes dos descritos em outros países (ABREU et al., 2006; CHACÓN et al., 2007; D'ARCE et al., 2008; DI FABIO et al., 2000; MONTASSIER et al., 2006; VILLARREAL et al., b). Neste contexto, é necessário um método de diagnóstico sensível às novas variantes, o que poderia não ser proporcionado se os AcMs fossem produzidos a partir do camundongo imunizado com o VBI clássico, pois pequenas diferenças no genoma do VBI poderiam impedir que os AcMs reconhecessem as variantes. Após as etapas de fusão celular entre os linfócitos B do camundongo imunizado com o VBI variante e células de mieloma (SP2) e de cultivo, triagem e clonagem dos hibridomas, foram obtidos dois hibridomas secretores de AcMs anti- VBI, denominados 2G4 e 5 A11. Os AcMs foram classificados em isotipos e caracterizados frente a capacidade de reconhecer o VBI clássico local e variante e quanto a especificidade frente a outros vírus aviários. O isotipo dos AcMs foi determinado através da utilização de um kit de isotipagem. Neste teste, os AcMs demonstraram absorbâncias maiores frente ao isotipo IgM, porém também apresentaram reações frente aos demais isotipos. Assim, para confirmar o isotipo dos AcMs obtidos foi realizado um SDS PAGE 12%, utilizando outros dois AcMs (anti-listeria), um do isotipo IgG (2D12) e outro do isotipo IgM (3F8) como controles. Como observado na Fig. 5 os AcMs 2G4 e 5 A11, assim como o AcM 3F8 (controle, IgM) apresentaram uma banda de aproximadamente 75 kda, correspondente a cadeia pesada, e outra de 25 kda, correspondente a cadeia leve, características do isotipo IgM quando reduzido, enquanto que o AcM 2D12 (controle, IgG) apresentou uma banda de 50 kda e outra de 25 kda, correspondentes as cadeias pesadas e leves, respectivamente, características de um anticorpo IgG. As imunoglobulinas IgM, IgD e IgE são mais fortemente glicosiladas, sendo que os carboidratos presentes nestes isotipos correspondem a 12-14% do seu peso. Várias são as funções desta glicosilação: ligação a lectinas do soro, como a lectina ligadora de manose (mannose binding lectina, MBL); manutenção da solubilidade e da conformação; facilitação do transporte subcelular, secreção e manutenção das funções efetoras, garantindo a ligação da porção Fc aos seus receptores. (RAMOS,
41 ). Este padrão de glicosilação pode variar em diferentes anticorpos e isso pode explicar a pequena diferença entre o padrão apresentado pelo AcM do isotipo utilizado como controle e o apresentado pelos AcMs obtidos neste estudo. Figura 5. SDS PAGE 12% para a determinação do isotipo dos AcMs anti-vbi obtidos a partir da fusão celular entre os linfócitos B do camundongo imunizado com o VBI variante e células de mieloma. 1. AcM 2D12 (Controle, IgG); 2. AcM 3F8 (Controle, IgM); 3. AcM 2G4; 4. AcM 5 A11; 5. Marcador de massa molecular (Spectra Multicolor Broad Range Protein Ladder). A IgM é uma imunoglobulina geralmente pentamérica, predominante no início das respostas imunitárias. A maioria dos AcMs obtidos em estudos relacionados pertencem aos isotipos IgG1, IgG2a e IgG2b. Nestes estudos, os animais recebiam de 3 a 4 doses e a imunização dos animais para obtenção de AcMs anti-vbi era realizada a intervalos maiores, de no mínimo 14 dias entre cada dose (MOCKETT; CAVANAGH; BROWN, 1984, CARDOZO et al., 2001; SOUZA et al., 2001; IGNJATOVIC; MCWATERS.,1991; KARACA; NAQI, 1992; CHEN; WANG; CHENG, 2011). Já o protocolo de imunização utilizado para a produção dos AcMs obtidos no presente estudo e do AcM 3F8, também do isotipo IgM e utilizado como controle no SDS PAGE, consistiu de 10 doses semanais. Após a confirmação da isotipagem, a concentração dos anticorpos foi determinada por espectrofotometria (280nm) e o cálculo foi realizado através do coeficiente de extinção de IgM (1,18). O AcM 2G4 obteve a concentração de 0,828 mg/ml e o AcM 5 A11 de 0,454 mg/ml. Na caracterização dos dois AcMs (2G4 e 5 A11) quanto a capacidade de reconhecerem a proteína na sua conformação nativa, através de ELISA indireto, foi observada uma forte reação dos AcMs com o VBI variante, apresentando absorbâncias de 0,815 e 0,891, respectivamente. Entretanto, quando testados com o VBI clássico, ambos AcMs tiveram um decréscimo acentuado na reação (0,441 e
42 42 0,337, Fig. 6), a qual foi semelhante a obtida contra o vírus da Bouba das aves, mas 2 vezes maior do que a obtida com a amostra de fluido alantóico. Figura 6. Reatividade dos AcMs anti-vbi (2G4 e 5A11) frente a diferentes vírus (VBI variante e clássico M41 local, vírus da Bouba das aves e de Newcastle) por ELISA indireto. Amostra de fluido alantóico foi utilizada como controle negativo. Como controle positivo foi utilizado o soro do animal imunizado antes da fusão celular (1:12800) e como soros controles negativos, o soro pré-imune do camundongo utilizado na fusão e o soro produzido contra as proteínas presentes na amostra de fluido alantóico (1:200). O ponto mais elevado de cada barra representa a densidade óptica (D.O., 450 nm) média de triplicatas. Os AcMs obtidos também não foram detectados através de um Kit ELISA comercial para diagnóstico de BI (IDEXX Corporation, Westbrook, ME, USA),o qual vem sensibilizado com o VBI clássico. Esses resultados sugerem que os AcMs obtidos não reagem com o VBI clássico ou reagem muito levemente (dados não demonstrados), o que pode ser explicado, primeiramente, pelo fato da imunidade induzida por inoculação com um sorotipo (no caso com o VBI variante) não induzir proteção eficaz a sorotipos heterólogos (CAVANAGH, 2003). Além disso, diferenças mínimas na subunidade S1 podem contribuir para a diminuição da proteção cruzada em experimentos de desafio em frangos (CAVANAGH; ELLIS; COOK, 1997). E, como um determinado sorotipo tem pouca capacidade de induzir proteção à infecção por outros sorotipos, as galinhas podem ser infectadas várias vezes, em um curto período de tempo (CAVANAGH et al., 1999). O soro coletado do camundongo ao final das imunizações, antes da fusão celular, foi utilizado como controle positivo. Este soro apresentou absorbância superior a obtida com os AcMs, não somente quando foi testado com o VBI variante
43 43 e clássico, mas também frente a amostra de fluido alantóico (Fig. 6). E todos os anticorpos avaliados reagiram inespecificamente com a amostra de fluido alantóico, exceto o soro pré-imune do camundongo utilizado na fusão. Como soros controles negativos foram utilizados também o soro pré-imune do camundongo utilizado na fusão (dia 0), o qual praticamente não apresentou reação frente a nenhum dos antígenos testados e o soro produzido contra as proteínas presentes na amostra de fluido alantóico. Essa amostra de soro controle negativo, obtida através da imunização de camundongos com a amostra de fluido alantóico, apresentou reação com todos os antígenos testados. Com exceção da reação com o VBI variante, as absorbâncias das reações deste soro com os outros antígenos foram semelhantes ou até mesmo superiores às obtidas com os AcMs, o que confirma a presença de grande quantidade de proteínas de fluido alantóico nas amostras virais. Além disso, estes resultados também podem sugerir que a amostra de fluido alantóico foi contaminada com o VBI, justificando desta forma as reações dos AcMs com essas proteínas. Os resultados obtidos no Western blot (Fig. 7) corroboram com os obtidos no ELISA indireto (Fig. 6). Observa-se que os dois AcMs reconheceram fortemente o VBI variante, sugerindo novamente que tenham maior especificidade para esta cepa. Ambos também reconheceram, embora com menos intensidade, o VBI clássico.
44 44 Figura 7. Perfil eletroforético e reatividade dos AcMs anti-vbi (2G4 e 5A11) frente a diferentes vírus (VBI variante e clássico M41 local, vírus da Bouba das aves e de Newcastle) por Western blot. A) SDS PAGE 12 % corado com Comassie Blue das diferentes amostras virais; B) Western blot das diferentes amostras virais com o AcM 2G4; C) Western blot das diferentes amostras virais com o AcM 5 A Amostra de fluido alantóico (controle negativo); 2. VBI clássico M41 local; 3. VBI variante, 4. Vírus de Newcastle, 5. Vírus da Bouba das Aves; 6. Marcador de massa molecular (Spectra Multicolor Broad Range Protein Ladder). Na figura 7B observa-se a reação do AcM 2G4 com uma proteína de aproximadamente 90 a 84 kda, peso molecular correspondente as subunidades da proteína S (S 1 e S 2 ). Como seus pesos moleculares são muito semelhantes, não foi possível determinar, através desta técnica, a subunidade que é reconhecida pelo AcM. AcMs gerados contra a subunidade S 1 são, geralmente, sorotipo-específicos (MOCKETT et al, 1984;. KOCH et al, 1990), embora um AcM contra um local conservado na subunidade S 1 tenha sido obtido (NIESTERS et al., 1987).Isso sugere que os AcMs obtidos no presente estudo sejam específicos a proteína S 1, pois além de um deles (2G4) reagir com uma banda de peso molecular correspondente a esta subunidade, eles também demonstram ser sorotipo-específicos, pois reconhecem mais fortemente o VBI variante (Fig. 6 e 7). AcMs específicos contra S 1 podem ser ferramentas úteis para o estudo das relações antigênicas entre amostras do VBI. No trabalho de CARDOZO et al., (2001) foram produzidos e caracterizados um painel de 12 AcMs específicos para as proteínas S 1, S 2, N e M do VBI amostra M41. Segundo os autores, o AcM anti-s 1 poderá ser utilizado para a detecção de M41 e amostras relacionadas antigenicamente. Mockett; Cavanagh e Brown (1984) caracterizaram AcMs específicos contra S 1, evidenciando serem estes amostra-específicos, ou seja, com capacidade neutralizante específica apenas contra M41. Dessa forma AcMs anti-s1 podem expressar atividade neutralizante e inibidora da hemaglutinação exclusivamente contra esse sorotipo, as quais são atividades biológicas relacionadas com S 1. (MOCKETT; CAVANAGH; BROWN, 1984, CARDOZO et al., 2001). O AcM 2G4 demonstrou maior especificidade a proteína S1 do VBI variante. Dessa forma, ensaios utilizando este AcM poderão ser desenvolvidos com a finalidade de detecção e estudo de amostras antigenicamente relacionadas com o VBI variante em tecidos e material experimentalmente ou naturalmente infectados, assim como a discriminação das relações antigênicas entre as amostras de campo
45 45 com a amostra M41. Além disso, o AcM também tem potencial para ser utilizado como ferramenta para monitorar as mutações que ocorrem nesta cepa. Neste mesmo ano, no país, foram produzidos AcMs contra as proteínas N (53kDa) e S 2 (84kDa) do VBI amostra M41 (SOUZA et al., 2001). O AcM contra S 2 comportou-se como uma boa ferramenta de diagnóstico do VBI e pode ser aplicado em ensaios de rotina laboratorial independentemente do sorotipo, especialmente no diagnóstico das doenças que se confundem com a BI nas galinhas, enquanto o AcM contra N demonstrou reconhecer uma região menos conservada entre as estirpes de VBI e pode ser útil em estudos comparativos entre isolados de VBI (SOUZA et al., 2001). O epítopo que foi reconhecido na subunidade S 1 pelo AcM desenvolvido por Ignjatovic e McWaters (1991) foi conservado em todas as estirpes isoladas do VBI na Austrália entre 1962 e Utilizando o AcM anti-s 1 em conjunto com outros dois AcMs, um anti-n e outro anti-m, produzidos neste mesmo trabalho, foi possível avaliar o grau de semelhança antigênica entre os isolados de VBI, a identificação de mutações no VBI variante e a diferenciação entre as estirpes de vírus dos sorotipos iguais ou diferentes, o que não era anteriormente possível. Estes AcMs foram testados por um ELISA direto para diferenciar antigenicamente estirpes do VBI (IGNJATOVIC; MCWATERS, 1991). Posteriormente, os AcMs produzidos por Ignjatovic e McWaters (1991) foram testados em um ELISA de Captura, o qual demonstrou ser um método sensível para a detecção e diferenciação antigênica dos vírus utilizados nas vacinas com as estirpes de campo. O tipo antigênico do VBI determinado no ELISA de captura corroborou com a tipificação antigênica obtida por vírus neutralização (VN), permitindo determinar rapidamente se a estirpe do VBI identificada é uma variante ou re-isolamento de um vírus da vacina. Este teste foi capaz de detectar o vírus na fase aguda da infecção, porém não conseguiu detectar a infecção com baixa dose de vírus (IGNJATOVIC; ASHTON, 1996). AcMs específicos a determinado sorogrupo são ferramentas importantes para determinar anticorpos específicos a determinado sorotipo no soro dos animais infectados, possibilitando monitorar os sorotipos prevalentes nos surtos e infecções (KARACA; NAQI, 1993; CHEN; WANG; CHENG, 2011). O ELISA de bloqueio apresentando no trabalho de Karaca e Naqi (1993), utilizando AcMs sorotipoespecíficos desenvolvidos pelos mesmos pesquisadores no ano anterior (KARACA; NAQI, 1992), demonstrou ter a sensibilidade do teste de ELISA indireto e
46 46 especificidade em relação ao sorotipo proporcionado pelo teste de VN. Os resultados do ELISA de bloqueio e VN indicam que os anticorpos produzidos durante a resposta primária são fortemente sorotipo-específicos, enquanto aqueles produzidos durante a resposta secundária reagem mais fortemente com o vírus homólogo, mas apresentam reatividade cruzada com antígenos heterólogos (KARACA; NAQI, 1993). Utilizando os mesmos AcMs anti-s1 sorotipo específicos citados anteriormente (KARACA; NAQI, 1992) também foi desenvolvido um ELISA de captura para a detecção e identificação do VBI dos sorotipos Arkansas, Connecticut e Massachusetts. O ensaio obteve melhores resultados quando o AcM anti-s 1, o antígeno e o soro teste eram do mesmo sorotipo. O ELISA de captura descrito neste trabalho contorna o problema de reatividade cruzada que ocorre utilizando somente o soro das aves. Neste ensaio, o AcM sorotipo-específico parece capturar principalmente a glicoproteína S 1 da amostra infectada, mas não o vírus inteiro, ou as proteína S 2, M ou N, pois os componentes que não participam da reação são removidos por lavagem antes da adição do soro de galinha. Este teste foi eficaz para detectar o vírus em fluido alantóico após passagem do VBI em ovos embrionados, porém diretamente em tecidos infectados homogeneizados não teve poder de detecção. O grupo de Chen; Wang e Cheng, (2011) desenvolveu um AcM contra a proteína S1 que demonstrou especificidade para estirpes de VBI de Taiwan e nenhuma reatividade cruzada com a estirpe vacinal H120. Desta forma, este AcM foi utilizado em um ELISA de bloqueio para detecção do VBI em isolados locais. Os resultados demonstraram 98,0% de sensibilidade e especificidade de 97,2% (n=390). O teste detectou todos os sorotipos de VBI de Taiwan, mas não três isolados de outros sorotipos, nem soros contra a gripe aviária e outros patógenos. Este AcM tem potencial para ser utilizado em um método rápido e confiável para diagnóstico de infecções do VBI de isolados de campo em Taiwan (CHEN; WANG; CHENG, 2011). Da mesma forma, os AcMs 2G4 e 5 A11, por demonstrarem maior reação com o VBI variante, podem ser utilizados para o diagnóstico de isolados locais. A especificidade dos AcMs em reconhecer somente o VBI foi avaliada testando-os com dois outros vírus aviários: vírus da Bouba das Aves e vírus de Newcastle. Os AcMs reagiram fracamente com estes vírus. A reação dos AcMs 2G4
47 47 e 5 A 11 obtida com o vírus da Bouba das Aves (0,567 e 0,322 respectivamente) e com vírus de Newcastle (0,269 e 0,031 respectivamente) é muito inferior à obtida com o VBI variante (0,815 e 0,891, respectivamente). (Fig. 6). No Western blot (Fig. 7) observa-se que os AcMs obtiveram reações fracas com o vírus de Newcastle e Bouba das Aves, sendo que o AcM 5 A11 (Fig. 6C) demonstrou reações ainda menos intensas. O teste de especificidade ao VBI foi realizado com estes dois vírus, pois ambos possuem genoma constituído de RNA, não têm relação filogenética com o VBI, também acometem o sistema respiratório de aves e, frequentemente, após a infecção por VBI ocorrem infecções secundárias por estes agentes, levando ao aumento da severidade e duração da doença (HIPÖLITO; SILVA; HSIUNG, 1979, KING; CAVANAGH, 1991, RESENDE, 2003). Diversos estudos relacionados utilizaram somente o vírus de Newcastle como antígeno negativo para avaliar a especificidade dos AcMs (IGNJATOVIC; WATERS, 1991; CARDOZO et al., 2001; SOUZA et al., 2001). Os testes também foram realizados com a amostra de fluido alantóico. As absorbâncias obtidas da reação dos AcMs frente as proteínas presentes na amostra de fluido alantóico foram semelhantes às obtidas frente aos vírus da Bouba das Aves e de Newcastle. No trabalho desenvolvido por lgnjatovic e Waters (1991) nenhum dos AcMs obtidos reagiu com o líquido alantóico não infectado ou com o vírus de Newcastle. Neste estudo, a purificação das amostras virais utilizadas para imunização dos animais foi realizada por centrifugação a g durante 16 h em gradientes de sacarose (25% a 55% de sacarose w / v em Tampão NET) diferente do processo de purificação realizado em nosso trabalho, onde as amostras foram purificadas por centrifugação a g durante 3 horas contra um gradiente de sacarose de 30%. No trabalho desenvolvido por Chen; Wang e Cheng (2011), o AcM obtido apresentou reações baixas, mas não inexistentes com a amostra SPF, sendo que as amostras virais foram submetidas a um processo de purificação semelhante ao descrito por Ignjatovic e Waters (1991). Apesar desta pequena reação inespecífica, o desempenho do AcM não foi comprometido e sua possível aplicação foi confirmada com altos índices de sensibilidade e especificidade através de um ELISA de bloqueio (CHEN; WANG; CHENG, 2011). Estes dados sugerem que, apesar dos nossos AcMs apresentarem uma pequena reação com a amostra de fluido alantóico,
48 48 esta reação pode ser considerada inespecífica e não irá influenciar na aplicabilidade dos AcMs. As absorbâncias das reações obtidas com os dois AcMs foram, de maneira geral, semelhantes. Entretanto, como podemos verificar na Fig. 6, o AcM 5 A11 demonstrou absorbâncias mais elevadas quando testado com o VBI variante e mais baixas quando testado com as demais amostras, sugerindo ser mais específico do que o AcM 2G4. Os resultados obtidos no Western blot (Fig. 7) também sugerem a maior especificidade do AcM 5 A11. Comparando os resultados obtidos nesta caracterização inicial dos AcMs 2G4 e 5 A11 com os resultados e aplicações dos AcMs produzidos e caracterizados em trabalhos semelhantes, acredita-se no potencial dos nossos AcMs para uso como ferramenta em testes de imunodiagnóstico para o VBI. No presente trabalho, a aplicação dos AcMs foi avaliada através de IQH. A técnica de IQH detecta moléculas (antígenos) teciduais, baseando-se no reconhecimento do antígeno por um anticorpo (Ac primário) associado a diversos tipos de processos de visualização. Esta técnica traz diversos benefícios para o diagnóstico rápido pois não requer processo de isolamento viral e o antígeno pode ser detectado diretamente dos tecidos de aves infectadas. Os AcMs foram testados em tecidos da traquéia, pulmão, rins e fígado de aves inoculadas experimentalmente via ocular. Ambos os AcMs marcaram principalmente células inflamatórias (Fig. 8), havendo pouca marcação de células epiteliais. O VBI é um vírus primariamente epiteliotrópico, replicando-se nas células epiteliais, nas células secretoras de muco e nas células dos pulmões e dos sacos aéreos (MENDONÇA et al., 2009). Sendo assim, as marcações características do VBI ocorrem preferencialmente nestas células. Entretanto, a visualização das células epiteliais marcadas em nosso teste foi dificultada devido ao background concentrado principalmente nesta região.
49 49 Figura 8. Imuno-histoquímica utilizando os AcMs 2G4 e 5 A11 (diluídos 1:50) em tecidos de aves infectadas experimentalmente via ocular com o VBI clássico (M41) local e coletados 4 dias após a infecção. A) Tecido de pulmão marcado com o AcM 2G4. Objetiva de 1000 vezes; B) Tecido de traquéia marcado com o AcM 5 A11; Objetiva de 40 vezes. C) Tecido de pulmão marcado com o AcM 5 A11. Objetiva de 40X; D) Tecido de pulmão marcado com o anticorpo comercial (AcM anti-vbi específico para a proteína N, controle positivo). Objetiva de 40 vezes; E) Tecido de pulmão no teste com PBS (controle negativo). Objetiva de 20 vezes Um AcM anti-vbi específico para a proteína N, já testado no trabalho de Mahdavi et al. (2007), foi utilizado em nossos testes como controle positivo. No trabalho desenvolvido por Mahdaviet et al.(2007), o antígeno viral foi detectado no
Métodos de Pesquisa e Diagnóstico dos Vírus
 Métodos de Pesquisa e Diagnóstico dos Vírus Estratégias Isolamento em sistemas vivos Pesquisa de antígeno viral Pesquisa de anticorpos Pesquisa do ácido nucléico viral (DNA ou RNA) Pré requisitos para
Métodos de Pesquisa e Diagnóstico dos Vírus Estratégias Isolamento em sistemas vivos Pesquisa de antígeno viral Pesquisa de anticorpos Pesquisa do ácido nucléico viral (DNA ou RNA) Pré requisitos para
Pestvirus. Msc. Anne Caroline Ramos dos Santos
 Pestvirus Msc. Anne Caroline Ramos dos Santos Artigo Material e Métodos Animais: o Leitões de 8 semanas de idade o Livres de BVDV Vírus: o BVDV-1b não-citopático estirpe St. Oedenrode isolado de tonsila
Pestvirus Msc. Anne Caroline Ramos dos Santos Artigo Material e Métodos Animais: o Leitões de 8 semanas de idade o Livres de BVDV Vírus: o BVDV-1b não-citopático estirpe St. Oedenrode isolado de tonsila
19/11/2009. Ricardo M. Hayashi Mestrando em Ciências Veterinárias UFPR
 BRONQUITE INFECCIOSA DAS GALINHAS Ricardo M. Hayashi Mestrando em Ciências Veterinárias UFPR CONCEITO: - Doença infecciosa viral, altamente contagiosa, que afeta principalmente o trato respiratório e reprodutivo
BRONQUITE INFECCIOSA DAS GALINHAS Ricardo M. Hayashi Mestrando em Ciências Veterinárias UFPR CONCEITO: - Doença infecciosa viral, altamente contagiosa, que afeta principalmente o trato respiratório e reprodutivo
Heterologous antibodies to evaluate the kinetics of the humoral immune response in dogs experimentally infected with Toxoplasma gondii RH strain
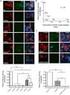 67 4.2 Estudo II Heterologous antibodies to evaluate the kinetics of the humoral immune response in dogs experimentally infected with Toxoplasma gondii RH strain Enquanto anticorpos anti-t. gondii são
67 4.2 Estudo II Heterologous antibodies to evaluate the kinetics of the humoral immune response in dogs experimentally infected with Toxoplasma gondii RH strain Enquanto anticorpos anti-t. gondii são
Análise de Tecnologias Prática. Renan Padron Almeida Analista de Tecnologia
 Análise de Tecnologias Prática Renan Padron Almeida Analista de Tecnologia Agenda Caracterização de Tecnologias Perfil Tecnológico Comunicação de Invenção Matriz de Priorização Agenda Caracterização de
Análise de Tecnologias Prática Renan Padron Almeida Analista de Tecnologia Agenda Caracterização de Tecnologias Perfil Tecnológico Comunicação de Invenção Matriz de Priorização Agenda Caracterização de
Guilherme H. F. Marques Diretor do Departamento de Saúde Animal/SDA/MAPA
 REGISTRO, FISCALIZAÇÃO E CONTROLE DE ESTABELECIMENTOS AVÍCOLAS DE REPRODUÇÃO E COMERCIAIS INSTRUÇÃO NORMATIVA Nº 56/07 Guilherme H. F. Marques Diretor do Departamento de Saúde Animal/SDA/MAPA Importância
REGISTRO, FISCALIZAÇÃO E CONTROLE DE ESTABELECIMENTOS AVÍCOLAS DE REPRODUÇÃO E COMERCIAIS INSTRUÇÃO NORMATIVA Nº 56/07 Guilherme H. F. Marques Diretor do Departamento de Saúde Animal/SDA/MAPA Importância
A portaria 29, de 17 de dezembro de 2013 SVS/MS, regulamenta o diagnóstico da infecção pelo HIV, no Brasil.
 Aula 3 Base racional da portaria 29 de 17/12/2013 SVS/MS A portaria 29, de 17 de dezembro de 2013 SVS/MS, regulamenta o diagnóstico da infecção pelo HIV, no Brasil. Ao se elaborar uma portaria para normatizar
Aula 3 Base racional da portaria 29 de 17/12/2013 SVS/MS A portaria 29, de 17 de dezembro de 2013 SVS/MS, regulamenta o diagnóstico da infecção pelo HIV, no Brasil. Ao se elaborar uma portaria para normatizar
Vacinas e Imunoterapia
 Como os organismos hospedeiros vertebrados podem adquirir Imunidade? Vacinas e Imunoterapia Prof. Helio José Montassier Imunidade Passiva É uma forma de imunidade temporária após transferência natural
Como os organismos hospedeiros vertebrados podem adquirir Imunidade? Vacinas e Imunoterapia Prof. Helio José Montassier Imunidade Passiva É uma forma de imunidade temporária após transferência natural
Resposta Imune Humoral Dr. Carlos R Prudencio
 Resposta Imune Humoral Dr. Carlos R Prudencio O Sistema Imune e os agentes infecciosos Técnicas sorológicas e de biologia molecular no diagnóstico de agentes infecciosos Órgãos do sistema linfóide Introdução:
Resposta Imune Humoral Dr. Carlos R Prudencio O Sistema Imune e os agentes infecciosos Técnicas sorológicas e de biologia molecular no diagnóstico de agentes infecciosos Órgãos do sistema linfóide Introdução:
Jean Berg Alves da Silva HIGIENE ANIMAL. Jean Berg Alves da Silva. Cronograma Referências Bibliográficas 09/03/2012
 Jean Berg Alves da Silva Médico Veterinário UFERSA (2001) Dr. Ciências Veterinárias UECE (2006) Professor do Departamentos de Ciências Animais da UFERSA HIGIENE ANIMAL Jean Berg Jean Berg Alves da Silva
Jean Berg Alves da Silva Médico Veterinário UFERSA (2001) Dr. Ciências Veterinárias UECE (2006) Professor do Departamentos de Ciências Animais da UFERSA HIGIENE ANIMAL Jean Berg Jean Berg Alves da Silva
FiberMax. Mais que um detalhe: uma genética de fibra.
 FiberMax. Mais que um detalhe: uma genética de fibra. Requisitos para o cultivo de algodoeiro GlyTol LibertyLink, além de boas práticas de manejo integrado de plantas daninhas. Cap 1: Descrição do Produto
FiberMax. Mais que um detalhe: uma genética de fibra. Requisitos para o cultivo de algodoeiro GlyTol LibertyLink, além de boas práticas de manejo integrado de plantas daninhas. Cap 1: Descrição do Produto
Processos de interação vírus célula. e replicação viral
 Processos de interação vírus célula e replicação viral Adsorção: ligação do receptor celular e antirreceptor viral. Exemplo poliovírus: 1 Adsorção: ligação do receptor celular e antirreceptor viral. Hepatite
Processos de interação vírus célula e replicação viral Adsorção: ligação do receptor celular e antirreceptor viral. Exemplo poliovírus: 1 Adsorção: ligação do receptor celular e antirreceptor viral. Hepatite
IDENTIFICAÇÃO DOS RISCOS BIOLÓGICOS DE ACORDO COM A NR 32
 IDENTIFICAÇÃO DOS RISCOS BIOLÓGICOS DE ACORDO COM A NR 32 1 PROCEDIMENTOS PARA AVALIAÇÃO E CONTROLE DE AGENTES BIOLÓGICOS Objetivo: Determinar a natureza, grau e o tempo de exposição dos trabalhadores
IDENTIFICAÇÃO DOS RISCOS BIOLÓGICOS DE ACORDO COM A NR 32 1 PROCEDIMENTOS PARA AVALIAÇÃO E CONTROLE DE AGENTES BIOLÓGICOS Objetivo: Determinar a natureza, grau e o tempo de exposição dos trabalhadores
Prevenção e controle das infecções virais
 Prevenção e controle das infecções virais 1 Medidas de prevenção de doenças virais Redução do risco de exposição Introdução de melhorias sanitárias (ex. infecções entéricas) Veiculação de informações para
Prevenção e controle das infecções virais 1 Medidas de prevenção de doenças virais Redução do risco de exposição Introdução de melhorias sanitárias (ex. infecções entéricas) Veiculação de informações para
SÍNDROME DA QUEDA DE POSTURA
 SÍNDROME DA QUEDA DE POSTURA Autores FOLHARI, Érica Pieroli VÁGULA, Maílha Ruiz Email: erica_vet@hotmail.com Discentes da Faculdade de Medicina Veterinária e Zootecnia de Garça FAMED PEREIRA, Rose Elisabeth
SÍNDROME DA QUEDA DE POSTURA Autores FOLHARI, Érica Pieroli VÁGULA, Maílha Ruiz Email: erica_vet@hotmail.com Discentes da Faculdade de Medicina Veterinária e Zootecnia de Garça FAMED PEREIRA, Rose Elisabeth
PNEUMONIAS ATÍPICAS Testes Moleculares GENÉTICA MOLECULAR GENÉTICA MOLECULAR
 GENÉTICA MOLECULAR GENÉTICA MOLECULAR PNEUMONIAS ATÍPICAS Testes Moleculares A Genética de Microorganismos do Hermes Pardini é reconhecida por oferecer uma gama de exames moleculares que auxiliam nas decisões
GENÉTICA MOLECULAR GENÉTICA MOLECULAR PNEUMONIAS ATÍPICAS Testes Moleculares A Genética de Microorganismos do Hermes Pardini é reconhecida por oferecer uma gama de exames moleculares que auxiliam nas decisões
Vacinas e Vacinação. cüéya ]xtç UxÜz 18/5/2010. Defesas orgânicas. Imunoprofilaxia. Imunoprofilaxia. Resistência à infecção.
![Vacinas e Vacinação. cüéya ]xtç UxÜz 18/5/2010. Defesas orgânicas. Imunoprofilaxia. Imunoprofilaxia. Resistência à infecção. Vacinas e Vacinação. cüéya ]xtç UxÜz 18/5/2010. Defesas orgânicas. Imunoprofilaxia. Imunoprofilaxia. Resistência à infecção.](/thumbs/53/32296701.jpg) cüéya ]xtç UxÜz Imunologia Resposta imune Mecanismo pelo qual o organismo é capaz de reconhecer e eliminar as substâncias heterólogas. Resposta imune Substâncias heterólogas Endógena células mortas Exógena
cüéya ]xtç UxÜz Imunologia Resposta imune Mecanismo pelo qual o organismo é capaz de reconhecer e eliminar as substâncias heterólogas. Resposta imune Substâncias heterólogas Endógena células mortas Exógena
Audiência Pública Situação das gripes H1N1 e H7N9 e a fabricação de vacinas antivirais no Brasil
 Audiência Pública Situação das gripes H1N1 e H7N9 e a fabricação de vacinas antivirais no Brasil Antonio Guilherme Machado de Castro Diretor do Centro Avançado de Pesquisa Tecnológica do Agronegócio Avícola
Audiência Pública Situação das gripes H1N1 e H7N9 e a fabricação de vacinas antivirais no Brasil Antonio Guilherme Machado de Castro Diretor do Centro Avançado de Pesquisa Tecnológica do Agronegócio Avícola
Advance technique for hamburger quality control
 Técnica avançada para controlar qualidade do hambúrguer Advance technique for hamburger quality control Sumário O maior risco para o consumidor, consequente da ingestão de hambúrguer mal conservado, é
Técnica avançada para controlar qualidade do hambúrguer Advance technique for hamburger quality control Sumário O maior risco para o consumidor, consequente da ingestão de hambúrguer mal conservado, é
Vírus da Diarréia Epidêmica Suína (PEDV) Albert Rovira, Nubia Macedo
 Vírus da Diarréia Epidêmica Suína (PEDV) Albert Rovira, Nubia Macedo Diarréia Epidêmica Suína PED é causada por um coronavírus (PEDV) PEDV causa diarréia e vômito em suínos de todas as idades Mortalidade
Vírus da Diarréia Epidêmica Suína (PEDV) Albert Rovira, Nubia Macedo Diarréia Epidêmica Suína PED é causada por um coronavírus (PEDV) PEDV causa diarréia e vômito em suínos de todas as idades Mortalidade
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N Professores. Carlos T. Hotta Ronaldo B.
 Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
RESSALVA. Atendendo solicitação do autor, o texto completo desta tese será disponibilizado somente a partir de 04/04/2016.
 RESSALVA Atendendo solicitação do autor, o texto completo desta tese será disponibilizado somente a partir de 04/04/2016. UNIVERSIDADE ESTADUAL PAULISTA UNESP CÂMPUS DE JABOTICABAL CARACTERIZAÇÃO EPIDEMIOLÓGICA
RESSALVA Atendendo solicitação do autor, o texto completo desta tese será disponibilizado somente a partir de 04/04/2016. UNIVERSIDADE ESTADUAL PAULISTA UNESP CÂMPUS DE JABOTICABAL CARACTERIZAÇÃO EPIDEMIOLÓGICA
Exames laboratoriais específicos
 Exames laboratoriais específicos para o diagnóstico de Dengue. Sônia Conceição Machado Diniz Especialista em diagnóstico laboratorial de doenças tropicais IMT/SP Responsável pelo Serviço de Virologia e
Exames laboratoriais específicos para o diagnóstico de Dengue. Sônia Conceição Machado Diniz Especialista em diagnóstico laboratorial de doenças tropicais IMT/SP Responsável pelo Serviço de Virologia e
Cargo: D-41 Técnico Laboratório - Biotecnologia - Análise de Proteínas
 da Prova Prática QUESTÃO 1: Cargo: D-41 Técnico Laboratório - Biotecnologia - Análise de Proteínas Apresenta-se abaixo um protocolo para preparação de géis SDS-PAGE a ser utilizado em uma análise de confirmação
da Prova Prática QUESTÃO 1: Cargo: D-41 Técnico Laboratório - Biotecnologia - Análise de Proteínas Apresenta-se abaixo um protocolo para preparação de géis SDS-PAGE a ser utilizado em uma análise de confirmação
HBsAg Quantitativo Sistema ARCHITECT / Abbott (Clareamento do HBsAg)
 HBsAg Quantitativo Sistema ARCHITECT / Abbott (Clareamento do HBsAg) USO PRETENDIDO O ensaio HBsAg é um imunoensaio de micropartículas por quimioluminescência (CMIA) para a determinação quantitativa do
HBsAg Quantitativo Sistema ARCHITECT / Abbott (Clareamento do HBsAg) USO PRETENDIDO O ensaio HBsAg é um imunoensaio de micropartículas por quimioluminescência (CMIA) para a determinação quantitativa do
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Nobilis Ma5 + Clone 30 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose: Substâncias ativas: Vírus vivo da Bronquite
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 14 1. NOME DO MEDICAMENTO VETERINÁRIO Nobilis Ma5 + Clone 30 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose: Substâncias ativas: Vírus vivo da Bronquite
Professor: David Vieira Valadão. Biologia
 Professor: David Vieira Valadão Biologia 1981 registro de casos atípicos de pneumonia entre homens homossexuais em Los Angeles (EUA). 1983 descoberta de um novo vírus em um paciente com AIDS. 1984 descoberta
Professor: David Vieira Valadão Biologia 1981 registro de casos atípicos de pneumonia entre homens homossexuais em Los Angeles (EUA). 1983 descoberta de um novo vírus em um paciente com AIDS. 1984 descoberta
Programa Analítico de Disciplina BIO270 Virologia Geral e Molecular
 Catálogo de Graduação 016 da UFV 0 Programa Analítico de Disciplina BIO70 Virologia Geral e Molecular Departamento de Biologia Geral - Centro de Ciências Biológicas e da Saúde Número de créditos: 6 Teóricas
Catálogo de Graduação 016 da UFV 0 Programa Analítico de Disciplina BIO70 Virologia Geral e Molecular Departamento de Biologia Geral - Centro de Ciências Biológicas e da Saúde Número de créditos: 6 Teóricas
Vigilância de sarampo e rubéola
 Vigilância de sarampo e rubéola Períodos na investigação de doenças em eliminação 1. Período de exposição / incubação; 2. Período de transmissibilidade ; 3. Período de aparecimento de casos secundários;
Vigilância de sarampo e rubéola Períodos na investigação de doenças em eliminação 1. Período de exposição / incubação; 2. Período de transmissibilidade ; 3. Período de aparecimento de casos secundários;
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS HEPATITES VIRAIS. Adriéli Wendlant
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS HEPATITES VIRAIS Adriéli Wendlant Hepatites virais Grave problema de saúde pública No Brasil, as hepatites virais
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS VETERINÁRIAS HEPATITES VIRAIS Adriéli Wendlant Hepatites virais Grave problema de saúde pública No Brasil, as hepatites virais
Esplanada dos Ministérios, Edifício Principal, 2º andar Brasília-DF Tel. (061) NOTA TÉCNICA N.º 161 /2010 DEVEP/SVS/MS
 MINISTÉRIO DA SAÚDE SECRETARIA DE VIGILÂNCIA EM SAÚDE DEPARTAMENTO DE VIGILÂNCIA EPIDEMIOLÓGICA Esplanada dos Ministérios, Edifício Principal, 2º andar 70.304-000 Brasília-DF Tel. (061) 3213-8095 NOTA
MINISTÉRIO DA SAÚDE SECRETARIA DE VIGILÂNCIA EM SAÚDE DEPARTAMENTO DE VIGILÂNCIA EPIDEMIOLÓGICA Esplanada dos Ministérios, Edifício Principal, 2º andar 70.304-000 Brasília-DF Tel. (061) 3213-8095 NOTA
Introdução a Virologia. Definição - O que é vírus? Composição e estrutura Genoma e Replicação
 Introdução a Virologia Definição - O que é vírus? Composição e estrutura Genoma e Replicação O que é vírus? Agentes infecciosos ultramicroscópicos Não são células São partículas filtráveis Só apresentam
Introdução a Virologia Definição - O que é vírus? Composição e estrutura Genoma e Replicação O que é vírus? Agentes infecciosos ultramicroscópicos Não são células São partículas filtráveis Só apresentam
Enfermidades Micóticas
 Enfermidades Micóticas Msc. Larissa Pickler Departamento de Medicina Veterinária Universidade Federal do Paraná Disciplina de Doenças das Aves Curitiba Paraná Brasil 2011 Enfermidades Micóticas Infecções
Enfermidades Micóticas Msc. Larissa Pickler Departamento de Medicina Veterinária Universidade Federal do Paraná Disciplina de Doenças das Aves Curitiba Paraná Brasil 2011 Enfermidades Micóticas Infecções
O que vamos compartilhar. Influenza Suína: avaliação de patogenicidade isolada ou combinada a outros agentes. O vírus. Publicações (Camp.
 Influenza Suína: avaliação de patogenicidade isolada ou combinada a outros agentes Edson Luiz Bordin MV, patologista A influenza suína (SIV) - ontem 1918» A SIV foi primeiro reconhecida clinicamente em
Influenza Suína: avaliação de patogenicidade isolada ou combinada a outros agentes Edson Luiz Bordin MV, patologista A influenza suína (SIV) - ontem 1918» A SIV foi primeiro reconhecida clinicamente em
Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194
 Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194 Imunologia das Viroses Monitor: Daniel Valente 1.Introdução...
Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194 Imunologia das Viroses Monitor: Daniel Valente 1.Introdução...
Retrovírus Felinos. Fernando Finoketti
 Retrovírus Felinos Fernando Finoketti Porto Alegre, Rio Grande do Sul, Brasil Maio de 2014 Retrovírus - Características Capsídeo icosaédrico. Possuem envelope. Genoma composto de duas moléculas idênticas
Retrovírus Felinos Fernando Finoketti Porto Alegre, Rio Grande do Sul, Brasil Maio de 2014 Retrovírus - Características Capsídeo icosaédrico. Possuem envelope. Genoma composto de duas moléculas idênticas
ESPECÍFICO DE ENFERMAGEM PROF. CARLOS ALBERTO
 ESPECÍFICO DE ENFERMAGEM PROF. CARLOS ALBERTO CONCURSO HOSPITAL UNIVERSITÁRIO ESPECÍFICO DE ENFERMAGEM TEMA 11 PROGRAMA NACIONAL DE IMUNIZAÇÃO DESENVOLVIMENTO DE VACINAS O que faz uma vacina? Estimula
ESPECÍFICO DE ENFERMAGEM PROF. CARLOS ALBERTO CONCURSO HOSPITAL UNIVERSITÁRIO ESPECÍFICO DE ENFERMAGEM TEMA 11 PROGRAMA NACIONAL DE IMUNIZAÇÃO DESENVOLVIMENTO DE VACINAS O que faz uma vacina? Estimula
Influenza aviária ( gripe aviária ) e o significado de sua transmissão aos humanos
 Influenza aviária ( gripe aviária ) e o significado de sua transmissão aos humanos Informativo (Fact sheet) - 15/01/2004 A doença nas aves: impacto e medidas de controle A influenza aviária é uma doença
Influenza aviária ( gripe aviária ) e o significado de sua transmissão aos humanos Informativo (Fact sheet) - 15/01/2004 A doença nas aves: impacto e medidas de controle A influenza aviária é uma doença
REDE LABORATORIAL DE DENGUE
 Capacitação em Eventos REDE LABORATORIAL Área de Produção Editorial e Gráfica Núcleo de Comunicação Secretaria de Vigilância em Saúde DE DENGUE 23 e 24 de junho de 2010 CGLAB/SVS/MS Vanessa.porto@saude.gov.br
Capacitação em Eventos REDE LABORATORIAL Área de Produção Editorial e Gráfica Núcleo de Comunicação Secretaria de Vigilância em Saúde DE DENGUE 23 e 24 de junho de 2010 CGLAB/SVS/MS Vanessa.porto@saude.gov.br
A BIOLOGIA MOLECULAR NA PRODUÇÃO DE IMUNOBIOLÓGICOS
 A BIOLOGIA MOLECULAR NA PRODUÇÃO DE IMUNOBIOLÓGICOS PRODUÇÃO DE INSUMOS BIOLÓGICOS GENE PLASMÍDEO HOSPEDEIRO TRANSCRIÇÃO - RNA TRADUÇÃO - PROTEÍNA PURIFICAÇÃO PLASMÍEO PADRÃO Amp R Ori Promotor Eco RI
A BIOLOGIA MOLECULAR NA PRODUÇÃO DE IMUNOBIOLÓGICOS PRODUÇÃO DE INSUMOS BIOLÓGICOS GENE PLASMÍDEO HOSPEDEIRO TRANSCRIÇÃO - RNA TRADUÇÃO - PROTEÍNA PURIFICAÇÃO PLASMÍEO PADRÃO Amp R Ori Promotor Eco RI
Universidade Federal de Pelotas Medicina Veterinária Zoonoses. Diagnóstico laboratorial Brucelose TESTE DO 2-MERCAPTOETANOL
 Universidade Federal de Pelotas Medicina Veterinária Zoonoses Diagnóstico laboratorial Brucelose TESTE DO 2-MERCAPTOETANOL Teste do 2-ME Confirmativa (infecção crônica) Laboratório credenciado / oficial
Universidade Federal de Pelotas Medicina Veterinária Zoonoses Diagnóstico laboratorial Brucelose TESTE DO 2-MERCAPTOETANOL Teste do 2-ME Confirmativa (infecção crônica) Laboratório credenciado / oficial
Infecções causadas por microrganismos multi-resistentes: medidas de prevenção e controle.
 INFORME TÉCNICO XXXVII Outubro 2010 Infecções causadas por microrganismos multi-resistentes: medidas de prevenção e controle. Definição de microorganismos multi-resistentes: São microrganismos resistentes
INFORME TÉCNICO XXXVII Outubro 2010 Infecções causadas por microrganismos multi-resistentes: medidas de prevenção e controle. Definição de microorganismos multi-resistentes: São microrganismos resistentes
Tuberculose. Definição Enfermidade infecto-contagiosa evolução crônica lesões de aspecto nodular - linfonodos e pulmão Diversos animais Zoonose
 1 2 3 Tuberculose Definição Enfermidade infecto-contagiosa evolução crônica lesões de aspecto nodular - linfonodos e pulmão Diversos animais Zoonose ETIOLOGIA Família: Mycobacteriaceae Ordem: Actinomycetalis
1 2 3 Tuberculose Definição Enfermidade infecto-contagiosa evolução crônica lesões de aspecto nodular - linfonodos e pulmão Diversos animais Zoonose ETIOLOGIA Família: Mycobacteriaceae Ordem: Actinomycetalis
Mastite ou mamite é um processo inflamatório da glândula mamária causada pelos mais diversos agentes. Os mais comuns são as bactérias dos gêneros
 1 Mastite ou mamite é um processo inflamatório da glândula mamária causada pelos mais diversos agentes. Os mais comuns são as bactérias dos gêneros estreptococos e estafilococos, além dos coliformes. A
1 Mastite ou mamite é um processo inflamatório da glândula mamária causada pelos mais diversos agentes. Os mais comuns são as bactérias dos gêneros estreptococos e estafilococos, além dos coliformes. A
PRINCIPAIS AVANÇOS NA PRODUÇÃO DO PIRARUCU:
 PRINCIPAIS AVANÇOS NA PRODUÇÃO DO PIRARUCU: OPORTUNIDADES, DESAFIOS E PERSPECTIVAS MARTIN HALVERSON DIRETOR TECNOLÓGICO: PROJETO PACU AQUICULTURA TEMAS GERAIS Estado da Tecnologia Oportunidades Problemas
PRINCIPAIS AVANÇOS NA PRODUÇÃO DO PIRARUCU: OPORTUNIDADES, DESAFIOS E PERSPECTIVAS MARTIN HALVERSON DIRETOR TECNOLÓGICO: PROJETO PACU AQUICULTURA TEMAS GERAIS Estado da Tecnologia Oportunidades Problemas
Ministério da Saúde Plano Brasileiro de Preparação para uma Pandemia de Influenza
 Ministério da Saúde Plano Brasileiro de Preparação para uma Pandemia de Influenza Jarbas Barbosa da Silva Jr Secretário de Vigilância em Saúde Rio de Janeiro, novembro de 2005 Cenário Mundial da Influenza
Ministério da Saúde Plano Brasileiro de Preparação para uma Pandemia de Influenza Jarbas Barbosa da Silva Jr Secretário de Vigilância em Saúde Rio de Janeiro, novembro de 2005 Cenário Mundial da Influenza
Carteira de VETPRADO. Hospital Veterinário 24h.
 Carteira de Carteira de VETPRADO Hospital Veterinário 24h www.vetprado.com.br Esquema de VacinaçãoGatos V5 Panleucopenia - Rinotraqueíte - Calicivirose Clamidiose - Leucemia Felina 90Dias 111Dias Raiva
Carteira de Carteira de VETPRADO Hospital Veterinário 24h www.vetprado.com.br Esquema de VacinaçãoGatos V5 Panleucopenia - Rinotraqueíte - Calicivirose Clamidiose - Leucemia Felina 90Dias 111Dias Raiva
de laboratório em pesquisas Segurança dos animais Segurança do experimentador
 Segurança no uso de animais de laboratório em pesquisas Segurança dos animais Ética no uso dos animais Segurança do experimentador Como em qualquer laboratório, pratique Boas Praticas Laboratoriais no
Segurança no uso de animais de laboratório em pesquisas Segurança dos animais Ética no uso dos animais Segurança do experimentador Como em qualquer laboratório, pratique Boas Praticas Laboratoriais no
VÍRUS QUE AFETAM O TRATO RESPIRATÓRIO (Parte 1)
 Universidade Federal do Rio Grande do Sul Departamento de Microbiologia, Imunologia e Parasitologia VÍRUS QUE AFETAM O TRATO RESPIRATÓRIO (Parte 1) Fabrício Souza Campos Pós-doc Laboratório de Virologia
Universidade Federal do Rio Grande do Sul Departamento de Microbiologia, Imunologia e Parasitologia VÍRUS QUE AFETAM O TRATO RESPIRATÓRIO (Parte 1) Fabrício Souza Campos Pós-doc Laboratório de Virologia
Tópicos de Imunologia Celular e Molecular (Parte 2)
 IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
MENINGITE E DOENÇA MENINGOCÓCICA. Profa. Maria Lucia Penna Disciplina de Epidemiologia IV
 MENINGITE E DOENÇA MENINGOCÓCICA Profa. Maria Lucia Penna Disciplina de Epidemiologia IV Quais são os principais agentes da meningite? Etiologia meningites Brasil 2007-2010 (fonte: SINAN) Etiologia
MENINGITE E DOENÇA MENINGOCÓCICA Profa. Maria Lucia Penna Disciplina de Epidemiologia IV Quais são os principais agentes da meningite? Etiologia meningites Brasil 2007-2010 (fonte: SINAN) Etiologia
(seleção, sexagem, vacinação, condições de armazenagem, temperatura umidade e ventilação da sala, expedição dos pintos).
 a arte de incubar parte 4 sala de pintos (seleção, sexagem, vacinação, condições de armazenagem, temperatura umidade e ventilação da sala, expedição dos pintos). Os manejos de Sala de Pintos dependem da
a arte de incubar parte 4 sala de pintos (seleção, sexagem, vacinação, condições de armazenagem, temperatura umidade e ventilação da sala, expedição dos pintos). Os manejos de Sala de Pintos dependem da
DEFINIÇÕES EM EPIDEMIOLOGIA MOLECULAR E CONCEITOS BÁSICOS EM BIOLOGIA MOLECULAR
 DEFINIÇÕES EM E DEFINIÇÕES EM E CONCEITOS BÁSICOS EM BIOLOGIA PARA QUE SERVE ESTA AULA 1. DEFINIÇÕES EM CONCEITUAÇÃO DE DIFERENCIAÇÃO ENTRE, TAXONOMIA E FILOGENIA 2. CONCEITOS EM BIOLOGIA APRESENTAR (REVER)
DEFINIÇÕES EM E DEFINIÇÕES EM E CONCEITOS BÁSICOS EM BIOLOGIA PARA QUE SERVE ESTA AULA 1. DEFINIÇÕES EM CONCEITUAÇÃO DE DIFERENCIAÇÃO ENTRE, TAXONOMIA E FILOGENIA 2. CONCEITOS EM BIOLOGIA APRESENTAR (REVER)
Universidade Federal de Pelotas Departamento de Veterinária Preventiva Toxoplasmose Zoonoses e Administração em Saúde Pública
 Universidade Federal de Pelotas Departamento de Veterinária Preventiva Toxoplasmose Zoonoses e Administração em Saúde Pública Fábio Raphael Pascoti Bruhn Por que estudar a toxoplasmose Zoonose Nos EUA,
Universidade Federal de Pelotas Departamento de Veterinária Preventiva Toxoplasmose Zoonoses e Administração em Saúde Pública Fábio Raphael Pascoti Bruhn Por que estudar a toxoplasmose Zoonose Nos EUA,
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 5 1. NOME DO MEDICAMENTO VETERINÁRIO PORCILIS APP, suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada dose de 2 ml contém:
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO Página 1 de 5 1. NOME DO MEDICAMENTO VETERINÁRIO PORCILIS APP, suspensão injetável para suínos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Cada dose de 2 ml contém:
15/10/2009 GENÉTICA BACTERIANA. Disciplina: Microbiologia Geral Curso: Nutrição Prof. Renata Fernandes Rabello. Informação genética essencial.
 GENÉTICA BACTERIANA GENOMA BACTERIANO Cromossoma (nucleóide) Informação genética essencial. Ácido desoxirribonucléico (DNA). Disciplina: Microbiologia Geral Curso: Nutrição Prof. Renata Fernandes Rabello
GENÉTICA BACTERIANA GENOMA BACTERIANO Cromossoma (nucleóide) Informação genética essencial. Ácido desoxirribonucléico (DNA). Disciplina: Microbiologia Geral Curso: Nutrição Prof. Renata Fernandes Rabello
A IMPORTÂNCIA DA VACINA CONTRA ROTAVÍRUS NA POPULAÇÃO PEDIÁTRICA
 A IMPORTÂNCIA DA VACINA CONTRA ROTAVÍRUS NA POPULAÇÃO PEDIÁTRICA BARCELLOS, R. C. * PIRES, T. B. O. * PEREIRA, A. S. M. ** AGUIAR, M. B. ** NEVES, K. S. *** MOTTA, C. F. **** COUTINHO, J. S. **** RESUMO
A IMPORTÂNCIA DA VACINA CONTRA ROTAVÍRUS NA POPULAÇÃO PEDIÁTRICA BARCELLOS, R. C. * PIRES, T. B. O. * PEREIRA, A. S. M. ** AGUIAR, M. B. ** NEVES, K. S. *** MOTTA, C. F. **** COUTINHO, J. S. **** RESUMO
Imunologia. Propriedades das Respostas imunes e órgãos linfóides. Bibliografia Básica. Introdução. Tipos de imunidade. Histórico 12/03/2012
 Bibliografia Básica Imunologia Prof. Dr. Gilson C. Macedo www.ufjf.br/imunologia Introdução Propriedades das Respostas imunes e órgãos linfóides Prof: Dr. Gilson C. Macedo Derivado do latim immunitas Refere-se
Bibliografia Básica Imunologia Prof. Dr. Gilson C. Macedo www.ufjf.br/imunologia Introdução Propriedades das Respostas imunes e órgãos linfóides Prof: Dr. Gilson C. Macedo Derivado do latim immunitas Refere-se
SORGO - UMA BOA ALTERNATIVA PARA REDUÇÃO DOS CUSTOS DE ALIMENTAÇÃO
 Data: Junho/2001 SORGO - UMA BOA ALTERNATIVA PARA REDUÇÃO DOS CUSTOS DE ALIMENTAÇÃO Estamos iniciando a colheita de uma safra de Sorgo, que segundo estimativas deve girar ao redor de 1,350 a 1,500 milhões
Data: Junho/2001 SORGO - UMA BOA ALTERNATIVA PARA REDUÇÃO DOS CUSTOS DE ALIMENTAÇÃO Estamos iniciando a colheita de uma safra de Sorgo, que segundo estimativas deve girar ao redor de 1,350 a 1,500 milhões
UNIVERSIDADE PRESBITERIANA MACKENZIE
 Unidade Universitária CENTRO DE CIÊNCIAS BIOLÓGICAS E DA SAÚDE Curso: Farmácia Disciplina: Imunologia Básica Código da Disciplina 02014890 Professor(es) Yoshimi Imoto Yamamoto Etapa 4ª. Carga horária:
Unidade Universitária CENTRO DE CIÊNCIAS BIOLÓGICAS E DA SAÚDE Curso: Farmácia Disciplina: Imunologia Básica Código da Disciplina 02014890 Professor(es) Yoshimi Imoto Yamamoto Etapa 4ª. Carga horária:
IMUNOLOGIA. Prof. Fausto de Souza Aula 10: Imunização Passiva e Ativa Vacinas
 IMUNOLOGIA Prof. Fausto de Souza Aula 10: Imunização Passiva e Ativa Vacinas Imunização passiva Imunização passiva transferência de anticorpos produzidos por um animal ou outro homem. Esse tipo de imunidade
IMUNOLOGIA Prof. Fausto de Souza Aula 10: Imunização Passiva e Ativa Vacinas Imunização passiva Imunização passiva transferência de anticorpos produzidos por um animal ou outro homem. Esse tipo de imunidade
KITS DE EXTRAÇÃO DNA E RNA
 ACERTE COM PRECISÃO KITS DE EXTRAÇÃO DNA E RNA A Linha Biopur para extração e purificação de DNA e RNA possui kits variados com tecnologia para procedimentos manual (Mini Spin e Mini Cent) e para automação
ACERTE COM PRECISÃO KITS DE EXTRAÇÃO DNA E RNA A Linha Biopur para extração e purificação de DNA e RNA possui kits variados com tecnologia para procedimentos manual (Mini Spin e Mini Cent) e para automação
Diagnóstico Laboratorial da Febre Amarela
 Diagnóstico Laboratorial da Febre Amarela Vinícius Lemes da Silva Seção de Virologia Laboratório Central de Saúde Pública Dr. Giovanni Cysneiros Diagnóstico laboratorial Finalidades: Confirmação laboratorial
Diagnóstico Laboratorial da Febre Amarela Vinícius Lemes da Silva Seção de Virologia Laboratório Central de Saúde Pública Dr. Giovanni Cysneiros Diagnóstico laboratorial Finalidades: Confirmação laboratorial
Assunto: Atualização da investigação de caso suspeito de sarampo em João Pessoa/PB - 22 de outubro de 2010
 MINISTÉRIO DA SAÚDE SECRETARIA DE VIGILÂNCIA EM SAÚDE Departamento de Vigilância Epidemiológica Esplanada dos Ministérios, Edifício Sede, 1º andar 70.058-900 Brasília-DF Tel. 3315 2755/2812 NOTA TÉCNICA
MINISTÉRIO DA SAÚDE SECRETARIA DE VIGILÂNCIA EM SAÚDE Departamento de Vigilância Epidemiológica Esplanada dos Ministérios, Edifício Sede, 1º andar 70.058-900 Brasília-DF Tel. 3315 2755/2812 NOTA TÉCNICA
Epidemiologia e Controle de Salmonella na Produção de Aves
 Mercolab Cascavel/PR, Brasil (09 Out. 2014) Epidemiologia e Controle de Salmonella na Produção de Aves Marcos H. Rostagno Consultor Técnico Global Professor Adjunto Salmonella e sua complexidade Daniel
Mercolab Cascavel/PR, Brasil (09 Out. 2014) Epidemiologia e Controle de Salmonella na Produção de Aves Marcos H. Rostagno Consultor Técnico Global Professor Adjunto Salmonella e sua complexidade Daniel
CAPÍTULO 6: COMPOSTOS ORGÂNICOS PROTEÍNAS CAP. 7: COMPOSTOS ORGÂNICOS ÁCIDOS NUCLEICOS E VITAMINAS
 CAPÍTULO 6: COMPOSTOS ORGÂNICOS PROTEÍNAS CAP. 7: COMPOSTOS ORGÂNICOS ÁCIDOS NUCLEICOS E VITAMINAS 1. Dentre os diferentes compostos orgânicos das células temos as proteínas. Sobre estas responda: a) Cite
CAPÍTULO 6: COMPOSTOS ORGÂNICOS PROTEÍNAS CAP. 7: COMPOSTOS ORGÂNICOS ÁCIDOS NUCLEICOS E VITAMINAS 1. Dentre os diferentes compostos orgânicos das células temos as proteínas. Sobre estas responda: a) Cite
FARMACOVIGILÂNCIA A QUALIDADE FQM EM SUAS MÃOS ENTENDA MANUAL COMO E POR QUE. RELATAR EventoS AdversoS
 FARMACOVIGILÂNCIA A QUALIDADE FQM EM SUAS MÃOS MANUAL ENTENDA COMO E POR QUE RELATAR EventoS AdversoS Apresentação O desastre da Talidomida no final da década de 50 foi um marco mundial na história da
FARMACOVIGILÂNCIA A QUALIDADE FQM EM SUAS MÃOS MANUAL ENTENDA COMO E POR QUE RELATAR EventoS AdversoS Apresentação O desastre da Talidomida no final da década de 50 foi um marco mundial na história da
SISTEMA IMUNITÁRIO ou IMUNOLÓGICO. O sangue e as defesas corporais
 SISTEMA IMUNITÁRIO ou IMUNOLÓGICO O sangue e as defesas corporais INTRODUÇÃO Promove o combate a microrganismos invasores e a limpeza do organismo (retirada de células mortas e de células alteradas) Altamente
SISTEMA IMUNITÁRIO ou IMUNOLÓGICO O sangue e as defesas corporais INTRODUÇÃO Promove o combate a microrganismos invasores e a limpeza do organismo (retirada de células mortas e de células alteradas) Altamente
COMPORTAMENTO HISTÓRICO DA PARTICIPAÇÃO DO SETOR RURAL NA COMPOSIÇÃO DO PIB DA PARAÍBA
 1 COMPORTAMENTO HISTÓRICO DA PARTICIPAÇÃO DO SETOR RURAL NA COMPOSIÇÃO DO PIB DA PARAÍBA Sérgio Furtado - Consultor do Projeto Cooperar 1 DESEMPENHO DAS ATIVIDADES ECONÔMICAS NO ESTADO DA PARAÍBA EM 2012
1 COMPORTAMENTO HISTÓRICO DA PARTICIPAÇÃO DO SETOR RURAL NA COMPOSIÇÃO DO PIB DA PARAÍBA Sérgio Furtado - Consultor do Projeto Cooperar 1 DESEMPENHO DAS ATIVIDADES ECONÔMICAS NO ESTADO DA PARAÍBA EM 2012
DIAGNÓSTICO IMUNOLÓGICO DAS INFECÇÕES POR DENGUE, CHIKUNGUNYA E ZIKA VÍRUS
 DIAGNÓSTICO IMUNOLÓGICO DAS INFECÇÕES POR DENGUE, CHIKUNGUNYA E ZIKA VÍRUS Prof. Dra. Edna Maria Vissoci Reiche Imunologia Clínica Diagnóstico Molecular PAC/CCS/UEL Dengue vírus da dengue Flavivírus RNA
DIAGNÓSTICO IMUNOLÓGICO DAS INFECÇÕES POR DENGUE, CHIKUNGUNYA E ZIKA VÍRUS Prof. Dra. Edna Maria Vissoci Reiche Imunologia Clínica Diagnóstico Molecular PAC/CCS/UEL Dengue vírus da dengue Flavivírus RNA
Depoimento sobre diagnóstico molecular
 Gumboro Doença Infecciosa da Bolsa de Fabrício (DIB) causa altos prejuízos econômicos aos produtores. A doença de Gumboro ou Doença Infecciosa da Bolsa de Fabrício (DIB) é uma infecção viral aguda, altamente
Gumboro Doença Infecciosa da Bolsa de Fabrício (DIB) causa altos prejuízos econômicos aos produtores. A doença de Gumboro ou Doença Infecciosa da Bolsa de Fabrício (DIB) é uma infecção viral aguda, altamente
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Nobilis RT+IBmulti+G+ND 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose de 0,5 ml: Substâncias ativas: ART estirpe But1#8544:
RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1. NOME DO MEDICAMENTO VETERINÁRIO Nobilis RT+IBmulti+G+ND 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose de 0,5 ml: Substâncias ativas: ART estirpe But1#8544:
GOVERNO DO ESTADO DO CEARÁ Secretaria da Saúde
 Considerando a confirmação de um caso de sarampo e quatro fortemente suspeitos no Ceará; Considerando a confirmação de surto de sarampo em Pernambuco e casos confirmados relacionados à importação, nos
Considerando a confirmação de um caso de sarampo e quatro fortemente suspeitos no Ceará; Considerando a confirmação de surto de sarampo em Pernambuco e casos confirmados relacionados à importação, nos
RESÍDUOS DE PRODUTOS VETERINÁRIOS E SEU CONTROLE PROGRAMA ELABORADO POR
 RESÍDUOS DE PRODUTOS VETERINÁRIOS E SEU CONTROLE PROGRAMA ELABORADO POR O QUE SÃO RESÍDUOS QUÍMICOS? São vestígios de substâncias que podem ser encontrados nos alimentos de origem animal (carne, leite
RESÍDUOS DE PRODUTOS VETERINÁRIOS E SEU CONTROLE PROGRAMA ELABORADO POR O QUE SÃO RESÍDUOS QUÍMICOS? São vestígios de substâncias que podem ser encontrados nos alimentos de origem animal (carne, leite
Prevenção e controle das viroses. Silvia Cavalcanti Universidade Federal Fluminense Departamento de Microbiologia e Parasitologia 2016
 Prevenção e controle das viroses Silvia Cavalcanti Universidade Federal Fluminense Departamento de Microbiologia e Parasitologia 2016 Prevenção e controle das viroses Entendimento da epidemiologia das
Prevenção e controle das viroses Silvia Cavalcanti Universidade Federal Fluminense Departamento de Microbiologia e Parasitologia 2016 Prevenção e controle das viroses Entendimento da epidemiologia das
Redalyc. Disponible en:
 Redalyc Sistema de Información Científica Red de Revistas Científicas de América Latina, el Caribe, España y Portugal Mendonça, Juliana Figueiredo Pitangui; Silva Martins, Nelson Rodrigo da; Carvalho,
Redalyc Sistema de Información Científica Red de Revistas Científicas de América Latina, el Caribe, España y Portugal Mendonça, Juliana Figueiredo Pitangui; Silva Martins, Nelson Rodrigo da; Carvalho,
2.Introdução A Doença Descrição...11
 Índice 1.Apresentação... 05 2.Introdução...07 3.A Doença... 11 3.1. Descrição...11 3.2. Epidemiologia... 11 3.2.1. Agente Etiológico e Ciclo Evolutivo...11 3.2.2. Reservatórios / Hospedeiros Intermediários...
Índice 1.Apresentação... 05 2.Introdução...07 3.A Doença... 11 3.1. Descrição...11 3.2. Epidemiologia... 11 3.2.1. Agente Etiológico e Ciclo Evolutivo...11 3.2.2. Reservatórios / Hospedeiros Intermediários...
BEM-ESTAR EM AVES. DEFINIÇÃO OIE (World Organization For Animal Health)
 Flávia Bornancini Borges Fortes Médica Veterinária, MsC. CRMV 8269 Fiscal Estadual Agropecuário Programa Estadual de Sanidade Avícola Seminário de Responsabilidade Técnica Sanidade Animal e Saúde Pública
Flávia Bornancini Borges Fortes Médica Veterinária, MsC. CRMV 8269 Fiscal Estadual Agropecuário Programa Estadual de Sanidade Avícola Seminário de Responsabilidade Técnica Sanidade Animal e Saúde Pública
EPIDEMIOLOGIA DAS INFECÇÕES VIRAIS L A B V I R - I C B S U F R G S 2015
 EPIDEMIOLOGIA DAS INFECÇÕES VIRAIS L A B V I R - I C B S U F R G S 2015 EPIDEMIOLOGIA Estudo das doenças em populações, investigando os seus determinantes, a sua dinâmica e distribuição. VÍRUS Partícula
EPIDEMIOLOGIA DAS INFECÇÕES VIRAIS L A B V I R - I C B S U F R G S 2015 EPIDEMIOLOGIA Estudo das doenças em populações, investigando os seus determinantes, a sua dinâmica e distribuição. VÍRUS Partícula
Tipificação e Classificação de Carcaças Bovinas (1/3) Será feita uma revisão bibliográfica seguindo o cronograma abaixo:
 Tipificação e Classificação de Carcaças Bovinas (1/3) Será feita uma revisão bibliográfica seguindo o cronograma abaixo: 1. Introdução e uma rápida revisão bibliográfica sobre o assunto. 2. Classificação
Tipificação e Classificação de Carcaças Bovinas (1/3) Será feita uma revisão bibliográfica seguindo o cronograma abaixo: 1. Introdução e uma rápida revisão bibliográfica sobre o assunto. 2. Classificação
artus EBV QS-RGQ Kit Características de desempenho Maio 2012 Sample & Assay Technologies Sensibilidade analítica plasma
 artus EBV QS-RGQ Kit Características de desempenho artus EBV QS-RGQ Kit, Versão 1, 4501363 Verificar a disponibilidade de novas revisões de rotulagem electrónica em www.qiagen.com/products/artuscmvpcrkitce.aspx
artus EBV QS-RGQ Kit Características de desempenho artus EBV QS-RGQ Kit, Versão 1, 4501363 Verificar a disponibilidade de novas revisões de rotulagem electrónica em www.qiagen.com/products/artuscmvpcrkitce.aspx
Imunoterapia - tumores. Material de apoio: Anderson (2009)
 Imunoterapia - tumores Material de apoio: Anderson (2009) Auto-antigénios / antigénios autólogos (self antigens) Antigénios / Antigénios heterólogos (non-self antigens) Tratamento com anticorpos (monoclonais)
Imunoterapia - tumores Material de apoio: Anderson (2009) Auto-antigénios / antigénios autólogos (self antigens) Antigénios / Antigénios heterólogos (non-self antigens) Tratamento com anticorpos (monoclonais)
Influenza aviária. 28ago
 28ago 2015 Influenza aviária Por Dra. Tania Maria de Paula Lyra* 1. Introdução A Influenza aviária é uma doença causada por um vírus, que possui diferentes subtipos. Até a data atual todos os vírus altamente
28ago 2015 Influenza aviária Por Dra. Tania Maria de Paula Lyra* 1. Introdução A Influenza aviária é uma doença causada por um vírus, que possui diferentes subtipos. Até a data atual todos os vírus altamente
PATOGENICIDADE BACTERIANA
 PATOGENICIDADE BACTERIANA Fatores de de Virulência Instituto Federal de Educação, Ciência e Tecnologia do Pará Instituto Federal de Educação, Ciência e Tecnologia do Pará Curso de Licenciatura Plena em
PATOGENICIDADE BACTERIANA Fatores de de Virulência Instituto Federal de Educação, Ciência e Tecnologia do Pará Instituto Federal de Educação, Ciência e Tecnologia do Pará Curso de Licenciatura Plena em
Criopreservação de Embriões
 UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA BIOTECNOLOGIA DA REPRODUÇÃO ANIMAL Criopreservação de Embriões Vicente José de F. Freitas Laboratório de Fisiologia e Controle da Reprodução www.uece.br/lfcr
UNIVERSIDADE ESTADUAL DO CEARÁ FACULDADE DE VETERINÁRIA BIOTECNOLOGIA DA REPRODUÇÃO ANIMAL Criopreservação de Embriões Vicente José de F. Freitas Laboratório de Fisiologia e Controle da Reprodução www.uece.br/lfcr
Vigilância Sanitária de Alimentos. Bactérias causadoras de Doenças Transmitidas por Alimentos (DTAs)- II
 Vigilância Sanitária de Alimentos Bactérias causadoras de Doenças Transmitidas por Alimentos (DTAs)- II Clostridium perfringens Intestino Microbiota normal Solo Água Produto cárneo Clostridium perfringens
Vigilância Sanitária de Alimentos Bactérias causadoras de Doenças Transmitidas por Alimentos (DTAs)- II Clostridium perfringens Intestino Microbiota normal Solo Água Produto cárneo Clostridium perfringens
Classificação viral segundo Baltimore. DNA dupla fita DNA simples fita DNA dupla fita DNA dupla fita RNA fita+ RNA fita + mrna RNA fita +
 Processos de Replicação Viral Vírus com genoma a RNA Classificação viral segundo Baltimore. DNA dupla fita DNA dupla fita RNA fita+ RNA fita + DNA dupla fita mrna DNA simples fita DNA dupla fita RNA fita
Processos de Replicação Viral Vírus com genoma a RNA Classificação viral segundo Baltimore. DNA dupla fita DNA dupla fita RNA fita+ RNA fita + DNA dupla fita mrna DNA simples fita DNA dupla fita RNA fita
Esta avaliação é composta de 13 questões, das quais você deverá escolher apenas 10 para responder.
 2º EM Biologia B Marli Av. Trimestral 30/10/15 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta prova
2º EM Biologia B Marli Av. Trimestral 30/10/15 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta prova
[ERLICHIOSE CANINA]
![[ERLICHIOSE CANINA] [ERLICHIOSE CANINA]](/thumbs/46/23432057.jpg) [ERLICHIOSE CANINA] 2 Erlichiose Canina A Erlichiose Canina é uma hemoparasitose causada pela bactéria Erlichia sp. Essa bactéria parasita, geralmente, os glóbulos brancos (neste caso, Erlichia canis)
[ERLICHIOSE CANINA] 2 Erlichiose Canina A Erlichiose Canina é uma hemoparasitose causada pela bactéria Erlichia sp. Essa bactéria parasita, geralmente, os glóbulos brancos (neste caso, Erlichia canis)
PROGRAMA DE DISCIPLINA
 PROGRAMA DE DISCIPLINA Disciplina: Doenças Infecciosas dos Animais Domésticos II Código da Disciplian: VET247 Curso: Medicina Veterinária Semestre de oferta da disciplina: 8 P Faculdade responsável: Medicina
PROGRAMA DE DISCIPLINA Disciplina: Doenças Infecciosas dos Animais Domésticos II Código da Disciplian: VET247 Curso: Medicina Veterinária Semestre de oferta da disciplina: 8 P Faculdade responsável: Medicina
Considerações práticas sobre o uso de enzimas em Poedeiras Comerciais
 Considerações práticas sobre o uso de enzimas em Poedeiras Comerciais Jeffersson Lecznieski Gerente Técnico DSM Produtos Nutricionais Brasil Introdução Devido aos altos e crescentes custos das matérias
Considerações práticas sobre o uso de enzimas em Poedeiras Comerciais Jeffersson Lecznieski Gerente Técnico DSM Produtos Nutricionais Brasil Introdução Devido aos altos e crescentes custos das matérias
Figura 7: Purificação da proteína recombinante MscuOBP8 por HPLC. Eletroforese em gel de poliacrilamida SDS PAGE Mini-PROTEAN TGX Gel Any kd
 Figura 7: Purificação da proteína recombinante MscuOBP8 por HPLC. Eletroforese em gel de poliacrilamida SDS PAGE Mini-PROTEAN TGX Gel Any kd TM (BIO-RAD, USA) submetido à 100 V por 40 minutos e corado
Figura 7: Purificação da proteína recombinante MscuOBP8 por HPLC. Eletroforese em gel de poliacrilamida SDS PAGE Mini-PROTEAN TGX Gel Any kd TM (BIO-RAD, USA) submetido à 100 V por 40 minutos e corado
Epidemiologia. Disciplina: Higiene e profilaxia animal. Fábio Raphael Pascoti Bruhn
 Epidemiologia Disciplina: Higiene e profilaxia animal Fábio Raphael Pascoti Bruhn Epidemiologia Conceito: epi (sobre) + demo (povo) Estudo da distribuição dos estados de saúde e eventos em populações,
Epidemiologia Disciplina: Higiene e profilaxia animal Fábio Raphael Pascoti Bruhn Epidemiologia Conceito: epi (sobre) + demo (povo) Estudo da distribuição dos estados de saúde e eventos em populações,
CARNE AVÍCOLA NOVEMBRO DE 2016
 DEPEC Departamento de Pesquisas e Estudos Econômicos CARNE AVÍCOLA NOVEMBRO DE 2016 O DEPEC BRADESCO não se responsabiliza por quaisquer atos/decisões tomadas com base nas informações disponibilizadas
DEPEC Departamento de Pesquisas e Estudos Econômicos CARNE AVÍCOLA NOVEMBRO DE 2016 O DEPEC BRADESCO não se responsabiliza por quaisquer atos/decisões tomadas com base nas informações disponibilizadas
SISTEMA RESPIRATÓRIO PROF. JAIR
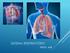 SISTEMA RESPIRATÓRIO PROF. JAIR Fisiologia do Sistema Respiratório A respiração pode ser interpretada como um processo de trocas gasosas entre o organismo e o meio, ou como um conjunto de reações químicas
SISTEMA RESPIRATÓRIO PROF. JAIR Fisiologia do Sistema Respiratório A respiração pode ser interpretada como um processo de trocas gasosas entre o organismo e o meio, ou como um conjunto de reações químicas
Vírus DNA tumorais: PAPILOMAVÍRUS HUMANO (HPV) Testes inespecíficos:
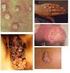 Vírus DNA tumorais: PAPILOMAVÍRUS HUMANO (HPV) Os vírus do papiloma humano são classificados na família Papillomaviridae, gênero Papilomavírus. São vírus envelopados, de simetria icosaédrica, com 72 capsômeros
Vírus DNA tumorais: PAPILOMAVÍRUS HUMANO (HPV) Os vírus do papiloma humano são classificados na família Papillomaviridae, gênero Papilomavírus. São vírus envelopados, de simetria icosaédrica, com 72 capsômeros
AÇÃO DA LUZ SOBRE AS AVES
 AÇÃO DA LUZ SOBRE AS AVES A luz exerce dupla ação nas aves: Estimula função sexual Estabelece o ciclo reprodutivo Alternância entre dia e noite permite sincronização entre animais Ovário (imaturo) = 12.000
AÇÃO DA LUZ SOBRE AS AVES A luz exerce dupla ação nas aves: Estimula função sexual Estabelece o ciclo reprodutivo Alternância entre dia e noite permite sincronização entre animais Ovário (imaturo) = 12.000
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO FACULDADE DE CIÊNCIAS AGRÁRIAS E VETERINÁRIAS CÂMPUS DE JABOTICABAL
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO FACULDADE DE CIÊNCIAS AGRÁRIAS E VETERINÁRIAS CÂMPUS DE JABOTICABAL IMUNIDADE CELULAR E HUMORAL NO TRATO RESPIRATÓRIO DE GALINHAS DESAFIADAS COM O
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO FACULDADE DE CIÊNCIAS AGRÁRIAS E VETERINÁRIAS CÂMPUS DE JABOTICABAL IMUNIDADE CELULAR E HUMORAL NO TRATO RESPIRATÓRIO DE GALINHAS DESAFIADAS COM O
Mecanismos da Patogenicidade Viral I
 Mecanismos da Patogenicidade Viral I Profa. Dra. Mônica Santos de Freitas Patogenicidade Viral Arquitetura do tecido e o sistema imunológico são obstáculos para a infecção viral. A diversidade viral introduz
Mecanismos da Patogenicidade Viral I Profa. Dra. Mônica Santos de Freitas Patogenicidade Viral Arquitetura do tecido e o sistema imunológico são obstáculos para a infecção viral. A diversidade viral introduz
Ontogenia do Linfócito T
 Ontogenia do Linfócito T Processamento e Apresentação de Antígenos para Reconhecimento por TCR Diferente da imunoglobulina, o receptor do linfócito T reconhece antígeno protéico somente quando associado
Ontogenia do Linfócito T Processamento e Apresentação de Antígenos para Reconhecimento por TCR Diferente da imunoglobulina, o receptor do linfócito T reconhece antígeno protéico somente quando associado
