Exercícios. Exercícios QUÍMICA LISTA DE EXERCÍCIOS 1 ANO. Capítulo 1 Introdução ao Estudo da Química. Capítulo 2 Estados Físicos da Matéria
|
|
|
- Herman Lancastre Fernandes
- 5 Há anos
- Visualizações:
Transcrição
1 Capítulo 1 Introdução ao Estudo da Química : 01 São substâncias puras: a) Um copo de água destilada, refrigerante aberto, granito. b) Barra de ouro, refrigerante sem agitar, ar atmosférico puro. c) Água + álcool, pedaço de giz, água. d) Pedaço de giz, anel de ouro, gás ozônio, e) água, álcool etílico, ouro 24 quilates 02 (CTU) Marque a alternativa correta para conceituar molécula, substância simples e composta, respectivamente: a) A menor quantidade de substância, formada de elementos químicos simples e compostos. b) A menor substância, formada de átomos simples e compostos. c) A menor parte de substância, formadas de átomos iguais e diferentes. d) A menor quantidade de matéria, formadas de átomos i- guais e diferentes. e) Nenhuma das afirmativas das letras a, b, c, d. 03 (CTU) Pode-se considerar uma transformação química. a) A obtenção do nitrogênio pela liquefação do ar. b) A transformação do gelo-seco em gás carbônico. c) A explosão da nitroglicerina. d) O fracionamento do petróleo. e) A evaporação da água. 04 É um fenômeno químico a (o): a) mudança de estado d) combustão b) acender uma lâmpada e) reflexão. c) movimento retilíneo 05 Leia os itens abaixo com atenção.tirar uma fotografia 1 Acender uma lâmpada. 2 Digerir alimentos. 3 Escrever neste papel a lápis. 4 Fumar um cigarro. 5 Dar um tiro com um revolver calibre Um avião a jato voando. 7 Ferver a água num fogareiro elétrico. 8 Ferver a água num fogareiro a lenha. 9 Chuva de granizo. 08 Marque a opção onde só aparecem substâncias simples. a) ferro (Fe), gás cloro (Cl 2), ozônio (O 3) b) glicose (C 6H 120 6), enxofre (S 8), álcool etílico (C 2H 6O) c) gasolina (C 8H 18+C 7H 16), vinagre (CH 3COOH+H 2O), hidrogênio (H 2) d) éter (C 2H 6O), tetracloreto de carbono (CCl 4), água (H 2O) e) cobre (Cu), mercúrio (Hg), gás de cozinha (C 3H 8+C 4H 10) 09 (UFMG) Todos os fenômenos descritos são exemplos de reações químicas, exceto: a) dissolução de um comprimido efervescente; b) eletrólise da água; c) enferrujamento de um prego exposto no ar; d) fusão de parafina; e) queima de uma vela. 10 (UFMG) Todos os fenômenos descritos são caracterizados como reações químicas, exceto: a) a queima de madeira; b) a fritura de batatas; c) o preparo de limonada; d) o amadurecimento de bananas; e) o tratamento da água de piscina. Capítulo 2 Estados Físicos da Matéria : 01 Todas as transformações abaixo ocorrem com absorção de calor, exceto: a) condensação de vapor d'água; b) fusão de uma barra de ferro; c) vaporização do álcool; d) transformação de gelo em água; e) transformação de iodo sólido em vapor de iodo. 02 Considerando T = 25 C e P = 1 atm, sublimação é uma mudança de estado que ocorre: a) com determinadas substâncias líquidas; b) com a maioria das substâncias sólidas; c) com todas as substâncias gasosas; d) com determinadas substâncias sólidas; e) com a maioria das substâncias gasosas. 03 (UFMG) Um sólido quimicamente puro é aquecido. Essa substância se funde, e, posteriormente, se vaporiza. As transformações ocorridas estão corretamente representadas pelo gráfico: a) d) São fenômenos químicos: a) 1, 2, 3, 5, 8 e 9 c) 3, 5, 6, 9 e 10 e) N.R.A. b) 1, 3, 5, 9 e 10 d) 1, 3, 5 06 Das alternativas abaixo, indique a única onde são mencionadas apenas substâncias compostas: a) He, Ne, Kr, Ar, Xe d) O 3, I 3 b) S 8, Cl 2 e) H 2O, H 2S, H 2Se c) F 2, Cl 2,Br 2, I 2 b) e) 07 São substância simples a) H 2O, O 2, F 2 c) Cl 2, NO, P 4 e) NaCI, H 2O, O 2 b) CO 2, H 2, HCl d) N 2, H 2, S 8 CADERNO DE EXERCÍCIOS 1
2 c) metálica superaquecida, observamos a transformação, rapidíssima, do estado líquido ao estado gasoso, denominado: a) calefação c) ebulição b) evaporação d) sublimação 08 (ESA) A água ao se solidificar: a) aumenta sua densidade c) aumenta sua massa b) diminui se volume d) diminui sua densidade 04 O gráfico que melhor representa a condensação do vapor d'água até transformá-lo em gelo, passando pelo estado líquido, é: a) d) b) e) 09 (CTU) O naftaleno, comercialmente conhecido como a naftalina, empregado para evitar baratas em roupas, funde em temperaturas superiores a 80 C. Sabe-se que bolinhas de naftalina, à temperatura ambiente, têm suas massas constantemente diminuídas terminando por desaparecer sem deixar resíduo. Essa observação pode ser explicada pelo fenômeno da: a) fusão c) solidificação e) ebulição b) sublimação d) liquefação 10 As mudanças de estado físico em que um corpo absorve calor são: a) fusão e solidificação d) liquefação e fusão b) fusão e vaporização e) vaporização e solidificação c) solidificação e liquefação Tarefa Extra Questões Discursivas c) 01 Qual é o estado físico das substâncias A, B e C, nas condições ambiente, sabendo que seus pontos de fusão e de ebulição são os seguintes: PF PE A -10 C 50 C B 150 C 800 C C -50 C 10 C 02 Com base nos dados da tabela abaixo, qual é o estado físico da cada substância: 05 (PUC) Dados os gráficos: Substância PF (1atm) PE (1atm) A -180ºC -45ºC B -35ºC 30ºC C 10ºC 120ºC D -60ºC 15ºC E 70ºC 320ºC a) nas condições ambiente (25 C, 1atm)? b) num dia frio, com temperatura de 5 C? c) num dia quente, com temperatura de 35 C? Capítulo 3 As Propriedades da Matéria Qual deles pode indicar o aquecimento de uma substância pura e sua fusão? a) I b) II c) III d) IV 06 (PUC) Considerando os gráficos da questão anterior, responda: Qual deles pode indicar o resfriamento de um líquido e sua solidificação? a) I b) II c) III d) IV e) V 07 (ESA) Ao aproximarmos gotas de água de uma placa 01 - Em uma industria, um operário misturou, inadvertidamente, polietileno (PE), policloreto de vinila (PVC) e poliestireno (PS), limpos e moídos. Para recuperar cada um desses polímeros, utilizou o seguinte método de separação: colocou a mistura em um tanque contendo água (densidade = 1g/cm 3 ), separando, então, a fração que flutuou (fração A) daquela que foi ao fundo (fração B), secou-a e colocou-a em outro tanque contendo solução salina (densidade = 1,10g/cm 3 ), se- CADERNO DE EXERCÍCIOS 2
3 parando o material que flutuou (fração C) daquele que afundou (fração D). POLIMERO DENSIDADE (g/cm 3 ) Polietileno (PE) 0,91 a,098 Poliestireno (PS) 1,04 a 1,06 Policloreto de vinila 1,35 a 1,42 (PVC) As frações A,C e D eram, respectivamente: a) PE, PS, PVC b) PS, PE, PVC c) PVC, PS, PE d) PS, PVC, PE e) PE, PVC, PS 02 Qual a propriedade da matéria de ocupar lugar no espaço? a) inércia d) extensão b) impenetrabilidade e) N.R.A. c) compressibilidade 03 Quando um ônibus pára, nós levamos um "arranco" porque nós adquirimos a velocidade do móvel naquele instante e a tendência é entrarmos em movimento. Que propriedade é essa? a) elasticidade c) peso e) compressibilidade b) divisibilidade d) inércia 04 Dois corpos não ocupam o mesmo lugar no espaço simultaneamente. Qual é a propriedade? (ao mesmo tempo). a) compressibilidade d) divisibilidade b) massa e) inércia c) impenetrabilidade 05 Ao aplicarmos uma força na matéria, causamos a diminuição do volume pela diminuição dos espaços intermoleculares. Qual é a propriedade? a) divisibilidade c) elasticidade e) atrito b) compressibilidade d) inércia 06 E quando cessamos a força que produziu a deformação, a matéria volta ao seu volume e forma iniciais. Qual é a propriedade? a) divisibilidade c) elasticidade e) inércia b) compressibilidade d) atrito 07 A quantidade de calor necessária para elevar a temperatura em 1 C de 1g de substância é o conceito de: a) densidade d) ponto de solidificação b) ponto de condensação e) calor especifico c) ponto de fusão 08 (UFMG) Qualquer das propriedades físicas abaixo pode ser usada para a caracterização de uma substância pura. Exceto: a) ponto de fusão c) solubilidade e) massa b) ponto de ebulição d) densidade 09 (UFMG) Uma coroa contém 579g de ouro (densidade 19,3g/cm 3 ), 90g de cobre (densidade 9,0g/cm 3 ), 105g de prata (densidade 10,5g/cm 3 ). Se o volume final dessa coroa corresponder à soma dos volumes de seus três componentes, a densidade dela, em g/cm 3, será: a) 10,5 b) 12,9 c) 15,5 d) 19,3 e) 38,8 10 Com relação à propriedade geral da matéria denominada EXTENSÃO, podemos afirmar que: a) existe média quantidade da inércia b) todo corpo ocupa lugar o espaço c) ocorre aumento de volume por descompressão d) entre as partículas da matéria há espaços vazios e) ocorre diminuição de volume por compressão. Capítulo 4 Combinação e Mistura 01 Uma mistura de água, álcool e benzeno em determinadas proporções foi submetida a destilação. Com o aquecimento, a temperatura subiu rapidamente a 64,8 C e mantevese invariável até o fim do processo. Trata-se de: a) combinação química c) solução azeotrópica e) n.r.a. b) mistura eutética d) liga eutética 02 Que são misturas eutéticas? a) São aquelas que apresentam uma temperatura constante desde o início até o fim da fusão. b) São as misturas que entram em ebulição a uma temperatura constante. c) São aquelas em que, durante o período da fusão, a temperatura é variável. d) São aquelas em que os seus constituintes não podem ser separados. e) São misturas exclusivamente formadas por três elementos químicos. 03 Pode ser citada como sistema trifásico a mistura de: a) nitrogênio, oxigênio e gás carbônico b) água, etanol e óleo c) água, óleo e areia d) solução aquosa de cloreto de sódio e areia e) vapor d'água, hidrogênio e metano 04 (UFMG) colocando-se em um frasco quantidades iguais de álcool etílico e água destilada, teremos: a) uma solução d) uma substância b) uma espécie química e) um sistema bifásico c) um sistema heterogêneo 05 (PUC-MG) Dados os sistemas: I nitrogênio (g) + oxigênio (g) III água (I) + sacarose (s) II álcool (I) + água (l) IV gasolina (l) + água (I) Constituem sempre sistema homogêneo, qualquer que seja a quantidade: a) somente I e Il c) somente II e IV e) somente I, II e III b) somente I e IV d) somente II e IIl 06 Realizando testes em laboratório, chegou-se as seguintes conclusões a respeito de uma amostra: Fusão de 48 a 55ºC d (g/cm 3 ) de 4,5 a 6,0 Cor amarela Solubilidade insolúvel em água Massa 25 g Podemos afirmar que: a) trata-se de uma substância pura, já que a massa é um número inteiro. b) Trata-se de uma mistura, já que a cor é definida. c) Trata-se de uma mistura, já que o PF e a densidade são variáveis. CADERNO DE EXERCÍCIOS 3
4 d) Não deve ser uma substância pura, já que é insolúvel em água. e) Os dados obtidos são insuficientes para classificar a amostra em substância pura ou mistura. 07 (UFMG) Considere o sistema ilustrado, constituído por água e gelo. Pode-se afirmar corretamente que esse sistema: a) apresenta dois componente b) apresenta três fases c) apresenta um componente e uma fase d) é constituído por uma substância pura e) é homogêneo 08 Sistemas heterogêneo, 4 fases e 6 componentes é a classificação de: a) água líquida com sal de cozinha dissolvido, oxigênio gasoso, vapor d'água, ferro e carvão b) oxigênio gasoso, água com açúcar dissolvido, pedaços de vidro, vapor d'água e gelo c) ouro, manganês, vapor d'água, oxigênio e água líquida com oxigênio dissolvido d) gelo, prata, cobre, água líquida, vapor d'água, oxigênio gasoso e também dissolvido na água e) platina, carvão, oxigênio, nitrogênio, dióxido de carbono e água. 09 Temos um sistema formado de pedaços de vidro, água líquida, sal em excesso, vapor d'água e gelo. Sua classificação quanto ao tipo de sistema, número de fases e de componentes é: a) sistema heterogêneo, 4 fases 3 componentes b) sistema homogêneo, 4 fases e 3 componentes c) sistema heterogêneo, 5 fases e 3 componentes d) sistema homogêneo, 1 fase e 3 componentes e) sistema heterogêneo, 5 fases e 5 componentes 10 (FESP) Considere um sistema formado por água + álcool + granito. Excluindo o recipiente e o ar, podemos afirmar que o sistema apresenta: a) três componentes e três fases b) três componentes e duas fases c) cinco componentes e quatro fases d) cinco componentes e cinco fases e) cinco componentes e duas fases Capítulo 5 Fracionamento de Misturas : 01 O aspirador de pó, através da sucção do ar, separa os componentes de uma mistura: a) homogênea sólido sólido d) heterogênea sólido gás b) homogênea sólido líquido e) homogênea sólido gás c) heterogênea sólido líquido 02 A melhor maneira de separar os três componentes de uma mistura de areia com solução aquosa de sal é: a) filtrar e destilar d) filtrar e decantar b) destilar e filtrar e) destilar e decantar c) decantar e filtrar 03 Em um recipiente, tem se uma mistura contendo ferro, sal e areia. Desejando se separar esses componentes, foram executadas as seguintes operações: a) separação magnética, dissolução em água filtração e destilação b) somente destilação seca fracionada c) apenas cristalização fracionada d) aquecimento da mistura e destilação fracionada e) aquecimento da mistura, dissolução em água e separação magnética. 04 Tem se uma mistura de magnésio e bismuto pulverizados. A densidade do magnésio é 1,74 g/ml e a do bismuto é 9,67 g/ml. Para separar esses dois metais, precisamos escolher um líquido adequado. Qual dos líquidos abaixo você escolheria? a) O líquido reage com ambos os metais e tem densidade 2,89 g/ml b) O líquido reage com um dos metais e tem densidade 2,89 g/ml c) O líquido não reage com nenhum dos dois metais e tem densidade 2,89 g/ml d) O líquido reage com um dos metais e tem densidade 1,24 g/ml. e) O líquido não reage com nenhum dos metais e tem densidade 1,24 g/ml. 05 Os sistemas água óleo e água areia podem ser separados, respectivamente, por: a) sedimentação fracionada e filtração d) decantação e destilação b) imantação e decantação e) destilação e filtração c) decantação e filtração 06 (UFMG) O sal de cozinha pode ser obtido da água do mar através de: a) centrifugação c) destilação e) filtração b) decantação d) eletrólise 07 (UFMG) Considere as misturas da tabela. Mistura I II III Componentes água e sal água e azeite ar e poeira Os componentes dessas misturas podem ser separados, respectivamente, pelos processos: a) I eletrólise; II filtração; III decantação b) I destilação; II filtração; III decantação c) I filtração; II destilação; III liquefação do ar d) I decantação; II destilação; III filtração e) I destilação; II decantação; III filtração 08 (PUC MG) Na tabela abaixo, a coluna 2 deve ser preenchida com o processo que é utilizado para a separação dos componentes das misturas da coluna 1. CADERNO DE EXERCÍCIOS 4
5 Coluna 1 (componentes) Frações de petróleo Cloreto de sódio e água Óleo e água Ferro e enxofre Coluna 2 (proc. de separação) I II III IV A complementação correta para a coluna 2 é, respectivamente: a) decantação, filtração, separação magnética, cristalização b) destilação fracionada, evaporação, decantação, separação magnética c) evaporação, separação magnética, flotação, destilação fracionada d) filtração, decantação, fusão fracionada, dissolução fracionada e) separação magnética, destilação fracionada, decantação, evaporação 09 Uma mistura é formada por dois sólidos finamente pulverizados, de densidades iguais a 1,2 g/ml e 1,8 g/ml, respectivamente. Para separar os componentes dessa mistura, u- sando um líquido que não dissolva os sólidos, a densidade desse liquido deve ser igual a: a) 0,6 g/ml c) 1,5 g/ml e) 3,0 g/ml b) 1,0 g/ml d) 2,0 g/ml 10 (PUC MG) Nos processos usados para separação de misturas heterogêneas do tipo sólido sólido, emprega se: I filtração II levigação III ventilação IV decantação A alternativa correta, em relação a afirmativa acima, é: a) I e II c) II, III e IV e) apenas III b) II e III d) III e IV GABARITO - Capítulo 1-01) E 02) C 03) C 04) D 05) D 06) E 07) D 08) A 09) 10) B - Capítulo 2-01) A 02) D 03) B 04) C 05) B 06) C 07) A 08) D 09) B 10) B - Capítulo 3-01) A 02) D 03) D 04) C 05) B 06) C 07) E 08) E 09) C 10) B - Capítulo 4-01) C 02) A 03) C 04) A 05) A 06) C 07) D 08) E 09) C 10) C - Capítulo 5-01) D 02) A 03) A 04) C 05) C 06) C 07) E 08) B 09) C 10) B CADERNO DE EXERCÍCIOS 5
BIMESTRAL QUÍMICA - 1ºBIMESTRE
 BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
FÍSICA PROFº JAISON MATTEI
 FÍSICA PROFº JAISON MATTEI A MATÉRIA E SUAS TRANSFORMAÇÕES As mudanças de estado físico da água. Diagrama de mudanças de estado físico. 01. Um cientista recebeu uma substância desconhecida, no estado sólido,
FÍSICA PROFº JAISON MATTEI A MATÉRIA E SUAS TRANSFORMAÇÕES As mudanças de estado físico da água. Diagrama de mudanças de estado físico. 01. Um cientista recebeu uma substância desconhecida, no estado sólido,
Separação de misturas
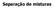 Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
SIMPLES SUBSTÂNCIA PURA COMPOSTA HOMOGÊNEO MISTURA HOMOGÊNEA SISTEMA SUBSTÂNCIA PURA HETEROGÊNEO MISTURA HETEROGÊNEA
 Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria.
 O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas:
 01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
CIÊNCIAS 9º Ano Ensino Fundamental
 CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
Tarefa 22 Professor Gustavo
 6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK
 PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO
 6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017
 ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
09) Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
Química B Extensivo V. 2
 Extensivo V. 2 Resolva Aula 5 5.01) A 5.02) C 5.03) Colocar água para separar o salitre e decantar ou filtrar. Depois pôr sulfeto de carbono no sólido restante para retirar o enxofre. que sobra é o carvão.
Extensivo V. 2 Resolva Aula 5 5.01) A 5.02) C 5.03) Colocar água para separar o salitre e decantar ou filtrar. Depois pôr sulfeto de carbono no sólido restante para retirar o enxofre. que sobra é o carvão.
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas:
 Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
Tarefa 09 à 12 Professor Willian. Com base no gráfico, assinale a alternativa que apresenta a afirmativa CORRETA.
 9º ano Química Tarefa 09 à 12 Professor Willian 01. Dois materiais sólidos, A e B, são aquecidos a uma velocidade de 10ºC.min 1. A figura a seguir representa o diagrama de aquecimento desses dois materiais.
9º ano Química Tarefa 09 à 12 Professor Willian 01. Dois materiais sólidos, A e B, são aquecidos a uma velocidade de 10ºC.min 1. A figura a seguir representa o diagrama de aquecimento desses dois materiais.
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
EXERCÍCIOS DE QUÍMICA
 INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
Curso Pré-ENEM. Química. Profª M.ª Juliana Silva Leite
 Curso Pré-ENEM Química Profª M.ª Juliana Silva Leite O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES
Curso Pré-ENEM Química Profª M.ª Juliana Silva Leite O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
Atividade extra. Questão 1 Cecierj Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
9 o EF. Jeosafá de P. Lima
 9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
QUÍMICA PROF. AMANDA THOMÉ
 QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma:
 TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
Lista de Exercício. 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada sistema?
 Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
26/08/15 SUBSTÂNCIAS E MISTURAS. Prof. Ms. Mayanderson (Xuxu)
 SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente:
 2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
PROMILITARES 09/08/2018 QUÍMICA. Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS
 QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
Composição Densidade (g/mol) Carvão 0,3 0,6 Ossos 1,7 2,0 Areia 2,0 2,4 Solo 2,6 2,8 Pedras 2,6 5,0
 QUÍMICA Arqueologistas usam diferenças de densidade para separar as misturas que eles obtêm por escavação. Indique a opção correta para uma mostra que contém a seguinte composição: Composição Densidade
QUÍMICA Arqueologistas usam diferenças de densidade para separar as misturas que eles obtêm por escavação. Indique a opção correta para uma mostra que contém a seguinte composição: Composição Densidade
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 1º. ALUNO(a):
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 1º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 1º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS. Escola de Civismo e Cidadania
 COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2018 QUESTÃO 01 O QUE É QUÍMICA? QUESTÃO 02 O QUE É MATÉRIA? QUESTÃO 03 O QUE É TEMPERATURA? QUESTÃO 04 O QUE É TRANSFORMAÇÃO(OU
COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2018 QUESTÃO 01 O QUE É QUÍMICA? QUESTÃO 02 O QUE É MATÉRIA? QUESTÃO 03 O QUE É TEMPERATURA? QUESTÃO 04 O QUE É TRANSFORMAÇÃO(OU
Química B Semiextensivo V. 1
 Química B Semiextensivo V. 1 Exercícios 01) A 02) C 03) A 04) E d = m v Densidade e massa são diretamente proporcionais, ou seja, quanto maior a massa da substância, maior será sua densidade. Já o volume
Química B Semiextensivo V. 1 Exercícios 01) A 02) C 03) A 04) E d = m v Densidade e massa são diretamente proporcionais, ou seja, quanto maior a massa da substância, maior será sua densidade. Já o volume
PROCESSOS DE SEPARAÇÃO. Prof. Ms. George Verçoza
 PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
QUÍMICA 1ª Série Ensino Médio
 LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES. Prof a. Giselle Blois. Estudo da matéria: substâncias, misturas, processos de separação Parte 2
 QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
LISTA B QUÍMICA TONI ATITUDE
 LISTA B QUÍMICA TONI ATITUDE Site: www.sosprofessor.xpg.com.br Lei da conservação (lei de Lavoisier)= em um sistema fechado a massa total não varia Lei da proporção constante (lei de Proust)= os elementos
LISTA B QUÍMICA TONI ATITUDE Site: www.sosprofessor.xpg.com.br Lei da conservação (lei de Lavoisier)= em um sistema fechado a massa total não varia Lei da proporção constante (lei de Proust)= os elementos
PLANTÕES DE FÉRIAS QUÍMICA
 Página 1 PLANTÕES DE FÉRIAS QUÍMICA Nome: Nº: Série: 9º ANO Profª BIANCA RIBEIRO Data: JULHO 2016 Roteiro de Estudos Primeiramente, revise em seu caderno algumas propriedades da matéria, como: o Densidade
Página 1 PLANTÕES DE FÉRIAS QUÍMICA Nome: Nº: Série: 9º ANO Profª BIANCA RIBEIRO Data: JULHO 2016 Roteiro de Estudos Primeiramente, revise em seu caderno algumas propriedades da matéria, como: o Densidade
O Que é Química? Pra que serve a Química?²
 O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
Apostila de Química 12 A Matéria
 Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
SUBSTÂNCIA PURA & MISTURAS
 SUBSTÂNCIA PURA & MISTURAS Química Professora: Danielle Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Sistemas Materiais Substância Pura Mistura Simples Composta Homogênea Heterogênea
SUBSTÂNCIA PURA & MISTURAS Química Professora: Danielle Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Sistemas Materiais Substância Pura Mistura Simples Composta Homogênea Heterogênea
2-Nos sistemas abaixo, diga quantos átomos, elementos, moléculas e substâncias estão representados:
 LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
SUBSTÂNCIAS E MISTURAS
 SUBSTÂNCIAS E MISTURAS SUBSTÂNCIAS Uma substância química (ou apenas substância) é um material que apresenta um conjunto de propriedades bem definido e constante e tem composição fixa, independente da
SUBSTÂNCIAS E MISTURAS SUBSTÂNCIAS Uma substância química (ou apenas substância) é um material que apresenta um conjunto de propriedades bem definido e constante e tem composição fixa, independente da
Estados de agregação da matéria. Mudanças de estado. Fenômenos
 Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
Estado Físico Características Macroscópicas Características Microscópicas
 Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS.
 SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
INTRODUÇÃO À QUÍMICA
 INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015
 Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
Conceitos importantes: a) Matéria : Tudo o que possui massa e ocupa lugar no espaço.
 SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g)
 Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
PROCESSOS DE SEPARAÇÃO. Professor Cassio Pacheco
 PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
QiD 1 1ª SÉRIE PARTE 3 FÍSICA
 QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
Química B Extensivo V. 1
 Química B Extensivo V. 1 Resolva Aula 1 Aula 3 1.01) O açúcar se divide e preenche os espaços vazios existentes na água. 3.01) C 1.0) Plástico. 1.03) Acidez. Aula.01) C I Condensação II Fusão S III Ebulição
Química B Extensivo V. 1 Resolva Aula 1 Aula 3 1.01) O açúcar se divide e preenche os espaços vazios existentes na água. 3.01) C 1.0) Plástico. 1.03) Acidez. Aula.01) C I Condensação II Fusão S III Ebulição
CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ
 PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A tabela
PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 3º BIMESTRE 9º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. A tabela
IX OSEQUIM - Olimpíada Sergipana de Química 2ª Etapa - Modalidade A
 Bom dia aluno! Está é a prova da segunda etapa da IX OSEQUIM, Olimpíada Sergipana de Química, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2015. Confira se a sua prova
Bom dia aluno! Está é a prova da segunda etapa da IX OSEQUIM, Olimpíada Sergipana de Química, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2015. Confira se a sua prova
Sumário. Química. Frente 1. Frente 2. Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88. Capítulo 4: A Tabela Periódica 96
 Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
Separação de Misturas
 Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
QUÍMICA. Lista de Exercícios / 1º ano. Professora: Geiziane Oliveira Data: / / Aluno(a):
 QUÍMICA Lista de Exercícios / 1º ano. Professora: Geiziane Oliveira Data: / / 2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
QUÍMICA Lista de Exercícios / 1º ano. Professora: Geiziane Oliveira Data: / / 2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016
 ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 1,0 ) I. Introdução Neste bimestre, sua média foi inferior a 6,0
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 1,0 ) I. Introdução Neste bimestre, sua média foi inferior a 6,0
QUÍMICA. Lista de Exercícios / 3º ano. Professora: Geiziane Oliveira Data: /02/2017. Aluno(a):
 QUÍMICA Lista de Exercícios / 3º ano. Professora: Geiziane Oliveira Data: /02/2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
QUÍMICA Lista de Exercícios / 3º ano. Professora: Geiziane Oliveira Data: /02/2017. Um novo com a tradição de sempre! Aluno(a): 1. (UESC BA) Uma análise da curva de aquecimento dessa amostra de material
Lista de exercícios 1- Dos processos abaixo, qual pode ser caracterizado como fenômeno físico?
 Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 1º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Pensamento cientifico Laboratório químico Estados físicos e as transformações
Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 1º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Pensamento cientifico Laboratório químico Estados físicos e as transformações
1. Estados físicos da matéria Mudanças de estado Substâncias puras Misturas 4 Exercícios Densidade 6 1.
 1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
1. Estados físicos da matéria 3 1.1 Mudanças de estado 3 1.2 Substâncias puras 4 1.3 Misturas 4 Exercícios 5 1.4 Densidade 6 1.5 Transformação da matéria 6 1.6 Alotropia 6 1.7 Diagramas de fases 6 1.8
+ Resposta da questão 1: [C]
![+ Resposta da questão 1: [C] + Resposta da questão 1: [C]](/thumbs/84/89370407.jpg) + Resposta da questão 1: Ao absorver o calor do sol, a água recebe a energia necessária para passar do estado líquido para o estado gasoso, processo denominado evaporação. Resposta da questão 2: [Resposta
+ Resposta da questão 1: Ao absorver o calor do sol, a água recebe a energia necessária para passar do estado líquido para o estado gasoso, processo denominado evaporação. Resposta da questão 2: [Resposta
Tarefa 11 Professor Negri. 01. O equipamento esquematizado abaixo pode ser utilizado para separar os componentes de:
 Tarefa 11 Professor Negri 01. O equipamento esquematizado abaixo pode ser utilizado para separar os componentes de: a) um sistema homogêneo líquido/líquido. b) qualquer sistema heterogêneo. c) uma mistura
Tarefa 11 Professor Negri 01. O equipamento esquematizado abaixo pode ser utilizado para separar os componentes de: a) um sistema homogêneo líquido/líquido. b) qualquer sistema heterogêneo. c) uma mistura
Química. A matéria, suas transformações e a energia Unidade 2
 Química A matéria, suas transformações e a energia Unidade 2 Matéria (p.23) É tudo aquilo que tem massa, volume e, por isso, ocupa um lugar no espaço. Não é possível compartilhar o espaço com outra porção
Química A matéria, suas transformações e a energia Unidade 2 Matéria (p.23) É tudo aquilo que tem massa, volume e, por isso, ocupa um lugar no espaço. Não é possível compartilhar o espaço com outra porção
AULA 1 FRENTE 1. Por causa do lançamento, na atmosfera, de grande quantidade de gás carbônico, causador do efeito estufa.
 Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
1) Se um corpo tem a massa de 20 g e um volume de 5 cm 3, quanto vale sua densidade? a) 10 g/cm 3 b) 4 g/cm 3 c) 5 g/cm 3 d) 15 g/cm 3 e) 20 g/cm 3
 1) Se um corpo tem a massa de 20 g e um volume de 5 cm 3, quanto vale sua densidade? a) 10 g/cm 3 b) 4 g/cm 3 c) 5 g/cm 3 d) 15 g/cm 3 e) 20 g/cm 3 2) Calcule o valor da massa de um objeto constituído
1) Se um corpo tem a massa de 20 g e um volume de 5 cm 3, quanto vale sua densidade? a) 10 g/cm 3 b) 4 g/cm 3 c) 5 g/cm 3 d) 15 g/cm 3 e) 20 g/cm 3 2) Calcule o valor da massa de um objeto constituído
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA
 ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
PROCESSOS DE SEPARAÇÃO. Jeosafá Lima
 PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
02- Quais das propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida?
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
MATÉRIA CORPO OBJETO
 A ciência QUÍMICA está voltada para o estudo da matéria, qualquer que seja sua origem. Observando a composição da matéria, suas transformações e a energia envolvida nesses processos MATÉRIA CORPO OBJETO
A ciência QUÍMICA está voltada para o estudo da matéria, qualquer que seja sua origem. Observando a composição da matéria, suas transformações e a energia envolvida nesses processos MATÉRIA CORPO OBJETO
LOUCOS POR QUÍMICA. PROF. Neif Nagib
 LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
PLANTÕES DE JULHO QUÍMICA AULA
 PLANTÕES DE JULHO QUÍMICA AULA 01 Nome: Nº: Série: 9º ANO Profª: BIANCA ARAUJO RIBEIRO Data: JULHO 2018 1) Para separar os componentes do sistema formado por sal de cozinha e carvão em pó, um estudante
PLANTÕES DE JULHO QUÍMICA AULA 01 Nome: Nº: Série: 9º ANO Profª: BIANCA ARAUJO RIBEIRO Data: JULHO 2018 1) Para separar os componentes do sistema formado por sal de cozinha e carvão em pó, um estudante
Módulo inicial Materiais: Diversidade e Constituição. Química 10.º ano Ano lectivo 2007/2008
 Química 10.º ano Ano lectivo 2007/2008 Escola Secundária José Saramago Marta Paulino e Ângela Patrício O que é um Material? É algo que tem massa e ocupa espaço. Classificação Materiais: Componentes Origem
Química 10.º ano Ano lectivo 2007/2008 Escola Secundária José Saramago Marta Paulino e Ângela Patrício O que é um Material? É algo que tem massa e ocupa espaço. Classificação Materiais: Componentes Origem
Ciências Físico-Químicas 7º ano Ficha de trabalho nº14 Separação dos componentes de uma mistura
 Para separar os constituintes de uma mistura pode-se recorrer a diferentes processos de separação. Os processos de separação permitem separar diferentes substâncias que inicialmente foram juntas, mantendo
Para separar os constituintes de uma mistura pode-se recorrer a diferentes processos de separação. Os processos de separação permitem separar diferentes substâncias que inicialmente foram juntas, mantendo
XXI Maratona Cearense de Química ABQ-CE
 XXI Maratona Cearense de Química ABQ-CE Ensino Fundamental 8 o Ano 1) O monitor de laboratório colocou massas iguais dos líquidos incolores água, benzeno e clorofórmio em frascos distintos mas esqueceu
XXI Maratona Cearense de Química ABQ-CE Ensino Fundamental 8 o Ano 1) O monitor de laboratório colocou massas iguais dos líquidos incolores água, benzeno e clorofórmio em frascos distintos mas esqueceu
SEPARAÇÃO DE MISTURAS
 SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
PROMILITARES 16/08/2018 QUÍMICA. Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS
 QUÍMICA Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS Misturas Mistura Homogênea: duas ou mais substâncias com 1 fase. Mistura Heterogênea: duas ou mais substâncias com mais de 1 fase. Processos de
QUÍMICA Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS Misturas Mistura Homogênea: duas ou mais substâncias com 1 fase. Mistura Heterogênea: duas ou mais substâncias com mais de 1 fase. Processos de
A MATÉRIA. O que é matéria? MATÉRIA: tudo que tem massa e ocupa espaço, isto é, volume.
 Disciplina: Química Prof.: Guilherme Turma: IU 16/ 03/2017 Tema da aula: A Matéria e suas Propriedades A MATÉRIA O que é matéria? MATÉRIA: tudo que tem massa e ocupa espaço, isto é, volume. - Massa e volume
Disciplina: Química Prof.: Guilherme Turma: IU 16/ 03/2017 Tema da aula: A Matéria e suas Propriedades A MATÉRIA O que é matéria? MATÉRIA: tudo que tem massa e ocupa espaço, isto é, volume. - Massa e volume
Processos de separação de misturas
 Disciplina: Química Prof.: Ivo Turma: IU 23/03/2017 Tema da aula: Métodos de separação de misturas Processos de separação de misturas 1) Separação de misturas heterogêneas Misturas sólido sólido Catação
Disciplina: Química Prof.: Ivo Turma: IU 23/03/2017 Tema da aula: Métodos de separação de misturas Processos de separação de misturas 1) Separação de misturas heterogêneas Misturas sólido sólido Catação
AULA 1 FRENTE 1. Por causa do lançamento, na atmosfera, de grande quantidade de gás carbônico, causador do efeito estufa.
 Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Disciplina: Química Professor: Cassio Pacheco Turma: 1 Ano
 Disciplina: Química Professor: Cassio Pacheco Turma: 1 Ano Roteiro de Estudos 1- A queima da gasolina; a sublimação da naftalina; o enferrujamento do prego e o derretimento de um bloco de gelo são respectivamente,
Disciplina: Química Professor: Cassio Pacheco Turma: 1 Ano Roteiro de Estudos 1- A queima da gasolina; a sublimação da naftalina; o enferrujamento do prego e o derretimento de um bloco de gelo são respectivamente,
DIAGRAMA DE FASES. 4) (ITA) Considere as seguintes afirmações relativas aos sistemas descritos a seguir, sob
 DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
Os estados físicos da matéria sólido, líquido e gasoso são chamados também de estados de agregação da matéria. No esquema abaixo,
 QUÍMICA (QUESTÕES 1 10) QUESTÃO 1 Os estados físicos da matéria sólido, líquido e gasoso são chamados também de estados de agregação da matéria. No esquema abaixo, marque a alternativa que representa CORRETAMENTE
QUÍMICA (QUESTÕES 1 10) QUESTÃO 1 Os estados físicos da matéria sólido, líquido e gasoso são chamados também de estados de agregação da matéria. No esquema abaixo, marque a alternativa que representa CORRETAMENTE
Recuperação Final Química 9º Ano Professor Diego Estudar: Caderno 1 páginas ; Caderno 2 páginas Exercícios
 Recuperação Final Química 9º Ano Professor Diego Estudar: Caderno 1 páginas 244-257; Caderno 2 páginas 258-280. Exercícios 1. As substâncias podem ser encontradas em três estados físicos, sólido, líquido
Recuperação Final Química 9º Ano Professor Diego Estudar: Caderno 1 páginas 244-257; Caderno 2 páginas 258-280. Exercícios 1. As substâncias podem ser encontradas em três estados físicos, sólido, líquido
Conhecimento. Senso comum Religioso Filosófico Cientifico. Química. A matéria. propriedades. gerais funcionais específicas
 Conhecimento Senso comum Religioso Filosófico Cientifico Química A matéria propriedades gerais funcionais específicas físicas químicas organolépticas Estados de agregação da matéria Estado sólido Forma
Conhecimento Senso comum Religioso Filosófico Cientifico Química A matéria propriedades gerais funcionais específicas físicas químicas organolépticas Estados de agregação da matéria Estado sólido Forma
FUVEST 1984 Primeira fase e Segunda fase
 FUVEST 1984 Primeira fase e Segunda fase Professora Sonia 9. A melhor maneira de separar os três componentes de uma mistura de areia com solução aquosa de sal é: CONHECIMENTOS GERAIS 5. O peso atômico
FUVEST 1984 Primeira fase e Segunda fase Professora Sonia 9. A melhor maneira de separar os três componentes de uma mistura de areia com solução aquosa de sal é: CONHECIMENTOS GERAIS 5. O peso atômico
XI OSEQUIM - Olimpíada Sergipana de Química 1ª Etapa - Modalidade A
 Bom dia aluno! Está é a prova da primeira etapa da OSEQUIM, Olimpíada Sergipana de Química 2017, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2017. Confira se a sua
Bom dia aluno! Está é a prova da primeira etapa da OSEQUIM, Olimpíada Sergipana de Química 2017, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2017. Confira se a sua
04) Sobre o elemento X 36 :
 01) O texto a seguir descreve um elemento. Leia-o atentamente e associe com o elemento correto nas alternativas abaixo: É o mais abundante dos halogênios, é usado na produção de compostos orgânicos e inorgânicos,
01) O texto a seguir descreve um elemento. Leia-o atentamente e associe com o elemento correto nas alternativas abaixo: É o mais abundante dos halogênios, é usado na produção de compostos orgânicos e inorgânicos,
SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS
 SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS 1) Em relação às partículas atômicas, a alternativa falsa é: a) a massa do próton é igual a massa do elétron. b) a massa do elétron é menor que a massa
SIMULADO de QUÍMICA 1 os anos 2008 TODOS COLÉGIOS 1) Em relação às partículas atômicas, a alternativa falsa é: a) a massa do próton é igual a massa do elétron. b) a massa do elétron é menor que a massa
