QiD 1 1ª SÉRIE PARTE 3 FÍSICA
|
|
|
- Adelina Estrela Ximenes
- 7 Há anos
- Visualizações:
Transcrição
1 QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta é cerca de 80 cm ou 0,8 m. 2. (1,0) Um professor na sala de aula, pede para um aluno medir dois objetos com duas réguas diferentes, calibradas com duas unidades diferentes. A régua 1 está calibra em centímetro, já a régua 2 calibrada em milímetro. Objeto 1 o aluno mede com a régua1, e meça 12,6 cm, já o objeto 2 mede com a régua 2 e meça 23,43 mm. Determine para os dois objetos: a) Quantidade de algarismo significativo. b) O algarismo duvidoso. 3. (1,0) Um americano ao chegar no Brasil, resolveu passear na orla do rio de janeiro.observando o termômetro localizado na orla da praia, verificou que marcava 45 C. Sabendo que a escala fahrenheit ( F) é utilizada eu seu país, resolveu calcular a temperatura correspondente na escala Fahrenheit ( F). Qual a temperatura encontrada. 4. (1,0) Um estudante aplicado resolveu criar uma escala, onde o ponto de fusão, - 20 W e ponto de ebulição 50 W. Determine a temperatura correspondente na escala W, quando a temperatura na escala Celsius marcar 20 C 5. (1,0) Uma pessoa, ao realizar a leitura da temperatura de determinado sistema, obteve o valor Considerando escalas usuais (Celsius, Fahrenheit e Kelvin), podemos afirmar que o termômetro utilizado certamente NÃO poderia estar graduado: (A) Apenas na escala Celsius. (B) Apenas na escala Fahrenheit (C) Apenas na escala Kelvin. (D) Nas escalas Celsius e Kelvin. (E) Nas escalas Fahrenheit e Kelvin. Este enunciado refere-se aos problemas seguintes. Dois corpos A e B são aquecidos simultaneamente, conforme mostra o gráfico quantidade de calor temperatura mostrada abaixo. A massa de B é o dobro da massa de A. 6. (1,0) Calcule a relação entre a capacidade térmica do corpo A e do corpo B. 7. (1,0) Calcule a relação entre o calor específico do corpo A e do corpo B.
2 QiD 1 1ª SÉRIE PARTE 3 FÍSICA 8. (1,0) Um homem bebe 200 g de água na temperatura de 6,5 o C. Calcule a quantidade de calor, em kcal, que o corpo da pessoa vai ceder à água. Suponha que a temperatura corporal seja 36,5 o C. 9. A quantidade de calor necessária para que 1,0 litro de água, inicialmente a 30 o C comece a ferver é de: (A) 30 kcal. (B) 40 kcal. (C) 70 kcal. (D) 100 kcal. (E) 120 kcal. 10. (1,0) Considere a definição de caloria como sendo: Sendo assim, obtenha o calor específico da água.
3 GABARITO QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. Para determinar o numero de passos é necessário fazer a razão entre, deslocamento do atleta e o tamanha de seu passo. Desta forma temos, N = 4,2 x 104 m 5,25 x 10 4 PPPPPP 0,8 Para estimar a ordem de grandeza deste numero temos que saber se, n > 3,16 ou n< 3,16 Neste caso, n = 5,25 Por tanto, 5,25 > 3, oo PPPPPP 2. a) Objeto 1: 3 algarismos - objeto 2: 4 algarismos b) Objeto 1: n : 6 duvidoso - objeto 2: n : 3 duvidoso 3. F 32 = C 9 5 F = 113 F W C W = 7C C 0 = 20 C W = 6 W 5. Letra d, nas escalas Celsius e Kelvin. 6. C = Q/Δθ C = 400/20 = 20 cal/ o C A C = 400/40 = 10 cal/ o C B Sendo assim, C / C = 2 A B 7. Seja m a massa do corpo A e 2 m a massa do corpo B. C = m c c = C/m c = 20/m = 20/m A c = 10/2m B c /c = 4 A B 8. Q = m c Δθ = = cal = 6,0 kcal
4 QiD 1 1ª SÉRIE PARTE 3 FÍSICA 9. GABARITO: C A quantidade de calor sensível é calculada pela seguinte expressão: Q = m c Δθ Sendo assim: Q = 1,0 kg 1,0 cal/g C 70 C = 70 kcal 10. Q = 1 cal m = 1 g θ = 1 C Q = m c θ c = Q/m θ cágua = 1 cal/g C
5 1. A = sólido e B = gasoso 2. GABARITO QiD 1 1ª SÉRIE PARTE 3 QUÍMICA 3. Mistura azeotrópica, pois é uma mistura em que o ponto de ebulição não se altera. A mudança do estado líquido para o gasoso ocorre à temperatura constante. 4. B e E A passagem de estado físico ocorre com temperatura constante. 5. I = físico; II = químico; III = químico; IV = químico; V = químico 6. Sólidos X, Y e Z. Apresentam suas densidades maiores que a da água (1 g/cm 3 ) A cortiça flutua na água, portanto W porque apresenta a densidade menor que a água V F F V V 1. Preparar cafezinho com café ( ) separação magnética solúvel 2. Preparar chá de saquinho ( ) destilação simples 3. Separar a areia do sal de ( 6 ) destilação fracionada cozinha 4. Coar um suco de laranja ( 4 ) filtração 5. Separar o soro do leite 6. Separação das frações do petróleo ( 5 ) centrifugação ( 3 ) dissolução fracionada ( 2 ) extração ( 1 ) dissolução
6 Atenção: Leia o texto a seguir e responda às questões 1, 2, 3 e 4. QiD 1 1ª SÉRIE PARTE 3 QUÍMICA No laboratório de uma indústria farmacêutica, foram obtidos dados de alguns materiais e colocados na tabela abaixo, relativos a propriedades a propriedades físicas dos mesmos. Substância Temperatura de Fusão (ºC) Temperatura de Ebulição (ºC) A a 1952 B C - 10 a D - 57 a a 120 E (1,0) Qual o estado físico das substâncias A e B na temperatura ambiente (25ºC)? 2. (1,0) Faça um gráfico com os pontos de fusão e ebulição e as transformações físicas do material D. 3. (1,0) Que tipo de mistura representa o material C? Justifique sua resposta. 4. (1,0) Quais correspondem à substâncias puras? Justifique sua resposta. 5. (1,0) Um estudante de Química listou os seguintes processos como exemplos de fenômenos físicos e químicos: I. sublimação da naftalina. II. maçã que escurece na salada de frutas. III. digestão. IV. processo de fermentação na cerveja. V. combustão da gasolina nos motores. Ajude o aluno a classificar esses fenômenos descritos acima. Atenção: Leia o texto a seguir e responda às questões 6, 7 e 8. Analise o gráfico referente a quatro sólidos Z, Y, Z e W: e responda: 6. (1,0) Quais os sólidos que não flutuam na água? Justifique sua resposta. 7. (1,0) Qual a densidade de X? Justifique mostrando o cálculo. 8. (1,0) Qual deles poderia pertencer a cortiça? Justifique sua resposta.
7 QiD 1 1ª SÉRIE PARTE 3 QUÍMICA 9. Numere a segunda coluna de acordo com a primeira. 1. Preparar cafezinho com café solúvel ( ) separação magnética 2. Preparar chá de saquinho ( ) destilação simples 3. Separar a areia do sal de cozinha ( ) destilação fracionada 4. Coar um suco de laranja ( ) filtração 5. Separar o soro do leite ( ) centrifugação 6. Separação das frações do petróleo ( ) dissolução fracionada ( ) extração ( ) dissolução 10. (1,0) Observe os seguintes sistemas: I. água e gelo II. Ferro em pó e enxofre III. Éter e água IV. Ar atmosférico V. Açúcar dissolvido em água. Julgue cada uma das afirmações a respeito dos sistemas e marque para cada uma delas verdadeiro (V) ou falso (F). ( ) O sistema I pode ser constituído por moléculas iguais, é uma substância pura, embora seja heterogênea. ( ) O sistema II é homogêneo, já que o ferro em pó e o enxofre se misturam perfeitamente constituindo uma única fase. Aliás a separação de seus componentes pode ser feita por decantação. ( ) O sistema III, por ser visualmente uniforme, é perfeitamente homogêneo. Essa afirmação só foi possível pelo fato de todas as moléculas do sistema serem iguais. ( ) O sistema IV, tendo seus componentes no estado gasoso, e homogêneo. A separação de seus componentes pode ser feita primeiramente por liquefação fracionada. ( ) O sistema V constitui uma mistura homogênea e separado através da destilação simples.
CIÊNCIAS 9º Ano Ensino Fundamental
 CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK
 PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
EXERCÍCIOS DE QUÍMICA
 INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
Atividade extra. Questão 1 Cecierj Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO
 6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Tarefa 22 Professor Gustavo
 6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
Processos físicos de separação de misturas
 Processos físicos de separação de misturas Misturas heterogêneas sólido-sólido Catação Peneiração Flutuação Separação Magnética Dissolução Fracionada Sublimação CATAÇÃO Baseia-se na identificação visual
Processos físicos de separação de misturas Misturas heterogêneas sólido-sólido Catação Peneiração Flutuação Separação Magnética Dissolução Fracionada Sublimação CATAÇÃO Baseia-se na identificação visual
FÍSICA PROFº JAISON MATTEI
 FÍSICA PROFº JAISON MATTEI A MATÉRIA E SUAS TRANSFORMAÇÕES As mudanças de estado físico da água. Diagrama de mudanças de estado físico. 01. Um cientista recebeu uma substância desconhecida, no estado sólido,
FÍSICA PROFº JAISON MATTEI A MATÉRIA E SUAS TRANSFORMAÇÕES As mudanças de estado físico da água. Diagrama de mudanças de estado físico. 01. Um cientista recebeu uma substância desconhecida, no estado sólido,
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES. Prof a. Giselle Blois. Estudo da matéria: substâncias, misturas, processos de separação Parte 2
 QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Separação de misturas
 Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Exercícios de Revisão Ensino Médio 2º Bimestre Química: Setor A 1ª Série Professor Diego
 Exercícios de Revisão Ensino Médio 2º Bimestre Química: Setor A 1ª Série Professor Diego 1. (UFES) Na perfuração de uma jazida petrolífera, a pressão dos gases faz com que o petróleo jorre para fora. Ao
Exercícios de Revisão Ensino Médio 2º Bimestre Química: Setor A 1ª Série Professor Diego 1. (UFES) Na perfuração de uma jazida petrolífera, a pressão dos gases faz com que o petróleo jorre para fora. Ao
QUÍMICA PROF. AMANDA THOMÉ
 QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
SIMPLES SUBSTÂNCIA PURA COMPOSTA HOMOGÊNEO MISTURA HOMOGÊNEA SISTEMA SUBSTÂNCIA PURA HETEROGÊNEO MISTURA HETEROGÊNEA
 Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Tratamento de água. Adaptado de Luciana de Araújo
 Tratamento de água Adaptado de Luciana de Araújo A Química está presente no tratamento da água que chega nas nossas casas? Se sim, como? Estados físicos da água Mudança de estado físico No vídeo... Ouvimos
Tratamento de água Adaptado de Luciana de Araújo A Química está presente no tratamento da água que chega nas nossas casas? Se sim, como? Estados físicos da água Mudança de estado físico No vídeo... Ouvimos
Química B Intensivo V. 1
 1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
Podemos definir como quente um corpo que tem suas moléculas agitando-se muito, ou seja, com alta energia cinética. Analogamente, um corpo frio, é
 Podemos definir como quente um corpo que tem suas moléculas agitando-se muito, ou seja, com alta energia cinética. Analogamente, um corpo frio, é aquele que tem baixa agitação das suas moléculas. Tem
Podemos definir como quente um corpo que tem suas moléculas agitando-se muito, ou seja, com alta energia cinética. Analogamente, um corpo frio, é aquele que tem baixa agitação das suas moléculas. Tem
Recursos para Estudo / Atividades
 Caro educando, você está recebendo o conteúdo de recuperação. Faça a lista de exercícios com atenção, ela norteará os seus estudos. Utilize o livro didático adotado pela escola como fonte de estudo. Se
Caro educando, você está recebendo o conteúdo de recuperação. Faça a lista de exercícios com atenção, ela norteará os seus estudos. Utilize o livro didático adotado pela escola como fonte de estudo. Se
9º Ano/Turma: Data / / ) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
 Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2015 C.Curricular: Ciências/ Química 1) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2015 C.Curricular: Ciências/ Química 1) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
Lista de Exercício. 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada sistema?
 Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
PROCESSOS DE SEPARAÇÃO. Prof. Ms. George Verçoza
 PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
4.1. Separação dos componentes de misturas heterogéneas
 4.1. Separação dos componentes de misturas heterogéneas Separação dos componentes de misturas heterogéneas Para separar os componentes de misturas utilizam-se processos físicos de separação. Durante o
4.1. Separação dos componentes de misturas heterogéneas Separação dos componentes de misturas heterogéneas Para separar os componentes de misturas utilizam-se processos físicos de separação. Durante o
Cópia autorizada. II
 II Sugestões de avaliação Ciências 9 o ano Unidade 1 5 Unidade 1 Nome: Data: 1. Qual é a importância do Sistema Internacional de Unidades (SI)? 2. O que diferencia as propriedades gerais e específicas
II Sugestões de avaliação Ciências 9 o ano Unidade 1 5 Unidade 1 Nome: Data: 1. Qual é a importância do Sistema Internacional de Unidades (SI)? 2. O que diferencia as propriedades gerais e específicas
O Que é Química? Pra que serve a Química?²
 O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas:
 01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS.
 SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
PROCESSOS DE SEPARAÇÃO. Professor Cassio Pacheco
 PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
Sumário. Química. Frente 1. Frente 2. Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88. Capítulo 4: A Tabela Periódica 96
 Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
JAMILE ROSA RAMPINELLI
 Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
Química B Extensivo V. 2
 Extensivo V. 2 Resolva Aula 5 5.01) A 5.02) C 5.03) Colocar água para separar o salitre e decantar ou filtrar. Depois pôr sulfeto de carbono no sólido restante para retirar o enxofre. que sobra é o carvão.
Extensivo V. 2 Resolva Aula 5 5.01) A 5.02) C 5.03) Colocar água para separar o salitre e decantar ou filtrar. Depois pôr sulfeto de carbono no sólido restante para retirar o enxofre. que sobra é o carvão.
9. (Uel 95) Uma escala de temperatura arbitrária X está relacionada com a escala Celsius, conforme o gráfico a seguir.
 1. (G1) Em uma determinada escala arbitrária o ponto de congelamento da água é de 10 unidades, enquanto que o ponto de ebulição é de 210 unidades. Todas as medidas feitas ao nível do mar. Qual é a temperatura
1. (G1) Em uma determinada escala arbitrária o ponto de congelamento da água é de 10 unidades, enquanto que o ponto de ebulição é de 210 unidades. Todas as medidas feitas ao nível do mar. Qual é a temperatura
SEPARAÇÃO DE MISTURAS
 SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
PROMILITARES 09/08/2018 QUÍMICA. Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS
 QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
CALORIMETRIA. 1 cal = 4,2 J.
 CALORIMETRIA Setor 1210 Prof. Calil A CALORIMETRIA estuda energia denominada CALOR que vai, de maneira natural, do corpo quente para o corpo frio. Calor não deve ser Calor sensivel confundido com a energia
CALORIMETRIA Setor 1210 Prof. Calil A CALORIMETRIA estuda energia denominada CALOR que vai, de maneira natural, do corpo quente para o corpo frio. Calor não deve ser Calor sensivel confundido com a energia
Lista de exercícios 1- Dos processos abaixo, qual pode ser caracterizado como fenômeno físico?
 Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 1º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Pensamento cientifico Laboratório químico Estados físicos e as transformações
Colégio FAAT Ensino Fundamental e Médio Lista de exercícios de Química - 1º Bimestre Nome: Ano: 9ºA/B/C Prof. Marcos Miranda N.: / /17 Pensamento cientifico Laboratório químico Estados físicos e as transformações
Atividade complementar de Química. Como escolher a melhor técnica de separação de misturas?
 Atividade complementar de Química Como escolher a melhor técnica de separação de misturas? Educação de Jovens e Adultos Existem inúmeras técnicas de separação de misturas, algumas muito simples que não
Atividade complementar de Química Como escolher a melhor técnica de separação de misturas? Educação de Jovens e Adultos Existem inúmeras técnicas de separação de misturas, algumas muito simples que não
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o SEMESTRE DE 2016
 ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o SEMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 2,0 ) I. Introdução Neste semestre, seu total de pontos foi inferior
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o SEMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 2,0 ) I. Introdução Neste semestre, seu total de pontos foi inferior
9 o EF. Jeosafá de P. Lima
 9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
Lista de exercícios. Temperatura e Dilatação Prof. Willian Rederde. 01-(Mackenzie-SP) Numa cidade da Europa, no decorrer de um ano, a temperatura
 Lista de exercícios Temperatura e Dilatação Prof. Willian Rederde 01-(Mackenzie-SP) Numa cidade da Europa, no decorrer de um ano, a temperatura mais baixa no inverno foi de 23 ºF e a mais alta no verão
Lista de exercícios Temperatura e Dilatação Prof. Willian Rederde 01-(Mackenzie-SP) Numa cidade da Europa, no decorrer de um ano, a temperatura mais baixa no inverno foi de 23 ºF e a mais alta no verão
Exercícios de Revisão
 Aluno: Ano: 9º Revisão: Avaliação Trimestral Disciplina: Física/Química Trimestre: 2º Nome do Professor: Marcos Benfica Exercícios de Revisão 1) Um garçom, desejoso por demonstrar suas habilidades, puxou
Aluno: Ano: 9º Revisão: Avaliação Trimestral Disciplina: Física/Química Trimestre: 2º Nome do Professor: Marcos Benfica Exercícios de Revisão 1) Um garçom, desejoso por demonstrar suas habilidades, puxou
4. (1,0) O gráfico representa a velocidade escalar de um atleta em função do tempo em uma competição olímpica.
 PARA A VALIDADE DO QiD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
PARA A VALIDADE DO QiD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS. Escola de Civismo e Cidadania
 COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2018 QUESTÃO 01 O QUE É QUÍMICA? QUESTÃO 02 O QUE É MATÉRIA? QUESTÃO 03 O QUE É TEMPERATURA? QUESTÃO 04 O QUE É TRANSFORMAÇÃO(OU
COLÉGIO ESTADUAL DA POLÍCIA MILITAR DE GOIÁS HUGO DE CARVALHO RAMOS ANO LETIVO 2018 QUESTÃO 01 O QUE É QUÍMICA? QUESTÃO 02 O QUE É MATÉRIA? QUESTÃO 03 O QUE É TEMPERATURA? QUESTÃO 04 O QUE É TRANSFORMAÇÃO(OU
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Classifique as transformações
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Classifique as transformações
Início. Substância pura simples. É formado por apenas um tipo de elemento químico. Exemplo: gás oxigênio (O 2), gás nitrogênio (N 2), ferro (Fe)
 Professores: Alinne Borges Tiago Albuquerque Sandro Sobreira Exercícios Substâncias puras e misturas Material que apresenta TF e TE constantes a uma dada pressão e densidade característica em determinada
Professores: Alinne Borges Tiago Albuquerque Sandro Sobreira Exercícios Substâncias puras e misturas Material que apresenta TF e TE constantes a uma dada pressão e densidade característica em determinada
BIMESTRAL QUÍMICA - 1ºBIMESTRE
 BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
1g / cm. 1g / cm. 80cal/ g
 1. (Unifesp 2015) Em um copo, de capacidade térmica 60cal / C e a 20 C, foram colocados 300mL de suco de laranja, também a 20 C, e, em seguida, dois cubos de gelo com 20 g cada um, a 0 C. Considere os
1. (Unifesp 2015) Em um copo, de capacidade térmica 60cal / C e a 20 C, foram colocados 300mL de suco de laranja, também a 20 C, e, em seguida, dois cubos de gelo com 20 g cada um, a 0 C. Considere os
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016
 ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 1,0 ) I. Introdução Neste bimestre, sua média foi inferior a 6,0
ROTEIRO DE RECUPERAÇÃO DE QUÍMICA 1 o BIMESTRE DE 2016 Nome: N o 9 o Ano Data: / / 2016 Professor(a): Andreza / Priscila Nota: ( Valor: 1,0 ) I. Introdução Neste bimestre, sua média foi inferior a 6,0
LOUCOS POR QUÍMICA. PROF. Neif Nagib
 LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
3. Existe uma temperatura que tem o mesmo valor na escala Celsius e na escala Fahrenheit. Qual é essa temperatura?
 FÍSICA CARLOS (A) 1. Maria usou um livro de receitas para fazer um bolo de fubá. Mas, ao fazer a tradução do livro do inglês para o português, a temperatura permaneceu em Fahrenheit (ºF). A receita disse
FÍSICA CARLOS (A) 1. Maria usou um livro de receitas para fazer um bolo de fubá. Mas, ao fazer a tradução do livro do inglês para o português, a temperatura permaneceu em Fahrenheit (ºF). A receita disse
PROCESSOS DE SEPARAÇÃO. Jeosafá Lima
 PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
Questão 2. (UFMG) Certas misturas podem ser separadas, usando-se uma destilação simples, realizável numa montagem, como a apresentada nesta figura:
 SE18 - Química LQUI1B2 - Separação de misturas Questão 1 (Cesgranrio 1992) Numa das etapas do tratamento da água que abastece uma cidade, a água é mantida durante um certo tempo em tanques para que os
SE18 - Química LQUI1B2 - Separação de misturas Questão 1 (Cesgranrio 1992) Numa das etapas do tratamento da água que abastece uma cidade, a água é mantida durante um certo tempo em tanques para que os
Prof. José Valter SEPARAÇÃO DE MISTURAS
 1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
PLANO DE ESTUDO TRIMESTRE: 1º
 C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 02 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 14/04/2018 DISCIPLINA : Química ANO/SÉRIE: 1º ANO
C O L É G I O K E N N E D Y / R E D E P I T Á G O R A S PLANO DE ESTUDO TRIMESTRE: 1º PLANO DE ESTUDO Nº 02 PROFESSORA: Rose Barbosa DATA DA AVALIAÇÃO: 14/04/2018 DISCIPLINA : Química ANO/SÉRIE: 1º ANO
2005 by Pearson Education. Capítulo 01
 QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução: matéria & medida David P. White O estudo da química A perspectiva molecular da química A matéria é o material físico do universo. A matéria é
QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução: matéria & medida David P. White O estudo da química A perspectiva molecular da química A matéria é o material físico do universo. A matéria é
Lista de Térmica Professor: Janer Telles
 Lista de Térmica Professor: Janer Telles Questão 01) Dois corpos A e B, de massas iguais, são aquecidos simultaneamente. O gráfico abaixo representa o comportamento térmico desses corpos durante o processo
Lista de Térmica Professor: Janer Telles Questão 01) Dois corpos A e B, de massas iguais, são aquecidos simultaneamente. O gráfico abaixo representa o comportamento térmico desses corpos durante o processo
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
https://edsonnossol.wordpress.com
 https://edsonnossol.wordpress.com enossol@ufu.br Classificação da matéria Química Fundamental I Prof. Edson Nossol Uberlândia, 12/04/2017 Matéria: é tudo aquilo que ocupa espaço e tem massa Química: estudo
https://edsonnossol.wordpress.com enossol@ufu.br Classificação da matéria Química Fundamental I Prof. Edson Nossol Uberlândia, 12/04/2017 Matéria: é tudo aquilo que ocupa espaço e tem massa Química: estudo
 ++ 12 131 12 1 = 234 25 6 ++ 12 123 14 5 12 123 45 6 12 123 14 5 + 123 45 6 12 + 12 123 45 6 + 12 123 43 12 1 = 234 25 6 H C CH CH C CH CH 3 2 2 2 3 O FC 3 O CH CH NH CH 2 3 1213 1 1 1 1 1 1 1 1 1 1 1
++ 12 131 12 1 = 234 25 6 ++ 12 123 14 5 12 123 45 6 12 123 14 5 + 123 45 6 12 + 12 123 45 6 + 12 123 43 12 1 = 234 25 6 H C CH CH C CH CH 3 2 2 2 3 O FC 3 O CH CH NH CH 2 3 1213 1 1 1 1 1 1 1 1 1 1 1
Os processos físicos de separação dos componentes das misturas são escolhidos de acordo com:
 Separação dos componentes de misturas heterogéneas (Pp. 55 a 58) Processos de separação dos componentes de misturas heterogéneas Separação magnética Peneiração Sublimação Dissolução fracionada Decantação
Separação dos componentes de misturas heterogéneas (Pp. 55 a 58) Processos de separação dos componentes de misturas heterogéneas Separação magnética Peneiração Sublimação Dissolução fracionada Decantação
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA
 ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 1º. ALUNO(a):
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 1º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 1º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
Colégio FAAT Ensino Fundamental e Médio
 Colégio FAAT Ensino Fundamental e Médio Lista de Exercícios 2_3 BIMESTRE Nome: Nº Turma: 9 EF Profa Kelly Data: Conteúdo: Calorimetria. 1 Um bloco de 600 g de prata, inicialmente a 20 C, é aquecido até
Colégio FAAT Ensino Fundamental e Médio Lista de Exercícios 2_3 BIMESTRE Nome: Nº Turma: 9 EF Profa Kelly Data: Conteúdo: Calorimetria. 1 Um bloco de 600 g de prata, inicialmente a 20 C, é aquecido até
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROFESSOR: JOÃO MEDEIROS
 COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
Química B Semiextensivo V. 1
 Química B Semiextensivo V. 1 Exercícios 01) A 02) C 03) A 04) E d = m v Densidade e massa são diretamente proporcionais, ou seja, quanto maior a massa da substância, maior será sua densidade. Já o volume
Química B Semiextensivo V. 1 Exercícios 01) A 02) C 03) A 04) E d = m v Densidade e massa são diretamente proporcionais, ou seja, quanto maior a massa da substância, maior será sua densidade. Já o volume
1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente:
 2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
Sala de Estudos FÍSICA - Lucas 1 trimestre Ensino Médio 2º ano classe: Prof.LUCAS Nome: nº CALORIMETRIA:
 Sala de Estudos FÍSICA - Lucas 1 trimestre Ensino Médio 2º ano classe: Prof.LUCAS Nome: nº CALORIMETRIA: Calor Sensível 1. (Uel 2012) O homem utiliza o fogo para moldar os mais diversos utensílios. Por
Sala de Estudos FÍSICA - Lucas 1 trimestre Ensino Médio 2º ano classe: Prof.LUCAS Nome: nº CALORIMETRIA: Calor Sensível 1. (Uel 2012) O homem utiliza o fogo para moldar os mais diversos utensílios. Por
Química B Extensivo V. 1
 Química B Extensivo V. 1 Resolva Aula 1 Aula 3 1.01) O açúcar se divide e preenche os espaços vazios existentes na água. 3.01) C 1.0) Plástico. 1.03) Acidez. Aula.01) C I Condensação II Fusão S III Ebulição
Química B Extensivo V. 1 Resolva Aula 1 Aula 3 1.01) O açúcar se divide e preenche os espaços vazios existentes na água. 3.01) C 1.0) Plástico. 1.03) Acidez. Aula.01) C I Condensação II Fusão S III Ebulição
MÉTODOS DE SEPARAÇÃO DE MISTURAS. 9º ano
 MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
Dados: - calor latente de vaporização da água: 540cal/g - calor específico da água: 10cal/g C
 1. (Fuvest 92) Adote: calor específico da água = 1 cal/g. C Um recipiente contendo 3600g de água à temperatura inicial de 80 C é posto num local onde a temperatura ambiente permanece sempre igual a 20
1. (Fuvest 92) Adote: calor específico da água = 1 cal/g. C Um recipiente contendo 3600g de água à temperatura inicial de 80 C é posto num local onde a temperatura ambiente permanece sempre igual a 20
Estados de agregação da matéria. Mudanças de estado. Fenômenos
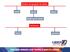 Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria.
 O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
TAREFÃO DE CIÊNCIAS (QUÍMICA) 9 ANO
 TAREFÃO DE CIÊNCIAS (QUÍMICA) 9 ANO NOME: PROFESSORA: CHRISTIANE FRÓES Capitulo 01 - Química: do macro ao micro um mundo em constante transformação. Capitulo 02 - Transformações, propriedades e composição
TAREFÃO DE CIÊNCIAS (QUÍMICA) 9 ANO NOME: PROFESSORA: CHRISTIANE FRÓES Capitulo 01 - Química: do macro ao micro um mundo em constante transformação. Capitulo 02 - Transformações, propriedades e composição
Sala de Estudos FÍSICA - Lucas 1 trimestre Ensino Médio 2º ano classe: Prof.LUCAS Nome: nº
 Sala de Estudos FÍSICA - Lucas 1 trimestre Ensino Médio 2º ano classe: Prof.LUCAS Nome: nº CALORIMETRIA: Calor Sensível 1. (Uel 2012) O homem utiliza o fogo para moldar os mais diversos utensílios. Por
Sala de Estudos FÍSICA - Lucas 1 trimestre Ensino Médio 2º ano classe: Prof.LUCAS Nome: nº CALORIMETRIA: Calor Sensível 1. (Uel 2012) O homem utiliza o fogo para moldar os mais diversos utensílios. Por
Disciplina: Química Segmento: EM Ano/Série: 1º Turma: TA Assunto: Roteiro de Estudos Para Recuperação da I Etapa /2019 Aluno (a): Nº: Nota:
 Disciplina: Química Segmento: EM Ano/Série: 1º Turma: TA Assunto: Roteiro de Estudos Para Recuperação da I Etapa /2019 Aluno (a): Nº: Nota: Valor: 5,0 Pontos Professor (a): Rodrigo Xavier Querido (a) aluno
Disciplina: Química Segmento: EM Ano/Série: 1º Turma: TA Assunto: Roteiro de Estudos Para Recuperação da I Etapa /2019 Aluno (a): Nº: Nota: Valor: 5,0 Pontos Professor (a): Rodrigo Xavier Querido (a) aluno
Separação de Misturas
 Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
Turma: 2301 Turno: Manhã Professor: Douglas Baroni
 Colégio Zaccaria TELEFAX: (0 XX 21) 3235-9400 www.zaccaria.g12.br Lista de exercícios Física II (Recuperação) 1º Período 2014 Aluno(a): N.º Turma: 2301 Turno: Manhã Professor: Douglas Baroni QUESTÃO 1
Colégio Zaccaria TELEFAX: (0 XX 21) 3235-9400 www.zaccaria.g12.br Lista de exercícios Física II (Recuperação) 1º Período 2014 Aluno(a): N.º Turma: 2301 Turno: Manhã Professor: Douglas Baroni QUESTÃO 1
Ficha de Avaliação Sumativa 5
 Ficha de Avaliação Sumativa 5 DISCIPLINA: Física e Química 7 ºAno de escolaridade 2015/2016 Data: Nome: Turma: N.º Classificação: (%) A Docente: E. E: As respostas às questões deste enunciado devem ser
Ficha de Avaliação Sumativa 5 DISCIPLINA: Física e Química 7 ºAno de escolaridade 2015/2016 Data: Nome: Turma: N.º Classificação: (%) A Docente: E. E: As respostas às questões deste enunciado devem ser
NOME: TURMA: 33AA / 33IA / 33MA Nº PROFESSOR: ELIO ASSALIN TRABALHO DE RECUPERAÇÃO DE FÍSICA (VALOR DE 2,0 PONTOS) NOTA:
 NOME: TURMA: 33AA / 33IA / 33MA Nº PROFESSOR: ELIO ASSALIN TRABALHO DE RECUPERAÇÃO DE FÍSICA (VALOR DE 2,0 PONTOS) NOTA: Questões do 1 bimestre: Conteúdo: Escalas termométricas, conversão de temperatura
NOME: TURMA: 33AA / 33IA / 33MA Nº PROFESSOR: ELIO ASSALIN TRABALHO DE RECUPERAÇÃO DE FÍSICA (VALOR DE 2,0 PONTOS) NOTA: Questões do 1 bimestre: Conteúdo: Escalas termométricas, conversão de temperatura
Estado Físico Características Macroscópicas Características Microscópicas
 Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Aulas Multimídias Santa Cecília Professor Tiago Quick Disciplina: Química Série: 9º ano EF
 Aulas Multimídias Santa Cecília Professor Tiago Quick Disciplina: Química Série: 9º ano EF Professor: Tiago Albuquerque Slides: Alinne Borges alinne.borges@gmail.com Exercícios Substâncias puras e misturas
Aulas Multimídias Santa Cecília Professor Tiago Quick Disciplina: Química Série: 9º ano EF Professor: Tiago Albuquerque Slides: Alinne Borges alinne.borges@gmail.com Exercícios Substâncias puras e misturas
Apostila de Química 12 A Matéria
 Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Exercícios de Recuperação
 Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2º Período Aluno(a): Nº Turma: 1-9 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Fenômenos 1. As transformações
Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2º Período Aluno(a): Nº Turma: 1-9 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Fenômenos 1. As transformações
2-Nos sistemas abaixo, diga quantos átomos, elementos, moléculas e substâncias estão representados:
 LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
Projeto de Recuperação Final - 1ª Série (EM)
 Projeto de Recuperação Final - 1ª Série (EM) FÍSICA MATÉRIA A SER ESTUDADA VOLUME CAPÍTULO ASSUNTO 5 16 Hidrostática II 5 18 Introdução à termometria 5 18 Dilatação térmica dos sólidos 6 20 Calorimetria
Projeto de Recuperação Final - 1ª Série (EM) FÍSICA MATÉRIA A SER ESTUDADA VOLUME CAPÍTULO ASSUNTO 5 16 Hidrostática II 5 18 Introdução à termometria 5 18 Dilatação térmica dos sólidos 6 20 Calorimetria
Lista - Separação dos componentes de um sistema
 ! Lista - Separação dos componentes de um sistema 1) (ENEM) O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo
! Lista - Separação dos componentes de um sistema 1) (ENEM) O principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo
26/08/15 SUBSTÂNCIAS E MISTURAS. Prof. Ms. Mayanderson (Xuxu)
 SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
Lista de Exercícios Clinton. Física
 Lista de Exercícios Clinton Física SÉRIE: 2º ANO DATA: 31 / 01 / 7 01. (UFSM-RS) Calor é: a) a energia contida em um corpo. b) a energia que se transfere de um corpo para outro, quando existe uma diferença
Lista de Exercícios Clinton Física SÉRIE: 2º ANO DATA: 31 / 01 / 7 01. (UFSM-RS) Calor é: a) a energia contida em um corpo. b) a energia que se transfere de um corpo para outro, quando existe uma diferença
