Universidade Federal de Santa Catarina UFSC, Departamento de química, Florianópolis-SC 2
|
|
|
- Caio Amaro Sanches
- 7 Há anos
- Visualizações:
Transcrição
1 NANOPARTÍCULAS OBTIDAS A PARTIR DA PROTEÍNA ISOLADA DE SOJA (SPI) PELO MÉTODO DE COACERVAÇÃO EM ÁGUA: EFEITO DA FORÇA IÔNICA E DAS CONCENTRAÇÕES DE PROTEÍNA E SURFACTANTE. Samira J. Fayad 1 *, Betina G. Z. Ramos 2, Edson Minatti 1, Valdir Soldi 1 1 Universidade Federal de Santa Catarina UFSC, Departamento de química, Florianópolis-SC *samira@qmc.ufsc.br 2 Universidade Federal de Santa Catarina UFSC, Departamento de ciências farmacêuticas, Florianópolis-SC Neste trabalho investigamos a obtenção de nanopartículas formadas pela SPI através da coacervação de suspensões aquosas em solução aquosa hostil. Tal método foi eficaz no preparo de partículas do biopolímero, com tamanho determinado por espalhamento de luz como sendo entre 200 a 400 nm. Investigamos o efeito de variáveis como concentração da proteína na suspensão aquosa, a concentração do surfactante Tween 80 e a força iônica na fase aquosa hostil. Os resultados preliminares são promissores, pois indicam um método eficaz e ecologicamente correto (sem solventes orgânicos) para o preparo de nanopartículas deste biopolímero. Estas partículas podem servir como matrizes para incorporação de fármacos, aditivos alimentares, fertilizantes, pesticidas e herbicidas, entre outros. Palavras-chave: Proteína Isolada de Soja, nanopartículas e espalhamento de luz. NANOPARTICLES MADE FROM SOY-BEAN PROTEIN ISOLATE BY COACERVATION IN WATER: EFFECT OF IONIC STRENGTH AND THE CONCENTRATIONS OF PROTEIN AND SURFACTANT We investigated the preparation of nanoparticles made from Soy Protein Isolate (SPI) through coacervation of SPI aqueous suspensions in hostile buffer. We succeed in obtaining particles with diameters ranging from 200 up to 400 nm using the coacervation method; we then explored the effects of SPI concentration before coacervation and the ionic strength and surfactant concentration of the hostile buffer. The preliminary results are promising and indicate a efficient and green (free of organic solvents) method to obtain nanoparticles from SPI. In addition, the observations from the emulsion/vaporization method also show that the protein can be easily crosslinked; thus, these particles may well be used as matrix for encapsulation of drugs, food additives, fertilizers, herbicides and others. Keywords: Soy Protein Isolate, nanoparticles, light scattering. Introdução Com mais de 90% de proteína, [01] a Proteína Isolada de Soja (SPI) é a forma mais refinada entre os derivados protéicos mais comuns. Encontra-se na forma de um pó de coloração creme e sabor suave, preparado a partir da fração protéica dos grãos de soja e separada dos componentes não-protéicos através de um processo de purificação baseado em sua solubilidade e reatividade química. [02,03] Após a retirada da casca e do óleo dos grãos de soja, uma farinha desengordurada é preparada, a partir da qual se obtém a SPI por meio de um processo de extração em fase aquosa que explora a variação da solubilidade da SPI em função do ph (Figura 1).
2 Figura 1. Diagrama de solubilidade para a SPI em função do ph da solução [04]. Produto praticamente livre de carboidratos e de gordura, a SPI é constituída pelas proteínas de armazenamento da soja e compreende um conjunto de macromoléculas de tamanhos e estruturas variadas. A SPI é utilizada como alternativa nutricional, funcional ou econômica em substituição a outros tipos de proteínas tradicionais em alimentos como bebidas, produtos de panificação, cereais, carne de frango, carne de gado e produtos de pescado. [05] Devido a sua biocompatibilidade e biodegradabilidade, os sistemas com nanopartículas de biopolímeros vêm sendo desenvolvidos visando inúmeras aplicações para fins terapêuticos e de liberação de fertilizantes e inseticidas. [06] Existem vários métodos relatados na literatura para a preparação de nanopartículas de biopolímeros. Independente do método de preparação os produtos são obtidos como suspensões coloidais aquosas. Todavia, durante o tempo de armazenamento, pode ocorrer a agregação das partículas no meio, procedendo na formação de precipitados, além de problemas de estabilidade química do biopolímero ou das demais matérias-primas presentes no meio. Consequentemente, a limitada estabilidade físico-química em função do tempo gera uma limitação para aplicações industriais das suspensões aquosas de nanopartículas. [06] O método de coacervação envolve a separação do material polimérico da sua solução através de alterações das características do meio que causam a dessolvatação da macromolécula, por exemplo, mudança de ph, aquecimento, adição de um não solvente, sal ou outro polímero incompatível ou alteração da carga do polímero envolvido. [07] Apesar de ser uma técnica muito utilizada, a coacervação é frequentemente prejudicada por resíduos de solventes e agentes coacervantes encontrados nas esferas. Na literatura, estão disponíveis muitos artigos de revisão referentes à nanopartículas direcionados principalmente aos diferentes métodos de preparação e às potencialidades terapêuticas destes sistemas. Entretanto, não são encontrados artigos direcionados especificamente à caracterização físico-química e à proposição das formas de associação de fármacos a nanocápsulas
3 e nanoesferas formadas por SPI. Este trabalho tem como objetivo investigar as metodologias de emulsificação/evaporação e coacervação para a obtenção de nanopartículas formadas pela SPI e efeitos de algumas variáveis nos métodos de preparação e nas características físico-químicas das partículas obtidas. Experimental Materiais A SPI (Supro 500E) utilizada foi fornecida pela The Solae Company, Brasil. O óleo mineral e o surfactante Tween 80 (monooleato de sorbitano etoxilado) foram adquiridos da VETEC Química Fina LTDA RJ, Brasil. O ácido acético glacial e o acetato de sódio usados para preparar a solução tampão e hidróxido de sódio usado para ajustar o ph das soluções poliméricas foram adquiridos da empresa Nuclear. Partículas preparadas pela técnica de coacervação Inicialmente, foram preparadas soluções aquosas de SPI (solução 1) em diferentes concentrações 0,1% a % (m/v) com ph ajustado para 10 através da adição de NaOH(aq) 1,5 mol L -1. Posterior ao ajuste de ph, as soluções permaneceram 24 horas sob agitação magnética a temperatura ambiente. Paralelamente, seguiu-se a preparação da solução tampão hostil, i.e., a solução com ph onde ocorre precipitação da SPI, conforme mostrado na Figura 1, e é usada para o processo de coacervação. A solução tampão ácido acético/acetato de sódio foi preparada com o ph ajustado para 5 pela adição de NaOH(aq) 1,5 mol L -1. Com esta solução tampão duas soluções de Tween 80 foram preparadas, respectivamente com % e 1,0% (m/m) de surfactante. Conforme o esquema da figura 2, depois de prontas as soluções, para cada formulação, 85 ml da solução tampão hostil foram submetidos a um dispersor (Quimis) sob uma velocidade de agitação de 6000 rpm e 3mL da solução 1 foram então adicionados por gotejamento. A mistura final permaneceu sob agitação por 1 minuto. Figura 2. Ilustração do método de coacervação.
4 Determinação de distribuição de tamanho das partículas A determinação da distribuição de tamanho das nanopartículas foi realizada a 25 C empregando-se um equipamento Zetasizer Nano Malvern. As medidas de tamanho e distribuição de tamanho das partículas dispersas foram feitas através da técnica de espalhamento de luz dinâmico (DLS). Esta técnica baseia-se no princípio de que uma partícula em suspensão sofre movimento Browniano e seu tamanho pode ser obtido usando a relação de Stokes-Einstein, que relaciona o coeficiente de difusão e o raio hidrodinâmico da partícula. [08] Os valores do índice de polidispersidade (PDI) variam de 0, para uma amostra idealmente monodispersa, a 1, para uma amostra com uma distribuição de tamanho bastante larga. O PDI foi determinado através de medidas de DLS no ângulo de 173 e deriva da fórmula PDI 2 σ =, 2 Ð H onde σ é o desvio médio da distribuição de tamanho (em nm) e Đ H é o diâmetro médio (em nm) da partícula. [08] Determinação do potencial Zeta das partículas As medidas de potencial Zeta das nanopartículas foram realizadas a 25 C empregando-se um equipamento Zetasizer Nano Malvern. As medidas de potencial Zeta refletem o potencial elétrico da superfície das nanopartículas, o qual é influenciado pelas mudanças na interface com o meio dispersante, em razão da dissociação de grupos funcionais na superfície da partícula ou da adsorção de espécies iônicas presentes no meio aquoso da dispersão. [09] O potencial Zeta é medido aplicando-se um campo elétrico através da dispersão. As partículas que possuem um potencial Zeta migram para o eletrodo de carga oposta com uma velocidade proporcional ao valor de seu potencial. Esta velocidade é medida usando a técnica Laser Doppler Anemometry. [08] Resultados e Discussão Obtenção e caracterização de nanopartículas obtidas pelo método de coacervação Obtivemos nanopartículas de SPI através do método de coacervação. Investigamos a distribuição de tamanho e potencial de superfície das partículas em função de algumas variáveis no método de preparação, tal como descrito a seguir. 1. Análise da distribuição de tamanho das nanopartículas 1. a)efeito da força iônica da solução tampão hostil
5 A solução que promove a coacervação é a solução tampão hostil, que consiste em uma solução de surfactante tamponada em ph = 5. A força iônica do tampão pode ser ajustada e apresenta grande efeito no tamanho das partículas, como ilustrado na Figura 3(a). A figura indica que o diâmetro médio das partículas é menor quando a força iônica é pequena; quando I=20mM as partículas passam a ter dimensões micrométricas. A figura também indica que a concentração de SPI(aq) na Solução 1 não tem um efeito muito pronunciado no tamanho das partículas, ao menos na faixa estudada. O aumento da força iônica também leva ao aumento da polidispersidade em tamanho das partículas, como visto na Figura 3(b). As partículas obtidas com I=1mM são as menos polidispersas, enquanto que o índice de polidispersidade chega a 1 para as partículas preparadas com I=20mM. Estas observações sugerem que o aumento de força iônica promove a coalescência das partículas menores, produzindo um sistema mais polidisperso e com maior população de partículas maiores. A explicação para este comportamento pode ser encontrada se considerarmos a teoria DLVO para o mecanismo de estabilidade de dispersões coloidais. De acordo com este modelo, o potencial total de interação entre duas partículas em uma dispersão é o somatório do potencial de atração (Equação 1), que tem origem em forças atrativas do tipo van der Waals, e do potencial de repulsão, que está relacionado à presença de carga na superfície das partículas. [10] A magnitude do potencial de repulsão V R é determinante na estabilidade de uma partícula. Este potencial (Equação 2) é uma função do raio a da partícula, do potencial de superfície Ψ 0 e da distância H entre as partículas. O fator exponencial κ é o recíproco do comprimento de Debye κ -1, que reflete a largura da dupla camada elétrica difusa de íons que orbita a partícula. Quanto maior for κ -1, maior será a barreira de repulsão elétrica para o processo de coalescência de duas partículas. Entretanto, como demonstrado na Equação 3, o comprimento de Debye diminui com o aumento da força iônica. [10,11] Em outras palavras, o aumento da força iônica promove a contração da dupla camada elétrica difusa e, consequentemente, diminui o potencial de repulsão V R. Isto facilita a coalescência das partículas, justificando o tamanho e a alta polidispersidade nas formulações com I=20mM. V = V + V (Eq. 1) T A R V R 2 2 εra Ψ0 κh = e (Eq. 2) R εrε0 = 2 (Eq.3) κ 2πF I
6 Polidispersidade 0,9 0,6 0,3 0,1 0,2 0,3 0,4 (b) 0, I/mM ,1 0,2 0,3 0,4 (a) D/nm I/mM Figura 3. (a) Diâmetro e (b) polidispersidade em função da força iônica da solução tampão hostil com % (m/m) de Tween b)efeito da concentração de surfactante na solução tampão hostil Outra variável de ajuste no preparo das emulsões foi a concentração do surfactante Tween 80 na solução tampão hostil (na força iônica I=1mM). A Figura 4(a) apresenta os valores do diâmetro médio das partículas de SPI obtidas em diferentes [SPI(aq)], para dois sistemas com diferentes concentrações do surfactante % e 1,0% (m/m) de Tween 80 na solução tampão hostil. A Figura 4(b) apresenta a polidispersidade em tamanho dos mesmos sistemas. Embora o efeito do aumento da concentração de surfactante não seja muito pronunciado, leva à diminuição do tamanho médio e da polidispersidade nas formulações com até 0,2% SPI e ao aumento do tamanho e da polidispersidade nas formulações mais concentradas. Este comportamento é justificado pelo seguinte mecanismo: as moléculas de Tween são adsorvidas na superfície das partículas formadas durante a coacervação. Quando a concentração de proteína é pequena, as moléculas de Tween atuam como agentes de estabilização estérica, prevenindo a coalescência. O excesso de Tween na fase aquosa, não
7 adsorvido na região interfacial, atua como um agente de estabilização por depleção. Ambos processos levam a partículas menores. Se a concentração de SPI for maior a população de partículas aumenta e, durante a coacervação, uma mesma molécula de Tween 80 pode ser adsorvida nas superfícies de duas ou mais partículas, levando a um processo de floculação-coagulação via ponte de Tween 80. Ainda, o aumento da concentração de SPI leva ao aumento da área superficial para adsorção de surfactante; isto diminui a estabilização por depleção, pois há menos moléculas de Tween dissolvidas na fase aquosa. Ambos os processos levam a um aumento do tamanho das partículas. 400 [Tween 80]/% 1,0 (a) 0,4 [Tween 80]/% 1,0 (b) D/nm 200 Polidispersidade 0,3 0,2 0,1 0 0,1 0,2 0,3 0,4 0,1 0,2 0,3 0,4 Figura 4. (a) Diâmetro e (b) polidispersidade em função da concentração de SPI na presença de diferentes concentrações de Tween 80 na solução tampão hostil. 2. Análise do potencial Zeta das partículas Uma partícula carregada atrai uma camada compacta de íons de carga oposta que são adsorvidos na superfície. Esta camada de íons é conhecida como camada de Stern e seu potencial elétrico como potencial de Stern (Ψ o ). A ação deste campo elétrico atrai uma camada difusa de íons ao redor da partícula, até a dissipação do potencial em distâncias maiores. Esta é chamada de dupla camada elétrica difusa, ou camada de Gouy-Chapman.[12] A interação entre partículas carregadas é governada predominantemente pela sobreposição das duplas camadas elétricas difusas e, portanto, do potencial de Stern. Este potencial se dissipa ao se afastar da superfície da partícula e pode ser descrito pelo modelo de Poisson Boltzmann, que dá o potencial a uma distância H do plano de Stern. [12] H ( H ) e κ 0 Ψ = Ψ (Eq. 4)
8 Entretanto, não há método experimental para a medida direta do potencial de Stern. O que se mede é o potencial elétrico na unidade eletrocinética, i.e., da partícula, dos íons e moléculas do solvente inclusos no plano de cisalhamento quando submetidos a um potencial elétrico. Este potencial eletrocinético é conhecido como potencial Zeta, ζ. Em geral, dispersões com partículas de potencial Zeta alto são consideradas estáveis, enquanto que partículas com valor menor tendem a coalescência e coagulação. 2. a)efeito da força iônica da solução tampão hostil Como as equações 3 e 4 sugerem, o aumento da força iônica promove a contração do comprimento de Debye e a diminuição do potencial Zeta. Isto foi verificado experimentalmente, tal como exibido na Figura 5. O potencial Zeta de todas as partículas é negativo, indicando que mesmo em ph = 5 a carga residual das cadeias de SPI é negativa. Observa-se ainda que, para uma mesma força iônica, o aumento da concentração de SPI leva a um aumento do potencial Zeta, indicando a formação de partículas com maior densidade de carga superficial ζ/mv -15 0,1-10 0,2 0,3-5 0, I/mM Figura 5. Potencial Zeta em função da força iônica da solução tampão hostil com % (m/m) de Tween 80. Como exibido na figura, o aumento da força iônica levou a diminuição do potencial Zeta; este fator favoreceu a coalescência das partículas e, como já exibido anteriormente, produziu partículas maiores e mais polidispersas. 2. b)efeito da concentração de surfactante na solução tampão hostil A Figura 6 mostra o efeito do aumento da concentração de proteína no potencial Zeta das partículas em soluções tampão hostil (na força iônica I=1mM) feitas com duas concentrações de surfactante Tween 80. Como visto anteriormente, o aumento da concentração de proteína leva ao aumento do potencial Zeta das partículas, devido ao aumento da quantidade de carga superficial. O efeito do aumento da concentração de surfactante é o de aumentar o potencial Zeta nas soluções com concentração de SPI <0,4%. Como já discutido, as moléculas de Tween adsorvem na
9 superfície das partículas. O impedimento estérico causado pelos segmentos das moléculas de surfactante desloca alguns íons do plano de cisalhamento e da camada de Stern, diminuindo a neutralização do potencial de superfície. Isto é observado através do aumento do potencial eletrocinético. Já em concentrações maiores de proteína o potencial Zeta medido foi ligeiramente menor quando a concentração de Tween 80 era de 1% (m/m). Neste caso, o efeito anterior pode ter sido compensado pelo aumento do diâmetro médio das partículas, tal como anteriormente demonstrado. Conforme a equação de Hückel (Equação 5), o potencial eletrocinético é diretamente proporcional à carga Q E da unidade eletrocinética e decresce com o aumento do raio a das partículas. [12] Como o aumento da concentração de surfactante levou ao aumento do tamanho das partículas obtidas com as soluções de concentrações de SPI mais alta, produziu partículas com menor potencial eletrocinético. ζ = E (Eq. 5) 4π a( εq 1+ κa ) [Tween 80]/% 1,0 ζ/mv ,1 0,2 0,3 0,4 Figura 6. Potencial Zeta em função da concentração de SPI na presença de diferentes concentrações de Tween 80 na solução tampão hostil. Conclusões O método de coacervação foi eficaz no preparo de nanopartículas de SPI com tamanho entre 200 a 400 nm. O aumento da força iônica na fase aquosa hostil levou à diminuição do potencial Zeta e ao aumento da distribuição de tamanho das partículas. O aumento da concentração do surfactante Tween 80 na fase aquosa hostil causou aumento do diâmetro médio e da polidispersidade e diminuição do potencial Zeta das partículas nas formulações com maior concentração de SPI. Já em concentrações menores de proteína, houve diminuição do tamanho e da polidispersidade e aumento do potencial Zeta com o aumento da concentração de surfactante. Na faixa estudada, a concentração de proteína não tem efeito pronunciado na distribuição de tamanho das partículas, porém, leva ao aumento do potencial Zeta das mesmas. Agradecimentos
10 CNPq, UFSC e The Solae Company. Referências Bibliográficas 1. A. Akesowan. Afr. J. Biotechnol. 2008, 7 (24), , 2. P. Lodha; A. N. Netravali. Ind. Crops Prod. 2005, 21, R. Kumar, et al. Ind. Crops Prod. 2002, 16, C. M. M. D. J. Lakemond, et al. J. Agric. Food. Chem. 2000, 48, The Solae Company. Disponível em: < Acesso em 4 fevereiro S. R. Schaffazick, et al. Quim. Nova. 2003, 26, P. J. Watts; M. C. Davies; C. D. Melia. Crit. Rev. Ther. Drug Carrier Syst. 1990, 7, Malvern Instruments. Disponível em: < Zeta_potential/Zeta_potential_LDE.htm>. Acesso em 15 maio Z. Dong; Q. Wang; Y. Du. J. Membr. Sci. 2006, 280, D. Myers. Surfaces, Interfaces, and Colloids: Principles and Applications, John Wiley & Sons, Ed.; New York, D. J. Shaw. Introduction to Colloid and Surface Chemistry, Butterworth-Heinemann, Ed.; M. J. Schick; A. T. Hubbard. Emulsions And Emulsion Stability, Taylor & Francis Group, LLC, Ed.; Santa Barbara, 2006.
NANOPARTÍCULAS DE PROTEÍNA ISOLADA DE SOJA EM ÁGUA: EFEITO DA FORÇA IÔNICA E DAS CONCENTRAÇÕES DE PROTEÍNA E SURFACTANTE
 Quim. Nova, Vol. 38, No. 1, 91-96, 2015 http://dx.doi.org/10.5935/0100-4042.20140295 NANOPARTÍCULAS DE PROTEÍNA ISOLADA DE SOJA EM ÁGUA: EFEITO DA FORÇA IÔNICA E DAS CONCENTRAÇÕES DE PROTEÍNA E SURFACTANTE
Quim. Nova, Vol. 38, No. 1, 91-96, 2015 http://dx.doi.org/10.5935/0100-4042.20140295 NANOPARTÍCULAS DE PROTEÍNA ISOLADA DE SOJA EM ÁGUA: EFEITO DA FORÇA IÔNICA E DAS CONCENTRAÇÕES DE PROTEÍNA E SURFACTANTE
Colóides: estruturas esféricas com dimensões típicas na faixa de 1 m a 1 nm.
 Colóides: estruturas esféricas com dimensões típicas na faixa de 1 m a 1 nm. Dispersões coloidais são compostas por uma fase dispersa (colóides) e uma fase contínua. Continuous phase Gas Liquid Solid Gas
Colóides: estruturas esféricas com dimensões típicas na faixa de 1 m a 1 nm. Dispersões coloidais são compostas por uma fase dispersa (colóides) e uma fase contínua. Continuous phase Gas Liquid Solid Gas
CQ110 : Princípios de FQ
 Fenômenos de Interface Devido às diferentes interações, as moléculas superficiais possuem uma maior energia, dessa forma, para deslocar uma molécula do interior do sistema para sua superfície, uma energia
Fenômenos de Interface Devido às diferentes interações, as moléculas superficiais possuem uma maior energia, dessa forma, para deslocar uma molécula do interior do sistema para sua superfície, uma energia
Relatório Aula Prática Nanopartícula de Prata/ Curva de Calibração da Curcumina. A) Método biológico utilizando extrato de planta (ipê branco)
 Victor Yuji Viski Luiz Claudio Ferreira Philipe Tegoshi Vinicius Souza Relatório Aula Prática Nanopartícula de Prata/ Curva de Calibração da Curcumina A) Método biológico utilizando extrato de planta (ipê
Victor Yuji Viski Luiz Claudio Ferreira Philipe Tegoshi Vinicius Souza Relatório Aula Prática Nanopartícula de Prata/ Curva de Calibração da Curcumina A) Método biológico utilizando extrato de planta (ipê
COLÓIDES. Colóide: partícula com uma dimensão linear entre 1nm e 1µm (1000 nm).
 COLÓIDES Colóide: partícula com uma dimensão linear entre 1nm e 1µm (1000 nm). Dispersão coloidal: Sistema heterogéneo de partículas coloidais (colóides) dispersas num fluido Dispersão coloidal (2 fases)
COLÓIDES Colóide: partícula com uma dimensão linear entre 1nm e 1µm (1000 nm). Dispersão coloidal: Sistema heterogéneo de partículas coloidais (colóides) dispersas num fluido Dispersão coloidal (2 fases)
O Estado Coloidal. Química dos Colóides e Superfícies. M.Sc. Maron Stanley Silva O. Gomes Site: marongomes.wix.
 Química dos Colóides e Superfícies Profº Janilson Lima Souza E-mail: Prof. janilsonlima@ifma.edu.br M.Sc. Maron Stanley Silva O. Gomes E-mail: maron@ifma.edu.br Site: marongomes.wix.com/maron A Ciência
Química dos Colóides e Superfícies Profº Janilson Lima Souza E-mail: Prof. janilsonlima@ifma.edu.br M.Sc. Maron Stanley Silva O. Gomes E-mail: maron@ifma.edu.br Site: marongomes.wix.com/maron A Ciência
Dispersões Coloidais
 Dispersões Coloidais As dispersões coloidais são misturas heterogêneas ( mesmo sendo uma mistura homogênea) nas quais a partícula da fase dispersa é invisível As dispersões coloidais são compostas por
Dispersões Coloidais As dispersões coloidais são misturas heterogêneas ( mesmo sendo uma mistura homogênea) nas quais a partícula da fase dispersa é invisível As dispersões coloidais são compostas por
COLÓIDES. Prof. Harley P. Martins filho SISTEMAS COLOIDAIS. Colóide: dispersão de pequenas partículas de um material em outro
 COLÓIDES Prof. Harley P. Martins filho SISTEMAS COLOIDAIS Colóide: dispersão de pequenas partículas de um material em outro Faixa de tamanho das partículas coloidais 10-9 a 10-6 m Classificação geral:
COLÓIDES Prof. Harley P. Martins filho SISTEMAS COLOIDAIS Colóide: dispersão de pequenas partículas de um material em outro Faixa de tamanho das partículas coloidais 10-9 a 10-6 m Classificação geral:
Mestrado em Ciência de Materiais Faculdade UnB - Planaltina. Prof. Alex Fabiano C. Campos, Dr
 Mestrado em Ciência de Materiais Faculdade UnB - Planaltina Introdução aos Sistemas Coloidais Prof. Alex Fabiano C. Campos, Dr Sistemas Dispersos DISPERSÃO é, genericamente, uma mistura de duas ou mais
Mestrado em Ciência de Materiais Faculdade UnB - Planaltina Introdução aos Sistemas Coloidais Prof. Alex Fabiano C. Campos, Dr Sistemas Dispersos DISPERSÃO é, genericamente, uma mistura de duas ou mais
Miniemulsão: - fase dispersa, fase contínua,emulsificante, co-emulsificante - Goticulas com diametro variando de 50 nm a 400 nm
 Emulsão de óleo em água O/A Emulsão de água em óleo A/O O A A O Nanoemulsão: - Goticulas com diametro < 100 nm -Termodinamicamente instável - transparente Miniemulsão: - fase dispersa, fase contínua,emulsificante,
Emulsão de óleo em água O/A Emulsão de água em óleo A/O O A A O Nanoemulsão: - Goticulas com diametro < 100 nm -Termodinamicamente instável - transparente Miniemulsão: - fase dispersa, fase contínua,emulsificante,
Forças de van der Waals e Estabilidade Coloidal
 Pós-Graduação em Ciência de Materiais Faculdade UnB - Planaltina Forças de van der Waals e Estabilidade Coloidal Prof. Alex Fabiano C. Campos, Dr Balanço de Interações em Colóides Convencionais Balanço
Pós-Graduação em Ciência de Materiais Faculdade UnB - Planaltina Forças de van der Waals e Estabilidade Coloidal Prof. Alex Fabiano C. Campos, Dr Balanço de Interações em Colóides Convencionais Balanço
Nanopartículas de Prata e. Curva de Calibração da Curcumina
 RELATÓRIODEAULAPRÁTICA Disciplina:NanotecnologiaFarmacêutica NanopartículasdePratae CurvadeCalibraçãodaCurcumina Grupo 4 Erick Nunes Garcia Fernanda Buzatto Gabriela do Amaral Gleicy Romão Manuela Pereira
RELATÓRIODEAULAPRÁTICA Disciplina:NanotecnologiaFarmacêutica NanopartículasdePratae CurvadeCalibraçãodaCurcumina Grupo 4 Erick Nunes Garcia Fernanda Buzatto Gabriela do Amaral Gleicy Romão Manuela Pereira
FLOCULAÇÃO E DISPERSÃO DAS ARGILAS
 1 FLOCULAÇÃO E DISPERSÃO DAS ARGILAS PROF. GILSON MOURA FILHO/SER/UFAL CURSO DE PÓSGRADUAÇÃO EM AGRONOMIA DISCIPLINA: FÍSICA DO SOLO 1. FORÇAS E ENERGIA NO SISTEMA SOLOÁGUA Forças de coesão e adesão Forças
1 FLOCULAÇÃO E DISPERSÃO DAS ARGILAS PROF. GILSON MOURA FILHO/SER/UFAL CURSO DE PÓSGRADUAÇÃO EM AGRONOMIA DISCIPLINA: FÍSICA DO SOLO 1. FORÇAS E ENERGIA NO SISTEMA SOLOÁGUA Forças de coesão e adesão Forças
Avaliação para Seleção de Mestrado em Agroquímica I. Número ou código do(a) candidato(a): INSTRUÇÕES
 Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2012-I Número ou código do(a) candidato(a): INSTRUÇÕES
Universidade Federal de Viçosa Departamento de Química Programa de Pós-Graduação em Agroquímica Avaliação para Seleção de Mestrado em Agroquímica - 2012-I Número ou código do(a) candidato(a): INSTRUÇÕES
2º ano do Ensino Médio Profª Luiza Martins
 2º ano do Ensino Médio Profª Luiza Martins Dispersão coloidal Ganache: é uma emulsão estável de gordura em água. A gordura vêm do creme de leite e do chocolate e a água do creme de leite. Bolo: A massa
2º ano do Ensino Médio Profª Luiza Martins Dispersão coloidal Ganache: é uma emulsão estável de gordura em água. A gordura vêm do creme de leite e do chocolate e a água do creme de leite. Bolo: A massa
Modelagem Computacional de Sistemas Coloidais
 Universidade Federal do Rio de Janeiro Programa de Engenharia Química / COPPE Modelagem Computacional de Sistemas Coloidais Eduardo Rocha de Almeida Lima Evaristo Chalbaud Biscaia Jr. Frederico Wanderley
Universidade Federal do Rio de Janeiro Programa de Engenharia Química / COPPE Modelagem Computacional de Sistemas Coloidais Eduardo Rocha de Almeida Lima Evaristo Chalbaud Biscaia Jr. Frederico Wanderley
INSTABILIDADE DAS DISPERSÕES COLOIDAIS
 Recapitulando: COLÓIDES (partículas com dimensões entre nm e μm) DISPERSÃO COLOIDL: Sistema heterogéneo de partículas coloidais (colóides) dispersas numa fase contínua INSTBILIDDE DS DISPERSÕES COLOIDIS
Recapitulando: COLÓIDES (partículas com dimensões entre nm e μm) DISPERSÃO COLOIDL: Sistema heterogéneo de partículas coloidais (colóides) dispersas numa fase contínua INSTBILIDDE DS DISPERSÕES COLOIDIS
NANOPARTICULAS DE GOMA DO CAJUEIRO MODIFICADA E QUITOSANA POR COMPLEXAÇÃO POLIELETROLÍTICA
 NANOPARTICULAS DE GOMA DO CAJUEIRO MODIFICADA E QUITOSANA POR COMPLEXAÇÃO POLIELETROLÍTICA Durcilene A. Silva 1, Marília de A. Oliveira 1, Jeanny S. Maciel 1, Haroldo C. B Paula 2, Regina C. M. de Paula
NANOPARTICULAS DE GOMA DO CAJUEIRO MODIFICADA E QUITOSANA POR COMPLEXAÇÃO POLIELETROLÍTICA Durcilene A. Silva 1, Marília de A. Oliveira 1, Jeanny S. Maciel 1, Haroldo C. B Paula 2, Regina C. M. de Paula
Sistemas Dispersos RESUMO TEÓRICO E EXERCÍCIOS. 4º ano 1º Semestre 2016/2017
 Sistemas Dispersos RESUMO TEÓRICO E EXERCÍCIOS TECNOLOGIA FARMACÊUTICA II GRUPO 1 JOANA LUZ, JOANA LOPES, SARA MAGALHÃES E SORAIA SANTOS 4º ano 1º Semestre 2016/2017 Sistemas coloidais Potencial Zeta Teoria
Sistemas Dispersos RESUMO TEÓRICO E EXERCÍCIOS TECNOLOGIA FARMACÊUTICA II GRUPO 1 JOANA LUZ, JOANA LOPES, SARA MAGALHÃES E SORAIA SANTOS 4º ano 1º Semestre 2016/2017 Sistemas coloidais Potencial Zeta Teoria
Relatório de Nanotecnologia Farmacêutica Nanopartículas de prata/curva de calibração da Cúrcuma
 Relatório de Nanotecnologia Farmacêutica Nanopartículas de prata/curva de calibração da Cúrcuma Camila Fiori Pereira NºUSP: 8526835 Gabriel Lencioni Lovate NºUSP: 8526303 Marina Severiano Soares NºUSP:
Relatório de Nanotecnologia Farmacêutica Nanopartículas de prata/curva de calibração da Cúrcuma Camila Fiori Pereira NºUSP: 8526835 Gabriel Lencioni Lovate NºUSP: 8526303 Marina Severiano Soares NºUSP:
PROPRIEDADES INTERFACIAIS DE COMPLEXOS ELETROSTÁTICOS DE LECITINA E QUITOSANA
 PROPRIEDADES INTERFACIAIS DE COMPLEXOS ELETROSTÁTICOS DE LECITINA E QUITOSANA A.M.N. Toledo 1, C.G. Rodrigues 1, C.S.F. Picone 2, A.C.K. Sato 1 1 Departamento de Engenharia de Alimentos Universidade Estadual
PROPRIEDADES INTERFACIAIS DE COMPLEXOS ELETROSTÁTICOS DE LECITINA E QUITOSANA A.M.N. Toledo 1, C.G. Rodrigues 1, C.S.F. Picone 2, A.C.K. Sato 1 1 Departamento de Engenharia de Alimentos Universidade Estadual
INFLUÊNCIA DA CONCENTRAÇÃO DE CITRATO DE SÓDIO NA FORMAÇÃO DE NANOPARTÍCULAS DE PRATA.
 INFLUÊNCIA DA CONCENTRAÇÃO DE CITRATO DE SÓDIO NA FORMAÇÃO DE NANOPARTÍCULAS DE PRATA. Resumo Guilherme Mosquim Lemes 1, Maiara Lima Castilho, Leandro Raniero. Laboratório de Nanossensores - Universidade
INFLUÊNCIA DA CONCENTRAÇÃO DE CITRATO DE SÓDIO NA FORMAÇÃO DE NANOPARTÍCULAS DE PRATA. Resumo Guilherme Mosquim Lemes 1, Maiara Lima Castilho, Leandro Raniero. Laboratório de Nanossensores - Universidade
TERNÁRIO EHL DE UM ÓLEO
 AULA PRÁTICA I DIAGRAMA TERNÁRIO DETERMINAÇÃO LABORATORIAL DO EHL DE UM ÓLEO Grupos: vários SUMÁRIO 2 Definição de emulsão; Classificação dos emulgentes e Escala EHL; Teoria das emulsões; Instabilidade
AULA PRÁTICA I DIAGRAMA TERNÁRIO DETERMINAÇÃO LABORATORIAL DO EHL DE UM ÓLEO Grupos: vários SUMÁRIO 2 Definição de emulsão; Classificação dos emulgentes e Escala EHL; Teoria das emulsões; Instabilidade
Conteúdo: ESTUDO DAS DISPERSÕES E SOLUÇÕES
 Atividade/Exercício: FIXAÇÃO DE ESTUDO DAS SOLUÇÕES Disciplina: QUÍMICA Educador: ENDERSON BASTANI 1ª Etapa 23/ 04 /2019 Ano/Série: 2º Educando(a): Turma: Conteúdo: ESTUDO DAS DISPERSÕES E SOLUÇÕES QUESTÃO
Atividade/Exercício: FIXAÇÃO DE ESTUDO DAS SOLUÇÕES Disciplina: QUÍMICA Educador: ENDERSON BASTANI 1ª Etapa 23/ 04 /2019 Ano/Série: 2º Educando(a): Turma: Conteúdo: ESTUDO DAS DISPERSÕES E SOLUÇÕES QUESTÃO
AS SOLUÇÕES. Soluções, colóides e suspensões. disperso), se distribui de maneira uniforme ao longo
 AS SOLUÇÕES Solução é um tipo mistura chamada de dispersão na qual uma substância, sob forma de pequenas partículas ( disperso), se distribui de maneira uniforme ao longo de toda a extensão de uma outra
AS SOLUÇÕES Solução é um tipo mistura chamada de dispersão na qual uma substância, sob forma de pequenas partículas ( disperso), se distribui de maneira uniforme ao longo de toda a extensão de uma outra
Professor: Fábio Silva SOLUÇÕES
 Professor: Fábio Silva SOLUÇÕES Solvente: Substância que apresenta o mesmo estado de agregação da solução; Substância encontrada em maior quantidade. SOLUÇÃO É uma mistura homogênea de dois ou mais componentes.
Professor: Fábio Silva SOLUÇÕES Solvente: Substância que apresenta o mesmo estado de agregação da solução; Substância encontrada em maior quantidade. SOLUÇÃO É uma mistura homogênea de dois ou mais componentes.
COAGULAÇÃO TEORIA CLÁSSICA APLICADA À ÁGUA DE ABASTECIMENTO. Dione Mari Morita Departamento de Engenharia Hidráulica e Ambiental
 COAGULAÇÃO TEORIA CLÁSSICA APLICADA À ÁGUA DE ABASTECIMENTO Dione Mari Morita Departamento de Engenharia Hidráulica e Ambiental Carga dispersa Camada difusa Carga líquida negativa superficial Plano de
COAGULAÇÃO TEORIA CLÁSSICA APLICADA À ÁGUA DE ABASTECIMENTO Dione Mari Morita Departamento de Engenharia Hidráulica e Ambiental Carga dispersa Camada difusa Carga líquida negativa superficial Plano de
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
TANINO E DERIVADOS DE QUITOSANA: MACROMOLÉCULAS DE ORIGEM NATURAL COMO AGENTES DE ESTABILIZAÇÃO DE SUSPENSÕES DE ALUMINA
 TANIN E DERIVADS DE QUITSANA: MACRMLÉCULAS DE RIGEM NATURAL CM AGENTES DE ESTABILIZAÇÃ DE SUSPENSÕES DE ALUMINA Juliana C. Lamas, Bianca M. Cerrutti, Douglas de Britto, Sérgio P. Campana Filho, Elisabete
TANIN E DERIVADS DE QUITSANA: MACRMLÉCULAS DE RIGEM NATURAL CM AGENTES DE ESTABILIZAÇÃ DE SUSPENSÕES DE ALUMINA Juliana C. Lamas, Bianca M. Cerrutti, Douglas de Britto, Sérgio P. Campana Filho, Elisabete
Raquel Marchetti Sparemberger 2, Larissa Daiane Wilrich de Melo 2, Ana Paula Tasquetto da Silva 2 e Luis Otavio Sousa Bulhões 3 RESUMO
 Disciplinarum Scientia. Série: Ciências Naturais e Tecnológicas, Santa Maria, v. 14, n. 1, p. 123-130, 2013. Recebido em: 02.04.2013. Aprovado em: 28.08.2013. ISSN 2176-462X ANÁLISE FÍSICO-QUÍMICA DE NANOCÁPSULAS
Disciplinarum Scientia. Série: Ciências Naturais e Tecnológicas, Santa Maria, v. 14, n. 1, p. 123-130, 2013. Recebido em: 02.04.2013. Aprovado em: 28.08.2013. ISSN 2176-462X ANÁLISE FÍSICO-QUÍMICA DE NANOCÁPSULAS
5 MATERIAIS E MÉTODOS
 - 93-5 MATERIAIS E MÉTODOS 5.1. Preparação da emulsão sintética Para preparar um litro de emulsão sintética misturaram-se 3g de óleo lubrificante Shell Talpa 30 e água destilada, através de um misturador
- 93-5 MATERIAIS E MÉTODOS 5.1. Preparação da emulsão sintética Para preparar um litro de emulsão sintética misturaram-se 3g de óleo lubrificante Shell Talpa 30 e água destilada, através de um misturador
COVEST/UFPE ª ETAPA
 COVEST/UFPE 2000 2ª ETAPA. A partir das entalpias padrão das reações de oxidação do ferro dadas abaixo: determine a quantidade de calor liberada a 298K e 1 atm na reação:. Iguais volumes de amônia e cloreto
COVEST/UFPE 2000 2ª ETAPA. A partir das entalpias padrão das reações de oxidação do ferro dadas abaixo: determine a quantidade de calor liberada a 298K e 1 atm na reação:. Iguais volumes de amônia e cloreto
Parte 1. Diagrama de fases ternário
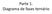 Parte 1. Diagrama de fases ternário Três componentes : água, citrato e poli(etileno glicol) 400 g/mol Observar passagem de sistema homogêneo para turvo cloud-point ou ponto de névoa em função da variação
Parte 1. Diagrama de fases ternário Três componentes : água, citrato e poli(etileno glicol) 400 g/mol Observar passagem de sistema homogêneo para turvo cloud-point ou ponto de névoa em função da variação
ESTUDO DO EFEITO DE NANOPARTÍCULAS MAGNÉTICAS BIOCOMPATÍVEIS NO FUNCIONAMENTO DE CORAÇÕES ISOLADOS DE RATOS
 ESTUDO DO EFEITO DE NANOPARTÍCULAS MAGNÉTICAS BIOCOMPATÍVEIS NO FUNCIONAMENTO DE CORAÇÕES ISOLADOS DE RATOS Laylla Silva RAMALHO, 1 Carlos Henrique de CASTRO, 2 Andris Figueiroa BAKUZIS, 1 1 Universidade
ESTUDO DO EFEITO DE NANOPARTÍCULAS MAGNÉTICAS BIOCOMPATÍVEIS NO FUNCIONAMENTO DE CORAÇÕES ISOLADOS DE RATOS Laylla Silva RAMALHO, 1 Carlos Henrique de CASTRO, 2 Andris Figueiroa BAKUZIS, 1 1 Universidade
EXTRAÇÃO POR SOLVENTES (QUIMICAMENTE ATIVA)
 INSTITUTO DE QUÍMICA ARARAQUARA QUÍMICA ORGÂNICA EXPERIMENTAL EXTRAÇÃO POR SOLVENTES (QUIMICAMENTE ATIVA) Prof. Dr. José Eduardo de Oliveira Prof. Dr. Leonardo Pezza Profª Juliana Rodrigues Grupo 6 Michelle
INSTITUTO DE QUÍMICA ARARAQUARA QUÍMICA ORGÂNICA EXPERIMENTAL EXTRAÇÃO POR SOLVENTES (QUIMICAMENTE ATIVA) Prof. Dr. José Eduardo de Oliveira Prof. Dr. Leonardo Pezza Profª Juliana Rodrigues Grupo 6 Michelle
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA
 PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
USO DE MEMBRANAS CERÂMICAS MICROPOROSAS NA PRODUÇÃO DE EMULSÕES ÓLEO DE GIRASSOL EM ÁGUA
 USO DE MEMBRANAS CERÂMICAS MICROPOROSAS NA PRODUÇÃO DE EMULSÕES ÓLEO DE GIRASSOL EM ÁGUA V. ZANATTA 1*, K. REZZADORI, F. M. PENHA 1, G. ZIN 1, J. C. C PETRUS 1, M. DI LUCCIO 1 1 Universidade Federal de
USO DE MEMBRANAS CERÂMICAS MICROPOROSAS NA PRODUÇÃO DE EMULSÕES ÓLEO DE GIRASSOL EM ÁGUA V. ZANATTA 1*, K. REZZADORI, F. M. PENHA 1, G. ZIN 1, J. C. C PETRUS 1, M. DI LUCCIO 1 1 Universidade Federal de
AULA 2 Adsorção: conceitos, classificações. Prof a Elenice Schons
 AULA 2 Adsorção: conceitos, classificações Prof a Elenice Schons ADSORÇÃO NA SUPERFÍCIE MINERAL Considera-se que uma determinada espécie química (iônica ou molecular), em solução, está adsorvida a uma
AULA 2 Adsorção: conceitos, classificações Prof a Elenice Schons ADSORÇÃO NA SUPERFÍCIE MINERAL Considera-se que uma determinada espécie química (iônica ou molecular), em solução, está adsorvida a uma
30/03/2017 Química Licenciatura Prof. Udo Eckard Sinks SOLUÇÕES E SOLUBILIDADE
 SOLUÇÕES E SOLUBILIDADE 1. Objetivos Aprender a preparar soluções usando balão volumétrico Reconhecer soluções diluídas, saturadas e supersaturadas Observar a termodinâmica do processo de dissolução 2.
SOLUÇÕES E SOLUBILIDADE 1. Objetivos Aprender a preparar soluções usando balão volumétrico Reconhecer soluções diluídas, saturadas e supersaturadas Observar a termodinâmica do processo de dissolução 2.
Variável (número da variável) Símbolo para variável (-) (+) Emulsão com Triton X-100 Oxigênio (1) a X 1 sem com Quantidade de amostra (2)
 95 5 Resultados e discussão: Comparação entre dois procedimentos de emulsificação para a determinação de Cr, Mo, V e Ti em óleo diesel e óleo combustível por ICP OES utilizando planejamento fatorial Neste
95 5 Resultados e discussão: Comparação entre dois procedimentos de emulsificação para a determinação de Cr, Mo, V e Ti em óleo diesel e óleo combustível por ICP OES utilizando planejamento fatorial Neste
6 RESULTADOS E DISCUSSÕES
 - 102-6 RESULTADOS E DISCUSSÕES A seguir, são apresentados os resultados e discussões obtidos nos ensaios de eletrocoagulação da emulsão óleo-água sintética. Os parâmetros iniciais de cada experimento
- 102-6 RESULTADOS E DISCUSSÕES A seguir, são apresentados os resultados e discussões obtidos nos ensaios de eletrocoagulação da emulsão óleo-água sintética. Os parâmetros iniciais de cada experimento
2 Teoria Geral sobre Eletroforese Capilar
 2 Teoria Geral sobre Eletroforese Capilar 2.1. Breve resumo sobre a técnica de eletroforese capilar A eletroforese é definida como o transporte, em solução eletrolítica, de compostos carregados eletricamente
2 Teoria Geral sobre Eletroforese Capilar 2.1. Breve resumo sobre a técnica de eletroforese capilar A eletroforese é definida como o transporte, em solução eletrolítica, de compostos carregados eletricamente
O 3. ou SnO 2. or SnO 2
 Influência das características ácido-básicas da superfície dos óxidos na estabilidade de suspensões cerâmicas d ou SnO 2 com dispersantes comerciais (Influence of acid-basic characteristic of Al 2 or SnO
Influência das características ácido-básicas da superfície dos óxidos na estabilidade de suspensões cerâmicas d ou SnO 2 com dispersantes comerciais (Influence of acid-basic characteristic of Al 2 or SnO
SOLUÇÕES PARTE 1. Giseli Menegat e Maira Gazzi Manfro
 SOLUÇÕES PARTE 1 Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br * dispersão É o sistema um sistema em que uma substância, sob a forma de pequenas
SOLUÇÕES PARTE 1 Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br * dispersão É o sistema um sistema em que uma substância, sob a forma de pequenas
AVALIAÇÃO DO PROCESSO DE OBTENÇÃO DE MICRO- ESFERAS DE PARAFINA ATRAVÉS DE METODOLOGIA DE SUPERFÍCIE DE RESPOSTA (MSR)
 AVALIAÇÃO DO PROCESSO DE OBTENÇÃO DE MICRO- ESFERAS DE PARAFINA ATRAVÉS DE METODOLOGIA DE SUPERFÍCIE DE RESPOSTA (MSR) H. R. TESTAI 1, K. L. RESENDE 1, T. J. LOPES 2, G. A. FERNANDES 1 1 Universidade Federal
AVALIAÇÃO DO PROCESSO DE OBTENÇÃO DE MICRO- ESFERAS DE PARAFINA ATRAVÉS DE METODOLOGIA DE SUPERFÍCIE DE RESPOSTA (MSR) H. R. TESTAI 1, K. L. RESENDE 1, T. J. LOPES 2, G. A. FERNANDES 1 1 Universidade Federal
Correlações Eletrostáticas e de Tamanho em Sistemas Coloidais
 Correlações Eletrostáticas e de Tamanho em Sistemas Coloidais VI Mostra da Pós-Graduação do Instituto de Física da UFRGS Alexandre Derivi 1 e Marcia Barbosa 2 1 agderivi@if.ufrgs.br 2 marcia.barbosa@ufrgs.br
Correlações Eletrostáticas e de Tamanho em Sistemas Coloidais VI Mostra da Pós-Graduação do Instituto de Física da UFRGS Alexandre Derivi 1 e Marcia Barbosa 2 1 agderivi@if.ufrgs.br 2 marcia.barbosa@ufrgs.br
NANOPACKSAFER: NANO-engineered PACKaging systems for improving quality, SAFEty and health characteristics of foods
 NANOPACKSAFER: NANO-engineered PACKaging systems for improving quality, SAFEty and health characteristics of foods Ana Cristina Pinheiro Departamento de Engenharia Biológica Universidade do Minho Objectivos
NANOPACKSAFER: NANO-engineered PACKaging systems for improving quality, SAFEty and health characteristics of foods Ana Cristina Pinheiro Departamento de Engenharia Biológica Universidade do Minho Objectivos
EXAME DE CAPACIDADE PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA
 EXAME DE CAPACIDADE PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PRIMEIRO SEMESTRE, 2015 NOME COMPLETO INSTRUÇÕES Escreva seu nome de forma legível no espaço acima. É expressamente proibido assinar ou fazer qualquer
EXAME DE CAPACIDADE PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PRIMEIRO SEMESTRE, 2015 NOME COMPLETO INSTRUÇÕES Escreva seu nome de forma legível no espaço acima. É expressamente proibido assinar ou fazer qualquer
Condutividade Elétrica
 FQE1 Exp. 1 Condutividade Elétrica 1. Introdução A condução elétrica é um fenômeno de transporte em que a carga elétrica (elétrons ou íons) se move através do sistema. A condutividade elétrica, também
FQE1 Exp. 1 Condutividade Elétrica 1. Introdução A condução elétrica é um fenômeno de transporte em que a carga elétrica (elétrons ou íons) se move através do sistema. A condutividade elétrica, também
PRODUÇÃO E CARACTERIZAÇÃO DE NANOPARTÍCULAS DE ÁCIDOS HÚMICOS POR NANOPRECIPITAÇÃO
 PRODUÇÃO E CARACTERIZAÇÃO DE NANOPARTÍCULAS DE ÁCIDOS HÚMICOS POR NANOPRECIPITAÇÃO B. A. G. MELO 1, F. L. MOTTA 1, M. H. A. SANTANA 1 1 Universidade Estadual de Campinas, Departamento de Engenharia de
PRODUÇÃO E CARACTERIZAÇÃO DE NANOPARTÍCULAS DE ÁCIDOS HÚMICOS POR NANOPRECIPITAÇÃO B. A. G. MELO 1, F. L. MOTTA 1, M. H. A. SANTANA 1 1 Universidade Estadual de Campinas, Departamento de Engenharia de
QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim
 QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim (mcoutrim@iceb.ufop.br) DISSOCIAÇÃO ÁCIDO/BASE Constante de dissociação de ácido: K a O ácido nitroso (HNO 2 ) é um ácido fraco, então Enquanto
QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim (mcoutrim@iceb.ufop.br) DISSOCIAÇÃO ÁCIDO/BASE Constante de dissociação de ácido: K a O ácido nitroso (HNO 2 ) é um ácido fraco, então Enquanto
E-book. Emulsões e Géis. com Lucas Portilho
 E-book Emulsões e Géis com Lucas Portilho Emulsões As emulsões são dispersões estabelecidas por uma fase dividida determinada como interna, dispersa ou descontinua, e por outra fase que cerca as gotículas,
E-book Emulsões e Géis com Lucas Portilho Emulsões As emulsões são dispersões estabelecidas por uma fase dividida determinada como interna, dispersa ou descontinua, e por outra fase que cerca as gotículas,
Processo de Seleção e Admissão aos Cursos de Mestrado e de Doutorado para o Semestre Edital n 001/PPGQMC/2015
 Processo de Seleção e Admissão aos Cursos de Mestrado e de Doutorado para o Semestre 2015-2 Edital n 001/PPGQMC/2015 EXAME DE SELEÇÃO PARA O MESTRADO Primeira Etapa: Provas de Química Analítica e de Físico-Química
Processo de Seleção e Admissão aos Cursos de Mestrado e de Doutorado para o Semestre 2015-2 Edital n 001/PPGQMC/2015 EXAME DE SELEÇÃO PARA O MESTRADO Primeira Etapa: Provas de Química Analítica e de Físico-Química
QFL Instruções para elaboração dos relatórios 2013
 GERAL QFL 2453 - Instruções para elaboração dos relatórios 2013 Todos os relatórios devem apresentar: 1) Capa contendo os nomes dos alunos, número USP, a turma da qual fazem parte, título e número da experiência,
GERAL QFL 2453 - Instruções para elaboração dos relatórios 2013 Todos os relatórios devem apresentar: 1) Capa contendo os nomes dos alunos, número USP, a turma da qual fazem parte, título e número da experiência,
Introdução à Bioquímica
 Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
OBTENÇÃO DE ESPUMAS ESTÁVEIS A PARTIR DE FORMULAÇÕES CONTENDO SURFACTANTES E NANOPARTÍCULAS INORGÂNICAS
 OBTENÇÃO DE ESPUMAS ESTÁVEIS A PARTIR DE FORMULAÇÕES CONTENDO SURFACTANTES E NANOPARTÍCULAS INORGÂNICAS Aluna: Beatriz Ribeiro Souza de Azevedo Orientadora: Aurora Pérez Gramatges Introdução As espumas
OBTENÇÃO DE ESPUMAS ESTÁVEIS A PARTIR DE FORMULAÇÕES CONTENDO SURFACTANTES E NANOPARTÍCULAS INORGÂNICAS Aluna: Beatriz Ribeiro Souza de Azevedo Orientadora: Aurora Pérez Gramatges Introdução As espumas
Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel
 Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Operações Unitárias: Sedimentação. Profª. Camila Ortiz Martinez UTFPR Campo Mourão
 Operações Unitárias: Sedimentação Profª. Camila Ortiz Martinez UTFPR Campo Mourão INTRODUÇÃO A operação unitária de separar pode envolver: separação de alimentos sólidos em sólido: peneiramento separação
Operações Unitárias: Sedimentação Profª. Camila Ortiz Martinez UTFPR Campo Mourão INTRODUÇÃO A operação unitária de separar pode envolver: separação de alimentos sólidos em sólido: peneiramento separação
CARACTERIZAÇÃO E ESTUDO DO POTENCIAL ZETA DE HEMATITAS ORIGINÁRIAS DO Quadrilátero FERRÍFERO E CARAJÁS
 CARACTERIZAÇÃO E ESTUDO DO POTENCIAL ZETA DE HEMATITAS ORIGINÁRIAS DO Quadrilátero FERRÍFERO E CARAJÁS A.B.Henriques 1, P.M.T. de Azevedo 1, G.R. da Silva 2, A.E.C. Peres 1 1 Departamento de Engenharia
CARACTERIZAÇÃO E ESTUDO DO POTENCIAL ZETA DE HEMATITAS ORIGINÁRIAS DO Quadrilátero FERRÍFERO E CARAJÁS A.B.Henriques 1, P.M.T. de Azevedo 1, G.R. da Silva 2, A.E.C. Peres 1 1 Departamento de Engenharia
EXTRAÇÃO, SEPARAÇÃO E PURIFICAÇÃO ENZIMÁTICA
 EXTRAÇÃO, SEPARAÇÃO E PURIFICAÇÃO ENZIMÁTICA EQB4383 _ Enzimologia Industrial Etapas de Extração, Separação e Purificação Enzimáticas remoção de material insolúvel separação dos produtos purificação e
EXTRAÇÃO, SEPARAÇÃO E PURIFICAÇÃO ENZIMÁTICA EQB4383 _ Enzimologia Industrial Etapas de Extração, Separação e Purificação Enzimáticas remoção de material insolúvel separação dos produtos purificação e
Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância.
 Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura, a sacarose (disperso)
Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura, a sacarose (disperso)
Pelas razões expostas e tendo em vista que a estruturação e posterior desestruturação do CAP é reversível, fica difícil aceitar o modelo atual.
 8 CONDUÇÃO A UM NOVO MODELO Depois das análises sobre o comportamento energético do CAP de forma genérica e de ter dado destaque a alguns pontos da teoria dos colóides que interessam diretamente ao CAP,
8 CONDUÇÃO A UM NOVO MODELO Depois das análises sobre o comportamento energético do CAP de forma genérica e de ter dado destaque a alguns pontos da teoria dos colóides que interessam diretamente ao CAP,
FENÓMENOS DE TRANSPORTE. Física Aplicada 2017/19 MICF FFUP
 FENÓMENOS DE TRANSPORTE ELETROFORESE ELETROFORESE:GENERALIDADES Movimento de partículas num campo elétrico externo Técnica usada para separar e às vezes purificar macromoléculas que diferem na carga, conformação
FENÓMENOS DE TRANSPORTE ELETROFORESE ELETROFORESE:GENERALIDADES Movimento de partículas num campo elétrico externo Técnica usada para separar e às vezes purificar macromoléculas que diferem na carga, conformação
Avaliação da casca de banana como potencial biossorvente natural na remoção de cobre da água (1).
 Avaliação da casca de banana como potencial biossorvente natural na remoção de cobre da água (1). Janaína Beatriz Toniello Vieira (2) ; Bruna Felipe da Silva (2). (1) Trabalho executado com recursos disponibilizados
Avaliação da casca de banana como potencial biossorvente natural na remoção de cobre da água (1). Janaína Beatriz Toniello Vieira (2) ; Bruna Felipe da Silva (2). (1) Trabalho executado com recursos disponibilizados
Experiência 1: Identificação de Amostras Sólidas por densidade 59
 Sumário Prefácio da 2 a Edição 17 Prefácio da 1 a edição 21 Capítulo 1: EQUIPAMENTOS BÁSICOS DE LABORATÓRIO 25 Capítulo 2: SEGURANÇA EM LABORATÓRIO 39 COMO MANTER UM AMBIENTE DE LABORATÓRIO SAUDÁVEL? 39
Sumário Prefácio da 2 a Edição 17 Prefácio da 1 a edição 21 Capítulo 1: EQUIPAMENTOS BÁSICOS DE LABORATÓRIO 25 Capítulo 2: SEGURANÇA EM LABORATÓRIO 39 COMO MANTER UM AMBIENTE DE LABORATÓRIO SAUDÁVEL? 39
Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio.
 ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
Físico-Química I. Profa. Dra. Carla Dalmolin. Misturas Simples. Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras
 Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Misturas Simples Misturas de substâncias que não reagem Modelo simples para
Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Misturas Simples Misturas de substâncias que não reagem Modelo simples para
Universidade de São Paulo. Relatório Prática 3 Nanopartículas de Prata e Curva de Calibração da Curcumina
 Universidade de São Paulo Faculdade de Ciências Farmacêuticas de Ribeirão Preto Relatório Prática 3 Nanopartículas de Prata e Curva de Calibração da Curcumina Eloísa Torró Estela Chiappetta Julia Pupim
Universidade de São Paulo Faculdade de Ciências Farmacêuticas de Ribeirão Preto Relatório Prática 3 Nanopartículas de Prata e Curva de Calibração da Curcumina Eloísa Torró Estela Chiappetta Julia Pupim
4. MATERIAIS E MÉTODOS
 58 4. MATERIAIS E MÉTODOS Neste capitulo são apresentados, os materiais, reagentes e equipamentos utilizados no estudo do processo de biossorção/flotação para a remoção de metais como, Mercúrio usando
58 4. MATERIAIS E MÉTODOS Neste capitulo são apresentados, os materiais, reagentes e equipamentos utilizados no estudo do processo de biossorção/flotação para a remoção de metais como, Mercúrio usando
Dois exercícios desta lista entrarão na primeira prova teórica
 Dois exercícios desta lista entrarão na primeira prova teórica 01. Quais são os três estados físicos da matéria? Quais as diferenças entre eles do ponto de vista de movimentação de moléculas e interações
Dois exercícios desta lista entrarão na primeira prova teórica 01. Quais são os três estados físicos da matéria? Quais as diferenças entre eles do ponto de vista de movimentação de moléculas e interações
Bacharelado em Engenharia de Pesca, Campus Ministro Reis Velloso.
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DO PIAUÍ PRÓ-REITORIA DE PESQUISA- PROPESQ COORDENAÇÃO DE INOVAÇÃO TECNOLÓGICA CITEC Programa Institucional de Bolsa em Desenvolvimento Tecnológico e Inovação
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DO PIAUÍ PRÓ-REITORIA DE PESQUISA- PROPESQ COORDENAÇÃO DE INOVAÇÃO TECNOLÓGICA CITEC Programa Institucional de Bolsa em Desenvolvimento Tecnológico e Inovação
QUÍMICA Tipos de soluções Edson Mesquita
 QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
Soluções, concentrações e diluições
 Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
Métodos de Determinação da Massa Molar. Fábio Herbst Florenzano
 Métodos de Determinação da Massa Molar Fábio Herbst Florenzano Importância da Massa Molar Média A maioria das propriedades mecânicas, termomecânicas, reológicas e outras dependem da massa molar média.
Métodos de Determinação da Massa Molar Fábio Herbst Florenzano Importância da Massa Molar Média A maioria das propriedades mecânicas, termomecânicas, reológicas e outras dependem da massa molar média.
SISTEMAS DISPERSOS SOLUÇÕES COLÓIDES SUSPENSÕES
 SISTEMAS DISPERSOS SOLUÇÕES COLÓIDES SUSPENSÕES SOLUÇÕES homogêneo COLÓIDES SUSPENSÕES heterogêneo Tamanho médio das partículas do disperso Homogeneidade do sistema Sedimentação das partículas Filtração
SISTEMAS DISPERSOS SOLUÇÕES COLÓIDES SUSPENSÕES SOLUÇÕES homogêneo COLÓIDES SUSPENSÕES heterogêneo Tamanho médio das partículas do disperso Homogeneidade do sistema Sedimentação das partículas Filtração
Cinética da Polimerização radicalar
 Cinética da Polimerização radicalar A polimerização por adição é uma reacção em cadeia que consiste numa sequência de 3 passos: iniciação, propagação e terminação Iniciação: Considera-se que envolve duas
Cinética da Polimerização radicalar A polimerização por adição é uma reacção em cadeia que consiste numa sequência de 3 passos: iniciação, propagação e terminação Iniciação: Considera-se que envolve duas
Exercícios sobre Solubilidade - conceitos e curvas
 Exercícios sobre Solubilidade - conceitos e curvas 01. (Ufrrj) Ao analisar o gráfico acima, percebe-se que a) a solubilidade do KCl é maior que a do KBr. b) à medida que a temperatura aumenta a solubilidade
Exercícios sobre Solubilidade - conceitos e curvas 01. (Ufrrj) Ao analisar o gráfico acima, percebe-se que a) a solubilidade do KCl é maior que a do KBr. b) à medida que a temperatura aumenta a solubilidade
DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL
 DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL Principais componentes do óleo de cravo obtidos pelo arraste DESTILAÇÃO FRACIONADA DE UMA SOLUÇÃO evaporações
DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL Principais componentes do óleo de cravo obtidos pelo arraste DESTILAÇÃO FRACIONADA DE UMA SOLUÇÃO evaporações
Titulação de precipitação
 Titulação de precipitação Volumetria de precipitação é baseada em reações que geram compostos de baixa solubilidade. Velocidade de formação de muitos precipitados limita o uso de reagentes que podem ser
Titulação de precipitação Volumetria de precipitação é baseada em reações que geram compostos de baixa solubilidade. Velocidade de formação de muitos precipitados limita o uso de reagentes que podem ser
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
Água e óleo. Solução de CuSO 4. Qual dos sistemas é uma dispersão? Por que?
 Solução de CuSO 4 Água e óleo Por que? Qual dos sistemas é uma dispersão? Solução de CuSO 4 Disperso Dispersante Sistema Distribuição uniforme de partículas Dispersão Os constituintes de uma substância
Solução de CuSO 4 Água e óleo Por que? Qual dos sistemas é uma dispersão? Solução de CuSO 4 Disperso Dispersante Sistema Distribuição uniforme de partículas Dispersão Os constituintes de uma substância
CQ049 FQ Eletroquímica. prof. Dr. Marcio Vidotti Terça / Quarta: 15:30 17:30
 CQ049 FQ Eletroquímica prof. Dr. Marcio Vidotti mvidotti@ufpr.br www.quimica.ufpr.br/mvidotti Terça / Quarta: 15:30 17:30 Espontaneidade de reações eletroquímicas redução A + e - A - oxidação A A + + e
CQ049 FQ Eletroquímica prof. Dr. Marcio Vidotti mvidotti@ufpr.br www.quimica.ufpr.br/mvidotti Terça / Quarta: 15:30 17:30 Espontaneidade de reações eletroquímicas redução A + e - A - oxidação A A + + e
DETERMINAÇÃO DE ÁCIDOS ORGÂNICOS EM AMOSTRAS DE ÁGUA CONATA POR ELETROFORESE CAPILAR
 DETERMINAÇÃO DE ÁCIDOS ORGÂNICOS EM AMOSTRAS DE ÁGUA CONATA POR ELETROFORESE CAPILAR Aluna: Nathalie Costa Torres Barbosa Orientadora: Tatiana Dillenburg Saint Pierre Co-Orientadora: Roberta Amorim de
DETERMINAÇÃO DE ÁCIDOS ORGÂNICOS EM AMOSTRAS DE ÁGUA CONATA POR ELETROFORESE CAPILAR Aluna: Nathalie Costa Torres Barbosa Orientadora: Tatiana Dillenburg Saint Pierre Co-Orientadora: Roberta Amorim de
Classificação e distribuição dos sólidos em função do tamanho
 UNIVERSIDADE FEDERAL DE OURO PRETO DECIV DEPARTAMENTO DE ENGENHARIA CIVIL Tratamento de Água: Coagulação DISCIPLINA: SANEAMENTO PROF. CARLOS EDUARDO F MELLO e-mail: cefmello@gmail.com Sólidos Presentes
UNIVERSIDADE FEDERAL DE OURO PRETO DECIV DEPARTAMENTO DE ENGENHARIA CIVIL Tratamento de Água: Coagulação DISCIPLINA: SANEAMENTO PROF. CARLOS EDUARDO F MELLO e-mail: cefmello@gmail.com Sólidos Presentes
Fonte: Netz e Ortega, 2002.
 1 Atividade A atividade é uma espécie de concentração efetiva. Para entender o que é uma concentração efetiva, podemos raciocinar do seguinte modo: As interações entre as moléculas em uma mistura fazem
1 Atividade A atividade é uma espécie de concentração efetiva. Para entender o que é uma concentração efetiva, podemos raciocinar do seguinte modo: As interações entre as moléculas em uma mistura fazem
PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS
 CENTRO DE CIÊNCIAS E TECNOLOGIA DISCIPLINA BIOQUÍMICA Profas. Roziana Jordão e Alexandra Salgueiro PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS I Objetivos Caracterizar a presença de proteínas; Verificar experimentalmente
CENTRO DE CIÊNCIAS E TECNOLOGIA DISCIPLINA BIOQUÍMICA Profas. Roziana Jordão e Alexandra Salgueiro PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS I Objetivos Caracterizar a presença de proteínas; Verificar experimentalmente
EFEITO DA SUBSTITUIÇÃO DOS CÁTIONS DE COMPENSAÇÃO DA ZEÓLITA NATURAL CLINOPTILOLITA SOBRE O POTENCIAL ZETA E O RAIO HIDRODINÂMICO
 EFEITO DA SUBSTITUIÇÃO DOS CÁTIONS DE COMPENSAÇÃO DA ZEÓLITA NATURAL CLINOPTILOLITA SOBRE O POTENCIAL ZETA E O RAIO HIDRODINÂMICO Marcelo L. Pereira 1 (marcelosmv@gmail.com), José Daniel R. de Campos (UnUCET-
EFEITO DA SUBSTITUIÇÃO DOS CÁTIONS DE COMPENSAÇÃO DA ZEÓLITA NATURAL CLINOPTILOLITA SOBRE O POTENCIAL ZETA E O RAIO HIDRODINÂMICO Marcelo L. Pereira 1 (marcelosmv@gmail.com), José Daniel R. de Campos (UnUCET-
Universidade Paulista Instituto de Ciências Exatas e Tecnologia Departamento de Engenharia Civil Professora Moema Castro, MSc.
 Universidade Paulista Instituto de Ciências Exatas e Tecnologia Departamento de Engenharia Civil Professora Moema Castro, MSc. C O M P L E M E N T O S D E M E C Â N I C A D O S S O L O S E F U N D A Ç
Universidade Paulista Instituto de Ciências Exatas e Tecnologia Departamento de Engenharia Civil Professora Moema Castro, MSc. C O M P L E M E N T O S D E M E C Â N I C A D O S S O L O S E F U N D A Ç
Concentração de soluções e diluição
 Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
DETERMINAÇÃO DE FERRO TOTAL EM SUPLEMENTOS ALIMENTARES POR ESPECTROMETRIA DE ABSORÇÃO MOLECULAR
 59 DETERMINAÇÃO DE FERRO TOTAL EM SUPLEMENTOS ALIMENTARES POR ESPECTROMETRIA DE ABSORÇÃO MOLECULAR Wendhy Carolina VICENTE 1 Natália Maria Karmierczak da SILVA 2 Amarildo Otavio MARTINS 3 Elisangela Silva
59 DETERMINAÇÃO DE FERRO TOTAL EM SUPLEMENTOS ALIMENTARES POR ESPECTROMETRIA DE ABSORÇÃO MOLECULAR Wendhy Carolina VICENTE 1 Natália Maria Karmierczak da SILVA 2 Amarildo Otavio MARTINS 3 Elisangela Silva
Química de Polímeros. Prof a. Dr a. Carla Dalmolin Polímeros em Solução
 Química de Polímeros Prof a. Dr a. Carla Dalmolin carla.dalmolin@udesc.br Polímeros em Solução Polímeros em Solução Indústria de tintas / vernizes / adesivos Formulação e controle de qualidade Baixo custo
Química de Polímeros Prof a. Dr a. Carla Dalmolin carla.dalmolin@udesc.br Polímeros em Solução Polímeros em Solução Indústria de tintas / vernizes / adesivos Formulação e controle de qualidade Baixo custo
SOLUÇÕES. 1. Concentração (C) 2. Concentração molar (M) C = massa de soluto / volume da solução. M = mol de soluto / volume de solução
 SOLUÇÕES Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanômetro. A solução ainda pode ser caracterizada por formar um sistema homogêneo (a olho nu e
SOLUÇÕES Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanômetro. A solução ainda pode ser caracterizada por formar um sistema homogêneo (a olho nu e
Dispersão: disperso dispersante ou dispergente
 Dispersão: disperso dispersante ou dispergente Dispersão: Suspensão, Solução Coloidal e Solução Verdadeira (solução) Mistura Heterogênea: Suspensão e Solução Coloidal Mistura Homogênea: Solução Verdadeira
Dispersão: disperso dispersante ou dispergente Dispersão: Suspensão, Solução Coloidal e Solução Verdadeira (solução) Mistura Heterogênea: Suspensão e Solução Coloidal Mistura Homogênea: Solução Verdadeira
Química Orgânica Experimental I BAC CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS
 Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
ELETROQUÍMICA. Prof a. Dr a. Carla Dalmolin
 ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CINÉTICA E MECANISMOS DAS REAÇÕES ELETROQUÍMICAS Eletrodo Transferência de Elétrons O + e R 5. Transferência de elétrons k c O 1. Difusão k d,o k a O Para uma
ELETROQUÍMICA Prof a. Dr a. Carla Dalmolin CINÉTICA E MECANISMOS DAS REAÇÕES ELETROQUÍMICAS Eletrodo Transferência de Elétrons O + e R 5. Transferência de elétrons k c O 1. Difusão k d,o k a O Para uma
) T, p. Processos Superficiais Tensão Superficial. Efeito de substâncias dissolvidas na tensão superficial de um solvente. RT ln (C 2 /C )) T, p
 - Lembrando da isoterma de Gibbs: para uma solução com dois componente Γ 2 = 1 RT ( γ ln a 2 ) T, p Considerando solução diluída ideal Γ 2 = 1 ( γ RT ln (C 2 /C )) T, p Γ 2 = C 2 RT ( γ C 2 ) T, p - de
- Lembrando da isoterma de Gibbs: para uma solução com dois componente Γ 2 = 1 RT ( γ ln a 2 ) T, p Considerando solução diluída ideal Γ 2 = 1 ( γ RT ln (C 2 /C )) T, p Γ 2 = C 2 RT ( γ C 2 ) T, p - de
Ácidos fracos. Ácidos fracos são apenas parcialmente ionizados em solução. Reagem com o solvente (H 2 O) doando um próton.
 Ácidos fracos Ácidos fracos são apenas parcialmente ionizados em solução. Reagem com o solvente (H 2 O) doando um próton. Existe uma mistura de íons e ácido não-ionizado em solução em quantidades significativas
Ácidos fracos Ácidos fracos são apenas parcialmente ionizados em solução. Reagem com o solvente (H 2 O) doando um próton. Existe uma mistura de íons e ácido não-ionizado em solução em quantidades significativas
Acidez e Basicidade de Compostos Orgânicos
 Acidez e Basicidade de Compostos Orgânicos 1. Teorias sobre ácidos e bases Teoria de Arrhenius (1884) Substâncias neutras dissolvidas em água formam espécies carregadas ou íons através de dissociação iônica
Acidez e Basicidade de Compostos Orgânicos 1. Teorias sobre ácidos e bases Teoria de Arrhenius (1884) Substâncias neutras dissolvidas em água formam espécies carregadas ou íons através de dissociação iônica
Material de apoio. Granulometria do Solo. Granulometria do Solo
 Universidade Paulista Instituto de Ciências Exatas e Tecnologia Departamento de Engenharia Civil Professora Moema Castro, MSc. Material de apoio 2 PINTO, C. de S. CursoBásicodeMecânicados Solos, Editora
Universidade Paulista Instituto de Ciências Exatas e Tecnologia Departamento de Engenharia Civil Professora Moema Castro, MSc. Material de apoio 2 PINTO, C. de S. CursoBásicodeMecânicados Solos, Editora
