PROGRAMA JAVA PARA ESTIMATIVAS DE PROPRIEDADES TERMOFÍSICAS POR CONTRIBUIÇÃO DE GRUPOS FUNCIONAIS
|
|
|
- Daniel Palha Clementino
- 7 Há anos
- Visualizações:
Transcrição
1 PROGRAMA JAVA PARA ESTIMATIVAS DE PROPRIEDADES TERMOFÍSICAS POR CONTRIBUIÇÃO DE GRUPOS FUNCIONAIS L. G. Oliveira, J. C. Rocha, S. P. Nascimento, J. A. Cavalcante, N. A. Costa Universidade Federal da Paraíba, Departamento de Engenharia Química para contato: RESUMO O presente trabalho tem por obetivo apresentar um programa JAVA para estimativas de propriedades termoísicas (propriedades críticas, temperatura normal de ebulição, temperatura de usão, capacidade caloríica a pressão constante, entalpia de ormação e energia livre de Gibbs de ormação) usando grupos uncionais. O proeto do programa oi dividido em quatro partes: a) banco de dados contendo os parâmetros do modelo de contribuição de grupos uncionais, b) criação de caixas de diálogos para interação do usuário com o programa, c) codiicações de subprogramas JAVA para as estimativas das propriedades termoísicas e d) validação dos resultados ornecidos pelo programa. O resultado inal é um aplicativo, para ins educacionais e/ou comerciais, capaz de ornecer estimativas das propriedades termoísicas das espécies por contribuição de grupos uncionais com rapidez e coniabilidade. 1. INTRODUÇÃO Os cálculos dos processos químicos, análises e proetos requerem propriedades características de uma substância pura, tais como: propriedades críticas; temperatura normal de ebulição; temperatura de usão e propriedades de gases ideais (capacidade caloríica e propriedades de ormação). Em vários casos, estes dados não são disponíveis, tornando-se necessárias predições dessas propriedades. Nos métodos de contribuições de grupos uncionais, as propriedades de uma substância são consideradas como sendo a soma das contribuições individuais de cada grupo estrutural, tais como: -CH 3, >CH 2, - OH e outros que, quando adicionados, ormam a molécula. Atualmente várias propriedades são preditas através dos métodos de contribuição de grupos uncionais: coeiciente de atividade; propriedades críticas; pressão de vapor; entalpia de vaporização; propriedades dos gases ideais; viscosidade e tensão supericial. JAVA é uma linguagem de programação orientada a obetos, de alto nível que permite o rápido desenvolvimento de aplicações com interace gráica. Sua escolha se deve à disponibilidade para as principais plataormas do mercado (Windows, Mac OS X, Linux) e acilidade de desenvolvimento. Após a compilação de um aplicativo JAVA é gerado um executável que pode ser executado em qualquer plataorma com suporte a linguagem JAVA e seus toolkits. Essa característica é possível pelo ato de que a aplicação JAVA é executada sobre uma máquina virtual, a JVM (Java Virtual Machine).
2 1.1. Contribuição de Grupos Reid et al. (1987), Poling et al. (2001) e Tester e Modell (1997) descrevem as equações e os parâmetros desenvolvidos por Joback e modiicados por Lyndersen para a contribuição dos grupos uncionais que predizem propriedades termoísicas descritas abaixo. Temperatura crítica: T T 0,584 0,965 é a temperatura normal de ebulição. c b T T Pressão crítica: P 0,113 0, 0032n de átomos da molécula. Volume crítico: V 17,5 v c A P c V 2 1, onde T c em K e T b 2, onde V c em cm³/mol; Temperatura normal de ebulição: T 178 v Temperatura de usão: T 122 v T b Tb, onde T em Kelvin;, onde P c em bar e n A é o número, onde T b em Kelvin kj/mol Energia livre de Gibbs de ormação: G 53,88 v G, onde em G Entalpia de ormação: H 68, 29 n H, onde em kj/mol; H Capacidade caloríica a pressão constante: CP A BT CT DT, onde C P em J/mol.K. Os coeicientes da Equação (8) são obtidos por contribuição de grupos uncionais através das seguintes relações: Coeicientes: A v a 37,93; B v b 0, 210 ; D n 2,06x10 d 7 4 c 3,91 10 e C n x, onde é a quantidade de grupos uncionais na molécula. As constantes características dos grupos uncionais T, P, V, Tb, T, G, H, a, b, c e d são ornecidas por Reid et al. (1987) e Poling et al. (2001). 2. METODOLOGIA
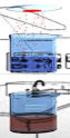
3 A metodologia adotada para o desenvolvimento dos subprogramas JAVA é esquematizada na Figura 1. Figura 1 Contribuição de Grupos Funcionais Temperatura crítica Pressão crítica Volume crítico crítico Contribuição de Grupos Funcionais Temperatura normal de ebulição Temperatura de usão Entalpia de ormação Energia livre de Gibbs de ormação Constantes da capacidade caloríica 2.1. Esquema do desenvolvimento do aplicativo Na Figura 2 é mostrada a anela principal do aplicativo desenvolvido em Java. Figura 2 Janela principal do aplicativo Java
4 2.2 Descrições das opções da anela principal Opção dados permite o acesso ao banco de dados contendo as constantes de 40 grupos uncionais do método de Joback reportadas por Poling et al. (1987) (Figura 3). Opção Salvar: abre a caixa de diálogo mostrada na Figura 4 que permite ao usuário especiicar o local e o nome do arquivo de saída de dados. Figura 3 Banco de dados do aplicativo Figura 4 Salvar resultados
5 Opção Auda: descrição resumida do modelo de contribuição de grupos uncionais de Joback (Figura 5). Opção Sobre: inormações sobre os autores do aplicativo (Figura 6). Figura 5 Resumo do método de Joback Figura 6 Inormações sobre os autores Opção Sair: echa o aplicativo (Figura 2). Lista dos grupos uncionais: apresenta a lista de grupos uncionais do método de Joback (Figura 2). Caixa de texto: permite especiicar a quantidade de cada grupo escolhido (Figura 2). Opção adicionar: permite ao usuário adicionar os grupos uncionais para conigurar a órmula estrutura da espécie química (Figura 2). Opção inalizar cálculo: inaliza os cálculos (Figura 2). Opção limpar: limpa a saída de dados e remove os locais de memória especiicados pelo usuário (Figura 2). 3. VALIDAÇÃO DO APLICATIVO A validação do aplicativo Java desenvolvido para as predições das propriedades termoísicas por contribuição de grupos uncionais oi realizada através da comparação dos valores reportados na literatura mundial com os ornecidos pelo aplicativo desenvolvido. Os valores da literatura (em negrito) oram reportados por: Tester e Modell (1997) para o tolueno e diclorometano e Poling et al. (2001) para o 2-etilenol. Nas Tabelas 1, 2 e 3 são apresentadas, respectivamente, as propriedades críticas e a temperatura normal de ebulição, as propriedades termodinâmicas dos gases ideais e as constantes da capacidade caloríica a pressão constante de gases ideais.
6 Tabela 1 - Propriedades críticas Espécie T b (K) T c (K) P c (bar) V c (cm 3 /mol) Tolueno 386,24 597,7 41,1 319,5 386,24 597,75 41,14 319,5 Diclorometano 297,14 478,55 51,91 189,5 297,14 478,55 51, ,5 2-etilenol 489,74 715,7 44,09 341,5 489,74 715,75 44, ,5 Espécie Tabela 2 - Propriedades termodinâmicas do gás ideal no estado padrão de Literatura (kj/mol) G Aplicativo (kj/mol) H G H Tolueno 48,72 120,47 48,72 120,47 Diclorometano -95,45-66,32-95,45-66,32 2-etilenol -149,23-25,73-149,23-25,73 Tabela 3 - C P = A + BT + CT 2 +DT 3 Espécie A B Cx10 4 Dx10 8 Tolueno -37,38 0,5899-3,88 9,80-37,38 0, ,882 9,76 Diclorometano -62,23 0,1124-7,10 1,90 27,761 0,1124-7,14 1,87 2-etilenol -47,209 0, ,984 2,419-47,209 0, ,9896 2,426 Foram veriicadas as excelentes concordâncias entre os resultados ornecidos pelo aplicativo com os valores reportados na literatura. As pequenas dierenças observadas nos cálculos mostrados ao longo do trabalho são devido às dierenças entre as precisões numéricas utilizadas pelos pesquisadores e pelo aplicativo. Na Tabela 3 ocorreu uma discordância no coeiciente A do diclorometano. Tester e Modell (1997) reporta que o grupo (-CH2-) possui um valor a = -9,09x10-1, o que esta de acordo com REID et al. (1988) e POLING et al. (2001). Entretanto, no cálculo do coeiciente A, os pesquisadores utilizaram a = -9,09x CONCLUSÃO Este trabalho apresenta um aplicativo capaz de ornecer com coniabilidade e rapidez as estimativas de propriedades termoísicas usando a metodologia de contribuição de grupos uncionais. Deve ser observado que a coniabilidade da estimativa de uma determinada propriedade termoísica está associada à eiciência do modelo ornecido pelo pesquisador e não por erros numéricos ou erros de codiicações dos subprogramas VBA. 6. REFERÊNCIAS
7 POLING, B. E.;PRAUSNITZ, J. M.; O CONNELL, J. P. The properties o gases and liquids. McGraw-Hill, Fith Edition, 2001 REID, R. C., PRAUSNITZ, J. M., POLING, B. E. The properties o gases and liquids. McGraw-Hill, Fourth Edition, TESTER, J. W., MODELL, M. Thermodynamics and its Applications. Prentice Hall, 3rd Edition, 1997
L. G. Oliveira, S. P. Nascimento, T. D. Romão, J. A. Cavalcante, N. A. Costa
 APLICATIVO EXCEL/VBA PARA ESTIMATIVAS DE COEFICIENTES DE ATIVIDADES A DILUIÇÃO INFINITA ATRAVÉS DO MODELO MOSCED E VERIFICAÇÃO DE AZEOTROPIA DE MISTURAS BINÁRIAS L. G. Oliveira, S. P. Nascimento, T. D.
APLICATIVO EXCEL/VBA PARA ESTIMATIVAS DE COEFICIENTES DE ATIVIDADES A DILUIÇÃO INFINITA ATRAVÉS DO MODELO MOSCED E VERIFICAÇÃO DE AZEOTROPIA DE MISTURAS BINÁRIAS L. G. Oliveira, S. P. Nascimento, T. D.
Termodinâmica das Reações de Transesterificação e de Esterificação
 UNIVERSIDADE FEDERAL DE SÃO CARLOS Laboratório de Catálise Termodinâmica das Reações de Transesterificação e de Esterificação Mini-curso: Biodiesel Demian Patrick Fabiano Outubro - 2007 1 Sumário A) Catálise
UNIVERSIDADE FEDERAL DE SÃO CARLOS Laboratório de Catálise Termodinâmica das Reações de Transesterificação e de Esterificação Mini-curso: Biodiesel Demian Patrick Fabiano Outubro - 2007 1 Sumário A) Catálise
TERMODINÂMICA QUÍMICA APLICADA II
 Disciplina : LOQ 4088 Turma : Engenharia Bioquímica - Química (20191D1) Lorena, fevereiro 2019 1 EMENTA 1- Propriedades Termodinâmicas de Fluidos 1.1- Equilíbrio Termodinâmico 1.2- Critérios de equilíbrio
Disciplina : LOQ 4088 Turma : Engenharia Bioquímica - Química (20191D1) Lorena, fevereiro 2019 1 EMENTA 1- Propriedades Termodinâmicas de Fluidos 1.1- Equilíbrio Termodinâmico 1.2- Critérios de equilíbrio
I. Propriedades Termodinâmicas de Fluidos
 I. Propriedades Termodinâmicas de Fluidos 1 OBJETIVOS Identificar o critério para o equilíbrio em sistemas sujeitos a diferentes restrições Determinar a estabilidade dos sistemas termodinâmicos. Aplicações:
I. Propriedades Termodinâmicas de Fluidos 1 OBJETIVOS Identificar o critério para o equilíbrio em sistemas sujeitos a diferentes restrições Determinar a estabilidade dos sistemas termodinâmicos. Aplicações:
Métodos de implementação de linguagens. Kellen Pinagé
 Métodos de implementação de linguagens Kellen Pinagé Sumário Métodos de implementação de linguagens Compilação Interpretação pura Híbrido Métodos de implementação de linguagens Principais componentes de
Métodos de implementação de linguagens Kellen Pinagé Sumário Métodos de implementação de linguagens Compilação Interpretação pura Híbrido Métodos de implementação de linguagens Principais componentes de
Profª. Drª. Ana Cláudia Kasseboehmer Monitor: Israel Rosalino
 Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química Laboratório de Investigações em Ensino de Ciências Naturais Profª. Drª. Ana Cláudia Kasseboehmer claudiaka@iqsc.usp.br
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química Laboratório de Investigações em Ensino de Ciências Naturais Profª. Drª. Ana Cláudia Kasseboehmer claudiaka@iqsc.usp.br
Balanço de Energia em Combustão
 Balanço de Energia em Combustão O primeira lei da termodinâmica traduzida pelo balanço de energia permite analisar dois conceitos importantes na combustão: temperatura adiabática e poder caloríico que
Balanço de Energia em Combustão O primeira lei da termodinâmica traduzida pelo balanço de energia permite analisar dois conceitos importantes na combustão: temperatura adiabática e poder caloríico que
I. Propriedades Termodinâmicas de Fluidos
 I. Propriedades Termodinâmicas de Fluidos 1 OBJETIVOS Identificar o critério para o equilíbrio em sistemas sujeitos a diferentes restrições Determinar a estabilidade dos sistemas termodinâmicos. Aplicações:
I. Propriedades Termodinâmicas de Fluidos 1 OBJETIVOS Identificar o critério para o equilíbrio em sistemas sujeitos a diferentes restrições Determinar a estabilidade dos sistemas termodinâmicos. Aplicações:
Estimação de Parâmetros em Modelos de Energia Livre de Gibbs em Excesso
 Estimação de Parâmetros em Modelos de Energia Livre de Gibbs em Excesso Cláudio T. Lima, Gustavo M. Platt, Departamento de Modelagem Computacional - IPRJ - UERJ 28630-050, Nova Friburgo, RJ E-mail: ctlima@iprj.uerj.br,
Estimação de Parâmetros em Modelos de Energia Livre de Gibbs em Excesso Cláudio T. Lima, Gustavo M. Platt, Departamento de Modelagem Computacional - IPRJ - UERJ 28630-050, Nova Friburgo, RJ E-mail: ctlima@iprj.uerj.br,
TERMODINÂMICA QUÍMICA APLICADA I
 Disciplina : LOQ 4087 Turma : 20191N1 Engenharia: Bioquímica - Química Lorena, Fevereiro 2019 1 EMENTA 1. Conceitos e definições básicas. 2. Propriedades de substâncias puras. 3. Primeira lei da termodinâmica.
Disciplina : LOQ 4087 Turma : 20191N1 Engenharia: Bioquímica - Química Lorena, Fevereiro 2019 1 EMENTA 1. Conceitos e definições básicas. 2. Propriedades de substâncias puras. 3. Primeira lei da termodinâmica.
Aula 14 Equilíbrio de Fases: Substâncias Puras
 Aula 14 Equilíbrio de Fases: Substâncias Puras 1. A condição de estabilidade Inicialmente precisamos estabelecer a importância da energia de Gibbs molar na discussão das transições de fase. A energia de
Aula 14 Equilíbrio de Fases: Substâncias Puras 1. A condição de estabilidade Inicialmente precisamos estabelecer a importância da energia de Gibbs molar na discussão das transições de fase. A energia de
Se um sistema sofre uma transformação física ou química tal que (A a F) então
 Química Geral 67 http://www.univ-ab.pt/disciplinas/dcet/qg67/ TERMODINÂMICA Os exercícios seguintes estão directamente relacionados com a matéria exposta no capítulo 3 do manual da disciplina de Química
Química Geral 67 http://www.univ-ab.pt/disciplinas/dcet/qg67/ TERMODINÂMICA Os exercícios seguintes estão directamente relacionados com a matéria exposta no capítulo 3 do manual da disciplina de Química
Lista de símbolos...7. Nota introdutória...9
 ÍNDICE Lista de símbolos...7 Nota introdutória...9 PARTE I. TEORIA CINÉTICA DOS GASES... 11 1. Introdução...13 2. O modelo físico. Pressão de um gás...15 3. Distribuição das velocidades moleculares...25
ÍNDICE Lista de símbolos...7 Nota introdutória...9 PARTE I. TEORIA CINÉTICA DOS GASES... 11 1. Introdução...13 2. O modelo físico. Pressão de um gás...15 3. Distribuição das velocidades moleculares...25
Diferença Média de Temperatura entre os Fluidos
 5.3..3 ierença Média de Temperatura entre os Fluidos Equipamentos de Troca Térmica - 134 A equação básica de transerência de calor a ser usada no projeto de trocadores de calor é: U U T da (5.3) A As temperaturas
5.3..3 ierença Média de Temperatura entre os Fluidos Equipamentos de Troca Térmica - 134 A equação básica de transerência de calor a ser usada no projeto de trocadores de calor é: U U T da (5.3) A As temperaturas
calculadora científica
 Lista de Exercícios Obs.:.. a maioria desses exercícios (além dos apresentados nos slides ) estão sendo resolvidos durante as aulas. Caso, não tenha comparecido em alguma aula, verifique com os colegas
Lista de Exercícios Obs.:.. a maioria desses exercícios (além dos apresentados nos slides ) estão sendo resolvidos durante as aulas. Caso, não tenha comparecido em alguma aula, verifique com os colegas
PRODUÇAO DE BIOCOMBUSTÍVEIS ALTERNATIVOS - HIDROGENAÇÃO DE ÓLEO VEGETAL ALTERNATIVE BIOFUEL PRODUCTION - VEGETABLE OIL HYDROGENATION
 12 PRODUÇAO DE BIOCOMBUSTÍVEIS ALTERNATIVOS - HIDROGENAÇÃO DE ÓLEO VEGETAL ALTERNATIVE BIOFUEL PRODUCTION - VEGETABLE OIL HYDROGENATION Moilton R. Franco Junior (1) Alex Anderson O. Moura (2) Nattácia
12 PRODUÇAO DE BIOCOMBUSTÍVEIS ALTERNATIVOS - HIDROGENAÇÃO DE ÓLEO VEGETAL ALTERNATIVE BIOFUEL PRODUCTION - VEGETABLE OIL HYDROGENATION Moilton R. Franco Junior (1) Alex Anderson O. Moura (2) Nattácia
Entropia e energia livre de Gibbs. Prof. Leandro Zatta
 Entropia e energia livre de Gibbs Prof. Leandro Zatta 1 Segunda e a terceira leis Ideias importantes Sentido Natural Desordem Medido por Energia livre de Gibbs 2 Chave para compreensão da ocorrência ou
Entropia e energia livre de Gibbs Prof. Leandro Zatta 1 Segunda e a terceira leis Ideias importantes Sentido Natural Desordem Medido por Energia livre de Gibbs 2 Chave para compreensão da ocorrência ou
Lista de exercícios Termoquímica
 Lista de exercícios Termoquímica Ludmila Ferreira, Miguel Almeida e Eliane de Sá Cavalcante Problema 1 (ITA - 2008) Assinale a opção ERRADA que apresenta (em kj/mol) a entalpia de formação ( H f ) da substância
Lista de exercícios Termoquímica Ludmila Ferreira, Miguel Almeida e Eliane de Sá Cavalcante Problema 1 (ITA - 2008) Assinale a opção ERRADA que apresenta (em kj/mol) a entalpia de formação ( H f ) da substância
Computadores podem ser úteis em problemas que envolvem: Grande número de dados. Grande número de cálculos. Complexidade. Precisão.
 O uso do computador Computadores podem ser úteis em problemas que envolvem: Grande número de dados. Grande número de cálculos. Complexidade. Precisão. Exemplos: Modelos meteorológicos. Cálculo estrutural.
O uso do computador Computadores podem ser úteis em problemas que envolvem: Grande número de dados. Grande número de cálculos. Complexidade. Precisão. Exemplos: Modelos meteorológicos. Cálculo estrutural.
Físico-Química I. Profa. Dra. Carla Dalmolin. Misturas Simples. Termodinâmica das Misturas Propriedades das Soluções Atividade
 Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
Físico-Química I. Profa. Dra. Carla Dalmolin. Termoquímica. Transformações físicas. Transformações químicas
 Físico-Química I Profa. Dra. Carla Dalmolin Termoquímica Transformações físicas Transformações químicas Termoquímica Estudo do calor trocado quando ocorrem reações químicas Sistema Sistema Vizinhança Se
Físico-Química I Profa. Dra. Carla Dalmolin Termoquímica Transformações físicas Transformações químicas Termoquímica Estudo do calor trocado quando ocorrem reações químicas Sistema Sistema Vizinhança Se
Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a. o resultado do movimento dos átomos e moléculas.
 TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
DESENVOLVIMENTO DE UM SIMULADOR DE PROCESSOS A PARTIR DA ABORDAGEM DE RESOLUÇÃO SEQUENCIAL MODULAR PACOTE TERMODINÂMICO.
 DESENVOLVIMENTO DE UM SIMULADOR DE PROCESSOS A PARTIR DA ABORDAGEM DE RESOLUÇÃO SEQUENCIAL MODULAR PACOTE TERMODINÂMICO. Sávio José Pontes da Rocha Barros 1 ; Lucas León Silva Luna 2 ; Isabella Targino
DESENVOLVIMENTO DE UM SIMULADOR DE PROCESSOS A PARTIR DA ABORDAGEM DE RESOLUÇÃO SEQUENCIAL MODULAR PACOTE TERMODINÂMICO. Sávio José Pontes da Rocha Barros 1 ; Lucas León Silva Luna 2 ; Isabella Targino
Conceitos Fundamentais
 Conceitos Fundamentais Introdução. Equilíbrio térmico. Temperatura. Medidas de temperatura. Introdução Escopo da Termodinâmica: A termodinâmica diz respeito ao estudo das propriedades macroscópicas dos
Conceitos Fundamentais Introdução. Equilíbrio térmico. Temperatura. Medidas de temperatura. Introdução Escopo da Termodinâmica: A termodinâmica diz respeito ao estudo das propriedades macroscópicas dos
Termoquímica Entalpia e Lei de Hess
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Termoquímica Entalpia e Lei de Hess Sistemas a Pressão Constante Quando o volume do sistema não é constante,
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Termoquímica Entalpia e Lei de Hess Sistemas a Pressão Constante Quando o volume do sistema não é constante,
QFL0406 FÍSICO- QUÍMICA 2018
 QFL0406 FÍSICO- QUÍMICA 2018 Farmácia Integral 1 a lista de exercícios 1. Na aluminotermia ocorre a reação representada por Fe2O3(s) + 2 Al(s) Al2O3(s) + 2 Fe(s) Calcule a variação de entalpia nessa reação,
QFL0406 FÍSICO- QUÍMICA 2018 Farmácia Integral 1 a lista de exercícios 1. Na aluminotermia ocorre a reação representada por Fe2O3(s) + 2 Al(s) Al2O3(s) + 2 Fe(s) Calcule a variação de entalpia nessa reação,
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação
 Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Refrigeração e Ar Condicionado
 Refrigeração e Ar Condicionado Revisão Filipe Fernandes de Paula filipe.paula@engenharia.ufjf.br Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal de Juiz de
Refrigeração e Ar Condicionado Revisão Filipe Fernandes de Paula filipe.paula@engenharia.ufjf.br Departamento de Engenharia de Produção e Mecânica Faculdade de Engenharia Universidade Federal de Juiz de
IDENTIFICAÇÃO: Atenção: Esteja atento à numeração das páginas Questão 1
 Atenção: Esteja atento à numeração das páginas Questão 1 Determine o volume molar (em unidades de L mol 1 ) e o fator de compressibilidade Z do vapor saturado de água à pressão de 1,00 bar e temperatura
Atenção: Esteja atento à numeração das páginas Questão 1 Determine o volume molar (em unidades de L mol 1 ) e o fator de compressibilidade Z do vapor saturado de água à pressão de 1,00 bar e temperatura
Gás Ideal (1) PMT2305 Físico-Química para Metalurgia e Materiais I César Yuji Narita e Neusa Alonso-Falleiros 2012
 Gás Ideal (1) Para um gás, uma equação de estado é uma relação entre pressão (P), volume (V), temperatura (T) e composição ou número de mols (n). O primeiro passo para a determinação de uma equação de
Gás Ideal (1) Para um gás, uma equação de estado é uma relação entre pressão (P), volume (V), temperatura (T) e composição ou número de mols (n). O primeiro passo para a determinação de uma equação de
Em tarefas de rotina, como a de preparação. Estimativa computacional de parâmetros físicos e termodinâmicos da água e do ar
 Estimativa computacional de parâmetros físicos e termodinâmicos da água e do ar SANTOS, Valdemir Alexandre dos ; VASCONCELOS, Eliane Cardoso de ; ANDRADE, Elaine Pimentel de Resumo A água e o ar são substâncias
Estimativa computacional de parâmetros físicos e termodinâmicos da água e do ar SANTOS, Valdemir Alexandre dos ; VASCONCELOS, Eliane Cardoso de ; ANDRADE, Elaine Pimentel de Resumo A água e o ar são substâncias
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
Termodinâmica. Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos. QUÍMICA GERAL Fundamentos
 Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos 1 Calor e Trabalho Calor e trabalho são formas relacionadas de energia Calor pode ser convertido em trabalho
Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos 1 Calor e Trabalho Calor e trabalho são formas relacionadas de energia Calor pode ser convertido em trabalho
Físico-Química Farmácia 2014/02
 Físico-Química Farmácia 2014/02 1 2 Aspectos termodinâmicos das transições de fase A descrição termodinâmica das misturas Referência: Peter Atkins, Julio de Paula, Físico-Química Biológica 3 Condição de
Físico-Química Farmácia 2014/02 1 2 Aspectos termodinâmicos das transições de fase A descrição termodinâmica das misturas Referência: Peter Atkins, Julio de Paula, Físico-Química Biológica 3 Condição de
Profª Eleonora Slide de aula. Revisão: Termodinâmica e Bioenergética
 Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
02 A prova pode ser feita a lápis. 03 Proibido o uso de calculadoras e similares. 04 Duração: 2 HORAS. x e) 21. x d) 20 SOLUÇÃO. log.
 UNIVERSIDADE FEDERAL DE ITAJUBÁ MATEMÁTICA PROVA DE TRANSFERÊNCIA INTERNA, EXTERNA E PARA PORTADOR DE DIPLOMA DE CURSO SUPERIOR 9/6/ CANDIDATO: CURSO PRETENDIDO: OBSERVAÇÕES: Prova sem consulta A prova
UNIVERSIDADE FEDERAL DE ITAJUBÁ MATEMÁTICA PROVA DE TRANSFERÊNCIA INTERNA, EXTERNA E PARA PORTADOR DE DIPLOMA DE CURSO SUPERIOR 9/6/ CANDIDATO: CURSO PRETENDIDO: OBSERVAÇÕES: Prova sem consulta A prova
Lisboa, 12 de Janeiro de 2008
 Prova escrita de: 2º Teste de iência de Materiais (orrecção) Lisboa, 12 de Janeiro de 2008 Nome: Número: urso: 1. onsidere a cementação da superície de uma roda dentada de um aço 1022 (0,22% ). (a) O coeiciente
Prova escrita de: 2º Teste de iência de Materiais (orrecção) Lisboa, 12 de Janeiro de 2008 Nome: Número: urso: 1. onsidere a cementação da superície de uma roda dentada de um aço 1022 (0,22% ). (a) O coeiciente
Existem três categorias principais de linguagem de programação: linguagem de máquina, linguagens assembly e linguagens de alto nível.
 Aula 3 SOFTWARE (programas) Um programa (software) consiste em uma sequência de instruções escritas numa linguagem precisa chamada linguagem de programação. Estas instruções são traduzidas em um compilador,
Aula 3 SOFTWARE (programas) Um programa (software) consiste em uma sequência de instruções escritas numa linguagem precisa chamada linguagem de programação. Estas instruções são traduzidas em um compilador,
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127. Termodinâmica
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Termodinâmica Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Energia e Trabalho Energia A capacidade de realizar
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Termodinâmica Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Energia e Trabalho Energia A capacidade de realizar
a) C 3 H 8 (g) 3C graf. + 4 H 2(g) C 3 H 8(g) b) C 2 H 6 O(l) 2C graf. + 3 H 2(g) + 1/2 O 2(g) C 2 H 6 O (l) c) Na 2 SO 4 (s)
 setor 30 300408 Aula 3 TERMOQUÍMICA. ENTALPIA DE FORMAÇÃO Estado Padrão = Estado físico e alotrópico mais estáveis em condição ambiente (5 C, atm). Substâncias Simples no Estado Padrão H FORM H FORM =
setor 30 300408 Aula 3 TERMOQUÍMICA. ENTALPIA DE FORMAÇÃO Estado Padrão = Estado físico e alotrópico mais estáveis em condição ambiente (5 C, atm). Substâncias Simples no Estado Padrão H FORM H FORM =
química química na abordagem do cotidiano
 Capítulo Lei de Hess e entalpias-padrão Respostas dos exercícios essenciais H C H 35 kj H total 60 kj B H 5 kj A H X H 3 0 kj Y H 4 40 kj H total 60 kj Z 3 H T H 6 30 kj U H 5 60 kj H total 30 kj S 5 a)
Capítulo Lei de Hess e entalpias-padrão Respostas dos exercícios essenciais H C H 35 kj H total 60 kj B H 5 kj A H X H 3 0 kj Y H 4 40 kj H total 60 kj Z 3 H T H 6 30 kj U H 5 60 kj H total 30 kj S 5 a)
TERMOQUÍMICA. 1 Fenômenos endotérmicos e exotérmicos
 TERMOQUÍMICA 1 Fenômenos endotérmicos e exotérmicos a) Processos exotérmicos: Ocorrem com liberação de calor. Possuem variação de entalpia ( H) negativa. Ex: Combustão do metano (CH4) CH4 (g) + 2 O2 (g)
TERMOQUÍMICA 1 Fenômenos endotérmicos e exotérmicos a) Processos exotérmicos: Ocorrem com liberação de calor. Possuem variação de entalpia ( H) negativa. Ex: Combustão do metano (CH4) CH4 (g) + 2 O2 (g)
CP Introdução à Informática Prof. Msc. Carlos de Salles
 CP 1015.1 Prof. Msc. Carlos de Salles PROGRAMA 1. CONCEITO DE SISTEMAS 1.1 Sistemas e sua classificação 1.2 Informações e Dados 1.3 O Processamento de Dados 1.4 O Computador e sua História 2. ESTRUTURA
CP 1015.1 Prof. Msc. Carlos de Salles PROGRAMA 1. CONCEITO DE SISTEMAS 1.1 Sistemas e sua classificação 1.2 Informações e Dados 1.3 O Processamento de Dados 1.4 O Computador e sua História 2. ESTRUTURA
10ª LISTA - EXERCÍCIOS DE PROVAS 2ª. Lei da Termodinâmica
 Pg. 1/5 1 a Questão A massa de 1,80 g de água pura, em um recipiente hermeticamente fechado, foi aquecida até a fervura, ao nível do mar. A equação abaixo representa a vaporização da água. H 2 O(l) H 2
Pg. 1/5 1 a Questão A massa de 1,80 g de água pura, em um recipiente hermeticamente fechado, foi aquecida até a fervura, ao nível do mar. A equação abaixo representa a vaporização da água. H 2 O(l) H 2
Equações de estado para líquidos
 Equações de estado para líquidos Capítulo 4 Há tempos, os cientistas especulam se os materiais orgânicos dessa atmosfera foram formados por mares e lagos de metano [...] O metano é um gás altamente inflamável
Equações de estado para líquidos Capítulo 4 Há tempos, os cientistas especulam se os materiais orgânicos dessa atmosfera foram formados por mares e lagos de metano [...] O metano é um gás altamente inflamável
TERMODINÂMICA APLICADA CAPÍTULO 2
 TERMODINÂMICA APLICADA CAPÍTULO 2 PROPRIEDADES DAS SUBSTÂNCIAS PURAS SUMÁRIO Neste capítulo o conceito de substância pura é introduzido e as várias fases, bem como as propriedades físicas dos processos
TERMODINÂMICA APLICADA CAPÍTULO 2 PROPRIEDADES DAS SUBSTÂNCIAS PURAS SUMÁRIO Neste capítulo o conceito de substância pura é introduzido e as várias fases, bem como as propriedades físicas dos processos
Energia, calor, entalpia e variação de entalpia.
 Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Combustíveis Energia e Ambiente De onde vem a energia dos combustíveis? Energia, calor, entalpia e variação de entalpia. Sistema; Universo; Sistema Aberto, Fechado e Isolado; Estado final e Inicial; Energia
Entalpia. O trabalho realizado por esta reação é denominado trabalho de pressão-volume (trabalho PV)
 Entalpia As reações químicas podem absorver ou liberar calor e também podem provocar a realização de trabalho. Quando um gás é produzido, ele pode ser utilizado para empurrar um pistão: Zn(s) + 2H + (aq)
Entalpia As reações químicas podem absorver ou liberar calor e também podem provocar a realização de trabalho. Quando um gás é produzido, ele pode ser utilizado para empurrar um pistão: Zn(s) + 2H + (aq)
3 Análise experimental do escoamento sobre uma placa plana com duas portas de injeção: interação entre gotas
 3 Análise experimental do escoamento sobre uma placa plana com duas portas de injeção: interação entre gotas Neste capítulo, a interação entre duas gotas de líquido escoando sobre um plano inclinado é
3 Análise experimental do escoamento sobre uma placa plana com duas portas de injeção: interação entre gotas Neste capítulo, a interação entre duas gotas de líquido escoando sobre um plano inclinado é
Conceitos primordiais da Termodinâmica
 Conceitos primordiais da Termodinâmica Miguel Almeida 1 Propriedades de Estado Propriedade de estado é aquela que sua variação não depende do "caminho" mas sim dos estados final e inicial. Pode ser equacionada
Conceitos primordiais da Termodinâmica Miguel Almeida 1 Propriedades de Estado Propriedade de estado é aquela que sua variação não depende do "caminho" mas sim dos estados final e inicial. Pode ser equacionada
Propriedades dos compostos moleculares
 Aula 10 Propriedades dos compostos moleculares Forças intermoleculares Van der Waals: Keesom, Debye, London Ligações de hidrogénio Propriedades Temperaturas de fusão e de ebulição Miscibilidade Viscosidade
Aula 10 Propriedades dos compostos moleculares Forças intermoleculares Van der Waals: Keesom, Debye, London Ligações de hidrogénio Propriedades Temperaturas de fusão e de ebulição Miscibilidade Viscosidade
Disciplina : Máquinas Térmicas e de Fluxo. Aula 2 Propriedades Termodinâmicas
 Disciplina : Máquinas Térmicas e de Fluxo Aula 2 Propriedades Termodinâmicas Prof. Evandro Rodrigo Dário, Dr. Eng. Líquido comprimido Considere-se um dispositivo de cilindropistão contendo água na fase
Disciplina : Máquinas Térmicas e de Fluxo Aula 2 Propriedades Termodinâmicas Prof. Evandro Rodrigo Dário, Dr. Eng. Líquido comprimido Considere-se um dispositivo de cilindropistão contendo água na fase
Termodinâmica. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química ermodinâmica Professora: Melissa Soares Caetano Disciplina QUI 217 Segundo Princípio da ermodinâmica
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química ermodinâmica Professora: Melissa Soares Caetano Disciplina QUI 217 Segundo Princípio da ermodinâmica
MODELAGEM TERMODINÂMICA DA REAÇÃO DE HIDRÓLISE DO ÓLEO DE SOJA
 MODELAGEM TERMODINÂMICA DA REAÇÃO DE HIDRÓLISE DO ÓLEO DE SOJA M. B. LOPES 1, I. G. NASCIMENTO 1, J. J. MARQUES 1 e A. L. D. RAMOS 1 1 Universidade Federal de Sergipe, Departamento de Engenharia Química
MODELAGEM TERMODINÂMICA DA REAÇÃO DE HIDRÓLISE DO ÓLEO DE SOJA M. B. LOPES 1, I. G. NASCIMENTO 1, J. J. MARQUES 1 e A. L. D. RAMOS 1 1 Universidade Federal de Sergipe, Departamento de Engenharia Química
PREDIÇÃO DAS PROPRIEDADES FÍSICAS E TERMODINÂMICAS DO ÓLEO DA POLPA DA MACAÚBA E BIODIESEL POR MÉTODO DE CONTRIBUIÇÃO DE GRUPOS
 PREDIÇÃO DAS PROPRIEDADES FÍSICAS E TERMODINÂMICAS DO ÓLEO DA POLPA DA MACAÚBA E BIODIESEL POR MÉTODO DE CONTRIBUIÇÃO DE GRUPOS G. C. RABELO SILVA 1 e M.H. CANO ANDRADE 2 1 Universidade Federal de São
PREDIÇÃO DAS PROPRIEDADES FÍSICAS E TERMODINÂMICAS DO ÓLEO DA POLPA DA MACAÚBA E BIODIESEL POR MÉTODO DE CONTRIBUIÇÃO DE GRUPOS G. C. RABELO SILVA 1 e M.H. CANO ANDRADE 2 1 Universidade Federal de São
INTRODUÇÃO À QUÍMICA FÍSICA
 FACULDADE DE CIÊNCIAS E TECNOLOGIA DEPARTAMENTO DE QUÍMICA, BIOQUÍMICA E FARMÁCIA Orientação tutorial INTRODUÇÃO À QUÍMICA FÍSICA 1º Ano Q/BQ/CF/F/MIEB/BT Ano Lectivo: 2008 / 2009 (5º Módulo) 2009 IQF
FACULDADE DE CIÊNCIAS E TECNOLOGIA DEPARTAMENTO DE QUÍMICA, BIOQUÍMICA E FARMÁCIA Orientação tutorial INTRODUÇÃO À QUÍMICA FÍSICA 1º Ano Q/BQ/CF/F/MIEB/BT Ano Lectivo: 2008 / 2009 (5º Módulo) 2009 IQF
Aula 2 Termodinâmica de substâncias puras: diagramas de fase
 Uniersidade Federal do ABC P O S M E C Aula 2 Termodinâmica de substâncias puras: diagramas de fase MEC202 Susbtância Pura Uma substancia que tem uma única composição. Exemplo: N 2, álcool, CO 2. Pode
Uniersidade Federal do ABC P O S M E C Aula 2 Termodinâmica de substâncias puras: diagramas de fase MEC202 Susbtância Pura Uma substancia que tem uma única composição. Exemplo: N 2, álcool, CO 2. Pode
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
Trabalho em uma transformação
 Trabalho em uma transformação Trabalho (W) é uma medida da energia transferida pela aplicação de uma força ao longo de um deslocamento W = a b F dx A unidade de trabalho, no SI, é o Joule (J); 1 J = 1
Trabalho em uma transformação Trabalho (W) é uma medida da energia transferida pela aplicação de uma força ao longo de um deslocamento W = a b F dx A unidade de trabalho, no SI, é o Joule (J); 1 J = 1
Temperatura Calor Transmissão de calor 1 a Lei da Termodinâmica
 Temperatura Calor Transmissão de calor 1 a Lei da Termodinâmica Temperatura Temperatura Temperatura: é o grau de agitação das partículas (átomos, moléculas) de um corpo. Lei zero da termodinâmica Se dois
Temperatura Calor Transmissão de calor 1 a Lei da Termodinâmica Temperatura Temperatura Temperatura: é o grau de agitação das partículas (átomos, moléculas) de um corpo. Lei zero da termodinâmica Se dois
QUÍMICA. Transformações Químicas e Energia. Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess - Parte 6
 QUÍMICA Transformações Químicas e Energia Entalpia, Equações e Lei de Hess - Parte 6 Prof ª. Giselle Blois Como ocorrem as reações químicas? - Afinidade química entre os reagentes; - Contato efetivo entre
QUÍMICA Transformações Químicas e Energia Entalpia, Equações e Lei de Hess - Parte 6 Prof ª. Giselle Blois Como ocorrem as reações químicas? - Afinidade química entre os reagentes; - Contato efetivo entre
Introdução à Computação para Engenharia MAC2166 Prof. Dr. Paulo Miranda IME-USP. Aula 1 Introdução à Computação
 Introdução à Computação para Engenharia MAC2166 Prof. Dr. Paulo Miranda IME-USP Aula 1 Introdução à Computação Eventos históricos: 1) Primeiro computador a válvulas, o Eletronic Numeric Integrator And
Introdução à Computação para Engenharia MAC2166 Prof. Dr. Paulo Miranda IME-USP Aula 1 Introdução à Computação Eventos históricos: 1) Primeiro computador a válvulas, o Eletronic Numeric Integrator And
PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 2 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI
 PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 2 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI ÁREA DE CONCENTRAÇÃO: FÍSICA E QUÍMICA DE MATERIAIS NÍVEL:
PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 2 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI ÁREA DE CONCENTRAÇÃO: FÍSICA E QUÍMICA DE MATERIAIS NÍVEL:
Laboratório 01 NetBeans
 Universidade Federal de Uberlândia Faculdade de Computação GGI030 Programação Orientada a Objetos 2o. Semestre de 2017 Prof. Renato Pimentel Atividade individual. Laboratório 01 NetBeans 1 Introdução Os
Universidade Federal de Uberlândia Faculdade de Computação GGI030 Programação Orientada a Objetos 2o. Semestre de 2017 Prof. Renato Pimentel Atividade individual. Laboratório 01 NetBeans 1 Introdução Os
Termodinâmica. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química ermodinâmica Professora: Melissa Soares Caetano Disciplina QUI 217 Segundo Princípio da ermodinâmica
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química ermodinâmica Professora: Melissa Soares Caetano Disciplina QUI 217 Segundo Princípio da ermodinâmica
2. Conceitos e Definições
 2. Conceitos e Definições Sistema e Volume de Controle Sistema Termodinâmico: região do espaço delimitada fisicamente por superfícies geométricas arbitrárias reais ou imaginárias, que podem ser fixas ou
2. Conceitos e Definições Sistema e Volume de Controle Sistema Termodinâmico: região do espaço delimitada fisicamente por superfícies geométricas arbitrárias reais ou imaginárias, que podem ser fixas ou
Informática I. Aula Aula 18-19/06/06 1
 Informática I Aula 18 http://www.ic.uff.br/~bianca/informatica1/ Aula 18-19/06/06 1 Correção da Prova 1 1. Qual dispositivo é considerado o primeiro ancestral do computador? Que operações podem ser realizadas
Informática I Aula 18 http://www.ic.uff.br/~bianca/informatica1/ Aula 18-19/06/06 1 Correção da Prova 1 1. Qual dispositivo é considerado o primeiro ancestral do computador? Que operações podem ser realizadas
Uma Escola Pensando em Você Aluno(a): nº Série: 2 col C Disciplina: Física. Ensino: Médio Professor: Renato Data:, de 2010
 Uma Escola Pensando em Você luno(a): nº Série: 2 col C Disciplina: Física Ensino: Médio Professor: Renato Data:, de 21 Trabalho de Recuperação de Física (1º e 2 imestres) Instruções: 1. O trabalho deverá
Uma Escola Pensando em Você luno(a): nº Série: 2 col C Disciplina: Física Ensino: Médio Professor: Renato Data:, de 21 Trabalho de Recuperação de Física (1º e 2 imestres) Instruções: 1. O trabalho deverá
Termodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem/2005 Resolução comentada Prof. Fabrício R. Sensato
 Termodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem/2005 Resolução comentada Prof. Fabrício R. Sensato 1) (1,0 ponto) a) Como é definido o fator de compressibilidade, Z, de um gás? b) Qual
Termodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem/2005 Resolução comentada Prof. Fabrício R. Sensato 1) (1,0 ponto) a) Como é definido o fator de compressibilidade, Z, de um gás? b) Qual
ESTIMAÇÃO DO COEFICIENTE DE ATIVIDADE DE UM SISTEMA BINÁRIO EM EQUÍLIBRIO LÍQUIDO-VAPOR UTILIZANDO O MÉTODO UNIFAC
 ESTIMAÇÃO DO COEFICIENTE DE ATIVIDADE DE UM SISTEMA BINÁRIO EM EQUÍLIBRIO LÍQUIDO-VAPOR UTILIZANDO O MÉTODO UNIFAC José Cleiton Sousa dos SANTOS (1); Marylane de SOUSA02 (2); Darlane Wellen Freitas de
ESTIMAÇÃO DO COEFICIENTE DE ATIVIDADE DE UM SISTEMA BINÁRIO EM EQUÍLIBRIO LÍQUIDO-VAPOR UTILIZANDO O MÉTODO UNIFAC José Cleiton Sousa dos SANTOS (1); Marylane de SOUSA02 (2); Darlane Wellen Freitas de
Atividades Práticas Supervisionadas (APS)
 Universidade Tecnológica Federal do Paraná Pro: Lauro Cesar Galvão Campus Curitiba Departamento Acadêmico de Matemática Cálculo Numérico Entrega: unto com a a parcial DATA DE ENTREGA: dia da a PROVA (em
Universidade Tecnológica Federal do Paraná Pro: Lauro Cesar Galvão Campus Curitiba Departamento Acadêmico de Matemática Cálculo Numérico Entrega: unto com a a parcial DATA DE ENTREGA: dia da a PROVA (em
Aula 7 Entalpia e Lei de Hess
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 7 Entalpia e Lei de Hess Dr. Tiago P. Camargo Entalpia Termodinâmica Num sistema de paredes rígidas V const.
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 7 Entalpia e Lei de Hess Dr. Tiago P. Camargo Entalpia Termodinâmica Num sistema de paredes rígidas V const.
Índice : 1-Objetivos Introdução Materiais utilizados Procedimento Resultados e análise dos resultados 09
 Índice : -Objetivos 0 -Introdução 03 3-Materiais utilizados 05 4-Procedimento 06 5-Resultados e análise dos resultados 09 6-Discussão e conclusão 6 7-Bibliografia 8 -Objetivos O aproveitamento de linguagens
Índice : -Objetivos 0 -Introdução 03 3-Materiais utilizados 05 4-Procedimento 06 5-Resultados e análise dos resultados 09 6-Discussão e conclusão 6 7-Bibliografia 8 -Objetivos O aproveitamento de linguagens
TERMODINÂMICA I 1º SEMESTRE DE 2015 Docente: Anderson H.R. Ferreira 2º LISTA DE EXERCÍCIOS UNIDADE II PROPRIEDADES TERMODINÂMICAS
 1 TERMODINÂMICA I 1º SEMESTRE DE 2015 Docente: Anderson H.R. Ferreira 2º LISTA DE EXERCÍCIOS Instruções: Tenha sempre em mãos uma Calculadora Científica, pois a mesma será utilizada exaustivamente no curso
1 TERMODINÂMICA I 1º SEMESTRE DE 2015 Docente: Anderson H.R. Ferreira 2º LISTA DE EXERCÍCIOS Instruções: Tenha sempre em mãos uma Calculadora Científica, pois a mesma será utilizada exaustivamente no curso
SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL
 ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL 1. CARACTERÍSTICAS GERAIS DA SOLUÇÃO IDEAL Para
ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL 1. CARACTERÍSTICAS GERAIS DA SOLUÇÃO IDEAL Para
1. INTRODUÇÃO Equilíbrio Líquido-vapor. V. A. de ABREU 1, A. T. SANTOS 1, W. R. O. PIMENTEL 1 e A. K. BRAGA 1
 AVALIAÇÃO DO EQUILÍBRIO LÍQUIDO VAPOR DE UMA MISTURA DE ETANOL + TOLUENO À TEMPERATURA CONSTANTE UTILIZANDO SIMULAÇÃO NUMÉRICA EM MATLAB PARA MODELOS DE COMPOSIÇÕES LOCAIS V. A. de ABREU 1, A. T. SANTOS
AVALIAÇÃO DO EQUILÍBRIO LÍQUIDO VAPOR DE UMA MISTURA DE ETANOL + TOLUENO À TEMPERATURA CONSTANTE UTILIZANDO SIMULAÇÃO NUMÉRICA EM MATLAB PARA MODELOS DE COMPOSIÇÕES LOCAIS V. A. de ABREU 1, A. T. SANTOS
5. Funções de afastamento e fugacidade
 QI 58 Fundamentos de rocessos em Engenharia Química II 009 5. Funções de afastamento e fugacidade Assuntos. Funções de afastamento. Fugacidade 3. Exercícios 5.. Funções de afastamento As relações estudadas
QI 58 Fundamentos de rocessos em Engenharia Química II 009 5. Funções de afastamento e fugacidade Assuntos. Funções de afastamento. Fugacidade 3. Exercícios 5.. Funções de afastamento As relações estudadas
PROFª. KAÍZA CAVALCANTI
 Processos Químicos Quando ocorre uma alteração qualitativa do sistema, dos tipos de substâncias presentes ou de suas proporções. Processos Físicos Quando ocorre uma alteração qualitativa do sistema, dos
Processos Químicos Quando ocorre uma alteração qualitativa do sistema, dos tipos de substâncias presentes ou de suas proporções. Processos Físicos Quando ocorre uma alteração qualitativa do sistema, dos
CALOR E PRIMEIRA LEI DA TERMODINÂMICA
 CALOR E PRIMEIRA LEI DA TERMODINÂMICA Calor é a energia transerida de um corpo para outro em irtude, basicamente, de uma dierença de temperatura. Capacidade Caloríica e Calor Especíico A quantidade de
CALOR E PRIMEIRA LEI DA TERMODINÂMICA Calor é a energia transerida de um corpo para outro em irtude, basicamente, de uma dierença de temperatura. Capacidade Caloríica e Calor Especíico A quantidade de
Diagramas de Energia
 Diagramas de Energia 1.1- Análise Gráfica Reação exotérmica Reação endotérmica (a) Energia de ativação (Ea) para a reação inversa (b) Energia de ativação (Ea) para a reação direta (c) ΔH 1.2- Entropia
Diagramas de Energia 1.1- Análise Gráfica Reação exotérmica Reação endotérmica (a) Energia de ativação (Ea) para a reação inversa (b) Energia de ativação (Ea) para a reação direta (c) ΔH 1.2- Entropia
A prova escrita é composta de 10 questões, sendo 4 obrigatórias e 6 eletivas.
 A prova escrita é composta de 10 questões, sendo 4 obrigatórias e 6 eletivas. O candidato deverá responder 8 questões: as 4 obrigatórias (questões de números 1 a 4) e outras 4 escolhidas dentre as eletivas
A prova escrita é composta de 10 questões, sendo 4 obrigatórias e 6 eletivas. O candidato deverá responder 8 questões: as 4 obrigatórias (questões de números 1 a 4) e outras 4 escolhidas dentre as eletivas
FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR
 FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR TEMPERATURA Grandeza Fundamental do S.I. Medida aproximada de agitação média de moléculas Unidade Principal: (Kelvin)
FÍSICA TÉRMICA TEMPERATURA, DILATAÇÃO TÉRMICA, CALORIMETRIA E TRANSMISSÃO DE CALOR TEMPERATURA Grandeza Fundamental do S.I. Medida aproximada de agitação média de moléculas Unidade Principal: (Kelvin)
Universidade Federal do Acre Engenharia Agronômica PET- Programa de Ensino Tutorial. Termoquímica
 Universidade Federal do Acre Engenharia Agronômica PET- Programa de Ensino Tutorial Termoquímica Bolsista: Joyce de Q. Barbosa Tutor: Dr. José Ribamar Silva Termodinâmica Conceitos Básicos Termoquímica
Universidade Federal do Acre Engenharia Agronômica PET- Programa de Ensino Tutorial Termoquímica Bolsista: Joyce de Q. Barbosa Tutor: Dr. José Ribamar Silva Termodinâmica Conceitos Básicos Termoquímica
Transformações Físicas
 Físico-Química I Profa. Dra. Carla Dalmolin Transformações Físicas Transições de Fase de Substâncias Puras Diagrama de Fases Transformações Físicas Transformações onde não ocorrem mudança na composição
Físico-Química I Profa. Dra. Carla Dalmolin Transformações Físicas Transições de Fase de Substâncias Puras Diagrama de Fases Transformações Físicas Transformações onde não ocorrem mudança na composição
INFORMÁTICA: Informação automática
 INTRODUÇÃO INFORMÁTICA: Informação automática Definição: é a ciência que estuda o tratamento automático e racional da informação (encarregada pelo estudo e desenvolvimento de máquinas e métodos para processar
INTRODUÇÃO INFORMÁTICA: Informação automática Definição: é a ciência que estuda o tratamento automático e racional da informação (encarregada pelo estudo e desenvolvimento de máquinas e métodos para processar
TERMODINÂMICA (Parte 1)
 TERMODINÂMICA (Parte 1) Estudo das transformações da energia. Baseia-se em duas leis: 1ª Lei: acompanha as variações de energia e permite o cálculo da quantidade de calor produzida numa reação. 2ª Lei:
TERMODINÂMICA (Parte 1) Estudo das transformações da energia. Baseia-se em duas leis: 1ª Lei: acompanha as variações de energia e permite o cálculo da quantidade de calor produzida numa reação. 2ª Lei:
DEPRESSÃO CRIOSCÓPIA POR ADIÇÃO DE UM ELECTRÓLITO FORTE E DE UM NÃO- ELECTRÓLITO TP5
 Escola uperior de Tecnologia e Gestão DEPREÃO CROCÓP POR DÇÃO DE UM ELECTRÓLTO FORTE E DE UM NÃO- ELECTRÓLTO TP5 LBORTÓRO DE ENGENHR QUÍMC 009/00 Escola uperior de Tecnologia e Gestão. Objectivo Estudar
Escola uperior de Tecnologia e Gestão DEPREÃO CROCÓP POR DÇÃO DE UM ELECTRÓLTO FORTE E DE UM NÃO- ELECTRÓLTO TP5 LBORTÓRO DE ENGENHR QUÍMC 009/00 Escola uperior de Tecnologia e Gestão. Objectivo Estudar
Termodinâmica e Estrutura da Matéria
 Termodinâmica e Estrutura da Matéria Conceitos básicos J. Seixas Sistema Índice da lição e Sistema Porque falamos de sistema? Para descrever um fenómeno físico precisamos de especificar do que estamos
Termodinâmica e Estrutura da Matéria Conceitos básicos J. Seixas Sistema Índice da lição e Sistema Porque falamos de sistema? Para descrever um fenómeno físico precisamos de especificar do que estamos
Programação Estruturada e OO Aula 1.2 Introdução a Paradigmas de Programação. Prof. Bruno Moreno
 Programação Estruturada e OO Aula 1.2 Introdução a Paradigmas de Programação Prof. Bruno Moreno bruno.moreno@ifrn.edu.br Motivação Por que existe mais de uma LP? Propósitos diferentes; Avanços tecnológicos;
Programação Estruturada e OO Aula 1.2 Introdução a Paradigmas de Programação Prof. Bruno Moreno bruno.moreno@ifrn.edu.br Motivação Por que existe mais de uma LP? Propósitos diferentes; Avanços tecnológicos;
QUÍMICA GERAL Termodinâmica
 QUÍMICA GERAL Termodinâmica Prof. Dr. Anselmo E. de Oliveira Instituto de Química, UFG anselmo.quimica.ufg.br anselmo.disciplinas@gmail.com 18 de Setembro de 2018 Agronomia Sistemas, Estados e Energia
QUÍMICA GERAL Termodinâmica Prof. Dr. Anselmo E. de Oliveira Instituto de Química, UFG anselmo.quimica.ufg.br anselmo.disciplinas@gmail.com 18 de Setembro de 2018 Agronomia Sistemas, Estados e Energia
TERMODINÂMICA INTRODUÇÃO PRIMEIRA LEI
 TERMODINÂMICA INTRODUÇÃO PRIMEIRA LEI Escola Politécnica da USP Departamento de Engenharia Metalúrgica e de Materiais A. C. Neiva 1 Começando: algumas definições meio abstratas, mas importantes Sistema
TERMODINÂMICA INTRODUÇÃO PRIMEIRA LEI Escola Politécnica da USP Departamento de Engenharia Metalúrgica e de Materiais A. C. Neiva 1 Começando: algumas definições meio abstratas, mas importantes Sistema
Campus Sete Lagoas Departamento de Ciências Agrárias TUTORIAL GRAPSI 2018 APLICATIVO PARA CÁLCULO DAS PROPRIEDADES PSICROMÉTRICAS DO AR
 Campus Sete Lagoas Departamento de Ciências Agrárias TUTORIAL GRAPSI 2018 APLICATIVO PARA CÁLCULO DAS PROPRIEDADES PSICROMÉTRICAS DO AR (Válido para temperaturas entre -100 e 372 o C) Elaborado por: Daniela
Campus Sete Lagoas Departamento de Ciências Agrárias TUTORIAL GRAPSI 2018 APLICATIVO PARA CÁLCULO DAS PROPRIEDADES PSICROMÉTRICAS DO AR (Válido para temperaturas entre -100 e 372 o C) Elaborado por: Daniela
DESENVOLVIMENTO DE UM SOFTWARE DIDÁTICO PARA O ENSINO E PROJETO DO COMPORTAMENTO DINÂMICO DE ESTRUTURAS
 DESENVOLVIMENTO DE UM SOFTWARE DIDÁTICO PARA O ENSINO E PROJETO DO COMPORTAMENTO DINÂMICO DE ESTRUTURAS José G. S. da Silva - jgss@uerj.br Depto. Engenharia Mecânica, Faculdade de Engenharia, FEN/UERJ
DESENVOLVIMENTO DE UM SOFTWARE DIDÁTICO PARA O ENSINO E PROJETO DO COMPORTAMENTO DINÂMICO DE ESTRUTURAS José G. S. da Silva - jgss@uerj.br Depto. Engenharia Mecânica, Faculdade de Engenharia, FEN/UERJ
PROVA DE QUÍMICA 44 PROVA DE QUÍMICA
 44 QUESTÃO 46 1 Uma certa quantidade de água é colocada em um congelador, cuja temperatura é de 20 o C. Após estar formado e em equilíbrio térmico com o congelador, o gelo é transferido para outro congelador,
44 QUESTÃO 46 1 Uma certa quantidade de água é colocada em um congelador, cuja temperatura é de 20 o C. Após estar formado e em equilíbrio térmico com o congelador, o gelo é transferido para outro congelador,
ESTUDO E ANÁLISE DA MISTURA DE ÁGUA E ETANOL ATRAVÉS DE EQUAÇÕES DE ESTADO.
 ESTUDO E ANÁLISE DA MISTURA DE ÁGUA E ETANOL ATRAVÉS DE EQUAÇÕES DE ESTADO. S. F. VASCONCELOS 1, F. J. F. CHAVES 1, C. V. FERNANDES 1, N. SILVA 1, H. BISPO 1 1 Universidade Federal de Campina Grande, Unidade
ESTUDO E ANÁLISE DA MISTURA DE ÁGUA E ETANOL ATRAVÉS DE EQUAÇÕES DE ESTADO. S. F. VASCONCELOS 1, F. J. F. CHAVES 1, C. V. FERNANDES 1, N. SILVA 1, H. BISPO 1 1 Universidade Federal de Campina Grande, Unidade
Chapter 4 Thermodynamic Variables and Relations
 Universidade de São Paulo Instituto de Física de São Carlos - IFSC Chapter 4 Thermodynamic Variables and Relations (Thermodynamics in Materials Science. DeHoff) Prof. Dr. José Pedro Donoso Capítulo 4 4.1-Definitions
Universidade de São Paulo Instituto de Física de São Carlos - IFSC Chapter 4 Thermodynamic Variables and Relations (Thermodynamics in Materials Science. DeHoff) Prof. Dr. José Pedro Donoso Capítulo 4 4.1-Definitions
Fabiano Moreira.
 Fabiano Moreira professor@fabianomoreira.com.br Um pouco de história Java 1.02 (250 classes, lenta) Java 1.1 (500 classes, um pouco mais rápida) Java 2, versões 1.2-1.4 (2300 classes, muito mais rápida)
Fabiano Moreira professor@fabianomoreira.com.br Um pouco de história Java 1.02 (250 classes, lenta) Java 1.1 (500 classes, um pouco mais rápida) Java 2, versões 1.2-1.4 (2300 classes, muito mais rápida)
Capítulos 7 e 8 Solidificação e Difusão atómica em sólidos
 Capítulos 7 e 8 Solidiicação e Diusão atómica em sólidos 1*. Considere a nucleação homogénea do gelo à temperatura de -40 C em que a energia livre de Gibbs de um agregado de moléculas é expressa por: 4
Capítulos 7 e 8 Solidiicação e Diusão atómica em sólidos 1*. Considere a nucleação homogénea do gelo à temperatura de -40 C em que a energia livre de Gibbs de um agregado de moléculas é expressa por: 4
TERMODINÂMICA TERMOQUÍMICA
 TERMODINÂMICA TERMOQUÍMICA Termodinâmica é a ciência que estuda as transformações de energia nas quais as variações de temperatura são importantes. A maioria das transformações químicas resulta em alterações
TERMODINÂMICA TERMOQUÍMICA Termodinâmica é a ciência que estuda as transformações de energia nas quais as variações de temperatura são importantes. A maioria das transformações químicas resulta em alterações
