Actividade ou v 0 ou v inicial =k cat [E S] v inicial = k cat [E S] = Vmax. v inicial = k cat [Etotal]/2 v inicial = Vmax/2. k cat
|
|
|
- Mateus Andrade Carmona
- 5 Há anos
- Visualizações:
Transcrição
1 Numa reacção enzímica existe um ciclo catalítico em que da ligação entre a enzima lire e o resulta a formação do complexo E S; o complexo E S pode dissociar-se mas também ai formando produto e regenerando enzima lire. Num ensaio enzímico enquanto a concentração de não baixar de forma significatia a concentração do complexo E S ai-se mantendo numa concentração estacionária. O alor da concentração estacionária de E S depende (1) da concentração de enzima, (2) da concentração de e k cat A elocidade de formação do produto é proporcional à concentração do complexo E S k cat [E S] Actiidade ou ou k cat [E S] k cat [Etotal]/2 /2 Se não há [E S] inicial Existe uma concentração de ( Km) em que metade das moléculas de (enzima hemisaturada) [E S] [E] [E S] [Etotal]/2 concentração de Km Se a concentração de é eleada quase todas as moléculas de [E S] [Etotal] k cat [Etotal] concentração de é saturante (3) da afinidade entre a enzima e o seu Se [S] < K m é quase proporcional a [S]...e menos de metade das moléculas de A actiidade enzímica para concentração saturante de... se a concentração de é eleada ariações moderadas na concentração do não afectam a actiidade para dosear enzimas é frequente usarem-se concentrações eleadas de porque o gráfico produto formado ersus tempo se mantém linear durante mais tempo. Se [S] K m / 2...e a enzima está hemisaturada 23 A partir da equação...pode deduzir-se o alor de para determinadas concentrações de. Km >> [S]... se Km>>[S] denominador Km [S] Km Km << [S] [ S] +... se Km<<[S] denominador [S] S [ ] 2 Km é directamente proporcional a [S] para baixas concentrações de S... se Km[S] denominador 2 [S] 2 não é afectado por 24[S] para altas concentrações de S
2 O Km é uma medida da afinidade da enzima para o seu...quando maior o alor do Km menor a afinidade e ie-ersa. O Km mede a afinidade da enzima para o seu 12...quando maior o alor do Km menor a afinidade. (mm) A enzima azul precisa de uma concentração de menor para ficar hemisaturada......porque tem maior afinidade para o que a enzima cinzenta. Em ambos os casos a enzima está hemisaturada Km < Km 25 A enzima azul já está hemisaturada ([E S][Et]/2) quando [S] 3 mm (Km 3 mm) tem alta afinidade para o A enzima ermelha está hemisaturada ([E S][Et]/2) quando [S] 1 mm (Km 1 mm) tem baixa afinidade para o 26 Estudar o alor do K m sere para caracterizar uma enzima mas também pode serir para compreender a sua regulação in io. 1- Duas isoenzimas podem distinguir-se por alores distintos no K m do (caso da hexocínase muscular e glicocínase hepática...). hexocínase muscular glicocínase hepática Em alguns casos foi possíel estudar in io a ariação da actiidade de enzimas com a concentração do. Num estudo de Brindle et al. (1989) estimulou-se electricamente o nero ciático de ratos e mediu-se, na musculatura da perna, por NMR (1) a concentração de ADP e (2) a incorporação de Pi no ATP (síntase do ATP). Alta actiidade contráctil Se o alor das concentrações fisiológicas do (in io; na célula) é conhecida, a comparação com o alor do K m Baixa actiidade contráctil...pode serir para estimar o efeito das ariações fisiológicas da concentração do 27 na actiidade da enzima. Brindle et al. (1989) Biochemistry 28:
3 Quando se estuda o efeito da concentração de na actiidade de algumas enzimas e se representa ersus [S] o gráfico pode ser não uma hipérbole mas um sigmóide. As teorias actualmente mais aceites para interpretar este tipo de comportamento cinético surgiram na década de 6 e isaam interpretar um fenómeno semelhante: a forma sigmoide do gráfico de saturação da hemoglobina. Essas teorias reelaram-se adequadas para interpretar as cinéticas de tipo sigmoide em enzimas com mais de um local de ligação ao por molécula de enzima (enzimas poliméricas). 29 A actiidade das enzimas pode ser diminuída ou aumentada pela adição ao sistema de ensaio de modificadores da actiidade enzímica (inibidores e actiadores). Adicionando a um meio de ensaio uma substância M (inibidor ou actiador) e mantendo constantes todas as outras condições de ensaio podemos obter diminuição (inibição) ou aumento (actiação) da actiidade enzímica. na ausência de inibidor 1 UI 3 UI Grau de inibição 3% Actiidade enzímica Grau de inibição ou grau de actiação inicial } o +inibidor o{ inicial na ausência de M +actiador 3 Um estudo mais aprofundado do efeito de um inibidor na actiidade duma enzima pode reelar que ele aumenta o K m do sem modificar. Quando se estuda a actiidade enzímica para ários alores de [S] podemos, multiplicando o número de tubos de ensaios, fazer esse estudo: na ausência e na presença de um inibidor I. Para explicar o comportamento deste sistema (I aumento do K m mas I não afecta ) poderemos admitir que o inibidor I e o S se ligam no centro actio da enzima competindo entre si. Algumas ezes obsera-se que: 1- Na presença do inibidor o alor de não se modifica; para concentrações de eleadas o inibidor I não tem efeito. O alor do K m obserado é maior na presença de I que na sua ausência; o grau de inibição é mais marcado para concentrações de baixas. Nestes casos falamos de inibição competitia Para [S] 4 grau inibição 5% 31 As possibilidades do modelo apresentado corresponder à realidade são reforçadas se as estruturas moleculares do e do inibidor forem semelhantes. O malonato compete com o succinato na 32 actiidade da desidrogénase do succinato
4 Um inibidor competitio aumenta o Km do com o qual compete se o inibidor está presente, para obter hemisaturação da enzima com, preciso de ter maior concentração do. O anadato é um inibidor competitio da fosfátase alcalina. sem anadato /2 anadato 2,5 µm Na ausência de inibidor esta concentração de permitia hemisaturação. O Km era 9. Mas na presença do inibidor para esta concentração de só 1/6 das moléculas de. Na presença do inibidor competitio preciso de aumentar a concentração de para 32 para obter hemisaturação com o. Na presença do inibidor 33 o Km (que era 9) aumentou para 32. Km (sem anadato) 1,1 mm Km (com anadato) 7,6 mm Seargeant & Stinson (1979) Biochem J. 181: 247. O anadato (HO 4 ) se adicionado a meios de ensaio que contenham paranitrofenilfosfato e fosfátase alcalina inibe a actiidade da enzima. 34 A inibição é de tipo competitio. H 2 O Quando se estuda de efeito de um inibidor para diferentes concentrações de podemos, eentualmente, obserar que a inibição não é de tipo competitio. Algumas ezes obsera-se que: A fosfátase alcalina catalisa a hidrólise do para-nitrofenilfosfato: para-nitrofenilfosfato + H 2 O para-nitrofenol + HPO 4 O anadato (HO 4 ) é um análogo estrutural do fosfato inorgânico (contém anádio em ez de fósforo). O fosfato é um produto da reacção e um dos resíduos do. O anadato (tal como o fosfato inorgânico) é um inibidor da fosfátase alcalina porque se liga no centro actio da enzima impedindo a ligação do. A ligação entre o anadato e a enzima não é de tipo coalente: o anadato liga-se à enzima por interacções de tipo electrostático e as formas ligada e desligada da enzima encontram-se em equilíbrio. Se se aumentar a concentração de mantendo a concentração de anadato a probabilidade de uma molécula de enzima se ligar ao aumenta enquanto a probabilidade de se ligar ao anadato diminui. No limite, para muito altas concentrações de o anadato deixa de ter efeito inibidor. O anadato é um inibidor competitio da fosfátase alcalina porque compete com o paranitrofenilfosfato para sua ligação à 35 enzima. 1- O é menor na presença de I que na sua ausência. Na presença de I o K m não se modifica; a concentração de para a qual se obsera um alor de actiidade que é metade de (ou de ) é igual na presença e na ausência de I. 3-O grau de inibição é independente da concentração de. No exemplo o grau de inibição 4% para todas as concentrações de Nestes casos diz-se que a inibição é não competitia. 36
5 Um modelo possíel para explicar a inibição de tipo não competitio é admitir a existência na enzima de um local de ligação diferente do centro actio cuja ligação ao inibidor impedisse a formação do produto. A par da classificação que diide os inibidores em competitios e não competitios existe uma outra que diide os modificadores (inibidores ou actiadores) em isostéricos ou alostéricos. Um modificador isostérico liga-se ao centro actio e é sempre inibidor: é um inibidor isostérico. Um ligando alostérico liga-se à enzima num sítio diferente do centro actio (um sítio alostérico) proocando uma alteração conformacional na enzima. Sítios alostéricos Inibidor alostérico Se a alteração conformacional diminuir a actiidade da enzima dizemos que há inibição alostérica. De acordo com este modelo tudo se passaria como se as moléculas de enzima ligadas ao inibidor estiessem excluídas do processo catalítico, isto é, a concentração de enzima tiesse baixado. 37 Actiador alostérico Se a alteração conformacional aumentar a actiidade da enzima dizemos que há actiação 38 alostérica. Quando uma fibra muscular se contrai aumenta a elocidade de hidrólise do ATP e aumenta a concentração de ADP (e AMP; 2 ADP AMP + ATP). O AMP liga-se à fosforílase muscular induzindo uma conformação mais actia o AMP é um actiador alostérico da fosforílase muscular. Fosforílase muscular na conformação tensa (inactia) AMP sítio alostérico Fosforílase muscular na conformação relaxada (actia) A cínase-1 da frutose-6-p (ATP+ Frutose-6-P ADP + Frutose-1,6-bisfosfato) o ATP é, simultaneamente, e inibidor alostérico. Para concentrações fisiológicas de ATP, o AMP é um actiador alostérico. (3) O AMP compete com o ATP pelo mesmo sítio alostérico impedindo a sua acção inibidora. AMP centro actio 39 (1) Um dos s da cínase da frutose-6-p é o ATP. (2) Contudo, existe na enzima um sítio alostérico onde o ATP se liga inibindo-a. Para concentrações fisiológicas de ATP essa acção inibidora é muito 4 marcada.
A velocidade das reacções enzímicas in vivo e in vitro
 A elocidade das reacções enzímicas in io e in itro Conceitos de de ia metabólica, coenzima, grupo prostético e cofactor. Os conceitos de da ia metabólica e coenzima só têm sentido se analisamos uma ia
A elocidade das reacções enzímicas in io e in itro Conceitos de de ia metabólica, coenzima, grupo prostético e cofactor. Os conceitos de da ia metabólica e coenzima só têm sentido se analisamos uma ia
[ S] [ S] se fizermos ensaios nas mesmas condições (temperatura, ph,
![[ S] [ S] se fizermos ensaios nas mesmas condições (temperatura, ph, [ S] [ S] se fizermos ensaios nas mesmas condições (temperatura, ph,](/thumbs/62/47257897.jpg) Quando se quer quantificar a atiidade de uma enzima adicionamos num tubo de ensaio a enzima ao(s) (s) e amos obserando ao longo do tempo como eolui a reação. Produto (micromoles) 1.5 1.5 Acumulação de
Quando se quer quantificar a atiidade de uma enzima adicionamos num tubo de ensaio a enzima ao(s) (s) e amos obserando ao longo do tempo como eolui a reação. Produto (micromoles) 1.5 1.5 Acumulação de
Estudar as enzimas in vitro (no tubo de ensaio) para quê?
 Estudar as enzimas in itro (no tubo de ensaio) para quê? A) O estudo das enzimas é muito útil em análises clínicas A) O enzimas na inestigação A1 - Doseamentos de enzimas plasmáticas (algumas enzimas só
Estudar as enzimas in itro (no tubo de ensaio) para quê? A) O estudo das enzimas é muito útil em análises clínicas A) O enzimas na inestigação A1 - Doseamentos de enzimas plasmáticas (algumas enzimas só
Estudar as enzimas in vitro (no tubo de ensaio) para quê?
 Estudar as enzimas in itro (no tubo de ensaio) para quê? A) O estudo das enzimas é muito útil em análises clínicas A) O estudo das enzimas é muito útil em inestigação A - Doseamentos de enzimas plasmáticas
Estudar as enzimas in itro (no tubo de ensaio) para quê? A) O estudo das enzimas é muito útil em análises clínicas A) O estudo das enzimas é muito útil em inestigação A - Doseamentos de enzimas plasmáticas
Cinética e regulação enzímicas (a velocidade das reações enzímicas in vitro e in vivo)
 Cinética e regulação enzímicas (a elocidade das reações enzímicas in itro e in io) Conceitos de substrato de ia metabólica, coenzima, grupo prostético e cofator. Ácido ATP gordo AMP + PPi CoASH Acil-CoA
Cinética e regulação enzímicas (a elocidade das reações enzímicas in itro e in io) Conceitos de substrato de ia metabólica, coenzima, grupo prostético e cofator. Ácido ATP gordo AMP + PPi CoASH Acil-CoA
Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) rui.fontes@mail.telepac.pt Laboratório de Bioquímica da Faculdade de edicina do Porto 1 As concentrações dos intermediários
Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) rui.fontes@mail.telepac.pt Laboratório de Bioquímica da Faculdade de edicina do Porto 1 As concentrações dos intermediários
Hidrólise da ureia pela urease
 Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) rui.fontes@mail.telepac.pt Laboratório de Bioquímica da Faculdade de Medicina do Porto 1 As concentrações dos intermediários
Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) rui.fontes@mail.telepac.pt Laboratório de Bioquímica da Faculdade de Medicina do Porto 1 As concentrações dos intermediários
Cinética e regulação enzímicas (a velocidade das reações enzímicas in vivo e in vitro)
 Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofator. Cinética e regulação enzímicas (a velocidade das reações enzímicas in vivo e in vitro) ruifonte@med.up.pt Departamento de
Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofator. Cinética e regulação enzímicas (a velocidade das reações enzímicas in vivo e in vitro) ruifonte@med.up.pt Departamento de
São moléculas catalíticas protéicas (exceto algumas que são RNA) - Prefixo que designa a reação: lactato desidrogenase, catalase
 1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
A actividade das enzimas e a sua regulação
 A actividade das enzimas e a sua regulação 1- A actividade das enzimas cujas reacções são fisiologicamente irreversíveis regula a velocidade de fluxo nas vias metabólicas onde intervêm Numa determinada
A actividade das enzimas e a sua regulação 1- A actividade das enzimas cujas reacções são fisiologicamente irreversíveis regula a velocidade de fluxo nas vias metabólicas onde intervêm Numa determinada
Cinética e regulação enzímicas (a velocidade das reações enzímicas in vivo e in vitro)
 Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofator. Cinética e regulação enzímicas (a velocidade das reações enzímicas in vivo e in vitro) ruifonte@med.up.pt Departamento de
Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofator. Cinética e regulação enzímicas (a velocidade das reações enzímicas in vivo e in vitro) ruifonte@med.up.pt Departamento de
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Enzimas que ultrapassam o limite difusivo
 Enzimas que ultrapassam o limite difusio Em certas condições é possíel obserar eficiências catalíticas superiores ao limite difusional do substrato e enzima. 1 - Canalização de substratos: Enzima 1 Enzima
Enzimas que ultrapassam o limite difusio Em certas condições é possíel obserar eficiências catalíticas superiores ao limite difusional do substrato e enzima. 1 - Canalização de substratos: Enzima 1 Enzima
Cinética enzimática. Cinética enzimática. Cinética enzimática 20/03/2012. Classificação sistemática das enzimas
 Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro)
 Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) ruifonte@med.up.pt Laboratório de
Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) ruifonte@med.up.pt Laboratório de
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS. Enzimas. Prof. Me. Cássio Resende de Morais
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro)
 Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) rui.fontes@mail.telepac.pt Laboratório
Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Cinética e regulação enzímicas (a velocidade das reacções enzímicas in vivo e in vitro) rui.fontes@mail.telepac.pt Laboratório
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores
 Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Enzimas. Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Enzimas e Actividade enzimática
 Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
O 2 CO 2 + H 2 O. Absorção da glicose, glicólise e desidrogénase do piruvato. ADP + Pi. nutrientes ATP
 Absorção da glicose, glicólise e desidrogénase do piruvato Em todas as células ocorre continuamente a hidrólise do ATP (formando ADP + a uma velocidade tal que, mesmo em repouso, todo o stock de ATP se
Absorção da glicose, glicólise e desidrogénase do piruvato Em todas as células ocorre continuamente a hidrólise do ATP (formando ADP + a uma velocidade tal que, mesmo em repouso, todo o stock de ATP se
ENZIMAS. Dra. Flávia Cristina Goulart. Bioquímica
 ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13
 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Biossíntese e degradação de glicogênio. Integração entre o controle da glicólise e da glicogenólise em diferentes tipos celulares
 Biossíntese e degradação de glicogênio Regulação da via glicolítica Integração entre o controle da glicólise e da glicogenólise em diferentes tipos celulares O glicogênio é o polissacarídio de reserva
Biossíntese e degradação de glicogênio Regulação da via glicolítica Integração entre o controle da glicólise e da glicogenólise em diferentes tipos celulares O glicogênio é o polissacarídio de reserva
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias.
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
A actividade das enzimas e o seu controlo na regulação do fluxo das vias metabólicas
 A actividade das enzimas e o seu controlo na regulação do fluxo das vias metabólicas Índice 1. A actividade das enzimas cujas reacções são fisiologicamente reversíveis é controlada pelas concentrações
A actividade das enzimas e o seu controlo na regulação do fluxo das vias metabólicas Índice 1. A actividade das enzimas cujas reacções são fisiologicamente reversíveis é controlada pelas concentrações
2- No dia estavam classificadas 4046 enzimas que podem ser consultadas em
 A maioria das enzimas são de natureza proteica e, relativamente aos outros catalisadores, têm uma grande especificidade em relação aos substratos e produtos da reacção. 1- A palavra enzima (do Grego: en,
A maioria das enzimas são de natureza proteica e, relativamente aos outros catalisadores, têm uma grande especificidade em relação aos substratos e produtos da reacção. 1- A palavra enzima (do Grego: en,
Proteínas II. (Enzimas) Bioquímica Prof. Dr. Marcelo Soares
 Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
DETERMINAÇÃO DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTOS DE CÉLULAS DE LEVEDURA. Glucose + 2Pi + 2ADP + 2NAD! 2CH COCOO " 2ATP " 2NADH " 2 H
 DETERMINAÇÃ DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTS DE CÉLULAS DE LEVEDURA 1. Introdução A glicólise é um caminho metabólico quase universal no qual a glucose é convertida em piruvato com síntese
DETERMINAÇÃ DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTS DE CÉLULAS DE LEVEDURA 1. Introdução A glicólise é um caminho metabólico quase universal no qual a glucose é convertida em piruvato com síntese
Enzimas - Sítio catalítico
 Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Enzimas versus outros catalisadores
 Enzimas versus outros catalisadores Catalisadores proteicos Elevados factores de aceleração das reacções Grande especificidade para os substratos Estereo-especificidade (também absoluta) Reduzido número
Enzimas versus outros catalisadores Catalisadores proteicos Elevados factores de aceleração das reacções Grande especificidade para os substratos Estereo-especificidade (também absoluta) Reduzido número
Aula de Bioquímica II SQM Fosforilação Oxidativa
 Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM
Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM
Conceitos de cinética enzimática e modelos clássicos de inibição enzimática
 Conceitos de cinética enzimática e modelos clássicos de inibição enzimática Índice 1 Conceitos básicos de cinética química.... 1 2 Natureza química das enzimas e modelos de interação com os seus substratos....
Conceitos de cinética enzimática e modelos clássicos de inibição enzimática Índice 1 Conceitos básicos de cinética química.... 1 2 Natureza química das enzimas e modelos de interação com os seus substratos....
1- Microrganismos e indústria alimentar 1.1 Fermentação e actividade enzimática
 Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
Exemplos: Exemplos: Síntase da hidroxi-metil-glutaril-coa
 A palavra síntase (não confundir com sintétase) está popularmente associado a algumas enzimas e as síntases podem pertencer a diferentes classes. Algumas vezes o nome que foi originalmente atribuído a
A palavra síntase (não confundir com sintétase) está popularmente associado a algumas enzimas e as síntases podem pertencer a diferentes classes. Algumas vezes o nome que foi originalmente atribuído a
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Catálise Enzimática. Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química.
 Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Aula INIBIÇÃO E REGULAÇÃO ENZIMÁTICA
 INIBIÇÃO E REGULAÇÃO ENZIMÁTICA META Entender como os inibidores enzimáticos e a regulação enzimática interferem na velocidade das reações enzimáticas. OBJETIVOS Ao final desta aula, o aluno deverá: definir
INIBIÇÃO E REGULAÇÃO ENZIMÁTICA META Entender como os inibidores enzimáticos e a regulação enzimática interferem na velocidade das reações enzimáticas. OBJETIVOS Ao final desta aula, o aluno deverá: definir
Sistemas de controle da transcrição gênica. Procariotos
 Sistemas de controle da transcrição gênica Procariotos Controle Positivo e Negativo: Há dois tipos de controle transcricional: Controle negativo: no qual uma proteína reguladora atua como um repressor
Sistemas de controle da transcrição gênica Procariotos Controle Positivo e Negativo: Há dois tipos de controle transcricional: Controle negativo: no qual uma proteína reguladora atua como um repressor
ENZIMAS CINÉTICA ENZIMÁTICA. Classificação. Natureza da reação catalisada. Disponibilidade comercial IMPORTÂNCIA INDUSTRIAL OBJETIVOS
 OBJETIO Medir as elocidades de transforação CINÉTICA ENZIMÁTICA Aaliar a influência de condições de reação (conc. de reagentes, enzias, teperatura, ph, etc..) nas elocidades de reação Correlacionar atraés
OBJETIO Medir as elocidades de transforação CINÉTICA ENZIMÁTICA Aaliar a influência de condições de reação (conc. de reagentes, enzias, teperatura, ph, etc..) nas elocidades de reação Correlacionar atraés
Revisão do Metabolismo da Glicose
 Gliconeogênese Revisão do Metabolismo da Glicose Esquema Geral da Glicólise lise 1 açúcar de 6 C 2 açúcares de 3 C A partir deste ponto as reações são duplicadas 2 moléculas de Piruvato (3C) Saldo 2 moléculas
Gliconeogênese Revisão do Metabolismo da Glicose Esquema Geral da Glicólise lise 1 açúcar de 6 C 2 açúcares de 3 C A partir deste ponto as reações são duplicadas 2 moléculas de Piruvato (3C) Saldo 2 moléculas
Respiração Celular. Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico. Prof. Ana Paula Jacobus
 Respiração Celular Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico Prof. Ana Paula Jacobus GLICOSE VIAS LINEARES (glicólise e gliconeogênese) PIRUVATO Ciclo do ácido cítrico ou
Respiração Celular Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico Prof. Ana Paula Jacobus GLICOSE VIAS LINEARES (glicólise e gliconeogênese) PIRUVATO Ciclo do ácido cítrico ou
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 581-
 Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos
 A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos mesmo quando (por razões de índole termodinâmica) apenas a reacção em que ocorre formação de ATP pode
A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos mesmo quando (por razões de índole termodinâmica) apenas a reacção em que ocorre formação de ATP pode
Problemas sobre o doseamento da actividade de enzimas
 Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
Gliconeogénese e Metabolismo do Glicogénio
 Página 1 de 5 Aulas de grupo 2001-02; Rui Fontes Gliconeogénese e Metabolismo do Glicogénio 1- Gliconeogénese 1- A gliconeogénese é um termo usado para incluir o conjunto de processos pelos quais o organismo
Página 1 de 5 Aulas de grupo 2001-02; Rui Fontes Gliconeogénese e Metabolismo do Glicogénio 1- Gliconeogénese 1- A gliconeogénese é um termo usado para incluir o conjunto de processos pelos quais o organismo
Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global.
 ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
Visão geral do metabolismo glicídico
 Visão geral do metabolismo glicídico 1. Todas as células do organismo podem usar glicose oxidando-a (processo exergónico) de forma acoplada com a formação de (processo endergónico). a) O catabolismo da
Visão geral do metabolismo glicídico 1. Todas as células do organismo podem usar glicose oxidando-a (processo exergónico) de forma acoplada com a formação de (processo endergónico). a) O catabolismo da
Aula de Bioquímica II. Fosforilação Oxidativa
 Aula de Bioquímica II Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo
Aula de Bioquímica II Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo
Enzimas Alostéricas e com Múltiplos Sítios Ativos
 Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Enzimas revisões. v o = V max [S] K m + [S]
![Enzimas revisões. v o = V max [S] K m + [S] Enzimas revisões. v o = V max [S] K m + [S]](/thumbs/67/57975399.jpg) nzimas revisões k 1 k + 3 + S k 2 S P v o = V max [S] K m + [S] quação de Michaelis-Menten V max é o valor para o qual tende a velocidade à medida que se aumenta a concentração de substrato; corresponde
nzimas revisões k 1 k + 3 + S k 2 S P v o = V max [S] K m + [S] quação de Michaelis-Menten V max é o valor para o qual tende a velocidade à medida que se aumenta a concentração de substrato; corresponde
QBQ 0102 Educação Física. Carlos Hotta. Enzimas 17/03/15
 QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
Glicogênio. Glicogênese. Glicogenólise. Glicose-6-fosfato. Glicólise. Gliconeogênese. Lactato
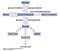 Glicogênio Glicogenólise Glicogênese Glicose-6-fosfato Glicólise Gliconeogênese Lactato Glicogênio: : polissacarídeo de reserva nas células animais hepatócito Glicogênio Principal polissacarídeo de reserva
Glicogênio Glicogenólise Glicogênese Glicose-6-fosfato Glicólise Gliconeogênese Lactato Glicogênio: : polissacarídeo de reserva nas células animais hepatócito Glicogênio Principal polissacarídeo de reserva
Aula 12: Enzimas Introdução e Cinética
 Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Biologia 12 Fermentação e actividade enzimática
 Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
Resumo esquemático da glicólise
 Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Enzimas regulatórias no controle do metabolismo 1
 Enzimas regulatórias no controle do metabolismo 1 1. Introdução A regulação do metabolismo é fundamental para que um organismo possa responder de modo rápido e eficiente a variações das condições ambientais,
Enzimas regulatórias no controle do metabolismo 1 1. Introdução A regulação do metabolismo é fundamental para que um organismo possa responder de modo rápido e eficiente a variações das condições ambientais,
Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional.
 Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional. A reacção de oxidação dos nutrientes pelo O 2 tem uma constante de equilíbrio tão elevada (>10 450 ) que tem tendência
Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional. A reacção de oxidação dos nutrientes pelo O 2 tem uma constante de equilíbrio tão elevada (>10 450 ) que tem tendência
As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos
 Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula!
 Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Acetil CoA e Ciclo de Krebs. Prof. Henning Ulrich
 Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
2 APLICAÇÕES INDUSTRIAIS Tabela 1: Enzimas aplicadas na indústria APLICAÇÃO ENZIMA
 CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA TEÓRICO-PRÁTICA
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA TEÓRICO-PRÁTICA
Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2011
 Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2011 Funções da Via Glicolítica Gerar ATP (rápido); Gerar intermediários para síntese; Regenerar NADH; 2 ATP em anaerobiose Rendimento
Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2011 Funções da Via Glicolítica Gerar ATP (rápido); Gerar intermediários para síntese; Regenerar NADH; 2 ATP em anaerobiose Rendimento
Aula de Bioquímica I. Tema: Cinética Enzimática. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Cinética Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física olecular DQF Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Cinética Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física olecular DQF Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
[ A][ B] [ A] [ B] v {[A] }= Vmáx
![[ A][ B] [ A] [ B] v {[A] }= Vmáx [ A][ B] [ A] [ B] v {[A] }= Vmáx](/thumbs/75/72105322.jpg) Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
ENZIMAS ENZIMAS ENZIMAS ENZIMAS ENZIMAS 31/03/2018. PROFº STUART - 1 TEORIA DA CATÁLISE A + B DEFINIÇÃO
 DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
Organelas Transdutoras de Energia: Mitocôndria - Respiração
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
Enzimas. Bianca Zingales IQ - USP
 Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Metabolismo e Regulação
 Metabolismo e Regulação PRBLEMAS - Série 1 Soluções 2009/2010 idratos de Carbono (Revisão) e Metabolismo Central 1 R: (α 1 4) (lineares) Ο (α1 6) (pontos de ramificação) 2. R: Locais de glicosilação são
Metabolismo e Regulação PRBLEMAS - Série 1 Soluções 2009/2010 idratos de Carbono (Revisão) e Metabolismo Central 1 R: (α 1 4) (lineares) Ο (α1 6) (pontos de ramificação) 2. R: Locais de glicosilação são
ENZIMAS ENZIMAS ENZIMAS 19/02/17 DEFINIÇÃO CLASSIFICAÇÃO ESTRUTURAL. ativa. inativa
 DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
 CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
Concentração aproximada de alguns elementos (na forma de íons metálicos) no exterior e interior das células -
 Concentração aproximada de alguns elementos (na forma de íons metálicos) no exterior e interior das células - sistemas de transporte de íons metálicos Elemento água do mar plasma sanguíneo citoplasma Na
Concentração aproximada de alguns elementos (na forma de íons metálicos) no exterior e interior das células - sistemas de transporte de íons metálicos Elemento água do mar plasma sanguíneo citoplasma Na
Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional.
 Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional. rui.fontes@mail.telepac.pt s vias metabólicas existem porque existem enzimas que têm especificidade para substratos
Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional. rui.fontes@mail.telepac.pt s vias metabólicas existem porque existem enzimas que têm especificidade para substratos
objetivo Ciclo da uréia Pré-requisito Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia.
 Ciclo da uréia A U L A 18 objetivo Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia. Pré-requisito Conhecimentos adquiridos na Aula 17. BIOQUÍMICA II Ciclo da uréia
Ciclo da uréia A U L A 18 objetivo Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia. Pré-requisito Conhecimentos adquiridos na Aula 17. BIOQUÍMICA II Ciclo da uréia
A atividade das enzimas e o seu controlo na regulação do fluxo das vias metabólicas
 A atividade das enzimas e o seu controlo na regulação do fluxo das vias metabólicas Índice 1. A atividade das enzimas cujas reações são fisiologicamente reversíveis é controlada pelas concentrações dos
A atividade das enzimas e o seu controlo na regulação do fluxo das vias metabólicas Índice 1. A atividade das enzimas cujas reações são fisiologicamente reversíveis é controlada pelas concentrações dos
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 10ª aula teórica 19 Outubro 2010 Príncipios gerais de enzimologia. Modo de acção das enzimas. Cinética enzimática (Eq. Michaelis-Menten; K M e V max
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 10ª aula teórica 19 Outubro 2010 Príncipios gerais de enzimologia. Modo de acção das enzimas. Cinética enzimática (Eq. Michaelis-Menten; K M e V max
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa
 Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
ENZIMAS. Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica. Prof.: Me.
 Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
Esquema simplificado da fermentação láctica
 BIOLOGIA 12º ANO ANO LECTIVO 2008/2009 NOME DO ALUNO PROFESSORA: Isabel Dias N.º Classificação: Teste 4 1. Analise os documentos 1 e 2, que se referem ao processo de fermentação utilizado na produção de
BIOLOGIA 12º ANO ANO LECTIVO 2008/2009 NOME DO ALUNO PROFESSORA: Isabel Dias N.º Classificação: Teste 4 1. Analise os documentos 1 e 2, que se referem ao processo de fermentação utilizado na produção de
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008. Disciplina de BIOQUÍMICA I Curso de MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Enzimologia Aula 2. Leitura sugerida. Biochemistry Voet & Voet 3ª edição Capítulo 10 parte 1Bb (página 323), parte 4A, 4B e 4C (páginas )
 Enzimologia Aula 2 Leitura sugerida Biochemistry Voet & Voet 3ª edição Capítulo 10 parte 1Bb (página 323), parte 4A, 4B e 4C (páginas 346-350) Structure and Mechanism in Protein Science Alan Fersht 1999
Enzimologia Aula 2 Leitura sugerida Biochemistry Voet & Voet 3ª edição Capítulo 10 parte 1Bb (página 323), parte 4A, 4B e 4C (páginas 346-350) Structure and Mechanism in Protein Science Alan Fersht 1999
Produção de alimentos e sustentabilidade
 Bio12 Unidade 4 e sustentabilidade Como produzir maiores quantidades de alimentos para resolver os problemas de alimentação? Capítulo 1.1. Fermentação e atividade enzimática Que fatores condicionam a atividade
Bio12 Unidade 4 e sustentabilidade Como produzir maiores quantidades de alimentos para resolver os problemas de alimentação? Capítulo 1.1. Fermentação e atividade enzimática Que fatores condicionam a atividade
Membrana interna. Cristas. Matriz Membrana externa. P i P i P i. 7,3 kcal/mol 7,3 kcal/mol 3,4 kcal/mol
 BIEERGÉTIA a célula milhares de compostos estão a ser sintetizados e degradados em simultâneo. Metabolismo: é o conjunto de todas as reacções envolvidas na manutenção deste estado dinâmico. o geral as
BIEERGÉTIA a célula milhares de compostos estão a ser sintetizados e degradados em simultâneo. Metabolismo: é o conjunto de todas as reacções envolvidas na manutenção deste estado dinâmico. o geral as
Mecanismos de catálise enzimática
 Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
Introdução e apresentação geral do metabolismo da glicose
 Introdução e apresentação geral do metabolismo da glicose Índice 1- O transporte transmembranar e a fosforilação da glicose...1 2- A glicólise e a oxidação da glicose a CO 2...1 3- A oxidação da glicose-6-fosfato
Introdução e apresentação geral do metabolismo da glicose Índice 1- O transporte transmembranar e a fosforilação da glicose...1 2- A glicólise e a oxidação da glicose a CO 2...1 3- A oxidação da glicose-6-fosfato
Inibidores Enzimáticos
 Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
Página 1 de 8. 1 Elaborar um protocolo experimental adequado ao assunto em estudo estudo de uma enzima.
 Página 1 de 8 ACTIVIDADE LABORATORIAL BIOLOGIA 12º Ano O que se pretende 1 Elaborar um protocolo experimental adequado ao assunto em estudo estudo de uma enzima. 2 Seleccionar material adequado ao estudo
Página 1 de 8 ACTIVIDADE LABORATORIAL BIOLOGIA 12º Ano O que se pretende 1 Elaborar um protocolo experimental adequado ao assunto em estudo estudo de uma enzima. 2 Seleccionar material adequado ao estudo
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
