Spin e Princípio de exclusão de Pauli
|
|
|
- Valdomiro Capistrano Meneses
- 7 Há anos
- Visualizações:
Transcrição
1 10 AULA Spin e Princípio de exclusão de Pauli
2 Spin e Princípio de exclusão de Pauli METAS: Introduzir o spin. Introduzir o formalismo utilizado na descrição de spin 1/2. Introduzir o Princípio de exclusão. Introduzir os princípios da descrição de átomos de muitos elétrons. OBJETIVOS: Ao fim da aula os alunos deverão ser capazes de: resolver problemas que envolvem o spin do elétron; utilizar o Princípio de exclusão; introduzir o conceito de configuração eletrônica para átomos de muitos elétrons; PRÉ-REQUISITOS: formalismo da mecânica quântica. Momento angular. Átomos de um elétron. 188
3 Introdução a Mecânica Quântica 10.1 Introdução A existência do spin do elétron um momento angular intrínseco que não se exprime em termos das coordenada da partícula e dos componentes do momento linear hoje é um fato bem conhecido. O spin foi proposto e, depois, introduzido na mecânica quântica para explicar os resultados da experiência de Stern e Gerlach. Porem, a descoberta do spin tornou possível a formulação de um dos princípios mais importantes da física: o Princípio de exclusão. Este princípio explica, no contexto da mecânica quântica, as configurações eletrônicas dos átomos de muitos elétrons e, deste modo, as propriedades químicas dos elementos e a tabela periódica. 10 AULA Uma série de experiências realizada por Otto Stern e Walter Gerlach em 1922 mostrou certas características inesperadas do momento magnético de alguns átomos. Mas o que é o momento magnético na mecânica quântica? 10.2 Momento magnético e spin Momento magnético Consideremos uma espira plana que carrega uma corrente elétrica I. Um campo magnético B exerce sobre a espira I B um torque τ dado por τ = µ B, (10.1) onde o momento magnético da espira µ é A Figura 10.1: Momento magnético de uma espira carregando uma corrente. µ = IA, (10.2) sendo A um vetor normal ao plano da espira e cujo módulo é igual à área limitada pela espira. 189
4 Spin e Princípio de exclusão de Pauli Uma partícula carregada clássica de massa m e carga q, movendo se com velocidade v ao longo de uma órbita circular de raio r, é equivalente a uma corrente I = q v 2πr, portanto, o módulo do memento magnético associado à partícula é igual a e o momento magnético é µ = IA = q v 2πr πr2 = q 2 vr µ = q 2m r p = q L, (10.3) 2m onde L é o momento angular da partícula. Assumimos que o operador do momento magnético do átomo do hidrogênio é dado por ˆµ = e 2m e ˆL. (10.4) Sendo proporcional ao momento angular, o momento magnético é quantizado. Os valores possíveis do módulo µ do momento magnético são onde l é o número quântico do momento angular e µ = µ B l(l+1), (10.5) µ B = e 2m e (10.6) e chamado magneton de Bohr. Os componentes do momento magnético também são quantizados. Para um dado valor l do número quântico do momento angular os valores possíveis de µ z, por exemplo 45, são µ z = µ B m l, m = l, l+1,...,l. (10.7) Substituindo os valores das constantes, obtemos para o magneton de Bohr µ B = 5, ev/t = 9, A m 2. (10.8) 45 Os valores possíveis de S x e S y são os mesmos, claro. No entanto, os observáveis S z e S x, por exemplo, não são compatíveis. 190
5 Introdução a Mecânica Quântica O átomo se comporta como um dipolo magnético. Na presença de um campo magnético B, a energia potencial associada à interação do campo com um dipolo magnético clássico á igual a 10 AULA V B = µ B. (10.9) Se o campo não e uniforme, a força exercida sobre o dipolo, F = (µ B) não é igual a zero. Voltando ao átomo do hidrogênio: na presença de um campo magnético B é necessário incluir no hamiltoniano o termo adicional Ĥ B = e 2m e ˆL ˆB, (10.10) onde os ˆB x, ˆB y, ˆB z são os operadores de multiplicação por B x, B y, B z, respectivamente. A ordem dos operadores na equação (10.10) não tem importância. Com efeito, ˆL ˆB = ˆB ˆL, porque o campo magnético satisfaz a equação B = A experiência da Stern-Gerlach z S Spin para cima x y N Imã Spin para baixo Figura 10.2: A experiência de Stern-Gerlach. 191
6 Spin e Princípio de exclusão de Pauli Em experiências, realizadas por Otto Stern e Walter Gerlach em 1922, foram feitas medidas do momento magnético de átomos de prata. Um desenho As experiências de Stern-Gerlach foram realizadas em 1922, isto é, antes do desenvolvimento da mecânica quântica. Mas a quantização do momento angular era conhecida na teoria de Sommerfeld-Wilson. da experiência é mostrado na Figura S N Figura 10.3: Seção transversal dos polos do imã na experiência de Stern-Gerlach. na saída do aparelho. Um feixe de átomos de prata atravessam a região entre os polos de um imã. Devido à forma dos polos, mostrada na Figura 10.3, o campo magnético na região não é constante e Bz z > 0. Os átomos com valor positivo do componente µ z do momento magnético são deflexionados para cima e os átomos com µ z negativo são deflexionados para baixo. Os átomos com µ z = 0 não sofrerão deflexão. Qualquer que seja o valor do número quântico l, na saída do aparelho terá um número impar de feixes de átomos, porque o número dos possíveis valores do número quântico magnético é igual a 2l+1, um número impar. Porém, foi observado um número par de feixes Spin Não foi só a experiência de Stern-Gerlach. Contribuíram para o surgimento da hipótese do spin análises do efeito Zeeman (desdobramento de linhas espectrais em um campo magnético) e as ideias teóricas de Wolfgang Pauli sobre o princípio de exclusão. A necessidade de um novo número quântico levou, em 1925, à hipótese do spin de George Eugene Uhlenbeck e Samuel Abraham Goudsmit. Logo depois, o spin foi incorporado no formalismo da mecânica quântica. O spin do elétron é um momento angular que existe independentemente do estado de movimento no qual a partícula se encontra. O número quântico 192
7 Introdução a Mecânica Quântica do spin s para o elétron é igual a 1/2. O módulo do spin é igual a S = 3 s(s+1) = 4, 10 AULA porém, nos referimos ao número quântico s dizendo que o elétron tem spin 1/2. O spin do elétron é quantizado e os valores possíveis do componente S z são ±1/2. Existem objetos com spin diferente de 1/2, inclusive, objetos com spin inteiro, isto é, com número quântico do spin inteiro. Porem, o caso mais interessante é o spin 1/2. Os elétrons, mas, também os prótons, os nêutrons e os quarks têm spin 1/2. Com a descoberta do spin, o momento angular, definido pelas equações (8.32) deixou de ser a única forma de momento angular conhecida. Vamos no referir a ele como momento angular orbital Spin 1/2 na mecânica quântica Spinors Para definir operadores do spin, precisamos de um espaço do spin. Consideremos o conjunto das matrizes-coluna da forma α 2 χ = α 1, (10.11) onde α 1 e α 2 são números complexos. O conjunto, cujos elemento vamos chamardespinors, é, deummodonatural, umespaçovetorialsobreoscomplexos. Uma matriz 2 2 com entradas complexas a 11 a 12 a 21 a 22 (10.12) 193
8 Spin e Princípio de exclusão de Pauli é, de um modo natural, um operador  no espaço de spinors, definido por Âχ = Produto interno a 11 a 12 a 21 a 22 α 1 α 2 a 11α 1 +a 12 α 2 a 21 α 1 +a 22 α 2. (10.13) Definiremos um produto interno no espaço de spinors. Seja χ o spinor (10.11) e β 2 η = β 1. O produto interno χ η é dado por β 2 χ η = ( α1 α2 ) β 1 = α1β 1 +α2β 2. (10.14) O operador hermitiano conjugado de um operador  no espaço dos spinors é um operador  tal que  χ η = χ Âη (10.15) para todo par de spinors χ, η. Um operador se diz hermitiano, se  =  Operadores do spin Definimos os três operadores, Ŝx, Ŝy, Ŝz, por Ŝ x = 2 σ x, Ŝ y = 2 σ y Ŝ z = 2 σ z (10.16) onde σ x, σ y, σ z são as matrizes de Pauli, σ x = 0 1, σ y = 0 i, σ z = 1 0. (10.17) 1 0 i Os operadores Ŝx, Ŝ y, Ŝ z são hermitianos e, além disso, satisfazem as mesmas relações de comutação que os operadores do momento angular orbital ˆL x, ˆL y, ˆL z : [Ŝx,Ŝy] = i Ŝz, [Ŝy,Ŝz] = i Ŝx, [Ŝz,Ŝx] = i Ŝy. (10.18) 194
9 Introdução a Mecânica Quântica Os quadrados dos operadores do spin são proporcionais ao operador identidade, Ŝ 2 x = Ŝ2 y = Ŝ2 z = 2 4, (10.19) 10 AULA portanto, comutam com todo operador. Fazendo a soma dos quadrados dos operadores do spin, obtemos Ŝ 2 Ŝ2 x +Ŝ2 y +Ŝ2 z = (10.20) Autovalores Decorre das relações (10.19) que o quadrado de qualquer autovalor de um operador do spin é igual a 2 /4. na verdade, cada um dos operadores Ŝx, Ŝy, Ŝ z possui dois autovalores, /2 e /2. Os spinors χ 1/2 = 1 0, χ 1/2 = 0 1 (10.21) são autovetores de Ŝz associados aos autovalores /2 e /2, respectivamente. Os vetores χ 1/2, χ 1/2 formam uma base no espaço de spinors. Todo spinor é representado por uma combinação linear dos spinores χ 1/2, χ 1/ Estados de spin Os estados de spin são representados por spinors normalizados. Um spinor χ é normalizado se χ χ = 1. (10.22) Dois spinors normalizados, χ 1 e χ 2, que diferem em um fator de fase apenas, isto é, χ 2 = e iφ χ 1, onde φ é um número real, representam o mesmo estado de spin. Existe uma infinidade de estados de spin, porém os estados determinados de S z são frequentemente usados. Os autovalores de S z têm a forma m s, onde o número quântico m s pode tomar os valores semi-inteiros ±1/2. O estado 195
10 Spin e Princípio de exclusão de Pauli de spin representado pelo spinor χ 1/2 é o estado determinado de S z com valor /2 de S z ( spin para cima ). O estado representado pelo spinor χ 1/2 é o estado com spin para baixo com valor determinado de S z igual a /2. A Figura 10.4 mostra esses estados, caracterizados por valores 1/2 e 1/2 do número quântico m s, respectivamente. z 1/2 y x 1/2 Figura 10.4: Estados de spin Estados de um elétron Os estados de uma partícula com spin 1/2 (um elétron, por exemplo) são representadas por funções no espaço com valores no espaço de spinors. O produto interno de duas funções, ψ(x,y,z) = f(x,y,z) g(x,y,z), ψ(x,y,z) = f(x,y,z) g(x,y,z), (10.23) é dado por ( ψ ψ = [f(x,y,z)] f(x,y,z)+[g(x,y,z)] g(x,y,z)) dxdydz. (10.24) 196
11 Introdução a Mecânica Quântica Uma função se diz normalizada, se ψ ψ = AULA Os estados do elétron são representados por funções normalizadas. Estados determinados de S z do elétron no átomo do hidrogênio são representadas por funções ψ nlml m s, sendo ψ nlml,1/2(r,θ,φ) = χ 1/2 ψnlm l (r,θ,φ), (10.25) ψ nlml, 1/2(r,θ,φ) = χ 1/2 ψnlm l (r,θ,φ), (10.26) onde ψ nlml são as funções que especificam estados do elétron sem spin, definidasnaaulaanterior. Onúmeroquânticom s estánoconjuntodenúmeros quânticos que especificam o estado Razão giromagnética Para o momento angular orbital, a razão giromagnética, isto é, o módulo do coeficiente de proporcionalidade entre o momento angular e o momento magnético, é igual a e/(2m e ), segundo a eq. (10.4). Para o spin a razão giromagnética e quase duas vezes maior: o operador do momento magnético ˆµ s associado ao spin é dado por ˆµ s = (2,00232) e 2m e Ŝ. (10.27) Na mecânica quântica não-relativística, não há uma explicação teórica para este valor da razão giromagnética, mas a teoria relativística, baseada na equação de Dirac, consegue explica-lo Momento angular total Considerando um elétron, definimos o vetor-operador do momento angular total Ĵ por Ĵ = ˆL+Ŝ. (10.28) 197
12 Spin e Princípio de exclusão de Pauli Exemplo Aplicando o operador à função ψ nlml m s, obtemos Ĵ z ψ nlml m s =( ˆLz +Ŝz Ĵ z = ˆL z +Ŝz = i φ (10.29) ) ) χ ms ψ nlml = χ msˆlz ψ nlml + (Ŝz χ ms ψ nlml =χ ms ( m l )ψ nlml + 2 χ m s ψ nlml = (m l +m s )ψ nlml m s. Sendo m l inteiro e m s semi-inteiro, a soma m l +m s é um numero semi-inteiro. Em unidades de, os valores possíveis do componente J z do momento angular total do elétron são semi-inteiros. Os operadores do momento angular orbital comutam com os operadores do spin, [ˆL, Ŝ] = 0. (10.30) Utilizando as equações (10.30), (8.33) e (10.18), podemos mostrar que os operadores Ĵx, Ĵy, Ĵz satisfazem as mesmas relações de comutação que os componentes do momento angular orbital e os do spin, [Ĵx,Ĵy] = i Ĵz, [Ĵy,Ĵz] = i Ĵx, [Ĵz,Ĵx] = i Ĵy. (10.31) Em decorrência disso, os autovalores do operador Ĵ2 são da forma 2 j(j +1) onde j é o número quântico do momento orbital total. Os operadores ˆL 2 e Ŝ2 comutam com Ĵ2. Para um dado valor de l (lembramos que o número quântico do spin s = 1/2 para o elétron) os valores possíveis de j são todos os números sei-inteiros que satisfazem as desigualdades l 1/2 s l+1/2. (10.32) Os operadores ˆL z e Ŝz não comutam com Ĵ2 e as funções ψ nlml m s não são, geralmente, autofunções de Ĵ2. 198
13 Introdução a Mecânica Quântica Exemplo Seja l = 0. As desigualdades (10.32) se reduzem a 1/2 j 1/2. 10 AULA Logo, j = 1/2. As função ψ n00ms é uma autofunção do operador Ĵ2 (associada ao autovalor 3 2 /4) e, também, do operador Ĵz (associada ao autovalor m s ). Exemplo Seja l = 1, logo j = 1/2,3/2. Verifica-se que Ĵ z ψ n,1,1,1/2 = 3 2 ψ n,1,1,1/2, Ĵ 2 ψ n,1,1,1/2 = 23 2 (3 2 +1)ψ n,1,1,1/2, logo, ψ n,1,1,1/2 é uma autofunção como de Ĵ2, tanto de Ĵz. Porém, a função ψ n,1, 1,1/2, por exemplo, não é uma autofunção de Ĵ2. O operador Ĵ2 comuta com ˆL 2 e Ŝ2, mas não comuta com ˆL e Ŝ Átomos de muitos elétrons e princípio de exclusão Átomos de muitos elétrons O número de elétrons em um átomo neutro é igual a carga do núcleo em unidades de e. Suponhamos que o núcleo do átomo estáem repousona origem. Na mecânica clássica, a energia do sistema é dada por E = Z i=1 p 2 i 2m e Z i=1 Ze 2 4πǫ 0 r i + Z i 1 i=2 j=1 e 2 4πǫ 0 r i r j, (10.33) onde r i e p i são o vetor-posição e o momento linear do i-ésimo elétron, respectivamente. Logo, o hamiltoniano do sistema na mecânica quântica terá a forma Ĥ = h2 2m e Z 2 i i=1 Z i=1 Ze 2 4πǫ 0 r i + Z i 1 i=2 j=1 e 2 4πǫ 0 r i r j, (10.34) onde i = i x i +j y i +k z i, i = 1,2,...,Z. 199
14 Spin e Princípio de exclusão de Pauli Como não é possível resolver a equação de Schrödinger independente do tempo Ĥψ(r 1,...,r n ) = Eψ(r 1,...,r n ) (10.35) até para um átomo com dois elétrons, vários métodos foram desenvolvidas para obter soluções aproximadas. A aproximação mais simples é baseada em uma grande simplificação do hamiltoniano. O último termo na eq. (10.34), que representa a interação entre os elétrons, é omitido. O movimento de cada elétron se torna independente dos outros porque o aproximado é uma soma onde, para cada i = 1,2,...,Z, Ĥ aprox = Z Ĥ i, i=1 Ĥ i = h2 2m e 2 i Ze2 4πǫ 0 r i (10.36) é o hamiltoniano para um átomo de um elétron. A equação Ĥ aprox ψ(r 1,...,r n ) = Eψ(r 1,...,r n ) (10.37) admite separação de variáveis e o problema se reduz ao sistema de problemas de autovalor independentes Ĥ i ψ i = Eψ i, i = 1,2,...,Z. (10.38) Os autovalores de Ĥi são dadas pela eq. (9.30) e as autofunções são ψ nlml m s = χ ms ψ nlml (10.39) onde ψ nlml é dada na eq. (9.31). Logo, os autovalores de Ĥaprox têm a forma E = Z E ni (10.40) e as autofunções separáveis são produtos de funções da forma onde ψ nlml são dadas na eq. (9.31). i=1 ψ nlml m s = χ ms ψ nlml, 200
15 Introdução a Mecânica Quântica Exemplo Consideremos um átomo com dois elétrons. Os autovalores do hamiltoniano são E n1 n 2 = E n1 +E n2, (10.41) 10 AULA onde n 1, n 2 são os dois valores do número quântico principal na especificação da autofunção ψ n1 l 1 m l1 m s1 ;n 2 l 2 m l2 m s2 (r 1,θ 1,φ 1 ;r 2,θ 2,φ 2 ) (10.42) =ψ n1 l 1 m l1 m s1 (r 1,θ 1,φ 1 )ψ n2 l 2 m l2 m s2 (r 2,θ 2,φ 2 ). Porém, notamos que a função ψ n2 l 2 m l2 m s2 ;n 1 l 1 m l1 m s1 (r 1,θ 1,φ 1 ;r 2,θ 2,φ 2 ) (10.43) =ψ n2 l 2 m l2 m s2 (r 1,θ 1,φ 1 )ψ n1 l 1 m l1 m s1 (r 2,θ 2,φ 2 ) também é uma autofunção do hamiltoniano, associada ao mesmo autovalor E n1 n Princípio de exclusão de Pauli Partículas idênticas As funções ψ n1 l 1 m l1 m s1 ;n 2 l 2 m l2 m s2 e ψ n2 l 2 m l2 m s2 ;n 1 l 1 m l1 m s1 representam estados diferentes do átomo? Aceitando uma resposta positiva, estamos admitindo a possibilidade de enumerar os elétrons no átomo. Com efeito, a energia do primeiro elétron seria igual a E n1 e a energia do segundo seria igual a E 2 no estado representado pela função ψ n1 l 1 m l1 m s1 ;n 2 l 2 m l2 m s2, eq. (10.42). No estado representado pela função ψ n2 l 2 m l2 m s2 ;n 1 l 1 m l1 m s1 os elétrons teriam as energias trocadas. Os operadores Ĥ1 e Ĥ2, dados pela eq. (10.36) para i = 1,2, representam os observáveis energia do primeiro elétron e energia do segundo elétron. Sempre que esses observáveis assumem valores distintos, podemos distinguir entre o primeiro elétron e o segundo elétron. Porém, não existem maneiras de enumerar os elétrons. 201
16 Spin e Princípio de exclusão de Pauli Todos os elétrons são idênticos. Duas moedas de mesmo valor são iguais, mas é sempre possível fazer uma marca que permitirá distinguir a primeira moeda da segunda. Esta possibilidade não existe para os elétrons. Uma função que representa um estado do átomo do hélio tem que sofrer uma mudança irrelevante na operação de troca dos estados dos dois elétrons. A única mudança irrelevante para uma função normalizada seria ganhar um fator de fase, isto é, receber um multiplicador da forma e iϕ onde ϕ é uma constante real. Existem apenas duas opções para a função que representa o estado no qual um dos elétrons é caracterizado por valores n 1, l 1,m l1,m s1 dos números quânticos e outro pelo conjunto de valores n 2, l 2,m l2,m s2. Essas opções são: a função simetrizada, isto é, uma combinação linear com coeficientes iguais das funções ψ n1 l 1 m l1 m s1 ;n 2 l 2 m l2 m s2 e ψ n2 l 2 m l2 m s2 ;n 1 l 1 m l1 m s1 ; a função antisimetrizada 1 2 [ψ n1 l 1 m l1 m s1 ;n 2 l 2 m l2 m s2 ψ n2 l 2 m l2 m s2 ;n 1 l 1 m l1 m s1 ]. (10.44) A argumentação para o caso de duas partículas pode ser generalizada para sistemas de qualquer número de partículas idênticas. A função que representa um estado físico do sistema é simétrica ou antisimétrica em relação a troca dos estados de um par de partículas. Bósons e férmions Partículas para as quis se realiza a primeira possibilidade (função simétrica em relação a trocas) são chamadas bósons. Partículas para os quais é válida a segunda opção (função antisimétrica) são chamadas férmions. Ocorre que todas as partículas com spin inteiro são bósons e todas as partículas com spin semi-inteiro são férmions. Então, quando o estados dos elétrons no átomo de hélio são caracterizados pelos valores n 1, l 1, m l1, m s1 e n 2, l 2, m l2, m s2, o 202
17 Introdução a Mecânica Quântica estado do átomo é representado pela função antisimetrizada (10.44). Isto é válido, se (n 1,l 2,m l1,m s1 ) (n 2,l 2,m l2,m s2 ). Porque, se (n 1,l 2,m l1,m s1 ) = (n 2,l 2,m l2,m s2 ), a função (10.44) é igual a zero e não representa um estado do átomo. As considerações podemos generalizar para átomos com qualquer número de elétrons. Assim, chegamos a uma das afirmativas mais importantes na física: o Princípio de exclusão. 10 AULA Princípio de exclusão de Pauli Em um dado sistema, dois elétrons não podem ocupar o mesmo estado. Este é o princípio foi formulado por Wolfgang Pauli em Configurações eletrônicas dos átomos Qual é o estado fundamental de um dado átomo? Se os elétrons fossem bósons, todososelétronsocuparãoestadoscomn = 1. Porém,oselétronssãoférmions. Os estados de um elétron, caracterizados por um dado valor do número quântico principal n, pertencem a uma camada. Todos os estados de uma dada camada têm distribuições radiais de probabilidade semelhantes (para as primeiras três camadas as distribuições são mostradas nas Figuras ). As camadas são designadas por letras maiúsculas, conforme a tabela a seguir. n Camada K L M N No estado fundamental do átomo do hidrogênio, o estado do único elétron do átomo é caracterizado por n = 1, l = 0. O elétron está na camada K e a configuração eletrônica do átomo do hidrogênio é designada por 1s. ComohélioterminaopreenchimentodacamadaK.Comefeito, nacamada K o valor número quântico principal n é igual a um, logo, l = 0, m l = 0 e existem dois estados que podem ser rotulados pelos valores ±1/2 do número quântico m s. A configuração eletrônica do hélio é (1s)
18 Spin e Princípio de exclusão de Pauli A camada L, cujo preenchimento se inicia com o lítio, contem duas subcamadas caracterizadas por l = 0 e l = 1. Na qual das subcamadas está um dos elétrons do lítio? Desprezando a interação entre os elétrons não podemos responder essa pergunta. Porém, métodos mais avançados permitem mostrar que a energia na subcamada 2s é um pouco menor do que a energia na subcamada 2p. A configuração eletrônica do lítio é 1s 2 2s. O preenchimento da segunda camada continua com o preenchimento da subcamada 2s e, depois da subcamada 2p. A tabela a seguir mostra as configurações eletrônicas dos elementos com Z 10. Elemento Símbolo Z Configuração eletrônica Hidrogênio H 1 1s Hélio He 2 1s 2 Lítio Li 3 1s 2 2s Berílio Be 4 1s 2 2s 2 Boro B 5 1s 2 2s 2 2p Carbono C 6 1s 2 2s 2 2p 2 Nitrogênio N 7 1s 2 2s 2 2p 3 Oxigênio O 8 1s 2 2s 2 2p 4 Flúor F 9 1s 2 2s 2 2p 5 Neônio Ne 10 1s 2 2s 2 2p Atividades ATIV Mostre que na experiência de Stern-Gerlach os átomos com projeção do momento angular sobre o eixo z positiva são, realmente, deflexionados para cima Conclusões Spin é um momento angular intrínseco do elétron. 204
19 Introdução a Mecânica Quântica O número quântico do spin do elétron s é igual a 1/2. O valor da razão giromagnética para o spin é (quase) duas vezes maior do que para o momento orbittal. 10 AULA Valores compatíveis dos quatro números quânticos n, l, m l e m s especificam um estado do átomo do hidrogênio. As partículas com spin inteiro são bosons. As partículas com spin semi-inteiro são férmions. Para os férmions e, em particular, para os elétrons, é válido o Princípio de exclusão. Os números quânticos que especificam o estado de um único elétron são usados na classificaç ao dos estados de átomos de muitos elétrons Resumo Um momento magnético é associado ao momento angular orbital de uma partícula carregada. O momento magnético é quantizado. Explicamos a experiência de Stern-Gerlach. Introduzimos o spin é o momento magnético associado ao spin. Introduzimos o conceito de partículas idênticas na mecânica quântica. Explicamos a diferença entre bósons e férmions. Introduzimos o Princípio de exclusão. Explicamos a descrição das configurações eletrônicas de átomos de muitos elétrons Glossário bóson camada férmion 205
20 Spin e Princípio de exclusão de Pauli magneton de Bohr matrizes de Pauli momento angular total princípio de exclusão razão giromagnética spin spin 1/2 spinor subcamada 10.9 Atividades ATIV Mostre que na experiência de Stern-Gerlach os átomos com componente do momento angular ao longo do eixo z positivo são, realmente, deflexionados para cima. ATIV Mostre que os operadores do spin Ŝx, Ŝy, Ŝz são hermitianos. ATIV Mostre que os operadores do spin satisfazem as relações de comutação (10.18). ATIV Ache autovetores do operador Ŝy, associados aos autovalores /2 e / Referências 1. EISBERG, R.; RESNICK, R. Física Quântica: Átomos, moléculas, sólidos, núcleos e partículas. Rio de Janeiro: Campus,
21 Introdução a Mecânica Quântica 2. GRIFFITHS, D. J. Mecânica Quântica. São Paulo: Pearson, GASIOROWICZ, S.Quantum physics. Thirdedition. New York: Wiley, AULA 4. GREINER,W.Quantum Mechanics: An Introduction. Berlin: Springer- Verlag,
22 Apêndice A Integral Gaussiana A antiderivada da função f(x) = e x2 não se exprime em termos de funções elementares. No entanto, a integral definida de e x2 em toda a reta real (a integral Gaussiana) pode ser facilmente calculada 1, e x2 dx = π 1/2. (A.1) A eq. (A.1) pode ser usada para avaliar várias integrais. Em particular, seja I(α) a função definida por I(α) = e αx2 dx. (A.2) para Rα > 0. Fazendo na integral (A.2) a mudança da variável x = α 1/2 y, encontramos ( π ) 1/2 I(α) =. (A.3) α Derivando ambos os membros da eq. (A.2), temos d n dα n I(α) = d n dx n e αx2 dx = ( 1) n x 2n e αx2 dx. (A.4) 1 Ver, por exemplo, wikipedia.org/wiki/gaussian_integral. 209
23 Por outro lado, derivando a eq. (A.3), temos Logo, d n dα n I(α) = (2n 1)! ( 1)n 2 2n 1 (n 1)! x 2n e αx2 dx = (2n 1)! 2 2n 1 (n 1)! π 1/2 α n+1/2. π 1/2 α n+1/2. (A.5) (A.6) 210
24 Apêndice B Constantes Constantes Velocidade da luz c = 2, m/s Permissividade do vácuo ɛ 0 = 8, C 2 /N m 2 Massa do elétron m e = 9, kg Módulo da carga do elétron e = 1, C Massa do próton m p = 1, kg Constante de Planck h = 6, J s Constante de Stefan-Boltzmann σ = 5, W m 2 K 4 Valor da constante na lei de Wien (constante de dispersão de Wien): 2, m K Fator de conversão de unidades 1 ev = 1, J 211
Física Quântica. Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli. Pieter Westera
 Física Quântica Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html Quantização do Momento Angular
Física Quântica Aula 11: Spin do Elétron, Princípio de Exclusão de Pauli Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html Quantização do Momento Angular
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/2 e de Dois Níveis
 Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Aula 17 Tudo sobre os Átomos
 Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
Física Quântica. Momentos de Dipolo Magnético e Spin. Prof. Dr. Walter F. de Azevedo Jr Dr. Walter F. de Azevedo Jr.
 2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momentos de Dipolo Magnético e Spin Prof. Dr. Walter F. de Azevedo Jr. 1 Momento de Dipolo Magnético Orbital Consideremos uma carga elétrica (e) que se
2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momentos de Dipolo Magnético e Spin Prof. Dr. Walter F. de Azevedo Jr. 1 Momento de Dipolo Magnético Orbital Consideremos uma carga elétrica (e) que se
A Experiência de Stern-Gerlach e o Spin do Elétron
 UFPR 28 de Abril de 2014 Figura: Placa Comemorativa. ela foi realizada em 1922; ela investiga os possíveis valores do momento de dipolo magnético, µ, de um átomo de prata; ela explora a dinâmica do dipolo
UFPR 28 de Abril de 2014 Figura: Placa Comemorativa. ela foi realizada em 1922; ela investiga os possíveis valores do momento de dipolo magnético, µ, de um átomo de prata; ela explora a dinâmica do dipolo
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
7. A teoria quântica do átomo de Hidrogênio
 7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
8. Spin do elétron e átomos complexos
 8. Spin do elétron e átomos complexos Sumário Revisão: momento magnético do elétron Efeito Zeeman Spin do elétron Experiência de Stern-Gerlach O princípio da exclusão de Pauli Configuração eletrônica Tabela
8. Spin do elétron e átomos complexos Sumário Revisão: momento magnético do elétron Efeito Zeeman Spin do elétron Experiência de Stern-Gerlach O princípio da exclusão de Pauli Configuração eletrônica Tabela
Átomo de Hidrogênio 1
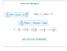 Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Revisão de conceitos de mecânica quântica
 Revisão de conceitos de mecânica quântica Quantização de energia A Radiação de corpo negro Estudos de Planck (1900) sobre a radiação de corpo negro, levaram a ideia de que a energia é dependente da frequência
Revisão de conceitos de mecânica quântica Quantização de energia A Radiação de corpo negro Estudos de Planck (1900) sobre a radiação de corpo negro, levaram a ideia de que a energia é dependente da frequência
Aula-11. (quase) Tudo sobre os átomos
 Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
Física Quântica. Momento de Dipolo Magnético. Prof. Dr. Walter F. de Azevedo Jr Dr. Walter F. de Azevedo Jr.
 2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momento de Dipolo Magnético Prof. Dr. Walter F. de Azevedo Jr. 1 Força de Lorentz Uma partícula deslocando numa região sujeita a um campo elétrico (E)
2019 Dr. Walter F. de Azevedo Jr. Física Quântica Momento de Dipolo Magnético Prof. Dr. Walter F. de Azevedo Jr. 1 Força de Lorentz Uma partícula deslocando numa região sujeita a um campo elétrico (E)
O spin do elétron. Vimos, na aula 2, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com 2 valores, com propriedades de momento angular.
 O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
Introdução. O spin é uma propriedade das partículas elementares, eminentemente quântica, sem equivalente no mundo clássico.
 Ressonância de Spin Introdução O spin é uma propriedade das partículas elementares, eminentemente quântica, sem equivalente no mundo clássico. Nos próximos slides apresentaremos, brevemente, alguns aspectos
Ressonância de Spin Introdução O spin é uma propriedade das partículas elementares, eminentemente quântica, sem equivalente no mundo clássico. Nos próximos slides apresentaremos, brevemente, alguns aspectos
Fundamentos de Química Quântica
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
harmônicos esféricos Os harmônicos esféricos são simultaneamente autofunções dos operadores
 A eq. de Schrödinger em 3D: Independente do tempo: Separação de variáveis: h m v Ψ + V ( r ) Ψ = h v ψ + V ( r ) ψ = m Ψ ih t Eψ ψ ( r, θ, ϕ) = R( r) Θ( θ ) Φ( ϕ) R n ( r) ; Θ ( θ ) ; Φ ( ϕ) Ylm l ( θ,
A eq. de Schrödinger em 3D: Independente do tempo: Separação de variáveis: h m v Ψ + V ( r ) Ψ = h v ψ + V ( r ) ψ = m Ψ ih t Eψ ψ ( r, θ, ϕ) = R( r) Θ( θ ) Φ( ϕ) R n ( r) ; Θ ( θ ) ; Φ ( ϕ) Ylm l ( θ,
Eq. de Dirac com campo magnético
 Eq. de Dirac com campo magnético Rafael Cavagnoli GAME: Grupo de Médias e Altas Energias Eletromagnetismo clássico Eq. de Schrödinger Partícula carregada em campo mag. Eq. de Dirac Partícula carregada
Eq. de Dirac com campo magnético Rafael Cavagnoli GAME: Grupo de Médias e Altas Energias Eletromagnetismo clássico Eq. de Schrödinger Partícula carregada em campo mag. Eq. de Dirac Partícula carregada
A teoria quântica antiga AULA
 3 AULA METAS: Mostrar as dificuldades enfrentadas pela física clássica na explicação da estabilidade dos átomos e da estrutura dos espectros atômicos. Introduzir o modelo de Bohr para o átomo de um elétron.
3 AULA METAS: Mostrar as dificuldades enfrentadas pela física clássica na explicação da estabilidade dos átomos e da estrutura dos espectros atômicos. Introduzir o modelo de Bohr para o átomo de um elétron.
n, l, m l, ms (1) quando estes quatro números quânticos são dados, o estado físico do sistema (no caso, um elétron) é então especificado.
 Introdução. Consideramos nos textos anteriores sistemas quantum mecânicos que possuem vários níveis de energia mas somente um elétron orbital, ou seja, consideramos até o presente momento átomos hidrogenóides.
Introdução. Consideramos nos textos anteriores sistemas quantum mecânicos que possuem vários níveis de energia mas somente um elétron orbital, ou seja, consideramos até o presente momento átomos hidrogenóides.
FF-296: Teoria do Funcional da Densidade I. Ronaldo Rodrigues Pela
 FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos O problema de 1 elétron O princípio variacional Função de onda tentativa Átomo de H unidimensional Íon H2 + unidimensional Equação
FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos O problema de 1 elétron O princípio variacional Função de onda tentativa Átomo de H unidimensional Íon H2 + unidimensional Equação
Átomo de Hélio. Tiago Santiago. 2 de novembro de Resumo
 Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
Física Moderna II Aula 03. Marcelo G Munhoz Pelletron, sala 245, ramal 6940
 Física Moderna II Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br Schroedinger X Bohr Qual a vantagem da teoria de Schroedinger sobre a teoria de Bohr do ponto de vista da observação
Física Moderna II Aula 03 Marcelo G Munhoz Pelletron, sala 245, ramal 6940 munhoz@if.usp.br Schroedinger X Bohr Qual a vantagem da teoria de Schroedinger sobre a teoria de Bohr do ponto de vista da observação
CF100 - Física Moderna II. 2º Semestre de 2018 Prof. Ismael André Heisler Aula 10/08/2018
 CF100 - Física Moderna II 2º Semestre de 2018 Prof. Ismael André Heisler Aula 10/08/2018 1 Átomos Multieletrônicos 2 Partículas Idênticas 3 Na física quântica, o princípio da incerteza impede a observação
CF100 - Física Moderna II 2º Semestre de 2018 Prof. Ismael André Heisler Aula 10/08/2018 1 Átomos Multieletrônicos 2 Partículas Idênticas 3 Na física quântica, o princípio da incerteza impede a observação
Universidade de São Paulo Instituto de Física. Física Moderna II. Profa. Márcia de Almeida Rizzutto 2 o Semestre de Física Moderna 2 Aula 5
 Universidade de São Paulo Instituto de Física Física Moderna II Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 19: experiência de Stern&Gerlach Proposta: Medir os valores possíveis do momento de
Universidade de São Paulo Instituto de Física Física Moderna II Profa. Márcia de Almeida Rizzutto o Semestre de 014 1 19: experiência de Stern&Gerlach Proposta: Medir os valores possíveis do momento de
Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento angular bem definido
 ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
AULA METAS: Introduzir o conceito de fóton no contexto. usar a teoria de Einstein para o efeito fotoelétrico
 METAS: Introduzir o conceito de fóton no contexto da teoria de Einstein para o efeito fotoelétrico. Introduzir a teoria elementar do efeito Compton. OBJETIVOS: Ao fim da aula os alunos deverão ser capazes
METAS: Introduzir o conceito de fóton no contexto da teoria de Einstein para o efeito fotoelétrico. Introduzir a teoria elementar do efeito Compton. OBJETIVOS: Ao fim da aula os alunos deverão ser capazes
Aula 12. (quase) Tudo sobre os átomos. Física Geral F-428
 Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
Mecânica Quântica. Spin 1/2 e a formulação da M. Q. Parte II. A C Tort 1. Instituto Física Universidade Federal do Rio de Janeiro
 Mecânica Quântica Spin 1/ e a formulação da M. Q. Parte II A C Tort 1 1 Departmento de Física Teórica Instituto Física Universidade Federal do Rio de Janeiro 10 de Maio de 01 Mais dois postulados, agora
Mecânica Quântica Spin 1/ e a formulação da M. Q. Parte II A C Tort 1 1 Departmento de Física Teórica Instituto Física Universidade Federal do Rio de Janeiro 10 de Maio de 01 Mais dois postulados, agora
Estrutura Atômica I. Química Quântica Prof a. Dr a. Carla Dalmolin. Átomo de Hidrogênio Átomos Hidrogenóides
 Estrutura Atômica I Química Quântica Prof a. Dr a. Carla Dalmolin Átomo de Hidrogênio Átomos Hidrogenóides Aplicações da Mecânica Quântica Soluções da Equação de Schrödinger independente do tempo Partícula
Estrutura Atômica I Química Quântica Prof a. Dr a. Carla Dalmolin Átomo de Hidrogênio Átomos Hidrogenóides Aplicações da Mecânica Quântica Soluções da Equação de Schrödinger independente do tempo Partícula
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
FF-296: Teoria do Funcional da Densidade I. Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Problema de 2 elétrons Férmions Hartree-Fock Troca
FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Problema de 2 elétrons Férmions Hartree-Fock Troca
Motivação 10/29/2018. Física: compreender as propriedades dos átomos (últimos ~ 100 anos) Experimentos mais precisos :
 Cap. 40 Tudo sobre átomos Algumas propriedades dos átomos: Agrupamentos; Emissão e absorção de luz; Momento angular e magnético. Experimento de Einstein de Haas: Momento angular e magnético ORBITAL. Experimento
Cap. 40 Tudo sobre átomos Algumas propriedades dos átomos: Agrupamentos; Emissão e absorção de luz; Momento angular e magnético. Experimento de Einstein de Haas: Momento angular e magnético ORBITAL. Experimento
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 10 ÁTOMOS COMPLEXOS Primeira Edição junho de 2005 CAPÍTULO 10 ÁTOMOS COMPLEXOS ÍNDICE 10-1- Introdução 10.2- Átomos com mais de um
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 10 ÁTOMOS COMPLEXOS Primeira Edição junho de 2005 CAPÍTULO 10 ÁTOMOS COMPLEXOS ÍNDICE 10-1- Introdução 10.2- Átomos com mais de um
A Estrutura Eletrônica dos Átomos. Prof. Fernando R. Xavier
 A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
3) Quais são os valores possíveis do número quântico magnético de spin? a) -1,- ½,0, ½,1 b) 0 e + ½ c) 1, 0 e +1 d) 0, 1, 2, 3,...
 Fundamentos de Física Capítulo 40 Tudo sobre átomos. Questões Múltipla escolha cap. 40 Fundamentos de Física Halliday Resnick Walker 1) Qual das opções abaixo não é uma propriedade dos átomos? a) Os átomos
Fundamentos de Física Capítulo 40 Tudo sobre átomos. Questões Múltipla escolha cap. 40 Fundamentos de Física Halliday Resnick Walker 1) Qual das opções abaixo não é uma propriedade dos átomos? a) Os átomos
QFL 2144 Parte 3A: Ressonância magnética nuclear
 QFL 2144 Parte 3A: Ressonância magnética nuclear Espectroscopia de RMN: espectroscopia associada com a mudança de estado energético de núcleos atômicos na presença de um campo magnético. Elementos básicos
QFL 2144 Parte 3A: Ressonância magnética nuclear Espectroscopia de RMN: espectroscopia associada com a mudança de estado energético de núcleos atômicos na presença de um campo magnético. Elementos básicos
n Camadas K L M N...
 Notação Espectroscópica para Configurações Eletrônicas em Átomos. Modelo de Partícula Independente. Podemos obter uma quantidade expressiva importante de informações sobre estados atômicos de sistemas
Notação Espectroscópica para Configurações Eletrônicas em Átomos. Modelo de Partícula Independente. Podemos obter uma quantidade expressiva importante de informações sobre estados atômicos de sistemas
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
CAPÍTULO 40 HALLIDAY, RESNICK. 8ª EDIÇÃO
 FÍSICA QUÂNTICA: ÁTOMOS Prof. André L. C. Conceição DAFIS CAPÍTULO 40 HALLIDAY, RESNICK. 8ª EDIÇÃO Tudo sobre os átomos Revisão 1) Modelo de Bohr: átomo de hidrogênio 1) O elétron de um átomo de hidrogênio
FÍSICA QUÂNTICA: ÁTOMOS Prof. André L. C. Conceição DAFIS CAPÍTULO 40 HALLIDAY, RESNICK. 8ª EDIÇÃO Tudo sobre os átomos Revisão 1) Modelo de Bohr: átomo de hidrogênio 1) O elétron de um átomo de hidrogênio
Átomos polieletrónicos
 Átomos polieletrónicos Química Teórica e Estrutural P.J.S.B. Caridade & U. Miranda 2/12/2013 5/11/2013, Aula 8 Química Teórica & Estrutural (2013) Caridade & Ulises 1 Átomo de hidrogénio O Hamiltoniano
Átomos polieletrónicos Química Teórica e Estrutural P.J.S.B. Caridade & U. Miranda 2/12/2013 5/11/2013, Aula 8 Química Teórica & Estrutural (2013) Caridade & Ulises 1 Átomo de hidrogénio O Hamiltoniano
Não serão aceitas respostas sem justificativa:
 Primeira Prova de Conceitos de Mecânica Quântica -(,5) Uma partícula de massa m encontra-se no estado ψ(x,t)= A exp[ω(mx /ħ+it)], onde A e a são constantes reais e positivas. a- Normalize ψ(x,t); b- Calcule
Primeira Prova de Conceitos de Mecânica Quântica -(,5) Uma partícula de massa m encontra-se no estado ψ(x,t)= A exp[ω(mx /ħ+it)], onde A e a são constantes reais e positivas. a- Normalize ψ(x,t); b- Calcule
2. No instante t = 0, o estado físico de uma partícula livre em uma dimensão é descrito pela seguinte função de onda:
 Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 03/08/2011 Nome do Candidato: Nível: Mestrado Doutorado 1. No cálculo da
Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 03/08/2011 Nome do Candidato: Nível: Mestrado Doutorado 1. No cálculo da
A teoria de Hartree. r r. r r
 A teoria de Hartree Vimos, na aula 4, a proposta de Hartree: tratamento autoconsistente Ou seja, V(r) obtido a posteriori, a partir das distribuições de carga dos e -, deve concordar com o V(r) usado para
A teoria de Hartree Vimos, na aula 4, a proposta de Hartree: tratamento autoconsistente Ou seja, V(r) obtido a posteriori, a partir das distribuições de carga dos e -, deve concordar com o V(r) usado para
Escola Politécnica FAP GABARITO DA P3 25 de novembro de 2008
 P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
Momento Angular. 8.1 Álgebra do Momento Angular
 Capítulo 8 Momento Angular Neste capítulo vamos estudar os autovalores e autovetores do momento angular. Este problema também pode ser analisado com o uso do método de operadores, o que faremos na primeira
Capítulo 8 Momento Angular Neste capítulo vamos estudar os autovalores e autovetores do momento angular. Este problema também pode ser analisado com o uso do método de operadores, o que faremos na primeira
Campo na matéria II. 1 Resumem da aula anterior. Aula de março de campo magnetizante
 Campo na matéria II Aula 4 3 de março de 11 1 Resumem da aula anterior A fim de explicar o magnetismo observado na matéria Ampère propões a existência de corrente internas, hoje conhecidas como correntes
Campo na matéria II Aula 4 3 de março de 11 1 Resumem da aula anterior A fim de explicar o magnetismo observado na matéria Ampère propões a existência de corrente internas, hoje conhecidas como correntes
1 O Átomo de Hidrogênio
 O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL
 UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL LOB1021 - FÍSICA IV Prof. Dr. Durval Rodrigues Junior Departamento de Engenharia de Materiais (DEMAR) Escola de Engenharia de Lorena (EEL) Universidade
UNIVERSIDADE DE SÃO PAULO Escola de Engenharia de Lorena EEL LOB1021 - FÍSICA IV Prof. Dr. Durval Rodrigues Junior Departamento de Engenharia de Materiais (DEMAR) Escola de Engenharia de Lorena (EEL) Universidade
Os Postulados da Mecânica Quântica
 Márcio H. F. Bettega Departamento de Física Universidade Federal do Paraná bettega@fisica.ufpr.br Postulados Introdução Vamos apresentar nestas notas os postulados da mecânica quântica de acordo com o
Márcio H. F. Bettega Departamento de Física Universidade Federal do Paraná bettega@fisica.ufpr.br Postulados Introdução Vamos apresentar nestas notas os postulados da mecânica quântica de acordo com o
1) A ESTRUTURA DOS ÁTOMOS
 A ESTRUTURA DOS ÁTOMOS.. Estrutura Atômica A matéria seja no estado líquido sólido ou gasoso é constituída por átomos. Os átomos são constituídos por partículas elementares: os prótons os nêutrons e os
A ESTRUTURA DOS ÁTOMOS.. Estrutura Atômica A matéria seja no estado líquido sólido ou gasoso é constituída por átomos. Os átomos são constituídos por partículas elementares: os prótons os nêutrons e os
FNC376N: Lista de março de ψ r ψ = Eψ. sin θ Y )
 FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
Equação de Schrödinger em 3D
 Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
3-FUNDAMENTOS DA MECÂNICA QUÂNTICA - PARTE 2
 TE069-Física de Semicondutores 3-FUNDAMENTOS DA MECÂNICA QUÂNTICA - PARTE 2 PROF. CÉSAR AUGUSTO DARTORA - UFPR E-MAIL: CADARTORA@ELETRICA.UFPR.BR CURITIBA-PR Roteiro do Capítulo: Poço de potencial duplo:
TE069-Física de Semicondutores 3-FUNDAMENTOS DA MECÂNICA QUÂNTICA - PARTE 2 PROF. CÉSAR AUGUSTO DARTORA - UFPR E-MAIL: CADARTORA@ELETRICA.UFPR.BR CURITIBA-PR Roteiro do Capítulo: Poço de potencial duplo:
Mecânica Quântica:
 Mecânica Quântica: 016-017 6 a Série 1. Considere as matrizes de Pauli, dadas por ( 0 1 0 i 1 0 σ x =, σ 1 0 y =, σ i 0 z = 0 1 ) 1.1. Demonstre que estas matrizes são Hermíticas. Determine os seus valores
Mecânica Quântica: 016-017 6 a Série 1. Considere as matrizes de Pauli, dadas por ( 0 1 0 i 1 0 σ x =, σ 1 0 y =, σ i 0 z = 0 1 ) 1.1. Demonstre que estas matrizes são Hermíticas. Determine os seus valores
N P P N. Ciências de Materiais I Prof. Nilson C. Cruz. Aula 2 Ligação Química. Átomos. Diferença entre materiais = Diferença entre arranjos atômicos e
 Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Átomos multi-eletrônicos. Indistinguibilidade
 Átomos multi-eletrônicos Indistinguibilidade Princípio de exclusão, de Pauli 1. Em um átomo multi-eletrônico nunca pode haver mais de 1 e- ocupando o mesmo estado quântico.. Um sistema constituído de vários
Átomos multi-eletrônicos Indistinguibilidade Princípio de exclusão, de Pauli 1. Em um átomo multi-eletrônico nunca pode haver mais de 1 e- ocupando o mesmo estado quântico.. Um sistema constituído de vários
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
O Método de Hartree-Fock
 O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
Momentos de dipolo magnético
 i z (Parênteses eletromagnético) Modelo de ohr: e circulando em torno do núcleo, produzindo uma corrente. dq e ev Uma espira de corrente produz um campo magnético, a i grandes distâncias, igual ao de um
i z (Parênteses eletromagnético) Modelo de ohr: e circulando em torno do núcleo, produzindo uma corrente. dq e ev Uma espira de corrente produz um campo magnético, a i grandes distâncias, igual ao de um
Não é permitido nenhum tipo de consulta!
 INSTRUÇÕES de PRÊMIO IFT-ICTP PARA JOVENS FÍSICOS Não escreva seu nome em nenhum lugar da prova. Em cada das seis folhas de questões, escreva o número do seu RG. Verifique que você tem as seis folhas de
INSTRUÇÕES de PRÊMIO IFT-ICTP PARA JOVENS FÍSICOS Não escreva seu nome em nenhum lugar da prova. Em cada das seis folhas de questões, escreva o número do seu RG. Verifique que você tem as seis folhas de
-> Foi laureado com o Nobel de Física e um dos fundadores da Mecânica Quântica.
 Werner Karl Heisenberg (5 de Dezembro de 1901, Würzburg 1 de Fevereiro de 1976, Munique, Alemanha). -> foi um físico alemão. -> Foi laureado com o Nobel de Física e um dos fundadores da Mecânica Quântica.
Werner Karl Heisenberg (5 de Dezembro de 1901, Würzburg 1 de Fevereiro de 1976, Munique, Alemanha). -> foi um físico alemão. -> Foi laureado com o Nobel de Física e um dos fundadores da Mecânica Quântica.
Física IV Escola Politécnica GABARITO DA P3 25 de novembro de 2014
 Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
+ E p. ψ(x) = E. ψ(x)
 Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
Princípios Gerais da Mecânica Quântica
 Princípios Gerais da Mecânica Quântica Vitor Oguri Departamento de Física Nuclear e Altas Energias (DFNAE) Instituto de Física Armando Dias Tavares (IFADT) Universidade do Estado do Rio de Janeiro (UERJ)
Princípios Gerais da Mecânica Quântica Vitor Oguri Departamento de Física Nuclear e Altas Energias (DFNAE) Instituto de Física Armando Dias Tavares (IFADT) Universidade do Estado do Rio de Janeiro (UERJ)
Física IV Escola Politécnica P3 7 de dezembro de 2017
 Física IV - 4323204 Escola Politécnica - 2017 P3 7 de dezembro de 2017 Questão 1 Uma partícula de massa m que se move em uma dimensão possui energia potencial que varia com a posição como mostra a figura.
Física IV - 4323204 Escola Politécnica - 2017 P3 7 de dezembro de 2017 Questão 1 Uma partícula de massa m que se move em uma dimensão possui energia potencial que varia com a posição como mostra a figura.
TEORIAS ATÔMICAS. Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807)
 TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
TEORIAS ATÔMICAS Átomo Menor partícula possível de um elemento (Grécia antiga) John Dalton (1807) 1. Os elementos são constituídos por partículas extremamente pequenas chamadas átomos; 2. Todos os átomos
Lista de Exercícios 1: Eletrostática
 Lista de Exercícios 1: Eletrostática 1. Uma carga Q é distribuída uniformemente sobre um fio semicircular de raio a, que está no plano xy. Calcule a força F com que atua sobre uma carga de sinal oposto
Lista de Exercícios 1: Eletrostática 1. Uma carga Q é distribuída uniformemente sobre um fio semicircular de raio a, que está no plano xy. Calcule a força F com que atua sobre uma carga de sinal oposto
Universidade de São Paulo em São Carlos Mecânica Quântica Aplicada Prova 2
 Universidade de São Paulo em São Carlos.7.04 Mecânica Quântica Aplicada Prova Nome: Questão : Método variacional (.5 pontos) Considere o oscilador harmônico descrito pelo hamiltoniano H = + m dx mω x.
Universidade de São Paulo em São Carlos.7.04 Mecânica Quântica Aplicada Prova Nome: Questão : Método variacional (.5 pontos) Considere o oscilador harmônico descrito pelo hamiltoniano H = + m dx mω x.
EUF. Exame Unificado
 EUF Exame Unificado das Pós-graduações em Física Para o primeiro semestre de 2016 14 de outubro de 2015 Parte 1 Instruções ˆ Não escreva seu nome na prova. Ela deverá ser identificada apenas através do
EUF Exame Unificado das Pós-graduações em Física Para o primeiro semestre de 2016 14 de outubro de 2015 Parte 1 Instruções ˆ Não escreva seu nome na prova. Ela deverá ser identificada apenas através do
Estrutura da Matéria Profª Fanny Nascimento Costa
 Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
Estrutura da Matéria Profª Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 08 Átomos multieletrônicos; Spin; Princípio da exclusão de Pauli; Periodicidade Onde está o elétron? https://www.youtube.com/watch?v=8rohpz0a70i
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE FÍSICA - DFIS PLANO DE ENSINO
 DEPARTAMENTO: Física PLANO DE ENSINO DISCIPLINA: Física Moderna I CARGA HORÁRIA: 72 horas-aula SIGLA: FMO1001 Pré-requisito: FGE4001 CURSO: Licenciatura em Física SEMESTRE/ANO: 02/2014 EMENTA: História
DEPARTAMENTO: Física PLANO DE ENSINO DISCIPLINA: Física Moderna I CARGA HORÁRIA: 72 horas-aula SIGLA: FMO1001 Pré-requisito: FGE4001 CURSO: Licenciatura em Física SEMESTRE/ANO: 02/2014 EMENTA: História
Equação de Dirac e o Átomo de Hidrogênio
 Equação de Dirac e o Átomo de Hidrogênio Rodrigo Andrade e Silva Mecânica Quântica 2 Introdução A equação de Dirac fornece o análogo da equação de Schrodinger para uma mecânica quantica relativistica,
Equação de Dirac e o Átomo de Hidrogênio Rodrigo Andrade e Silva Mecânica Quântica 2 Introdução A equação de Dirac fornece o análogo da equação de Schrodinger para uma mecânica quantica relativistica,
O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana
 Universidade Federal do Paraná Setor de Ciências Exatas Departamento de Física O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana Introdução O Hélio é, depois do Hidrogênio, o átomo mais simples
Universidade Federal do Paraná Setor de Ciências Exatas Departamento de Física O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana Introdução O Hélio é, depois do Hidrogênio, o átomo mais simples
CONTEÚDO PROGRAMÁTICO EMENTA
 UNIVERSIDADE FEDERAL DO AMAZONAS INSTITUTO DE CIÊNCIAS EXATAS DEPARTAMENTO DE FÍSICA AV. GAL. RODRIGO OTÁVIO JORDÃO RAMOS, 3000 JAPIIM CEP: 69077-000 - MANAUS-AM, FONE/FAX (92) 3305-2829 CONTEÚDO PROGRAMÁTICO
UNIVERSIDADE FEDERAL DO AMAZONAS INSTITUTO DE CIÊNCIAS EXATAS DEPARTAMENTO DE FÍSICA AV. GAL. RODRIGO OTÁVIO JORDÃO RAMOS, 3000 JAPIIM CEP: 69077-000 - MANAUS-AM, FONE/FAX (92) 3305-2829 CONTEÚDO PROGRAMÁTICO
Aula 17 Tudo sobre os Átomos
 Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
Aula 17 Tudo sobre os Átomos Física 4 Ref. Halliday Volume4 Sumário Algumas propriedades dos átomos; O spin do elétron; Momento Angular e momento magnético; O experimento de Stern-Gerlach; O princípio
Gases quânticos sem interação
 UFABC - Mecânica Estatística Curso 2018.1 Prof. Germán Lugones CAPÍTULO 6 Gases quânticos sem interação!1 Regime clássico e regime quântico Para um gás ideal clássico em equilíbrio térmico a uma temperatura
UFABC - Mecânica Estatística Curso 2018.1 Prof. Germán Lugones CAPÍTULO 6 Gases quânticos sem interação!1 Regime clássico e regime quântico Para um gás ideal clássico em equilíbrio térmico a uma temperatura
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
Física IV Escola Politécnica GABARITO DA PS 3 de dezembro de 2013
 Física IV - 4320402 Escola Politécnica - 2013 GABARITO DA PS 3 de dezembro de 2013 Questão 1 Uma onda eletromagnética plana harmônica, de comprimento de onda λ, propaga-se no vácuo no sentido positivo
Física IV - 4320402 Escola Politécnica - 2013 GABARITO DA PS 3 de dezembro de 2013 Questão 1 Uma onda eletromagnética plana harmônica, de comprimento de onda λ, propaga-se no vácuo no sentido positivo
Átomos e Moléculas. Ligações moleculares. Energia do ion. A molécula de hidrogênio H 2
 Ligações moleculares Átomos e Moléculas Energia do ion H 2 + A molécula de hidrogênio Ligações moleculares Uma molécula é formada por um conjunto de átomos que interagem formando um sistema com energia
Ligações moleculares Átomos e Moléculas Energia do ion H 2 + A molécula de hidrogênio Ligações moleculares Uma molécula é formada por um conjunto de átomos que interagem formando um sistema com energia
A Equação de Onda de Schröedinger. O Princípio da Incerteza de Heisenberg. λ =
 O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
FF-296: Teoria do Funcional da Densidade I. Ronaldo Rodrigues Pela
 FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos HF Dois elétrons N elétrons Thomas Fermi Átomo de Hélio 1D Energia exata: 3,154 H Vamos resolver este problema usando o método
FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos HF Dois elétrons N elétrons Thomas Fermi Átomo de Hélio 1D Energia exata: 3,154 H Vamos resolver este problema usando o método
Lista Considere um oscilador harmonico tridimencional com o potencial, resolve a Equação de Schrödinger independente no tempo
 Lista 8. Considere um oscilador harmonico tridimencional com o potencial, V = m 2 ( ω 2 x x 2 + ω 2 yy 2 + ω 2 zz 2), onde ω x, ω y e ω z representam as frequências deste oscilador (clássico) nas direções,
Lista 8. Considere um oscilador harmonico tridimencional com o potencial, V = m 2 ( ω 2 x x 2 + ω 2 yy 2 + ω 2 zz 2), onde ω x, ω y e ω z representam as frequências deste oscilador (clássico) nas direções,
Mecânica Quântica. Ênfase nos Primeiros Postulados (continuação)
 Mecânica Quântica Ênfase nos Primeiros Postulados (continuação) Postulado Três da MQ http://x-journals.com/wp-content/uploads/2009/03/quantummechanics1.jpg Citamos a seguir um dos fatos surpreendentes
Mecânica Quântica Ênfase nos Primeiros Postulados (continuação) Postulado Três da MQ http://x-journals.com/wp-content/uploads/2009/03/quantummechanics1.jpg Citamos a seguir um dos fatos surpreendentes
Capítulo 40: Tudo sobre os Átomos
 Capítulo 40: Tudo sobre os Átomos Sumário Algumas Propriedades dos Átomos O Spin do Elétron Momento Ângular e Momento Magnético O experimento destern-gerlach Resonância Magnética Princípio da Exclusão
Capítulo 40: Tudo sobre os Átomos Sumário Algumas Propriedades dos Átomos O Spin do Elétron Momento Ângular e Momento Magnético O experimento destern-gerlach Resonância Magnética Princípio da Exclusão
ESTRUTURA ELETRÔNICA DOS ÁTOMOS
 ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
Elétrons como ondas? Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química
 OS ELÉTRONS O MODELO DA MECÂNICA QUÂNTICA E AS ENERGIAS ELETRÔNICAS Modelo atual se baseia na MECÂNICA QUÂNTICA Considera os conceitos da quantização da energia eletrônica (Bohr), fornecendo uma explicação
OS ELÉTRONS O MODELO DA MECÂNICA QUÂNTICA E AS ENERGIAS ELETRÔNICAS Modelo atual se baseia na MECÂNICA QUÂNTICA Considera os conceitos da quantização da energia eletrônica (Bohr), fornecendo uma explicação
FNC Física Moderna 2 Aula 26
 FNC 0376 - Física Moderna Aula 6 1 Física Nuclear: cronologia do início Descoberta da Radioatividade (Becquerel) 1896 Separação química do Ra (Marie e Pierre Curie) 1898 Modelo atômico de Rutherford 1911
FNC 0376 - Física Moderna Aula 6 1 Física Nuclear: cronologia do início Descoberta da Radioatividade (Becquerel) 1896 Separação química do Ra (Marie e Pierre Curie) 1898 Modelo atômico de Rutherford 1911
LCE0143 Química Geral. Estrutura Atômica. Wanessa Melchert Mattos.
 LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
Introdução à Física Atômica e Molecular
 4005 Introdução à Física Atômica e Molecular Átomos Multieletrônicos Referências: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos. P. Atkins e R. Friedman, Molecular Quantum Mechanics,
4005 Introdução à Física Atômica e Molecular Átomos Multieletrônicos Referências: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos. P. Atkins e R. Friedman, Molecular Quantum Mechanics,
Breve Revisão de Mecânica
 Capítulo 1 Breve Revisão de Mecânica Quântica Seguimos as secções 5.1 a 5.3 do Griffiths [1] e a secção 1.1 do meu texto de Introdução à Teoria de Campo []. É assumido como pré-requisito o conhecimento
Capítulo 1 Breve Revisão de Mecânica Quântica Seguimos as secções 5.1 a 5.3 do Griffiths [1] e a secção 1.1 do meu texto de Introdução à Teoria de Campo []. É assumido como pré-requisito o conhecimento
Universidade Federal do Tocantins
 Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
Aula 3 Estrutura Atômica cont
 Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Aula 3 Estrutura Atômica cont Tabela Periódica Mecânica quântica e orbitais atômicos Schrödinger propôs uma equação que contém os termos onda e partícula. A resolução da equação leva às funções de onda.
Ligações Químicas - I
 Ligações Químicas - I Orbitais atômicos e números quânticos A tabela periódica; propriedades Ligações químicas A ligação iônica Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
Ligações Químicas - I Orbitais atômicos e números quânticos A tabela periódica; propriedades Ligações químicas A ligação iônica Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White
 QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
Física IV - FAP2204 Escola Politécnica GABARITO DA P3 8 de dezembro de 2009
 P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
Tarefa 23 Professor Gustavo
 Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
Química Tarefa Professor Gustavo 01. Entre as afirmações abaixo, assinale a opção ERRADA. a) Os íons He +, Li +, Be +, no estado gasoso são exemplos de hidrogenóides. b) No átomo de hidrogênio, os orbitais
Professor: André Luiz de Oliveira. PLANO DE ENSINO-Disponível em:
 Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas Departamento de Física PLANO DE ENSINO-Disponível em: http://www.joinville.udesc.br/portal/professores/andre 1. Identificação Curso:
Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas Departamento de Física PLANO DE ENSINO-Disponível em: http://www.joinville.udesc.br/portal/professores/andre 1. Identificação Curso:
