Introdução. O que é Mieloma?
|
|
|
- Thiago Palhares Estrela
- 9 Há anos
- Visualizações:
Transcrição
1
2 Índice Introdução...4 O Que é Mieloma?...4 Produção de Proteína Monoclonal pela Célula do Mieloma...5 Histórico...7 Epidemiologia Fisiopatologia Doença Óssea Anemia Disfunção Renal Disfunção de Outros Órgãos Tipos de Mieloma Sintomas Clínicos Estadiamento e Fatores Prognósticos Definição de Resposta Clínica Tratamento Tratamento Anti-Mieloma Sistêmico Transplante Radioterapia Terapia de Manutenção Terapia de Suporte Controle da Doença Refratária ou Recidivada Tratamentos Novos e em Estudo Referências Sobre a IMF
3 Introdução Esta Revisão Concisa do Mieloma e das Opções de Tratamento, preparada pela IMF, é uma visão geral do mieloma, com uma discussão da fisiopatologia, das características clínicas e das opções de tratamento. Esperamos que as informações sejam úteis para médicos e pacientes. O que é Mieloma? O mieloma é um câncer dos plasmócitos da medula óssea. É, portanto, uma neoplasia maligna hematológica muito parecida com a leucemia. Os plasmócitos malignos (vide Figura 1), também conhecidos como células do mieloma, acumulam-se na medula óssea e apenas raramente entram na corrente sanguínea como ocorre em uma leucemia verdadeira. As principais características do mieloma resultam desse acúmulo progressivo de células do mieloma na medula, que provoca: Comprometimento da função da medula óssea normal, que costuma ser refletido pela presença de anemia. Dano aos ossos adjacentes. Liberação da proteína monoclonal (Proteína M) pelo mieloma na corrente sanguínea e/ou na urina. Supressão da função imunológica normal, refletida por níveis mais baixos de imunoglobulinas normais e maior susceptibilidade a infecções. As células do mieloma também podem crescer na forma de tumores localizados ou plasmocitomas. Esses plasmocitomas podem ser únicos ou múltiplos e podem ficar restritos à medula óssea e ao osso (medular) ou se desenvolver fora do osso em tecidos moles. Os plasmocitomas fora do osso são denominados extramedulares. Quando existem vários plasmocitomas dentro e fora do osso, a condição também é conhecida como mieloma múltiplo. PRODUÇÃO DE PROTEÍNA MONOCLONAL PELA CÉLULA DO MIELOMA A propriedade característica das células do mieloma é produzir e liberar (ou secretar) proteína monoclonal no sangue e/ou na urina. A quantidade de proteína monoclonal produzida pelas células do mieloma varia consideravelmente de paciente para paciente. Quando se trata de mieloma é muito importante saber se as células do mieloma de um paciente secretam altas ou baixas quantidades de proteína, ou mesmo se são não secretoras (sem proteína liberada no sangue ou na urina). Assim que a relação entre o nível de proteínas e a quantidade de mieloma na medula óssea é conhecida, é possível interpretar e entender a relação entre um nível de proteína específico e a quantidade de células do mieloma. A proteína monoclonal também é chamada de proteína-m, proteína do mieloma, paraproteína ou pico monoclonal. A denominação pico para a proteína monoclonal é devido à forma como aparece na eletroforese protéica, uma técnica laboratorial usada para separar e identificar proteínas (vide Figura 2). Figura 2: pico monoclonal A proteína monoclonal é uma imunoglobulina ou um componente/fragmento de uma imunoglobulina. A Figura 3 ilustra a estrutura de uma molécula de imunoglobulina normal. Nas células do mieloma, houve uma ou mais mutações nos genes responsáveis pela produção de imunoglobulinas. Portanto, a sequência de aminoácidos e a estrutura das proteínas do mieloma são anormais. Caracteristicamente, ocorre perda da função normal da imunoglobulina como anticorpo e a estrutura tridimensional da molécula pode ser anormal. Figura 1: Plasmócitos (células do mieloma) Essa alteração de função e estrutura tem várias consequências: O excesso de proteína-m aumenta na corrente sanguínea e/ou excretado na urina como um pico monoclonal. As moléculas monoclonais anormais podem se aderir umas às outras e/ou aos tecidos, tais como células sanguíneas, parede dos vasos sanguíneos e outros componentes do sangue. Com isso, a circulação e o fluxo do sangue diminuem, causando a síndrome da hiperviscosidade, que será discutida a seguir. 4 5
4 Figura 3: Estrutura da Molécula de Imunoglobulina As proteínas de Bence Jones livres também podem se aderir umas às outras e/ou a outros tecidos (da mesma forma que a imunoglobulina inteira). Nesse caso, o resultado final é: 1. Amiloidose - Doença em que ocorre ligação cruzada das cadeias leves de Bence Jones de forma ß-pregueada altamente simétrica e deposição dessas cadeias no tecido adjacente ao osso, como, por exemplo, no rim, nos nervos e no tecido cardíaco. 2. Doença da Deposição de Cadeias Leves - As cadeias leves depositam-se de forma mais desordenada, mas mais especificamente nos vasos sanguíneos de pequeno calibre dos olhos e dos rins. É importante ressaltar que os resultados dos exames de sangue de rotina podem estar muito alterados em decorrência da hiperviscosidade das amostras de sangue com mieloma nos equipamentos de análise bioquímica automatizados e/ou da interferência em reações químicas necessárias para os exames de rotina. HISTÓRICO Aproximadamente 30% do tempo, a produção de cadeias leves é maior do que a necessária para combinação com as cadeias pesadas e formação de uma molécula inteira de imunoglobulina. Essas cadeias leves em excesso são as proteínas de Bence Jones (vide Histórico). As proteínas de Bence Jones livres têm peso molecular de daltons e são pequenas o suficiente para passarem livremente para a urina, resultando em um nível elevado de proteínas urinárias em 24 horas que gera o pico monoclonal de Bence Jones. As proteínas monoclonais anormais também podem apresentar muitas outras propriedades, entre elas: Ligação a fatores de coagulação sanguíneos normais, acarretando aumento da tendência a sangramento ou da coagulação sanguínea ou flebite. Ligação a substâncias químicas ou hormônios circulantes, resultando em uma variedade de disfunções endócrinas ou metabólicas. Figura 4: Fases da Doença O Dr. Henry Bence Jones foi o primeiro a investigar uma proteína estranha na urina de um paciente com mieloma. O que chamou sua atenção foi uma proteína da urina que se dissolvia em fervura, mas reprecipitava ao esfriar: o que são agora chamadas de cadeias leves de Bence Jones. Esse paciente também tinha uma doença óssea muito estranha, que nós agora chamamos de mieloma. A seguir um breve resumo comentado do progresso na pesquisa e tratamento para mieloma múltiplo e doenças relacionadas daquela época até o presente. ANO DESCRIÇÃO Primeiras descrições de casos de mieloma denominado mollities e fragilitas ossium (ossos moles e frágeis). O primeiro paciente, Thomas Alexander McBean, foi diagnosticado em 1845 pelo Dr. William Macintyre, um especialista da Harley Street em Londres. O problema urinário incomum por ele descoberto foi minuciosamente investigado pelo Dr. Henry Bence Jones, que publicou suas observações em Em 1846, o cirurgião John Dalrymple relatou que havia observado que os ossos que apresentavam a doença continham células que, posteriormente, foram identificadas como sendo plasmócitos. O Dr. Macintyre publicou um relato detalhado desse caso de mieloma de Bence Jones em Há relato de que o Dr. Samuel Solly publicou um caso de mieloma (Sarah Newbury) em Rustizky introduziu o termo mieloma múltiplo para designar a presença de múltiplas lesões com plasmócitos no osso Otto Kahler publicou uma descrição clínica detalhada de mieloma múltiplo, doença de Kahler Ramon y Cajal forneceu a primeira descrição microscópica acurada dos plasmócitos Wright descobriu que as células do mieloma múltiplo são plasmócitos. 6 7
5 1903 Weber observou que a doença de mieloma ósseo (lesões líticas) é detectável usando raios-x Weber sugeriu que os plasmócitos na medula óssea causam a destruição óssea do mieloma. Década de 30 O diagnóstico de rotina de mieloma continuou difícil até a década de 30, quando aspirações de medula óssea foram usadas em larga escala pela primeira vez. O desenvolvimento de ultracentrífugas e eletroforese de proteínas do soro/urina melhoraram tanto a triagem quanto o diagnóstico A imunoeletroforese permitiu a identificação exata das proteínas monoclonais do mieloma. A imunofixação foi introduzida como um método mais sensível desde então Korngold e Lipari notaram que as proteínas de Bence Jones (BJ) estão relacionadas às gamaglobulinas séricas normais assim como as proteínas séricas anormais. Em suas homenagens, os dois tipos de proteínas de Bence Jones são chamadas kappa (K) e lambda (y ou L) Descoberta da sarcolisina na URSS. Desta, foi derivada o melfalano (Alkeran ). Pela primeira vez o tratamento era possível Waldeströn enfatizou a importância da diferenciação entre gamopatias monoclonais e policlonais. Ele associou proteínas IgM monoclonais com macroglobulinemia, sendo distinta de mieloma Primeiro relato de tratamento bem sucedido de mieloma com melfalano (Alkeran ) por Bergsagel Primeiro relato de tratamento bem sucedido de mieloma com ciclofosfamida (Cytoxan ) por Korst. Resultados com ciclofosfamida provaram ser similares aos resultados com melfalano Foi demonstrado por Alexanian que melfalano combinado com prednisona produzia resultado melhores que o melfalano sozinho O sistema de Durie/Salmon para estadiamento de mieloma foi introduzido. Os pacientes eram classificados para avaliar os benefícios da quimioterapia em diferentes estágios da doença (I, II, III, A ou B) Várias combinações de agentes quimioterápicos foram testadas, incluindo o regime M2 (VBMCP), VMCP-VBAP e ABCM, com alguns indícios de superioridade em relação ao MP. No entanto, em 1992, uma metanálise comparativa (Gregory) apresentou resultados equivalentes para todas as combinações Introdução do índice de marcação (análise da fração de crescimento) como teste para mieloma e doenças relacionadas. Identificação da fase de platô ou remissão estável do mieloma. Trata-se do período em que a fração de crescimento (LI%) dos plasmócitos residuais na medula óssea é igual a zero % Transplantes entre gêmeos realizados por Fefer e Osserman como tratamento para mieloma Microglobulina ß-2 sérica usada pela primeira vez como teste prognóstico (Bataille, Child e Durie) Barlogie e Alexanian introduzem a quimioterapia VAD Primeiros relatos de transplantes alogênicos em mieloma múltiplo por vários investigadores Grande número de estudos avaliando terapia de altas doses com medula óssea autóloga ou resgate com células-tronco por vários investigadores. Introdução dos procedimentos de transplante único (McElwain) e duplo (Barlogie) Primeiro estudo randomizado indicando possível benefício da terapia de altas doses com transplante de medula óssea versus quimioterapia padrão (Attal). Estudo randomizado do bisfosfonato pamidronato (Aredia ) versus placebo indica redução dos problemas ósseos ( problemas relacionados ao esqueleto ) Evidência de que os vírus podem estar envolvidos no desencadeamento do mieloma. O mieloma é mais comum em pacientes com HIV e hepatite C. O vírus do herpes humano 8 (HHV-8) é encontrado em células dendríticas da medula óssea. É encontrado no sangue RNA com especificidade para o vírus SV-40 causador de câncer em macacos Pesquisa contínua sobre o papel da quimioterapia de altas doses com transplantes autólogos ou alogênicos. A magnitude do benefício e das populações de pacientes que podem se beneficiar continuam incertas. Demonstrou-se que o transplante realizado como parte da terapia inicial (indução) produz resultados semelhantes aos do transplante realizado na primeira recidiva. Demonstrou-se que deleções no cromossomo 13 é um fator prognóstico desfavorável para transplante bem como outras terapias. Novo estudo reconfirma a prednisona como terapia de manutenção útil com prolongamento da remissão. Demonstrou-se novamente o benefício do interferon alfa no prolongamento da remissão Demonstrou-se que a talidomida é um agente antimieloma efetivo em pacientes com doença recidivante/refratária. Transplante minialogênico é introduzido como método menos tóxico para atingir o efeito enxerto vs. mieloma. Estudo randomizado francês demonstra que não há grandes benefícios do transplante autólogo duplo versus transplante simples. O segmento em longo prazo demonstra que o tratamento contínuo por 2 anos com Aredia é útil. 8 9
6 2000 Pela primeira vez, a terapia para mieloma tem diversas novas abordagens promissoras. Novos estudos clínicos incluem análogos da talidomida (p. ex. Revlimid ), análogos de Adriamycin de longa ação (p.ex. doxorrubicina peguilada ou Doxil ), trióxido de arsênio (Trisenox ), agentes antiangiogênese (p.ex. o inibidor de tirosina quinase VEGF), agentes bloqueadores de adesão celular e inibidores de proteassoma (p.ex. VELCADE ) É proposto um novo sistema de classificação para mieloma e doenças relacionadas (veja Tabela 1 abaixo), O IFM (Grupo de Estudo Francês) define 3 grupos de risco com base na microglobulina ß-2 sérica e presença/ausência de anormalidades do cromossomo 13 por análise FISH Resultados de um estudo randomizado do ECOG comparando talidomida mais dexametasona versus dexametasona sozinha para mieloma não tratado anteriormente indicam uma taxa de resposta de 59% com a combinação versus 41% com a dexametasona sozinha (Critérios ECOG). Resultados de um estudo randomizado multi-institucional comparando VELCADE com dexametasona demonstram superioridade do VELCADE (detalhes discutidos no texto). Resultados iniciais com VELCADE na condição de primeira linha demonstram excelentes resultados: taxa de resposta de 83% para VELCADE /dexametasona e 94% com VELCADE /Adriamycin / dexametasona e a habilidade de coletar células tronco com transplante e enxertia bem sucedidos. É introduzido um novo sistema de estadiamento de mieloma, o ISS (International Staging System). Veja página E vidências de eficácia de novos agentes em estudos clínicos, incluindo VELCADE (Fase III, Millennium) e Revlimid (Fase III, Celgene). A talidomida combinada com dexametasona como terapia de primeira linha para mieloma produz taxa de resposta de aproximadamente 70%. O MRC no Reino Unido relata resultados de autotransplante no encontro anual da ASH (American Society of Hematology). É notado benefício global, especialmente para pacientes com microglobulina ß2 sérica elevada (>7,5 mg/l) Dois grandes estudos de Fase III demonstram que Revlimid (lenalidomida) mais dexametasona é superior à dexametasona sozinha em mieloma recidivante (tempo para progressão > 15 meses vs. 5 meses). VELCADE recebe aprovação total da FDA para o tratamento de pacientes com mieloma após uma terapia anterior. O International Staging System (ISS) desenvolvido pelo International Myeloma Working Group (IMWG) da International Myeloma Foundation (IMF) é publicado (veja página 17). Vários novos agentes em desenvolvimento inicial. Inibidores de proteína de choque térmico (HSP)-90 entram em estudos de Fase I-II. Adição de talidomida a regimes padrão de melfalano/prednisona apresentam benefícios adicionais significativos. Diversos estudos iniciais estão em andamento A FDA aprova VELCADE (bortezomibe; anteriormente PS-341) como tratamento para mieloma ativamente recidivante após pelo menos duas terapias anteriores. Resultados de autotransplante do MRC fornecem o segundo conjunto de dados randomizados indicando o benefício do autotransplante versus quimioterapia em doses padrão. Resultados publicados de um estudo do IFM comparando transplante único com duplo demonstram benefício global com o transplante duplo após mais de quatro anos de segmento. No entanto, não há benefício adicional aparente para pacientes já em remissão completa após o primeiro transplante. O grupo Little Rock (Shaugnessy/Barlogie) demonstra que a doença óssea em mieloma está associada com a produção de uma proteína específica chamada DKK Novos critérios de resposta para avaliação do benefício do tratamento são desenvolvidos e publicados. Revlimid recebe aprovação da FDA para o tratamento de mieloma em combinação com dexametasona em pacientes que receberam pelo menos uma terapia anterior. Vários novos agentes continuam sendo desenvolvidos
7 A FDA aceita um NDA suplementar para o uso de VELCADE mais Doxil para tratar mieloma recidivante ou refratário em pacientes que não receberam VELCADE anteriormente e que receberam ao menos uma terapia anterior. Combinação de talidomida/dexametasona mais Doxil comparada com talidomida/dexametasona em um estudo de fase III para mieloma recém-diagnosticado. Novos agentes em desenvolvimento incluem: inibidores de HSP-90, novos inibidores de proteassoma e novos agentes imunomoduladores. Surgem evidências de que algumas das novas terapias podem superar alguns fatores de alto-risco. A talidomida é aprovada pela EMEA na Europa como parte do regime MPT (melfalano/prednisona/talidomida) para terapia de primeira linha. VELCADE é aprovado pela FDA nos EUA como parte do regime VMP (VELCADE /melfalano/prednisona) para terapia de primeira linha. Vários novos medicamentos em desenvolvimento e estudos em andamento. O inibidor de proteassoma de segunda geração carfilzomibe (PR-171) se mostra promissor em estudos iniciais. Mozobil (plerixafor) é aprovado em combinação com G-CSF para a coleta de células tronco para transplante autólogo em pacientes com mieloma. Continua o desenvolvimento de novos medicamentos, incluindo resultados encorajadores dos inibidores de proteassoma de segunda geração carfilzomibe e NP-0052; inibidores de HDCA vorinostate e panobinostate; desregulador de HSP-90 tanespimicina; anticorpo monoclonal elotuzumabe; e agente imunomodulador de terceira geração pomalidomida. Análise do IMWG mostra que anormalidades citogenéticas e em FISH combinadas com o estágio ISS são prognósticas; algumas novas terapias superam fatores de risco baixos A FDA dos EUA aprova uma estratégia de mitigação e avaliação de riscos (REMS) para assegurar o uso seguro de agentes estimuladores de eritropoiese (ESAs), os quais podem promover crescimento tumoral, reduzir a sobrevida e aumentar o risco de eventos adversos cardiovasculares. Identificação preliminar de receptores Epo em células de mieloma. O desenvolvimento de novos medicamentos continua, incluindo mais resultados encorajadores de estudos com inibidor de proteassoma de segunda geração carfilzomibe; inibidores de HDCA vorinostate e panobinostate; anticorpo monoclonal elotuzumabe; e agente imunomodulador de terceira geração pomalidomida. Diversos estudos sugerem um papel para lenalidomida como terapia de manutenção. Terapia de primeira linha com os novos agentes pode ser tão efetiva quanto transplantes em pacientes elegíveis. Zometa (ácido zoledrônico) pode ter um efeito antimieloma; higiene dental efetiva reduziu a ocorrência de ONJ. EPIDEMIOLOGIA A incidência de mieloma nos EUA é de 3-4/ , o que representa aproximadamente 1,3% de todos os tipos de câncer. A American Cancer Society estima que em 2010, aproximadamente americanos seriam diagnosticados com mieloma, e pessoas morreriam da doença. (Estimativas para 2011 não estavam disponíveis no momento desse texto). Atualmente há cerca de americanos sob tratamento para a doença. O mieloma é mais comum em Afro- Americanos do que em Caucasianos. Por exemplo, no município de Los Angeles, a incidência entre homens afro-americanos é de 9,8/ contra 4,3/ em homens caucasianos). A incidência varia de país para país, indo de <1/ na China para aproximadamente 4/ na maioria dos países industrializados ocidentais. A proporção homens:mulheres é de 1,25:1 nos EUA. A incidência aumenta com a idade. Técnicas de diagnóstico melhores e a idade média maior da população em geral podem explicar em parte a incidência crescente nas últimas décadas. A tendência ao aumento da frequência de mieloma em pacientes com menos de 55 anos implica em fatores ambientais causadores importantes nos últimos 60 anos. Vários estudos recentes tem avaliado a causa ou pré-disposição ao Mieloma, GMSI e outras doenças relacionadas. Bombeiros e indivíduos em várias outras ocupações com exposição a agentes tóxicos bem como indivíduos com obesidade tem risco aumentado de desenvolver mieloma. A ingestão de frutos do mar e peixes contaminados com metais pesados e/ou produtos químicos pode ser um fator de risco para mieloma. Outras condições médicas incluindo distúrbios do sistema imunológico e infecções podem ser fatores subjacentes e/ou desencadeantes. Vários estudos estão focando os fatores de risco genéticos para o mieloma
8 Tabela 1: Definições de mieloma e gamopatias monoclonais relacionadas Nomenclatura Padrão GMSI (MGUS - Gamopatia Monoclonal de Significância Indeterminada) Mieloma Indolente ou Assintomático Mieloma sintomático ou ativo *Os danos dos órgãos classificados como CRAB : Novo Nome Proposto Proteína monoclonal presente Nenhum distúrbio de plasmócitos ativo Nível da doença mais alto que o GMSI, mas, ainda sem sintomas ou danos aos órgãos. Pode ser classificado em baixo ou alto risco baseado em chance maior ou menor de transição para mieloma ativo. Proteína monoclonal presente e; Presença de um ou mais fatores CRAB C - Elevação do Cálcio (> 10 mg/l) R - Disfunção Renal (creatinina > 2 mg/dl) A - Anemia (hemoglobina < 10g/dL ou diminuição de 2 g/dl do normal do paciente) B - Doença Óssea (lesões líticas ou osteoporose) UM OU MAIS são necessários para o diagnóstico de MIELOMA SINTOMÁTICO. Outras características menos comuns também podem ser critérios para um paciente individual, incluindo: Infecções graves recorrentes Neuropatia relacionada a mieloma Amiloidose ou deposição de componente-m Outras características únicas FISIOPATOLOGIA O crescimento descontrolado das células do mieloma tem muitas consequências, entre elas, destruição óssea, insuficiência da medula óssea, aumento do volume e viscosidade plasmático, supressão da produção de imunoglobulina normal e insuficiência renal. No entanto, a doença pode permanecer assintomática por muitos anos, conforme mencionado na discussão sobre GMSI. Na fase sintomática, a queixa mais comum é dor óssea. O nível de proteína-m sérica e/ou urinária é elevado e, caracteristicamente, em elevação no momento do diagnóstico. (Deve-se observar que a letra M é usada para Monoclonal, Mieloma, Imunoglobulina Monoclonal e Componente M, que apesar de não serem totalmente idênticos, são usados como sinônimos). O curso geral da doença está ilustrado na Figura 4. É importante notar que podem ocorrer vários períodos de remissão e recidiva. A Tabela 2 resume a fisiopatologia do mieloma de forma esquemática. DOENÇA ÓSSEA Desde o reconhecimento do mieloma pela primeira vez em 1844, houve conhecimento sobre um tipo não usual e único de doença óssea. Apenas muito recentemente os mecanismos envolvidos foram determinados. A primeira pista foi que ambas as células do mieloma e um número elevado de osteoclastos estão presentes nos sítios de destruição óssea. A compreensão dos mecanismos evoluiu da observação de que as células do mieloma produzem fatores de ativação de osteoclastos (FAOs) para a caracterização das citoquinas locais, como IL-1ß, IL-6 e TNF e ß, das quimioquinas como a MIP- e dos processos de adesão entre células que envolvem a av ß3 integrina, todos importantes para o aumento da quantidade e atividade dos osteoclastos. Mais recentemente, uma substância denominada ligante RANK (RANK L) foi identificada como um mediador fundamental para a ativação dos osteoclastos. Muitos detalhes sobre os mecanismos de doença óssea em mieloma agora são compreendidos. Diversos alvos para abordagens de tratamento foram identificados. Além da ativação dos osteoclastos, a outra característica importante da doença óssea do mieloma é a inibição dos osteoblastos, que são responsáveis pelo remodelamento e reparo ósseos normal. O acoplamento entre as funções dos osteoclastos e osteoblastos é responsável pelo reparo e remodelamento dos ósseos normais. Os mecanismos responsáveis pelo desacoplamento no mieloma também estão sendo investigados. Uma nova observação importante é que as estatinas hipocolesterolêmicas (inibidores de HMG-CoA redutase, p. ex., Lipitor, Mevacor ), podem intensificar a atividade dos osteoblastos e promover a cicatrização do osso. Além disso, VELCADE e lenalidomida (Revlimid ) demonstraram promover cicatrização óssea, além de exercerem uma atividade anti-mieloma potente. Já estão em andamento estudos para maiores investigações sobre os benefícios dessas novas terapias ósseas. ANEMIA A anemia é uma característica típica do mieloma. Apesar de o simples deslocamento físico dos precursores de eritrócitos da medula ser indubitavelmente uma causa, a inibição específica da produção de eritrócitos pela citoquina microambiental e os efeitos de adesão molecular são uma explicação mais funcional. As causas exatas da anemia relacionada ao mieloma estão sendo investigadas por diversas equipes de pesquisa. A melhora da anemia ocorre com tratamento bem-sucedido do mieloma. Eritropoietina recombinante (Epo) (p. ex. Epogen ou Procrit ) deve ser usada com cautela, sob a luz de relatos recentes da associação de Epo com crescimento tumoral aumentado e sobrevida reduzida em pacientes com câncer, e na identificação de receptores Epo em células de mieloma. DISFUNÇÃO RENAL O comprometimento da função renal é uma complicação comum observada em pacientes com mieloma. No entanto, isso não significa que todo paciente terá este problema. Em alguns pacientes as proteínas de mieloma, especialmente as cadeias leves de Bence Jones, provocam dano renal por meio de uma série de mecanismos que vão do dano tubular por grande acúmulo de cadeias leves precipitadas até os efeitos das proteínas do mieloma depositadas como amilóide, ou dano tubular seletivo resultando nos efeitos metabólicos de uma entidade chamada Síndrome de Fanconi. A Síndrome de Fanconi é um defeito tubular renal seletivo com extravasamento de aminoácidos e fosfatos na urina, o que pode causar doença óssea metabólica. Outros fatores importantes relacionados a disfunção renal em pacientes com mieloma múltiplo são níveis elevados de cálcio e/ou ácido úrico, infecção e efeitos tóxicos dos medicamentos, 14 15
9 como antibióticos nefrotóxicos, antiinflamatórios não-esteroides (NSAIDS) ou agentes de contraste usados em exames diagnósticos. Uma nova e importante observação é o efeito tóxico em potencial do agentes de contraste baseados em gadolínio usados em exames de ressonância magnética. Pacientes com problemas renais devem discutir o uso de gadolínio com seus médicos. A consciência de danos renais potenciais e a ingestão suficiente de líquidos é particularmente importante para pacientes com mieloma, pois ajuda a prevenir os possíveis efeitos prejudiciais desses fatores diversos. 16 DISFUNÇÃO DE OUTROS ÓRGÃOS As células do mieloma podem acumular-se na medula óssea e/ou em vários tecidos, causando uma grande diversidade de complicações possíveis. Efeitos Neurológicos - em pacientes com mieloma, o tecido nervoso costuma ser afetado tanto pelos efeitos diretos de anticorpo exercidos pelas proteínas do mieloma contra os nervos (p. ex., bainhas de mielina) como pela deposição de fibrilas amiloides nos nervos, prejudicando dessa forma sua função. Esses efeitos resultam em neuropatias periféricas que devem ser diferenciadas de outras causas de neuropatia, como, por exemplo, diabetes mellitus ou distúrbios nervosos como esclerose múltipla, doença de Parkinson, entre outros. Devido à susceptibilidade de pacientes com mieloma a infecções, é bastante comum ocorrerem infecções virais no tecido nervoso, mais particularmente varicela zóster (cobreiro), herpes zóster (cobreiro), vírus de Epstein-Barr (mononucleose), ou citomegalovírus, o qual pode resultar em paralisia de Bell (paralisia parcial da face) ou outras complicações. Plasmocitomas - Podem causar compressão ou deslocamento dos nervos, da medula espinhal ou até mesmo do tecido cerebral, tanto em ossos como em tecidos moles. Esses efeitos de compressão normalmente representam uma emergência médica e requerem tratamento imediato com doses elevadas de corticosteroides, radioterapia ou neurocirurgia. Infecções - a predisposição a infecções talvez seja a característica única mais representativa de pacientes com mieloma, além da tendência forte a doença óssea. Os mecanismos responsáveis pela suscetibilidade a infecção ainda não são totalmente compreendidos. A presença de mieloma ativo na medula óssea resulta em inibição das funções imunológicas normais, incluindo inibição da produção normal de anticorpos (manifestada pela hipogamaglobulinemia), comprometimento da função dos linfócitos T e função de monócitos/macrófagos ativada, porém anômala. Alguns estudos indicam que um fator proveniente dos macrófagos ativados tanto intensifica a atividade do mieloma quanto inibe a função dos linfócitos T e a produção de imunoglobulinas normais. Os pacientes com mieloma são susceptíveis a infecções virais e infecções por bactérias encapsuladas como os pneumococos. Contudo, devido à neutropenia e aos efeitos da quimioterapia de alta dose, além dos efeitos locais adicionais de cateteres implantados (p. ex., catéteres de Hickman ou Groshon ou linhas PICC), os pacientes com mieloma submetidos a terapia podem apresentar uma ampla variedade de infecções bacterianas, fúngicas e oportunistas. Resumindo, os aspectos-chave das infecções em pacientes com mieloma são: Imunidade reduzida devida ao mieloma Contagem de leucócitos reduzidas devido ao crescimento do mieloma na medula óssea e/ou ao impacto do tratamento. Infecção, ou qualquer indício de infecção, não devem ser ignorados. Um análise de pronto é requerida para avaliar a necessidade de terapia imediata com antibióticos e/ou antivirais. Muitos pacientes aprendem a ter terapias à mão para o caso de emergências. ALTERAÇÕES ÓSSEAS EFEITOS ASSOCIADOS A DESTRUIÇÃO ÓSSEA MIELOMA EXTRAMEDULAR SANGUE PERIFÉRICO ALTERAÇÕES DE PROTEÍNAS PLASMÁTICAS ANORMALIDADES RENAIS Tabela 2: Esquema da fisiopatologia Lesões osteolíticas solitárias ou múltiplas. Osteoporose difusa (osteopenia). Cálcio sérico elevado. Hipercalciúria (aumento do cálcio na urina). Fraturas ósseas. Diminuição da estatura (colapso vertebral). Envolvimento de tecido mole, mais frequentemente na região da cabeça/ pescoço (p. ex., nasofaringe); também no fígado, nos rins em outros locais em tecidos moles. Anemia. Coagulação anormal. Leucopenia. Trombocitopenia. Leucemia de plasmócitos. Linfócitos B monoclonais circulantes precursores das células do mieloma). Hiperproteinemia (proteína elevada). Hipervolemia (expansão do volume). Imunoglobulinas monoclonais (IgG, IgD, IgA, IgM, IgE, cadeias leves). Diminuição do gap aniônico (nível baixo de sódio sérico). ß2-microglobulina sérica elevada. Albumina sérica baixa. Nível sérico elevado de IL-6 e Proteína C-Reativa. Proteinúria, cilindros sem leucócitos ou eritrócitos. Disfunção tubular com acidose. Uremia (insuficiência renal). Amiloidose e disfunção renal. TIPOS DE MIELOMA O tipo de proteína monoclonal produzida varia de paciente para paciente. A mais comum é a IgG e a mais rara é a IgE. A Tabela 3 mostra a porcentagem dos diferentes tipos de mieloma. Cada tipo está associado a padrões de doença ligeiramente diferentes. Por exemplo, o mieloma IgA costuma estar mais associado a doença fora do osso (doença extra medular), enquanto o mieloma IgD é mais comumente associado à leucemia de plasmócitos e ao dano renal. 17
10 Tabela 3: Tipos de proteína monoclonal (%) Soro % Totais IgG IgA IgD IgE Urina (apenas cadeias de Bence Jones ou leves) tipos k Duas ou mais paraproteínas monoclonais Apenas cadeias pesadas (G ou A) Ausência de paraproteína monoclonal IgM (raramente mieloma, caracteristicamente associada à Macroglobulinemia de Waldenstrom) <0,01 <1 <1 1 75% 11% 2% 12% Totais 100% Fonte: Dados de pacientes com MM coletados e analisados por Pruzanski e Ogryzlo, SINTOMAS CLÍNICOS Cerca de 70% dos pacientes com mieloma apresentam dor de intensidade variada, frequentemente na região lombar ou costelas. A dor intensa repentina pode ser um sinal de fratura ou colapso de um corpo vertebral. Mal-estar geral e queixas indefinidas são frequentes. Perda de peso significativa é rara. Tanto a neutropenia como a hipogamaglobulinemia aumentam a probabilidade de infecções. Embora a pneumonia pneumocócica seja a infecção clássica associada ao mieloma no diagnóstico, outras bactérias, como os estreptococos e os estafilococos, são agora frequentemente isoladas. Também ocorrem herpes zóster e infecções por hemófilos. A hipercalcemia, encontrada em 30% dos pacientes no diagnóstico, causa cansaço, sede e náusea. A precipitação dos sais de cálcio pode resultar em deterioração da função renal. É importante destacar que nos últimos anos a incidência de hipercalcemia em pacientes recém diagnosticados caiu para 10-15% provavelmente devido a diagnóstico precoce. Na América Latina e em algumas partes da Ásia onde o diagnóstico tardio é comum, a hipercalcemia continua mais comum. A hiperviscosidade devido aos níveis elevados de proteína do mieloma, pode provocar problemas como hematomas, sangramento nasal, visão turva, cefaleia, sangramento gastrintestinal, sonolência e uma variedade de sintomas neurológicos isquêmicos causados pela redução do suprimento de sangue e oxigênio ao tecido nervoso. A hiperviscosidade ocorre em < 10% dos pacientes com mieloma e em cerca de 50% dos pacientes com macroglobulinemia de Waldenstrom (paraproteína IgM ou componente M). O aumento do sangramento é normalmente acentuado pela trombocitopenia, assim como pela ligação das proteínas monoclonais a fatores de coagulação e/ou plaquetas. O envolvimento neurológico pode resultar em problemas específicos, dependendo da localização dos nervos afetados. Compressão da medula espinal, meningite e síndrome do túnel do carpo são problemas particularmente comuns. Embora os dois primeiros eventos sejam decorrentes da formação ou infiltração de tumor de plasmócitos, a síndrome do túnel do carpo normalmente é causada pela deposição de substância amilóide (deposição de proteínas de Bence Jones em uma forma ß-pregueada especial). Estadiamento e Fatores Prognósticos O prognóstico em mieloma é determinado tanto pelo número quanto pelas propriedades específicas das células do mieloma em um determinado paciente. Essas propriedades específicas incluem a taxa de crescimento (fração) das células do mieloma, a taxa de produção de proteínas monoclonais e a produção ou não-produção de várias citoquinas e substâncias químicas que danificam ou comprometem significativamente outros tecidos, órgãos ou funções orgânicas. Em 1975, o sistema de estadiamento de Durie/Salmon foi desenvolvido (vide Tabela 4). Esse sistema reúne os principais parâmetros clínicos correlacionados à massa celular de mieloma medida (número total de células do mieloma no organismo). O sistema de estadiamento de Durie/Salmon continua a ser usado no mundo todo, principalmente porque ele fornece a melhor correlação direta com características clínicas individuais do paciente. Pacientes em estágio I tem doença indolente, pacientes com estágios II e III tem mieloma ativo. Em 2005 um novo sistema de estadiamento foi desenvolvido pelo International Myeloma Working Group, patrocinado pela IMF. Dados clínicos e laboratoriais foram coletados de pacientes com mieloma sintomático não tratados previamente, de 17 instituições localizadas na América do Norte, Europa e Ásia. Fatores prognósticos potenciais foram avaliados usando uma variedade de técnicas estatísticas. Surgiram como fatores prognósticos importantes a ß2- microglobulina sérica (Sß2M), albumina sérica, número de plaquetas, creatinina sérica e idade, sendo então adicionalmente analisados. A combinação de ß2-microglobulina sérica (Sß2M) e albumina sérica forneceu a melhor, mais poderosa, mais simples e reproduzível classificação de três estádios. Este novo Sistema de Estadiamento, International Staging System (ISS) foi completamente validado e está demonstrado na tabela 5. O ISS foi adicionalmente validado ao demonstrar sua efetividade em pacientes na América do Norte, Europa e Ásia, com mais e menos de 65 anos de idade; com terapia padrão ou transplante autólogo em comparação com Sistema Durie/Salmon. O ISS é simples, baseado em variáveis fáceis de serem usadas (ß2-microglobulina sérica e albumina sérica) e foi introduzida para uso mais abrangente. O mieloma pode ainda ser classificado baseado em risco genético utilizando a técnica de hibridização fluorescente in situ (FISH) e características citogenéticas identificadas nas células de mieloma da medula óssea. Tal classificação tem implicações importantes para o tratamento. Doença de maior risco é definida como a presença de quaisquer das mutações genéticas a seguir: t(4;14), t(14;16), t(14;20), deleção do 17p por FISH, ou deleção do cromossomo 13 ou hipodiploidia por citogenética de metáfase convencional. É crucial estar consciente de que o risco genético é muito influenciado pelo tratamento selecionado. Por exemplo, a deleção de 17p por FISH é o único fator que consistentemente correlaciona com resultados desfavoráveis com todas as terapias disponíveis em Mutuamente, a presença de t(4;14), a qual tem sido notada como um fator de risco desfavorável no passado, tem sido largamente superada com a introdução de regimes de combinação de VELCADE (bortezomibe). Em diversos estudos de Revlimid houve também um impacto positivo de regimes de contenção de lenalidomida- (Revlimid ) em pacientes com t(4;14); Um relato recente de um grupo IFM francês indicou que a presença de t(14;16) também não era mais um fator prognóstico preditivo nos seus estudos. É antecipado que novos e melhores sistemas 19
11 de classificação serão introduzidos com o tempo e irão possivelmente oferecer melhor seleção de tratamento, baseado em resultados documentados de tratamento com novas abordagens de combinação. 20 Tabela 4: Sistema de Estadiamento de Durie e Salmon Critérios ESTADIO I (massa celular baixa) Todos os itens seguintes: Valor de hemoglobina > 10 g/dl Valor de cálcio sérico normal ou < 10,5 mg/dl Raio X ósseo, estrutura óssea normal (escala 0) ou apenas plasmocitoma ósseo solitário Taxa baixa de produção do componente M: Valor de IgG < 5,0 g/dl Valor de IgA < 3,0 g/dl Componente M de cadeia leve na urina por eletroforese < 4 g/24h ESTADIO II (massa celular intermediária). Não se enquadra nem no estádio I nem no III. ESTADIO III (massa celular elevada) Um ou mais dos seguintes itens: Valor de hemoglobina < 8,5 g/dl Valor de cálcio sérico > 12 mg/dl Lesões ósseas líticas avançadas (escala 3) Taxa elevada de produção do componente M: Valor de IgG > 7,0 g/dl Valor de IgA > 5,0 g/dl Componente M de cadeia leve na urina poreletroforese > 12 g/24h SUBCLASSIFICAÇÃO (A ou B) A: função renal relativamente normal valor de creatinina sérica < 2,0 mg/dl B: função renal anormal valor de creatinina sérica > 2,0 mg/dl Exemplos: Estadio IA (massa celular baixa com função renal normal) Estadio IIIB (massa celular elevada com função renal anormal) *células do mieloma no corpo todo Massa de células do mieloma medida (células do mieloma em bilhões/m²)* 600 bilhões* 600 a bilhões* > bilhões* DEFINIÇÃO DE RESPOSTA CLÍNICA Os novos critérios de resposta uniforme do International Myeloma Working Group (IMWG) são recomendados para classificar a resposta (veja tabela 7). As melhoras em componente-m devem ser associados a evidências de melhora clínica (tais como diminuição da dor óssea, melhora da contagem de eritrócitos). É importante ter em mente que uma regressão percentual maior não confere automaticamente maior sobrevida. Quando há doença residual, as características das células do mieloma resistentes ao medicamento remanescente irão determinar o resultado. Essas células do mieloma remanescentes podem, ou frequentemente não podem, ter uma tendência a re-crescimento imediato (recidiva). Se não há re-crescimento, isto é o que é chamado de fase platô : doença residual, porém estável. A fração de células do mieloma resistentes depende principalmente das características moleculares intrínsecas do mieloma individual e da carga do tumor pré-tratamento ou estádio. Os pacientes que respondem ao tratamento vão do alto risco para um risco mais baixo até que idealmente não apresentem mais nenhum sinal de mieloma ou até que atinjam fase platô estável, mas com doença residual mensurável. O tempo necessário para atingir a fase platô é variável, variando de 3 a 6 meses (resposta rápida) a 12 a 18 meses (resposta lenta). Por favor, faça referência à Figura 4 na página 6. Conforme os tratamentos melhoraram, se tornou mais importante avaliar a resposta ao tratamento da forma mais precisa possível. Além da profundidade da resposta, a qual é indicada pela RP (melhora 50%) ou RPMB (Resposta Parcial Muito Boa) ( 90%) precisa-se considerar a duração da resposta. Dois importantes termos são: TTP - Time to Progression - (Tempo para Progressão): é o tempo do início do tratamento até recidiva. PFS Progression Free Survival - (Sobrevida Livre da Progressão da Doença): a duração da sobrevida na qual o paciente ainda está em remissão*. * A remissão é geralmente considerada uma resposta ( ao mesmos remissão parcial) que dura no mínimo 6 meses. I II III ESTADIO Tabela 5: International Staging System CRITÉRIO ß-2 microglobulina sérica < 3,5 mg/dl Albumina sérica 3,5 g/dl ß-2 microglobulina sérica < 3,5 mg/dl Albumina sérica < 3,5 g/dl Ou ß-2 microglobulina sérica 3,5 5,5 mg/dl ß-2 microglobulina sérica > 5,5 mg/dl *Existem duas categorias para o estadio II ß -2 microglobulina sérica < 3,5 mg/l, mas albumina sérica < 3,5 g/dl, ou ß -2 microglobulina 3,5-5,5 mg/l independente da albumina sérica. 21
12 22 TRATAMENTO VISÃO GERAL Consulte a seção Histórico para uma visão geral da evolução dos tratamentos usados atualmente. Desde a introdução da Melfalano em 1962, vários regimes quimioterápicos de combinação tem sido utilizados e tentativas têm sido feitas para melhorar os resultados usando regimes quimioterápicos da altas doses com transplante de medula óssea (TMO) ou transplante de células-tronco sanguíneas periféricas (TCTP). No tipo padrão de TMO ou TCTP, o transplante é um resgate com célulastronco normais de medula óssea quando ocorre destruição das células-tronco do organismo pela quimioterapia de alta dose (geralmente Melfalano). Até o momento não há consenso sobre a melhor forma de tratar o mieloma. Contudo, algumas orientações são apresentadas a seguir. Nas décadas de 80 e 90, Melfalano em alta e resgate de célula tronco era uma das poucas técnicas/tratamentos disponíveis para reduzir o fardo do tumor de mieloma e atingir resultados melhores. Com a introdução de talidomida para o tratamento de mieloma em 1997, as opções subitamente mudaram. Resposta completas podiam ser atingidas com um único agente oral. Novos agentes adicionais seguiram em rápida sucessão: primeiro VELCADE, então Revlimid, e agora carfilzomibe e pomalidomida, os quais estão colocados para aprovação precoce pela FDA. Outros agentes, tais como elotuzimabe, vorinostate, panobinostate e outros, estão mostrando resultados promissores. Não há resposta única para a questão da melhor opção de tratamento disponível em Felizmente há inúmeros regimes que produzem respostas muito profundas (mais do que 90% de redução do componente-m [RPMB]), respostas duráveis (remissões durando 2 anos) e sobrevida geral melhorada. A melhor escolha para cada paciente depende de fatores individuais, como idade, estádio, características genéticas, estado dos rins, e, claramente, preferência pessoal. Tem se tornado um questão aberta se é necessário transplante autólogo imediato como parte do primeiro tratamento ou se pode ser oferecido como uma opção na primeira recidiva, por exemplo. É importante que pacientes com mieloma estejam conscientes da necessidade da discussão cuidadosa com seus médicos. EXCLUIR GMSI OU MIELOMA ASSINTOMÁTICO A primeira e mais importante decisão é certificar-se de que a terapia é necessária. Os pacientes com GMSI e mieloma assintomático (Tabela 1) devem ser atentamente observados, mais do que tratados. Atualmente, não existem terapias capazes de intensificar a regulação imunológica do mieloma inicial ou reduzir a probabilidade de ativação da doença. Entretanto, há diversos estudos de pesquisa em andamento para avaliar se o tratamento precoce é benéfico em certos pacientes. Um grande estudo cooperativo em grupo (ECOG/SWOG combinado) foi iniciado em setembro de Pacientes com mieloma indolente de alto risco são randomizados em Revlimid vs. placebo. A terapia com bisfosfonato pode ser usada para pacientes com doença óssea no estagio inicial. Eritropoietina poderia ser considerada para tratamento da anemia isolada, tendo em mente as ressalvas relacionadas a esse agente. Tratamento anti mieloma específico é recomendado quando mieloma evolui para sintomático, sendo refletido por um aumento no componente M e/ou problemas clínicos iminentes ou emergentes ou fatores CRAB (Tabela 1). Os problemas que justificam o tratamento incluem destruição óssea (lesões líticas e/ou osteoporose), insuficiência renal, redução progressiva em contagens sanguíneas (p. ex., anemia, neutropenia), cálcio sanguíneo elevado, dano neural ou outro dano significativo a tecido ou órgão causado pelo mieloma ou pela proteína do mieloma. Essas indicações para necessidade de iniciar o tratamento podem ser sumarizadas como características CRAB: elevação do Cálcio, problemas Renais, Anemia ou problemas Ósseos. Os objetivos gerais do tratamento são resolver problemas específicos e controlar a doença de um modo geral. O resumo dos tipos de tratamento pode ser encontrado na Tabela 6 e as drogas quimioterápicas mais usadas são detalhadas na Tabela Quimioterapia Tabela 6: Opções de Tratamento para Mieloma 2. Quimioterapia de alta dose com transplante de células-tronco hematopoiéticas. 3. Radiação 4. Terapia de manutenção 5. Terapia de suporte: Eritropoietina* Analgésicos Bisfosfonatos Fatores de crescimento Antibióticos Ortose/colete Exercícios Tratamento de emergência (p. ex., diálise, plasmaferese, cirurgia, radiação). 6. Controle de doença refratária ou resistente a medicamento. 7. Tratamentos novos e emergentes: Talidomida e Revlimid, e IMiD de próxima geração, pomalidomida, em estudos clínicos VELCADE (inibidores de proteossomo) e inibidores de proteossomo de próxima geração, p. ex. carfilzomibe, NPI-0052, em estudos clínicos. Doxil (doxorubicina lipossomal peguilada) para substituir Adriamycin injetável. Trisenox (trioxido de arsênico) e ZI)-101 (arsênico orgânico) em estudos clínicos. Transplante mini-alogênico (não mieloablativo). Inibidores de histona deacetilase (HDAC), p. ex. vorinostate, panobinostate, em estudo clínicos. Anticorpos monoclonais em estudos clínicos, p. ex. elotuzumabe. * com ressalvas 23
13 1. TRATAMENTO ANTI-MIELOMA SISTÊMICO Introdução O primeiro tratamento específico para o mieloma foi a Melfalano, introduzida em Embora o uso da combinação oral simples de Melfalano com prednisona ainda seja uma abordagem válida, vários fatores podem agora influenciar na escolha deste tipo de terapia. Melfalano pode danificar as células-tronco normais da medula óssea e, portanto, é evitada em pacientes que planejam coletar células-tronco. Como idade avançada (> 70 anos) não é um empecilho absoluto para a coleta e transplante de células-tronco, a opção do transplante de célula-tronco deve ser considerada para cada paciente individualmente. RECOMENDAÇÕES de tratamento SE A COLETA DE CÉLULAS TRONCO NÃO É UMA OPÇÃO PLANEJADA A abordagem do tratamento mudou substancialmente com a introdução dos novos agentes talidomida, bortezomibe (VELCADE ), lenalidomida (Revlimid ). Embora Melfalano/prednisona (MP) ainda seja uma opção para pacientes mais idosos, duas novas combinações com MP (Tabela 9) emergiram e são superiores a MP para pacientes que não são elegíveis para transplante: Melfalano/prednisona/talidomida (MPT) e bortezomibe (VELCADE )/Melfalano/prednisona (VMP). Além dessas, tanto talidomida com dexametasona (Tal/Dex), bem como lenalidomida (Revlimid ) com baixas doses de dexametasona (RevloDex) estão disponíveis para uso em ambientes de exclusão de transplante. Melfalano/Prednisona/Talidomida (MPT): NCCN (National Comprehensive Câncer Network Rede Nacional Compreensiva de Câncer) escolha de categoria 1* - Três estudos randomizados compararam MP com MPT. Todos os estudos demonstraram uma taxa de resposta mais alta, remissão mais longa e sobrevida livre de progressão da doença (SLP) com MPT. O risco de eventos de trombose venosa requerem profilaxia apropriada, dependendo de características individuais do paciente. (Veja as diretrizes do International Myeloma Working Group para prevenção da trombose relacionada à talidomida e lenalidomida em mieloma). * Categorias de Evidência e Consenso NCCN são: Categoria 1: a recomendação é baseada em evidência de alto nível (p.ex. estudos randomizados controlados) e há consenso NCCN uniforme; Categoria 2A: a recomendação é baseada em evidência de menor nível e há consenso NCCN uniforme; Categoria 2B: a recomendação é baseada em evidência de menor nível e não há consenso NCCN uniforme (mas sem grandes desacordos); e Categoria 3: a recomendação é baseada em qualquer nível de evidência mas reflete desacordos importantes. Melfalano/Prednisona/Revlimid (MPR): NCCN escolha de categoria 2A Resultados de um estudo MM-015 italiano em andamento demonstraram que MPR confere uma vantagem significativa sobre MP na sobrevida livre de progressão. No entanto, preocupações surgiram sobre toxicidades desfavoráveis, incluindo um pequeno risco de desenvolvimento de novos cânceres primários. Este risco está atualmente sob investigação. Tabela 7 - Critérios de Resposta Uniforme do International Myeloma Working Group: RC e Outras Categorias de Resposta Subcategoria de resposta RCE (scr) (Resposta Completa Estrita) RC (CR) (Resposta Completa) RPMB (VGPR) (Resposta Parcial Muito Boa) Critério de Resposta A RC definida conforme os critérios abaixo, mais: Razão de FLC normal, e Ausência de células clonais na medula ósseab, avaliado por imunohistoquímica ou imunoflorescênciac Imunofixação negativa no sangue ou na urina, e Desaparecimento de plasmocitomas de partes moles, e Plasmócitos na medula óssea 5%b Proteína M no soro e na urina detectável por imunofixação, mas não mais mensuráveis pela eletroforese, ou Redução de 90% ou mais do nível de Proteína-M no soro mais nível de Proteína M na urina < 100mg por 24h. Redução 50% na proteína M no soro e redução da Proteína M na urina em 24h 90% ou para < 200mg por 24h; Se a proteína M for imensurável no soro e na urina, uma diminuição 50% na diferença entre os níveis de FLC envolvidos e não envolvidos é necessária no lugar do critério de Proteína M. RP (PR) (Resposta Parcial) Se a Proteína M foi imensurável no soro e na urina, e a cadeia leve no soro também não é mensurável, uma redução dos plasmócitos 50% é requerida no lugar da Proteína M, desde que o percentual de base de plasmócitos na medula óssea fosse 30%. Além dos critérios acima listados, se presente no período basal, uma redução 50% no tamanho de plasmocitomas de partes moles também é necessária. Não atendendo aos critérios de RC, RPMB, RP ou doença em progressão (não recomendada para uso como indicador DE (SD) (Doença Estável) de resposta, a estabilidade da doença é melhor descrita ao fornecer estimativa do tempo para a progressão). a - Todas as categorias de resposta requerem duas checagens consecutivas feitas em qualquer momento antes da instituição de qualquer nova terapia; todas as categorias também necessitam de evidência conhecida de progressão ou novas lesões ósseas caso tenham sido feitos estudos radiográficos. Estudos radiográficos não são necessários para satisfazer estes critérios de resposta. b - Confirmação com repetição de biópsia de medula não é necessária. c - Presença/ausência de células clonais é baseado na razão k/. Uma razão anormal por imunohistoquímica e/ ou imunofluorescência requer um mínimo de 100 plasmócitos para análise. Uma razão anormal refletindo a presença de um clone anormal é uma razão k/ de >4:1 ou <1:
14 Bortezomibe (VELCADE )/Melfalano/Prednisona (VMP): NCCN escolha de categoria 1 - Um estudo randomizado de grande porte (Estudo VISTA) envolvendo 682 pacientes com idade média de 71 anos, demonstrou resultados melhorados com VMP versus MP e resultou na aprovação do FD para VELCADE neste ambiente de primeira linha. A resposta, a duração da remissão e a sobrevida geral foram superiores com VMP. A ressalva mais importante é que 13% dos pacientes que receberam VMP tiveram neuropatia grave (Grau 3 ou 4) com a combinação com VELCADE. Embora a neuropatia foi reversível na maioria dos pacientes, essa é uma preocupação importante. Bortezomibe (VELCADE )/Melfalano/Prednisona/Talidomida (VMPT): Ainda não listada por NCCN - VELCADE semanal com um dose reduzida de talidomida em combinação com MP (estudo GIMEMA) demonstrou uma resposta aumentada e maior sobrevida livre de progressão em comparação com VMP, com taxas reduzidas de neuropatia periférica e descontinuação de terapia. Talidomida/dexametasona (Tal/Dex): NCCB escolha de categoria 2B e lenalidomida (Revlimid )/ dexametasona baixa dose (RevloDex): NCCB escolha de categoria 1 Embora ainda não testadas exclusivamente no ambiente de transplante não planejado, Tal/Dex e RevloDex podem ser opções àqueles que não queiram proceder ao transplante imediatamente, bem como para aqueles que são elegíveis ao transplante. Com a aprovação do regime lenalidomida/dexametasona (Rev/dex) no ambiente de recidiva e com estudos muito promissores em andamento no ambiente de primeira linha, a combinação RevloDex tem se tornado uma opção popular para terapia de indução. Um importante estudo ECOG (E4A03) mostrou resultados excelentes com Revlimid mais dexametasona baixa dose (semanal) contra Revlimid mais dexametasona convencional (pulso de 4 dias); As porcentagens de efeitos colaterais precoces foram muito baixas com RevloDex, assim como a chance de mortalidade precoce, que foi de apenas 0,5% (dentro dos 4 primeiros meses). Assim, RevloDex se tornou uma excelente opção para indução. A única precaução maior é para pacientes desejando reter a opção de coleta de células-tronco. Pesquisadores na Mayo Clinic notaram menores rendimentos de células-tronco após indução com Rev/dex, com uma pequena porção de pacientes não coletando células-tronco adequadas para transplante usando apenas fator de crescimento Neupogen para coleta. No presente momento, 98% dos pacientes recebem terapia de indução nos EUA com pelo menos um dos novos agentes. Um cadastro realizado recentemente mostrou que combinações de Revlo/ Dex e VELCADE são usadas em números aproximadamente iguais no ambiente de primeira linha, com talidomida/dex sendo menos frequentemente usada. Bortezomibe (VELCADE )/Dexametasona (RVD): NCCN escolha de categoria 2B Estudos demonstraram até o momento resultados muito promissores para essa combinação. Estudos de Fase III nos ambientes de diagnóstico recente e de recidiva estão em andamento. Enquanto ainda não aprovados pela FDA tanto no ambiente de primeira linha quanto no de recidiva, esse regime não é frequentemente prescrito nos Estados Unidos. Um desenvolvimento recente importante foi o estudo randomizado de Fase III de liderança francesa no qual a eficácia e toxicidade de VELCADE subcutâneo e intravenoso foram avaliadas. O estudo determinou que a eficácia foi igual em ambos os braços, e que neuropatia periférica de grau 2 ou maior foi reduzida no braço subcutâneo. VISÃO GERAL DAS RECOMENDAÇÕES DE TERAPIA INICIAL PARA PACIENTES NÃO ELEGIVEIS AO TRANSPLANTE MPT e VMP são opções recomendadas e apoiadas por excelentes resultados de estudo de Fase III. Um acompanhamento mais longo é necessário para avaliar os resultados em prazo mais longo com MPT e VMP. Dados iniciais sugerem que VMP possa superar o impacto negativo das características desfavoráveis de prognóstico dos cromossomos. O risco de TVP é uma preocupação com MPT, mas não com VMP. MPT é um regime completamente oral, enquanto VMP incorpora o componente intravenoso (IV) VELCADE. A neuropatia dolorosa com VMP é possivelmente uma preocupação maior, embora a redução da frequência de VELCADE para uma vez por semana pode aliviar esse problema. Alternativamente, as opções simples de duas drogas, MP, Tal/Dex, RevloDex ou Vel/Dex, podem ser consideradas dependendo da situação clínica. SE A COLETA DE CELULAS-TRONCO É PLANEJADA A abordagem para terapia de primeira linha ou de indução evoluiu e mudou consideravelmente nas duas últimas décadas. Quimioterapia com VAD: Categoria NCCN de escolha 2B - O protocolo VAD, introduzido em 1984, tornou-se uma alternativa popular à indução com MP ou CP. Desvantagens significativas, incluindo possíveis infecções e problemas de coagulação sanguínea, assim como taxas de resposta superiores talidomida/dexametasona, Revlimid /dexamestasona, e bortezomibe com ou sem dexametasona, fizeram o VAD se tornar uma opção menos comum ao redor do mundo no momento. Talidomida/dexametasona (Tal/Dex): Categoria NCCN de escolha 2B Thal/dex é uma opção padrão para terapia de primeira linha, com uma taxa de reposta 64%. Aumento da taxa de resposta e uma incidência bem menor de neuropatia periférica com RevloDex tornaram esta nova combinação em uma opção preferida, onde e quando disponíveis. VELCADE : Categoria NCCN de escolha 1 - Em junho de 2008 VELCADE foi aprovado nos Estados Unidos para uso em ambiente de primeira linha. Embora seja um agente único muito eficaz, espera-se que ele seja usado principalmente em terapias de combinação, acrescentando ao arsenal de opções disponíveis para pacientes recém diagnosticado, bem como para aqueles com doenças recidivantes ou refratárias. Várias combinações com bortezomibe (VELCADE ) estão disponíveis: Bortezomibe/talidomida/dexametasona (VTD) Categoria NCCN de escolha 1 Cavo et al recentemente compararam talidomida/dexametasona ao VTD em um estudo controlado randomizado envolvendo 256 pacientes. A RC mais a RPMB após 3 ciclos de 21 dias foi significativamente mais alta para VTD (60%) comparado com talidomida/dexametasona (27%)
15 Tabela 8 - Medicamentos Quimioterápicos Mais Comumente Utilizados Nome do Medicamento (Substância ativa) AGENTES COMUNS Nome Comercial Comentários Melfalano* (M)** Alkeran (VO ou IV) Primeiro agente único para tratamento de mieloma Ciclofosfamida* (C ou CY)** Prednisona (P)** Dexametasona (D)** Vincristina (V ou O)** Doxorrubicina (A)** Bussulfano* (B ou BU)** VP-16 Cisplatina (CP ou P)** NOVOS AGENTES Doxorrubicina Lipossomal Peguilada* Bortezomibe (B,V ou P)** Talidomida (T) Lenalidomida (R ou L) Cytoxan (VO ou IV) Prednisolona (semelhante) (normalmente VO) Decadron (VO ou IV) Oncovin (IV) Adriamicyn (IV) Myleran (VO ou IV) Etoposide (IV) Platinol (IV) Doxil (IV) VELCADE (IV) Thalomid (VO) Revlimid (VO) **Agentes Alquilantes **Abreviaturas comuns Eficácia semelhante à de M, mas com maior toxicidade GI e GU e menor dano a células-tronco da medula óssea. Diretamente ativo, funciona bem com M, C e B. Não causa supressão da medula óssea. Semelhante à prednisona, porém mais potente. Mais efeitos colaterais graves. Não é mais usada comumente como parte do regime de indução VAD, que mostrou ser inferior a VELCADE +Adriamycina +dex Atividade moderada, usada em combinações (p. ex., VAD, ABCM, (VMCP-VBAP). Atividade semelhante à de M e C, geralmente faz parte do tratamento de alta dose e transplante (p. ex., regime BU/CY). Atividade moderada, usado em monoterapia ou terapia combinada. Atividade mínima sozinha; mas usada com VP-16 (E) como parte de combinações (p.ex. EDAP e DT-PACE) Em combinações, atividade promissora, menos toxicidade do que A. Ativo diretamente usado sozinho ou combinações. Ativo diretamente, aprovado para uso em combinação com dexametasona, utilizada em outras combinações. Ativo diretamente, aprovado para uso em combinação com dexametasona, utilizada em outras combinações. Bortezomibe/dexametasona (categoria NCCN de escolha 1) versus VAD Vários estudos demonstraram taxas de respostas globais iniciais (ORR) de 70%-90% com bortezomibe/ dexametasona (Vel/dex) como terapia inicial. Em um estudo recentemente apresentado, Harousseau et al compararam Vel/dex com VAD como indução pré transplante. As taxas de RC + RPMB foram: Vel/dex 47% versus VAD 19% pré-transplante e Vel/dex 62% versus VAD 42% pós transplante autólogo com células-tronco ambas com diferenças significativas. Outras combinações com bortozemibe: Várias combinações com bortezomibe (VELCADE ) estão sendo avaliadas atualmente. Muitas têm apresentado resultados promissores em estudos de Fase II-III, incluindo: VCD (VELCADE /Cytoxan /Dex, também conhecido como CyborD) categoria NCCN de escolha 2A; VELCADE /Doxil ± Dex categoria NCCN de escolha 2B; VRD (VELCADE /Revlimid /Dex) - categoria NCCN de escolha 2B. Um estudo Mayo recente de VRD vs. VCD vs. VCRD (VELCADE / Cytoxan /Revlimid /Dex) indicou que todos os regimes tinham eficácia similar, mas que a combinação de quatro medicamentos causava maior toxicidade e requeria redução de dose mais frequentemente. Dados de acompanhamento de longo prazo ainda estão sendo coletados e avaliados. Mayo antecipou que conduz um estudo comparando VCD e VRD. Adicionalmente, bortezomibe é parte de diversas novas combinações de medicamentos nas quais a sinergia é esperada (veja seção Medicamento Recidiva/Novo nas páginas 35-37). Combinações de Revlimid em ambiente pré transplante - Os resultados com a lenalidomida (Revlimid )/ dexametasona já foram mencionados. Na essência, Rev/Dex pode ser usado para indução quando há intenção de se prosseguir para a coleta e transplante de células-tronco, embora não tenha sido a prioridade nos estudos conduzidos até agora. Os resultados da indução são excelentes e comparáveis aos das combinações com bortezomibe. Para o cultivo de células-tronco pode ser necessária a administração de fator de crescimento mais ciclofosfamida ou plerixafor (Mozobil ) versus fator de crescimento sozinho (ex. Neupogen ). Mais estudos são necessários para explorar o uso de Revlimid no ambiente pré transplante. Recomendações de Terapia de Indução para Candidatos ao Transplante - As opções apoiadas por estudos randomizados Fase III são: Tal/Dex (TD) VELCADE /Dex (VD) VELCADE /Talidomida/Dex (VTD) Revlimid / Dex em baixa dose (RevloDex - Rd) Todos os quatros regimes podem produzir respostas rápidas e em taxas altas. TD e Rd são esquemas exclusivamente orais; VTD e VD tem o componente intravenoso VELCADE. Ambos TD e Rd apresentam risco aumentado de coágulos sanguíneos (trombose venosa profunda, ou TVP) e requerem tratamento com ácido acetilsalicílico (aspirina) ou outro tratamento anticoagulante. A neuropatia é uma das preocupações dos regimes com talidomida e VELCADE. É um desafio selecionar o melhor tratamento para cada paciente. É preciso considerar os primeiros riscos precoces do tratamento, respostas e duração da remissão, riscos de TVP e neuropatia, conveniência e custos. A presença de características genéticas de alto risco e/ou comprometimento renal podem direcionar a escolha para as combinações com VELCADE. É crucial que haja um diálogo aberto para avaliação de prós e contras
16 MP CP ABCM VAD D ou MD ou CD TD MPT MPR VMP VMPT RD ou Rd BD ou VD RVD CVD ( CyborD ) Tabela 9 - Combinações Frequentemente Utilizadas Primeira combinação padrão para terapia inicial. Alternativa a MP. Combinação usada na Europa, particularmente no Reino Unido. Poucos benefícios adicionais em comparação a MP. Já foi a combinação alternativa a MP mais comum, agora sendo cada vez mais substituída por combinações mais ativas, incluindo novas terapias. D sozinha ou combinada a M ou C pode ser usada como alternativa ao VAD. Torna desnecessária a infusão por 4 dias. (Tal/Dex) - combinação de primeira linha, agora sendo substituída por Ver/dex nos EUA (MP + Tal) - aumenta eficácia de MP (MP + Rev) - para aumentar a eficácia de MP. (MP+VELCADE ) aprovação do FDA para uso de primeira linha. (MP+frequência reduzida de VELCADE e dose reduzida de talidomida). Para aumentar a eficácia de MP com menos neuropatia. (Rev/Dex) - combinação cada vez mais popular para terapia de primeira linha (categoria NCCN 1). D = dose completa de Dex. d = baixas doses de Dex, um dia por semana. (VELCADE /Dex) aprovado pela FDA para terapia de primeira linha. (Revlimid +VELCADE +dex) Combinação promissora em estudos clínicos recentes tanto para mieloma recidivante quanto recém diagnosticado. (Cytoxan +VALCADE +dex) Combinação promissora em estudos tanto para mieloma recidivante quanto recém diagnosticado. 2. TRANSPLANTE TERAPIA DE ALTA DOSE (HDT) COM TRANSPLANTE AUTÓLOGO DE CÉLULAS-TRONCO (ASCT) O papel do transplante autólogo tem sido extensamente revisto. Foi demonstrado que terapias de alta dose com transplante autólogo de células-tronco melhora ambas as taxas de resposta e de sobrevida em pacientes com mieloma. Entretanto esta abordagem não é curativa. Com a introdução de novas abordagens combinatórias, somadas ao ASCT, alguns investigadores estão introduzindo a noção de que um subgrupo de pacientes ( risco bom ) podem ter sobrevida estendida e podem atingir cura funcional (definida como remissão completa por 4 anos). Taxa de remissão completa com terapia de alta dose como parte planejada da terapia de primeira linha pode ser 90% com novas estratégias pré e pós-transplante. O benefício adicionado da incorporação (ou não) do auto-transplante está sob revisão no momento. Morbidade e mortalidade Com os fatores de crescimentos atuais, antibióticos, e outros cuidados de suporte à saúde, a mortalidade relacionada ao procedimento com HDT é muito baixa: <5%. A maioria dos centros usam somente a Melfalano de alta dosagem intravenosa a uma dose de 200 mg/m2 como um regime preparativo. Como o uso de irradiação corporal total (TBI) adiciona toxicidade sem benefícios claros na sobrevida, poucos centros recomendam TBI como parte do regime de preparação. Análises de qualidade de vida e de custo/benefício têm sido conduzidas comparando terapia de alta dose com quimioterapia de dose padrão. O Nordic Myeloma Study demonstrou tanto melhorias na qualidade de vida quanto aumento de sobrevida (sobrevida mediana de 62 meses versus 44), porém com altos cultos adicionais. Recomendações atuais Altas doses de quimioterapia com transplante autólogo de células tronco deve ser fortemente considerado como parte da terapia de primeira linha para pacientes recém diagnosticados com mieloma sintomático. a) O regime de condicionamento padrão é melfalano 200 mg/m2. Radiação corporal total não é recomendada. b) O transplante de células tronco não é recomendado devido a custos adicionais sem aumento de benefícios clínicos. c) Células troncos sanguíneas-periféricas são recomendadas ao invés da medula óssea tanto pela facilidade de coleta como pelo enxerto mais rápido. d) Os regimes pré-transplantes são discutidos acima. e) Várias combinações de novas terapias estão sendo introduzidas como regime pré-transplante
17 PAPEL DO TRANSPLANTE NO MOMENTO DA PRIMEIRA RECIDIVA Parte do processo de decisão pelo autotransplante envolve conhecimento do impacto de espera, com vista do transplante na recidiva. Dados de dois estudos randomizados franceses não indicarem redução na sobrevida geral à partir da espera até o momento do transplante na recidiva. A qualidade de vida torna-se uma consideração importante. Por um lado, se o transplante não for realizado como uma estratégia primária planejada, então a terapia adicional típica, incluindo a manutenção é exigida, com efeitos colaterais e toxicidade correspondentes. Por outro lado, o maior impacto do transplante é deferido, o qual é uma escolha pessoal para alguns pacientes. Terapias combinadas que incluem novos agentes Revlimid, talidomida, e VELCADE como tratamentos de primeira linha são resultantes e a frequência livre de progressão comparáveis a isso de ASCT, permitindo pacientes e seus médicos escolher e adiar ASCT sem sacrificar a eficácia. Um estudo amplo, randomizado, EUA e França de linha de frente de VRD vs.vrd + ASCT ajudará a determinar se a adição de ASCT a nova terapia promoverá benefício adicional ou não. COLETA E ARMAZENAMENTO DE CÉLULAS TRONCO PARA USO POSTERIOR Há uma forte relutância em vários centros que coletam células tronco sem um plano claro de uso, usualmente para uso imediato. Esta relutância surge de prioridades do protocolo, restrições de custo/benefício para a coleta e armazenamento, assim como outros fatores. Entretanto, muitos pacientes exigem e aguardam que suas células tronco sejam extraídas, mesmo que eles não estejam entusiasmados sobre terapia de alta dose imediata. Recomendações Atuais a) A coleta com o armazenamento para uso futuro é recomendada com a revisão baseada em cada caso. b) Há justificativas médicas e científicas para guardar células-tronco para uso posterior. c) O atraso no transplante é uma opção de tratamento viável. Um segundo transplante em um paciente é uma opção viável, especialmente se uma primeira remissão de >2 anos ocorreu. (Veja a discussão abaixo de duplo transplante). O PAPEL DO TRANSPLANTE DUPLO OU TANDEM No momento atual o benefício adicional do transplante duplo ou em tandem versus um transplante autólogo único não está claro. Os resultados com o transplante primário em tandem planejado (Terapia Total 1, 2, 3, 4, e 5 na Universidade do Arkansas) tem sido satisfatórios. A sobrevida média global tem sido de 68 meses, com alguns subgrupos apresentando sobrevidas ainda maiores. Terapia Total 3, que incorpora o uso de VELCADE, parece oferecer taxas de resposta precoces e aumentadas, embora pacientes com certos fatores de risco, incluindo idade avançada, alto LDH, citogenética anormal, ou doença avançada, não são tão prováveis a atingir um benefício estendido. Estudos comparativos recentes, incluindo os estudos randomizados franceses, demonstraram benefícios predominantemente para uma subgrupo de pacientes (aqueles que não estão em CR). É possível que um segmento maior irá mostrar benéficos adicionais. Recomendações Atuais a) Até o momento, transplantes tandem continuam a ser uma opção clínica de estudo nesta abordagem. Um segundo transplante planejado pode ser considerado em pacientes apresentando <VGPR com um primeiro autotransplante. b) Um segundo transplante em um paciente que respondeu bem com um primeiro transplante e recidivou após >2 anos é uma opção útil e viável (Sirohi, 2001). c) Guardar e armazenar células tronco suficiente para um transplante adicional, se adequado, é extremamente recomendado. O PAPEL DO TRANSPLANTE ALOGÊNICO Apesar da melhora médica ao longo das últimas duas décadas, transplante alogênico completo, mesmo com a combinação perfeita de um doador irmão, é um procedimento de alto risco no gerenciamento do mieloma múltiplo. A morbidade e mortalidade iniciais relacionadas ao tratamento são altas. Mesmo em centros com a maior experiência, e em uma cenário de melhor risco, a mortalidade inicial é de pelo menos de 15 a 20%. Em outros centos, é frequentemente relatada uma mortalidade de 20 a 30% ou maior. Complicações pulmonares são geralmente as mais críticas em pacientes com mieloma. As vantagens potenciais do transplante alogênico são as células-tronco livres de mieloma e enxerto versus o efeito do mieloma. Mas, apesar destes fatores, a cura a longo prazo é rara. A taxa de recidiva continua de 7% ao ano com segmento em longo prazo. O enxerto versus o portador da doença podem também ser um problema recorrente, exigindo terapia e reduzindo a qualidade de vida. O enxerto versus o efeito do mieloma podem ser aumentados usando infusões de linfócitos do doador e tem sido clínicamente benéfica em alguns casos. Um estudo recente cooperativo avaliou 710 pacientes randomizados para transplante mini alogênico ou não mieloablativos versus transplantes autólogos em tandem foi apresentado na ASH 2010 (Krishnan et al.) Infelizmente, este estudo demonstrou decisivamente que uma adição planejada do mini transplante alogênico como parte de uma abordagem inicial de transplante duplo introduziu um risco adicional significativo sem benefício de sobrevida sobre o transplante autólogo em tandem. Portanto, uma consideração de rotina desta abordagem não é mais recomendada. Recomendações Atuais a) Transplante totalmente pareado alogênico convencional é raramente recomendado como uma estratégia primária, devido aos altos riscos. b) Transplante mini alogênico é somente recomendado em uma ambiente de estudo clínico. c) Transplante entre gêmeos idênticos, ou singênicos, é uma opção rara, o qual é um procedimento seguro com bom resultado é recomendado como uma consideração quando um gêmeo idêntico estiver disponível. 3. RADIOTERAPIA A radioterapia é uma modalidade importante para o tratamento do mieloma. Em pacientes com problemas locais graves como destruição óssea, dor grave e/ou pressão sobre os nervos ou sobre a medula espinal, o uso de radiação local pode ser dramaticamente eficaz. A principal desvantagem é que a radioterapia danifica permanentemente as células-tronco normais da medula óssea na região tratada. A radiação de campo amplo abrangendo grandes regiões da medula óssea normal deve ser evitada. Uma estratégia geral é contar com a quimioterapia sistêmica para controlar a doença de um modo geral, limitando o uso da radioterapia local a áreas com problemas particulares
18 Radiação Coporal Total (TBI): A radiação corporal total ou sequencial de metade do corpo pode ser usada como parte de uma estratégia global de terapia com altas doses e transplante e/ou no controle de doença refratária recidivante. Embora tenha sido usada no passado como um esquema preparatório para o transplante, estudos recentes demonstraram que não há benefícios adicionais e, infelizmente, a toxicidade é maior. Portanto, a TBI não é mais recomendada como parte de esquemas preparatórios. Em pacientes com doença refratária, a radiação sequencial em metade do corpo pode ser usada para controlar temporariamente a doença. O sucesso desse procedimento raramente dura muito tempo, particularmente em pacientes com mieloma ativo e agressivo. Também há a desvantagem de a radiação com campo amplo destruir a medula óssea normal e dificultar, quando não impossibilitar, o uso de outras opções de tratamento após o seu uso TERAPIA DE MANUTENÇÃO Interferon Alfa - Nos últimos 15 anos, muitos investigadores avaliaram a eficácia do interferon, um agente que mostrou prolongar a remissão obtida com terapia padrão ou de alta dose. Os resultados obtidos foram conflitantes, mas foi observado um pequeno benefício de 10%-15% no prolongamento da remissão e da sobrevida. Diferenças de 10%-15% (p. ex., 6-9 meses) são difíceis de serem comprovadas em estudos clínicos. Embora alguns investigadores acreditem que o interferon alfa tenha um papel definitivo, embora pequeno, no controle do mieloma, os efeitos colaterais associados podem ter um impacto adverso na qualidade de vida do paciente. Prednisona - Tem sido difícil encontrar uma terapia capaz de prolongar as remissões e a sobrevida em mieloma sem comprometer a qualidade de vida, como é o caso do interferon alfa. No entanto, novos estudos confirmaram observações iniciais da década de 80 de que a prednisona é um agente de manutenção eficaz e, provavelmente, superior ao interferon alfa. A prednisona administrada 3 vezes por semana (p. ex., dose inicial de 50 mg) apresenta toxicidade aceitável e pode prolongar tanto a remissão como a sobrevida. Uma vantagem particular é que os pacientes podem tomar prednisona por muitos anos sem desenvolver células de mieloma resistentes. No entanto, é necessário ter cuidado devido aos efeitos colaterais em longo prazo, e reduções de dose costumam ser necessárias. Fármacos Imunomoduladores (IMiDs) Resultados promissores estão sendo acumulados sobre o papel de Revlimid no ambiente de manutenção. Como relatado no encontro anual da ASH de 2010, a terapia de manutenção com Revlimid prolonga significantemente o tempo até a progressão comparado ao placebo quando administrado em pacientes com doença estável, ou melhores após Melfalano alta dose/asct (CALGB, McCarthy et al.), e prolonga significantemente a sobrevida livre de progressão quando administrado a pacientes após ASCT como uma terapia de consolidação seguida por uma dose menor de Revlimid para uma terapia de manutenção (Attal et al.). Dados de segmento do estudo CALGB indicam que Revlimid pós-manutenção de ASCT não somente dobra a sobrevida livre de progressão quando comprado ao placebo, mas também aumenta sobrevida geral. Balanceado contra esses dados favoráveis é o risco baixo, porém aumentado de uma segunda malignidade no braço placebo do estudo. Análises posteriores estão em andamento para determinar a natureza desse risco. VELCADE O estudo HOVON/GMMG de fase III comparando VELCADE, Adriamyacin, e dexametasona (PAD) + manutenção de VELCADE a vincristina, Adriamyacin, e dexametasona (VAD) + manutenção de talidomida, foi apresentada na ASH Não somente VELCADE resultou em melhora na sobrevida global e PFS, mas seu uso como terapia de manutenção administrada em um cronograma de a cada quinze dias foi bem tolerado e resultou em respostas adicionais. Os resultados iniciais também indicaram benefício em pacientes com a deleção do 17p de risco desfavorável no quadro genético do FISH. 5. TERAPIA DE SUPORTE Eritropoietina - A eritropoietina é um hormônio natural atualmente obtido por técnicas de engenharia genética. A eritropoietina é administrada para melhorar o nível de hemoglobina em pacientes com anemia persistente. As injeções de eritropoietina (p. ex., unidades SC por semana) podem demonstrar benefícios muito importantes para o nível de hemoglobina e na capacidade funcional. Seu uso deve ser fortemente considerado em pacientes com anemia persistente. No entanto, sob novas diretrizes estritas, a eritropoietina só deverá ser usada em um ambiente de paciente recebendo tratamento ativo para o mieloma. A eritropoietina só deve ser continuada em pacientes que demonstrarem beneficio claro. Pode ser necessário suplementação com ferro para obter o benefício máximo. Sob as novas diretrizes da FDA, pode ser necessário que os pacientes assinem um termo de consentimento esclarecido para tomar eritropoietina. Como observado anteriormente, Epo recombinante (ex., Epogen ou Procrit ) devem ser usados com precaução devido aos relatos recentes de associação a Epo do aumento no crescimento tumoral e redução da sobrevida em pacientes com câncer, e da identificação de receptores de Epo em células de mieloma, embora isto exija investigação adicional. Figura 5: Como o pamidronato funciona Bisfosfonatos - Os bisfosfonatos são uma classe de substâncias químicas que se ligam à superfície dos ossos danificados em pacientes com mieloma. Essa ligação inibe a destruição óssea em progressão e pode melhorar as chances de cicatrização óssea e recuperação da força e da densidade óssea. Um estudo randomizado com o bisfosfonato pamidronato (Aredia ) mostrou benefício particular em pacientes respondendo à quimioterapia em andamento. Hoje se recomenda que a terapia com bisfosfonatos seja uma medida adjuvante em pacientes com mieloma que apresentam problemas ósseos (vide Figura 5). Outros bisfosfonatos estão disponíveis atualmente, entre eles, o clodronato (Bonefos ), uma formulação oral usado na Europa para o tratamento de doença óssea de mieloma, e o ácido zoledrônico (Zometa ), aprovado nos EUA e na Europa para tratamento de hipercalcemia e doença óssea. Vários bisfosfonatos novos estão sendo testados em estudos clínicos para mieloma. Um, chamado de ibandronato (Boniva ), está sendo usado na Europa. Nos EUA, é atualmente aprovado pelo FDA somente para o uso da osteoporose pósmenopausa. No encontro anual da Sociedade Americana de Hematologia de 2010, uma comparação 35
19 randomizada de ácido zoledrônico com clodronato como parte do estudo MRC Mieloma IX (Morgan et al.) mostrou que o ácido zoledrônico não era apenas superior ao clodronato na prevenção relacionada a eventos ósseos (SRE), mas também fornecia um benefício na sobrevida independente da redução de SER, apoiando a atividade antimieloma do ácido zolêdronico. Várias preocupações surgiram em relação ao uso crônico dos bisfosfonatos. Duas destas, o dano renal e a condição chamada osteonecrose da mandíbula (ONJ) são abordadas em detalhes em outros materiais educacionais da IMF (Myeloma Minute e Mieloma Today, e Understanding Bisphosphonate Therapy ). Ambas as condições felizmente são relativamente incomuns, mas a conscientização destes problemas em potencial é a chave para a prevenção. A função renal deve ser monitorada seriamente (especialmente a creatinina sérica antes de cada dose do tratamento), particularmente com o uso do Zometa. Se a creatinina sérica aumentar de 0,5 para 1,0 mg/dl, a dose e/ou ajustes no esquema de administração de Aredia ou Zometa podem ser necessários. Para o Zometa um dos ajustes mais simples é estender o tempo de infusão de 15 minutos para minutos, o que reduz o risco de insuficiência renal. Uma publicação da American Academy of Oral Medicine sobre o controle da osteonecrose mandibuar relacionada ao uso de bisfosfonatos foi publicado no The Journal of the American Dental Association em dezembro de A primeira recomendação é a prevenção da BONJ através da realização de check-ups odontológicos regulares. Se for encontrado algum problema, é recomendado o encaminhamento para um especialista (ex: cirurgião dentista). Qualquer cirurgia importante da mandíbula ou extrações dentárias devem ser evitada até que a consulta com um especialista seja feita. Infecções podem requerer o uso de antibióticos. A Mayo Clinic publicou o Mayo Consensus Statement for the Use of Bisphosphonates in Multiple Myeloma em agosto de 2006 que incluía o seguinte: O pamidronato é preferível ao acido zoledrônico até que mais dados estejam disponíveis sobre o risco de complicações (osteonecrose mandibular). Algumas modificações a estas diretrizes foram propostas pelo International Myeloma Working Group (IMWG) da IMF e publicadas em março de 2007 no Mayo Clinic Proceedings. No encontro anual de 2009 da Sociedade Americana de Hematologia, líderes de opiniões importantes observaram que a incidência de ONJ parece ter diminuir drasticamente, provavelmente devido a melhora da higiene dental. No entanto, preocupações adicionais surgiram com o uso em logo prazo de tratamentos com bisfosfonatos. Fraturas atípicas (subtrocantéricas) do fêmur são raras, e há dados que estabelecem uma associação de cinco ou mais anos de tratamento de bisfosfonatos com a sua ocorrência. Em outubro de 2010, o FDA adicionou fratura sobtrocantérica do fêmur a seção de Precauções e Advertências da bula de todos os bisfosfonatos. Duas recentes publicações discutiram a possível associação entre os bisfosfonatos orais e o câncer de esôfago. Usando o mesmo banco de dados, um grupo não encontrou associação (Cardwell et al.), enquanto outro grupo relatou um risco aumentado (Green et al.) Estes achados exigem exame adicional. O IMWG recomenda a descontinuação do uso dos bisfosfonatos após um ano de terapia para pacientes que tenham alcançado a remissão completa e/ou fase platô. Para pacientes com doença ativa, que não tenham alcançado uma resposta ou que tenham doença óssea severa por mais de 2 anos, a terapia com bisfosfonatos pode ser diminuída para uma administração a cada três meses. Diretrizes atuais sobre o papel dos bisfosfonatos no mieloma múltiplo da Sociedade Americana de Oncologia Clínica (ASCO) (Kyle et al., J Clin Oncology 2007) recomendam tratamento por dois anos, e então considerar a descontinuação de bisfosfonatos para pacientes cuja a doença é responsiva ou estável O uso contínuo dos bisfosfonatos deve ser a critério do médico. Antibióticos - As infecções são um problema comum e recorrente em pacientes com mieloma. É 36 necessário manter uma conduta cuidadosa no controle das infecções. A terapia com antibióticos deve ser imediatamente instituída se houver suspeita de infecção ativa. O uso de antibióticos preventivos ou profiláticos com infecção recorrente é controverso. Um recente estudo comparativo (URCC/ECOG, Vesole et al.) apresentado na ASH 2010 concluiu que o o uso de antibióticoterapia não diminuiu a incidência de infecção séria (> grau 3 e/ou hospitalização) ou não houve nenhuma infecção nos dois primeiros meses de tratamento Com base nesse estudos, os autores recomendam que os antibióticos devam ser mantidos nos dois primeiros meses de tratamento, mas cada caso deve ser considerado individualmente. A continuação de antibióticos profiláticos pode aumentar a chance de resistência a antibióticos, mas também pode reduzir a chance de complicações por infecções recorrentes. O uso de gamaglobulina em alta dose pode ser necessário em pacientes com infecções recorrentes agudas e graves. A GM-CSF pode ser útil para melhorar os níveis de leucócitos como tentativa de vencer as complicações infecciosas. O uso de G- ou CM-CSF é útil na fase de recuperação após o transplante de medula óssea ou células-tronco. G e GM-CSF também são usados na coleta de células-tronco. Antivirais - O aumento na incidência de Herpes zóster (cobreiro) tem sido observado em algumas populações de pacientes com mieloma (mas não em outras malignidades) que são tratadas com VELCADE. Portanto, terapia antiviral profilática deverá ser considerada na terapia com VELCADE. Isto levou a recomendações aos pacientes em estudos clínicos de carfilzomibe, um inibidor proteossômico de segunda geração, a receberem profilaxia antiviral. Os pacientes com mieloma são advertidos a não tomar a vacina para Herpes zóster (Zostavax ), por ser uma vacina não atenuada que impõe um risco significante para aqueles que estão com a imunidade comprometida. 6. CONTROLE DA DOENÇA REFRATÁRIA OU RECIDIVADA Conforme ilustrado na seção fisiopatologia, um problema frequente em mieloma é a recidiva que ocorre após uma remissão de 1 a 3 anos. Embora a terapia de manutenção seja útil em prolongar o período de remissão inicial, a recidiva, que ocorre inevitavelmente, requer uma quimioterapia de re-indução. A seguir, apresentamos a estratégia geral para o controle da doença recidivante. Se uma primeira recidiva ocorrer após uma remissão de, no mínimo, 6 meses a 1 ano, a primeira estratégia é considerar reutilizar a terapia que produziu a remissão em primeiro lugar. Cerca de 50% dos pacientes apresentarão uma segunda remissão com a mesma terapia que causou a primeira. Isso é particularmente verdadeiro para pacientes cuja doença está em remissão por mais de 1 ano após a tentativa inicial de indução. Por exemplo, um paciente que recebeu MP e cujo mieloma entrou em remissão por 2 anos pode novamente receber indução com MP. Se a remissão durou menos de 6 meses, normalmente será necessário usar uma terapia alternativa. Este também é o caso se a recidiva ocorrer após o segundo ou o terceiro uso da terapia de indução original. O uso de regimes contendo Adriamycin ou Doxil é uma consideração importante nesse ambiente. Figura 6: célula de mieloma MDR 37
20 VELCADE (Bortezomibe) para mieloma recidivado A disponibilidade de VELCADE para tratamento da recidiva é um importante avanço. Após sua aprovação para pacientes com mieloma múltiplo que receberam pelo menos duas terapias anteriores e demonstraram progressão da doença na última terapia, VELCADE foi então avaliado em um estudo APEX multicêntrico, randomizado, de fase III comparando VELCADE a dexametasona de alta dose em 669 pacientes com mieloma em 80 centros cujas recidivas se apresentaram de uma a três linhas de terapias. O desfecho primário foi o tempo até a progressão. APEX também avaliou o papel de VELCADE como terapia de manutenção em responsivos. Este estudo recrutou internacionalmente e foi o maior estudo já concluído em mieloma múltiplo. De maneira geral, houve uma melhora de aproximadamente 30% na sobrevida durante o primeiro ano com bortezomibe (VELCADE ) em comparação a dexametasona. Isto foi obviamente uma informação muito útil, e levou ao papel do VELCADE como uma plataforma para basear terapias de combinação para recidiva (Vel/Doxil, VR, VRD, VCD, etc.). Outras opções É importante lembrar que uma variedade de protocolos de quimioterapia simples e combinados estão disponíveis para o controle da doença recidiva e refratária. Dependendo do problema exato, uma variedade de intervenções pode ser possível. Por exemplo, se a recidiva está associada com o desenvolvimento de uma ou duas lesões ósseas, a radiação no(s) local(ais) com comprometimento ósseo pode ser uma maneira satisfatória de tratar a recidiva. Se ocorrer recidiva geral, dexametasona como agente único pode ser muito útil para se atingir o controle geral da doença. O uso da dexametasona é atraente porque pode ser administrado por via oral e não causa efeitos colaterais significativos como perda ou redução capilar ou redução nas contagens sanguíneas. Outro ponto importante é que a recidiva após terapia de alta dose com transplante, em muitos casos, tem um padrão similar à recidiva após abordagens padrão. Segundas, e às vezes terceiras remissões podem ser alcançadas após recidiva seguindo o transplante de medula óssea. Ainda não é claro se uma segunda terapia de alta dose com transplante é a estratégia mais apropriada em comparação à outras abordagens com doses mais baixas de quimioterapia, e devem ser baseadas nas considerações individuais dos pacientes. Dado a taxa rápida contínua de desenvolvimentos de novas terapias para mieloma, incluindo inibidores de proteossomo de segunda geração, fármacos imunomodulatórios de terceira geração, anticorpos monoclonais, e terapias alvo, assim como a investigação de novos agentes existentes e novas combinações, o tratamento no contexto de estudos clínicos pode ser uma opção para pacientes com mieloma recidivante. Uma faixa completa de suporte à saúde é crucial para o gerenciamento do mieloma. Quando primeiramente diagnosticado, um número de procedimentos emergenciais é exigido, incluindo diálise, plasmaferese, cirurgia, e radiação para reduzir a pressão no nervo, na medula espinhal, ou outros órgãos cruciais. O controle da dor é essencial para o cuidado inicial dos pacientes com mieloma. Isto pode ser difícil até que o controle inicial da doença seja adquirido. Não há razão para pacientes com mieloma terem dores importantes em andamento com a disponibilidade de novos fármacos e estratégias. importante na recuperação da força óssea e da mobilidade e pode ajudar na redução da dor em geral. Tabela 10 - Testes Necessários para Monitorar a Resposta à Terapia EXAMES DE SANGUE Contagens sanguíneas de rotina. Exames bioquímicos. Provas da função hepática. Determinação da proteína do mieloma (eletroforese de proteína sérica + imunoglobulinas quantitativas). Análise de cadeia leve sérica livre (Freelite TM ) ß2-microglobulina sérica. Proteína C-reativa. Índice de marcação no sangue periférico (LI). Nível sérico de eritropoietina. URINA Urinálise de rotina. Urina de 24 horas para determinação de proteínas totais, eletroforese e imunoeletroforese. Urina de 24 horas para depuração de creatinina se a creatinina sérica estiver elevada. AVALIAÇÃO ÓSSEA Mapeamento por raio X. RM/TC para problemas especiais. FDG/PET de corpo inteiro, se o status da doença não estiver claro. Determinação da densidade óssea (DEXA) como valor inicial e para avaliar o benefício dos bisfosfonatos. MEDULA ÓSSEA Aspiração e biópsia para diagnóstico e monitoramento periódico. Testes especiais para avaliar prognóstico buscando vários cariótipos potenciais e anormalidade FISH (nº de cromossomos, translocações, deleções - ex: FISH 13q-, t[4:14], 1q21, etc.). OUTROS EXAMES Amiloidose. Neuropatia. Complicações renais ou infecciosas. Pode haver por parte do paciente e/ou do médico em implementar procedimentos de controle completo da dor devido a preocupações sobre dependência. O controle da dor deve ser sempre a primeira prioridade. Uma cinta ou colete pode ajudar a estabilizar a espinha ou outra área, reduzindo o movimento e a dor. Exercício moderado também é 38 39
21 40 Tabela 11 - Terapia com Altas Doses Tipo Vantagens Desvantagens Transplante Autólogo Único Transplante Autólogo Duplo Transplante Alogênico Tradicional Transplante Mini-Alo Transplante entre gêmeos 50% de remissões excelentes. Pelo menos tão boa quanto a terapia padrão em relação à sobrevida global e provavelmente melhor para pacientes com Sß2M elevada. Base para estratégias para obtenção de remissão verdadeira ou cura em longo prazo. Novos esquemas de condicionamento podem produzir remissão completa verdadeira. Atualização em 2002 dos dados franceses indicam benefícios de sobrevida para os pacientes que não estão em CR ou VGPR. Resultados excelentes com transplante (vide texto). Sem risco de contaminação da medula/células tronco com mieloma. Possível efeito enxerto versus mieloma prolonga a remissão. Forma de Alo menos tóxica. Quimioterapia preparatória geralmente bem tolerada. Resultados em enxerto imune antimieloma. Sem risco de contaminação de mieloma nas células transplantadas. Muito menos arriscado do que o transplante alogênico. Padrão de recidiva similar ao da quimioterapia padrão. Mais tóxico e mais caro. Ainda não são claramente identificados os pacientes que decisivamente se beneficiam do transplante. Terapia de manutenção ainda necessária/ recomendada. O papel do duplo vs. único ainda não está claro. Muito mais tóxico em comparação ao transplante único. Sem benefício de sobrevida em CR ou VGPR após o primeiro transplante. Mesmo para irmãos com HLA idênticos, há risco significativo de complicações iniciais e mesmo óbito (25-30%). O risco de complicações é imprevisível. Restrito a pacientes com idade <55 anos. Mais tóxico e caro em comparação ao autólogo. Nenhuma quimioterapia antimieloma é administrada. Ainda produz doença enxerto versus hospedeiro. Os benefícios totais ainda não são claros. Risco de mortalidade inicial de aproximadamente 17% Sem efeito enxerto versus hospedeiro. Necessidade de gêmeo idêntico <55 7. TRATAMENTOS NOVOS E EM ESTUDO A maioria dos tratamentos novos está disponível no ambiente de estudos clínicos. As fases de estudos clínicos estão listadas na Tabela 11. Toda uma faixa de agentes está atualmente em estudos clínicos, incluindo inibidores de proteossomo e agentes imunomoduladores, anticorpos monoclonais, inibidores de histona desacetilase (HDAC), inibidores de proteína de choque térmico (HSP), agentes quimioterápicos, e terapias voltadas para vias específicas do mieloma. Os pacientes são encorajados a contatar o IMF através do telefone ( CURE [2873] nos Estados Unidos e no Canadá e em outras localidades) ou via internet (myeloma.org) e verificar com os respectivos médicos sobre a disponibilidade de novos estudos clínicos. Para maiores informações solicite o The Myeloma Matrix, uma publicação da IMF disponível com atualizações regulares e listas de todas as drogas atualmente em estudos clínicos. Ótimos resumos sobre novas terapias são apresentadas nos relatos IMF de ASH, ASCO, EHA e IMWG (todos disponíveis ao contatar o IMF via telefone ou pela internet em myeloma.org). I II III IV Tabela 12: Fases dos Estudos Clínicos Testes iniciais para avaliar dosagem, tolerabilidade e a toxicidade em pacientes. Novos testes para avaliar a eficácia do tratamento na dose e no esquema selecionados. Comparação do novo tratamento com tratamento(s) anterior(es) para determinar se o novo tratamento é melhor. Normalmente conduzido após a aprovação do FDA para avaliar a custo-eficácia, o impacto sobre a qualidade de vida e outras questões comparativas. REFERÊNCIAS Geral Bataille R, Harousseau JL. Multiple myeloma. N Engl J Med. 1997; 336: Berenson James R. Biology and Management of Multiple Myeloma. Humana Press ISBN Gahrton G, Durie BGM, Samson DM. Multiple Myeloma and Related Disorders. Oxford University Press 2004 ISBN: Kyle RA, Rajkumar SV. Multiple myeloma. Blood. 2008;111(6): Mehta J, Singhal S, eds. Myeloma, Dunitz M. Taylor and Francis Group, 2002: ISBN Palumbo A, Anderson L. Multiple Myeloma. N Engl J Med. 2011; 364: História Kyle RA. History of multiple myeloma. In: Neoplastic Diseases of the Blood, 3rd edition. (Wiernik PH, Canellos GP, Kyle RA, Schiffer CA, eds. New York: Churchill Livingstone, Kyle RA. History of multiple myeloma. In: Neoplastic Diseases of the Blood, 2nd edition.(wiernik PH, Canellos GP, Kyle RA, Schiffer CA, eds). New York: Churchill Livingstone, 1991:
22 Epidemiologia American Cancer Society. Cancer Facts & Figures Atlanta: American Cancer Society; Birmann BM, Giovannucci E, Rosner B, Anderson KC, Colditz GA. Body mass index, physical activity, and risk of multiple myeloma. Cancer Epidemiol Biomarkers Prev 2007; 16(7): Brenner H, Gondos A, Pulte D. Recent major improvement in long-term survival of younger patients with multiple myeloma. Blood. 2008; 111: Brown LM, Gridley G, Check D, Landgren O. Risk of multiple myeloma and monoclonal gammopathy of undetermined significance among white and black make United States veterans with prior autoimmune, infectious, inflammatory, and allergic disorders. Blood 2008; 111(7): Herrington LJ, Weiss NS, Olshan AF. The epidemiology of myeloma. In: Myeloma Biology and Management (Malpas JS, Bergsagel DE, Kyle RA eds.). Oxford, England, Oxford University Press: 1995: Infante PF. Benzene exposure and multiple diagnosis: A detailed meta-analysis of Benzene cohort studies. Ann NY Acad Sci. 2006;1076: Jemal A, Thomas A, Murray T, Thun M. Cancer statistics CA Cancer J Clin 2002; 52: Jemal A, Siegel R, Xu J, Ward E. Cancer Statistics, CA Cancer J Clin. 2010; 60(5): Kirkeleit J, Riise T, Bratveit M, Moen BE. Increased risk of acute myelogenous leukemia and multiple myeloma in a historical cohort of upstream petroleum workers exposed to crude oil. Cancer Causes Control 2008;19: Kumar SK, Rajkumar SV, Dispenzieri A, et al. Improved survival in multiple myeloma and the impact of novel therapies. Blood 2008; 111: LeMasters GK, Genaidy AM, Succop P, et al. Cancer risk among firefighters: A review and metaanalysis of 32 studies. J Occup Environ Med 2006;48(11): Lynch HT, Ferrara K, Barlogie B, et al. Familial Myeloma. N Engl J Med 2008; 259(2): Schottenfeld D, Fraumeni JF Jr. (eds). Cancer Epidemiology and Prevention, 2nd edn. New York: Oxford University Press; 1996: Schwartz GG. Multiple myeloma: clusters, clues, and dioxins. Cancer Epidemiol Biomarkers Prev. 1997; 6: Doença òssea Bataille R, et al. Mechanism of bone destruction in multiple myeloma. The importance of an unbalanced process in determining the severity of lytic bone disease. J Clin Oncol 1989; 7: Berenson J, et al. Long-term pamidronate treatment of advanced multiple myeloma reduces skeletal events. J Clin Oncol 1998; 16: Berenson J, et al. Efficacy of pamidronate in reducing skeletal events in patients with advanced multiple myeloma. N Engl J Med 1996; 334: Bredella MA, Steinbach L, Caputo G, et al. Value of FDG PET in the assessment of patients with multiple myeloma. AJR Am J Roentgenol 2005;184: Dimopoulos M, Terpos E, Comenzo RL, et al. International myeloma working group (IMWG) consensus statement and guidelines regarding the current role of imaging techniques in the diagnosis and monitoring of multiple myeloma. Leukemia 2009; 23: Durie BGM, Salmon SE, Mundy GR. Relation to osteoclast activating factor production to extent of bone disease in multiple myeloma. Br J Haematol 1981; 47: Durie BGM, Waxman AD, D Agnolo A, Williams CM. Whole-body (18) F-FDG PET identifies high-risk myeloma. J Nucl Med 2002; 43: Jadvar H, Conti PS. Diagnostic utility of FDG PET in multiple myeloma. Skeletal Radiol 2002;31: Kato T, Tsukamoto E, Nishioka T, et al. Early detection of bone marrow involvement in extramedullary plasmacytoma by wholebody F-18 FDG positron emission tomography. Clin Nucl Med 2000;25: Major P, et al. Zoledronic acid is superior to pamidronate in the treatment of hypercalcemia of malignancy: a pooled analysis of two randomised, controlled clínical trials. J Clin Oncol 2001; 19, Markowitz GS, Appel GB, Fine PL, Fenves AZ, Loon NR, Jagannath S et al. Collapsing focal segmental glomerulosclerosis following treatment with high-dose pamidronate. J Am Soc Nephrol 2001; 12: McCloskey EV, et al. A randomised trial of the effect of clodronate on skeletal morbidity in multiple myeloma. Br J Haematol 1998; 100: Moulopoulos LA, Dimopoulos MA, Weber D, et al. Magnetic resonance imaging in the staging of solitary plasmacytoma of bone. J Clin Oncol 1993;11: Mundy, GR, Yoneda T. Bisphosphonates as anticancer drugs. N Engl J Med 1998; 339: Orchard K, Barrington S, Buscombe J, et al. Fluoro-deoxyglucose positron emission tomography imaging for the detection of occult disease in multiple myeloma. Br J Hematol 2002;117: Roodman, GD. Bone building with bortezomib. J Clinic Invest 2008; 118(2): Rosen LS, Gordon D, Antonio BS, et al. Zoledronic acid versus pamidronate in the treatment of skeletal metastases in patients with breast cancer or osteolytic lesions of multiple myeloma: a phase II, double blind, comparative trial. Cancer J. 2001; 7: Schirrmeister H, Bommer M, Buck AK, et al. Initial results in the assessment of multiple myeloma using 18F-FDG PET. Eur J Nucl Med Mol Imaging : Terpos E, Sezer O, Croucher P, Dimopoulos M-A. Myeloma bone disease and proteasome inhibition therapies. Blood 2007; 110(4): Walker R, Barologie B, Haessler J, et al. Magnetic resonance imaging in multiple myeloma: Diagnostic and clínical implications. J Clin Oncol 2007; 25(9); ANEMIA Becker, PS, Miller CP, Wood BL, et al. Expression of erythropoietin receptors by plasma cells from patients with multiple myeloma: Potential relevance to pharmacological use of erythropoietin. J Clin Oncol 28:15s, 2010 (suppl; abstr 8124). 43
23 SINTOMAS CLÍNICOS Pruzanski W, Ogryzlo MA. Abnormal proteinuria in malignant diseases. Adv Clin Chem 1970;13: CROMOSSOMOS Arzoumanian V, Hoering A, Sawyer J, et al. Suppression of abnormal karyotype predicts superior survival in multiple myeloma. Leukemia 2008; 22: Avet-Loiseau H, Leleu X, Roussel M, et al. Bortezomib plus dexamethasone induction improves outcome of patients with t(4;14) myeloma but not outcome of patients with del(17p). J Clin Oncol 2010; 28(30): Dewald GW, Therneau T, et al. Relationship of patient survival and chromosome anomalies detected in metaphase and/or interphase cells at diagnosis of myeloma. Blood. 2005;106(10): Dispenzieri A, Rajkumar SV, Gertz MA, et al. Treatment of newly diagnosed multiple myeloma based on Mayo stratification of myeloma and risk-adapted therapy (msmart): Consensus statement. Mayo Clin Proc 2007; 82(3): Durie BGM, et al. Cytogenetic abnormalities in multiple myeloma. Epidemiology and Biology of Multiple Myeloma. New York: Springer-Verlag, 1991: Fonseca R, Avet-Loiseau H, et al. International myeloma working group molecular classification of multiple myeloma: spotlight review. Leukemia 2009; 23: Jaksic W, Trudel S, Chang H, et al. clínical outcomes in t(4,14) multiple myeloma: a chemotherapy sensitive disease characterized by rapid relapse and alkylating agent resistance. J Clin Oncol 2005;23(28): Konigsberg R, Zojer N, Ackermann J, et al. Predictive role of interphase cytogenetics for survival of patients with multiple myeloma. J Clin Oncol. 2000; 18: Stewart AK: A risk-adapted approach to myeloma therapy. ASCO Educational Book. 2008: (ISSN: ). MIELOMA MGUS E ASSINTOMÁTICO Kyle RA, Therneau TM, Rajkumar SV, Offord JR. A long-term study of prognosis in mono-clonal gammopathy of undetermined significance. N Engl J Med. 2002; 346: Kyle RA, Greipp PR. Smoldering multiple myeloma. N Engl J Med. 1980; 302: Weber DM, et al. Prognostic features of asymptomatic multiple myeloma. Br J Haematol. 1997; 97: FATORES DE ADAPTAÇÃO E PROGNÓSTICO: Bataille R, Boccadoro M, Klein B, et al. C-reactive protein and ß2 - microglobulin produce a simple and powerful myeloma staging system. Blood 1992; 80: Durie BGM, Stock-Novack D, Salmon SE, et al. Prognostic value of pre-treatment serum ß2-microglobulin in myeloma: a Southwest Oncology Group study. Blood 1990; 75: Durie BGM, Salmon SE. A clínical staging system for multiple myeloma. Cancer 1975; 36: Facon T, et al. Chromosome 13 abnormalities identified by FISH analysis and serum ß2-microglobulin produce a powerful myeloma staging system for patients receiving high-dose therapy. Blood 2001; 97: Gahrton G, Durie BGM, Samson DM, editors. Multiple Myeloma and Related Disorders, The role of imaging in myeloma. A Hodder Arnold Publication, Oxford University Press, 2004; pp Greipp PR, Durie, BGM, et al. International Staging System for multiple myeloma. J Clin Oncol. 2005:23(15): Greipp RR, San Miguel JF, Fonesca R, Avet-Loiseau H, Jacobson JL, Durie BGM. Development of an International Prognostic Index (IPI) for myeloma: report of the International Myeloma Working Group. Haematol J 2003; 4 (suppl.1): p 7.1, S43-S44. Greipp PR, et al. Value of ß2 - microglobulin level and plasma cell labeling indices as prognostic factors in patients with newly diagnosed myeloma. Blood 1988; 72: Hungria VTM, Maiolino A, Martinez G, et al. Confirmation of the utility of the International Staging System and identification of a unique pattern of disease in Brazilian patients with multiple myeloma. haematologica 2008; 93: Jacobson J, Hussein M, Barlogie B, Durie BGM, Crowley J. A new staging system for multiple myeloma patients based on the Southwest Oncology Group (SWOG) experience. Br J Haematol 2003; 122: Kumar SK, Rajkumar SV, Dispenzieri A, et al. Improved survival in multiple myeloma and the impact of novel therapies. Blood 2008; 111(5): Ludwig H, Durie BGM, Bolejack V, et al. Myeloma in patients younger than age 50 years presents with more favorable features and shows better survival: an analysis of patients from the International Myeloma Working Group. Blood 2008; 111(8): Zojer N, et al. Deletion of 13q14 remains an independent prognostic variable in multiple myeloma despite its frequent detection by interphase fluorescence in situ hybridization. Blood 2001; 95: CRITÉRIOS DE RESPOSTA : Durie BGM, Harousseau J-L, Miguel JS, et al. International uniform response criteria for multiple myeloma. Leukemia 2006; 20: Rajkumar SV, Durie BGM. Eliminating the complete response penalty from myeloma response criteria. Blood 2008; 111(12):5759. TRATAMENTO DE QUIMIOTERAPIA E RADIAÇÃO : Alexanian R, et al. Primary dexamethasone treatment of multiple myeloma. Blood 1992; 80: Alexanian R, Barlogie B, Tucker S. VAD-based regimens as primary treatment for myeloma. Am J Hematol 1990; 33: Alexanian R, et al. Treatment for multiple myeloma: combination chemotherapy with different melphalan dose regimens. JAMA 1969; 208: Durie BGM, Jacobson J, Barlogie B, et al. Magnitude of Response with Myeloma Frontline Therapy Does Not Predict Outcome: Importance of Time to Progression in Southwest Oncology Group Chemotherapy Trials. J Clin Oncol 2004; 22: Durie BGM, Kyle RA, Belch A, et al. Myeloma management guidelines, a consensus report from the Scientific Advisors of the International Myeloma Foundation. The Hematology Journal 2003; 4:
24 Kumar A, Loughran MA, Durie BGM, et al. Management of multiple myeloma: a systematic review and critical appraisal of published studies. Lancet Oncology 2003; 4: MacLennan ICM, et al, for the MRC Working Party on Leukaemia in Adults. Combined chemotherapy with ABCM versus melphalan for treatment of myelomatosis. Lancet 1992; 339: Myeloma Trialists Collaborative Group. Combination chemotherapy versus melphalan plus prednisone as treatment for multiple myeloma: an overview of 6,633 patients from 27 randomized trials. J Clin Oncol 1998; 16: DOENÇA REFRATÁRIA: Alexanian R, Dimopoulus M. The treatment of multiple myeloma. N Engl J Med 1994; 330: Buzaid AC, Durie BGM. Management of refractory myeloma -a review. J Clin Oncol 1988; 6: Richardson P, Barlogie B, Berenson J, et al. A phase II multicenter study of the protease inhibitor bortezomib (VELCADE formerly PS-341) in multiple myeloma patients (pts) with relapsed/refractory disease. N Engl J Med 2003; 348: TRANSDUÇÃO DE SINAL E CITOCINA: Bladé J, Estve J. Viewpoint on the impact of interferon in the treatment of multiple myeloma: benefit for a small proportion of patients? Med Oncology 2000; Hideshima T, Bergsagel PL, Kuehl WM et al. Advances in biology of multiple myeloma: clínical applications. Blood 2004; 104: Ludwig H, Fritz E, Kotzmann H, et al. Erythropoietin treatment of anemia associated with multiple myeloma. N Engl J Med 1990; 322: Mandelli F, et al. Maintenance treatment with alpha 2b recombinant interferon significantly improves response and survival duration in multiple myeloma patients responding to conventional induction chemotherapy. Results of an Italian randomized study. N Engl J Med 1990; 322: Musto P, et al. clínical results of recombinant erythropoietin in transfusion-dependent patients with refractory multiple myeloma: role of cytokines and monitoring of erythropoiesis. Eur J Haematol 1997; 58: TRANSPLANTE AUTÓLOGO: Abdelkefi A, Ladeb S, Torjman L, et al. Single autologous stem-cell transplantation followed by maintenance therapy with thalidomide is superior to double autologous transplantation in multiple myeloma: Results of a multicenter randomized clínical trial. Blood 2008; 111(4): Attal M, Harousseau JL, Stoppa A-M, et al. A prospective, randomized trial of autologous bone marrow transplantation and chemotherapy in multiple myeloma. N Engl J Med 1996; 335: Attal M, Harousseau JL, Facon T, et al. Single versus double autologous stem-cell transplantation for multiple myeloma. N Engl J Med 2003;349: Badros A, Barlogie B, Morris C, et al. High response rate in refractory and poor-risk multiple myeloma after allotransplantation using a nonmyeloablative conditioning regimen and donor lymphocyte infusions. Blood 2001;97: Barlogie B, Jagannath S, Desikan KR, et al. Total therapy with tandem transplants for newly diagnosed multiple myeloma. Blood 1999; 93: Barlogie B, Kyle RA, Anderson KC, et al. Standard chemotherapy compared with high-dose chemoradiotherapy for multiple myeloma: final results of phase III US Intergroup Trial S9321. J Clin Oncol 2006;24: Bensinger WI. The Role of Hematopoietic Stem Cell Transplantation in the Treatment of Multiple Myeloma. J NCCN 2004; 2: Bruno B, Rotta M, Patriarca F, et al. A comparison of allografting with autografting for newly diagnosed myeloma. M Engl J Med 2007;356: Cavo M, Zamagni E, Tosi P, et al. Superiority of thalidomide and dexamethasone over vincristine-doxorubicin-dexamethasone (VAD) as primary therapy in preparation for autologous transplantation for multiple myeloma. Blood. 2005;106:35-9. Cunningham D, et al. A randomized trial of maintenance interferon following high-dose chemotherapy in multiple myeloma: long-term follow-up results. Br J Haematol 1998; 102: Desikan KR, Barlogie B, Sawyer J, et al. Results of high-dose therapy for 100 patients with multiple myeloma: durable complete remissions and superior survival in the absence of chromosome 13 abnormalities. Blood 2000; 95: Dispenzieri A, Kyle RA, Lacy MQ, et al. Superior survival in primary systemic amyloidosis patients undergoing peripheral blood stem cell transplantation: a case-control study. Blood 2004; 103: Fernand JP, Ravaud P, Chevert S, et al. High-dose therapy and autologous peripheral blood stem cell transplantation in multiple myeloma: upfront or rescue treatment? Results of a multicenter sequential randomized clínical trail. Blood 1998; 92: Fernand JP, Katsahian S, Divine M, et al. High-dose therapy and autologous blood stem-cell transplantation compared with conventional treatment in myeloma patients aged years: long term results of a randomized control trial from the Group Myelome-Autogreffe. J Clin Oncol 2005;23: Garban F, Attal M, Michallet M, et al. Prospective comparison of autologous stem cell transplantation followed by dose-reduced allograft (IFM99-03 trial) with tandem autologous stem cell transplantation (IFM99-04 trial) in high-risk de novo multiple myeloma. Blood 2006;107: Gore ME, Viner C, Meldrum M. Intensive treatment of multiple myeloma and criteria for complete remission. Lancet 1989; 14: Martinelli G, Terragna C, Zamagni E, et al. Molecular remission after allogeneic or autologous transplantation of hematopoietic stem cells for multiple myeloma. J Clin Oncol 2000; 18: McElwain TJ, Powles RL. High-dose intravenous melphalan for plasma-cell leukaemia and myeloma. Lancet 1983; 2: Mehta J, Powles RL. Autologous blood and marrow transplantation. In: Leukaemia and Associated Diseases. ( Whittaker JA, Holmes JA, eds). Oxford: Blackwell Science, 1998;
25 TRANSPLANTE ALOGÊNICO E SINGÊNICO: Bensinger WI, Buckner CD, Anasetti C, et al. Allogeneic marrow transplantation for multiple myeloma: an analysis of risk factors on outcome. Blood 1996; 88: Bensinger WI, Demirer, T, Buckner CD, et al. Syngeneic marrow transplantation in patients with multiple myeloma. Bone Marrow Transplant 1996; 18: Durie BGM, Gale RP, Horowitz MM. Allogeneic and twin transplants for multiple myeloma: an IBMTR analysis. Multiple myeloma. From biology to therapy. Current concepts. INSERM, Mulhouse, October, 1994 (abstract). Gahrton G, et al. Progress in allogeneic hematopoietic stem cell transplantation for multiple myeloma. Bone Marrow Transplant 2000; 25 (suppl. 1): S54. Gahrton G,. et al. Allogeneic bone marrow transplantation in multiple myeloma. Br J Haematol 1996; 92: Maloney DG, Sahebi F, Stockerl-Goldstein KE, et al. Combining an allogeneic graft-vs.-myeloma effect with high-dose autologous stem cell rescue in the treatment of multiple myeloma [abstract]. Blood 2001; 98 (11. pt 1): 435a Abstract Samson D. The current position of allogeneic and autologous BMT in multiple myeloma. Leukemia and Lymphoma 1992; 7:33. MANUTENÇÃO: Attal M, Cristini C, Marit G, et al. Lenalidomide maintenance after transplantation for myeloma. J Clin Oncol 2010;28:15s (suppl; abstr 8018). McCarthy PL, Owzar K, Anderson KC, et al. Phase III intergroup study of lenalidomide versus placebo maintenance therapy following single autologous stem cell transplant (ASCT) for multiple myeloma (MM): CALGB J Clin Oncol 2010;28:15s (suppl; abstr 8017). SUPORTE À SAÚDE: Abrahamsen B, Eiken P, Eastell R. Subtrochanteric and diaphyseal femur fractures in patients treated with alendronate: a registerbased national cohort study. J Bone Miner Res 2009;24: Bertolotti P, Bilotti E, Colson K, et al. Management of side effects of novel therapies for multiple myeloma: Consensus statements developed by the International Myeloma Foundation s Nurse Leadership Board. Clin J Oncol Nursing 2008;S12(3):9-12. Cardwell CR, Abnet CC, Cantwell MM, et al. Exposure to oral bisphosphonates and risk of esophageal cancer. JAMA 2010; 204: Chanan-Khan A, Sonneveld P, Schuster MW, et al. Analysis of herpes zoster events among bortezomib-treated patients in the phase III APEX study. J Clin Oncol 2008;26: Chapel HM, Lee M, Hargreaves R, et al. Randomized trial of intravenous immunoglobulin as prophylaxis against infection in plateau-phase multiple myeloma. Lancet. 1994; 343: Faiman B, Bilotti E, Mangan PA, Rogers K, IMF NLB. Steroid-associated side effects in patients with multiple myeloma: Consensus statement of the IMF Nurse Leadership Board. Clin J Oncol Nursing 2008;S12(3): Green J, Czanner G, Reeves G, et al. Oral bisphosphonates and risk of cancer of the oesophagus, stomach, and colorectum: casecontrol analysis within a UK primary care cohort. BMJ 2010; 341c4444 doi: /bmj/c Hussein MA, Vrionis FD, Allison R, et al. The role of vertebral augmentation in multiple myeloma: International Myeloma Working Group Consensus Statement. Leukemia 2008; 22: Johnson WJ, Kyle RA, Pineda AA, et al. Treatment of renal failure associated with multiple myeloma. Plasmapheresis, hemodialysis and chemotherapy. Arch Int Med. 1990; 150: Kyle RA, Gertz MA. Primary systemic amyloidosis: clínical and laboratory features in 474 cases. Semin Hematol. 1995; 32: Kyle RA, Yee GC, Somerfield MR, et al. American Society of clínical Oncology 2007 clínical practice guideline update on the role of bisphosphonates in multiple myeloma. J Clin Oncol 2007;25: Ludwig H, Fritz E, Kotsmann H, et al. Erythropoietin treatment of anemia associated with multiple myeloma. N Engl J Med 1990; 233: Mateos MV. Management of treatment-related adverse events in patients with multiple myeloma. Cancer Treat Rev 2010;36:Suppl2:S Miceli T, Colson K, Gavino M, Lilleby K, IMF NLB. Myelosuppression associated with novel therapies in patients with multiple myeloma: Consensus statement of the IMF Nurse Leadership Board. Clin J Oncol Nursing 2008;S12(3): Morgan G, Davies F, Gregory W, et al. Evaluating the effects of zoledronic acid (ZOL) on overall survival (OS) in patients (Pts) with multiple myeloma (MM): Results of the Medical Research Council (MRC) Myeloma IX study. J Clin Oncol 2010; 28:15s, (suppl; abstr 8021). Oken M, Pomeroy C, Weisdorf D, et al. Prophylactic antibiotics for the prevention of early infection in multiple myeloma. Am J Med. 1996; 100: Osterborg A, Boogaerts MA, Cimino R, et al. Recombinant human erythropoietin in trans-fusiondependent anemic patients with multiple myeloma and non-hodgkin s lymphoma-a randomized multicenter study. Blood 1996; 87: Palumbo A, Rajkumar SV, Dimopoulos MA, et al. Prevention of thalidomide and lenalidomide associated thrombosis in myeloma. Leukemia 2008; 22: Rajkumar SV, Durie BGM. Eliminating the complete response penalty from myeloma response criteria. Blood 2008; 111(12):5759. Rome S, Doss D, Miller K, Westphal J, IMF NLB. Thromboembolic events associated with novel therapies in patients with multiple myeloma: Consensus statement of the IMF Nurse Leadership Board. Clin J Oncol Nursing 2008;S12(3): Smith LC, Bertolotti P, Curran K, Jenkins B, IMF NLB. Gastrointestinal side effects associated with novel therapies in patients with multiple myeloma: Consensus statement of the IMF Nurse Leadership Board. Clin J Oncol Nursing 2008;S12(3): Tariman JD, Love G, McCullagh E, Sandifer S, IMF NLB. Peripheral neuropathy associated with novel therapies in patients with multiple myeloma: Consensus statement of the IMF Nurse Leadership Board. Clin J Oncol Nursing 2008;S12(3): Vickrey E, Allen S, Mehta J, Singhal S. Acyclovir to prevent reactivation of varicella zoster virus (herpes zoster) in multiple myeloma patients receiving bortezomib therapy. Cancer 2009;115: Novas Terapias: Arzoumanian V, Hoering A, Sawyer J, et al. Suppression of abnormal karyotype predicts superior survival in multiple myeloma. Leukemia 2008; 22:
26 Barlogie B, Anaissie E, Bolejack V, et al. High CR and near-cr rates with bortezomib incorporated into up-front therapy of multiple myeloma with tandem transplants. J Clin Oncol 2006; 24: abstract #7519. Barlogie B, Desikan KR, Eddelman P, et al. Extended survival in advanced and refractory multiple myeloma after single-agent thalidomide: identification of prognostic factors in a phase 2 study of 169 patients. Blood 2001; 32: Barlogie B, Shaughnessy Jr. JD, Crowley J. Duration of survival in patients with myeloma treated with thalidomide. New Engl J Med 2008; 359(2): Berenson JR, Boccia R, Sigel D, et al. Efficacy and safety of melphalan, arsenic trioxide and ascorbic acid combination therapy in patients with relapsed or refractory multiple myeloma: a prospective, multicenter, phase II, single-arm study. Br J Haem 2006; 135: Bruno B, Rotta M, Giaccone L, et al. New drugs for treatment of multiple myeloma Lancet Oncology 2004; 5( July) Dimopoulos MA, Kastritis E, Rajkumar SV. Treatment of plasma cell dyscrasias with lenalidomide. Leukemia 2008; 22: Facon T, Mary JY, Hulin C, et al. Melphalan and prednisone plus thalidomide versus melphalan and prednisone alone or reducedintensity autologous stem cell transplantation in elderly patients with multiple myeloma (IFM 99-06): A randomized trial. The Lancet 2007; 370: Harousseau J-L, Marit G, Caillot D, et al. VELCADE/dexamethasone vs VAD as induction treatment prior to ASCT in newly diagnosed multiple myeloma: A preliminary analysis of the IFM randomized multicenter phase 3 trial. Blood 2006; 108:abstract #56. Hussein MA, Mason J, Ravandi F, Rifkin R. A phase II clínical study of arsenic trioxide (ATO) in patients with relapsed or refractory multiple myeloma; a preliminary report. Blood 2001; 98: 378a. Jagannath S, Durie BGM, et al. Bortezomib therapy alone and in combination with dexamethasone for previously untreated symptomatic multiple myeloma. Br J Haematol. 2005;129: Niesvizky R, Jayabalan DS, Christos PJ, et al. BiRD (Biaxin [clarithromycin]/revlimid [lenalidomide]/dexamethasone) combination therapy results in high complete- and overallresponse rates in treatment-naïve symptomatic multiple myeloma. Blood 2008;111(3): Niesvizsky R, Jayabalan DS, Furst JR, et al. Clarithromycin, lenalidomide and dexamethasone combination therapy as primary treatment of multiple myeloma. J Clin Oncol 2006; 24: abstract #7545. Oakervee HE, Popat R., et al. PAD combination therapy (PS341/bortezomib, doxorubicin and dexamethasone) for previously untreated patients with multiple myeloma. Br J Haematol. 2005;129: Orlowski RZ, Peterson BL, Sanford B, et al. Bortezomib and pegylated liposomal doxorubicin as induction therapy for adult patients with symptomatic multiple myeloma: Cancer and Leukemia Group B study Blood 2006; 108: abstract #797. Orlowski RZ, Zhuang SH, Parekh T, et al. The combination of pegylated liposomal doxorubicin and bortezomib significantly improves time to progression of patients with relapsed/refractory multiple myeloma compared with bortezomib alone: results from a planned interim analysis of a randomized phase III study. Blood 2006; 108: abstract #404. Palumbo A, Ambrosini MT, Benevolo G, et al. Bortezomib, melphalan, prednisone, and thalidomide for relapsed multiple myeloma. Blood 2007; 109(7): Palumbo A, Facon T, Sonneveld P, et al. Thalidomide for treatment of multiple myeloma: 10 years later. Blood 2007; 111(8): Palumbo A, Ambrosini MT, Benevolo G, et al. Combination of bortezomib, melphalan, prednisone and thalidomide ( VMPT) for relapsed multiple myeloma: results of a phase I/II clínical trial. Blood 2006; 108: abstract #407. Palumbo A, Flaco P, Falcone A, et al. Oral Revlimid plus melphalan and prednisone (R-MP) for newly diagnosed multiple myeloma: results of a multicenter phase I/II study. Blood 2006; 108: abstract #800. Palumbo A, Bertola A, et al. A prospective randomized trial of oral melphalan, prednisone, thalidomide (MPT) vs. oral melphalan, prednisone (MP): an interim analysis. [abstract] Blood. 2005;104(11):63a. Abstract 207. Pineda-Roman M, Zangari M, van Rhee F, et al. VTD combination therapy with bortezomibthalidomide-dexamethasone is highly effective in advanced and refractory multiple myeloma. Leukemia 2008; 22: Rajkumar SV, Hussein M, Catalano J, et al. A multicenter, randomized, double-blind, placebocontrolled study of thalidomide plus dexamethasone versus dexamethasone alone as initial therapy for newly diagnosed multiple myeloma (MM 003). Blood 2006; 108: abstract #795. Rajkumar SV, Rosinal L, Hussein M, et al. Multicenter, randomized, double-blind, placebocontrolled study of thalidomide plus dexamethasone compared with dexamethasone as initial therapy for newly diagnosed multiple myeloma. J Clin Oncol 2008;26(13): Rajkumar SV, Hayman SR. Controversies surrounding the initial treatment of multiple myeloma. ASCO Educational Book 2008; Rajkumar SV and Kyle R. Multiple Myeloma: Diagnosis and Treatment. Mayo Clinic Proc. 2005;80(10): Rajkumar SV, Jacobus S, Callender N, et al. A randomized phase III trial of lenalidomide plus high-dose dexamethasone versus lenalidomide plus low-dose dexamethasone in newly diagnosed multiple myeloma (E4A03): a trial coordinated by the Eastern Cooperative Oncology Group. Blood 2006; 108: abstract #799. Rajkumar SV. Multiple myeloma: the death of VAD as initial therapy. Blood. 2005;106:2. Rajkumar SV, Hayman SR, Lacy MQ, et al. Combination therapy with CC-5013 (lenalidomide; Revlimid) plus dexamethasone (Rev/ Dex) for newly diagnosed myeloma (MM) [abstract]. Blood. 2004;104:98a. Abstract 331. Richardson PG, Jagannath S, Avigen DE, et al. Lenalidomide plus bortezomib (Rev-VEl) in relapsed and/or refractory multiple myeloma (MM): final results of a multicenter phase 1 trial. Blood 2006; 108: abstract #405. Richardson P, Schlossman RL, Hideshima F, et al. A Phase I study of oral CC5013, an immunomodulatory thalidomide (Thal) derivative, in patients with relapsed and refractory multiple myeloma. Blood 2001; 98: 775a. Richardson PG, Briemberg H, Jagannath S, et al. Frequency, characteristics, and reversibility of peripheral neuropathy during treatment of advanced multiple myeloma with bortezomib. J Clin Oncol 2006;24:
27 Richardson PG, Chanan-Khan A, Schlossman R, et al. Single-agent bortezomib in previously untreated, symptomatic multiple myeloma (MM): results of a phase 2 multicenter study. J Clin Oncol 2006; 24: abstract #7504. Richardson PG, Sonneveld P, Schuster MW, et al. Bortezomib or high-dose dexamethasone for relapsed multiple myeloma. New Engl J Med 2005;352: Richardson PG, Barlogie B, Berenson J, et al. Phase II study of the proteasome inhibitor PS341 in multiple myeloma patients with relapsed/refractory disease. Proc Am Soc Clin Oncol 2002; 21: 11a. San-Miguel J, Harousseau J-L, Joshua D, Anderson KC. Individualizing treatments of patients with myeloma in the era of novel agents. J Clin Oncol 2008; 26(16): Thomas D, Cortes J, O Brian SM, et al. R115777, a farnesyl transferase inhibitor (FTI), has significant anti-leukaemia activity in patients with chronic myeloid leukaemia (CML). Blood 2001; 98: 727a. SOBRE A IMF Uma pessoa pode fazer a diferença. Duas podem fazer um milagre. Brian D. Novis Fundador da IMF O Mieloma é um câncer da medula óssea pouco conhecido, complexo, que frequentemente é sub-diagnosticado, que ataca e destrói o osso. O Mieloma afeta aproximadamente a pessoas nos Estados Unidos, com mais de casos novos diagnosticados a cada ano. Enquanto não existe cura conhecida para o Mieloma, médicos tem muitas formas de ajudar os pacientes com Mieloma a viver mais e melhor. A International Myeloma Foundation -IMF foi fundada em 1990 por Brian e Susie Novis, logo após o diagnóstico do Mieloma de Brian aos 33 anos de idade. O sonho de Brian era que no futuro os pacientes pudessem ter acesso fácil à informação médica e suporte emocional na sua batalha contra o Mieloma. Quando ele fundou a IMF, três eram suas metas: tratamento, educação e pesquisa. Ele buscou fornecer um amplo espectro de serviços para pacientes, suas famílias, amigos e profissionais da saúde. Embora Brian tenha morrido 4 anos após seu diagnóstico inicial, seu sonho não morreu. Hoje a IMF possui mais de membros em todo o mundo. A IMF é a primeira organização dedicada unicamente ao Mieloma, e ainda hoje permanece a maior. A IMF fornece programas e serviços para ajudar na pesquisa, diagnóstico, tratamento e gerenciamento do Mieloma. Com a IMF ninguém estará sozinho na luta contra o Mieloma. Nós damos apoio aos pacientes hoje, enquanto trabalhamos em busca da cura. A IMF LATIN AMERICA foi fundada em 2004 por Christine Jerez Telles Battistini, filha de uma paciente que por oito anos travou dura luta contra a doença, e Dra. Vânia Tietsche de Moraes Hungria, médica hematologista, Professora Adjunta da Disciplina de Hematologia e Oncologia da Faculdade de Ciências Médicas da Santa Casa de Misericórdia de São Paulo e membro do Conselho Científico da International Myeloma Foundation desde A IMF Latin América traz aos pacientes e a comunidade médica da America Latina os mesmos serviços hoje disponíveis nos Estados Unidos, Europa e Japão. Como a IMF pode ajudá-lo? A IMF dedica-se a melhorar a qualidade de vida dos pacientes com Mieloma enquanto trabalha em direção à prevenção e à cura. Kit Informativo sobre o Mieloma O Kit Informativo IMF fornece informações amplas sobre opções de tratamento e gerenciamento da doença. Disponível gratuitamente, o Kit inclui o Manual do Paciente, Revisão Concisa da Doença e Opções de Tratamento, informações sobre eventos futuros e outras publicações e serviços da IMF. Hot Line Nosso Hot Line está em fase de implantação. Em breve estaremos disponibilizando uma linha direta 52 53
28 entre você e a IMF. Aguarde. Acesso à Internet Através de nosso site, nosso compromisso é fornecer a você informações sempre atualizadas sobre o Mieloma Múltiplo incluindo pesquisas e avanços no tratamento, bem como informações sobre a IMF, eventos e nossos programas de educação, pesquisa, apoio e direitos do paciente. Seminários para Pacientes & Familiares Desde 1993 a IMF vem conduzindo Seminários para Pacientes e Familiares em cidades por todo o mundo. Estes encontros educacionais fortalecem pacientes e seus familiares à medida que são informados sobre os últimos avanços no tratamento e gerenciamento do Mieloma, apresentados por um grupo multidisciplinar de especialistas. Cobrindo uma grande variedade de tópicos que refletem as mais avançadas modalidades de tratamento e avanço em pesquisa, estes seminários oferecem uma oportunidade única para contato pessoal com experts em Mieloma e a troca de experiências com outras pessoas que enfrentam os mesmos problemas. Serviços para Médicos Em 1992 a IMF realizou a primeira Conferência Clínica para Mieloma Múltiplo. Desde então a IMF vem conduzindo encontros médicos em todo o mundo. A IMF LA realiza na América Latina conferências clinicas e científicas para médicos, incluindo mesas redondas e think tanks. 54
MIELOMA MÚLTIPLO. Gislaine Oliveira Duarte. médica assistente Hematologia Hemocentro - Unicamp
 MIELOMA MÚLTIPLO Gislaine Oliveira Duarte médica assistente Hematologia Hemocentro - Unicamp incidênciaidê i ~ 20,000 casos novos e ~10.000 mortes relacionadas ao mieloma nos EUA(2010) Mais comum em homens
MIELOMA MÚLTIPLO Gislaine Oliveira Duarte médica assistente Hematologia Hemocentro - Unicamp incidênciaidê i ~ 20,000 casos novos e ~10.000 mortes relacionadas ao mieloma nos EUA(2010) Mais comum em homens
Revisão Concisa. do Mieloma e Opções de Tratamento. Improving Lives Finding the Cure. Mieloma Múltiplo Câncer da Medula Óssea
 Mieloma Múltiplo Câncer da Medula Óssea Revisão Concisa do Mieloma e Opções de Tratamento 2015 Preparado por Brian G.M. Durie, MD Rua Jandiatuba, 630 - Torre B - conj. 333 Vila Andrade - São Paulo CEP:
Mieloma Múltiplo Câncer da Medula Óssea Revisão Concisa do Mieloma e Opções de Tratamento 2015 Preparado por Brian G.M. Durie, MD Rua Jandiatuba, 630 - Torre B - conj. 333 Vila Andrade - São Paulo CEP:
Revisão Concisa. da Doença e Opções de Tratamento. Improving Lives Finding the Cure. Mieloma Múltiplo Câncer da Medula Óssea
 Mieloma Múltiplo Câncer da Medula Óssea Revisão Concisa da Doença e Opções de Tratamento Edição 2017 Elaborado por Brian G.M. Durie, MD Rua Jandiatuba, 630 - Torre B - cj 334 - São Paulo - SP - CEP 05716-150
Mieloma Múltiplo Câncer da Medula Óssea Revisão Concisa da Doença e Opções de Tratamento Edição 2017 Elaborado por Brian G.M. Durie, MD Rua Jandiatuba, 630 - Torre B - cj 334 - São Paulo - SP - CEP 05716-150
Testes Freelite e Hevylite
 Mieloma Múltiplo Câncer de Medula Óssea Entendendo Testes Freelite e Hevylite Rua Jandiatuba, 630 - Torre B - conj. 333 Vila Andrade - São Paulo CEP: 05716-150 Fone: 11 3726.5037 www. 2015, International
Mieloma Múltiplo Câncer de Medula Óssea Entendendo Testes Freelite e Hevylite Rua Jandiatuba, 630 - Torre B - conj. 333 Vila Andrade - São Paulo CEP: 05716-150 Fone: 11 3726.5037 www. 2015, International
PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS
 Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS MIELOMA MÚLTIPLO Versão 00/2015 ELABORADO POR Dra. Bruma Rosa Viana Carvalho Versão: 00/2015
Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS MIELOMA MÚLTIPLO Versão 00/2015 ELABORADO POR Dra. Bruma Rosa Viana Carvalho Versão: 00/2015
Revlimid (lenalidomida)
 Revlimid (lenalidomida) Cápsula dura 5 mg 10mg 15 mg 25 mg Revlimid lenalidomida APRESENTAÇÕES Cada embalagem contém 21 cápsulas duras de 5 mg, 10 mg, 15 mg ou 25 mg. USO ORAL USO ADULTO ACIMA DE 18 ANOS
Revlimid (lenalidomida) Cápsula dura 5 mg 10mg 15 mg 25 mg Revlimid lenalidomida APRESENTAÇÕES Cada embalagem contém 21 cápsulas duras de 5 mg, 10 mg, 15 mg ou 25 mg. USO ORAL USO ADULTO ACIMA DE 18 ANOS
Testes Freelite e Hevylite
 Mieloma Múltiplo Câncer de Medula Óssea Rua Jandiatuba, 630 - Torre B - conj. 333 Vila Andrade - São Paulo CEP: 05716-150 Fone: 11 3726.5037 www. Latin America Entendendo Testes Freelite e Hevylite 12650
Mieloma Múltiplo Câncer de Medula Óssea Rua Jandiatuba, 630 - Torre B - conj. 333 Vila Andrade - São Paulo CEP: 05716-150 Fone: 11 3726.5037 www. Latin America Entendendo Testes Freelite e Hevylite 12650
Mieloma Múltiplo. Priscila Hernandez Microsoft [Escolha a data]
![Mieloma Múltiplo. Priscila Hernandez Microsoft [Escolha a data] Mieloma Múltiplo. Priscila Hernandez Microsoft [Escolha a data]](/thumbs/62/47548075.jpg) Mieloma Múltiplo Priscila Hernandez Microsoft [Escolha a data] Mieloma Múltiplo Autoria: Associação Brasileira de Hematologia e Hemoterapia e Terapia Celular Elaboração Final: 30 de outubro de 2013 Participantes:
Mieloma Múltiplo Priscila Hernandez Microsoft [Escolha a data] Mieloma Múltiplo Autoria: Associação Brasileira de Hematologia e Hemoterapia e Terapia Celular Elaboração Final: 30 de outubro de 2013 Participantes:
Câncer e Sistema Imune
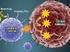 Câncer e Sistema Imune Causas de morte no ocidente Doenças cardiovasculares Câncer Tumores (neoplasias) Tumores benignos: incapazes de crescer indefinidamente, não invadem tecidos vizinhos saudáveis Tumores
Câncer e Sistema Imune Causas de morte no ocidente Doenças cardiovasculares Câncer Tumores (neoplasias) Tumores benignos: incapazes de crescer indefinidamente, não invadem tecidos vizinhos saudáveis Tumores
Caso 1 Citometria de Fluxo Detecção de Múltiplos Clones
 Caso 1 Citometria de Fluxo Detecção de Múltiplos Clones Glicínia Pimenta Serviço de Hematologia/UFRJ Laboratório Sergio Franco/DASA Caso 1 LSP, 85 anos, branca, empresário aposentado, natural RJ QP: Fraqueza
Caso 1 Citometria de Fluxo Detecção de Múltiplos Clones Glicínia Pimenta Serviço de Hematologia/UFRJ Laboratório Sergio Franco/DASA Caso 1 LSP, 85 anos, branca, empresário aposentado, natural RJ QP: Fraqueza
Tópicos de Imunologia Celular e Molecular (Parte 2)
 IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
Gamapatias monoclonais de significado indeterminado.
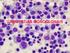 Gamapatias monoclonais de significado indeterminado. Normas orientadoras Objectivos: 1- Uniformização do protocolo de avaliação inicial e de diagnóstico das gamapatias monoclonais e vigilância. 2- Seleccionar
Gamapatias monoclonais de significado indeterminado. Normas orientadoras Objectivos: 1- Uniformização do protocolo de avaliação inicial e de diagnóstico das gamapatias monoclonais e vigilância. 2- Seleccionar
Tratamentos do Câncer. Prof. Enf.º Diógenes Trevizan
 Tratamentos do Câncer Prof. Enf.º Diógenes Trevizan As opções de tratamento oferecidas para os pacientes com câncer devem basear-se em metas realistas e alcançáveis para cada tipo de câncer específico.
Tratamentos do Câncer Prof. Enf.º Diógenes Trevizan As opções de tratamento oferecidas para os pacientes com câncer devem basear-se em metas realistas e alcançáveis para cada tipo de câncer específico.
T E R M O D E C O N S E N T I M E N T O E S C L A R E C I D O TRANSPLANTE DE MEDULA ÓSSEA TRANSPLANTE AUTÓLOGO
 Clínica: Unidade de Transplante Considerando o artigo 22 do Código de Ética Médica (Resolução CFM 1931/2009) e os artigos 6 III e 39 VI da Lei 8.078/90 (Código de Defesa do Consumidor), que garantem ao
Clínica: Unidade de Transplante Considerando o artigo 22 do Código de Ética Médica (Resolução CFM 1931/2009) e os artigos 6 III e 39 VI da Lei 8.078/90 (Código de Defesa do Consumidor), que garantem ao
Revisão Concisa. Mieloma Múltiplo. da Doença e Opções de Tratamento. Câncer da Medula Óssea. International Myeloma Foundation Latin America
 Revisão Concisa da Doença e Opções de Tratamento Mieloma Múltiplo Câncer da Medula Óssea International Myeloma Foundation Latin America Preparado Por Brian G.M Durie, MD Ed 2009 ÍNDICE Introdução O Que
Revisão Concisa da Doença e Opções de Tratamento Mieloma Múltiplo Câncer da Medula Óssea International Myeloma Foundation Latin America Preparado Por Brian G.M Durie, MD Ed 2009 ÍNDICE Introdução O Que
O Cancro - Aspectos gerais O termo Cancro é aplicado e utilizado genericamente para identificar um vasto conjunto de doenças que são os tumores malign
 presentes na Leucemia Daniela Bessa O Cancro - Aspectos gerais O termo Cancro é aplicado e utilizado genericamente para identificar um vasto conjunto de doenças que são os tumores malignos, também designamos
presentes na Leucemia Daniela Bessa O Cancro - Aspectos gerais O termo Cancro é aplicado e utilizado genericamente para identificar um vasto conjunto de doenças que são os tumores malignos, também designamos
Sistema Urinário. Patrícia Dupim
 Sistema Urinário Patrícia Dupim Insuficiência Renal Ocorre quando os rins não conseguem remover os resíduos metabólicos do corpo. As substância normalmente eliminadas na urina acumulam-se nos líquidos
Sistema Urinário Patrícia Dupim Insuficiência Renal Ocorre quando os rins não conseguem remover os resíduos metabólicos do corpo. As substância normalmente eliminadas na urina acumulam-se nos líquidos
Vasculite sistémica primária juvenil rara
 www.printo.it/pediatric-rheumatology/br/intro Vasculite sistémica primária juvenil rara Versão de 2016 2. DIAGNÓSTICO E TRATAMENTO 2.1 Quais são os tipos de vasculite? Como é a vasculite classificada?
www.printo.it/pediatric-rheumatology/br/intro Vasculite sistémica primária juvenil rara Versão de 2016 2. DIAGNÓSTICO E TRATAMENTO 2.1 Quais são os tipos de vasculite? Como é a vasculite classificada?
EDVAN DE QUEIROZ CRUSOÉ
 EDVAN DE QUEIROZ CRUSOÉ ANÁLISE DAS TAXAS DE RESPOSTA DE DIFERENTES ESQUEMAS DE QUIMIOTERAPIA DE INDUÇÃO ANTES E APÓS TRANSPLANTE AUTÓLOGO DE CÉLULAS PROGENITORAS HEMATOPOÉTICAS EM PACIENTES COM MIELOMA
EDVAN DE QUEIROZ CRUSOÉ ANÁLISE DAS TAXAS DE RESPOSTA DE DIFERENTES ESQUEMAS DE QUIMIOTERAPIA DE INDUÇÃO ANTES E APÓS TRANSPLANTE AUTÓLOGO DE CÉLULAS PROGENITORAS HEMATOPOÉTICAS EM PACIENTES COM MIELOMA
SELEÇÃO DE MÉDICOS RESIDENTES PARA 2017 ÁREA DE ATUAÇÃO COM PRÉ-REQUISITO GABARITO
 SELEÇÃO DE MÉDICOS RESIDENTES PARA 2017 ÁREA DE ATUAÇÃO COM PRÉ-REQUISITO PROGRAMA:. PRÉ-REQUISITO: Hematologia e Hemoterapia. GABARITO QUESTÃO A B C D 1 2 3 4 5 6 7 8 9 10 Comissão de Residência Médica
SELEÇÃO DE MÉDICOS RESIDENTES PARA 2017 ÁREA DE ATUAÇÃO COM PRÉ-REQUISITO PROGRAMA:. PRÉ-REQUISITO: Hematologia e Hemoterapia. GABARITO QUESTÃO A B C D 1 2 3 4 5 6 7 8 9 10 Comissão de Residência Médica
Entendendo A Técnica de Detecção de Cadeias Leves Livres no Soro
 International Myeloma Foundation Fale Conosco: 0800 771 0355 Rua Jandiatuba, 630 - Torre B - CJ. 333 São Paulo / SP 05716-150 - Brasil Fone: +55 11 3726.5037 / 0800 771 0355 e-mail: [email protected]
International Myeloma Foundation Fale Conosco: 0800 771 0355 Rua Jandiatuba, 630 - Torre B - CJ. 333 São Paulo / SP 05716-150 - Brasil Fone: +55 11 3726.5037 / 0800 771 0355 e-mail: [email protected]
CONTEÚDO. Introdução O que é Bortezomibe (VELCADE ) e como ele atua? O uso do Bortezomibe (VELCADE ) na prática clínica...
 CONTEÚDO Introdução... 02 O que é Bortezomibe (VELCADE ) e como ele atua?... 02 O uso do Bortezomibe (VELCADE ) na prática clínica... 05 Quais são os possíveis efeitos colaterais do Bortezomibe (VELCADE
CONTEÚDO Introdução... 02 O que é Bortezomibe (VELCADE ) e como ele atua?... 02 O uso do Bortezomibe (VELCADE ) na prática clínica... 05 Quais são os possíveis efeitos colaterais do Bortezomibe (VELCADE
Distúrbios dos Plasmócitos e Doenças Correlatas
 capítulo Distúrbios dos Plasmócitos e Doenças Correlatas Vânia Tietsche de Moraes Hungria Ângelo Maiolino Manuella de Souza Sampaio Almeida Edvan de Queiroz Crusoé GAMOPATIAS MONOCLONAIS As gamopatias
capítulo Distúrbios dos Plasmócitos e Doenças Correlatas Vânia Tietsche de Moraes Hungria Ângelo Maiolino Manuella de Souza Sampaio Almeida Edvan de Queiroz Crusoé GAMOPATIAS MONOCLONAIS As gamopatias
GESF no Transplante. Introdução
 GESF no Transplante Introdução A glomeruloesclerose segmentar e focal (GESF) é um padrão histológico de lesão renal que pode apresentar diferentes etiologias, incluindo doenças imunológicas, genéticas,
GESF no Transplante Introdução A glomeruloesclerose segmentar e focal (GESF) é um padrão histológico de lesão renal que pode apresentar diferentes etiologias, incluindo doenças imunológicas, genéticas,
UNIVERSIDADE REGIONAL DO NOROESTE DO ESTADO DO RIO GRANDE DO SUL- IJUÍ UNIJUÍ CURSO DE PÓS-GRADUAÇÃO EM HEMATOLOGIA LABORATORIAL PATRÍCIA AHLERT
 UNIVERSIDADE REGIONAL DO NOROESTE DO ESTADO DO RIO GRANDE DO SUL- IJUÍ UNIJUÍ CURSO DE PÓS-GRADUAÇÃO EM HEMATOLOGIA LABORATORIAL PATRÍCIA AHLERT CONHECENDO O MIELOMA MÚLTIPLO REVISÃO DE LITERATURA Ijuí-RS
UNIVERSIDADE REGIONAL DO NOROESTE DO ESTADO DO RIO GRANDE DO SUL- IJUÍ UNIJUÍ CURSO DE PÓS-GRADUAÇÃO EM HEMATOLOGIA LABORATORIAL PATRÍCIA AHLERT CONHECENDO O MIELOMA MÚLTIPLO REVISÃO DE LITERATURA Ijuí-RS
Resposta Imune Contra Tumores
 Resposta Imune Contra Tumores Evidências da reatividade imune contra tumores; alterações nas características celulares devido a malignidade; componentes do tumor e do hospedeiro que afetam a progressão
Resposta Imune Contra Tumores Evidências da reatividade imune contra tumores; alterações nas características celulares devido a malignidade; componentes do tumor e do hospedeiro que afetam a progressão
DISCIPLINA DE HEMATOLOGIA HEMATÓCRITO
 DISCIPLINA DE HEMATOLOGIA HEMATÓCRITO Profª.: Aline Félix HEMATÓCRITO Indica a porcentagem do volume de glóbulos vermelhos presente em uma certa quantidade de sangue. Faz parte de um exame chamado de Hemograma
DISCIPLINA DE HEMATOLOGIA HEMATÓCRITO Profª.: Aline Félix HEMATÓCRITO Indica a porcentagem do volume de glóbulos vermelhos presente em uma certa quantidade de sangue. Faz parte de um exame chamado de Hemograma
Mieloma Múltiplo. por Citometria de Fluxo. Dra Maura R Valério Ikoma Laboratório de Citometria de Fluxo
 Mieloma Múltiplo Doença a Residual MínimaM por Citometria de Fluxo Dra Maura R Valério Ikoma Laboratório de Citometria de Fluxo MONITORAMENTO DE DRM Avaliação rápida do potencial de resposta terapêutica
Mieloma Múltiplo Doença a Residual MínimaM por Citometria de Fluxo Dra Maura R Valério Ikoma Laboratório de Citometria de Fluxo MONITORAMENTO DE DRM Avaliação rápida do potencial de resposta terapêutica
Tumores renais. 17/08/ Dra. Marcela Noronha.
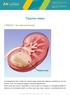 Tumores renais 17/08/2017 - Dra. Marcela Noronha As neoplasias do trato urinário em crianças quase sempre são malignas e localizam-se, em sua maioria, no rim. Os tumores de bexiga e uretra são bastante
Tumores renais 17/08/2017 - Dra. Marcela Noronha As neoplasias do trato urinário em crianças quase sempre são malignas e localizam-se, em sua maioria, no rim. Os tumores de bexiga e uretra são bastante
ESPECÍFICO DE ENFERMAGEM PROF. CARLOS ALBERTO
 ESPECÍFICO DE ENFERMAGEM PROF. CARLOS ALBERTO CONCURSO HOSPITAL UNIVERSITÁRIO ESPECÍFICO DE ENFERMAGEM TEMA 11 PROGRAMA NACIONAL DE IMUNIZAÇÃO DESENVOLVIMENTO DE VACINAS O que faz uma vacina? Estimula
ESPECÍFICO DE ENFERMAGEM PROF. CARLOS ALBERTO CONCURSO HOSPITAL UNIVERSITÁRIO ESPECÍFICO DE ENFERMAGEM TEMA 11 PROGRAMA NACIONAL DE IMUNIZAÇÃO DESENVOLVIMENTO DE VACINAS O que faz uma vacina? Estimula
RASTREANDO CLONES DE PLASMÓCITOS NA MEDULA ÓSSEA
 RASTREANDO CLONES DE PLASMÓCITOS NA MEDULA ÓSSEA Maura R Valério Ikoma Laboratório de Citometria de Fluxo Serviço de Transplante de Medula Óssea Hospital Amaral Carvalho - Jau Maura R Valério Ikoma Residência
RASTREANDO CLONES DE PLASMÓCITOS NA MEDULA ÓSSEA Maura R Valério Ikoma Laboratório de Citometria de Fluxo Serviço de Transplante de Medula Óssea Hospital Amaral Carvalho - Jau Maura R Valério Ikoma Residência
1) Qual translocação é característica da Leucemia mielóide crônica? a) t(14;18) b) t(9,21) c) t(9;22) d) t(22,9) e) t(7;22)
 Questões Hematologia P2 Turma B 1) Qual translocação é característica da Leucemia mielóide crônica? a) t(14;18) b) t(9,21) c) t(9;22) d) t(22,9) e) t(7;22) 2) Paciente, sexo masculino, 68 anos, encaminhando
Questões Hematologia P2 Turma B 1) Qual translocação é característica da Leucemia mielóide crônica? a) t(14;18) b) t(9,21) c) t(9;22) d) t(22,9) e) t(7;22) 2) Paciente, sexo masculino, 68 anos, encaminhando
Biologia. Transplantes e Doenças Autoimunes. Professor Enrico Blota.
 Biologia Transplantes e Doenças Autoimunes Professor Enrico Blota www.acasadoconcurseiro.com.br Biologia HEREDITARIEDADE E DIVERSIDADE DA VIDA- TRANSPLANTES, IMUNIDADE E DOENÇAS AUTOIMUNES Os transplantes
Biologia Transplantes e Doenças Autoimunes Professor Enrico Blota www.acasadoconcurseiro.com.br Biologia HEREDITARIEDADE E DIVERSIDADE DA VIDA- TRANSPLANTES, IMUNIDADE E DOENÇAS AUTOIMUNES Os transplantes
Após um episódio de ITU, há uma chance de aproximadamente 19% de aparecimento de cicatriz renal
 Compartilhe conhecimento: Devemos ou não continuar prescrevendo antibiótico profilático após diagnóstico da primeira infecção urinária? Analisamos recente revisão sistemática e trazemos a resposta. Em
Compartilhe conhecimento: Devemos ou não continuar prescrevendo antibiótico profilático após diagnóstico da primeira infecção urinária? Analisamos recente revisão sistemática e trazemos a resposta. Em
AULA 1: Introdução à Quimioterapia Antineoplásica
 FARMACOLOGIA DOS QUIMIOTERÁPICOS AULA 1: Introdução à Quimioterapia Antineoplásica Profª. MsC Daniele Cavalheiro Oliveira Zampar Farmacêutica Especialista em Oncologia - Sobrafo Campo Grande, 29/09/2012
FARMACOLOGIA DOS QUIMIOTERÁPICOS AULA 1: Introdução à Quimioterapia Antineoplásica Profª. MsC Daniele Cavalheiro Oliveira Zampar Farmacêutica Especialista em Oncologia - Sobrafo Campo Grande, 29/09/2012
ENFERMAGEM DOENÇAS INFECCIOSAS E PARASITÁRIAS. HIV/AIDS Aula 2. Profª. Tatiane da Silva Campos
 ENFERMAGEM DOENÇAS INFECCIOSAS E PARASITÁRIAS HIV/AIDS Aula 2 Profª. Tatiane da Silva Campos Diagnóstico - investigação laboratorial após a suspeita de risco de infecção pelo HIV. janela imunológica é
ENFERMAGEM DOENÇAS INFECCIOSAS E PARASITÁRIAS HIV/AIDS Aula 2 Profª. Tatiane da Silva Campos Diagnóstico - investigação laboratorial após a suspeita de risco de infecção pelo HIV. janela imunológica é
Ritha Capelato 4⁰ ano Medicina UFGD MIELOMA MULTIPLO
 MIELOMA MULTIPLO 18.06.08 É uma neoplasia de uma cel terminal neoplasia de plasmocito. Depois dele, nada mais existe, não tem nenhuma cel que vai diferenciar ou desdiferenciar. É uma cel terminal, fim
MIELOMA MULTIPLO 18.06.08 É uma neoplasia de uma cel terminal neoplasia de plasmocito. Depois dele, nada mais existe, não tem nenhuma cel que vai diferenciar ou desdiferenciar. É uma cel terminal, fim
TECIDO HEMATOPOIÉTICO E SANGUÍNEO
 TECIDO HEMATOPOIÉTICO E SANGUÍNEO CARACTERÍSTICAS Denomina-se hematopoiese o processo de formação dos elementos figurados do sangue; A hematopoiese antes do nascimento ocorre no saco vitelínico do embrião
TECIDO HEMATOPOIÉTICO E SANGUÍNEO CARACTERÍSTICAS Denomina-se hematopoiese o processo de formação dos elementos figurados do sangue; A hematopoiese antes do nascimento ocorre no saco vitelínico do embrião
Sessão Clínica 28/05/2012. Relatora: Dra. Nayara ( R2 ) Debatedor: Dra. Fernanda Morais ( R1 )
 Hospital Escola Álvaro Alvim Serviço de Clínica Médica Faculdade de Medicina de Campos Sessão Clínica 28/05/2012 Orientador: Prof. Luiz E. Castro Relatora: Dra. Nayara ( R2 ) Debatedor: Dra. Fernanda Morais
Hospital Escola Álvaro Alvim Serviço de Clínica Médica Faculdade de Medicina de Campos Sessão Clínica 28/05/2012 Orientador: Prof. Luiz E. Castro Relatora: Dra. Nayara ( R2 ) Debatedor: Dra. Fernanda Morais
Leucemias Agudas: 2. Anemia: na leucemia há sempre anemia, então esperamos encontrar valores diminuídos de hemoglobina, hematócrito e eritrócitos.
 Leucemias Agudas: Leucemias são disfunções graves da hematopoese, consideradas neoplasias hematológicas, que resultam em grandes alterações na composição do sangue. Na maioria das leucemias, todo o hemograma
Leucemias Agudas: Leucemias são disfunções graves da hematopoese, consideradas neoplasias hematológicas, que resultam em grandes alterações na composição do sangue. Na maioria das leucemias, todo o hemograma
φ Fleury Stem cell Mastócitos Mieloblastos Linfócito pequeno Natural Killer (Grande linfócito granular) Hemácias Linfócito T Linfócito B Megacariócito
 Hemopoese Marcos Fleury [email protected] Hematopoese É o processo de formação, maturação e liberação das células sanguíneas Eritropoese Leucopoese Trombopoese - Hemácias - Leucócitos - Plaquetas Tem como
Hemopoese Marcos Fleury [email protected] Hematopoese É o processo de formação, maturação e liberação das células sanguíneas Eritropoese Leucopoese Trombopoese - Hemácias - Leucócitos - Plaquetas Tem como
ENFERMAGEM. DOENÇAS HEMATOLÓGICAS Parte 1. Profª. Tatiane da Silva Campos
 ENFERMAGEM DOENÇAS HEMATOLÓGICAS Parte 1 Profª. Tatiane da Silva Campos Composição do Sangue: Doenças Hematológicas Plasma = parte liquida; 55% sangue; é constituído por 90% de água, sais minerais, proteínas
ENFERMAGEM DOENÇAS HEMATOLÓGICAS Parte 1 Profª. Tatiane da Silva Campos Composição do Sangue: Doenças Hematológicas Plasma = parte liquida; 55% sangue; é constituído por 90% de água, sais minerais, proteínas
EFEITOS BIOLÓGICOS DAS RADIAÇÕES IONIZANTES
 A radiação perde energia para o meio provocando ionizações Os átomos ionizados podem gerar: Alterações moleculares Danos em órgãos ou tecidos Manifestação de efeitos biológicos 1 MECANISMOS DE AÇÃO Possibilidades
A radiação perde energia para o meio provocando ionizações Os átomos ionizados podem gerar: Alterações moleculares Danos em órgãos ou tecidos Manifestação de efeitos biológicos 1 MECANISMOS DE AÇÃO Possibilidades
OSTEOPOROSE: DIAGNÓSTICO E TRATAMENTO Bruno Ferraz de Souza Abril de 2018
 OSTEOPOROSE: DIAGNÓSTICO E TRATAMENTO Bruno Ferraz de Souza Abril de 2018 1. BREVE INTRODUÇÃO A osteoporose (OP) é uma doença osteometabólica sistêmica caracterizada por alterações da quantidade e/ou qualidade
OSTEOPOROSE: DIAGNÓSTICO E TRATAMENTO Bruno Ferraz de Souza Abril de 2018 1. BREVE INTRODUÇÃO A osteoporose (OP) é uma doença osteometabólica sistêmica caracterizada por alterações da quantidade e/ou qualidade
PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS
 Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS LEUCEMIA LINFOCÍTICA CRÔNICA Versão 00/2015 ELABORAÇÃO Dra. Renata Lygia Vieira Vasconcelos
Fundação de Hematologia e Hemoterapia de Pernambuco - HEMOPE PROTOCOLOS DE TRATAMENTO DE DOENÇAS HEMATOLÓGICAS LEUCEMIA LINFOCÍTICA CRÔNICA Versão 00/2015 ELABORAÇÃO Dra. Renata Lygia Vieira Vasconcelos
TRANSPLANTE DE MEDULA ÓSSEA
 TRANSPLANTE DE MEDULA ÓSSEA JOSÉ ULYSSES AMIGO FILHO fevereiro de de 2012 Dr.Donall Thomas Dr.Ricardo Pasquini Transplante de medula óssea TIPOS DE TRANSPLANTE SINGÊNICOS ALOGÊNICOS - aparentados haploidênticos
TRANSPLANTE DE MEDULA ÓSSEA JOSÉ ULYSSES AMIGO FILHO fevereiro de de 2012 Dr.Donall Thomas Dr.Ricardo Pasquini Transplante de medula óssea TIPOS DE TRANSPLANTE SINGÊNICOS ALOGÊNICOS - aparentados haploidênticos
R1CM HC UFPR Dra. Elisa D. Gaio Prof. CM HC UFPR Dr. Mauricio Carvalho
 R1CM HC UFPR Dra. Elisa D. Gaio Prof. CM HC UFPR Dr. Mauricio Carvalho CASO CLÍNICO Homem, 45 anos, com cirrose por HCV foi admitido com queixa de fraqueza e icterícia de início recente. O paciente possuía
R1CM HC UFPR Dra. Elisa D. Gaio Prof. CM HC UFPR Dr. Mauricio Carvalho CASO CLÍNICO Homem, 45 anos, com cirrose por HCV foi admitido com queixa de fraqueza e icterícia de início recente. O paciente possuía
Síndrome Periódica Associada à Criopirina (CAPS)
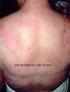 www.printo.it/pediatric-rheumatology/br/intro Síndrome Periódica Associada à Criopirina (CAPS) Versão de 2016 1. O QUE É A CAPS 1.1 O que é? A Síndrome Periódica Associada à Criopirina (CAPS) compreende
www.printo.it/pediatric-rheumatology/br/intro Síndrome Periódica Associada à Criopirina (CAPS) Versão de 2016 1. O QUE É A CAPS 1.1 O que é? A Síndrome Periódica Associada à Criopirina (CAPS) compreende
Resposta Imunológica humoral. Alessandra Barone
 Resposta Imunológica humoral Alessandra Barone Estimulada por antígenos extracelulares Mediada por anticorpos produzidos por plasmócitos. Linfócito B Resposta T independente: Estimulada diretamente por
Resposta Imunológica humoral Alessandra Barone Estimulada por antígenos extracelulares Mediada por anticorpos produzidos por plasmócitos. Linfócito B Resposta T independente: Estimulada diretamente por
EXAMES LABORATORIAIS PROF. DR. CARLOS CEZAR I. S. OVALLE
 EXAMES LABORATORIAIS PROF. DR. CARLOS CEZAR I. S. OVALLE EXAMES LABORATORIAIS Coerências das solicitações; Associar a fisiopatologia; Correlacionar os diversos tipos de exames; A clínica é a observação
EXAMES LABORATORIAIS PROF. DR. CARLOS CEZAR I. S. OVALLE EXAMES LABORATORIAIS Coerências das solicitações; Associar a fisiopatologia; Correlacionar os diversos tipos de exames; A clínica é a observação
Sepse Professor Neto Paixão
 ARTIGO Sepse Olá guerreiros concurseiros. Neste artigo vamos relembrar pontos importantes sobre sepse. Irá encontrar de forma rápida e sucinta os aspectos que você irá precisar para gabaritar qualquer
ARTIGO Sepse Olá guerreiros concurseiros. Neste artigo vamos relembrar pontos importantes sobre sepse. Irá encontrar de forma rápida e sucinta os aspectos que você irá precisar para gabaritar qualquer
Dia Mundial de Combate ao Câncer: desmistifique os mitos e verdades da doença
 Dia Mundial de Combate ao Câncer: desmistifique os mitos e verdades da doença Enviado por Link Comunicação 03-Abr-2014 PQN - O Portal da Comunicação Link Comunicação É mito ou verdade? Câncer tem cura?
Dia Mundial de Combate ao Câncer: desmistifique os mitos e verdades da doença Enviado por Link Comunicação 03-Abr-2014 PQN - O Portal da Comunicação Link Comunicação É mito ou verdade? Câncer tem cura?
Emergências Oncológicas - Síndrome de. Compressão Medular na Emergência
 Emergências Oncológicas - Síndrome de Compressão Medular na Emergência Autores e Afiliação: José Maurício S C Mota. Instituto do Câncer do Estado de São Paulo, ex-médico assistente da Unidade de Emergência,
Emergências Oncológicas - Síndrome de Compressão Medular na Emergência Autores e Afiliação: José Maurício S C Mota. Instituto do Câncer do Estado de São Paulo, ex-médico assistente da Unidade de Emergência,
BIOLOGIA. Hereditariedade e Diversidade da Vida Câncer. Prof. Daniele Duó
 BIOLOGIA Hereditariedade e Diversidade da Vida Câncer Prof. Daniele Duó A palavra câncer é um termo amplo que abrange mais de 200 doenças que possuem duas características em comum: - Um crescimento celular
BIOLOGIA Hereditariedade e Diversidade da Vida Câncer Prof. Daniele Duó A palavra câncer é um termo amplo que abrange mais de 200 doenças que possuem duas características em comum: - Um crescimento celular
O QUE É? O RABDOMIOSARCOMA
 O QUE É? O RABDOMIOSARCOMA Músculo O RABDOMIOSARCOMA O QUE SIGNIFICA ESTADIO? O QUE É O RABDOMIOSARCOMA? O rabdomiosarcoma é um tumor dos tecidos moles (tecidos que suportam e ligam as várias partes do
O QUE É? O RABDOMIOSARCOMA Músculo O RABDOMIOSARCOMA O QUE SIGNIFICA ESTADIO? O QUE É O RABDOMIOSARCOMA? O rabdomiosarcoma é um tumor dos tecidos moles (tecidos que suportam e ligam as várias partes do
Biologia 12º ano Imunidade e controlo de doenças; Biotecnologia no diagnóstico e terapêutica
 Escola Básica e Secundária Prof. Reynaldo dos Santos Biologia 12º ano Imunidade e controlo de doenças; Biotecnologia no diagnóstico e terapêutica Teste de Avaliação Leia atentamente os textos das perguntas,
Escola Básica e Secundária Prof. Reynaldo dos Santos Biologia 12º ano Imunidade e controlo de doenças; Biotecnologia no diagnóstico e terapêutica Teste de Avaliação Leia atentamente os textos das perguntas,
REVISÃO RESUMIDA MIELOMA MÚLTIPLO INTERNATIONAL MYELOMA FOUNDATION. Câncer da Medula Óssea DO MIELOMA E DAS OPÇÕES DE TRATAMENTO
 INTERNATIONAL MYELOMA FOUNDATION REVISÃO RESUMIDA DO MIELOMA E DAS OPÇÕES DE TRATAMENTO MIELOMA MÚLTIPLO Câncer da Medula Óssea EDIÇÃO DE 2003 PREPARADA PELO DR. BRIAN G. M. DURIE International Myeloma
INTERNATIONAL MYELOMA FOUNDATION REVISÃO RESUMIDA DO MIELOMA E DAS OPÇÕES DE TRATAMENTO MIELOMA MÚLTIPLO Câncer da Medula Óssea EDIÇÃO DE 2003 PREPARADA PELO DR. BRIAN G. M. DURIE International Myeloma
Outras Anemias: Vamos lá? NAC Núcleo de Aprimoramento científico Hemograma: Interpretação clínica e laboratorial do exame. Jéssica Louise Benelli
 Outras Anemias: A anemia por si só não é uma doença, e sim uma consequência de algum desequilíbrio entre os processos de produção e perda de eritrócitos, que leva a diminuição de hemoglobina. A inúmera
Outras Anemias: A anemia por si só não é uma doença, e sim uma consequência de algum desequilíbrio entre os processos de produção e perda de eritrócitos, que leva a diminuição de hemoglobina. A inúmera
GABARITO RESIDÊNCIA MÉDICA R1-2017
 RESIDÊNCIA MÉDICA R1-2017 1 D 21 D 41 C 61 A 81 B 2 A 22 A 42 A 62 A 82 C 3 B 23 B 43 C 63 C 83 A 4 B 24 C 44 D 64 D 84 B 5 C 25 A 45 B 65 A 85 C 6 C 26 D 46 C 66 A 86 D 7 B 27 C 47 A 67 C 87 D 8 C 28
RESIDÊNCIA MÉDICA R1-2017 1 D 21 D 41 C 61 A 81 B 2 A 22 A 42 A 62 A 82 C 3 B 23 B 43 C 63 C 83 A 4 B 24 C 44 D 64 D 84 B 5 C 25 A 45 B 65 A 85 C 6 C 26 D 46 C 66 A 86 D 7 B 27 C 47 A 67 C 87 D 8 C 28
André Luís Montillo UVA
 André Luís Montillo UVA Definição: É uma doença sistêmica de origem desconhecida que determina alteração no Processo de Remodelação Óssea. É determinada por osteoclastos anormais que aceleram o remodelamento
André Luís Montillo UVA Definição: É uma doença sistêmica de origem desconhecida que determina alteração no Processo de Remodelação Óssea. É determinada por osteoclastos anormais que aceleram o remodelamento
MAGNÉSIO DIMALATO. FÓRMULA MOLECULAR: C4H6Mg2O7. PESO MOLECULAR: 396,35 g/mol
 MAGNÉSIO DIMALATO FÓRMULA MOLECULAR: C4H6Mg2O7 PESO MOLECULAR: 396,35 g/mol Importante para mais de 300 processos biológicos no organismo, o magnésio é um mineral essencial utilizado na síntese de proteínas
MAGNÉSIO DIMALATO FÓRMULA MOLECULAR: C4H6Mg2O7 PESO MOLECULAR: 396,35 g/mol Importante para mais de 300 processos biológicos no organismo, o magnésio é um mineral essencial utilizado na síntese de proteínas
Metástases ósseas em Câncer de Próstata Há algo além dos bisfosfonatos?
 Metástases ósseas em Câncer de Próstata Há algo além dos bisfosfonatos? Dr. João Paulo Solar Vasconcelos Oncologista Clínico Conflito de Interesses De acordo com a Norma 1595/2000 do Conselho Federal de
Metástases ósseas em Câncer de Próstata Há algo além dos bisfosfonatos? Dr. João Paulo Solar Vasconcelos Oncologista Clínico Conflito de Interesses De acordo com a Norma 1595/2000 do Conselho Federal de
AVALIAÇÃO BIOQUÍMICA NO IDOSO
 C E N T R O U N I V E R S I T Á R I O C AT Ó L I C O S A L E S I A N O A U X I L I U M C U R S O D E N U T R I Ç Ã O - T U R M A 6 º T E R M O D I S C I P L I N A : N U T R I Ç Ã O E M G E R I AT R I A
C E N T R O U N I V E R S I T Á R I O C AT Ó L I C O S A L E S I A N O A U X I L I U M C U R S O D E N U T R I Ç Ã O - T U R M A 6 º T E R M O D I S C I P L I N A : N U T R I Ç Ã O E M G E R I AT R I A
Febre recorrente relacionada com NLRP12
 www.printo.it/pediatric-rheumatology/pt/intro Febre recorrente relacionada com NLRP12 Versão de 2016 1. O QUE É A FEBRE RECORRENTE RELACIONADA COM NLRP12 1.1 O que é? A febre recorrente relacionada com
www.printo.it/pediatric-rheumatology/pt/intro Febre recorrente relacionada com NLRP12 Versão de 2016 1. O QUE É A FEBRE RECORRENTE RELACIONADA COM NLRP12 1.1 O que é? A febre recorrente relacionada com
Tratamento Com freqüência, é possível se prevenir ou controlar as cefaléias tensionais evitando, compreendendo e ajustando o estresse que as ocasiona.
 CEFALÉIAS As cefaléias (dores de cabeça) encontram-se entre os problemas médicos mais comuns. Alguns indivíduos apresentam cefaléias freqüentes, enquanto outros raramente as apresentam. As cefaléias podem
CEFALÉIAS As cefaléias (dores de cabeça) encontram-se entre os problemas médicos mais comuns. Alguns indivíduos apresentam cefaléias freqüentes, enquanto outros raramente as apresentam. As cefaléias podem
Introdução a imunologia clínica. Alessandra Barone
 Introdução a imunologia clínica Alessandra Barone Definições Imunógeno: Substância que induz uma resposta imune específica. Antígeno (Ag): Substância que reage com os produtos de uma resposta imune específica.
Introdução a imunologia clínica Alessandra Barone Definições Imunógeno: Substância que induz uma resposta imune específica. Antígeno (Ag): Substância que reage com os produtos de uma resposta imune específica.
Farmacologia dos Antiinflamatórios Esteroidais (GLICOCORTICÓIDES)
 Farmacologia dos Antiinflamatórios Esteroidais (GLICOCORTICÓIDES) Profª Drª Flávia Cristina Goulart Universidade Estadual Paulista CAMPUS DE MARÍLIA Faculdade de Filosofia e Ciências UNESP Mecanismo de
Farmacologia dos Antiinflamatórios Esteroidais (GLICOCORTICÓIDES) Profª Drª Flávia Cristina Goulart Universidade Estadual Paulista CAMPUS DE MARÍLIA Faculdade de Filosofia e Ciências UNESP Mecanismo de
Dissertação Artigo de Revisão Bibliográfica. Mestrado Integrado em Medicina 2014/2015
 Mestrado Integrado em Medicina 2014/2015 A Evolução da Abordagem Terapêutica do Mieloma Múltiplo nos últimos 20 anos Autor: Sara Maria Mosca Ferreira da Silva Orientador: Dra. Cristina Maria Andrade Pereira
Mestrado Integrado em Medicina 2014/2015 A Evolução da Abordagem Terapêutica do Mieloma Múltiplo nos últimos 20 anos Autor: Sara Maria Mosca Ferreira da Silva Orientador: Dra. Cristina Maria Andrade Pereira
Transplante de Células Tronco Hematopoéticas
 Transplante de Células Tronco Hematopoéticas Fábio Rodrigues Kerbauy Andreza Alice Feitosa Ribeiro Introdução Transplante de células tronco hematopoéticas (TCTH) é uma modalidade de tratamento baseado
Transplante de Células Tronco Hematopoéticas Fábio Rodrigues Kerbauy Andreza Alice Feitosa Ribeiro Introdução Transplante de células tronco hematopoéticas (TCTH) é uma modalidade de tratamento baseado
RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR
 RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR DCI carfilzomib N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5688304 Frasco para injetáveis
RELATÓRIO PÚBLICO DE AVALIAÇÃO PRÉVIA DO MEDICAMENTO EM MEIO HOSPITALAR DCI carfilzomib N.º Registo Nome Comercial Apresentação/Forma Farmacêutica/Dosagem Titular de AIM 5688304 Frasco para injetáveis
Tratamento adjuvante sistêmico (como decidir)
 Tópicos atuais em câncer de mama Tratamento adjuvante sistêmico (como decidir) Dr. André Sasse Oncologista Clínico [email protected] Centro de Evidências em Oncologia HC UNICAMP Centro de Evidências em
Tópicos atuais em câncer de mama Tratamento adjuvante sistêmico (como decidir) Dr. André Sasse Oncologista Clínico [email protected] Centro de Evidências em Oncologia HC UNICAMP Centro de Evidências em
Explicação do conteúdo
 Ítens do exame Explicação do conteúdo Nível normal Os níveis regulares (normais) podem variar de acordo a como o exame é realizado. Procure se informar no local onde realizou o exame, os níveis básicos
Ítens do exame Explicação do conteúdo Nível normal Os níveis regulares (normais) podem variar de acordo a como o exame é realizado. Procure se informar no local onde realizou o exame, os níveis básicos
Conteúdo. Introdução. O que são Bisfosfonatos? Introdução O que são os bisfosfonatos? Os bisfosfonatos são um tipo de quimioterapia?...
 Conteúdo Introdução... 3 O que são os bisfosfonatos?... 3 Os bisfosfonatos são um tipo de quimioterapia?... 4 Quem se beneficia dos bisfosfonatos?... 4 Quais os diferentes tipos de bisfosfonatos?... 5
Conteúdo Introdução... 3 O que são os bisfosfonatos?... 3 Os bisfosfonatos são um tipo de quimioterapia?... 4 Quem se beneficia dos bisfosfonatos?... 4 Quais os diferentes tipos de bisfosfonatos?... 5
KYPROLIS. Mieloma Múltiplo. Entendendo. (carfilzomibe) para injeção Uma Publicação da International Myeloma Foundation
 Mieloma Múltiplo Câncer da Medula Óssea Entendendo KYPROLIS (carfilzomibe) para injeção Uma Publicação da International Myeloma Foundation Dedicada a melhorar a qualidade de vida dos pacientes com mieloma
Mieloma Múltiplo Câncer da Medula Óssea Entendendo KYPROLIS (carfilzomibe) para injeção Uma Publicação da International Myeloma Foundation Dedicada a melhorar a qualidade de vida dos pacientes com mieloma
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS
 CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS A radiação perde energia para o meio provocando ionizações Os átomos ionizados podem gerar: Alterações moleculares
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS A radiação perde energia para o meio provocando ionizações Os átomos ionizados podem gerar: Alterações moleculares
O que é e para que serve a Próstata
 O que é e para que serve a Próstata A próstata é uma glândula que faz parte do aparelho genital masculino. Está localizada abaixo da bexiga, atravessada pela uretra. Seu tamanho e forma correspondem a
O que é e para que serve a Próstata A próstata é uma glândula que faz parte do aparelho genital masculino. Está localizada abaixo da bexiga, atravessada pela uretra. Seu tamanho e forma correspondem a
ESTUDO DA INFLAMAÇÃO ATRAVÉS DA VIA DE EXPRESSÃO GÊNICA DA GLUTATIONA PEROXIDASE EM PACIENTES RENAIS CRÔNICOS
 ESTUDO DA INFLAMAÇÃO ATRAVÉS DA VIA DE EXPRESSÃO GÊNICA DA GLUTATIONA PEROXIDASE EM PACIENTES RENAIS CRÔNICOS ALUNA: Roberta Gomes Batista ORIENTADOR: Profa. Dra. Flávia de Sousa Gehrke UNIVERSIDADE PAULISTA
ESTUDO DA INFLAMAÇÃO ATRAVÉS DA VIA DE EXPRESSÃO GÊNICA DA GLUTATIONA PEROXIDASE EM PACIENTES RENAIS CRÔNICOS ALUNA: Roberta Gomes Batista ORIENTADOR: Profa. Dra. Flávia de Sousa Gehrke UNIVERSIDADE PAULISTA
INTRODUÇÃO AO LINFOMA EM GATOS
 INTRODUÇÃO AO LINFOMA EM GATOS Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria Linfoma em gatos (sinônimos) Linfoma Século XXI
INTRODUÇÃO AO LINFOMA EM GATOS Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria Linfoma em gatos (sinônimos) Linfoma Século XXI
TECIDO HEMATOPOIETICO E SANGUÍNEO
 TECIDO HEMATOPOIETICO E SANGUÍNEO CARACTERÍSTICAS O sangue é o único tecido conjuntivo líquido do copo; Funções: + Transporte (O 2, CO 2, nutrientes, resíduos, hormônios); + Regulação (ph, temperatura,
TECIDO HEMATOPOIETICO E SANGUÍNEO CARACTERÍSTICAS O sangue é o único tecido conjuntivo líquido do copo; Funções: + Transporte (O 2, CO 2, nutrientes, resíduos, hormônios); + Regulação (ph, temperatura,
Reações de Hipersensibilidade
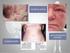 UNIVERSIDADE FEDERAL DE JUIZ DE FORA Reações de Hipersensibilidade Conceito Todos os distúrbios causados pela resposta imune são chamados de doenças de Hipersensibilidade Prof. Gilson C.Macedo Classificação
UNIVERSIDADE FEDERAL DE JUIZ DE FORA Reações de Hipersensibilidade Conceito Todos os distúrbios causados pela resposta imune são chamados de doenças de Hipersensibilidade Prof. Gilson C.Macedo Classificação
AO SEU LADO. Homem que e homem se previne.
 AO SEU LADO Homem que e homem se previne. Novembro foi escolhido como o mês para conscientizar sobre o câncer de próstata. De tabu a solução, o Novembro Azul tem ajudado milhares de homens a se prevenir
AO SEU LADO Homem que e homem se previne. Novembro foi escolhido como o mês para conscientizar sobre o câncer de próstata. De tabu a solução, o Novembro Azul tem ajudado milhares de homens a se prevenir
Síndrome Periódica Associada à Criopirina (CAPS)
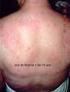 www.printo.it/pediatric-rheumatology/pt/intro Síndrome Periódica Associada à Criopirina (CAPS) Versão de 2016 1. O QUE É A CAPS 1.1 O que é? A Síndrome Periódica Associada à Criopirina (CAPS) compreende
www.printo.it/pediatric-rheumatology/pt/intro Síndrome Periódica Associada à Criopirina (CAPS) Versão de 2016 1. O QUE É A CAPS 1.1 O que é? A Síndrome Periódica Associada à Criopirina (CAPS) compreende
GLOMERULOPATIAS. 5º ano médico. André Balbi
 GLOMERULOPATIAS 5º ano médico André Balbi Definição e apresentação clínica Glomerulopatias: alterações das propriedades dos glomérulos Apresentação clínica: SÍNDROME NEFRÍTICA SÍNDROME NEFRÓTICA OBS :
GLOMERULOPATIAS 5º ano médico André Balbi Definição e apresentação clínica Glomerulopatias: alterações das propriedades dos glomérulos Apresentação clínica: SÍNDROME NEFRÍTICA SÍNDROME NEFRÓTICA OBS :
 www.printo.it/pediatric-rheumatology/br/intro Doença de Kawasaki Versão de 2016 2. DIAGNÓSTICO E TRATAMENTO 2.1 Como é diagnosticada? A DK é uma doença de diagnóstico clínico ou de cabeceira. Isto significa
www.printo.it/pediatric-rheumatology/br/intro Doença de Kawasaki Versão de 2016 2. DIAGNÓSTICO E TRATAMENTO 2.1 Como é diagnosticada? A DK é uma doença de diagnóstico clínico ou de cabeceira. Isto significa
INTRODUÇÃO LESÃO RENAL AGUDA
 INTRODUÇÃO Pacientes em tratamento imunossupressor com inibidores de calcineurina estão sob risco elevado de desenvolvimento de lesão, tanto aguda quanto crônica. A manifestação da injuria renal pode se
INTRODUÇÃO Pacientes em tratamento imunossupressor com inibidores de calcineurina estão sob risco elevado de desenvolvimento de lesão, tanto aguda quanto crônica. A manifestação da injuria renal pode se
Alessandra Comparotto de Menezes IHOC-2013
 Alessandra Comparotto de Menezes IHOC-2013 DEFINIÇÃO: - Proliferação neoplásica clonal de uma linhagem de células do sistema hematopoético Representam um grupo heterogêneo de desordens hematopoéticas malignas
Alessandra Comparotto de Menezes IHOC-2013 DEFINIÇÃO: - Proliferação neoplásica clonal de uma linhagem de células do sistema hematopoético Representam um grupo heterogêneo de desordens hematopoéticas malignas
GABARITO RESIDÊNCIA MÉDICA (UERJ-FCM) 2018 PROVA DISCURSIVA PRÉ-REQUISITO R3 TRANSPLANTE DE MEDULA ÓSSEA (307)
 QUESTÃO 01) Trombocitopenia da gravidez (TG) OU trombocitopenia incidental da gravidez; Púrpura trombocitopênica imunológica (PTI); Trombocitopenia espúria OU erro laboratorial; Doença de von Willebrand;
QUESTÃO 01) Trombocitopenia da gravidez (TG) OU trombocitopenia incidental da gravidez; Púrpura trombocitopênica imunológica (PTI); Trombocitopenia espúria OU erro laboratorial; Doença de von Willebrand;
I Curso de Choque Faculdade de Medicina da UFMG INSUFICIÊNCIA DE MÚLTIPLOS ÓRGÃOS MODS
 I Curso de Choque Faculdade de Medicina da UFMG INSUFICIÊNCIA DE MÚLTIPLOS ÓRGÃOS MODS Alterações Hematológicas Anatomia. Circulação. Distribuição. Função. Adaptação x Disfunção. Alterações Hematológicas
I Curso de Choque Faculdade de Medicina da UFMG INSUFICIÊNCIA DE MÚLTIPLOS ÓRGÃOS MODS Alterações Hematológicas Anatomia. Circulação. Distribuição. Função. Adaptação x Disfunção. Alterações Hematológicas
Manipulação Genética
 Manipulação Genética O que é Biotecnologia? Biotecnologia significa, qualquer aplicação tecnológica que utilize sistemas biológicos, organismos vivos, ou seus derivados, para fabricar ou modificar produtos
Manipulação Genética O que é Biotecnologia? Biotecnologia significa, qualquer aplicação tecnológica que utilize sistemas biológicos, organismos vivos, ou seus derivados, para fabricar ou modificar produtos
Doenças Adquiridas do Neurônio Motor. Msc. Roberpaulo Anacleto
 Doenças Adquiridas do Neurônio Motor Msc. Roberpaulo Anacleto ESCLEROSE LATERAL AMIOTRÓFICA Unidade motora: Esclerose Lateral Amiotrófica Doença degenerativa e progressiva, afetando os neurônios motores
Doenças Adquiridas do Neurônio Motor Msc. Roberpaulo Anacleto ESCLEROSE LATERAL AMIOTRÓFICA Unidade motora: Esclerose Lateral Amiotrófica Doença degenerativa e progressiva, afetando os neurônios motores
Tipo histológico influencia no manejo local das metástases. Fabio Kater oncologista da BP oncologia
 Tipo histológico influencia no manejo local das metástases Fabio Kater oncologista da BP oncologia Introdução Metástases cerebrais primários mais comuns Tumores mais frequentes do sistema nervoso central
Tipo histológico influencia no manejo local das metástases Fabio Kater oncologista da BP oncologia Introdução Metástases cerebrais primários mais comuns Tumores mais frequentes do sistema nervoso central
