ESTUDO DO POTENCIAL TERAPÊUTICO DA MAITENINA EM CÉLULAS DE CÂNCER DE COLO UTERINO
|
|
|
- João Guilherme Alcântara Pinto
- 6 Há anos
- Visualizações:
Transcrição
1 0 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO FACULDADE DE CIÊNCIAS FARMACÊUTICAS CÂMPUS DE ARARAQUARA ANA EMÍLIA BRUMATTI GALIARDI ESTUDO DO POTENCIAL TERAPÊUTICO DA MAITENINA EM CÉLULAS DE CÂNCER DE COLO UTERINO ARARAQUARA-SP 2015
2 1 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO FACULDADE DE CIÊNCIAS FARMACÊUTICAS CÂMPUS DE ARARAQUARA ANA EMÍLIA BRUMATTI GALIARDI ESTUDO DO POTENCIAL TERAPÊUTICO DA MAITENINA EM CÉLULAS DE CÂNCER DE COLO UTERINO Dissertação apresentada ao Programa de Pós- Graduação em Biociências e Biotecnologia Aplicadas à Farmácia da Faculdade de Ciências Farmacêuticas de Araraquara, da Universidade Estadual Paulista Júlio de Mesquita Filho para obtenção do título de Mestre em Biociências e Biotecnologia Aplicadas à Farmácia. Orientadora: Profa a. Dr a. Christiane Pienna Soares Co-orientadora: Prof a. Dr a. Valeria Valente ARARAQUARA-SP 2015
3 2
4 Dedico este trabalho aos meus pais, que sempre acreditaram no meu potencial, e não mediram esforços para que eu pudesse concluir mais esta etapa em minha vida. À minha irmã, pela amizade e companheirismo. Ao meu noivo pelo incentivo e apoio incondicional. 3
5 4 AGRADECIMENTOS À Deus pela vida, benção, proteção e por ter colocado em meu caminho pessoas boas e oportunidades. Aos meus pais Vania e Valmir, pela educação, carinho, amor e incentivo. À minha irmã Maria Eliza por sempre estar presente em minha vida. Ao meu noivo Samuel, pessoa que me traz calma, que sempre me apoiou em todas as minhas escolhas. À professora Christiane Pienna Soares, minha orientadora, por acreditar em meu potencial abrindo as portas de seu laboratório. Tenho profunda admiração por sua competência, e sou muito grata a tudo que fez por mim. À professora Valeria Valente, minha co-orientadora, por sua disponibilidade irrestrita, paciência, incentivo e pelo acompanhamento do meu trilhar desde o início, compartilhando seu conhecimento. Aos colegas do laboratório de Citologia Clínica e Biologia Celular, pelo convívio e ajuda neste trabalho: Geovana, Felipe, Juliana Ferreira, Juliana Sorbo, Luís Fernando, Patrícia, Rodolfo e Thaís. À Júnya, do Núcleo de Proteômica, primeira pessoa que conheci em Araraquara e que me ajudou muito no início desse processo. As meninas com quem morei: Ariane, Pamela, Fabi, Baby, Araguaia, Cinthia, Gabriela Favero e Gabriela Alves pela amizade e por todos os momentos de descontração. Ao Laboratório de Bioquímica Clínica (professores Iguatemi e Amanda), ao Núcleo de Proteômica da Faculdade de Ciências Farmacêuticas de Araraquara e ao Centro de Citometria de Fluxo da Faculdade de Ciências Farmacêuticas de Ribeirão Preto USP por permitirem que parte deste trabalho pudesse ser desenvolvida. À todos os funcionários da Faculdade de Ciências Farmacêuticas de Araraquara que trabalham para tornar nosso trabalho mais fácil: às meninas da limpeza, do café, o pessoal da portaria, da administração e às funcionárias da seção de pós-graduação: Cláudia, Daniela, Flávia e Joyce. À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior - CAPES, pelo apoio financeiro. Enfim, agradeço a todos da minha família, todos os meus amigos e a todas as pessoas que torceram por mim, contribuíram, acreditaram e me ajudaram na concretização desse sonho, seja de forma direta ou indireta.
6 A mente que se abre a uma nova ideia jamais voltará ao seu tamanho original (Albert Einstein). 5
7 6 SUMÁRIO 1. INTRODUÇÃO Câncer de colo uterino e Papilomavírus Humano (HPV) HPV - Biologia e ciclo de vida Aspectos gerais do gênero e da espécie Maytenus ilicifolia OBJETIVOS Objetivo geral Objetivos específicos MATERIAIS E MÉTODOS Isolamento e purificação dos triterpenos quinonametídeos da planta jovem de 22 Maytenus ilicifolia Cultura de células SiHa, C-33A e HaCaT Citotoxicidade com Sulforodamina B Ensaios de Apoptose Ensaio citomofológico de marcação com Hoechst e iodeto de propídeo Atividade de Caspase Ciclo celular Avaliação de genotoxicidade via citometria de fluxo utilizando anti-γh2ax Ensaio de proliferação celular com cristal violeta Ensaio do micronúcleo Análises Estatísticas RESULTADOS Citotoxicidade Ensaios de apoptose Ensaio citomofológico de marcação com Hoechst e iodeto de propídeo Atividade de caspase Ciclo celular Avaliação de genotoxicidade via citometria de fluxo utilizando anti-γh2ax Ensaio de proliferação celular com cristal violeta Ensaio do micronúcleo DISCUSSÃO CONCLUSÕES REFERÊNCIAS BIBLIOGRÁFICAS... 58
8 7 LISTA DE FIGURAS Figura 1. Representação esquemática do genoma viral do HPV Figura 2. Ciclo viral do Papilomavírus Humano (HPV) Figura 3. Integração do DNA viral ao DNA da célula hospedeira Figura 4. Maytenus ilicifolia ou Espinheira-Santa Figura 5. Estrutura da maitenina Figura 6. Ensaio de citotoxicidade. Comparação entre a concentração de maitenina e a porcentagem de células SiHa, C-33 A e HaCaT vivas no tempo de tratamento de 24 horas Figura 7. Ensaio de citotoxicidade. Comparação entre a concentração de maitenina e a porcentagem de células SiHa, C-33 A e HaCaT vivas no tempo de tratamento de 6, 12 e 24 horas Figura 8. Figura representativa do ensaio de Hoechst e Iodeto de Propídeo nas linhagens SiHa, C-33 A e HaCaT... 34/35 Figura 9. Apoptose por coloração Hoechst/IP em células SiHa nos tempos de tratamento de 6 e 12 horas Figura 10. Apoptose por coloração Hoechst/IP em células C-33 A nos tempos de tratamento de 6 e 12 horas Figura 11. Apoptose por coloração Hoechst/IP em células HaCaT nos tempos de tratamento de 6 e 12 horas Figura 12. Atividade de caspase-3 em células SiHa tratadas por 6, 8 e 12 horas Figura 13. Atividade de caspase-3 em células C-33 A tratadas por 6, 8 e 12 horas Figura 14. Atividade de caspase-3 em células HaCaT tratadas por 6 e 8 horas Figura 15. Ensaio de ciclo celular em células SiHa, C-33 A e HaCaT tratadas com maitenina por 12 horas, seguido de pós-tratamento de 24, 48 e 72 horas... 43
9 8 Figura 16. Ensaio de genotoxicidade em células SiHa, C-33 A e HaCaT tratadas com maitenina por 6 horas Figura 17. Ensaio de proliferação celular com cristal violeta com as linhagens SiHa, C-33 A e HaCaT Figura 18. Figura representativa do ensaio de micronúcleo em células SiHa, C-33 A e HaCaT tratadas com maitenina por 6 horas, seguido de pós-tratamento de 24 horas Figura 19. Ensaio de micronúcleo em células SiHa, C-33 A e HaCaT tratadas com uma concentração de maitenina abaixo do CI50 por 24 horas... 49
10 9 LISTA DE ABREVIATURAS E SIGLAS Ac-DMQD-AMC Acetil-Asp-Met-Gln-Asp-amino-4-metilcumarina ANOVA Análise de Variância ATCC American Type Culture Collection CI50 CP CV Concentração capaz de reduzir em 50% a viabilidade celular Controle positivo Controle de veículo C-33 A Células de carcinoma cervical humano não infectadas pelo HPV-16 DAF Diacetato de fluoresceína DMEM Meio de Eagle modificado por Dulbelco (Dulbeco s Modified Eagle s Medium) DMSO Dimetilsulfóxido DP Desvio padrão E Early EDTA ácido etilenodiaminotetraacético E2F Fator epitelial 2 FITC Isotiocianato de fluoresceína F10 Mistura de nutrientes F10 de Ham (Ham s F10 Nutrient mixture) HaCaT Queratinócitos humanos imortalizados HO Hoechst HPV Papilomavírus humano IP Iodeto de propídeo L Late LCR Long control region NuBBe Núcleo de Bioensaios, Biossíntese e Ecofisiologia de Produtos Naturais PBS Solução salina tamponada com fosfato prb Proteína do retinoblastoma p53 Proteína p53 SiHa Linhagem de carcinoma cervical humano infectada pelo HPV-16 SFB Soro fetal bovino URR Upstream regulatory region
11 10 RESUMO O câncer de colo de útero é um problema de saúde pública mundial, especialmente nos países em desenvolvimento, configurando a quarta neoplasia feminina mais comum no mundo. A infecção pelo Papilomavírus Humano (HPV) é o principal fator de risco para o desenvolvimento do referido câncer, estando presente em 90% dos casos de câncer de colo uterino na população mundial. Frente a busca por novos agentes quimioterapêuticos, os produtos naturais tem contríbuido intensamente para a identificação dessas substâncias e o desenvolvimento da terapêutica moderna. Maitenina, é um triterpeno quinonametídeo extraído das raízes da plana Maytenus ilicifolia, que possui algumas atividades biológicas já relatadas, como antifúngica, antiprotozoária e principalmente ação antitumoral. No momento não existem relatos na literatura relacionando a atividade da maitenina em células infectadas por HPV-16. O objetivo do presente estudo foi avaliar a citotoxicidade da maitenina em linhagem de carcinoma cervical infectada por HPV-16 (SiHa), não-infectada pelo vírus (C-33 A) e queratinócitos humanos imortalizados (HaCaT), bem como verificar a indução de apoptose e/ou necrose pelo ensaio de Hoechst e Iodeto de Propídeo e indução de apoptose pela atividade de caspase-3 nas três linhagens celulares, além de verificar alterações no ciclo celular das células tratadas com maitenina e o potencial de genotoxicidade e mutagenicidade, além de avaliar a proliferação das três linhagens. O ensaio de citotoxicidade foi realizado pelo método da sulforodamina B, e as três linhagens celulares foram tratadas durante 6, 12 ou 24 horas. Foi possível observar um efeito concentração e tempo resposta nas três linhagens analisadas. O CI50 foi de 3,26, 8,49 e 3,09 µm para as linhagens SiHa, C-33 A e HaCaT respectivamente, no tempo de tratamento de 24 horas. Com o intuito de avaliar o potencial efeito indutor de apoptose foi realizado o ensaio citomorfológico de marcação com Hoechst e Iodeto de Propídeo nos tempos de tratamento de 6 e 12 horas, e para as três linhagens celulares foi possível observar um efeito tempo-dependente. Além disso, foi observado para as três linhagem, um perfil de morte mista, ou seja, a morte celular ocorre por apoptose e necrose, com predominância de apoptose para as linhagens SiHa e C-33 A e os mesmos níveis de apoptose e necrose para a linhagem HaCaT. Ainda, a linhagem SiHa se mostrou mais sensível que as linhagens C-33 A e HaCaT no tempo de tratamento de 12 horas, demonstrando uma possível seletividade da maitenina. Para complementar este ensaio, foi realizado o ensaio de atividade de caspase-3, no entanto não houve indução da enzima caspase-3 para as linhagens SiHa e C-33 A em nenhum dos tempos testados sugerindo que a morte celular possa ocorrer independente de caspases, enquanto para a linhagem HaCaT foi detectada atividade de caspase-3 no tempo de tratamento de 6 horas. O ensaio de ciclo celular foi realizado nas três linhagens celulares tratadas por 12 horas, seguido de pós-tratamento de 24, 48 e 72 horas, e foi possível notar alterações no ciclo celular para as três linhagens com diminuição na população G1 e aumento das fases S e G2, ocorrendo parada de ciclo celular na fase G2/M para a linhagem SiHa, S e G2/M para linhagem C-33 A e S para a linhagem HaCaT. Através do ensaio de genotoxicidade, onde as linhagens SiHa, C-33 A e HaCaT foram tratadas durante 6 horas, foi possível observar que a maitenina causa danos à dupla fita de DNA para as três linhagens, o que provavelmente ocasionou a parada de ciclo celular. A linhagem C-33 A é a que apresentou maior taxa proliferativa, seguida pelas linhagens SiHa e HaCaT que proliferaram de maneira semelhante. Apesar do potencial genotóxico apresentado pela maitenina, ela não demonstrou mutagenicidade, sendo portanto, considerada segura para uso terapêutico. O dano a dupla fita de DNA, seguido de parada de ciclo celular e morte celular por apoptose e necrose parece explicar a redução da viabilidade celular causada pela maitenina nas três linhagens. Palavras-chave: câncer cervical, HPV, maitenina.
12 11 ABSTRACT Cervical cancer is a worldwide public health problem, especially in developing countries, setting the fourth most common female cancer in the world. The infection by human papillomavirus (HPV) is the main risk factor for the development of this cancer, being present in 90% of cases of cervical cancer in the world population. Forward the search for new chemotherapeutic agents, natural products have strongly contributed to the identification of these substances and the development of modern therapeutics. Maytenin is a quinonemethide triterpene extracted from the roots of Maytenus ilicifolia plant, which has some biological activities previously reported as an antifungal, antiprotozoal and especially antitumor action. At the moment there are no reports in the literature relating the activity of maytenin in infected cells by HPV-16. The aim of this study was to evaluate the cytotoxicity of maytenin in cervical carcinoma line infected by HPV-16 (SiHa), non-infected by the virus (C-33 A) and by immortalized human keratinocytes (HaCaT), as well as verifying the induction of apoptosis and / or necrosis by Hoechst test and propidium iodide and the induction of apoptosis by caspase-3 activity in all three cell lines, in addition to check for changes in the cell cycle of treated cells with maytenin and the potential of genotoxicity and mutagenicity, and to evaluate the proliferation of the three cell lines. The cytotoxicity assay was performed by sulforhodamine B method and the three cell lines were treated during 6, 12 or 24 hours. It was possible to observe a concentration effect and response time in three lines analyzed. The IC50 was 3,26, 8,49 and 3,09 µm for SiHa, C-33 A and HaCaT lines respectively, in 24 hours treatment time. In order to evaluate the potential inductive effect of apoptosis it was performed a marking cytomorphological test with Hoechst and propidium iodide in 6 and 12 hours treatment times, and for the three cell lines it was possible to observe a time-dependent effect. Furthermore, it was observed for the three lines, a mixed death profile, that is, the cell death occurs by apoptosis and necrosis, especially by apoptosis for SiHa and C-33 A lines and the same levels of apoptosis and necrosis for HaCaT line. Still, SiHa line was revealed more sensitive than C-33 A and HaCaT lines in 12 hours treatment time, demonstrating a possible selectivity of maytenin. To complement this test it was performed the caspase-3 activity test, however there was no induction of caspase-3 enzyme for SiHa and C-33 A lines in any tested times suggesting that the cell death can occur independent of caspases, while for HaCaT line it was detected caspase-3 activity in 6 hours treatment time. The cell cycle test was performed in the three cell lines treated by 12 hours, followed by post-treatment of 24, 48 and 72 hours, and it was possible to observe changes in the cell cycle for the three lines with a decrease in G1 population and an increase in S and G2 phases, occurring a cell cycle arrest in the G2 / M phase for SiHa line, S and G2 / M phases for C-33 A line and S phase for HaCaT line. Through the genotoxicity test, where the SiHa, C-33 A and HaCaT lines were treated for 6 hours, it was observed that the maytenin causes damages to double-stranded DNA for the three lines, which probably caused the cell cycle arrest. The C-33 A line is the one that presented the highest proliferative rate, followed by SiHa and HaCaT lines that proliferated similarly. Despite the genotoxic potential presented by maytenin, it didn t show mutagenicity, therefore it was considered safe for therapeutic use. The damage to double-stranded DNA, followed by cell cycle arrest and cell death by apoptosis and necrosis appears to explain the reduction of cell viability caused by maytenin in the three lines. Keywords: cervical cancer, HPV, maytenin
13 12 1. INTRODUÇÃO 1.1. Câncer de colo uterino e Papilomavírus Humano (HPV) Câncer é a denominação dada a um grupo de mais de 100 patologias que têm em comum o crescimento desordenado de células (maligno) que invadem os órgãos e tecidos, e podem se espalhar (metástase) para outros lugares do corpo (INCA, 2015). A célula cancerígena caracteriza-se pela perda de função em decorrência da ausência de diferenciação, proliferação descontrolada, invasão dos tecidos adjacentes e metástase. A origem dessa célula é resultante de alterações genéticas que podem ser produzidas por diversos mecanismos como a inativação de genes supressores de tumor, ativação de oncogenes, inativação de genes responsáveis pela apoptose e mutações produzidas por agentes físicos, biológicos e químicos (CARVALHO et al., 2006). Se estas células se dividirem rapidamente, tendem a ser muito agressivas e incontroláveis, determinando assim a formação de tumores (acúmulo de células cancerosas) ou neoplasias malignas. No entanto, se estas células se multiplicarem lentamente e formarem uma massa localizada se trata de um tumor benigno, raramente constituindo risco de vida (INCA, 2015). As causas do câncer são variadas, podendo ser internas ou externas, estando ambas inter-relacionadas. As causas internas são, geralmente, pré-determinadas e estão ligadas à capacidade do organismo de se defender de agressões externas. As causas externas relacionam-se ao meio ambiente e aos hábitos ou costumes próprios de um ambiente social e cultural. Cerca de 80% a 90% dos cânceres estão relacionados a fatores ambientais (INCA, 2015). O câncer de colo de útero é um sério problema de saúde entre mulheres em todo o mundo, especialmente em países em desenvolvimento. É o quarto tipo mais comum de câncer em mulheres no mundo, com aproximadamente mil novos casos e mil mortes no ano de 2012 (WHO, 2015). No Brasil, estimativas mostram que o câncer do colo do útero é a terceira neoplasia mais comum na população feminina, atrás apenas do câncer de mama e do colorretal, e a quarta causa de morte por câncer entre mulheres de acordo com dados absolutos sobre a incidência e mortalidade por câncer divulgada pelo Instituto Nacional de Câncer. Para o ano de 2014 a estimativa foi de novos casos, com risco estimado de 15,33 novos a cada 100 mil mulheres. Por regiões é mais incidente na região Norte (23,57/100 mil), seguido da regiões Centro-Oeste (22,19/100 mil), Nordeste (18,79/ 100 mil), Sul (15,87/100 mil) e Sudeste (10,15/ 100 mil), respectivamente (INCA, 2015).
14 13 Aproximadamente 80% dos novos casos que são diagnosticados anualmente na população mundial ocorrem nos países em desenvolvimento e estimativas mostram que até 2020 deverá haver um aumento de 90% dos casos (MACIAS et al., 2000; LIN et al., 2001; BOSCH & SANJOSÉ, 2003; ZUR HAUSEN, 2009). A infecção pelo Papilomavírus Humano (HPV) é o principal fator de risco para o desenvolvimento do referido câncer, estando presente em 90% dos casos de câncer de colo uterino na população mundial. A infecção genital por este vírus é muito frequente e na maioria das vezes não causa doença. No entanto, no pequeno número de casos em que a infecção persiste, ocorrem alterações celulares que poderão evoluir para o câncer. Se estas alterações forem rapidamente descobertas são curáveis na maioria dos casos (INCA, 2015). Além de aspectos relacionados à própria infecção pelo HPV, outros fatores tais como uso de contraceptivos orais, grande número de parceiros sexuais, alimentação, raça, tabaco, álcool, fatores imunológicos e outros agentes infecciosos responsáveis por Doenças Sexualmente Transmissíveis (DST), aumentam o risco de desenvolvimento do câncer de colo uterino (IARC, 2005; SPPV, 2013). Assim, fatores ligados ao comportamento sexual, genética e imunidade, parecem influenciar os mecanismos ainda incertos que determinam a regressão ou persistência da infecção e também progressão para lesões precursoras ou câncer (INCA, 2015) O HPV se destaca como uma das doenças sexualmente transmissíveis (DST) mais comuns no mundo, sendo o Brasil um dos líderes mundiais em incidência por este vírus. As mulheres entre 15 e 25 anos são principais vítimas, embora a doença também acometa os homens, fato este atribuído a baixa procura dos homens por serviços de urologia, por fatores como o preconceito ou a falta de informação. A transmissão do HPV ocorre através do contato genital com a pessoa infectada e por via sangüínea, de mãe para filho na hora do parto (BRASIL, 2013). Os HPVs são vírus epiteliotróficos presentes na pele (cutaneotrófico) e mucosa (mucosatrófico) e mais de 100 tipos já foram descritos nos seres humanos, (TUNGTEAKKHUN e DUERKSEN-HUGHES, 2008) e destes 40 são conhecidos por infectar o trato genital, sendo classificados como HPV de alto ou baixo potencial oncogênico com base na prevalência de câncer cervical e seus precursores. Os HPV com baixo potencial oncogênico são principalmente os de tipo 6 e 11 que induzem lesões benignas com o mínimo risco de progressão para malignidade. Os HPV com alto potencial oncogênico são principalmente os tipos 16, 18, 31, 33 e 45. Cerca de 99% dos casos de câncer de colo
15 14 uterino contêm DNA de tipos de HPV de alto risco, sendo o HPV-16 o tipo mais prevalente, seguindo pelos tipos 18,31,33 e 35 (BOULET, 2007). A detecção precoce do câncer de colo de útero em mulheres assintomáticas (rastreamento), através do exame citopatológico (Papanicolaou), permite a detecção das lesões precursoras e da doença em estágios iniciais, antes mesmo dos sintomas aparecerem (BRASIL, 2002). Este exame consiste no estudo das células descamadas esfoliadas da parte interna (endocérvice) e externa (ectocérvice) do colo uterino, e é o método mais utilizado na rede de atenção básica por ser barato, indolor e eficaz. O Ministério da Saúde oferece esse exame gratuitamente por meio do programa nacional de controle de colo de útero, cujo objetivo é reduzir a morbimortalidade pelo referido câncer (BEZERRA, 2005). O rastreamento é a melhor forma para diminuir a incidência e mortalidade por esse câncer. A vacina é uma importante ferramenta na profilaxia ao câncer de colo uterino. Atualmente, existem duas formas de vacinas profiláticas contra o HPV. A vacina quadrivalente protege contra os tipos oncogênicos 6 e 11 e não oncogênicos 16 e 18, e a vacina bivalente que protege contra os tipos oncogênicos 16 e 18 (DROLET, 2015). Em 2015 o Ministério da Saúde, implementou a vacinação de meninas de 9 a 13 anos com a vacina quadrivalente. No entanto, a vacina não elimina as ações de prevenção e de detecção precoce pelo rastreamento através do exame de Papanicolau que busca lesões precursoras e câncer em mulheres assintomáticas (INCA, 2015). A terapia habitual é a quimioterapia, radioterapia e a cirurgia, no entanto, o tipo de tratamento dependerá de alguns fatores como estadiamento da doença, tamanho do tumor e fatores pessoais tais como idade e desejo de ter filhos (INCA, 2015) HPV - Biologia e ciclo de vida Os Papilomavírus humano (HPV) são pequenos vírus não envelopados de DNA de fita dupla, pertencentes à família Papillomaviridae. Possuem capsídeo protéico (composto por duas proteínas estruturais) que se organizam em 72 subunidades (capsômeros), de padrão icosaédrico, com 55 nm de diâmetro. (HORVATH et al., 2010). Seu genoma (Figura 1) apresenta pares de bases, sendo organizado em oito Open Reading Frames (ORFs) e pode ser dividido em dois domínios (BOULET et al., 2007) O primeiro domínio é a região não codificadora denominada LongControlRegion (LCR) ou UpstreamRegulatoryRegion (URR) (KANODIA et al., 2007; PSYRRI & DIMAIO, 2008) que está localizada entre os genes L1 e o início da região precoce e possui
16 15 aproximadamente pb. Esta região não tem qualquer função codificadora proteica, mas contém os elementos promotores, locais de ligação do fator de transcrição e a origem de replicação viral (DOORBAR, et al., 2015). Assim, a região LCR representa 15% do genoma viral (SOUSA et al., 1990; CHEAH e LOOI, 1998). Um segundo domínio da partícula viral codifica as proteínas virais da região L (late) ou região tardia com aproximadamente pb, e região E (early) ou região precoce com aproximadamente pb que representam respectivamente 40% e 45% do genoma do HPV (ZUR HAUSEN, 2002; PSYRRI e DIMAIO, 2008; ZUR HAUSEN, 2009; HORVATH 2010). Os genes da região tardia, L1 e L2, formam sequências altamente conservadas em todos os papilomavírus. Esses genes codificam proteínas do capsídeo viral que são responsáveis por sua antigenicidade, sendo a proteína L1, de 54 kda como principal, e L2, de 52 kda como secundária (MUNGER e HOWLEY 2002; ZUR HUNSEN 2002, 2009; ZHENG e BAKER, 2006; HORVARTH, 2010). Os genes precoces são responsáveis pela replicação do DNA e controle de transcrição de genes alvos (gene E1), controle de transcrição (gene E2), maturação do vírus e alteração da matriz e citoesqueleto celular (gene E4), e no estímulo da proliferação e manutenção da transformação celular (genes E5, E6 e E7) (BOULET, 2007). Figura 1: Representação esquemática do genoma do HPV: genes da região precoce (E), genes da região tardia (L) e a região não codificadora (LCR ou URR) (MUÑOZ et al., 2006). O HPV tem afinidade por células epiteliais da pele e mucosas. Dependendo do tipo de vírus, pode causar proliferação benigna ou maligna. Os diferentes tipos de HPV são definidos como tendo mais de 10 % de diferença em regiões específicas do seu genoma. Portanto,
17 16 determinados tipos virais com diferentes formas de interação determinam, em conjunto, o potencial oncogênico do vírus. (ZUR HUNSEN, 2002) O ciclo de vida do HPV (figura 2) está diretamente ligado ao ciclo de diferenciação das células epiteliais do hospedeiro infectado e inicia-se quando partículas infecciosas entram nas células da camada basal (única camada de células proliferativas indiferenciadas) das mucosas ou epiderme que são capazes de proliferação através de microlesões, de modo a criar um ambiente competente de replicação, o que permite à amplificação do genoma e acondicionamento em partículas infecciosas. (BOULET, 2007; STANLEY, 2008; DOORBAR, 2015). Liberação de partículas virais Progressão e diferenciação Replicação do DNA viral e formação de partículas infectantes Infecção primária de células da camada basal, geralmente através de microlesões Expansão lateral Membrana basal Figura 2: Ciclo viral do Papilomavírus Humano (HPV). Através de microlesões o HPV é capaz de infectar células da camada basal do epitélio. Ao migrar para as camadas suprabasais os genes virais são ativados, o DNA do vírus é replicado e as proteínas do capsômero são sintetizadas. As partículas virais formadas são liberadas na superfície da mucosa onde podem infectar outras células (adaptado de ZUR HUNSEN, 2002). No início da infecção, baixos níveis de DNA viral são sintetizados nas células infectadas da camada basal, formando aproximadamente 50 a 100 cópias epissomais do genoma viral por célula (PETT e COLEMAN, 2007). A infecção das células basais pelo HPV leva à ativação de uma cascata de expressão de genes virais que resulta na replicação de seu genoma, no entanto, a expressão destes genes é amplamente reprimida, existindo apenas uma limitada expressão de genes virais específicos da região precoce. Os genes virais E1 e E2 (fatores de replicação) são os primeiros a serem expressos e formam um complexo que se liga à origem de replicação e atua no sentido de recrutamento de polimerases celulares e proteínas acessórias que mediam a replicação de DNA (KANODIA, 2007). Após a entrada em camadas
18 17 suprabasais, o genoma viral circular é então replicado e proteínas estruturais são formadas. Nas camadas superiores da epiderme ou mucosa, as partículas virais completas são montadas e liberadas, infectando assim outras células (ZUR HUNSEN, 2002). O HPV utiliza a maquinaria celular da célula hospedeira para se replicar, e este processo ocorre no núcleo celular. Inicicialmente após a infecção, o HPV é identificado em partículas virais extracromossômicas (epissoma), replicando seu material genético concomitantemente com os cromossomos da célula hospeira, permanecendo em uma fase latente, um processo relativamente benigno (ALBERTS, 2010). Um passo crucial na progressão para o câncer é a integração do DNA viral ao DNA da célula hospedeira. (PARFENOV, 2014) (figura 3): Figura 3: Integração do DNA viral ao DNA da célula hospedeira. Os papilomavírus possuem cromossomos de DNA circular de fita dupla que normalmente são mantidos de maneira estável nas células basais do epitélio, replicando seu cromossomo concomitantemente com os cromossomos da célula hospedeira (esquerda). Acidentes podem causar a integração de um fragmento do cromossomo dos papilomavírus ao cromossomo do hospedeiro, alterando o ambiente dos genes virais nas células basais, rompendo o controle normal da expressão gênica viral. A expressão desregulada das proteínas virais interfere com o controle da divisão celular nas células basais, ajudando no processo de carcinogenese (direita). (Adaptado de ALBERTS, 2010). As moléculas essenciais na replicação viral e transformação maligna são E6 e E7 que inativam dois importantes genes supressores de tumor. Ambas as proteínas induzem a proliferação, imortalização e transformação maligna das células infectadas (BOULET, 2007). A proteína E7 associa-se com prb, um regulador negativo do ciclo celular que normalmente previne a progressão da fase G1 para a fase S por se associar ao fator de transcrição E2F. Ao
19 18 se ligar a E7, prb é degradada liberando E2F, a qual estimulará a transcrição de genes alvos associados a replicação do DNA, resultando na proliferação celular desordenada (ZUR HAUSEN, 2002; MOTOYAMA et al., 2004; IARC, 2005). A proteína viral E6 completa o papel de E7, prevenindo a apoptose em resposta à entrada não programada na fase S induzida por E7. A associação da proteína E6 dos tipos de HPV de alto risco, com a proteína p53 da célula hospedeira resulta na degradação da p53, comprometendo a interrupção do crescimento celular e a ativação da apoptose induzida por erros no DNA genômico. A perda do controle do ciclo celular mediado por p53 favorece a instabilidade cromossômica e acúmulo de mutações na célula infectada (DOORBAR e CUBIE, 2005). Sugere-se então que a integração do DNA viral ao DNA da célula hospedeira pode alterar a expressão gênica viral levando ao câncer (MADKAN et al., 2007). Os estudos estão direcionados na compreensão da interação entre a célula hospedeira e o HPV mostrando como a pesquisa básica pode contribuir para prevenção do câncer (ZUR HAUSEN, 2002) Aspectos gerais do gênero e da espécie Maytenus ilicifolia Os metabólitos secundários isolados de fontes naturais desempenham um papel fundamental na busca de novos agentes anticâncer (COSTA et al., 2008). A maioria dos fármacos utilizados atualmente na clínica contra o câncer foram descobertos de plantas e microrganismos (MANN, 2002). Dessa forma, o gênero Maytenus é constituído por cerca de 200 espécies distribuídas nos trópicos. A flora brasileira possui 76 espécies desse gênero, sendo 15 referidas para a Amazônia. A ocorrência é ampla, desde a Amazônia até o sul do país (CARVALHO-OKANO e LEITÃO FILHO, 2004). Plantas do gênero Maytenus são extensivamente investigadas visando a obtenção de compostos bioativos, pois são amplamente usadas na medicina popular e tiveram algumas ações investigadas, incluindo inseticida (NÚÑEZ et al., 2004b), citotóxica (OHSAKI et al., 2004; NAKAO et al., 2004), antitumoral (GONZÁLES et al., 2000; COSTA et al., 2008), antioxidante (CORSINO et al., 2003), antiplasmódica (TAHIR et al., 1999), antiulcerogênica (GONZALEZ et al., 2001; DI STASI et al., 2001; DUARTE e DEBUR, 2005; BERSANI- AMADO et al., 2000), anti-inflamatória (JORGE et al., 2004) e antimicrobiana (MOUJIR et al., 1990; RODRÍGUES et al., 2005). Exibem diversas classes de metabólitos secundários,
20 19 incluindo flavonóides (CORSINO et al., 2003; VILEGAS et al., 1999, 2001), triterpenos quinonametídeos (BUFFA FILHO et al., 2000, 2002, 2004; CORSINO et al., 1998c), dímeros de triterpenos (ITOKAWA et al., 1990; GONZÁLEZ et al., 2000; SHIROTA et al., 2004a), triterpenóides tetracíclicos (NÚÑES et al., 2004a), alcalóides piridínicos sesquiterpênicos (CORSINO et al., 1998a, 1998b; SHIROTA et al., 2004b; SANTOS et al., 2012), glicosídeos fenólicos (VILEGAS et al., 1999 e 2001), e maitansinóides (PULLEN et al., 2003), com interessante espectro de atividades biológicas. A espécie Maytenus ilicifolia Martius ex Reiss. (figura 4) é popularmente conhecida como espinheira-santa, "cancorosa-de-sete-espinhos" e "maiteno", dentre outros nomes (OLIVEIRA, 2009). A espécie M. ilicifolia é uma planta nativa do Brasil, e ocorre no subbosque das florestas de Araucária ou às margens de rios, é encontrada predominantemente na região sul do Brasil e a ocorrência nos estados de São Paulo e Mato Grosso do Sul é pouco abundante. (FRANÇA e PEREIRA, 1997). Dentre as espécies do gênero, é a mais conhecida e explorada economicamente, devido a sua aplicabilidade na medicina popular e na indústria de Fitoterápicos, principalmente pela potente ação antiulcerogênica, tendo sua ação comprovada no tratamento de úlceras gástricas. Em 1988, foi incluído como fitoterápico no programa de fitoterapia coordenado pela Central de Medicamentos (DI STASI, 2004). Atualmente, muitas indústrias farmacêuticas produzem e comercializam fitofarmácos contendo essas espécies (SOARES et al., 2004). Segundo o uso popular acredita-se que a M. ilicifolia possa combater várias doenças, dentre as quais podem-se destacar, gastrites e dispepsias. Ainda, acredita-se que possui ações tônicas, analgésicas, antissépticas, cicatrizantes, diuréticas e laxativas (OLIVEIRA, 2009). Figura 4: Maytenus ilicifolia ou Espinheira-Santa
21 20 Triterpenos quinonametídeos são metabólicos secundários restritos a plantas da família Celastraceae, sendo portanto, considerados marcadores quimiotaxômicos desta família. Várias atividades biológicas já foram relatadas para membros deste classe, incluindo atividade antifúngica (GULLO et al., 2012), anti-inflamatória (KIM et al., 2009), antiprotozoária (dos SANTOS et al., 2013), antioxidante (dos SANTOS et al., 2010), antimicrobiana (SETZER et al., 2001), e principalmente ação antitumoral (NGASSAPA et al., 1994; WU et al., 2005; COSTA et al., 2008). Recentemente os triterpenos quinonametídeos mostraram notável atividade antitumoral contra mieloma (NI et al., 2014), câncer hepático (YAN et al., 2014), câncer de próstata (LIU et al., 2014), glioblastoma (BORIDY et al., 2014) e câncer pancreático (DEEB et al., 2014). A maitenina apresenta-se como cristais amorfos alaranjados e pertence à classe dos triterpenos quinonametídeos. Sua estrutura foi descrita por Monache et al (MONACHE et al., 1973) por métodos químicos e espectrais. Apresenta uma estrutura química complexa, por isso não é possível realizar sua síntese química, sendo obtida através das plantas. Nos últimos anos, tem despertado especial atenção, pois é altamente citotóxica para um painel de linhagens celulares (PAZ et al., 2013). Até o momento não existem trabalhos na literatura relacionando células infectadas com HPV-16 e a ação da maitenina. Com o intuito de buscar novos agentes terapêuticos contra câncer de colo uterino em substâncias isoladas de produtos naturais, foi obtido das cascas das raízes da planta Maytenus ilicifolia o triterpeno quinonametídeo denominado maitenina (figura 5), que foi utilizado neste estudo. Figura 5: Estrutura da maitenina (C 28H 36O 3)
22 21 2. OBJETIVOS 2.1. Objetivo Geral O presente estudo teve por objetivo verificar o potencial terapêutico da maitenina, por meio de experimentos in vitro, utilizando células de carcinoma cervical infectadas por HPV-16 (SiHa), não infectadas pelo vírus (C33-A), e queratinócitos humanos imortalizados (HaCaT) Objetivos Específicos Avaliar se a maitenina induz citotoxicidade nas linhagens SiHa, C-33 A e HaCaT através do ensaio de sulforodamina B. Avaliar qualitativa e quantitativamente a apoptose e necrose celular, para diferenciação de apoptose precoce, tardia e necrose, utilizando os corantes de Hoechst e iodeto de propídeo, nas linhagens SiHa, C-33 A e HaCaT. Avaliar quantitativamente sinais intracelulares de ativação da apoptose, verificando os níveis de caspases efetoras de apoptose (caspase-3), nas linhagens SiHa, C-33 A e HaCaT tratadas com maitenina. Avaliar a distribuição das células tratadas com maitenina no ciclo celular através da análise do conteúdo de DNA, nas linhagens SiHa, C-33 A e HaCaT. Avaliar se a maitenina induz genotoxicidade nas linhagens SiHa, C-33 A e HaCaT, via citometria de fluxo utilizando marcação com anticorpo anti-γh2ax. Avaliar a taxa de proliferação das linhagens SiHa, C-33 A e HaCaT através do ensaio de cristal violeta. Avaliar se a maitenina induz mutagenicidade nas linhagens SiHa, C-33 A e HaCaT através do ensaio do micronúcleo.
23 22 3. MATERIAIS E MÉTODOS Isolamento e purificação dos triterpenos quinonametídeos da planta jovem de Maytenus ilicifolia O processo de obtenção do triterpeno quinonametídeo denominado maitenina, foi realizado nas dependências do Núcleo de Bioensaios, Biossíntese e Ecofisiologia de Produtos Naturais (NuBBE), Departamento de Química Orgânica, Instituto de Química, Universidade Estadual Paulista Júlio de Mesquita Filho (UNESP), pela aluna Vânia Aparecida de Freitas Formenton Macedo dos Santos sob supervisão da Profª. Dra. Maysa Furlan. O estudo fitoquímico das cascas das raízes da planta adulta de M. ilicifolia foi realizado tendo como objetivo o isolamento dos triterpenos quinonametídeos, os quais seriam utilizados em experimentos de biossíntese. No entanto, a análise cromatográfica do extrato etanólico e das frações de partição não evidenciou a presença dos triterpenos quinonametídeos, mas outra classe de metabólito secundário, os alcalóides piridínicos sesquiterpênicos. Estes foram encontrados como metabólitos secundários majoritários em plantas adultas. Posteriormente, a análise por CLAE-DAD do extrato das raízes da planta jovem (3 anos) mostrou o acúmulo dos triterpenos quinonametídeos como metabólito majoritário, sendo estas selecionadas para o isolamento desta classe de substância. As raízes foram congeladas em N2 líquido, trituradas utilizando gral e pistilo, e como solvente extrator foi utilizado o DCM. Posteriormente, o extrato DCM foi filtrado e evaporado obtendo-se 4,90 g de extrato. Após análise e determinação da condição cromatográfica no modo isocrático por CLAE-DAD das frações coletadas, duas (F2 e F3) foram selecionadas para serem submetidas à purificação. A fração F2 (280,0 mg) foi submetida a purificação por CLAE-UV preparativa (condição: coluna Phenomenex C18, 10 m (250x21,2 mm); eluente: MeOH: H2O (9:1); fluxo 10 ml. min -1, tempo de análise: 40 min e = 254 nm). A purificação resultou na coleta de 6 frações das quais a fração F2.5 (59,0 mg), após análise por CLAE-DAD apresentou-se pura. A fração F3 (240,0 mg) também foi submetida à análise por CLAE-UV preparativa (Condição: coluna Phenomenex C18, 10 m (250x21,2 mm); eluente: MeOH: H2O (4:1); fluxo 12 ml. min -1, tempo de análise: 30 min e = 254 nm) e foram coletadas 5 frações. Foi
24 23 observado por CLAE-DAD que a fração coletada F3.5 apresentava algumas impurezas, sendo assim, esta foi submetida a repurificação obtendo-se a maitenina Cultura de células SiHa, C-33A e HaCaT As linhagens celulares utilizadas neste estudo foram: SiHa (ATCC HTB-35): Linhagem celular de origem de neoplasia de cérvice uterina escamosa humana de grau II, com propriedade aderente e morfologia semelhante à célula epitelial. Contém de 1 a 2 cópias por célula do Papilomavírus Humano do tipo 16. Hipertriplóide (69 a 72 cromossomos). Genes p53 e prb sem mutações. C-33 A (ATCC HTB-31): Linhagem celular de origem de neoplasia de cérvice uterina humana metastática, com propriedade aderente e morfologia semelhante à célula epitelial. Negativas para o DNA e RNA do Papilomavírus Humano, pseudodiploides (70% das células tem 46 cromossomos). Genes p53 e prb com mutações. HaCaT (CLS ): Células originárias de pele histologicamente normal (queratinócitos), transformadas espontaneamente in vitro. Aneuplóide (hipotetraplóide). Genes p53 com mutações (LEHMAN et al., 1993; HENSELEIT et al., 1997; BOUKAMP et al., 1998). Os efeitos da maitenina foram avaliados nas três linhagens celulares que foram cultivadas em uma mistura 1:1 (v/v) DMEM e Ham s F10 (Sigma Co., St. Louis, USA) acrescido de 100 U/mL de penicilina, 100 µg/ml de estreptomicina, 0,25 µg/ml de anfotericina B, 0,1 mg/ml de kanamicina (Sigma) e 10 % de soro fetal bovino (Cultlab, Campinas, Brasil). As células foram cultivadas em frascos de cultura, mantidas a 5% de CO2 e a temperatura de 37 ºC até que a monocamada celular estivesse confluente. Posteriormente, as células foram lavadas com 5 ml de solução de Hanks (0,4 g de KCl, 0,06 g de KH2PO4, 0,04 g de Na2HPO4, 0,35 g de NaHCO3, 1 g de glicose, H2O q.s.p ml) e tripsinizadas com 3 ml de Tripsina-EDTA 0,05% (Gibco, Waltham, MA, EUA). Após o desprendimento do tapete celular, as células foram homogeneizadas com volumes variados do meio acrescido de 10 % de soro fetal bovino. A suspensão celular obtida em uma garrafa foi transferida para outras garrafas, procedimento este que foi repetido até obter quantidade de células suficientes para os experimentos.
25 Citotoxicidade com Sulforodamina B O ensaio de sulforodamina B (SRB) é usado para determinar a densidade celular, baseada na mensuração do conteúdo de proteína celular. A Sulforodamina B (SRB) é um corante aniônico que se combina eletrostaticamente às proteínas. O corante fixado, medido fotometricamente após a solubilização, é correlacionado com a taxa de síntese proteica total e, então, com a viabilidade celular. Todo protocolo técnico será seguido conforme as recomendações do fabricante (sigma-aldrich S1402). Para determinação da citotoxicidade e seletividade sobre as linhagens, as células foram cultivas em placas de cultura de células de 96 poços, na concentração de 1 x 10 5 células/ml, em estufa a 37ºC com atmosfera com 5% de CO2, durante 24 horas, antes dos tratamentos com as amostras. As três linhagens celulares foram tratadas com concentrações de maitenina que variaram de 0,23 a 29,7 µm durante 24 horas para a determinação do CI50. Após a determinação do CI50 as células foram tratadas também por 6 ou 12 horas com a concentração mais próxima do CI50, uma acima e uma abaixo dessa concentração para cada linhagem celular afim de verificar o efeito tempo-resposta e definir os tempos e concentrações para os próximos ensaios. Doxorrubicina foi utilizada como controle positivo e DMSO 0,125% como controle de veículo. Após a incubação, as células foram fixadas com ácido tricloroacético 50% (m/v) por 60 minutos a 4ºC. Após a fixação, as placas foram lavadas com água destilada, e secas em temperatura ambiente. As células foram então coradas com SRB 0,4% (diluída em ácido acético 1%) durante 30 minutos, e posteriormente lavadas com ácido acético 1%. Após a secagem das placas, o corante ligado a proteínas das células foi solubilizado com solução Tris-base 10mM (ph10,5), sob agitação durante 5 minutos. E então a absorbância foi medida a 570 nm (SKEHAN et al., 1990; VOIGT, 2005). A porcentagem de células vivas foi calculada em relação ao controle de veículo, representando a citotoxicidade de cada tratamento, de acordo com a seguinte fórmula: Células vivas (%) = Absorbância do teste Absorbância do branco x 100 Absorbância do controle de veículo Absorbância do branco
26 Ensaios de Apoptose Ensaio citomofológico de marcação com Hoechst e iodeto de propídeo O ensaio citomorfológico de marcação com Hoechst (HO) e iodeto de propídeo (IP) permite a diferenciação entre apoptose precoce, tardia e necrose, utilizando o método de exclusão de fluorocromos e alterações na morfologia celular (DUARTE, 2010). Corantes fluorescentes como o Hoechst são amplamente utilizados para determinar a concentração de DNA e para corar núcleos avaliados por microscopia de fluorescência e citometria de fluxo que emite fluorescência azul quando se liga ao DNA. A bisbenzidina Hoechst é permeável nas membranas celulares e se une a ligações adenina-timina, sendo utilizados para avaliação de ciclo celular, apoptose e quantificação de células viáveis. Este corante é frequentemente incubado na presença de substâncias indutoras de apoptose, juntamente com células vivas por minutos até horas (KIECHLER & ZHANG 2003). Este corante é rapidamente absorvido pelas células durante as fases iniciais da apoptose, enquanto a membrana citoplasmática íntegra está impermeável ao IP. Fases tardias da apoptose apresentam corpos apoptóticos e são acompanhadas pelo aumento da permeabilidade da membrana celular, o que permite a entrada de IP nas células. Desta forma, a combinação do Hoechst e o IP têm sido intensamente utilizadas para a diferenciação dos estágios de apoptose precoce, apoptose tardia e necrose. Pode-se também adicionar o corante diacetato de fluoresceína (DAF) que marca células com membrana celular intacta, mesmo as apoptóticas de verde, sendo um ensaio de três espectros coloridos diferentes. Assim as células são avaliadas de acordo com a coloração e morfologia em citoplasma verde e núcleo azul intacto (células viáveis), encolhimento celular com núcleo azul condensado e descolamento do substrato (apoptose precoce), núcleo vermelho condensado e fragmentado (apoptose tardia) e núcleo intacto vermelho com célula aderida ao substrato (necrose) (HASHIMOTO et al., 2003, RELLO et al., 2005). Para o ensaio, as células foram cultivadas em placas de 96 poços a uma concentração de 5x10 4 células/ml e tratadas durante 6 ou 12 horas nas concentrações de 3,71µM para a linhagem SiHa e HaCaT e 7,42µM para a linhagem C-33 A. Doxorrubicina foi utilizada como controle de necrose e curcumina como controle de apoptose. DMSO 0,125% foi utilizado como controle de veículo. Ao completar o tempo de incubação do tratamento, a placa foi centrifugada a rpm por 5 minutos a 4 C, para sedimentar as células que estavam flutuando. O meio com tratamento foi removido e foi adicionado 100 µl de PBS 1X gelado a
27 26 cada poço e a placa foi centrifugada novamente a rpm por 5 minutos a 4 C. O PBS 1X foi removido e foi adicionada 100 µl da solução de fluorocromos em cada poço, contendo 25% de IP em solução aquosa (1 mg/ml), 35% de diacetato de fluoresceína (DAF) em acetona (5 mg/ml), 15% de HO em solução aquosa (1 mg/ml) e 25% de PBS 1x (NaCl 137 mm, KCl 2,7 mm, Na2HPO4 10,1 mm, KH2PO4 1,8 mm ph7,4). A reação foi incubada por 10 minutos a temperatura ambiente. A placa foi centrifugada por 30 segundos a 3700 rpm (spin de 30 segundos) e as imagens foram capturadas no aparelho IN cellanalyser modelo 2000, no laboratório de Proteômica da Faculdade de Ciências Farmacêuticas da Unesp- Araraquara. A apoptose foi avaliada qualitativa e quantitativamente, através da determinação da porcentagem de células em apoptose precoce, tardia e em necrose, levando-se em consideração a morfologia e coloração celular Atividade de Caspase-3 Caspases são um conjunto de cisteína-proteases que são ativadas especificamente em células apoptóticas, sendo consideradas os executores centrais da apoptose (ELMORE, 2007). Caspases são sintetizadas na forma de precursores inativos, chamados procaspases, que agem no ínicio da cascata proteolítica clivando e ativando outras caspases, chamadas caspases executoras que clivam proteínas alvo nas células levando à morte celular (ALBERTS, 2010). Entre as caspases executoras, caspase-3 é uma protease de morte que pode ser ativada através da via intrínseca (via liberação de citocromo c das mitocôndrias) ou extrínseca (ativada pela ligação de ligantes extracelulares à receptores de morte na superfície celular que culminam com a ativação de uma cascata de caspases citoplasmáticas até atingir a caspase-3 também denominada de caspase efetora) (ELMORE, 2007). Sendo assim a ativação de caspase-3 está intimamente relacionada à ativação de apoptose. Para este ensaio, as células foram plaqueadas a uma concentração de 2x10 5 cél./ml em placa de 96 poços de fundo preto, própria para leitura fluorimétrica, e foram incubadas por 24 horas a 37 C e 5% de CO2 em atmosfera úmida. As células foram tratadas com a maitenina utilizando as concentrações de 1,85, 3,71 e 7,42 µm para as linhagens SiHa e HaCaT e 3,71 e 7,42 e 14,85 µm para a linhagem C-33 A. As linhagens SiHa e C-33 A foram tratadas por 6, 8 e 12 horas e a linhagem HaCaT foi tratada por 6 e 8 horas. Curcumina 75 µm foi utilizada como controle positivo e DMSO 0,125% como controle de veículo. Imediatamente após o término do tempo de tratamento, a placa foi colocada em gelo. O meio contendo as substâncias de tratamento foi removido e cada poço recebeu 100 µl de tampão de lise (50
28 27 mm Tris ph 7,4; 150 mm NaCl; 0,5% Triton X-100; EDTA 2 mm; DTT 5 mm). A placa foi então incubada em gelo por 20 minutos e, em seguida, cada poço recebeu 100 µl do substrato Ac-DMQD-AMC a 20 µm, preparado no mesmo tampão. Durante o tempo de incubação foi preparada a curva padrão de AMC, com concentrações decrescentes em 50% partindo de 4 µm. A placa foi levada para leitura top em fluorímetro (FLx800 Fluorescence Reader, BioTek - Winooski, VT, EUA; excitação 360/40 nm e emissão 460/40 nm) e agitada automaticamente pelo equipamento antes do início da leitura de fluorescência, que foi feita a 37 C. Os resultados foram expressos em concentração de AMC, com base na curva padrão. Este ensaio foi realizado em colaboração com o Laboratório de Bioquímica Clínica da Faculdade de Ciências Farmacêuticas de Araraquara UNESP Ciclo celular Ciclo celular é o ciclo de duplicação e divisão das células, e é a maneira como todos os seres vivos se reproduzem. Sua função básica é duplicar a grande quantidade de DNA nos cromossomos e dividir as cópias em duas células filhas geneticamente idênticas. O ciclo celular é constituído de 4 fases: G1, S, G2 e M. A duplicação dos cromossomos ocorre durante a fase S do ciclo celular. Durante a fase M, ocorre a mitose, e os cromossomos replicados são segregados em núcleos individuais e a célula se divide em duas células filhas. A fase G1 e G2 são fases de intervalo compreendidas entre S e M que regulam a progressão do ciclo celular. Quando a célula falha em completar um processo essencial para a continuidade do ciclo celular, ou quando encontra condições ambientais ou intracelulares desfavoráveis ocorre interrupção do ciclo celular e a célula interrompe a proliferação (ALBERTS, 2010). Sendo assim, o ensaio de ciclo celular permite a avaliação da distribuição no ciclo celular das células tratadas com maitenina, através da análise do conteúdo de DNA, para verificar se o tratamento é capaz de interromper o ciclo celular das células em estudo. Para o ensaio as células foram plaqueadas a uma concentração de 1,4 x 10 5 células/ml, em placa de 24 poços, e tratadas nas concentrações de 3,71µM para a linhagem SiHa e HaCaT e 7,42µM para a linhagem C-33 A. As células foram tratadas por 12 horas, seguido de póstratamento de 24, 48 e 72 horas. DMSO 0,125% foi utilizado como controle de veículo. Após o tratamento, as células foram coletadas e fixadas com etanol 70% overnight. No dia seguinte, o pellet foi ressuspendido em 45 µl de PBS 1X. Logo após foi adicionado 5 µl de RNAse A, e o pellet incubado por 30 minutos a 37C. Após incubação, foi adicionado
29 28 iodeto de propídio (100 µg/ml) e a leitura foi realizada por citometria de fluxo (FACSCanto) (BD - Becton, Dickinson and Company, New Jersey, EUA), nas dependências da Faculdade de Ciências Farmacêuticas de Ribeirão Preto USP, em colaboração com o aluno de doutorado Rodolfo Bortolozo Serafim orientado da Professora Doutora Valeria Valente Avaliação de genotoxicidade via citometria de fluxo utilizando anti-γh2ax H2AX é uma variante específica da família de histonas H2A que sofre fosforilação na serina 139 de sua porção C-terminal em resposta à danos na dupla fita do DNA. A fosforilação de H2AX representa um evento precoce na resposta à danos no DNA, e desempenha um papel central na detecção e reparação destas lesões (SÁNCHEZ-FLORES et al., 2015). A proteína fosforilada é conhecida por γh2ax (gama-h2ax). A detecção de γh2ax por citometria de fluxo tem se tornado uma alternativa mais rápida e robusta ao clássico ensaio do cometa (WATTERS et al., 2009). Para o ensaio, as células foram plaqueadas a uma concentração de 1,4x10 5 células/ml, em placa de 24 poços. Após 24 horas de incubação a 37 C e 5% de CO2 em atmosfera úmida, as células foram tratadas nas concentrações de 3,71 µm para a linhagem SiHa e HaCaT e 7,42 µm para a linhagem C-33 A durante 6 horas. Finalizado o tratamento, as células foram tripsinizadas e centrifugadas a rpm por 5 minutos. O pellet de células foi suspendido em 200 µm de PBS 1X e em seguida foi adicionado 800 µl de metanol (solução de fixação: metanol 80%) e armazenado a -20 C até o dia da citometria. Na etapa seguinte, as células foram centrifugadas a rpm por 5 minutos e foram suspensas em 150 µl PBS-Tween 0,1% e incubadas por 20 minutos, sendo na sequência centrifugadas a rpm por 5 minutos e ressuspensas em 300 µl PBS-SFB 10% e incubadas por 1 hora. Na sequência as células foram incubadas com anticorpo primário anti-h2ax por uma hora. Novamente, as células foram centrifugadas a rpm por 5 minutos. Em seguida, foram incubadas por 1 hora com anticorpo secundário conjugado com AlexaFluor 488. Uma vez mais, as suspensões celulares foram centrifugadas a rpm por 5 minutos sendo por fim suspendidas em 60 µl de PBS 1X e analisadas por citometria de fluxo em equipamento FACSCanto (BD - Becton, Dickinson and Company, New Jersey, EUA), nas dependências da Faculdade de Ciências Farmacêuticas de Ribeirão Preto USP, em colaboração com o aluno de doutorado Rodolfo Bortolozo Serafim orientado da Professora Doutora Valeria Valente.
30 Ensaio de Proliferação celular com cristal violeta O ensaio de proliferação celular com cristal violeta é um teste simples que avalia a densidade de células em um poço ao marcar seu DNA. O cristal violeta é um corante básico que cora o núcleo das células (GILLIES et al., 1986). Para o ensaio as células foram plaqueadas a uma concentração de 1x10 3 células por poço, em 6 placas de 96 poços. Após 3, 24, 48, 72, 96 e 120 horas do plaqueamento, o meio de cultura de cada poço foi retirado e foi feita uma lavagem com PBS 1X, e fixação das células com etanol 70% por 30 minutos. Após fixação, foi realizada nova lavagem com PBS 1X e o DNA das células corados com solução de violeta cristal 0,05% por 30 minutos. Após coloração, foram realizadas 5 lavagens com PBS 1X para retirar excesso do corante e foi adicionada solução de ácido acético 10% por 30 minutos para leitura em leitor de placas em 540 nm. Foram feitas curvas de crescimento para as três linhagens avaliadas neste estudo (SiHa, C-33 A e HaCaT), afim de correlacionar a taxa proliferativa com os resultados obtidos nos demais ensaios Ensaio do micronúcleo Micronúcleos são marcadores de eventos genotóxicos e instabilidade cromossômica. Se originam a partir de fragmentos de cromossomos acêntricos ou cromossomos inteiros que não conseguem ser incluídos nos núcleos das células filhas durante a mitose (FENECH, 2011). Devido a sua simplicidade, confiabilidade e sensibilidade, o teste de micronúcleo tem sido requisitado para a avaliação de mutagenicidade de compostos, entre eles produtos naturais, os quais podem exercer atividades clastogênicas (capacidade ou predisposição a quebra cromossômica), aneugênicas (capacidade ou predisposição de alterar o fuso mitótico resultando na perda de cromossomo), ou ambas (TOROUS et al., 1998). O ensaio do micronúcleo foi realizado segundo protocolo do IN CellAnalyzer Para o ensaio, as células foram plaqueadas na concentração de 5x10 4 células/ml em placas de 96 poços, e tratadas com a maitenina nas concentrações de 3,71 µm para a linhagem SiHa e HaCaT e 7,42 µm para a linhagem C-33 A durante 6 horas seguido de pós tratamento de 24 horas. As células também foram, tratadas durante 24 horas, com uma concentração inferior ao CI50 determinado no ensaio de citotoxicidade de 24 horas, sendo assim as linhagens SiHa e
31 30 HaCaT foram tratadas com 1,85 µm de maitenina e a linhagem C-33 A foi tratada com 3,71 µm de maitenina. Como controle positivo, foi utilizado o peróxido de hidrogênio na concentração de 1mM por 15 minutos seguido de pós-tratamento de 24 horas, e como controle de veículo DMSO 0,125%. Após os tratamentos, foi feito o bloqueio da citocinese com 100 µl/poço de citocalasina B na concentração de 6 µg/ml por 36 horas. Após o bloqueio da citocinese celular, a placa foi lavada com PBS 1X e as células foram fixadas com 100 µl de etanol (PA) por poço por 30 minutos, em temperatura ambiente. Após a fixação das células, foi adicionado FITC diluído em PBS 1X (marcador de citoplasma) na concentração de 1 µg/ml por 30 minutos, os poços também foram lavados por 3 vezes com PBS 1X e adicionado o outro marcador, o Hoechst na concentração de 10 µg/ml por 15 minutos, afim de marcar o núcleo (Hoechest 33342) e o citoplasma das células (FITC). As imagens foram capturadas no aparelho IN cellanalyser modelo 2000, no núcleo de Proteômica da Faculdade de Ciências Farmacêuticas da Unesp-Araraquara. Foram capturadas no mínimo 1000 células por concentração e controles. A contagem foi feita manualmente Análises Estatísticas Para comparar os valores das variáveis contínuas entre os grupos foram utilizados testes de Análise de Variância (ANOVA). O pós-teste mais adequado foi utilizado para identificação do grupo significativamente diferente. As análises foram realizadas através do software GraphPad Prism Version 5.01 (GraphPad Software Inc., La Jolla, CA, EUA). O nível de significância adotado para os testes estatísticos foi de 5%, ou seja, p<0.05.
32 31 4. RESULTADOS 4.1. Citotoxicidade A citotoxicidade da maitenina foi avaliada nas concentrações de 0,23 a 29,7 µm, solubilizadas em meio de cultura nas linhagens celulares SiHa (linhagem de carcinoma cervical infectada pelo HPV-16), C-33 A (linhagem de carcinoma cervical não infectada pelo HPV-16) e queratinócitos humanos imortalizados (HaCaT) no tempo de tratamento de 24 horas. Para determinação do CI50 (concentração capaz de reduzir em 50% a viabilidade celular) foram feitas linhas de tendências lineares e por meio das equações das retas obtidas, os valores foram definidos. Os resultados obtidos para as três linhagens são demostrados na figura 6: SiHa tratada com maitenina C-33 A tratada com maitenina Viabilidade celular CV CP 0,23 0,46 0,93 1,85 3,71 7,42 14,85 29,7 concentração de maitenina ( M) Viabilidade celular CV CP HaCaT tratada com maitenina ** 0,23 0,46 0,93 1,85 3,71 7,42 14,85 29,7 concentração de maitenina ( M) Viabilidade celular CV CP 0,23 0,46 0,93 1,85 3,71 7,42 14,85 29,7 Figura 6: Ensaio de citotoxicidade. Comparação entre a concentração de maitenina e a porcentagem de células SiHa, C-33 A e HaCaT vivas no tempo de tratamento de 24 horas. Os dados referem-se a três experimentos independentes. CP: controle positivo, doxorrubicina 92µM; CV: controle de veículo, DMSO 0,125%. Os concentração de maitenina ( M)
33 32 asteriscos indicam a significância estatística em relação ao CV. ANOVA one-way, com pós-teste de Tukey. *p<0,05; **p<0,01; p<0,001. Foi possível observar um aumento da citotoxicidade proporcionalmente ao aumento da concentração (efeito concentração-resposta) da substância testada na linhagem SiHa, onde na maior concentração houve menor porcentagem de células vivas, ou seja, maior taxa de morte celular. Já nas menores concentrações as porcentagens de morte celular são baixas e com pouca variação entre elas, evidenciando um baixo poder citotóxico da substância nessas concentrações. A análise estatística foi realizada com o teste One WayANOVA com pós-teste de Tukey. CI50 maitenina para a linhagem SiHa em 24 horas: 3,26 µm (y = -33,359x + 95,775). Com a linhagem C-33 A também foi possível observar o efeito concentração-resposta onde nas maiores concentrações houve a maior taxa de morte celular, enquanto nas menores concentrações as taxas de morte foram baixas. No entanto, a linhagem C-33 A mostrou-se mais resistente do que a linhagem SiHa no tempo de tratamento de 24 horas, com CI50 de 8,49 µm. A análise estatística foi realizada com o teste One Way ANOVA com pós-teste de Tukey. CI50 da maitenina para a linhagem C-33 A em 24 horas: 8,49 µm (y = -17,071x + 111). Os resultados obtidos para a linhagem HaCaT são bastante semelhantes aos obtidos com a linhagem SiHa e também foi possível observar o efeito concentração-resposta. A análise estatística foi realizada com o teste One Way ANOVA com pós-teste de Tukey. CI50 da maitenina para a linhagem HaCaT em 24 horas: 3,09 µm (y = -49,477x + 114,45). Afim de avaliar o efeito tempo-resposta da maitenina, foram selecionadas três concentrações (a mais próxima do CI50, uma abaixo e uma acima do CI50 de cada linhagem celular) e as três linhagens celulares foram tratadas também por 6 e 12 horas. Sendo assim as linhagens SiHa e HaCaT foram tratadas com 1,85, 3,71 e 7,42 µm de maitenina e a linhagem C-33 A foi tratada com 3,71, 7,42 e 14,85 µm de maitenina. Os resultados obtidos são mostrados na figura 7:
34 33 Viabilidade celular SiHa HORAS ** * ** 12 HORAS HORAS Viabilidade celular C-33 A HORAS ** * * ** 12 HORAS 80 * ** 24 HORAS 0 CV CP 1,85 3,71 concentração de maitenina ( M ) 7,42 0 CV CP 3,71 7,42 14,85 concentração de maitenina ( M ) Viabilidade celular HaCaT HORAS * 12 HORAS 80 ** ** 24 HORAS 0 CV CP 1,85 3,71 concentração de maitenina ( M ) 7,42 Figura 7: Ensaio de citotoxicidade. Comparação entre a concentração de maitenina e a porcentagem de células SiHa, C-33 A e HaCaT vivas no tempo de tratamento de 6, 12 e 24 horas. Os dados referem-se a três experimentos independentes. CP: controle positivo, doxorrubicina 92 µm; CV: controle de veículo, DMSO 0,125%. Os asteriscos indicam a significância estatística em relação ao CV. ANOVA one-way, com pós-teste de Tukey. *p<0,05; **p<0,01; p<0,001. Como pode ser observado na figura 7 houve uma resposta tempo-dependente nas três linhagens, onde a maior morte celular ocorre no tempo de tratamento de 24 horas. Na linhagem SiHa tratada por 6 horas verificou-se diferença estatística com relação ao controle de veículo nas concentrações de 3,71 e 7, 42 µm, indicando que a morte celular começa a ocorrer com este tempo de tratamento e aumentou no período de 12 horas, ou seja, a morte é tempo - dependente. O mesmo ocorreu com a linhagem C-33 A, onde se verificou diferença estatística em relação ao controle de veículo nas concentrações de 7,42 e 14,85 µm nos tempos de 6 e 12 horas. Na linhagem HaCaT só houve diferença estatística em relação ao controle de veículo na maior concentração testada (7,42 µm) nos tempos de 6 e 12 horas. A partir do ensaio de citotoxicidade, foram selecionados os tempos de tratamento de 6 e 12 horas e a concentração de 3,71µM para as linhagem SiHa e HaCaT e 7,42µM para a
35 34 linhagem C-33 A para a realização do ensaio citomorfológico de marcação com Hoechst e Iodeto de Propídeo Ensaios de apoptose Ensaio citomorfológico de marcação com Hoechst e Iodeto de Propídeo A avaliação do tipo de morte celular causada pela maitenina foi avaliada nas concentrações de 3,71 µm para a linhagem SiHa e HaCaT e 7,42 µm para a linhagem C-33 A nos tempos de tratamento de 6 e 12 horas. Curcumina e doxorrubicina foram utilizados como controle de apoptose e necrose, respectivamente. Foram analisadas 500 células por tratamento e elas foram classificadas em: células em apoptose precoce, apoptose tardia e necrose. Para a quantificação, todas as células contadas foram comparadas à sua imagem no campo claro para verificação de critérios morfológicos, pois células em apoptose tornam-se retraídas e perdem sua capacidade de adesão ao substrato, enquanto células em necrose permanecem firmemente ligadas ao substrato e também podem apresentar bolhas em sua superfície, as quais são decorrentes da perda da integridade da membrana plasmática (RELLO et al., 2005). A figura 8 mostra imagens representativas do ensaio de Hoechst e Iodeto de Propídeo, onde podemos observar células vivas (setas laranjas), células em apoptose precoce (setas brancas), apoptose tardia (seta vermelha) e células em necrose (setas amarelas): SiHa
36 35 C-33 A HaCaT Figura 8: Figura representativa do ensaio de Hoechst e Iodeto de Propídeo nas linhagens SiHa, C-33 A e HaCaT, mostrando células vivas (setas laranjas), células em apoptose precoce (setas brancas), apoptose tardia (seta vermelha) e células em necrose (setas amarelas). Imagens capturadas no IN Cell Analyzer 2000 com a objetiva de 20X. A figura 9 mostra os gráficos com a quantificação das células que foram classificadas em apoptose precoce, apoptose tardia e necrose para a linhagem SiHa (esquerda) e traz a relação entre apoptose total (apoptose precoce + apoptose tardia) e necrose (direita), nos tempos de tratamento de 6 e 12 horas:
37 36 % células mortas SiHa 6 horas * APOPTOSE PRECOCE APOPTOSE TARDIA NECROSE % células mortas SiHa 6 horas 100 APOPTOSE TOTAL NECROSE ** * 20 0 CV DOXORRUBICINA CURCUMINA MAITENINA 0 CV DOXORRUBICINA CURCUMINA MAITENINA % células mortas SiHa 12 horas APOPTOSE PRECOCE APOPTOSE TARDIA NECROSE % células mortas SiHa 12 horas 100 APOPTOSE TOTAL NECROSE * ** 20 0 CV DOXORRUBICINA CURCUMINA MAITENINA 0 CV DOXORRUBICINA CURCUMINA MAITENINA Figura 9: Apoptose por coloração Hoechst/IP em células SiHa nos tempos de tratamento de 6 e 12 horas. Resultados estão expressos como a média de três experimentos independentes e desvio padrão (M ± DP), analisados por one-way ANOVA com pós-teste de Tukey (tratados vs CV). CP: doxorrubicina 92µM e curcumina 28 µm; CV: controle de veículo DMSO 0,125 %; * p < 0,05; ** p < 0,01; p < 0,001. Para a linhagem SiHa o efeito da maitenina foi tempo-dependente, ou seja, a morte celular foi maior no tempo de tratamento de 12 horas do que no tempo de tratamento de 6 horas, com significância estatística apenas no tempo de 12 horas (p < 0,001). Ainda, foi possível observar uma morte celular predominantemente por apoptose, logo nas primeiras 6 horas de exposição, aumentando significativamente no tempo de tratamento de 12 horas. Comparada com a apoptose, a morte por necrose foi menor nos tempos de 6 e 12 horas. A morte celular portanto ocorreu principalmente por apoptose, no entanto com presença de necrose, indicando uma morte mista.
38 37 Ainda, a linhagem apresentou um comportamento semelhante à curcumina, substância sabidamente indutora de apoptose utilizada como controle do experimento, principalmente no tempo de tratamento de 12 horas. A figura 10 mostra os gráficos com a quantificação das células que foram classificadas em apoptose precoce, apoptose tardia e necrose para a linhagem C-33 A (esquerda) e traz a relação entre apoptose total (apoptose precoce + apoptose tardia) e necrose (direita), nos tempos de tratamento de 6 e 12 horas: % células mortas C-33 A 6 horas * APOPTOSE PRECOCE APOPTOSE TARDIA NECROSE % células mortas C-33 A 6 HORAS 100 APOPTOSE TOTAL NECROSE CV DOXORRUBICINA CURCUMINA MAITENINA 0 CV DOXORRUBICINA CURCUMINA MAITENINA % células mortas C-33 A 12 horas ** CV DOXORRUBICINA CURCUMINA MAITENINA APOPTOSE PRECOCE APOPTOSE TARDIA NECROSE % células mortas C-33 A 12 HORAS ** CV DOXORRUBICINA CURCUMINA ** ** MAITENINA APOPTOSE TOTAL NECROSE Figura 10: Apoptose por coloração Hoechst/IP em células C-33 A nos tempos de tratamento de 6 e 12 horas. Resultados estão expressos como a média de três experimentos independentes e desvio padrão (M ± DP), analisados por one-way ANOVA com pós-teste de Tukey (tratados vs CV). CP: doxorrubicina 92µM e curcumina 28 µm; CV: controle de veículo DMSO 0,125 %; * p < 0,05; ** p < 0,01; p < 0,001.
39 38 Para a linhagem C-33 A também foi possível observar o efeito tempo-dependente, ou seja, a morte celular foi maior no tempo de tratamento de 12 horas do que no tempo de tratamento de 6 horas, com significância estatística apenas no tempo de tratamento de 12 horas (p < 0,01). Para a linhagem C-33 A, no tempo de tratamento de 6 horas não foi encontrada significância estatística da maitenina em relação ao controle de veículo nem para apoptose nem para necrose, mas com o aumento do tempo de tratamento, houve significância estatística para apoptose, bem como para necrose, indicando uma morte celular mista, com uma predominância de apoptose. A figura 11 mostra os gráficos com a quantificação das células que foram classificadas em apoptose precoce, apoptose tardia e necrose para a linhagem HaCaT (esquerda) e traz a relação entre apoptose total (apoptose precoce + apoptose tardia) e necrose (direita), nos tempos de tratamento de 6 e 12 horas: % células mortas HaCaT 6 horas * APOPTOSE PRECOCE APOPTOSE TARDIA NECROSE % células mortas HaCaT 6 horas * * APOPTOSE TOTAL NECROSE 0 CV DOXORRUBICINA CURCUMINA MAITENINA 0 CV DOXORRUBICINA CURCUMINA MAITENINA % células mortas CV HaCaT 12 horas DOXORRUBICINA CURCUMINA MAITENINA APOPTOSE PRECOCE APOPTOSE TARDIA NECROSE % células mortas CV HaCaT 12 horas ** DOXORRUBICINA CURCUMINA ** MAITENINA APOPTOSE TOTAL NECROSE Figura 11: Apoptose por coloração Hoechst/IP em células HaCaT nos tempos de tratamento de 6 e 12 horas.
40 39 Resultados estão expressos como a média de três experimentos independentes e desvio padrão (M ± DP), analisados por one-way ANOVA com pós-teste de Tukey (tratados vs CV). CP: doxorrubicina 92µM e curcumina 14 µm; CV: controle de veículo DMSO 0,125 %; * p < 0,05; ** p < 0,01; p < 0,001. Para a linhagem HaCaT também foi possível observar o efeito tempo-dependente, ou seja, a morte celular foi maior no tempo de tratamento de 12 horas do que no tempo de tratamento de 6 horas, com significância estatística em relação ao controle de veículo (p < 0,001) apenas no tempo de tratamento de 12 horas. Para a linhagem HaCaT, no tempo de tratamento de 6 horas não foi encontrada significância estatística da maitenina em relação ao controle de veículo nem para apoptose nem para necrose, mas com o aumento do tempo de tratamento (12 horas), houve significância estatística para apoptose, bem como para necrose, indicando uma morte celular mista, com a mesma significância estatística (p < 0,001) para apoptose e necrose. Quando comparamos as três linhagens, observamos que em nenhuma delas houve um padrão único de morte celular, demostrando que a morte celular para as três linhagens é do tipo mista, ou seja, ocorre por apoptose e necrose. Ainda, a linhagem SiHa mostrou-se mais mais sensível que a linhagem C-33 A, mesmo esta estando numa concentração mais alta. Quando comparamos a linhagem SiHa à linhagem HaCaT, observamos que a linhagem SiHa mostrou-se mais sensível, pois a taxa de morte celular no tratamento de 12 horas foi muito maior na linhagem SiHa (85,07%) do que na linhagem HaCaT (40,93%) (figuras 9 e 11) Atividade de Caspase-3 A avaliação da atividade de caspase- 3 como um indicador de apoptose foi determinada pela liberação de aminometilcumarina (AMC), medida em comprimentos de excitação e emissão 360/40 nm e 460/40 nm, respectivamente. O ensaio foi realizado por fluorescência, utilizando um substrato, contendo a sequência peptídica Ac-DMQD-AMC, que após a clivagem pela caspase libera AMC resultando em fluorescência, a qual é quantificada pela ativação de caspase-3 nas células. Para este experimento, as linhagens SiHa e HaCaT foram tratadas com 1,85, 3,71 e 7,42 µm de maitenina e a linhagem C-33 A foi tratada com 3,71, 7,42 e 14,85 µm de maitenina. As linhagem SiHa e C-33 A foram tratadas durante 6,8 e 12 horas e a linhagem HaCaT foi tratada durante 6 e 8 horas.
41 40 A figura 12 refere-se a resposta da atividade da enzima caspase-3 na linhagem SiHa exposta ao tratamento com a maitenina por 6, 8 e 12 horas: SiHa 6 horas SiHa 8 horas AMC liberada ( M) AMC liberada ( M) CV CURCUMINA 1,85 3,71 MAITENINA ( M) 7, CV CURCUMINA 1,85 3,71 MAITENINA ( M) 7, SiHa 12 horas AMC liberada ( M) CV CURCUMINA 1,85 3,71 7,42 MAITENINA ( M) Figura 12: Atividade de caspase-3 em células SiHa tratadas por 6, 8 e 12 horas. Resultados estão expressos como a média de três experimentos independentes e desvio padrão (M ± SD), analisados por one-way ANOVA com pós-teste de Tukey (tratados vs CV). CP: curcumina 75 µm; CV: controle de veículo DMSO 0,125 %; * p < 0,05; ** p < 0,01; p < 0,001. Como podemos observar, para a linhagem SiHa em nenhuma das concentrações testadas e nenhum dos tempos de tratamento houve indução da enzima caspase-3. Somente houve indução de caspase-3 no controle positivo (curcumina 75µM) já partir de 6 horas de tratamento, aumentou com 8 horas e com 12 horas já não houve mais indução.
42 41 A figura 13 refere-se a resposta da atividade da enzima caspase-3 na linhagem C-33 A exposta ao tratamento com a maitenina por 6, 8 e 12 horas: C-33 A 6 horas C-33 A 8 horas AMC liberada ( M) AMC liberada ( M) CV CURCUMINA 3,71 7,42 MAITENINA ( M) 14, CV CURCUMINA 3,71 7,42 14,85 MAITENINA ( M) 0.6 C-33 A 12 horas AMC liberada ( M) CV CURCUMINA 3,71 7,42 14,85 MAITENINA ( M) Figura 13: Atividade de caspase-3 em células C-33 A tratadas por 6, 8 e 12 horas. Resultados estão expressos como a média de três experimentos independentes e desvio padrão (M ± SD), analisados por one-way ANOVA com pós-teste de Tukey (tratados vs CV). CP: curcumina 75 µm; CV: controle de veículo DMSO 0,125 %; * p < 0,05; ** p < 0,01; p < 0,001. A linhagem C-33 A demonstrou um comportamento semelhante ao da linhagem SiHa, sendo que em nenhuma das concentrações testadas e nenhum dos tempos de tratamento houve indução da enzima caspase-3. Somente houve indução de caspase-3 no controle positivo (curcumina 75µM) já partir de 6 horas de tratamento, aumentou com 8 horas e com 12 horas já não houve mais indução.
43 42 Estes resultados sugerem que a morte celular para as linhagens SiHa e C-33 A é independente de caspase-3. A figura 14 refere-se a resposta da atividade da enzima caspase-3 na linhagem HaCaT exposta ao tratamento com a maitenina por 6 e 8 horas: HaCaT 6 horas HaCaT 8 horas AMC liberada ( M) ** AMC liberada ( M) * 0.0 CV CURCUMINA 1,85 3,71 7,42 MAITENINA ( M) 0.0 CV CURCUMINA 1,85 3,71 7,42 MAITENINA ( M) Figura 14: Atividade de caspase-3 em células HaCaT tratadas por 6 e 8 horas. Resultados estão expressos como a média de três experimentos independentes e desvio padrão (M ± SD), analisados por one-way ANOVA com pósteste de Tukey (tratados vs CV). CP: curcumina 75 µm; CV: controle de veículo DMSO 0,125 %; * p < 0,05; ** p < 0,01; p < 0,001. Para a linhagem HaCaT foi verificada ativação de caspase-3 após 6 horas de exposição à maitenina nas duas maiores concentrações testadas (3,71 e 7,42 µm), bem como no controle positivo, sugerindo que a ativação de apoptose é um dos mecanismo através do qual a maitenina induz morte celular nas células normais. Com 8 horas de tratamento não foi verificada significância estatística em relação à nenhuma das concentrações de maitenina testadas, e a indução de caspase-3 no controle positivo também foi menor do que no tempo de tratamento de 6 horas, indicando que a ativação de caspase-3 e consequentemente apoptose para a linhagem HaCaT começa rápido, logo com 6 horas de exposição ao composto. Para a linhagem HaCaT, estes resultados de caspase, comparados ao ensaio de Hoechst e Iodeto de Propídeo, realizado após 12 horas de tratamento com o composto, sugerem que a maitenina é capaz de ativar ambas as vias, a de necrose e a de apoptose Ciclo celular
44 43 A distribuição das células tratadas com maitenina no ciclo celular através da análise do conteúdo de DNA foi avaliada nas concentrações de 3,71 µm para a linhagem SiHa e HaCaT e 7,42 µm para a linhagem C-33 A. As células foram tratadas por 12 horas, seguido póstratamento de 24, 48 e 72 horas. Os resultados obtidos para as três linhagens são mostrados na figura 15: Figura 15: Ensaio de ciclo celular em células SiHa, C-33 A e HaCaT tratadas com maitenina por 12 horas, seguido de pós-tratamento de 24, 48 e 72 horas. Resultados estão expressos como a média de três experimentos
45 44 independentes e desvio padrão (M ± SD), analisados por one-way ANOVA com pós-teste de Bonferroni. CV: controle de veículo DMSO 0,125 %; * p < 0,05; ** p < 0,01; p < 0,001. Conforme podemos observar, após tratamento com maitenina, ocorreu parada de ciclo celular para as três linhagens avaliadas. Para a linhagem SiHa, 24 horas pós-tratamento, não houve alterações de ciclo celular, no entanto com o aumento do tempo pós-tratamento (48 e 72 horas) observamos parada de ciclo celular em G2/M. Já a linhagem C-33 A, 24 horas póstratamento mostrou diminuição significativa em G1, e com o aumento do tempo póstratamento (48 e 72 horas) houve parada de ciclo celular nas fases S e G2/M. Para a linhagem HaCaT, 24 horas pós-tratamento não houve alterações em ciclo celular, com 48 horas póstratamento já foi possível observar aumento da fase S, mas parada significativa de ciclo celular em fase S só foi evidenciada pós-tratamento de 72 horas. A parada de ciclo celular ocorre em resposta à algum tipo de estresse sofrido pelas células, como por exemplo danos ao DNA. Sendo assim, na sequência desse estudo foi realizado o ensaio de genotoxicidade via citometria de fluxo utilizando anti-γh2ax, afim de determinar se a parada de ciclo celular está relacionada à quebras na dupla fita de DNA Avaliação de genotoxicidade via citometria de fluxo utilizando anti-γh2ax Para avaliar a possível indução de genotoxicidade causada pela maitenina nas linhagens SiHa, C-33 A e HaCaT foi realizado o ensaio utilizando marcação com anticorpo anti-γh2ax. As linhagens SiHa e HaCaT foram tratadas na concentração 3,71 µm de maitenina e a linhagem C-33 A foi tratada na concentração de 7,42 µm de maitenina durante 6 horas. Peróxido de hidrogênio foi utilizado como controle positivo e DMSO 0,125% como controle de veículo. Os resultados obtidos para as três linhagens são mostrados na figura 16, onde os gráficos da esquerda trazem a intensidade média de fluorescência que é diretamente proporcional à frequência de quebras duplas no DNA induzidas pelos tratamentos e os gráficos da direita trazem a % de células marcadas, ou seja, mostra as células que estão marcadas com o anticorpo anti-γh2ax, não medindo portanto a quantidade de danos:
46 45 Figura 16: Ensaio de genotoxicidade em células SiHa, C-33 A e HaCaT tratadas com maitenina por 6 horas. Resultados estão expressos como a média de três experimentos independentes e desvio padrão (M ± SD),
47 46 analisados por one-way ANOVA com pós-teste de Dunnet. CV: controle de veículo DMSO 0,125 %; CP: peróxido de hidrogênio 1 mm por 15 minutos; * p < 0,05; ** p < 0,01; p < 0,001. Como podemos observar para as três linhagens celulares tratadas com maitenina foram observadas quebras da dupla fita de DNA. Para a linhagem SiHa, embora não tenha sido observado aumento significativo na intensidade média de fluorescência, foi observado quebras na dupla fita de DNA pois o número de células marcadas com anticorpo anti-γh2ax foi estatisticamente significante quando comparado ao controle de veículo. A baixa intensidade de fluorescência emitida pelas células tratadas com maitenina significa que a quantidade de dano em cada célula não é grande. Para a linhagem SiHa, ainda foi observado intensidade de fluorescência no controle de veículo (embora sem significância estatística), ou seja, a célula tem um nível basal de danos no DNA, ocasionado provavelmente pela presença do HPV-16. A % de células marcadas para a maitenina é semelhante ao controle positivo. Para a linhagem C-33 A também foi possível observar um aumento significativo na taxa de danos ao DNA nas células tratadas com maitenina em relação ao controle de veículo. A porcentagem de células marcadas foi parecida com a linhagem SiHa, mas quando analisamos a intensidade de fluorescência notamos que a linhagem C-33 A teve uma quantidade de quebras muito maior que a linhagem SiHa. Já a linhagem HaCaT, foi a que teve a maior quantidade de danos ao DNA, evidenciados pela intensidade de fluorescência e % de células marcadas. Com estes dados, podemos concluir que a maitenina é genotóxica em relação as três linhagens avaliadas Ensaio de proliferação celular com cristal violeta O ensaio de proliferação celular com cristal violeta teve como objetivo traçar as curvas de crescimento das linhagens SiHa, C-33 A e HaCaT na ausência de tratamentos e correlacionar a taxa proliferativa com os resultados obtidos nos demais ensaios. A figura 17 mostra os resultados obtidos para as linhagens SiHa, C-33 A e HaCaT:
48 47 Figura 17: Ensaio de Proliferação Celular com cristal violeta com as linhagens SiHa, C-33 A e HaCaT. Os dados referem-se a média de três experimentos independentes e desvio padrão (M ± DP), analisados por one-way ANOVA com pós-teste de Tukey; * p < 0,05. Como podemos observar, as três linhagens celulares proliferam de maneira semelhante até 72 horas, no entanto com 96 horas notou-se diferença significativamente estatística entre a linhagem C-33 A e as linhagens HaCaT e SiHa. Com 120 horas após o tratamento só foi notada diferença estatística da linhagem C-33 A para a linhagem HaCaT. Os dados mostram que a linhagem que prolifera mais rápido é a linhagem C-33 A, e que as linhagens SiHa e HaCaT proliferam de maneira semelhante Ensaio do micronúcleo Para avaliar a possível indução de mutagenicidade causada pela maitenina nas linhagens SiHa, C-33 A e HaCaT foi realizado o ensaio do micronúcleo. Primeiramente, as linhagens SiHa e HaCaT foram tratadas na concentração 3,71 µm de maitenina e a linhagem C-33 A foi tratada na concentração de 7,42 µm de maitenina durante 6 horas, seguido de póstratamento de 24 horas. Peróxido de hidrogênio foi utilizado como controle positivo e DMSO 0,125% como controle de veículo. No entanto, como mostra a figura 18, nesta condição, a análise de micronúcleos não pode ser realizada, pois os micronúcleos são danos transmitidos as células filhas, portanto é necessário que as células tratadas tenham sua capacidade de divisão celular preservada após o tratamento. Ao contrário do que foi observado para o
49 48 controle de veículo e controle positivo, nas linhagens tratadas com maitenina não foram observadas células binucleadas, o que sugere que as poucas células que sobrevivem ao tratamento perdem sua capacidade de divisão, sendo assim tem baixo potencial mutagênico. Figura 18 : Figura representativa do ensaio de micronúcleo em células SiHa, C-33 A e HaCaT tratadas com maitenina por 6 horas, seguido de pós-tratamento de 24 horas. Imagens capturadas no IN Cell Analyzer 2000 com a objetiva de 20X. CV: DMSO 0,125%; CP: Peróxido de hidrogênio (1mM por 15 minutos, seguido de pós tratamento de 24 horas). As setas brancas indicam células binucleadas, e as setas amarelas indicam células binucleadas com micronúcleo. No entanto, para confirmar a hipótese de baixo potencial mutagênico causado pela maitenina nas linhagens avaliadas, foi realizado um segundo protocolo de tratamento: as células foram tratadas com uma concentração abaixo do CI50 determinado no ensaio de citotoxicidade de 24 horas, sendo assim as linhagens SiHa e HaCaT foram tratadas com 1,85µM de maitenina e a linhagem C-33 A foi tratada com 3,71 µm de maitenina durante 24 horas. Nessa concentração, a maioria das células permaneceram vivas, e a análise de
Vírus DNA tumorais: PAPILOMAVÍRUS HUMANO (HPV) Testes inespecíficos:
 Vírus DNA tumorais: PAPILOMAVÍRUS HUMANO (HPV) Os vírus do papiloma humano são classificados na família Papillomaviridae, gênero Papilomavírus. São vírus envelopados, de simetria icosaédrica, com 72 capsômeros
Vírus DNA tumorais: PAPILOMAVÍRUS HUMANO (HPV) Os vírus do papiloma humano são classificados na família Papillomaviridae, gênero Papilomavírus. São vírus envelopados, de simetria icosaédrica, com 72 capsômeros
Cultura de Células Animais. Aula 4 - Fases do Crescimento Celular. Prof. Me. Leandro Parussolo
 Cultura de Células Animais Aula 4 - Fases do Crescimento Celular Prof. Me. Leandro Parussolo NOVA CÉLULA Introdução A dinâmica de uma cell é + bem compreendida examinandose o curso de sua vida; divisão
Cultura de Células Animais Aula 4 - Fases do Crescimento Celular Prof. Me. Leandro Parussolo NOVA CÉLULA Introdução A dinâmica de uma cell é + bem compreendida examinandose o curso de sua vida; divisão
Patogêneses virais II. Profa Dra Mônica Santos de Freitas
 Patogêneses virais II Profa Dra Mônica Santos de Freitas 09.11.2011 1 Determinante da patogênese Interação com o tecido alvo; Acesso ao tecido alvo; Presença de receptores; Estabilidade das partículas
Patogêneses virais II Profa Dra Mônica Santos de Freitas 09.11.2011 1 Determinante da patogênese Interação com o tecido alvo; Acesso ao tecido alvo; Presença de receptores; Estabilidade das partículas
Cultura de Células Animais. Aula 5 - Linhagens Permanentes e Primárias. Prof. Me. Leandro Parussolo
 Cultura de Células Animais Aula 5 - Linhagens Permanentes e Primárias Prof. Me. Leandro Parussolo Biologia da Célula em Cultura Cultura de Cells Crítica - Cell faz parte de um microambiente não reproduzido
Cultura de Células Animais Aula 5 - Linhagens Permanentes e Primárias Prof. Me. Leandro Parussolo Biologia da Célula em Cultura Cultura de Cells Crítica - Cell faz parte de um microambiente não reproduzido
Vírus Características Gerais
 Vírus Características Gerais Características Gerais Do latim veneno Agentes diminutos visíveis por microscopia eletrônica 10 a 100 vezes menores que bactérias 20-30 nm Estruturalmente muito simples Apenas
Vírus Características Gerais Características Gerais Do latim veneno Agentes diminutos visíveis por microscopia eletrônica 10 a 100 vezes menores que bactérias 20-30 nm Estruturalmente muito simples Apenas
NEWS artigos CETRUS Ano 2 - Edição 16 - Dezembro/2010
 NEWS artigos CETRUS Ano 2 - Edição 16 - Dezembro/2010 Atualização em Patologia do Trato Genital Inferior e Colposcopia - Capítulo II - Infecção por HPV e Lesões HHV-Induzidas Prof. Dr. Flávio Zucchi -
NEWS artigos CETRUS Ano 2 - Edição 16 - Dezembro/2010 Atualização em Patologia do Trato Genital Inferior e Colposcopia - Capítulo II - Infecção por HPV e Lesões HHV-Induzidas Prof. Dr. Flávio Zucchi -
MULTIPLICAÇÃO VIRAL Danielly Cantarelli
 MULTIPLICAÇÃO VIRAL Danielly Cantarelli 1 Os vírus não possuem enzimas para a produção de energia nem para a síntese protéica Para que um vírus se multiplique, ele deve invadir uma célula hospedeira e
MULTIPLICAÇÃO VIRAL Danielly Cantarelli 1 Os vírus não possuem enzimas para a produção de energia nem para a síntese protéica Para que um vírus se multiplique, ele deve invadir uma célula hospedeira e
Bioensaios celulares: Princípios e Aplicações
 Bioensaios celulares: Princípios e Aplicações Letícia Veras Costa Lotufo Laboratório de Oncologia Experimental Departamento de Fisiologia e Farmacologia, UFC lvcosta@secrel.com.br PROGRAMA: 11/02 aula
Bioensaios celulares: Princípios e Aplicações Letícia Veras Costa Lotufo Laboratório de Oncologia Experimental Departamento de Fisiologia e Farmacologia, UFC lvcosta@secrel.com.br PROGRAMA: 11/02 aula
Papilomavirus humanos (HPV)
 Papilomavirus humanos (HPV) - Capsídio icosaédrico de 55-60 nm, sem envoltório - 72 capsômeros pentaméricos formados por 2 proteínas (cinco cópias de L1 fora, 1 L2 dentro) - Família Papillomaviridae, gênero
Papilomavirus humanos (HPV) - Capsídio icosaédrico de 55-60 nm, sem envoltório - 72 capsômeros pentaméricos formados por 2 proteínas (cinco cópias de L1 fora, 1 L2 dentro) - Família Papillomaviridae, gênero
Características Gerais dos Vírus
 Características Gerais dos Vírus Vírus Agentes causadores de infecções no homem, outros animais, vegetais e bactérias. São desprovidos de organelas e sem metabolismo próprio. Parasitas intracelulares obrigatórios.
Características Gerais dos Vírus Vírus Agentes causadores de infecções no homem, outros animais, vegetais e bactérias. São desprovidos de organelas e sem metabolismo próprio. Parasitas intracelulares obrigatórios.
PREVENÇÃO E TRANSMISSÃO DA INFECÇÃO POR HPV. UNITAU-SP SETOR DE GENITOSCOPIA Prof. Dr André Luis F Santos
 PREVENÇÃO E TRANSMISSÃO DA INFECÇÃO POR HPV UNITAU-SP SETOR DE GENITOSCOPIA Prof. Dr André Luis F Santos 2010 DÚVIDAS MAIS FREQUENTES A transmissão pelo HPV é só sexual? Peguei do meu parceiro? Quando?
PREVENÇÃO E TRANSMISSÃO DA INFECÇÃO POR HPV UNITAU-SP SETOR DE GENITOSCOPIA Prof. Dr André Luis F Santos 2010 DÚVIDAS MAIS FREQUENTES A transmissão pelo HPV é só sexual? Peguei do meu parceiro? Quando?
CAPÍTULO 6: COMPOSTOS ORGÂNICOS PROTEÍNAS CAP. 7: COMPOSTOS ORGÂNICOS ÁCIDOS NUCLEICOS E VITAMINAS
 CAPÍTULO 6: COMPOSTOS ORGÂNICOS PROTEÍNAS CAP. 7: COMPOSTOS ORGÂNICOS ÁCIDOS NUCLEICOS E VITAMINAS 1. Dentre os diferentes compostos orgânicos das células temos as proteínas. Sobre estas responda: a) Cite
CAPÍTULO 6: COMPOSTOS ORGÂNICOS PROTEÍNAS CAP. 7: COMPOSTOS ORGÂNICOS ÁCIDOS NUCLEICOS E VITAMINAS 1. Dentre os diferentes compostos orgânicos das células temos as proteínas. Sobre estas responda: a) Cite
Introdução ao Cultivo Celular. Professora Melissa Kayser
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES CURSO TÉCNICO EM BIOTECNOLOGIA Introdução ao
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES CURSO TÉCNICO EM BIOTECNOLOGIA Introdução ao
Replicação dos Vírus. Células 26/04/2012. Ciclo celular. Vírus: não apresentam estrutura celular. ausência de metabolismo
 Replicação dos Vírus Profª Maria Luzia da Rosa e Silva Vírus: não apresentam estrutura celular ausência de metabolismo Entretanto, a produção de novas partículas (Replicação) Requer síntese de macromoléculas
Replicação dos Vírus Profª Maria Luzia da Rosa e Silva Vírus: não apresentam estrutura celular ausência de metabolismo Entretanto, a produção de novas partículas (Replicação) Requer síntese de macromoléculas
PROPRIEDADES GERAIS DOS VIRUS. Charlotte Marianna Hársi
 PROPRIEDADES GERAIS DOS VIRUS Charlotte Marianna Hársi ICB-USP 2009 H1N1 poliomielite Vírus? HIV meningite Dengue resfriados Influenza ebola gastrenterite Febre amarela hepatite sarampo herpes catapora
PROPRIEDADES GERAIS DOS VIRUS Charlotte Marianna Hársi ICB-USP 2009 H1N1 poliomielite Vírus? HIV meningite Dengue resfriados Influenza ebola gastrenterite Febre amarela hepatite sarampo herpes catapora
Vírus - Caracterização Geral
 Noções de Vírus By Profª. Cynthia Vírus - Caracterização Geral Vírus = veneno ou fluído venenoso (Latim) Acelulares/ Partículas Infecciosas Composição química de nucleoproteínas (DNA ou RNA+Proteínas)
Noções de Vírus By Profª. Cynthia Vírus - Caracterização Geral Vírus = veneno ou fluído venenoso (Latim) Acelulares/ Partículas Infecciosas Composição química de nucleoproteínas (DNA ou RNA+Proteínas)
EXERCÍCIOS DE MONITORIA 2º PERÍODO AGOSTO BIOLOGIA RECUP. PARCIAL
 1ª série Ens. Médio 1. A figura a seguir refere-se à hereditariedade: a) EXERCÍCIOS DE MONITORIA 2º PERÍODO AGOSTO BIOLOGIA RECUP. PARCIAL b) Explique de que forma a molécula de DNA atua no fenômeno da
1ª série Ens. Médio 1. A figura a seguir refere-se à hereditariedade: a) EXERCÍCIOS DE MONITORIA 2º PERÍODO AGOSTO BIOLOGIA RECUP. PARCIAL b) Explique de que forma a molécula de DNA atua no fenômeno da
Tópicos de Imunologia Celular e Molecular (Parte 2)
 IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
IMUNOLOGIA BÁSICA Tópicos de Imunologia Celular e Molecular (Parte 2) Prof. M. Sc. Paulo Galdino Os três outros tipos de hipersensibilidade ( II, III e IV) têm em comum uma reação exagerada do sistema
Jamile Andrade Oliveira
 1 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Ciências Farmacêuticas ATIVIDADE CITOTÓXICA E APOPTÓTICA DE NITENSIDINA A E B EM CÉLULAS DE CARCINOMA CERVICAL IMORTALIZADAS PELO PAPILOMA
1 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Ciências Farmacêuticas ATIVIDADE CITOTÓXICA E APOPTÓTICA DE NITENSIDINA A E B EM CÉLULAS DE CARCINOMA CERVICAL IMORTALIZADAS PELO PAPILOMA
ONCOLOGIA. Aula I Profª.Enfª: Darlene Carvalho (www.darlenecarvalho.webnode.com.br)
 ONCOLOGIA Aula I Profª.Enfª: Darlene Carvalho (www.darlenecarvalho.webnode.com.br) CLASSIFICAÇÃO DAS CÉLULAS Lábeis Estáveis Perenes CLASSIFICAÇÃO DAS CÉLULAS Células lábeis: São aquelas em constante renovação
ONCOLOGIA Aula I Profª.Enfª: Darlene Carvalho (www.darlenecarvalho.webnode.com.br) CLASSIFICAÇÃO DAS CÉLULAS Lábeis Estáveis Perenes CLASSIFICAÇÃO DAS CÉLULAS Células lábeis: São aquelas em constante renovação
INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES METROPOLITANAS UNIDAS
 16 TÍTULO: REVISÃO DE CONCEITO CITOMORFOLÓGICO PARA DIAGNÓSTICO DE ADENOCARCINOMA CATEGORIA: EM ANDAMENTO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES
16 TÍTULO: REVISÃO DE CONCEITO CITOMORFOLÓGICO PARA DIAGNÓSTICO DE ADENOCARCINOMA CATEGORIA: EM ANDAMENTO ÁREA: CIÊNCIAS BIOLÓGICAS E SAÚDE SUBÁREA: BIOMEDICINA INSTITUIÇÃO: CENTRO UNIVERSITÁRIO DAS FACULDADES
FELIPE DE OLIVEIRA SOUZA
 UNIVERSIDADE ESTADUAL PAULISTA "JULIO DE MESQUITA FILHO" FACULDADE DE CIÊNCIAS FARMACÊUTICAS CÂMPUS DE ARARAQUARA FELIPE DE OLIVEIRA SOUZA Atividade citotóxica, pró-apoptótica, genotóxica e mutagênica
UNIVERSIDADE ESTADUAL PAULISTA "JULIO DE MESQUITA FILHO" FACULDADE DE CIÊNCIAS FARMACÊUTICAS CÂMPUS DE ARARAQUARA FELIPE DE OLIVEIRA SOUZA Atividade citotóxica, pró-apoptótica, genotóxica e mutagênica
especiais, que através do sistema do encaixe ou ajuste induzido unem-se ao
 VÍRUS: CARACTERÍSTICAS GERAIS A palavra vírus significa veneno, e é o nome dado à pequenas estruturas infecciosas dotadas de uma capa e material genético. Essas estruturas são mais pequenas do que as menores
VÍRUS: CARACTERÍSTICAS GERAIS A palavra vírus significa veneno, e é o nome dado à pequenas estruturas infecciosas dotadas de uma capa e material genético. Essas estruturas são mais pequenas do que as menores
Métodos imunológicos na avaliação da resposta à vacinação.
 Métodos imunológicos na avaliação da resposta à vacinação. Patrícia Neves Laboratório de Tecnologia Imunológica VDTEC/Biomanguinhos Proteção vacinal A identificação de marcadores imunológicos que se correlacionem
Métodos imunológicos na avaliação da resposta à vacinação. Patrícia Neves Laboratório de Tecnologia Imunológica VDTEC/Biomanguinhos Proteção vacinal A identificação de marcadores imunológicos que se correlacionem
Disciplina Biologia Celular
 Disciplina Biologia Celular Profª Cristina Lacerda Soares Petrarolha Silva Curso de Biotecnologia FISMA / FEA Aula 3: Tecnologia da Biologia Celular Parte II Bio Cel Profª Cristina 1 1- Citoquímica Estudo
Disciplina Biologia Celular Profª Cristina Lacerda Soares Petrarolha Silva Curso de Biotecnologia FISMA / FEA Aula 3: Tecnologia da Biologia Celular Parte II Bio Cel Profª Cristina 1 1- Citoquímica Estudo
3ª Série / Vestibular _ TD 08 _ 19 de abril
 3ª Série / Vestibular _ TD 08 _ 19 de abril 21. As células caracterizam-se por possuir uma membrana plasmática, separando o meio intracelular do meio extracelular. A manutenção da integridade dessa membrana
3ª Série / Vestibular _ TD 08 _ 19 de abril 21. As células caracterizam-se por possuir uma membrana plasmática, separando o meio intracelular do meio extracelular. A manutenção da integridade dessa membrana
Citoplasma. ocorrem as reações químicas. 1. Contém uma substância gelatinosa onde. 2. Local onde estão submersas as organelas.
 CITOLOGIA Citoplasma 1. Contém uma substância gelatinosa onde ocorrem as reações químicas. 2. Local onde estão submersas as organelas. Citoesqueleto 1. Formado por proteínas que mantém a forma celular;
CITOLOGIA Citoplasma 1. Contém uma substância gelatinosa onde ocorrem as reações químicas. 2. Local onde estão submersas as organelas. Citoesqueleto 1. Formado por proteínas que mantém a forma celular;
Apoptose, ou morte celular programada
 Apoptose, ou morte celular programada é um processo essencial para a manutenção do desenvolvimento dos seres vivos, sendo importante para eliminar células supérfluas ou defeituosas. As células têm um conjunto
Apoptose, ou morte celular programada é um processo essencial para a manutenção do desenvolvimento dos seres vivos, sendo importante para eliminar células supérfluas ou defeituosas. As células têm um conjunto
MÉTODOS DE ESTUDO DE BACTÉRIAS BUCAIS
 LABORATÓRIO DE ANAERÓBIOS http://www.icb.usp.br/bmm/mariojac MÉTODOS DE ESTUDO DE BACTÉRIAS BUCAIS Prof. Dr. Mario J. Avila-Campos Para que isolar microrganismos? - Conhecer os diferentes tipos microbianos
LABORATÓRIO DE ANAERÓBIOS http://www.icb.usp.br/bmm/mariojac MÉTODOS DE ESTUDO DE BACTÉRIAS BUCAIS Prof. Dr. Mario J. Avila-Campos Para que isolar microrganismos? - Conhecer os diferentes tipos microbianos
Perspectivas da introdução das vacinas contra HPV junto aos programas de rastreio
 Perspectivas da introdução das vacinas contra HPV junto aos programas de rastreio Trocando Idéias XIV 27-29 de agosto de 2009 Rio de Janeiro Fábio Russomano Evidências da efetividade do rastreio citológico
Perspectivas da introdução das vacinas contra HPV junto aos programas de rastreio Trocando Idéias XIV 27-29 de agosto de 2009 Rio de Janeiro Fábio Russomano Evidências da efetividade do rastreio citológico
Taninos. Profa. Wânia Vianna 1S/2014
 Taninos Profa. Wânia Vianna 1S/2014 Estudo Metabólitos Secundário Aspectos Importantes Identificar aspectos característicos da estrutura química; Caracterizar a polaridade da molécula: escolha do solvente
Taninos Profa. Wânia Vianna 1S/2014 Estudo Metabólitos Secundário Aspectos Importantes Identificar aspectos característicos da estrutura química; Caracterizar a polaridade da molécula: escolha do solvente
Ajustar o ph para 7,4. Filtrar o meio em 0,22 µm no fluxo e depois acrescentar o antibiótico/antimicótico. Armazenar de 2ºC a 8ºC.
 ANEXO I - SOLUÇÕES A Para expansão dos hibridomas Meio de cultura (solução-estoque) Meio RPMI - Roswell Park Memorial 10,4 g Institute (Gibco, Invitrogen) NaHCO 3 2 g HEPES 4,68 g Antibiótico/antimicótico
ANEXO I - SOLUÇÕES A Para expansão dos hibridomas Meio de cultura (solução-estoque) Meio RPMI - Roswell Park Memorial 10,4 g Institute (Gibco, Invitrogen) NaHCO 3 2 g HEPES 4,68 g Antibiótico/antimicótico
Introdução a Virologia. Definição - O que é vírus? Composição e estrutura Genoma e Replicação
 Introdução a Virologia Definição - O que é vírus? Composição e estrutura Genoma e Replicação O que é vírus? Agentes infecciosos ultramicroscópicos Não são células São partículas filtráveis Só apresentam
Introdução a Virologia Definição - O que é vírus? Composição e estrutura Genoma e Replicação O que é vírus? Agentes infecciosos ultramicroscópicos Não são células São partículas filtráveis Só apresentam
Relembrando: Material genético
 REGULAÇÃO GÉNICA Relembrando: Material genético O MATERIAL GENÉTICO é o suporte físico do conjunto de padrões de informações hereditárias, transmitidas ao longo das gerações. GENE é a unidade de informação
REGULAÇÃO GÉNICA Relembrando: Material genético O MATERIAL GENÉTICO é o suporte físico do conjunto de padrões de informações hereditárias, transmitidas ao longo das gerações. GENE é a unidade de informação
AULA PRÁTICA 3-02/06/2015. Roteiro de aula prática. Infecção de macrófagos por Leishmania (Leishmania) amazonensis
 AULA PRÁTICA 3-02/06/2015 Roteiro de aula prática Infecção de macrófagos por Leishmania (Leishmania) amazonensis Macrófagos previamente plaqueados e infectados com formas promastigotas de Leishmania (Leishmania)
AULA PRÁTICA 3-02/06/2015 Roteiro de aula prática Infecção de macrófagos por Leishmania (Leishmania) amazonensis Macrófagos previamente plaqueados e infectados com formas promastigotas de Leishmania (Leishmania)
Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio.
 ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
Introdução ao Cultivo Celular. Professora Melissa Kayser
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES CURSO TÉCNICO EM BIOTECNOLOGIA Introdução ao
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES CURSO TÉCNICO EM BIOTECNOLOGIA Introdução ao
UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA
 UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Genética Bacteriana Disciplina: Biologia de Microrganismos Professora: Alessandra Machado Genética Bacteriana
UNIVERSIDADE FEDERAL DE JUIZ DE FORA DEPARTAMENTO DE PARASITOLOGIA, MICROBIOLOGIA E IMUNOLOGIA Genética Bacteriana Disciplina: Biologia de Microrganismos Professora: Alessandra Machado Genética Bacteriana
Imunoensaios no laboratório clínico
 Imunoensaios no laboratório clínico Onde pesquisamos Ag e Ac?? Imunoensaios detecção e quantificação de antígeno e anticorpo: Doenças infecciosas: diagnóstico da doença diferenciação da fase da doença
Imunoensaios no laboratório clínico Onde pesquisamos Ag e Ac?? Imunoensaios detecção e quantificação de antígeno e anticorpo: Doenças infecciosas: diagnóstico da doença diferenciação da fase da doença
Métodos de Pesquisa e Diagnóstico dos Vírus
 Métodos de Pesquisa e Diagnóstico dos Vírus Estratégias Isolamento em sistemas vivos Pesquisa de antígeno viral Pesquisa de anticorpos Pesquisa do ácido nucléico viral (DNA ou RNA) Pré requisitos para
Métodos de Pesquisa e Diagnóstico dos Vírus Estratégias Isolamento em sistemas vivos Pesquisa de antígeno viral Pesquisa de anticorpos Pesquisa do ácido nucléico viral (DNA ou RNA) Pré requisitos para
Professor: David Vieira Valadão. Biologia
 Professor: David Vieira Valadão Biologia 1981 registro de casos atípicos de pneumonia entre homens homossexuais em Los Angeles (EUA). 1983 descoberta de um novo vírus em um paciente com AIDS. 1984 descoberta
Professor: David Vieira Valadão Biologia 1981 registro de casos atípicos de pneumonia entre homens homossexuais em Los Angeles (EUA). 1983 descoberta de um novo vírus em um paciente com AIDS. 1984 descoberta
PRINCÍPIOS GERAIS DA RECOMBINAÇÃO DO DNA
 PRINCÍPIOS GERAIS DA RECOMBINAÇÃO DO DNA ÍNDICE Introdução Evolução: mutação e recombinação do DNA Erros de Recombinação: Câncer? Engenharia Genética e Transgênicos Recombinação homóloga - Modelo Holliday
PRINCÍPIOS GERAIS DA RECOMBINAÇÃO DO DNA ÍNDICE Introdução Evolução: mutação e recombinação do DNA Erros de Recombinação: Câncer? Engenharia Genética e Transgênicos Recombinação homóloga - Modelo Holliday
Regulação da expressão gênica em Procariotos. John Wiley & Sons, Inc.
 Regulação da expressão gênica em Procariotos Cada célula tem todos os genes, mas em um tecido apenas parte deles está ativa REGULAÇÃO DA EXPRESSÃO GÊNICA Diferenciação celular: diferentes tipos celulares
Regulação da expressão gênica em Procariotos Cada célula tem todos os genes, mas em um tecido apenas parte deles está ativa REGULAÇÃO DA EXPRESSÃO GÊNICA Diferenciação celular: diferentes tipos celulares
AIDS e HPV Cuide-se e previna-se!
 AIDS e HPV Cuide-se e previna-se! O que é AIDS? Existem várias doenças que são transmissíveis através das relações sexuais e por isso são chamadas DSTs (doenças sexualmente transmissíveis). As mais conhecidas
AIDS e HPV Cuide-se e previna-se! O que é AIDS? Existem várias doenças que são transmissíveis através das relações sexuais e por isso são chamadas DSTs (doenças sexualmente transmissíveis). As mais conhecidas
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N Professores. Carlos T. Hotta Ronaldo B.
 Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
PROJETO DE LEI DO SENADO Nº, DE 2009
 PROJETO DE LEI DO SENADO Nº, DE 2009 Altera a Lei nº 11.664, de 29 de abril de 2008, para incluir a pesquisa de biomarcadores entre as ações destinadas à detecção precoce das neoplasias malignas de mama
PROJETO DE LEI DO SENADO Nº, DE 2009 Altera a Lei nº 11.664, de 29 de abril de 2008, para incluir a pesquisa de biomarcadores entre as ações destinadas à detecção precoce das neoplasias malignas de mama
INTRODUÇÃO Á BIOQUÍMICA
 INTRODUÇÃO Á BIOQUÍMICA BIOQUÍMICA ENFERMAGEM FIO Faculdades Integradas de Ourinhos. Prof. Esp. Roberto Venerando Fundação Educacional Miguel Mofarrej. FIO robertovenerando@fio.edu.br 1 - Introdução à
INTRODUÇÃO Á BIOQUÍMICA BIOQUÍMICA ENFERMAGEM FIO Faculdades Integradas de Ourinhos. Prof. Esp. Roberto Venerando Fundação Educacional Miguel Mofarrej. FIO robertovenerando@fio.edu.br 1 - Introdução à
Jonas Alves de Araujo Junior
 Jonas Alves de Araujo Junior Graduação: Universidade Estadual de Londrina- UEL Aprimoramento: Faculdade de Medicina de Botucatu- UNESP Mestrado: Faculdade de Ciências Farmacêuticas- USP Doutorando: Faculdade
Jonas Alves de Araujo Junior Graduação: Universidade Estadual de Londrina- UEL Aprimoramento: Faculdade de Medicina de Botucatu- UNESP Mestrado: Faculdade de Ciências Farmacêuticas- USP Doutorando: Faculdade
Clique para editar o estilo do título mestre
 sub 23/07/2014 1 23/07/2014 1 AU09 Estrutura título e Função mestre do Material Genético Nalini subtítulo Drieli Josviak mestre Doutorado drinaly@gmail.com 23/07/2014 2 23/07/2014 2 Material Genético:
sub 23/07/2014 1 23/07/2014 1 AU09 Estrutura título e Função mestre do Material Genético Nalini subtítulo Drieli Josviak mestre Doutorado drinaly@gmail.com 23/07/2014 2 23/07/2014 2 Material Genético:
Introdução à Bioquímica
 Introdução à Bioquímica Nucleotídeos e Ácidos Nucléicos Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto - SP. Genoma! O genoma de um organismo
Introdução à Bioquímica Nucleotídeos e Ácidos Nucléicos Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto - SP. Genoma! O genoma de um organismo
Bactérias Vírus Fungos Protozoários O QUE SÃO
 Bactérias Vírus Fungos Protozoários RESUMO DOS PRINCIPAIS MICRORGANISMOS, O QUE SÃO MEIOS DE PROLIFERAÇÃO... Diferença entre as células Bactérias São seres muito simples, unicelulares e com célula procariótica
Bactérias Vírus Fungos Protozoários RESUMO DOS PRINCIPAIS MICRORGANISMOS, O QUE SÃO MEIOS DE PROLIFERAÇÃO... Diferença entre as células Bactérias São seres muito simples, unicelulares e com célula procariótica
PRÁ-SABER DIGITAL: Informações de Interesse à Saúde SISCOLO Porto Alegre 2007
 1 SISCOLO RELATÓRIO 2007 2 Prefeitura Municipal de Porto Alegre Prefeito José Fogaça Secretaria Municipal da Saúde Secretário Eliseu Santos Coordenadoria Geral de Vigilância em Saúde Coordenador José Ângelo
1 SISCOLO RELATÓRIO 2007 2 Prefeitura Municipal de Porto Alegre Prefeito José Fogaça Secretaria Municipal da Saúde Secretário Eliseu Santos Coordenadoria Geral de Vigilância em Saúde Coordenador José Ângelo
Vírus. Leonardo Rodrigues EEEFM GRAÇA ARANHA
 Vírus Leonardo Rodrigues EEEFM GRAÇA ARANHA Virologia Virologia. Ramo da Biologia que estuda os vírus e suas propriedades. Vírus é totalmente inerte fora da sua célula hospedeira; Dependem totalmente da
Vírus Leonardo Rodrigues EEEFM GRAÇA ARANHA Virologia Virologia. Ramo da Biologia que estuda os vírus e suas propriedades. Vírus é totalmente inerte fora da sua célula hospedeira; Dependem totalmente da
Avaliação do Índice Apoptótico em Adenomas Pleomórficos de Glândulas Salivares
 PONTIFÍCIA UNIVERSIDADE CATÓLICA DE MINAS GERAIS Faculdade de Odontologia Avaliação do Índice Apoptótico em Adenomas Pleomórficos de Glândulas Salivares Paulo César de Lacerda Dantas Belo Horizonte- MG
PONTIFÍCIA UNIVERSIDADE CATÓLICA DE MINAS GERAIS Faculdade de Odontologia Avaliação do Índice Apoptótico em Adenomas Pleomórficos de Glândulas Salivares Paulo César de Lacerda Dantas Belo Horizonte- MG
Processos de interação vírus célula. e replicação viral
 Processos de interação vírus célula e replicação viral Adsorção: ligação do receptor celular e antirreceptor viral. Exemplo poliovírus: 1 Adsorção: ligação do receptor celular e antirreceptor viral. Hepatite
Processos de interação vírus célula e replicação viral Adsorção: ligação do receptor celular e antirreceptor viral. Exemplo poliovírus: 1 Adsorção: ligação do receptor celular e antirreceptor viral. Hepatite
folder_saude_da_mulher.pdf 1 19/07/16 16:48 VIVER BEM ADRIANA JUSSARA EM A MULHER QUE VALIA POR MUITAS CMY SAÚDE DA MULHER
 folder_saude_da_mulher.pdf 1 19/07/16 16:48 VIVER BE ADRIANA JUSSARA E A ULHER QUE VALIA POR UITAS SAÚDE DA ULHER folder_saude_da_mulher.pdf 2 19/07/16 16:48 Leia o código e assista a história de Adriana
folder_saude_da_mulher.pdf 1 19/07/16 16:48 VIVER BE ADRIANA JUSSARA E A ULHER QUE VALIA POR UITAS SAÚDE DA ULHER folder_saude_da_mulher.pdf 2 19/07/16 16:48 Leia o código e assista a história de Adriana
HPV E SUA INFLUÊNCIA NO CÂNCER DE COLO DE ÚTERO
 HPV E SUA INFLUÊNCIA NO CÂNCER DE COLO DE ÚTERO Jader Iury de Souza Mercante Graduando em Fisioterapia, Faculdades Integradas de Três Lagoas FITL/AEMS Rafaela Giuzeppe Rodrigues Graduanda em Fisioterapia,
HPV E SUA INFLUÊNCIA NO CÂNCER DE COLO DE ÚTERO Jader Iury de Souza Mercante Graduando em Fisioterapia, Faculdades Integradas de Três Lagoas FITL/AEMS Rafaela Giuzeppe Rodrigues Graduanda em Fisioterapia,
Bases ecológicas da resistência bacteriana às drogas
 Bases ecológicas da resistência bacteriana às drogas Drogas antimicrobianas: mecanismo de ação Um aspecto do controle do crescimento dos microrganismos envolve a utilização de fármacos no tratamento de
Bases ecológicas da resistência bacteriana às drogas Drogas antimicrobianas: mecanismo de ação Um aspecto do controle do crescimento dos microrganismos envolve a utilização de fármacos no tratamento de
Genética Molecular. Tema 1: Genética Molecular. Prof. Leandro Parussolo
 Instituto Federal de Santa Catarina Câmpus Florianópolis Unidade Curricular: Biologia I Tema 1: Genética Molecular Genética Molecular Prof. Leandro Parussolo leandro.parussolo@ifsc.edu.br Genética Estuda
Instituto Federal de Santa Catarina Câmpus Florianópolis Unidade Curricular: Biologia I Tema 1: Genética Molecular Genética Molecular Prof. Leandro Parussolo leandro.parussolo@ifsc.edu.br Genética Estuda
15/10/2009 GENÉTICA BACTERIANA. Disciplina: Microbiologia Geral Curso: Nutrição Prof. Renata Fernandes Rabello. Informação genética essencial.
 GENÉTICA BACTERIANA GENOMA BACTERIANO Cromossoma (nucleóide) Informação genética essencial. Ácido desoxirribonucléico (DNA). Disciplina: Microbiologia Geral Curso: Nutrição Prof. Renata Fernandes Rabello
GENÉTICA BACTERIANA GENOMA BACTERIANO Cromossoma (nucleóide) Informação genética essencial. Ácido desoxirribonucléico (DNA). Disciplina: Microbiologia Geral Curso: Nutrição Prof. Renata Fernandes Rabello
CIÊNCIAS EJA 5ª FASE PROF.ª SARAH DOS SANTOS PROF. SILONE GUIMARÃES
 CIÊNCIAS EJA 5ª FASE PROF.ª SARAH DOS SANTOS PROF. SILONE GUIMARÃES CONTEÚDOS E HABILIDADES Unidade II Ser Humano e Saúde 2 CONTEÚDOS E HABILIDADES Aula 11.2 Conteúdo Doenças Sexualmente Transmissíveis
CIÊNCIAS EJA 5ª FASE PROF.ª SARAH DOS SANTOS PROF. SILONE GUIMARÃES CONTEÚDOS E HABILIDADES Unidade II Ser Humano e Saúde 2 CONTEÚDOS E HABILIDADES Aula 11.2 Conteúdo Doenças Sexualmente Transmissíveis
Apoptose. Prof. Tiago Collares, Dr. (MSN) ( )
 Apoptose Prof. Tiago Collares, Dr. tiago_collares@hotmail.com (MSN) collares.t@gmail.com (e-mail ) $99.50 $82.74 $31.86 Necessidades de Morte Celular em Organismos Multicelulares - Característica latente;
Apoptose Prof. Tiago Collares, Dr. tiago_collares@hotmail.com (MSN) collares.t@gmail.com (e-mail ) $99.50 $82.74 $31.86 Necessidades de Morte Celular em Organismos Multicelulares - Característica latente;
Nutrigenômica x Nutrigenética - doenças relacionadas
 Nutrigenômica x Nutrigenética - doenças relacionadas Início Projeto Genoma Humano 20.000 genes (120.000 inicialmente estimados) Diversidade nucleotídica: 0,1 a 0,4% pares de base correspondente a aproximadamente
Nutrigenômica x Nutrigenética - doenças relacionadas Início Projeto Genoma Humano 20.000 genes (120.000 inicialmente estimados) Diversidade nucleotídica: 0,1 a 0,4% pares de base correspondente a aproximadamente
Introdução à Histologia e Técnicas Histológicas. Prof. Cristiane Oliveira
 Introdução à Histologia e Técnicas Histológicas Prof. Cristiane Oliveira Visão Geral Corpo humano organizado em 4 tecidos básicos: Epitelial Conjuntivo Muscular Nervoso Visão Geral - Tecidos consistem
Introdução à Histologia e Técnicas Histológicas Prof. Cristiane Oliveira Visão Geral Corpo humano organizado em 4 tecidos básicos: Epitelial Conjuntivo Muscular Nervoso Visão Geral - Tecidos consistem
PERFIL EPIDEMIOLÓGICO DE PACIENTES COM NEOPLASIA DE MAMA EM TRATAMENTO COM TRANSTUZUMABE EM HOSPITAL NO INTERIOR DE ALAGOAS
 PERFIL EPIDEMIOLÓGICO DE PACIENTES COM NEOPLASIA DE MAMA EM TRATAMENTO COM TRANSTUZUMABE EM HOSPITAL NO INTERIOR DE ALAGOAS Andreia Herculano da Silva Casa de Saúde e Maternidade Afra Barbosa Andreiah.silva@hotmail.com
PERFIL EPIDEMIOLÓGICO DE PACIENTES COM NEOPLASIA DE MAMA EM TRATAMENTO COM TRANSTUZUMABE EM HOSPITAL NO INTERIOR DE ALAGOAS Andreia Herculano da Silva Casa de Saúde e Maternidade Afra Barbosa Andreiah.silva@hotmail.com
Cultivo de células animais e humanas
 MINISTÉRIO DA EDUCAÇÃO Universidade Federal de Alfenas. Unifal-MG Rua Gabriel Monteiro da Silva, 700. Alfenas/MG. CEP 37130-000 Fone: (35) 3299-1000. Fax: (35) 3299-1063 Minicurso: Cultivo de células animais
MINISTÉRIO DA EDUCAÇÃO Universidade Federal de Alfenas. Unifal-MG Rua Gabriel Monteiro da Silva, 700. Alfenas/MG. CEP 37130-000 Fone: (35) 3299-1000. Fax: (35) 3299-1063 Minicurso: Cultivo de células animais
Mutagênese... a prevenção é o espelho do índice cultural de uma nação.
 Pontifícia Universidade Católica de Goiás Pró-Reitoria de Graduação Departamento de Biologia Mutagênese Raimundo Jr, M.Sc. Genética / BIO1240 2013/1 Considerações Gerais Objetivando uma melhor qualidade
Pontifícia Universidade Católica de Goiás Pró-Reitoria de Graduação Departamento de Biologia Mutagênese Raimundo Jr, M.Sc. Genética / BIO1240 2013/1 Considerações Gerais Objetivando uma melhor qualidade
Exercício de Fixação: Características Gerais dos Vírus
 Exercício de Fixação: Características Gerais dos Vírus 01-2017 1- Quais foram as observações feitas por Adolf Mayer que permitiram concluir que o agente etiológico da Doença do Mosaico do tabaco era um
Exercício de Fixação: Características Gerais dos Vírus 01-2017 1- Quais foram as observações feitas por Adolf Mayer que permitiram concluir que o agente etiológico da Doença do Mosaico do tabaco era um
Hibridação de ácidos nucleicos. de cromossomo a chip de DNA
 Hibridação de ácidos nucleicos de cromossomo a chip de DNA Hibridação de ácidos nucleicos Pareamento complementar de bases entre duas fitas simples de ácido nucleico DNA DNA RNA RNA DNA - RNA Hibridação
Hibridação de ácidos nucleicos de cromossomo a chip de DNA Hibridação de ácidos nucleicos Pareamento complementar de bases entre duas fitas simples de ácido nucleico DNA DNA RNA RNA DNA - RNA Hibridação
Um modelo de múltiplas escalas para avaliar a eficácia de terapias do câncer com nanopartículas
 Um modelo de múltiplas escalas para avaliar a eficácia de terapias do câncer com nanopartículas Letícia R. Paiva e Marcelo L. Martins* Departamento de Física Universidade Federal de Viçosa *Instituto Nacional
Um modelo de múltiplas escalas para avaliar a eficácia de terapias do câncer com nanopartículas Letícia R. Paiva e Marcelo L. Martins* Departamento de Física Universidade Federal de Viçosa *Instituto Nacional
Profº André Montillo
 Profº André Montillo www.montillo.com.br Definição: É um polímero, ou seja, uma longa cadeia de nucleotídeos. Estrutura Molecular dos Nucleotídeos: Os nucleotídeos são constituídos por 3 unidades: Bases
Profº André Montillo www.montillo.com.br Definição: É um polímero, ou seja, uma longa cadeia de nucleotídeos. Estrutura Molecular dos Nucleotídeos: Os nucleotídeos são constituídos por 3 unidades: Bases
AU10. Princípios Básicos de Genética Molecular 2: Regulação da Expressão Gênica. Juliana da Silveira Schauren
 AU10 Princípios Básicos de Genética Molecular 2: Regulação da Expressão Gênica Juliana da Silveira Schauren Doutoranda PPG-GEN julianaschauren@gmail.com Resumo Introdução: revisão transcrição e tradução
AU10 Princípios Básicos de Genética Molecular 2: Regulação da Expressão Gênica Juliana da Silveira Schauren Doutoranda PPG-GEN julianaschauren@gmail.com Resumo Introdução: revisão transcrição e tradução
Biologia Professor Leandro Gurgel de Medeiros
 Biologia Professor Leandro Gurgel de Medeiros Divisão Celular Ciclo Celular e Mitose; Meiose. 1. Aspectos Mantidos na Divisão Celular Constância do volume celular; Relação área x volume. Lei de Driesch
Biologia Professor Leandro Gurgel de Medeiros Divisão Celular Ciclo Celular e Mitose; Meiose. 1. Aspectos Mantidos na Divisão Celular Constância do volume celular; Relação área x volume. Lei de Driesch
Seleção de clones e screening de bibliotecas genômicas
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO PÓLO AVANÇADO DE XERÉM GRADUAÇÃO EM BIOTECNOLOGIA CURSO MELH. GEN. E OGMs (XBT353) TURMA 2015/2 Seleção de clones e screening de bibliotecas genômicas Prof. Dr. Silas
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO PÓLO AVANÇADO DE XERÉM GRADUAÇÃO EM BIOTECNOLOGIA CURSO MELH. GEN. E OGMs (XBT353) TURMA 2015/2 Seleção de clones e screening de bibliotecas genômicas Prof. Dr. Silas
VIVER BEM ÂNGELA HELENA E A PREVENÇÃO DO CÂNCER NEOPLASIAS
 1 VIVER BEM ÂNGELA HELENA E A PREVENÇÃO DO CÂNCER NEOPLASIAS 2 3 Como muitas mulheres, Ângela Helena tem uma vida corrida. Ela trabalha, cuida da família, faz cursos e também reserva um tempo para cuidar
1 VIVER BEM ÂNGELA HELENA E A PREVENÇÃO DO CÂNCER NEOPLASIAS 2 3 Como muitas mulheres, Ângela Helena tem uma vida corrida. Ela trabalha, cuida da família, faz cursos e também reserva um tempo para cuidar
Perguntas para o roteiro de aula. 1) Descreva as principais características estruturais gerais das moléculas de DNA e
 Perguntas para o roteiro de aula Professora: Drª Marilda S. Gonçalves Propriedades físico-químicas dos ácidos nucléicos 1) Descreva as principais características estruturais gerais das moléculas de DNA
Perguntas para o roteiro de aula Professora: Drª Marilda S. Gonçalves Propriedades físico-químicas dos ácidos nucléicos 1) Descreva as principais características estruturais gerais das moléculas de DNA
Professor Dr Flavio Zucchi CRM Médico Ginecologista Especialista em HPV (Papilomavirus Humano)
 Professor Dr Flavio Zucchi CRM 27311 Médico Ginecologista Especialista em HPV (Papilomavirus Humano) Atividades: Chefe de ambulatório no setor de Genitoscopia da disciplina de Ginecologia da escola paulista
Professor Dr Flavio Zucchi CRM 27311 Médico Ginecologista Especialista em HPV (Papilomavirus Humano) Atividades: Chefe de ambulatório no setor de Genitoscopia da disciplina de Ginecologia da escola paulista
Água A superfície da Terra é constituída de três quartos de água, cerca de 70%, a maior parte está concentrada nos oceanos e mares, cerca de 97,5%, o
 A química da Vida Água A superfície da Terra é constituída de três quartos de água, cerca de 70%, a maior parte está concentrada nos oceanos e mares, cerca de 97,5%, o restante 2,5% está concentrado em
A química da Vida Água A superfície da Terra é constituída de três quartos de água, cerca de 70%, a maior parte está concentrada nos oceanos e mares, cerca de 97,5%, o restante 2,5% está concentrado em
PROCESSOS PATOLÓGICOS GERAIS. Prof. Archangelo P. Fernandes
 PROCESSOS PATOLÓGICOS GERAIS Prof. Archangelo P. Fernandes www.profbio.com.br Aula 1: Conceitos gerais para o estudo de Patologia. Grego: pathos = sofrimento e logos = estudo Investigação das causas das
PROCESSOS PATOLÓGICOS GERAIS Prof. Archangelo P. Fernandes www.profbio.com.br Aula 1: Conceitos gerais para o estudo de Patologia. Grego: pathos = sofrimento e logos = estudo Investigação das causas das
IMPORTÂNCIA DA GENÉTICA PARA ÁREA DA SAÚDE: Diagnóstico clínico: alteração no número ou estrutura dos cromossomos (síndrome de Down)
 Aplicações: IMPORTÂNCIA DA GENÉTICA PARA ÁREA DA SAÚDE: Diagnóstico clínico: alteração no número ou estrutura dos cromossomos (síndrome de Down) Mapeamento genético e identificação: mapeamento de genes
Aplicações: IMPORTÂNCIA DA GENÉTICA PARA ÁREA DA SAÚDE: Diagnóstico clínico: alteração no número ou estrutura dos cromossomos (síndrome de Down) Mapeamento genético e identificação: mapeamento de genes
. a d iza r to u a ia p ó C II
 II Sugestões de avaliação Ciências 8 o ano Unidade 3 5 Unidade 3 Nome: Data: 1. As bactérias não têm núcleo nem DNA. Você concorda com essa afirmação? Justifique. 2. Uma mulher de 40 anos de idade está
II Sugestões de avaliação Ciências 8 o ano Unidade 3 5 Unidade 3 Nome: Data: 1. As bactérias não têm núcleo nem DNA. Você concorda com essa afirmação? Justifique. 2. Uma mulher de 40 anos de idade está
Curso Técnico em Análises Químicas Disciplina: Microbiologia. Aula 3.1 Bactérias
 Curso Técnico em Análises Químicas Disciplina: Microbiologia Aula 3.1 Bactérias CLASSIFICAÇÃO: Bactérias Quanto a respiração: Aeróbicas: crescem apenas na presença de O 2. Anaeróbicas: crescem em ausência
Curso Técnico em Análises Químicas Disciplina: Microbiologia Aula 3.1 Bactérias CLASSIFICAÇÃO: Bactérias Quanto a respiração: Aeróbicas: crescem apenas na presença de O 2. Anaeróbicas: crescem em ausência
CÂNCER DE COLO ÚTERINO: DIAGNÓSTICOS E PREVENÇÃO, TRATAMENTO.
 CÂNCER DE COLO ÚTERINO: DIAGNÓSTICOS E PREVENÇÃO, TRATAMENTO. Allef Ravely Dias Gonzaga¹ Neilma Santos Cavalcanti De Andrade¹, Rúbia De Souza Porto¹, Simone De Carvalho Rocha¹ Giovanni Tavares De Sousa²
CÂNCER DE COLO ÚTERINO: DIAGNÓSTICOS E PREVENÇÃO, TRATAMENTO. Allef Ravely Dias Gonzaga¹ Neilma Santos Cavalcanti De Andrade¹, Rúbia De Souza Porto¹, Simone De Carvalho Rocha¹ Giovanni Tavares De Sousa²
FUNDAMENTOS DE CITOMETRIA DE FLUXO. Dayane Alves Costa Priscilla Ramos Costa Programa de Alergia e Imunopatologia- LIM 60 USP
 FUNDAMENTOS DE CITOMETRIA DE FLUXO Dayane Alves Costa Priscilla Ramos Costa Programa de Alergia e Imunopatologia- LIM 6 USP CITOMETRIA DE FLUXO CITO METRIA DE FLUXO CÉLULA MEDIDA MOVIMENTO Caracterização
FUNDAMENTOS DE CITOMETRIA DE FLUXO Dayane Alves Costa Priscilla Ramos Costa Programa de Alergia e Imunopatologia- LIM 6 USP CITOMETRIA DE FLUXO CITO METRIA DE FLUXO CÉLULA MEDIDA MOVIMENTO Caracterização
7.012 Soluções do Conjunto de Problemas 6
 Nome Seção 7.012 Soluções do Conjunto de Problemas 6 Pergunta 1 A família de vírus Orthomyxoviridae inclui os vírus influenza A, B e C. Esses vírus possuem um genoma (-)ssrna envolto por um capsídeo composto
Nome Seção 7.012 Soluções do Conjunto de Problemas 6 Pergunta 1 A família de vírus Orthomyxoviridae inclui os vírus influenza A, B e C. Esses vírus possuem um genoma (-)ssrna envolto por um capsídeo composto
Vídeo didático LISOSSOMOS E DIGESTÃO CELULAR. Disponível em: https://www.youtube.com/watch?v=qaemvl3enxk
 1 Vídeo didático Contato e texto didático www.nuepe.ufpr LISOSSOMOS E DIGESTÃO CELULAR Disponível em: https://www.youtube.com/watch?v=qaemvl3enxk Este vídeo didático foi construído com base em imagens
1 Vídeo didático Contato e texto didático www.nuepe.ufpr LISOSSOMOS E DIGESTÃO CELULAR Disponível em: https://www.youtube.com/watch?v=qaemvl3enxk Este vídeo didático foi construído com base em imagens
Todos tem uma grande importância para o organismo.
 A Química da Vida ÁGUA A água é um composto químico formado por dois átomos de hidrogênio e um de oxigênio. Sua fórmula química é H2O. A água pura não possui cheiro nem cor. Ela pode ser transformada em
A Química da Vida ÁGUA A água é um composto químico formado por dois átomos de hidrogênio e um de oxigênio. Sua fórmula química é H2O. A água pura não possui cheiro nem cor. Ela pode ser transformada em
Vacinação contra HPV e Controle do câncer de colo do útero no SUS Claudio Pompeiano Noronha
 Vacinação contra HPV e Controle do câncer de colo do útero no SUS Claudio Pompeiano Noronha Coordenação Geral de Ações Estratégicas CGAE Instituto Nacional de Câncer - INCA Ministério da Saúde junho de
Vacinação contra HPV e Controle do câncer de colo do útero no SUS Claudio Pompeiano Noronha Coordenação Geral de Ações Estratégicas CGAE Instituto Nacional de Câncer - INCA Ministério da Saúde junho de
DNA: Replicação e Transcrição. Professora: MSc Monyke Lucena
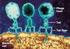 EXTRA, EXTRA Se a mãe for (DD) e o pai (D), nenhum dos descendentes será daltónico nem portador. Se a mãe (DD) e o pai for (d), nenhum dos descendentes será daltônico, porém as filhas serão portadoras
EXTRA, EXTRA Se a mãe for (DD) e o pai (D), nenhum dos descendentes será daltónico nem portador. Se a mãe (DD) e o pai for (d), nenhum dos descendentes será daltônico, porém as filhas serão portadoras
Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194
 Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194 Imunologia das Viroses Monitor: Daniel Valente 1.Introdução...
Universidade Federal da Bahia Faculdade de Medicina Departamento de Anatomia Patológica e Medicina Legal Disciplina de Imunologia MED 194 Imunologia das Viroses Monitor: Daniel Valente 1.Introdução...
Antivirais. Profa Dra Mônica Santos de Freitas Sunday, December 2, 12
 Antivirais Profa Dra Mônica Santos de Freitas 21.11.2012 As vacinas são ótimas na prevenção de doenças O que acontece quando o indivíduo esta doente? A vacina é o melhor tratamento? Existem aproximadamente
Antivirais Profa Dra Mônica Santos de Freitas 21.11.2012 As vacinas são ótimas na prevenção de doenças O que acontece quando o indivíduo esta doente? A vacina é o melhor tratamento? Existem aproximadamente
Divisão celular. A única situação em que dividir e multiplicar significam a mesma coisa
 Divisão celular A única situação em que dividir e multiplicar significam a mesma coisa Todos as células se dividem: 1. Em organismos unicelulares, divisão celular é o modo principal de reprodução 2. Em
Divisão celular A única situação em que dividir e multiplicar significam a mesma coisa Todos as células se dividem: 1. Em organismos unicelulares, divisão celular é o modo principal de reprodução 2. Em
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM)
 Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
PALAVRAS-CHAVE Neoplasias do colo do útero. Epidemiologia. Patologia
 14. CONEX Apresentação Oral Resumo Expandido - ISSN 2238-9113 1 ISSN 2238-9113 ÁREA TEMÁTICA: (marque uma das opções) ( ) COMUNICAÇÃO ( ) CULTURA ( ) DIREITOS HUMANOS E JUSTIÇA ( ) EDUCAÇÃO ( ) MEIO AMBIENTE
14. CONEX Apresentação Oral Resumo Expandido - ISSN 2238-9113 1 ISSN 2238-9113 ÁREA TEMÁTICA: (marque uma das opções) ( ) COMUNICAÇÃO ( ) CULTURA ( ) DIREITOS HUMANOS E JUSTIÇA ( ) EDUCAÇÃO ( ) MEIO AMBIENTE
Estudo da estabilidade do sistema Paratest usado para diagnóstico das parasitoses intestinais Rev.00 10/01/2011
 1 Estudo da estabilidade do sistema Paratest usado para diagnóstico das parasitoses intestinais Rev.00 10/01/2011 1. Introdução As parasitoses intestinais representam sério problema de saúde pública, em
1 Estudo da estabilidade do sistema Paratest usado para diagnóstico das parasitoses intestinais Rev.00 10/01/2011 1. Introdução As parasitoses intestinais representam sério problema de saúde pública, em
Anabolismo Nuclear e Divisão Celular
 1. (UFRN) Uma proteína X codificada pelo gene Xp é sintetizada nos ribossomos, a partir de um RNAm. Para que a síntese aconteça, é necessário que ocorram, no núcleo e no citoplasma, respectivamente, as
1. (UFRN) Uma proteína X codificada pelo gene Xp é sintetizada nos ribossomos, a partir de um RNAm. Para que a síntese aconteça, é necessário que ocorram, no núcleo e no citoplasma, respectivamente, as
CATÁLOGO DE KITS DE EXTRAÇÃO
 CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
Partículas sujeitas à análise: célula eucariótica; organelas citoplasmáticas; cromossomos; células agregadas (ex: células tumorais); bactérias;
 O QUE É: Processo no qual células, ou outras partículas biológicas, são forçadas a passar, num filete único, por sensores que são capazes de analisar as características físicas ou químicas das células
O QUE É: Processo no qual células, ou outras partículas biológicas, são forçadas a passar, num filete único, por sensores que são capazes de analisar as características físicas ou químicas das células
