Ligação de O 2 a Mioglobina e a Hemoglobina
|
|
|
- Fátima Rocha da Conceição
- 6 Há anos
- Visualizações:
Transcrição
1 Ligação de O 2 a Mioglobina e a Hemoglobina
2 A Mioglobina possui 1 sítio de ligação para o O 2 ** 8 α-helical segments ** contains one heme ** MW 16,700 ** Single O 2 binding site ** reversible protein-ligand interaction ** Oxygen storage
3 A Hemoglobina possui 4 sítios de ligação ao O 2 - Estrutura Quaternária 2 unidades α e 2 unidades β -Interação forte entre as subunidades α e β.
4 A Comparison of The Structure of Myoglobin and The β-subunit of Hemoglobin
5 1. Reversible Binding of Proteins to a Ligand: Oxygen Binding Proteins Heme : contain iron. Anéis pirrólicos Porfirina Protophorphyrin IX
6 A Histidina 93 coordena com o Ferro e auxilia a sua ligação ao O 2 Distal histidine Fe 2+ (His 93 ) Proximal histidine
7 O grupo heme visto de lado Coordination bond Molecular oxygen Globin molecule
8 Brahimi-Horn, M. C. & Pouysségur, J. (2007) Oxygen, a source of life and stress. FEBS Letters 581, Fig. 1. Physiological and pathophysiological oxygen partial pressures (po2). The po2 of inspired air drops progressively as oxygen passes from the lungs into the circulation, which irrigates the tissues of major organs, and then in the venous system before re-oxygenation in the lungs. The po2 of solid tumours (insert) is generally low compared to that of non-malignant tissues.
9 Ligação de O 2 à Mioglobina Tecidos Pulmão
10 A ligação de O 2 altera a conformação das subunidades da hemoglobina TENSO DEOXI-Hb RELAXADO OXI-Hb
11 Ligação de O 2 a Hemoglobina R T
12 O grupo Heme em seu ambiente na cadeia da Hb humana sem Ligante
13 A ligação de O 2 altera a conformação local da cadeia peptídica... Azul forma T Rosa forma R
14 .resultando na alteração da conformação total do tetrâmero Fig. 5-10
15 Cooperatividade entre as subunidades resulta numa curva de ligação de O 2 sigmoidal R-state DesoxiHb (T) capta O 2 no pulmão, convertendo-se para o estado R, o qual por sua vez, capta mais O 2 T-state OxiHb (R) volta aos tecidos onde a pressão de O 2 é baixa e inicia a liberação de O 2, promovendo a conversão da Hb em desoxihb (T)
16 2,3-BisFosfoGlicerato (BFG) liga-se a Hb reduzindo a sua afinidade por O 2 Hb pura libera apenas 8 % do O 2 Hb + 2,3-BFG libera 66 % do O 2 2,3-BFG é um efetor alostérico (allos=outro; stereo=estrutura) 2,3-BFG estabiliza a estrutura T (desoxi) da Hb
17
18 Efeito do ph na ligação da Hb ao O 2 (Efeito Bohr, Christian Bohr 1904) A diminuição do ph afeta a ionização de Histidinas... No ph menor a His 146 está protonada, estabilizando a estrutura T da Hb A diminuição do ph aumenta a liberação de O 2 nos tecidos
19
20
21 Endergônico Exergônico
22 Vias Metabólicas Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos). Note que: as vias são interconectadas Pontos importantes: (pontos de cruzamento). - conhecer as principais avenidas (vias), - os cruzamentos mais importantes (intermediários comuns) e - como o fluxo nessas vias são controladas (regulação)...
23
24 Visão Geral do Catabolismo
25
26 1. Introdução: Enzimas 1. Duas condições fundamentais para a vida : (1) capacidade de se autoreplicar (2) capacidade de catalisar reações químicas eficiente e seletivamente Ex. : Açúcar pode ser estocado por anos, mas no organismo ele libera energia química em segundos catálise Energia 2. Catalisadores em sistema biológico: AS ENZIMAS..Proteínas altamente especializadas que possuem eficiência catalítica extraordinária alto grau de especificidade aceleram as reações químicas
27 Enzimas são catalisadores extraordinários e altamente específicos!
28 A maior parte da História da Bioquímica coincide com a História das Enzimas 1850 Louis Pasteur..Fermentação em células vivas ( força vital, vitalismo) 1878 Fredrich Wilhelm Kuhne Enzima (en=no e zyme=levedura) 1897 Eduard Buchner Extrato de levedura livre de células capaz de realizar a fermentação 1894 Emil Fischer Hipótese chave-fechadura 1926 James Sumner. Cristalização da Urease do Feijão Preto Demonstrou que enzimas são proteinas J.B.S. Haldane Interações Enzima-Substrato (Escreveu um tratado sobre Enzimas)
29 Atividade catalítica depende da conformação proteica Se a Enzima é desnaturada ou dissociada em subunidades ela perde a atividade catalítica!! Glucose
30
31
32
33
34
35
36
37 Isomerização: aldose cetose
38 Enzima alostérica
39 Clivagem da frutose 1,6-bifosfato
40 Grupo Prostético - Componente químico adicional requerido por certas enzimas - Estão firmemente ligados às enzimas Cofatores : compostos inorgânicos Fe 2+, Mg 2+, Mn 2+, Zn 2+ Coenzimas : compostos orgânicos. Normalmente derivado de vitaminas Holoenzima = Apoenzima (porção proteica) + coenzima ou cofator
41 Cofatores : compostos inorgânicos (Fe 2+, Mg 2+, Mn 2+, Zn 2+ ) Coenzimas : compostos orgânicos. (Normalmente derivado de vitaminas)
42 Classificação São classificadas de acordo com o tipo de reação que catalisam Código para Enzimas : EC ATP glicose fosfotransferase Classe Transferase Subclasse Fosfotransferase
43 2. Como as enzimas trabalham? A função termodinâmica denominada de energia livre (G) é importante para compreender como as enzimas trabalham. Parâmetros termodinâmicos que deve-se considerar: 1) A variação de energia livre ( G) entre produtos e reagentes 2) A energia necessária (energia de ativação) para iniciar a conversão dos reagentes em produtos G: indica a espontaneidade da reação Energia de ativação: determina a velocidade da reação As enzimas afeta apenas a energia de ativação!
44 Sob condições de temperatura e pressão constantes... ΔG = ΔH -TΔS ΔH - que reflete os tipos e o número de ligações químicas e interações não-covalentes quebrados e formados ΔS que reflete a variação da desordem do sistema
45 ΔG = ΔH -TΔS ΔG<0 (negativo) : Reações espontâneas > produtos têm menos energia livre que os reagentes, a qual pode ser utilizada para realizar trabalho são reações exergônicas. ΔG >0 (positivo): Pecisam que seja fornecida energia são reações endergônicas.
46 ΔG o negativo ΔG o positivo G reagentes > G produtos Reação ocorre espontaneamente sob condições padrão. G reagentes < G produtos Reação ocorre no sentido reverso, caso seja iniciada com a concentração 1 M (condições padrão) Lembrem-se todas as reações químicas tendem a ocorrer no sentido que resulta na diminuição de energia livre do sistema.
47 Energia Livre de Ativação
48 No interior das células as reações químicas ocorrem devido à presença de enzimas Enzimas: catalisadores capazes de aumentar enormemente a velocidade de reações químicas específicas sem serem consumidos no processo. Elas dimimuem a energia de ativação. Energia de ativação (ΔG*): energia extra necessária para que a reação ocorra.
49
50 Enzimas afetam a velocidade mas não o equilíbrio químico Reação Química : S P 1. Catalisador não afeta a posição e nem a direção do equilíbrio 2. Um equilíbrio favorável não significa que a conversão de S P ocorra em uma velocidade mensurável 3. A velocidade depende da Energia de Ativação: energia necessária para o alinhamento dos grupos químicos reagentes, formação de cargas transientes, rearranjos de ligações e outras transformações necessária para que a reação ocorra em uma das direções
51 O equilíbrio da reação está relacionado à variação de energia livre padrão Um grande valor negativo de ΔG o indica um equilíbrio de reação favorável á formação dos produtos, mas não significa que ela ocorra a uma velocidade considerável.
52 2. Como as enzimas trabalham? As enzimas fornecem um ambiente específico (SÍTIO ATIVO) onde uma dada reação é energeticamente mais fovorável. SÍTIO ATIVO SUBSTRATO (ligante) Tamanho: Enzima >>> Substrato Quimotripsina
53 Enzimas afetam a velocidade mas não o equilíbrio químico Estado de transição Reação Química : S P Energia de Ativação Variação de Energia Livre Padrão Bioquímico Estado Fundamental Ponto de Partida para a reação de ida ou de volta.
54 Enzimas aceleram a velocidade da reação diminuindo a energia de ativação (A enzima não é gasta no processo e não afeta o ponto de equilíbrio) E + S ES EP E + P ENERGIA DE ATIVAÇÃO
55 Complexo Enzima Substrato Formas complementares de um Substrato e seu Sítio Ativo (Chave-Fechadura, Emil Fischer) Diidrofolato Redutase NADP + liga-se a uma cavidade complementar à sua forma e propriedades iônicas. NADP + Tetraidrofolato Conceito chave-fechadura sugere um encaixe perfeito entre E e S. O que resultaria numa enzima pouco eficiente!!
56 Enzima imaginária ( bastonase ) projetada para catalisar a quebra de um bastão de metal Modelo Chave-Fechadura A cavidade complementar ao substrato estabiliza-o mas não o quebra. O substrato estabiliza o estado de transição do complexo ES, diminuindo a energia de ativação. Algumas interações fracas são formadas no complexo ES, mas a totalidade das interações fracas é estabelecida apenas no estado de transição.
57 O papel da energia de ligação para a catálise 1. A energia de ligação confere especificidade e catálise. 2. E + S ES: A interações fracas formadas entre E e S fornecem a maior parte da energia necessária para a catálise. Energia de ligação
58 3. Cinética Enzimática Estuda o mecanismo de reações catalisadas enzimaticamente através do estudo da velocidade da reação enzimática e como ela se altera em função de mudanças nos parâmetros experimentais
59 1913: Teoria geral da ação das enzimas 1 2 E + S ES E + P 1. Inicialmente a enzima se combina reversivelmente com o substrato para formar o complexo ES, um passo relativamente rápido;
60 A concentração do substrato afeta a velocidade das reações catalisadas enzimaticamente E + S ES E + P Enzima está saturada com S (todas as enzimas econtramse complexadas com o substrato) 1. Velocidade Inicial ( V 0 ) : velocidade no tempo inicial quando a [S] >>> [E] 2. Velocidade máxima ( V max ) : ponto em que não ocorre variações em V 0 com o aumento da [S]. [S] << [E]: Grande quantidade de enzimas livres.
61 Equação de Michaelis-Menten Equação que relaciona [S] e a Vmax de forma quantitativa. Michaelis-Mentem derivaram a reação partindo da hipótese de que o passo limitante da reação é a quebra do complexo ES. E + S ES E + P 1. E + S ES reversível e relativamente rápida 2. ES E + P, Quebra do complexo ES é LENTA! 3. Velocidade total é dependente da [ES] 4. Quando [S] a maioria de E está na forma livre mas quando [S], a maoria de E está complexada.. Enzima está saturada Onde: V o : velocidade no tempo inicial quando a [S] >>> [E] V max : V máximo [S]: concentração do substrato K m : constante de Michaelis
62 Significado do K m K M = [S] quando v o = 1/2 Vmax. Em geral, quanto menor o K M, mais forte é ligação do substrato pela enzima. K M é usado como uma medida da afinidade da enzima pelo substrato
63
64 Transformação da equação de Michaelis e Mentem Gráfico do Duplo-Recíproco (Equação de Lineweaver- Burk)
65 Enzimas estão sujeitas à inibição 1. Importância Farmacêutica do estudo da inibição enzimática Inibidores enzimáticos são agentes moleculares que interferem na catálise, diminuindo ou acelerando a velocidade da reação esse é o mecanismo de ação da grande maioria de agentes farmacêuticos. Ex. : Aspirina Inibidor da síntese de Prostaglandinas Antiinflamatório 2. Classificação: 1) Inibição Reversível: Inibição Competitiva Inibição Não-Competitiva
66 As especificidades das fosfolipases
67 Arachidonic acid an some eicosanoid derivatives (response to hormonal signals)
68 Aspirin, acetaminophen,... Inhibiting the enzyme cyclooxygenase
69 Inibição competitiva
70 Inibição competitiva (I liga-se somente a E) Cinética na presença de [I] cresce Ki: constante de dissociação do inibidor Ki=[E][I]/[EI] Qto < Ki, mais potente é a inibição. 1. Vmax não se altera
71 1 K M (1 + I/K i ) = x v V M S V M K M aumenta; V max igual
72 Inibição competitiva Exemplo: Intoxicação por Metanol Desidrogenase alcoolica converte metanol em formaldeído (tóxico!) que pode resultar em cegueira. Tratamento: ETANOL O etanol compete com o metanol pelo sítio ativo da enzima
73 Inibição Não-Competitiva Inibidor liga-se a enzima em um sítio diferente a do sítio ativo do substrato.
74 Inibição Não-Competitiva (I liga-se a E ou ES) 1. Vmax diminui
75 1 K M = x v V M / (1 + I/K i ) S V M / (1 + I/K i ) K M igual; V max diminui
76 Inibição Irreversível Inibidores irreversíveis combinam-se com um grupo funcional na molécula da enzima ou o destroem ou ainda formam uma associação covalente bastante estável. São úteis como ferramentas no estudo de mecanismo de reação, principalmente para a identificação de aminoácidos importantes para a catálise no sítio ativo. Quimotripsina Diisopropylfluorophosphate Forma permanentemente inativa
77 5. Enzimas Alostéricas Enzimas reguladas pela ligação não-covalente de compostos reguladores chamados, moduladores alostéricos. A regulação enzimática envolve alterações conformacionais similares a da Hemoglobina
78 Enzimas Regulatórias
79
80 5. Enzimas Alostéricas São proteínas compostas de subunidades (Estrutura Quaternária) e exibe cooperatividade Possuem sítios distintos de ligação: Sítio regulatório e sítio catalítico (ativo). Sítio regulatório localiza-se em um sítio distinto do sítio ativo. Esses sítios podem estar localizados em uma mesma subunidade ou em subunidades distintas.
81 5. Enzimas Alostéricas Em muitas enzimas alostéricas o sítio de ligação do substrato e o(s) sítio(s) de ligação do substrato estão em subunidades diferentes. O modulador pode ser Estimulatório ou Inibitório Ligação do modulador causa MUDANÇAS na CONFORMAÇÃO.
82 5. Enzimas Alostéricas As propriedades cinéticas das enzimas alostéricas divergem do comportamento de Michaelis-Mentem 1. As enzimas alostéricas apresentam relações entre V o e S que diferem da cinética de Michaelis-Menten. 2. Curva sigmoidal em vez de hiperbólica. 3. Ao invés de K m tem-se um K 0,5
83 5. Enzimas Alostéricas Efeitos de um modulador positivo e negativo sobre a enzima alostérica Positive modulator Negative modulator
84 Glicólise
85 Exemplo de enzima alostérica Fosfofrutoquinase Tetrâmero Substratos F6P ATP Efetores Alostéricos PEP, ATP (negativo) ADP (positivo) Sítio Ativo ADP Monômero
86 5. Enzimas Alostéricas Fosfofrutoquinase é regulada alostericamente por ATP Modulador negativo
87 Regulação Alostérica Lembrar dos estados T e R da Hemoglobina Inibidores alostéricos favorecem o estado T (menor afinidade) Ativadores alostéricos favorecem o estado R (maior afinidade)
88 2 modelos de Cooperatividade Concerted Symmetry driven- all R or All T. Substrate stabilizes R. Sequential Ligand induced neighboring unoccupied subunits are variably affected
89 Modificação Covalente
90 Glicogênio fosforilase
91
92 Atividade de uma enzima Habilidade catalítica em converter S em P. Medida: Unidades de Atividade. 1U=1µmole produto/min. (em condições ótimas) Atividade específica: atividade enzimática quantidade de enzimas Expresso em: unidades/mg proteína
93
94 Catálise Enzimática A catálise é um processo que aumenta a velocidade com o qual a reação chega ao equilíbrio. Duas propriedades importantes para a catálise: 1. Especificidade pela ligação ao substrato 2. Organização otimizada dos grupos catalíticos
95 Mecanismos de catálise 1) Catálise ácido-base 2) Catálise Covalente 3) Catálise por Íons Metálicos
96 Catálise ácido-base A reação não-catalisada ocorre lentamente devido à alta energia do estado de transição. Na catálise ácida-geral, a transferência de um próton, diminui a energia do estado de transição. Na catálise básica-geral, a abstração de um próton por uma base, ajuda a estabilizar o estado de transição.
97 N NH Não-ionizado" Catalisador Básico" (proton 'sink')" +H -H N H NH Ionizado" Catalisador ácido" (proton source)"
98 Reação não-catalisada Formação de um carbânion no estado de transição
99 Reação não-catalisada Catálise ácida (transferência de prótons para o estado de transição) A doação de um próton ao átomo de oxigênio, reduz o caráter de carbânion do estado de transição, diminuindo a energia de ativação e acelerando a reação.
100 Reação não-catalisada Catálise básica (remoção de prótons por uma Base) A remoção parcial de um próton por uma base diminui a energia do estado de transição. Algumas reações são simultaneamente sujeitas a catálise ácida e básica
101 Exemplo: Reação da RNAse A - Catálise ácido-básica geral Catálise Básica Geral Catálise Ácida Geral
102 Exemplo: Reação da RNAse A - Catálise ácido-básica geral Catálise Ácida Geral Catálise Básica Geral
103 Catálise Covalente Formação transitória de uma ligação covalente entre o catalisador e o substrato. H 2 O A-B A + B A-B + :X A-X + B H 2 O A + B + :X
104
105 Exemplo: Descarboxilação do Acetoacetato
106 Exemplo: Descarboxilação do Acetoacetato
107 Exemplo: Descarboxilação do Acetoacetato
108 Exemplo: Descarboxilação do Acetoacetato
109
110 Catálise por Íons Metálicos Cerca de 1/3 de todas as enzimas conhecidas necessita de íons metálicos para que tenha atividade catalítica Metais ligam-se a substratos de modo a orientá-los de forma apropriada para a reação Metais promovem reações de oxi-redução Metais conferem estabilização de cargas
111 Enolase
112 Enolase
113 Enolase 2 íon de Mg 2+ coordenam com a carboxila Estabilização da forma enólica pelos Mg 2+ Extração de um próton (catálise básica geral)
114 Enolase Eliminação de hidróxido por catálise ácida geral
115 Catálise Eletrostática A ligação de um substrato normalmente exclui água do sítio ativo Grupos carregados no sítio ativo da enzima que tem constante dielétrica baixa organizam-se de maneira a estabilizarem o complexo de transição.
São moléculas catalíticas protéicas (exceto algumas que são RNA) - Prefixo que designa a reação: lactato desidrogenase, catalase
 1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
Cinética enzimática. Cinética enzimática. Cinética enzimática 20/03/2012. Classificação sistemática das enzimas
 Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Proteínas II. (Enzimas) Bioquímica Prof. Dr. Marcelo Soares
 Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS. Enzimas. Prof. Me. Cássio Resende de Morais
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
Enzimas - Sítio catalítico
 Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Aula de Bioquímica I. Tema: Enzimas. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
QBQ 0102 Educação Física. Carlos Hotta. Enzimas 17/03/15
 QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Introdução ao bloco II Enfermagem. Monica Montero Lomeli Sylvia Alquéres
 Introdução ao bloco II Enfermagem Monica Montero Lomeli Sylvia Alquéres Programação de aulas 16/set 21/set 23/set 28/set 30/set 05/out 07/out 12/out 14/out Apresentação do bloco + Enzimas I (cinéeca) Enzimas
Introdução ao bloco II Enfermagem Monica Montero Lomeli Sylvia Alquéres Programação de aulas 16/set 21/set 23/set 28/set 30/set 05/out 07/out 12/out 14/out Apresentação do bloco + Enzimas I (cinéeca) Enzimas
Enzimas. Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
ENZIMAS. Osmundo Brilhante
 ENZIMAS Osmundo Brilhante Introdução Condições Fundamentais para a Vida Auto replicação; O organismo deve ser capaz de catalisar as reações químicas; Metabolismo celular e manutenção da via Enzimas Doenças;
ENZIMAS Osmundo Brilhante Introdução Condições Fundamentais para a Vida Auto replicação; O organismo deve ser capaz de catalisar as reações químicas; Metabolismo celular e manutenção da via Enzimas Doenças;
Enzimas. As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica.
 Enzimas As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica. Diferem dos catalisadores comuns em vários aspectos Velocidades de reações catalisadas por
Enzimas As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica. Diferem dos catalisadores comuns em vários aspectos Velocidades de reações catalisadas por
Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global.
 ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
Aula 2: Estrutura e Função de Proteínas
 Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
ENZIMAS ENZIMAS ENZIMAS 19/02/17 DEFINIÇÃO CLASSIFICAÇÃO ESTRUTURAL. ativa. inativa
 DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores
 Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
1- Microrganismos e indústria alimentar 1.1 Fermentação e actividade enzimática
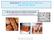 Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13
 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
ENZIMAS. Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica. Prof.: Me.
 Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
Enzimas. Bianca Zingales IQ - USP
 Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Enzimas e Actividade enzimática
 Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos
 Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
Função de proteínas As funções de muitas proteínas envolvem a ligação reversível de outras moléculas - ligandos Um ligando liga-se ao local de ligação que lhe é complementar. A interacção é específica.
Aula de Bioquímica I. Tema: Enzimas. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula!
 Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
5/4/2011. Metabolismo. Vias Metabólicas. Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos).
 Metabolismo Vias Metabólicas Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos). 1 Endergônico Exergônico Catabolismo Durante o catabolismo de carboidratos,
Metabolismo Vias Metabólicas Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos). 1 Endergônico Exergônico Catabolismo Durante o catabolismo de carboidratos,
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias.
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa
 Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Aula de Bioquímica I. Mecanismos de Catálise Enzimática
 Aula de Bioquímica I Tema: Mecanismos de Catálise Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP
Aula de Bioquímica I Tema: Mecanismos de Catálise Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP
BIOENERGÉTICA INTRODUÇÃO
 INTRODUÇÃO BIOENERGÉTICA Hoje, mais do que nunca, estamos conscientes de que a energia, a capacidade de produzir trabalho, é vital para a nossa civilização moderna. Nas suas diversas formas (elétrica,
INTRODUÇÃO BIOENERGÉTICA Hoje, mais do que nunca, estamos conscientes de que a energia, a capacidade de produzir trabalho, é vital para a nossa civilização moderna. Nas suas diversas formas (elétrica,
ENZIMAS. Prof. Dr. Vagne Oliveira. Medicina Veterinária
 ENZIMAS Disciplina: Bioquímica, Prof. Dr. Vagne Oliveira Medicina Veterinária I. VISÃO GERAL A enzima B Cada traço representa uma enzima Catalizadores biológicos: substâncias de origem biológicas que aceleram
ENZIMAS Disciplina: Bioquímica, Prof. Dr. Vagne Oliveira Medicina Veterinária I. VISÃO GERAL A enzima B Cada traço representa uma enzima Catalizadores biológicos: substâncias de origem biológicas que aceleram
Inibidores Enzimáticos
 Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
LIGAÇÃO PEPTÍDICA. ligação peptídica DIPEPTÍDEO AMINOÁCIDOS
 PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
Enzimas versus outros catalisadores
 Enzimas versus outros catalisadores Catalisadores proteicos Elevados factores de aceleração das reacções Grande especificidade para os substratos Estereo-especificidade (também absoluta) Reduzido número
Enzimas versus outros catalisadores Catalisadores proteicos Elevados factores de aceleração das reacções Grande especificidade para os substratos Estereo-especificidade (também absoluta) Reduzido número
A B A B. Espontaneidade vs. Velocidade de Reações. Enzimas como Catalisadores. Velocidade das reações depende da Energia de Ativação
 Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
Universidade Federal do Pampa Campus Itaqui Bioquímica. Profa. Dra. Marina Prigol
 Universidade Federal do Pampa Campus Itaqui Bioquímica Profa. Dra. Marina Prigol 1 1) O organismo deve ser capaz de se autoreplicar 2) O organismo deve ser capaz de catalisar reações químicas com eficiência
Universidade Federal do Pampa Campus Itaqui Bioquímica Profa. Dra. Marina Prigol 1 1) O organismo deve ser capaz de se autoreplicar 2) O organismo deve ser capaz de catalisar reações químicas com eficiência
accad.osu.edu/~vberezin/ibp/progress.htm Interações - e - mantém tetrâmero Hemoglobina é formada por cadeias e A G B D
 accad.osu.edu/~vberezin/ibp/progress.htm Hemoglobina é formada por cadeias e Interações - e - mantém tetrâmero 2 2 A G H B E D F C 1 Mioglobina e Hemoglobina O grupo heme Heme é um grupo prostético. Proteína
accad.osu.edu/~vberezin/ibp/progress.htm Hemoglobina é formada por cadeias e Interações - e - mantém tetrâmero 2 2 A G H B E D F C 1 Mioglobina e Hemoglobina O grupo heme Heme é um grupo prostético. Proteína
Professora: Erika Liz. C i n é t i c a. E n z i m á t i c a
 rofessora: Erika Liz C i n é t i c a E n z i m á t i c a Elementos da Enzimologia Reações Químicas Termodinâmica estuda a viabilidade e a reversibilidade das reações, a partir da análise do conteúdo energético
rofessora: Erika Liz C i n é t i c a E n z i m á t i c a Elementos da Enzimologia Reações Químicas Termodinâmica estuda a viabilidade e a reversibilidade das reações, a partir da análise do conteúdo energético
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
Enzimas e Coenzimas. União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Enzimas e Coenzimas Prof. Dra. Narlize Silva Lira Cavalcante Março /2015 Enzimas Praticamente todas as
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Enzimas e Coenzimas Prof. Dra. Narlize Silva Lira Cavalcante Março /2015 Enzimas Praticamente todas as
Processos catalíticos mediados por enzimas que contém metais
 Processos catalíticos mediados por enzimas que contém metais Shriver e Atkins, cap 26 Catálise ácido-base Pense: muitas reações catalisadas por ácidos ou bases requerem concentrações de H + ou de OH -
Processos catalíticos mediados por enzimas que contém metais Shriver e Atkins, cap 26 Catálise ácido-base Pense: muitas reações catalisadas por ácidos ou bases requerem concentrações de H + ou de OH -
Metabolismo e Endocrinologia
 Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Proteínas funcionais: hemoglobina e mioglobina
 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008 9ª aula teórica Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H. Freeman & Company,
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008 9ª aula teórica Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H. Freeman & Company,
BIOQUÍMICA. Profº André Montillo
 BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Glicólise. Professora Liza Felicori
 Glicólise Professora Liza Felicori Glicose Glicose (combustível metabólico) Fígado: Serve como tampão para manter o nível de glicose no sangue (liberação controlada de glicose) Glicose GLICOGÊNIO Estoque
Glicólise Professora Liza Felicori Glicose Glicose (combustível metabólico) Fígado: Serve como tampão para manter o nível de glicose no sangue (liberação controlada de glicose) Glicose GLICOGÊNIO Estoque
OBJETIVOS BIBLIOGRAFIA ENZIMAS E INIBIDORES ENZIMÁTICOS
 OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
Biossistemas e Biorreações
 Biossistemas e Biorreações Prof. Maria Alice Zarur Coelho Programa de Pós-graduação em Tecnologia de Processos Químicos e Bioquímicos Escola de Química UFRJ Metabolismo nosso principal ator Top-down versus
Biossistemas e Biorreações Prof. Maria Alice Zarur Coelho Programa de Pós-graduação em Tecnologia de Processos Químicos e Bioquímicos Escola de Química UFRJ Metabolismo nosso principal ator Top-down versus
Termodinâmica. Estudo das formas de energia que afetam a matéria. Sistemas (moléculas + solutos) X ambiente (sistema - universo)
 Termodinâmica Estudo das formas de energia que afetam a matéria Sistemas (moléculas + solutos) X ambiente (sistema - universo) Possibilita prever se processos bioquímicos são possíveis Aplicações: conformação
Termodinâmica Estudo das formas de energia que afetam a matéria Sistemas (moléculas + solutos) X ambiente (sistema - universo) Possibilita prever se processos bioquímicos são possíveis Aplicações: conformação
Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
 CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
Enzimas Alostéricas e com Múltiplos Sítios Ativos
 Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Faculdade Anhanguera Curso de Graduação em Educação Física
 Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Macromoléculas. Biologia IV Aula 2 Bioquímica Proteínas
 Biologia IV Aula 2 Bioquímica Proteínas Carla Silva Martins 08 de agosto de 2016 Macromoléculas Água Carboidratos Aminoácidos (proteínas/enzimas) Lipídeos Ácidos nucléicos (Biologia Molecular) 1 Introdução
Biologia IV Aula 2 Bioquímica Proteínas Carla Silva Martins 08 de agosto de 2016 Macromoléculas Água Carboidratos Aminoácidos (proteínas/enzimas) Lipídeos Ácidos nucléicos (Biologia Molecular) 1 Introdução
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa
 OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
Enzimas são polímeros biológicos que catalisam as reações químicas que tornam a vida possível como a conhecemos.
 ENZIMAS Enzimas são polímeros biológicos que catalisam as reações químicas que tornam a vida possível como a conhecemos. A presença e a manutenção dum conjunto completo e balanceado de enzimas é essencial
ENZIMAS Enzimas são polímeros biológicos que catalisam as reações químicas que tornam a vida possível como a conhecemos. A presença e a manutenção dum conjunto completo e balanceado de enzimas é essencial
Aula INIBIÇÃO E REGULAÇÃO ENZIMÁTICA
 INIBIÇÃO E REGULAÇÃO ENZIMÁTICA META Entender como os inibidores enzimáticos e a regulação enzimática interferem na velocidade das reações enzimáticas. OBJETIVOS Ao final desta aula, o aluno deverá: definir
INIBIÇÃO E REGULAÇÃO ENZIMÁTICA META Entender como os inibidores enzimáticos e a regulação enzimática interferem na velocidade das reações enzimáticas. OBJETIVOS Ao final desta aula, o aluno deverá: definir
Exercícios de Proteínas
 Exercícios de Proteínas 1. As são compostos formados por unidos (as) por ligações e as são orgânicos, de natureza sensíveis às variações de temperatura. Os termos que corretamente preenchem as lacunas
Exercícios de Proteínas 1. As são compostos formados por unidos (as) por ligações e as são orgânicos, de natureza sensíveis às variações de temperatura. Os termos que corretamente preenchem as lacunas
Tabela 1: Aumento de velocidade de reação proporcionado por certas enzimas Enzima Velocidade da reação não catalisada
 Bioquímica Metabólica Noturno Prof. Roberto K. Salinas 2. Cinética enzimática Enzimas são catalisadores em sistemas biológicos. As características mais notáveis das enzimas são o seu poder catalítico e
Bioquímica Metabólica Noturno Prof. Roberto K. Salinas 2. Cinética enzimática Enzimas são catalisadores em sistemas biológicos. As características mais notáveis das enzimas são o seu poder catalítico e
Prof. Leonardo F. Stahnke
 Prof. Leonardo F. Stahnke Moléculas orgânicas mais abundantes nos seres vivos, sendo importantes tanto na estrutura como funcionamento das células. São encontrados na carne vermelha, de frango ou peixe,
Prof. Leonardo F. Stahnke Moléculas orgânicas mais abundantes nos seres vivos, sendo importantes tanto na estrutura como funcionamento das células. São encontrados na carne vermelha, de frango ou peixe,
Aula de Bioquímica II SQM Fosforilação Oxidativa
 Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM
Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM
Termodinâmica em Bioquímica
 Instituto de Química de São Carlos IQSC Universidade de São Paulo Termodinâmica em Bioquímica Disciplina: Bioquímica I Docente: Profa. Dra. Fernanda Canduri Sugestão de leitura: Cap. 1 do Lehninger A vida
Instituto de Química de São Carlos IQSC Universidade de São Paulo Termodinâmica em Bioquímica Disciplina: Bioquímica I Docente: Profa. Dra. Fernanda Canduri Sugestão de leitura: Cap. 1 do Lehninger A vida
QBQ 0204 Bioquímica. Carlos Hotta. Glicólise 13/05/17
 QBQ 0204 Bioquímica Carlos Hotta Glicólise 13/05/17 Uma visão geral do metabolismo Ribose 5P (5) NUCLEOTÍDEOS Algumas reações são irreversíveis Vias de síntese e degradação precisam ser separadas Uma visão
QBQ 0204 Bioquímica Carlos Hotta Glicólise 13/05/17 Uma visão geral do metabolismo Ribose 5P (5) NUCLEOTÍDEOS Algumas reações são irreversíveis Vias de síntese e degradação precisam ser separadas Uma visão
Aula de Bioquímica II. Fosforilação Oxidativa
 Aula de Bioquímica II Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo
Aula de Bioquímica II Tema: Fosforilação Oxidativa Síntese de ATP Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Ciclo de Krebs ou Ciclo do ácido cítrico. Prof. Liza Felicori
 Ciclo de Krebs ou Ciclo do ácido cítrico Prof. Liza Felicori VISÃO GERAL Em circunstâncias aeróbicas piruvato é descarboxilado CO 2 C4 + C2 C6 C6 C6 C6 C5 CO 2 CO 2 C5 C4 C4 C4 C4 NAD+ & FAD 3 Íons H-
Ciclo de Krebs ou Ciclo do ácido cítrico Prof. Liza Felicori VISÃO GERAL Em circunstâncias aeróbicas piruvato é descarboxilado CO 2 C4 + C2 C6 C6 C6 C6 C5 CO 2 CO 2 C5 C4 C4 C4 C4 NAD+ & FAD 3 Íons H-
Biologia 12 Fermentação e actividade enzimática
 Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
Equipe de Biologia. Biologia
 Aluno (a): Série: 3ª Turma: TUTORIAL 4B Ensino Médio Equipe de Biologia Data: Biologia ENZIMAS CONCEITOS GERAIS E FUNÇÕES As enzimas são proteínas especializadas na catálise de reações biológicas. Elas
Aluno (a): Série: 3ª Turma: TUTORIAL 4B Ensino Médio Equipe de Biologia Data: Biologia ENZIMAS CONCEITOS GERAIS E FUNÇÕES As enzimas são proteínas especializadas na catálise de reações biológicas. Elas
Trabalhos de Bioquímica
 Trabalhos de Bioquímica Professora Liza Felicori Bioquímica do Exercício Bioquímica do Câncer Bioquímica do Envelhecimento Bioquímica do Diabetes Bioquímica da Obesidade 5 pontos : material Fórum Moodle
Trabalhos de Bioquímica Professora Liza Felicori Bioquímica do Exercício Bioquímica do Câncer Bioquímica do Envelhecimento Bioquímica do Diabetes Bioquímica da Obesidade 5 pontos : material Fórum Moodle
estuda a transferência,conversão e utilização da energia em sistemas biológicos exemplos: conversão de moléculas dos nutrientes em outras moléculas
 estuda a transferência,conversão e utilização da energia em sistemas biológicos exemplos: conversão de moléculas dos nutrientes em outras moléculas Obter energia química por degradação de nutrientes formar/degradar
estuda a transferência,conversão e utilização da energia em sistemas biológicos exemplos: conversão de moléculas dos nutrientes em outras moléculas Obter energia química por degradação de nutrientes formar/degradar
PROTEÍNAS GLOBULARES E
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
Profa Alessandra Barone.
 Profa Alessandra Barone www.profbio.com.br Bioenergética Parte da bioquímica que trata do estudo dos fenômenos energéticos nos seres vivos, bem como sua forma de obtenção, armazenamento, mobilização e
Profa Alessandra Barone www.profbio.com.br Bioenergética Parte da bioquímica que trata do estudo dos fenômenos energéticos nos seres vivos, bem como sua forma de obtenção, armazenamento, mobilização e
Proteínas. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Proteínas Estrutura Tridimensional de proteína Conformação Estabilidade de proteínas Ligação peptídica Estrutura Secundária
Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Proteínas Estrutura Tridimensional de proteína Conformação Estabilidade de proteínas Ligação peptídica Estrutura Secundária
Fisiologia do Exercício
 Fisiologia do Exercício REAÇÕES QUÍMICAS Metabolismo inclui vias metabólicas que resultam na síntese de moléculas Metabolismo inclui vias metabólicas que resultam na degradação de moléculas Reações anabólicas
Fisiologia do Exercício REAÇÕES QUÍMICAS Metabolismo inclui vias metabólicas que resultam na síntese de moléculas Metabolismo inclui vias metabólicas que resultam na degradação de moléculas Reações anabólicas
Introdução à Bioquímica
 Introdução à Bioquímica Enzimas Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto.. SP. Enzimas Toda enzima é uma proteína, mas nem toda
Introdução à Bioquímica Enzimas Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física.. UNESP São José do Rio Preto.. SP. Enzimas Toda enzima é uma proteína, mas nem toda
Pr P o r f o a f Al A essan a d n r d a r a B ar a o r n o e n
 Profa Alessandra Barone www.profbio.com.br Metabolismo Conjunto de reações realizadas a partir da transformação de substâncias com a finalidade de suprimento de energia, renovação de moléculas e manutenção
Profa Alessandra Barone www.profbio.com.br Metabolismo Conjunto de reações realizadas a partir da transformação de substâncias com a finalidade de suprimento de energia, renovação de moléculas e manutenção
Metabolismo e Bioenergética
 Metabolismo e Bioenergética METABOLISMO Mas o que é metabolismo? Metabolismo é o nome que damos ao conjunto das reações químicas que ocorrem dentro das células. O fato é que todas as reações químicas que
Metabolismo e Bioenergética METABOLISMO Mas o que é metabolismo? Metabolismo é o nome que damos ao conjunto das reações químicas que ocorrem dentro das células. O fato é que todas as reações químicas que
Utilização de glicose pelas células. A glicólise é a via metabólica mais conservada nos sistemas biológicos
 Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células vivas. Principais
Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células vivas. Principais
Fundamentos da Bioquímica II Aminoácidos Diferencia as propriedades físicoquímicas dos aminoácidos
 Fundamentos da Bioquímica II Aminoácidos Diferencia as propriedades físicoquímicas dos aminoácidos Amina R O α Carboxila N 2 C C O Na água: Zwitterion R O N + 3 α C C O - Carbono: Aspectos estruturais:
Fundamentos da Bioquímica II Aminoácidos Diferencia as propriedades físicoquímicas dos aminoácidos Amina R O α Carboxila N 2 C C O Na água: Zwitterion R O N + 3 α C C O - Carbono: Aspectos estruturais:
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
CQ110 : Princípios de FQ. Imagens de Rorschach
 Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Profª Eleonora Slide de aula. Metabolismo de Carboidratos
 Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
Enzimas regulatórias no controle do metabolismo 1
 Enzimas regulatórias no controle do metabolismo 1 1. Introdução A regulação do metabolismo é fundamental para que um organismo possa responder de modo rápido e eficiente a variações das condições ambientais,
Enzimas regulatórias no controle do metabolismo 1 1. Introdução A regulação do metabolismo é fundamental para que um organismo possa responder de modo rápido e eficiente a variações das condições ambientais,
PRINCIPAIS VIAS METABÓLICAS
 PRINCIPAIS VIAS METABÓLICAS DEGRADAÇÃO DO GLIGOGÊNIO GLICÓLISE VIA DAS PENTOSES FOSFATO GLICONEOGÊNESE SÍNTESE DE CORPOS CETÔNICOS DEGRADAÇÃO DE AMINOÁCIDOS E CICLO DA URÉIA CICLO DE KREBS Β-OXIDAÇÃO DE
PRINCIPAIS VIAS METABÓLICAS DEGRADAÇÃO DO GLIGOGÊNIO GLICÓLISE VIA DAS PENTOSES FOSFATO GLICONEOGÊNESE SÍNTESE DE CORPOS CETÔNICOS DEGRADAÇÃO DE AMINOÁCIDOS E CICLO DA URÉIA CICLO DE KREBS Β-OXIDAÇÃO DE
Dividido em: Anabolismo Catabolismo
 Metabolismo Somatória de todas as transformações químicas de uma célula ou organismo responsáveis pela organização molecular, obtenção de energia e síntese/degradação de moléculas específicas Via metabólica
Metabolismo Somatória de todas as transformações químicas de uma célula ou organismo responsáveis pela organização molecular, obtenção de energia e síntese/degradação de moléculas específicas Via metabólica
- O processo de síntese de ATP, microrganismos envolvidos, a glicólise, ácido pirúvico, e produtos finais. - A glicólise como via
 Objectivos Conteúdos Métodos Recursos Avaliação de Alimentos Fermentação - Perceber a como um outro síntese de ATP - Observar e compreender a via metabólica da e as suas - O síntese de ATP, microrganismos
Objectivos Conteúdos Métodos Recursos Avaliação de Alimentos Fermentação - Perceber a como um outro síntese de ATP - Observar e compreender a via metabólica da e as suas - O síntese de ATP, microrganismos
ENZIMAS. FCAV/UNESP Jaboticabal Dezembro de W.J.Melo
 ENZIMAS FCAV/UNESP Jaboticabal Dezembro de 1991 CONCEITO E EXEMPLOS!Conceito #São biomoléculas de natureza predominantemente protéica cuja função é catalisar reações termodinamicamente possíveis!exemplos
ENZIMAS FCAV/UNESP Jaboticabal Dezembro de 1991 CONCEITO E EXEMPLOS!Conceito #São biomoléculas de natureza predominantemente protéica cuja função é catalisar reações termodinamicamente possíveis!exemplos
PROTEÍNAS Professores: Manoela e Marco Aurélio 2017
 PROTEÍNAS Professores: Manoela e Marco Aurélio 2017 Bioquímica Celular Elementos químicos da matéria viva Principais substâncias presentes na matéria viva Proteínas - Nutriente construtor (função plástica)
PROTEÍNAS Professores: Manoela e Marco Aurélio 2017 Bioquímica Celular Elementos químicos da matéria viva Principais substâncias presentes na matéria viva Proteínas - Nutriente construtor (função plástica)
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
O QUE É O METABOLISMO????
 O QUE É O METABOLISMO???? Metabolismo é a somatória de todas as transformações químicas de uma célula ou organismo Uma atividade celular altamente coordenada na qual diversos sistemas multienzimáticos
O QUE É O METABOLISMO???? Metabolismo é a somatória de todas as transformações químicas de uma célula ou organismo Uma atividade celular altamente coordenada na qual diversos sistemas multienzimáticos
E Z N I Z MAS INT N RO R D O U D Ç U Ã Ç O
 ENZIMAS INTRODUÇÃO A manutenção da vida celular depende da contínua ocorrência de um conjunto de reações, que devem atender 2 exigências fundamentais: 1 a As reações devem ocorrer em velocidades adequadas
ENZIMAS INTRODUÇÃO A manutenção da vida celular depende da contínua ocorrência de um conjunto de reações, que devem atender 2 exigências fundamentais: 1 a As reações devem ocorrer em velocidades adequadas
Introdução ao Metabolismo. Profª Eleonora Slide de aula
 Introdução ao Metabolismo Profª Eleonora Slide de aula Metabolismo Profª Eleonora Slide de aula Relacionamento energético entre as vias catabólicas e as vias anabólicas Nutrientes que liberam energia Carboidratos
Introdução ao Metabolismo Profª Eleonora Slide de aula Metabolismo Profª Eleonora Slide de aula Relacionamento energético entre as vias catabólicas e as vias anabólicas Nutrientes que liberam energia Carboidratos
Caracterização de Disciplina
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DE PELOTAS PRÓ-REITORIA DE GRADUAÇÃO CURSO DE BACHARELADO EM ZOOTECNIA Caracterização de Disciplina Disciplina Bioquímica Caráter da Disciplina Obrigatório Pré-Requisito
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DE PELOTAS PRÓ-REITORIA DE GRADUAÇÃO CURSO DE BACHARELADO EM ZOOTECNIA Caracterização de Disciplina Disciplina Bioquímica Caráter da Disciplina Obrigatório Pré-Requisito
Hidrólise da ureia pela urease
 Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Sumário. 1 Introdução: matéria e medidas 1. 2 Átomos, moléculas e íons Estequiometria: cálculos com fórmulas e equações químicas 67
 Prefácio 1 Introdução: matéria e medidas 1 1.1 O estudo da química 1 1.2 Classificações da matéria 3 1.3 Propriedades da matéria 8 1.4 Unidades de medida 12 1.5 Incerteza na medida 18 1.6 Análise dimensional
Prefácio 1 Introdução: matéria e medidas 1 1.1 O estudo da química 1 1.2 Classificações da matéria 3 1.3 Propriedades da matéria 8 1.4 Unidades de medida 12 1.5 Incerteza na medida 18 1.6 Análise dimensional
MÓDULO 2 - METABOLISMO. Bianca Zingales IQ-USP
 MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
