V ENALIC/IV Seminário Nacional do Pibid 8-12 de dezembro de 2014, Natal, RN O PROJETO INTERDISCIPLINAR DOPING NO ESPORTE
|
|
|
- Victor Cortês Sintra
- 6 Há anos
- Visualizações:
Transcrição
1 O PROJETO INTERDISCIPLINAR DOPING NO ESPORTE Patrick Andersson Barreto Frasão 1, Henry Porto Vieira de Assis 1, Maria de Fátima Teixeira Gomes 2 e Denise Gutman Almada 3 1 Licenciatura em Química, Instituto de Química, bolsista Pibid-Química, UERJ. 2 DQGI, Instituto de Química, Coordenadora Subprojeto Pibid-Química, UERJ. 3 C. E. Prof. E. Faria, SEEDUC-RJ, Supervisora Subprojeto Pibid-Química, UERJ. RESUMO O projeto Doping no esporte foi desenvolvido com estudantes do Ensino Médio em nove momentos. O Momento 1, construção do conceito de doping genético a partir da leitura e discussão de três reportagens recentes sobre o tema, além da revisão de conceitos básicos sobre células animais e DNA e acompanhada da realização de um experimento de extração de DNA humano. No Momento 2 - compressão de como ocorre o doping sanguíneo - os estudantes fizeram previsões sobre as estratégias mais eficazes para aumentar a circulação de oxigênio no organismo, considerando para tal, o mecanismo de transporte do oxigênio pela oxiemoglobina e o Princípio de Le Chatelier. No Momento 3, o conceito de doping sanguíneo foi aprofundado a partir da leitura de um texto e da exibição de um vídeo. No Momento 4, grupos de substâncias que acusam o doping (hormônios, diuréticos, estimulantes e analgésicos) foram apresentados aos estudantes. No Momento 5, os alunos realizaram pesquisas sobre medicamentos de uso comum que possuem substâncias ilegais na perspectiva do doping, indicando suas fórmulas, os grupos a que pertencem e seus efeitos no organismo. No Momento 6, após a discussão da pesquisa, os alunos foram apresentados aos exames legais e no Momento 7, foram introduzidos os conceitos de amostra, branco, controle, etc., utilizados nas análises. No Momento 8, foi realizada uma simulação de um laboratório antidoping - os alunos realizaram análises químicas qualitativas de algumas amostras de urina artificial de supostos atletas e o teste respiratório para deteccão de álcool (bafômetro). No último encontro, Momento 9, os estudantes, a partir dos relatórios elaborados na simulação, discutiram e emitiram o julgamento dos supostos atletas. Consideramos que o projeto desenvolvido favoreceu o protagonismo dos estudantes, a aquisão de conceitos e procedimentos, além de promover discussões sobre aspectos éticos e sociais na prática de esportes. Palavras-chave: doping; projeto escolar, ensino de química. INTRODUÇÃO Na sociedade atual a escola básica não é mais a principal fonte de geração de conhecimento ou de difusão de informação científica para os estudantes, juntam-se a ela várias outras instituições, públicas e privadas, de pesquisa, culturais, desportivas etc., além dos meios de comunicação, cada vez mais ágeis e eficientes na transmissão de dados e imagens. Neste contexto em que não falta informação, cabe à escola formar
2 cidadãos aptos a buscá-la e capacitados a filtrá-la por meio de conhecimentos conceituais e procedimentais, que promovam sua assimilação crítica. A sociedade em que vivemos é também a do aprendizado contínuo, assim, aprender a aprender se constitui em uma das demandas essenciais que a escola deve satisfazer. Em contrapartida, também a forma como os conhecimentos são ensinados deve necessariamente ser modificada. Como apontam as DCNEB (BRASIL, 2013): Essas novas exigências requerem um novo comportamento dos professores que devem deixar de ser transmissores de conhecimentos para serem mediadores, facilitadores da aquisição de conhecimentos; devem estimular a realização de pesquisas, a produção de conhecimentos e o trabalho em grupo. Essa transformação necessária pode ser traduzida pela adoção da pesquisa como princípio pedagógico. (Pág. 103). A pesquisa como princípio pedagógico ainda está praticamente ausente nas propostas educativas das instituições de Ensino Médio, que em grande parte visam prioritariamente os processos seletivos para ingresso na Educação Superior. Uma estratégia apropriada para viabilizar a pesquisa na Educação Básica é associá-la a projetos escolares interdisciplinares e contextualizados que objetivem a elaboração de um produto final a ser exibido em sala de aula ou para a comunidade em Feiras de Ciências ou Culturais. O desenvolvimento de projetos escolares possibilita a abordagem de diversos temas (científicos, sociais, ambientais, políticos etc.) transversalmente aos conteúdos conceituais, além de dar aos alunos oportunidades de planejar e executar trabalhos e pesquisas. Como estratégia de ensino favorece o aprendizado de conceitos, atitudes e procedimentos, especialmente, quando as atividades são desenvolvidas em grupo, o que irá requerer a divisão de trabalhos e responsabilidades e o compartilhamento de ideias. Martins (2007, p.97) define projeto escolar de pesquisa como: uma atividade didática de ensino-aprendizagem, organizada dentro dos princípios da metodologia da ciência, destinada a pesquisar um fato, estudar um assunto, realizar um trabalho, individualmente ou em grupo, pela aplicação de procedimentos específicos, visando a obter certos resultados ou confeccionar um produto final. Neste artigo relatamos o projeto escolar de pesquisa desenvolvido sobre o tema Doping no esporte. Não é um problema normalmente abordado nos programas escolares, mas que os estudantes conhecem através dos meios de comunicação, e que 2
3 ganhou maior relevância com a realização, no Brasil, da Copa do Mundo da FIFA 2014 e por estarmos a dois anos da realização das Olimpíadas, no Rio de janeiro. O doping é caracterizado pelo uso de substâncias químicas ou métodos proibidos visando melhorar artificialmente o desempenho em uma atividade física ou mental, o qual deveria ser alcançado mediante um condicionamento realizado em condições saudáveis. Na história das Olimpíadas há registros de diversos casos do emprego de substâncias químicas na tentativa de obter um aumento do rendimento desportivo como, por exemplo, o uso de esteroides anabolizantes para aumentar a massa e a força muscular e de anfetaminas como estimulantes, alguns deles resultando em casos fatais. Fármacos como diuréticos, betabloqueadores, corticosteroides e esteroides anabólicos, desenvolvidos para o tratamento de diversas doenças, foram extensivamente utilizados por atletas durante os anos 70. Com o advento da biotecnologia, uma nova classe de substâncias chegou ao mercado na década de noventa, a das proteínas, dentre elas a insulina e seus derivados, o hormônio do crescimento (GH), o hormônio adrenocorticotrófico (ACTH) e a eritropoetina ou EPO (hormônio responsável pela produção de glóbulos vermelhos). Infelizmente essas substâncias também passaram a ser utilizadas na dopagem (PEREIRA, PADILHA e AQUINO NETO, 2011). Na eventualidade de um atleta necessitar de uma medicação, por razões de saúde ou por indicação médica (asma, hipertensão, diabete etc.), que tenha na sua formulação uma substância proibida, seu uso deverá ser autorizado pela federação esportiva competente. Dentre os métodos proibidos, estão os que se caracterizam pelo aumento da transferência de oxigênio e constituem o chamado doping sanguíneo, que pode ocorrer tanto por transfusão de sangue (autóloga, homóloga ou heteróloga), como pelo uso de substâncias químicas que interferem na produção de eritrócitos (glóbulos vermelhos), como a eritropoietina. Os bons resultados alcançados pela terapia genética no tratamento de doenças ligadas ao enfraquecimento muscular levou ao uso de outro método proibido, o doping genético, com o objetivo de melhorar o desempenho atlético. (PEREIRA, PADILHA e AQUINO NETO, 2011). O controle de doping no esporte pode ser realizado em sangue ou urina e sua análise é hoje um campo multidisciplinar de estudo, pois associa conhecimentos diversos de Química Orgânica, Bioquímica, Química Analítica, além de Farmacologia, Genética e Fisiologia Humana. METODOLOGIA 3
4 O projeto Doping no esporte foi desenvolvido com um grupo de seis estudantes do 3 ano do Ensino Médio do Colégio Estadual Professor Ernesto Faria, situado no bairro de São Cristovão, no Rio de Janeiro, no âmbito do Subprojeto Pibid- Química-UERJ. Foi idealizado para ser executado, no contraturno, em nove encontros semanais, cada um de aproximadamente uma hora, que denominamos de momentos, cujos objetivos e ações desenvolvidas estão descritas na tabela 1. Os resultados do projeto foram apresentados na Feira de Ciências realizada no Colégio. Tabela 1: Momentos, objetivos e ações desenvolvidas no projeto Doping no esporte MOMENTO OBJETIVOS AÇÕES DESENVOLVIDAS Construir o conceito de doping e de doping genético. - Construir o conceito de doping sanguíneo. - Consolidar o conceito de doping sanguíneo. - Conhecer as principais classes de substâncias químicas proibidas. - Discutir a intencionalidade do doping. - Conhecer os exames legais antidoping. - Construir conceitos relativos a análises químicas. - Simular um laboratório antidoping - Simular uma comissão jurídica de esportes - Leitura e discussão de três reportagens recentes sobre doping; - Revisão de conceitos básicos sobre células animais e DNA apresentados em slides; - Atividade prática de extração de DNA humano. - Estudo do mecanismo de transporte do oxigênio até todas as células do organismo. - Equilíbrio químico hemoglobinaoxiemoglobina. - Leitura e discussão de um texto sobre doping sanguíneo; - Exibição de um vídeo, divulgado pela BBC Brasil, que aborda essa forma de doping. - Apresentação em PowerPoint sobre classes de substâncias, tais como hormônios, diuréticos, estimulantes e analgésicos, proibidas na perspectiva do doping. - Realização de pesquisa, pelos alunos, sobre medicamentos de uso comum que possuem substâncias ilegais na perspectiva do doping. - Apresentação aos alunos dos processos de coleta de amostras para o exame antidoping. - Apresentação de conceitos utilizados em análises como amostra, branco, controle e ensaio preliminar e específico. - Realização de análises químicas qualitativas de algumas amostras de urina artificial de supostos atletas. - Elaboração de relatório conclusivo sobre o julgamento dos supostos atletas. 4
5 DISCUSSÃO DAS AÇÕES DESENVOLVIDAS E DOS RESULTADOS No Momento 1, os estudantes leram três reportagens sobre doping, que podem ser encontradas nos endereços eletrônicos citados ao final das referências. A primeira foi sobre o lutador de UFC Chael Sonnen flagrado com anastrozol e clomifeno em um teste surpresa realizado pela Comissão Atlética de Nevada (NSAC). O anastrozol é usado normalmente para o tratamento de câncer de mama, enquanto o clomifeno costuma ser utilizado para casos de infertilidade feminina. Sonnen já tinha sido diagnosticado com hipogonadismo e fazia terapia de reposição de testosterona (TRT), antes de o tratamento ser considerado um método ilícito pela NSAC. Em agosto de 2010, Chael Sonnen foi flagrado com índices elevados de testosterona e a NSAC o suspendeu por um ano. A segunda reportagem versou sobre as acusações de possíveis casos de doping entre nadadores da China e dos Estados Unidos nos Jogos Olímpicos de Pequim. Os alvos eram a nadadora chinesa Ye Shiwen, que surpreendeu a todos por sua grande atuação na prova dos 400 m medley, na qual bateu o recorde mundial, e o americano Michael Phelps, que quebrou sete recordes. A terceira reportagem tratou de alguns casos curiosos de doping 'acidental'. A partir da leitura dessas reportagens, os alunos foram instigados a elaborar um conceito de doping para, então, estudar as suas modalidades. Preparando os alunos para a compreensão do doping genético, foi realizado, ainda neste encontro, um breve estudo das células animais e dos seus ácidos nucléicos (DNA, principalmente), o que contou com uma atividade prática de extração dos DNA s dos próprios alunos. A atividade prática de extração de DNA humano consistiu em fazer um bochecho, durante um minuto, com uma solução aquosa de cloreto de sódio. A solução do bochecho foi transferida para um béquer, no qual se adicionou gotas de detergente. Com o auxílio de um bastão de vidro, a mistura foi homogeneizada sem formação de espuma e, em seguida, verteu-se lentamente uma porção de etanol, no qual se adicionou um corante, pelas paredes do béquer. Após cerca de cinco minutos, foi possível observar uma massa branca fofa, o agregado do DNA com diversas proteínas. O doping genético é caracterizado pela inserção, no material celular de um atleta, de um gene que induz a produção de proteínas ou outras moléculas de interesse da indústria do doping. No momento 2, o doping sanguíneo foi abordado com base no mecanismo de transporte do oxigênio pela hemoglobina (Hem) ao se converter em oxiemoglobina (HemO 2 ), representado pela equação química a seguir: 5
6 Hem (aq) + O 2 (g) HemO 2 (aq) H < 0 Com os alunos cientes do Princípio de Le Chatelier, foi provocada a elaboração de estratégias eficazes para aumentar a circulação de oxigênio no organismo, ou seja, aumentar a concentração de oxiemoglobina no sangue. O doping sanguíneo envolve guardar e injetar o próprio sangue (doping autólogo) ou o sangue de outras pessoas (doping homólogo) ou animais (doping heterólogo) antes de treinamentos ou competições com o objetivo de aumentar o número de glóbulos vermelhos em circulação pelo corpo, como bem esclarece o vídeo da BBC Brasil Londres 2012: entenda o que é o doping sanguíneo que também foi exibido para os estudantes no Momento 3. No momento 3, foi lida a reportagem em que um perito apontava suspeitas de doping sanguíneo ao analisar o padrão invulgar dos valores sanguíneos do ciclista norteamericano Lance Armstrong durante a Volta à França. As percentagens de glóbulos vermelhos e de hemoglobina deveriam diminuir no decorrer da prova devido ao exercício intenso, mas elas permaneceram praticamente constantes. Assim, com a exibição do vídeo e com a leitura do texto, alguns aspectos do doping sanguíneo puderam ser abordados, como os tipos de doping sanguíneo, os perigos da sua prática e as formas de detectá-lo. Os Momentos 4 e 5 se complementaram através das investigações, em sites, solicitadas pelo professor aos estudantes sobre medicamentos de uso comum, que possuem substâncias ilegais na perspectiva do doping, indicando suas fórmulas, os grupos a que pertencem e seus efeitos no organismo. Neste ponto, julgamos interessante levar os estudantes a reconhecer que nem sempre o doping é um ato intencional. A apresentação aos alunos dos processos de coleta de amostras para o exame antidoping (Momento 6) foi feita consultando cartilhas tipo as normalmente distribuídas para os atletas (TIME BRASIL, 2011). No Momento 8, após definir, no Momento 7, conceitos como amostra, branco, controle e ensaio preliminar e específico, corriqueiros em ambientes de análises biológica e química, cada um dos estudantes recebeu um kit representativo de um atleta anônimo, composto por um pissete e por um béquer contendo urina artificial. O pissete podia conter (ou não) etanol ( CH 2 OH) e foi utilizado para reproduzir um teste respiratório - teste do bafômetro - caracterizado pela oxidação do álcool a aldeído pelo dicromato de potássio (K 2 Cr 2 O 7 ), em meio sulfúrico (H 2 SO 4 ), o que é facilmente 6
7 evidenciado pela mudança de coloração da solução de laranja para verde. A reação entre solução de dicromato de potássio e etanol, em meio ácido, é representada pela equação abaixo: K 2 Cr 2 O 7(aq) + 4 H 2 SO 4(aq) + 3 CH 2 OH (aq) 3 CHO (aq) + K 2 SO 4(aq) + Cr 2 (SO 4 ) 3(aq) + 7H 2 O (l) A urina artificial dos supostos atletas consistiu de uma solução insaturada de ureia. Sua análise química foi feita em três passos: observação de aspectos físicoquímicos (coloração da urina e ph), realização de testes preliminares e de testes específicos, onde, desses três, o único que permite a confirmação da presença de uma espécie química na amostra é o ensaio específico. A urina artificial dos supostos atletas poderiam conter, além de ureia e água, cloreto de sódio e até duas substâncias acusadoras de doping, provenientes de medicamentos de uso comum. A precipitação com nitrato de prata foi utilizada para verificar o teor de sais na urina. Desta forma, se a amostra de urina analisada apresentasse maior precipitação de cloreto de prata do que o controle, havia indícios que levariam a suspeitar que o atleta estava, no instante do exame, sob efeito de diuréticos. As duas substâncias acusadoras de doping utilizadas foram o isometepteno (encontrado na Neosaldina ) e a pseudoefedrina (encontrada no Tylenol Sinus ) cujas estruturas seguem representadas abaixo: H 3 C OH HN HN Isometepteno Pseudoefedrina As duas substâncias foram identificadas na urina artificial principalmente pelos ensaios preliminares e específicos, uma vez que as observações físico-químicas não foram conclusivas. Entretanto, para fins didáticos, se insistiu que os alunos descrevessem suas respectivas amostras com anotações sobre a coloração e o ph dos sistemas. As amostras eram incolores e os ph s oscilaram no intervalo considerado normal para a urina humana entre 5,0 e 7,0, mesmo com os medicamentos dissolvidos. Como ensaio preliminar, foi utilizado o teste de Bayer, um teste que, apesar de ser pouco seletivo, respondendo positivamente na presença de qualquer redutor, é 7
8 descrito, a princípio, como o descoramento da solução violeta de permanganato de potássio (KMnO 4 ) por ligações duplas ou triplas, com formação de um precipitado marrom de dióxido de manganês (MnO 2 ). Assim, o ensaio preliminar foi positivo para os dois medicamentos, visto que as duas substâncias possuem grupamentos redutores - no isometepteno, uma insaturação, e, na pseudoefedrina, uma hidroxila. As estruturas dos produtos da oxidação do isometepteno e da pseudoefedrina estão representadas abaixo: OH O H 3 C H 3 C OH HN HN Produto do isometepteno Produto da pseudoefedrina O teste com água de bromo, um ensaio específico utilizado para indicar a presença de insaturação em compostos orgânicos, foi proposto para identificação do isometepteno na urina artificial. Se, ao gotejar água de bromo (de coloração amarelo alaranjado) à solução que se deseja testar, ocorrer o descoramento da solução de bromo (a solução passa a incolor), isto é um indicativo que o composto possui insaturação C-C, dupla ou tripla. O isometepteno dá teste positivo para bromo e a pseudoefedrina, negativo. Assim, se o teste de bromo deu positivo para uma amostra de urina artificial, está confirmado que o atleta fez uso de um medicamento proibido, a Neosaldina. Segue abaixo a estrutura do produto formado pela adição de bromo à dupla ligação da molécula do isometepteno: Br H 3 C H 3 C Br HN Isometepteno após a bromação Para identificar a pseudoefedrina em solução aquosa, as interações das possíveis substâncias com a molécula de iodo. Assim, durante a análise, os tubos de ensaio da amostra, do branco e do controle receberam, cada um, um grão de iodo sólido e foram aquecidos até que a mistura entrasse em ebulição. A presença ou não da pseudoefedrina seria constatada a partir de um teste colorimétrico, com a análise da cor da mistura imediatamente após o aquecimento e cerca de quinze minutos depois. 8
9 A urina artificial (solução de ureia), ao interagir com iodo, promove o aparecimento de uma coloração castanho amarelada, típica de soluções aquosas ou alcoólicas de iodo, devido a formação de complexos de tranferência de carga entre os átomos de oxigênio e o iodo. O mesmo ocorre para a amostra de urina que contém apenas pseudoefedrina. Todavia, nas amostras que continham apenas isometepteno, as interações dessa substância com o iodo levavam ao aparecimento de uma coloração rosada e, nas amostras que continham pseudoefedrina com isometepteno, a cor observada de imediato era o rosa e, esperados os quinze minutos, era o amarelo. A partir das análises químicas de cinco amostras de urina artificial (contidas nos béqueres) e do conteúdo dos pissetes (bafômetro), os estudantes isoladamente chegaram a conclusões a respeito de possíveis casos de doping e elaboraram seus relatórios individuais. No último encontro (Momento 9), simulando uma comissão jurídica de esporte, os estudantes reunidos discutiram e emitiram os julgamentos dos supostos atletas. A tabela 2 exibe a composição das cinco amostras estudadas, que correspondem a cinco atletas da mesma modalidade esportiva, e os resultados obtidos nas análises, onde cada aluno teriam realizado o teste anti-doping para um atleta. Tabela 2: Amostras estudadas e suas análises ATLETA AMOSTRA RESULTADO DAS ANÁLISES Teste do Teste para Teste para Teste para bafômetro diuréticos pseudoefedrina isometepteno 1 A Positivo Positivo Positivo Positivo 2 B Positivo Positivo Negativo Negativo 3 C Negativo Positivo Positivo Negativo 4 D Negativo Negativo Negativo Negativo 5 E Negativo Positivo Positivo Positivo As composição das amostras A, B, C, D e E são as descritas a seguir. AMOSTRA A: Béquer: concentração de cloreto de sódio maior do que no controle, pseudoefedrina e isometepteno. Pissete: etanol e água. AMOSTRA B: Béquer: concentração de cloreto de sódio maior do que no controle; Pissete: etanol e água. 9
10 AMOSTRA C: Béquer: concentração de cloreto de sódio igual a do controle e pseudoefedrina; Pissete: água. AMOSTRA D: Béquer: concentração de cloreto de sódio menor do que no controle; Pissete: água. AMOSTRA E: Béquer: concentração de cloreto de sódio maior do que no controle, pseudoefedrina e isometepteno; Pissete: água. No julgamento, foi combinado que, para cada doping detectado, o atleta seria punido com um ano de afastamento da modalidade esportiva. Essa medida punitiva não corresponde, necessariamente, à realidade, mas teve um fim meramente didático. Assim, baseado no relatório da análise feita para o Atleta 3, o mesmo foi punido (injustamente) com dois anos de afastamento, quando, na verdade, deveria sofrer com apenas um. Esse inconveniente deu abertura para que a importância do químico analista e a seriedade do seu trabalho fossem discutidas, levando, também, à reflexão de algumas atitudes éticas e morais. No dia da Feira do Conhecimento, os alunos apresentaram o tema doping com cartazes e algumas experiências. CONSIDERAÇÕES FINAIS Na Feira de Ciências realizada no Colégio os estudantes expuseram cartazes com descrições breves com os seguintes itens: O que é doping? ; Doping genético; Doping sanguíneo; Substâncias proibidas ou de uso restrito; dentre outros. Os experimentos realizados foram exibidos em uma bancada com suas explicações dadas através de slides, expostos em um notebook. Consideramos que o projeto interdisciplinar Doping no esporte favoreceu o protagonismo dos estudantes, a aquisisão de conceitos e procedimentos, além de promover discussões sobre aspectos éticos e sociais na prática de esportes. AGRADECIMENTOS A Capes pela ajuda financeira e a concessão de bolsas Pibid. 10
11 REFERÊNCIAS BRASIL. Ministério da Educação. Secretaria de Educação Básica. Secretaria de Educação Continuada, Alfabetização, Diversidade e Inclusão. Conselho Nacional da Educação. Diretrizes Curriculares Nacionais Gerais da Educação Básica. Brasília: MEC, SEB, DICEI, Disponível em: mid=1152. Acessado em 09 de outubro de MARTINS, Jorge Santos. Projetos de Pesquisa: estratégias de ensino e aprendizagem em sala de aula. 2. ed. Campinas: Armazém do Ipê, PEREIRA, Henrique Marcelo G.; PADILHA, Monica C.; AQUINO NETO, Francisco Radler de. A química e o controle de dopagem no esporte. São Paulo: Sociedade Brasileira de Química, Coleção Química no cotidiano, v. 3. TIME BRASIL. Informações sobre o uso de medicamentos no esporte ed. Rio de Janeiro, Março Disponível em: Acessado em 09 de outubro de ENDEREÇOS ELETRÔNICOS CONSULTADOS (na ordem em que foram empregados no texto) Acessado em 19 de junho de Acessado em 19 de junho de Acessado em 19 de junho de Acessado em 19 de junho de guineo_olimpiada_rw.shtml. Acessado em 19 de junho de BR.pdf. Acessado em 19 de junho de Acessado em 19 de junho de Acessado em 19 de junho de
DOPING NO ESPORTE O PROJETO INTERDISCIPLINAR
 O PROJETO INTERDISCIPLINAR DOPING NO ESPORTE Patrick Andersson Barreto Frasão 1, Henry Porto Vieira de Assis 1, Maria de Fátima Teixeira Gomes 2 e Denise Gutman Almada 3 1 Licenciatura em Química, Instituto
O PROJETO INTERDISCIPLINAR DOPING NO ESPORTE Patrick Andersson Barreto Frasão 1, Henry Porto Vieira de Assis 1, Maria de Fátima Teixeira Gomes 2 e Denise Gutman Almada 3 1 Licenciatura em Química, Instituto
Colégio Estadual Professor Ernesto Faria Feira de Ciências. A Química do doping
 Colégio Estadual Professor Ernesto Faria Feira de Ciências A Química do doping Dados sobre o projeto Tema: A Química do doping; Responsáveis: Denise Gutman (Supervisora); Patrick Andersson e Henry de Assis
Colégio Estadual Professor Ernesto Faria Feira de Ciências A Química do doping Dados sobre o projeto Tema: A Química do doping; Responsáveis: Denise Gutman (Supervisora); Patrick Andersson e Henry de Assis
QUÍMICA. Química Orgânica. Tipos de Reações Orgânicas: Oxidação, Redução e Polimerização. Prof. Giselle Blois
 QUÍMICA Química Orgânica Tipos de Reações Orgânicas: Prof. Giselle Blois REAÇÕES DE OXIDAÇÃO São reações nas quais ocorre adição de oxigênio na molécula orgânica ou há liberação de hidrogênio na mesma.
QUÍMICA Química Orgânica Tipos de Reações Orgânicas: Prof. Giselle Blois REAÇÕES DE OXIDAÇÃO São reações nas quais ocorre adição de oxigênio na molécula orgânica ou há liberação de hidrogênio na mesma.
Polimerização e Reações Orgânicas
 Polimerização e Reações Orgânicas Material de Apoio para Monitoria 1. (FATEC-SP) A polimerização por adição consiste na reação entre moléculas de uma mesma substância, na qual em sua estrutura, ocorre
Polimerização e Reações Orgânicas Material de Apoio para Monitoria 1. (FATEC-SP) A polimerização por adição consiste na reação entre moléculas de uma mesma substância, na qual em sua estrutura, ocorre
GRUPO 15 NITROGÊNIO E SEUS COMPOSTOS
 GRUPO 15 NITROGÊNIO E SEUS COMPOSTOS O nitrogênio é um gás, sendo o principal componente da nossa atmosfera com cerca de 78% em massa do ar atmosférico. O elemento é também dotado de uma alta energia de
GRUPO 15 NITROGÊNIO E SEUS COMPOSTOS O nitrogênio é um gás, sendo o principal componente da nossa atmosfera com cerca de 78% em massa do ar atmosférico. O elemento é também dotado de uma alta energia de
RELATÓRIO DE EXPERIMENTO Equilíbrio químico
 UNIVERSIDADE FEDERAL DO VALE DO SÃO FRANCISCO CURSO DE ENGENHARIA DA COMPUTAÇÃO DISCIPLINA: QUÍMICA GERAL PROFESSORA: FERNANDA SANTOS CARVALHO DOS ANJOS RELATÓRIO DE EXPERIMENTO Equilíbrio químico Aluno:
UNIVERSIDADE FEDERAL DO VALE DO SÃO FRANCISCO CURSO DE ENGENHARIA DA COMPUTAÇÃO DISCIPLINA: QUÍMICA GERAL PROFESSORA: FERNANDA SANTOS CARVALHO DOS ANJOS RELATÓRIO DE EXPERIMENTO Equilíbrio químico Aluno:
Química. A) 645 kj/mol B) 0 kj/mol C) 645 kj/mol D) 945 kj/mol E) 1125 kj/mol 37.
 Química 7. Dados: Entalpia de ligação H H = 45 kj/mol N H = 9 kj/mol A reação de síntese da amônia, processo industrial de grande relevância para a indústria de fertilizantes e de explosivos, é representada
Química 7. Dados: Entalpia de ligação H H = 45 kj/mol N H = 9 kj/mol A reação de síntese da amônia, processo industrial de grande relevância para a indústria de fertilizantes e de explosivos, é representada
Uma Abordagem Diferenciada para o Ensino de Funções Orgânicas através da Temática Medicamentos
 S u b p r o j e t o d e Q u í m i c a Uma Abordagem Diferenciada para o Ensino de Funções Orgânicas através da Temática Medicamentos Revista Química Nova na Escola, vol. 34, Nº 1, p. 21-25, fev., 2012
S u b p r o j e t o d e Q u í m i c a Uma Abordagem Diferenciada para o Ensino de Funções Orgânicas através da Temática Medicamentos Revista Química Nova na Escola, vol. 34, Nº 1, p. 21-25, fev., 2012
Observe o gráfico, cujas curvas representam as variações das massas desses radioisótopos ao longo das duas horas de duração do experimento.
 Revisão Específicas 1. (UERJ 2015) Os preços dos metais para reciclagem variam em função da resistência de cada um à corrosão: quanto menor a tendência do metal à oxidação, maior será o preço. Na tabela,
Revisão Específicas 1. (UERJ 2015) Os preços dos metais para reciclagem variam em função da resistência de cada um à corrosão: quanto menor a tendência do metal à oxidação, maior será o preço. Na tabela,
Experimento 1: Efeito do íon comum equilíbrio de ionização da amônia
 Experimento Deslocamento de equilíbrios químicos (Princípio de Le Chatelier) Objetivo: Estudar e compreender alguns fatores que deslocam equilíbrios químicos. Experimento 1: Efeito do íon comum equilíbrio
Experimento Deslocamento de equilíbrios químicos (Princípio de Le Chatelier) Objetivo: Estudar e compreender alguns fatores que deslocam equilíbrios químicos. Experimento 1: Efeito do íon comum equilíbrio
DOPING. Francisco Pinto
 DOPING Francisco Pinto DEFINIÇÃO Administração ou uso por parte de qualquer atleta de qualquer substância fisiológica tomada em quantidade anormal ou por via anormal sendo a única intenção a de aumentar
DOPING Francisco Pinto DEFINIÇÃO Administração ou uso por parte de qualquer atleta de qualquer substância fisiológica tomada em quantidade anormal ou por via anormal sendo a única intenção a de aumentar
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
QUÍMICA PRIMEIRA ETAPA - 1999 QUESTÃO 46 Um limão foi espremido num copo contendo água e as sementes ficaram no fundo do recipiente. A seguir, foi adicionado ao sistema um pouco de açúcar, que se dissolveu
3016 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4
 6 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4 CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Classificação
6 Oxidação do ácido ricinoléico a ácido azeláico (a partir de óleo de rícino) com KMnO 4 CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Classificação
2 NH 3 (g) + CO 2 (g)
 PROCESSO SELETIVO 2007 1 O DIA GABARITO 4 7 QUÍMICA QUESTÕES DE 16 A 30 16. O equilíbrio de ionização da água pura é dado pela equação abaixo, cuja constante do produto iônico é 2,5x10-14, a 37 o C. H
PROCESSO SELETIVO 2007 1 O DIA GABARITO 4 7 QUÍMICA QUESTÕES DE 16 A 30 16. O equilíbrio de ionização da água pura é dado pela equação abaixo, cuja constante do produto iônico é 2,5x10-14, a 37 o C. H
16. Em soluções aquosas o ânion dicromato está em equilíbrio dinâmico com o ânion cromato, segundo a reação representada por:
 PROCESSO SELETIVO 2007 1 O DIA GABARITO 2 7 QUÍMICA QUESTÕES DE 16 A 30 16. Em soluções aquosas o ânion dicromato está em equilíbrio dinâmico com o ânion cromato, segundo a reação representada por: Cr
PROCESSO SELETIVO 2007 1 O DIA GABARITO 2 7 QUÍMICA QUESTÕES DE 16 A 30 16. Em soluções aquosas o ânion dicromato está em equilíbrio dinâmico com o ânion cromato, segundo a reação representada por: Cr
2 KClO 3 2 KCl + 3 O 2
 PROCESSO SELETIVO 2007 1 O DIA GABARITO 1 7 QUÍMICA QUESTÕES DE 16 A 30 16. O ânion cloreto (Cl - ), o argônio (Ar) e o cátion potássio (K + ) têm em comum o mesmo número: a) de prótons. b) de elétrons.
PROCESSO SELETIVO 2007 1 O DIA GABARITO 1 7 QUÍMICA QUESTÕES DE 16 A 30 16. O ânion cloreto (Cl - ), o argônio (Ar) e o cátion potássio (K + ) têm em comum o mesmo número: a) de prótons. b) de elétrons.
CH 3. ) tem massa molecular e ponto de ebulição comparáveis ao do n-pentano (C 5 H 12
 QUÍMICA Questão 01 O éter dietílico (CH 3 CH 2 OCH 2 CH 3 ) tem massa molecular e ponto de ebulição comparáveis ao do n-pentano (C 5 H 12 ). O éter, em contraste, apresenta solubilidade em água à temperatura
QUÍMICA Questão 01 O éter dietílico (CH 3 CH 2 OCH 2 CH 3 ) tem massa molecular e ponto de ebulição comparáveis ao do n-pentano (C 5 H 12 ). O éter, em contraste, apresenta solubilidade em água à temperatura
Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula.
 Aula 01 Composição química de uma célula O que é uma célula? Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula. Toda célula possui a capacidade de crescer,
Aula 01 Composição química de uma célula O que é uma célula? Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula. Toda célula possui a capacidade de crescer,
BC-1302 QUÍMICA DOS ELEMENTOS
 PRÁTICA 5: Oxigênio e Enxofre Objetivos Preparar o gás oxigênio, por método laboratorial e estudar algumas de suas propriedades. Estudar o enxofre nas suas variações alotrópicas e algumas de suas reações.
PRÁTICA 5: Oxigênio e Enxofre Objetivos Preparar o gás oxigênio, por método laboratorial e estudar algumas de suas propriedades. Estudar o enxofre nas suas variações alotrópicas e algumas de suas reações.
CRONOGRAMA DE RECUPERAÇÃO ATIVIDADE DE RECUPERAÇÃO
 CRONOGRAMA DE RECUPERAÇÃO SÉRIE: 2ª série do EM DISCIPLINA: QUÍMICA 1 Caderno Número(s) da(s) Assuntos aula(s) 06 15, 16 e 17 Misturas de soluções com reação e titulação. 06 18 e 19 Termoquímica 07 28
CRONOGRAMA DE RECUPERAÇÃO SÉRIE: 2ª série do EM DISCIPLINA: QUÍMICA 1 Caderno Número(s) da(s) Assuntos aula(s) 06 15, 16 e 17 Misturas de soluções com reação e titulação. 06 18 e 19 Termoquímica 07 28
INTERVENÇÃO. EXTRAÇÃO DO DNA DO MORANGO (Fragaria ananassa). PLANO DE INTERVENÇÃO
 INTERVENÇÃO EXTRAÇÃO DO DNA DO MORANGO (Fragaria ananassa). Autor: Lucas Fagundes de Souza PLANO DE INTERVENÇÃO CONTEXTUALIZAÇÃO A constituição química e a localização dos componentes celulares podem ser
INTERVENÇÃO EXTRAÇÃO DO DNA DO MORANGO (Fragaria ananassa). Autor: Lucas Fagundes de Souza PLANO DE INTERVENÇÃO CONTEXTUALIZAÇÃO A constituição química e a localização dos componentes celulares podem ser
Relatório de Prática de Ensino de Química
 Relatório de Prática de Ensino de Química Aluna: Renata Alves da Silva Disciplina: Química Geral (QFL0605) Docentes: Denise Freitas Siqueira Petri Ana Maria da Costa Ferreira Introdução Com o intuito de
Relatório de Prática de Ensino de Química Aluna: Renata Alves da Silva Disciplina: Química Geral (QFL0605) Docentes: Denise Freitas Siqueira Petri Ana Maria da Costa Ferreira Introdução Com o intuito de
Saber Escolar e Formação Docente na Educação Básica
 Saber Escolar e Formação Docente na Educação Básica Subprojeto de Química Coord. Prof.ª Fátima Gomes Escolas parceiras/ Equipe 2 C. E. Prof. Ernesto Faria Supervisora: Denise Gutman C. E. Prof. Herbert
Saber Escolar e Formação Docente na Educação Básica Subprojeto de Química Coord. Prof.ª Fátima Gomes Escolas parceiras/ Equipe 2 C. E. Prof. Ernesto Faria Supervisora: Denise Gutman C. E. Prof. Herbert
Escola Secundária de Alcácer do Sal Química 12º ano teste 5 25/05/2004
 Escola Secundária de Alcácer do Sal Química 12º ano teste 5 25/05/2004 I Escreva na sua folha de respostas a letra correspondente à alternativa correcta que seleccionar para cada item. A indicação de mais
Escola Secundária de Alcácer do Sal Química 12º ano teste 5 25/05/2004 I Escreva na sua folha de respostas a letra correspondente à alternativa correcta que seleccionar para cada item. A indicação de mais
Reações de identificação dos cátions dos grupos 1 e 2
 Reações de identificação dos cátions dos grupos 1 e 2 Na, K e NH 4 São os maiores cátions do período que pertencem, possuem carga pequena e estrutura de gás nobre. O íon amônio está incluído porque apresenta
Reações de identificação dos cátions dos grupos 1 e 2 Na, K e NH 4 São os maiores cátions do período que pertencem, possuem carga pequena e estrutura de gás nobre. O íon amônio está incluído porque apresenta
PROVA DE QUÍMICA. Adaptada da Tabela Periódica da IUPAC/versão 2007 Acesso: PROVA DE QUÍMICA - Caderno 1
 PROVA DE QUÍMICA Adaptada da Tabela Periódica da IUPAC/versão 2007 Acesso: http://wwwiupacorg/reports/periodic_table/ 18 PROVA DE QUÍMICA - Caderno 1 QUESTÃO 25 1 Na extração do ouro, os garimpeiros costumam
PROVA DE QUÍMICA Adaptada da Tabela Periódica da IUPAC/versão 2007 Acesso: http://wwwiupacorg/reports/periodic_table/ 18 PROVA DE QUÍMICA - Caderno 1 QUESTÃO 25 1 Na extração do ouro, os garimpeiros costumam
Programa de Pós-Graduação
 Programa de Pós-Graduação Mestrado Profissional Tecnologia em Química e Bioquímica - IQ-USP Exame de Capacidade 1º Semestre 2016 PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA E BIOQUÍMICA Nome: Instruções:
Programa de Pós-Graduação Mestrado Profissional Tecnologia em Química e Bioquímica - IQ-USP Exame de Capacidade 1º Semestre 2016 PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA E BIOQUÍMICA Nome: Instruções:
O BAFÔMETRO COMO RECURSO FACILITADOR DO ENSINO DAS REAÇÕES DE OXI-REDUÇÃO E DA CONCIENTIZAÇÃO DOS DISCENTES
 O BAFÔMETRO COMO RECURSO FACILITADOR DO ENSINO DAS REAÇÕES DE OXI-REDUÇÃO E DA CONCIENTIZAÇÃO DOS DISCENTES Jaqueline dos Santos Fidelis; Círio Samuel Cardoso da Silva; Fabrícia Bezerra Vieira do Nascimento;
O BAFÔMETRO COMO RECURSO FACILITADOR DO ENSINO DAS REAÇÕES DE OXI-REDUÇÃO E DA CONCIENTIZAÇÃO DOS DISCENTES Jaqueline dos Santos Fidelis; Círio Samuel Cardoso da Silva; Fabrícia Bezerra Vieira do Nascimento;
ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
 Prova de Acesso de Química Maiores de 23 Anos Candidatura 2016-2017 14 de Junho de 2017 10h00 12h30 Nome CCnº ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
Prova de Acesso de Química Maiores de 23 Anos Candidatura 2016-2017 14 de Junho de 2017 10h00 12h30 Nome CCnº ATENÇÃO: assinale ou apresente cuidadosamente as respostas e apresente TODOS os cálculos efectuados.
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da
 Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
Experiência 10: Estudo do equilíbrio cromato-dicromato
 1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015/1 Experiência 10: Estudo do equilíbrio cromato-dicromato 1. Equilíbrio químico Muitas reações químicas são reversíveis,
1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015/1 Experiência 10: Estudo do equilíbrio cromato-dicromato 1. Equilíbrio químico Muitas reações químicas são reversíveis,
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
UNIVERSIDADE ESTADUAL DO PARANÁ UNESPAR PRÓ-REITORIA DE ENSINO DE GRADUAÇÃO PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID
 UNIVERSIDADE ESTADUAL DO PARANÁ UNESPAR PRÓ-REITORIA DE ENSINO DE GRADUAÇÃO PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID Plano/ Relatório de Atividades (PIBID/UNESPAR) Tipo do produto:
UNIVERSIDADE ESTADUAL DO PARANÁ UNESPAR PRÓ-REITORIA DE ENSINO DE GRADUAÇÃO PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID Plano/ Relatório de Atividades (PIBID/UNESPAR) Tipo do produto:
RELATÓRIO DE ATIVIDADES
 RELATÓRIO DE ATIVIDADES ESCOLA MUNICIPAL DE ENSINO FUNDAMENTAL CARLOTA VIEIRA DA CUNHA Coordenadores: Analía del Valle Garnero e Ronaldo Erichsen Supervisora: Maria Aparecida Lousada da Silva Bolsista
RELATÓRIO DE ATIVIDADES ESCOLA MUNICIPAL DE ENSINO FUNDAMENTAL CARLOTA VIEIRA DA CUNHA Coordenadores: Analía del Valle Garnero e Ronaldo Erichsen Supervisora: Maria Aparecida Lousada da Silva Bolsista
REAÇÕES QUÍMICAS REAGENTES E PRODUTOS DE REAÇÃO
 REAÇÕES QUÍMICAS Os materiais podem sofrer transformações químicas ou transformações físicas. As transformações químicas são aquelas em que ocorre a formação de novas substâncias com propriedades diferentes
REAÇÕES QUÍMICAS Os materiais podem sofrer transformações químicas ou transformações físicas. As transformações químicas são aquelas em que ocorre a formação de novas substâncias com propriedades diferentes
8ª LISTA - EXERCÍCIOS DE PROVAS Equilíbrio de Solubilidade
 Pg. 1/6 1 a Questão De acordo com as equações abaixo, a 25 ºC, faça o que se pede. BaF 2 (s) Ba 2+ (aq) + 2F - (aq) K ps (BaF 2 ) = 1,7 x 10-6 BaSO 4 (s) Ba 2+ (aq) + SO 2-4 (aq) K ps (BaSO 4 ) = 1,0 x
Pg. 1/6 1 a Questão De acordo com as equações abaixo, a 25 ºC, faça o que se pede. BaF 2 (s) Ba 2+ (aq) + 2F - (aq) K ps (BaF 2 ) = 1,7 x 10-6 BaSO 4 (s) Ba 2+ (aq) + SO 2-4 (aq) K ps (BaSO 4 ) = 1,0 x
Química Oxi-Redução Balanceamento de Equações Difícil [10 Questões]
![Química Oxi-Redução Balanceamento de Equações Difícil [10 Questões] Química Oxi-Redução Balanceamento de Equações Difícil [10 Questões]](/thumbs/55/36760464.jpg) Química Oxi-Redução Balanceamento de Equações Difícil [10 Questões] 01 - (UNIFESP SP) Substâncias orgânicas, quando despejadas em sistemas aquáticos, podem sofrer diferentes reações em função, principalmente,
Química Oxi-Redução Balanceamento de Equações Difícil [10 Questões] 01 - (UNIFESP SP) Substâncias orgânicas, quando despejadas em sistemas aquáticos, podem sofrer diferentes reações em função, principalmente,
QUÍMICA. Processo Seletivo/UNIFAL - julho ª Prova Comum TIPO 1 QUESTÃO 41 QUESTÃO 42
 QUÍMICA QUESTÃO 41 A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa de
QUÍMICA QUESTÃO 41 A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa de
BIOLOGIA. Moléculas, células e tecidos. A química da vida. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos A química da vida Professor: Alex Santos Tópicos em abordagem: A Química da Vida I Conceitos fundamentais; II Componentes químicos da célula; III Compostos inorgânicos;
BIOLOGIA Moléculas, células e tecidos A química da vida Professor: Alex Santos Tópicos em abordagem: A Química da Vida I Conceitos fundamentais; II Componentes químicos da célula; III Compostos inorgânicos;
O Zn ETENO H H 2 C CH 2 + O 2 O + O C
 62) O metanal, um composto orgânico, também é chamado de aldeído fórmico ou formaldeído. É um gás incolor, com cheiro muito forte e irritante. É muito solúvel em água e usado como solução aquosa, contendo
62) O metanal, um composto orgânico, também é chamado de aldeído fórmico ou formaldeído. É um gás incolor, com cheiro muito forte e irritante. É muito solúvel em água e usado como solução aquosa, contendo
Exercícios Equilíbrio Iônico
 Exercícios Equilíbrio Iônico 1. O ph tem uma importância significativa nos processos de laboratório, da indústria e dos organismos vivos. Ele pode ser avaliado de forma simples, usando-se substâncias chamadas
Exercícios Equilíbrio Iônico 1. O ph tem uma importância significativa nos processos de laboratório, da indústria e dos organismos vivos. Ele pode ser avaliado de forma simples, usando-se substâncias chamadas
QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim
 QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim (mcoutrim@iceb.ufop.br) REAÇÕES DE OXI REDUÇÃO / EQUAÇÃO DE NERNST Avaliação da espontaneidade da reação potencial da reação pelo potencial
QUI219 QUÍMICA ANALÍTICA (Farmácia) Prof. Mauricio X. Coutrim (mcoutrim@iceb.ufop.br) REAÇÕES DE OXI REDUÇÃO / EQUAÇÃO DE NERNST Avaliação da espontaneidade da reação potencial da reação pelo potencial
Compreender a constante de equilíbrio, sua expressão matemática e seu significado;
 AULA 8 Equilíbrio iônico em solução OBJETIVOS Compreender o conceito de estado de equilíbrio químico; Compreender a constante de equilíbrio, sua expressão matemática e seu significado; Empregar o Princípio
AULA 8 Equilíbrio iônico em solução OBJETIVOS Compreender o conceito de estado de equilíbrio químico; Compreender a constante de equilíbrio, sua expressão matemática e seu significado; Empregar o Princípio
O aluno deverá elaborar resumos teóricos dos textos do livro e de outras fontes sobre os tópicos do conteúdo.
 Disciplina QUÍMICA Curso ENSINO MÉDIO Professor GUILHERME Série 3ª SÉRIE ROTEIRO DE ESTUDOS DE RECUPERAÇÃO E REVISÃO 1º SEMESTRE / 2012 Aluno (a): Número: 1 - Conteúdo: Forças intermoleculares e geometria
Disciplina QUÍMICA Curso ENSINO MÉDIO Professor GUILHERME Série 3ª SÉRIE ROTEIRO DE ESTUDOS DE RECUPERAÇÃO E REVISÃO 1º SEMESTRE / 2012 Aluno (a): Número: 1 - Conteúdo: Forças intermoleculares e geometria
Edital Pibid n 11 /2012 CAPES PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID Plano de Atividades (PIBID/UNESPAR)
 Edital Pibid n 11 /2012 CAPES PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID Plano de Atividades (PIBID/UNESPAR) Tipo do produto: Plano de aula oficina. 1 IDENTIFICAÇÃO NOME DO SUBPROJETO:
Edital Pibid n 11 /2012 CAPES PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID Plano de Atividades (PIBID/UNESPAR) Tipo do produto: Plano de aula oficina. 1 IDENTIFICAÇÃO NOME DO SUBPROJETO:
Escola Secundária de Lagoa. Ficha de Trabalho 15. Física e Química A 11º Ano Paula Melo Silva. Escola Secundária de Lagoa Paula Melo Silva Página 1
 Escola Secundária de Lagoa Física e Química A 11º Ano Paula Melo Silva AL 1.1. Síntese do Ácido Acetilsalicílico. Objetivo geral: Realizar a síntese do ácido acetilsalicílico e determinar o rendimento.
Escola Secundária de Lagoa Física e Química A 11º Ano Paula Melo Silva AL 1.1. Síntese do Ácido Acetilsalicílico. Objetivo geral: Realizar a síntese do ácido acetilsalicílico e determinar o rendimento.
29/03/ TRANSFORMAÇÕES QUÍMICAS PROVA 1 GABARITO - prova tipo A
 29/03/2016 - TRANSFORMAÇÕES QUÍMICAS PROVA 1 GABARITO - prova tipo A Texto para as questões 1 a 10: O permanganato de potássio (KMnO 4 ) é um forte agente oxidante. Em laboratório, pode ser empregado para
29/03/2016 - TRANSFORMAÇÕES QUÍMICAS PROVA 1 GABARITO - prova tipo A Texto para as questões 1 a 10: O permanganato de potássio (KMnO 4 ) é um forte agente oxidante. Em laboratório, pode ser empregado para
ANÁLISE DE MANGANÊS NA PIROLUSITA
 Fase Condensada: matéria em estado líquido ou sólido ANÁLISE DE MANGANÊS NA PIROLUSITA OBJETIVO: Determinar o teor de dióxido de manganês (MnO 2 ) em uma amostra de pirolusita, minério de manganês Impurezas:
Fase Condensada: matéria em estado líquido ou sólido ANÁLISE DE MANGANÊS NA PIROLUSITA OBJETIVO: Determinar o teor de dióxido de manganês (MnO 2 ) em uma amostra de pirolusita, minério de manganês Impurezas:
BIOQUÍMICA CELULAR. Ramo das ciências naturais que estuda a química da vida. Prof. Adaianne L. Teixeira
 BIOQUÍMICA CELULAR Ramo das ciências naturais que estuda a química da vida Prof. Adaianne L. Teixeira Principais elementos químicos dos seres vivos CARBONO (C) (Essencial) HIDROGÊNIO (H) OXIGÊNIO (O) NITROGÊNIO
BIOQUÍMICA CELULAR Ramo das ciências naturais que estuda a química da vida Prof. Adaianne L. Teixeira Principais elementos químicos dos seres vivos CARBONO (C) (Essencial) HIDROGÊNIO (H) OXIGÊNIO (O) NITROGÊNIO
LISTA DE EXERCÍCIOS DE RECUPERAÇÃO FINAL QUÍMICA
 LISTA DE EXERCÍCIOS DE RECUPERAÇÃO FINAL QUÍMICA ALUNO(a): Valor: Nº: SÉRIE: 2ª TURMA: 20,0 UNIDADE: VV JC JP PC DATA: / /2018 Obs.: Esta lista deve ser entregue resolvida no dia da prova de Recuperação.
LISTA DE EXERCÍCIOS DE RECUPERAÇÃO FINAL QUÍMICA ALUNO(a): Valor: Nº: SÉRIE: 2ª TURMA: 20,0 UNIDADE: VV JC JP PC DATA: / /2018 Obs.: Esta lista deve ser entregue resolvida no dia da prova de Recuperação.
XVIII MARATONA CEARENSE DE QUÍMICA. 8 O Ano. Experiência. Recicláveis Desunidos
 8 O Ano Experiência Recicláveis Desunidos Material: 1. Frasco de vidro com tampa 2. 100mL de Água destilada 3. 100mL de Álcool isopropílico 4.Anéis de plástico de tampas de refrigerantes de cores variadas
8 O Ano Experiência Recicláveis Desunidos Material: 1. Frasco de vidro com tampa 2. 100mL de Água destilada 3. 100mL de Álcool isopropílico 4.Anéis de plástico de tampas de refrigerantes de cores variadas
ALQ1.3 - Efeito da variação de temperatura e da variação de concentração na progressão global de uma reação
 ALQ1.3 - Efeito da variação de temperatura e da variação de concentração na progressão global de uma reação A situação de equilíbrio de um sistema químico pode alterar-se quando lhe provocamos uma perturbação:
ALQ1.3 - Efeito da variação de temperatura e da variação de concentração na progressão global de uma reação A situação de equilíbrio de um sistema químico pode alterar-se quando lhe provocamos uma perturbação:
2º dia. 5 O verso da capa e as páginas em branco deste Caderno servirão para rascunho.
 2º dia 1 Na parte inferior desta capa, preencha todos os espaços destinados à sua identificação. Se, em qualquer outro local deste Caderno, você assinar, rubricar, escrever mensagem, etc., será automaticamente
2º dia 1 Na parte inferior desta capa, preencha todos os espaços destinados à sua identificação. Se, em qualquer outro local deste Caderno, você assinar, rubricar, escrever mensagem, etc., será automaticamente
Quí. Quí. Monitor: Rodrigo Pova
 Quí. Professor: Allan Rodrigues Monitor: Rodrigo Pova Eletroquímica 07 nov EXERCÍCIOS DE AULA 1. Texto I Biocélulas combustíveis são uma alternativa tecnológica para substituição das baterias convencionais.
Quí. Professor: Allan Rodrigues Monitor: Rodrigo Pova Eletroquímica 07 nov EXERCÍCIOS DE AULA 1. Texto I Biocélulas combustíveis são uma alternativa tecnológica para substituição das baterias convencionais.
Composição química da célula
 Composição química da célula Introdução Evidência da evolução Todas as formas de vida tem a mesma composição química! Substâncias inorgânicas Substâncias orgânicas Água e sais minerais Carboidratos, lipídios,
Composição química da célula Introdução Evidência da evolução Todas as formas de vida tem a mesma composição química! Substâncias inorgânicas Substâncias orgânicas Água e sais minerais Carboidratos, lipídios,
ANEXO II EDITAL Nº 80/2013/PIBID/UFG PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID
 ANEXO II EDITAL Nº 80/2013/PIBID/UFG PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID FORMULÁRIO DE DETALHAMENTO DO SUBPROJETO POR ÁREA DE CONHECIMENTO 1. Nome da Instituição: 2. UF Universidade
ANEXO II EDITAL Nº 80/2013/PIBID/UFG PROGRAMA INSTITUCIONAL DE BOLSA DE INICIAÇÃO À DOCÊNCIA - PIBID FORMULÁRIO DE DETALHAMENTO DO SUBPROJETO POR ÁREA DE CONHECIMENTO 1. Nome da Instituição: 2. UF Universidade
Equilíbrio Heterogéneo
 Equilíbrio Heterogéneo Aulas 7 Equilíbrio Heterogéneo: Produto de Solubilidade Efeito do ião comum, ph e iões complexos Titulações de precipitação Equilíbrio Heterogéneo Um equilíbrio heterogéneo (sólido-líquido)
Equilíbrio Heterogéneo Aulas 7 Equilíbrio Heterogéneo: Produto de Solubilidade Efeito do ião comum, ph e iões complexos Titulações de precipitação Equilíbrio Heterogéneo Um equilíbrio heterogéneo (sólido-líquido)
Equipe de Química QUÍMICA
 Aluno (a): Série: 3ª Turma: TUTORIAL 12R Ensino Médio Equipe de Química Data: QUÍMICA Mistura de soluções que não reagem entre si: Misturas de soluções de mesmo soluto quando misturamos soluções de mesmo
Aluno (a): Série: 3ª Turma: TUTORIAL 12R Ensino Médio Equipe de Química Data: QUÍMICA Mistura de soluções que não reagem entre si: Misturas de soluções de mesmo soluto quando misturamos soluções de mesmo
Índice. 4 o Relatório de Química Orgânica realizado por Marta Carvalho e Mafalda Gonçalves. Resumo 1. Procedimento Experimental 1.
 4 o Relatório de Química Orgânica realizado por Marta Carvalho e Mafalda Gonçalves Índice Resumo 1 Procedimento Experimental 1 Resultados 4 Discussão de Resultados 5 Resposta às questões adicionais 6 Conclusão
4 o Relatório de Química Orgânica realizado por Marta Carvalho e Mafalda Gonçalves Índice Resumo 1 Procedimento Experimental 1 Resultados 4 Discussão de Resultados 5 Resposta às questões adicionais 6 Conclusão
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO
 UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
11. O uso de pérolas ou pedaços de vidro ou ainda de cerâmica porosa no aquecimento de soluções tem por objetivo:
 ASSISTENTE DE LABORATÓRIO 4 CONHECIMENTOS ESPECÍFICOS QUESTÕES DE 11 A 25 11. O uso de pérolas ou pedaços de vidro ou ainda de cerâmica porosa no aquecimento de soluções tem por objetivo: a) Acelerar a
ASSISTENTE DE LABORATÓRIO 4 CONHECIMENTOS ESPECÍFICOS QUESTÕES DE 11 A 25 11. O uso de pérolas ou pedaços de vidro ou ainda de cerâmica porosa no aquecimento de soluções tem por objetivo: a) Acelerar a
PLURALIDADE CULTURAL: DIVERSIDADE E CIDADANIA RELATO DE EXPERIÊNCIA
 PLURALIDADE CULTURAL: DIVERSIDADE E CIDADANIA RELATO DE EXPERIÊNCIA Introdução BENÍCIO, Débora Regina Fernandes 1 UEPB Campus III debora_rfb@yahoo.com.br O PIBID (Programa Institucional de Bolsas de Iniciação
PLURALIDADE CULTURAL: DIVERSIDADE E CIDADANIA RELATO DE EXPERIÊNCIA Introdução BENÍCIO, Débora Regina Fernandes 1 UEPB Campus III debora_rfb@yahoo.com.br O PIBID (Programa Institucional de Bolsas de Iniciação
1ª Parte - Escolha a opção correta em cada questão ( 5 pontos/questão)
 TESTE DE AVALIAÇÃO FINAL -MÓDULO Q2 versão2 Física e Química Data: / fev / 15 Cursos Profissionais Turma : Aluno: nº Classificação: Professora: Enc.Educação: 1ª Parte - Escolha a opção correta em cada
TESTE DE AVALIAÇÃO FINAL -MÓDULO Q2 versão2 Física e Química Data: / fev / 15 Cursos Profissionais Turma : Aluno: nº Classificação: Professora: Enc.Educação: 1ª Parte - Escolha a opção correta em cada
FUVEST ª Fase (Questões 8 a 13)
 1ª Fase (Questões 8 a 13) 1. (Questão 8) Um funcionário de uma empresa ficou encarregado de remover resíduos de diferentes polímeros que estavam aderidos a diversas peças. Após alguma investigação, o funcionário
1ª Fase (Questões 8 a 13) 1. (Questão 8) Um funcionário de uma empresa ficou encarregado de remover resíduos de diferentes polímeros que estavam aderidos a diversas peças. Após alguma investigação, o funcionário
ESTEQUIOMETRIA Folha 02 João Roberto Mazzei
 01. (CFT MG 2008) Cada mililitro de um medicamento antiácido contém 0,06 g de hidróxido de alumínio. A massa de ácido clorídrico do suco gástrico que é neutralizada pela ingestão de 26 ml desse medicamento
01. (CFT MG 2008) Cada mililitro de um medicamento antiácido contém 0,06 g de hidróxido de alumínio. A massa de ácido clorídrico do suco gástrico que é neutralizada pela ingestão de 26 ml desse medicamento
REAÇÕES QUÍMICAS. Elaboradores: Bruno Reis Martins Jordana Dinorá de Lima Karolayne Gonçalves da Silva Rafael de OIiveira Fratoni.
 REAÇÕES QUÍMICAS Elaboradores: Bruno Reis Martins Jordana Dinorá de Lima Karolayne Gonçalves da Silva Rafael de OIiveira Fratoni Aplicadores: Bruno Reis Martins Jordana Dinorá de Lima Karolayne Gonçalves
REAÇÕES QUÍMICAS Elaboradores: Bruno Reis Martins Jordana Dinorá de Lima Karolayne Gonçalves da Silva Rafael de OIiveira Fratoni Aplicadores: Bruno Reis Martins Jordana Dinorá de Lima Karolayne Gonçalves
Ba 2+ (aq) + CrO 4. 2 (aq)
 Experiência 9: ESTUDO DO EQUILÍBRIO CROMATO-DICROMATO 1. Objetivos Ao final desta atividade experimental espera-se que o aluno seja capaz de: - A partir da equação química de um sistema em equilíbrio escrever
Experiência 9: ESTUDO DO EQUILÍBRIO CROMATO-DICROMATO 1. Objetivos Ao final desta atividade experimental espera-se que o aluno seja capaz de: - A partir da equação química de um sistema em equilíbrio escrever
Perguntas Frequentes / FAQ. 2. Como são realizados os controles nos competidores? 3. Os exames são feitos somente quando há suspeitas?
 Perguntas Frequentes / FAQ 1. Qual é a definição de dopagem no mundo esportivo? Considera- se dopagem a utilização de substâncias ou métodos capazes de aumentar artificialmente o desempenho esportivo,
Perguntas Frequentes / FAQ 1. Qual é a definição de dopagem no mundo esportivo? Considera- se dopagem a utilização de substâncias ou métodos capazes de aumentar artificialmente o desempenho esportivo,
Kits Didáticos. Laboratórios Portáteis
 Kits Didáticos Laboratórios Portáteis Kit pedagógico de genética A Procura do Suspeito (Papiloscopia - Jogo) Kit na forma de jogo para o ensino fundamental e médio para ensino de genética de herança mendeliana
Kits Didáticos Laboratórios Portáteis Kit pedagógico de genética A Procura do Suspeito (Papiloscopia - Jogo) Kit na forma de jogo para o ensino fundamental e médio para ensino de genética de herança mendeliana
A IMPORTÂNCIA DA UTILIZAÇÃO DOS EXPERIMENTOS DEMONSTRATIVOS NAS AULAS DE QUÍMICA
 A IMPORTÂNCIA DA UTILIZAÇÃO DOS EXPERIMENTOS DEMONSTRATIVOS NAS AULAS DE QUÍMICA Yuri Miguel da Silva 1 ; Sebastião Lucas de Farias 2 ; Magadã Lira 3 ; 1 Instituto Federal de Pernambuco - Campus Vitória
A IMPORTÂNCIA DA UTILIZAÇÃO DOS EXPERIMENTOS DEMONSTRATIVOS NAS AULAS DE QUÍMICA Yuri Miguel da Silva 1 ; Sebastião Lucas de Farias 2 ; Magadã Lira 3 ; 1 Instituto Federal de Pernambuco - Campus Vitória
Fisiologia: Digestão, Respiração e Circulação
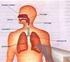 Fisiologia: Digestão, Respiração e Circulação Fisiologia: Digestão, Respiração e Circulação 1. Um laboratório analisou algumas reações ocorridas durante o processo de digestão do amido em seres humanos.
Fisiologia: Digestão, Respiração e Circulação Fisiologia: Digestão, Respiração e Circulação 1. Um laboratório analisou algumas reações ocorridas durante o processo de digestão do amido em seres humanos.
QUESTÃO 46 QUESTÃO 47 QUESTÃO 48 P R O V A D E Q UÍMICA I
 18 P R O V A D E Q UÍMICA I QUESTÃO 46 O número de oxidação (ox) de um elemento quantifica seu estado de oxidação. Qual é o ox de Cr no ânion Cr 2 O 7 2-? a) +3 b) +5 c) +6 d) +7 QUESTÃO 47 Considere o
18 P R O V A D E Q UÍMICA I QUESTÃO 46 O número de oxidação (ox) de um elemento quantifica seu estado de oxidação. Qual é o ox de Cr no ânion Cr 2 O 7 2-? a) +3 b) +5 c) +6 d) +7 QUESTÃO 47 Considere o
FUVEST 1999 Prova de Química. Magnésio e seus compostos podem ser produzidos a partir da água do mar, como mostra o esquema a seguir:
 Q.01 Magnésio e seus compostos podem ser produzidos a partir da água do mar, como mostra o esquema a seguir: a) Identifique X, Y e Z, dando suas respectivas fórmulas. b) Escreva a equação que representa
Q.01 Magnésio e seus compostos podem ser produzidos a partir da água do mar, como mostra o esquema a seguir: a) Identifique X, Y e Z, dando suas respectivas fórmulas. b) Escreva a equação que representa
1 a QUESTÃO: (2,0 pontos) Avaliador Revisor
 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Considere a reação exotérmica de formação do trióxido de enxofre, a partir do dióxido: 2SO 2(g) + O 2(g) 2SO 3(g) A 900 K, K p = 40,5 atm -1 e ΔH = -198 kj.
1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Considere a reação exotérmica de formação do trióxido de enxofre, a partir do dióxido: 2SO 2(g) + O 2(g) 2SO 3(g) A 900 K, K p = 40,5 atm -1 e ΔH = -198 kj.
Processo Seletivo 2005
 Prova Discursiva - 4º dia Biologia Le i a a te n ta m e n te a s i n s tr uç õ e s : 1ð Preencha integralmente, na parte inferior desta capa, o espaço próprio para Identificação do Candidato. Você será
Prova Discursiva - 4º dia Biologia Le i a a te n ta m e n te a s i n s tr uç õ e s : 1ð Preencha integralmente, na parte inferior desta capa, o espaço próprio para Identificação do Candidato. Você será
QUÍMICA. Questão 01. Questão 02
 Questão 01 QUÍMICA A fenil-etil-amina é considerada um componente responsável pela sensação do bem-estar decorrente da ingestão do chocolate, que contém, também, substâncias inorgânicas. Na tabela a seguir
Questão 01 QUÍMICA A fenil-etil-amina é considerada um componente responsável pela sensação do bem-estar decorrente da ingestão do chocolate, que contém, também, substâncias inorgânicas. Na tabela a seguir
ROTEIRO PRÁTICO DE QUÍMICA GERAL
 ROTEIRO PRÁTICO DE QUÍMICA GERAL 1- Objetivo 1. Estimar o ph de água destilada e de soluções aquosas usando indicadores ácidobase. 2. Diferenciar o comportamento de uma solução tampão. 2 Introdução Eletrólitos
ROTEIRO PRÁTICO DE QUÍMICA GERAL 1- Objetivo 1. Estimar o ph de água destilada e de soluções aquosas usando indicadores ácidobase. 2. Diferenciar o comportamento de uma solução tampão. 2 Introdução Eletrólitos
Identificação de compostos orgânicos
 Identificação de compostos orgânicos Trabalho realizado por: Ana Patrícia Filipe nº62829 Gonçalo Rodrigues nº62827 MEBM Índice 1.Resumo... 3 2.Introdução... 3 3.Procedimento... 4 4.Resultados... 5 5.Discussão/Questões...
Identificação de compostos orgânicos Trabalho realizado por: Ana Patrícia Filipe nº62829 Gonçalo Rodrigues nº62827 MEBM Índice 1.Resumo... 3 2.Introdução... 3 3.Procedimento... 4 4.Resultados... 5 5.Discussão/Questões...
t RESOLUÇÃO COMECE DO BÁSICO
 t RESOLUÇÃO COMECE DO BÁSICO - o processo I sugere a evaporação (transformação física) dos componentes do medicamento. - a decomposição das substâncias (transformação química) que constituem o princípio
t RESOLUÇÃO COMECE DO BÁSICO - o processo I sugere a evaporação (transformação física) dos componentes do medicamento. - a decomposição das substâncias (transformação química) que constituem o princípio
Determinação de cloretos na água do mar pelo método de Mohr
 Determinação de cloretos na água do mar pelo José Guerchon Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Determinação de cloretos na água do mar pelo José Guerchon Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
3ª Série / Vestibular. As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar que, na reação:
 3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
PROVA DE QUÍMICA. Tendo em vista as propriedades coligativas dessas soluções, é CORRETO afirmar
 17 PROVA DE QUÍMICA Q U E S T Ã O 2 6 Z e X são elementos químicos que apresentam respectivamente 2 e 6 elétrons no nível de valência. A fórmula química resultante da combinação entre átomos dos elementos
17 PROVA DE QUÍMICA Q U E S T Ã O 2 6 Z e X são elementos químicos que apresentam respectivamente 2 e 6 elétrons no nível de valência. A fórmula química resultante da combinação entre átomos dos elementos
Prática 01 Reações e equações químicas
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 01 Reações e equações químicas 1. Introdução
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 01 Reações e equações químicas 1. Introdução
OXIDAÇÃO DE METAIS INTRODUÇÃO
 OXIDAÇÃO DE METAIS INTRODUÇÃO Oxidação é uma palavra do âmbito da química que significa a perda de elétrons, mesmo que não seja causada pelo oxigênio. Indica também o processo de oxidar, ou seja, de combinar
OXIDAÇÃO DE METAIS INTRODUÇÃO Oxidação é uma palavra do âmbito da química que significa a perda de elétrons, mesmo que não seja causada pelo oxigênio. Indica também o processo de oxidar, ou seja, de combinar
UFU 2008/2-1ª FASE. 1-A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina).
 UFU 2008/2-1ª FASE 1-A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa
UFU 2008/2-1ª FASE 1-A substância, representada pela fórmula estrutural abaixo, é bastante utilizada como analgésico (aspirina). Com base nessas informações, marque a alternativa correta. A) Uma massa
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS
 PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS (Decreto-Lei n.º 64/2006, de 21 de março) 2014 PROVA DE QUÍMICA Data da prova:
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS (Decreto-Lei n.º 64/2006, de 21 de março) 2014 PROVA DE QUÍMICA Data da prova:
Química. Questão 17 A gasolina é uma mistura de hidrocarbonetos diversos que apresenta, dentre outros, os seguintes componentes:
 Questão 16 Uma molécula de água, isolada, não apresenta certas propriedades físicas - como ponto de fusão e de ebulição - que dependem de interações entre moléculas. Em 1998, um grupo de pesquisadores
Questão 16 Uma molécula de água, isolada, não apresenta certas propriedades físicas - como ponto de fusão e de ebulição - que dependem de interações entre moléculas. Em 1998, um grupo de pesquisadores
Escola Secundária de Alcácer do Sal Química 12º ano teste 3 17/02/2004
 Escola Secundária de Alcácer do Sal Química 12º ano teste 3 17/02/2004 I Escreva na sua folha de respostas a letra correspondente à alternativa correcta que seleccionar para cada item. A indicação de mais
Escola Secundária de Alcácer do Sal Química 12º ano teste 3 17/02/2004 I Escreva na sua folha de respostas a letra correspondente à alternativa correcta que seleccionar para cada item. A indicação de mais
Ficha Informativa n.º 2 Tipos de Reações Químicas
 FÍSICO-QUÍMICA 8º ANO DE ESCOLARIDADE Ficha Informativa n.º 2 Tipos de Reações Químicas Nome: Data: / /20 INTRODUÇÃO TEÓRICA Reações Químicas Nas reações químicas, uma ou várias substâncias iniciais (reagentes)
FÍSICO-QUÍMICA 8º ANO DE ESCOLARIDADE Ficha Informativa n.º 2 Tipos de Reações Químicas Nome: Data: / /20 INTRODUÇÃO TEÓRICA Reações Químicas Nas reações químicas, uma ou várias substâncias iniciais (reagentes)
V ENALIC/IV Seminário Nacional do Pibid 8-12 de dezembro de 2014, Natal, RN APRENDENDO SOBRE DOPING COM UM BONECO INTERATIVO
 APRENDENDO SOBRE DOPING COM UM BONECO INTERATIVO Henry Porto Vieira de Assis 1, Patrick Andersson Barreto Frasão 1, Maria de Fátima Teixeira Gomes 2 e Denise Gutman Almada 3 1 Licenciatura em Química,
APRENDENDO SOBRE DOPING COM UM BONECO INTERATIVO Henry Porto Vieira de Assis 1, Patrick Andersson Barreto Frasão 1, Maria de Fátima Teixeira Gomes 2 e Denise Gutman Almada 3 1 Licenciatura em Química,
Preparar e fazer cálculos prévios para o preparo de soluções diluídas a partir de soluções estoque.
 AULA 6 Indicadores ácido-base e ph OBJETIVOS Verificar o ph de soluções ácidas e básicas, concentradas e diluídas; Entender os efeitos da diluição na concentração dos componentes; Preparar e fazer cálculos
AULA 6 Indicadores ácido-base e ph OBJETIVOS Verificar o ph de soluções ácidas e básicas, concentradas e diluídas; Entender os efeitos da diluição na concentração dos componentes; Preparar e fazer cálculos
2º trimestre Química Data: 08/2018 Ensino Médio 1º ano classe: Prof. Valéria
 2º trimestre Química Data: 08/2018 Ensino Médio 1º ano classe: Prof. Valéria A Patrícia, que é uma excelente aluna, esteve a determinar o ph de oito soluções, durante o decorrer de uma aula experimental.
2º trimestre Química Data: 08/2018 Ensino Médio 1º ano classe: Prof. Valéria A Patrícia, que é uma excelente aluna, esteve a determinar o ph de oito soluções, durante o decorrer de uma aula experimental.
Atividade extra de Química sobre o vírus influenza A (H 1 N 1 ) e a ação do álcool-gel
 Atividade extra de Química sobre o vírus influenza A (H 1 N 1 ) e a ação do álcool-gel 1) Fatec/jun-09O alcoolismo é um grave problema de saúde pública no Brasil, assim como em vários outros países. Estima-se
Atividade extra de Química sobre o vírus influenza A (H 1 N 1 ) e a ação do álcool-gel 1) Fatec/jun-09O alcoolismo é um grave problema de saúde pública no Brasil, assim como em vários outros países. Estima-se
Universidade de São Paulo Instituto de Química
 Universidade de São Paulo Instituto de Química QBQ-5825 Prática de Ensino de Química e Bioquímica Monitoria da disciplina QFL-0137 Química Geral e Inorgânica Básica Profª. Drª. Denise Freitas Siqueira
Universidade de São Paulo Instituto de Química QBQ-5825 Prática de Ensino de Química e Bioquímica Monitoria da disciplina QFL-0137 Química Geral e Inorgânica Básica Profª. Drª. Denise Freitas Siqueira
a) Escreva os nomes das substâncias presentes nos frascos A, B e C. A B C
 PROVA DE QUÍMICA 2ª ETAPA do VESTIBULAR 2006 (cada questão desta prova vale até cinco pontos) Questão 01 Foram encontrados, em um laboratório, três frascos A, B e C, contendo soluções incolores e sem rótulos.
PROVA DE QUÍMICA 2ª ETAPA do VESTIBULAR 2006 (cada questão desta prova vale até cinco pontos) Questão 01 Foram encontrados, em um laboratório, três frascos A, B e C, contendo soluções incolores e sem rótulos.
QUÍMICA. Lista de Exercícios Funções Orgânicas LISTA 1
 QUÍMA Prof. Rodrigo Rocha Lista de Exercícios Funções rgânicas LSTA 1 1. Um produto industrial consiste na substância orgânica formada no sentido direto do equilíbrio químico representado pela seguinte
QUÍMA Prof. Rodrigo Rocha Lista de Exercícios Funções rgânicas LSTA 1 1. Um produto industrial consiste na substância orgânica formada no sentido direto do equilíbrio químico representado pela seguinte
EXPERIÊNCIA 9 PRINCÍPIO DE LE CHATELIER E EQUILÍBRIO QUÍMICO
 EXPERIÊNCIA 9 PRINCÍPIO DE LE CHATELIER E EQUILÍBRIO QUÍMICO 1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Dada a equação química de um equilíbrio, escrever a expressão para a constante
EXPERIÊNCIA 9 PRINCÍPIO DE LE CHATELIER E EQUILÍBRIO QUÍMICO 1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Dada a equação química de um equilíbrio, escrever a expressão para a constante
PROPOSTA DISCIPLINAR QUÍMICA
 1.Título: Função Química PROPOSTA DISCIPLINAR QUÍMICA 2. Conteúdos: Conteúdo estruturante: Matéria e sua natureza, biogeoquímica e química sintética Conteúdo Básico: Funções Inorgânicas Conteúdo específico:
1.Título: Função Química PROPOSTA DISCIPLINAR QUÍMICA 2. Conteúdos: Conteúdo estruturante: Matéria e sua natureza, biogeoquímica e química sintética Conteúdo Básico: Funções Inorgânicas Conteúdo específico:
Gabriel da S. Pereira e Mª de Fátima T. Gomes
 JOGANDO COM O EQUILÍBRIO QUÍMICO: um jogo didático para ensinar os fatores que deslocam o equilíbrio químico Gabriel da S. Pereira e Mª de Fátima T. Gomes Aprendendo através do lúdico Os jogos pedagógicos
JOGANDO COM O EQUILÍBRIO QUÍMICO: um jogo didático para ensinar os fatores que deslocam o equilíbrio químico Gabriel da S. Pereira e Mª de Fátima T. Gomes Aprendendo através do lúdico Os jogos pedagógicos
DURAÇÃO DA PROVA: 03 HORAS
 DURAÇÃO DA PROVA: 03 HORAS Nº de Inscrição do Candidato PROCESSO SELETIVO 2014/2 - CPS CURSO DE GRADUAÇÃO EM MEDICINA PROVA DISCURSIVA DE QUÍMICA INSTRUÇÕES: 1. Só abra a prova quando autorizado. 2. Veja
DURAÇÃO DA PROVA: 03 HORAS Nº de Inscrição do Candidato PROCESSO SELETIVO 2014/2 - CPS CURSO DE GRADUAÇÃO EM MEDICINA PROVA DISCURSIVA DE QUÍMICA INSTRUÇÕES: 1. Só abra a prova quando autorizado. 2. Veja
