Fenômenos de Transporte III. Aula 9. Prof. Gerônimo
|
|
|
- Maria de Begonha Capistrano Filipe
- 6 Há anos
- Visualizações:
Transcrição
1 Fenômenos de Transporte III ula 9 Prof. Gerônimo
2 Transferência de massa entre fases Introdução às operações de transferência de massa 2
3 1- bsorção e desabsorção de gases 1.1 Introdução s operações de absorção e desabsorção de gases são de emprego generalizado na indústria química, do petróleo, petroquímica e alimentícia, bem como nos equipamentos de controle de poluição. bsorção de gases: visa retirar um ou mais componentes de uma mistura de gases pelo contato direto com um líquido. remoção de um componente (CO 2, SO 2, NH 3, Cl 2...) de um gás (ar,...) para um líquido por meio de: - dissolução simples do componente da fase gasosa para a fase líquida; - reação química entre o componente e algum reagente na fase líquida, com o produto da reação a permanecer na fase líquida; 3
4 Desabsorção de gases: é a operação inversa de absorção e cujo objetivo é retirar os componentes mais voláteis de uma mistura líquida por meio de um gás que se faz passar pelo líquido e com ele entra em contato direto. lguns eemplos de sistemas comuns de absorção: Soluto Solvente Reagente CO 2, H 2 S água CO 2, H 2 S água K 2 CO 3, Na 2 CO 3,... CO 2 HCl, HF carbonato de propileno Água HCl, HF Água NaOH Cl 2 SO 2 Água Água SO 2 Água NH 3, NaOH,... NH 3 Água HCN Água NaOH NO 2 Água 4
5 Para que a transferência de massa seja possível, deve-se: - aumentar a área da interface o tanto quanto possível (área superficial específica); - uso de gotículas de líquido (colunas de pulverização Spra Towers); - enchimento de colunas de modo a que se formem filmes delgados de líquido (colunas de enchimento); - a vazão de líquido deve situar-se abaio da vazão de inundação (coluna inundada = coluna totalmente cheia); - ou emprego de pratos como nas colunas de destilação. 5
6 bsorção e transferência de massa da bolha de gás para o líquido do gás para a gotícula de líquido do gás para um filme de líquido delgado
7 Tipos de colunas de absorção Câmara de pulverização pulverizadores saída de gás limpo separador de neblina O líquido é pulverizado e remove o soluto do gás que flui no sentido ascendente na câmara Usa elevada quantidade de água: 3 a 14 litros/m 3 de gás presenta reduzida área superficial para a absorção Rendimento: % entrada de gás sujo
8 Tipos de colunas de absorção Coluna de pratos saída de gás limpo prato dreno espuma entrada de líquido entrada de gás sujo O líquido desce em cascata por uma série de pratos onde entra em contato com o gás impuro, removendo o soluto deste. O gás limpo flui no sentido ascendente. saída de líquido
9 Tipos de colunas de absorção Coluna de enchimento entrada de líquido saída de gás limpo distribuidores de líquido O líquido é pulverizado e remove o soluto do gás que flui no sentido ascendente na câmara Usa reduzida quantidade de água: 1 a 3 litros/m 3 de gás redistribuidor de líquido presenta elevada área superficial para a absorção enchimento casual Rendimento: > 90 % suporte do enchimento entrada de gás sujo saída de líquido
10 Como eemplo de coluna de absorção e desabsorção em série, a amônia (NH 3 ) é absorvida pela água na coluna de absorção, formando NH 4 OH, sendo transportada para a coluna de desabsorção onde a NH 3 gasosa é recuperada a partir do ar, seguido de elevação de temperatura. 10
11 1.2 Elementos de cálculo Os cálculos de absorção e desabsorção são feitos pela aplicação de balanços materiais e de energia, relações de equilíbrio e equações de velocidade. Balanços materiais: permitem relacionar as quantidades produzidas com as alimentadas, utilizando as composições correspondentes. s correntes internas do equipamento também são calculadas por meio de balanços materiais, assim como as recuperações e rendimentos. Balanços de energia: são envolvidos nos cálculos porque na absorção, quando há uma operação eotérmica, os efeitos energéticos deverão ser considerados. Relações de equilíbrio: juntamente com os balanços materiais, constituem a base do cálculo do número de estágios teóricos necessários para realizar a operação. São do tipo: X = /(1 ) ; Y = /(1 ) Equações de velocidade: são utilizadas para dimensionar os equipamentos (absorvedores e desabsorvedores), assim como as equações de velocidade de transferência de calor servem para dimensionar trocadores de calor. São semelhantes à conhecida q = U..T para trocadores de calor, pois envolvem o produto dos mesmos três fatores: coeficiente global, área de transferência e força propulsora. São do tipo: N = K c..c. 11
12 1.3 Transferência de massa entre fases Figura 1 ilustra a situação na qual o soluto migra da fase leve (fase G) à pesada (fase ) e está representada por G. Nessa Figura supõe-se que as fases leve e pesada estão situadas em filmes estagnados de espessuras e, respectivamente. Nas fases G e eistem misturas binárias soluto/inerte, em que o soluto é o mesmo em ambas as fases (E.: NH 3 ), enquanto que os inertes são distintos entre sí (e.: r e Água). movimento do soluto (transporte de massa) G G i Interface gás-líquido i Figura 1
13 Foi visto anteriormente na introdução (ula 1) que o fenômeno da transferência de massa, de algum modo, está vinculado ao binômio causa-efeito, no qual para uma determinada causa decorre o efeito, havendo uma resistência ao transporte à ação da causa: Fluo de matéria força motriz resistência ao transporte Para a difusão, identificou-se à resistência o inverso da mobilidade que o soluto tem em relação à solução (ou seja, o coeficiente de difusão); enquanto que a força motriz era o gradiente de concentração. O princípio é o mesmo para o fenômeno da convecção mássica: i. há uma causa força motriz; ii. há um efeito fluo de matéria; iii. há uma mobilidade associada para vencer a resistência ao transporte coeficiente convectivo de transferência de massa ( 1 )
14 Como decorrência dessas considerações, escreve-se o seguinte fluo molar para a convecção mássica: N C C, Z m ( 2 ) N em que: C m,z C diferença de concentração (força motriz ao transporte); fluo molar do soluto na direção z; coeficiente convectivo de transferência de massa (coeficiente fenomenoló gico). Conclui-se, após inspecionar a definição 2, que: m 1 Resistência à convecção mássica 14
15 partir da Figura 1, o fluo global do soluto na fase leve é dado por: N ( 3 ), z G O parâmetro é definido como coeficiente de transferência de massa da fase gasosa, cuja força motriz é a diferença de fração molar do soluto no seio da fase e em uma determinada fronteira. Esse coeficiente apresenta a seguinte unidade: mols de área. tempo. ou em função da pressão parcial: N P P ( 4 ), z G G com G = /P, em que P é a pressão total do sistema. Utiliza-se o coeficiente G, quando estamos analisando a fase gasosa, cuja força motriz é epressa pela diferença da pressão parcial do soluto. mols de G área. tempo. unidade de pressão i i 15
16 Na fase pesada, o fluo global de é descrito, em função de sua fração molar ou em termos da sua concentração molar, respectivamente, de acordo com: N ( 5 ), z i O parâmetro é definido como coeficiente de transferência de massa da fase líquida, cuja força motriz é a diferença de fração molar do soluto no seio da fase e em uma determinada fronteira. Esse coeficiente apresenta a seguinte unidade: mols de área.tempo. N C C ( 6 ), z i com = (M / ), sendo M e a massa molecular e a densidade da solução líquida. Utiliza-se o coeficiente, quando estamos analisando a fase líquida, cuja força motriz é epressa pela diferença da concentração molar do soluto. mols de área. tempo. unidade de concentração molar de 16
17 Para soluções diluídas, temos: ', G ' G, ', ' Estes coeficientes podem ser denominados como coeficientes individuais de transferência de massa. O termo individual é devido a esses coeficientes estarem relacionados à resistência específica de uma fase ao transporte do soluto: 1/ e 1/ G referem-se às resistências individuais ao transporte do soluto na fase G, enquanto que 1/ e 1/ associam-se às resistências individuais ao transporte de na fase. 17
18 Equilíbrio termodinâmico de fases Interface i Fase gasosa i i Fase líquida i Curva de equilíbrio ou de solubilidade i Reta de equilíbrio ou reta de solubilidade m m i i m = H/P Concentrada i Diluída i 18
19 Determinação eperimental da composição de equilíbrio da fase gás/líquido Os valores de i e i podem ser determinados eperimentalmente. Eemplo, para SO 2 -ar-água a 1 atm e 20C: Uma determinada quantidade de mistura com todos os componentes é colocada num vaso fechado, bem agitado a uma data T e P até que se atinja o equilíbrio. Retiram-se amostras do gás e do líquido e determina-se a concentração de SO 2 na fase gasosa e na fase líquida. Prepara-se uma nova mistura com diferentes concentrações e repete-se a eperiência até que se obtenha um número representativo de dados i e i. Obs.: Eistem dados de equilíbrio disponíveis na literatura para muitos sistemas. OSD I 1-19
20 Determinação eperimental da composição de equilíbrio da fase gás/líquido solubilidade de um gás dissolvido em um líquido é proporcional à pressão parcial do gás acima do líquido. Este é o enunciado da lei de Henr: P Com o valor da composição do SO 2 na fase líquida obtido por análise química e com o valor de H = 29,6 atm para o SO 2, determina-se a pressão parcial do SO 2 na fase líquida. dmitindo fase gasosa ideal tem-se a lei de Dalton: P Com o valor de P = 1 atm e de P i, obtem-se o valor de i do SO 2. Para outras composições de SO 2 -ar-água, realiza-se o mesmo procedimento e ao final tem-se os valores tabelados de i e i. No equilíbrio termodinâmico tem-se a igualdade das leis de Henr e Dalton para soluções ideais e diluídas: i i i H i m P m = H/P i i OSD I 1-20
21 figura abaio representa os dados eperimentais para o sistema SO 2 -ar-água a 1 atm e 20C face aos calculados pela lei de Henr (da literatura, H = 29,6 atm/fração) pso2 (atm) H = 29,6 atm/fração ei de Henr Pi ih P T m i i SO2 (mol/mol) i m i 21
22 Teoria das duas resistências teoria das duas resistências considera que a interface i não oferece resistência ao transporte do soluto. o considerar a eistência do equilíbrio termodinâmico na interface e supondo válida a teoria das duas resistências, é possível estabelecer a continuidade do fluo de na fronteira entre as fases. Portanto, igualando as equações (1) e (3), temos: G i G i ( 7 ) i i equação (5) epressa a relação entre as resistências individuais da fase gasosa e da fase líquida em função das forças motrizes em cada fase. 22
23 figura a seguir mostra o posicionamento da equação (5) em relação a reta de equilíbrio. G i i G i O m G solução diluída M i figura acima é útil para a determinação dos coeficientes individuais envolvidos na operação de transferência de massa em um determinado ponto do equipamento de separação, desde que se conheçam as composições do soluto na interface ( i, i ). inclinação dada pela equação (5), presente na figura em análise, é a mesma para qualquer ponto da altura do equipamento, isto é fruto da hipótese de a solução ser diluída ( i = m i ). 23
24 Eemplo 01: Esboce a linha OM referenciada à reta de equilíbrio para a operação G. Solução: Supondo que a reta de equilíbrio possa ser dada por i = m i, lançaremos mão da teoria das duas resistências para G. Dessa maneira, os fluos para a fase e G são, respectivamente: N N,z,z i i G ( 1 ) ( 2 ) Da teoria das duas resistências: (1) = (2) ou i ( 3 ) G i Rearranjando (3): G i ( 4 ) i 24
25 figura a seguir mostra o posicionamento da equação (4) em relação a reta de equilíbrio. ( 4 ) G i i G solução diluída i G M m O i figura acima é útil para a determinação dos coeficientes individuais envolvidos na operação de transferência de massa em um determinado ponto do equipamento de separação, desde que se conheçam as composições do soluto na interface ( i, i ). inclinação dada pela equação (4), presente na figura em análise, é a mesma para qualquer ponto da altura do equipamento, isto é fruto da hipótese de a solução ser diluída ( i = m i ). 25
26 Eemplo 01: Construa as curvas de solubilidade (equilíbrio) para os seguintes sistemas: a) mônia-água na temperatura de 30C e 1atm. b) SO 2 -água na temperatura de 20C e 1 atm. c) Por intermédio de uma estimativa para m, procure mostrar qual fase controlará o processo de separação do soluto nas situações apresentadas nos itens a e b. d) partir do resultado obtido no item b, determine a relação / para um certo ponto da torre com: = 4,010-3 e G = 1, Dados: mônia-água na temperatura de 30C e 1atm i 0 0,0126 0,0208 0,0309 0,0405 0,0737 0,1370 i 0 0,0151 0,0254 0,0309 0,0527 0,1050 0,2350 SO 2 -água na temperatura de 20C e 1 atm i 0 5, , , , , , i 0 6, , , , ,212 0,917 26
27 a) NH 3 -água a 30C e 1 atm: amônia é muito solúvel em água e o valor de m é pequeno, assim a fase gasosa controlará o processo de separação nesta faia de composição e temperatura. 2,510-1 Curva de equilíbrio 2,010-1 Regressão linear i 1, ,010-1 m = 1,7338 5,010-2 i = 1,7338 i 0,0-0,02 0,00 0,02 0,04 0,06 0,08 0,10 0,12 0,14 i 27
28 b) SO 2 -água a 20C e 1 atm: O valor de m é muito grande e a fase líquida controlará o processo de separação. 1, ,010-1 Curva de equilíbrio Regressão linear 6,010-1 m = 33,73 i 4,010-1 i = 33,73 i 2, / 0,0 ( = ; = ) 0,0 5, , , , , ,010-2 i 28
29 G i i G G 0,001 0,004 i = 33,73 i 0,001 33,73 i 0,004 33,73 i i i - / 0 0 0,25 5, , ,23 2, , ,21 8, , ,54 2, , ,69 6, , ,59 2, ,917 39,67 29
30 Coeficientes globais de transferência de massa Considere que a resistência oferecida ao transporte do soluto de uma das fases seja desprezível em relação a outra. Como consequência, os coeficientes globais de transferência de massa nascem como alternativa para a determinação do fluo de matéria, sendo definidos para as fases G e, respectivamente, como: N * K, Z G ( 8 ) * N, Z K ( 9 ) em que K e K são os coeficientes globais de transferência de massa referenciados às fases G e, as quais podem ser identificadas às fases gasosa e líquida, respectivamente; * é a fração molar do soluto na fase gasosa em equilíbrio com a fração molar do soluto no seio da fase líquida ( ); * é a fração molar do soluto na fase líquida em equilíbrio com a fração molar do soluto no seio da fase gasosa ( G ), sendo que para sistema diluído e validade da lei de Henr, são determinadas por: * m ( 10 ) * m ( 11 ) G
31 Representação da relação entre as resistências globais junto à reta de equilíbrio G m G i * m Global G m * * Global i * 31
32 s relações entre os coeficientes individuais e globais de transferência de massa são obtidas igualando-se os fluos molares em cada fase. * K G ( fase gasosa ) i G K * 1/K G global 1/ ( 12 ) G i G epressão (12) indica a relação entre as resistências global e individual, referenciada à fase gasosa (G). Essa epressão também está associada às forças motrizes individual e global. nalogamente, para a fase líquida (), temos: * K i ( fase líquida ) K 1/K 1/ * i global ( 13 ) s equações (12) e (13) apresentam a relação entre as resistências global e individual de transferência de massa.
33 Relação entre a resistência global, referenciada a uma certa fase, com as individuais Considerando que uma das resistências de transferência do soluto seja desprezível, temos: N G *, Z K ( 8 ) 1 G K N,Z * 1 K * G i i ( 14 ) N N,Z,Z Substituindo as equações de equilíbrio na interface; m i i * m Na equação (14), temos: 1 K m G i i ( 15 ) N N,Z,Z
34 Identificando os coeficientes individuais de transferência de massa por intermédio das equações ( 3 ) e ( 5 ) na equação ( 15 ), obtém-se: 1 G i i m K N,Z N,Z 1 1 G 1 K 1 m ( 16 ) equação ( 16 ) representa a relação entre a resistência global, referenciada à fase G, e as resistências individuais e. Por um procedimento semelhante a partir da equação ( 9 ), a equação ( 17 ) epressa a relação entre a resistência global, referenciada a fase, e as resistências individuais e. G 1 K 1 1 ( 17 ) m
35 Observando as equações ( 16 ) e ( 17 ), podemos concluir: a) Para um gás altamente solúvel na fase líquida (absorção de NH 3 por H 2 O), temos m 0 na equação ( 16 ), e verificamos: 1 K 1 m 1 K 1 ( 18 ) Nesse caso diz-se que a resistência da fase gasosa controla o processo o processo de transferência de massa. O equipamento utilizado para este tipo de separação é uma torre de spra. Figura 2
36 b) Para um sistema envolvendo um gás pouco solúvel na fase líquida (absorção de CO 2 por H 2 O), a constante m é muito grande, de modo que 1/m 0 na equação ( 17 ), notamos: 1 K 1 m 1 1 K 1 ( 19 ) qui a resistência da fase liquida controla o processo o processo de transferência de massa. Nesta situação pode-se utilizar as torres de borbulhamento. Figura 3 36
37 Utilizam-se torres de recheio quando as duas fases ( + G) controlam o processo de transferência de massa ou quando operam com elevadas taas de vapor em relação às de líquido, bem como o inverso. Essas torres são largamente utilizadas na absorção e na desabsorção de gases, podendo ser aplicada também na destilação etrativa bem como no caso da etração líquido-líquido. configuração desta torre é a de um leito fio recheado com particulados de formas peculiares. Selas Berl Selas Intalo nel Raschig nel essing nel Pall Tellerette Figura 4 37
38 Recheios de colunas de enchimento Os recheios cerâmicos ou de PVC são muito utilizados na transferência de massas por apresentarem boa resistência química e baio custo de instalação. fim de que possamos selecionar o tipo de recheio devemos levar em conta: 1- Sua eficiência 2- Sua área superficial 3- Sua capacidade de manuseio de carga de líquido e gás com pequena variação na eficiência 4- Sua capacidade de distribuição do líquido 5- Sua alta capacidade de vazão 6- Sua resistência mecânica para suportar as cargas normais de serviço 7- Sua elevada resistência química 8- Sua reduzida queda de pressão 9- Seu peso mínimo e menor esforço na parede da torre 10- Seu baio custo Devido a compactação do recheio, a quantidade de peças por m 3 torna-se maior com o aumento da relação, diâmetro da torre e diâmetro do recheio.
39 Tipos de recheios utilizados em colunas de enchimento Selas Reno Selas Berl néis Raschig néis Pall néis Cross-Partition néis essing
40 Eistem dois modos de os recheios serem dispostos no interior da coluna: aleatoriamente ou de maneira ordenada (organizada). No primeiro caso, utilizam basicamente os recheios, tais como, anel de raschig, anel de pall, sela berl, sela intalo, etc, levando-os a denominarem-se recheios randômicos. No segundo caso, os recheios são montados de forma ordenada, criando canais preferenciais para o escoamento das fases. Esses recheios são denominados tradicionalmente de estruturados. Eistem casos em que a disposição dos recheios randômicos, cuja ordenação é estruturada, como é o caso de anéis raschig (d s > 75 mm) os quais são empilhados sempre na vertical, possibilitando maior eficiência de separação e menor perda de carga. 40
41 Tabela 1: Características dos recheios randômicos. d S : diâmetro nominal mm (in) 13 (1/2) 16 (5/8) 19 (3/4) 25 (1) 38 (3/2) 50 (2) 76 (3) néis de Raschig Densidade (g/m 3 ) Quantidade (peças/m 3 ) a s : área superficial (m 2 /m 3 ) néis Raschig
42 Tabela 2: Características de recheios randômicos. d S : diâmetro nominal mm (in) 13 (1/2) 16 (5/8) 19 (3/4) 25 (1) 38 (3/2) 50 (2) 76 (3) Selas de Berl Densidade (g/m 3 ) Quantidade (peças/m 3 ) a s : área superficial (m 2 /m 3 ) Selas Berl
43 Tabela 3: Características de recheios estruturados metálicos de alta eficiência. Características Mellapa 250 ( placa perfuradas ) Sulzer-BX ( telas ) ltura da corrugação, h, (mm) 12,7 6,4 Base do canal, B, (mm) 25,4 12,7 ado do canal, S, (mm) 18,0 8,9 Raio hidráulico, rh, (mm) -- 1,8 Diâmetro equivalente, d e, (mm) 14,2 7,2 a s : Área superficial (m 2 /m 3 ) Porosidade 0,93 0,90 Ângulo de escoamento com horizontal, h B 43
44 Eemplo 02: Para um sistema diluído em que o componente é transferido da fase líquida à gasosa (torres de desabsorção), a relação de equilíbrio é dada por i = 0,75 i. Em um certo ponto do equipamento eperimental, o líquido contém 90% em mols de e a composição de nas fase gasosa é de 45% em mols. O coeficiente individual de transferência de massa do filme gasoso é 2,710-3 gmol/(m 2.s. ) e a resistência individual da fase gasosa é 60% da global. Determine: a) O coeficiente global K ; b) s concentrações interfaciais de nas duas fases; c) O fluo molar de. Solução: a) G Dados: Coeficiente individual da fase gasosa: = 2,710-3 gmol/(m 2.s. ) Reta de equilíbrio: i = 0,75 i Frações molares de no seio da mistura e da solução em um ponto específico da coluna: no seio do gás: G = 0,45; no seio do líquido: = 0,90 Informações sobre as resistências: 1/ = 0,60(1/K ) 44
45 Portanto, o coeficiente global de transferência de massa na fase gasosa é obtido por: K = 0,6 = 0,6 2,710-3 gmol/(m 2.s. ) = 1, gmol/(m 2.s. ) b) i e i? Essas frações se relacionam com as resistências dada pela equação (5): G G i i i = 0,75 i Substituindo os valores, temos: 2, ,45 0,90 0,75 Para calcular i devemos determinar o valor de pela equação (16), com m = 0,75: i i G 1 K 1 m 1 1, , ,75 = 3, gmol/(m 2.s. ) 45
46 Portanto, tendo os valores de e de, temos: 3,0410 0,45 0,75-3 i -3 2,710 0,90 i 0,78 i i 0,75 0,750,78 0,585 i i c) Visto que G, o fluo é N,Z = ( i ). ssim sendo, podemos substituir nessa epressão os valores de, e i, possibilitando determinar o valor do fluo molar de : N N,Z,Z (3,0410 3, ) 0,9 gmol/(m 0,78 2.s) 46
47 Coeficientes volumétricos de transferência de massa para torre de recheios Os fluos dados pelas equações (3), (5), (8) e (9) são obtidos pressupondo que se conheça a área onde está havendo o transporte do soluto. Pelas Figuras (2) e (3), nota-se que essas áreas estão relacionadas às das gotas (Torre de spra) e das bolhas (Torre de borbulhamento), respectivamente. Em se tratando de uma coluna de recheio, percebe-se a dificuldade para fiar a área interfacial de contato entre as fases, principalmente pelo fato de haver inúmeros tipos de recheios. Para considerar o efeito da presença de tais áreas na taa ou fluo de transferência de massa, introduz-se um fator empírico a nas equações de fluo de matéria. Esse fator, conhecido como área interfacial específica para transferência de massa, é dado por: a área interfacial para transferência de massa unidade de volume da torre No caso de recheios estruturados de alta eficiência essas áreas são praticamente equivalentes, o que não acontece quando se trabalha com recheios randômicos, os quais apresentam área a menor que a área superficial do recheio (a s ). 47
48 Para colunas recheadas, destinadas a qualquer técnica de separação, deve-se utilizar os coeficientes volumétricos de transferência de massa (ou coeficiente de capacidade de transferência de massa). Para a técnica de separação G, temos: N, Za a G i ( 20 ) onde a é o coeficiente de capacidade individual de transferência de massa ou coeficiente volumétrico de transferência de massa. a (volume) (tempo) mols de (força motriz em função da fração molar de ) Para o fluo global, referenciado à fase gasosa, tem-se a correção na equação (18): N a, Z K a G * ( 21 ) onde K a é o coeficiente de capacidade global de transferência de massa ou coeficiente volumétrico global de transferência de massa, com as mesmas unidades de a.
49 Como consequência, as relações entre as resistências individuais e globais são postas como: G 1 K a 1 a m a ( 22 ) G 1 K a 1 m a 1 a ( 23 ) pesar dos coeficientes de transferência de massa ( ou K) e área interfacial efetiva de transferência de massa (a) comporem os coeficientes volumétricos de transferência de massa (a ou Ka), vimos que as condições operacionais da coluna os influenciam de maneiras diferenciadas. estimativa dos coeficientes volumétricos advém da composição das correlações de Onda et al (1968), equações (24) e (25) ou (26); assim como da combinação entre as equações (24)-(25), para a fase G; e (24)-(26), para a fase.
50 a a W s Re Fr We c c c c Onda et al.(1968) para recheios randômicos com a/a 1,0 u a ν s asu g 2 ρu a s 2 c ep 1,45 (Renolds) (Froud) (Weber) ; 0,3 75 dinas/cm (aço) ; ; 0,04 2,510 1,210 c c c 0,75-9 / Re -8 c 0,1 Re Fr We 2 Fr 0,05 We 500 1,810 0,27 56 dinas/cm (carvão); 61dinas/cm (cerâmica) 33 dinas/cm (polietileno); 20 dinas/cm (parafina) 0,2-2 w 1 73 dinas/cm (vidro); 40 dinas/cm (cloreto de polivinila) ( 24 ) equação (24) é aplicada em absorção; destilação em escala de laboratório, com recheios: anéis de Raschig, selas de Berl e esferas, com erro absoluto médio de 22%. 50
51 Re Onda et al. (1968) 5,23a u a ν s G G s D B G (d s a s ) (Renolds) para 2,0 ; P RT Sc recheios G 0,7 ReG Sc νg D B randômicos G 1/3 G (fase gasosa) (Schmidt) ( 25 ) equação (25) é aplicada em absorção; destilação em escala de laboratório. Para anéis de Raschig e selas de Berl com diâmetro nominal menor do que 15mm, utilizar a constante 2,0 no lugar de 5,23 na equação (25). equação (26) é recomendada para líquidos não-viscosos. Re 5,110 u a ν s 3 Onda ρ M (gν (Renolds) et al.(1968) ) 1/3 ; para 0,4 a (dsas) a ν Sc D recheios B s w Re 2/3 Sc (Schmidt) randômicos 1/ 2 (fase líquida) ( 26 ) 51
52 a a s Re 0,5 9,8 z ug a ν s G Bravo e Fair (1982) para recheios randômicos 6Re Ca (Renolds) ; Ca Re Ca ; (N/m) G 0,5 0,4 G 0,392 u ν (capilaridade admensiona l) ( 27 ) equação (27) é utilizada para destilação em escala industrial; 11 sistemas distintos; recheios: anéis Pall; faia de aplicação para o diâmetro nominal de recheio: 13mm a 76mm; erro absoluto médio de 22%. Na impossibilidade de se determinar, na prática, os coeficientes individuais ( e/ou ) e a área interfacial específica (a) para transferência de massa ou na hipótese de não se dispor de informações para uma situação particular, sobre esses parâmetros, pode-se utilizar as correlações para o coeficiente volumétrico individual de transferência de massa ( a), conforme equações a seguir: 52
53 ρ u 530DB M ν a Normam (1961) Fase líquida 0,75 Sc 1/2 ( 28 ) equação (28) é baseada nos trabalhos de Sherwood e Hollowa (1940) e Moltad et al. (1942). Entretanto, Sherwood e Hollowa utilizaram uma coluna de 50,8 cm de diâmetro. Válida para recheios tipos anéis, selas. Erro absoluto médio de 22%. ρ M 0,5 a 0,0025 Sc u a Mohunta 0,1 u 0, ,6 et al (1969) Fase líquida u G Sc D d ρ ρ C S G s 3/4 42 g/m 1,22 g/m 1055 νa g 150 mm 15,1cm 2 s.s 2 2 / 3.s ν g 2 5/36 ( 29 ) 53
54 Eemplo 03: Construiu-se uma torre de recheios na intenção de absorver CO 2 do ar, utilizando-se água pura a 20C como solvente e com velocidade superficial igual a 0,013 m/s, assim como anéis de Raschig cerâmicos de 13 mm. Considerando que o dióido de carbono esteja diluído em relação aos inertes das duas fases e sabendo que a fase líquida é que controla a operação, estime o coeficiente volumétrico individual de transferência de massa utilizando as correlações apresentadas anteriormente. Dados: g = 9,81 m/s 2 e visto o CO 2 estar diluído em água, as propriedades da corrente líquida serão tomadas como sendo às da água. Tabela a seguir apresenta os dados da literatura para água. Obs.: = tensão superficial da água a 20C = massa específica da água a 20 C = viscosidade cinemática da água a 20 C D B = coeficiente de difusão do CO 2 dissolvido na água a 20 C ρ (g/m 3 ) ν (m 2 /s) (N/m) M (g/gmol) D B (m 2 /s) 998,2 1, , ,015 1,
55 Solução: Considerando os dados fornecidos pelo problema e as equações vistas anteriormente, temos: - Cálculo do coeficiente volumétrico individual de transferência de massa: ρ u 530DB M ν a Normam (1961) Fase líquida 0,75 Sc 1/2 ( 1 ) Com os dados fornecidos, temos: Sc Sc ν D B 1,0110 1,6910 (Número de Schmidt) ,63 ( 2 ) 55
56 Sabendo que u = 0,013 m/s (velocidade superficial da água), substituiremos as informações presentes na Tabela deste eemplo em conjunto com (2) e (1): 9 a 5301, ,63 a 1,466 gmol/m 3.s 998,2 0,013 18,0151, ,75 1/2 Mohunta et al (1969) Fase líquida ρ M 0,5 a 0,0025 Sc u a s 3/4 νa g s 2/3 ν g 2 5/36 ( 3 ) Sabendo que u = 0,013 m/s, g = 9,81 m/s 2 e a s =400 m 2 /m 3 (Tabela 1), temos: 6 998,2 0,5 3/4 1, a 0,0025 (593,67) 0, a 18,015 1,28 gmol/m 3.s 9,81 2/3 1, ,81-6 5/36 56
57 Onda 5,110 et al.(1968) 3 ρ M (gν para ) 1/3 (d recheios s a s ) 0,4 a a s w randômicos Observe que necessitamos determinar a área molhada a W, a qual advém da equação (22): Re 2/3 Sc 1/ 2 ( 4 ) Onda a a W s et al.(1968) 1,0 Cálculo da área molhada a w : u Re a ν Fr We s a su g para recheios randômicos com a/a c ep1,45 s 2 ρu a 2 0,013 0, , ,013 9,81 998,20,013 Re , ,1 Fr 6,8910 We 0,05 0,2 32, , w 1 ( 5 ) ( 6 ) ( 7 ) ( 8 )
58 Com o valor de c = N/m (recheio cerâmico) obtido da Tabela da equação (24), temos: c , ,842 ( 9 ) Substituindo os resultados das equações (6) a (9) em (5), temos: a a a a W s W s 1,0 0,562 ep 1,45 0,75 0,1 3 0,842 32,178 6,8910 0,05 3 5,8210 0,2 Visto que a s = 400 m 2 /m 3, temos: a W , ,8 m / m ( 10 )
59 Cálculo do coeficiente individual de transferência de massa, após substituir o resultado da equação (6) e (10) em (4). 5, , ,2 18,015 gmol/m -6 1/3 3 0, ,178 9,81 1, s ( 11 ) 224,8 2/3 597,63 0,5 O valor do coeficiente volumétrico individual da fase líquida é obtido do produto dos resultados (10) e (11) considerando a = a w : a 224,8 m / m 7,1310 gmol/m.s 3 a 1,603 gmol/m.s Esse valor de ( a) provavelmente está superestimado, pois o modelo de Onda et al. (1968) assume a/a w = 1. No fenômeno de adsorção física, como é o caso deste eemplo, a relação entre áreas é a/a w 1. 59
Dimensionamento de Colunas
 de Colunas Coluna Recheada Prof. Universidade Federal do Pampa BA310 Curso de Engenharia Química Campus Bagé 04 de outubro de 2016 Colunas Recheadas 1 / 37 Introdução Colunas Recheadas 2 / 37 Introdução
de Colunas Coluna Recheada Prof. Universidade Federal do Pampa BA310 Curso de Engenharia Química Campus Bagé 04 de outubro de 2016 Colunas Recheadas 1 / 37 Introdução Colunas Recheadas 2 / 37 Introdução
3 Modelagem Física e Matemática
 3 Modelagem Física e Matemática omo mencionado no capítulo introdução, o objetivo do presente trabalho consiste em identificar a importância dos mecanismos de absorção química para previsão da absorção
3 Modelagem Física e Matemática omo mencionado no capítulo introdução, o objetivo do presente trabalho consiste em identificar a importância dos mecanismos de absorção química para previsão da absorção
Roteiro das Práticas 1 a 3
 Roteiro das Práticas 1 a 3 Destilação e Absorção/Umidificação Prof. Universidade Federal do Pampa Curso de Engenharia Química Campus Bagé 10 de agosto de 2017 Destilação e Absorção 1 / 13 Operações por
Roteiro das Práticas 1 a 3 Destilação e Absorção/Umidificação Prof. Universidade Federal do Pampa Curso de Engenharia Química Campus Bagé 10 de agosto de 2017 Destilação e Absorção 1 / 13 Operações por
20/11/2015. Absorção de Ácido Nítrico
 FINALIDADE: A absorção de gases (designada em língua inglesa por GasAbsorption ou ainda por Scrubbing ) é uma operação destinada a remover preferencialmente um ou mais componentes de uma mistura gasosa
FINALIDADE: A absorção de gases (designada em língua inglesa por GasAbsorption ou ainda por Scrubbing ) é uma operação destinada a remover preferencialmente um ou mais componentes de uma mistura gasosa
PRINCÍPIOS DO TRANSPORTE DE MASSA...
 Sumário Capítulo 1 PRINCÍPIOS DO TRANSPORTE DE MASSA...1 1.1 Mecanismo do Transporte de Massa....1 1.1.1 Velocidade de Difusão....1 1.1.2 Difusão Molecular....3 1.1.2.1 Difusividade...3 1.1.3 Difusão em
Sumário Capítulo 1 PRINCÍPIOS DO TRANSPORTE DE MASSA...1 1.1 Mecanismo do Transporte de Massa....1 1.1.1 Velocidade de Difusão....1 1.1.2 Difusão Molecular....3 1.1.2.1 Difusividade...3 1.1.3 Difusão em
Curso de Farmácia. Operações Unitárias em Indústria Prof.a: Msd Érica Muniz 6 /7 Período DESTILAÇÃO Parte 2
 Curso de Farmácia Operações Unitárias em Indústria Prof.a: Msd Érica Muniz 6 /7 Período DESTILAÇÃO Parte 2 1 Destilação Fracionada As operações até agora descritas propiciam pouco enriquecimento do vapor
Curso de Farmácia Operações Unitárias em Indústria Prof.a: Msd Érica Muniz 6 /7 Período DESTILAÇÃO Parte 2 1 Destilação Fracionada As operações até agora descritas propiciam pouco enriquecimento do vapor
Curso de Engenharia Química. Prof. Rodolfo Rodrigues. Formulário para a Prova 1 11/10/2016
 Curso de Engenharia Química Operações Unitárias II 206/2 Prof. Rodolfo Rodrigues Formulário para a Prova /0/206 Destilação Flash ˆ Volatilidade relativa: F, z Flash V, y α AB = K A K B = y A/x A y B /x
Curso de Engenharia Química Operações Unitárias II 206/2 Prof. Rodolfo Rodrigues Formulário para a Prova /0/206 Destilação Flash ˆ Volatilidade relativa: F, z Flash V, y α AB = K A K B = y A/x A y B /x
) (8.20) Equipamentos de Troca Térmica - 221
 onde: v = &m = Cp = h lv = U = A = T = t = volume específico vazão em massa (Kg/h) calor específico calor latente de vaporização coeficiente global de troca térmica área de transmissão de calor temperatura
onde: v = &m = Cp = h lv = U = A = T = t = volume específico vazão em massa (Kg/h) calor específico calor latente de vaporização coeficiente global de troca térmica área de transmissão de calor temperatura
Tabela 5.1- Características e condições operacionais para a coluna de absorção. Altura, L Concentração de entrada de CO 2, C AG
 5 Resultados Neste capítulo, são apresentados sob forma de tabelas os dados operacionais e as propriedades físico-químicas utilizados no processo de absorção CO 2 -MEA. Em seguida são apresentados a comparação
5 Resultados Neste capítulo, são apresentados sob forma de tabelas os dados operacionais e as propriedades físico-químicas utilizados no processo de absorção CO 2 -MEA. Em seguida são apresentados a comparação
Prof. MSc. David Roza José 1/26
 1/26 Mecanismos Físicos A condensação ocorre quando a temperatura de um vapor é reduzida para abaixo da temperatura de saturação. Em equipamentos industriais o processo normalmente decorre do contato entre
1/26 Mecanismos Físicos A condensação ocorre quando a temperatura de um vapor é reduzida para abaixo da temperatura de saturação. Em equipamentos industriais o processo normalmente decorre do contato entre
Curso de Engenharia Química. Prof. Rodolfo Rodrigues
 Curso de Engenharia Química Operações Unitárias II 26/2 Prof. Rodolfo Rodrigues Lista 5: Absorção e Regeneração Exercício * (Geankoplis, 23, Exemplo.3-2) Deseja-se absorver 9% da acetona de uma corrente
Curso de Engenharia Química Operações Unitárias II 26/2 Prof. Rodolfo Rodrigues Lista 5: Absorção e Regeneração Exercício * (Geankoplis, 23, Exemplo.3-2) Deseja-se absorver 9% da acetona de uma corrente
EM-524 : aula 13. Capítulo 06 Escoamento Externo Efeitos Viscosos e Térmicos
 EM-54 : aula Capítulo 06 Escoamento Eterno Efeitos Viscosos e érmicos 6.6 Coeficiente de ransferência de Calor por Convecção; 6.7 ransferência de Calor por Convecção Forçada; 6.8 ransferência de Calor
EM-54 : aula Capítulo 06 Escoamento Eterno Efeitos Viscosos e érmicos 6.6 Coeficiente de ransferência de Calor por Convecção; 6.7 ransferência de Calor por Convecção Forçada; 6.8 ransferência de Calor
P4 PROVA DE QUÍMICA GERAL 02/12/08
 P4 PROVA DE QUÍMICA GERAL 0/1/08 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Constantes e equações: R = 0,08 atm L mol -1 K -1 = 8,314
P4 PROVA DE QUÍMICA GERAL 0/1/08 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Constantes e equações: R = 0,08 atm L mol -1 K -1 = 8,314
Operações Unitárias Parte II
 Operações Unitárias Parte II Apresentação Aula anterior: - Grandezas físicas; - Balanço de massa; - Balanço de energia; - Conversão; - Reciclo; - Rendimento; - Fração convertida; - Umidade relativa; -
Operações Unitárias Parte II Apresentação Aula anterior: - Grandezas físicas; - Balanço de massa; - Balanço de energia; - Conversão; - Reciclo; - Rendimento; - Fração convertida; - Umidade relativa; -
Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 4ª Lista de Exercícios (parte B Extração Líquido-Líquido)
 Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 4ª Lista de Exercícios (parte B Extração Líquido-Líquido) Profº Carlos Henrique Ataíde (novembro de 2013) 1ª) Concurso Petrobras Químico (a)
Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 4ª Lista de Exercícios (parte B Extração Líquido-Líquido) Profº Carlos Henrique Ataíde (novembro de 2013) 1ª) Concurso Petrobras Químico (a)
TRANSPORTE DE MASSA. Alda Simões CEQ / MEF / 2015
 Livro de apoio: Christie Geankoplis, Transport Processes and Unit Operations, 3rd ed, 1993, Prentice Hall, cap 6 TRANSPORTE DE MASSA CEQ / MEF / 2015 Alda Simões Transporte molecular de massa Lei de Fick
Livro de apoio: Christie Geankoplis, Transport Processes and Unit Operations, 3rd ed, 1993, Prentice Hall, cap 6 TRANSPORTE DE MASSA CEQ / MEF / 2015 Alda Simões Transporte molecular de massa Lei de Fick
EVAPORAÇÃO. Profa. Marianne Ayumi Shirai EVAPORAÇÃO
 Universidade Tecnológica Federal do Paraná Campus Londrina Operações Unitárias na Indústria de Alimentos EVAPORAÇÃO Profa. Marianne Ayumi Shirai EVAPORAÇÃO É a remoção parcial da água de mistura de líquidos,
Universidade Tecnológica Federal do Paraná Campus Londrina Operações Unitárias na Indústria de Alimentos EVAPORAÇÃO Profa. Marianne Ayumi Shirai EVAPORAÇÃO É a remoção parcial da água de mistura de líquidos,
Dimensionamento de Colunas
 Dimensionamento de Colunas Coluna de Pratos Prof. Universidade Federal do Pampa BA310 Curso de Engenharia Química Campus Bagé 27 de setembro de 2016 Colunas de Pratos 1 / 30 Introdução Colunas de Pratos
Dimensionamento de Colunas Coluna de Pratos Prof. Universidade Federal do Pampa BA310 Curso de Engenharia Química Campus Bagé 27 de setembro de 2016 Colunas de Pratos 1 / 30 Introdução Colunas de Pratos
UNIVERSIDADE DE SÃO PAULO ENGENHARIA QUÍMICA LOQ4085 OPERAÇÕES UNITÁRIAS I
 UNIVERSIDADE DE SÃO PAULO ENGENHARIA QUÍMICA LOQ4085 OPERAÇÕES UNITÁRIAS I Profa. Lívia Chaguri E-mail: lchaguri@usp.br Conteúdo Bombas Parte 1 - Introdução - Classificação - Bombas sanitárias - Condições
UNIVERSIDADE DE SÃO PAULO ENGENHARIA QUÍMICA LOQ4085 OPERAÇÕES UNITÁRIAS I Profa. Lívia Chaguri E-mail: lchaguri@usp.br Conteúdo Bombas Parte 1 - Introdução - Classificação - Bombas sanitárias - Condições
Transmissão de Calor I - Prof. Eduardo Loureiro
 Camada limite de velocidade As partículas de fluido em contato com a superfície têm velocidade nula. Essas partículas atuam no retardamento do movimento das partículas da camada de fluido adjacente superior
Camada limite de velocidade As partículas de fluido em contato com a superfície têm velocidade nula. Essas partículas atuam no retardamento do movimento das partículas da camada de fluido adjacente superior
Catálise heterogênea. Catalisador sólido. Reação na interface sólido-fluido
 Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
Catálise heterogênea Catalisador sólido Reação na interface sólido-fluido Tipos de catalisadores Poroso: elevada área superficial Tipos de catalisadores Peneiras moleculares: capacidade de distinção entre
3 Introdução à Transferência de Massa. 7a. Aula
 3 Introdução à Transferência de Massa 7a. Aula Transporte Molecular Transporte de Energia (condução) Transporte de Massa (difusão) Exemplo: vidro de perfume aberto numa sala com ar parado Transporte Molecular
3 Introdução à Transferência de Massa 7a. Aula Transporte Molecular Transporte de Energia (condução) Transporte de Massa (difusão) Exemplo: vidro de perfume aberto numa sala com ar parado Transporte Molecular
Utilizado quando se necessita rejeitar calor a baixas temperaturas. O uso do AR como meio de resfriamento tem as seguintes vantagens:
 TROCADORES DE CALOR ALETADOS E/OU COMPACTOS Utilizado quando se necessita rejeitar calor a baixas temperaturas. Pode-se utilizar como meios de resfriamento: ÁGUA ou AR O uso do AR como meio de resfriamento
TROCADORES DE CALOR ALETADOS E/OU COMPACTOS Utilizado quando se necessita rejeitar calor a baixas temperaturas. Pode-se utilizar como meios de resfriamento: ÁGUA ou AR O uso do AR como meio de resfriamento
TRATAMENTO DE BIOGÁS PARA ATENUAR O EFEITO CORROSIVO
 TRATAMENTO DE BIOGÁS PARA ATENUAR O EFEITO CORROSIVO F. G. M. PORTO 1, M. L. BEGNINI 1 e J. R. D. FINZER 1 1 Universidade de Uberaba, Curso de Engenharia Química fabriciomenezesporto@hotmail.com RESUMO
TRATAMENTO DE BIOGÁS PARA ATENUAR O EFEITO CORROSIVO F. G. M. PORTO 1, M. L. BEGNINI 1 e J. R. D. FINZER 1 1 Universidade de Uberaba, Curso de Engenharia Química fabriciomenezesporto@hotmail.com RESUMO
Condensação
 Condensação Condensação Condensação Condensação Condensação Condensação em Filme Tal como no caso de convecção forçada, a transferência de calor em condensação depende de saber se o escoamento é laminar
Condensação Condensação Condensação Condensação Condensação Condensação em Filme Tal como no caso de convecção forçada, a transferência de calor em condensação depende de saber se o escoamento é laminar
PARTÍCULAS SÓLIDAS PARA AS OPERAÇÕES ABAIXO, O CONHECIMENTO DAS PROPRIEDADES DAS PARTÍCULAS SÓLIDAS É FUNDAMENTAL:
 PARTÍCULAS SÓLIDAS PARA AS OPERAÇÕES ABAIXO, O CONHECIMENTO DAS PROPRIEDADES DAS PARTÍCULAS SÓLIDAS É FUNDAMENTAL: FRAGMENTAÇÃO PENEIRAMENTO FLUIDIZAÇÃO MISTURA ARMAZENAMENTO SEPARAÇÕES MECÂNICAS ESCOAMENTO
PARTÍCULAS SÓLIDAS PARA AS OPERAÇÕES ABAIXO, O CONHECIMENTO DAS PROPRIEDADES DAS PARTÍCULAS SÓLIDAS É FUNDAMENTAL: FRAGMENTAÇÃO PENEIRAMENTO FLUIDIZAÇÃO MISTURA ARMAZENAMENTO SEPARAÇÕES MECÂNICAS ESCOAMENTO
Experimento 3. Determinação do coeficiente de difusão em fase gasosa em regime pseudoestacionário. Prof. Dr. Gilberto Garcia Cortez
 Experimento 3 eterminação do coeficiente de difusão em fase gasosa em regime pseudoestacionário. Prof. r. Gilberto Garcia Cortez Introdução Um método simples e bastante preciso para a determinação de difusividade
Experimento 3 eterminação do coeficiente de difusão em fase gasosa em regime pseudoestacionário. Prof. r. Gilberto Garcia Cortez Introdução Um método simples e bastante preciso para a determinação de difusividade
P1 - PROVA DE QUÍMICA GERAL 09/04/11
 P1 - PROVA DE QUÍMICA GERAL 09/04/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) =
P1 - PROVA DE QUÍMICA GERAL 09/04/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) =
Lista de exercícios Caps. 7 e 8 TMEC-030 Transferência de Calor e Massa Período especial 2017/2
 Lista de exercícios Caps. 7 e 8 TMEC-030 Transferência de Calor e Massa Período especial 2017/2 1. (Incropera et al., 6 ed., 7.2) Óleo de motor a 100ºC e a uma velocidade de 0,1 m/s escoa sobre as duas
Lista de exercícios Caps. 7 e 8 TMEC-030 Transferência de Calor e Massa Período especial 2017/2 1. (Incropera et al., 6 ed., 7.2) Óleo de motor a 100ºC e a uma velocidade de 0,1 m/s escoa sobre as duas
Capítulo 6: Escoamento Externo Hidrodinâmica
 Capítulo 6: Escoamento Externo Hidrodinâmica Conceitos fundamentais Fluido É qualquer substância que se deforma continuamente quando submetido a uma tensão de cisalhamento, ou seja, ele escoa. Fluidos
Capítulo 6: Escoamento Externo Hidrodinâmica Conceitos fundamentais Fluido É qualquer substância que se deforma continuamente quando submetido a uma tensão de cisalhamento, ou seja, ele escoa. Fluidos
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Escoamento Interno Viscoso
 Escoamento Interno Viscoso Escoamento Laminar e Turbulento Número de Reynolds Re VD ρ --> massa específica ou densidade V --> velocidade D --> comprimento característico μ --> viscosidade numero de Reynolds
Escoamento Interno Viscoso Escoamento Laminar e Turbulento Número de Reynolds Re VD ρ --> massa específica ou densidade V --> velocidade D --> comprimento característico μ --> viscosidade numero de Reynolds
Escoamento completamente desenvolvido
 Escoamento completamente desenvolvido A figura mostra um escoamento laminar na região de entrada de um tubo circular. Uma camada limite desenvolve-se ao longo das paredes do duto. A superfície do tubo
Escoamento completamente desenvolvido A figura mostra um escoamento laminar na região de entrada de um tubo circular. Uma camada limite desenvolve-se ao longo das paredes do duto. A superfície do tubo
Universidade Estadual de São Paulo Escola de Engenharia de Lorena. Importância da Transferência de Oxigênio
 Universidade Estadual de São Paulo Escola de Engenharia de Lorena Importância da Transferência de Oxigênio Agitação e aeração Para todos os processos aeróbios é necessário o dimensionamento adequado do
Universidade Estadual de São Paulo Escola de Engenharia de Lorena Importância da Transferência de Oxigênio Agitação e aeração Para todos os processos aeróbios é necessário o dimensionamento adequado do
Transferência de Massa
 Transferência de Massa Docente: Prof. José Joaquim C. Cruz Pinto Ano Lectivo: 2003/2004 Curso(s): Licenciatura em Engenharia Química Escolaridade: 2h T - 2h TP - 0h P Unidades de Crédito: 3.5 O B J E C
Transferência de Massa Docente: Prof. José Joaquim C. Cruz Pinto Ano Lectivo: 2003/2004 Curso(s): Licenciatura em Engenharia Química Escolaridade: 2h T - 2h TP - 0h P Unidades de Crédito: 3.5 O B J E C
OPERAÇÕES UNITÁRIAS II AULA 4: - DIMENSIONAMENTO DE TROCADORES DE CALOR A
 OPERAÇÕES UNITÁRIAS II AULA 4: - DIMENSIONAMENTO DE TROCADORES DE CALOR A PLACAS - ANÁLISE DE TROCADORES: MLDT E NUT Profa. Dra. Milena Martelli Tosi TROCADOR DE CALOR A PLACAS http://rpaulsingh.com/animations/plateheat
OPERAÇÕES UNITÁRIAS II AULA 4: - DIMENSIONAMENTO DE TROCADORES DE CALOR A PLACAS - ANÁLISE DE TROCADORES: MLDT E NUT Profa. Dra. Milena Martelli Tosi TROCADOR DE CALOR A PLACAS http://rpaulsingh.com/animations/plateheat
OPERAÇÕES UNITÁRIAS II AULA 1: REVISÃO TRANSFERÊNCIA DE CALOR. Profa. Dra. Milena Martelli Tosi
 OPERAÇÕES UNITÁRIAS II AULA 1: REVISÃO TRANSFERÊNCIA DE CALOR Profa. Dra. Milena Martelli Tosi A IMPORTÂNCIA DA TRANSFERÊNCIA DE CALOR NA INDÚSTRIA DE ALIMENTOS Introdução Revisão: Mecanismos de transferência
OPERAÇÕES UNITÁRIAS II AULA 1: REVISÃO TRANSFERÊNCIA DE CALOR Profa. Dra. Milena Martelli Tosi A IMPORTÂNCIA DA TRANSFERÊNCIA DE CALOR NA INDÚSTRIA DE ALIMENTOS Introdução Revisão: Mecanismos de transferência
Lista de Exercícios Perda de Carga Localizada e Perda de Carga Singular
 Lista de Exercícios Perda de Carga Localizada e Perda de Carga Singular 1. (Petrobrás/2010) Um oleoduto com 6 km de comprimento e diâmetro uniforme opera com um gradiente de pressão de 40 Pa/m transportando
Lista de Exercícios Perda de Carga Localizada e Perda de Carga Singular 1. (Petrobrás/2010) Um oleoduto com 6 km de comprimento e diâmetro uniforme opera com um gradiente de pressão de 40 Pa/m transportando
Fenômenos de Transporte
 Fenômenos de Transporte Introdução a Fenômenos de Transporte Prof. Dr. Felipe Corrêa Introdução a Fenômenos de Transporte Fenômenos de Transporte Refere-se ao estudo sistemático e unificado da transferência
Fenômenos de Transporte Introdução a Fenômenos de Transporte Prof. Dr. Felipe Corrêa Introdução a Fenômenos de Transporte Fenômenos de Transporte Refere-se ao estudo sistemático e unificado da transferência
HIDROMETALURGIA E ELETROMETALURGIA
 A melhoria das propriedades das resinas orgânicas incentivou a aplicação para o processo de troca iônica devido a sua estabilidade e elevada capacidade. As primeiras tentativas para aplicação da troca
A melhoria das propriedades das resinas orgânicas incentivou a aplicação para o processo de troca iônica devido a sua estabilidade e elevada capacidade. As primeiras tentativas para aplicação da troca
Torres. Unidade 1. Monitoramento e controle de processos. Construção ...
 Unidade 1 A Torres s torres, também denominadas colunas, servem para realizar destilação, absorção e retificação, extração, reações etc. Construção São compostas de um casco cilíndrico vertical, fechado
Unidade 1 A Torres s torres, também denominadas colunas, servem para realizar destilação, absorção e retificação, extração, reações etc. Construção São compostas de um casco cilíndrico vertical, fechado
TÉCNICAS AVANÇADAS DE MODELAÇÃO E SIMULAÇÃO
 Universidade de Coimbra Faculdade de Ciência e Tecnologia Departamento de Engenharia Química TÉCNICAS AVANÇADAS DE MODELAÇÃO E SIMULAÇÃO PROFESSOR NUNO DE OLIVEIRA MODELAGEM DE UM SEPARADOR POR MEMBRANA
Universidade de Coimbra Faculdade de Ciência e Tecnologia Departamento de Engenharia Química TÉCNICAS AVANÇADAS DE MODELAÇÃO E SIMULAÇÃO PROFESSOR NUNO DE OLIVEIRA MODELAGEM DE UM SEPARADOR POR MEMBRANA
Termodinâmica. Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos. QUÍMICA GERAL Fundamentos
 Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos 1 Calor e Trabalho Calor e trabalho são formas relacionadas de energia Calor pode ser convertido em trabalho
Termodinâmica é o estudo das mudanças de energia que acompanham os processos físicos e químicos 1 Calor e Trabalho Calor e trabalho são formas relacionadas de energia Calor pode ser convertido em trabalho
C + 2H 2 CH 4. 3 o LISTA DE EXERCÍCIOS DE TRANSFERÊNCIA DE MASSA. Prof. Dr. Gilberto Garcia Cortez
 3 o LIST DE EXEÍIOS DE TNSFEÊNI DE MSS 1- Em um reator catalítico, partículas de carbono em forma de cilindro são consumidas pela passagem de um fluxo de hidrogênio para formar metano através da seguinte
3 o LIST DE EXEÍIOS DE TNSFEÊNI DE MSS 1- Em um reator catalítico, partículas de carbono em forma de cilindro são consumidas pela passagem de um fluxo de hidrogênio para formar metano através da seguinte
Extração e Purificação do Limoneno Parte II
 Extração e Purificação do Limoneno Parte II Alan Cesar Pilon Andrey Pinheiro Técnicas para extração e purificação do Limoneno Extração com Solvente Destilação por arraste de vapor Destilação Fracionada
Extração e Purificação do Limoneno Parte II Alan Cesar Pilon Andrey Pinheiro Técnicas para extração e purificação do Limoneno Extração com Solvente Destilação por arraste de vapor Destilação Fracionada
Prática 10 Determinação da constante de equilíbrio entre íons Fe 3+ e SCN -
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
OPERAÇÕES UNITÁRIAS II AULA 9: EVAPORAÇÃO EM SIMPLES EFEITO. Profa. Dra. Milena Martelli Tosi
 OPERAÇÕES UNITÁRIAS II AULA 9: EVAPORAÇÃO EM SIMPLES EFEITO Profa. Dra. Milena Martelli Tosi EVAPORAÇÃO EM SIMPLES EFEITO Características da evaporação e do líquido a ser evaporado Principais tipos de
OPERAÇÕES UNITÁRIAS II AULA 9: EVAPORAÇÃO EM SIMPLES EFEITO Profa. Dra. Milena Martelli Tosi EVAPORAÇÃO EM SIMPLES EFEITO Características da evaporação e do líquido a ser evaporado Principais tipos de
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos
 Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
Equilíbrio Químico. Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação
 Equilíbrio Químico 1 Equilíbrio Químico Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação Equilíbrio dinâmico: as reações direta e inversa ocorrem
Equilíbrio Químico 1 Equilíbrio Químico Estágio da reação química em que não existe mais tendência a mudar a composição da mistura de uma reação Equilíbrio dinâmico: as reações direta e inversa ocorrem
Metal, Não Metal e Metaloide
 Metal, Não Metal e Metaloide 1 Metal, Não Metal e Metaloide Metal: conduz eletricidade, tem brilho, é maleável e dúctil Ex: cobre Não metal: não... Ex: Enxofre Metaloide: aparência e algumas propriedades
Metal, Não Metal e Metaloide 1 Metal, Não Metal e Metaloide Metal: conduz eletricidade, tem brilho, é maleável e dúctil Ex: cobre Não metal: não... Ex: Enxofre Metaloide: aparência e algumas propriedades
ESZO Fenômenos de Transporte
 Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Propriedades Termodinâmicas Propriedades Termodinâmicas
Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Propriedades Termodinâmicas Propriedades Termodinâmicas
Estudo Físico-Químico dos Gases
 19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
Capítulo 7 Introdução à Convecção Mássica
 Prof. Dr. Édler L. de lbuquerque, Eng. Química IFB Prof. Dr. Édler L. de lbuquerque, Eng. Química IFB 04/10/017 Transf. de Massa - ENG 54, apítulo 7 Transferência de Massa ENG 54 apítulo 7 Introdução à
Prof. Dr. Édler L. de lbuquerque, Eng. Química IFB Prof. Dr. Édler L. de lbuquerque, Eng. Química IFB 04/10/017 Transf. de Massa - ENG 54, apítulo 7 Transferência de Massa ENG 54 apítulo 7 Introdução à
Capítulo 9 - Convecção Natural
 Capítulo 9 - Convecção Natural Movimento do fluido ocorre quando a força de corpo age num fluido com gradiente de densidade (causado por eemplo por Δ) força de empuo Velocidades são menores do que na convecção
Capítulo 9 - Convecção Natural Movimento do fluido ocorre quando a força de corpo age num fluido com gradiente de densidade (causado por eemplo por Δ) força de empuo Velocidades são menores do que na convecção
1) A principal caracterís0ca de uma solução é:
 1) A principal caracterís0ca de uma solução é: a) possuir sempre um líquido com outra substância dissolvida. b) ser um sistema com mais de uma fase. c) ser homogênea ou heterogênea, dependendo das condições
1) A principal caracterís0ca de uma solução é: a) possuir sempre um líquido com outra substância dissolvida. b) ser um sistema com mais de uma fase. c) ser homogênea ou heterogênea, dependendo das condições
Transferência de Massa
 Transferência de Massa Docente: Prof. José Joaquim C. Cruz Pinto Ano Lectivo: 2005/2006 Curso(s): Licenciatura em Engenharia Química Escolaridade: 2h T - 2h TP - 0h P Unidades de Crédito: 3.5 O B J E C
Transferência de Massa Docente: Prof. José Joaquim C. Cruz Pinto Ano Lectivo: 2005/2006 Curso(s): Licenciatura em Engenharia Química Escolaridade: 2h T - 2h TP - 0h P Unidades de Crédito: 3.5 O B J E C
Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 2ª Lista de Exercícios (parte A) Profº Carlos Henrique Ataíde (julho de 2013)
 Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 2ª Lista de Exercícios (parte A) Profº Carlos Henrique Ataíde (julho de 2013) 1) Concurso Petrobras: Engenheiro de Processamento Junior (questão
Faculdade de Engenharia Química (FEQUI) Operações Unitárias 2 2ª Lista de Exercícios (parte A) Profº Carlos Henrique Ataíde (julho de 2013) 1) Concurso Petrobras: Engenheiro de Processamento Junior (questão
ESZO Fenômenos de Transporte
 Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Mecanismos de Transferência de Calor Calor Calor pode
Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Mecanismos de Transferência de Calor Calor Calor pode
SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL
 ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL 1. CARACTERÍSTICAS GERAIS DA SOLUÇÃO IDEAL Para
ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL 1. CARACTERÍSTICAS GERAIS DA SOLUÇÃO IDEAL Para
Seminário de química orgânica Experimental I Destilação fracionada do limoneno. Edvan Ferreira de Oliveira Letícia Naomi Higa
 Seminário de química orgânica Experimental I Destilação fracionada do limoneno Edvan Ferreira de Oliveira Letícia Naomi Higa *Introdução *Destilação *Explicação da destilação fracionada *Coluna de fracionamento
Seminário de química orgânica Experimental I Destilação fracionada do limoneno Edvan Ferreira de Oliveira Letícia Naomi Higa *Introdução *Destilação *Explicação da destilação fracionada *Coluna de fracionamento
Controle de Processos Aula: Principais váriaveis em controle de processos químicos
 107484 Controle de Processos Aula: Principais váriaveis em controle de processos químicos Prof. Eduardo Stockler Tognetti Departamento de Engenharia Elétrica Universidade de Brasília UnB 1 o Semestre 2015
107484 Controle de Processos Aula: Principais váriaveis em controle de processos químicos Prof. Eduardo Stockler Tognetti Departamento de Engenharia Elétrica Universidade de Brasília UnB 1 o Semestre 2015
Absorção & Regeneração
 Absorção & Regeneração Prof. Universidade Federal do Pampa BA310 Curso de Engenharia Química Campus Bagé 06 de setembro de 2016 Absorção & Regeneração 1 / 28 Introdução Absorção & Regeneração 2 / 28 Introdução
Absorção & Regeneração Prof. Universidade Federal do Pampa BA310 Curso de Engenharia Química Campus Bagé 06 de setembro de 2016 Absorção & Regeneração 1 / 28 Introdução Absorção & Regeneração 2 / 28 Introdução
ÁREA DE ESTUDO: CÓDIGO 16 TERMODINÂMICA APLICADA, MECÂNICA DOS FLUIDOS E OPERAÇÕES UNITÁRIAS
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO CEARÁ DIRETORIA DE GESTÃO DE PESSOAS COMISSÃO COORDENADORA DE CONCURSOS CONCURSO PÚBLICO PROFESSOR EFETIVO EDITAL Nº 10/DGP-IFCE/2010 ÁREA DE ESTUDO:
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO CEARÁ DIRETORIA DE GESTÃO DE PESSOAS COMISSÃO COORDENADORA DE CONCURSOS CONCURSO PÚBLICO PROFESSOR EFETIVO EDITAL Nº 10/DGP-IFCE/2010 ÁREA DE ESTUDO:
Agitação e mistura. Revisão sobre agitação Exercícios
 Agitação e mistura Revisão sobre agitação Exercícios Material/ objetivo Transporte Mistura Separação Modificação de tamanho Fluidos: líquidos e gases Bombeamento Ventilação ompressão Agitação e Misturas
Agitação e mistura Revisão sobre agitação Exercícios Material/ objetivo Transporte Mistura Separação Modificação de tamanho Fluidos: líquidos e gases Bombeamento Ventilação ompressão Agitação e Misturas
3.ª ED., IST PRESS (2017) ÍNDICE
 ENGENHARIA DE PROCESSOS DE SEPARAÇÃO 3.ª ED., IST PRESS (2017) ÍNDICE PREFÁCO LISTA DE SÍMBOLOS 1 ENGENHARIA DE PROCESSOS DE SEPARAÇÃO1 1.1 Processos de Separação 1.2 Mecanismos de Separação 1.2.1 Separação
ENGENHARIA DE PROCESSOS DE SEPARAÇÃO 3.ª ED., IST PRESS (2017) ÍNDICE PREFÁCO LISTA DE SÍMBOLOS 1 ENGENHARIA DE PROCESSOS DE SEPARAÇÃO1 1.1 Processos de Separação 1.2 Mecanismos de Separação 1.2.1 Separação
7 Resultados. 7.1 Validação modelo simplificado
 55 7 Resultados 7.1 Validação modelo simplificado De acordo com os dados de entrada e da metodologia de cálculo alguns resultados foram extraídos das análises. Primeiramente um comparativo entre o modelo
55 7 Resultados 7.1 Validação modelo simplificado De acordo com os dados de entrada e da metodologia de cálculo alguns resultados foram extraídos das análises. Primeiramente um comparativo entre o modelo
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA - EEL. Prof. Geronimo
 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA - EEL Prof. Geronimo BALANÇO MATERIAL EM PROCESSOS COM REAÇÃO QUÍMICA Mecanismos responsáveis pela variação da massa no interior dos sistemas: Fluxos
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA - EEL Prof. Geronimo BALANÇO MATERIAL EM PROCESSOS COM REAÇÃO QUÍMICA Mecanismos responsáveis pela variação da massa no interior dos sistemas: Fluxos
Física e Química A 715 (versão 1)
 Exame (Resolução proposta por colaboradores da Divisão de Educação da Sociedade Portuguesa de Física) Física e Química A 715 (versão 1) 0 de Junho de 008 1. 1.1. Átomos de ferro A espécie redutora é o
Exame (Resolução proposta por colaboradores da Divisão de Educação da Sociedade Portuguesa de Física) Física e Química A 715 (versão 1) 0 de Junho de 008 1. 1.1. Átomos de ferro A espécie redutora é o
Química Geral e Experimental II Equilíbrio químico Resolução comentada de exercícios selecionados versão equilíbrio_v1_2005 Prof. Fabricio R.
 Química Geral e Experimental II Equilíbrio químico comentada de exercícios selecionados versão equilíbrio_v1_2005 Prof. Fabricio R. Sensato 1) A constante de equilíbrio K c da reação: H 2 (g) + Cl 2 (g)
Química Geral e Experimental II Equilíbrio químico comentada de exercícios selecionados versão equilíbrio_v1_2005 Prof. Fabricio R. Sensato 1) A constante de equilíbrio K c da reação: H 2 (g) + Cl 2 (g)
4º Laboratório de EME 502 MEDIDAS DE VAZÃO
 Universidade Federal de Uberlândia Instituto de Engenharia Mecânica 4º Laboratório de EME 502 MEDIDAS DE VAZÃO Profa. Ana Lúcia Fernandes de Lima e Silva http://www.iem.unifei.edu.br/labtc/ana.html Objetivos
Universidade Federal de Uberlândia Instituto de Engenharia Mecânica 4º Laboratório de EME 502 MEDIDAS DE VAZÃO Profa. Ana Lúcia Fernandes de Lima e Silva http://www.iem.unifei.edu.br/labtc/ana.html Objetivos
EQUIPAMENTOS EQUIPAMENTOS
 OPERAÇÕES UNITÁRIAS MECÂNICA DOS FLUÍDOS TRANSMISSÃO DE CALOR AGITAÇÃO E MISTURA SEPARAÇÃO MANUSEIO COM SÓLIDOS BOMBAS MECÂNICA DOS FLUÍDOS DESLOCAMENTO POSITIVO CINÉTICAS ALTERNATIVAS ROTATIVAS CENTRÍFUGAS
OPERAÇÕES UNITÁRIAS MECÂNICA DOS FLUÍDOS TRANSMISSÃO DE CALOR AGITAÇÃO E MISTURA SEPARAÇÃO MANUSEIO COM SÓLIDOS BOMBAS MECÂNICA DOS FLUÍDOS DESLOCAMENTO POSITIVO CINÉTICAS ALTERNATIVAS ROTATIVAS CENTRÍFUGAS
EQUIPAMENTOS EQUIPAMENTOS EQUIPAMENTOS OPERAÇÕES UNITÁRIAS TECNOLOGIA DE PROCESSOS QUÍMICOS II MECÂNICA DOS FLUÍDOS TRANSMISSÃO DE CALOR
 OPERAÇÕES UNITÁRIAS MECÂNICA DOS FLUÍDOS TRANSMISSÃO DE CALOR AGITAÇÃO E MISTURA SEPARAÇÃO MANUSEIO COM SÓLIDOS MECÂNICA DOS FLUÍDOS DESLOCAMENTO POSITIVO ALTERNATIVAS ROTATIVAS BOMBAS CINÉTICAS CENTRÍFUGAS
OPERAÇÕES UNITÁRIAS MECÂNICA DOS FLUÍDOS TRANSMISSÃO DE CALOR AGITAÇÃO E MISTURA SEPARAÇÃO MANUSEIO COM SÓLIDOS MECÂNICA DOS FLUÍDOS DESLOCAMENTO POSITIVO ALTERNATIVAS ROTATIVAS BOMBAS CINÉTICAS CENTRÍFUGAS
ESTE Aula 2- Introdução à convecção. As equações de camada limite
 Universidade Federal do ABC ESTE013-13 Aula - Introdução à convecção. As equações de camada limite EN 41: Aula As equações de camada limite Análise das equações que descrevem o escoamento em camada limite:
Universidade Federal do ABC ESTE013-13 Aula - Introdução à convecção. As equações de camada limite EN 41: Aula As equações de camada limite Análise das equações que descrevem o escoamento em camada limite:
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2. prof. Daniela Szilard 23 de maio de 2016
 Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
SOLUÇÕES - SOLUÇÃO IDEAL E AS PROPRIEDADES COLIGATIVAS
 ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES - SOLUÇÃO IDEAL E AS PROPRIEDADES COLIGATIVAS 1. TIPOS DE SOLUÇÕES Solução é uma mistura homogênea de
ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES - SOLUÇÃO IDEAL E AS PROPRIEDADES COLIGATIVAS 1. TIPOS DE SOLUÇÕES Solução é uma mistura homogênea de
TÉCNICO DE LABORATÓRIO/HIDRÁULICA
 A B R A S O M E N T E Q U A N D O A U T O R I Z A D O Concurso Público Edital PROAD 74/2016 TÉCNICO DE LABORATÓRIO/HIDRÁULICA Leia atentamente as instruções abaixo: 1. Aguarde permissão para iniciar a
A B R A S O M E N T E Q U A N D O A U T O R I Z A D O Concurso Público Edital PROAD 74/2016 TÉCNICO DE LABORATÓRIO/HIDRÁULICA Leia atentamente as instruções abaixo: 1. Aguarde permissão para iniciar a
Campus de Ilha Solteira. Disciplina: Fenômenos de Transporte
 Campus de Ilha Solteira CONCEITOS BÁSICOS B E VISCOSIDADE Disciplina: Fenômenos de Transporte Professor: Dr. Tsunao Matsumoto INTRODUÇÃO A matéria de Fenômenos de Transporte busca as explicações de como
Campus de Ilha Solteira CONCEITOS BÁSICOS B E VISCOSIDADE Disciplina: Fenômenos de Transporte Professor: Dr. Tsunao Matsumoto INTRODUÇÃO A matéria de Fenômenos de Transporte busca as explicações de como
Exercícios e exemplos de sala de aula Parte 1
 PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
ROTEIRO DE EXPERIMENTOS ENG1120 LABORATÓRIO DE HIDRÁULICA
 PONTIFÍCIA UNIVERSIDADE CATÓLICA DE GOIÁS ROTEIRO DE EXPERIMENTOS ENG0 LABORATÓRIO DE HIDRÁULICA GOIÂNIA 07- Sumário ª Experiência: Determinação da vazão real no Tubo Diafragma... ª Experiência: Determinação
PONTIFÍCIA UNIVERSIDADE CATÓLICA DE GOIÁS ROTEIRO DE EXPERIMENTOS ENG0 LABORATÓRIO DE HIDRÁULICA GOIÂNIA 07- Sumário ª Experiência: Determinação da vazão real no Tubo Diafragma... ª Experiência: Determinação
CONCURSO PÚBLICO EDITAL Nº 03 / 2015
 MINISTÉRIO DA EDUCAÇÃO INSTITUTO FEDERAL DO ESPÍRITO SANTO REITORIA Avenida Rio Branco, 50 Santa Lúcia 29056-255 Vitória ES 27 3357-7500 CONCURSO PÚBLICO EDITAL Nº 03 / 2015 Professor do Magistério do
MINISTÉRIO DA EDUCAÇÃO INSTITUTO FEDERAL DO ESPÍRITO SANTO REITORIA Avenida Rio Branco, 50 Santa Lúcia 29056-255 Vitória ES 27 3357-7500 CONCURSO PÚBLICO EDITAL Nº 03 / 2015 Professor do Magistério do
Correção das curvas da bomba hidráulica
 Correção das curvas da bomba hidráulica Já estudamos a influência da instalação na CCB! Já corrigimos a CCB pela rotação (n), o que será que estudaremos desse ponto em diante? Estaremos refletindo sobre
Correção das curvas da bomba hidráulica Já estudamos a influência da instalação na CCB! Já corrigimos a CCB pela rotação (n), o que será que estudaremos desse ponto em diante? Estaremos refletindo sobre
Capítulo 08 - TRANSFERÊNCIA DE CALOR POR CONDUÇÃO EM REGIME TRANSIENTE
 Os exercícios e figuras deste texto foram retirados de diversas referências bibliográficas listadas no programa da disciplina 1 FENÔMENOS DE TRANSPORTE Capítulo 08 - TRANSFERÊNCIA DE CALOR POR CONDUÇÃO
Os exercícios e figuras deste texto foram retirados de diversas referências bibliográficas listadas no programa da disciplina 1 FENÔMENOS DE TRANSPORTE Capítulo 08 - TRANSFERÊNCIA DE CALOR POR CONDUÇÃO
T constante 0 1 X 1. líquido. Líquido + vapor. vapor X 1
 1 PR UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ - UTFPR DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA BACHARELADO EM QUÍMICA / LICENCIATURA
1 PR UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ - UTFPR DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA BACHARELADO EM QUÍMICA / LICENCIATURA
LISTA DE EXERCÍCIOS PARA RECAPTULAÇÃO DOS CONTEÚDOS
 Curso : Engenharia civil Disciplina: Fenômeno dos transportes Professor(a): Nome do(s) Aluno(a)(s): LISTA DE EXERCÍCIOS PARA RECAPTULAÇÃO DOS CONTEÚDOS Período Letivo: 2014.2 Unidade: I Nota: Semestre:
Curso : Engenharia civil Disciplina: Fenômeno dos transportes Professor(a): Nome do(s) Aluno(a)(s): LISTA DE EXERCÍCIOS PARA RECAPTULAÇÃO DOS CONTEÚDOS Período Letivo: 2014.2 Unidade: I Nota: Semestre:
Física Geral e Experimental III. Dilatação
 Física Geral e Experimental III Dilatação 6. Em um dia quente em Las Vegas um caminhão-tanque foi carregado com 37.000 L de óleo diesel. Ele encontrou tempo frio ao chegar a Payson, Utha, onde a temperatura
Física Geral e Experimental III Dilatação 6. Em um dia quente em Las Vegas um caminhão-tanque foi carregado com 37.000 L de óleo diesel. Ele encontrou tempo frio ao chegar a Payson, Utha, onde a temperatura
Convecção (natural e forçada) Prof. Dr. Edval Rodrigues de Viveiros
 Convecção (natural e forçada) Prof. Dr. Edval Rodrigues de Viveiros Convecção natural Convecção forçada Convecção natural A transmissão de calor por convecção natural ocorre sempre quando um corpo é
Convecção (natural e forçada) Prof. Dr. Edval Rodrigues de Viveiros Convecção natural Convecção forçada Convecção natural A transmissão de calor por convecção natural ocorre sempre quando um corpo é
Transferência de Calor 1
 Transferência de Calor Guedes, Luiz Carlos Vieira. G94t Transferência de calor : um / Luiz Carlos Vieira Guedes. Varginha, 05. 80 slides; il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World
Transferência de Calor Guedes, Luiz Carlos Vieira. G94t Transferência de calor : um / Luiz Carlos Vieira Guedes. Varginha, 05. 80 slides; il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World
Prática 08 Determinação da Massa Molar da Ureia via Ebuliometria
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 08 Determinação da Massa Molar da Ureia
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 08 Determinação da Massa Molar da Ureia
MODELAGEM E SIMULAÇÃO DO SISTEMA ACETONA- METANOL PARA OBTENÇÃO DE METANOL EM COLUNAS DE DESTILAÇÃO
 MODELAGEM E SIMULAÇÃO DO SISTEMA ACETONA- METANOL PARA OBTENÇÃO DE METANOL EM COLUNAS DE DESTILAÇÃO SILVA J. O (1); MARCELINO T. O. A. C (1); SILVA M. C (2) e RAMOS B. W (4) Universidade Federal de Campina
MODELAGEM E SIMULAÇÃO DO SISTEMA ACETONA- METANOL PARA OBTENÇÃO DE METANOL EM COLUNAS DE DESTILAÇÃO SILVA J. O (1); MARCELINO T. O. A. C (1); SILVA M. C (2) e RAMOS B. W (4) Universidade Federal de Campina
Fundamentos de Fenômenos de Transporte. Prof. Dr. Geronimo Virginio Tagliaferro
 Fundamentos de Fenômenos de Transporte Prof. Dr. Geronimo Virginio Tagliaferro Ementa 1. Conceitos ligados ao escoamento de fluídos e equações fundamentais: 2. Escoamento incompressível de fluidos não
Fundamentos de Fenômenos de Transporte Prof. Dr. Geronimo Virginio Tagliaferro Ementa 1. Conceitos ligados ao escoamento de fluídos e equações fundamentais: 2. Escoamento incompressível de fluidos não
PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 1 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI
 PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 1 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI ÁREA DE CONCENTRAÇÃO: FÍSICA E QUÍMICA DE MATERIAIS NÍVEL:
PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 1 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI ÁREA DE CONCENTRAÇÃO: FÍSICA E QUÍMICA DE MATERIAIS NÍVEL:
QUÍMICA PRIMEIRA ETAPA
 QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
QUÍMICA PRIMEIRA ETAPA - 1998 QUESTÃO 01 Uma mistura de hidrogênio, H 2 (g), e oxigênio, O 2 (g), reage, num recipiente hermeticamente fechado, em alta temperatura e em presença de um catalisador, produzindo
P1 - PROVA DE QUÍMICA GERAL 09/09/11
 P1 - PROVA DE QUÍMICA GERAL 09/09/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R = 0,081 atm L -1 K -1 T (K) = T ( C) + 73,15
P1 - PROVA DE QUÍMICA GERAL 09/09/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0 Dados R = 0,081 atm L -1 K -1 T (K) = T ( C) + 73,15
ESCOLA SECUNDÁRIA DE CASQUILHOS
 ESCOLA SECUNDÁRIA DE CASQUILHOS 8.º Teste sumativo de FQA 16. março. 015 10.º Ano Turma A Professora: Maria do Anjo Albuquerque Versão 1 Duração da prova: 90 minutos. Este teste é constituído por 7 páginas
ESCOLA SECUNDÁRIA DE CASQUILHOS 8.º Teste sumativo de FQA 16. março. 015 10.º Ano Turma A Professora: Maria do Anjo Albuquerque Versão 1 Duração da prova: 90 minutos. Este teste é constituído por 7 páginas
a) Qual deverá ser o volume do PFR para converter 80% de A em fase líquida? Considerar alimentação a 44 L min -1 e C A0 = C B0 = 1 mol L -1
 501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
Exame de Ingresso ao PPG- AEM 2014/1sem
 Universidade de São Paulo Escola de Engenharia de São Carlos Exame de Ingresso ao PPG- AEM 2014/1sem Nome do Candidato: R.G.: Data: Assinatura: Indique a área de concentração de interesse (em ordem decrescente
Universidade de São Paulo Escola de Engenharia de São Carlos Exame de Ingresso ao PPG- AEM 2014/1sem Nome do Candidato: R.G.: Data: Assinatura: Indique a área de concentração de interesse (em ordem decrescente
TRANSMISSÃO DE CALOR resumo
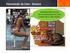 TRANSMISSÃO DE CALOR resumo convecção forçada abordagem experimental ou empírica Lei do arrefecimento de Newton Taxa de Transferência de Calor por Convecção 𝑞"#$ ℎ𝐴 𝑇 𝑇 ℎ 1 𝐴 ℎ - Coeficiente Convectivo
TRANSMISSÃO DE CALOR resumo convecção forçada abordagem experimental ou empírica Lei do arrefecimento de Newton Taxa de Transferência de Calor por Convecção 𝑞"#$ ℎ𝐴 𝑇 𝑇 ℎ 1 𝐴 ℎ - Coeficiente Convectivo
Química Geral e Experimental II
 Química Geral e Experimental II Resolução comentada da P1 2º Sem/2005; 28.10.2005 Engenharia Materiais Tópicos Propriedades coligativas Gases Termoquímica Prof. Fabrício R. Sensato 1) (1,0 ponto) Em geral,
Química Geral e Experimental II Resolução comentada da P1 2º Sem/2005; 28.10.2005 Engenharia Materiais Tópicos Propriedades coligativas Gases Termoquímica Prof. Fabrício R. Sensato 1) (1,0 ponto) Em geral,
