Química Geral Classificação Periódica
|
|
|
- João Gabriel Espírito Santo Jardim
- 8 Há anos
- Visualizações:
Transcrição
1 Química Geral Classificação Periódica 1. (G1 - cftmg 2014) Um elemento X possui 6 camadas eletrônicas preenchidas e 7 elétrons no último nível. Portanto esse elemento localiza-se na família do(s) e no período. Os termos que completam, corretamente, as lacunas são a) halogênios e sexto. b) nitrogênio e quinto. c) carbono e segundo. d) calcogênios e sétimo. 2. (Ufg 2014) Catalão, Niquelândia, Crixás e Barro Alto são cidades goianas que têm se destacado nacionalmente pela produção mineral de nióbio, níquel, ouro e cobre, respectivamente. As mesorregiões das cidades goianas e os símbolos dos elementos químicos citados são, respectivamente, a) Sul Goiano, Noroeste Goiano, Centro Goiano e Norte Goiano Nb, Ni, Au e Co. b) Sul Goiano, Norte Goiano, Noroeste Goiano e Centro Goiano Nb, Ni, Au e Cu. c) Sul Goiano, Centro Goiano, Norte Goiano e Noroeste Goiano Nb, Ni, Ag e Cu. d) Sul Goiano, Norte Goiano, Nordeste Goiano e Centro Goiano Ni, Nb, Ag e Co. e) Sul Goiano, Nordeste Goiano, Centro Goiano e Norte Goiano Ni, Nb, Au e Cu. 3. (Pucrj 2014) A tabela periódica dos elementos é uma base de dados que possibilita prever o comportamento, propriedades e características dos elementos químicos. Com as informações que podem ser obtidas da tabela periódica, relacione os elementos apresentados na coluna da esquerda com a informação da coluna à direita que indica a respectiva distribuição dos elétrons nos subníveis do último nível de energia ocupado no estado fundamental. Elemento químico I. Bromo II. Estanho III. Polônio IV. Rádio Configuração no último nível X. Y. Z. 2 s 2 4 sp 2 2 sp Estão corretas as associações: a) I X, II Y e III Z b) I X, II Z e III Y c) I Z, II X e IV Y d) II Z, III Y e IV X e) II Y, III Z e IV X Página 1 de 17
2 4. (Udesc 2014) Assinale a alternativa correta em relação às Leis periódicas. a) Todos os elementos do grupo 14 da tabela periódica possuem 4 elétrons em suas camadas de valência, logo, não formam ligações iônicas, pois dão preferência ao compartilhamento de elétrons. b) Os não-metais possuem alta eletropositividade e formam compostos tipicamente moleculares entre si. c) Os gases nobres possuem baixas energias de ionização por possuírem suas camadas eletrônicas de valência completas. d) A carga nuclear é responsável pela contração do raio iônico ao longo de um determinado período da tabela periódica. e) O cátion Li + ao receber um elétron tem seu raio reduzido, pois há uma maior atração entre o núcleo deste átomo e a sua eletrosfera. 5. (G1 - cftrj 2014) O elemento químico A apresenta os subníveis mais energéticos iguais a 4s 2 3d 1. O cátion A 3+ é isoeletrônico do elemento químico B. Com relação a esse texto, pode-se afirmar que: a) o elemento químico A apresenta menor eletronegatividade que o elemento químico rubídio (Rb). b) o elemento químico A apresenta menor raio atômico que o elemento químico selênio (Se). c) o elemento químico B pertence à família dos gases nobres, sendo B = Kr (criptônio). d) o elemento químico A apresenta maior energia de ionização que o elemento químico potássio (K). 6. (G1 - ifce 2014) Os elementos A, B e C têm as seguintes configurações eletrônicas em suas camadas de valência: A: 3s 2 3p 3 B: 4s 2 4p 5 C: 3s 2 Com base nestas informações, é falso dizer-se que a) o elemento A é um não metal. b) o elemento B é um halogênio. c) o elemento C é um metal alcalino terroso. d) os elementos A e C pertencem ao terceiro período da Tabela Periódica. e) os elementos A, B e C pertencem ao mesmo grupo da Tabela Periódica. 7. (Ufrgs 2014) A usina nuclear de Fukushima continua apresentando problemas de vazamento de materiais radioativos. Estima-se que grandes quantidades de césio e estrôncio radioativo teriam chegado ao Oceano Pacífico, através da água subterrânea acumulada no subsolo da usina. Os isótopos radioativos mais significativos nesses vazamentos seriam césio- 134, césio-137 e estrôncio-90. Sobre os átomos de césio e estrôncio, considere as afirmações abaixo. I. Césio é o mais eletropositivo e o de menor potencial de ionização entre todos os elementos químicos, à exceção do frâncio que tecnicamente tem sua abundância considerada como zero em termos práticos. II. O isótopo radioativo estrôncio-90 representa um sério risco, tendo em vista que pode substituir com facilidade o cálcio dos ossos, pois ambos formam cátions com carga 2+ e apresentam raios iônicos com valores relativamente próximos. III. Os átomos dos isótopos de césio-134, de césio-137 e de estrôncio-90 emitem radiações altamente ionizantes devido à grande eletronegatividade desses isótopos. Quais estão corretas? a) Apenas I. b) Apenas III. c) Apenas I e II. d) Apenas II e III. e) I, II e III. Página 2 de 17
3 8. (Uepa 2014) A tabela periódica foi uma das maiores criações do homem para comunicação e padronização científica. Sobre a tabela periódica, onde estão representados todos os elementos químicos que compõem a matéria, são feitas as afirmações abaixo: I. A família XVIII representa os gases nobres, e estes não se combinam com os demais elementos em condições normais. II. A família II representa os metais alcalino-terrosos, que comportam 2 elétrons na sua última camada eletrônica. III. Todos os metais são sólidos, conduzem eletricidade e são maleáveis à temperatura ambiente. IV. Os não-metais têm tendência a receber elétrons, se transformando em ânions. V. Os Calcogênios tornam-se estáveis quando recebem dois elétrons completando seu octeto. A alternativa que contém todas as afirmativas corretas é: a) I, II, III e IV b) I, II, III e V c) II, III, IV e V d) I, II, IV e V e) I, III, IV e V 9. (Fuvest 2014) Observe a posição do elemento químico ródio (Rh) na tabela periódica. Assinale a alternativa correta a respeito do ródio. a) Possui massa atômica menor que a do cobalto (Co). b) Apresenta reatividade semelhante à do estrôncio (Sr), característica do 5º período. c) É um elemento não metálico. d) É uma substância gasosa à temperatura ambiente. e) É uma substância boa condutora de eletricidade. 10. (Uerj 2014) A tabela abaixo apresenta o nome de alguns minerais e a fórmula química da substância que constitui cada um deles. Mineral Fórmula química da substância Calcita CaCO 3 Cerussita PbCO 3 Estroncianita SrCO 3 Magnesita MgCO 3 Rodocrosita MnCO 3 Siderita FeCO 3 Witherita BaCO 3 Considerando a tabela, apresente o nome do mineral cujo metal no estado fundamental possui quatro elétrons na sua camada de valência. Apresente, também, a fórmula química da substância que contém o metal de maior raio atômico. Página 3 de 17
4 11. (Ifsc 2014) Muito utilizados em equipamentos eletrônicos, os semicondutores são sólidos capazes de mudar sua condição de isolante para condutores com grande facilidade. [...] A condutividade dos semicondutores pode ser alterada variando-se a temperatura, o que faz com que atinjam uma condutividade semelhante a dos metais. [...] Os semicondutores podem ser de silício ou germânio, utilizados para a fabricação de componentes eletrônicos, como, por exemplo, os transistores. Disponível em: Acesso: 10 out Assinale a soma da(s) proposição(ões) CORRETA(S) sobre os propriedades dos elementos químicos. 01) Metais são sólidos na sua maioria e bons condutores de eletricidade. 02) O silício citado no texto acima é um metal com características diferenciadas dos demais metais. 04) Os elementos citados no texto pertencem à família do carbono da Tabela Periódica, portanto podem doar dois elétrons quando fazem ligações químicas. 08) O silício localiza-se no terceiro período da Tabela Periódica e na família 4A, portanto sua camada de valência é a camada 4. 16) O germânio localiza-se abaixo do silício na Tabela Periódica, numa mesma família, o que indica que ele possui maior eletronegatividade que o silício. 32) Se comparados ao cobre, o silício e o germânio são melhores isolantes, em temperaturas baixas. 12. (Uece 2014) O raciocínio indutivo se desenvolve a partir do que já é conhecido, mas requer uma etapa adicional para descrever o que ainda é desconhecido. (Jacob Bronowski A escalada do homem). Foi o raciocínio indutivo que permitiu ao cientista Mendeleiev a) sugerir a existência do germânio e do gálio até então desconhecidos. b) montar a tabela periódica na ordem crescente de números atômicos. c) estabelecer a primeira lei periódica conhecida como a lei das oitavas. d) descobrir, a partir de outros elementos, a estrutura dos gases nobres. TEXTO PARA A PRÓXIMA QUESTÃO: Uma atração turística da Áustria é Salzburgo, cidade natal de Mozart, construída na Antiguidade graças às minas de sal. Salzburgo significa castelo do sal, pois nessa cidade está localizada a mina de sal mais antiga do mundo, em atividade desde a Idade do Ferro (1000 a.c.). No passado, o sal era um importante e quase insubstituível conservante alimentar e, além de cair bem ao nosso paladar, ele é uma necessidade vital, pois, sem o sódio presente no sal, o organismo seria incapaz de transmitir impulsos nervosos ou mover músculos, entre eles o coração. (terra.com.br/turismo/roteiros/2000/11/10/009.htm Acesso em: Adaptado) 13. (G1 - cps 2014) O símbolo do elemento que, segundo o texto, permite a transmissão de impulsos nervosos é a) S b) So c) Sd d) N e) Na Página 4 de 17
5 TEXTO PARA A PRÓXIMA QUESTÃO: Água coletada em Fukushima em 2013 revela radioatividade recorde A empresa responsável pela operação da usina nuclear de Fukushima, Tokyo Electric Power (Tepco), informou que as amostras de água coletadas na central em julho de 2013 continham um nível recorde de radioatividade, cinco vezes maior que o detectado originalmente. A Tepco explicou que uma nova medição revelou que o líquido, coletado de um poço de observação entre os reatores 1 e 2 da fábrica, continha nível recorde do isótopo radioativo estrôncio-90. ( Adaptado.) 14. (Unesp 2014) O estrôncio, por apresentar comportamento químico semelhante ao do cálcio, pode substituir este nos dentes e nos ossos dos seres humanos. No caso do isótopo Sr- 90, radioativo, essa substituição pode ser prejudicial à saúde. Considere os números atômicos do Sr = 38 e do Ca = 20. É correto afirmar que a semelhança de comportamento químico entre o cálcio e o estrôncio ocorre porque a) apresentam aproximadamente o mesmo raio atômico e, por isso, podem ser facilmente intercambiáveis na formação de compostos. b) apresentam o mesmo número de elétrons e, por isso, podem ser facilmente intercambiáveis na formação de compostos. c) ocupam o mesmo grupo da Classificação Periódica, logo têm o mesmo número de elétrons na camada de valência e formam cátions com a mesma carga. d) estão localizados no mesmo período da Classificação Periódica. e) são dois metais representativos e, por isso, apresentam as mesmas propriedades químicas. 15. (G1 - cftrj 2013) As informações físicas e químicas dos elementos foram essenciais para a construção das tabelas de classificação periódicas ao longo dos tempos, pelo agrupamento de elementos com propriedades semelhantes. A seguir, são apresentadas algumas características de um elemento genericamente representado pela letra X. I. É um elemento representativo. II. Forma com o enxofre um composto de fórmula XS. III. O elemento X não apresenta subnível p na camada de valência. Considerando seus conhecimentos sobre as classificações periódicas dos elementos, identifique o grupo a que pertence o elemento X. a) metal alcalino b) metal alcalino-terroso c) família 2B d) calcogênio 16. (Ibmecrj 2013) De acordo com o a tabela periódica abaixo, assinale a alternativa incorreta quanto à posição dos algarismos romanos que estão substituindo os símbolos dos elementos químicos: a) O elemento químico representado por II é um gás nobre. b) O elemento químico representado por VII possui número atômico igual a 36. c) O elemento químico representado por IX possui número de massa igual a 133. d) O elemento químico representado por I é um gás a temperatura ambiente. e) O elemento químico representado por X pode ser classificado por metal alcalino terroso. Página 5 de 17
6 17. (Mackenzie 2013) Abaixo são fornecidas as distribuições eletrônicas das camadas de valência dos átomos neutros X, Y e Z em seus estados fundamentais. X: 2s 2 ; 2p 5 Y: 6s 1 Z: 4s 2 ; 4p 5 A partir dessas informações, é correto afirmar que a) o elemento Y é um metal alcalino-terroso. b) os elementos X e Z pertencem ao mesmo período, todavia X é mais eletronegativo do que Z. c) o elemento X apresenta maior afinidade eletrônica do que o elemento Y. d) o elemento Z apresenta maior raio atômico do que Y. e) X, Y e Z são elementos de transição. 18. (Unicamp 2013) Na década de 1970, a imprensa veiculava uma propaganda sobre um fertilizante que dizia: contém N, P, K, mais enxofre. Pode-se afirmar que o fertilizante em questão continha em sua formulação, respectivamente, os elementos químicos a) nitrogênio, fósforo, potássio e enxofre, cujo símbolo é S. b) níquel, potássio, criptônio e enxofre, cujo símbolo é Ex. c) nitrogênio, fósforo, potássio e enxofre, cujo símbolo é Ex. d) níquel, potássio, cálcio e enxofre, cujo símbolo é S. 19. (Udesc 2013) Os elementos químicos situados entre as colunas 3 a 12 na tabela periódica: a) apresentam o subnível d completo. b) tendem a ganhar elétrons, quando participam de ligações químicas. c) são encontrados na natureza somente em estado sólido. d) são denominados metais de transição. e) aumentam o raio atômico de acordo com o número da coluna. 20. (Fuvest 2013) Um aluno estava analisando a Tabela Periódica e encontrou vários conjuntos de três elementos químicos que apresentavam propriedades semelhantes. Assinale a alternativa na qual os conjuntos de três elementos ou substâncias elementares estão corretamente associados às propriedades indicadas no quadro abaixo. Números atômicos consecutivos Reatividades semelhantes Mesmo estado físico à temperatura ambiente a) Pt, Au, Hg H 2, He, Li C 2, Br 2, I 2 b) C, Br,I O 2, F 2, Ne Ne, Ar, Kr c) Li, Na, K O 2, F 2, Ne Pt, Au, Hg d) Ne, Ar, Kr Mg, Ca, Sr 2 C, Br 2, I 2 e) Pt, Au, Hg Li, Na, K Ne, Ar, Kr Página 6 de 17
7 21. (G1 - utfpr 2013) Na classificação periódica, os elementos químicos situados nas colunas IA e VIIA são denominados, respectivamente, de: a) metais alcalinos terrosos e calcogênios. b) metais e gases nobres. c) metais alcalinos e halogênios. d) halogênios e calcogênios. e) metais alcalinos terrosos e halogênios. 22. (Uern 2013) De acordo com as propriedades da tabela periódica, marque a alternativa INCORRETA. a) Quanto maior um átomo, menor é a energia de ionização. b) O sódio apresenta um raio atômico maior do que o magnésio. c) Eletroafinidade é a energia absorvida quando um elétron é adicionado a um átomo neutro. d) A eletronegatividade aumenta de baixo para cima nas famílias da tabela periódica e, da esquerda para a direita, nos períodos. 23. (Ufsj 2013) As terras raras constituem um grupo de elementos cobiçado devido à sua utilização em produtos de alta tecnologia: superímãs, telas de tablets, computadores, celulares, painéis solares, geradores eólicos, carros elétricos e outros. Sobre as terras raras, é CORRETO afirmar que são formadas pelos elementos a) Sc, Y, Zr, Os, Po. b) Be, Mg, Ca, Sr, Ra. c) Ac, Th, U, Bk, Cf. d) La, Nd, Eu, Dy, Lu. 24. (Uerj 2013) Em uma das primeiras classificações periódicas, os elementos químicos eram organizados em grupos de três, denominados tríades. Os elementos de cada tríade apresentam propriedades químicas semelhantes, e a massa atômica do elemento central equivale aproximadamente à média aritmética das massas atômicas dos outros dois. Observe as tríades a seguir: Li C S Na Br X K l Te Com base nos critérios desta classificação, a letra X corresponde ao seguinte elemento químico: a) O b) As c) Se d) Po 25. (Ufpr 2013) A tabela periódica dos elementos está organizada em grupos e períodos. Cada grupo possui uma característica, que tem pequena variação nos períodos. Tendo posse da informação sobre o número de prótons e nêutrons de um átomo, é possível associá-lo a um grupo e um período e assim prever seu comportamento. Um átomo de um elemento X possui 16 prótons e 16 nêutrons. A partir dessa informação, considere as seguintes afirmativas: 1. A substância pura de X é sólida à temperatura ambiente. 2. O íon mais estável de X possui carga O hidreto desse composto possui massa molar igual a 34 g.mol O produto da reação de combustão de X é um óxido covalente. Assinale a alternativa correta. a) Somente a afirmativa 1 é verdadeira. b) Somente as afirmativas 1 e 2 são verdadeiras. c) Somente as afirmativas 2, 3 e 4 são verdadeiras. d) Somente as afirmativas 1, 3 e 4 são verdadeiras. e) As afirmativas 1, 2, 3 e 4 são verdadeiras. Página 7 de 17
8 26. (Ufrn 2013) O efeito fotoelétrico está presente no cotidiano, por exemplo, no mecanismo que permite o funcionamento das portas dos shoppings e nos sistemas de iluminação pública, por meio dos quais as lâmpadas acendem e apagam. Esse efeito acontece porque, nas células fotoelétricas, os metais emitem elétrons quando são iluminados em determinadas condições. O potássio e o sódio são usados na produção de determinadas células fotoelétricas pela relativa facilidade de seus átomos emitirem elétrons quando ganham energia. Segundo sua posição na Tabela Periódica, o uso desses metais está relacionado com a) o baixo valor do potencial de ionização dos átomos desses metais. b) o alto valor da afinidade eletrônica dos átomos desses metais. c) o alto valor da eletronegatividade dos átomos desses metais. d) o alto valor do potencial de ionização dos átomos desses metais. TEXTO PARA A PRÓXIMA QUESTÃO: TEXTO 01 Vozes da Seca (Composição: Luiz Gonzaga e Zé Dantas) Seu dotô os nordestino Têm muita gratidão Pelo auxílio dos sulista Nessa seca do sertão Mas dotô uma esmola A um home qui é são Ou lhe mata de vergonha Ou vicia o cidadão [...] TEXTO 04 Dessalinização Entre as ações assistencialistas de combate à seca de cidades nordestinas, está a implantação de dessalinizadores para obtenção de água potável a partir de águas subterrâneas. O processo consiste em forçar a água subterrânea sob pressão a passar por uma membrana semipermeável que retém as partículas de sal e permite a passagem da água. A água dessalinizada torna-se potável, no entanto, o potencial poluidor do resíduo salino é muito alto. Se mal descartado ou não aproveitado para outros fins, esses resíduos podem contaminar mananciais e fontes de água diminuindo, gradativamente, a produtividade das terras da região. TEXTO 03 A RESOLUÇÃO CONAMA n 396, de 3 de abril de 2008, dispõe sobre a classificação e diretrizes ambientais para o enquadramento das águas subterrâneas brasileiras. O Quadro 1 apresenta alguns componentes comumente encontrados em águas subterrâneas e seus respectivos valores máximos permitidos para cada um dos usos considerados como preponderantes. Página 8 de 17
9 Quadro 1 Usos preponderantes da água n Componente 1 μg L Consumo Dessendentação humano de animais Irrigação Recreação 1 Sódio Ferro Cloreto Alumínio Chumbo Cobre Sulfato Zinco Disponível em Leia os textos para responder à(s) questão(ões). 27. (Uepb 2013) Quais dos componentes do Quadro 1 apresentam elementos químicos que não são metais na forma elementar? a) 1, 3, 5 e 7 b) 1, 2, 4, 5, 6 e 8 c) 3 e 7 d) 3, 4, 5 e 7 e) 2, 4, 6 e (Uepg 2012) Com relação à classificação periódica dos elementos, assinale o que for correto. 01) Quanto maior o tamanho do átomo menor o potencial de ionização. 02) Os gases nobres são também denominados de inertes, porque dificilmente participam de reações químicas. 04) Dentre os metais alcalinos, os de maior ocorrência são o sódio e o potássio. 08) A eletronegatividade de um átomo mede sua tendência em atrair elétrons. Página 9 de 17
10 29. (Unesp 2012) A tabela periódica é uma notável realização da ciência. Ela ajuda a organizar o que de outra forma seria um arranjo confuso dos elementos e de suas propriedades. A base da classificação periódica atual é a tabela do químico russo Mendeleev, proposta em 1869, com a diferença de que as propriedades dos elementos variam periodicamente com seus números atômicos e não com os pesos atômicos. Analisando a classificação periódica, mesmo sem conhecer todos os elementos que ela apresenta, é possível afirmar que a) os não metais podem ser deformados com golpes de martelo. b) os metais alcalino-terrosos são mais densos que os metais alcalinos. c) os halogênios, em condições normais de temperatura e pressão, são líquidos coloridos. d) o oxigênio e o nitrogênio são gases à temperatura ambiente e seus átomos apresentam seis elétrons na camada mais externa. e) os elementos de uma mesma família da classificação periódica possuem propriedades semelhantes porque eles ocorrem no mesmo lugar da Terra. 30. (Uerj 2012) Recentemente, a IUPAC reconheceu a existência de dois novos elementos químicos, cujos símbolos são Uuq e Uuh. Apesar de possuírem átomos instáveis, podem-se prever algumas de suas propriedades com base na Classificação Periódica dos Elementos. Indique o número de elétrons do átomo Uuq no estado fundamental. Em seguida, identifique o tipo de geometria molecular da substância cuja fórmula seja UuhH 2. Dado: Página 10 de 17
11 Gabarito: Resposta da questão 1: [A] Se o elemento possui 7 elétrons na sua camada de valência, pertence à família 7A, ou ao grupo 17 da tabela periódica, ou seja, da família dos halogênios. Esse elemento ainda possui 6 camadas eletrônicas, ou seja, pertence ao 6º período da tabela. Resposta da questão 2: [B] As mesorregiões das cidades goianas e os símbolos dos elementos químicos citados são, respectivamente: Sul Goiano, Norte Goiano, Noroeste Goiano e Centro Goiano Nb (nióbio), Ni (níquel), Au (ouro) e Cu (cobre). Resposta da questão 3: [D] Teremos: 2 5 I. Bromo (família VIIA): s p 2 2 II. Estanho (família IVA): s p (Z) 2 4 III. Polônio (família VIA): s p (Y) 2 IV. Rádio (família IIA): s (X) Resposta da questão 4: [D] Quanto maior a carga nuclear (número de prótons) menor o raio atômico. Como a carga nuclear cresce da esquerda para a direita (num mesmo período) na tabela periódica, consequentemente o raio atômico diminui. Resposta da questão 5: [D] O elemento químico A apresenta os subníveis mais energéticos iguais a 4s 2 3d 1, como a distribuição energética termina em d, conclui-se que se trata de um elemento de transição. 4s 2 3d 1 significa que o elemento A está posicionado no quarto período da tabela periódica e na coluna 3 de transição K :1s 2s 2p 3s 3p 4s. O cátion A 3+ é isoeletrônico do elemento químico B, então: A : 1s 2s 2p 3s 3p 4s 3d (maior eletronegatividade do que o rubídio) A : 1s 2s 2p 3s 3p B : 1s 2s 2p 3s 3p (Ar argônio gás nobre) O elemento químico A apresenta maior energia de ionização que o elemento químico potássio (K), pois está localizado mais a direita e abaixo na tabela periódica. Página 11 de 17
12 Resposta da questão 6: [E] Teremos: A: 3s 2 3p 3 (grupo 15 ou família VA - ametal ou não metal - terceiro período) B: 4s 2 4p 5 (grupo 17 ou família VIIA - halogênio - quarto período) C: 3s 2 (grupo 2 ou família IIA - alcalino terroso - terceiro período) Os elementos A e C pertencem ao mesmo período (terceiro) da Tabela Periódica. Os elementos A, B e C pertencem a grupos diferentes da Tabela Periódica. Resposta da questão 7: [C] [I] Césio (6 camadas e 1 elétron de valência) é o mais eletropositivo e o de menor potencial de ionização entre todos os elementos químicos, à exceção do frâncio que tecnicamente tem sua abundância considerada como zero em termos práticos. [II] O isótopo radioativo estrôncio-90 (família IIA, dois elétrons de valência) representa um sério risco, tendo em vista que pode substituir com facilidade o cálcio dos ossos, pois ambos formam cátions com carga 2+ e apresentam raios iônicos com valores relativamente próximos. [III] O césio apresenta eletronegatividade de Linus Pauling 0,7 e o estrôncio 1,0. Resposta da questão 8: [D] [I] Correta. A família XVIII, formada pelos gases nobres assim chamados por serem pouco reativos em condições ambiente. [II] Correta. O 2º grupo da Tabela Periódica são chamados de alcalino-terrosos e apresentam 2 elétrons na camada de valência. [III] Incorreta. O mercúrio é um metal que se apresenta líquido em condições ambiente. [IV] Correta. Os não-metais possuem a tendência de receber elétrons transformando-se em ânions. [V] Correta. Os calcogênios possuem 6e- na sua camada de valência e de acordo com a teoria do octeto, precisam de 2e - para se estabilizar. Resposta da questão 9: [E] O ródio (Rh) é um metal de transição sólido à temperatura ambiente e condutor de eletricidade. Possui massa atômica maior do que o cobalto (Co), pois está posicionado no quinto período da tabela periódica e o cobalto (Co) no quarto. O ródio (Rh) não possui as mesmas propriedades do estrôncio (Sr - grupo 2), pois está posicionado no grupo 9. Página 12 de 17
13 Resposta da questão 10: Para o chumbo teremos: Pb 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p A camada mais externa (camada de valência) do Pb será: 2 2 6s 6p (cerussita). O raio atômico varia na Tabela Periódica, simplificadamente da seguinte forma: Assim sendo, os elementos mais posicionados à esquerda (menor número de prótons) e mais abaixo da tabela (maior número de camadas) seriam: Ca, Sr, Mg, Ba e Pb, sendo o de maior raio pela junção dos 2 fatores o Bário. Portanto, o mineral será a Witherita. Resposta da questão 11: = 33. [01] Correta. A grande maioria dos metais são bons condutores de calor e eletricidade e sólidos a temperatura ambiente. [02] Incorreta. O silício é classificado como um semimetal. [04] Incorreta. Os elementos citados no texto (silício e germânio) embora pertençam a mesma família que o carbono, não podem doar 2 elétrons, e sim compartilhar 4 elétrons para ficar com 8 elétrons em sua camada de valência. [08] Incorreta. O germânio localiza-se no 4º Período da Tabela Periódica. [16] Incorreta. Em um grupo a eletronegatividade aumenta de baixo para cima, portanto, o germânio é menos eletronegativo que o silício. [32] Correta. Conforme o texto relata, a condutividade dos semicondutores pode ser variada, mudando a temperatura, podendo se comportar como isolantes em baixas temperaturas, diferentemente do cobre. Resposta da questão 12: [A] Foi o raciocínio indutivo que permitiu ao cientista Mendeleyev sugerir a existência do germânio e do gálio até então desconhecidos. Entre 1869 e 1871 Mendeleyev revisou e aprimorou sua tabela com os elementos químicos ainda não conhecidos, ou seja, ele previu a existência de elementos como o gálio e germânio e, além disso, estimou suas propriedades químicas. Propriedades do germânio Previsões de 1871 Dados atuais Massa atômica 72 72,59 Densidade 5,5 g/cm 3 5,32 g/cm 3 Ponto de fusão muito elevado 937,4 C Página 13 de 17
14 Resposta da questão 13: [E] O símbolo do elemento que, segundo o texto, permite a transmissão de impulsos nervosos é Na (sódio). Resposta da questão 14: [C] A semelhança química entre os elementos cálcio e estrôncio ocorre, devido ao fato de ocuparem o mesmo grupo na Classificação Periódica. Fazendo a distribuição eletrônica de ambos teremos: Ca = 1s 2s 2p 3s 3p 4s Sr = 1s 2s 2p 3s 3p 4s 3d 4p 5s Assim, observa-se que ambos possuem 2e - na sua camada de valência, e podem formar cátions bivalentes. Resposta da questão 15: [B] Teremos: [I] É um elemento representativo, então pertence aos grupos A da tabela periódica. [II] Forma com o enxofre um composto de fórmula XS, então tem valência 2+. [III] O elemento X não apresenta subnível p na camada de valência, então está na família IIA ou 2, ou seja, é um metal alcalino terroso. Resposta da questão 16: [E] O elemento químico representado por X pode ser classificado por metal alcalino elemento de transição. Resposta da questão 17: [C] O elemento X (2s 2 ; 2p 5 ) apresenta maior afinidade eletrônica (7 elétrons de valência e 2 camadas) do que o elemento Y (6s 1-1 elétron de valência e 6 camadas). Resposta da questão 18: [A] A propaganda sobre um fertilizante dizia: contém N, P, K, mais enxofre. Conclusão: N: nitrogênio. P: fósforo (phophorus). K: potássio (kalium). S: enxofre (súlfur). Página 14 de 17
15 Resposta da questão 19: [D] Os elementos químicos situados entre as colunas 3 a 12 na tabela periódica são conhecidos como metais de transição externa ou metais de transição. Resposta da questão 20: [E] Verifica-se que os elementos Pt, Au e Hg estão localizados na mesma linha da tabela periódica (mesmo período) e são consecutivos (números atômicos crescentes). Os elementos Li, Na e K pertencem ao mesmo grupo ou família (metais alcalinos; um elétron de valência), por isso possuem a mesma reatividade. Os elementos Ne, Ar e Kr pertencem ao grupo dos gases nobres, e apresentam o mesmo estado físico (gasoso) à temperatura ambiente. Resposta da questão 21: [C] Elementos da coluna IA (Grupo 1) são metais alcalinos que possuem configuração eletrônica na camada de valência ns 1. Elementos da coluna VIIA (Grupo 17) são halogênios que possuem configuração eletrônica na camada de valência ns 2 np 5. Resposta da questão 22: [C] De acordo com as propriedades da tabela periódica eletroafinidade ou energia de afinidade é a energia liberada quando um elétron é adicionado a um átomo neutro em condições específicas. Resposta da questão 23: [D] Terras raras: elementos com número atômico entre Z = 57 e Z = 71, isto é do lantânio ao lutécio, e também o escândio (Z=21) e o ítrio (Z=39), neste caso La, Nd, Eu, Dy, Lu. Resposta da questão 24: [C] Nas tríades a média aritmética das massas dos elementos laterais se aproxima da massa do elemento central. mli mk 7 39 mna mna 23 mna 2 2 mc mi 35,5 127 m m 81,25 80 m 2 2 ms mte ,6 mx mx 79,8 mx 2 2 X é o selênio. Br Br Br Página 15 de 17
16 Resposta da questão 25: [E] Um átomo de um elemento enxofre (S) possui 16 prótons e 16 nêutrons. 1. O enxofre puro é sólido à temperatura ambiente. 2. O íon mais estável do enxofre (S; família VIA) possui carga O hidreto desse composto (H2S) possui massa molar igual a 34 g.mol O produto da reação de combustão do enxofre é um óxido covalente (SO2 ou SO 3). Resposta da questão 26: [A] O potencial de ionização é uma medida da energia envolvida na perda de um elétron por um elemento em seu estado gasoso. A partir dessa medida, avalia-se a capacidade de perda de elétrons de elementos. Os metais alcalinos, em geral, apresentam baixos valores de potencial de ionização. Isto significa dizer, em termos gerais, que seus elétrons de valência necessitam de baixos valores de energia para serem retirados de suas eletrosferas. Resposta da questão 27: [C] n Componente 1 Sódio (metal) 2 Ferro (metal) 4 Alumínio (metal) 3 Cloreto (ânion de ametal) 5 Chumbo (metal) 6 Cobre (metal) 7 Sulfato (ânion formado por ametais) 8 Zinco (metal) Resposta da questão 28: = 15. Quanto maior o número de camadas de um átomo ( tamanho ), menor a energia de ionização. Os gases nobres são inertes nas condições padrão. O sódio e o potássio são os metais alcalinos mais abundantes no planeta. A eletronegatividade de um átomo mede sua tendência em atrair elétrons de uma ligação covalente. Página 16 de 17
17 Resposta da questão 29: [B] Para medirmos a densidade de um elemento químico devemos dividir a massa de um mol de átomos pelo volume ocupado por esta quantidade de átomos: d M(molar) V (molar) De maneira imprecisa pode-se generalizar, que a densidade aumenta no sentido do elemento químico ósmio, consequentemente a densidade dos metais alcalino-terrosos é maior do que os metais alcalinos: Dentre os elementos destacam-se, como os mais densos, o ósmio (Os) (d = 22,61 g/cm 3 ) e o irídio (Ir) (d = 22,65 g/cm 3 ). Resposta da questão 30: Teremos: Uuq tem 114 elétrons, pois seu número atômico é 114. A geometria molecular da substância cuja fórmula seja UuhH 2 é angular, pois o átomo central (Uuh) está localizado na família VI A. Página 17 de 17
Energias de ionização (ev) 1ª 2ª 3ª 4ª 5ª 6ª 7ª 8ª X 5,4 75,6 122,4 Y 13,6 35,2 54,9 77,4 113,9 138,1 739,1 871,1
 1. (Cefet MG 2014) Na tabela a seguir, estão representadas as energias de ionização de dois elementos X e Y pertencentes ao segundo período do quadro periódico. Elementos Energias de ionização (ev) 1ª
1. (Cefet MG 2014) Na tabela a seguir, estão representadas as energias de ionização de dois elementos X e Y pertencentes ao segundo período do quadro periódico. Elementos Energias de ionização (ev) 1ª
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
Tabela periódica e propriedades periódicas
 Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
Apostila de Química Geral
 Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
AULA 02: TABELA PERIÓDICA
 AULA 02: TABELA PERIÓDICA 1. INTRODUÇÃO A Tabela Periódica é, efetivamente, um instrumento organizador de conhecimentos sobre os elementos químicos, onde estes estão ordenados por ordem crescente de número
AULA 02: TABELA PERIÓDICA 1. INTRODUÇÃO A Tabela Periódica é, efetivamente, um instrumento organizador de conhecimentos sobre os elementos químicos, onde estes estão ordenados por ordem crescente de número
TD nº 02 Química 2 1º ano - 2011
 Prof. Willame TD nº 02 Química 2 1º ano - 2011 TABELA PERIÓDICA 1. A organização dos elementos Com a descoberta de uma grande variedade de átomos, tornou-se necessária à criação de uma sistemática de classificação.
Prof. Willame TD nº 02 Química 2 1º ano - 2011 TABELA PERIÓDICA 1. A organização dos elementos Com a descoberta de uma grande variedade de átomos, tornou-se necessária à criação de uma sistemática de classificação.
Química. Resolução das atividades complementares. Q36 Classificação de elementos
 Resolução das atividades complementares 3 Química Q36 Classificação de elementos p. 24 1 (Fatec-SP) Imagine que a tabela periódica seja o mapa de um continente, e que os elementosquímicos constituem as
Resolução das atividades complementares 3 Química Q36 Classificação de elementos p. 24 1 (Fatec-SP) Imagine que a tabela periódica seja o mapa de um continente, e que os elementosquímicos constituem as
Química. Resolução das atividades complementares. Q42 Ligação metálica
 Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
Química Atomística Profª: Bruna Villas Bôas. Exercícios
 NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling
 Guia do Professor Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling I Introdução A atividade Distribuição Eletrônica favorece o desenvolvimento de
Guia do Professor Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling I Introdução A atividade Distribuição Eletrônica favorece o desenvolvimento de
Lista exercícios N1 Química Geral Tabela Periódica, distribuição eletrônica e ligações químicas.
 1 Parte I - Considere as informações abaixo: Lista exercícios N1 Química Geral Tabela Periódica, distribuição eletrônica e ligações químicas. Núcleo: Prótons e nêutrons. Eletrosfera: elétrons Os átomos
1 Parte I - Considere as informações abaixo: Lista exercícios N1 Química Geral Tabela Periódica, distribuição eletrônica e ligações químicas. Núcleo: Prótons e nêutrons. Eletrosfera: elétrons Os átomos
Goiânia, / / 2014. Elemento Configuração 1 1s 2 2s 2 2p 6 3s 1 2 1s 2 2s 2 2p 4 3 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 4 1s 2 2s 2 2p 6 3s 2 3p 6
 Lista de exercícios - Química Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Goiânia, / / 2014. Questão 01) Localize na Tabela Periódica o elemento químico de número atômico
Lista de exercícios - Química Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Goiânia, / / 2014. Questão 01) Localize na Tabela Periódica o elemento químico de número atômico
Química A Intensivo V. 1
 1 Química A Intensivo V. 1 Exercícios 01) 10 01. Incorreta. O modelo atômico de Dalton não prevê a existência de elétrons. 02. Correta. Segundo Dalton, os átomos eram indestrutíveis e, durante uma reação
1 Química A Intensivo V. 1 Exercícios 01) 10 01. Incorreta. O modelo atômico de Dalton não prevê a existência de elétrons. 02. Correta. Segundo Dalton, os átomos eram indestrutíveis e, durante uma reação
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS PARTE 1 01. A classificação periódica apresenta os elementos na: a) seqüência crescente de números de massa; b) ordem de reatividade química; c) seqüência crescente
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS PARTE 1 01. A classificação periódica apresenta os elementos na: a) seqüência crescente de números de massa; b) ordem de reatividade química; c) seqüência crescente
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Paralela. 2ª Etapa 2014. 1ª série Turma: FG
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
Tabel e a l P rió dica
 Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
Lista 1 Atomística e tabela periódica
 Lista 1 Atomística e tabela periódica 1. (Ufrn 2013) A Lei Periódica e sua representação gráfica, a Tabela Periódica, são dois conhecimentos essenciais para a química e para os químicos. D. Mendeleev (1834-1907),
Lista 1 Atomística e tabela periódica 1. (Ufrn 2013) A Lei Periódica e sua representação gráfica, a Tabela Periódica, são dois conhecimentos essenciais para a química e para os químicos. D. Mendeleev (1834-1907),
1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)?
 EXERCÍCIOS REVISÃO 1ª série 1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)? 2. Qual a fórmula do composto formado entre o potássio, K (Z = 19) e o enxofre, S (Z =
EXERCÍCIOS REVISÃO 1ª série 1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)? 2. Qual a fórmula do composto formado entre o potássio, K (Z = 19) e o enxofre, S (Z =
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007
 Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Próton Nêutron Elétron
 Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II. Elétron de diferenciação e elétrons de valência. Distribuição eletrônica de íons
 DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II Elétron de diferenciação e elétrons de valência O elétron de diferenciação é definido como o último elétron do subnível mais energético de um
DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II Elétron de diferenciação e elétrons de valência O elétron de diferenciação é definido como o último elétron do subnível mais energético de um
Tabela Periódica. Li C S Na Br X K l Te
 1. (Ufg 2013) Para estimular um estudante a se familiarizar com os números atômicos de alguns elementos químicos, um professor cobriu as teclas numéricas de uma calculadora com os símbolos dos elementos
1. (Ufg 2013) Para estimular um estudante a se familiarizar com os números atômicos de alguns elementos químicos, um professor cobriu as teclas numéricas de uma calculadora com os símbolos dos elementos
ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos
 Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Ligações Químicas Ligação Iônica Ligação Metálica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Química A Intensivo V. 1
 Química A Intensivo V. 1 Exercícios 01)A A ideia apresentada na alternativa A, além de algo impossível, não estava incluída na teoria de Dalton que afirmava que átomos iguais pertenciam ao mesmo elemento
Química A Intensivo V. 1 Exercícios 01)A A ideia apresentada na alternativa A, além de algo impossível, não estava incluída na teoria de Dalton que afirmava que átomos iguais pertenciam ao mesmo elemento
Elementos do bloco p
 Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
A) a existência do oceano líquido é uma hipótese possível, pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida.
 TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
O Átomo. a + thomos = sem divisão
 O Átomo 1. O nome átomo tem origem na Grécia Antiga no sec. V a.c. Os pensadores antigos falavam da existência de partículas invisíveis e indivisíveis que formariam toda matéria. a + thomos = sem divisão
O Átomo 1. O nome átomo tem origem na Grécia Antiga no sec. V a.c. Os pensadores antigos falavam da existência de partículas invisíveis e indivisíveis que formariam toda matéria. a + thomos = sem divisão
APSA 2 - Tabela Periódica 10º Ano Novembro de 2011
 1. Dada a distribuição eletrónica dos elementos a seguir, indique qual deles apresenta maior e menor raio atómico 3Li: 1s 2 2s 1 7N: 1s 2 2s 2 2p 3 9F: 1s 2 2s 2 2p 5 R: Maior raio Atómico = Li Menor raio
1. Dada a distribuição eletrónica dos elementos a seguir, indique qual deles apresenta maior e menor raio atómico 3Li: 1s 2 2s 1 7N: 1s 2 2s 2 2p 3 9F: 1s 2 2s 2 2p 5 R: Maior raio Atómico = Li Menor raio
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Teoria Atômica. Constituição da matéria. Raízes históricas da composição da matéria. Modelos atômicos. Composição de um átomo.
 Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
A ESTRUTURA ATÔMICA REPRESENTAÇÃO
 A ESTRUTURA ATÔMICA O modelo nuclear admite que o átomo é formado por uma região central extremamente pequena, o núcleo, em torno do qual giram diminutas partículas, constituindo uma outra região, a eletrosfera.
A ESTRUTURA ATÔMICA O modelo nuclear admite que o átomo é formado por uma região central extremamente pequena, o núcleo, em torno do qual giram diminutas partículas, constituindo uma outra região, a eletrosfera.
Próton Nêutron Elétron
 Próton Nêutron Elétron Próton Nêutron Elétron Número de prótons: 54 2 Nome do elemento: BORO BERÍLIO HÉLIO Esta Os quantidade diferentes tipos de prótons de átomos recebe (elementos o nome químicos) de
Próton Nêutron Elétron Próton Nêutron Elétron Número de prótons: 54 2 Nome do elemento: BORO BERÍLIO HÉLIO Esta Os quantidade diferentes tipos de prótons de átomos recebe (elementos o nome químicos) de
Lista de Exercícios de Recuperação do 3 Bimestre
 Lista de Exercícios de Recuperação do 3 Bimestre Instruções gerais: Resolver os exercícios à caneta e em folha de papel almaço ou monobloco (folha de fichário). Copiar os enunciados das questões. Entregar
Lista de Exercícios de Recuperação do 3 Bimestre Instruções gerais: Resolver os exercícios à caneta e em folha de papel almaço ou monobloco (folha de fichário). Copiar os enunciados das questões. Entregar
Lista de exercícios 12 Propriedades periódicas
 Lista de exercícios 12 Propriedades periódicas 01. (UEG) O gráfico a seguir indica a primeira variação do potencial de ionização, em função dos números atômicos. Analise o gráfico, consulte a tabela periódica
Lista de exercícios 12 Propriedades periódicas 01. (UEG) O gráfico a seguir indica a primeira variação do potencial de ionização, em função dos números atômicos. Analise o gráfico, consulte a tabela periódica
Lista de exercícios 11 Classificação periódica
 Lista de exercícios 11 Classificação periódica 01. (UNESP) Associar os números das regiões da tabela periódica esquematizada a seguir com: a) os metais alcalinos, b) os não-metais, c) os gases nobres,
Lista de exercícios 11 Classificação periódica 01. (UNESP) Associar os números das regiões da tabela periódica esquematizada a seguir com: a) os metais alcalinos, b) os não-metais, c) os gases nobres,
Esse grupo já foi conhecido como gases raros e gases inertes.
 GASES NOBRES GRUPO 18 OU VIIIA Esse grupo já foi conhecido como gases raros e gases inertes. Gases raros não é apropriado porque o argônio (Ar) não é raro (é mais abundante que o CO 2 no ar). Gases Inertes
GASES NOBRES GRUPO 18 OU VIIIA Esse grupo já foi conhecido como gases raros e gases inertes. Gases raros não é apropriado porque o argônio (Ar) não é raro (é mais abundante que o CO 2 no ar). Gases Inertes
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS
 Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Nível 1 2 3 4 5 6 7 Camada K L M N O P Q Número máximo de elétrons 2 8 18 32 32 18 2
 DISTRIBUIÇÃO ELETRÔNICA E TABELA PERIÓDICA dos ELEMENTOS INTRODUÇÃO O conhecimento químico é necessário para uma melhor compreensão sobre as propriedades físicas, químicas e mecânicas dos materiais utilizados,
DISTRIBUIÇÃO ELETRÔNICA E TABELA PERIÓDICA dos ELEMENTOS INTRODUÇÃO O conhecimento químico é necessário para uma melhor compreensão sobre as propriedades físicas, químicas e mecânicas dos materiais utilizados,
2) Um átomo T apresenta menos 2 prótons que um átomo Q. Com base nessa informação, assinale a opção falsa.
 1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
LIGAÇÕES QUÍMICAS TEORIA CORPUSCULAR
 LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
Configurações eletrônicas
 Configurações eletrônicas Metais de transição Depois de Ar, os orbitais d começam a ser preenchidos. Depois que os orbitais 3d estiverem preenchidos, os orbitais 4p começam a ser preenchidos. Metais de
Configurações eletrônicas Metais de transição Depois de Ar, os orbitais d começam a ser preenchidos. Depois que os orbitais 3d estiverem preenchidos, os orbitais 4p começam a ser preenchidos. Metais de
Resoluções das Atividades
 Resoluções das Atividades Sumário Módulo 1 Teoria atômica básica e leis ponderais Evolução dos modelos atômicos Modelo atômico atual 1 Módulo 2 Números quânticos; Distribuição eletrônica Paramagnetismo,
Resoluções das Atividades Sumário Módulo 1 Teoria atômica básica e leis ponderais Evolução dos modelos atômicos Modelo atômico atual 1 Módulo 2 Números quânticos; Distribuição eletrônica Paramagnetismo,
EXERCÍCIOS - TABELA PERIÓDICA - 2012
 EXERCÍCIOS - TABELA PERIÓDICA - 2012 1- (CEUB) Examine atentamente o gráfico que mostra a variação de determinada propriedade X com o número atômico Z. A) A propriedade X é uma propriedade periódica. B)
EXERCÍCIOS - TABELA PERIÓDICA - 2012 1- (CEUB) Examine atentamente o gráfico que mostra a variação de determinada propriedade X com o número atômico Z. A) A propriedade X é uma propriedade periódica. B)
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 1º FG Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 1º FG Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista
Hidrogênio x Hidrogênio Hidrogênio x Não metal Não metal x Não metal
 LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
PROPRIEDADES PERIÓDICAS I
 PROPRIEDADES PERIÓDICAS I Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 Considere as primeiras, segundas, terceiras e quartas energias de ionização dos elementos
PROPRIEDADES PERIÓDICAS I Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 Considere as primeiras, segundas, terceiras e quartas energias de ionização dos elementos
NÚMERO DE OXIDAÇÃO. Porém, nem todos os compostos que existem são formados por íons. Observe a seguinte estrutura: METANO H C
 NÚMER DE XIDAÇÃ INTRDUÇÃ Na química há reações chamadas reações de óxido-redução que são de extrema importância no nosso dia-a-dia. Essas reações (que serão estudadas na próxima unidade) podem apresentar
NÚMER DE XIDAÇÃ INTRDUÇÃ Na química há reações chamadas reações de óxido-redução que são de extrema importância no nosso dia-a-dia. Essas reações (que serão estudadas na próxima unidade) podem apresentar
= 0 molécula. cada momento dipolar existente na molécula. Lembrando que u R
 Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE
 LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
2) Um átomo T apresenta menos 2 prótons que um átomo Q. Com base nessa informação, assinale a opção falsa.
 1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
1) Um átomo, cujo número atômico é 18, está classificado na Tabela Periódica como: a) metal alcalino b) metal alcalinoterroso c) metal terroso d) ametal e) gás nobre 2) Um átomo T apresenta menos 2 prótons
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. A) São elementos que pertencem à família dos gases nobres, portanto, apresentam as camadas de valência completas, o que faz com que a energia necessária para a retirada
SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. A) São elementos que pertencem à família dos gases nobres, portanto, apresentam as camadas de valência completas, o que faz com que a energia necessária para a retirada
Química Geral I. Experimento 3 Tendências Periódicas
 Universidade Estadual do Norte Fluminense Centro de Ciência e Tecnologia Laboratório de Ciências Químicas Química Geral I Experimento 3 Tendências Periódicas 1 - OBJETIVOS Relacionar a reatividade química
Universidade Estadual do Norte Fluminense Centro de Ciência e Tecnologia Laboratório de Ciências Químicas Química Geral I Experimento 3 Tendências Periódicas 1 - OBJETIVOS Relacionar a reatividade química
Química. Química 3 SUMÁRIO. e Pré-vestibular
 Química SUMÁRIO Química 1 MÓDULO 1 Estrutura da matéria - Atomística... 3 Estrutura da matéria: modelos atômicos, Z, A, isótopos e íons Estrutura da matéria: A eletrosfera MÓDULO 2 Classificação periódica
Química SUMÁRIO Química 1 MÓDULO 1 Estrutura da matéria - Atomística... 3 Estrutura da matéria: modelos atômicos, Z, A, isótopos e íons Estrutura da matéria: A eletrosfera MÓDULO 2 Classificação periódica
Qualidade Ambiental Química
 Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
TABELA PERIÓDICA. [Ar] 4s 3d 4p. a) Cu + b) Sn + c) Cd d) Ge + e) Zn + Página 1 de 7
![TABELA PERIÓDICA. [Ar] 4s 3d 4p. a) Cu + b) Sn + c) Cd d) Ge + e) Zn + Página 1 de 7 TABELA PERIÓDICA. [Ar] 4s 3d 4p. a) Cu + b) Sn + c) Cd d) Ge + e) Zn + Página 1 de 7](/thumbs/81/82979659.jpg) 1. (Ufg 013) Para estimular um estudante a se familiarizar com os números atômicos de alguns elementos químicos, um professor cobriu as teclas numéricas de uma calculadora com os símbolos dos elementos
1. (Ufg 013) Para estimular um estudante a se familiarizar com os números atômicos de alguns elementos químicos, um professor cobriu as teclas numéricas de uma calculadora com os símbolos dos elementos
Interbits SuperPro Web
 1. (G1 - cftmg 2012) A Química Inorgânica é uma ciência que estuda vários elementos químicos, dentre eles o enxofre que a) é representado pelo símbolo Se. b) é classificado como um gás nobre. c) pertence
1. (G1 - cftmg 2012) A Química Inorgânica é uma ciência que estuda vários elementos químicos, dentre eles o enxofre que a) é representado pelo símbolo Se. b) é classificado como um gás nobre. c) pertence
UFJF CONCURSO VESTIBULAR 2011-2 GABARITO DA PROVA DISCURSIVA DE QUÍMICA
 UFJF CNCURS VESTIBULAR 2011-2 GABARIT DA PRVA DISCURSIVA DE QUÍMICA Questão 1 Sabe-se que compostos constituídos por elementos do mesmo grupo na tabela periódica possuem algumas propriedades químicas semelhantes.
UFJF CNCURS VESTIBULAR 2011-2 GABARIT DA PRVA DISCURSIVA DE QUÍMICA Questão 1 Sabe-se que compostos constituídos por elementos do mesmo grupo na tabela periódica possuem algumas propriedades químicas semelhantes.
QUÍMICA Profª Msc. Érika Almeida
 TABELA PERIÓDICA. Mendeleev (869): organizou os elementos da tabela periódica em ordem crescente de massa atômica e de propriedades; 2. Moseley (887-95): organizou os elementos químicos com base no número
TABELA PERIÓDICA. Mendeleev (869): organizou os elementos da tabela periódica em ordem crescente de massa atômica e de propriedades; 2. Moseley (887-95): organizou os elementos químicos com base no número
Exercícios Sobre LigaÇões iônicas
 Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
 Lista de exercícios - Bloco 1 - Aula 21 a 24 - Tabela Periódica. 1. (Uerj 2017) O rompimento da barragem de contenção de uma mineradora em Mariana (MG) acarretou o derramamento de lama contendo resíduos
Lista de exercícios - Bloco 1 - Aula 21 a 24 - Tabela Periódica. 1. (Uerj 2017) O rompimento da barragem de contenção de uma mineradora em Mariana (MG) acarretou o derramamento de lama contendo resíduos
Propriedades Químicas
 Álvaro Montebelo Barcelos Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Álvaro Montebelo Barcelos Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
PROPRIEDADES PERIÓDICAS II
 PROPRIEDADES PERIÓDICAS II EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Com relação à classificação periódica dos elementos, pode-se afirmar que o: a) hidrogênio é um metal alcalino localizado na 1ª coluna. b)
PROPRIEDADES PERIÓDICAS II EXERCÍCIOS DE APLICAÇÃO 01 (PUC-RS) Com relação à classificação periódica dos elementos, pode-se afirmar que o: a) hidrogênio é um metal alcalino localizado na 1ª coluna. b)
ESPECTRO ELETROMAGNÉTICO
 COLÉGIO ESTADUAL RAINHA DA PAZ, ENSINO MÉDIO REPOSIÇÃO DAS AULAS DO DIA 02 e 03/07/2012 DAS 1 ª SÉRIES: A,B,C,D,E e F. Professor MSc. Elaine Sugauara Disciplina de Química ESPECTRO ELETROMAGNÉTICO As ondas
COLÉGIO ESTADUAL RAINHA DA PAZ, ENSINO MÉDIO REPOSIÇÃO DAS AULAS DO DIA 02 e 03/07/2012 DAS 1 ª SÉRIES: A,B,C,D,E e F. Professor MSc. Elaine Sugauara Disciplina de Química ESPECTRO ELETROMAGNÉTICO As ondas
Como sendo aquelas cujos valores variam apenas com o número atômico e não com a ordem da Tabela Periódica. São propriedades que não se repetem em
 Como sendo aquelas cujos valores variam apenas com o número atômico e não com a ordem da Tabela Periódica. São propriedades que não se repetem em ciclos, períodos ou famílias. O Calor Específico varia
Como sendo aquelas cujos valores variam apenas com o número atômico e não com a ordem da Tabela Periódica. São propriedades que não se repetem em ciclos, períodos ou famílias. O Calor Específico varia
Química 1 Química Geral 1
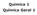 α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS. Aluno(a): Turma:
 IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
CADERNO DE EXERCÍCIOS 1D
 CADERNO DE EXERCÍCIOS 1D Ensino Fundamental Ciências da Natureza II Questão Conteúdo Habilidade da Matriz da EJA/FB 01 Propriedades e aplicação dos materiais H55/H56 02 Propriedades específicas, físicas
CADERNO DE EXERCÍCIOS 1D Ensino Fundamental Ciências da Natureza II Questão Conteúdo Habilidade da Matriz da EJA/FB 01 Propriedades e aplicação dos materiais H55/H56 02 Propriedades específicas, físicas
Lista de Exercício de Química - N o 6
 Lista de Exercício de Química - N o 6 Profa. Marcia Margarete Meier 1) Arranje em ordem crescente de energia, os seguintes tipos de fótons de radiação eletromagnética: raios X, luz visível, radiação ultravioleta,
Lista de Exercício de Química - N o 6 Profa. Marcia Margarete Meier 1) Arranje em ordem crescente de energia, os seguintes tipos de fótons de radiação eletromagnética: raios X, luz visível, radiação ultravioleta,
Gabarito - Química - Grupo A
 1 a QUESTÃO: (1,5 ponto) Avaliador Revisor A estrutura dos compostos orgânicos começou a ser desvendada nos meados do séc. XIX, com os estudos de ouper e Kekulé, referentes ao comportamento químico do
1 a QUESTÃO: (1,5 ponto) Avaliador Revisor A estrutura dos compostos orgânicos começou a ser desvendada nos meados do séc. XIX, com os estudos de ouper e Kekulé, referentes ao comportamento químico do
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE
 -2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
05 - (UEL PR/1994) Localize na tabela periódica o elemento químico de número atômico 20 e escolha a(s)
 01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
Polaridade de moléculas
 Polaridade de moléculas 01. (Ufscar) É molécula polar: a) C 2 H 6. b) 1,2-dicloroetano. c) CH 3 Cl. d) p-diclorobenzeno. e) ciclopropano. 02. (Mackenzie) As fórmulas eletrônicas 1, 2 e 3 a seguir, representam,
Polaridade de moléculas 01. (Ufscar) É molécula polar: a) C 2 H 6. b) 1,2-dicloroetano. c) CH 3 Cl. d) p-diclorobenzeno. e) ciclopropano. 02. (Mackenzie) As fórmulas eletrônicas 1, 2 e 3 a seguir, representam,
Nº máximo 2 8 18 32 32 18 2. Camadas K L M N O P Q 20 Ca (Z=20) 2 8??
 Ligações químicas Na natureza, todos os sistemas tendem a adquirir a maior estabilidade possível. Os átomos ligam-se uns aos outros para aumentar a sua estabilidade. Os gases nobres são as únicas substâncias
Ligações químicas Na natureza, todos os sistemas tendem a adquirir a maior estabilidade possível. Os átomos ligam-se uns aos outros para aumentar a sua estabilidade. Os gases nobres são as únicas substâncias
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014
 RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL
 RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
Nesse sistema de aquecimento,
 Enem 2007 1- Ao beber uma solução de glicose (C 6 H 12 O 6 ), um corta-cana ingere uma substância: (A) que, ao ser degradada pelo organismo, produz energia que pode ser usada para movimentar o corpo. (B)
Enem 2007 1- Ao beber uma solução de glicose (C 6 H 12 O 6 ), um corta-cana ingere uma substância: (A) que, ao ser degradada pelo organismo, produz energia que pode ser usada para movimentar o corpo. (B)
[A] Incorreta. O amálgama é uma liga metálica, ou seja, uma mistura homogênea, em que o principal componente é o mercúrio. [Xe] 6s 4f 5d.
![[A] Incorreta. O amálgama é uma liga metálica, ou seja, uma mistura homogênea, em que o principal componente é o mercúrio. [Xe] 6s 4f 5d. [A] Incorreta. O amálgama é uma liga metálica, ou seja, uma mistura homogênea, em que o principal componente é o mercúrio. [Xe] 6s 4f 5d.](/thumbs/63/49104574.jpg) Gabarito: Resposta da questão 1: A representação do elemento químico do átomo da espécie responsável pela coloração pertence à família dos metais alcalinos-terrosos da tabela periódica, ou seja, família
Gabarito: Resposta da questão 1: A representação do elemento químico do átomo da espécie responsável pela coloração pertence à família dos metais alcalinos-terrosos da tabela periódica, ou seja, família
Projeto Embuá Unidade de Aprendizagem: ENERGIA
 Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
AULA 1: EXERCÍCIOS DE FIXAÇÃO QUÍMICA AULA 1: EXERCÍCIOS DE FIXAÇÃO ELEMENTOS QUÍMICOS, TABELA PERIÓDICA, PROPRIEDADES PERIÓDICAS.
 QUÍMICA AULA 1: EXERCÍCIOS DE FIXAÇÃO ELEMENTOS QUÍMICOS, TABELA PERIÓDICA, PROPRIEDADES PERIÓDICAS. Professora Priscila Miranda E-mail: miranda.educacao@gmail.com WhatsApp: +5511976100005 Turmas de Agosto
QUÍMICA AULA 1: EXERCÍCIOS DE FIXAÇÃO ELEMENTOS QUÍMICOS, TABELA PERIÓDICA, PROPRIEDADES PERIÓDICAS. Professora Priscila Miranda E-mail: miranda.educacao@gmail.com WhatsApp: +5511976100005 Turmas de Agosto
Respostas da terceira lista de exercícios de química. Prof a. Marcia M. Meier
 Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
TABELA PERIÓDICA Propriedades periódicas e aperiódicas
 TABELA PERIÓDICA Propriedades periódicas e aperiódicas De um modo geral, muitas propriedades dos elementos químicos variam periodicamente com o aumento de seus números atômicos (portanto, ao longo dos
TABELA PERIÓDICA Propriedades periódicas e aperiódicas De um modo geral, muitas propriedades dos elementos químicos variam periodicamente com o aumento de seus números atômicos (portanto, ao longo dos
ATENÇÃO: O DESENVOLVIMENTO TEÓRICO DAS QUESTÕES É OBRIGATÓRIO
 IX Olimpíada Capixaba de Química 2011 Prova do Grupo II 2 a série do ensino médio Fase 02 Aluno: Idade: Instituição de Ensino: Coordenador da Instituição de Ensino: ATENÇÃO: O DESENVOLVIMENTO TEÓRICO DAS
IX Olimpíada Capixaba de Química 2011 Prova do Grupo II 2 a série do ensino médio Fase 02 Aluno: Idade: Instituição de Ensino: Coordenador da Instituição de Ensino: ATENÇÃO: O DESENVOLVIMENTO TEÓRICO DAS
Ministério da Educação Universidade Federal do Paraná Setor Palotina
 Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 5 Íons e Introdução a Tabela Periódica Prof. Isac G. Rosset Prof. Isac G. Rosset - UFPR - Palotina - Ciências Exatas 2 1 d p s
Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 5 Íons e Introdução a Tabela Periódica Prof. Isac G. Rosset Prof. Isac G. Rosset - UFPR - Palotina - Ciências Exatas 2 1 d p s
Química. Resolução das atividades complementares. Q49 Polaridade das moléculas
 Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
PROF: Alex LISTA 7 DATA: 21/08/2011 Propriedades Periódicas e Ligações (Exercícios Gerais)
 NOME: PROF: Alex LISTA 7 DATA: 21/08/2011 Propriedades Periódicas e Ligações (Exercícios Gerais) 01 - (UDESC SC/2011) De acordo com as propriedades periódicas dos elementos químicos, analise as proposições
NOME: PROF: Alex LISTA 7 DATA: 21/08/2011 Propriedades Periódicas e Ligações (Exercícios Gerais) 01 - (UDESC SC/2011) De acordo com as propriedades periódicas dos elementos químicos, analise as proposições
Aluno (a): Professor:
 3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves
 Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Tecnologia Mecânica MATERIAIS. Roda de aço. Mapa do Brasil em cobre. Prof. Marcio Gomes
 Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
Associação de Geradores
 Associação de Geradores 1. (Epcar (Afa) 2012) Um estudante dispõe de 40 pilhas, sendo que cada uma delas possui fem igual a 1,5 V e resistência interna de 0,25. Elas serão associadas e, posteriormente,
Associação de Geradores 1. (Epcar (Afa) 2012) Um estudante dispõe de 40 pilhas, sendo que cada uma delas possui fem igual a 1,5 V e resistência interna de 0,25. Elas serão associadas e, posteriormente,
Correção da ficha de trabalho N.º3
 Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
Química A Semiextensivo V. 2
 Química A Semiextensivo V. Exercícios 0) B 0) A 0) A Símbolo N: elemento Nitrogênio Símbolo P: elemento Fósforo (do latim Phosphorus) Símbolo K: elemento Potássio (do latim Kalium) Trata-se de uma questão
Química A Semiextensivo V. Exercícios 0) B 0) A 0) A Símbolo N: elemento Nitrogênio Símbolo P: elemento Fósforo (do latim Phosphorus) Símbolo K: elemento Potássio (do latim Kalium) Trata-se de uma questão
LIGAÇÕES QUÍMICAS. Um novo jeito de se aprender química Helan Carlos e Lenine Mafra- Farmácia- 2014.2
 ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
UFSC. Química (Amarela) 31) Resposta: 43. Comentário
 UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
Tarefa online 9º ano Química Juliana
 Tarefa online 9º ano Química Juliana 1) Um elemento químico X apresenta configuração eletrônica 1s2 2s2 2p4. Podemos afirmar que, na tabela periódica, esse elemento químico está localizado no a) 2 º período,
Tarefa online 9º ano Química Juliana 1) Um elemento químico X apresenta configuração eletrônica 1s2 2s2 2p4. Podemos afirmar que, na tabela periódica, esse elemento químico está localizado no a) 2 º período,
Química A Extensivo V. 3
 Extensivo V. 3 Exercícios 01) a) Z = 17-1s 2 2s 2 2p 6 3s 2 3p 5 - C - 3 período b) Z = 20-1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 - Ca - 4 período c) Z = 32-1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 2 - Ge - 4 período
Extensivo V. 3 Exercícios 01) a) Z = 17-1s 2 2s 2 2p 6 3s 2 3p 5 - C - 3 período b) Z = 20-1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 - Ca - 4 período c) Z = 32-1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 2 - Ge - 4 período
