ARTIGO ÍON BEH + EM CAMPO ELÉTRICO UNIFORME INTENSO
|
|
|
- Ricardo Damásio Azambuja
- 7 Há anos
- Visualizações:
Transcrição
1 ARTIGO ÍON BEH + EM CAMPO ELÉTRICO UNIFORME INTENSO Assis Francisco Moro Righi Departamento de Química - Universidade Federal de Santa Catarina - Florianópolis - SC Carlos Alberto Kuhnen Departamento de Física - Universidade Federal de Santa Catarina - Florianópolis - SC Recebido em 6/3/98; aceito em 5/0/98 ÍON BEH + ON INTENSE ELETRIC FIELD. The influence of a strong external electric field in chemical bonding is not extensively studied. In this work, the behavior of the potential energy curves of the BeH + ion in an external electric field is investigated by means of variational calculations using molecular orbitals. For simplicity we consider the case where the external field is parallel to the molecular axis, in the direction of the dipole moment, which raises the polarization of the ion. The effects on dissociation are investigated. Keywords: total energy; slater exponents; elétric field; dipole moment. INTRODUÇÃO O íon hidreto de berílio, BeH +, contrariamente à molécula LiH que também tem quatro elétrons, não tem sido muito estudado teoricamente ou experimentalmente. Trabalhos experimentais foram realizados por Koontz, Watson e Humphreys 2 e Knave 3. Do ponto de vista teórico, o estado fundamental X + tem sido investigado em detalhes -7 e alguns trabalhos sobre o estado A + foram divulgados recentemente 8 0. Todos estes trabalhos estudam o íon BeH + na ausência de um campo externo. O efeito de um campo elétrico externo nos níveis eletrônicos em geral é investigado usando-se a teoria de perturbações -2. Neste caso, o estudo se limita a situações em que o campo externo não é muito intenso (em torno de 0 6 V/m ou 0-5 u.a.). É interessante investigar a influência de campos mais fortes, próximos de 0 - u.a., na ligação química. A curva de energia potencial do estado fundamental do íon BeH + em campos desta intensidade é determinada neste trabalho. Algumas propriedades do estado fundamental do íon BeH + são obtidas fazendo-se um cálculo variacional com uma base de orbitais moleculares formados com uma combinação linear de orbitais atômicos do tipo de Slater (STOs). Uma abordagem alternativa para obter as integrais de um e dois centros que aparecem na resolução da equação de Schrödinger foi recentemente desenvolvida por nós e aplicada com sucesso na molécula LiH 3. A partir dos STOs envolvidos, os programas desenvolvidos na linguagem de manipulação algébrica REDUCE calculam estas integrais de um e de dois elétrons. Os resultados são fornecidos em forma analítica e podem ser usados por linguagens de programação convencional como o FORTRAN. Estas soluções reduzem o tempo necessário para recalcular as integrais quando são feitas alterações na distância internuclear ou nos expoentes dos orbitais atômicos (expoentes de Slater). CURVAS DE ENERGIA POTENCIAL O operador hamiltoniano para o íon BeH + tem a seguinte forma (em unidades atômicas): H = 2 2 k Z a Z b r + k= ak 2 r bk r i r k + Z a Z b () R i k= Nesta equação Z a é a carga do núcleo de hidrogênio e Z b é a carga do núcleo de berílio, R é a distância entre os dois núcleos, r ak (r bk ) é a distância do elétron k ao núcleo a (b) e k 2 é o operador Laplaciano atuando sobre as coordenadas eletrônicas. Neste trabalho a equação de Schrödinger é resolvida fazendo-se um cálculo variacional através do método dos orbitais moleculares 3, onde a função de onda (função tentativa) consiste em uma determinada combinação de determinantes de Slater. Ao invés de se utilizar o método de Roothaan 5-6, faz-se diretamente a otimização dos coeficientes lineares e não lineares da função de onda utilizando-se a rotina ZXMIN (que determina o mínimo de uma função de N variáveis através do método de quase-newton) do pacote comercial de rotinas matemáticas IMSL. Os orbitais moleculares são construídos a partir de orbitais atômicos do tipo de Slater. Os STOs foram escolhidos pois descrevem corretamente a densidade de carga perto do núcleo e também à grandes distâncias, enquanto que os orbitais do tipo gaussiano (GTO) não satisfazem estes critérios. Além disso, uma pequena base de STOs é suficiente para fornecer os mesmos resultados que os obtidos com uma grande base de GTOs. Entretanto, as integrais com STO são muito mais difíceis de serem resolvidas O seguinte conjunto mínimo de orbitais atômicos necessário para descrever o estado eletrônico da molécula é utilizado para formar os orbitais moleculares: χ s ( r r a ) = χ s ( r r b ) = ζ 3 a π e ζ ar a ζ 3 b π e ζ b r b χ * 2s ( r b ) = ζ 5 2 2rb 3π e ζ rb χ 2 p ( r b ) = ζ 5 3 π e ζ 3 r b r b cosθ b Nestas equações, o núcleo de Be está representado pela letra b e o núcleo de H pela letra a; r a é a distância ao núcleo a e r b é a distância ao núcleo b; o eixo polar coincide com o eixo internuclear; θ é o ângulo entre este eixo e o raio vetorial r r b do elétron; ζ i é o expoente de Slater do orbital atômico. O QUÍMICA NOVA, 22(3) (999) 39
2 orbital molecular u, ocupado pelos elétrons internos do átomo de berílio, é formado pelo orbital atômico s (χ s ( r b ) ), e os orbitais moleculares u m e u m são construídos com os orbitais atômicos 2 s e 2 p do berílio (χ * 2s ( rb) r e χ 2 p ( rb)) r e o orbital s do hidrogênio (χ s ( r a )). A função de onda Ψ, do tipo singleto, tem seguinte a forma: Ψ= (u l ) 2 (u m ) α (u m) β - (u l ) 2 (u m ) β(u m ) α (2) Esta configuração foi escolhida pois o estado fundamental deve ser antissimétrico à troca dos spins e simétrico à troca das coordenadas espaciais. O valor esperado da energia eletrônica do íon BeH + é igual a: E (Ψ) = [I mm + I m m + 2I + 2 so ( so I + I mm ) + J mm + J + 2J lm +2J lm - K lm - K lm +so 2 J ll + so < ll mm > 2so < lm lm >+K mm ]/(+ so 2 ) r 2 r 2 + Z a Z b (3) R Nesta equação, so é a integral de superposição entre os orbitais moleculares u m e u m, ou seja: so = u m u m e: I λλ = µ * λ ( r k ) 2 2 k Z a Z b r ak r bk J λµ = u µ (r r ) 2 u λ ( r 2 ) 2 r 2 r dr 3 3 dr 2 µ λ (r 3 r k )dr k K λµ = u * µ ( r )u λ ( r )u µ ( r 2 )u * λ ( r 2 ) r 2 r dr 3 3 dr 2 I λλ é o valor médio do hamiltoniano de elétrons individuais, J λµ é a energia de interação coulombiana entre os orbitais moleculares e K λµ é a energia de troca. Além dos termos de coulomb e de troca também aparece outra forma de interação entre os orbitais moleculares do tipo: < lm lm >= r 2 u * l ( r )u m ( )u l ( r 2 )u m r r 2 * ( r 2 ) dr dr 2 Estas equações foram obtidas através de programação algébrica com o REDUCE, uma linguagem de programação que tem como principal característica a possibilidade de se fazer cálculos algébricos no computador, além dos cálculos numéricos convencionais. ENERGIA POTENCIAL ELÉTRICA Uma molécula diatômica num campo externo uniforme tem uma energia potencial adicional associada a este campo do tipo: Z a +Z b U E = E(Z a R r bi cosθ bi ) () onde E é o campo externo uniforme, Z a (Z b ) é a carga do núcleo a (b), e θ bi é o ângulo entre o eixo internuclear e o raio vetorial do elétron i ( r r bi ) em relação ao núcleo b. Outra expressão semelhante também pode ser facilmente obtida: Z a +Z b U E = E( Z b R r ai cosθ ai ) (5) onde θ ai é o ângulo entre o eixo internuclear e o raio vetorial do elétron i( r r ai ) em relação ao núcleo a. Essas expressões são válidas para moléculas diatômicas neutras, pois neste caso a energia potencial elétrica relacionada ao campo externo independe do ponto de referência em que o potencial é escolhido como nulo. Entretanto, para íons o resultado depende deste ponto de referência. Considere o íon hídreto de berílio BeH + num campo externo uniforme paralelo ao momento de dipolo. Escolhendo-se o potencial nulo sobre o átomo de berílio, a energia potencial elétrica extra relacionada com o campo externo tem a seguinte forma: U E = E(R r bi cosθ bi ) (6) onde o núcleo do Berílio está localizado no ponto b. Mas definindo o potencial nulo no centro de massa da molécula se obtém: m Be U E = E( R r bi cosθ bi ) m H + m (7) Be na qual m H é a massa atômica de hidrogênio e m Be é a massa atômica do berílio. É importante considerar o caso mais simples de duas cargas + u.a. e u.a. num campo elétrico externo uniforme E aplicado paralelamente ao dipolo. A energia potencial elétrica do sistema é igual a: U = R ER onde R é a distância entre as cargas. Para valores grandes de R o segundo termo é predominante e descreve uma diminuição linear da energia potencial (que é uma característica dos processos de separação iônica). Então, considerando uma molécula num campo, se a energia potencial diminuir a partir de determinado valor da separação nuclear, significa que a dissociação deve ser do tipo iônica. Com uma função de onda Ψ do tipo singleto, o valor esperado da equação (6) tem a forma: < U E >= E{R ( + so 2 ) [ 2 < u l rcosθ u l > <u m rcosθ u m >- <u m rcosθ u m >+2so(so < u l rcosθ u l >+<u m rcosθ u m >) ] } Nesta expressão, é preciso avaliar integrais de um elétron contendo no integrando a quantidade r cosθ. A seguir é mostrada a solução analítica para uma destas integrais, obtida por programação algébrica, com técnicas desenvolvidas por nós em trabalho anterior 3 (integais deste tipo também aparecem no cálculo do momento de dipolo que é discutido a seguir). < χ p ( r r b ) r b cosθ b χ s ( r r a ) >= (8. ζ 3 ζ a (.e Rζ 3 (6.(7.ζ 2 a + ζ 2 3 )R 2 ζ a + (5.ζ 2 a + ζ 2 3 )(ζ a + ζ 3 ) (ζ a ζ 3 )R Rζ 2 a + 96.ζ a )ζ 3 + e Rζ a (.(ζ 2 a +7.ζ 2 3 ) (ζ a + ζ 3 )(ζ a ζ 3 )R (ζ a + 3.ζ 3 )(ζ a 3.ζ 3 )R 2 ζ 3 + (ζ a + ζ 3 ) 3 (ζ a ζ 3 ) 3 R 5 2.(ζ a + ζ 3 ) 2 (ζ a ζ 3 ) 2 R ζ Rζ ζ 3 )ζ a )ζ a ζ 2 3 )/ (e (Rζ a +Rζ 3 ) (ζ a + ζ 3 ) 5 (ζ a ζ 3 ) 5 R 3 ) (8) 320 QUÍMICA NOVA, 22(3) (999)
3 onde χ 2p ( r r b ) é o orbital 2 P centrado no núcleo b, χ s ( r r a ) é o orbital s centrado no núcleo a, ζ 3 e ζ a são os respectivos expoentes destes orbitais atômicos e R é a distância entre os núcleos. MOMENTO DE DIPOLO O momento de dipolo µ de uma molécula diatômica na direção do eixo molecular é definido pela equação: expoentes fixos são aqueles otimizados em R = 2,5 bohrs, ou seja, na região de equilíbrio. Outra causa desta diferença reside no fato de que a função de onda molecular por nós utilizada descreve bem o estado de equilíbrio, mas o comportamento assintótico não é bem descrito por esta função. Entretanto, acreditamos que esta diferença pode ser eliminada com um refinamento nos cálculos, ampliando o conjunto de funções da base. µ e (R) = e r i cosθ i + e Z n R n (9) i onde Z n é a carga do núcleo n, R n é a distância ao núcleo n, r i é a distância ao elétron i (da origem do sistema de coordendas) e θ i é o ângulo entre o eixo internuclear e o raio vetorial do elétron i( r r i ). O momento de dipolo independe da origem do sistema de coordenadas para moléculas neutras. Para íons, entretanto, o resultado depende da origem escolhida. Para o íon hidreto de berílio, escolhendo a origem das coordenadas no átomo de berílio, se obtém: µ e (R) = e r i cosθ i + er (0) i= onde R é a separação nuclear. De acordo com esta equação, o momento de dipolo negativo indica que a nuvem eletrônica está parcialmente deslocada para o átomo de hidrogênio (µ< 0 se refere a configuração Be +δ + H δ- ). Esta equação é semelhante a equação (6) para a energia potencial adicional devida ao campo externo. O valor esperado do momento de dipolo com uma função de onda do tipo singleto tem, portanto, uma forma semelhante a equação (8). 5. RESULTADOS PARA O ÍON BEH + A Figura mostra as curvas de energia eletrônica para o estado X + do íon hidreto de berílio BeH +, com um conjunto fixo de expoentes dos orbitais atômicos e com um conjunto de expoentes otimizados. Próximo ao ponto de equilíbrio as duas curvas coincidem, pois o conjunto fixo de expoentes usado consiste dos expoentes ótimos calculados para R = 2,5 bohrs. A diferença entre as duas curvas torna-se mais evidente para valores de R maiores do que bohrs. Nestes cálculos de energia eletrônica se obtém uma distância internuclear de equilíbrio R e = 2,537 bohrs, que está próxima do resultado experimental R ex = 2,79 bohrs. A energia eletrônica em R ex é E = -, 863 hartrees. Este valor é quase o limite de Hartree-Fock obtido por Machado e Ornellas 0 E = -, 850 hartrees, onde eles usaram uma grande base de orbitais gaussianos: (3s9pdf)/ [9s7pdf] para o Be e (8s2p2d)/[5s2p2d] para o H, resultando em 87 funções gaussianas contraídas. Há uma pequena diferença entre estes valores, e a base de funções utilizada neste trabalho usa somente orbitais σ, confirmando que o método fornece resultados precisos para a energia não-correlacionada usando uma base mínima de orbitais. Nosso valor está também acima do melhor valor para o íon BeH+ obtido por Machado e Ornellas 0, E = -,937 hartrees, num cálculo de interação de configurações (CI) com uma grande base de orbitais gaussianos. A diferença de energia entre estes valores e nossos resultados é da ordem de grandeza da energia de correlação. A energia de dissociação obtida neste trabalho é de 0,0882 u.a. (2,0 ev) para o cálculo com os expoentes otimizados. Por outro lado, a energia de dissociação para o cálculo não otimizado é de 0, u.a. (3,02 ev). Como o valor experimental para a energia de dissociação é 3,28eV, vemos que o resultado para o cálculo não otimizado tem um erro percentual menor (8%) do que o obtido com a otimização (27%). A diferença entre estas energias de dissociação pode ser explicada notando-se que os Figura. Curva de energia eletrônica para o estado X + do íon BeH +. Resultados (a) com expoentes fixos e (b) com expoentes otimizados..u.a. = 27,209 e V. Os expoentes dos orbitais, em função da separação nuclear, são mostrados na Figura 2 para os orbitais atômicos s (H), 2s (Be) e 2p (Be). O expoente do orbital atômico s (Be) permanece praticamente constante, porque o orbital ocupado pelos elétrons internos do átomo de berílio não se superpõe aos outros orbitais da molécula. Nesta figura se percebe que ocorre uma suave diminuição dos expoentes no processo de dissociação. Ocorre, portanto, um pequeno alongamento radial dos orbitais atômicos com o aumento da separação nuclear. Isto significa que há um alargamento da nuvem eletrônica à medida que ocorre a dissociação. Para o orbital 2p observamos um maior alongamento, indicando uma maior participação na ligação para os valores grandes de R. Com relação a confiabilidade dos resultados, a utilização da computação algébrica diminui muito as possibilidades de erro. Além disso, como podemos observar na Figura 2, o expoente do orbital s do H tende a,0 no processo de dissociação, que é o valor exato para este expoente no átomo isolado. O momento de dipolo calculado em várias distâncias internucleares é mostrado na Figura 3 com a origem no átomo de berílio. Para valores grandes de R o momento de dipolo se anula, indicando que ocorre dissociação do tipo Be + + H. A Figura compara o momento de dipolo obtido neste trabalho com o calculado por Machado e Ornellas, considerando a origem do sistema de coordenadas no centro de massa. Os resultados concordam muito bem e para R = 2,5 bohrs nós obtivemos µ = -,2366 u.a. para o momento de dipolo enquanto que Machado e Ornellas obtiveram µ= -.60 u.a.. A Figura 5 mostra as curvas de energia potencial do íon BeH + em um campo elétrico externo paralelo ao eixo molecular. Estas curvas foram obtidas considerando-se nulo o potencial associado ao campo externo no átomo de Be. As curvas são semelhantes se o potencial nulo for escolhido sobre o centro de massa do íon. Em campos mais intensos, a energia potencial diminui a partir de determinado valor da separação nuclear. Essa diminuição é uma característica de dissociação iônica do tipo Be ++ + H -. Quando íons colidem com uma QUÍMICA NOVA, 22(3) (999) 32
4 moléculas também pode produzir, em colisões, um campo elétrico com intensidade suficiente para que a dissociação iônica ocorra. Figura 2. Expoentes dos orbitais em função da distância internuclear. Figura 5. Curvas de energia eletrônica para o estado X + do íon BeH + em campo elétrico E uniforme. (a) E = 0,00 u.a.; (b) E = 0,0 u.a.; (c) E = 0,08 u.a.; (d) E = 0,2 u.a.; (e) E = 0,6 u.a.; Os expoentes dos orbitais em função do campo elétrico externo são mostrados na Figura 6 para R = 2,50 bohrs. Pode-se ver que há uma redução do expoente do orbital do átomo de hidrogênio quando o campo elétrico externo aumenta. Para átomos neutros se observa um resultado semelhante ao obtido na molécula LiH 3, ou seja, o campo elétrico externo causa um alongamento radial do orbital atômico que é proporcional a intensidade do campo externo. Os orbitais do íon Be + mostram, entretanto, um comportamento diferente, ou seja, eles se contraem com o aumento do campo externo. O efeito da carga nuclear do íon berílio Be + deve predominar sobre o campo elétrico externo. Figura 3. Momento de dipolo do íon BeH + com origem no átomo de Berílio..u.a. = 2,58 D. Figura 6. Expoentes dos orbitais em função do campo elétrico, em R = 2,5 bohrs. Figura. Momento de dipolo do íon BeH + com origem no centro de massa: (a) obtido neste trabalho; (b) calculado por Machado e Ornellas. molécula de BeH + produzem campos não uniformes mas próximos a 0, u.a., nos quais ocorre dissociação iônica da molécula BeH +. Além disso, o momento de dipolo de algumas Os expoentes ótimos também foram calculados considerando que o potencial associado ao campo externo é nulo no centro de massa do sistema. Estes expoentes são iguais aos calculados escolhendo-se o potencial nulo no átomo de Be. Este resultado é esperado pois como os expoentes descrevem fisicamente o comportamento da nuvem eletrônica, eles devem ser independentes 322 QUÍMICA NOVA, 22(3) (999)
5 do ponto de referência em que o potencial é nulo, embora as curvas de energia potencial dependam do mesmo. A Figura 7 mostra as curvas obtidas para o momento de dipolo do íon BeH + num campo elétrico externo uniforme, considerando a origem do sistema de coordenadas no átomo de Be. Para valores altos do campo elétrico, E = 0,2 u.a. e E = 0,6 u.a., se observa que µ cresce linearmente, caracterizando dissociação iônica do tipo Be ++ + H -. Hartree-Fock com uma base mínima de funções. Além disso, os resultados obtidos para o momento de dipolo do BeH + concordam com outros cálculos realizados usando uma base com um grande número de funções e interação de configurações. AGRADECIMENTOS Os programas em REDUCE foram desenvolvidos com a versão 3.. do Departamento de Informática e Estatística da UFSC e os programas em FORTRAN rodaram no compilador f90 instalado no Centro Nacional de Supercomputação da UFRGS. REFERÊNCIAS Figura 7. Momento de dipolo do íon BeH + em campo elétrico E uniforme. (a) E = 0,00 u.a.; (b) E = 0,0 u.a.; (c) E = 0,08 u.a.; (d) E = 0,2 u.a.; (e) E = 0,6 u.a.. 6. CONCLUSÃO Os cálculos no íon BeH + sem campo externo mostram que os expoentes otimizados diminuem à medida que a separação nuclear aumenta, indicando um efeito de alongamento radial dos orbitais atômicos quando a dissociação ocorre, semelhante ao obtido para a molécula LiH 3. Este efeito implica numa interação mais forte entre os átomos e também num alargamento da nuvem eletrônica dos átomos durante a dissociação. Um campo elétrico externo muito intenso modifica as características do processo de dissociação molecular pois se observa uma diminuição das curvas de energia potencial a partir de determinado valor das separação nuclear, a qual é uma característica dos processos de dissociação de íons. Sem campo externo ou em campos fracos o íon BeH + se dissocia em Be + e H, mas em campos mais fortes ocorre dissociação do tipo Be ++ e H -. As curvas de momento de dipolo em função da separação nuclear, na presença de um campo externo, também confirmam estes resultados. A otimização dos expoentes é importante para bases pequenas pois se obteve valores muito próximos do limite de. Koontz, P. G.; Phys. Rev. 935, 8, Watson, W. W.; Humphreys, R. F.; Phys. Rev. 937, 52, Knave, E. B.; Dissertation, Uppsala University Rosmus, P.; Meyer, W.; J. Chem. Phys. 977, 66, Ornellas, F. R.; J. Phys. B 982, 5, Ornellas, F. R.; J. Mol. Struct. 983, 92, Ornellas, F. R.; Stwalley, W.C.; Zemke, W. T.; J. Chem. Phys. 983, 79, Ornellas, F. R.; J. Chem. Phys. 985, 82, Machado, F. B. C.; Ornellas, F. R.; J. Molec. Struct. (Theochem) 990, 20, Machado, F. B. C.; Ornellas, F. R.; J. Chem. Phys. 99, 9, Herzberg, G.; Molecular Spectra and Molecular Structure, Vol. I, Spectra of Diatomic Molecules, Van Nostrand Reinhold, New York Lowe, J. P.; Quantum Chemistry, Academic Press Limited, London Righi, A. F. M.; Kuhnen, C. A.; Intern. J. Mod. Phys. C. 997, 8, 59. Hearn, A. C.; REDUCE User s Manual, Version 3., RAND publication CP78, Santa Mônica, CA Kotani, M.; Ohmo, K.; Kayama, K.; Quantum Mechanics of Eletronic structure of Simple Molecules, Encyclopedia of Physics, 37, Springer Verlag, Berlin Slater, J. C.; Quantum Theory of Molecules and Solids,, McGraw-Hill Book Company, New York Bouferguene, A.; Rinaldi, D; Int. J. Quantum Chem. 99, 50, Bouferguene, A; Fares, M.; Rinaldi, D.; J. Chem. Phys. 99, 00, Jones, H. W.; Phys. Rev. A. 988, 38, Jones, H. W.; Wetherford, C. A.; J. Molec. Struct. (Theochem) 989, 99, Jones, H. W.; J. Comput. Chem. 99, 2, Jones, H. W.; Int. J. Quantum Chem. 992,, 79. QUÍMICA NOVA, 22(3) (999) 323
O Método de Hartree-Fock
 O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
O Método de Hartree-Fock CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do Paraná
Introdução ao Método de Hartree-Fock
 Introdução ao Método de Hartree-Fock CF352 - Fundamentos de Física Atômica e Molecular Departamento de Física Universidade Federal do Paraná M. H. F. Bettega (UFPR) CF352 1 / 24 Preliminares Aproximação
Introdução ao Método de Hartree-Fock CF352 - Fundamentos de Física Atômica e Molecular Departamento de Física Universidade Federal do Paraná M. H. F. Bettega (UFPR) CF352 1 / 24 Preliminares Aproximação
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 11 MOLÉCULAS Primeira Edição junho de 2005 CAPÍTULO 11 MOLÉCULAS ÍNDICE 11-1- Introdução 11.2- Ligação por Tunelamento e a Molécula
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Aproximação de Hartree-Fock A maior preocupação da química quântica é encontrar e descrever
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Aproximação de Hartree-Fock A maior preocupação da química quântica é encontrar e descrever
Moléculas. Usamos a aproximação de Born- Oppenheimer, que considera os núcleos fixos, apenas o e - se movimenta.
 Moléculas Moléculas é uma coleção de 2 ou mais núcleos e seus elétrons associados, com todas as ligações complexas unidas pelas forças Os tipos mais importantes de ligação molecular são: covalente, iônica
Moléculas Moléculas é uma coleção de 2 ou mais núcleos e seus elétrons associados, com todas as ligações complexas unidas pelas forças Os tipos mais importantes de ligação molecular são: covalente, iônica
Átomo de Hélio. Tiago Santiago. 2 de novembro de Resumo
 Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
Átomo de Hélio Tiago Santiago de novembro d015 Resumo Nesse trabalho o átomo de Hélio é abordado definindo-se o hamiltoniano e utilizando métodos de aproximação para estimar a energia do ground state.
Átomos e Moléculas. Ligações moleculares. Energia do ion. A molécula de hidrogênio H 2
 Ligações moleculares Átomos e Moléculas Energia do ion H 2 + A molécula de hidrogênio Ligações moleculares Uma molécula é formada por um conjunto de átomos que interagem formando um sistema com energia
Ligações moleculares Átomos e Moléculas Energia do ion H 2 + A molécula de hidrogênio Ligações moleculares Uma molécula é formada por um conjunto de átomos que interagem formando um sistema com energia
Seminário. Teoria de Ligação de Valência - TLV UMA ABORDAGEM MECÂNICO QUÂNTICA DAS LIGAÇÕES COVALENTES
 Seminário Teoria de Ligação de Valência - TLV UMA ABORDAGEM MECÂNICO QUÂNTICA DAS LIGAÇÕES COVALENTES Autor: Marcelo Alves de Souza Mestrando UFABC 2015 Disciplina Química Integrada 1 O modelo de repulsão
Seminário Teoria de Ligação de Valência - TLV UMA ABORDAGEM MECÂNICO QUÂNTICA DAS LIGAÇÕES COVALENTES Autor: Marcelo Alves de Souza Mestrando UFABC 2015 Disciplina Química Integrada 1 O modelo de repulsão
O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana
 Universidade Federal do Paraná Setor de Ciências Exatas Departamento de Física O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana Introdução O Hélio é, depois do Hidrogênio, o átomo mais simples
Universidade Federal do Paraná Setor de Ciências Exatas Departamento de Física O estado fundamental do átomo de Hélio Prof. Ricardo L. Viana Introdução O Hélio é, depois do Hidrogênio, o átomo mais simples
Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel
 Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Ligações químicas Universidade do Estado de Santa Catarina UDESC - CCT Química Geral Profª Fabíola Corrêa viel Ligações Químicas Sacarina Vitamina E Amônia Fulereno LIGAÇÕES IÔNICAS Acontece por atração
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 MQ átomos > < Moléculas moléculas e sólidos núcleos e partículas Moléculas
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto 1o. Semestre de 2008 1 MQ átomos > < Moléculas moléculas e sólidos núcleos e partículas Moléculas
Cálculos de Propriedades Elétricas de Cadeias de HCN
 álculos de Propriedades Elétricas de adeias de Idney Resplandes Brandão Leite 1 ; Tertius Lima da FOSEA 2 1, 2 Instituto de Física, Universidade Federal de Goiás, P 131, 74001-970, Goiânia, GO, Brazil.
álculos de Propriedades Elétricas de adeias de Idney Resplandes Brandão Leite 1 ; Tertius Lima da FOSEA 2 1, 2 Instituto de Física, Universidade Federal de Goiás, P 131, 74001-970, Goiânia, GO, Brazil.
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
E(r) = 2. Uma carga q está distribuída uniformemente por todo um volume esférico de raio R.
 1. O campo elétrico no interior de uma esfera não-condutora de raio R, com carga distribuída uniformemente em seu volume, possui direção radial e intensidade dada por E(r) = qr 4πɛ 0 R 3. Nesta equação,
1. O campo elétrico no interior de uma esfera não-condutora de raio R, com carga distribuída uniformemente em seu volume, possui direção radial e intensidade dada por E(r) = qr 4πɛ 0 R 3. Nesta equação,
FF-296: Teoria do Funcional da Densidade I. Ronaldo Rodrigues Pela
 FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos O problema de 1 elétron O princípio variacional Função de onda tentativa Átomo de H unidimensional Íon H2 + unidimensional Equação
FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos O problema de 1 elétron O princípio variacional Função de onda tentativa Átomo de H unidimensional Íon H2 + unidimensional Equação
FÍSICA III 1/2008 Lista de Problemas 02 Campos elétricos
 FÍSICA III 1/2008 Lista de roblemas 02 Campos elétricos A C Tort 18 de Março de 2008 roblema 1 H.M. Nussenzveig: Curso de Física básica, vol. 3, Eletromagnetismo, Cap. 3, problema 4. Dois fios retilíneos
FÍSICA III 1/2008 Lista de roblemas 02 Campos elétricos A C Tort 18 de Março de 2008 roblema 1 H.M. Nussenzveig: Curso de Física básica, vol. 3, Eletromagnetismo, Cap. 3, problema 4. Dois fios retilíneos
Fundamentos de QO Aula 1
 UNIVERSIDADE FEDERAL DE SÃO CARLOS Fundamentos de QO Aula 1 Prof. Marco Antonio B Ferreira marcoantbf@gmail.com 3351-8075 www.lqbo.ufscar.br 1 Avaliação Aprovado: (P1 + P2 + P3)/3 6 17/09 1ª Avaliação
UNIVERSIDADE FEDERAL DE SÃO CARLOS Fundamentos de QO Aula 1 Prof. Marco Antonio B Ferreira marcoantbf@gmail.com 3351-8075 www.lqbo.ufscar.br 1 Avaliação Aprovado: (P1 + P2 + P3)/3 6 17/09 1ª Avaliação
Estrutura Hiperfina e Efeito Zeeman para Muônio e Positrônio
 Estrutura Hiperfina e Efeito Zeeman para Muônio e Positrônio Armando Valter Felicio Zuffi 05 de dezembro de 014 Resumo Neste trabalho, serão exploradas algumas correções da hamiltoniana do átomo de hidrogênio.
Estrutura Hiperfina e Efeito Zeeman para Muônio e Positrônio Armando Valter Felicio Zuffi 05 de dezembro de 014 Resumo Neste trabalho, serão exploradas algumas correções da hamiltoniana do átomo de hidrogênio.
Teoria do Orbital Molecular (TOM)
 Orbitais Moleculares Alguns aspectos da ligação não são explicados pela TLV. Por ex., por que o O 2 interage com um campo magnético? Teoria do Orbital Molecular (TOM) Nos átomos, os elétrons são encontrados
Orbitais Moleculares Alguns aspectos da ligação não são explicados pela TLV. Por ex., por que o O 2 interage com um campo magnético? Teoria do Orbital Molecular (TOM) Nos átomos, os elétrons são encontrados
ESTRUTURA MOLECULAR. Prof. Harley P. Martins filho
 ESTRUTURA MOLECULAR Prof. Harley P. Martins filho o A aproximação de Born-Oppenheimer Núcleos são muito mais pesados que elétrons dinâmica dos elétrons pode ser estudada com os núcleos parados (aproximação
ESTRUTURA MOLECULAR Prof. Harley P. Martins filho o A aproximação de Born-Oppenheimer Núcleos são muito mais pesados que elétrons dinâmica dos elétrons pode ser estudada com os núcleos parados (aproximação
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
7. A teoria quântica do átomo de Hidrogênio
 7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
Física Moderna 2. Aula 9. Moléculas. Tipos de ligações. Íon H2 + Iônica Covalente Outras: ponte de hidrogênio van der Waals
 Física Moderna 2 Aula 9 Moléculas Tipos de ligações Iônica Covalente Outras: Íon H2 + ponte de hidrogênio van der Waals 1 Moléculas Uma molécula é um arranjo estável de dois ou mais átomos. Por estável
Física Moderna 2 Aula 9 Moléculas Tipos de ligações Iônica Covalente Outras: Íon H2 + ponte de hidrogênio van der Waals 1 Moléculas Uma molécula é um arranjo estável de dois ou mais átomos. Por estável
Teorias de Ligação. Teoria dos Orbitais Moleculares
 Teorias de Ligação Orbitais moleculares Ordem de ligação Ligações em Moléculas Diatômicas Ligações em moléculas poliatômicas Limitações da Teoria de Lewis O oxigênio é paramagnético Compostos deficientes
Teorias de Ligação Orbitais moleculares Ordem de ligação Ligações em Moléculas Diatômicas Ligações em moléculas poliatômicas Limitações da Teoria de Lewis O oxigênio é paramagnético Compostos deficientes
Física III-A /2 Lista 1: Carga Elétrica e Campo Elétrico
 Física III-A - 2018/2 Lista 1: Carga Elétrica e Campo Elétrico 1. (F) Duas partículas com cargas positivas q e 3q são fixadas nas extremidades de um bastão isolante de comprimento d. Uma terceira partícula
Física III-A - 2018/2 Lista 1: Carga Elétrica e Campo Elétrico 1. (F) Duas partículas com cargas positivas q e 3q são fixadas nas extremidades de um bastão isolante de comprimento d. Uma terceira partícula
FF-296: Teoria do Funcional da Densidade I. Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Problema de 2 elétrons Férmions Hartree-Fock Troca
FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Problema de 2 elétrons Férmions Hartree-Fock Troca
Introdução à Física Atômica e Molecular
 4300315 Introdução à Física Atômica e Molecular Átomo de Hélio * : Estado Fundamental II *Referência Principal: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos Átomo de Hélio Aproximação
4300315 Introdução à Física Atômica e Molecular Átomo de Hélio * : Estado Fundamental II *Referência Principal: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos Átomo de Hélio Aproximação
Ligação Covalente. O íon molecular H 2
 O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados por um único elétron O que acontece à medida que os núcleos se aproximam? 4 O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados
O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados por um único elétron O que acontece à medida que os núcleos se aproximam? 4 O íon molecular H 2 + Dois núcleos de hidrogênio estão ligados
Aplicação do Método Variacional na Mecânica Quântica:
 Aplicação do Método Variacional na Mecânica Quântica: Átomo de Hélio Milena Menezes Carvalho 1 1 Instituto de Física de São Carlos, Universidade de São Paulo E-mail: glowingsea@gmail.com 1. Introdução
Aplicação do Método Variacional na Mecânica Quântica: Átomo de Hélio Milena Menezes Carvalho 1 1 Instituto de Física de São Carlos, Universidade de São Paulo E-mail: glowingsea@gmail.com 1. Introdução
FNC376N: Lista de junho de A energia de dissociação às vezes é expressa em quilocalorias por mol (kcal/mol). No SI se utiliza kj/mol.
 FNC376N: Lista 7 23 de junho de 2004 9-1 Ligação iônica 9-1. A energia de dissociação às vezes é expressa em quilocalorias por mol (kcal/mol). No SI se utiliza kj/mol. a) Determine a relação entre ev/molécula
FNC376N: Lista 7 23 de junho de 2004 9-1 Ligação iônica 9-1. A energia de dissociação às vezes é expressa em quilocalorias por mol (kcal/mol). No SI se utiliza kj/mol. a) Determine a relação entre ev/molécula
Ligações Químicas - II. Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
 Ligações Químicas - II Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares 1 Revisão: Estruturas de Lewis G.N. Lewis (~1916) Representação das ligações químicas Compartilhamento
Ligações Químicas - II Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares 1 Revisão: Estruturas de Lewis G.N. Lewis (~1916) Representação das ligações químicas Compartilhamento
Métodos de Química Computacional
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Métodos de Química Computacional Professora: Melissa Soares Caetano Métodos Semi-empíricos Expressão
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Métodos de Química Computacional Professora: Melissa Soares Caetano Métodos Semi-empíricos Expressão
Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento angular bem definido
 ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
Física III-A /1 Lista 1: Carga Elétrica e Campo Elétrico
 Física III-A - 2018/1 Lista 1: Carga Elétrica e Campo Elétrico Prof. Marcos Menezes 1. Duas partículas com cargas positivas q e 3q são fixadas nas extremidades de um bastão isolante de comprimento d. Uma
Física III-A - 2018/1 Lista 1: Carga Elétrica e Campo Elétrico Prof. Marcos Menezes 1. Duas partículas com cargas positivas q e 3q são fixadas nas extremidades de um bastão isolante de comprimento d. Uma
Maxwell Severo da COSTA; Freddy Fernandes GUIMARÃES
 Comparação entre a aproximação Z+1 e o cálculo de buraco de camada real no estudo da dinâmica nuclear dos isômeros do dicloroetileno induzida pela foto-ionização dos elétrons da camada K do cloro (ClK)
Comparação entre a aproximação Z+1 e o cálculo de buraco de camada real no estudo da dinâmica nuclear dos isômeros do dicloroetileno induzida pela foto-ionização dos elétrons da camada K do cloro (ClK)
Click to edit Master title style
 Teoria das orbitais moleculares (TOM) Contrariamente à TEV, esta teoria assume que os electrões que fazem a ligação não estão de facto localizados em determinada ligação mas pertencem à molécula como um
Teoria das orbitais moleculares (TOM) Contrariamente à TEV, esta teoria assume que os electrões que fazem a ligação não estão de facto localizados em determinada ligação mas pertencem à molécula como um
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA
 NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 10 ÁTOMOS COMPLEXOS Primeira Edição junho de 2005 CAPÍTULO 10 ÁTOMOS COMPLEXOS ÍNDICE 10-1- Introdução 10.2- Átomos com mais de um
NOTAS DE AULAS DE ESTRUTURA DA MATÉRIA Prof. Carlos R. A. Lima CAPÍTULO 10 ÁTOMOS COMPLEXOS Primeira Edição junho de 2005 CAPÍTULO 10 ÁTOMOS COMPLEXOS ÍNDICE 10-1- Introdução 10.2- Átomos com mais de um
Dr. Tiago P. Camargo. Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia
 Dr. Tiago P. Camargo Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Teoria de ligação de Valência - TLV Como fica a hibridização do oxygênio em O 2? Falhas na TLV
Dr. Tiago P. Camargo Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Teoria de ligação de Valência - TLV Como fica a hibridização do oxygênio em O 2? Falhas na TLV
PROPRIEDADES PERIÓDIOCAS
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I PROPRIEDADES PERIÓDIOCAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br Sala GQI 308,
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I PROPRIEDADES PERIÓDIOCAS Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br Sala GQI 308,
Correlação Eletrônica - CI e MP2
 Correlação Eletrônica - CI e MP2 CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do
Correlação Eletrônica - CI e MP2 CF740 Tópicos Especiais de Física Atômica e Molecular Cálculos de Estrutura Eletrônica Utilizando Funcionais de Densidade Departamento de Física Universidade Federal do
03/02/2014. Falha da TLV. Teoria do Orbital Molecular. Teoria dos Orbitais Moleculares - TOM
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Campus JK Diamantina - MG Prof a. Dr a. Flaviana Tavares Vieira Falha da TLV -As estruturas de Lewis falham na descrição correta da ligação em um
Universidade Federal dos Vales do Jequitinhonha e Mucuri Campus JK Diamantina - MG Prof a. Dr a. Flaviana Tavares Vieira Falha da TLV -As estruturas de Lewis falham na descrição correta da ligação em um
PPGQTA. Prof. MGM D Oca
 PPGQTA Prof. Polarizabilidade: Dureza e Moleza A polarizabilidade está relacionada ao tamanho do átomo e da capacidade deste estabilizar elétrons na nuvem eletrônica, esta matematicamente correlacionada
PPGQTA Prof. Polarizabilidade: Dureza e Moleza A polarizabilidade está relacionada ao tamanho do átomo e da capacidade deste estabilizar elétrons na nuvem eletrônica, esta matematicamente correlacionada
LIGAÇÃO COVAL COV AL NT
 LIGAÇÃO COVALENTE INTRODUÇÃO Resulta do compartilhamento de elétrons. Ex: H 2 Os dois átomos de hidrogênio se aproximam devido à força de atração que depois de determinada distância diminuem surgindo as
LIGAÇÃO COVALENTE INTRODUÇÃO Resulta do compartilhamento de elétrons. Ex: H 2 Os dois átomos de hidrogênio se aproximam devido à força de atração que depois de determinada distância diminuem surgindo as
Química Orgânica Ambiental
 Química Orgânica Ambiental Aula 1 Estrutura Eletrônica e ligação química Prof. Dr. Leandro Vinícius Alves Gurgel 1. Introdução: O átomo Os átomos são formados por nêutrons, prótons e elétrons: Prótons
Química Orgânica Ambiental Aula 1 Estrutura Eletrônica e ligação química Prof. Dr. Leandro Vinícius Alves Gurgel 1. Introdução: O átomo Os átomos são formados por nêutrons, prótons e elétrons: Prótons
Física Moderna II - FNC376
 Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
Universidade de São Paulo Instituto de Física Física Moderna II - FNC376 Profa. Márcia de Almeida Rizzutto o. Semestre de 008 Conteúdo (P) Cap. 7, 8 e 9 Eisberg (/ do 9.7), Cap. 7 do Tipler, Cap. 7 e parte
Introdução à Física Atômica e Molecular
 4005 Introdução à Física Atômica e Molecular Átomos Multieletrônicos Referências: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos. P. Atkins e R. Friedman, Molecular Quantum Mechanics,
4005 Introdução à Física Atômica e Molecular Átomos Multieletrônicos Referências: D. Vianna, A. Fazzio e S. Canuto, Teoria Quântica de Moléculas e Sólidos. P. Atkins e R. Friedman, Molecular Quantum Mechanics,
(Versão 2014/2) (b) (d)
 MOVIMENTO HARMÔNICO SIMPLES (Versão 2014/2) 1. INTRODUÇÃO Um dos movimentos mais importantes que observamos na natureza é o movimento oscilatório. Chamado também movimento periódico ou vibracional. Em
MOVIMENTO HARMÔNICO SIMPLES (Versão 2014/2) 1. INTRODUÇÃO Um dos movimentos mais importantes que observamos na natureza é o movimento oscilatório. Chamado também movimento periódico ou vibracional. Em
Click to edit Master title style
 Moléculas poliatómicas Considere-se a molécula H 2 O As ligações nesta molécula seriam explicadas com base na coalescência de duas orbitais p do átomo de oxigénio com orbitais 1s dos átomos de hidrogénio.
Moléculas poliatómicas Considere-se a molécula H 2 O As ligações nesta molécula seriam explicadas com base na coalescência de duas orbitais p do átomo de oxigénio com orbitais 1s dos átomos de hidrogénio.
Lei de Ampere. 7.1 Lei de Biot-Savart
 Capítulo 7 Lei de Ampere No capítulo anterior, estudamos como cargas em movimento (correntes elétricas) sofrem forças magnéticas, quando na presença de campos magnéticos. Neste capítulo, consideramos como
Capítulo 7 Lei de Ampere No capítulo anterior, estudamos como cargas em movimento (correntes elétricas) sofrem forças magnéticas, quando na presença de campos magnéticos. Neste capítulo, consideramos como
Disciplina: SiComLíMol 1
 Disciplina: SiComLíMol 1 A matéria é composta por átomos e moléculas Geralmente, fazemos simplificações e desenvolvemos modelos O estudo teórico não permite tratar quantidades macroscópicas da matéria.
Disciplina: SiComLíMol 1 A matéria é composta por átomos e moléculas Geralmente, fazemos simplificações e desenvolvemos modelos O estudo teórico não permite tratar quantidades macroscópicas da matéria.
N P P N. Ciências de Materiais I Prof. Nilson C. Cruz. Aula 2 Ligação Química. Átomos. Diferença entre materiais = Diferença entre arranjos atômicos e
 Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Universidade Federal do Espírito Santo Centro de Ciências Exatas Programa de Pós-Graduação em Física
 Universidade Federal do Espírito Santo Centro de Ciências Exatas Programa de Pós-Graduação em Física Av. Fernando Ferrari, 514, 29075-910. Vitória, ES - Brasil. E-mail: ppgfis.ufes@gmail.com. Telefone:
Universidade Federal do Espírito Santo Centro de Ciências Exatas Programa de Pós-Graduação em Física Av. Fernando Ferrari, 514, 29075-910. Vitória, ES - Brasil. E-mail: ppgfis.ufes@gmail.com. Telefone:
Geralmente, fazemos simplificações e desenvolvemos modelos. A matéria é composta por átomos e moléculas
 Disciplina: SiComLíMol 1 A matéria é composta por átomos e moléculas Geralmente, fazemos simplificações e desenvolvemos modelos O estudo teórico não permite tratar quantidades macroscópicas da matéria.
Disciplina: SiComLíMol 1 A matéria é composta por átomos e moléculas Geralmente, fazemos simplificações e desenvolvemos modelos O estudo teórico não permite tratar quantidades macroscópicas da matéria.
Ligações Químicas - I
 Ligações Químicas - I Orbitais atômicos e números quânticos A tabela periódica; propriedades Ligações químicas A ligação iônica Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
Ligações Químicas - I Orbitais atômicos e números quânticos A tabela periódica; propriedades Ligações químicas A ligação iônica Ligação covalente Orbitais moleculares (LCAO) Hibridização Geometrias moleculares
H α H β H γ H δ H ε H ξ H 6562,2 Å 4861,3 Å 4340,5 Å 4101,7 Å 3970,1 3889,1
 1 Departamento de Física - Universidade Federal de Santa Catarina Laboratório de Física Moderna- FSC 5151. ESPECTROS DO HIDROGÊNIO E DO HÉLIO OBJETIVOS a) Medir os comprimentos de onda das raias espectrais
1 Departamento de Física - Universidade Federal de Santa Catarina Laboratório de Física Moderna- FSC 5151. ESPECTROS DO HIDROGÊNIO E DO HÉLIO OBJETIVOS a) Medir os comprimentos de onda das raias espectrais
FF-296: Teoria do Funcional da Densidade I. Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785
 FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Hartree-Fock e Thomas-Fermi Hartree-Fock Caso de N
FF-296: Teoria do Funcional da Densidade I Prof. Dr. Ronaldo Rodrigues Pelá Sala 2602A-1 Ramal 5785 rrpela@ita.br www.ief.ita.br/~rrpela Tema de hoje: Hartree-Fock e Thomas-Fermi Hartree-Fock Caso de N
Teoria de bandas nos sólidos
 Teoria de bandas nos sólidos Situação: átomos idênticos, distantes níveis de energia desse sistema têm degenerescência de troca dupla. A parte espacial da autofunção eletrônica pode ser uma combinação
Teoria de bandas nos sólidos Situação: átomos idênticos, distantes níveis de energia desse sistema têm degenerescência de troca dupla. A parte espacial da autofunção eletrônica pode ser uma combinação
Átomos multi-eletrônicos. Indistinguibilidade
 Átomos multi-eletrônicos Indistinguibilidade Princípio de exclusão, de Pauli 1. Em um átomo multi-eletrônico nunca pode haver mais de 1 e- ocupando o mesmo estado quântico.. Um sistema constituído de vários
Átomos multi-eletrônicos Indistinguibilidade Princípio de exclusão, de Pauli 1. Em um átomo multi-eletrônico nunca pode haver mais de 1 e- ocupando o mesmo estado quântico.. Um sistema constituído de vários
UMA SIMPLIFICAÇÃO DO MÉTODO HARTREE-FOCK
 UMA SIMPLIFICAÇÃO DO MÉTODO HARTREE-FOCK Lucas Modesto da Costa Instituto de Física - DFGE - USP 8 de outubro de 2008 1 / 39 Slater, J. C. Época Aproximação de Thomas-Fermi 2 / 39 Slater, J. C. Slater,
UMA SIMPLIFICAÇÃO DO MÉTODO HARTREE-FOCK Lucas Modesto da Costa Instituto de Física - DFGE - USP 8 de outubro de 2008 1 / 39 Slater, J. C. Época Aproximação de Thomas-Fermi 2 / 39 Slater, J. C. Slater,
Fundamentos da modelagem Molecular - 1
 Fundamentos da modelagem Molecular - 1 Departamento de Física UFPel ufpellogo Introdução Rotas para a pesquisa Conexão entre experimento, simulação e teoria Sistema real Fazer modelos do sistema Fazer
Fundamentos da modelagem Molecular - 1 Departamento de Física UFPel ufpellogo Introdução Rotas para a pesquisa Conexão entre experimento, simulação e teoria Sistema real Fazer modelos do sistema Fazer
Teoria dos Orbitais Moleculares. Prof. Fernando R. Xavier
 Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
Teoria dos Orbitais Moleculares Prof. Fernando R. Xavier UDESC 013 Antecedentes... A teoria de ligação de valência (TLV) não cosnsegue explicar com eficiência a formação de moléculas poliatômicas. Uma
TEORIA DA LIGAÇÃO DE VALÊNCIA - TLV
 TEORIA DA LIGAÇÃO DE VALÊNCIA - TLV Walter Heitler, Fritz London, John Slater e Linus Pauling: 1ª descrição sobre ligações covalentes que levou em consideração os orbitais atômicos. Teoria da Ligação de
TEORIA DA LIGAÇÃO DE VALÊNCIA - TLV Walter Heitler, Fritz London, John Slater e Linus Pauling: 1ª descrição sobre ligações covalentes que levou em consideração os orbitais atômicos. Teoria da Ligação de
Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares
 Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares 1) Construa os orbitais moleculares para H 2 O e NO 2 baseado nos SALCs de
Disciplina: Química Inorgânica I Professor: Fabio da Silva Miranda. Lista de exercícios sobre Teoria dos Orbitais Moleculares 1) Construa os orbitais moleculares para H 2 O e NO 2 baseado nos SALCs de
FF-296: Teoria do Funcional da Densidade I. Ronaldo Rodrigues Pela
 FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos HF Dois elétrons N elétrons Thomas Fermi Átomo de Hélio 1D Energia exata: 3,154 H Vamos resolver este problema usando o método
FF-296: Teoria do Funcional da Densidade I Ronaldo Rodrigues Pela Tópicos HF Dois elétrons N elétrons Thomas Fermi Átomo de Hélio 1D Energia exata: 3,154 H Vamos resolver este problema usando o método
1.1 Interações de van der Waals. Quem inclue eficientemente?
 Interações de van der Waals: Quem inclue eficientemente? Amaury Melo, Evanildo Gomes Lacerda Júnior, José Maximiano F. Pinheiro Júnior Física At^omica e Molecular, IFUSP, 2009/1 Docente: Prof. Sylvio Canuto.
Interações de van der Waals: Quem inclue eficientemente? Amaury Melo, Evanildo Gomes Lacerda Júnior, José Maximiano F. Pinheiro Júnior Física At^omica e Molecular, IFUSP, 2009/1 Docente: Prof. Sylvio Canuto.
Interações Atômicas e Moleculares
 Interações Atômicas e Moleculares 6. O Princípio Variacional Prof. Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/iam.html Na aula anterior, tratando de moléculas
Interações Atômicas e Moleculares 6. O Princípio Variacional Prof. Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/iam.html Na aula anterior, tratando de moléculas
Interações Atômicas e Moleculares
 Interações Atômicas e Moleculares 7. Interações Intermoleculares Prof. Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/iam.html São de natureza eletromagnética.
Interações Atômicas e Moleculares 7. Interações Intermoleculares Prof. Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/iam.html São de natureza eletromagnética.
PERIODICIDADE. Química Geral Augusto Freitas
 PERIODICIDADE Química Geral Augusto Freitas 1 1 A organização da Tabela Periódica As colunas são denominadas Grupos ou Famílias As linhas são denominadas Períodos. 2 1 A organização da Tabela Periódica
PERIODICIDADE Química Geral Augusto Freitas 1 1 A organização da Tabela Periódica As colunas são denominadas Grupos ou Famílias As linhas são denominadas Períodos. 2 1 A organização da Tabela Periódica
FÍSICA III 1/2008 Lista de Problemas 01 A lei de Coulomb
 FÍSICA III 1/2008 Lista de Problemas 01 A lei de Coulomb A C Tort 8 de Março de 2008 Problema 1 H.M. Nussenzveig: Curso de Física básica, vol. 3, Eletromagnetismo, Cap. 2, problema 1. Mostre que a razão
FÍSICA III 1/2008 Lista de Problemas 01 A lei de Coulomb A C Tort 8 de Março de 2008 Problema 1 H.M. Nussenzveig: Curso de Física básica, vol. 3, Eletromagnetismo, Cap. 2, problema 1. Mostre que a razão
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
CÁLCULO DA ESTRUTURA ELETRÔNICA DO ÓXIDO DE GRAFENO
 CÁLCULO DA ESTRUTURA ELETRÔNICA DO ÓXIDO DE GRAFENO Nome do Aluno 1 ; Nome do Orientador 2 ; Nome do Co-orientador 3 (apenas quando estiver oficialmente cadastrado como co-orientador junto ao PIBIC/PIVIC)
CÁLCULO DA ESTRUTURA ELETRÔNICA DO ÓXIDO DE GRAFENO Nome do Aluno 1 ; Nome do Orientador 2 ; Nome do Co-orientador 3 (apenas quando estiver oficialmente cadastrado como co-orientador junto ao PIBIC/PIVIC)
A Dualidade Onda-Partícula
 A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
A Dualidade Onda-Partícula O fato de que as ondas têm propriedades de partículas e viceversa se chama Dualidade Onda-Partícula. Todos os objetos (macroscópicos também!) são onda e partícula ao mesmo tempo.
O spin do elétron. Vimos, na aula 2, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com 2 valores, com propriedades de momento angular.
 O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
Física IV - FAP2204 Escola Politécnica GABARITO DA P3 8 de dezembro de 2009
 P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
Átomo de Hidrogênio 1
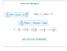 Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Química Orgânica. Compostos orgânicos contêm carbono. O carbono não ganha nem cede elétrons
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 1 Estrutura Eletrônica e Ligação Química Ácidos e Bases Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Química Orgânica
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 1 Estrutura Eletrônica e Ligação Química Ácidos e Bases Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Química Orgânica
Fundamentos de Química Quântica
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A /2 Data: 17/09/2018
 Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A - 2018/2 Data: 17/09/2018 Seção 1: Múltipla Escolha (7 0,8 = 5,6 pontos) 3. O campo elétrico
Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A - 2018/2 Data: 17/09/2018 Seção 1: Múltipla Escolha (7 0,8 = 5,6 pontos) 3. O campo elétrico
Modelos Atômicos e Princípios Quânticos Parte II
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
INTERAÇÕES INTERMOLECULARES
 INTERAÇÕES INTERMOLECULARES Serão abordados: as forças íon-dipolo, dipolo-dipolo, dispersão de London e ligação de hidrogênio e a relação entre propriedade física e interação intermolecular. As partículas
INTERAÇÕES INTERMOLECULARES Serão abordados: as forças íon-dipolo, dipolo-dipolo, dispersão de London e ligação de hidrogênio e a relação entre propriedade física e interação intermolecular. As partículas
Forças intermoleculares. Formação de fases condensadas Forças íon-dipolo Forças dipolo-dipolo Forças de London Ligação de hidrogênio
 Forças intermoleculares Formação de fases condensadas Forças íon-dipolo Forças dipolo-dipolo Forças de London Ligação de hidrogênio Estado gasoso O estado da matéria mais simples é o gás. Descrevemos esse
Forças intermoleculares Formação de fases condensadas Forças íon-dipolo Forças dipolo-dipolo Forças de London Ligação de hidrogênio Estado gasoso O estado da matéria mais simples é o gás. Descrevemos esse
Ligações Atômicas e Bandas de Energia. Livro Texto - Capítulo 2
 40 Ligações Atômicas e Bandas de Energia Livro Texto - Capítulo 2 Ligação Atômica 41 Porque estudar a estrutura atômica? As propriedades macroscópicas dos materiais dependem essencialmente do tipo de ligação
40 Ligações Atômicas e Bandas de Energia Livro Texto - Capítulo 2 Ligação Atômica 41 Porque estudar a estrutura atômica? As propriedades macroscópicas dos materiais dependem essencialmente do tipo de ligação
TEORIA DOS ORBITAIS MOLECULARS. QFL QUIMICA GERAL 1 (1o sem 2017)
 TEORIA DOS ORBITAIS MOLECULARS QFL1101 - QUIMICA GERAL 1 (1o sem 017) Teoria de Ligação pela Valência Linus Pauling; Os elétrons de valência estão localizados entre os átomos (ou são pares isolados); Orbitais
TEORIA DOS ORBITAIS MOLECULARS QFL1101 - QUIMICA GERAL 1 (1o sem 017) Teoria de Ligação pela Valência Linus Pauling; Os elétrons de valência estão localizados entre os átomos (ou são pares isolados); Orbitais
Estrutura Atômica. Química Quântica Prof a. Dr a. Carla Dalmolin. Átomos Polieletrônicos
 Estrutura Atômica Química Quântica Prof a. Dr a. Carla Dalmolin Átomos Polieletrônicos Átomos Polieletrônicos Átomos que possuem mais de 1 elétron A Eq. de Schrödinger pode ser resolvida exatamente apenas
Estrutura Atômica Química Quântica Prof a. Dr a. Carla Dalmolin Átomos Polieletrônicos Átomos Polieletrônicos Átomos que possuem mais de 1 elétron A Eq. de Schrödinger pode ser resolvida exatamente apenas
Física IV Escola Politécnica GABARITO DA P3 25 de novembro de 2014
 Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
1.1. Motivação Objetivos
 1 Introdução As Unidades de Processamento Gráfico (GPUs), ou Placas Gráficas, foram originalmente desenvolvidas com o propósito de renderização gráfica. Contudo, nos últimos anos, o desempenho na realização
1 Introdução As Unidades de Processamento Gráfico (GPUs), ou Placas Gráficas, foram originalmente desenvolvidas com o propósito de renderização gráfica. Contudo, nos últimos anos, o desempenho na realização
Configurações eletrônicas e a tabela periódica. Os grupos 1 e 2 têm elétrons nos orbitais s. Os grupos 13 ao 18 têm elétrons nos orbitais p
 TABELA PERIÓDICA 32 18 Configurações eletrônicas e a tabela periódica A tabela periódica pode ser utilizada como um guia para as configurações eletrônicas. O número do período é o valor de n. Os grupos
TABELA PERIÓDICA 32 18 Configurações eletrônicas e a tabela periódica A tabela periódica pode ser utilizada como um guia para as configurações eletrônicas. O número do período é o valor de n. Os grupos
PROBLEMA DE FÍSICA INDUÇÃO ASSIMÉTRICA
 PROBLEMA DE FÍSICA INDUÇÃO ASSIMÉTRICA Enunciado: É dado um condutor de formato esférico e com cavidade (interna) esférica, inicialmente neutra (considere que esse condutor tenha espessura não-desprezível).
PROBLEMA DE FÍSICA INDUÇÃO ASSIMÉTRICA Enunciado: É dado um condutor de formato esférico e com cavidade (interna) esférica, inicialmente neutra (considere que esse condutor tenha espessura não-desprezível).
QB70C:// Química (Turmas S71/S72) Ligação Química
 QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
QB70C:// Química (Turmas S71/S72) Ligação Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Formação das Ligações O modelo RPECV, baseado principalmente nas estruturas de Lewis,
Mecânica Quântica. Veremos hoje: Dualidade onda partícula Princípio da Incerteza Formulações da MQ Equação de Schrodinger Partícula numa caixa
 Mecânica Quântica Veremos hoje: Dualidade onda partícula Princípio da Incerteza Formulações da MQ Equação de Schrodinger Partícula numa caixa Limitações do modelo de Bohr A teoria de Bohr não era capaz
Mecânica Quântica Veremos hoje: Dualidade onda partícula Princípio da Incerteza Formulações da MQ Equação de Schrodinger Partícula numa caixa Limitações do modelo de Bohr A teoria de Bohr não era capaz
Capítulo 5 - Aplicações das leis de Newton. Hoje reconhecemos 4 forças da natureza. São elas (em ordem crescente de
 Capítulo 5 - Aplicações das leis de Newton Hoje reconhecemos 4 forças da natureza. São elas (em ordem crescente de intensidade) Força Gravitacional Força Fraca Intensidade Força Eletromagnética Força Forte
Capítulo 5 - Aplicações das leis de Newton Hoje reconhecemos 4 forças da natureza. São elas (em ordem crescente de intensidade) Força Gravitacional Força Fraca Intensidade Força Eletromagnética Força Forte
2 Diferença de Potencial e Potencial Eletrostático
 Universidade Federal do Rio de Janeiro Instituto de Física Física III 2014/2 Cap. 3 - Potencial Eletrostático Prof. Elvis Soares Nesse capítulo, estudaremos o potencial eletrostático criado por cargas
Universidade Federal do Rio de Janeiro Instituto de Física Física III 2014/2 Cap. 3 - Potencial Eletrostático Prof. Elvis Soares Nesse capítulo, estudaremos o potencial eletrostático criado por cargas
Cap. 2 - Lei de Gauss
 Universidade Federal do Rio de Janeiro Instituto de Física Física III 2014/2 Cap. 2 - Lei de Gauss Prof. Elvis Soares Nesse capítulo, descreveremos a Lei de Gauss e um procedimento alternativo para cálculo
Universidade Federal do Rio de Janeiro Instituto de Física Física III 2014/2 Cap. 2 - Lei de Gauss Prof. Elvis Soares Nesse capítulo, descreveremos a Lei de Gauss e um procedimento alternativo para cálculo
Raios atômicos Física Moderna 2 Aula 6
 Raios atômicos 1 2 8 8 18 18 32 2 Energias de ionização 3 Espectros de R-X A organização da tabela periódica reflete a distribuição dos e - nas camadas mais externas dos átomos. No entanto, é importante
Raios atômicos 1 2 8 8 18 18 32 2 Energias de ionização 3 Espectros de R-X A organização da tabela periódica reflete a distribuição dos e - nas camadas mais externas dos átomos. No entanto, é importante
Campo Elétrico Linhas de Campo
 Campo Elétrico Linhas de Campo 1 Campo Elétrico uma carga elétrica q cria um campo elétrico E 2 1 Campo Elétrico forças à distância linhas de força elétrica linhas de campo 3 linhas de campo: Campo Elétrico:
Campo Elétrico Linhas de Campo 1 Campo Elétrico uma carga elétrica q cria um campo elétrico E 2 1 Campo Elétrico forças à distância linhas de força elétrica linhas de campo 3 linhas de campo: Campo Elétrico:
Aula 12. (quase) Tudo sobre os átomos. Física Geral F-428
 Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
momento de dipólo induzido apolar Esta é a força responsável pela conhecida atração de pequeninos pedaços de papel por um pente carregado polares
 DIPÓLO ELÉTRICO Embora os átomos e as moléculas sejam eletricamente neutros, são afetados pelos campos elétricos, pois têm cargas positivas e negativas. Em alguns átomos ou moléculas, a nuvem de elétron
DIPÓLO ELÉTRICO Embora os átomos e as moléculas sejam eletricamente neutros, são afetados pelos campos elétricos, pois têm cargas positivas e negativas. Em alguns átomos ou moléculas, a nuvem de elétron
