HOMERO JOSÉ DE FARIAS E MELO
|
|
|
- Antônia das Neves Lameira
- 6 Há anos
- Visualizações:
Transcrição
1 HOMERO JOSÉ DE FARIAS E MELO APERFEIÇOAMENTO DE UMA TÉCNICA DE ESPECTROSCOPIA POR RESSONÂNCIA MAGNÉTICA PARA DIFERENCIAÇÃO DE NÓDULOS E MASSAS ADRENAIS Tese apresentada à Universidade Federal de São Paulo Escola Paulista de Medicina para obtenção do Título de Doutor em Ciências Radiológicas. Orientadora: Prof. Dra. Suzan M. Goldman Co-orientador: Prof. Dr. Jacob Szejnfeld SÃO PAULO 2010
2 Melo, HJF Aperfeiçoamento de uma técnica de espectroscopia por ressonância magnética para diferenciação de nódulos e massas adrenais/ Homero José de Farias e Melo. -- São Paulo, xiv, 93f. Tese (Doutorado) Universidade Federal de São Paulo. Escola Paulista de Medicina. Programa de Pós-graduação em Radiologia e Ciências Radiológicas. Título em inglês: MR spectroscopy technical development for adrenals nodules and masses differentiation. 1. Espectroscopia. 2. Câncer Supra-renal. 3. Ressonância Magnética. Copyright 2010 by Homero José de Farias e Melo
3 UNIVERSIDADE FEDERAL DE SÃO PAULO ESCOLA PAULISTA DE MEDICINA DEPARTAMENTO DE DIAGNÓSTICO POR IMAGEM Chefe do Departamento: Prof. Dr. Sergio Ajzen Coordenador da Pós-graduação: Prof. Dr. Giuseppe D Ippolito iii
4 Dedicatória Dedico este trabalho àquelas pessoas que sempre acreditaram em mim, inclusive nos momentos em que eu deixei de acreditar, dando-me a base, a força e a compreensão necessárias para me confortar e me fazer seguir em frente. Não tenho dúvidas da importância de vocês nesta grande conquista: Ao meu pai, Roberval (in memoriam); À minha mãe, Suely; À minha esposa, Cândida; Aos meus irmãos, Rútilo e Andréa; Às minhas sobrinhas, Mariana, Sophia e Letícia; Às minhas avós, Albertina (in memoriam) e Beatriz; Aos meus tios Almany e Pompéia; Aos meus tios Nilton e Edna; Aos meus tios Gerardo Magella (in memoriam) e Carmem; Aos meus tios Reinaldo e Vera; Aos meus tios Geraldo e Conceição; Aos meus tios Albérgio e Nídia; Ao restante da minha querida família: tios, tias, primos, primas, sogro, sogra, cunhados e cunhadas; Aos amigos, em especial a Paulo Fernando Immisch, Altino S. Meira, Marcelo B. Musciônico e Thiago A. Fedele. iv
5 Agradecimentos A Deus, por tudo. v
6 À Profa. Dra. Suzan M. Goldman, por ser minha orientadora, dando-me o suporte e a orientação necessários, valorizando-me e me inserindo em outras linhas de pesquisa. Sinto-me honrado em sempre ser lembrado na área acadêmica e profissional. Ao Prof. Dr. Jacob Szejnfeld, por continuar acreditando no meu potencial, por apoiar e incentivar o meu desenvolvimento e o meu trabalho, dando-me o suporte e a orientação necessários no seu papel de co-orientador. Aos funcionários do DDI, em especial, à Célia, Andréa, Patrícia e Júlio e técnicos, biomédicos e tecnólogos: Luiz Carnielo, Cláudio Carratu, Herbert Souza, Cláudio Riberti, Juliano e Lucivaldo Santos pela cumplicidade e ajuda nos momentos mais difíceis. Aos pós-graduandos do Departamento de Diagnóstico por Imagem, pelo apoio e ajuda acadêmica. Ao Dr. Juliano Faria, fundamental para o desenvolvimento deste projeto, pelo apoio e ajuda acadêmica. À Dra. Martha Huayllas, pós-graduanda do Departamento de Endocrinologia, pelo encaminhamento e acompanhamento dos pacientes, apoio e ajuda acadêmica. Aos médicos, biomédicos, tecnólogos e técnicos da ressonância magnética e tomografia computadorizada do Centro de Ultrassonografia e Radiologia Aplicada (CURA), pelo apoio, incentivo e compreensão. Aos médicos e biomédicos da ressonância magnética (em especial ao Altino Meira, José Adilson e Irineu Shito) da Santa Casa de Misericórdia de São Paulo, pelo vi
7 ensino da ressonância magnética, apoio, incentivo e compreensão. Não teria conseguido se não fosse por vocês. Guardo um carinho e amizade por todos. Aos médicos e biomédicos da ressonância magnética e tomografia computadorizada (Paulo Naputano, Décio Godenberg, Fabiana Gondenberg, Tatiana Schiller, Leandro de Pino, Carolina Burim, Herbert Souza, Silvana Fernandes, Ingrid Canedo Equipe de 2003 a 2006) do Hospital São Luiz, pelo ensino da ressonância magnética e tomografia computadorizada, apoio, incentivo e compreensão. Sinto saudades de todos. Aos colegas professores da Universidade Nove de Julho (UNINOVE), em especial, ao Prof. Amaury de Castro Júnior, Prof. Bergman Munhoz e Dr. Humberto Dêlle, e Universidade Cidade de São Paulo (UNICID), em especial, ao Dr. Décio Caly, Dra. Sueli Andrade, Dra. Maria José Tucunduva, Dra. Roosecelis Brasil, Dra. Karina Ferrassa Damas, Dr. Fábio Passos, Dr. Dante Simionato e Dra. Fernanda Góes, pela confiança, apoio e incentivo. providencial. À minha mãe, esposa, irmãos e família, pelo apoio incondicional, irrestrito e vii
8 Agradecimento especial À Fundação Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES) pelo incentivo e pelo apoio desta pesquisa, contribuindo assim, com os avanços da ciência e da Medicina. N.º do curso: M5 Nível: doutorado viii
9 Sumário Dedicatória... Agradecimentos... Listas... Resumo... iv v xi xvii 1 INTRODUÇÃO Objetivo REVISÃO DA LITERATURA Histórico Bases Físicas Bases Químicas Espectroscopia por Ressonância Magnética Metabolismo da Glândula Adrenal na ERM Metabolismo da Colina Metabolismos da Creatina Metabolismos do Lactato Metabolismos da Glutamina MÉTODO Casuística Critérios de Inclusão Critérios de Não-inclusão Critérios de Exclusão Protocolos de Exame Preparo e Posicionamento do Paciente Técnica do Exame Protocolo de Aquisição de Imagens por RM Protocolo para captação dos dados espectroscópicos Análise dos dados espectroscópicos Análise dos Metabólitos ix
10 3.2.4 Análise estatística RESULTADOS DISCUSSÃO CONCLUSÃO ANEXOS REFERÊNCIAS Abstract Bibliografia Consultada x
11 Lista de Figuras Figura 1. Spin Atômico... 6 Figura 2. Paralelismo e antiparalelismo do spin... 6 Figura 3. Gráficos Mxy (Magnetização Transversa) X t (Tempo) e Mz (Magnetização Longitudinal) X t (Tempo)... 8 Figura 4. Declínio de Indução Livre (DIL) e o efeito T2*... 9 Figura 5. Voxels elegíveis no Espaço K da sequência PRESS Figura 6. Aldosterona Figura 7. Biossíntese e metabolismo dos esteróides endógenos Figura 8. Cortisol Figura 9. Androstenodiona Figura 10. Dehidroepiandrosterona (DHEA) Figura 11. DHEA sulfato (DHEA-S) Figura 12. Epinefrina Figura 13. Norepinefrina Figura 14. Biossíntese das catecolaminas Figura 15. Metabolização das catecolaminas Figura 16. Metanefrina Figura 17 Normetanefrina Figura 18. Ácido Vanilmandélico Figura 19. Fosfatidilcolina Figura 20. Metabolismo da fosfatidilcolina (PtdCho) Figura 21. Creatina Figura 22. Metabolismo da creatina Figura 23. Lactato xi
12 Figura 24. Via glicolítica demonstrando a espontaneidade da formação do piruvato (via aeróbia) e a formação do lactato tanto por via anaeróbica, quanto pela ação da lactato-desidrogenase que converte piruvato em lactato Figura 25. Glutaminólise Figura 26. Diagrama de fluxo de estudo Figura 27. Bobinas utilizadas na aquisição de imagens por RM e dos gráficos espectroscópicos na ERM Figura 28. Ajuste do posicionamento e tamanho do CDV e da área do shimming Figura 29. Figura 30. Figura 31. Figura 32. Programação final da ERM 1 H da adrenal... Alteração d e escala no pós-processamento da ERM 1 H da adrenal... Gráfico de barras relacionando o número de massas ou nódulos (N) versus tamanho da lesão... Gráficos espectroscópicos da adrenal em quatro diferentes massas Figura 33. Figura 34. Figura 35. Gráficos espectroscópicos da adrenal em três diferentes massas evidenciando os respectivos picos de Cho, Cr, Lip, Glx, Lac e H 2 O que estão assinalados nas curvas Curva ROC da relação Lac/Cr entre os grupos adenoma (A) e carcinoma (B) com o feocromocitoma Gráficos de dispersão com regressão linear do comportamento entre o tamanho da massa e a relação Glx/Cr Figura 36. Lipídeos presentes nos nódulos ou massas adrenais estudados Figura 37. Curva ROC para determinação do ponto de corte do lipídeo de maior amplitude nas massas ou nódulos de adrenal xii
13 Lista de quadros e tabelas Quadro 1 PARÂMETROS DAS SEQÜÊNCIAS DE RM UTILIZADAS NO PROTOCOLO Quadro 2 PARÂMETROS DA SEQÜÊNCIA DE ERM UTILIZADA NO PROTOCOLO Tabela 1 Tabela 2 ANÁLISE DESCRITIVA DOS GRUPOS ESTUDADOS PARA AS RELAÇÕES CHO/CR E PPM/CR ANÁLISE DESCRITIVA DOS GRUPOS ESTUDADOS PARA AS RELAÇÕES Glx/Cr E Lac/Cr Tabela 3 ANÁLISE DESCRITIVA DOS LIPÍDEOS NOS GRUPOS ESTUDADOS xiii
14 Lista de abreviaturas e símbolos 0 Constante de blindagem Desvio químico Fase Razão giromagnética ou magnetogírica Frequência precessional (de ressonância) Momento mangnético do spin µv micro Volts A i ATP FWHM B 0 B 1 BASING CDV CHESS Cho Cr COMT CSI DHEA DHEA-S Amplitude do pulso de RF Adenosina trifosfato Largura do pico na metade da altura Potência do campo magnético Campo magnético adicional (secundário) Banda de radiofrequência de inversão seletiva com gradiente de defasamento Campo de visão Pulso de Desvio Químico Seletivo Colina Creatina Catecol-O-metiltransferase Imageamento pelo desvio químico Dehidroepiandrosterona DHEA sulfato xiv
15 DIL DOMA ENO ERM Fat Sat G Glx h HASTE ou RARE J Lac Lip M MAO MEGA mm mmol/l MOPEG MOPGAL M xy M z p PCho PET Declínio de Indução Livre Ácido 3,4-diidroximandélico Efeito nuclear Overhauser Espectroscopia por Ressonância Magnética Saturação de Gordura Gauss Somatório dos picos da glutamina e glutamato Altura do pico ou amplitude Tomada única metade-fourier turbo spin eco Acoplamento escalar Lactato Lipídeo Molar Monoamina oxidase Geração de Frequência Seletiva Coerente mili Molar mili mol por litro 3-metoxi-4-hidroxifeniletilenoglicol 3-metoxi-4-hidroxifenilglicoaldeído Magnetização Transversa Magnetização Longitudinal Significância estatística Fosfocolina Tomografia por emissão de pósitrons xv
16 P i ppm PRESS PtdCho RF RM ROC RSR Single-shot SMASH SP STEAM T T 1 T 2 TE TR VDI VIBE VMA VME VPP ρ HO PO 2-3, íon ortofosfato Partes por milhão Espectroscopia por Determinação de Pontos Fosfatidilcolina Pulso de Radiofrequência Ressonância magnética Curva da Característica Operativa do Receptor Relação Sinal-Ruído Imagem em tomada única Aquisição Simultânea com a Harmônica Espacial Bobina de RF SPINE Modo de aquisição de eco estimulado Tesla Tempo de relaxamento Declínio spin-spin Tempo de Eco Tempo de Repetição Volume de interesse Exame em Apnéia com Interpolação Volumétrica Ácido vanilmandélico Vetor de Magnetização Efetiva Valor Preditivo Positivo Coeficiente Linear de Pearson xvi
17 Resumo Objetivo: Aperfeiçoar um protocolo de ERM do 1 H para a diferenciação de nódulos e massas das glândulas adrenais, em especial adenomas, feocromocitomas, carcinomas e metástases. Métodos: Foram avaliados, por estudo prospectivo, 118 pacientes (36 homens e 82 mulheres), com média de idade de 57,3 ± 13,3 anos, portadores de 138 nódulos ou massas adrenais. Os exames foram realizados em equipamento de 1.5 T e gradiente de 43 mt/m (Magnetom Sonata; Siemens Medical Systems, Erlangen, Alemanha) e em equipamento de 1.5 T e gradiente de 33 mt/m (Magnetom Espree; Siemens Medical Systems, Erlangen, Alemanha). Utilizou-se um sistema de múltiplos volumes adquirido pela sequência PRESS CSI 2D híbrida disponível comercialmente pela Siemens Medical Systems (Erlangen, Alemanha). O ajuste crânio-caudal da grade de múltiplos volumes foi feito com três sequências sagitais (respiração livre, inspiração e expiração máximas) e látero-lateral e ântero-posterior acrescentando as sequências coronal e axial. Definimos também uma sistemática de pós-processamento e análise para todas as massas. O pós-processamento foi realizado numa estação de trabalho (LEONARDO ; Siemens Medical Systems) com programa dedicado à análise da espectroscopia. A análise da espectroscopia foi interpretada por inspeção visual e pelo levantamento das amplitudes dos picos dos metabólitos de interesse, lipídeo (Lip), colina (Cho), creatina (Cr) e catecolaminas (4,0 4,3 ppm) além do Lactato (Lac), Glutamina e Glutamato (Glx). Separamos também os diferentes picos de lipídeos presentes em cada grupo. Foram aplicadas as relações matemáticas implantadas previamente (Cho/Cr; 4,0-4,3/Cr; Lip/Cr e Cho/Lip) e testadas outras (Lac/Cr e Glx/Cr). Estudou-se também a correlação entre o tamanho da lesão e a razão Glx/Cr. Resultados: Utilizando-se as sequências indicadas na metodologia da ERM do 1 H e a sistemática de pós-processamento e análise foi possível a realização do exame em 123 (89,13%) das massas incluídas com reprodução dos resultados anteriormente publicados. A relação Lac/Cr -7,449 teve sensibilidade de 90,9% e especificidade de 77,8% na diferenciação entre feocromocitoma e carcinoma. Não houve diferença entre os grupos para a relação Glx/Cr (p>0,05), mas inferiu-se uma correlação entre o tamanho da lesão e o valor desta razão no adenoma, feocromocitoma e carcinoma. A androstenodiona, DHEA-S, aldosterona e o cortisol foram encontrados em todas as massas estudadas e o adenoma diferenciou-se dos demais por apresentar níveis de xvii
18 cortisol aumentados. Conclusão: A partir do protocolo de ERM do 1 H apresentado foi possível estabelecer um protocolo eficaz para a diferenciação dos nódulos e massas das glândulas adrenais. Este protocolo de aquisição de imagem e ERM permitiram a realização do exame em 123 (89,13%) das massas com lesão superior a 1,0 cm. A sistemática de pós-processamento foi eficaz na diferenciação dos nódulos. xviii
19 1 INTRODUÇÃO As glândulas adrenais, também chamadas de supra-renais, são afetadas por processos fisiológicos e neoplásicos complexos. Adicionado a isso, as glândulas são pequenas e localizadas no retroperitônio que por si só já representa uma dificuldade no exame físico. (1) Qualquer suspeita de massa na glândula adrenal requer anamnese e exame físico completos, avaliação bioquímica de todos os hormônios pertinentes e estudos por imagem adicionais. A insuficiência adrenal se dá quando há destruição de mais de 90% da glândula. (2) Algoritmos de testes endocrinológicos e de imagem são utilizados para investigar a etiologia das massas adrenais, que incluem hiperaldosteronismo primário, feocromocitoma, virilização e síndrome de Cushing. A diferenciação entre massas malignas e benignas é de fundamental importância uma vez que as metástases nas glândulas supra-renais são comuns, representando o quarto sítio no organismo. O adenocarcinoma cortical da adrenal, por outro lado, tem baixa prevalência, mas permanece com o interesse clínico devido à alta taxa de mortalidade. (3) A ressonância magnética (RM) e a tomografia computadorizada (TC) são comumente utilizadas para avaliar a lesão adrenal incidental ou não. (2, 4, 5) Porém a imagem morfológica, apesar da sua utilidade, é limitada por sua relativa especificidade. Para suprir esta limitação, há a possibilidade de realização da RM funcional. Este mesmo método de imagem, devidamente dedicado, pode trazer informações metabólicas dos nódulos e massas da glândula adrenal. As técnicas funcionais na RM se baseiam na concentração de lipídeo intracelular na massa (4, 6, 7), as diferenças de perfusão entre massas malignas e benignas (5, 8) e a atividade metabólica da massa. (9-11) Além das características funcionais, a RM possui a melhor resolução de contraste para a avaliação adrenal quando comparada com outros métodos de imagem. Ela possui resolução espacial adequada para detecção das lesões pequenas com até 0,5 cm. Já a supressão de gordura é usada em imagens fortemente ponderadas em T2 que não são degradas por artefatos de desvio químico da gordura
20 2 ao redor das glândulas adrenais. Imagens multiplanares ajudam a detectar extensão das massas adrenais em estruturas adjacentes. (5) Dentre as técnicas funcionais da RM, destacamos a espectroscopia por RM (ERM) do próton de hidrogênio ( 1 H) que é uma técnica não-invasiva e livre de riscos potenciais com a qual se pode monitorar os estágios, agudo ou crônico, de uma doença. O desenvolvimento de métodos de localização espacial de amostras, com níveis relativos de metabólitos móveis em um volume definido a partir de imagens por RM, é a base para a integração das informações obtidas por esta técnica. A associação das informações anatômicas e patológicas obtidas, com as imagens por RM, proporciona uma nova forma de se entender as origens e a evolução das doenças. (12) A Universidade Federal de São Paulo (UNIFESP) conta há mais de dez anos com o Grupo de Estudo Avançado de Patologia de Adrenal, que incluem as disciplinas de Diagnóstico por Imagem, Endocrinologia e Urologia. Ao longo destes anos, estudamos pelo menos duas centenas de casos de massas adrenais e tivemos a oportunidade de iniciarmos o projeto piloto de avaliação funcional por ERM do 1 H de massas adrenais, experiência inicial, publicado em 2007 (10). No entanto, muito no que diz respeito ao tema ainda precisou ser aprimorado desde então. Dada à perspectiva real da melhora significativa no diagnóstico etiológico das massas nas glândulas adrenais com a ERM, procuramos a partir do projeto já estabelecido desenvolver e definir o protocolo de aquisição e pós-processamento de dados espectroscópicos no Departamento de Diagnóstico por Imagem do Hospital São Paulo Escola Paulista de Medicina (UNIFESP).
21 3 1.1 Objetivo Aperfeiçoar um protocolo de ERM do 1 H para a diferenciação de nódulos e massas das glândulas adrenais, em especial adenomas, feocromocitomas, carcinomas e metástases.
22 4 2 REVISÃO DA LITERATURA 2.1 Histórico A imagem por RM, amplamente conhecida por sua utilidade tanto pela variedade de imagens obtidas do interior do corpo de modo inofensivo e não invasivo quanto por ser uma ferramenta importante de diagnóstico médico, tem seus alicerces dispostos há mais de 60 anos a partir de experimentos físicos desenhados para medir as propriedades dos spins nucleares do 1 H. (13) O fenômeno da ressonância magnética foi primeiro descrito independentemente em 1946 por Purcell et al (14) e Bloch et al (15). Cinco anos depois, Proctor e Yu (16) observaram que a frequência de ressonância de um núcleo depende do ambiente químico onde ele se encontra, o qual produz uma pequena, mas suficiente, mudança na frequência de ressonância de Larmor do núcleo. Esse comportamento nuclear foi denominado desvio químico (chemical shift - ), e é causado pelo campo magnético gerado pela movimentação dos elétrons ao redor do núcleo, interagindo com o campo magnético principal. Em 1973 Lauterbur descreveu a zeugmatografia para o estudo espacial da distribuição do núcleo dentro da amostra com a utilização de gradientes. (17) Porém somente em 1974, o primeiro espectro in vivo (fósforo - 31 P) foi adquirido utilizando a RM a partir do músculo esquelético de um rato. (18) Mansfield e Maudsley em colaboração realizaram a primeira imagem de RM do hidrogênio ( 1 H) in vivo de um dedo em (19) Com o advento dos magnetos supercondutores foi possível obter informações espectrais de uma série de tecidos e órgãos humanos. Nesse panorama, Bottomley et al. (20), em 1983, descreveram o primeiro gráfico espectroscópico de 31 P de cérebro adulto. No ano seguinte, a mesma equipe comparou espectros cerebrais de 1 H, 13 C e 31 P em voluntários. (21) Em 1989, Leroy-Willig et al. (22), baseados em seus achados de ERM do 1 H in vitro publicados dois anos antes (23), mediram o conteúdo lipídico in vivo de 22 lesões adrenais utilizando uma sequência de imagem espectroscópica publicada por Dixon (24) em Nesta aquisição, precursora de outros métodos sensíveis à fase, obtinha-se um mapa espectral da água e da gordura em-fase e fora-de-fase. Em seguida,
23 5 calculava-se a amplitude de cada espectro, relacionando-os e media-se a quantidade de gordura da glândula. Os resultados in vivo foram compatíveis com os in vitro e demonstraram que os adenomas possuem uma quantidade de lipídeo maior que o carcinoma. Desde então, a ERM do 1 H não foi mais usada para caracterizar nódulos e massas da supra-renal já que todos os esforços se concentraram nos aspectos morfofuncionais a partir das imagens de TC (25-28), RM (4, 29, 30) e PET (31, 32). Em 2007, Faria et al. (10) publicaram os resultados iniciais do protocolo para a realização da ERM do 1 H multi-voxel da glândula supra-renal desenvolvido por nosso grupo no Departamento de Diagnóstico por Imagem do Hospital São Paulo Escola Paulista de Medicina (UNIFESP). Em 2009, Kim et al. (11) utilizaram uma sequência de ERM do 1 H single-voxel com compensação respiratória para avaliar massas adrenais suspeitas de feocromocitoma. 2.2 Bases Físicas As imagens e gráficos espectroscópicos por RM exploram as propriedades magnéticas nucleares. Em geral, a ERM in vivo obtém os sinais de ressonância a partir de moléculas presentes nos tecidos e células, enquanto o imageamento por RM produz sinais de ressonância limitados pela água intra e extracelular e alguns lipídios. (33) Ambas se baseiam no fenômeno em que o núcleo de certos átomos possui o denominado momento magnético (μ 0 ), apresentando, com isso, uma polarização, também chamada de dipólo magnético. O magnetismo nuclear origina-se a partir de uma propriedade intrínseca do núcleo denominada momento angular spin, representado na Figura 1. A orientação do spin determina o M 0 necessário para a aquisição de imagem e espectro por RM. Exemplos incluem o 1 H, o 13 C, o 31 P e o 19 F. O isótopo mais utilizado no diagnóstico médico, atualmente, é o 1 H, porque é o mais abundante no organismo e possui maior M 0 do que qualquer outro átomo, produzindo um sinal facilmente detectado.
24 6 O dipólo magnético, na ausência de influências externas, é orientado aleatoriamente, e o somatório de todos eles é igual a zero. O M 0 a partir de átomos individuais é muito fraco e não pode ser detectado com uma tecnologia convencional. Um magnetismo de tal intensidade que possa ser detectado pode ser criado alinhandose os spins de milhares de átomos, fazendo com que seus magnetismos se combinem, coerentemente. (34) Figura 1 - Spin atômico. Representação esquemática do movimento rotacional e da polarização protônica. (35) Desta forma, na presença de um campo magnético externo, o núcleo, precessará ao redor desse campo. Quando o 1 H é colocado dentro de um campo magnético, o dipólo alinha-se com o campo em uma dentre duas formas: seja na direção do campo (paralela) ou oposta ao campo (antiparalela). Estas orientações correspondem a estados de menor e maior energia, respectivamente. Figura 2 - Paralelismo e antiparalelismo do spin. Representação do comportamento paralelo e antiparalelo dos prótons no interior do campo magnético principal. (35) No estado de equilíbrio, um pequeno excesso final de dipólos, alinha-se na direção de menor energia (paralela) em comparação com a direção de maior energia
25 7 (antiparalela). O excesso é denominado magnetização final. Este excesso gera o sinal medido na RM. (Figura 2) A magnetização final aumenta com a força do campo magnético externo, bem como a diferença do nível de energia entre os estados, paralelo e antiparalelo. Por essas razões, a intensidade do sinal de RM aumenta proporcionalmente ao campo magnético externo. A frequência precessional ou frequência de ressonância ( 0 ) representa o número de vezes em que o vetor de magnetização efetiva (VME) realiza a trajetória de precessão e é característica para cada núcleo ativo. Para o 1 H, num campo magnético de 1.0 T, é de 42,57 mega-hertz (MHz). A 0 de um dipólo magnético depende da intensidade do campo magnético externo. Esta frequência precessional é representada pela equação de Larmor: 0 = B 0 (I), Onde é a razão giromagnética ou magnetogírica e é dada em mega-hertz por tesla (MHz/T) e B 0 representa a potência do campo e é dada em tesla (T). (36) Para reorientar os spins paralelos ao B 0 numa direção perpendicular a ele, aplica-se um pulso de radiofrequência (RF), que por sua vez gerará um campo magnético adicional (B 1 ), e, com isso, os VME s se afastarão, em movimento precessional, da direção longitudinal, dirigindo-se ao plano transverso. A intensidade de B 1 é da ordem de 0,1 Gauss (G). Quando a RF é aplicada a uma amostra, somente o componente B 1 do campo que é perpendicular ao B 0, atua no VME, variando com o tempo e com a ω 0. Desta forma, o M 0 começará a precessar ao redor de B 1 novamente, de acordo com a equação de Larmor: ω 1 = B 1 (II), onde ω 1 representa a frequência precessional em B 1. Essa condição necessária para a ressonância permite o VME rotacionar ao redor de B 0 e B 1, simultaneamente. Pode-se rotacionar o VME em qualquer ângulo desejado a partir de B 0, pelo ajuste da amplitude e duração do pulso de RF aplicado. Este ângulo é chamado de ângulo de inclinação. Quanto maior a energia fornecida pelo pulso de RF, maior o
26 8 ângulo de inclinação e o sinal captado pela antena receptora ligada ao plano transverso. (34) Quando se retira o pulso de RF, o VME passa novamente a sofrer a influência de B 0 e tenta realinhar-se com este, perdendo a energia dada pelo pulso. Este processo é chamado de relaxamento. De maneira simultânea, porém independente, os μ 0 do VME perdem a magnetização transversa devido à defasagem dos spins. O relaxamento leva à recuperação da magnetização no plano longitudinal (recuperação T1) e ao declínio da magnetização no plano transverso (declínio T2). (Figura 3) Na recuperação T1 os prótons perdem energia para o ambiente, enquanto que no declínio T2 os prótons trocam energia entre si, promovendo a defasagem. Estes dois fenômenos ocorrem simultaneamente e de forma independente. Quando se diminui o grau de magnetização transversa, o mesmo se dá com a magnitude do sinal (voltagem) induzida no fio receptor. A redução do sinal induzido é denominada sinal de declínio da indução livre (DIL). A amplitude inicial do DIL é proporcional ao número de prótons presentes na amostra (densidade de prótons). A razão de declínio é caracterizada pelo termo de declínio exponencial T2*. (37) t t Figura 3 Gráficos M xy (Magnetização Transversa) X t (Tempo) e M z (Magnetização Longitudinal) X t (Tempo). Representação gráfica dos efeitos de relaxação T1 e T2. (38)
27 9 As imagens por RM podem ser consideradas como um método de localização espectral aprimorada, por produzirem um mapa espacial da distribuição da água e da gordura. Em geral, esse mapa é usado na obtenção de informações anatômicas. A base de ERM é o desvio químico. Então, somente metabólitos presentes em concentrações mensuráveis e com mobilidade à RM podem ser adquiridos numa escala de tempo. (39) Em geral, a ERM, diferentemente das imagens por RM, utiliza a direção da codificação de frequência para a aquisição de dados dos desvios químicos em um determinado tempo a partir do DIL. O sinal decai rapidamente a sua oscilação de alta frequência de acordo com a Figura 4. Isto ocorre porque os dados são adquiridos sem aplicação do gradiente. Z B o Z Bo Z Bo M o Y M xy M xy Y M xy M xy Y M xy X X X tempo tempo tempo Z B 0 Z B 0 Z B 0 M 0 X M xy X M xy X M xy tempo tempo tempo Figura 4 Declínio de Indução Livre (DIL) e o efeito T2*. A aquisição espectroscópica depende do efeito T2*, para a mensuração do movimento molecular. (37) Então, uma simples seqüência de pulso, adquirida em 90 o, produz o DIL, onde todos os spins simplesmente precessam em frequências determinadas pelo campo magnético principal, permitindo que o espectro a ser obtido possa fornecer informações químicas detalhadas a cerca dos tecidos a partir de cálculos matemáticos baseados na transformada de Fourier. (12) A resolução espectral aumenta com o B 0 e é definida na ERM como a capacidade de se diferenciar um metabólito de outro, numa mesma área, é limitada
28 10 pela homogeneidade do campo magnético determinado, quantitativamente, pelo decaimento T2* do sinal com o tempo (DIL), ou a largura da linha do sinal espectral. Em contra partida, os efeitos de susceptibilidade magnética, que alargam as linhas espectrais e reduzem o decaimento T2*, aumentam com a intensidade do campo magnético. Com isso, a habilidade em se determinar o sinal de um metabólito é limitada à mobilidade molecular. Pequenas moléculas dão um pequeno, mas bem delimitado, sinal, já as macromoléculas possuem um grande, mas mal delimitado, sinal. A qualidade do espectro é largamente determinada pela relação sinal-ruído (RSR), já que o ruído se acumula incoerentemente e o sinal coerentemente, o aumento da RSR pode ser realizado pelo acúmulo de excitações. Com o ruído não corrigido, a RSR aumenta com a raiz quadrada do número de aquisições. A multiplicação do número de aquisições faz com que a RSR dobre, aumentando o tempo de aquisição espectroscópica. Outra forma de aumentar a RSR é aumentando o volume medido. Quanto maior, mais núcleos serão excitados e melhor RSR obtida. Contudo, este tipo de ganho de RSR degrada a resolução espacial. (35) O tempo de repetição (TR), definido como o tempo entre um pulso excitatório até o próximo pulso excitatório, é responsável pelo equilíbrio da magnetização, determinando a amplitude do sinal. TR s curtos resultam em picos menores e justos, enquanto TR s longos resultam em picos maiores e não ajustados. Um TR longo permite maior relaxação longitudinal (efeito T1), causando, por esta razão, um alto equilíbrio de magnetização. A otimização da RSR por unidade de tempo é conseguido se o TR for aproximadamente igual ao valor do tempo T1 dos metabólitos a serem examinados. O tempo de eco (TE), definido como o tempo entre o pulso excitatório e a leitura do sinal, é responsável pela seletividade metabólica. TE s curtos fazem com que haja ganho de sinal, acarretando em muitos picos e menor nível de ruído aparente entre os picos. Metabólitos de alto e baixo pesos moleculares são identificados ao se utilizar TE s curtos. TE s longos acarretam em perda de sinal, determinando poucos e menores picos, com maior nível de ruído aparente entre os picos. Metabólitos de baixo peso
29 11 molecular são identificados utilizando-se TE alto. Outro efeito que a escolha de um TE longo pode causar é potencializar o acoplamento spin-spin (T2). (40) Teoricamente, a representação da frequência da oscilação pura é uma linha espectral com uma posição definida da frequência de ressonância 0. Na prática, por conta do decaimento do sinal T2* e do limite de tempo de aquisição de dados, o alargamento da curva torna o pico menos distinto. Um pico é caracterizado pela 0 ; altura do pico ou amplitude (h); largura do pico na metade da altura (b); e área. Nas representações espectrais usadas na RM, o eixo da frequência sempre é colocado da direita para esquerda. (35) A necessidade de se obter um espectro específico do tecido alvo foi prontamente reconhecida como prioridade na ERM in vivo. Inicialmente, esta condição foi conseguida utilizando-se bobinas de RF de superfície local. (41) As bobinas de RF são instrumentos com a finalidade de detectar o sinal da magnetização transversa em forma de um DIL ou de um eco, e algumas, também aplicam ao paciente um pulso de RF, à frequência de Larmor. Nas bobinas de transmissão, o subsistema de RF sintetiza e transmite o sinal de RF à frequência ressonante pela bobina transmissora ao espécime em estudo. Em geral, essas bobinas são grandes, com uniformidade de RF elevada para a excitação. A não necessidade de um controle fino da frequência para a transmissão torna possível usarem-se ganhos elevados ao amplificador. Já as bobinas receptoras têm um efeito acentuado sobre a RSR do sistema, sendo, pois importantes na obtenção de uma ótima qualidade de imagem. Após ser detectado pelas bobinas receptoras, o sinal passa por um pré-amplificador para aumentar sua potência. Um desmodulador subtrai, então, o sinal detectado de um sinal referência à frequência de Larmor, de modo que as informações do sinal da imagem possam ser processadas na faixa de kilo-hertz (khz) e não de MHz. (37) Embora seja adequada para tecidos superficiais, a maioria das ERM s in vivo requer a combinação com as imagens e, além disso, o conceito da espectroscopia é de ser não-invasiva. Em experimentos com animais, os tecidos profundos e órgãos eram expostos cirurgicamente e a amostragem era realizada com a colocação da bobina de superfície diretamente no órgão. Para a aplicação clínica, contudo, o objetivo é ter a
30 12 capacidade de obter-se uma ou várias regiões, selecionáveis, usando métodos de localização espacial sem a necessidade de um procedimento cirúrgico. Todo sinal de RM, I(t), quer para produzir uma imagem ou um gráfico espectroscópico, possui três componentes: I(t) = A i cos ( i t + i ) i onde A, é a amplitude do sinal de RF e, a fase. Denomina-se como fase a posição de cada momento magnético na trajetória precessional em torno de B 0. Os momentos magnéticos que estão em-fase encontram-se no mesmo ponto da trajetória precessional em torno de B 0 num dado momento, enquanto os momentos magnéticos que estão fora-de-fase não estão no mesmo ponto na trajetória precessional. Nas imagens clínicas, utiliza-se a do sinal para codificar a informação espacial em uma direção (codificação da frequência) e a fase numa segunda direção (codificação da fase), e a amplitude contém informações sobre a intensidade da imagem. O exato valor da intensidade da imagem é determinado pelas propriedades dos spins da água no tecido, pela densidade dos spins, pelos efeitos T1 e T2, e pela (III) (12, 38, 39, 42, 43) seqüência de pulso usada para adquirir as imagens. Adicionalmente, a frequência do sinal usado não codifica a informação espacial, mas, preferivelmente, registra as diferenças de frequências naturais causadas pelo campo magnético local, responsável pelo desvio químico. Quando o DIL é adquirido com uma simples seqüência de aquisição de pulso, o sinal é composto de informações de, o qual contém o desvio químico, e de amplitude, o qual informa sobre a área da ressonância. A é utilizada somente para a diferenciação entre as frequências positivas e negativas. (41) O processo de localização da ERM é realizado principalmente empregando as bobinas de RF, gradientes de B 0 estático, ou gradientes de pulso espacial, ou a (44, 45) combinação deles. Existem duas classificações básicas de metodologias de localização espectroscópica. A primeira classificação leva em consideração o DIL, e dividem-se em três tipos. O primeiro tipo inclui métodos nos quais todos os spins exceto aqueles dentro da área de interesse são efetivamente removidos. (38)
31 13 excitados. A segunda classe inclui métodos os quais somente os spins desejáveis são E a terceira classe de métodos envolve o uso de protocolos de codificação espacial como a codificação por Fourier e por Hadamard. Como exemplo, inclui-se localização das imagens pelo desvio químico (CSI). (35, 46) A segunda forma de classificação considera-se o campo magnético em B 1 e B 0. Os métodos de localização em B 1 levam em consideração, de alguma forma, o perfil não-uniforme da bobina de RF utilizada para obter a localização espectroscópica. As bobinas são projetadas para produzir uma excitação espacialmente uniforme da amostra, por isso são de forma cilíndrica e requerem que a amostra seja colocada no interior do cilindro. Já os métodos de localização em B 0 fazem uso dos gradientes na obtenção da localização espectroscópica. Tanto os métodos de volume individual (single-voxel) quanto de múltiplos volumes (multi-voxel) são bastante empregados clinicamente. Exemplos dessas metodologias incluem o modo de aquisição de eco estimulado (STEAM), a espectroscopia por determinação de pontos (PRESS) (12, 35, 38, 42, 46) e a (35, 46) CSI. O CSI é uma técnica que permite a aquisição do espectro a partir de voxels separados de uma amostra. Pode consumir bastante tempo porque requer várias codificações de fase para conseguir uma resolução espacial adequada. (47) O aumento da resolução espacial pelo CSI é baseado no simples fato que a variabilidade do campo dentro do voxel é muito menor que através de toda a amostra. (48) O alinhamento dos desvios calculados para cada voxel é proporcional às variações do campo magnético da amostra e pode ser usado para mapear o campo magnético estático e, desta maneira, registrar os metabólitos. A sensibilidade perdida, proporcional a resolução espacial, restringe o uso do CSI apenas para casos com RSR favorável. Por isso, o CSI é complementado com outros métodos de seleção espectral espacial (por exemplo, PRESS) que minimizam a baixa sensibilidade por registrar espectros a partir de voxels maiores. (47) Já a PRESS é uma técnica de localização disponível para a obtenção da 1 H ERM multi-voxel. A seleção do volume por esta técnica resulta em variações espaciais
32 14 das relações metabólicas nas margens do volume selecionado devido a artefatos de desvio químico. Esses erros são dependentes da largura de banda dos pulsos de RF, do tamanho da região selecionada e da frequência ressonante e por esta razão se tornará mais proeminente com o aumento da potência do campo. Uma forma de reduzir o artefato de desvio químico é determinar que o campo de visão (CDV) da PRESS seja maior que a região de interesse, utilizando-se os voxels centrais da matriz espectroscópica de acordo com a Figura 5. (49) Figura 5 Voxels elegíveis no Espaço K da sequência PRESS. Espaço-K. (2) Amostragem reduzida elipticamente. (3) Amostragem elegível. (1) Amostragem completa do Tanto o método de volume único quanto o de múltiplos volumes são bastante empregados na aquisição espectroscópica, porém existem algumas diferenças que precisam ser observadas. No método, utilizando um volume único, a aquisição e o processamento são mais rápidos e práticos. Porém, não se obtém referência interna para comparação e o posicionamento adequado do volume é fundamental. Apresenta, após a aquisição, um único espectro, representando a média do volume selecionado. Já com os volumes múltiplos, a aquisição e o pós-processamento são mais complexos e demorados, comparando-se com o volume único. Porém, dispensa a necessidade de se saber à localização exata da afecção, podendo ser aquisição bidimensional ou tridimensional. Na aquisição com volumes múltiplos, estudam-se os vários componentes de uma lesão num único tempo de exame. (10, 12, 35, 38, 39, 42, 43, 50) O sinal protônico predominante da maioria dos tecidos é originado da água. Em média, um tecido do corpo humano é constituído de 80% de água. Apesar dessa característica corporal ser fundamental na produção de imagens por RM, na espectroscopia, ao contrário, essa alta concentração prejudica a detecção e determinação dos metabólitos. (12)
33 15 Os prótons da água produzem um sinal, que resulta numa concentração de 88 molar (M), enquanto a maioria dos metabólitos de importância clínica estão numa concentração entre 1 e 20 mm. Então, a diferença da intensidade de sinal resultante é da ordem de 10 4 a O instrumental da RM não permite que pequenos sinais sejam observados na presença de um muito grande. Por esta razão, é necessário suprimir o sinal da água. Existem, comumente, duas classificações de métodos de supressão: a não-excitação seletiva e a saturação do sinal da água propriamente dita. Um ou ambos os métodos de supressão podem ser (12, 35) usados, produzindo uma maior supressão. Uma forma de minimizar a contaminação com sinais fora do volume espectral de interesse é a utilização das barras externas de saturação de sinal. São compostos de pulsos de pré-saturação que anulam o sinal dos tecidos e dos núcleos em fluxo, de forma a minimizar a contaminação lipídica, quando o sinal dos lipídeos das regiões fora do volume de interesse interfere no estudo espectroscópico. (44, 45) 2.3 Bases Químicas A ERM se utiliza do fato de que a do núcleo atômico é alterada pelo ambiente químico, causando uma pequena, mas fundamental, alteração nesta frequência chamada de desvio químico ( ). Este fenômeno é causado pelos campos magnéticos gerados pelos elétrons circulantes ao redor do núcleo que protegem o núcleo do B 0 externo. A extensão do desvio químico depende do número e do tipo de átomos adjacentes e das estruturas moleculares. (35, 51) Por conta das diferenças entre, os sinais de núcleos idênticos podem ocupar posições diferentes num gráfico espectroscópico, por estarem ligados a diferentes elementos ou componentes moleculares. Com isso, é possível distinguir e identificar componentes metabólicos. (35) O campo magnético local, produzido pelo movimento dos elétrons, na presença de B 0 tem a tendência de se posicionar de forma oposta ao B 0 (antiparalelismo). Desta
34 16 forma, o B 0 influencia o movimento dos elétrons e a velocidade, afetando diretamente a intensidade e a direção desse campo magnético produzido. A frequência na qual o spin precessa é proporcional ao B 0. Com o aumento de B 0, aumenta o desvio químico, aumentando também a resolução espectral. Então, uma espécie protônica em particular, que possui uma, obedece à seguinte equação: = (B 0 + B) (IV) onde B é proporcional ao B 0. Por esta razão, pode-se definir uma quantidade, (constante de blindagem), que é dependente de B 0. = B 0 / B (V) Substituindo: = B 0 (1 + ) (VI) Consequentemente, a frequência do desvio aumenta com o campo magnético. Se a for positiva, existe um campo maior ao redor do núcleo do que àquele aplicado externamente por B 0. Por convenção, a medida espectral da blindagem é colocada na abscissa do plano cartesiano. Desta forma, os sinais de núcleos com blindagem fraca resultam em alta, localizando-se à esquerda do gráfico, e os sinais de núcleos com blindagem forte, resultam em baixa, localizando-se à direita do gráfico. (12, 35) O desvio químico, geralmente, não pode ser considerado como um simples valor associado à. Na realidade, a funciona como uma força, significando que se pode ter diferentes valores para direções diferentes. (12) Em geral, os desvios químicos são relativamente pequenos, comparados com a frequência de referência. Por esta razão, eles são representados em partes por milhão (ppm). Na química analítica, o ponto zero do desvio químico é definido em relação ao tetra-metil-silano (TMS). Porém, esta substância não é observada na ERM in vivo. Desta forma, o ponto zero é definido por um valor determinado pelo sistema e levado em consideração no momento da aquisição espectroscópica.
35 17 Este ponto de referência sofre influência da temperatura, pois o da água na temperatura ambiente é de 4.9 ppm, enquanto que o da água no organismo é de 4.7 ppm. Já para os outros metabólitos, a influência da temperatura pode ser desconsiderada. (35) Outro importante parâmetro, resultante das interações das ligações entre elétrons, é o acoplamento spin-spin, também chamado de acoplamento escalar ou acoplamento J. A explicação para essa interação de acoplamento foi primeiramente proposta por Ramsey e Purcell em (38) Este acoplamento origina-se a partir das interações indiretas de dois spins nucleares intervindo na estrutura eletrônica da molécula. Diferentemente do desvio químico, em que não há indução pelo B 0 externo e, por esta razão, está sempre presente, o acoplamento spin-spin surge a partir do campo produzido por um spin nuclear que interage com elétrons próximos a ele, na presença de B 0. Estes se dobram para dentro da estrutura molecular, interagindo com outros elétrons, influenciando o campo dos núcleos vizinhos. A intensidade dessa interação é medida em hertz (Hz) e é chamada de constante de acoplamento escalar (J). O valor do J não se modifica com a intensidade (12, 35) do campo, explicando o porquê de se medir este valor em Hz ao invés de ppm. Não há dependência da orientação, com relação ao B 0 estático externo, do J como ocorre com o desvio químico anisotrópico. Porém, o efeito da intensidade do campo no acoplamento escalar origina um padrão complexo de múltiplos picos. Para altos campos, todos os acoplamentos spin-spin são considerados como tendo um padrão de acoplamento fraco. Isto ocorre quando a intensidade do campo é grande o suficiente para que a diferença de desvio químico (Hz) entre as ressonâncias acopladas seja muito maior do que o J. J (VII) Quando esta condição não é mantida, o sistema spin passa a ser chamado de regime de acoplamento forte. Num equipamento de 1.5 T, é possível para alguns sistemas spin de aminoácidos, como o glutamato, estar no regime de acoplamento forte. Isto significa que as regras para a avaliação da influência do acoplamento spinspin no acoplamento forte não são aplicadas. Algumas sequências de localização, como a STEAM, são altamente influenciadas pelos efeitos de acoplamento, produzindo
36 18 efeitos não só na identificação dos picos, mas também na quantificação dos metabólitos. (12) O desvio químico e o acoplamento spin-spin são as duas interações que produzem um campo magnético local no núcleo, contudo os spins nucleares criam um campo magnético local próprio, influenciando outros spins vizinhos. Esta interação, chamada dipolo-dipolo, não precisa de elétrons ou ligações químicas na transmissão do campo magnético para os núcleos vizinhos. 2.4 Espectroscopia por Ressonância Magnética A ERM do 1 H não é uma nova tecnologia e vem sendo utilizada para produzir informações bioquímicas dos tecidos biológicos por mais de 30 anos. Foi aprovada pelo Food and Drug Administration (FDA) e é amplamente usada na avaliação do cérebro (51, 52) e da próstata (42, 50). Apresenta-se como uma técnica não-invasiva e livre de riscos potenciais com o qual se pode monitorar os estágios, agudo ou crônico, de uma doença. O desenvolvimento de métodos de localização espacial de amostras, com níveis relativos de metabólitos móveis em um volume definido a partir de imagens por RM, é a base para a integração das informações obtidas por esta técnica. A associação das informações anatômicas e patológicas obtidas, com as imagens por RM, proporciona uma nova forma de se entender as origens e a evolução das patologias. (38, 42) Em muitas doenças, as alterações metabólicas podem preceder as alterações anatômicas. A espectroscopia se apresenta, pois, como um método de detecção precoce destas alterações, por ser potencialmente sensível a estas mudanças. No entanto, a ERM é uma forma de espectroscopia inerentemente fraca. Requer que as substâncias químicas ou metabólitos estejam presentes em concentrações maiores que 1mM e, portanto, a detecção de concentrações menores é possível somente em circunstâncias especiais, o que prejudica a sua aplicação sistemática. Assim, ainda que a ERM seja um poderoso recurso na obtenção não-invasiva de informações bioquímicas in vivo, existe uma limitação em termos dos metabólitos que se pode monitorar. (40)
37 19 Na ERM, a posição de cada pico ao longo da linha central horizontal, também chamada de linha química do deslocamento ou linha central da frequência, é governada pelo campo magnético principal. Assim, os 1 H, em grupos moleculares diferentes de moléculas distintas, fazem com que seus picos correspondentes apareçam em posições diferentes na linha central da frequência, ou seja, cada metabólito ressona em uma frequência diferente, de acordo com o campo magnético gerado pelos agrupamentos moleculares de seus prótons. A amplitude do pico determina a quantidade de metabólito. A concentração de um determinado metabólito é calculada através da área do pico. A área do pico é usada por não ser tão influenciada por alguns fatores físicos como a homogeneidade do campo magnético, nível de ruído e o tempo de relaxação. (38) A quantificação absoluta do espectro, isto é, a interpretação das áreas dos picos possui certo grau de dificuldade. A simples calibração das áreas dos picos usando soluções padrão de concentrações conhecidas é especialmente difícil pelo fato da sensibilidade das bobinas mudarem com a carga. Além disso, a dependência do efeito T2 nos sinais dos metabólitos influencia a quantificação metabólica absoluta. A simples determinação da área do pico pode ser impedida pela possibilidade dos sinais se sobreporem e que os reservatórios de metabólitos não contribuam para o sinal, por conta da baixa mobilidade. Por esta razão, se utiliza a intensidade de sinal relativa no estudo espectroscópico, comparando-se a relação dos metabólitos numa mesma região ou em regiões diferentes no mesmo paciente, ou fazendo estas relações para pacientes diferentes. (35) 2.5 Metabolismo da Glândula Adrenal na ERM A glândula adrenal é composta de um córtex externo, derivado do mesoderma, e de uma fina medula interna, originada a partir da crista neural, que corresponde a cerca de um décimo do seu peso. O córtex é subdividido em três zonas, glomerulosa (externa), fasciculada (mediana) e a reticular (interna). (53) A zona glomerulosa secreta os mineralocorticóides sendo a aldosterona, que na curva espectral está situada entre 1,17 e 1,20 ppm (Figura 6), o principal hormônio desta classe. A ação primária destes hormônios esteróides, compostos de 21 átomos
38 20 de carbono, é regular o balanço de água, sódio (Na + ) e potássio (K + ) no sangue, retendo os primeiros e excretando o último. Com isso, é fundamental para o equilíbrio hidromineral do organismo. (54) A aldosterona é sintetizada a partir do colesterol que é convertido em pregnenolona no interior das mitocôndrias, envolvendo uma série de hidroxilações e quebra da sua cadeia lateral. A seguir, através de uma sequência de hidroxilações que ocorrem no retículo endoplasmático, a pregnenolona é transformada em desoxicortisol. Este composto é transferido novamente para o interior das mitocôndrias, onde é hidroxilado para formar o cortisol. A seguir, o grupo metil na posição 18 do cortisol é hidroxilado por enzimas mitocondriais, dando origem à aldosterona (Figura 7). (55) Figura 6. Aldosterona. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 600 MHz. (54) Já a zona fasciculada, que corresponde a 75% da região cortical, secreta hormônios glicocorticóides, compostos de 21 átomos de carbono, que apresentam importantes efeitos no aumento da concentração de glicose no sangue, opondo-se à insulina. O cortisol, localizado na curva espectroscópica em 0,88 e 1,46 ppm, (Figura 8) é o glicocorticóide mais importante no ser humano. Além disso, é essencial à vida em face dos seus efeitos sobre o metabolismo de carboidratos, lipídeos e de proteínas. Está envolvido na resposta ao estresse, no aumento da pressão arterial, na infertilidade feminina e na supressão do sistema imune. (54)
39 21 Figura 7. Biossíntese e metabolismo dos esteróides endógenos. (56) Figura 8. Cortisol. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 600 MHz. (54) A síntese do cortisol, pelas células da zona fasciculada, segue as mesmas etapas que ocorrem na zona glomerulosa, até a sua formação (Figura 7). É mínima a quantidade de cortisol armazenada nas células da zona fasciculada, de modo que o hormônio é continuamente sintetizado e a velocidade de síntese adapta-se
40 22 rapidamente às necessidades do organismo. A quantidade de cortisol presente no soro possui uma variação durante o dia, com altos níveis presentes pela manhã e baixos níveis ao anoitecer. (55) A zona reticular, mais interna, secreta os esteróides sexuais, andrógenos e estrógenos, além de seus precursores, que contribuem para o aparecimento e manutenção dos caracteres sexuais secundários. Dentre os precursores produzidos os de maiores quantidades são a androstenodiona com posição espectral em 0,92 e 1,21 ppm (Figura 9), dehidroepiandrosterona (DHEA) localizada entre 0,88 e 1,03 ppm (Figura 10) e seu sulfato (DHEA-S) situado entre 1,22 e 1,33 ppm (Figura 11). Figura 9. Androstenodiona. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54) Na mulher, as adrenais são responsáveis por 50-60% da produção de andrógenos. Sua importância é pequena para o homem, em face da grande produção de testosterona pelos testículos. As células da zona reticular podem ainda formar pequenas quantidades de estradiol e de estrona a partir da testosterona e androsterona. (54) Os esteróides sexuais são sintetizados pelas células da zona reticular a partir da 17-hidroxipregnenolona e da 17-hidroxiprogesterona (Figura 7). Por uma reação semelhante, a cadeia lateral dos carbonos é removida dá origem, respectivamente, à DHEA e à androstenodiona. A DHEA é reversamente conjugada ao
41 23 sulfato pela sulfotransferase primariamente nas adrenais, no fígado e intestino delgado. Os níveis de DHEA naturalmente sofrem variações ao longo do dia, enquanto que a concentração de DHEA-S se mantém estável. (55) Figura 10. Dehidroepiandrosterona (DHEA).a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54) Figura 11. DHEA sulfato (DHEA-S). a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54)
42 24 Já a parte interna da glândula supra-renal, a medula, é de origem ectodérmica (células da crista neural) semelhante aos gânglios do sistema nervoso simpático. As células endócrinas do sistema simpático-adrenal têm a capacidade de sintetizar e segregar catecolaminas (dopamina, norepinefrina e epinefrina). São chamadas de células cromafins, pelo fato de apresentarem uma reação histoquímica característica, após contacto com agentes oxidantes (dicromato de potássio K 2 Cr 2 O 7 ). (57) Os hormônios do sistema simpático-adrenal, conquanto dispensável à vida, são necessários para as adaptações do estresse agudo e crônico. A epinefrina, ou adrenalina, localizada em 2,76 ppm (Figura 12) constitui aproximadamente 80% das catecolaminas na medula adrenal, e não é sintetizada em tecidos extramedulares. Figura 12. Epinefrina. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54) Em contraste, a maior parte da norepinefrina, ou noradrenalina, situada em 6,95 ppm (Figura 13), presente nos órgãos enervados pelos nervos simpáticos, é sintetizada in situ (80% do total), e o restante, é formado em outras terminações nervosas e alcança as células-alvo pela circulação. (54) A biossíntese das catecolaminas, esquematizada na Figura 14, inicia-se a partir da hidroxilação da tirosina, reação catalisada pela tirosina-hidroxilase, que a transforma
43 25 em desidroxifenilalanina (L-DOPA). A L-DOPA, sob a ação da dopa-descarboxilase, é descarboxilada para dopamina, que sob a ação da dopamina-β-hidroxilase, forma, dentro dos grânulos, a noradrenalina. A maior parte da noradrenalina migra para o citoplasma, onde é metilada pela feniletanolamina N-metiltransferase, convertendo-se em adrenalina. (55) Figura 13. Norepinefrina. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54) Figura 14. Biossíntese das catecolaminas. (55) Na Figura 15 estão descritas as diferentes vias metabólicas para a adrenalina e a noradrenalina. Estas são inicialmente desaminadas oxidativamente ao nível das
44 26 mitocôndrias pela monoamina oxidase (MAO), a 3,4-diidroxifenilglicoaldeído (DOPGAL). Este aldeído é, posteriormente, ou reduzido a 3,4-diidroxifeniletilenoglicol (DOPEG) por ação da aldeído-redutase, ou sofre oxidação catalisada pela aldeído oxidase/desidrogenase, com a formação do ácido 3,4-diidroximandélico (DOMA). A adrenalina e a noradrenalina que entram na circulação são extensamente metiladas no citoplasma pela catecol-o-metiltransferase (COMT), à metanefrina, de localização espectral em 3,81 ppm (Figura 16), ou à normetanefrina, situada em 3,89 ppm e 6,95 ppm (Figura 17), respectivamente. Figura 15. Metabolização das catecolaminas. (58) A normetanefrina e a metanefrina podem posteriormente sofrer oxidação, catalisada pela MAO, originando o 3-metoxi-4-hidroxifenilglicoaldeído (MOPGAL). O MOPGAL pode, por sua vez, ou ser reduzido a 3-metoxi-4-hidroxifeniletilenoglicol (MOPEG) por ação da aldeído redutase ou ser oxidado, pela aldeído oxidase, a ácido vanilmandélico (VMA), de posição espectroscópica em 3,85 ppm (Figura 18). Estes dois últimos compostos podem, igualmente, formar-se pela ação da COMT sobre o DOPEG e DOMA, respectivamente. Por ação de uma álcool oxidase, o
45 27 metabólito MOPEG livre é extensamente convertido em VMA, constituindo-se este como o principal metabólito das catecolaminas excretado na urina. (58) Figura 16. Metanefrina. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54) Figura 17. Normetanefrina. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54)
46 28 Figura 18. Ácido Vanilmandélico. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54) O feocromocitoma, tumor produtor de catecolaminas, pode levar a uma morbidade e mortalidade significante. Corresponde a uma causa frequente de massas adrenais clinicamente invisíveis (cerca de 1,5 a 23%). A prevalência de hipertensão secundária devido ao feocromocitoma, controlada ou com alterações significativas, é estimada em 0,1 a 0,5%. Os achados clínicos mais freqüentes são dor de cabeça, palpitações, sudorese e ansiedade. Hipertensões severas ocasionalmente evoluem com encefalopatia, retinopatia e proteinúria. (3) 2.6 Metabolismo da Colina A ressonância da colina na ERM 1 H, utilizando-se uma potência de campo magnético de 1.5T, não é específica de um único componente e pode ter a contribuição de outros metabólitos como a fosfocolina, fosfatidilcolina, glicerofosfocolina, etanolamina, fosfoetaloamina, taurina, além da própria colina, ou seja, não possui resolução suficiente que permita a identificação individual destes picos. (42, 43, 50, 51)
47 29 A colina, amina quaternária, é um nutriente essencial fornecido através da dieta. É precursora da acetilcolina e da fosfatidilcolina, situada em 3,21 ppm (Figura 19). A síntese da primeira ocorre somente no interior dos neurônios colinérgicos, enquanto as demais células utilizam a colina para sintetizar fosfatidilcolina, cuja concentração é a maior na membrana celular. Além da fosfatidilcolina (lecitinas), a colina está presente na membrana celular, em menor concentração, também na forma de fosfocolina e glicerofosfocolina e colina livre. (38, 42, 51) Figura 19. Fosfatidilcolina. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 600 MHz. (54) A Figura 20 mostra a biossíntese da fosfatidilcolina (PtdCho) a partir do citosol (cyt), passando pela membrana do retículo endoplasmático (ER), através de uma cascata de três etapas enzimáticas. Inicia-se na fosforilação da colina (Cho) pela colina-quinase (ck) em fosfocolina (PCho), em seguida tem-se a conversão da PCho em citidina-difosfato-colina (CDP-Cho) pela citidiltransferase (ct) que se incorpora à membrana do ER e, por fim, a formação da PtdCho mediada pela PCho-transferase (pct). (59) A elevação do pico da colina total na ERM do 1 H in vivo pode ser atribuída ao aumento da taxa de proliferação celular, da densidade celular em regiões com câncer e na alteração da composição da membrana celular. O aumento dos níveis deste metabólito é observado como sendo característico de uma série de neoplasias,
48 30 incluindo tumores de encéfalo (21, 33, 38, 43, 51, 52), próstata (40-42, 50), mama (39), suprarenal (10), dentre outros. Figura 20. Metabolismo da fosfatidilcolina (PtdCho). Legenda: fosfolipase A (pla), fosfolipase C (plc), fosfolipase D (pld), lisofosfolipase ou fosfolipase B (lpl), membrana (memb), lisofosfotidilcolina (Lyso- PtdCho), glicofosfocolina (GPC), glicerol-3-fosfato (G3P), fosfodiesterase (pd), acetilcoenzima A (AcylCoA), ácido fosfatídico (PA), diacilglicerol (DG), triacilglicerol (TG). (59) 2.7 Metabolismos da Creatina A creatina (Figura 21) ressona aproximadamente em 3.03 ppm e, geralmente, é encontrada na dieta usual, sendo que no homem é sintetizada no interior do fígado, rins e pâncreas. A creatina tem a função de reserva energética, sendo convertida em fosfocreatina pela enzima creatino-quinase, utilizando adenosina trifosfato (ATP). Quando a fosfocreatina cede o fósforo inorgânico no fornecimento energético, libera na corrente sanguínea a creatinina, excretada principalmente pelos rins. (43, 50)
49 31 Figura 21. Creatina. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54) Figura 22. Metabolismo da creatina. (60)
50 32 Três aminoácidos, glicina, arginina e metionina, estão diretamente envolvidos na biossíntese da creatina, como demonstrado na Figura 22. A primeira reação, que ocorre no rim, é aquela de transaminação da arginina para glicina, para formar o ácido guanidoacético (glicociamida). A síntese é completada pela metilação da glicociamida no fígado. Nesta ação, a metionina ativa é o doador de metila. (60) O pico da creatina contém contribuições da creatina fosfato, ácido - aminobutírico, lisina e glutationa, além da própria creatina. Por conta de sua estabilidade em muitos processos patológicos, ela pode ser usada como controle, com níveis de outros metabólitos expressados como uma razão com a creatina. 2.8 Metabolismos do Lactato Já o pico do lactato (Figura 23) é verificado em 1,32 ppm. Sua configuração espectral consiste em um pico que se divide em dois, denominado dubleto. Isto é causado pelo acoplamento J. (51) Figura 23. Lactato. a) Representação da estrutura química. b) Representação da estrutura química com os hidrogênios numerados. c) ERM 1 H in vitro em 500 MHz. (54)
51 33 Outra característica é que existe uma dificuldade de distinguí-lo das ressonâncias dos lipídios por conta da sobreposição dos picos, sejam os presentes no tecido estudado, sejam pelos que estão nas áreas adjacentes e contaminam o espectro. Vários protocolos são usados para distinguir o lactato do lipídeo, porém o mais simples é o uso do TE em torno de 140 ms, fazendo com que ele se apresente invertido (fora-de-fase) em relação aos outros metabólitos. (61) A formação de ácido láctico ou lactato (Figura 24) nos tecidos é chamada de acidose láctica. Normalmente, o ácido láctico é oxidado aos produtos finais dióxido de carbono (CO 2 ) e H 2 O através do ciclo de Krebs, ou ainda reconvertido à glicose no fígado pela gliconeogênese num processo denominado ciclo de Cori. A diminuição dos níveis de oxigênio (O 2 ) aumenta a produção de lactato e a diminuição de sua utilização energética. Figura 24. Via glicolítica demonstrando a espontaneidade da formação do piruvato (via aeróbia) e a formação do lactato tanto por via anaeróbica, quanto pela ação da lactato-desidrogenase que converte piruvato em lactato. Legenda:, -PO 3 2- ; P i, HO PO 3 2- ; Θ, inibição. (62)
52 34 Nas células tumorais, existe uma atividade elevada das enzimas hexoquinase, fosfofrutoquinase e piruvatoquinase, o que produz uma alta capacidade glicolítica em condições aeróbias. Comparadas com as células normais, as tumorais, usam praticamente toda sua capacidade de degradar a glicose, independente da quantidade de oxigênio presente. Porém, este consumo em condições anaeróbias pode ser até 20 vezes maior que na aerobiose. (63) Além disso, vários pesquisadores demonstraram que o lactato estimula a angiogênese. (64) 2.9 Metabolismos da Glutamina A regulação da glicólise pelo oxigênio nas células tumorais em condições de baixa concentração de glicose ou do seu polímero, o glicogênio, se dá através de vias alternativas envolvendo outros carboidratos notadamente a glutamina, num processo chamado de glutaminólise. (65) Com os baixos índices de glicose, os níveis de frutose-1,6-bifosfato, representado na Figura 24, estão muito diminuídos. Como resultado, ocorre a desativação da enzima piruvatoquinase, a não-conversão do piruvato e nenhuma ATP é sintetizada. Com isso, o pouco piruvato disponível para oxidação vem pelo ciclo do ácido tricarboxílico (ciclo de Krebs) ou pela fermentação do ácido lático. Por outro lado, a conversão da ATP produz o íon ortofosfato, que ativa a glutaminase para a conversão da glutamina. (63) Aparentemente nenhuma das duas vias é essencial à formação de neoplasias. Representam oportunidades estrategicamente favoráveis à sobrevivência e proliferação em circunstâncias de carência de nutrientes e oxigênio. Normalmente é aceito que neoplasias altamente malignas "cresçam" com pouca vascularização, portanto, altas taxas glicolíticas e glutaminolíticas suprem essa falta de vascularização, permitindo que o tumor sobreviva em áreas de hipóxia. (66) A glutaminólise (conversão da glutamina à lactato), a semelhança da glicólise, tem como principal função regenerar a energia, produzindo glutamato, citrato e aspartato, como mostrado na Figura 25. Tem, ainda, a vantagem de manter os níveis de glutamina constantemente altos nos tecidos e tumores sólidos. (65)
53 35 Figura 25. Glutaminólise. Interface com o ciclo de Krebs, com produção de lactato em condições de baixa concentração de glicose. (63) A ERM do 1 H in vivo não consegue separar a glutamina do glutamato, sendo comumente representado pelo somatório (Glx), considerando-se o pico entre 2,1 a 2,5 ppm. (12, 21, 35, 38, 43, 49, 51, 52, 54, 61) (35, 40-42, 50, 54) Já o citrato é encontrado em 2.60 ppm.
54 36 3 MÉTODO Este estudo foi aprovado pelo Comitê de ética em pesquisa da Universidade Federal de São Paulo/Hospital São Paulo e o termo de consentimento informado foi obtido de todos os pacientes ou de seus responsáveis. 3.1 Casuística Foram avaliados, por estudo prospectivo, 118 pacientes portadores de nódulos ou massas adrenais (36 homens e 82 mulheres), com média de idade de 57,3 ± 13,3 anos. Todos os pacientes foram previamente examinados por TC de adrenal com protocolo dedicado (medida de densidade na fase pré-contraste) e cálculo da velocidade de clareamento absoluto do contraste endovenoso ou por RM com sequências ponderadas em: T1 em-fase e fora-de-fase (para detecção de lípide intracelular), e em T2 e pós-contraste. Quarenta e cinco nódulos ou massas localizavam-se exclusivamente na glândula adrenal direita, e 53 na adrenal esquerda. Vinte pacientes apresentaram massas ou nódulos bilaterais, totalizando 138 nódulos. Todos os pacientes realizaram ressonância magnética com protocolo proposto de ERM 1 H. Os pacientes foram encaminhados para o Departamento de Diagnóstico por Imagem da UNIFESP pelos setores de Endocrinologia e Urologia. A coleta de dados do estudo ocorreu entre janeiro de 2007 e dezembro de Critérios de Inclusão Os pacientes foram selecionados de acordo com os seguintes critérios de inclusão: 1. Paciente com nódulo ou massa adrenal com diâmetro acima de 1,0 cm e exame prévio de TC ou RM com protocolo dedicado ao estudo da adrenal; 2. Confirmação histopatológica por biópsia ou cirurgia, nos casos de feocromocitoma, carcinoma, adenomas funcionantes ou lesões incaracterísticas; 3. Estabilidade da lesão por mais de 12 meses por TC ou RM em paciente com diagnóstico de adenoma.
55 Critérios de Não-inclusão Os critérios de não-inclusão para este estudo foram: 1. Pacientes incluídos em protocolos de quimioterapia ou com biópsia/cirurgia de adrenal prévia; 2. Pacientes em que não foi possível a programação da sequência ERM 1 H Critérios de Exclusão Alguns pacientes que foram selecionados acabaram excluídos por apresentarem: 1. Lesões com diâmetro acima de 1,0 cm e que não apresentaram pelo menos um voxel elegível para análise; 2. Pacientes com nódulo ou massa adrenal com diâmetro próximo de 1,0 cm e apresentaram contaminação nas curvas espectroscópicas. Desta forma, dos 20 pacientes com massas ou nódulos bilaterais, em seis apenas a lesão com maior diâmetro foi analisada e em outros dois, ambas foram excluídas. Dos pacientes com lesão unilateral, dois não foram incluídos, um por não ser colaborativo durante a realização do exame e o outro por apresentar um nódulo com diâmetro inferior a 1,0 cm. Cinco pacientes foram excluídos por portarem adenomas com diâmetro próximo a 1,0 cm, nos quais não foi possível a obtenção de nenhum voxel elegível para análise. Com isso, 109 pacientes preencheram todos os critérios do estudo para análise final (34 homens e 75 mulheres), com média de idade de 57,8 ± 13,1 anos, portadores de lesão adrenal maior do que 1,0 cm (média ± desvio-padrão: 3,67 ± 2,39 cm), perfazendo um total de 123 massas ou nódulos separados em quatro grupos (adenoma, carcinoma, feocromocitoma e metástase), demonstrados na Figura 26.
56 38 Figura 26. Diagrama de fluxo do estudo. 3.2 Protocolos de Exame Preparo e Posicionamento do Paciente O preparo do paciente para realizar o exame se resumiu ao jejum de quatro horas, aplicação de droga anti-espasmódica (Buscopan ) por via endovenosa 10 minutos antes do exame, e aplicação do questionário de contra-indicações à RM. O posicionamento do paciente foi feito com os pés primeiro em relação ao equipamento de RM, braços estendidos ao longo do corpo e em decúbito dorsal por sobre a bobina de coluna (SP - spine). Uma vez o paciente centrado na mesa de exame, pôs-se a bobina de arranjo-de-fase (phased-array) anterior (Figura 27) Técnica do Exame Protocolo de Aquisição de Imagens por RM
57 39 Os exames foram realizados em um equipamento de 1.5 T e gradiente de 43 mt/m (Magnetom Sonata; Siemens Medical Systems, Erlangen, Alemanha), no Departamento de Diagnóstico por Imagem da Escola Paulista de Medicina UNIFESP e em um equipamento de 1.5 T e gradiente de 33 mt/m (Magnetom Espree; Siemens Medical Systems, Erlangen, Alemanha), no Centro de Ultrassonografia e Radiologia Aplicada (CURA). O período de experiência (10) para aprendizado e desenvolvimento foi de agosto de 2004 a dezembro de 2006 para auxiliar na adequação do protocolo e sequências do exame. A bobina de RF de corpo, presente no próprio equipamento, foi usada para a excitação, e a bobina de arranjo-de-fase combinada com bobina de coluna foram usadas na recepção do sinal de RM, de acordo com a figura 27. Não houve necessidade de se conectar a monitorização respiratória. Figura 27 - Bobinas utilizadas na aquisição de imagens por RM e dos gráficos espectroscópicos na ERM. SP (spine) à esquerda e arranjo-de-fase (phased-array) à direita. (35) O exame de RM foi realizado no nível da massa adrenal e consistiu de sequências de tomada única metade-fourier turbo spin-eco (HASTE) ponderadas em T2 e imagens T1 CSI, em-fase e fora-de-fase. No Quadro 1, tem-se um resumo dos parâmetros físicos das sequências utilizadas nos dois serviços. As sequências HASTE foram realizadas nos três planos ortogonais para a localização tridimensional (3D) da massa para o planejamento da ERM 1 H. Para se determinar a inserção correta do volume de interesse (VDI), realizaram-se três sequências sagitais localizadoras HASTE, com as mesmas características de programação, em inspiração e expiração máximas, e em respiração livre. Deste modo, foram obtidos os intervalos de posição e mobilidade da glândula, do mais alto (expiração) ao mais baixo (inspiração) com a determinação da região em que se tem a possível localização do nódulo ou massa da adrenal durante a aquisição
58 40 da ERM 1 H em respiração livre. Assim, aumentou-se a probabilidade da glândula adrenal e a massa se localizassem neste intervalo. Quadro 1 - PARÂMETROS DAS SEQUÊNCIAS DE RM UTILIZADAS NO PROTOCOLO. Sequência N o de imagens Espessura (mm) TR (ms) TE (ms) Matriz CDV (mm) Axial T2 HASTE 24 3, x Axial T2 HASTE Fat Sat* 24 3, x Coronal T2 HASTE 20 3, x Sagital T2 HASTE Axial T1 CSI em-fase Axial T1 CSI fora-de-fase Axial VIBE T1 Gd** 13 3, x , ,8 167 x , ,4 167 x ,0 5,45 2, x * Fat Sat = Saturação de gordura. ** VIBE = Exame em apnéia com interpolação volumétrica Protocolo para captação dos dados espectroscópicos Utilizou-se um sistema de múltiplos volumes, na seleção do volume espectroscópico de interesse, adquirido pela seqüência PRESS CSI 2D híbrida disponível comercialmente pela Siemens Medical Systems (Erlangen, Alemanha), de forma a minimizar possíveis artefatos das estruturas peri-adrenais. A programação da ERM foi realizada com as imagens ponderadas em T2 HASTE em duas etapas. Na primeira, utilizaram-se apenas as imagens sagitais em inspiração máxima, expiração máxima e respiração livre, e posicionou-se cuidadosamente a grade multivoxel do volume de interesse no centro da lesão, com o uso de todos os três planos sagitais, de acordo com a Figura 28 para incluir o máximo
59 41 de área de lesão possível ou, preferencialmente, para incluir toda a lesão e parte do tecido gorduroso adjacente. Figura 28. Ajuste do posicionamento e tamanho do CDV e da área do shimming. Uma vez determinada as dimensões do CDV e da área de reforço da homogeneidade (shimming) (Figura 28), fez-se a segunda etapa da programação que contou com os três planos ortogonais em expiração. O objetivo deste procedimento foi determinar a espessura do voxel, habilitar apenas a bobina de RF mais próxima à massa ou nódulo e posicionar as barras de saturação externa, conforme a Figura 29. Figura 29. Programação final da ERM 1 H da adrenal. Além de ser angulada livremente, sem prejuízo na aquisição espectroscópica, a seqüência de ERM ofereceu a possibilidade de se utilizar seis barras de saturação externa, com 30 mm de espessura, posicionadas ao redor da glândula adrenal, minimizando os efeitos da não-homogeneização de campo pelo efeito de susceptibilidade magnética, originadas no ar do parênquima pulmonar, nas estruturas ósseas, na gordura peri-adrenal e nos líquidos presentes na árvore biliar e rins.
60 42 Para a espectroscopia de adrenal (Quadro 2) utilizou-se a supressão espectral da água fazendo com que os lipídeos presentes na glândula estivessem presentes na aquisição. Para isso, se aplicou pulsos de supressão espectral de água descrito como geração de frequência seletiva coerente (MEGA). (67) Quadro 2 - PARÂMETROS DA SEQÜÊNCIA DE ERM UTILIZADA NO PROTOCOLO Volume do Voxel (cm 3 ) CDV (cm) Excitações TR (ms) TE (ms) Fator Delta Tempo (min) , ,4 7:00-11:45 O tempo total de exame, incluindo o posicionamento do paciente, a aquisição de imagens de RM e dos dados espectroscópicos, ficou em torno de 30 minutos Análise dos dados espectroscópicos Os gráficos adquiridos foram analisados por dois examinadores (H.J.F.M. e S.M.G.) em consenso. O pós-processamento foi realizado numa estação de trabalho (LEONARDO ; Siemens Medical Systems) com um programa dedicado à análise da espectroscopia. Utilizou-se o filtro Gaussiano de 1000 Hz e priorizou-se a transformação de Fourier em duas direções espaciais, aplicando-se o filtro Hamming. Ajustou-se a matriz da ERM 1 H nos três planos ortogonais utilizados na programação, determinando-se então quais voxels seriam elegíveis para a análise. Um voxel foi considerado elegível quando possuía 100% de sua área no interior do tecido tumoral. Voxels localizados no tecido adiposo adjacente não foram incluídos nas análises espectrais. Convencionou-se a análise espectral com início cranial e sentido caudal e da esquerda para a direita. Uma vez selecionado o voxel para a análise, ampliou-se o eixo das abscissas a fim de se usar uma amplitude de ppm suficiente (0,5 a 8,5) para a realização da correção da fase do pico da água com os demais metabólitos. Em seguida, reduziu-se o intervalo de ppm (0,5 a 4,7) com o objetivo de aumentar a resolução espectral. Em ambas oportunidades a análise da espectroscopia foi interpretada por inspeção visual e pelo cálculo das amplitudes dos picos dos metabólitos de interesse,
61 43 lipídeo (Lip), colina (Cho), creatina (Cr) e catecolaminas (4,0 4,3 ppm) (54). Procedeuse também a anotação e quantificação de outros picos significativamente distintos dos primeiros. Quando esta redução de faixa de ppm não era suficiente para mensurar a Cho e/ou a Cr, reduziu-se ainda mais o intervalo de 2,5 a 3,5 ppm para que esta diferenciação e quantificação pudessem ser feitas, exemplificadas pela Figura 30. O tempo de análise para cada paciente variou de acordo com o número de voxels elegíveis, variando de 10 minutos nas lesões menores a 50 minutos no caso das massas de grandes dimensões. Figura 30. Alteração d e escala no pós-processamento da ERM 1 H da adrenal. (A) de 0,5 ppm a 8,5 ppm; (B) de 0,5 ppm a 4,7 ppm; (C) de 2,5 ppm a 3,5 ppm Análise dos Metabólitos Uma vez mensuradas as amplitudes dos metabólitos de interesse, calculou-se as seguintes relações metabólicas: Cho/Cr, ppm/Cr, Lip/Cr e Cho/Lip. Levou-se em consideração para diferenciar as massas ou nódulos apenas as duas primeiras relações que se mostraram, desde o primeiro trabalho (10), como as de maior sensibilidade e especificidade na diferenciação entre adenomas, carcinomas, feocromocitomas e metástases. Num primeiro momento, foi verificada a reprodutibilidade dos resultados com o nosso trabalho anterior. No sentido de se utilizar outros metabólitos para o estudo espectroscópico da glândula adrenal, trabalhou-se também com a glutamina e glutamato (Glx) e com o
62 44 lactato (Lac). Tomadas as amplitudes destes metabólitos, fez-se a relação matemática com a creatina (Glx/Cr e Lac/Cr). Os picos dos lipídeos mensuráveis foram também analisados e caracterizados. Procurou-se também determinar os de maior amplitude nos gráficos espectrais e foram comparados de acordo com os grupos constituídos. Consideramos o cortisol entre 1,40 ppm e 1,70 ppm, o DHEA-S entre 1,22 e 1,33 ppm; a aldosterona entre 1,15 e 1,21 ppm; e a androstenodiona entre 0,75 e 1,14 ppm Análise estatística A amostra foi estudada utilizando-se os programas Excel e BioEstat 4.0 para melhor caracterizar as relações metabólicas das massas ou nódulos nos quatro grupos em análise (adenoma, carcinoma, feocromocitoma e metástase). Para isso, os valores de tendência central (média e moda) e de dispersão (desvio padrão e amplitude) foram calculados para cada um dos grupos. Aplicou-se também o teste t de Student para amostras pareadas, comparando-se as médias das razões metabólicas nos diferentes grupos, e o Qui-quadrado, para correlacionar as diferenças entre as relações, com a correção de Yates ou o teste exato de Fisher quando o valor da caséola fosse menor que cinco. Fez-se ainda a curva da característica operativa do receptor (ROC) para se determinar o ponto de corte da relação em que as massas ou nódulos apresentaram diferenças entre os grupos e avaliou-se o poder de análise das tabelas. A sensibilidade, especificidade, valor preditivo positivo (VPP) e acurácia foram calculados a partir dos pontos de corte determinados. A significância dos testes foi indicada para o valor menor que 0,05 (p 0,05). Estudou-se ainda a significância entre a razão Glx/Cr e o tamanho da massa ou nódulo, utilizando-se o teste de correlação linear de Pearson (ρ) para medir o grau de associação entre essas variáveis.
63 45 4 RESULTADOS A partir das sequências propostas e metodologia de leitura, conseguimos realizar o exame em 123 (89,13%) das massas ou nódulos estudados. Das lesões excluídas, 10 (7,25%) correspondiam a lesões com maior diâmetro inferior a 1,0 cm. O restante (cinco nódulos 3,62%) foi retirado do estudo por não possuir o voxel elegível, mesmo com tamanho do nódulo acima do pré-estabelecido. Mesmo assim, das 123 massas ou nódulos incluídos neste estudo, 32 (25,2%) apresentaram tamanho entre 1,0 e 1,9 cm (média de 1,64 ± 0,27 cm), acordo com a Figura 31. Figura 31. Gráfico de barras relacionando o número de massas ou nódulos (N) versus tamanho da lesão. (Lengenda: D=Diâmetro) A Tabela 1 mostra que foi possível a reprodução dos resultados obtidos no trabalho anterior (10) utilizando-se a relação Cho/Cr 1,2 para diferenciar adenoma e feocromocitoma de carcinoma e metástase, com sensibilidade de 100%, especificidade de 98,2%, valor preditivo positivo (VPP) de 83,3% e acurácia de 98,4% com um poder de análise de 0,9872; e a relação ppm/cr 1,5 para diferenciar carcinoma e feocromocitoma do adenoma e metástase, com sensibilidade de 92,3%, especificidade de 96,9%, VPP de 89,3% e acurácia de 95,93% com um poder de análise de 0,7843. A Figura 32 mostra o comportamento espectroscópico das massas estudadas.
64 46 Tabela 1 ANÁLISE DESCRITIVA DOS GRUPOS ESTUDADOS PARA AS RELAÇÕES Cho/Cr E ppm/Cr Cho/Cr ppm/cr Grupo Média ± DP Mín-Máx Média ± DP Mín-Máx Adenoma 0,09 ± 0,12 0 0,67 0,60 ± 0,50 0 1,45 Feocromocitoma 0,78 ± 0,34 0 1,17 6,36 ± 8,86 1,5 34,55 Carcinoma 1,72 ± 0,40 1,25 2,35 4,28 ± 1,98 1,69 7,98 Metástase 1,42 ± 0,21 1,28 1,67 0,92 ± 0,32 0,57 1,22 Legenda: DP = Desvio padrão; Mín = Valor Mínimo; Máx = Valor Máximo. p < 0,01 Figura 32. Gráficos espectroscópicos da adrenal em quatro diferentes massas. (A) Metástase; (B) Feocromocitoma; (C) Adenoma; (D) Carcinoma. Os respectivos picos de Cho, Cr, Lip, Glx e H 2 O estão assinalados em suas respectivas curvas.
65 47 Incluímos também em nossa avaliação os metabólitos Glx e Lac uma vez que percebemos a presença dos seus picos na grande maioria das massas analisadas. A avaliação dos mesmos também foi feita por meio da relação com a Cr. Para as relações Glx/Cr e Lac/Cr, os grupos se comportaram de acordo com a Tabela 2. Tabela 2 ANÁLISE DESCRITIVA DOS GRUPOS ESTUDADOS PARA AS RELAÇÕES Glx/Cr E Lac/Cr Glx/Cr Lac/Cr Grupo Média ± DP Mín-Máx Média ± DP Mín-Máx Adenoma 1,99 ± 1,67 0,0 8,75-4,61 ± 7,77-38,84 0,0 Feocromocitoma 1,41 ± 0,80 0,17 3,0-2,64 ± 3,24-10,02 0,0 Carcinoma 2,49 ± 2,12 0,56 7,65-12,43 ± 7,31-21, ,63 Metástase 2,13 ± 2,05 0,0 4,1-2,43 ± 4,22-7,31 0,0 Legenda: DP = Desvio padrão; Mín = Valor Mínimo; Máx = Valor Máximo. Não houve diferença estatisticamente significante (p>0,05) da relação Glx/Cr entre as massas analisadas. Porém, para a diferenciação específica entre feocromocitoma e carcinoma e entre feocromocitoma e adenoma (Figura 33), a relação Lac/Cr se mostrou estatisticamente significante (p<0,05). Figura 33. Gráficos espectroscópicos da adrenal em três diferentes massas evidenciando os respectivos picos de Cho, Cr, Lip, Glx, Lac e H 2 O que estão assinalados nas curvas. (A) Feocromocitoma; (B) Carcinoma; e (C) Adenoma.
66 48 A curva ROC calculada para a diferenciação entre o grupo feocromocitoma e adenoma demonstrada na Figura 34A determinou um ponto de corte de -4,79, com sensibilidade de 65,3%, especificidade de 72,7%, VPP 91,44%, acurácia de 66,65% e poder de análise de 0,67. Já a curva ROC para diferenciação entre o grupo feocromocitoma e carcinoma (Figura 34B) determinou um ponto de corte de -7,449, com sensibilidade de 90,9%, especificidade de 77,8%, VPP 83,35%, acurácia de 85,01% e poder de análise de 0,93. A B Figura 34. Curva ROC da relação Lac/Cr entre os grupos adenoma (A) e carcinoma (B) com o feocromocitoma. A. Lac/Cr -4,79 (adenoma). B. Lac/Cr -7,449 (carcinoma). Percebemos durante a análise que o Glx está associado ao tamanho da massa, sendo diretamente proporcional ao tamanho do adenoma e carcinoma e inversamente proporcional ao feocromocitoma. Não foi possível esta associação com metástases devido ao número reduzido da amostra e semelhança de dimensões. Os gráficos de dispersão abaixo (Figura 35) especificam este achado. Aplicou-se o teste ρ para medir a intensidade de associação entre a relação Glx/Cr e o tamanho da massa ou nódulo. Obteve-se ρ de 0,17; 0,28; e -0,28 (p>0,05) para os grupos adenoma, carcinoma e feocromocitoma, respectivamente. Existem diferentes picos de lípides detectáveis nas massas adrenais. Tentamos identificar e caracterizar se existem picos de lípides que permitam diferenciar as massas. A Figura 36 mostra os lipídeos encontrados nas massas.
67 49 Figura 35. Gráficos de dispersão com regressão linear do comportamento entre o tamanho da massa e a relação Glx/Cr. Adenoma (IC 95% = -1,35 a 0,43), no feocromocitoma (IC 95% = -4,83 a - 0,69) e no carcinoma (IC 95% = a -0.87). Para o adenoma encontramos 52,2% de cortisol; 22,3% de DHEA-S; 7,5% de aldosterona e 18% de androstenodiona. Para o feocromocitoma encontramos 41,8% de cortisol; 19,4% de DHEA-S; 7,8% de aldosterona e 31% de androstenodiona. Para o carcinoma encontramos 41,5% de cortisol; 18,8% de DHEA-S; 18,2% de aldosterona e 21,5% de androstenodiona. Já para a metástase encontramos 57,5% de cortisol; 12,3% de DHEA-S; 13,7% de aldosterona e 16,5% de androstenodiona. Figura 36. Lipídeos presentes nos nódulos ou massas adrenais estudados. Androstenodiona (0,75 1,14 ppm); Aldosterona (1,15 1,21 ppm); DHEA-S (1,22 1,33 ppm); e Cortisol (1,40 1,70 ppm).
68 50 A Tabela 3 descreve as principais características dos lipídeos encontrados em maior concentração nos grupos estudados. Verificou-se que existe uma diferença estatisticamente significante (p<0,05) entre o tipo de lipídeo, caracterizado por sua posição na abscissa, presente no adenoma em relação aos outros grupos. Determinou-se um ponto de corte através da curva ROC (Figura 37) de 1,397 ppm, com sensibilidade de 67,3%, especificidade de 52,7%, VPP de 79,29%, acurácia de 63,34% e poder de análise de 0,88. Tabela 3 ANÁLISE DESCRITIVA DOS LIPÍDEOS NOS GRUPOS ESTUDADOS Lipídeo (ppm) Grupo Média ± DP Mín-Máx Moda Adenoma 1,49 ± 0,19 0,98 2,04 1,6 Feocromocitoma 1,39 ± 0,21 0,7 1,79 1,39 Carcinoma 1,39 ± 0,26 0,75-1,89 1,16 Metástase 1,29 ± 0,17 0,97 1,54 1,24 Legenda: DP = Desvio padrão; Mín = Valor Mínimo; Máx = Valor Máximo. Figura 37. Curva ROC para determinação do ponto de corte do lipídeo de maior amplitude nas massas ou nódulos de adrenal. Lipídeo 1,397 ppm (adenoma).
69 51 DISCUSSÃO A utilização de técnicas de ERM de alta sensibilidade e resolução espacial se faz necessária por conta da localização profunda das glândulas adrenais, da complexidade de sua anatomia e fisiologia zonal, proximidade de regiões que apresentam efeito significativo de susceptibilidade magnética e da natureza heterogênea dos nódulos e massas que as acometem. Para que o estudo espectroscópico in vivo alcance a sensibilidade adequada com o tempo de aquisição clinicamente aceitável e distribuição dos sinais dos diferentes tecidos de modo resoluto, faz-se necessário um campo magnético estático de pelo menos 1,5 T. (68) Esta condição é relevante porque a polarização ou a intensidade do vetor depende diretamente do B 0 aplicado externamente. (12) As bobinas de gradiente são também incorporadas para produzir campos magnéticos que variam linearmente através da amostra. Com isso, é possível utilizar uma (1D), duas (2D) ou três (3D) dimensões do gradiente de codificação de fase na obtenção do espectro. (51) Para este estudo usou-se uma sequência espectroscópica 2D aliando resolução espacial adequada com um tempo de aquisição clinicamente viável, cerca de 7 minutos para lesões grandes e de aproximadamente 12 minutos para lesões pequenas. Para corrigir a distribuição do campo magnético através da amostra adequadamente, utilizaram-se estratégias chamadas de reforço passivo e ativo. Graças às bobinas de reforço (shimming), principalmente o ativo, obteve-se mais segurança nas medidas espectrais, pois o campo magnético produzido foi o mais uniforme possível dentro do volume de interesse (VDI), reduzindo o tempo de aquisição. (69) A função primária do sistema de RF é a de transmitir pulsos e receber o sinal de RM. Este sistema é também desenhado para potencializar o baixo sinal intrínseco de RM, pois enquanto a voltagem de saída da transmissão é da ordem de 10 6 V, a voltagem de entrada da bobina receptora é da 0,1 µv. Com isso, a escolha das bobinas é muito importante e é influenciada pela questão clínica, área de interesse, peso e tamanho do corpo do paciente. (12) Os avanços técnicos na aquisição de imagens por RM do abdome passaram pelo desenvolvimento da bobina de RF de arranjo-de-fase ou bobinas receptoras
70 52 múltiplas (phased-array), seja na utilização de bobinas únicas, mas com elementos anteriores e posteriores ao paciente, seja pelo uso de bobinas diferentes, os quais podem se combinar ou serem usadas individualmente. A interface da bobina de arranjo-de-fase inclui várias portas de entrada e saída de sinal. Cada uma das portas de saída está associada com um receptor ligado ao sistema de imagem por RM. A interface elétrica acopla seletivamente pelo menos duas entradas de sinal em relação a um grande número de conexões de entrada. (70) Com isso, esta bobina oferece uma RSR, sensibilidade uniforme e resolução espacial de uma bobina de superfície, porém com aumento do CDV. Esta característica normalmente é utilizada para o imageamento do abdome sem aumento do tempo de aquisição. Pode ser aplicada não só para a produção de imagens como também na aquisição dos gráficos espectroscópicos, sem restrição quanto ao tipo de sequência de pulso a ser aplicada. Além disso, o aspecto mais importante das propriedades da bobina arranjo-defase é a de minimizar o artefato de acoplamento mútuo entre bobinas de superfície muito próximas. Isto causa a separação das frequências de ressonância e interrompe o padrão de transmissão e recepção do sinal. (71) Logo depois da introdução das bobinas arranjo-de-fase, foi reconhecido que elas poderiam também ser usadas para reduzir ainda mais o tempo de aquisição das imagens pela amostragem do sinal de RM de modo paralelo. A base dessa técnica está no conceito de que o tempo de aquisição é proporcional ao número de linhas de codificação de fase numa abordagem Cartesiana. Na imagem de RM em paralelo, o uso das antenas de arranjo-de-fase é importante para diminuir ou prevenir artefatos de dobramento. (72) As técnicas de imageamento parcial em paralelo em aquisição simultânea com a harmônica espacial (SMASH) vêm sendo combinada com protocolos de imagem em tomada única (single shot) como aquisições ecoplanares, de ruptura e tomada única metade-fourier turbo spin eco (HASTE ou RARE). Esta última, usada neste estudo, caracteriza-se por ser uma sequência de RM ponderada em T2 ultra-rápida que em adquire mais da metade de uma imagem 2D no Espaço K depois de um único pulso de excitação por meio de um trem de eco separado por pulsos de refocalização. Esta sequência é menos sensível ao movimento e pode ser adquirida em apnéia. (73)
71 53 O método PRESS foi utilizado para a localização espectroscópica deste estudo. Esse método excita diretamente o volume de interesse com mínima excitação do restante da amostra. A codificação do volume, seja ele único ou múltiplo, pode ser obtida por uma única seqüência de pulso, com três pulsos seletivos, cada qual ao longo das direções x, y e z, para obter a localização. A metodologia PRESS pode ser precedida pelos pulsos de desvio químico seletivo (CHESS) e o protocolo de BASING para que se obtenha a supressão da água. A supressão realizada pelas barras de saturação externas também podem ser programadas antes da aquisição espectroscópica. (12, 35) Pelo método de supressão espectral, a magnetização transversa é seletivamente retirada de fase antes e depois do segundo pulso de spin-eco. A retirada de fase afeta a água somente entre 4.0 a 5.4 (12, 35) ppm. Adicionalmente ao PRESS, utilizou-se para este experimento o método de localização CSI adquirido de forma multidimensional. A aquisição de dados é realizada na ausência do gradiente de codificação de frequência, com isso a informação do desvio químico pode ser conservada. É classificada em seqüência com spin eco e sem spin eco. A vantagem do método com eco, aplicado neste estudo, é a movimentação com a aquisição dos dados, ligando os gradientes, e permitindo que todas as ressonâncias entrem em fase na codificação de fase. Dentre os problemas da CSI tem-se a interferência da intensidade do pico para espécies de tempo T2 curto e a necessidade de um grande número de codificações para se obter um simples volume. Contudo, é excelente para se obter mapas metabólicos. (12, 35) Os primeiros estudos de ERM do 1 H in vivo da glândula adrenal foram realizados utilizando imagens espectroscópicas, como forma de seleção da região de interesse espectroscópico. Apesar dos primeiros resultados terem sido satisfatórios, algumas limitações desta metodologia precisam ser destacadas: a impossibilidade de se construir os gráficos espectrais, a visualização da massa ou nódulo em apenas um plano ortogonal, o baixo valor de B 0, e restrição em se visualizar apenas a água e a gordura. (22) Kim et al. em 2009 propuseram o uso da ERM do 1 H in vivo single-voxel com monitoração respiratória para o estudo da glândula supra-renal. Mesmo com os
72 54 primeiros resultados animadores, os problemas em se usar a localização single-voxel permanecem, quer seja na inabilidade de acesso da distribuição espacial das alterações metabólicas observadas; na dificuldade de comparação dos níveis metabólicos entre duas regiões diferentes; no posicionamento do volume que deve ser realizado no momento do exame, baseando-se nas imagens da RM, na qual a região de interesse pode ser difícil de localizar; e, ainda, limitando-se a massas relativamente grandes (8cm 3 27cm 3 ) e TE curto. (11) Com o objetivo de superar estas limitações, começou-se a utilizar o volume múltiplo 2D, como forma de seleção da região de interesse espectroscópico, com a ativação de dois gradientes, a partir do plano sagital da glândula supra-renal. (10) A aquisição de volumes múltiplos nega a necessidade de se saber a exata localização do câncer, fornecendo informações espectrais sobre a sua extensão espacial e heterogeneidade metabólica. (42) Em nosso estudo houve a necessidade de realizar algumas modificações nas etapas de aquisição e pós-processamento do protocolo da ERM do 1 H da adrenal quando comparadas com as fases iniciais do projeto. (10) Além da bi dimensionalidade da sequência de pulso espectral, a não angulação do multi-voxel, a melhoria do ajuste do CDV à massa ou nódulo e o equilíbrio da RSR após este ajuste são itens de grande impacto nesta otimização. Mantivemos a aquisição de três planos sagitais (respiração livre, inspiração máxima e expiração máxima) para determinar o local mais provável da lesão estar situada, restringindo o shimming nesta região. Este método não é perfeito, mas compensa a falta de monitoramento respiratório na sequência multivoxel. No que se refere ao pós-processamento, as alterações protocolares evoluíram juntamente com os novos aplicativos disponibilizados pela Siemens Medical Systems que possibilitaram uma melhor análise dos dados espectroscópicos. O pósprocessamento com escalas diferentes de uma amplitude maior (0,5 a 8,5 ppm) para uma menor (0,5 a 4,7 ppm) permitiu um melhor ajuste da linha de base levando-se em consideração o pico da água com os demais metabólitos na determinação automática e manual da fase e da frequência do espectro. Nos casos em que havia necessidade, estreitou-se ainda mais o eixo x (2,5 a 3,5 ppm) no sentido de se evidenciar melhor amplificando os picos da colina e da creatina e o volume do voxel foi aumentado ou
73 55 diminuído de acordo com o tamanho da massa. Tudo isso fez com que a determinação do voxel elegível fosse realizada com mais segurança e rapidez. Mesmo com o impacto positivo dado por estas alterações, os critérios matemáticos determinados em nosso trabalho anterior se mantiveram satisfatórios na determinação de adenomas, carcinomas, feocromocitomas e metástases. Desta forma, a amostra atual mostrou uma sensibilidade de 100%, especificidade de 98,2%, VPP de 83,3% e acurácia de 98,4% para a relação Cho/Cr 1,20 para diferenciação do carcinoma e metástase do adenoma e feocromocitoma. Anteriormente, em nosso primeiro trabalho, havíamos obtido 92%, 96%, 86% e 95%, respectivamente. Enquanto que para a relação 4,0-4,3 ppm/cr 1,50 obteve-se uma sensibilidade de 92,3%, especificidade de 96,9%, VPP de 89,3% e acurácia de 95,93% para diferenciar carcinoma e feocromocitoma do adenoma e metástase contra 87%, 98%, 98% e 95% do primeiro trabalho, respectivamente. Na nossa análise percebemos a frequente presença dos picos de Glx e Lac. Decidimos, à semelhança do que foi feito para os outros metabólitos, incluí-los na nossa análise sob a forma de relação com a Cr. A relação Glx/Cr não apresentou diferença estatisticamente significante na diferenciação das massas ou nódulos, mas mostrou que está relacionada com o tamanho da lesão, diretamente proporcional ao adenoma e carcinoma e inversamente proporcional ao feocromocitoma. Talvez em um futuro próximo possamos estabelecer um valor para esta relação e com uma correlação ρ de moderada a forte. Já para a relação Lac/Cr, obteve-se uma diferença estatisticamente significante quando foi comparado o grupo do feocromocitoma com os grupos adenoma e carcinoma. A curva ROC mostrou que esta razão metabólica quando acima de -7,449 possui sensibilidade de 90,9%, especificidade de 77,8%, VPP 83,35%, acurácia de 85,01% para separar carcinomas de feocromocitomas, que representava uma das maiores dificuldades em relação ao estudo anterior, portanto somando-se esta nova relação aumentamos a capacidade de diagnóstico e diferenciação. Este estudo também procurou caracterizar os tipos de lipídeos presentes nos grupos e qual deles possuía maior concentração. Verificamos quatro componentes
74 56 presentes nos quatro grupos estudados em quantidades mensuráveis à ERM do 1 H (androstenodiona, aldosterona, DHEA-S e cortisol). Notamos também que o cortisol é o metabólito mais frequente dentre todos os outros em seus respectivos grupos, já que acima de 41,5% dos lípides presentes nas massas ou nódulos de adrenal estão entre 1,40 e 1,70 ppm. Quando comparamos os lipídeos de maior amplitude presentes na curva espectral verificamos que existe uma diferença estatisticamente significante do adenoma em relação aos outros grupos. Porém, este dado não se mostrou eficiente suficiente para servir como critério de análise espectroscópica na diferenciação das massas. Em nossos estudos paralelos estamos tentando comparar as concentrações dos lipídeos obtidas nos gráficos espectrais com provas laboratoriais e desta forma diferenciar massas de adrenal funcionantes de não-funcionantes.
75 57 6 CONCLUSÃO A partir da sequência de ERM do 1 H apresentado foi possível estabelecer um protocolo eficaz para a diferenciação dos nódulos e massas das glândulas adrenais. Este protocolo de aquisição de imagem e ERM permitiram a realização do exame em 123 (89,13%) das massas com lesão superior a 1,0 cm. A sistemática de pós-processamento foi eficaz na diferenciação dos nódulos.
76 58 7 ANEXOS Anexo 1 Quadro de identificação dos pacientes por grupo Carcinoma NOME IDADE SEXO TAMANHO (cm) Cho/Cr ppm/Cr Lac/Cr Glx/Cr DIAGNÓSTICO APP 17 M 7,33 1,3438 7,983-0,6305 2,9054 AFS 13 F 5,46 2,3556 3, ,8961 1,6677 FAS 52 M 8,48 1,7179 5, ,3829 7,6488 FAS 52 M 3,55 1,2464 3,9022-9,1603 1,729 GAJ 59 M 10,85 1,4652 2, ,8019 2,2319 LMGL 49 F 6,31 1,7728 5, ,6071 0,5672 MAF 40 F 6,99 2,191 1,6999-9,3085 1,1662 MHFG 73 F 1,53 2,0629 3,0263-4,2454 1,1979 SDG 49 M 1,9 1,3499 4, ,8167 3,3581 Adenocarcinoma Adenocarcinoma Adenocarcinoma Adenocarcinoma Adenocarcinoma Adenocarcinoma Adenocarcinoma Adenocarcinoma Feocromocitoma Metástase NOME IDADE SEXO TAMANHO (cm) Cho/Cr ppm/Cr Lac/Cr Glx/Cr DIAGNÓSTICO LFCB 68 M 3,07 1,3066 0,5757 0,0 4,1003 Metástase PVN 75 M 2,75 1,2829 0,9555-7,3092 2,3036 Metástase RI 57 F 14,35 1,6667 1,2222 0,0 0,0 Adenoma Feocromocitoma NOME IDADE SEXO TAMANHO (cm) Cho/Cr ppm/Cr Lac/Cr Glx/Cr DIAGNÓSTICO AB 41 M 1,69 0,0 1,5 0,0 2,7604 Feocromocitoma AFF 73 M 9,61 1,0872 8,1402-2,0949 0,1679 Feocromocitoma CMS 29 F 7,51 1,1756 1,6835-0,9485 0,78665 Feocromocitoma EMG 55 F 2,25 1,1406 4,3185-2,2244 3,0058 Adenoma EGV 47 F 2,31 0,9935 1,5467 0,0 8,7752 Feocromocitoma EMES 61 F 3,18 0,75 3,2917 0,0 1,7292 Adenoma FZC 42 M 9,01 0,9106 7,6775-6,5742 1,1079 Feocromocitoma IMJ 63 F 8,73 0,7524 2, ,0245 2,1019 Feocromocitoma
77 59 JG 54 M 4,49 0,8846 1,94-0,9167 1,5666 Feocromocitoma JG 54 M 7,44 1,1035 1,6325-0,2222 1,0736 Feocromocitoma JS 21 F 4,42 1,0713 2,9426-3,4083 0,4528 Feocromocitoma MAB 62 F 7,1 0, ,9166-7,4490 1,0912 Feocromocitoma MAT 52 F 2,64 0,8822 1,9874-0,5183 1,5984 Feocromocitoma MOM 53 F 6,85 0, ,5506-3,5115 1,2513 Feocromocitoma MMF 70 F 2,1 0,5 23,3667 0,0 1,1667 Feocromocitoma NC 60 F 1,59 0,9259 2,0555-4,6111 0,4444 Feocromocitoma PCCF 2,39 0,9357 1,5478 0,0 0,4979 Feocromocitoma PCCF 30 F 3,54 0,7133 2,4909 0,0 7,5729 Feocromocitoma RMN 63 M 6,92 0,6296 2,4799 0,0 0,7109 Adenoma Adenoma NOME IDADE SEXO TAMANHO (cm) Cho/Cr ppm/Cr Lac/Cr Glx/Cr DIAGNÓSTICO AMC 70 F 2,39 1,0 0,6333 0,0 0,7 Adenoma AMC 73 F 2,17 0,8363 0,0 0,0 0,3409 Adenoma AA 79 F 2,88 0,8417 0,8917 0,0 0,0 Adenoma AA 79 F 1,53 1,0 0,8333 0,0 2,8333 Adenoma AFS 73 F 2,45 1,125 1,4583-1,0 0,9375 Feocromocitoma ASA 49 F 2,78 1,0184 1,0632 0,0 1,1756 Adenoma ASA 49 F 5,3 0,0 0,0-3, ,4786 Adenoma MAS 70 M 1,63 0,0 0,0 0,0 2,1042 Adenoma AGL 63 M 5,54 0,7475 1,4015-4,7899 1,5229 Hiperplasia congênita AGL 64 F 5,02 1,1511 1,3898-2,3408 1,4970 Hiperplasia congênita ASM 69 F 2,47 1,1146 1,0 0,0 2,6116 Adenoma BL 69 F 2,31 1,0769 1,0 0,0 2,4722 Adenoma CPBL 45 F 1,98 0,7685 0, ,0417 1,2062 Adenoma CM 61 M 1,78 0,0 0,0 0,0 1,3701 Adenoma CM 61 M 2,01 0,0 0,0 0,0 2,1 Adenoma CPS 54 M 3,18 0,4396 0,0-1,2418 1,8485 Adenoma CRS 67 F 1,43 1,0 0,75 0,0 1,375 Adenoma
78 60 CCS 64 F 3,98 0,9797 1,142-8,2265 2,5516 Adenoma CPZ 57 F 1,99 1,125 0,475-8,0 4,56 Adenoma DMLM 56 F 1,19 0,9167 0,0 0,0 1,5333 Adenoma DS 48 F 6,92 1,2 0,9-2,5667 7,3444 Adenoma SEM 47 F 6,16 1, , ,8441 3,2122 Adenoma EMI 50 F 1,49 0,0 0,0 0,0 2,2738 Mielolipoma EBBS 47 F 5,37 0,9645 0,9818-8,3916 2,6416 Adenoma EPS 61 F 2,47 1,0 1,0 0,0 4,6 Adenoma EFM 62 F 2,87 0,351 0,0-4,7954 1,7121 Adenoma EGB 58 F 3,19 0,8917 0,0 0,0 3,5234 Hiperplasia bilateral EGB 58 F 1,68 0,7738 0,0 0,0 1,9712 Hiperplasia bilateral ENS 57 F 2,8 1,0 1,0-18,9567 4,5317 Adenoma SEM 50 F 1,87 0,9148 1,1071-6,2645 0,5857 Adenoma EVS 66 M 3,22 0,9383 0,6333 0,0 2,8974 Adenoma FEO 64 F 1,24 0,9524 0,9524 0,0 0,4286 Adenoma FMC 87 F 1,93 0,0 0,0 0,0 1,9167 Adenoma FCVF 62 M 2,65 0,3461 0,459-2,6051 2,3243 Adenoma FCVF 62 M 1,19 1,0444 0, ,0937 3,4284 Adenoma FSB 70 M 3 0,7197 0,8258-1,5818 0,4848 Adenoma GFS 60 F 3,18 1,0867 0,3-0,7333 5,3833 Adenoma GC 71 M 5,52 0,7835 0, ,238 1,3256 Adenoma IDPF 72 F 2,75 0,9762 0,5714-7,7857 2,2619 Adenoma ICFB 53 F 2,65 1,0972 0,75-7,4167 1,4028 Hamartoma JNP 72 M 1,89 0,1 0,0 0,0 2,205 Cisto JHS 60 M 2,36 0,9487 0,875-0,225 1,395 Adenoma JP 52 M 5,15 1,0079 1,0762-3,8329 0,8182 Adenoma JOS 80 M 1,31 0,8889 0,0-34 3,6667 Adenoma JM 49 F 2,12 0,3059 1, ,9119 1,1083 Adenoma LAVM 71 F 3,46 0,9927 0,0-2,7917 6,4551 Adenoma LFBN 51 F 1,99 0,5 0,0 0,0 1,75 Adenoma LCS 47 F 3,34 0,3945 0,0 0,0 0,0 Adenoma
79 61 LMM 44 F 3,37 0,9995 0,6111 0,0 2,5962 Hiperplasia bilateral LMM 44 F 1,12 0,8958 0,0-1,9167 1,7917 Hiperplasia bilateral LMM 45 F 1,5 0,8587 0,5982 0,0 1,005 Hiperplasia bilateral LMM 45 F 3,25 1,0885 0,3784-5,5732 1,6189 Hiperplasia bilateral LBF 78 F 2,56 0,8229 1,2083-1,6667 1,7153 Hiperplasia bilateral LBF 78 F 1,7 0,0909 0,0606 0,0 1,0 Hiperplasia bilateral LBF 79 F 2,61 0,0 0,0 0,0 1,7291 Histoplasmose LAM 76 M 5,99 1,0575 1, ,2899 2,7439 Histoplasmose LAM 76 M 6,1 0,9283 1,2863-6,8331 0,4646 Adenoma MAM 62 F 2,09 0,9035 0,0 0,0 4,3158 Adenoma MPS 55 M 2,04 0,9286 1,0 0,0 1,0357 Adenoma MPS 55 M 1,93 1,0 0,0-7,8889 1,2222 Adenoma MRGZ 48 F 2,54 1,0 1,0-15,3889 1,9507 Adenoma MRGZ 48 F 3,35 0,995 1,0121-4,8 1,5798 Adenoma MAFM 45 F 1,96 1,0746 0,7714 0,0 1,6333 Adenoma MCPS 59 F 2,19 0,8424 0, ,5714 1,2381 Adenoma MCSM 57 F 1,81 1,0543 0,0-5,9566 1,4235 Adenoma MCPM 55 F 11,48 0,9264 1,332-5,9758 0,0 Adenoma MGA 75 F 1,82 0,8571 1,0 0,0 1,7857 Adenoma MHS 60 F 2,86 0,2430 1, ,6133 1,6081 Adenoma MHS 60 F 2,93 0,2 0,0-13,7 8,75 Adenoma MLSS 56 F 3,41 0,9928 0,9059 0,0 2,7667 Adenoma MLSS 58 F 3,57 1,0127 0,7324-6,0889 1,1544 Adenoma MNRB 56 F 3,93 1,0574 1,2558 0,0 1,0026 Adenoma MTSR 38 F 7,02 1,034 1,2731 0,0 1,6795 Adenoma MAA 42 F 2,74 0,9687 1,0-4,1646 4,4687 Adenoma MCA 66 M 1,47 1,1151 0,0-1,3056 0,0 Adenoma MCA 66 M 3,61 0,0 0,0 0,0 2,0617 Adenoma NGF 45 F 2,33 0,2631 0,3947-0,3684 2,1561 Adenoma PTV 64 M 2,31 0,0 0,0 0,0 1,5359 Adenoma PE 76 M 1,69 0,8352 1, ,2037 0,0 Hiperplasia bilateral
80 62 RC 64 M 2,05 0,7333 0,8267 0,0 2,22 Hiperplasia bilateral RSS 53 F 4,68 0,0375 0,6826 0,0 0,1439 Mielolipoma RFS 53 M 7,35 0,6636 1,1706-6,6554 5,4606 Adenoma RLJ 63 M 10,67 1,1597 0, ,8318 3,3664 Adenoma SDT 56 M 4 0,36 0,0 0,0 0,5 Adenoma VLG 58 F 4 0,7414 0,5824 0,0 0,0 Adenoma VAM 46 F 1,19 0,4167 0,645 0,0 1,75 Adenoma VLB 51 F 4,32 0,0 0,0 0,0 0,2292 Adenoma VLSB 61 F 1,96 0,0 0,0 0,0 0,0 Adenoma VHG 57 M 3,29 1,0267 1, ,6039 4,1348 Adenoma WGB 62 M 1,49 1,0 0,0 0,0 1,0086 Adenoma YK 65 F 2,97 0,9587 0,0 0,0 0,7076 Adenoma ZCA 80 F 6,14 1,2053 1,1787-2,4716 0,339 Adenoma
81 63 Anexo 2 Planilha para a realização da análise da espectroscopia por ressonância magnética. ESPECTROSCOPIA DA GLÂNDULA ADRENAL Nome: Data do exame: / / Idade: Volume da massa: x x Voxel Posição ppm Cho Cr Lip Lac ppm Glx Lip 2
82 Anexo 3 Projeto de pesquisa submetido à aprovação do Comitê de Ética Médica da UNIFESP 64
OBI Uso de imagens no planejamento radioterápico
 OBI Uso de imagens no planejamento radioterápico CBCT Kv / Kv Ressonância Magnética Flávia Aparecida Franck Dosimetrista Téc. Fernando Assi Introdução Núcleos ativos em RM Escolha do hidrogênio Aspectos
OBI Uso de imagens no planejamento radioterápico CBCT Kv / Kv Ressonância Magnética Flávia Aparecida Franck Dosimetrista Téc. Fernando Assi Introdução Núcleos ativos em RM Escolha do hidrogênio Aspectos
Imagens por Ressonância Magnética: Princípios e Aplicações
 UNIVERSIDADE DE SÃO PAULO Instituto de Física de São Carlos Centro de Imagens e Espectroscopia In Vivo por Ressonância Magnética Imagens por Ressonância Magnética: Princípios e Aplicações Fernando F Paiva
UNIVERSIDADE DE SÃO PAULO Instituto de Física de São Carlos Centro de Imagens e Espectroscopia In Vivo por Ressonância Magnética Imagens por Ressonância Magnética: Princípios e Aplicações Fernando F Paiva
Ressonância Magnética. Considerações técnicas práticas
 Ressonância Magnética Considerações técnicas práticas PULSO DE RADIOFREQUÊNCIA Como consequência da aplicação do pulso de RF observa-se que o VME afasta-se do alinhamento em relação a linha paralela de
Ressonância Magnética Considerações técnicas práticas PULSO DE RADIOFREQUÊNCIA Como consequência da aplicação do pulso de RF observa-se que o VME afasta-se do alinhamento em relação a linha paralela de
IMAGEM POR RESSONÂNCIA MAGNÉTICA (MRI) Prof. Sérgio Francisco Pichorim
 IMAGEM POR RESSONÂNCIA MAGNÉTICA (MRI) Prof. Sérgio Francisco Pichorim Imagem por Ressonância Magnética Não usa radiação ionizante Efeito biológico não mensurável Aparentemente seguro Imagens em cortes
IMAGEM POR RESSONÂNCIA MAGNÉTICA (MRI) Prof. Sérgio Francisco Pichorim Imagem por Ressonância Magnética Não usa radiação ionizante Efeito biológico não mensurável Aparentemente seguro Imagens em cortes
Exame não invasivo I: Imagem por. Ressonância. Magnética. Nuclear
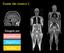 Exame não invasivo I: Imagem por Ressonância Magnética Nuclear Histórico da IRMN 1873 Maxwell - Equações para campos elétricos e magnéticos 1887 Hertz - Radiofreqüência 1924 Pauli - Magnetismo Nuclear
Exame não invasivo I: Imagem por Ressonância Magnética Nuclear Histórico da IRMN 1873 Maxwell - Equações para campos elétricos e magnéticos 1887 Hertz - Radiofreqüência 1924 Pauli - Magnetismo Nuclear
Ressonância Magnética Prática, Catherine Westbrook e Carolyn Kaut. TR, TE, Flip Angle
 Ressonância Magnética Prática, Catherine Westbrook e Carolyn Kaut TR, TE, Flip Angle Além de proporcionar o contraste nas IRM, ambos os parâmetros de TR, TE e ângulo de inclinação, também influenciam a
Ressonância Magnética Prática, Catherine Westbrook e Carolyn Kaut TR, TE, Flip Angle Além de proporcionar o contraste nas IRM, ambos os parâmetros de TR, TE e ângulo de inclinação, também influenciam a
Ressonância Magnética. Prof. Luciano Santa Rita
 Ressonância Magnética Prof. Luciano Santa Rita tecnologo@lucianosantarita.pro.br www.lucianosantarita.pro.br Sumário Introdução e Histórico Princípio de funcionamento de ressonância magnética - RM (abordagem
Ressonância Magnética Prof. Luciano Santa Rita tecnologo@lucianosantarita.pro.br www.lucianosantarita.pro.br Sumário Introdução e Histórico Princípio de funcionamento de ressonância magnética - RM (abordagem
Faculdade de Tecnologia de Bauru Sistemas Biomédicos. Ressonância Magnética Nuclear. Profª. Wangner Barbosa da Costa
 Faculdade de Tecnologia de Bauru Sistemas Biomédicos Ressonância Magnética Nuclear Profª. Wangner Barbosa da Costa Tópicos Introdução Princípios Físicos da RMN O Exame de Ressonância Magnética Nuclear
Faculdade de Tecnologia de Bauru Sistemas Biomédicos Ressonância Magnética Nuclear Profª. Wangner Barbosa da Costa Tópicos Introdução Princípios Físicos da RMN O Exame de Ressonância Magnética Nuclear
Radiologia Blog Dr. Ricardo
 Radiologia WWW.cedav.com.br Blog Dr. Ricardo Dr. Ricardo Ferreira Mestre em radiologia UFTP Prof. Adj. Radiologia FEPAR Prof. Ass. Anatomia FEPAR Diretor Centro do Diagnostico Água Verde Md radiologista
Radiologia WWW.cedav.com.br Blog Dr. Ricardo Dr. Ricardo Ferreira Mestre em radiologia UFTP Prof. Adj. Radiologia FEPAR Prof. Ass. Anatomia FEPAR Diretor Centro do Diagnostico Água Verde Md radiologista
TOMOGRAFIA POR RESSONÂNCIA MAGNÉTICA NUCLEAR. Prof. Dr. Paulo Mazzoncini de Azevedo Marques Centro de Ciências das Imagens e Física Médica FMRP/USP
 TOMOGRAFIA POR RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Paulo Mazzoncini de Azevedo Marques Centro de Ciências das Imagens e Física Médica FMRP/USP Ressonância Magnética nuclear (RMN) permite obter estudos
TOMOGRAFIA POR RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Paulo Mazzoncini de Azevedo Marques Centro de Ciências das Imagens e Física Médica FMRP/USP Ressonância Magnética nuclear (RMN) permite obter estudos
Análise de Compostos Orgânicos RESSONÂNCIA MAGNÉTICA NUCLEAR
 Análise de Compostos Orgânicos Capítulo III O Retorno de Jedi RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Roberto Berlinck História: Kekulé, 854: Chemistry will never reveal the structure of the molecules,
Análise de Compostos Orgânicos Capítulo III O Retorno de Jedi RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Roberto Berlinck História: Kekulé, 854: Chemistry will never reveal the structure of the molecules,
A perda de magnetização (sinal) pela relaxação transversal é predominante: COM relaxação: sinal observado pela bobina
 Largura do sinal de NMR A perda de magnetização (sinal) pela relaxação transversal é predominante: SEM relaxação: sinal observado pela bobina espectro (delta) t COM relaxação: sinal observado pela bobina
Largura do sinal de NMR A perda de magnetização (sinal) pela relaxação transversal é predominante: SEM relaxação: sinal observado pela bobina espectro (delta) t COM relaxação: sinal observado pela bobina
Resumo sobre magnetização nuclear [ ] o = !!!! Frequência de Larmor = frequencia do movimento de precessão = frequencia de ressonancia RMN!!!
![Resumo sobre magnetização nuclear [ ] o = !!!! Frequência de Larmor = frequencia do movimento de precessão = frequencia de ressonancia RMN!!! Resumo sobre magnetização nuclear [ ] o = !!!! Frequência de Larmor = frequencia do movimento de precessão = frequencia de ressonancia RMN!!!](/thumbs/83/87093138.jpg) Resumo sobre magnetização nuclear M = µ N ( ) N ( ) [ ] 0 mag ω o = γ B o ν o = o γ B 2π!!!! Frequência de Larmor = frequencia do movimento de precessão = frequencia de ressonancia RMN!!! Magnetização
Resumo sobre magnetização nuclear M = µ N ( ) N ( ) [ ] 0 mag ω o = γ B o ν o = o γ B 2π!!!! Frequência de Larmor = frequencia do movimento de precessão = frequencia de ressonancia RMN!!! Magnetização
Ressonância Magnética Nuclear
 Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
RM: PRINCÍPIOS FÍSICOS QUAL É A MÁGICA? PTC2892 Princípios da Formação e Processamento de Imagens Médicas. Ressonância Magnética
 Plano da aula de hoje PTC2892 Princípios da Formação e Processamento de Imagens Médicas Ressonância Magnética Prof. S Furuie Princípios físicos de Ressonância Magnética Formação de imagens em Ressonância
Plano da aula de hoje PTC2892 Princípios da Formação e Processamento de Imagens Médicas Ressonância Magnética Prof. S Furuie Princípios físicos de Ressonância Magnética Formação de imagens em Ressonância
Princípio da técnica FT em RMN 1) Mudança da orientação da magnetização, produzida por núcleos atômicos, através de um pulso curto de RF.
 Princípio da técnica FT em RMN 1) Mudança da orientação da magnetização, produzida por núcleos atômicos, através de um pulso curto de RF. 2) O pulso resultante contém a frequência principal e uma banda
Princípio da técnica FT em RMN 1) Mudança da orientação da magnetização, produzida por núcleos atômicos, através de um pulso curto de RF. 2) O pulso resultante contém a frequência principal e uma banda
RESSONÂNCIA MAGNÉTICA
 Centro Federal de Educação Tecnológica de Santa Catarina Gerência Educacional de Eletrônica RESSONÂNCIA MAGNÉTICA CURSO TÉCNICO DE RADIOLOGIA Prof. Flávio Augusto Soares, M. Eng. Prof. Henrique Batista
Centro Federal de Educação Tecnológica de Santa Catarina Gerência Educacional de Eletrônica RESSONÂNCIA MAGNÉTICA CURSO TÉCNICO DE RADIOLOGIA Prof. Flávio Augusto Soares, M. Eng. Prof. Henrique Batista
ESPECTROSCOPIA DE RESSONANCIA MAGNÉTICA NUCLEAR
 ESPECTROSCOPIA DE RESSONANCIA MAGNÉTICA NUCLEAR Histórico 1924: W. Pauli descreveu a base teórica da RMN; 1946: Bloch (Stanford) e Purcell (Harvard) demonstraram a teoria de absorção de radiação eletromagnética
ESPECTROSCOPIA DE RESSONANCIA MAGNÉTICA NUCLEAR Histórico 1924: W. Pauli descreveu a base teórica da RMN; 1946: Bloch (Stanford) e Purcell (Harvard) demonstraram a teoria de absorção de radiação eletromagnética
Movimento de precessão e magnetização
 Movimento de precessão e magnetização ω o = γ Bo ω o = 2π ν o a) Um momento magnético (spin nuclear), orientado parcialmente com relação a Bo, executa um movimento de precessão em torno do campo magnético.
Movimento de precessão e magnetização ω o = γ Bo ω o = 2π ν o a) Um momento magnético (spin nuclear), orientado parcialmente com relação a Bo, executa um movimento de precessão em torno do campo magnético.
Relembrando - RMN. quebra a degenerescência dos níveis de energia. provoca transições entre os níveis de energia
 Relembrando - RMN Alto campo magnético externo Campo eletromagnético oscilante cria uma magnetização (alinha os spins) quebra a degenerescência dos níveis de energia gira a magnetização provoca transições
Relembrando - RMN Alto campo magnético externo Campo eletromagnético oscilante cria uma magnetização (alinha os spins) quebra a degenerescência dos níveis de energia gira a magnetização provoca transições
Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN. Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques
 Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques Introdução A espectroscopia por Ressonância Magnética Nuclear (RMN)
Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques Introdução A espectroscopia por Ressonância Magnética Nuclear (RMN)
MENINGIOMA VS LESÃO SECUNDÁRIA
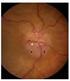 MENINGIOMA VS LESÃO SECUNDÁRIA Joana Martins Fialho 28-9-13 Sessão Científica Espectroscopia por RM Espectroscopia Método analítico utilizado na Química que permite a identificação e quantificação de metabolitos,
MENINGIOMA VS LESÃO SECUNDÁRIA Joana Martins Fialho 28-9-13 Sessão Científica Espectroscopia por RM Espectroscopia Método analítico utilizado na Química que permite a identificação e quantificação de metabolitos,
Resumo dos pontos importantes
 Resumo dos pontos importantes Equação básica da espectroscopia de RMN. γ X o ν X = B (1 σ X ) π Espectros de RMN e deslocamentos químicos. v X ν ref 6 δ ( ppm) = 10 ν ref 2 δ ( Hz) = δ ( ppm) ν 10 = 6
Resumo dos pontos importantes Equação básica da espectroscopia de RMN. γ X o ν X = B (1 σ X ) π Espectros de RMN e deslocamentos químicos. v X ν ref 6 δ ( ppm) = 10 ν ref 2 δ ( Hz) = δ ( ppm) ν 10 = 6
HISTERESE FERROMAGNÉTICA
 HISTERESE FERROMAGNÉTICA Introdução Um material magnetizado é descrito pelo seu vetor de magnetização M definido como o momento de dipolo magnético por unidade de volume. M = dm dv (1) De acordo com o
HISTERESE FERROMAGNÉTICA Introdução Um material magnetizado é descrito pelo seu vetor de magnetização M definido como o momento de dipolo magnético por unidade de volume. M = dm dv (1) De acordo com o
RESSONÂNCIA MAGNÉTICA. Tecngº Diego Moura
 RESSONÂNCIA MAGNÉTICA Tecngº Diego Moura diegomouraprof@gmail.com Estado de um sistema que vibra em frequência própria, com amplitude acentuadamente maior, como resultado de estímulos externos que possuem
RESSONÂNCIA MAGNÉTICA Tecngº Diego Moura diegomouraprof@gmail.com Estado de um sistema que vibra em frequência própria, com amplitude acentuadamente maior, como resultado de estímulos externos que possuem
ν L : frequência de Larmor.
 Ressonância Magnética Nuclear β (+) N β = N α e - E/KT Núcleo de spin I= ½ ( 1 H, 13 C, 15 N, 19 F, 31 P) α β E = hν rf = γhb 0 α (-) N α sem campo com campo B 0 Campo estático externo B 0 desdobramento
Ressonância Magnética Nuclear β (+) N β = N α e - E/KT Núcleo de spin I= ½ ( 1 H, 13 C, 15 N, 19 F, 31 P) α β E = hν rf = γhb 0 α (-) N α sem campo com campo B 0 Campo estático externo B 0 desdobramento
Journal Club (set/2010)
 Journal Club (set/2010) van Werven et al Academic Medical Center University of Amsterdam Netherland Thiago Franchi Nunes Orientador: Dr. Rogério Caldana Escola Paulista de Medicina Universidade Federal
Journal Club (set/2010) van Werven et al Academic Medical Center University of Amsterdam Netherland Thiago Franchi Nunes Orientador: Dr. Rogério Caldana Escola Paulista de Medicina Universidade Federal
E = - N m i ħb o E = N ħb o
 Resumo de pontos fundamentais A maioria dos núcleos atômicos apresentam um comportamento magnético I mag I = [I N (I N + 1)] 1/2 ħ I z = (-I N, -I N +1,., +I N )ħ = m i ħ Energia do núcleo num campo magnético
Resumo de pontos fundamentais A maioria dos núcleos atômicos apresentam um comportamento magnético I mag I = [I N (I N + 1)] 1/2 ħ I z = (-I N, -I N +1,., +I N )ħ = m i ħ Energia do núcleo num campo magnético
Aplicação de um protocolo de espectroscopia por ressonância magnética das adrenais: experiência com mais de 100 casos *
 Artigo Original Melo HJF et al. / Aplicação da espectroscopia por RM em mais de 100 adrenais Aplicação de um protocolo de espectroscopia por ressonância magnética das adrenais: experiência com mais de
Artigo Original Melo HJF et al. / Aplicação da espectroscopia por RM em mais de 100 adrenais Aplicação de um protocolo de espectroscopia por ressonância magnética das adrenais: experiência com mais de
Momento Magnético Momento de Dipolo
 Propriedades Magnéticas I Magnetismo Fenômeno pelo qual certos materiais exercem uma força ou influência atrativa e repulsiva sobre outros materiais Aplicações mais importantes Geradores de potência elétrica
Propriedades Magnéticas I Magnetismo Fenômeno pelo qual certos materiais exercem uma força ou influência atrativa e repulsiva sobre outros materiais Aplicações mais importantes Geradores de potência elétrica
Análise de alimentos II Introdução aos Métodos Espectrométricos
 Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
PLANO DE TRABALHO TECNOLOGIA EM RM - I
 UNIVERSIDADE FEDERAL DE MINAS GERAIS FACULDADE DE MEDICINA CURSO SUPERIOR DE TECNOLOGIA EM RADIOLOGIA PLANO DE TRABALHO TECNOLOGIA EM RM - I TURMA 1 PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1. EMENTA:
UNIVERSIDADE FEDERAL DE MINAS GERAIS FACULDADE DE MEDICINA CURSO SUPERIOR DE TECNOLOGIA EM RADIOLOGIA PLANO DE TRABALHO TECNOLOGIA EM RM - I TURMA 1 PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1. EMENTA:
BE066 - Fisiologia do Exercício BE066 Fisiologia do Exercício. Bioenergética. Sergio Gregorio da Silva, PhD
 BE066 Fisiologia do Exercício Bioenergética Sergio Gregorio da Silva, PhD Objetivos Definir Energia Descrever os 3 Sistemas Energéticos Descrever as diferenças em Produção de Energia Bioenergética Estuda
BE066 Fisiologia do Exercício Bioenergética Sergio Gregorio da Silva, PhD Objetivos Definir Energia Descrever os 3 Sistemas Energéticos Descrever as diferenças em Produção de Energia Bioenergética Estuda
RESSONÂNCIA MAGNÉTICA
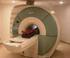 RESSONÂNCIA MAGNÉTICA A ressonância magnética (RM) é um método radiológico que utiliza radiação eletromagnética na formação da imagem e que não depende nem da capacidade de absorção dos raios X pelos tecidos,
RESSONÂNCIA MAGNÉTICA A ressonância magnética (RM) é um método radiológico que utiliza radiação eletromagnética na formação da imagem e que não depende nem da capacidade de absorção dos raios X pelos tecidos,
QFL (a) Aqui se trata de mero uso de fórmula e uso da constante magnetogírica do próton. 2πν
 QFL-2144-2013 Roteiro da 1 a Lista de exercícios de RMN 1.) A maioria dos espectrômetros de RMN utilizados para estudos em Química utiliza campos magnéticos fixos tais que a freqüência de ressonância de
QFL-2144-2013 Roteiro da 1 a Lista de exercícios de RMN 1.) A maioria dos espectrômetros de RMN utilizados para estudos em Química utiliza campos magnéticos fixos tais que a freqüência de ressonância de
Aula 12. (quase) Tudo sobre os átomos. Física Geral F-428
 Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
Aula 1 (quase) Tudo sobre os átomos Física Geral F-48 1 Algumas propriedades atômicas: Átomos são estáveis (quase sempre); Os átomos podem ser agrupados em famílias (propriedades periódicas, com o número
PLANO DE TRABALHO 1 SEMESTRE 2018 TECNOLOGIA EM RM - I
 PLANO DE TRABALHO 1 SEMESTRE 2018 TECNOLOGIA EM RM - I PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1. EMENTA: Introdução de conhecimentos básicos sobre o equipamento de Ressonância Magnética, seu funcionamento
PLANO DE TRABALHO 1 SEMESTRE 2018 TECNOLOGIA EM RM - I PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1. EMENTA: Introdução de conhecimentos básicos sobre o equipamento de Ressonância Magnética, seu funcionamento
Eletromagnetismo Aplicado
 Eletromagnetismo Aplicado Unidade 3 Prof. Marcos V. T. Heckler 1 Conteúdo Introdução Materiais dielétricos, polarização e permissividade elétrica Materiais magnéticos, magnetização e permeabilidade magnética
Eletromagnetismo Aplicado Unidade 3 Prof. Marcos V. T. Heckler 1 Conteúdo Introdução Materiais dielétricos, polarização e permissividade elétrica Materiais magnéticos, magnetização e permeabilidade magnética
PLANO DE TRABALHO 2 SEMESTRE 2015 DISCIPLINA TECNOLOGIA RESSONÂNCIA MAGNÉTICA II
 PLANO DE TRABALHO 2 SEMESTRE 2015 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
PLANO DE TRABALHO 2 SEMESTRE 2015 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. [D] Primeiramente é necessário encontrar o sentido da força magnética. Para tal, é direto verificar, utilizando a regra da mão esquerda, que o sentido desta força
SOLUÇÃO PRATIQUE EM CASA SOLUÇÃO PC1. [D] Primeiramente é necessário encontrar o sentido da força magnética. Para tal, é direto verificar, utilizando a regra da mão esquerda, que o sentido desta força
Seleção de um Método Analítico. Validação e protocolos em análises químicas. Validação de Métodos Analíticos
 Seleção de um Método Analítico Capítulo 1 SKOOG, D.A.; HOLLER, F.J.; NIEMAN, T.A. Princípios de Análise Instrumental. 5 a edição, Ed. Bookman, Porto Alegre, 2002. Validação e protocolos em análises químicas
Seleção de um Método Analítico Capítulo 1 SKOOG, D.A.; HOLLER, F.J.; NIEMAN, T.A. Princípios de Análise Instrumental. 5 a edição, Ed. Bookman, Porto Alegre, 2002. Validação e protocolos em análises químicas
MÉTODOS DE CALIBRAÇÃO
 MÉTODOS DE CALIBRAÇÃO Sinais obtidos por equipamentos e instrumentos devem ser calibrados para evitar erros nas medidas. Calibração, de acordo com o INMETRO, é o conjunto de operações que estabelece, sob
MÉTODOS DE CALIBRAÇÃO Sinais obtidos por equipamentos e instrumentos devem ser calibrados para evitar erros nas medidas. Calibração, de acordo com o INMETRO, é o conjunto de operações que estabelece, sob
PLANO DE TRABALHO 1 SEMESTRE 2019 TECNOLOGIA EM RM - I
 PLANO DE TRABALHO 1 SEMESTRE 2019 TECNOLOGIA EM RM - I PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1. EMENTA: Introdução de conhecimentos básicos sobre o equipamento de Ressonância Magnética, seu funcionamento
PLANO DE TRABALHO 1 SEMESTRE 2019 TECNOLOGIA EM RM - I PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1. EMENTA: Introdução de conhecimentos básicos sobre o equipamento de Ressonância Magnética, seu funcionamento
PLANO DE TRABALHO 1 SEMESTRE 2015 DISCIPLINA TECNOLOGIA RESSONÂNCIA MAGNÉTICA II
 PLANO DE TRABALHO 1 SEMESTRE 2015 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
PLANO DE TRABALHO 1 SEMESTRE 2015 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
Fundamentos da Ressonância Magnética Nuclear
 Fundamentos da Ressonância Magnética Nuclear José Daniel Figueroa-Villar Grupo de Química Medicinal Departamento de Química Instituto Militar de Engenharia Rio de Janeiro, Brasil figueroa@ime.eb.br Por
Fundamentos da Ressonância Magnética Nuclear José Daniel Figueroa-Villar Grupo de Química Medicinal Departamento de Química Instituto Militar de Engenharia Rio de Janeiro, Brasil figueroa@ime.eb.br Por
PRÁTICA 11: LEI DE HOOKE E OSCILADOR MASSA-MOLA MOLA
 PRÁTICA 11: LEI DE HOOKE E OSCILADOR MASSA-MOLA MOLA O entendimento de determinados tipos de forças, como a força de uma mola sobre um corpo, é a chave para a compreensão do mundo quântico. Por exemplo,
PRÁTICA 11: LEI DE HOOKE E OSCILADOR MASSA-MOLA MOLA O entendimento de determinados tipos de forças, como a força de uma mola sobre um corpo, é a chave para a compreensão do mundo quântico. Por exemplo,
PLANO DE TRABALHO 1 SEMESTRE 2017 DISCIPLINA TECNOLOGIA RESSONÂNCIA MAGNÉTICA II
 PLANO DE TRABALHO 1 SEMESTRE 2017 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
PLANO DE TRABALHO 1 SEMESTRE 2017 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
5. Resultados e Discussão
 47 5. Resultados e Discussão 5.1.1. Faixa de trabalho e Faixa linear de trabalho As curvas analíticas obtidas são apresentadas na Figura 14 e Figura 16. Baseado no coeficiente de determinação (R 2 ) encontrado,
47 5. Resultados e Discussão 5.1.1. Faixa de trabalho e Faixa linear de trabalho As curvas analíticas obtidas são apresentadas na Figura 14 e Figura 16. Baseado no coeficiente de determinação (R 2 ) encontrado,
RESSONÂNCIA MAGNÉTICA
 Belo Horizonte Faculdade de Tecnologia Novo Rumo FACULDADE DE TECNOLOGIA NOVO RUMO Rua Paraíba, 75, Funcionários, Belo Horizonte Minas Gerais. CEP.: 30130-140 Fone: (31) 3226-2858 Site: www.novorumo.com.br
Belo Horizonte Faculdade de Tecnologia Novo Rumo FACULDADE DE TECNOLOGIA NOVO RUMO Rua Paraíba, 75, Funcionários, Belo Horizonte Minas Gerais. CEP.: 30130-140 Fone: (31) 3226-2858 Site: www.novorumo.com.br
FDG PET no Câncer de Pulmão: Influências das doenças granulomatosas
 FDG PET no Câncer de Pulmão: Influências das doenças granulomatosas Bruno Hochhegger MD, PhD Médico Radiologista do Pavilhão Pereira Filho e Hospital São Lucas da PUCRS Professor de Radiologia da UFCSPA
FDG PET no Câncer de Pulmão: Influências das doenças granulomatosas Bruno Hochhegger MD, PhD Médico Radiologista do Pavilhão Pereira Filho e Hospital São Lucas da PUCRS Professor de Radiologia da UFCSPA
Experimento 1D. Consiste de dois períodos, nos quais sequências complexas de pulsos intercalados com tempos de espera podem ocorrer.
 Experimento 1D Consiste de dois períodos, nos quais sequências complexas de pulsos intercalados com tempos de espera podem ocorrer. preparação dos spins através de pulsos e de tempos de espera detecção
Experimento 1D Consiste de dois períodos, nos quais sequências complexas de pulsos intercalados com tempos de espera podem ocorrer. preparação dos spins através de pulsos e de tempos de espera detecção
Preparando a amostra
 Preparando a amostra Cuidados ao preparar a amostra: concentração ~1 mm (~100 um pode ser medido em cryoprobe) solvente ou tampão apropriado adicionar 5 a 10% de D 2 O (lock) adicionar ~100 um de DSS (referência)
Preparando a amostra Cuidados ao preparar a amostra: concentração ~1 mm (~100 um pode ser medido em cryoprobe) solvente ou tampão apropriado adicionar 5 a 10% de D 2 O (lock) adicionar ~100 um de DSS (referência)
Leis de Biot-Savart e de Ampère
 Leis de Biot-Savart e de Ampère 1 Vimos que uma carga elétrica cria um campo elétrico e que este campo exerce força sobre uma outra carga. Também vimos que um campo magnético exerce força sobre uma carga
Leis de Biot-Savart e de Ampère 1 Vimos que uma carga elétrica cria um campo elétrico e que este campo exerce força sobre uma outra carga. Também vimos que um campo magnético exerce força sobre uma carga
HISTERESE E RELAXAÇÃO FERROMAGNÉTICA
 HISTERESE E RELAXAÇÃO FERROMAGNÉTICA Introdução Um material magnetizado é descrito pelo seu vetor de magnetização M definido como o momento de dipolo magnético por unidade de volume. M = dm dv (1) De acordo
HISTERESE E RELAXAÇÃO FERROMAGNÉTICA Introdução Um material magnetizado é descrito pelo seu vetor de magnetização M definido como o momento de dipolo magnético por unidade de volume. M = dm dv (1) De acordo
2 Tomografia Computadorizada de Raios X
 2 Tomografia Computadorizada de Raios X 2.1 Fundamentos Teóricos de Tomografia Computadorizada de Raios X A Tomografia Computadorizada de Raios X é uma técnica que permite a avaliação de modo não destrutivo
2 Tomografia Computadorizada de Raios X 2.1 Fundamentos Teóricos de Tomografia Computadorizada de Raios X A Tomografia Computadorizada de Raios X é uma técnica que permite a avaliação de modo não destrutivo
Transmissão e comunicação de dados. Renato Machado
 Renato Machado UFSM - Universidade Federal de Santa Maria DELC - Departamento de Eletrônica e Computação renatomachado@ieee.org renatomachado@ufsm.br 23 de Abril de 2012 Sumário 1 2 3 4 Térmico de Intermodulação
Renato Machado UFSM - Universidade Federal de Santa Maria DELC - Departamento de Eletrônica e Computação renatomachado@ieee.org renatomachado@ufsm.br 23 de Abril de 2012 Sumário 1 2 3 4 Térmico de Intermodulação
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa
 OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
Física IV Poli Engenharia Elétrica: 20ª Aula (04/11/2014)
 Física IV Poli Engenharia Elétrica: ª Aula (4/11/14) Prof. Alvaro Vannucci a última aula vimos: Átomos multi-eletrônicos: as energias dos estados quânticos podem ser avaliadas através da expressão: 13,6
Física IV Poli Engenharia Elétrica: ª Aula (4/11/14) Prof. Alvaro Vannucci a última aula vimos: Átomos multi-eletrônicos: as energias dos estados quânticos podem ser avaliadas através da expressão: 13,6
PLANO DE TRABALHO 2 SEMESTRE 2016 TECNOLOGIA EM RM - I
 UNIVERSIDADE FEDERAL DE MINAS GERAIS FACULDADE DE MEDICINA CURSO SUPERIOR DE TECNOLOGIA EM RADIOLOGIA PLANO DE TRABALHO 2 SEMESTRE 2016 TECNOLOGIA EM RM - I PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1.
UNIVERSIDADE FEDERAL DE MINAS GERAIS FACULDADE DE MEDICINA CURSO SUPERIOR DE TECNOLOGIA EM RADIOLOGIA PLANO DE TRABALHO 2 SEMESTRE 2016 TECNOLOGIA EM RM - I PROFESSOR RESPONSÁVEL: Luiz Cláudio Souza 1.
Métodos Físicos de Análise - RESSONÂNCIA MAGNÉTICA NUCLEAR. Métodos Físicos de Análise. Métodos Físicos de Análise
 - RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos Fiocruz Docente do Programa
- RESSONÂNCIA MAGNÉTICA NUCLEAR Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos Fiocruz Docente do Programa
Aula 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Espectroscopia de RMN
 Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
Comentários sobre a 3a Prova
 s sobre a 3a Prova 1) (2,0 pontos) O espectro de RMN de 13 C do acetaldeído, CH 3 CHO, é relativamente simples, e fácil de prever conforme discutido em aula. Agora, vamos testar o conhecimento por trás
s sobre a 3a Prova 1) (2,0 pontos) O espectro de RMN de 13 C do acetaldeído, CH 3 CHO, é relativamente simples, e fácil de prever conforme discutido em aula. Agora, vamos testar o conhecimento por trás
Lista de Exercícios 5 Corrente elétrica e campo magnético
 Lista de Exercícios 5 Corrente elétrica e campo magnético Exercícios Sugeridos (13/04/2010) A numeração corresponde ao Livros Textos A e B. A22.5 Um próton desloca-se com velocidade v = (2 î 4 ĵ + ˆk)
Lista de Exercícios 5 Corrente elétrica e campo magnético Exercícios Sugeridos (13/04/2010) A numeração corresponde ao Livros Textos A e B. A22.5 Um próton desloca-se com velocidade v = (2 î 4 ĵ + ˆk)
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA TEÓRICO-PRÁTICA
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA TEÓRICO-PRÁTICA
Cap. 5 Espectroscopia Molecular ESPECTROSCOPIA DE RESSONÂNCIA MAGNÉTICA NUCLEAR
 Cap. 5 Espectroscopia Molecular ESPECTROSCOPIA DE RESSONÂNCIA MAGNÉTICA NUCLEAR Espectro RMN de baixa resolução O-C 2 -C 3 5.1ppm 3.7 ppm 1.2 ppm Campo alto, Campo baixo O espectro explica-se pelo efeito
Cap. 5 Espectroscopia Molecular ESPECTROSCOPIA DE RESSONÂNCIA MAGNÉTICA NUCLEAR Espectro RMN de baixa resolução O-C 2 -C 3 5.1ppm 3.7 ppm 1.2 ppm Campo alto, Campo baixo O espectro explica-se pelo efeito
DISCIPLINA TECNOLOGIA RESSONÂNCIA MAGNÉTICA II
 PLANO DE TRABALHO 1 SEMESTRE 2018 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
PLANO DE TRABALHO 1 SEMESTRE 2018 DISCIPLINA TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA II PROFESSOR: Luiz Cláudio de Souza 1. EMENTA: A disciplina desenvolve as bases operacionais e técnicas referentes aos diferentes
Escola Bahiana de Medicina e Saúde Pública PROSEF MEDICINA PADRÃO DE RESPOSTAS
 Escola Bahiana de Medicina e Saúde Pública PROSEF 2018.2 MEDICINA Espera-se que o Candidato PADRÃO DE RESPOSTAS Questão 01 Escreva os nomes das classes funcionais comuns da codeína e da hidrocodona. Os
Escola Bahiana de Medicina e Saúde Pública PROSEF 2018.2 MEDICINA Espera-se que o Candidato PADRÃO DE RESPOSTAS Questão 01 Escreva os nomes das classes funcionais comuns da codeína e da hidrocodona. Os
NOME: QFL ª Prova (15 pontos) Tabela de deslocamentos químicos de 13 C em sistemas orgânicos
 NOME: QFL 2144 2008 3ª Prova (15 pontos) Tabela de deslocamentos químicos de 13 C em sistemas orgânicos Fragmentações e fragmentos comuns em espectrometria de massa Íon fragmento Neutro Perdido Massa do
NOME: QFL 2144 2008 3ª Prova (15 pontos) Tabela de deslocamentos químicos de 13 C em sistemas orgânicos Fragmentações e fragmentos comuns em espectrometria de massa Íon fragmento Neutro Perdido Massa do
Novo Princípio de Medição de Umidade de BIOMASSA através de Ressonância Magnética.
 Novo Princípio de Medição de Umidade de BIOMASSA através de Ressonância Magnética. Lasse Kauppinen lasse.kauppinen@metso.com Metso Automation Kajaani Finlândia Samuel Macedo samuel.macedo@metso.com Metso
Novo Princípio de Medição de Umidade de BIOMASSA através de Ressonância Magnética. Lasse Kauppinen lasse.kauppinen@metso.com Metso Automation Kajaani Finlândia Samuel Macedo samuel.macedo@metso.com Metso
Espectroscopia no IV
 Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
HORMÔNIOS ESTERÓIDES
 UNIVERSIDADE FEDERAL DE PERNAMBUCO CENTRO DE CIÊNCIAS BIOLÓGICAS DEPARTAMENTO DE BIOQUÍMICA HORMÔNIOS ESTERÓIDES Prof a. Dr a. Nereide Magalhães Recife, fevereiro de 2005 HORMÔNIOS ESTERÓIDES Hormônios
UNIVERSIDADE FEDERAL DE PERNAMBUCO CENTRO DE CIÊNCIAS BIOLÓGICAS DEPARTAMENTO DE BIOQUÍMICA HORMÔNIOS ESTERÓIDES Prof a. Dr a. Nereide Magalhães Recife, fevereiro de 2005 HORMÔNIOS ESTERÓIDES Hormônios
Sinopse. 1. Introdução
 COTEQ-204 VARIÁVEIS QUE INFLUENCIAM OS RESULTADOS DO ENSAIO DE MATERIAIS FERROMAGNÉTICOS PELA ANÁLISE DO RUÍDO MAGNÉTICO BARKHAUSEN Silvério Ferreira da Silva Júnior 1, Donizete Anderson de Alencar 2,
COTEQ-204 VARIÁVEIS QUE INFLUENCIAM OS RESULTADOS DO ENSAIO DE MATERIAIS FERROMAGNÉTICOS PELA ANÁLISE DO RUÍDO MAGNÉTICO BARKHAUSEN Silvério Ferreira da Silva Júnior 1, Donizete Anderson de Alencar 2,
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Introdução ao Metabolismo. Profª Eleonora Slide de aula
 Introdução ao Metabolismo Profª Eleonora Slide de aula Metabolismo Profª Eleonora Slide de aula Relacionamento energético entre as vias catabólicas e as vias anabólicas Nutrientes que liberam energia Carboidratos
Introdução ao Metabolismo Profª Eleonora Slide de aula Metabolismo Profª Eleonora Slide de aula Relacionamento energético entre as vias catabólicas e as vias anabólicas Nutrientes que liberam energia Carboidratos
HISTERESE FERROMAGNÉTICA
 HISTERESE FERROMAGNÉTICA Introdução Um material magnetizado é descrito pelo seu vetor de magnetização M definido como o momento de dipolo magnético por unidade de volume. M = dm dv (1) De acordo com o
HISTERESE FERROMAGNÉTICA Introdução Um material magnetizado é descrito pelo seu vetor de magnetização M definido como o momento de dipolo magnético por unidade de volume. M = dm dv (1) De acordo com o
UNIVERSIDADE ESTADUAL PAULISTA
 GLICÓLISE Dra. Flávia Cristina Goulart CIÊNCIAS FISIOLÓGICAS UNIVERSIDADE ESTADUAL PAULISTA Campus de Marília flaviagoulart@marilia.unesp.br Glicose e glicólise Via Ebden-Meyerhof ou Glicólise A glicólise,
GLICÓLISE Dra. Flávia Cristina Goulart CIÊNCIAS FISIOLÓGICAS UNIVERSIDADE ESTADUAL PAULISTA Campus de Marília flaviagoulart@marilia.unesp.br Glicose e glicólise Via Ebden-Meyerhof ou Glicólise A glicólise,
Deise Schäfer. 14 de dezembro de 2011
 Ressonância Ferromagnética Ressonância Ferromagnética Deise Schäfer 14 de dezembro de 2011 Deise Schäfer 14 de dezembro de 2011 1 / 35 Ressonância Ferromagnética 1 Introdução 2 Teoria 3 Resumo e aplicações
Ressonância Ferromagnética Ressonância Ferromagnética Deise Schäfer 14 de dezembro de 2011 Deise Schäfer 14 de dezembro de 2011 1 / 35 Ressonância Ferromagnética 1 Introdução 2 Teoria 3 Resumo e aplicações
ARTIGO ORIGINAL. Resumo INTRODUÇÃO. Kelser de Souza Kock 1,2, Maria Fernanda Nicolau 3, Cicero Inacio da Silva 4
 ARTIGO ORIGINAL Kelser de Souza Kock 1,2, Maria Fernanda Nicolau 3, Cicero Inacio da Silva 4 Resumo : INTRODUÇÃO que, de forma complementar ao raciocínio médico, possibilitam a determinação e o acompanhamento
ARTIGO ORIGINAL Kelser de Souza Kock 1,2, Maria Fernanda Nicolau 3, Cicero Inacio da Silva 4 Resumo : INTRODUÇÃO que, de forma complementar ao raciocínio médico, possibilitam a determinação e o acompanhamento
Aula-11. (quase) Tudo sobre os átomos
 Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Aula-11 (quase) Tudo sobre os átomos Algumas propriedades: Átomos são estáveis (quase sempre) Os átomos se combinam (como o fazem é descrito pela mecânica quântica) Os átomos podem ser agrupados em famílias
Conversão de energia Mitocôndria - Respiração
 Universidade de São Paulo (USP) Escola de Engenharia de Lorena (EEL) Engenharia Ambiental Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Conversão de
Universidade de São Paulo (USP) Escola de Engenharia de Lorena (EEL) Engenharia Ambiental Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Conversão de
Métodos de diagnósticos por imagem do tumor cerebral astrocitário
 Métodos de diagnósticos por imagem do tumor cerebral astrocitário Natália Botão Lemos 1, Marjorie do Val Ietsugu 2 1 Graduanda do curso de Tecnologia em Radiologia - Faculdade de Tecnologia FATEC Botucatu,
Métodos de diagnósticos por imagem do tumor cerebral astrocitário Natália Botão Lemos 1, Marjorie do Val Ietsugu 2 1 Graduanda do curso de Tecnologia em Radiologia - Faculdade de Tecnologia FATEC Botucatu,
Metabolismo de aminoácidos de proteínas
 Metabolismo de aminoácidos de proteínas Profa Dra Mônica Santos de Freitas 12.09.2012 1 transporte DE AMINOÁCIDOS DENTRO DA CÉLULA O metabolismo de aminoácidos ocorre dentro da célula; A concentração intracelular
Metabolismo de aminoácidos de proteínas Profa Dra Mônica Santos de Freitas 12.09.2012 1 transporte DE AMINOÁCIDOS DENTRO DA CÉLULA O metabolismo de aminoácidos ocorre dentro da célula; A concentração intracelular
QBQ-0230 Bioquímica do Metabolismo Biologia Noturno
 QBQ-0230 Bioquímica do Metabolismo Biologia Noturno O que é, e para que serve a vias das pentoses fosfato. A via das pentoses fosfato é uma via alternativa de oxidação da glicose. A via das pentoses fosfato
QBQ-0230 Bioquímica do Metabolismo Biologia Noturno O que é, e para que serve a vias das pentoses fosfato. A via das pentoses fosfato é uma via alternativa de oxidação da glicose. A via das pentoses fosfato
Medição. Os conceitos fundamentais da física são as grandezas que usamos para expressar as suas leis. Ex.: massa, comprimento, força, velocidade...
 Universidade Federal Rural do Semi Árido UFERSA Pro Reitoria de Graduação PROGRAD Disciplina: Mecânica Clássica Professora: Subênia Medeiros Medição Os conceitos fundamentais da física são as grandezas
Universidade Federal Rural do Semi Árido UFERSA Pro Reitoria de Graduação PROGRAD Disciplina: Mecânica Clássica Professora: Subênia Medeiros Medição Os conceitos fundamentais da física são as grandezas
PLANO DE TRABALHO: TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA I
 PLANO DE TRABALHO: TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA I PROFESSOR: Rodrigo Modesto Gadelha Gontijo 1. EMENTA: Introdução de conhecimentos básicos sobre o equipamento de Ressonância Magnética, seu funcionamento
PLANO DE TRABALHO: TECNOLOGIA EM RESSONÂNCIA MAGNÉTICA I PROFESSOR: Rodrigo Modesto Gadelha Gontijo 1. EMENTA: Introdução de conhecimentos básicos sobre o equipamento de Ressonância Magnética, seu funcionamento
Descoberta do Núcleo
 Unidade 3 Núcleo Atômico Descoberta do Núcleo Propriedades dos Núcleos Forças Nucleares Estabilidade Nuclear Ressonância Magnética Nuclear Consultas http://hyperphysics.phy-astr.gsu.edu/hbase/nuccon.html#nuccon
Unidade 3 Núcleo Atômico Descoberta do Núcleo Propriedades dos Núcleos Forças Nucleares Estabilidade Nuclear Ressonância Magnética Nuclear Consultas http://hyperphysics.phy-astr.gsu.edu/hbase/nuccon.html#nuccon
Lista de Exercícios 3 Corrente elétrica e campo magnético
 Lista de Exercícios 3 Corrente elétrica e campo magnético Exercícios Sugeridos (16/04/2007) A numeração corresponde ao Livros Textos A e B. A22.5 Um próton desloca-se com velocidade v = (2i 4j + k) m/s
Lista de Exercícios 3 Corrente elétrica e campo magnético Exercícios Sugeridos (16/04/2007) A numeração corresponde ao Livros Textos A e B. A22.5 Um próton desloca-se com velocidade v = (2i 4j + k) m/s
Fontes de Campo Magné0co
 FONTES Fontes de Campo Magné0co * Imã e * corrente elétrica (movimento de carga elétrica) Fio reto Espira circular Solenóide LINHAS Densidade de linhas n o de linhas α B área (Gauss) spin * Microscopicamente
FONTES Fontes de Campo Magné0co * Imã e * corrente elétrica (movimento de carga elétrica) Fio reto Espira circular Solenóide LINHAS Densidade de linhas n o de linhas α B área (Gauss) spin * Microscopicamente
Profª Eleonora Slide de aula. Revisão: Termodinâmica e Bioenergética
 Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Revisão: Termodinâmica e Bioenergética Revisão:Termodinâmica As leis da termodinâmica governam o comportamento de s bioquímicos As leis da termodinâmica são princípios gerais aplicados a todos os processos
Medição dimensional e de movimento. Dr. Evandro Leonardo Silva Teixeira Faculdade Gama
 Dr. Evandro Leonardo Silva Teixeira Faculdade Gama Sensor por efeito piezo-elétrico: Funciona a partir do efeito piezo-elétrico; Fenômeno físico reversível; Fornece tensão com a deformação do elemento
Dr. Evandro Leonardo Silva Teixeira Faculdade Gama Sensor por efeito piezo-elétrico: Funciona a partir do efeito piezo-elétrico; Fenômeno físico reversível; Fornece tensão com a deformação do elemento
02/06/2013. Espectros de RMN com desacoplamento de spin: técnica comum em espectroscopia de 13 C
 0/0/0 Princípio básico de desacoplamento de spin: saturar a transição do núcleo responsável pelo acoplamento Espectros de RMN com desacoplamento de spin: técnica comum em espectroscopia de C (a) Representação
0/0/0 Princípio básico de desacoplamento de spin: saturar a transição do núcleo responsável pelo acoplamento Espectros de RMN com desacoplamento de spin: técnica comum em espectroscopia de C (a) Representação
Organelas Transdutoras de Energia: Mitocôndria - Respiração
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
Espectrometria de Ressonância Magnética Nuclear
 Espectrometria de Ressonância Magnética Nuclear 2002 - Prof. Hamilton M. Viana 1 Introdução Semelhante ao IR, Ação do campo magnético Absorção de radiação eletromagnética Espectro freqüências x intensidades
Espectrometria de Ressonância Magnética Nuclear 2002 - Prof. Hamilton M. Viana 1 Introdução Semelhante ao IR, Ação do campo magnético Absorção de radiação eletromagnética Espectro freqüências x intensidades
no âmbito da história da Física Moderna e suas atuais aplicaçõ
 A Ressonância ncia Magnética Nuclear no âmbito da história da Física Moderna e suas atuais aplicaçõ ções Tito J. Bonagamba LEAR / IFSC / USP Ressonância Magnética Nuclear (RMN) História Ressonância Magnética
A Ressonância ncia Magnética Nuclear no âmbito da história da Física Moderna e suas atuais aplicaçõ ções Tito J. Bonagamba LEAR / IFSC / USP Ressonância Magnética Nuclear (RMN) História Ressonância Magnética
Este será o primeiro Ensaio Interlaboratorial em Etanol Combustível a usar a Norma ABNT NBR ISO 4259:2008.
 Comparação Interlaboratorial da Concentração de Ferro, Cobre e Sódio em Álcool Etílico Combustível pelo método da Espectrofotometria de Absorção Atômica 1. Introdução Nos trabalhos de revisão da Norma
Comparação Interlaboratorial da Concentração de Ferro, Cobre e Sódio em Álcool Etílico Combustível pelo método da Espectrofotometria de Absorção Atômica 1. Introdução Nos trabalhos de revisão da Norma
Organelas e suas funções. A energética celular:
 Organelas e suas funções Capitulo 15- Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular: Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição
Organelas e suas funções Capitulo 15- Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular: Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição
