Estrutura Atômica - Prof. J. D. Ayala - 1 -
|
|
|
- Ayrton Geovane Bergler Salgado
- 7 Há anos
- Visualizações:
Transcrição
1 Estrutura Atômica - Prof. J. D. Ayala MODELO ATÔMICO PLANETÁRIO Supondo que o elétron tem uma massa m, desprezível em relação ao núcleo, cuja carga é Ze. Neste caso o núcleo permanecerá em repouso e o elétron gira ao redor deste em uma órbita de raio r com velocidade v. Portanto a energia total do elétron é a soma de suas E c e E p. E = E c + E p...(1) E c 1 dx = m...() dt E p qq' = κ...(3) r como q = Ze ; q = -e κ = 8,98755x10 9 J C m -1 (constante de Coulomb) E p Ze = κ...(3b) r portanto: 1 Ze E = mv - k...(4) r De acordo com a segunda lei de Newton, a força elétrica é: F e = m a...(5) onde a = aceleração = v /r e substituindo a lei de Coulomb em (5) temos: Ze mv κ =...(6) r r simplificando, temos: κze = r mv...(7) Comparando a equação (1) com a (3b), tem-se: -E p = E c...(8) portanto podemos escrever a energia total em função de E c ou E p : E = -Ec = ou 1 mv...(9) E = E p κze =...(10) r A energia deste modelo atômico é negativa, pois quando: r aumenta, E zero (equação 10) v diminui, E zero (equação 9)
2 Estrutura Atômica - Prof. J. D. Ayala - - Bor postulou que o momento angular é: mvr = n n = 1,, (11) onde n é o número quântico de Bor e = π Combinando as equação (7) e (11), temos: n = com n = 1,, 3,......(1) 4π κze m rn substituindo-se todas as constantes física, temos: r n 11 n = 5,9x10...(13) Z onde 5,9x10-11 m é denominado raio de Bor (a o ) a = 4π κe m = κe m εo = πme portanto o...(14) 1 ε o = (permissividade do vácuo)...(15) 4πκ portanto: n r = a o...(16) Z Como a freqüência do elétron em sua órbita está relacionada com a energia e a energia total depende da energia potencial (equação 10), podemos escrever a equação da energia em função do raio: 4 π κ Z e m E = n = 1,, 3,...(17) n ou melor, podemos escreve-la em função de a o : 4π κe m kz e E =. n...(18) κz e 1 E =. a n o
3 Estrutura Atômica - Prof. J. D. Ayala DUALIDADE ONDA-PARTÍCULA Luis Victor de Broglie calculou o comprimento de onda de partículas em movimento: λ = =...(19) mv p Esta equação fundamenta o conceito da dualidade onda-partícula, ou seja, todas as partículas de matéria em movimento também devem apresentar propriedades ondulatórias. (ver equação 11) O PRINCÍPIO DE INCERTEZA Para localizar um elétron com a ajuda de um fóton, deve aver uma colisão entre os dois. Um fóton de comprimento de onda λ possui um momento p = /λ sendo que uma fração qualquer do momento do fóton será transferida para o elétron no instante da colisão. Ao determinar a posição do elétron com uma precisão x ±λ, produz-se uma incerteza no seu momento, equivalente a p., λ portanto: p. x. λ = (Princípio de Incerteza de Heisenberg) λ
4 Estrutura Atômica - Prof. J. D. Ayala EQUAÇÃO DE SCHRÖDIGER Pela mecânica clássica: E = E c + E p...(1) 1 dx E = m c...() dt e como o momento é dado por p = m.v, podemos escrever a equação (1) como: p E = + E p...(1) m aplicando-se um operador no momento p, temos: d p...() i dx p d d = -...(3) i dx dx portanto a energia pode ser escrita como: d E = + E m dx p...(4) d O termo é somente um operador, ou seja, um símbolo matemático que nos diz m dx especificamente o que faz a função ψ, portanto, a equação 4 deve ser escrita como: Eψ = m d ψ + E dx p ψ...(5) Esta equação representa a equação de Scrödinger independente do tempo e unidimensional da função de onda a qual descreve a propriedade de onda da partícula de massa m. Em três dimensões temos: m ψ + (E E p ) ψ = 0...(6) onde é o operador de transformada de Laplace, ou seja, uma equação diferencial de segunda ordem: x y z = (7) portanto, a equação 6 fica: m + E p z x,y, ou simplesmente: ψ = Eψ...(8)
5 Estrutura Atômica - Prof. J. D. Ayala H ψ = Eψ...(9) Onde: H Operador amiltoniano ψ Função de onda de um corpo no espaço (três coordenadas: x, y e z) A função de onde ψ deve satisfazer certas condições: 1 - Deve apresentar um valor único, contínuo e diferencial em todos os pontos do espaço; - Deve ser finita para todos os valores de x, y e z; 3 - Deve ser normalizada. Isto significa que ψ dτ = 1, ou seja, a integral do quadrado da função de onda sobre todo espaço deve ser igual a 1. ψ não tem uma interpretação física, pois não apresenta necessariamente valores reais, pode ser uma função complexa, porém, o quadrado de um número complexo se define como o produto dele pelo seu conjugado: a + ib = (a +ib).(a - ib) = a + b (sempre real), sendo assim, ψ (ou ψψ*) calculado para um ponto particular em um instante particular é proporcional à probabilidade de encontrar experimentalmente o corpo naquele lugar e naquele instante. + ψ dv...(30) Esta integral não pode ser negativa nem i e se for: 0 a partícula não existe a partícula estará em toda parte simultaneamente ORBITAIS ATÔMICOS PARA ÁTOMOS HIDROGENÓIDES O objeto modelo que representa um átomo de idrogênio consiste de um núcleo, de massa M e carga Ze e um elétron, com massa m e e carga -e, separados por uma distância r. Ambas partículas se consideram como cargas pontuais, portanto a equação de Scrödinger será: M N m e e Ze κ r ψ = E T ψ...(31) Nesta equação, ψ é função de seis coordenadas, ou seja, x N, y N e z N (coordenadas no núcleo) e x e, y e e z e (coordenadas do elétron). Scrödinger mostrou que a mudança destas seis coordenadas por um conjunto adequado de outras seis coordenadas, conduz a separação da equação 31 em duas partes: uma expressa e determina o movimento translação do átomo e a outra, fundamentalmente eletrônica, que descreve o movimento
6 Estrutura Atômica - Prof. J. D. Ayala relativo do elétron respeito ao núcleo, ou seja, a função de onda ψ pode ser expressa como o produto da função ψ N, que depende das coordenadas do centro de massa do átomo (X, Y e Z) respeito a uma origem arbitrária e por uma função ψ, eletrônica, das coordenadas relativas do elétron (x, y e z) como mostra a figura a seguir: As coordenadas polares esféricas r, θ, φ em um ponto P apresenta as seguintes interpretações: r = x + + y z comprimento do raio vetor da origem O (+Ze) ao ponto P (-e) θ = ângulo entre o raio vetor e o eixo +z (ângulo zenital) φ = arc tg x y ângulo entre a projeção do raio vetor no plano xy e o eixo +x, medido na direção antiorário (ângulo azimutal) x = r sin θ cos φ y = r sin θ sin φ z = r cos θ Portanto a equação de Scrödinger torna-se:
7 Estrutura Atômica - Prof. J. D. Ayala ψ 1 ψ 1 ψ µ Ze r sen( ) E + = θ + + r r r r sen( ) r sen ( ) + κ r θ θ θ θ φ ψ Rearranjando, temos: 0...(3) sen θ r r ψ + sen θ r θ ψ ψ µ r sen sen θ + + θ φ θ Z e 4 π ε o + E ψ = 0 r...(33) onde: m em µ =, ou seja, a massa reduzida do sistema núcleo-elétron (9,10458x10-31 kg para o idrogênio) m + M e A equação 33 é uma equação a derivadas parciais para a função de onda ψ do elétron em um átomo de idrogênio. Juntamente com as várias condições às quais ψ deve obedecer, ou seja, ψ tem apenas um e somente um valor para cada ponto r, θ,φ. Esta equação escrita em coordenadas polares esféricas, é facilmente separada em três equações independentes, cada qual envolvendo apenas uma única variável, ou seja: R(r) que depende apenas de r; Θ(θ) que depende apenas de θ e Φ(φ) que depende apenas de φ, portanto a função de onda do elétron é dada por: ψ(r,θ,φ) = R(r) Θ(θ) Φ(φ)... (34) A função R(r) descreve como ψ do elétron varia ao longo do raio vetor a partir do núcleo com θ e φ. A função Θ(θ) descreve como ψ varia com o ângulo zenital θ ao longo de um meridiano sobre a esfera centrada no núcleo, com r e φ constantes. A função Φ(φ) descreve como ψ varia com o ângulo azimutal φ ao longo de um paralelo sobre uma esfera centrada no núcleo, com r e θ constantes. O produto entre as funções Θ(θ) e Φ(φ) é igual a função Y, camada armônica esférica, que é função de θ, φ e dos números quânticos l (Número Quântico Momento Angular Orbital) e m l, (Número Quântico Orbital Magnético), enquanto que R é função apenas dos números quânticos n (Número Quântico Principal) e l, portanto podemos escrever a equação 34 como: ml ψ n, l,m = R l n, l.yl...(35) O valor de R n, l calculado pela mecânica quântica vem dado por: 1 3 Z (n l 1)! ρ l l+ 1 R n, (r) e ρ L n ( ρ) 3 na l = + l...(36) o [(n + )!] n l onde:
8 Zr ρ = ; a o Estrutura Atômica - Prof. J. D. Ayala l+ L 1 + l ( ρ) é o polinômio associado de Laguerre, dado por: n b a L ( ρ) = ( 1) a a! ρ (a b)! (a b) a(a b) ρ 1! (a b 1) a(a 1)(a b)(a b 1) + ρ! (a b ) a(a )(a 1)(a b)(a b 1)(a b ) ρ 3! (a b 3) +... A tabela a seguir mostra alguns valore da função radial do átomo de idrogênio: Probabilidade de Encontrar o Elétron Para determinar a probabilidade que tem o elétron de se encontrar à distância r do núcleo, devemos integrar todos os elementos de volume entre r e r+dr. Tal probabilidade é: P = R dv...(37) Onde dv é o volume da casca esférica compreendida entre r e r+dr (figura abaixo); P é a probabilidade radial independente de θ e φ, portanto o volume da casca esférica dv (dr 0) vem dado por: dv = 4πr dr...(38) portanto, a equação 37 fica:
9 Estrutura Atômica - Prof. J. D. Ayala P = R l 4πr dr...(39) n As funções de distribuição radial (densidades radiais), calculadas pela equação 39 para R 10 a R 3 são mostradas na figura a seguir. Podemos observar que o número de picos vem dado por n-l. Estes picos são regiões de alta densidade eletrônica. As regiões de alta densidade eletrônica são separadas por nodos; os nodos são regiões onde a densidade eletrônica é nula (P = 0). As funções de distribuição eletrônica são de muito interesse na discussão do efeito de blindagem dos elétrons nos átomos com muitos elétrons. Para uma dada carga nuclear, à medida que o número quântico principal aumenta, as regiões de alta densidade eletrônica se estendem cada vez mais além do núcleo. Pela mecânica quântica, encontramos que o valor médio do raio é dado por: a o r = [3n Z l ( l+ 1)]...(40)
10 Estrutura Atômica - Prof. J. D. Ayala
11 Estrutura Atômica - Prof. J. D. Ayala Examinando a figura anterior, onde n é constante, nota-se que muito embora a localização mais provável de um elétron 3d seja mais próxima do núcleo que um elétron 3p e 3s, a densidade eletrônica mais próxima ao núcleo é maior para o orbital 3s do que 3p e 3d. Em virtude disto, dizemos que o elétron 3s penetra mais próximo ao núcleo do que um elétron 3p ou 3d. O orbital 3s tem três densidades eletrônicas, 3p, duas e 3d uma. Podemos generalizar e dizer que o poder de penetração dos orbitais segue a ordem: s > p > d > f > g > >... A função ml Y descreve a forma de uma onda estacionária em três dimensões. Fazendo-se l uma alanogia com uma mola, ml Y dá informações análogas ao número de nodos, anti-nodos e amplitude l de vibração estacionária da mola. 1 (ml+ ml ) m (l+ 1) ( l m )! l l im lφ ml Y l = ( 1) e Pl (cos( θ))...(41) 4π ( l+ m l )! onde P m l l (cos( θ)) são as funções associadas de Legendre de primeira classe. ml As tabelas a seguir mostram alguns valores para a função Y. l
12 radial R 10 e a angular = R100Y0 Estrutura Atômica - Prof. J. D. Ayala Para construirmos a função de onda eletrônica 1s devemos obter o produto entre a função 0 Y 0 : ψ...(4) ψ 100 = Z a o 3 e 1 4π Zr a o 1...(4a) Como podemos notar, a função de onda ψ 100, bem como ψ n00, são independentes de θ e φ, ou seja, a armônica esférica é sempre constate 1 4 π 1 para qualquer direção especificada pelos ângulos θ e φ, portanto o gráfico destas funções em coordenadas esféricas polares sempre será uma esfera centrada na origem, como podemos observar na figura abaixo: probabilidade. O quadrado desta função representa a contribuição da parte angular do orbital na densidade de
13 Estrutura Atômica - Prof. J. D. Ayala
14 Estrutura Atômica - Prof. J. D. Ayala
15 Estrutura Atômica - Prof. J. D. Ayala As distribuições dos orbitais p são cilindricamente simétricas. Os mapas de contorno para os orbitais p z e 3p z são mostrados nas figuras a seguir: Os três orbitais p de um dado n é designado como np x, np y e np z, os subscritos indicam os eixos onde cada orbital está localizado.
16 Estrutura Atômica - Prof. J. D. Ayala Funções d Existem seis funções d idênticas, exceto nas suas orientações espaciais que satisfazem a solução da equação de Scrödinger para um átomo idrogenóide. Um mapa de contorno para uma das funções d é mostrado na figura a seguir: Cada uma destas funções têm quatro lóbulos direcionados aos vértices de um quadrado. Destas, duas funções semelantes encontram-se em cada plano cartesiano, as quais ambos lóbulos estão ao longo dos eixos ou planos cartesianos. funções. Como só pode existir cinco orbitais d, estes são constituídos como combinação linear das seis Os orbitais d xy, d xz e d yz, apresentam, respectivamente, lóbulos nos planos xy, xz e yz e o orbital d apresenta o lóbulos ao longo dos eixos x e y. O quinto orbital d ( d ) é um íbrido, ou seja, x y é a combinação das funções d e d, portanto, este orbital ( d ) consiste de dois lóbulos z x z y z x y principais ao longo do eixo z e uma tumefação (incaço) acomodada no plano xy. Nota-se que os orbitais 3d apresentam duas superfícies nodais passando através núcleo, enquanto que no orbital 3 d as superfícies nodais são convertidas em cones com ápice no núcleo. z As figuras a seguir mostram os cinco tipos de orbitais d. z
17 Estrutura Atômica - Prof. J. D. Ayala
18 Estrutura Atômica - Prof. J. D. Ayala A figura a seguir mostra os sete tipos de orbitais f.
Comportamento ondulatório da matéria
 Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Problemas de Duas Partículas
 Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2,
7. A teoria quântica do átomo de Hidrogênio
 7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
7. A teoria quântica do átomo de Hidrogênio Sumário A equação de Schrödinger para o átomo de hidrogênio Autovalores de energia Números quânticos Momento de dipolo magnético Autofunções de energia Orbitais
Equação de Schrödinger em 3D
 Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
UNIVERSIDADE DE SÃO PAULO
 UNIVERSIDADE DE SÃO PAULO - Instituto de Química - Estrutura Atômica As propriedades ondulatórias do elétron Hermi F. Brito hefbrito@iq.usp.br QFL 1101 Química Geral I, -03-2017 Dualidade onda-partícula
UNIVERSIDADE DE SÃO PAULO - Instituto de Química - Estrutura Atômica As propriedades ondulatórias do elétron Hermi F. Brito hefbrito@iq.usp.br QFL 1101 Química Geral I, -03-2017 Dualidade onda-partícula
h mc 2 =hν mc 2 =hc/ λ
 Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Estrutura atômica. Modelo quântico do átomo
 Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento angular bem definido
 ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
B) [N] é uma constante de normalização indicando que a probabilidade de encontrar o elétron em qualquer lugar do espaço deve ser unitária. R n,l (r) é
![B) [N] é uma constante de normalização indicando que a probabilidade de encontrar o elétron em qualquer lugar do espaço deve ser unitária. R n,l (r) é B) [N] é uma constante de normalização indicando que a probabilidade de encontrar o elétron em qualquer lugar do espaço deve ser unitária. R n,l (r) é](/thumbs/71/66033065.jpg) QUÍMICA I AULA 04: ESTRUTURA ELETRÔNICA DOS ÁTOMOS TÓPICO 05: ORBITAL ATÔMICO 5.1 A EQUAÇÃO DE SCHRODINGER E O ÁTOMO DE HIDROGÊNIO: Como o elétron tem propriedades ondulatórias, ele pode ser descrito como
QUÍMICA I AULA 04: ESTRUTURA ELETRÔNICA DOS ÁTOMOS TÓPICO 05: ORBITAL ATÔMICO 5.1 A EQUAÇÃO DE SCHRODINGER E O ÁTOMO DE HIDROGÊNIO: Como o elétron tem propriedades ondulatórias, ele pode ser descrito como
Mecânica Quântica. Química Quântica Prof a. Dr a. Carla Dalmolin. A Equação de Schrödinger Postulados da Mecânica Quântica
 Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin A Equação de Schrödinger Postulados da Mecânica Quântica Mecânica Clássica O movimento de uma partícula é governado pela Segunda Lei de Newton:
Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin A Equação de Schrödinger Postulados da Mecânica Quântica Mecânica Clássica O movimento de uma partícula é governado pela Segunda Lei de Newton:
Fundamentos de Química Quântica
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
PROPRIEDADES ONDULATÓRIAS DO ELÉTRON
 MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
Modelos Atômicos e Princípios Quânticos Parte II
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: miranda@vm.uff.br
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
Escola Politécnica FAP GABARITO DA P3 25 de novembro de 2008
 P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
P3 Física IV Escola Politécnica - 2008 FAP 2204 - GABARITO DA P3 25 de novembro de 2008 Questão 1 É realizado um experimento onde fótons são espalhados por elétrons livres inicialmente em repouso. São
Estrutura Atômica I. Química Quântica Prof a. Dr a. Carla Dalmolin. Átomo de Hidrogênio Átomos Hidrogenóides
 Estrutura Atômica I Química Quântica Prof a. Dr a. Carla Dalmolin Átomo de Hidrogênio Átomos Hidrogenóides Aplicações da Mecânica Quântica Soluções da Equação de Schrödinger independente do tempo Partícula
Estrutura Atômica I Química Quântica Prof a. Dr a. Carla Dalmolin Átomo de Hidrogênio Átomos Hidrogenóides Aplicações da Mecânica Quântica Soluções da Equação de Schrödinger independente do tempo Partícula
+ E p. ψ(x) = E. ψ(x)
 Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
Partícula na Caixa. Química Quântica Prof a. Dr a. Carla Dalmolin
 Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
1 O Átomo de Hidrogênio
 O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas Equação de Schrödinger em 3D: 2 = 1 r 2 # % r $ r2 r & (+ ' 1 r 2 senθ # θ senθ & % (+ $ θ ' 1 r 2 sen 2 θ 2 φ 2 Podemos, então, escrever a eq. de Schrödinger
A eq. de Schrödinger em coordenadas esféricas Equação de Schrödinger em 3D: 2 = 1 r 2 # % r $ r2 r & (+ ' 1 r 2 senθ # θ senθ & % (+ $ θ ' 1 r 2 sen 2 θ 2 φ 2 Podemos, então, escrever a eq. de Schrödinger
pessoal.utfpr.edu.br/renan
 Aula 2: Espectro de emissão do hidrogênio: Balmer e Rydberg O átomo de Bohr Princípio da incerteza Partícula na caixa Prof. Renan Borsoi Campos pessoal.utfpr.edu.br/renan O espectro eletromagnético da
Aula 2: Espectro de emissão do hidrogênio: Balmer e Rydberg O átomo de Bohr Princípio da incerteza Partícula na caixa Prof. Renan Borsoi Campos pessoal.utfpr.edu.br/renan O espectro eletromagnético da
Exame Unificado das Pós-graduações em Física EUF
 Exame Unificado das Pós-graduações em Física EUF º Semestre/01 Parte 1 4/04/01 Instruções: NÃO ESCREVA O SEU NOME NA PROVA. Ela deverá ser identificada apenas através do código (EUFxxx). Esta prova constitui
Exame Unificado das Pós-graduações em Física EUF º Semestre/01 Parte 1 4/04/01 Instruções: NÃO ESCREVA O SEU NOME NA PROVA. Ela deverá ser identificada apenas através do código (EUFxxx). Esta prova constitui
Teoria da Ligação Química. Radiação electromagnética. ν =
 Teoria da Ligação Química Radiação electromagnética λxν=c ν = 1 λ Mecânica clássica : 1. Uma partícula move-se numa trajectória com um caminho e uma velocidade precisos em cada instante.. A uma partícula
Teoria da Ligação Química Radiação electromagnética λxν=c ν = 1 λ Mecânica clássica : 1. Uma partícula move-se numa trajectória com um caminho e uma velocidade precisos em cada instante.. A uma partícula
Função de Onda e Equação de Schrödinger
 14/08/013 Função de Onda e Equação de Schrödinger Prof. Alex Fabiano C. Campos, Dr A Função de Onda (ψ) A primeira formulação para esta nova interpretação da Mecânica, a Mecânica Quântica, teoria foi proposta
14/08/013 Função de Onda e Equação de Schrödinger Prof. Alex Fabiano C. Campos, Dr A Função de Onda (ψ) A primeira formulação para esta nova interpretação da Mecânica, a Mecânica Quântica, teoria foi proposta
Física Quântica. Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio. Pieter Westera
 Física Quântica Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html A Equação
Física Quântica Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio Pieter Westera pieter.westera@ufabc.edu.br http://professor.ufabc.edu.br/~pieter.westera/quantica.html A Equação
FNC376N: Lista de março de ψ r ψ = Eψ. sin θ Y )
 FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
24/Abr/2014 Aula /Abr/2014 Aula 15
 /Abr/014 Aula 15 Ondas de matéria; comprimento de onda de de Broglie. Quantização do momento angular no modelo de Bohr. Difracção e interferência. Função de onda; representação matemática do pacote de
/Abr/014 Aula 15 Ondas de matéria; comprimento de onda de de Broglie. Quantização do momento angular no modelo de Bohr. Difracção e interferência. Função de onda; representação matemática do pacote de
Física IV - FAP2204 Escola Politécnica GABARITO DA P3 8 de dezembro de 2009
 P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
P3 Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA P3 8 de dezembro de 2009 Questão 1 Numaexperiência deespalhamentocompton, umelétrondemassam 0 emrepousoespalha um fóton de comprimento de onda
Vimos que a radiação eletromagnética comportase como onda e partícula Dualidade ondapartícula da radiação eletromagnética
 Estrutura eletrônica dos átomos Vimos que a radiação eletromagnética comportase como onda e partícula Dualidade ondapartícula da radiação eletromagnética Onda Com propriedades como comprimento de onda,
Estrutura eletrônica dos átomos Vimos que a radiação eletromagnética comportase como onda e partícula Dualidade ondapartícula da radiação eletromagnética Onda Com propriedades como comprimento de onda,
Parte II. Interacção Radiação-Matéria: Espectroscopia Molecular. Cap. 4 Introdução à Mecânica Quântica. Estrutura Molecular
 Parte II Interacção Radiação-Matéria: Espectroscopia Molecular Cap. 4 Introdução à Mecânica Quântica. Estrutura Molecular E z Onda Electromagnética (onda progressiva) onda estacionária H x Velocidade da
Parte II Interacção Radiação-Matéria: Espectroscopia Molecular Cap. 4 Introdução à Mecânica Quântica. Estrutura Molecular E z Onda Electromagnética (onda progressiva) onda estacionária H x Velocidade da
Universidade de São Paulo em São Carlos Mecânica Quântica Aplicada Prova 1
 Universidade de São Paulo em São Carlos 9514 Mecânica Quântica Aplicada Prova 1 Nome: Questão 1: Sistema de dois níveis (3 pontos) Considere um sistema de dois estados 1 e ortonormais H do sistema seja
Universidade de São Paulo em São Carlos 9514 Mecânica Quântica Aplicada Prova 1 Nome: Questão 1: Sistema de dois níveis (3 pontos) Considere um sistema de dois estados 1 e ortonormais H do sistema seja
Lista de Exercícios 1: Eletrostática
 Lista de Exercícios 1: Eletrostática 1. Uma carga Q é distribuída uniformemente sobre um fio semicircular de raio a, que está no plano xy. Calcule a força F com que atua sobre uma carga de sinal oposto
Lista de Exercícios 1: Eletrostática 1. Uma carga Q é distribuída uniformemente sobre um fio semicircular de raio a, que está no plano xy. Calcule a força F com que atua sobre uma carga de sinal oposto
Física IV - FAP2204 Escola Politécnica GABARITO DA PS 15 de dezembro de 2009
 PS Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA PS 15 de dezembro de 2009 Questão 1 Considere os campos elétrico E = (0,E y,0) e magnético B = (0,0,B z ) onde E y (x,t) = A e a(x ct) e B z
PS Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA PS 15 de dezembro de 2009 Questão 1 Considere os campos elétrico E = (0,E y,0) e magnético B = (0,0,B z ) onde E y (x,t) = A e a(x ct) e B z
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Físico-Química 01 Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 2014 Prof. Dr. Anselmo E
Física IV Poli Engenharia Elétrica: 12ª Aula (25/09/2014)
 Física IV Poli Engenaria Elétrica: 1ª Aula (5/9/14) Prof. Alvaro Vannucci Na última aula vimos: Modelo de Bor para o átomo de idrogênio: órbitas permitidas são as que possuem momento angular: L r p mvr
Física IV Poli Engenaria Elétrica: 1ª Aula (5/9/14) Prof. Alvaro Vannucci Na última aula vimos: Modelo de Bor para o átomo de idrogênio: órbitas permitidas são as que possuem momento angular: L r p mvr
AS ONDAS ESTACIONÁRIAS
 AS ONDAS ESTACIONÁRIAS Comportamento de um elétron em um átomo: semelhante ao de uma onda estacionária tridimensional. Onda estacionária: não se movimenta em uma única direção (ao contrário de uma onda
AS ONDAS ESTACIONÁRIAS Comportamento de um elétron em um átomo: semelhante ao de uma onda estacionária tridimensional. Onda estacionária: não se movimenta em uma única direção (ao contrário de uma onda
4 e 6/Maio/2016 Aulas 17 e 18
 9/Abril/016 Aula 16 Princípio de Incerteza de Heisenberg. Probabilidade de encontrar uma partícula numa certa região. Posição média de uma partícula. Partícula numa caixa de potencial: funções de onda
9/Abril/016 Aula 16 Princípio de Incerteza de Heisenberg. Probabilidade de encontrar uma partícula numa certa região. Posição média de uma partícula. Partícula numa caixa de potencial: funções de onda
h (1 cos θ) onde, m e é a massa do elétron, θ é o ângulo pelo qual a direção do fóton muda λ 1 é o comprimento de onda do fóton antes do espalhamento,
 Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 09/06/2014 Nome do Candidato: Nível: Mestrado Doutorado 1. A função de
Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 09/06/2014 Nome do Candidato: Nível: Mestrado Doutorado 1. A função de
As Oscilações estão presentes no nosso dia a dia como o vento que balança uma linha de transmissão elétrica, as vibrações da membrana de um
 As Oscilações estão presentes no nosso dia a dia como o vento que balança uma linha de transmissão elétrica, as vibrações da membrana de um alto-falante, ou de um instrumento de percussão. Um terremoto
As Oscilações estão presentes no nosso dia a dia como o vento que balança uma linha de transmissão elétrica, as vibrações da membrana de um alto-falante, ou de um instrumento de percussão. Um terremoto
O átomo de Rutherford
 O átomo de Rutherford Elétrons orbitando o núcleo F Elétrica F Centrifúga Quando uma carga elétrica muda de velocidade ou direção, ela deve irradiar energia. Radiação Eletromagnética É o produto de campos
O átomo de Rutherford Elétrons orbitando o núcleo F Elétrica F Centrifúga Quando uma carga elétrica muda de velocidade ou direção, ela deve irradiar energia. Radiação Eletromagnética É o produto de campos
A Equação de Onda de Schröedinger. O Princípio da Incerteza de Heisenberg. λ =
 O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
Física IV Escola Politécnica PS 14 de dezembro de 2017
 Física IV - 432324 Escola Politécnica - 217 PS 14 de dezembro de 217 Questão 1 Uma espaçonave de comprimento próprio L move-se com velocidade,5 c em relação à Terra. Um meteorito, que também se move com
Física IV - 432324 Escola Politécnica - 217 PS 14 de dezembro de 217 Questão 1 Uma espaçonave de comprimento próprio L move-se com velocidade,5 c em relação à Terra. Um meteorito, que também se move com
Mecânica Analítica. Dinâmica Hamiltoniana. Licenciatura em Física. Prof. Nelson Luiz Reyes Marques MECÂNICA ANALÍTICA PARTE 2
 Mecânica Analítica Dinâmica Hamiltoniana Licenciatura em Física Prof. Nelson Luiz Reyes Marques Princípio de Hamilton O caminho real que uma partícula percorre entre dois pontos 1 e 2 em um dado intervalo
Mecânica Analítica Dinâmica Hamiltoniana Licenciatura em Física Prof. Nelson Luiz Reyes Marques Princípio de Hamilton O caminho real que uma partícula percorre entre dois pontos 1 e 2 em um dado intervalo
2. No instante t = 0, o estado físico de uma partícula livre em uma dimensão é descrito pela seguinte função de onda:
 Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 03/08/2011 Nome do Candidato: Nível: Mestrado Doutorado 1. No cálculo da
Universidade Federal do Pará Instituto de Ciências Exatas e Naturais Programa de Pós-Graduação em Física Exame de Seleção - Data: 03/08/2011 Nome do Candidato: Nível: Mestrado Doutorado 1. No cálculo da
Física IV Escola Politécnica GABARITO DA P3 25 de novembro de 2014
 Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Física IV - 4320402 Escola Politécnica - 2014 GABARITO DA P3 25 de novembro de 2014 Questão 1 Um elétron em repouso espalha um fóton incidente que possui comprimento de onda λ. Observa-se que o fóton espalhado
Rotor quântico. Quanticamente o rotor é descrito por uma função de onda, tal que: l A função de onda do estado estacionário é dada por:
 Rotor quântico Vamos tratar o caso da rotação de um corpo rígido, que corresponde a 2 massas pontuais, ligadas por uma barra rígida e sem massa. Consideremos rotação livre em torno de um eixo perpendicular
Rotor quântico Vamos tratar o caso da rotação de um corpo rígido, que corresponde a 2 massas pontuais, ligadas por uma barra rígida e sem massa. Consideremos rotação livre em torno de um eixo perpendicular
Estrutura da Matéria Prof. Fanny Nascimento Costa
 Estrutura da Matéria Prof. Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 07 Revisão da última aula Orbitais Números quânticos O átomo de hidrogênio Natureza ondulatória da luz Todas as ondas têm
Estrutura da Matéria Prof. Fanny Nascimento Costa (fanny.costa@ufabc.edu.br) Aula 07 Revisão da última aula Orbitais Números quânticos O átomo de hidrogênio Natureza ondulatória da luz Todas as ondas têm
E(r) = 2. Uma carga q está distribuída uniformemente por todo um volume esférico de raio R.
 1. O campo elétrico no interior de uma esfera não-condutora de raio R, com carga distribuída uniformemente em seu volume, possui direção radial e intensidade dada por E(r) = qr 4πɛ 0 R 3. Nesta equação,
1. O campo elétrico no interior de uma esfera não-condutora de raio R, com carga distribuída uniformemente em seu volume, possui direção radial e intensidade dada por E(r) = qr 4πɛ 0 R 3. Nesta equação,
Física III IQ 2014 ( )
 Atividade de treinamento - Introdução: Esta atividade tem dois objetivos: 1) Apresentar os conceitos de distribuições contínuas de carga e momento de dipolo ) Revisar técnicas de cálculo e sistemas de
Atividade de treinamento - Introdução: Esta atividade tem dois objetivos: 1) Apresentar os conceitos de distribuições contínuas de carga e momento de dipolo ) Revisar técnicas de cálculo e sistemas de
Sétima Lista. MAT0216 Cálculo Diferencial e Integral III Prof. Daniel Victor Tausk 14/04/2019
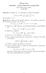 Sétima Lista MAT216 Cálculo iferencial e Integral III Prof. aniel Victor Tausk 14/4/219 Exercício 1. ados a, b, c >, determine o volume do elipsóide {(x, y, z) R 3 : x2 a 2 + y2 b 2 + z2 } c 2 1 de semi-eixos
Sétima Lista MAT216 Cálculo iferencial e Integral III Prof. aniel Victor Tausk 14/4/219 Exercício 1. ados a, b, c >, determine o volume do elipsóide {(x, y, z) R 3 : x2 a 2 + y2 b 2 + z2 } c 2 1 de semi-eixos
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
NÚMEROS QUÂNTICOS. As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons.
 NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
NÚMEROS QUÂNTICOS As teorias da MECÂNICA QUÂNTICA (Planck, De Broglie, Schrödinger e Heisenberg e outros), auxiliam na identificação dos elétrons. Prof. Ailey Aparecida Coelho Tanamati Mecânica = movimento
Física IV. Escola Politécnica FGE GABARITO DA PS 11 de dezembro de 2007
 PS Física IV Escola Politécnica - 2007 FGE 2203 - GABARITO DA PS 11 de dezembro de 2007 Questão 1 Um capacitor de placas paralelas é formado por dois discos circulares de raio a separados por uma distância
PS Física IV Escola Politécnica - 2007 FGE 2203 - GABARITO DA PS 11 de dezembro de 2007 Questão 1 Um capacitor de placas paralelas é formado por dois discos circulares de raio a separados por uma distância
Estrutura Eletrônica dos átomos
 Estrutura Eletrônica dos átomos 3- Os espectros de emissão dos gases Como a equação de Rydberg poderia ser explicada? Os estados de energia do átomo de hidrogênio Se n f é menor que n i, o e- move-se para
Estrutura Eletrônica dos átomos 3- Os espectros de emissão dos gases Como a equação de Rydberg poderia ser explicada? Os estados de energia do átomo de hidrogênio Se n f é menor que n i, o e- move-se para
A Estrutura Eletrônica dos Átomos. Prof. Fernando R. Xavier
 A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
Física IV Escola Politécnica GABARITO DA PR 4 de fevereiro de 2016
 Física IV - 43242 Escola Politécnica - 215 GABARITO DA PR 4 de fevereiro de 216 Questão 1 (I) Um farol A emite luz verde de frequência f 1 = 6 1 14 Hz. Outro farol B, em repouso em relação ao farol A,
Física IV - 43242 Escola Politécnica - 215 GABARITO DA PR 4 de fevereiro de 216 Questão 1 (I) Um farol A emite luz verde de frequência f 1 = 6 1 14 Hz. Outro farol B, em repouso em relação ao farol A,
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
TÓPICO. Fundamentos da Matemática II APLICAÇÕES DAS DERIVADAS PARCIAIS9. Licenciatura em Ciências USP/ Univesp. Gil da Costa Marques
 APLICAÇÕES DAS DERIVADAS PARCIAIS9 TÓPICO Gil da Costa Marques 9. Introdução 9. Derivadas com significado físico: o gradiente de um Campo Escalar 9.3 Equação de Euler descrevendo o movimento de um fluido
APLICAÇÕES DAS DERIVADAS PARCIAIS9 TÓPICO Gil da Costa Marques 9. Introdução 9. Derivadas com significado físico: o gradiente de um Campo Escalar 9.3 Equação de Euler descrevendo o movimento de um fluido
ATOMÍSTICA PROF. ADRIANO ALVES
 ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
ATOMÍSTICA PROF. ADRIANO ALVES Demócrito Aristóteles Dalton Thomson Bohr Rutherford Sommerfeld Heisenberg Schrödinger De Broglie DALTON 1. Toda matéria é formada de partículas fundamentais, os átomos.
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS Edição de agosto de 2008 CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS ÍNDICE 8.1- Introdução 8.2- Problema da Força Central
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS Edição de agosto de 2008 CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS ÍNDICE 8.1- Introdução 8.2- Problema da Força Central
Átomo de Hidrogênio 1
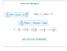 Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
1ª AULA ONDAS E PARTÍCULAS
 1ª AULA ONDAS E PARTÍCULAS 1) Caracterização de um corpúsculo em movimento ) Caracterização de uma onda progressiva 3) Relação de De Broglie 4) Princípio de Incerteza 1 Feixe de electrões Onde há? Tubos
1ª AULA ONDAS E PARTÍCULAS 1) Caracterização de um corpúsculo em movimento ) Caracterização de uma onda progressiva 3) Relação de De Broglie 4) Princípio de Incerteza 1 Feixe de electrões Onde há? Tubos
Aula de Física II - Cargas Elétricas: Força Elétrica
 Prof.: Leandro Aguiar Fernandes (lafernandes@iprj.uerj.br) Universidade do Estado do Rio de Janeiro Instituto Politécnico - IPRJ/UERJ Departamento de Engenharia Mecânica e Energia Graduação em Engenharia
Prof.: Leandro Aguiar Fernandes (lafernandes@iprj.uerj.br) Universidade do Estado do Rio de Janeiro Instituto Politécnico - IPRJ/UERJ Departamento de Engenharia Mecânica e Energia Graduação em Engenharia
Átomo de hidrogênio. Átomo de de Broglie Equação de Schrödinger Átomo de hidrogênio Transições de níveis
 Átomo de hidrogênio Átomo de de Broglie Equação de Schrödinger Átomo de hidrogênio Transições de níveis Teoria de Bohr para H Na teoria de Bohr, foi necessário postular a existência de números quânticos.
Átomo de hidrogênio Átomo de de Broglie Equação de Schrödinger Átomo de hidrogênio Transições de níveis Teoria de Bohr para H Na teoria de Bohr, foi necessário postular a existência de números quânticos.
Física IV Escola Politécnica GABARITO DA REC 14 de fevereiro de 2019
 Física IV - 43304 Escola Politécnica - 018 GABARITO DA REC 14 de fevereiro de 019 Questão 1 Luz monocromática de comprimento de onda λ incide sobre duas fendas idênticas, cujos centros estão separados
Física IV - 43304 Escola Politécnica - 018 GABARITO DA REC 14 de fevereiro de 019 Questão 1 Luz monocromática de comprimento de onda λ incide sobre duas fendas idênticas, cujos centros estão separados
Estrutura eletrônica dos átomos. Mestranda Daniele Potulski Disciplina Química Madeira I
 Estrutura eletrônica dos átomos Mestranda Daniele Potulski danielepotulski@ufpr.br Disciplina Química Madeira I Estrutura geral dos átomos -PRÓTONS situados no núcleo do átomo (representados por +) -NÊUTRONS
Estrutura eletrônica dos átomos Mestranda Daniele Potulski danielepotulski@ufpr.br Disciplina Química Madeira I Estrutura geral dos átomos -PRÓTONS situados no núcleo do átomo (representados por +) -NÊUTRONS
Física III Escola Politécnica GABARITO DA P1 9 de abril de 2015
 Física III - 4323203 Escola Politécnica - 205 GABARITO DA P 9 de abril de 205 uestão Considere o sistema abaixo, mantido fixo por forças externas, que consiste numa partícula pontual de carga q > 0 e massa
Física III - 4323203 Escola Politécnica - 205 GABARITO DA P 9 de abril de 205 uestão Considere o sistema abaixo, mantido fixo por forças externas, que consiste numa partícula pontual de carga q > 0 e massa
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
Série IV - Momento Angular (Resoluções Sucintas)
 Mecânica e Ondas, 0 Semestre 006-007, LEIC Série IV - Momento Angular (Resoluções Sucintas) 1. O momento angular duma partícula em relação à origem é dado por: L = r p a) Uma vez que no movimento uniforme
Mecânica e Ondas, 0 Semestre 006-007, LEIC Série IV - Momento Angular (Resoluções Sucintas) 1. O momento angular duma partícula em relação à origem é dado por: L = r p a) Uma vez que no movimento uniforme
ESTRUTURA ELETRÔNICA DOS ÁTOMOS
 ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
ESTRUTURA ELETRÔNICA DOS ÁTOMOS 2 Natureza ondulatória da luz 3 Natureza ondulatória da luz 4 Natureza ondulatória da luz 5 Natureza ondulatória da luz 6 Energia quantizada e fótons Planck quantum h é
Física III-A /1 Lista 3: Potencial Elétrico
 Física III-A - 2018/1 Lista 3: Potencial Elétrico Prof. Marcos Menezes 1. Qual é a diferença de potencial necessária para acelerar um elétron do repouso até uma velocidade igual a 40% da velocidade da
Física III-A - 2018/1 Lista 3: Potencial Elétrico Prof. Marcos Menezes 1. Qual é a diferença de potencial necessária para acelerar um elétron do repouso até uma velocidade igual a 40% da velocidade da
Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A /2 Data: 17/09/2018
 Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A - 2018/2 Data: 17/09/2018 Seção 1: Múltipla Escolha (7 0,8 = 5,6 pontos) 3. O campo elétrico
Universidade Federal do Rio de Janeiro Instituto de Física Primeira Prova (Diurno) Disciplina: Física III-A - 2018/2 Data: 17/09/2018 Seção 1: Múltipla Escolha (7 0,8 = 5,6 pontos) 3. O campo elétrico
QUÍMICA I. Teoria atômica Capítulo 6. Aula 2
 QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
Resposta: (A) o traço é positivo (B) o determinante é negativo (C) o determinante é nulo (D) o traço é negativo (E) o traço é nulo.
 MESTRADO INTEGRADO EM ENG. INFORMÁTICA E COMPUTAÇÃO 201/2018 EIC0010 FÍSICA I 1º ANO, 2º SEMESTRE 12 de junho de 2018 Nome: Duração 2 horas. Prova com consulta de formulário e uso de computador. O formulário
MESTRADO INTEGRADO EM ENG. INFORMÁTICA E COMPUTAÇÃO 201/2018 EIC0010 FÍSICA I 1º ANO, 2º SEMESTRE 12 de junho de 2018 Nome: Duração 2 horas. Prova com consulta de formulário e uso de computador. O formulário
Equação de Schrödinger
 Maria Inês Barbosa de Carvalho Equação de Schrödinger Apontamentos para a disciplina Física dos Estados da Matéria 00/0 Licenciatura em Engenharia Electrotécnica e de Computadores Faculdade de Engenharia
Maria Inês Barbosa de Carvalho Equação de Schrödinger Apontamentos para a disciplina Física dos Estados da Matéria 00/0 Licenciatura em Engenharia Electrotécnica e de Computadores Faculdade de Engenharia
Atomística. Prof. Fernando R. Xavier
 Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
Atomística Prof. Fernando R. Xavier UDESC 2013 Nem sempre foi tão fácil observar um átomo... Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson 400 a.c. até 1897 d.c. O Modelo de
Exame de Ingresso na Pós-graduação
 Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 09 de Junho de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3 (três)
Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 09 de Junho de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3 (três)
Eletromagnetismo I. Prof. Daniel Orquiza. Eletromagnetismo I. Prof. Daniel Orquiza de Carvalho
 Eletromagnetismo I Prof. Daniel Orquiza Eletromagnetismo I Prof. Daniel Orquiza de Carvalo Equação de Laplace (Capítulo 6 Páginas 160 a 172) Eq. de Laplace Solução numérica da Eq. de Laplace Eletromagnetismo
Eletromagnetismo I Prof. Daniel Orquiza Eletromagnetismo I Prof. Daniel Orquiza de Carvalo Equação de Laplace (Capítulo 6 Páginas 160 a 172) Eq. de Laplace Solução numérica da Eq. de Laplace Eletromagnetismo
Escola Politécnica FGE GABARITO DA SUB 6 de julho de 2006
 PS Física III Escola Politécnica - 2006 FGE 2203 - GABARITO DA SUB 6 de julho de 2006 Questão 1 Uma esfera dielétrica de raio a está uniformemente carregada com densidade volumétrica ρ A esfera está envolvida
PS Física III Escola Politécnica - 2006 FGE 2203 - GABARITO DA SUB 6 de julho de 2006 Questão 1 Uma esfera dielétrica de raio a está uniformemente carregada com densidade volumétrica ρ A esfera está envolvida
Física IV Escola Politécnica P3 7 de dezembro de 2017
 Física IV - 4323204 Escola Politécnica - 2017 P3 7 de dezembro de 2017 Questão 1 Uma partícula de massa m que se move em uma dimensão possui energia potencial que varia com a posição como mostra a figura.
Física IV - 4323204 Escola Politécnica - 2017 P3 7 de dezembro de 2017 Questão 1 Uma partícula de massa m que se move em uma dimensão possui energia potencial que varia com a posição como mostra a figura.
Segunda Lista - Lei de Gauss
 Segunda Lista - Lei de Gauss FGE211 - Física III 1 Sumário O fluxo elétrico que atravessa uma superfície infinitesimal caracterizada por um vetor de área A = Aˆn é onde θ é o ângulo entre E e ˆn. Φ e =
Segunda Lista - Lei de Gauss FGE211 - Física III 1 Sumário O fluxo elétrico que atravessa uma superfície infinitesimal caracterizada por um vetor de área A = Aˆn é onde θ é o ângulo entre E e ˆn. Φ e =
Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA. Eliana Midori Sussuchi Danilo Oliveira Santos
 Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA META Aplicar os conceitos de mecânica quântica aos orbitais atômicos; Descrever a distribuição dos elétrons nos átomos. OBJETIVOS Ao final desta aula,
Aula 3 ORBITAIS ATÔMICOS E DISTRIBUIÇÃO ELETRÔNICA META Aplicar os conceitos de mecânica quântica aos orbitais atômicos; Descrever a distribuição dos elétrons nos átomos. OBJETIVOS Ao final desta aula,
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/2 e de Dois Níveis
 Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
SEGUNDA PROVA - F789. angular orbital. O estado da partícula, Ψ, tem componentes Ψ ± (r) =
 SEGUNDA PROVA - F789 NOME: RA:. Considere uma partícula de spin. Seja S seu spin e L seu momento angular orbital. O estado da partícula, Ψ, tem componentes Ψ ± (r) = r, ± Ψ na base r, ± de autoestados
SEGUNDA PROVA - F789 NOME: RA:. Considere uma partícula de spin. Seja S seu spin e L seu momento angular orbital. O estado da partícula, Ψ, tem componentes Ψ ± (r) = r, ± Ψ na base r, ± de autoestados
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva Uma outra vez a experiência da dupla fenda 18/11/015 Prof. Dr. Lucas Barboza Sarno da Silva Probabilidade de chegada do elétron, com a fenda fechada: * 1 1 1 * Probabilidade
Prof. Dr. Lucas Barboza Sarno da Silva Uma outra vez a experiência da dupla fenda 18/11/015 Prof. Dr. Lucas Barboza Sarno da Silva Probabilidade de chegada do elétron, com a fenda fechada: * 1 1 1 * Probabilidade
Fundamentos da Eletrostática Aula 05 A Lei de Coulomb e o Campo Elétrico
 A lei de Coulomb Fundamentos da Eletrostática Aula 5 A Lei de Coulomb e o Campo Elétrico Prof. Alex G. Dias Prof. Alysson F. Ferrari Conforme mencionamos anteriormente, trataremos neste curso de distribuções
A lei de Coulomb Fundamentos da Eletrostática Aula 5 A Lei de Coulomb e o Campo Elétrico Prof. Alex G. Dias Prof. Alysson F. Ferrari Conforme mencionamos anteriormente, trataremos neste curso de distribuções
FEP Física Geral e Experimental para Engenharia I
 FEP2195 - Física Geral e Experimental para Engenharia I Prova Substitutiva - Gabarito 1. Dois blocos de massas 4, 00 kg e 8, 00 kg estão ligados por um fio e deslizam para baixo de um plano inclinado de
FEP2195 - Física Geral e Experimental para Engenharia I Prova Substitutiva - Gabarito 1. Dois blocos de massas 4, 00 kg e 8, 00 kg estão ligados por um fio e deslizam para baixo de um plano inclinado de
Física III-A /2 Lista 1: Carga Elétrica e Campo Elétrico
 Física III-A - 2018/2 Lista 1: Carga Elétrica e Campo Elétrico 1. (F) Duas partículas com cargas positivas q e 3q são fixadas nas extremidades de um bastão isolante de comprimento d. Uma terceira partícula
Física III-A - 2018/2 Lista 1: Carga Elétrica e Campo Elétrico 1. (F) Duas partículas com cargas positivas q e 3q são fixadas nas extremidades de um bastão isolante de comprimento d. Uma terceira partícula
Notas de aula resumo de mecânica. Prof. Robinson RESUMO DE MECÂNICA
 RESUMO DE MECÂNICA Ano 2014 1 1. DINÂMICA DE UMA PARTÍCULA 1.1. O referencial inercial. O referencial inercial é um sistema de referência que está em repouso ou movimento retilíneo uniforme ao espaço absoluto.
RESUMO DE MECÂNICA Ano 2014 1 1. DINÂMICA DE UMA PARTÍCULA 1.1. O referencial inercial. O referencial inercial é um sistema de referência que está em repouso ou movimento retilíneo uniforme ao espaço absoluto.
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 PROPRIEDADES ONDULATÓRIAS DA MATÉRIA Edição de junho de 2014 CAPÍTULO 4 PROPRIEDADES ONDULATÓRIAS DA MATÉRIA ÍNDICE 4.1- Postulados de
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 PROPRIEDADES ONDULATÓRIAS DA MATÉRIA Edição de junho de 2014 CAPÍTULO 4 PROPRIEDADES ONDULATÓRIAS DA MATÉRIA ÍNDICE 4.1- Postulados de
Escoamento potencial
 Escoamento potencial J. L. Baliño Escola Politécnica - Universidade de São Paulo Apostila de aula 2017, v.1 Escoamento potencial 1 / 26 Sumário 1 Propriedades matemáticas 2 Escoamento potencial bidimensional
Escoamento potencial J. L. Baliño Escola Politécnica - Universidade de São Paulo Apostila de aula 2017, v.1 Escoamento potencial 1 / 26 Sumário 1 Propriedades matemáticas 2 Escoamento potencial bidimensional
Programa de Pós-Graduação Processo de Seleção 2º Semestre de 2019 Exame de Conhecimentos em Física. Caderno de respostas
 1 Programa de Pós-Graduação Processo de Seleção 2º Semestre de 2019 Exame de Conhecimentos em Física Caderno de respostas Questão Alternativas (a) (b) (c) (d) (e) 01 X 02 X 03 X 04 X 05 X 06 X 07 X 08
1 Programa de Pós-Graduação Processo de Seleção 2º Semestre de 2019 Exame de Conhecimentos em Física Caderno de respostas Questão Alternativas (a) (b) (c) (d) (e) 01 X 02 X 03 X 04 X 05 X 06 X 07 X 08
LCE0143 Química Geral. Estrutura Atômica. Wanessa Melchert Mattos.
 LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
LCE0143 Química Geral Estrutura Atômica Wanessa Melchert Mattos wanemelc@usp.br Princípio da Incerteza Elétron dualidade onda-partícula W. Heisenberg: impossível fixar a posição de um elétron em um átomo
Segundo Semestre de 2009
 AC TORT 1/2009 1 Instituto de Física UFRJ 2 a Avaliação a Distância de Física 3A - AD2 Pólo : Nome : Assinatura : Segundo Semestre de 2009 Data: 1 o Q 2 o Q 3 o Q 4 o Q Nota Problema 1 Considere um elétron
AC TORT 1/2009 1 Instituto de Física UFRJ 2 a Avaliação a Distância de Física 3A - AD2 Pólo : Nome : Assinatura : Segundo Semestre de 2009 Data: 1 o Q 2 o Q 3 o Q 4 o Q Nota Problema 1 Considere um elétron
Mecânica Quântica. Veremos hoje: Dualidade onda partícula Princípio da Incerteza Formulações da MQ Equação de Schrodinger Partícula numa caixa
 Mecânica Quântica Veremos hoje: Dualidade onda partícula Princípio da Incerteza Formulações da MQ Equação de Schrodinger Partícula numa caixa Limitações do modelo de Bohr A teoria de Bohr não era capaz
Mecânica Quântica Veremos hoje: Dualidade onda partícula Princípio da Incerteza Formulações da MQ Equação de Schrodinger Partícula numa caixa Limitações do modelo de Bohr A teoria de Bohr não era capaz
Capítulo 18 Movimento ondulatório
 Capítulo 18 Movimento ondulatório 18.1 Ondas mecânicas Onda: perturbação que se propaga Ondas mecânicas: Por exemplo: som, ondas na água, ondas sísmicas, etc. Se propagam em um meio material. No entanto,
Capítulo 18 Movimento ondulatório 18.1 Ondas mecânicas Onda: perturbação que se propaga Ondas mecânicas: Por exemplo: som, ondas na água, ondas sísmicas, etc. Se propagam em um meio material. No entanto,
