Problemas de Duas Partículas
|
|
|
- Maria Luiza Machado Barreto
- 8 Há anos
- Visualizações:
Transcrição
1 Problemas de Duas Partículas Química Quântica Prof a. Dr a. Carla Dalmolin Massa reduzida Rotor Rígido
2 Problemas de Duas Partículas Partícula 1: coordenadas x 1, y 1, z 1 Partícula 2: coordenadas x 2, y 2, z 2 Coordenadas relativas: coordenadas da Partícula 2 num sistema em que a origem são as coordenadas da Partícula 1 x x 2 x 1 x 2, y 2, z 2 = (x, y, z) y y 2 y 1 z z 2 z 1 (0,0,0) Energia potencial Depende apenas das coordenadas relativas do sistema Para partículas que apresentam carga elétrica, V é a energia de interação das partículas e é dada pela Lei de Coulomb Depende da carga e da distância r entre as partículas: r = x 2 + y 2 + z 2 1 2
3 Centro de Massa e Massa Reduzida Em um tratamento de sistemas de massas pontuais o centro de massa é o ponto onde se supõe concentrada toda a massa do sistema. O conceito utilizado para análises físicas nas quais não é importante considerar a distribuição de massa. O conceito de massa reduzida (μ) surge a partir de resultados matemáticos associados à análise da dinâmica de dois corpos com massas m 1 e m 2 que, devido à interação entre eles, gravitam mutuamente o centro de massa do sistema que constituem. μ = m 1m 2 m 1 +m 2 Um sistema de duas partículas pode ser reduzido a um sistema de uma partícula de igual centro de massa e massa reduzida
4 Tratamento Clássico A energia do sistema de duas partículas é dado pela soma da energia cinética de translação do sistema, da energia cinética do movimento de uma partícula em relação a outra e da energia potencial de interação entre as partículas A energia cinética de translação depende do movimento do centro de massa, que tem a massa total do sistema: M = m 1 + m 2 e coordenadas X, Y, Z As energias relativas entre as duas partículas dependem do movimento da partícula fictícia de massa reduzida μ H = 1 2μ p x 2 + p y 2 + p z 2 + V(x, y, z) + 1 2M p X 2 + p Y 2 + p Z 2 Movimento relativo das partículas Translação do centro de massa
5 Separação de Variáveis H = 1 2μ p x 2 + p y 2 + p z 2 + V(x, y, z) + 1 2M p X 2 + p Y 2 + p Z 2 Partícula fictícia de massa μ e energia potencial V(x, y, z) Partícula fictícia de massa M e V = 0 Não existe termo para qualquer interação entre as duas partículas fictícias O hamiltoniano pode ser separado: H μ e H M A energia total do sistema é a soma das energias descritas por cada hamiltoniano: E = E μ + E M O mesmo tratamento pode ser feito para a mecânica quântica: H μ ψ μ (x, y, z) = E μ ψ μ (x, y, z) H M ψ M (X, Y, Z) = E M ψ M (X, Y, Z)
6 Rotor Rígido de Duas Partículas Duas partículas de massa m 1 e m 2 confinadas a permanecerem a uma distância r fixa uma da outra Rotação de moléculas diatômicas A energia do sistema é totalmente cinética e V = 0 A energia cinética do sistema é a soma da energia translacional e do movimento interno (rotacional) das partículas: K = E = E μ + E M O movimento interno é a rotação de duas partículas com distância fixa entre elas e pode ser reduzido ao problema de uma partícula de massa μ girando em uma esfera de raio r
7 Coordenadas Esféricas Sistemas com simetria esférica são mais convenientes de serem trabalhados usando coordenadas esféricas Raio (r): distância até o centro (origem) da esfera; pode variar de 0 a Colatitude (θ): ângulo definido com o eixo z; pode variar de 0 a π Ângulo azimutal (φ): ângulo definido no plano xy; pode variar de 0 a 2π Relação entre os sistemas de coordenadas: x = r sin Θ cos φ y = r sin Θ sin φ z = r cos θ Elemento de volume (dτ) dτ = r 2 sin θ drdθdφ
8 Coordenadas Esféricas Laplaciano ( 2 ) transformado para coordenadas esféricas: 2 = 2 r r Onde o operador legendriano (Λ 2 ) é definido como: Para o modelo esférico: r é constante ψ varia apenas com θ e φ e as derivadas em relação a r são zeradas Equação de Schrödinger: r + 1 r 2 Λ2 Λ 2 = 1 2 sin 2 θ φ sin θ θ 2 = 1 r 2 Λ2 Hψ = Eψ onde V = 0 ħ2 1 2μ r 2 Λ2 ψ = E μ ψ sin θ θ
9 Resolução Equação de Schrödinger para o rotor rígido: ħ2 2μ 1 r 2 Λ2 ψ = E μ ψ Como I = μr 2 Λ 2 ψ = εψ, onde ε = 2IE ħ 2 Separação de variáveis: ψ θ, φ = Θ(θ)Φ(φ) Φ d2 Φ sin θ + dφ2 Θ d dθ sin θ dθ dθ + ε sin2 θ = 0 Rotor no plano xy (partícula no anel) Funções associadas de Legendre Depende de m l Dependem de l l = 0,1,2 m l = l, l 1,, 0,, l + 1, l
10 Funções de Onda As funções associadas de Legendre são tabeladas para cada função de onda resultante da Equação de Schrödinger Dois números quânticos Número quântico do momento angular orbital (l): l = 0, 1, 2, 3 Número quântico magnético ou azimutal (m l ): m l = l, l 1,, 0,, l Harmônicos Esféricos: Y l,ml (θ, φ) Energia (E μ ou E rot ) E = l l + 1 ħ2 ; l = 0,1,2, 2I Os números quânticos l e m l determinam a função de onda rotacional, mas E rot depende apenas de l Cada nível rotacional é (2l + 1) vezes degenerado Não existe energia rotacional no ponto zero
11 Probabilidades (ψ 2 ) e Energia 2 ψ l,ml E rot não depende do m l Funções com mesmo l e m l diferentes são degeneradas E rot ħ 2 2I
12 Momento Angular De maneira análoga ao modelo da partícula no anel, o momento angular também é quantizado: J = 2IE 1 2 = l l As funções Y l,ml (harmônicos esféricos) são autofunções do operador de momento angular ao longo do eixo z, com a parte Θ(θ) constante: J z = ħ i φ J z = m l ħ Para um dado valor de l, o vetor momento angular assume algumas orientações definidas ao longo do eixo z: quantização espacial
13 Quantização Espacial O operador J z não comuta com os operadores J x e J y Princípio da incerteza: conhecendo J z com exatidão, é impossível determinar J x e J y. Cada folha cônica representa um estado com m l definido, tendo a folha cônica projeção no eixo z de módulo m l ħ. Projeções em x e y são indefinidas
Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento angular bem definido
 ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
ÁTOMO DE HIDROGÊNIO Primeiro sistema tratado quanticamente por Schrödinger Modelo de Bohr Elétrons se movem ao redor do núcleo em órbitas circulares (atração Coulombiana) Cada órbita n possui um momento
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas Equação de Schrödinger em 3D: 2 = 1 r 2 # % r $ r2 r & (+ ' 1 r 2 senθ # θ senθ & % (+ $ θ ' 1 r 2 sen 2 θ 2 φ 2 Podemos, então, escrever a eq. de Schrödinger
A eq. de Schrödinger em coordenadas esféricas Equação de Schrödinger em 3D: 2 = 1 r 2 # % r $ r2 r & (+ ' 1 r 2 senθ # θ senθ & % (+ $ θ ' 1 r 2 sen 2 θ 2 φ 2 Podemos, então, escrever a eq. de Schrödinger
Partícula na Caixa. Química Quântica Prof a. Dr a. Carla Dalmolin
 Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
Partícula na Caixa Química Quântica Prof a. Dr a. Carla Dalmolin Caixa unidimensional Caixa tridimensional Degenerescência Partícula no anel (mov. de rotação) Partícula na Caixa Partícula numa caixa unidimensional
Fundamentos de Química Quântica
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Aula 3 Professora: Melissa Soares Caetano Átomo de Hidrogênio Um núcleo
Mecânica Quântica. Química Quântica Prof a. Dr a. Carla Dalmolin. A Equação de Schrödinger Postulados da Mecânica Quântica
 Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin A Equação de Schrödinger Postulados da Mecânica Quântica Mecânica Clássica O movimento de uma partícula é governado pela Segunda Lei de Newton:
Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin A Equação de Schrödinger Postulados da Mecânica Quântica Mecânica Clássica O movimento de uma partícula é governado pela Segunda Lei de Newton:
Equação de Schrödinger em 3D
 Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Equação de Schrödinger em 3D Conteúdo básico: extensão do que foi feito em 1D: p 2 /2m + V(x,y,z) = E; Equação independente do tempo: 2m 2 ψ +V(x, y, z)ψ = Eψ A interpretação probabilística envolve a integração
Rotor quântico. Quanticamente o rotor é descrito por uma função de onda, tal que: l A função de onda do estado estacionário é dada por:
 Rotor quântico Vamos tratar o caso da rotação de um corpo rígido, que corresponde a 2 massas pontuais, ligadas por uma barra rígida e sem massa. Consideremos rotação livre em torno de um eixo perpendicular
Rotor quântico Vamos tratar o caso da rotação de um corpo rígido, que corresponde a 2 massas pontuais, ligadas por uma barra rígida e sem massa. Consideremos rotação livre em torno de um eixo perpendicular
1 O Átomo de Hidrogênio
 O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
O modelo de Bohr para o átomo de hidrogênio, embora forneça valores corretos para as energias dos estados atômicos e do espectro da radiação emitida, não pode ser correto do ponto de vista da mecânica
FNC376N: Lista de março de ψ r ψ = Eψ. sin θ Y )
 FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
FNC376N: ista 3 31 de março de 5 Tipler - Capítulo 7 7-7 Considere a função de onda ψ = A r a e r/a cos θ, onde A é uma constante e a = /µkze é o raio de Bohr dividido por Z a) Mostre que éla é uma solução
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS Edição de agosto de 2008 CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS ÍNDICE 8.1- Introdução 8.2- Problema da Força Central
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS Edição de agosto de 2008 CAPÍTULO 8 ÁTOMOS MONOELETRÔNICOS ÍNDICE 8.1- Introdução 8.2- Problema da Força Central
MOVIMENTO DE ROTAÇÃO: O ROTOR RÍGIDO
 MOVIMENTO DE ROTAÇÃO: O ROTOR RÍGIDO Prof. Harey P. Martins Fiho o Rotação em duas dimensões Partícua de massa m descrevendo trajetória circuar no pano xy: Momento anguar da partícua: J z = rp = mrv Ser
MOVIMENTO DE ROTAÇÃO: O ROTOR RÍGIDO Prof. Harey P. Martins Fiho o Rotação em duas dimensões Partícua de massa m descrevendo trajetória circuar no pano xy: Momento anguar da partícua: J z = rp = mrv Ser
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 8 ÁTOMOS DE UM ELÉTRON Primeira Edição junho de 2005 CAPÍTULO 08 ÁTOMOS DE UM ELÉTRON ÍNDICE 8.1- Introdução 8.2- Força Central 8.3- Equação
Física Quântica. Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio. Pieter Westera
 Física Quântica Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio Pieter Westera [email protected] http://professor.ufabc.edu.br/~pieter.westera/quantica.html A Equação
Física Quântica Aula 10: Equação de Schrödinger em Coordenadas Esféricas, Átomo de Hidrogênio Pieter Westera [email protected] http://professor.ufabc.edu.br/~pieter.westera/quantica.html A Equação
Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui
 FÍSICA MODERNA Aula 6a: Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui Tema 5: Física dos átomos e moléculas 5.1. Átomo de hidrogénio;
FÍSICA MODERNA Aula 6a: Física dos Átomos e Moléculas a) O problema do átomo de hidrogénio O Docente Regente: Prof. Doutor Rogério Uthui Tema 5: Física dos átomos e moléculas 5.1. Átomo de hidrogénio;
Fundamentos de Química Quântica
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Professora: Melissa Soares Caetano Partícula na caixa Sistema ideal
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Fundamentos de Química Quântica Professora: Melissa Soares Caetano Partícula na caixa Sistema ideal
Modelos Atômicos e Princípios Quânticos Parte II
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: [email protected]
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA I Modelos Atômicos e Princípios Quânticos Parte II Prof. Fabio da Silva Miranda e-mail: [email protected]
Função de Onda e Equação de Schrödinger
 14/08/013 Função de Onda e Equação de Schrödinger Prof. Alex Fabiano C. Campos, Dr A Função de Onda (ψ) A primeira formulação para esta nova interpretação da Mecânica, a Mecânica Quântica, teoria foi proposta
14/08/013 Função de Onda e Equação de Schrödinger Prof. Alex Fabiano C. Campos, Dr A Função de Onda (ψ) A primeira formulação para esta nova interpretação da Mecânica, a Mecânica Quântica, teoria foi proposta
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
A Estrutura Eletrônica dos Átomos. Prof. Fernando R. Xavier
 A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
A Estrutura Eletrônica dos Átomos Prof. Fernando R. Xavier UDESC 2015 Estrutura Atômica, Antencedentes... Modelos de Demócrito, Dalton, Thomson, etc 400 a.c. até 1897 d.c. Nascimento da Mecânica Quântica
Postulados da Mecânica Quântica
 Postulados da Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin Operadores Propriedades Princípio da Incerteza Princípios da Mecânica Quântica A função de onda contém toda a informação que
Postulados da Mecânica Quântica Química Quântica Prof a. Dr a. Carla Dalmolin Operadores Propriedades Princípio da Incerteza Princípios da Mecânica Quântica A função de onda contém toda a informação que
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/2 e de Dois Níveis
 Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Aplicações dos Postulados da Mecânica Quântica Para Simples Casos: Sistema de Spin 1/ e de Dois Níveis Bruno Felipe Venancio 8 de abril de 014 1 Partícula de Spin 1/: Quantização do Momento Angular 1.1
Comportamento ondulatório da matéria
 Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Louis de Broglie investigou as propriedades ondulatórias da na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tina associado a ele um λ. Ele igualou as duas expressões conecidas
Átomo de Hidrogênio 1
 Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Átomo de Hidrogênio 1 Potencial central Solução: separação de variáveis satisfaz a equação para qualquer valor de m l. g() deve satisfazer a condição m l deve ser inteiro. 3 Solução: separação de variáveis
Química Teórica e Estrutural: Aula 4a
 Química Teórica e Estrutural: Aula 4a P.J.S.B. Caridade & U. Miranda October 16, 2012 Partícula na caixa de potencial: Exemplos práticos Caridade & Miranda TP: aula 4a 2 Postulados da Mecânica Quântica
Química Teórica e Estrutural: Aula 4a P.J.S.B. Caridade & U. Miranda October 16, 2012 Partícula na caixa de potencial: Exemplos práticos Caridade & Miranda TP: aula 4a 2 Postulados da Mecânica Quântica
h mc 2 =hν mc 2 =hc/ λ
 Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Louis de Broglie investigou as propriedades ondulatórias da matéria na década de 30. Ele supôs que o e-, em seu movimento ao redor do núcleo, tinha associado a ele um λ. Ele igualou as duas expressões
Aula anterior. Equação de Schrödinger a 3 dimensões. d x 2m - E -U. 2m - E -U x, y, z. x y z x py pz cin cin. E E ( x, y,z ) - 2m 2m x y z
 6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
6/Maio/2013 Aula 21 Efeito de túnel quântico: decaimento alfa. Aplicações: nanotecnologias; microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. Átomo de hidrogénio Modelo de Bohr 8/Maio/2013
Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change
 Físico-Química Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 24 Prof. Dr. Anselmo E de Oliveira
Físico-Química Apresentações com base no material disponível no livro: Atkins, P.; de Paula, J.; Friedman, R. Physical Chemistry Quanta, Matter, and Change, 2nd Ed., Oxford, 24 Prof. Dr. Anselmo E de Oliveira
Não serão aceitas respostas sem justificativa:
 Primeira Prova de Conceitos de Mecânica Quântica -(,5) Uma partícula de massa m encontra-se no estado ψ(x,t)= A exp[ω(mx /ħ+it)], onde A e a são constantes reais e positivas. a- Normalize ψ(x,t); b- Calcule
Primeira Prova de Conceitos de Mecânica Quântica -(,5) Uma partícula de massa m encontra-se no estado ψ(x,t)= A exp[ω(mx /ħ+it)], onde A e a são constantes reais e positivas. a- Normalize ψ(x,t); b- Calcule
B) [N] é uma constante de normalização indicando que a probabilidade de encontrar o elétron em qualquer lugar do espaço deve ser unitária. R n,l (r) é
![B) [N] é uma constante de normalização indicando que a probabilidade de encontrar o elétron em qualquer lugar do espaço deve ser unitária. R n,l (r) é B) [N] é uma constante de normalização indicando que a probabilidade de encontrar o elétron em qualquer lugar do espaço deve ser unitária. R n,l (r) é](/thumbs/71/66033065.jpg) QUÍMICA I AULA 04: ESTRUTURA ELETRÔNICA DOS ÁTOMOS TÓPICO 05: ORBITAL ATÔMICO 5.1 A EQUAÇÃO DE SCHRODINGER E O ÁTOMO DE HIDROGÊNIO: Como o elétron tem propriedades ondulatórias, ele pode ser descrito como
QUÍMICA I AULA 04: ESTRUTURA ELETRÔNICA DOS ÁTOMOS TÓPICO 05: ORBITAL ATÔMICO 5.1 A EQUAÇÃO DE SCHRODINGER E O ÁTOMO DE HIDROGÊNIO: Como o elétron tem propriedades ondulatórias, ele pode ser descrito como
Universidade Estadual de Santa Cruz
 Universidade Estadual de Santa Cruz PROFÍSICA Programa de Pós-graduação em Física Seleção 2009. Prova Escrita 2/0/2009 Candidato (nome legível): - Esta prova consta de oito questões distribuídas da seguinte
Universidade Estadual de Santa Cruz PROFÍSICA Programa de Pós-graduação em Física Seleção 2009. Prova Escrita 2/0/2009 Candidato (nome legível): - Esta prova consta de oito questões distribuídas da seguinte
F 789 A - MECÂNICA QUÂNTICA II -Prof. Eduardo Granado - PROVA 1 (01/04/2015) (θ,ϕ), em que u k,l. (r). Nesta equação, E k,l e l (l+1)ħ 2 são os
 F 789 A - MECÂNICA QUÂNTICA II -Prof. Eduardo Granado - PROVA 1 (01/04/2015) 1) Considere um sistema de duas partículas de massa m 1 e m 2 que interagem através de um potencial central V(r), onde r é a
F 789 A - MECÂNICA QUÂNTICA II -Prof. Eduardo Granado - PROVA 1 (01/04/2015) 1) Considere um sistema de duas partículas de massa m 1 e m 2 que interagem através de um potencial central V(r), onde r é a
5.1: Aplicação da Equação de Schrödinger ao átomo de Hidrogênio
 http://www.if.ufrgs.br/~marcia/textos.html UNIDADE Aula 5 Átomo de Hidrogênio * * Tradução e adaptação livre das aulas do Professor Rick Trebino em: www.physics.gatech.edu/frog 5.1 Aplicação da Equação
http://www.if.ufrgs.br/~marcia/textos.html UNIDADE Aula 5 Átomo de Hidrogênio * * Tradução e adaptação livre das aulas do Professor Rick Trebino em: www.physics.gatech.edu/frog 5.1 Aplicação da Equação
Representação grande
 Capítulo 5 Representação grande canônica 5.1 Introdução Distribuição de probabilidades Vimos no Capítulo 1 que um sistema constituído por partículas que interagem por meio de forças conservativas em contato
Capítulo 5 Representação grande canônica 5.1 Introdução Distribuição de probabilidades Vimos no Capítulo 1 que um sistema constituído por partículas que interagem por meio de forças conservativas em contato
Translação e Rotação Energia cinética de rotação Momentum de Inércia Torque. Física Geral I ( ) - Capítulo 07. I. Paulino*
 ROTAÇÃO Física Geral I (1108030) - Capítulo 07 I. Paulino* *UAF/CCT/UFCG - Brasil 2012.2 1 / 25 Translação e Rotação Sumário Definições, variáveis da rotação e notação vetorial Rotação com aceleração angular
ROTAÇÃO Física Geral I (1108030) - Capítulo 07 I. Paulino* *UAF/CCT/UFCG - Brasil 2012.2 1 / 25 Translação e Rotação Sumário Definições, variáveis da rotação e notação vetorial Rotação com aceleração angular
Momento Angular. 8.1 Álgebra do Momento Angular
 Capítulo 8 Momento Angular Neste capítulo vamos estudar os autovalores e autovetores do momento angular. Este problema também pode ser analisado com o uso do método de operadores, o que faremos na primeira
Capítulo 8 Momento Angular Neste capítulo vamos estudar os autovalores e autovetores do momento angular. Este problema também pode ser analisado com o uso do método de operadores, o que faremos na primeira
Aplicações de Semicondutores em Medicina
 Aplicações de Semicondutores em Medicina A estrutura dos cristais semicondutores Luiz Antonio Pereira dos Santos CNEN-CRCN PRÓ-ENGENHARIAS UFS-IPEN-CRCN Aracaju Março - 010 Como é a estrutura da matéria?
Aplicações de Semicondutores em Medicina A estrutura dos cristais semicondutores Luiz Antonio Pereira dos Santos CNEN-CRCN PRÓ-ENGENHARIAS UFS-IPEN-CRCN Aracaju Março - 010 Como é a estrutura da matéria?
A Equação de Onda de Schröedinger. O Princípio da Incerteza de Heisenberg. λ =
 O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
O Modelo Mecânico-Quântico Louis de Broglie apresentou a idéia de que, se as ondas luminosas exibiam características de partícula, então talvez as partículas de matéria pudessem mostrar propriedades ondulatórias.
Instituto de Física - UFF Profissional - 11 de Dezembro de 2009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das
 Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 11 de Dezembro de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3
Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 11 de Dezembro de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3
O ÁTOMO DE HIDROGÊNIO
 O ÁTOMO DE HIDROGÊNIO Alessandra de Souza Barbosa 04 de dezembro de 013 O átomo de hidrogênio Alessandra de Souza Barbosa CF37 - Mecânica Quântica I /36 Sistema de duas particulas um elétron e um próton;
O ÁTOMO DE HIDROGÊNIO Alessandra de Souza Barbosa 04 de dezembro de 013 O átomo de hidrogênio Alessandra de Souza Barbosa CF37 - Mecânica Quântica I /36 Sistema de duas particulas um elétron e um próton;
Introdução à Modelagem Molecular
 Introdução à Modelagem Molecular Prof. Alex Fabiano C. Campos, Dr Introdução Métodos teóricos e técnicas computacionais para modelar ou imitar o comportamento de moléculas e sistemas atômicos. Empregados
Introdução à Modelagem Molecular Prof. Alex Fabiano C. Campos, Dr Introdução Métodos teóricos e técnicas computacionais para modelar ou imitar o comportamento de moléculas e sistemas atômicos. Empregados
Quantização. Quantização da energia (Planck, 1900) hc h. Efeito fotoelétrico (Einstein, 1905) Espectros atômicos (linhas discretas) v 2
 Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Mecânica Quântica Quantização e o modelo de Bohr (revisão) Dualidade Onda-Partícula Princípio da Incerteza Equação de Schrödinger Partícula na Caixa Átomo de Hidrogênio Orbitais Atômicos Números Quânticos
Lista 6: CDCI2 Turmas: 2AEMN e 2BEMN. 1 Divergente e Rotacional de Campos Vetoriais
 Lista 6: CDCI Turmas: AEMN e BEMN Prof. Alexandre Alves Universidade São Judas Tadeu Divergente e Rotacional de Campos Vetoriais Exercício : Calcule a divergência e o rotacional dos seguintes campos vetoriais:
Lista 6: CDCI Turmas: AEMN e BEMN Prof. Alexandre Alves Universidade São Judas Tadeu Divergente e Rotacional de Campos Vetoriais Exercício : Calcule a divergência e o rotacional dos seguintes campos vetoriais:
Lista de Exercícios 1: Eletrostática
 Lista de Exercícios 1: Eletrostática 1. Uma carga Q é distribuída uniformemente sobre um fio semicircular de raio a, que está no plano xy. Calcule a força F com que atua sobre uma carga de sinal oposto
Lista de Exercícios 1: Eletrostática 1. Uma carga Q é distribuída uniformemente sobre um fio semicircular de raio a, que está no plano xy. Calcule a força F com que atua sobre uma carga de sinal oposto
Teoria Clássica de Campos
 Teoria Quântica de Campos I 7 No passo (1) o que estamos fazendo é quantizar (transformar em operadores) uma função definida em todo espaço (um campo) e cuja equação de movimento CLÁSSICA é de Dirac ou
Teoria Quântica de Campos I 7 No passo (1) o que estamos fazendo é quantizar (transformar em operadores) uma função definida em todo espaço (um campo) e cuja equação de movimento CLÁSSICA é de Dirac ou
PROPRIEDADES ONDULATÓRIAS DO ELÉTRON
 MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
MODELO QUÂNTICO PROPRIEDADES ONDULATÓRIAS DO ELÉTRON EINSTEIN: usou o efeito fotoelétrico para demonstrar que a luz, geralmente imaginada como tendo propriedades de onda, pode também ter propriedades de
Estrutura atômica. Modelo quântico do átomo
 Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Estrutura atômica Modelo quântico do átomo Um bom modelo deve ser capaz de explicar propriedades atômicas, propriedades periódicas, ligação química Mecânica quântica - mecânica ondulatória Elétrons como
Sétima Lista. MAT0216 Cálculo Diferencial e Integral III Prof. Daniel Victor Tausk 14/04/2019
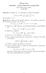 Sétima Lista MAT216 Cálculo iferencial e Integral III Prof. aniel Victor Tausk 14/4/219 Exercício 1. ados a, b, c >, determine o volume do elipsóide {(x, y, z) R 3 : x2 a 2 + y2 b 2 + z2 } c 2 1 de semi-eixos
Sétima Lista MAT216 Cálculo iferencial e Integral III Prof. aniel Victor Tausk 14/4/219 Exercício 1. ados a, b, c >, determine o volume do elipsóide {(x, y, z) R 3 : x2 a 2 + y2 b 2 + z2 } c 2 1 de semi-eixos
Operadores e Função de Onda para Muitos Elétrons. Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros
 Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Operadores e Função de Onda para Muitos Elétrons Introdução à Física Atômica e Molecular UEG Prof. Renato Medeiros Livro texto: Modern Quantum Chemistry Introduction to Advanced Elecronic Structure Theory
Exame de Ingresso na Pós-graduação
 Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 09 de Junho de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3 (três)
Exame de Ingresso na Pós-graduação Instituto de Física - UFF Profissional - 09 de Junho de 009 Resolva 6 (seis) questões, com pelo menos uma questão de cada uma das seções. A duração da prova é de 3 (três)
O spin do elétron. Vimos, na aula 2, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com 2 valores, com propriedades de momento angular.
 O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
O spin do elétron Vimos, na aula, que Goudsmit e Uhlenbeck propõem uma variável, quantizada, com valores, com propriedades de momento angular. Analogia com o momento angular orbital e e com e foram observadas
Mecânica Clássica 1 - Lista de natal - Ho Ho Ho Professor: Gabriel T. Landi
 Mecânica Clássica 1 - Lista de natal - Ho Ho Ho Professor: Gabriel T. Landi O campo vetorial 1 Aquecimento: quadri-potencial e os campos elétrico e magnético O objeto fundamental do eletromagnetismo é
Mecânica Clássica 1 - Lista de natal - Ho Ho Ho Professor: Gabriel T. Landi O campo vetorial 1 Aquecimento: quadri-potencial e os campos elétrico e magnético O objeto fundamental do eletromagnetismo é
NOTAS DE AULA INTRODUÇÃO À ENGENHARIA BIOMÉDICA 70
 NOTAS DE AULA INTRODUÇÃO À ENGENHARIA BIOMÉDICA 70 4.2 CINETICA DO CORPO HUMANO a. Sistemas de massa A seção anterior considerou cinemática de corpo humano e definiu as equações pertinentes. Recorde que
NOTAS DE AULA INTRODUÇÃO À ENGENHARIA BIOMÉDICA 70 4.2 CINETICA DO CORPO HUMANO a. Sistemas de massa A seção anterior considerou cinemática de corpo humano e definiu as equações pertinentes. Recorde que
Átomos polieletrónicos
 Átomos polieletrónicos Química Teórica e Estrutural P.J.S.B. Caridade & U. Miranda 2/12/2013 5/11/2013, Aula 8 Química Teórica & Estrutural (2013) Caridade & Ulises 1 Átomo de hidrogénio O Hamiltoniano
Átomos polieletrónicos Química Teórica e Estrutural P.J.S.B. Caridade & U. Miranda 2/12/2013 5/11/2013, Aula 8 Química Teórica & Estrutural (2013) Caridade & Ulises 1 Átomo de hidrogénio O Hamiltoniano
Física IV - FAP2204 Escola Politécnica GABARITO DA PS 15 de dezembro de 2009
 PS Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA PS 15 de dezembro de 2009 Questão 1 Considere os campos elétrico E = (0,E y,0) e magnético B = (0,0,B z ) onde E y (x,t) = A e a(x ct) e B z
PS Física IV - FAP2204 Escola Politécnica - 2009 GABARITO DA PS 15 de dezembro de 2009 Questão 1 Considere os campos elétrico E = (0,E y,0) e magnético B = (0,0,B z ) onde E y (x,t) = A e a(x ct) e B z
Eq. de Dirac com campo magnético
 Eq. de Dirac com campo magnético Rafael Cavagnoli GAME: Grupo de Médias e Altas Energias Eletromagnetismo clássico Eq. de Schrödinger Partícula carregada em campo mag. Eq. de Dirac Partícula carregada
Eq. de Dirac com campo magnético Rafael Cavagnoli GAME: Grupo de Médias e Altas Energias Eletromagnetismo clássico Eq. de Schrödinger Partícula carregada em campo mag. Eq. de Dirac Partícula carregada
Aula de Física II - Cargas Elétricas: Força Elétrica
 Prof.: Leandro Aguiar Fernandes ([email protected]) Universidade do Estado do Rio de Janeiro Instituto Politécnico - IPRJ/UERJ Departamento de Engenharia Mecânica e Energia Graduação em Engenharia
Prof.: Leandro Aguiar Fernandes ([email protected]) Universidade do Estado do Rio de Janeiro Instituto Politécnico - IPRJ/UERJ Departamento de Engenharia Mecânica e Energia Graduação em Engenharia
O ÁTOMO DE HIDROGÊNIO
 FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
FÍSICA PARA ENGENHARIA ELÉTRICA José Fernando Fragalli Departamento de Física Udesc/Joinville O ÁTOMO DE HIDROGÊNIO A elegância, a riqueza, a complexidade e a diversidade dos fenômenos naturais que decorrem
4 e 6/Maio/2016 Aulas 17 e 18
 9/Abril/016 Aula 16 Princípio de Incerteza de Heisenberg. Probabilidade de encontrar uma partícula numa certa região. Posição média de uma partícula. Partícula numa caixa de potencial: funções de onda
9/Abril/016 Aula 16 Princípio de Incerteza de Heisenberg. Probabilidade de encontrar uma partícula numa certa região. Posição média de uma partícula. Partícula numa caixa de potencial: funções de onda
Desenvolvimento. Em coordenadas esféricas:
 Desenvolvimento Para que possamos resolver a equação da onda em coordenadas esféricas, antes é necessária a dedução do operador Laplaciano nessas coordenadas, portanto temos: Em coordenadas esféricas:
Desenvolvimento Para que possamos resolver a equação da onda em coordenadas esféricas, antes é necessária a dedução do operador Laplaciano nessas coordenadas, portanto temos: Em coordenadas esféricas:
Equação de Schrödinger
 Maria Inês Barbosa de Carvalho Equação de Schrödinger Apontamentos para a disciplina Física dos Estados da Matéria 00/0 Licenciatura em Engenharia Electrotécnica e de Computadores Faculdade de Engenharia
Maria Inês Barbosa de Carvalho Equação de Schrödinger Apontamentos para a disciplina Física dos Estados da Matéria 00/0 Licenciatura em Engenharia Electrotécnica e de Computadores Faculdade de Engenharia
Física I 2010/2011. Aula 13 Rotação I
 Física I 2010/2011 Aula 13 Rotação I Sumário As variáveis do movimento de rotação As variáveis da rotação são vectores? Rotação com aceleração angular constante A relação entre as variáveis lineares e
Física I 2010/2011 Aula 13 Rotação I Sumário As variáveis do movimento de rotação As variáveis da rotação são vectores? Rotação com aceleração angular constante A relação entre as variáveis lineares e
Mecânica Clássica Curso - Licenciatura em Física EAD. Profº. M.Sc. Marcelo O Donnell Krause ILHÉUS - BA
 Mecânica Clássica Curso - Licenciatura em Física EAD Profº. M.Sc. Marcelo O Donnell Krause ILHÉUS - BA Aula 1 : Cinemática da partícula Aula 1 : Cinemática da partícula Exemplos Um tubo metálico, retilíneo
Mecânica Clássica Curso - Licenciatura em Física EAD Profº. M.Sc. Marcelo O Donnell Krause ILHÉUS - BA Aula 1 : Cinemática da partícula Aula 1 : Cinemática da partícula Exemplos Um tubo metálico, retilíneo
+ E p. ψ(x) = E. ψ(x)
 Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
Erwin Schrödinger: E c E p = E E c. ψ(x) E p. ψ(x) = E. ψ(x) h 8π m d ψ(x) dx E p. ψ(x) = E. ψ(x) Equação de onda a uma dimensão (x), independente do tempo: que traduz o comportamento de uma partícula
As variáveis de rotação
 Capítulo 10 Rotação Neste capítulo vamos estudar o movimento de rotação de corpos rígidos sobre um eixo fixo. Para descrever esse tipo de movimento, vamos introduzir os seguintes conceitos novos: -Deslocamento
Capítulo 10 Rotação Neste capítulo vamos estudar o movimento de rotação de corpos rígidos sobre um eixo fixo. Para descrever esse tipo de movimento, vamos introduzir os seguintes conceitos novos: -Deslocamento
TÓPICO. Fundamentos da Matemática II APLICAÇÕES DAS DERIVADAS PARCIAIS9. Licenciatura em Ciências USP/ Univesp. Gil da Costa Marques
 APLICAÇÕES DAS DERIVADAS PARCIAIS9 TÓPICO Gil da Costa Marques 9. Introdução 9. Derivadas com significado físico: o gradiente de um Campo Escalar 9.3 Equação de Euler descrevendo o movimento de um fluido
APLICAÇÕES DAS DERIVADAS PARCIAIS9 TÓPICO Gil da Costa Marques 9. Introdução 9. Derivadas com significado físico: o gradiente de um Campo Escalar 9.3 Equação de Euler descrevendo o movimento de um fluido
Capítulo 10. Rotação. Copyright 2014 John Wiley & Sons, Inc. All rights reserved.
 Capítulo 10 Rotação Copyright 10-1 Variáveis Rotacionais Agora estudaremos o movimento de rotação Aplicam-se as mesmas leis Mas precisamos de novas variáveis para expressá-las o o Torque Inércia rotacional
Capítulo 10 Rotação Copyright 10-1 Variáveis Rotacionais Agora estudaremos o movimento de rotação Aplicam-se as mesmas leis Mas precisamos de novas variáveis para expressá-las o o Torque Inércia rotacional
Mini_Lista11: Rotação de Corpos Rígidos: Eixo Fixo
 Mini_Lista11: Rotação de Corpos Rígidos: Eixo Fixo Lembrete 11.1 Em equações rotacionais, deve usar ângulos expressos em radianos. Lembrete 11.2 Na resolução de problemas de rotação, deve especificar um
Mini_Lista11: Rotação de Corpos Rígidos: Eixo Fixo Lembrete 11.1 Em equações rotacionais, deve usar ângulos expressos em radianos. Lembrete 11.2 Na resolução de problemas de rotação, deve especificar um
Exame Unificado das Pós-graduações em Física EUF
 Exame Unificado das Pós-graduações em Física EUF 1º Semestre/01 Parte 1 04/10/011 Instruções: NÃO ESCREVA O SEU NOME NA PROVA. Ela deverá ser identificada apenas através do código (EUFxxx). Esta prova
Exame Unificado das Pós-graduações em Física EUF 1º Semestre/01 Parte 1 04/10/011 Instruções: NÃO ESCREVA O SEU NOME NA PROVA. Ela deverá ser identificada apenas através do código (EUFxxx). Esta prova
Capítulo 9 - Rotação de Corpos Rígidos
 Aquino Lauri Espíndola 1 1 Departmento de Física Instituto de Ciências Exatas - ICEx, Universidade Federal Fluminense Volta Redonda, RJ 27.213-250 1 de dezembro de 2010 Conteúdo 1 e Aceleração Angular
Aquino Lauri Espíndola 1 1 Departmento de Física Instituto de Ciências Exatas - ICEx, Universidade Federal Fluminense Volta Redonda, RJ 27.213-250 1 de dezembro de 2010 Conteúdo 1 e Aceleração Angular
Estrutura da Matéria Prof. Fanny Nascimento Costa
 Estrutura da Matéria Prof. Fanny Nascimento Costa ([email protected]) Aula 07 Revisão da última aula Orbitais Números quânticos O átomo de hidrogênio Natureza ondulatória da luz Todas as ondas têm
Estrutura da Matéria Prof. Fanny Nascimento Costa ([email protected]) Aula 07 Revisão da última aula Orbitais Números quânticos O átomo de hidrogênio Natureza ondulatória da luz Todas as ondas têm
