BIOQUÍMICA. Professora: Marina Santiago de Mello
|
|
|
- Maria Laura Palha Carlos
- 7 Há anos
- Visualizações:
Transcrição
1 BIOQUÍMICA Professora: Marina Santiago de Mello 2010
2 SUMÁRIO 1) PROTEÍNAS... 3 Aminoácidos... 3 Tipos De Aminoácidos... 4 Propriedades estruturais importantes dos Aminoácidos... 6 Ligações Peptídicas... 6 Níveis De Organização Protéica... 6 Lipoproteínas... 8 Glicoproteínas... 8 Desnaturação da Proteína... 8 ESTUDO DIRIGIDO ) ENZIMAS... 9 Especificidade das Enzimas Cofatores ou Coenzimas Moduladores da Atividade Enzimática Taxa de Reação Enzimática Tipos de Reações Enzimáticas ESTUDO DIRIGIDO ) CARBOIDRATOS Monossacarídeos Derivados de Açúcares Polissacarídeos Glicoproteínas ESTUDO DIRIGIDO ) LIPÍDEOS Classificação dos Lipídeos Ácidos Graxos Triacilgliceróis = Triglicerídeos Fosfoglicerídeos = Glicerofosfolipídeos Eicosanóides Esteróides Cerídeos Lipoproteínas Glicolipídeos ESTUDO DIRIGIDO ) BIOENERGÉTICA Produção de ATP Metabolismo Anaeróbio Metabolismo Aeróbio ESTUDO DIRIGIDO ) VITAMINAS e SAIS MINERAIS Vitaminas Lipossolúveis Vitaminas Hidrossolúveis Sais Minerais ESTUDO DIRIGIDO REFERÊNCIAS BIBLIOGRÁFICAS
3 1) PROTEÍNAS As proteínas possuem uma infinidade de atuações nas células. Possuem funções dinâmicas como: transporte, controle metabólico, contração e catálise de transformações químicas. Possuem também funções estruturais, ex.: as proteínas fornecem matriz para o tecido conjuntivo propriamente dito e para o osso. As proteínas são as moléculas orgânicas mais abundantes e importantes nas células e perfazem 50% ou mais de seu peso seco. São encontradas em todas as partes de todas as células, uma vez que são fundamentais sob todos os aspectos da estrutura e função celulares. As enzimas são proteínas dinâmicas importantes, pois catalisam reações químicas, convertendo um substrato em um produto no sítio ativo da enzima. Quase todas as milhares de reações químicas que ocorrem em organismos vivos exigem uma enzima catalisadora específica. Os traços genéticos são expressos através da síntese de enzimas, que catalisam reações que estabelecem o fenótipo. Existem várias doenças genéticas que resultam de níveis alterados em uma determinada enzima ou na sua seqüência de aminoácidos. Ex.: hipercolesterolemia familiar. Temos proteínas de transporte importantes, como: a hemoglobina e a mioglobina, que transportam oxigênio no sangue e no músculo, respectivamente. A transferrina transporta ferro (Fe) no sangue. Proteínas transportadoras ligam-se carregam hormônios esteróides no sangue, de seu local de síntese para seu local de ação. Muitas drogas e compostos tóxicos são transportados ligados à proteínas. As proteínas actina e miosina estão envolvidas no processo de contração muscular. Existem proteínas com função protetora, ex.: imunoglobulinas (anticorpos) e interferon são proteínas que protegem o homem de infecções. A fibrina é importante para manter a hemostasia, ou seja, ajuda no impedimento da perda sangüínea quando ocorre lesão vascular. O homem possui hormônios protéicos como: insulina, tireotropina, somatotropina (=hormônio do crescimento), hormônio luteinizante e hormônio folículo estimulante. Existem também os hormônios peptídicos (com menos de 50 aminoácidos), são eles: hormônio adrenocorticotrófico, hormônio antidiurético, glucagon e calcitonina. As proteínas controlam e regulam a transcrição e tradução de genes. Ex.: histonas. Possuímos proteínas estruturais importantes, como: colágeno, que formam a matriz óssea; e a elastina, que proporciona força e elasticidade aos ligamentos; e a -queratina, que forma a estrutura do tecido epitelial de revestimento. Então, podemos concluir que para o entendimento do funcionamento normal e patológico do homem e de outros mamíferos depende do claro entendimento das propriedades das proteínas. Aminoácidos As proteínas são polímeros de aminoácidos. As proteínas são formadas por aminoácidos ligados entre si por ligações peptídicas. Uma ligação peptídica é a união do grupo amino (-NH 2 ) de um aminoácido com o grupo carboxila (-COOH) de outro aminoácido, através da formação de uma amida. Todas as proteínas são construídas a partir de um conjunto básico de 20 aminoácidos, arranjados em várias seqüências específicas. Logo, existem 20 aminoácidos para os quais códons de DNA são conhecidos. A transcrição e a tradução resultam na polimerização de aminoácido numa seqüencia de linear específica característica da proteína. Os aminoácidos comuns contêm um átomo central, um carbono-alfa ( ), ao qual um grupo carboxílico, um grupo amino, um átomo de hidrogênio e uma cadeia lateral (R) estão covalentemente ligados. 3
4 Um átomo de carbono com quatro substituintes diferentes arranjados na configuração tetraédrica é assimétrico e existe em duas formas enantiomorfas. Portanto, cada um dos aminoácidos apresenta isomeria óptica, exceto a glicina. A figura abaixo apresenta a projeção de Fischer para mostrar a direção espacial. O grupo -COO- é direcionado para cima e para trás do plano da página. Os grupos -H e - + NH 3 estão posicionados na posição do leitor. Um aminoácido considerado dessa forma projeta seu grupo + -NH 3 ou para a esquerda ou para direita do átomo de carbono-. Se o -NH + 3 está projetado para a + esquerda, o aminoácido tem configuração absoluta L. Logo seu enantiômero óptico possui o -NH 3 com projeção para a direita, e tem uma configuração D. As designações L e D referem-se a capacidade de girar o plano de luz polarizada para a esquerda (L, levo) ou direita (D, dextro) de seu plano de polarização. Tipos De Aminoácidos 4
5 5
6 Propriedades estruturais importantes dos Aminoácidos a) tamanho; b) núcleo compacto; c) carga; d) polaridade; e) participação em pontes de hidrogênio; f) hidrofobicidade; g) características específicas. Ligações Peptídicas A polimerização de 20 aminoácidos comuns em cadeias de polipeptídicas nas células é catalisada por enzimas e está associada com ribossomos. Quimicamente, essa polimerização é uma reação de desidratação. O grupo -carboxílico de um aminoácido com cadeia R1 forma uma ligação peptídica covalente com o grupo -amino do aminoácido com cadeia lateral R2 pela eliminação de uma molécula de água. Logo um dipeptídeo é composto por dois aminoácidos ligados por uma única ligação peptídica. Um tripeptídeo possui 3 aminoácidos ligados, um tetrapeptídeo possui 4 aminoácidos ligados, um polipeptídeo possui n<99 aminoácidos, enquanto uma proteína possui mais de 100 aminoácidos. Níveis De Organização Protéica Estrutura Primária de Proteínas É a seqüência de aminoácidos de uma proteína e suas ligações peptídicas. É o nível estrutural mais simples e mais importante, pois dele deriva todo o arranjo espacial da proteína. A estrutura primária da proteína resulta em uma longa cadeia de aminoácidos semelhante a um "colar de pérolas", com uma extremidade "amino terminal" e uma extremidade "carboxi terminal. 6
7 A estrutura primária de uma proteína é destruída por hidrólise química ou enzimática das ligações peptídicas, com liberação de peptídeos menores e aminoácidos livres. Sua estrutura é somente a seqüência dos aminoácidos, sem se preocupar com a orientação espacial da molécula. O entendimento da estrutura primária da proteína é essencial para a compreensão de seu mecanismo de ação a nível molecular e sua relação com outras proteínas com papeis fisiológicos semelhantes. Estrutura Primária Estrutura Secundária de Proteínas Refere-se ao enovelamento tridimensional local da cadeia polipeptídica numa proteína. É dada pelo arranjo espacial de aminoácidos próximos entre si na seqüência primária da proteína. É o último nível de organização das proteínas fibrosas, mais simples estruturalmente. Ocorre graças à possibilidade de rotação das ligações entre os carbonos a dos aminoácidos e seus grupamentos amina e carboxila. O arranjo secundário de um polipeptídeo pode ocorrer de forma regular; isso acontece quando os ângulos das ligações entre carbonos a e seus ligantes são iguais e se repetem ao longo de um segmento da molécula. Estrutura em -hélice Estrutura em Fita- Estrutura Terciária de Proteínas Refere-se à estrutura tridimensional do polipeptídeo. Inclui as relações conformacionais das cadeias laterais no espaço e a relação geométrica entre regiões distantes da cadeia polipeptídica. É a forma tridimensional como a proteína se "enrola". Ocorre nas proteínas globulares, mais complexas estrutural e funcionalmente. Estrutura Quaternária de Proteínas Refere-se à estrutura e às interações de associação não covalente de subunidades polipeptídicas discretas numa proteína com subunidades múltiplas. Nem todas as proteínas têm estrutura quaternária. É dada pela distribuição espacial de mais de uma cadeia polipeptídica no espaço, as subunidades da molécula. As subunidades podem atuar de forma independente ou cooperativamente no desempenho da função bioquímica da proteína. 7
8 Estrutura Quaternária Lipoproteínas As lipoproteínas são complexos constituídos por proteínas e lipídeos, que formam agregados moleculares distintos. Cada tipo de lipoproteína tem massa molecular, tamanho, composição química, densidade e papel fisiológico característicos. A proteína e o lipídeo no complexo são unidos por forças não-covalentes. Ex.: HDL (lipoproteína de alta densidade), LDL (lipoproteína de baixa densidade), VLDL (lipoproteína de muito baixa densidade). Glicoproteínas As glicoproteínas constituem muitas das proteínas de membrana. Algumas podem ser antígenos que determinam o sistema ABO e o sistema de histocompatibilidade determinantes de transplantes de um indivíduo. Alterações nas glicoproteínas de membrana podem ser correlacionadas com tumorigênese e transformação maligna no câncer. A maioria das proteínas plasmáticas, exceto a albumina, são glicoproteínas. Alguns hormônios protéicos são glicoproteínas (ex.: hormônio folículo estimulante FSH). A percentagem de carboidrato nas glicoproteínas é variável. As imunoglobulinas contêm pequena quantidade de carboidrato (4%), enquanto que a glicoproteína gástrica possui 82% de carboidrato. Desnaturação da Proteína A desnaturação ocorre quando uma proteína perde a sua estrutura nativa secundária, terciária e/ou quaternária. A estrutura primária não é necessariamente quebrada pela desnaturação. O estado desnaturado está sempre relacionado com a perda da função da proteína. A perda da função não é sinônimo de desnaturação, pois pequenas alterações conformacionais podem levar a perda da função, mesmo sem ocorrer a desnaturação. A concentração de uma proteína na célula é controlada por sua velocidade de síntese e degradação. Entender o processo que controla a degradação de uma proteína é tão importante quanto entender o processo que regula a síntese. Logo, a desnaturação da proteína é a etapa que controla a velocidade de sua degradação. Enzimas celulares e organelas digerem proteínas desnaturadas. A desnaturação pode ocorrer devido a adição de uréia, detergentes, base forte, ácido forte, solvente orgânico e aquecimento. ESTUDO DIRIGIDO 1 1) Cite três papeis fundamentais das proteínas para a vida dos seres vivos. 2) Descreva ou esquematize a estrutura de um aminoácido comum. 3) Quantos aminoácidos existem para construção de nossas proteínas? 4) Qual a diferença entre um aminoácido L e um aminoácido D? 8
9 5) Quais são as propriedades estudadas em um aminoácido? 6) O que é uma ligação peptídica? 7) Quantos aminoácidos possuem um(a): (a) dipeptídeo, (b) tripeptídeo, (c) tetrapeptídeo, (d) polipeptídeo, e (e) proteína. 8) Descreva os quatro níveis de organização de uma proteína. 9) Diferencie: lipoproteína e glicoproteína. 10) O que é a desnaturação protéica? O que pode causar a desnaturação protéica? 2) ENZIMAS As enzimas são proteínas especializadas que funcionam na aceleração de reações químicas. Muitas reações, necessárias para a atividade normal das células, não aconteceriam em velocidade suficientemente altas, no ph e na temperatura do corpo, sem essas proteínas especializadas. O termo que define rapidez de uma reação química, se catalisada ou não, é taxa ou velocidade. Taxa (=velocidade) é a variação na quantidade (mol, gramas) de materiais iniciais ou de produtos por unidade de tempo. Enzimas aumentam a velocidade atuando como catalisadores. Um catalisador aumenta a velocidade de uma reação química, mas não é alterado no processo. Uma enzima pode ficar temporariamente ligada à molécula que está sendo transformada durante estágios intermediários da reação, mas no final da reação a enzima estará, novamente, na sua forma original, quando o produto é liberado. Sendo assim, a enzima não é alterada como resultado da catálise. Em função de uma enzima não ser modificada ou utilizada diretamente na reação que ela catalisa, ela é apresentada na equação da reação do seguinte modo: A + B + Enzima C + D + Enzima ou A + B ENZIMA C + D Em reações catalisadas por enzimas os reagentes são denominados substratos. Como uma enzima aumenta a taxa de uma reação? Em termos termodinâmicos, ela reduz a energia de ativação tornando mais provável que a reação se inicie. As enzimas fazem isto, porque ao se ligarem às moléculas reagentes agrupam-nas na melhor posição, para que possam reagir umas com as outras. Sem enzimas, a reação dependeria da colisão ao acaso das moléculas reagentes até que estas se agrupassem de modo a poder reagir. Observe na figura abaixo que não houve alteração do conteúdo de energia livre inicial nem final dos substratos e produtos. 9
10 A maioria das enzimas são grandes moléculas de proteína com formas tridimensionais complexas. Em casa molécula de uma enzima há uma região denominada sítio de ligação, que é a parte da molécula da proteína que realmente se liga aos substratos. Quando a ligação enzima-substrato ocorre, as moléculas do substrato são colocadas juntas umas das outras e do sítio ativo da enzima, a região que promove a reação dos substratos entre si. Por muitos anos pensou-se que o sítio de ligação tinha o formato para encaixar-se ao substrato de modo exato, do mesmo modo que uma chave se encaixa em uma fechadura. Hoje os cientistas descobriram que o sítio de ligação e os substratos não necessitam ajustar-se de modo exato. O sítio de ligação somente necessita atrair os substratos para aquela região da enzima. Então, à medida que o sítio de ligação e os substratos começam a interagir, o sítio de ligação muda seu formato para ajustar-se mais proximamente aos substratos. Este modelo denomina-se adaptação induzida. De acordo com este modelo, o sítio de ligação possui um formato intermediário que pode modificar-se para ajustar-se tanto ao substrato quanto ás moléculas produzidas. Esta característica possibilita uma enzima se ligar tanto ao substrato quanto ao produto, portanto seja capaz de catalisar uma única reação em ambas as direções. Especificidade das Enzimas A maioria das enzimas reage somente a um conjunto de substratos ou a um grupo de substratos similares. A capacidade de uma enzima de catalisar uma determinada reação ou um grupo de reações intimamente relacionadas é denominada especificidade. Algumas enzimas são muito específicas nas reações que catalisam. Ex.: glicocinase liga um grupo fosfato na glicose, quando a glicose entra na célula. Outras enzimas atuam em grupos inteiros de moléculas. As enzimas peptidases atuam sobre ligações peptídicas de polipeptídeos sem considerar quais os dois aminoácidos que estão reunidos por estas ligações. Logo, as peptidases não são muito especificas em suas reações. Para dar o nome a enzima os substratos são colocados primeiro, seguidos pelo tipo de reação aos quais a terminação ase é afixada. Ex.: álcool desidrogenase e glicocinase. Algumas enzimas possuem dois nomes. Estas enzimas foram descobertas antes de 1972, quando os atuais padrões para a 10
11 denominação das enzimas foram adotados pela 1ª vez. Sendo assim, o nome antigo e o novo nome podem ser utilizados. Um conjunto pequeno de enzimas apresenta uma variedade de formas relacionadas denominadas: isoenzimas. As isoenzimas (=isozimas) são variantes que catalisam a mesma reação química, mas sob condições distintas ou em tecidos diferentes. Suas estruturas diferem levemente, o que determina a variabilidade na sua atividade. Ex.: lactato desidrogenase possui várias isoenzimas no coração, músculo estriado esquelético e no fígado. Algumas enzimas não estão prontas para catalisar a reação quando elas são sintetizadas. Estas enzimas produzidas como moléculas inativas denominadas proenzimas ou zimogênios. Quando tais enzimas são necessárias, uma ou mais poções da molécula são cortadas fora, e a enzima torna-se ativa. Este processo é chamado de Ativação Proteolítica. As enzimas envolvidas na coagulação sangüínea e na digestão são proenzimas. Se uma enzima possui as formas inativa e ativa. A forma inativa é denominada pela adição do sufixo ogênio ao nome da enzima ativa. Ex.: Pepsinogênio é a forma inativa e pepsina é a forma ativa. Cofatores ou Coenzimas Algumas vezes a ativação de uma enzima requer a presença de uma molécula adicional ou íon, denominado cofator. Cofatores podem ser moléculas inorgânicas ou moléculas orgânicas não protéicas. Cofatores inorgânicos são íons. Ex.: Ca 2+ ou Mg 2+. Eles devem ligar-se à enzima para que os substratos possam se associar ao sítio de ligação. Cofatores orgânicos são denominados coenzimas. São freqüentemente derivadas de vitaminas. As coenzimas não alteram o sítio de ligação da enzima como os cofatores o fazem. As coenzimas atuam como receptores e carreadores de átomos ou grupos funcionais que são removidos a partir dos substratos durante a reação. As coenzimas são necessárias, mas em pequenas quantidades. Moduladores da Atividade Enzimática A capacidade de uma enzima aumentar a reação pode ser alterada por vários fatores, incluindo a temperatura, o ph ou moléculas que interagem com a enzima. Um fator que influencia a atividade de uma enzima é denominado modulador. Se um modulador ativa uma enzima, a taxa de reação catalisada pela enzima irá aumentar. Se um modulador inativa a enzima, a taxa de reação irá diminuir, podendo até parar por completo. Existem dois mecanismos pelos quais a modulação ocorre: (1) O modulador muda a capacidade de ligação do substrato ao sítio de ligação da enzima; e (2) O modulador muda a capacidade da enzima para alterar a energia de ativação da reação. 11
12 Moduladores que alteram a taxa de reação MUDANÇAS NO SUBSTRATO DE LIGAÇÃO DO SÍTIO ATIVO Inibidor Competitivo Modulador Alostérico (Ativador ou Inibidor) ph Temperatura Compete diretamente com o substrato pela ligação ao sítio ativo. Liga-se à enzima longe do sítio ativo, e muda o sítio ativo. Processo reversível. Ex.: proteínas regulatórias Os íons H + alteram a forma tridimensional da enzima pela quebra das pontes de hidrogênio ou de enxofre. Pode ser um processo irreversível se a proteína desnaturar. Alteram a forma tridimensional da enzima porque quebram as pontes de hidrogênio ou de enxofre. Pode ser um processo irreversível se a proteína desnaturar. MUDANÇAS NA CAPACIDADE DA ENZIMA DE DIMINUIR ENERGIA DE ATIVAÇÃO DA REAÇÃO Modulação Covalente Liga-se covalentemente à enzima e muda sua capacidade de alterar a energia de ativação. Ex.: adição ou remoção de grupos fosfatos. Taxa de Reação Enzimática A taxa de reação é medida através do monitoramento da velocidade em que os seus produtos são sintetizados ou em que os seus substratos desaparecem. Se a quantidade presente da enzima ou a concentração do substrato mudam, a taxa de reação também mudará. Um importante determinante da taxa de reação enzimática é a quantidade de enzima presente. Logo, a taxa de reação é proporcional à quantidade de enzima. O relacionamento entre a concentração da enzima e a taxa de reação é um caminho importante pelo qual as células regulam os seus processos fisiológicos. As células controlam a quantidade de enzima por regularem a sua síntese e degradação. Se a síntese de uma enzima excede a degradação, a enzima se acumula e a velocidade de reação aumenta. Se a degradação da enzima excede a síntese, a quantidade da enzima diminui, e também a velocidade de reação. Quando a quantidade de enzima é constante, o turnover é fixo. Se a concentração de enzima for constante, a taxa de reação irá variar de acordo com a concentração de substrato. Em baixas concentrações de substrato, a taxa de reação é diretamente proporcional à concentração deste substrato. Mas quando a concentração de substrato aumenta, o número de moléculas de enzima fica limitado e não existem mais sítios de ligação livres para as moléculas de substrato se ligarem. A enzima, mesmo catalisando reações rapidamente, pode chegar num limite máximo = saturação. 12
13 Algumas reações são reversíveis. Deste modo a reação pode acontecer de A+B C+D ou C+D A+B. Na reação inversa, os produtos tornam-se reagentes e os reagentes tornam-se produtos. As reações reversíveis se direcionam a um estado de equilíbrio, onde a taxa de reação na direção posterior (A+B C+D) é exatamente igual à taxa da reação inversa (C+D A+B). no equilíbrio, não existe mudança no total da quantidade de reagente e produto. Tão rápido quanto A e B convertem-se em C e D, a reação inversa acontece na mesma taxa. Se a concentração de substrato (A e B) ou produto (C e D) muda, o equilíbrio é interrompido. O sistema então ajusta as concentrações de substrato e produto até que a relação de equilíbrio seja restaurada. À medida que a concentração de substrato muda, a mudança se reflete nas concentrações dos produtos. Tipos de Reações Enzimáticas TIPO DE REAÇÃO O QUE ACONTECE ENZIMAS REPRESENTATIVAS 1) OXIRREDUÇÃO Adiciona ou subtrai elétrons ou H + a) Oxidada Transfere elétrons de um doador para o oxigênio Remove elétrons e H + Oxidase Desidrogenase b) Reduzida Ganha elétrons Redutase 2) HIDRÓLISE e DESIDRATAÇÃO Adiciona ou subtrai água Hidrolase a) Hidrólise Divide moléculas grandes pela adição de água Protease, Lipase b) Desidratação Remove água. Usado para fazer grandes moléculas a partir de várias moléculas menores 3) TRANSFERÊNCIA DE GRUPOS Adiciona, subtrai ou muda grupos entre QUÍMICOS moléculas a) Reação de troca Fosfato Grupo Amina b) Adição de um Grupo Fosfato Grupo Amina c) Subtração de um Grupo Fosfato Grupo Amina 4) LIGAÇÃO Liga dois substratos usando a energia a partir do ATP Cinase Transaminase Fosforilase Aminase Fosfatase Deaminase Sintetase ESTUDO DIRIGIDO 2 1) O que é uma enzima? 2) Defina: (a) taxa de reação, (b) catalisador, (c) substrato, (d) produto, (e) sítio de ligação, (f) sítio ativo 3) Como uma enzima aumenta a taxa de uma reação? 4) Qual a diferença entre o modelo de chave e fechadura e o modelo de adaptação induzida? 5) O que é especificidade enzimática? Todas as enzimas possuem alta especificidade? 6) Caracterize: (a) isoenzimas e (b) proenzimas 7) Como uma proenzima se torna ativa? 8) Qual a importância de um cofator? Qual a diferença entre cofator e coenzima? 13
14 9) Explique como atuam os seguintes moduladores enzimáticos: (a) ph, (b) temperatura, (c) inibidor competitivo, (d) modular alostérico de ativação, (e) modulador alostérico de inibição, (f) modulação covalente. 10) Como medimos a taxa de reação enzimática? 11) Quais fatores podem alterar a taxa de reação enzimática? 12) O que é satura enzimática? 13) Denomine os quatro tipos de reações enzimáticas. 3) CARBOIDRATOS O nome carboidrato provém da sua estrutura: literalmente, carbono com água. A fórmula básica dos carboidratos é (CH 2 O) n, mostrando que para cada carbono existem dois hidrogênios e um oxigênio, a mesma razão H:O encontrada na água. O n após os parênteses representa o número de repetições da unidade CH 2 O: C n H 2n O n. Ex.: a glicose ou hexose, C 6 H 12 O 6, tem um n=6. A glicose é um exemplo da um açúcar simples, sendo o menor tipo de carboidrato. Os carboidratos também podem ser denominados: glicídios, ou hidratos de carbono, ou sacarídeos. Os nomes de todos os açúcares simples terminam com o sufixo ose. Existem dois tipos de açúcares simples, os monossacarídeos (mono= um + sakcharon= açúcar), e os dissacarídeos (di=dois). Os monossacarídeos são as unidades de construção dos carboidratos complexos e têm tanto cinco carbonos, como a ribose, quanto seis carbonos, como a glicose (dextrose), frutose e galactose. Quando dois monossacarídeos ligam-se entre si, eles formam uma molécula de dissacarídeo. São dissacarídeos típicos a maltose, lactose (açúcar do leite) e a sacarose (açúcar de mesa). Quando muitas moléculas de glicose juntam-se umas com as outras, elas formam moléculas muito grandes. Estas moléculas complexas de carboidratos são denominadas polissacarídeos (poly= muitos). Uma molécula grande formada por unidades que se repetem é denominada polímero. Deste modo, todos os carboidratos complexos são polímeros de glicose. Como estes polímeros têm um único tipo de molécula, a glicose, as diferenças entre os polissacarídeos ocorrem pelo modo em que as moléculas de glicose estão ligadas. Todas as células de um organismo vivo armazenam glicose como fonte de energia sob a forma de polissacarídeos, e algumas células também produzem polissacarídeos com um propósito estrutural. Ex.: leveduras e bactérias produzem um polímero de armazenamento de glicose denominado dextran. Muitos animais invertebrados sintetizam um polissacarídeo estrutural denominado quitina. Plantas produzem dois tipos de polissacarídeos: uma molécula de armazenagem denominada amido, digerível pelos humanos, e uma molécula estrutural denominada celulose, não digerível pelos humanos. Infelizmente não somos capazes de digerir a celulose e obter sua energia, pois trata-se da molécula orgânica mais abundante no planeta. Células animais produzem um polissacarídeo de armazenamento denominado glicogênio que é encontrado em todos os tecidos corporais, principalmente no músculo estriado esquelético e no fígado. A glicose é um dos principais combustíveis do corpo. Ela circula na corrente sangüínea e é a unidade básica na produção de glicogênio. Durante a absorção digestiva de um alimento para a corrente sangüínea, a glicose fornece a maior parte da energia necessária ao corpo. O excesso é convertido em glicogênio e gordura. A ribose e a desoxirribose são dois monossacarídeos de cinco carbonos, pentoses, biologicamente importantes como constituintes de outro grupo importante de compostos orgânicos denominados ácidos nucléicos, e suas unidades básicas são denominadas nucleotídeos. Os carboidratos são também muito importantes na composição da substância fundamental dos tecidos conjuntivos, esses carboidratos são denominados mucopolissacarídeos. Essa substância fundamental e as proteínas fibrosas embebidas nela constituem a matriz extracelular do tecido conjuntivo (substância intercelular). 14
15 Os carboidratos não catalisam reações químicas complexas como as proteínas, nem se replicam como os ácidos nucléicos. Devido ao fato de os polissacarídeos não serem construídos de acordo com um molde genético, como as proteínas e os ácidos nucléicos, eles tendem a ser muito mais heterogêneos tanto em tamanho como em composição do que outras moléculas biológicas. Entretanto, tornou-se claro que a variação estrutural dos carboidratos é fundamental para sua atividade biológica. As organizações aparentemente casuais dos carboidratos nas proteínas e na superfície das células são a chave para muitos eventos de reconhecimento entre as proteínas e entre as células. A compreensão da estrutura dos carboidratos, desde o mais simples monossacarídeo até o mais complexo polissacarídeo ramificado, é essencial para o reconhecimento das diversas funções dos carboidratos nos sistemas biológicos. Monossacarídeos Os monossacarídeos, ou açúcares simples, são sintetizados a partir de precursores menores, originalmente derivados de CO 2 e H 2 O pela fotossíntese. Os monossacarídeos são aldeídos ou cetonas derivados de poliidroxialcoóis de cadeia linear contendo pelo menos três átomos de carbono. Eles são classificados de acordo com a natureza química de seu grupo carbonila e pelo número de seus átomos de carbono. Se o grupo carbonila for um aldeído, o açúcar será uma aldose. Se o grupo carbonila for uma cetona, o açúcar será uma cetose. Os monossacarídeos menores, com três átomos de carbono, são as trioses. Aqueles com quatro, cinco, seis, sete ou mais átomos de carbono são, respectivamente, tetroses, pentoses, hexoses, heptoses, etc. Ex.: aldose D-glicose (CH 2 O) 6 A indicação D ou L nas aldoses é feita de acordo com a convenção de Fisher. Os L açúcares são as imagens especulares de seus D açúcares. O prefixo D é freqüentemente omitido porque os L açúcares, são biologicamente muito menos abundantes do que os D açúcares. Os açúcares que se diferem apenas pela configuração em torno de um átomo de C são denominados epímeros uns dos outros. Portanto, a D-glicose e a D-manose são epímeros em relação ao C2. Os açúcares de seis carbonos glicose, manose e galactose são as aldoses mais comuns. 15
16 Algumas cetoses são denominadas de acordo com a inserção ul anterior ao sufixo ose do nome da aldose correspondente; assim: D-xilulose é a Cetose correspondente à aldose D-xilose. As cetoses mais comuns são diidroxiacetona, ribulose e frutose, as quais encontramos em nossos estudos do metabolismo. 16
17 IMPORTANTE: um açúcar com um anel de seis membros é conhecido com piranose. Os açúcares com anéis de cinco membros são denominados furanoses. Derivados de Açúcares Devido ao fato das formas lineares e cíclicas das aldoses e das cetoses se interconverterem, esses açúcares sofrem reações típicas de aldeídos e cetonas. 1) A oxidação química branda ou a oxidação enzimática de uma aldose converte seus grupo aldeído a um grupo carboxílico ácido, produzindo um ácido aldônico como o ácido glicônico. 2) A oxidação específica do álcool das aldoses produz ácidos urônicos, que são nomeados por meio da adição do sufixo urônico à raiz do nome da aldose parental.ex.: ácido glicurônico. 17
18 3) As aldoses e as cetoses podem ser reduzidas sob condições amenas para produzir poliidroxialcoóis acíclicos conhecidos como alditóis. Ex.: Ribitol (componente da coenzima flavina), glicerol e o mioinositol (componente lipídico importante) e xilitol (adoçante utilizados em chicletes sem açúcar ). 4) As unidades monossacarídicas nas quais um grupo OH é substituído por H são conhecidas como desoxiaçúcares. O de maior importância é a -D-2-desoxirribose (açúcar do DNA). A L-fucose é um L-açúcar componente dos polissacarídeos. 5) Nos aminoaçúcares, um ou mais grupos OH foram substituídos por um grupo amina. Ex.: D- glicosamina e D-galactosamina. Polissacarídeos Formam polímeros ramificados e lineares. Isso ocorre porque as ligações glicosídicas podem ser formadas por qualquer grupo hidroxila de um monossacarídeo. São classificados em homopolissacarídeos ou heteropolissacarídeos se consistirem de um ou mais tipos de monossacarídeos. Apesar de as seqüências de monossacarídeos dos heteropolissacarídeos poderem, ser mais variadas do que as das proteínas, muitos são compostos por apenas poucos tipos de monossacarídeos que se alternam em uma seqüência repetitiva. Os dissacarídeos são os polissacarídeos mais simples. O dissacarídeo mais abundante é a sacarose. 18
19 As plantas possuem paredes rígidas que suportam diferenças de pressão osmótica entre os espaços extra e intracelular de até 20atm. Em plantas grandes, como árvores, a parede celular também tem a função de sustentação. A celulose, o componente estrutural principal da parede celular das plantas, é responsável por mais da metade do carbono presente na biosfera. A quitina é o principal componente estrutural do exoesqueleto de invertebrados, como: crustáceos, insetos e aranhas, estando também presente na parede celular algumas algas. É tão abundante quanto à celulose. O amido é um polissacarídeo de reserva energética. É depositado nos cloroplastos das células vegetais como grânulos insolúveis compostos por -amilose e amilopectina. 19
20 O glicogênio, polissacarídeo de reserva dos animais, está presente em todas as células, mas é mais abundante no músculo estriado esquelético e no fígado, onde ocorre sob a forma de grânulos citoplasmáticos. A estrutura primaria do glicogênio assemelha-se a da amilopectina, mas o glicogênio é mais ramificado, com pontos de ramificação ocorrendo a cada 8 a 14 resíduos de glicose. Os carboidratos da substância fundamental conhecidos como mucopolissacarídeos, são heteropolissacarídeos (heteros= outros), isto é, eles são compostos de duas diferentes unidades de monossacarídeos. Essas unidades de açúcares são de dois tipos: os que têm um grupo ácido (açúcares ácidos) e aquelas que têm um grupo amino (açúcares aminados). O mucopolissarídeo mais abundante é o ácido hialurônico, no qual o ácido glicurônico e a N-acetilglicosamina alternam-se regularmente em uma cadeia não ramificada. Outros importantes mucopolissarídeos são os sulfatos de condroitina, encontrados principalmente na substância fundamental da matriz cartilaginosa. Nas cadeias desses mucopolissacarídeos, a galactosamina contém um grupo sulfato alternando-se com o ácido glicurônico. Os mucopolissacarídeos podem estar combinados com pequenas quantidades de proteínas, denominadas mucoproteínas ou proteoglicanas. 20
21 Glicoproteínas As glicoproteínas constituem muitas das proteínas de membrana. Algumas podem ser antígenos que determinam o sistema ABO e o sistema de histocompatibilidade determinantes de transplantes de um indivíduo. Alterações nas glicoproteínas de membrana podem ser correlacionadas com tumorigênese e transformação maligna no câncer. A maioria das proteínas plasmáticas, exceto a albumina, são glicoproteínas. Alguns hormônios protéicos são glicoproteínas (ex.: hormônio folículo estimulante FSH). A percentagem de carboidrato nas glicoproteínas é variável. As imunoglobulinas contêm pequena quantidade de carboidrato (4%), enquanto que a glicoproteína gástrica possui 82% de carboidrato. ESTUDO DIRIGIDO 3 1) Explique a fórmula básica do carboidrato. 2) Quais são os dois tipos de açúcares simples? Qual a diferença entre eles? 3) Caracterize: (a) mucopolissacarídeo e (b) glicoproteína. 4) O que são açúcares epímeros? 5) Diferencie: furanose e piranose. 6) O que é um derivado de açúcar? Cite três exemplos. 7) Defina polissacarídeo. Qual a diferença entre um homopolissacarídeo e um heteropolissacarídeo. 8) Qual a importância dos seguintes polissacarídeos: (a) amido, (b) glicogênio, (c) celulose, e (d) quitina 4) LIPÍDEOS Os lipídeos são biomoléculas feitas de carbono, hidrogênio e oxigênio, como os carboidratos, mas possuem muito menos oxigênio. Uma característica importante é que os lipídeos não são muito solúveis em água, devido à sua estrutura apolar. Tecnicamente, em temperatura ambiente, os lipídeos são denominados gorduras, quando no estado sólido, e óleos, quando no estado líquido. Muitos lipídeos derivados de animais, como a banha e a manteiga, são gorduras, enquanto que muitos lipídeos derivados de vegetais são óleos. Os lipídeos são o grupo mais diverso de biomoléculas. Devido à sua hidrofobicidade, os lipídeos não se misturam em água, no entanto são solúveis em solventes orgânicos, como: clorofórmio, éter, benzeno e metanol. Em geral, os lipídeos desempenham três funções biológicas: 1) As moléculas de lipídeos, na forma de uma bicamada lipídica, são componentes essenciais, juntamente com as proteínas, das membranas biológicas. 2) Os lipídeos que contêm cadeias de hidrocarbonetos servem como reservas energéticas. 3) Muitos eventos de sinalização intra e intercelulares envolvem moléculas de lipídeos. Embora os lipídeos sejam uma classe distinta de biomoléculas, veremos que eles geralmente ocorrem combinados, seja covalentemente ou através de ligações fracas para produzir moléculas híbridas tais como: glicolipídeos e lipoproteínas. Classificação dos Lipídeos A classificação baseia-se na estrutura de seu esqueleto. Os lipídeos complexos, que contêm ácidos graxos como componentes, incluem os acilgliceróis, os fosfatoglicerídeos, os esfingolipídeos e as ceras, que diferem na estrutura dos esqueletos aos quais os ácidos graxos estão covalentemente ligados. Eles também são denominados lipídeos saponificáveis, uma vez que produzem sabões (sais de ácidos graxos) sob hidrólise alcalina. 21
22 O outro grupo principal de lipídeo consiste nos lipídeos simples, que não contêm ácidos graxos e, portanto não são saponificáveis. Classificação dos Lipídeos Tipo de Lipídeo Complexo (saponificável) Acilgliceróis (triglicerídeos) Fosfoglicerídeos Esfingolipídeos Ceras Simples (não-saponificáveis) Terpenos Esteróides Eicosanóides Esqueleto Glicerol Glicerol-3-fosfato Esfingosina Alcoóis não-polares de peso molecular elevado Ácidos Graxos Embora os ácidos graxos ocorram em quantidades muitos grandes como blocos construtivos componentes dos lipídeos saponificáveis, eles ocorrem apenas em traços na forma livre nas células e tecidos. Existem mais de 100 tipos de ácidos graxos. Todos possuem uma longa cadeia hidrocarbonada e um grupo carboxílicos terminal. A cadeia hidrocarbonada pode ser saturada (ex.: ácido palmítico), ou pode possuir uma ou mais duplas ligações (ex.: ácido oléico); alguns ácidos graxos contém triplas ligações. Os ácidos graxos diferem um do outro no comprimento da cadeia e no número e posição de suas ligações insaturadas. 22
23 Os ácidos graxos mais abundantes têm um número par de átomos de carbono com cadeias entre 14 e 22 átomos de carbono de comprimento, mas aqueles com 16 a 18 carbonos predominam. Os mais comuns entre os ácidos graxos saturados são o ácido palmítico (C 16 ) e o ácido esteárico (C 18 ) e, entre os ácidos graxos insaturados, o ácido oléico (C 18 ). Os ácidos graxos insaturados predominam sobre os saturados, particularmente nas plantas superiores e em animais que vivem em baixas temperaturas. Ácidos graxos insaturados têm pontos de fusão mais baixos do que ácidos graxos saturados de mesmo comprimento de cadeia. Ácidos graxos com um número ímpar de átomos de carbono ocorrem somente em quantidades vestigiais nos animais terrestres, mas ocorrem em quantidades significantes em muitos organismos marinhos. Triacilgliceróis = Triglicerídeos As gorduras e os óleos existentes em plantas e em animais consistem, na sua maioria, em misturas de triglicerídeos. Essas substâncias apolares e insolúveis em água são triésteres de glicerol com ácidos graxos. Os ácidos graxos no corpo ligam-se ao glicerol para formar mono-, di-, triglicerídeos. Os triglicerídeos atuam como reservas de energia em animais, sendo a mais abundante classe de lipídeos, apesar de não serem componentes das membranas celulares. Concentrações de triglicerídeos no sangue são preditores de doenças arteriais; uma concentração elevada de triglicerídeos em jejum está relacionada a um maior risco de desenvolvimento de doenças vasculares. 23
24 As gorduras são uma forma altamente eficiente de armazenamento de energia metabólica, pois os triglicerídeos são menos oxidados do que os carboidratos ou as proteínas, fornecendo significativamente mais energia, por unidade de massa, na sua oxidação completa. As gorduras fornecem em torno de seis vezes mais energia do que um glicogênio hidratado. Nos animais os adipócitos (células de gordura) são células especializadas na síntese e no armazenamento de triglicerídeos. Enquanto outros tipos celulares têm apenas algumas gotículas de gordura dispersas no seu citosol, os adipócitos podem estar quase inteiramente preenchidos com glóbulos de gordura. O tecido adiposo é mais abundante na camada subcutânea e na cavidade abdominal. O conteúdo gorduroso dos seres humanos normais (20% nos homens e 27% nas mulheres) permite que eles sobrevivam a um jejum de dois ou três meses. De modo diferente, o suprimento normal de glicogênio, que funciona como uma reserva energética de curta duração, pode fornecer a energia necessária ao organismo por menos de 1 dia. A camada gordurosa subcutânea também fornece isolamento térmico, o que é particularmente importante para animais aquáticos de sangue quente, como baleias, focas, gansos e pingüins, os quais são rotineiramente expostos a baixas temperaturas. Fosfoglicerídeos = Glicerofosfolipídeos Os fosfoglicerídeos são o principal componente lipídico das membranas biológicas; somente quantidades muito pequenas de fosfoglicerídeos ocorrem em outros locais da célula. Muitos fosfoglicerídeos são diglicerídeos com um grupo de fosfato ligado ao único carbono que não possui um ácido graxo. Geralmente existe um ácido graxo saturado e um insaturado, o último na posição 2 do glicerol. Os fosfoglicerídeos são inadequadamente chamados por: fosfolipídeos ou fosfatídeos. Devido ao fato dos fosfoglicerídeos possuírem uma cabeça polar além de suas caudas hidrocarbonadas não-polares, eles são chamados de lipídeos anfipáticos ou polares. Os diferentes tipos de fosfoglicerídeos diferem em tamanho, forma e carga elétrica de seus grupos polares da cabeça. Cada tipo de fosfoglicerídeo pode existir em muitas espécies químicas diferentes, diferindo em seus ácidos graxos substituintes. 24
25 Membrana Plasmática A membrana plasmática (MP) também pode ser denominada membrana celular. A MP regula as trocas entre a célula e seu meio ambiente e é o receptor de sinais do meio ambiente próximo ou distante se adaptando prontamente às alterações necessárias para manter a homeostase da célula e do organismo. A MP é constituída principalmente por fosfoglicerídeos e proteínas. Sua espessura varia de 65 a 100 angstrons; isto é, menor que um milionésimo de uma polegada de espessura. A MP consiste em uma camada dupla de fosfoglicerídeos, na qual estão incrustadas proteínas. As proteínas são livres para se movimentar no interior da membrana. Em conseqüência, não estão distribuídas uniformemente, mas formam um mosaico em constantes mudanças. Aberturas minúsculas, ou poros, variando entre 7 e 10 angstrons de diâmetro se estendem através da membrana. Os fosfoglicerídeos formam duas camadas paralelas (designadas como dupla camada) com suas cabeças hidrofílicas voltadas para o meio aquoso, na superfície das membranas, e suas caudas hidrofóbicas voltadas para o interior da membrana. Proteínas interdispersas penetram parcial ou completamente na dupla camada fosfolipídica. As duas funções importantes da MP são conter os componentes da célula e regular a passagem de substância para dentro e para fora da célula. Uma troca altamente seletiva de substâncias acontece através da membrana limitante e envolve vários tipos de processos ativos e passivos. A permeabilidade da MP depende dos seguintes fatores: estrutura da membrana, tamanho das moléculas, carga iônica, solubilidade em lipídios, presença de moléculas transportadoras, e diferenças de pressão. As MPs de certas células são altamente especializadas para facilitar funções específicas. As células colunares que revestem o lúmen (porção oca) do trato intestinal têm numerosas projeções finas (= microvilos) que auxiliam no processo de absorção na digestão. Uma única célula colunar pode ter cerca de microvilos na porção exposta da MP. Certos órgãos sensoriais contêm células que têm MPs especializadas. Os fotorreceptores bastonetes e cones do olho, sensíveis aos raios luminosos têm dupla camada de membranas em forma de disco denominadas cálices ópticos. Estas estruturas contêm pigmentos associados com a visão. 25
26 Dentro do órgão de Corti no ouvido interno estão as células sensoriais internas (pêlos). Estes receptores táteis (toque) são estimulados por vibração mecânica. Esquema da MP Eicosanóides Os eicosanóides são derivados do ácido araquidônico. As prostaglandinas e compostos relacionados prostaciclinas, tromboxanas, leucotrienos e lipoxinas são conhecidos como eicosanóides, porque são todos compostos de 20 carbonos (C 20 ). Os eicosanóides agem em concentrações muito baixas e estão envolvidos no surgimento de dor e febre, e na regulação da pressão arterial, da coagulação sangüínea e da reprodução. De modo diferente dos hormônios, os eicosanóides não são transportados pela corrente sangüínea aos seus sítios de ação, tendendo a agir localmente, próximo às células que os produzem. Na verdade, a maioria dos eicosanóides decompõe-se em segundos ou em minutos, o que limita seu efeito a tecidos vizinhos. Nos seres humanos, o precursor mais importante do eicosanóide é o ácido araquidônico, um ácido graxo poliinsaturado com 4 ligações duplas. O araquidonato é armazenado nas membranas. Os produtos específicos do araquidonato são tecido-dependente. Ex.: plaquetas produzem praticamente tromboxanas, mas as células endoteliais sintetizam prostaciclinas. 26
27 Esteróides Os esteróides, a maioria de origem eucariótica, são derivados do ciclopentanoperidrofenantreno (composto por 4 anéis não-planares fusionados). O colesterol é o esteróide mais abundante nos animais, e é um componente importante na membrana plasmática dos animais. Nos mamíferos, o colesterol é o precursor metabólico dos hormônios esteróides, substâncias que regulam uma grande variedade de funções fisiológicas. Os hormônios esteróides são classificados de acordo com a resposta fisiológica que desencadeiam: 1) Os glicocorticóides, como o cortisol (C 21 ) afetam o metabolismo dos carboidratos, de proteínas e lipídeos e influenciam outras funções vitais, como reações inflamatórias e a capacidade de lidar com o estresse. 2) A aldosterona e outros mineralocorticóides regulam a excreção de sal e água pelos rins. 3) Os androgênios e os estrogênios afetam o desenvolvimento e a função sexual. A testosterona (C 19 ) é o hormônio sexual masculino responsável pelos caracteres sexuais masculinos, produção de esperma e libido. 27
28 Cerídeos Ceras são ésteres sólidos de ácidos graxos muito grandes, insolúveis em água, com alcoóis graxos monoidroxílicos de cadeia longa ou esteróis. Elas são macias e maleáveis quando levemente aquecidas, mas são duras quando frias. As ceras são encontradas como revestimentos protetores na pele, nos pêlos e nas penas, em folhas e frutos de plantas superiores, e no exoesqueleto de alguns insetos. Lipoproteínas As lipoproteínas são complexos constituídos por proteínas e lipídeos, que formam agregados moleculares distintos. Cada tipo de lipoproteína tem massa molecular, tamanho, composição química, densidade e papel fisiológico característicos. A proteína e o lipídeo no complexo são unidos por forças não-covalentes. Ex.: HDL (lipoproteína de alta densidade), LDL (lipoproteína de baixa densidade), VLDL (lipoproteína de muito baixa densidade). Glicolipídeos São moléculas de lipídeos ligadas à carboidratos. São compostos por uma ceramida (esfingosina + ácido graxo) e um glicídeo de cadeia curta. É um componente fundamental do glicocálix e membrana. Entre os principais glicídeos que formam parte dos glicolipídios encontramos a: galactose, manose, frutose, glicose, N-acetilglicosamina, e N-acetilgalactosamina. Temos os: 1) cerebrosídios que são encontrados nas membranas das células neurais. São importantes componentes dos músculos e da membrana celular do nervos, moléculas do sistema nervoso central e periférico, que formam parte da bainha de mielina dos nervos. O mais conhecido é a mielina; e 2) gangliosídios que são encontrados em grande quantidade nas células ganglionares do sistema nervoso central, especialmente nas terminações nervosas. ESTUDO DIRIGIDO 4 1) Diferencie: gordura e óleo. 2) Quais são as tres principais funções dos lipídeos? 3) Explique a classificação em lipídeos complexos e simples? 4) Caracterize: (a) ácido graxo, (b) triglicerídeo, (c) fosfoglicerídeo, (d) eicosanóide, (e) esteróide, (f) cerídeo, (g) lipoproteína, e (h) glicolipídeo. 5) Explique a estrutura da membrana plasmática. 6) Onde armazenamos os triglicerídeos? 5) BIOENERGÉTICA A eficiência das vias metabólicas como produtoras de energia é freqüentemente medida em quantidade de adenosina trifosfato (ATP) que as mesmas podem produzir. O ATP é um nucleotídeo que contém na sua molécula três grupos fosfato. O terceiro grupo fosfato é mantido na molécula por uma ligação covalente que necessita de energia. A energia é estocada nesta ligação de fosfato de alta energia e é liberada quando esta ligação é quebrada a partir da remoção do grupo fosfato. Esta relação é demonstrada pela seguinte relação: ADP + P i + energia ADP ~P (=ATP) O til significa uma ligação de alta energia e o P i é a abreviatura do fosfato inorgânico. A quantidade estimada de energia livre liberada. A ligação de alta energia formada é facilmente quebrada na presença de enzimas especializadas (ATPases), liberando a energia para o sistema reacional, em um processo exergônico. 28
29 Não só o ATP exerce essa função, mas há uma prevalência de reações intracelulares que o utilizam como a molécula fornecedora de calor para as reações endotérmicas, talvez por um preciosismo evolucionário que preferiu utilizar uma moeda única para as transações energéticas celulares. A molécula de ATP não é, entretanto, uma molécula de reserva energética por excelência, uma vez que perde muito rapidamente seu Pi, sendo, por isso, utilizada mais em reações que necessitem da liberação rápida de calor. As melhores moléculas de armazenamento real de energia são o amido, glicogênio e triglicerídeos que podem liberar a principal molécula precursora da síntese do ATP, a acetil-coa. O ATP não é a única molécula capaz de receber e liberar energia térmica para as reações bioquímicas. A condição primordial para uma molécula ser considerada "altamente" energética é ter a capacidade de transferir grupamentos químicos durante reações bioquímicas, liberando a energia para o meio (reação exergônica) possibilitando que os substratos da reação absorvam esta energia para ser produzido os produtos. Moléculas Altamente Energéticas que Participam dos Processos Bioquímicos Essenciais Molécula Energética Grupo de Transferência Exemplos de reações que participam ATP (Adenosina trifosfato) UTP (Uridina trifosfato) GTP (Guanosina trifosfato) Creatina-fosfato NADH (Nicotinamida-adenina-dinucleotídeo) NADPH (NAD-fosfato) FADH 2 (Flavina-adenina-dinucleotídeo) P i (Fosfato inorgânico) Elétrons, hidrogênio Glicólise, ciclo de Krebs, cadeia respiratória e síntese da creatina Síntese do ácido láctico, ciclo de Krebs e cadeia respiratória Acetil-CoA (Acetil Coenzima A) Grupo acil Ciclo de Krebs, -Oxidação, Síntese de aminoácidos e lipídeos Biotina Gás carbônico (CO 2 ) Ciclo de Krebs THC (Tetra-hidro-folato) Carbono simples Síntese de aminoácidos TPP (Tiamina-priofosfato) Aldeído Ciclo de Krebs, Sínes de Acetil-CoA adomet (S-adenosilmetionina) Metil Síntese e Degradação de aminoácidos Uridina-bi-fosfato-glicose Glicose Síntese do amido e glicogênio As vias metabólicas que produzem a maioria das moléculas de ATP são aquelas que necessitam de oxigênio (O 2 ) denominadas vias aeróbias ou oxidativas. As vias anaeróbias podem ocorrer sem O 2 também produzem moléculas de ATP, porém em quantidades muito menores. Produção de ATP As vias catabólicas que extraem energia a partir das biomoléculas e a transferem para o ATP são: Glicólise, Ciclo de Krebs e Sistema de Transporte de Elétrons. A produção aeróbia de ATP segue duas vias comuns: Glicólise e Ciclo de Krebs. Essas duas vias produzem uma pequena quantidade de ATP diretamente, porém sua contribuição mais importante são os elétrons de alta energia carreados pelo NADH e FADH 2 para o Sistema de Transporte de Elétrons na mitocôndria. O Sistema de Transporte de Elétrons transfere energia dos elétrons para as ligações fosfato de alta energia do ATP. Em vários pontos do processo produz CO 2 e água (H 2 O). A água pode ser usada pela célula, as o CO 2 é um produto de excreção e deve ser removido do corpo. As biomoléculas utilizadas para produzir energia são: carboidratos, lipídeos e proteínas. Os carboidratos são os alimentos energéticos por excelência, apesar de os lipídios serem mais calóricos. Os lipídios são compostos primários de reserva energética na maioria dos animais justamente pelo fato de serem primeiro armazenados como indicativo de excesso de calorias na alimentação. Os nutrientes energéticos ingeridos diariamente, rapidamente são consumidos. As reservas de glicogênio sintetizado a partir de excesso de glicose duram, no máximo, 24 horas, enquanto que as reservas de lipídios armazenadas nos adipócitos podem fornecer, em tese, energia para cerca de um mês sem a ingestão de alimentos. Entretanto, a produção de compostos secundários a degradação dos lipídios (os corpos cetônicos) possuem ação danosa ao organismo, o que faz que um animal que não se alimente por mais de duas semanas morra por inanição. Os animais hibernantes são exceção a essa regra, pois os lipídios armazenados durante as estações quentes garantem a energia e água necessárias durante o inverno, sem haver a ação danosa dos corpos cetônicos, mas sim seu aproveitamento total no 29
Proteínas. Dra. Flávia Cristina Goulart. Bioquímica
 Proteínas Dra. Flávia Cristina Goulart Bioquímica Os aa. e as proteínas Nos animais, as proteínas correspondem à cerca de 80% do peso dos músculos desidratados, cerca de 70% da pele e 90% do sangue seco.
Proteínas Dra. Flávia Cristina Goulart Bioquímica Os aa. e as proteínas Nos animais, as proteínas correspondem à cerca de 80% do peso dos músculos desidratados, cerca de 70% da pele e 90% do sangue seco.
FRENTE III QUÍMICA ORGÂNICA BIOQUÍMICA: CARBOIDRATOS E LIPIDEOS
 CARBOIDRATOS Os carboidratos são as biomoléculas mais abundantes na natureza. Estima-se que, por meio da fotossíntese, as plantas produzem 6.000.000 de toneladas do carboidrato celulose por hora no mundo.
CARBOIDRATOS Os carboidratos são as biomoléculas mais abundantes na natureza. Estima-se que, por meio da fotossíntese, as plantas produzem 6.000.000 de toneladas do carboidrato celulose por hora no mundo.
LIPÍDIOS. 1º ano Pró Madá
 LIPÍDIOS 1º ano Pró Madá O QUE SÃO? Também chamados de gorduras Compostos com estrutura molecular variada principalmente, por moléculas de hidrogênio, oxigênio, carbono Característica principal insolubilidade
LIPÍDIOS 1º ano Pró Madá O QUE SÃO? Também chamados de gorduras Compostos com estrutura molecular variada principalmente, por moléculas de hidrogênio, oxigênio, carbono Característica principal insolubilidade
Membranas Biológicas. Profª Eleonora Slide de aula
 Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
A Química da Vida. Anderson Dias Felipe Knak
 A Química da Vida Anderson Dias Felipe Knak A ÁGUA NAS CÉLULAS A água é imprescindível à vida dos indivíduos, independendo da espécie, idade, metabolismo e/ou grupo celular. A água exerce função de transporte
A Química da Vida Anderson Dias Felipe Knak A ÁGUA NAS CÉLULAS A água é imprescindível à vida dos indivíduos, independendo da espécie, idade, metabolismo e/ou grupo celular. A água exerce função de transporte
AMINOÁCIDOS E PROTEÍNAS
 AMINOÁCIDOS E PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição
AMINOÁCIDOS E PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição
Membranas Biológicas. Profª Eleonora Slide de aula
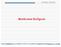 Membranas Biológicas Profª Eleonora Slide de aula Membranas biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Membranas Biológicas Profª Eleonora Slide de aula Membranas biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Átomos Moléculas Íons Biomoléculas. Matéria é formada por Átomos. Obs.: teoria confirmada apenas no início do século XX.
 Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
10/10/2012 CARBOIDRATOS CARBOIDRATOS CARBOIDRATOS
 ARBIDRATS ARBIDRATS I Ê N I A S M L E U L A R E S E E L U L A R E S P R F ª. F E R N A N D A. E S T E V E S D E L I V E I R A arboidratos (ou hidratos de carbono ou glicídios ou açúcares) compostos por
ARBIDRATS ARBIDRATS I Ê N I A S M L E U L A R E S E E L U L A R E S P R F ª. F E R N A N D A. E S T E V E S D E L I V E I R A arboidratos (ou hidratos de carbono ou glicídios ou açúcares) compostos por
Composição Química da Célula
 Composição Química da Célula Inorgânicos Caracteriza-se pela pequena complexidade e baixa quantidade de energia. São eles: Água Sais Minerais Orgânicos São complexas e ricas em energia. Podem ser: Proteínas
Composição Química da Célula Inorgânicos Caracteriza-se pela pequena complexidade e baixa quantidade de energia. São eles: Água Sais Minerais Orgânicos São complexas e ricas em energia. Podem ser: Proteínas
Estrutura e Função de Proteínas
 Estrutura e Função de Proteínas As Proteínas As proteínas observadas na natureza evoluíram pela pressão selectiva para efetuar funções específicas. As propriedades funcionais das proteínas dependem da
Estrutura e Função de Proteínas As Proteínas As proteínas observadas na natureza evoluíram pela pressão selectiva para efetuar funções específicas. As propriedades funcionais das proteínas dependem da
Bioenergética FONTES ENERGÉTICAS. BE066 Fisiologia do Exercício. Sergio Gregorio da Silva, PhD. Definição de Energia! Capacidade de realizar trabalho
 BE066 Fisiologia do Exercício Bioenergética Sergio Gregorio da Silva, PhD FONTES ENERGÉTICAS Definição de Energia! Capacidade de realizar trabalho Definição de Trabalho! Aplicação de força através de uma
BE066 Fisiologia do Exercício Bioenergética Sergio Gregorio da Silva, PhD FONTES ENERGÉTICAS Definição de Energia! Capacidade de realizar trabalho Definição de Trabalho! Aplicação de força através de uma
TRANSPORTE DE SOLUTOS ATRAVÉS DAS MEMBRANAS CELULARES. Prof. Dr. ROBERTO CEZAR LOBO DA COSTA
 TRANSPORTE DE SOLUTOS ATRAVÉS DAS MEMBRANAS CELULARES Prof. Dr. ROBERTO CEZAR LOBO DA COSTA TIPOS DE TRANSPORTES A) SIMPLASTO: termo usado para caracterizar os protoplastos interconectados e seus plasmodesmas
TRANSPORTE DE SOLUTOS ATRAVÉS DAS MEMBRANAS CELULARES Prof. Dr. ROBERTO CEZAR LOBO DA COSTA TIPOS DE TRANSPORTES A) SIMPLASTO: termo usado para caracterizar os protoplastos interconectados e seus plasmodesmas
02/03/2012. Unidade III: Bioquímica Celular. Componentes Químicos da Célula. Composição Química Atmosfera. Composição Química das Células
 Componentes Químicos da Célula Unidade III: Bioquímica Celular Disciplina: Biologia Celular e Molecular Centro de Ciências da Saúde Profa. Dra. Marilanda Ferreira Bellini marilanda.bellini@usc.br Pró Reitoria
Componentes Químicos da Célula Unidade III: Bioquímica Celular Disciplina: Biologia Celular e Molecular Centro de Ciências da Saúde Profa. Dra. Marilanda Ferreira Bellini marilanda.bellini@usc.br Pró Reitoria
Introdução - Definição
 Lipídios Introdução - Definição Lipídios ou lípidos engloba todas as substâncias gordurosas existentes no reino animal e vegetal (do grego lipos = gordura). Lipídios Introdução - Definição Caracterizam-se
Lipídios Introdução - Definição Lipídios ou lípidos engloba todas as substâncias gordurosas existentes no reino animal e vegetal (do grego lipos = gordura). Lipídios Introdução - Definição Caracterizam-se
constituídos por moléculas orgânicas de Estas são formadas por um número
 Constituintes básicos de uma célula Moléculas da vida Todos os seres vivos, logo, as suas células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por
Constituintes básicos de uma célula Moléculas da vida Todos os seres vivos, logo, as suas células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por
Metabolismo dos Carboidratos
 Metabolismo dos Carboidratos Disciplina: Nutrição Aplicada a Educação Física Prof ₐ Mda. Vanessa Ribeiro dos Santos Definição O que são carboidratos? Os carboidratos são compostos orgânicos que contêm:
Metabolismo dos Carboidratos Disciplina: Nutrição Aplicada a Educação Física Prof ₐ Mda. Vanessa Ribeiro dos Santos Definição O que são carboidratos? Os carboidratos são compostos orgânicos que contêm:
PROGRAMA DE DISCIPLINA VERSÃO CURRICULAR: 2014/2 PERÍODO: 1º DEPARTAMENTO: BIQ
 PROGRAMA DE DISCIPLINA DISCIPLINA: Bioquímica Aplicada à Enfermagem CÓDIGO: BIQ004 COORDENADOR: CARGA HORÁRIA TEÓRICA CARGA HORÁRIA PRÁTICA CRÉDITOS INÍCIO TÉRMINO 30 30 4 VERSÃO CURRICULAR: 2014/2 PERÍODO:
PROGRAMA DE DISCIPLINA DISCIPLINA: Bioquímica Aplicada à Enfermagem CÓDIGO: BIQ004 COORDENADOR: CARGA HORÁRIA TEÓRICA CARGA HORÁRIA PRÁTICA CRÉDITOS INÍCIO TÉRMINO 30 30 4 VERSÃO CURRICULAR: 2014/2 PERÍODO:
Fisiologia do Exercício. cio. Aula 1
 Aula 1 Conceito É a capacidade de realizar trabalho. É tudo que pode modificar a matéria TRABALHO É o produto da força ou componente da força na direção do deslocamento, pelo deslocamento. Portanto, para
Aula 1 Conceito É a capacidade de realizar trabalho. É tudo que pode modificar a matéria TRABALHO É o produto da força ou componente da força na direção do deslocamento, pelo deslocamento. Portanto, para
Cat Ca ab a olismo Anab a ol o ismo
 A acção das enzimas Metabolismo celular É o conjunto de reacções químicas que ocorrem numa célula. Catabolismo moléculas complexas são convertidas em moléculas mais simples, com libertação de energia.
A acção das enzimas Metabolismo celular É o conjunto de reacções químicas que ocorrem numa célula. Catabolismo moléculas complexas são convertidas em moléculas mais simples, com libertação de energia.
Ácidos Nucléicos Duplicação do DNA e Síntese de PROTEÍNAS. Paulo Dutra
 Ácidos Nucléicos Duplicação do DNA e Síntese de PROTEÍNAS Paulo Dutra ÁCIDOS NUCLEICOS Nucleotídeos É a unidade formadora dos ácidos nucléicos: DNA e RNA. É composto por um radical fosfato, uma pentose
Ácidos Nucléicos Duplicação do DNA e Síntese de PROTEÍNAS Paulo Dutra ÁCIDOS NUCLEICOS Nucleotídeos É a unidade formadora dos ácidos nucléicos: DNA e RNA. É composto por um radical fosfato, uma pentose
Introdução - Definição
 Apostila 6 Frente D Introdução - Definição Lipídios ou lípidos engloba todas as substâncias gordurosas existentes no reino animal e vegetal (do grego lipos = gordura). Lipídios Introdução - Definição Caracterizam-se
Apostila 6 Frente D Introdução - Definição Lipídios ou lípidos engloba todas as substâncias gordurosas existentes no reino animal e vegetal (do grego lipos = gordura). Lipídios Introdução - Definição Caracterizam-se
Proteínas e aminoácidos
 Proteínas e aminoácidos Digestão Absorção Metabolismo Disciplina de Bioquímica Profa. Dra. Celene Fernandes Bernardes Proteínas da dieta Proteínas endógenas Proteínas endógenas Síntese de aminoácidos não
Proteínas e aminoácidos Digestão Absorção Metabolismo Disciplina de Bioquímica Profa. Dra. Celene Fernandes Bernardes Proteínas da dieta Proteínas endógenas Proteínas endógenas Síntese de aminoácidos não
POTENCIAL DE PRODUÇÃO DE PLANTAS FORRAGEIRAS. Maria Aparecida Salles Franco Curso de Veterinária Disciplina: Forragicultura e Plantas Tóxicas
 POTENCIAL DE PRODUÇÃO DE PLANTAS FORRAGEIRAS Maria Aparecida Salles Franco Curso de Veterinária Disciplina: Forragicultura e Plantas Tóxicas Um pouco sobre nutrientes nos alimentos Do ano de 1917 para
POTENCIAL DE PRODUÇÃO DE PLANTAS FORRAGEIRAS Maria Aparecida Salles Franco Curso de Veterinária Disciplina: Forragicultura e Plantas Tóxicas Um pouco sobre nutrientes nos alimentos Do ano de 1917 para
Estas aminas são bases de Lewis já que sobram elétrons no átomo de nitrogênio e como tal podem reagir com ácidos.
 01. Os compostos mostrados são respectivamente amina primária, amina secundária e amina terciária. O composto III, por não apresentar ligações (pontes) de hidrogênio, é o menos solúvel em água, tornando
01. Os compostos mostrados são respectivamente amina primária, amina secundária e amina terciária. O composto III, por não apresentar ligações (pontes) de hidrogênio, é o menos solúvel em água, tornando
INTEGRAÇÃO E REGULAÇÃO HORMONAL DO METABOLISMO
 INTEGRAÇÃO E REGULAÇÃO HORMONAL DO METABOLISMO INTEGRAÇÃO E REGULAÇÃO HORMONAL DO METABOLISMO 1) MECANISMOS DE REGULAÇÃO METABÓLICA 2) ESPECIALIZAÇÃO DOS ÓRGÃOS Cérebro, Músculos, Tecido Adiposo e Fígado
INTEGRAÇÃO E REGULAÇÃO HORMONAL DO METABOLISMO INTEGRAÇÃO E REGULAÇÃO HORMONAL DO METABOLISMO 1) MECANISMOS DE REGULAÇÃO METABÓLICA 2) ESPECIALIZAÇÃO DOS ÓRGÃOS Cérebro, Músculos, Tecido Adiposo e Fígado
Síntese de Ácidos Graxos. Síntese de Ácidos Graxos. Síntese de Ácidos Graxos. Síntese de Ácidos Graxos. Síntese de Ácidos Graxos 11/11/2012
 Síntese e degradação de ácidos graxos e triglicerídeos O organismo animal tem capacidade de sintetizar os triglicerídeos basicamente a partir de acetilcoa. Também deve sintetizar fosfolipídeos e esfingolipídeos,
Síntese e degradação de ácidos graxos e triglicerídeos O organismo animal tem capacidade de sintetizar os triglicerídeos basicamente a partir de acetilcoa. Também deve sintetizar fosfolipídeos e esfingolipídeos,
Enzimas e Energia. Bases do metabolismo. Enzimas
 Enzimas e Energia Bases do metabolismo Enzimas 1 Enzimas - Proteínas. - Permitem que as reacções químicas ocorram à temperatura corporal - catalizadoras Enzimas catalizadoras: - Não se modificam na reacção
Enzimas e Energia Bases do metabolismo Enzimas 1 Enzimas - Proteínas. - Permitem que as reacções químicas ocorram à temperatura corporal - catalizadoras Enzimas catalizadoras: - Não se modificam na reacção
Reação de neutralização:
 01 Reação de neutralização: Ácido entanodioico Hidróxido de sódio Etanoato de sódio Água (oxálico) 1 02 Deslocamento do hidrogênio: Propanoato de sódio (A) Neutralização: Propanoato de sódio (B) Liberação
01 Reação de neutralização: Ácido entanodioico Hidróxido de sódio Etanoato de sódio Água (oxálico) 1 02 Deslocamento do hidrogênio: Propanoato de sódio (A) Neutralização: Propanoato de sódio (B) Liberação
Geralmente é arredondado e único por célula, mas existem núcleos com outras formas e células com mais de um núcleo
 Núcleo Celular Geralmente é arredondado e único por célula, mas existem núcleos com outras formas e células com mais de um núcleo Núcleo Celular Algumas células não têm núcleo (são anucleadas), como as
Núcleo Celular Geralmente é arredondado e único por célula, mas existem núcleos com outras formas e células com mais de um núcleo Núcleo Celular Algumas células não têm núcleo (são anucleadas), como as
Estudo Sobre As Substâncias Químicas Em Alimentos: Relato De Atividade Interdisciplinar
 Estudo Sobre As Substâncias Químicas Em Alimentos: Relato De Atividade Interdisciplinar Márcia de Lourdes Bezerra dos Santos 1, Anderson Moreira Sá 1, Cleomar Porto Bezerra 2, Paulo Henrique Almeida da
Estudo Sobre As Substâncias Químicas Em Alimentos: Relato De Atividade Interdisciplinar Márcia de Lourdes Bezerra dos Santos 1, Anderson Moreira Sá 1, Cleomar Porto Bezerra 2, Paulo Henrique Almeida da
Ribossomos e síntese protéica
 Ribossomos e síntese protéica SÍNTESE PROTÉICA DNA Transcrição RNA Tradução T A U T A U C G C G C G C G C C G C T A U G C G G C G O código genético é DEGENERADO PROTEÍNA Phe Ala Trp MAQUINARIA GENÉTICA
Ribossomos e síntese protéica SÍNTESE PROTÉICA DNA Transcrição RNA Tradução T A U T A U C G C G C G C G C C G C T A U G C G G C G O código genético é DEGENERADO PROTEÍNA Phe Ala Trp MAQUINARIA GENÉTICA
Definição: Catalisadores biológicos; Longas cadeias de pequenas moléculas chamadas aminoácidos.
 Enzimas baraobiologia.com Definição: Catalisadores biológicos; Longas cadeias de pequenas moléculas chamadas aminoácidos. Função: Viabilizar a atividade das células, quebrando moléculas ou juntando-as
Enzimas baraobiologia.com Definição: Catalisadores biológicos; Longas cadeias de pequenas moléculas chamadas aminoácidos. Função: Viabilizar a atividade das células, quebrando moléculas ou juntando-as
CÉLULA VEGETAL E PAREDE CELULAR
 Universidade Federal do Pampa Campus de São Gabriel Centro de Ciências Rurais Curso de Ciências Biológicas CÉLULA VEGETAL E PAREDE CELULAR Monitora: Rosangela Gonçalves Célula Vegetal As células vegetais
Universidade Federal do Pampa Campus de São Gabriel Centro de Ciências Rurais Curso de Ciências Biológicas CÉLULA VEGETAL E PAREDE CELULAR Monitora: Rosangela Gonçalves Célula Vegetal As células vegetais
Francisco Hevilásio F. Pereira Fisiologia Vegetal
 FISIOLOGIA VEGETAL Nutrição Mineral de plantas Parte II Pombal PB Transporte de íons na planta Transporte passivo e ativo Transporte passivo É aquele que ocorre a favor do gradiente de potencial químico
FISIOLOGIA VEGETAL Nutrição Mineral de plantas Parte II Pombal PB Transporte de íons na planta Transporte passivo e ativo Transporte passivo É aquele que ocorre a favor do gradiente de potencial químico
Características gerais
 Citoplasma Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Neurônio
Citoplasma Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Citoplasma Características gerais Um vertebrado é formado por dezenas de tipos de células. Neurônio
Constituintes básicos de uma célula
 Constituintes básicos de uma célula Biomoléculas As moléculas da vida São as moléculas constituintes dos seres vivos. São formadas principalmente por C e H, ainda que também possam estar presentes na sua
Constituintes básicos de uma célula Biomoléculas As moléculas da vida São as moléculas constituintes dos seres vivos. São formadas principalmente por C e H, ainda que também possam estar presentes na sua
Revisão de Química Orgânica
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Revisão de Química Orgânica Prof. Dra. Narlize Silva Lira Cavalcante A Química Orgânica e a Vida A uímica
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Revisão de Química Orgânica Prof. Dra. Narlize Silva Lira Cavalcante A Química Orgânica e a Vida A uímica
METABOLISMO DE AMI OÁCIDOS
 METABOLISMO DE AMI OÁCIDOS As proteínas constituintes dos organismos estão continuamente sendo renovadas (turnover das proteínas). * Os aminoácidos presentes nas células animais originam-se das proteínas
METABOLISMO DE AMI OÁCIDOS As proteínas constituintes dos organismos estão continuamente sendo renovadas (turnover das proteínas). * Os aminoácidos presentes nas células animais originam-se das proteínas
Início: 14/03 Término: 11/04. Horário de aulas: 2ª e 4º de 08:00 às 12:00 horas
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO INSTITUTO DE BIOQÍMICA MÉDICA DISCIPLINA: BIOQUÍMICA A ENFERMAGEM BMQ 121 BLOCO I: Estrutura de Proteínas e Biologia Molecular Início: 14/03 Término: 11/04 Horário
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO INSTITUTO DE BIOQÍMICA MÉDICA DISCIPLINA: BIOQUÍMICA A ENFERMAGEM BMQ 121 BLOCO I: Estrutura de Proteínas e Biologia Molecular Início: 14/03 Término: 11/04 Horário
Prof. ÉDER LIPÍDIOS. vol. 04 e 06 frente A módulo 03
 Prof. ÉDER LIPÍDIOS vol. 04 e 06 frente A módulo 03 O que são lipídios? Formados basicamente de ácidos graxos e álcool. Ao contrário das outras classes de compostos orgânicos, não são caracterizadas por
Prof. ÉDER LIPÍDIOS vol. 04 e 06 frente A módulo 03 O que são lipídios? Formados basicamente de ácidos graxos e álcool. Ao contrário das outras classes de compostos orgânicos, não são caracterizadas por
A matéria constituinte dos seres vivos. Biologia Humana
 A matéria constituinte dos seres vivos Biologia Humana Quais os compostos químicos que constituem os seres vivos? Compostos inorgânicos água e sais minerais Compostos orgânicos glícidos, lípidos, prótidos,
A matéria constituinte dos seres vivos Biologia Humana Quais os compostos químicos que constituem os seres vivos? Compostos inorgânicos água e sais minerais Compostos orgânicos glícidos, lípidos, prótidos,
Prof. Giovani - Biologia
 Prof. Giovani - Biologia 1.(UFRS) Tanto em uma célula eucarionte quanto em uma procarionte podemos encontrar: a) membrana plasmática e retículo endoplasmático. b) ribossomos e aparelho de Golgi. c) mitocôndrias
Prof. Giovani - Biologia 1.(UFRS) Tanto em uma célula eucarionte quanto em uma procarionte podemos encontrar: a) membrana plasmática e retículo endoplasmático. b) ribossomos e aparelho de Golgi. c) mitocôndrias
LIPÍDIOS. São ácidos carboxílicos com cadeia grande e sem ramificações (acima de 10C). São solúveis em óleo
 Prof. Borges LIPÍDIOS É importante lembrarmos de alguns conceitos básicos antes de iniciarmos a aula de bioquímica. Todo hidrocarboneto é apolar e, portanto insolúvel em água e solúvel em óleo. Ácidos
Prof. Borges LIPÍDIOS É importante lembrarmos de alguns conceitos básicos antes de iniciarmos a aula de bioquímica. Todo hidrocarboneto é apolar e, portanto insolúvel em água e solúvel em óleo. Ácidos
Lipídios, Proteínas e Vitaminas
 Lipídios, Proteínas e Vitaminas Aula ao Vivo Lipídios Substâncias orgânicas insolúveis em água e solúveis em certos solventes orgânicos apolares, álcool, benzina e éter. Proteínas Componentes fundamentais
Lipídios, Proteínas e Vitaminas Aula ao Vivo Lipídios Substâncias orgânicas insolúveis em água e solúveis em certos solventes orgânicos apolares, álcool, benzina e éter. Proteínas Componentes fundamentais
Metabolismo do Exercício -1ª parte
 Metabolismo do Exercício -1ª parte INTRODUÇÃO Nenhum outro estresse a que o corpo é normalmente exposto, sequer se aproxima dos estresses extremos decorrente do exercício vigoroso. INTRODUÇÃO De fato,
Metabolismo do Exercício -1ª parte INTRODUÇÃO Nenhum outro estresse a que o corpo é normalmente exposto, sequer se aproxima dos estresses extremos decorrente do exercício vigoroso. INTRODUÇÃO De fato,
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Universidade Federal dos Vales do Jequitinhonha e Mucuri - UFVJM. Fisiologia Gastrintestinal - Digestão e Absorção -
 Universidade Federal dos Vales do Jequitinhonha e Mucuri - UFVJM Fisiologia Gastrintestinal - Digestão e Absorção - Prof. Dr. Wagner de Fátima Pereira Departamento de Ciências Básicas Faculdade de Ciências
Universidade Federal dos Vales do Jequitinhonha e Mucuri - UFVJM Fisiologia Gastrintestinal - Digestão e Absorção - Prof. Dr. Wagner de Fátima Pereira Departamento de Ciências Básicas Faculdade de Ciências
FRENTE III QUÍMICA ORGÂNICA BIOQUÍMICA: AMINOACIDOS, PEPTIDEOS E PROTEINAS
 INTRODUÇÃO Os organismos vivos são constituídos por moléculas, átomos e íons, que por si só, não possuem vida. Mas o que distingue organismos vivos objetos? - Capacida se reproduzir; - Capacida extrair,
INTRODUÇÃO Os organismos vivos são constituídos por moléculas, átomos e íons, que por si só, não possuem vida. Mas o que distingue organismos vivos objetos? - Capacida se reproduzir; - Capacida extrair,
24/02/2014. É o limite externo da célula. Vera Andrade http://histologiavvargas.wordpress.com/
 Vera Andrade http://histologiavvargas.wordpress.com/ Membrana plasmática Mitocôndrias Retículo Endoplasmático Aparelho de Golgi Lisossomos e peroxissomos Centríolos Ribossomos Inclusões Citoplasmáticas
Vera Andrade http://histologiavvargas.wordpress.com/ Membrana plasmática Mitocôndrias Retículo Endoplasmático Aparelho de Golgi Lisossomos e peroxissomos Centríolos Ribossomos Inclusões Citoplasmáticas
QUÍMICA ORGÂNICA É A QUÍMICA DO CARBONO E SEUS COMPOSTOS. MOLÉCULAS ORGÂNICAS
 É A QUÍMICA DO CARBONO E SEUS COMPOSTOS. MOLÉCULAS ORGÂNICAS Um dos objetivos da Química Orgânica é relacionar a estrutura de uma molécula e suas reações, para poder estudar as etapas que ocorrem em cada
É A QUÍMICA DO CARBONO E SEUS COMPOSTOS. MOLÉCULAS ORGÂNICAS Um dos objetivos da Química Orgânica é relacionar a estrutura de uma molécula e suas reações, para poder estudar as etapas que ocorrem em cada
Sistema Circulatório: O Sangue
 Sistema Circulatório: O Sangue A composição do sangue Embora o sangue tenha uma aparência homogênea, se observado ao microscópio, logo se notará sua composição heterogênea. Isto significa que o sangue
Sistema Circulatório: O Sangue A composição do sangue Embora o sangue tenha uma aparência homogênea, se observado ao microscópio, logo se notará sua composição heterogênea. Isto significa que o sangue
Sangue Professor: Fernando Stuchi
 Zoologia e Histologia Animal Sangue Professor: Fernando Stuchi Sangue Em animais invertebrados o líquido circulante no interior do sistema cardiovascular é a hemolinfa. Nos vertebrados esse liquido é o
Zoologia e Histologia Animal Sangue Professor: Fernando Stuchi Sangue Em animais invertebrados o líquido circulante no interior do sistema cardiovascular é a hemolinfa. Nos vertebrados esse liquido é o
Origem da vida. Professor Fláudio
 Origem da vida Professor Fláudio Origem da vida Objetivos desta aula Entender as teorias que explicam a origem dos primeiros seres vivos. Diferentes tipos de células e seus componentes químicos. Níveis
Origem da vida Professor Fláudio Origem da vida Objetivos desta aula Entender as teorias que explicam a origem dos primeiros seres vivos. Diferentes tipos de células e seus componentes químicos. Níveis
Biologia Professor Leandro Gurgel de Medeiros
 Biologia Professor Leandro Gurgel de Medeiros Aula 02: Biologia Celular (Membrana Plásmática) Biologia celular é o ramo da biologia que estuda as células no que diz respeito à sua estrutura, suas funções
Biologia Professor Leandro Gurgel de Medeiros Aula 02: Biologia Celular (Membrana Plásmática) Biologia celular é o ramo da biologia que estuda as células no que diz respeito à sua estrutura, suas funções
A CÉLULA. Natércia Charruadas 2011. Biologia e Geologia 10º ano
 A CÉLULA Natércia Charruadas 2011 Biologia e Geologia 10º ano O entendimento dos processos biológicos depende do conhecimento da célula enquanto unidade fundamental da Vida. As dimensões das células, geralmente
A CÉLULA Natércia Charruadas 2011 Biologia e Geologia 10º ano O entendimento dos processos biológicos depende do conhecimento da célula enquanto unidade fundamental da Vida. As dimensões das células, geralmente
Metabolismo Energético das Células. Processos Exergônicos: Respiração Celular Fermentação
 Metabolismo Energético das Células Processos Exergônicos: Respiração Celular Fermentação Introdução Processos endergônicos - Característica: Precisam receber energia. - Ex.: Fotossíntese e quimiossíntese.
Metabolismo Energético das Células Processos Exergônicos: Respiração Celular Fermentação Introdução Processos endergônicos - Característica: Precisam receber energia. - Ex.: Fotossíntese e quimiossíntese.
Conteúdo. Unidade 01 composição química dos alimentos
 LIPÍDEOS AULA 01 Conteúdo Unidade 01 composição química dos alimentos - Carboidratos; - Proteínas; - Lipídeos; - Enzimas; - Vitaminas e minerais; - Substâncias bioativas; - Pigmentos Lipídeos Por que estudar?
LIPÍDEOS AULA 01 Conteúdo Unidade 01 composição química dos alimentos - Carboidratos; - Proteínas; - Lipídeos; - Enzimas; - Vitaminas e minerais; - Substâncias bioativas; - Pigmentos Lipídeos Por que estudar?
3 Membranas Biológicas
 3 Membranas Biológicas 3.1 Os limites das células Figura. 3.1 Estrutura de uma célula animal. (modificada de Biologia Molecular da Célula, 4ª edição, Alberts, B., Bray, D., Lewis,J., Artmed editora, 2004.)
3 Membranas Biológicas 3.1 Os limites das células Figura. 3.1 Estrutura de uma célula animal. (modificada de Biologia Molecular da Célula, 4ª edição, Alberts, B., Bray, D., Lewis,J., Artmed editora, 2004.)
Biologia Molecular e Celular II: Transporte através da membrana
 Biologia Molecular e Celular II: Transporte através da membrana Princípios do transporte Há diferenças entre a composição dentro e fora da célula; A distribuição de íons dentro e fora da célula é controlada
Biologia Molecular e Celular II: Transporte através da membrana Princípios do transporte Há diferenças entre a composição dentro e fora da célula; A distribuição de íons dentro e fora da célula é controlada
18/9/2010. Prof. Mst. Sandro de Souza consultoriass@gmail.com sandrodesouza.wordpress.com
 Distribuição das Áreas de conhecimento sobre Fisiologia do Exercício BIOENERGÉTICA SISTEMA CARDIORRESPIRATÓRIO TREINAMENT DESPORTIVO SISTEMA MUSCULAR SISTEMA NERVOSO Fisiologia do Exercício Prof. Mst.
Distribuição das Áreas de conhecimento sobre Fisiologia do Exercício BIOENERGÉTICA SISTEMA CARDIORRESPIRATÓRIO TREINAMENT DESPORTIVO SISTEMA MUSCULAR SISTEMA NERVOSO Fisiologia do Exercício Prof. Mst.
Ciências E Programa de Saúde
 Governo do Estado de São Paulo Secretaria de Estado da Educação Ciências E Programa de Saúde 10 CEEJA MAX DADÁ GALLIZZI PRAIA GRANDE - SP 0 A Educação sozinha não faz grandes mudanças, mas nenhuma grande
Governo do Estado de São Paulo Secretaria de Estado da Educação Ciências E Programa de Saúde 10 CEEJA MAX DADÁ GALLIZZI PRAIA GRANDE - SP 0 A Educação sozinha não faz grandes mudanças, mas nenhuma grande
Membrana celular: Transporte
 Membrana celular: Transporte Processos de Transporte Transporte em grande quantidade Transporte de íons e moléculas 1 Processos de Transporte: Transporte de íons e moléculas Qual a importância da manutenção
Membrana celular: Transporte Processos de Transporte Transporte em grande quantidade Transporte de íons e moléculas 1 Processos de Transporte: Transporte de íons e moléculas Qual a importância da manutenção
1) (Fuvest-SP) 2) (Mackenzie-SP) 3) (UDESC-SC) 4) (ENEM) 5) (UNIOESTE-PR)
 1) (Fuvest-SP) As mitocôndrias são consideradas as casas de força das células vivas. Tal analogia refere-se ao fato de as mitocôndrias: a) estocarem moléculas de ATP produzidas na digestão de alimentos.
1) (Fuvest-SP) As mitocôndrias são consideradas as casas de força das células vivas. Tal analogia refere-se ao fato de as mitocôndrias: a) estocarem moléculas de ATP produzidas na digestão de alimentos.
ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO
 ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO Água A molécula de água é triatômica e possui estrutura tetraédrica. Tem baixo peso molecular, pequeno volume e é diamagnética. Apresentaria um ângulo de
ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO Água A molécula de água é triatômica e possui estrutura tetraédrica. Tem baixo peso molecular, pequeno volume e é diamagnética. Apresentaria um ângulo de
1. O que é citoplasma e quais são suas subdivisões? 3. O que é citoesqueleto, do que ele é composto e qual sua função?
 Estudo Dirigido: Citoplasma, Citoesqueleto, Citosol, Retículo Endoplasmático, Aparelho de Golgi, Lisossomos e Peroxissomos Disciplina: Biologia Celular e Molecular Docente: Profa. Dra. Marilanda Ferreira
Estudo Dirigido: Citoplasma, Citoesqueleto, Citosol, Retículo Endoplasmático, Aparelho de Golgi, Lisossomos e Peroxissomos Disciplina: Biologia Celular e Molecular Docente: Profa. Dra. Marilanda Ferreira
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2
 I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
A síntese de DNA tem como objetivo replicar, de modo exato, o genoma. Já a síntese de RNA está relacionada com a própria expressão gênica.
 A síntese de DNA tem como objetivo replicar, de modo exato, o genoma. Já a síntese de RNA está relacionada com a própria expressão gênica. O processo de síntese de RNA, a partir de um molde de DNA, é denominado
A síntese de DNA tem como objetivo replicar, de modo exato, o genoma. Já a síntese de RNA está relacionada com a própria expressão gênica. O processo de síntese de RNA, a partir de um molde de DNA, é denominado
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2009_2010_1º Teste 16/11/2009
 BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2009_2010_1º Teste 16/11/2009 (Duração: 1,5 h) Nome do Aluno: Nº: Curso: Cada uma das questões de escolha múltipla (1 à 32) tem a cotação de 0,6 valores. Será descontado
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2009_2010_1º Teste 16/11/2009 (Duração: 1,5 h) Nome do Aluno: Nº: Curso: Cada uma das questões de escolha múltipla (1 à 32) tem a cotação de 0,6 valores. Será descontado
Biologia e Bioquímica II 2009/2010
 Biologia e Bioquímica II 009/010 Módulo II - Mitocôndria Sessão 6 Ficha de trabalho 1. Qual a importância energética da glicólise se no balanço final só há produção de ATP e, por cada molécula de glicose
Biologia e Bioquímica II 009/010 Módulo II - Mitocôndria Sessão 6 Ficha de trabalho 1. Qual a importância energética da glicólise se no balanço final só há produção de ATP e, por cada molécula de glicose
01. O inseticida DDT tem fórmula estrutural como mostrada na figura a seguir. Sabendo-se que sua solubilidade em água é 1,0x10 6 g/l, responda:
 Isomeria 2 - Isomeria Espacial 01. O inseticida DDT tem fórmula estrutural como mostrada na figura a seguir. Sabendo-se que sua solubilidade em água é 1,0x10 6 g/l, responda: a) Existem DDT levógiro e
Isomeria 2 - Isomeria Espacial 01. O inseticida DDT tem fórmula estrutural como mostrada na figura a seguir. Sabendo-se que sua solubilidade em água é 1,0x10 6 g/l, responda: a) Existem DDT levógiro e
A ORIGEM DA VIDA. Hipótese autotrófica e heterotrófica
 A ORIGEM DA VIDA Hipótese autotrófica e heterotrófica HIPÓTESE AUTOTRÓFICA Necessidade de alimento Seres autotróficos: capazes de produzir o alimento necessário plantas clorofiladas e algumas bactérias
A ORIGEM DA VIDA Hipótese autotrófica e heterotrófica HIPÓTESE AUTOTRÓFICA Necessidade de alimento Seres autotróficos: capazes de produzir o alimento necessário plantas clorofiladas e algumas bactérias
Alimentação Saudável A Nutrição & Os Nutrientes. O que são Nutrientes? Quais as funções dos Nutrientes?
 Alimentação Saudável A Nutrição & Os Nutrientes O que são Nutrientes? Quais as funções dos Nutrientes? Os Nutrientes Os nutrientes são substâncias indispensáveis ao funcionamento do organismo, e que obtemos
Alimentação Saudável A Nutrição & Os Nutrientes O que são Nutrientes? Quais as funções dos Nutrientes? Os Nutrientes Os nutrientes são substâncias indispensáveis ao funcionamento do organismo, e que obtemos
Estrutura Celular. Célula Animal
 Estrutura Celular Membrana Plasmática Hialoplasma(Citoplasma )& Citoesqueleto Parede Celular (exclusivo célula Vegetal) Núcleo Organelas celulares Célula Animal Hialoplasma Composição: 70 a 80% de água
Estrutura Celular Membrana Plasmática Hialoplasma(Citoplasma )& Citoesqueleto Parede Celular (exclusivo célula Vegetal) Núcleo Organelas celulares Célula Animal Hialoplasma Composição: 70 a 80% de água
Exercícios de Equílíbrio Químico ENEM Resolução Comentada Professora Simone
 Exercícios de Equílíbrio Químico ENEM Resolução Comentada Professora Simone 1. O equilíbrio químico se caracteriza por ser uma dinâmica em nível microscópico. Para se ter uma informação quantitativa da
Exercícios de Equílíbrio Químico ENEM Resolução Comentada Professora Simone 1. O equilíbrio químico se caracteriza por ser uma dinâmica em nível microscópico. Para se ter uma informação quantitativa da
Lisossomos. Os lisossomos são organelas citoplasmáticas possuem cerca de 40 enzimas hidrolíticas.
 Lisossomos Os lisossomos são organelas citoplasmáticas possuem cerca de 40 enzimas hidrolíticas. Essas enzimas atuam em um em grande número de substratos. A principal função destas organelas é a digestão
Lisossomos Os lisossomos são organelas citoplasmáticas possuem cerca de 40 enzimas hidrolíticas. Essas enzimas atuam em um em grande número de substratos. A principal função destas organelas é a digestão
Estrutura dos músculos e tecidos anexos. Prof. Sandra R. S. T. de Carvalho Departamento de Zootecnia - UFSC
 Estrutura dos músculos e tecidos anexos Prof. Sandra R. S. T. de Carvalho Departamento de Zootecnia - UFSC CARNE tecido muscular tecido conjuntivo tecido epitelial tecido nervoso Tecido muscular células
Estrutura dos músculos e tecidos anexos Prof. Sandra R. S. T. de Carvalho Departamento de Zootecnia - UFSC CARNE tecido muscular tecido conjuntivo tecido epitelial tecido nervoso Tecido muscular células
Composição química. Profª Maristela. da célula
 Composição química Profª Maristela da célula Compostos inorgânicos Água Sais minerais Compostos orgânicos Carboidratos Lipídios Proteínas Ácidos nucleicos Vitaminas Água Solvente universal Atua no transporte
Composição química Profª Maristela da célula Compostos inorgânicos Água Sais minerais Compostos orgânicos Carboidratos Lipídios Proteínas Ácidos nucleicos Vitaminas Água Solvente universal Atua no transporte
Biomoléculas mais abundantes Terra
 Biomoléculas mais abundantes Terra A cada ano mais de 100 bilhões de tonelada de CO 2 e H 2 O são transformados em carboidratos pelo processo fotossintético CO 2 + H 2 O O 2 + (CH 2 O) n Luz Moléculas
Biomoléculas mais abundantes Terra A cada ano mais de 100 bilhões de tonelada de CO 2 e H 2 O são transformados em carboidratos pelo processo fotossintético CO 2 + H 2 O O 2 + (CH 2 O) n Luz Moléculas
O que você precisa saber sobre óleos e gorduras ÓLEOS E GORDURAS
 ÓLEOS E GORDURAS Óleos e gorduras comestíveis são fundamentais na alimentação humana, pois, fornecem calorias (9 Kcal/g), auxiliam no transporte de vitaminas lipossolúveis (A, D, E e K) para o interior
ÓLEOS E GORDURAS Óleos e gorduras comestíveis são fundamentais na alimentação humana, pois, fornecem calorias (9 Kcal/g), auxiliam no transporte de vitaminas lipossolúveis (A, D, E e K) para o interior
Aula 3 Organelas. Níveis de organização dos seres vivos: Observe, abaixo, a célula animal com as principais organelas. Citoplasma Membrana plasmática
 Aula 3 Organelas Organelas ou organóides são estruturas encontradas no citoplasma celular com função específica, que auxiliam no seu funcionamento, como iremos descrever. Níveis de organização dos seres
Aula 3 Organelas Organelas ou organóides são estruturas encontradas no citoplasma celular com função específica, que auxiliam no seu funcionamento, como iremos descrever. Níveis de organização dos seres
UNIDADE 3 METABOLISMO DE LIPÍDEOS. 3.1 Noções de digestão e absorção de lipídeos simples. 3.1 Noções de digestão e absorção de lipídeos simples.
 UNIDADE 3 METABOLISMO DE LIPÍDEOS 3.1 Noções de digestão e absorção de lipídeos UNIDADE 3 METABOLISMO simples. DE LIPÍDEOS 3.1 Noções de digestão e absorção de lipídeos simples. - C, H, O (N e P) - Insolúveis
UNIDADE 3 METABOLISMO DE LIPÍDEOS 3.1 Noções de digestão e absorção de lipídeos UNIDADE 3 METABOLISMO simples. DE LIPÍDEOS 3.1 Noções de digestão e absorção de lipídeos simples. - C, H, O (N e P) - Insolúveis
REAÇÕES QUÍMICAS ORGÂNICAS
 REAÇÕES QUÍMICAS ORGÂNICAS REAÇÕES QUÍMICAS ORGÂNICAS Como tudo começou? REAÇÕES QUÍMICAS ORGÂNICAS BERZELIUS "Somente os seres vivos podem transformar substâncias minerais em orgânicas." (Teoria da Força
REAÇÕES QUÍMICAS ORGÂNICAS REAÇÕES QUÍMICAS ORGÂNICAS Como tudo começou? REAÇÕES QUÍMICAS ORGÂNICAS BERZELIUS "Somente os seres vivos podem transformar substâncias minerais em orgânicas." (Teoria da Força
INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA
 INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA Principios de Termodinâmica Termodinamica determina se um processo fisicoquímico é possível (i.e. espontaneo) Termodinamica não providencia informação sobre
INTRODUÇÃO À CINETICA E TERMODINÂMICA QUÍMICA Principios de Termodinâmica Termodinamica determina se um processo fisicoquímico é possível (i.e. espontaneo) Termodinamica não providencia informação sobre
SERVIÇO PÚBLICO FEDERAL MINISTÉRIO DA EDUCAÇÃO E DO DESPORTO FACULDADE DE ENFERMAGEM PROGRAMA DE DISCIPLINA CARGA HORÁRIA TEÓRICA:
 SERVIÇO PÚBLICO FEDERAL MINISTÉRIO DA EDUCAÇÃO E DO DESPORTO FACULDADE DE ENFERMAGEM PROGRAMA DE DISCIPLINA DISCIPLINA: Bioquimica GRADE: RESOLUÇÃO CEPEC Nº 831 MATRIZ CURRICULAR: BACHARELADO E LICENCIATURA
SERVIÇO PÚBLICO FEDERAL MINISTÉRIO DA EDUCAÇÃO E DO DESPORTO FACULDADE DE ENFERMAGEM PROGRAMA DE DISCIPLINA DISCIPLINA: Bioquimica GRADE: RESOLUÇÃO CEPEC Nº 831 MATRIZ CURRICULAR: BACHARELADO E LICENCIATURA
Colágeno. O principal tecido conjuntivo que interfere na qualidade da carne é o COLÁGENO (30% das proteínas dos organismos)
 Colágeno Ana Maria Bridi ambridi@uel.br Professora dodepartamento de Zootecnia da UEL Tecido conjuntivo O principal tecido conjuntivo que interfere na qualidade da carne é o COLÁGENO (30% das proteínas
Colágeno Ana Maria Bridi ambridi@uel.br Professora dodepartamento de Zootecnia da UEL Tecido conjuntivo O principal tecido conjuntivo que interfere na qualidade da carne é o COLÁGENO (30% das proteínas
A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios.
 A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios. Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas. As proteínas respiratórias
A circulação de um fluido (sangue ou hemolinfa) acelera a distribuição dos gases respiratórios. Entretanto, os gases, especialmente oxigênio, são pouco solúveis em soluções aquosas. As proteínas respiratórias
Concurso de seleção 2004-2 Química Página 1 QUÍMICA
 Concurso de seleção 004- Química Página 1 QUÍMICA QUESTÃO 51 Uma das conseqüências da poluição ambiental é a chuva ácida, que, em alguns casos, pode causar danos irreparáveis à natureza. Substâncias básicas
Concurso de seleção 004- Química Página 1 QUÍMICA QUESTÃO 51 Uma das conseqüências da poluição ambiental é a chuva ácida, que, em alguns casos, pode causar danos irreparáveis à natureza. Substâncias básicas
Biomoléculas mais abundantes Terra
 Biomoléculas mais abundantes Terra A cada ano mais de 100 bilhões de tonelada de CO 2 e H 2 O são transformados em carboidratos pelo processo fotossintético CO 2 + H 2 O O 2 + (CH 2 O) n Luz Moléculas
Biomoléculas mais abundantes Terra A cada ano mais de 100 bilhões de tonelada de CO 2 e H 2 O são transformados em carboidratos pelo processo fotossintético CO 2 + H 2 O O 2 + (CH 2 O) n Luz Moléculas
UNIVERSIDADE FEDERAL DE PERNAMBUCO CENTRO DE CIÊNCIAS BIOLÓGICAS DEPARTAMENTO DE BIOQUÍMICA HORMÔNIOS E REGULAÇÃO METABÓLICA
 UNIVERSIDADE FEDERAL DE PERNAMBUCO CENTRO DE CIÊNCIAS BIOLÓGICAS DEPARTAMENTO DE BIOQUÍMICA HORMÔNIOS E REGULAÇÃO METABÓLICA Prof a. Dr a. Nereide Magalhães Recife, fevereiro de 2005 HORMÔNIOS Sinais hormonais
UNIVERSIDADE FEDERAL DE PERNAMBUCO CENTRO DE CIÊNCIAS BIOLÓGICAS DEPARTAMENTO DE BIOQUÍMICA HORMÔNIOS E REGULAÇÃO METABÓLICA Prof a. Dr a. Nereide Magalhães Recife, fevereiro de 2005 HORMÔNIOS Sinais hormonais
1
 Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
Níveis de dificuldade das Questões Fácil Pontifícia Universidade Católica do Rio Grande do Sul Médio Difícil Resolução da Prova de Química Vestibular Verão PUCRS 2005 Prof. Emiliano Chemello www.quimica.net/emiliano
Biomoléculas mais abundantes Terra
 Biomoléculas mais abundantes Terra A cada ano mais de 100 bilhões de tonelada de CO 2 e H 2 O são transformados em carboidratos pelo processo fotossintético CO 2 + H 2 O O 2 + (CH 2 O) n Luz Moléculas
Biomoléculas mais abundantes Terra A cada ano mais de 100 bilhões de tonelada de CO 2 e H 2 O são transformados em carboidratos pelo processo fotossintético CO 2 + H 2 O O 2 + (CH 2 O) n Luz Moléculas
Propriedades Físicas dos Compostos Orgânicos
 Propriedades Físicas dos Compostos Orgânicos Orientadora: Drª Lucília Alves Linhares Professor Monitor: Gabriel Silveira Forças Intermoleculares - Ponto de Fusão - Ponto de Ebulição - Polaridade - Solubilidade
Propriedades Físicas dos Compostos Orgânicos Orientadora: Drª Lucília Alves Linhares Professor Monitor: Gabriel Silveira Forças Intermoleculares - Ponto de Fusão - Ponto de Ebulição - Polaridade - Solubilidade
Do grego, hydton, tecido + logos, estudos. Cada grupo de células reunidas para executar uma função específica é chamado de tecido.
 Do grego, hydton, tecido + logos, estudos. Cada grupo de células reunidas para executar uma função específica é chamado de tecido. Além das células, os tecidos contêm material extracelular ou intercelular
Do grego, hydton, tecido + logos, estudos. Cada grupo de células reunidas para executar uma função específica é chamado de tecido. Além das células, os tecidos contêm material extracelular ou intercelular
A disposição da vida na Terra
 Aula 01 A disposição da vida na Terra O que é a vida? Existe vida em outros planetas? Podemos viver sem o Sol? O nosso sistema solar possui os seguintes planetas: Mercúrio, Vênus, Terra, Marte Júpiter,
Aula 01 A disposição da vida na Terra O que é a vida? Existe vida em outros planetas? Podemos viver sem o Sol? O nosso sistema solar possui os seguintes planetas: Mercúrio, Vênus, Terra, Marte Júpiter,
LISTA DE EXERCÍCIOS REAÇÕES ORGÂNICAS
 Nome: nº: Ensino: Curso Pré-Vestibular ano/série: Componente Curricular: Química Professor: Ricardo Honda Data: / / 2011 LISTA DE EXERCÍCIOS REAÇÕES ORGÂNICAS 1) (FUVEST 2010 1ª Fase) Em um experimento,
Nome: nº: Ensino: Curso Pré-Vestibular ano/série: Componente Curricular: Química Professor: Ricardo Honda Data: / / 2011 LISTA DE EXERCÍCIOS REAÇÕES ORGÂNICAS 1) (FUVEST 2010 1ª Fase) Em um experimento,
A massa de uma proteína é expressa em daltons
 Proteínas Globulares Apesar de proteínas fibrosas terem só um tipo de estrutura secundária, as proteínas globulares podem ter diversos tipos de estrutura secundária em uma mesma molécula. As proteínas
Proteínas Globulares Apesar de proteínas fibrosas terem só um tipo de estrutura secundária, as proteínas globulares podem ter diversos tipos de estrutura secundária em uma mesma molécula. As proteínas
Química Orgânica I. Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas.
 Química Orgânica I Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas Aula 4 (Parte I) Profa. Alceni Augusta Werle Profa Tânia Márcia Sacramento
Química Orgânica I Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas Aula 4 (Parte I) Profa. Alceni Augusta Werle Profa Tânia Márcia Sacramento
Aula 8 Síntese de proteínas
 Aula 8 Síntese de proteínas As proteínas que podem ser enzimas, hormônios, pigmentos, anticorpos, realizam atividades específicas no metabolismo dos seres vivos. São produzidas sob o comando do DNA. Observe
Aula 8 Síntese de proteínas As proteínas que podem ser enzimas, hormônios, pigmentos, anticorpos, realizam atividades específicas no metabolismo dos seres vivos. São produzidas sob o comando do DNA. Observe
Modificação Covalente
 Controle Celular Sistema de Controle Celular Governa a Maquinaria do Ciclo Celular Ativação e desativação cíclica Ativação e Inativação Proteínas chaves e dos complexos protéicos Iniciam ou regulam Replicação
Controle Celular Sistema de Controle Celular Governa a Maquinaria do Ciclo Celular Ativação e desativação cíclica Ativação e Inativação Proteínas chaves e dos complexos protéicos Iniciam ou regulam Replicação
