Fenômenos de Transporte III. Aula 06. Prof. Gerônimo
|
|
|
- Mafalda Van Der Vinne Salvado
- 5 Há anos
- Visualizações:
Transcrição
1 Fenômenos de Transporte III ula 6 Prof. Gerônimo
2 6..- Difusão pseudo-estacionária num filme gasoso estagnado Figura a seguir ilustra um capilar semipreenchido por líquido puro volátil. Supondo que sobre esse líquido exista um filme gasoso estagnado B, deseja-se avaliar o coeficiente de difusão do vapor de nessa película. pós um intervalo de tempo considerável, nota-se a variação do nível do líquido, a partir do topo do capilar desde Z (t = ) até Z (t = t ). equação que descreve o fluxo mássico de um soluto desde Z até Z em um filme de gás estagnado B em um tubo capilar de dimensões infinitas é: N,.D,B d d B Z ( t = ) Z ( t = t )
3 O fluxo de na direção oposta de é: d N D, Z B N,Z d onsiderando o fluxo de B estagnado, temos: N B, Z N B, Z N N,Z,Z D ( Z Z d B D d ) d B,t,S d N N,Z,Z D Ln D Ln Ln B B,t,t,S,S
4 .D,B,t N, Ln Z Z ( ),S Z = altura entre o topo da coluna e a superfície do líquido antes de iniciar o processo de difusão de em B ( t = ); Z = altura entre o topo da coluna e a superfície do líquido após iniciar o processo de difusão de em B ( t = qualquer );,t = fração molar de no topo do tubo;, S = fração molar de na superfície do líquido; = concentração molar global na coluna gasosa; D,B = coeficiente de difusão de em B. Em muitas operações de transferência de massa, uma das condições de contorno pode mover-se com o tempo. O modelo pseudo-estacionário pode ser usado quando a difusão varia em pequena quantidade sobre um longo período de tempo. ssim, o fluxo molar N,Z em regime pseudo-estacionário será dado por: N, d d.v.. ( ) dt dt 4
5 Substituindo a equação ( ) na equação ( ) para regime pseudo-estacionário, temos: d. dt.d Z,B Z Ln,t, S ( ) = concentração mássica de ; = massa molecular de. Determine o tempo final de difusão de em B (ou num instante qualquer) e o coeficiente de difusão D,B para um determinado instante qualquer. d. dt.d Z,B Ln,t,S t dt ρ..d,b Ln,t,S Z Z.d 5
6 Ln..D ρ t Ln..D ρ t,s,t,b,s,t,b Ln..D ρ t,s,t,b Onde: t é tempo final de difusão da espécie em B desde Z a Z, ou: Ln..t ρ D,S,t B, Onde: D,B é o coeficiente de difusão da espécie em B no tempo t, desde Z a Z. ( 4 ) ( 5 ) 6
7 Exemplo : célula de rnold é um dispositivo que, de forma simples, permite a medição de coeficientes de difusão mássica. Na figura a seguir, é mostrado um esboço da célula. r (B) N, Z, nível em t = Líquido Z, nível em t = t 7
8 No experimento, em um intervalo de tempo t = t, mede-se a quantidade de líquido evaporado através da variação do nível Z = Z Z. difusividade de em B é então determinada por: D B..Ln em que é a massa específica do líquido ; a sua massa molar; é a concentração molar global na coluna gasosa;,t e,s são as frações molares de no topo da célula e sobre a superfície do líquido, respectivamente.,t,s.t Z. Z O modelo que permite essa relação tem como hipóteses: sistema binário ( + B ); o gás B insolúvel em ; fluxo difusivo de ao longo da célula dado pela seguinte equação: regime pseudo-estacionário; sistema a T e P constantes; difusividade D,B constante. d N,.D,B N, d N B, 8
9 a) Determine a difusividade mássica de clorofórmio () no ar (B), sabendo que, em um experimento com uma célula de rnold, em horas (6. s), a distância entre a superfície do clorofórmio e do topo da célula passou de Z = 7,4 cm ( t = ) para Z = 7,84 cm ( t = t ). onsidere que no topo da célula escoava ar puro, ou seja,,t =, e que na superfície do clorofórmio as condições eram de saturação. temperatura e a pressão mantiveram-se constantes e iguais a 98 K e, kpa, respectivamente. pressão de vapor do clorofórmio nessa temperatura é igual a 6,6 kpa. presente o resultado da difusividade em m /s utiliando o mesmo número de algarismos significativos empregados para representar a distância Z. b) Qual é a característica do processo que permite a adoção de regime pseudo-estacionário na sua modelagem? Dados: 48 Kg/m, 9 Kg/Kmol,,49 Kmol/m VP P,S 6,6 kpa a), S,6 P, kpa Z Z D..,B,t.Ln.t,s 48 Kg/m D,B.. 9 Kg/Kmol,49 Kmol/m.Ln.6 s,6 D,B 9,8. 6 m /s,784m,74m b) É o fato de a taxa de evaporação ser muito pequena. 9
10 Exemplo 4: Um capilar de cm de altura contém cm de etanol. alcule o tempo necessário para que o nível do álcool decresça em, cm, considerando que o capilar esteja preenchido por ar seco e estagnado a atm e 5. Suponha que o vapor de etanol seja totalmente arrastado no topo do capilar. Nessas condições, são conhecidos: ρ,787 g/cm ; P vap Etanol; B r seco 6,75 mmhg ; r seco,t = 46,69 g/mol N, cm cm Etanol Z = 8cm, nível em t =,,S = P VP /P Z = 8,cm, nível em t = t,,s = P VP /P
11 Solução: t ρ..d,b Ln, t,s vap, S P P 6,75 mmhg 76 mmhg,5 P [gmol/cm ] T atm 8,5atm.cm / gmol.k 98,5K 4,88x 6 gmol/cm D B, cm /s (Tabela... remasco)
12 746,8 s ou horas t 8, 8,,5 Ln /s., cm gmol/cm 46,69g/gmol.4,88x,787g/cm t Ln..D ρ t -6,S, t,b
13 6..4- Difusão pseudo-estacionário num filme gasoso estagnado. evalidação do experimento da esfera isolada. diferença básica entre os estados estacionários (regime permanente) e o pseudoestacionário é que o último considera a variação espacial no tempo de uma das fronteiras da região onde ocorre a difusão. taxa de evaporação do líquido (ou da sublimação de um sólido) de um certo corpode-prova, em coordenadas esféricas é dado pela seguinte equação: ρ dv W, r dt ( 6 ) na qual é a massa específica de, e V é o volume do corpo-de-prova considerado: V 4 dv 4 d ( 7 )
14 Substituindo (6) em (7) torna-se: ρ d 4, r ( 8 ) dt W omo há decréscimo de, a equação ( 8 ) é posta como: ρ d 4, r ( 9 ) dt W equação (9) fornece, por exemplo, a taxa molar de evaporação de uma gota líquida ou da sublimação de um sólido como consequência da variação do raio do corpo-de-prova de uma esfera. Entretanto, a taxa molar decorrente da distribuição da concentração do soluto no meio difusivo é dado pela equação (8) (ula 5): W, r 4..DBLn ( 8 ) 4
15 Igualando-se a equação (8) com a equação (9) e integrando, obtém-se: ) (t (t) ρ.t Ln.D ρ t Ln.D d dt Ln.D dt d ρ Ln.D dt d 4 Ln..D 4 B (t) ) (t t B (t) ) (t t B B B 5
16 Portanto, o coeficiente de difusão D B é dado por: D B.t ρ Ln t t ( ) Quando a contribuição convectiva puder ser considerada despreível em face à difusiva e não se encontrar traços do soluto antes de começar o fenômeno difusivo no meio considerado, iguala-se a equação () (ula 5) com a equação (9) e integra-se: W 4..D ( ), r B ρ d, r 4 ( 9 ) dt W 6
17 ) (t (t) ρ.t.d ρ t.d d dt.d dt d ρ.d dt d ρ 4..D 4 B (t) ) (t t B (t) ) (t s t B B B ρ.t D t t B ( ) 7
18 Exemplo : efaça o exemplo, considerando o fenômeno pseudoestacionário. onsidere o término do experimento em t = min. Solução: o observar os dados do exemplo anterior, verifica-se: t = ; (t ) =,85cm e para t = min; (t) =,8cm =,457x -7 gmol/cm omo no exemplo, o meio convectivo foi despreível, pelo fato de e =. ssim o coeficiente de difusão é calculado pela seguinte equação: D B.t ρ t t D B (,47x 7 gmol/cm,4g/cm (,85cm) )(x6s) 8,6g/gmol (,8cm) D B,765cm /s 8
19 Há de se perceber que esse resultado é para T = 45,5K (7) e o parâmetro de comparação é T = 5 (98,5K). dmitindo a predição do D B para essa nova temperatura, temos: D D D B T98,5K B T98,5K B T98,5K D B T45,5K,765cm,59 cm /s T T /s,75 98,5K 45,5K omo o valor experimental é igual a D B =,6cm /s, determina-se o desvio relativo por:,75 D. D. cal. exp. exp.,9% x%,59,6 x%,6 Verifica-se que ao adotar o modelo do regime pseudo-estacionário houve uma diminuição do valor do desvio relativo. Neste caso foi considerado a variação do raio do naftaleno, o qual torna o modelo mais preciso para o cálculo do D B. 9
20 6..5- ontradifusão equimolar Este fenômeno ocorre, por exemplo, na simultaneidade da condensação e evaporação de espécies químicas distintas, mas de características físicoquímicas semelhantes como o beneno e tolueno. Para cada mol de tolueno condensado, um mol de beneno evapora. Outra situação é aquela em que há dois reservatórios ( e ) interligados por um tubo. Nesses reservatórios estão contidas misturas binárias e B. No reservatório, >> B ; situação inversa para o reservatório, B. o provocarmos o contato entre os reservatórios, teremos para cada mol de que migra de para ; um mol de B irá de para. N, N B, Figura : ontradifusão equimolar (reservatórios interligados)
21 relação entre os fluxos molares das espécies e B é: a qual caracteria a contradifusão equimolar. Distribuição de concentração de : N, = - N B, ( ) omo o regime de transferência é permanente e o meio difusivo não é racional, a equação da continuidade de que rege a contradifusão equimolar, é dado por: t.n ''' dn,.n ( ) d
22 Pela equação, observe que devemos conhecer o fluxo molar de, o qual é obtido depois de substituir a igualdade da equação na equação do fluxo molar da espécie, ou seja: d N, Z DB N, Z N d NB,Z B, Z N, Z D B d d N d D ( ) B d, Z
23 Substituindo a equação na equação e considerando o sistema a temperatura e pressão constantes: d d ( 4 ) solução da equação 4 é uma distribuição linear da concentração de : () ( 5 ) s condições de contorno advêm da análise da Figura : : : em em ; ; ( 6 )
24 4 plicando as condições de contorno (6) na equação (5), obtém-se o seguinte sistema de equações: esolvendo o sistema (7), chega-se nas seguintes constantes: ( 7 ) ( 8 ) ( 9 )
25 Substituindo as soluções das constantes e na equação 5, obtém-se a distribuição da concentração do soluto : ( ) Fluxo de matéria de : O fluxo global de é obtido da equação em conjunto coma as condições de contorno 6. Visto que o fluxo é constante, temos: Z N, Z d D B d Z 5
26 D B N, Z ( ) o admitirmos que o fenômeno da transferência de massa ocorra em um meio gasoso ideal, podemos faer = P /T. Desse modo, o fluxo global de é dado, em termos de pressão parcial de : D B N, Z P P T( ) ( ) partir da equação, para a espécie B, temos: N, Z NB, Z D B NB, Z P P T( ) ( ) 6
27 Estas equações, e implicam que a concentração molar (ou fração molar) e a pressão parcial de qualquer gás variam linearmente durante a contradifusão equimolar. É interessante notar que a mistura é estacionária numa base molar, mas não é estacionária em uma base mássica, a menos que as massas molares de e B sejam iguais. Embora a vaão líquida molar através do canal seja ero, a vaão mássica líquida da mistura através do canal não é ero e pode ser determinada através de: m m m B W W B B ( 4 ) Pela equação temos: N, Z N B, Z Se multiplicarmos pela área da seção transversal do tubo por onde escoam os gases, fica: N Z W N, B,Z, WB, ( 5 ) 7
28 plicando a relação 5 na equação 4, fica: m m m B W ( B ) ( 6 ) Note que a direção da vaão mássica líquida é a direção do escoamento do gás com a maior massa molar. Um dispositivo de medida de velocidade, como um anemômetro, colocado no canal indicaria uma velocidade de v = ṁ/, onde é a densidade (ou concentração mássica) total da mistura no local da medida. Exemplo : pressão em uma tubulação que transporta gás hélio a uma taxa de kg/s é mantida a atm pela ventilação de hélio para a atmosfera através de um tubo de 5 mm de diâmetro interno, que se estende 5 m no ar, como mostrado na Figura. Supondo que ambos, o hélio e o ar atmosférico, estão a 5, determinar: (a) a vaão mássica de hélio perdido para a atmosfera através do tubo, (b) a vaão e a fração mássica de ar que se infiltra na tubulação, (c) a velocidade do escoamento no fundo do tubo onde este está ligado à tubulação que vai ser medida por um anemômetro em regime permanente 8
29 r (B) P = atm T = 5 He x = 5 m 5 mm Hélio () P = atm T = 5 He r ṁ = kg/s x = Suposições: - Existem condições de funcionamento permanentes. - O hélio e o ar atmosférico são gases ideais. - Não ocorrem reações químicas no tubo. 4- concentração de ar na tubulação e a concentração de hélio na atmosfera são insignificantes, de forma que a fração molar do hélio é na tubulação e na atmosfera (vamos verificar essa hipótese depois). 9
30 Dados: O coeficiente de difusão do hélio no ar (ou ar no hélio) em condições atmosféricas normais é D B = 7,x -5 m /s. s massas molares do ar e do hélio são 9 e 4 kg/kmol, respectivamente. constante universal dos gases = 8,4 kpa.m /kmol.k Solução: Este é um processo típico de contradifusão equimolar, uma ve que o problema envolve dois grandes reservatórios de misturas de gases ideais ligados entre si por um canal e as concentrações das espécies em cada reservatório (a tubulação e a atmosfera) permanecem constantes. a) vaão mássica de hélio perdido para a atmosfera através do tubo. área do escoamento, que é a área da seção do tubo, é: πd 4 π(,5m) 4,96x 5 m
31 Notando que a pressão parcial do hélio é de atm ( = ) no fundo do tubo (x = ) e ero ( = ) no topo (x = 5m), a sua vaão (ou taxa) molar é determinada a partir da equação como: W W W,, N,,,96x 8,4kPa.m,85x DB T( kmol/s ) P 5 5 m 7,x m /s /kmol.k 98K (5m) P atm,kpa atm Portanto, a vaão mássica do hélio, ṁ, é dado por: m m m W,85x kmol/s4kg/kmol,54x kg/s
32 (b) a vaão e a fração mássica de ar que se infiltra na tubulação. Observando que W = -W B, durante um processo contradifusão equimolar, a vaão molar de ar para dentro da tubulação é igual a vaão molar do hélio dentro da tubulação. Portanto, a vaão mássica de ar para dentro da tubulação é: m m m B B B W fração mássica de ar na tubulação é: B B,85x kmol/s 9kg/kmol,x kg/s w w B B m m B total 5,6x,x,x kg/s,54x kg/s o que valida a suposição inicial de ar despreível na tubulação.
33 c) vaão mássica líquida através do tubo capilar. m m líquida líquida m m B 9,66x,54x kg/s,x kg/s fração de massa do ar no fundo do tubo é muito pequena, como demonstrado anteriormente e, assim, a densidade da mistura em x = pode simplesmente ser considerada a densidade do hélio, que é de: He He P T,67,kPa 4kg/kmol 8,4kPa.m /kmol.k 98K kg/m Então, a velocidade média do escoamento na parte do fundo do tubo se torna: v v mliq ρ,x 9,66x,67 kg/m 4kg/kmol 5 m/s kg/s
Fenômenos de Transporte III. Prof. Dr. Gilberto Garcia Cortez
 Fenômenos de Transporte III Prof. Dr. Gilberto Garcia orte 6- DIFUSÃO EM REGIME PERMETE SEM REÇÃO QUÍMI 6.- onsiderações a respeito onsidere uma sala ampla contendo ar a, atm e 5. oloque no centro da sala
Fenômenos de Transporte III Prof. Dr. Gilberto Garcia orte 6- DIFUSÃO EM REGIME PERMETE SEM REÇÃO QUÍMI 6.- onsiderações a respeito onsidere uma sala ampla contendo ar a, atm e 5. oloque no centro da sala
Experimento 3. Determinação do coeficiente de difusão em fase gasosa em regime pseudoestacionário. Prof. Dr. Gilberto Garcia Cortez
 Experimento 3 eterminação do coeficiente de difusão em fase gasosa em regime pseudoestacionário. Prof. r. Gilberto Garcia Cortez Introdução Um método simples e bastante preciso para a determinação de difusividade
Experimento 3 eterminação do coeficiente de difusão em fase gasosa em regime pseudoestacionário. Prof. r. Gilberto Garcia Cortez Introdução Um método simples e bastante preciso para a determinação de difusividade
C + 2H 2 CH 4. 3 o LISTA DE EXERCÍCIOS DE TRANSFERÊNCIA DE MASSA. Prof. Dr. Gilberto Garcia Cortez
 3 o LIST DE EXEÍIOS DE TNSFEÊNI DE MSS 1- Em um reator catalítico, partículas de carbono em forma de cilindro são consumidas pela passagem de um fluxo de hidrogênio para formar metano através da seguinte
3 o LIST DE EXEÍIOS DE TNSFEÊNI DE MSS 1- Em um reator catalítico, partículas de carbono em forma de cilindro são consumidas pela passagem de um fluxo de hidrogênio para formar metano através da seguinte
Fenômenos de Transporte III. Aula 05. Prof. Gerônimo
 Fenômenos e Transporte III ula 5 Prof. Gerônimo 6- DIFUSÃO EM REGIME PERMETE SEM REÇÃO QUÍMIC 6.- Consierações a respeito Consiere uma sala ampla conteno ar a atm e 5C. Coloque no centro a sala uma mesa
Fenômenos e Transporte III ula 5 Prof. Gerônimo 6- DIFUSÃO EM REGIME PERMETE SEM REÇÃO QUÍMIC 6.- Consierações a respeito Consiere uma sala ampla conteno ar a atm e 5C. Coloque no centro a sala uma mesa
Capítulo 6 Processos Envolvendo Vapores
 Capítulo 6 Processos Envolvendo Vapores Pressão de vapor Define-se vapor como um componente no estado gasoso que se encontra a pressão e temperatura inferiores às do ponto crítico. Assim, um vapor pode
Capítulo 6 Processos Envolvendo Vapores Pressão de vapor Define-se vapor como um componente no estado gasoso que se encontra a pressão e temperatura inferiores às do ponto crítico. Assim, um vapor pode
3 Introdução à Transferência de Massa. 7a. Aula
 3 Introdução à Transferência de Massa 7a. Aula Transporte Molecular Transporte de Energia (condução) Transporte de Massa (difusão) Exemplo: vidro de perfume aberto numa sala com ar parado Transporte Molecular
3 Introdução à Transferência de Massa 7a. Aula Transporte Molecular Transporte de Energia (condução) Transporte de Massa (difusão) Exemplo: vidro de perfume aberto numa sala com ar parado Transporte Molecular
Tabela 5.1- Características e condições operacionais para a coluna de absorção. Altura, L Concentração de entrada de CO 2, C AG
 5 Resultados Neste capítulo, são apresentados sob forma de tabelas os dados operacionais e as propriedades físico-químicas utilizados no processo de absorção CO 2 -MEA. Em seguida são apresentados a comparação
5 Resultados Neste capítulo, são apresentados sob forma de tabelas os dados operacionais e as propriedades físico-químicas utilizados no processo de absorção CO 2 -MEA. Em seguida são apresentados a comparação
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos
 Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
TRANSPORTE DE MASSA. Alda Simões CEQ / MEF / 2015
 Livro de apoio: Christie Geankoplis, Transport Processes and Unit Operations, 3rd ed, 1993, Prentice Hall, cap 6 TRANSPORTE DE MASSA CEQ / MEF / 2015 Alda Simões Transporte molecular de massa Lei de Fick
Livro de apoio: Christie Geankoplis, Transport Processes and Unit Operations, 3rd ed, 1993, Prentice Hall, cap 6 TRANSPORTE DE MASSA CEQ / MEF / 2015 Alda Simões Transporte molecular de massa Lei de Fick
Hidrodinâmica: Fluidos em Movimento
 Hidrodinâmica: Fluidos em Movimento Renato Akio Ikeoka FLUIDOS EM MOVIMENTO Fluido subdivisão de elementos de volume suficientemente pequenos para que possamos tratar cada um deles como uma partícula e
Hidrodinâmica: Fluidos em Movimento Renato Akio Ikeoka FLUIDOS EM MOVIMENTO Fluido subdivisão de elementos de volume suficientemente pequenos para que possamos tratar cada um deles como uma partícula e
DETERMINAÇÃO DO COEFICIENTE DE DIFUSÃO DO ETANOL 1 DETERMINATION OF THE ETHANOL DIFFUSION COEFFCIENT
 DETERMINAÇÃO DO COEFICIENTE DE DIFUSÃO DO ETANOL 1 DETERMINATION OF THE ETHANOL DIFFUSION COEFFCIENT Anderson Luís Gay 2, Gabriela Zorzetto Do Nascimento 3, Mônica Lima Gonçalves 4, Fernanda Da Cunha Pereira
DETERMINAÇÃO DO COEFICIENTE DE DIFUSÃO DO ETANOL 1 DETERMINATION OF THE ETHANOL DIFFUSION COEFFCIENT Anderson Luís Gay 2, Gabriela Zorzetto Do Nascimento 3, Mônica Lima Gonçalves 4, Fernanda Da Cunha Pereira
W sen = v h A. Considerando o somatório das forças: Vamos calcular o número de Reynolds: F 2 Re=1264 5, Re=28
 Exercícios da lista do Módulo 1 [5] Na figura ao lado, se o fluido é a glicerina a ⁰ C e a largura entre as placas é 6 mm, qual a tensão de cisalhamento necessária (em Pa) para mover a placa superior a
Exercícios da lista do Módulo 1 [5] Na figura ao lado, se o fluido é a glicerina a ⁰ C e a largura entre as placas é 6 mm, qual a tensão de cisalhamento necessária (em Pa) para mover a placa superior a
Disciplina : Termodinâmica. Aula 10 Análise da massa e energia aplicadas a volumes de controle
 Disciplina : Termodinâmica Aula 10 Análise da massa e energia aplicadas a volumes de controle Prof. Evandro Rodrigo Dário, Dr. Eng. Conservação da Massa A massa, assim como a energia, é uma propriedade
Disciplina : Termodinâmica Aula 10 Análise da massa e energia aplicadas a volumes de controle Prof. Evandro Rodrigo Dário, Dr. Eng. Conservação da Massa A massa, assim como a energia, é uma propriedade
Lista de Exercícios de Operações Unitárias I
 Lista de Exercícios de Operações Unitárias I Bombas Prof. Dra. Lívia Chaguri Monitor Victor Ferreira da Motta L. Fonseca ¹Exercício 1) Considere a instalação mostrada na Figura 1. Azeite de Oliva a 20
Lista de Exercícios de Operações Unitárias I Bombas Prof. Dra. Lívia Chaguri Monitor Victor Ferreira da Motta L. Fonseca ¹Exercício 1) Considere a instalação mostrada na Figura 1. Azeite de Oliva a 20
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2. prof. Daniela Szilard 23 de maio de 2016
 Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
HIDROSTÁTICA. Priscila Alves
 HIDROSTÁTICA Priscila Alves priscila@demar.eel.usp.br OBJETIVOS Exemplos a respeito da Lei de Newton para viscosidade. Variação da pressão em função da altura. Estática dos fluidos. Atividade de fixação.
HIDROSTÁTICA Priscila Alves priscila@demar.eel.usp.br OBJETIVOS Exemplos a respeito da Lei de Newton para viscosidade. Variação da pressão em função da altura. Estática dos fluidos. Atividade de fixação.
Instrumentação Eletroeletrônica. Prof. Afrânio Ornelas Ruas Vilela
 Instrumentação Eletroeletrônica Prof. Afrânio Ornelas Ruas Vilela Medição de Vazão Na maioria das operações realizadas nos processos industriais é muito importante efetuar a medição e o controle da quantidade
Instrumentação Eletroeletrônica Prof. Afrânio Ornelas Ruas Vilela Medição de Vazão Na maioria das operações realizadas nos processos industriais é muito importante efetuar a medição e o controle da quantidade
LABORATÓRIO DE ENGENHARIA QUÍMICA I
 LABORATÓRIO DE ENGENHARIA QUÍMICA I Prof. Gerônimo Virgínio Tagliaferro FENÔMENOS DE TRANSPORTE EXPERIMENTAL Programa Resumido 1) Cominuição e classificação de sólidos granulares 2) Medidas de Vazão em
LABORATÓRIO DE ENGENHARIA QUÍMICA I Prof. Gerônimo Virgínio Tagliaferro FENÔMENOS DE TRANSPORTE EXPERIMENTAL Programa Resumido 1) Cominuição e classificação de sólidos granulares 2) Medidas de Vazão em
FENÔMENO DE TRANSPORTE EXPERIMENTAL
 FENÔMENO DE TRANSPORTE EXPERIMENTAL Prof. MSc.. Sérgio S R. Montoro 1º semestre de 2013 EMENTA: FENÔMENOS DE TRANSPORTE EXPERIMENTAL Experimento 1: Estudo do tempo de escoamento de líquidos l em função
FENÔMENO DE TRANSPORTE EXPERIMENTAL Prof. MSc.. Sérgio S R. Montoro 1º semestre de 2013 EMENTA: FENÔMENOS DE TRANSPORTE EXPERIMENTAL Experimento 1: Estudo do tempo de escoamento de líquidos l em função
Física Experimental II. Exercícios
 Física Experimental II Lista de exercícios e problema preparatório para a Prova P2 Exercícios 1) Foi realizado um experimento para determinar o tipo de movimento de um corpo. Mediu-se a posição deste corpo
Física Experimental II Lista de exercícios e problema preparatório para a Prova P2 Exercícios 1) Foi realizado um experimento para determinar o tipo de movimento de um corpo. Mediu-se a posição deste corpo
TERMODINÂMICA APLICADA
 TERMODINÂMICA APLICADA LEONARDO DE QUEIROZ MOREIRA Propriedades de uma substância pura GOIÂNIA, 29 DE AGOSTO DE 2016. Objetivo Apresentar como algumas propriedades termodinâmicas se correlacionam: Temperatura;
TERMODINÂMICA APLICADA LEONARDO DE QUEIROZ MOREIRA Propriedades de uma substância pura GOIÂNIA, 29 DE AGOSTO DE 2016. Objetivo Apresentar como algumas propriedades termodinâmicas se correlacionam: Temperatura;
UNIVERSIDADE EDUARDO MONDLANE
 UNIVERSIDADE EDUARDO MONDLANE Faculdade de Engenharia Transmissão de calor Aula prática Nº 11 1 Aula Prática-11 Transferência de Massa Problema -8.1(I) Um recipiente contem um refrigerante gaseificado
UNIVERSIDADE EDUARDO MONDLANE Faculdade de Engenharia Transmissão de calor Aula prática Nº 11 1 Aula Prática-11 Transferência de Massa Problema -8.1(I) Um recipiente contem um refrigerante gaseificado
Lista de Exercícios - Unidade 10 Buscando o equilíbrio
 Lista de xercícios - Unidade 10 uscando o equilíbrio Hidrostática Primeira lista de exercícios: 1. Um recipiente contém 6,0 litros de água. Sabendo que a densidade da água é 1,0 g / cm 3, qual a massa
Lista de xercícios - Unidade 10 uscando o equilíbrio Hidrostática Primeira lista de exercícios: 1. Um recipiente contém 6,0 litros de água. Sabendo que a densidade da água é 1,0 g / cm 3, qual a massa
Primeira Lista de Exercícios de Biofísica II. c n
 Primeira Lista de Exercícios de Biofísica II 1. Considere uma célula composta por um corpo celular ao qual está preso um longo e fino processo tubular (por exemplo, o axônio de um neurônio ou o flagelo
Primeira Lista de Exercícios de Biofísica II 1. Considere uma célula composta por um corpo celular ao qual está preso um longo e fino processo tubular (por exemplo, o axônio de um neurônio ou o flagelo
Resoluções dos exercícios propostos
 1 P.109 p a) AB corresponde a uma fusão (passagem da Sólido F fase sólida para a fase líquida). A B Líquido G b) B corresponde a uma vaporização E (passagem da fase líquida para a fase de D Vapor vapor).
1 P.109 p a) AB corresponde a uma fusão (passagem da Sólido F fase sólida para a fase líquida). A B Líquido G b) B corresponde a uma vaporização E (passagem da fase líquida para a fase de D Vapor vapor).
Lista de Exercícios 1
 Universidade de Brasília Faculdade de Tecnologia Departamento de Engenharia Elétrica 107484 Controle de Processos 1 o Semestre 2015 Lista de Exercícios 1 Para os exercícios abaixo considere (exceto se
Universidade de Brasília Faculdade de Tecnologia Departamento de Engenharia Elétrica 107484 Controle de Processos 1 o Semestre 2015 Lista de Exercícios 1 Para os exercícios abaixo considere (exceto se
Exercício 1. Exercício 2.
 Exercício 1. Como resultado de um aumento de temperatura de 32 o C, uma barra com uma rachadura no seu centro dobra para cima (Figura). Se a distância fixa for 3,77 m e o coeficiente de expansão linear
Exercício 1. Como resultado de um aumento de temperatura de 32 o C, uma barra com uma rachadura no seu centro dobra para cima (Figura). Se a distância fixa for 3,77 m e o coeficiente de expansão linear
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL CURSOS DE ENGENHARIA DE ENERGIA E MECÂNICA MEDIÇÕES TÉRMICAS Prof. Paulo Smith Schneider
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL CURSOS DE ENGENHARIA DE ENERGIA E MECÂNICA MEDIÇÕES TÉRMICAS Prof. Paulo Smith Schneider Exercícios sobre medição de vazão Considere um grande reservatório (figura
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL CURSOS DE ENGENHARIA DE ENERGIA E MECÂNICA MEDIÇÕES TÉRMICAS Prof. Paulo Smith Schneider Exercícios sobre medição de vazão Considere um grande reservatório (figura
Massa Atômica e Molecular, Mol
 Capítulo Massa Atômica e Molecular, Mol Leia o texto seguinte, referente ao espectrógrafo de massa, e a seguir resolva os exercícios de a 6. É um aparelho capaz de fornecer a composição isotópica qualitativa
Capítulo Massa Atômica e Molecular, Mol Leia o texto seguinte, referente ao espectrógrafo de massa, e a seguir resolva os exercícios de a 6. É um aparelho capaz de fornecer a composição isotópica qualitativa
LISTA DE EXERCÍCIOS Nº 4
 LISTA DE EXERCÍCIOS Nº 4 Questões 1) Materiais A, B e C são sólidos que estão em suas temperaturas de fusão. O material A requer 200J para fundir 4kg, o material B requer 300J para fundir 5kg e o material
LISTA DE EXERCÍCIOS Nº 4 Questões 1) Materiais A, B e C são sólidos que estão em suas temperaturas de fusão. O material A requer 200J para fundir 4kg, o material B requer 300J para fundir 5kg e o material
Lista de Exercícios Transferência de Massas
 Lista de Exercícios Transferência de Massas Autor: Prof. Édler Lins de Albuquerque 2015 1 Questão 1: Se um cubo de açúcar for colocado em uma xícara de café, responda sobre o fenômeno de transferência
Lista de Exercícios Transferência de Massas Autor: Prof. Édler Lins de Albuquerque 2015 1 Questão 1: Se um cubo de açúcar for colocado em uma xícara de café, responda sobre o fenômeno de transferência
Lista 1 - Física II. (g) Nenhuma das opções anteriores. Figura 1: Questão 1.
 Lista 1 - Física II Questão 1. Considere o tubo com vasos comunicantes de mesma seção reta e preenchido com um fluido incompressível em equilíbrio no campo gravitacional terrestre como na Figura 1. Em
Lista 1 - Física II Questão 1. Considere o tubo com vasos comunicantes de mesma seção reta e preenchido com um fluido incompressível em equilíbrio no campo gravitacional terrestre como na Figura 1. Em
MECÂNICA DOS FLUIDOS LISTA DE EXERCÍCIOS
 MECÂNICA DOS FLUIDOS LISTA DE EXERCÍCIOS 1- A vazão do equipamento é de 4800m³/h. Considerando que a velocidade do ar é de 4m/s, qual é a largura dos dutos. Considere altura dos dutos como sendo de 0,25cm.
MECÂNICA DOS FLUIDOS LISTA DE EXERCÍCIOS 1- A vazão do equipamento é de 4800m³/h. Considerando que a velocidade do ar é de 4m/s, qual é a largura dos dutos. Considere altura dos dutos como sendo de 0,25cm.
Disciplina : Máquinas Térmicas e de Fluxo. Aula 2 Propriedades Termodinâmicas
 Disciplina : Máquinas Térmicas e de Fluxo Aula 2 Propriedades Termodinâmicas Prof. Evandro Rodrigo Dário, Dr. Eng. Líquido comprimido Considere-se um dispositivo de cilindropistão contendo água na fase
Disciplina : Máquinas Térmicas e de Fluxo Aula 2 Propriedades Termodinâmicas Prof. Evandro Rodrigo Dário, Dr. Eng. Líquido comprimido Considere-se um dispositivo de cilindropistão contendo água na fase
Mecânica dos Fluidos. Aula 18 Exercícios Complementares. Prof. MSc. Luiz Eduardo Miranda J. Rodrigues
 Aula 18 Exercícios Complementares Tópicos Abordados Nesta Aula. Exercícios Complementares. 1) A massa específica de uma determinada substância é igual a 900kg/m³, determine o volume ocupado por uma massa
Aula 18 Exercícios Complementares Tópicos Abordados Nesta Aula. Exercícios Complementares. 1) A massa específica de uma determinada substância é igual a 900kg/m³, determine o volume ocupado por uma massa
3 a VOCÊ TERÁ 04 (QUATRO) HORAS PARA RESPONDER ÀS QUESTÕES DISCURSIVAS E DE IMPRESSÕES SOBRE A PROVA.
 Instruções CADERNO DE QUESTÕES 1- Você está recebendo o seguinte material: a) este caderno com o enunciado das 10 (dez) questões discursivas e das questões relativas às suas impressões sobre a prova, assim
Instruções CADERNO DE QUESTÕES 1- Você está recebendo o seguinte material: a) este caderno com o enunciado das 10 (dez) questões discursivas e das questões relativas às suas impressões sobre a prova, assim
) (8.20) Equipamentos de Troca Térmica - 221
 onde: v = &m = Cp = h lv = U = A = T = t = volume específico vazão em massa (Kg/h) calor específico calor latente de vaporização coeficiente global de troca térmica área de transmissão de calor temperatura
onde: v = &m = Cp = h lv = U = A = T = t = volume específico vazão em massa (Kg/h) calor específico calor latente de vaporização coeficiente global de troca térmica área de transmissão de calor temperatura
Calcule o valor mínimo de M para permitir o degelo (e recongelação) do bloco à medida que é atravessado pela barra.
 Termodinâmica Aplicada (PF: comunicar eventuais erros para pmmiranda@fc.ul.pt) Exercícios 7. Uma barra metálica rectangular fina, com 0 cm de comprimento e mm de largura, está assente num bloco de gelo
Termodinâmica Aplicada (PF: comunicar eventuais erros para pmmiranda@fc.ul.pt) Exercícios 7. Uma barra metálica rectangular fina, com 0 cm de comprimento e mm de largura, está assente num bloco de gelo
AULA 4 CINEMÁTICA DOS FLUIDOS EQUAÇÃO DA CONTINUIDADE. Prof. Gerônimo V. Tagliaferro
 AULA 4 CINEMÁTICA DOS FLUIDOS EQUAÇÃO DA CONTINUIDADE Prof. Gerônimo V. Tagliaferro Regimes ou movimentos variado e permanente Regime permanente é aquele em que as propriedades do fluido são invariáveis
AULA 4 CINEMÁTICA DOS FLUIDOS EQUAÇÃO DA CONTINUIDADE Prof. Gerônimo V. Tagliaferro Regimes ou movimentos variado e permanente Regime permanente é aquele em que as propriedades do fluido são invariáveis
FENÔMENOS DE TRANSPORTES AULA 1 FLUIDOS PARTE 1
 FENÔMENOS DE TRANSPORTES AULA 1 FLUIDOS PARTE 1 PROF.: KAIO DUTRA Definição de Um Fluido Definição elementar: Fluido é uma substância que não tem uma forma própria, assume o formato do meio. Definição
FENÔMENOS DE TRANSPORTES AULA 1 FLUIDOS PARTE 1 PROF.: KAIO DUTRA Definição de Um Fluido Definição elementar: Fluido é uma substância que não tem uma forma própria, assume o formato do meio. Definição
Condensação
 Condensação Condensação Condensação Condensação Condensação Condensação em Filme Tal como no caso de convecção forçada, a transferência de calor em condensação depende de saber se o escoamento é laminar
Condensação Condensação Condensação Condensação Condensação Condensação em Filme Tal como no caso de convecção forçada, a transferência de calor em condensação depende de saber se o escoamento é laminar
AULA PRÁTICA 2 PROPRIEDADES FUNDAMENTAIS DOS FLUIDOS
 ! AULA PRÁTICA 2 PROPRIEDADES FUNDAMENTAIS DOS FLUIDOS 1) - M A S S A E S P E C Í F I C A ( ρ ) OU DENSIDADE ABSOLUTA (ρ ). - É o quociente entre a Massa do fluido e o Volume que contém essa massa. m ρ
! AULA PRÁTICA 2 PROPRIEDADES FUNDAMENTAIS DOS FLUIDOS 1) - M A S S A E S P E C Í F I C A ( ρ ) OU DENSIDADE ABSOLUTA (ρ ). - É o quociente entre a Massa do fluido e o Volume que contém essa massa. m ρ
1ª QUESTÃO Valor 1,0 = 1. Dados: índice de refração do ar: n 2. massa específica da cortiça: 200 kg/m 3. 1 of :36
 1ª QUESTÃO Valor 1,0 Uma lâmpada é colocada no fundo de um recipiente com líquido, diretamente abaixo do centro de um cubo de cortiça de 10 cm de lado que flutua no líquido. Sabendo que o índice de refração
1ª QUESTÃO Valor 1,0 Uma lâmpada é colocada no fundo de um recipiente com líquido, diretamente abaixo do centro de um cubo de cortiça de 10 cm de lado que flutua no líquido. Sabendo que o índice de refração
DESTILAÇÃO Lei de Raoult
 DESTILAÇÃO Operação que consiste na separação de líquidos de suas eventuais misturas, por passagem de vapor e posterior condensação com retorno ao estado líquido, com auxílio de calor e/ou por redução
DESTILAÇÃO Operação que consiste na separação de líquidos de suas eventuais misturas, por passagem de vapor e posterior condensação com retorno ao estado líquido, com auxílio de calor e/ou por redução
UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS FENÔMENOS DE TRANSPORTE ATIVIDADE SEGUNDA AVALIAÇÃO
 UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS FENÔMENOS DE TRANSPORTE ATIVIDADE SEGUNDA AVALIAÇÃO 1 1) Considere o escoamento de ar em torno do motociclista que se move em
UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS FENÔMENOS DE TRANSPORTE ATIVIDADE SEGUNDA AVALIAÇÃO 1 1) Considere o escoamento de ar em torno do motociclista que se move em
Controle de Processos Aula: Principais váriaveis em controle de processos químicos
 107484 Controle de Processos Aula: Principais váriaveis em controle de processos químicos Prof. Eduardo Stockler Tognetti Departamento de Engenharia Elétrica Universidade de Brasília UnB 1 o Semestre 2015
107484 Controle de Processos Aula: Principais váriaveis em controle de processos químicos Prof. Eduardo Stockler Tognetti Departamento de Engenharia Elétrica Universidade de Brasília UnB 1 o Semestre 2015
SISTEMAS TÉRMICOS PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução desse material sem a
 PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS INTRODUÇÃO E CONCEITOS INICIAIS ALBERTO HERNANDEZ NETO PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução
PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS INTRODUÇÃO E CONCEITOS INICIAIS ALBERTO HERNANDEZ NETO PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução
a) Qual deverá ser o volume do PFR para converter 80% de A em fase líquida? Considerar alimentação a 44 L min -1 e C A0 = C B0 = 1 mol L -1
 501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
Disciplina: Sistemas Térmicos
 Disciplina: Sistemas Térmicos Definição de Substância Pura Equilíbrio de Fases Líquido-Vapor de uma Substância Pura Diagrama de Temperatura versus Volume Específico Título de uma Substância com Fases Líquida
Disciplina: Sistemas Térmicos Definição de Substância Pura Equilíbrio de Fases Líquido-Vapor de uma Substância Pura Diagrama de Temperatura versus Volume Específico Título de uma Substância com Fases Líquida
Fenômenos Térmicos : primeiro conjunto de problemas
 Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
GASES. https://www.youtube.com/watch?v=wtmmvs3uiv0. David P. White. QUÍMICA: A Ciência Central 9ª Edição Capítulo by Pearson Education
 GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
3 Modelagem Física e Matemática
 3 Modelagem Física e Matemática omo mencionado no capítulo introdução, o objetivo do presente trabalho consiste em identificar a importância dos mecanismos de absorção química para previsão da absorção
3 Modelagem Física e Matemática omo mencionado no capítulo introdução, o objetivo do presente trabalho consiste em identificar a importância dos mecanismos de absorção química para previsão da absorção
Gases. 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação?
 Capítulo 2 Gases 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação? Van der Waals verificou que o fato do gás real não se comportar como o gás ideal é
Capítulo 2 Gases 1. Qual a equação de Van der Waals para o gás real e qual o significado de cada termo dessa equação? Van der Waals verificou que o fato do gás real não se comportar como o gás ideal é
Hidrostática e Calorimetria PROF. BENFICA
 Hidrostática e Calorimetria PROF. BENFICA benfica@anhanguera.com www.marcosbenfica.com LISTA 1 Conceitos Iniciais/Hidrostática 1) Calcular o peso específico, o volume específico e a massa específica de
Hidrostática e Calorimetria PROF. BENFICA benfica@anhanguera.com www.marcosbenfica.com LISTA 1 Conceitos Iniciais/Hidrostática 1) Calcular o peso específico, o volume específico e a massa específica de
mol L -1 min -1. Um PFR com reciclo será
 401) A reação em fase líquida A 2B + C ocorre isotermicamente em um PFR de 800 L. Calcule a taxa de produção de B considerando que a alimentação contém 3,5 mol L -1 de A, o tempo espacial é de 8 min e
401) A reação em fase líquida A 2B + C ocorre isotermicamente em um PFR de 800 L. Calcule a taxa de produção de B considerando que a alimentação contém 3,5 mol L -1 de A, o tempo espacial é de 8 min e
Capítulo 08 - TRANSFERÊNCIA DE CALOR POR CONDUÇÃO EM REGIME TRANSIENTE
 Os exercícios e figuras deste texto foram retirados de diversas referências bibliográficas listadas no programa da disciplina 1 FENÔMENOS DE TRANSPORTE Capítulo 08 - TRANSFERÊNCIA DE CALOR POR CONDUÇÃO
Os exercícios e figuras deste texto foram retirados de diversas referências bibliográficas listadas no programa da disciplina 1 FENÔMENOS DE TRANSPORTE Capítulo 08 - TRANSFERÊNCIA DE CALOR POR CONDUÇÃO
Resolução de Curso Básico de Física de H. Moysés Nussenzveig Capítulo 07 - Vol. 2
 HTTP://WWW.COMSIZO.COM.BR/ Resolução de Curso Básico de Física de H. Moysés Nussenzveig Capítulo 7 - Vol. Engenharia Física 9 Universidade Federal de São Carlos /1/9 1 Uma esfera oca de alumínio tem um
HTTP://WWW.COMSIZO.COM.BR/ Resolução de Curso Básico de Física de H. Moysés Nussenzveig Capítulo 7 - Vol. Engenharia Física 9 Universidade Federal de São Carlos /1/9 1 Uma esfera oca de alumínio tem um
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
Prática 05 Determinação Da Massa Molar Do Magnésio
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 05 Determinação Da Massa Molar Do Magnésio
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 05 Determinação Da Massa Molar Do Magnésio
ENGENHARIA DE MATERIAIS. Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa)
 ENGENHARIA DE MATERIAIS Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br TRANSFERÊNCIA DE
ENGENHARIA DE MATERIAIS Fenômenos de Transporte em Engenharia de Materiais (Transferência de Calor e Massa) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br TRANSFERÊNCIA DE
Lista de Exercícios Solução em Sala
 Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
Observações: 2 R diâmetros (D) das equações pelos diâmetros hidráulicos (D H) e nada se altera.
 O cãozinho chamado lemão nasceu com HIDROCEFLI (acúmulo excessivo de líquido cefalorraquidiano dentro do crânio, que leva ao inchaço cerebral) e mesmo contra os diagnósticos conviveu comigo durante 3 anos,
O cãozinho chamado lemão nasceu com HIDROCEFLI (acúmulo excessivo de líquido cefalorraquidiano dentro do crânio, que leva ao inchaço cerebral) e mesmo contra os diagnósticos conviveu comigo durante 3 anos,
Lei de Fourier. Considerações sobre a lei de Fourier. A lei de Fourier é fenomenológica, isto é, desenvolvida de fenômenos observados.
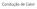 Condução de Calor Lei de Fourier A lei de Fourier é fenomenológica, isto é, desenvolvida de fenômenos observados Considerações sobre a lei de Fourier q x = ka T x Fazendo Δx 0 q taxa de calor [J/s] ou
Condução de Calor Lei de Fourier A lei de Fourier é fenomenológica, isto é, desenvolvida de fenômenos observados Considerações sobre a lei de Fourier q x = ka T x Fazendo Δx 0 q taxa de calor [J/s] ou
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
CONCURSO PÚBLICO EDITAL Nº 03 / 2015
 MINISTÉRIO DA EDUCAÇÃO INSTITUTO FEDERAL DO ESPÍRITO SANTO REITORIA Avenida Rio Branco, 50 Santa Lúcia 29056-255 Vitória ES 27 3357-7500 CONCURSO PÚBLICO EDITAL Nº 03 / 2015 Professor do Magistério do
MINISTÉRIO DA EDUCAÇÃO INSTITUTO FEDERAL DO ESPÍRITO SANTO REITORIA Avenida Rio Branco, 50 Santa Lúcia 29056-255 Vitória ES 27 3357-7500 CONCURSO PÚBLICO EDITAL Nº 03 / 2015 Professor do Magistério do
CADERNO DE EXERCÍCIOS DE MECÂNICA DOS FLUIDOS
 CADERNO DE EXERCÍCIOS DE MECÂNICA DOS FLUIDOS Prof. Jesué Graciliano da Silva https://jesuegraciliano.wordpress.com/aulas/mecanica-dos-fluidos/ 1 Prof. Jesué Graciliano da Silva Refrigeração - Câmpus São
CADERNO DE EXERCÍCIOS DE MECÂNICA DOS FLUIDOS Prof. Jesué Graciliano da Silva https://jesuegraciliano.wordpress.com/aulas/mecanica-dos-fluidos/ 1 Prof. Jesué Graciliano da Silva Refrigeração - Câmpus São
Roteiro das Práticas 1 a 3
 Roteiro das Práticas 1 a 3 Destilação e Absorção/Umidificação Prof. Universidade Federal do Pampa Curso de Engenharia Química Campus Bagé 10 de agosto de 2017 Destilação e Absorção 1 / 13 Operações por
Roteiro das Práticas 1 a 3 Destilação e Absorção/Umidificação Prof. Universidade Federal do Pampa Curso de Engenharia Química Campus Bagé 10 de agosto de 2017 Destilação e Absorção 1 / 13 Operações por
Física Geral II. Aula 1 - Teoria cinética dos gases. D. Valin 1. Universidade do Estado de Mato Grosso. Sinop-MT, April 25, 2017
 Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Fenômenos de Transporte PROF. BENFICA
 Fenômenos de Transporte PROF. BENFICA benfica@anhanguera.com www.marcosbenfica.com LISTA 1 Conceitos Iniciais 1) Faça as seguintes conversões de unidades: a) 45 km/h em m/s. b) 100 m/s em km/h. c) 600
Fenômenos de Transporte PROF. BENFICA benfica@anhanguera.com www.marcosbenfica.com LISTA 1 Conceitos Iniciais 1) Faça as seguintes conversões de unidades: a) 45 km/h em m/s. b) 100 m/s em km/h. c) 600
FENÔMENO DE TRANSPORTE EXPERIMENTAL
 FENÔMENO DE TRANSPORTE EXPERIMENTAL Prof. MSc.. Sérgio S R. Montoro 1º semestre de 2012 EMENTA: FENÔMENOS DE TRANSPORTE EXPERIMENTAL Experimento 1: Estudo do tempo de escoamento de líquidos l em função
FENÔMENO DE TRANSPORTE EXPERIMENTAL Prof. MSc.. Sérgio S R. Montoro 1º semestre de 2012 EMENTA: FENÔMENOS DE TRANSPORTE EXPERIMENTAL Experimento 1: Estudo do tempo de escoamento de líquidos l em função
Condução unidimensional em regime estacionário, Sistemas Radiais
 Com freqüência, em sistemas cilíndricos e esféricos há gradientes de temperatura somente na direção radial, o que permite analisá-los como sistemas unidimensionais. Um exemplo comum é o cilindro oco, cujas
Com freqüência, em sistemas cilíndricos e esféricos há gradientes de temperatura somente na direção radial, o que permite analisá-los como sistemas unidimensionais. Um exemplo comum é o cilindro oco, cujas
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
PROVA MODELO 1: AVALIAÇÃO DE MECÂNICA DOS FLUIDOS
 PROVA MODELO 1: AVALIAÇÃO DE MECÂNICA DOS FLUIDOS 1- A vazão do equipamento é de 3400m³/h. Considere a velocidade do ar dentro dos dutos como sendo de 5m/s. Considere a altura de todos os dutos como sendo
PROVA MODELO 1: AVALIAÇÃO DE MECÂNICA DOS FLUIDOS 1- A vazão do equipamento é de 3400m³/h. Considere a velocidade do ar dentro dos dutos como sendo de 5m/s. Considere a altura de todos os dutos como sendo
3. Um gás ideal passa por dois processos em um arranjo pistão-cilindro, conforme segue:
 1. Um arranjo pistão-cilindro com mola contém 1,5 kg de água, inicialmente a 1 Mpa e título de 30%. Esse dispositivo é então resfriado até o estado de líquido saturado a 100 C. Calcule o trabalho total
1. Um arranjo pistão-cilindro com mola contém 1,5 kg de água, inicialmente a 1 Mpa e título de 30%. Esse dispositivo é então resfriado até o estado de líquido saturado a 100 C. Calcule o trabalho total
1) Quantidade de Matéria (N)
 GRANDEZAS DA QUÍMICA E DA ENGENHARIA QUÍMICA (Transparências) Objetivo: Apresentar modificações ocorridas com algumas grandezas, principalmente sob o ponto de vista das unidades relacionadas com essas
GRANDEZAS DA QUÍMICA E DA ENGENHARIA QUÍMICA (Transparências) Objetivo: Apresentar modificações ocorridas com algumas grandezas, principalmente sob o ponto de vista das unidades relacionadas com essas
Capítulo 2 Propriedades de uma Substância Pura
 Capítulo 2 Propriedades de uma Substância Pura 2.1 - Definição Uma substância pura é aquela que tem composição química invariável e homogênea. Pode existir em mais de uma fase Composição química é igual
Capítulo 2 Propriedades de uma Substância Pura 2.1 - Definição Uma substância pura é aquela que tem composição química invariável e homogênea. Pode existir em mais de uma fase Composição química é igual
Lista de exercícios Caps. 7 e 8 TMEC-030 Transferência de Calor e Massa Período especial 2017/2
 Lista de exercícios Caps. 7 e 8 TMEC-030 Transferência de Calor e Massa Período especial 2017/2 1. (Incropera et al., 6 ed., 7.2) Óleo de motor a 100ºC e a uma velocidade de 0,1 m/s escoa sobre as duas
Lista de exercícios Caps. 7 e 8 TMEC-030 Transferência de Calor e Massa Período especial 2017/2 1. (Incropera et al., 6 ed., 7.2) Óleo de motor a 100ºC e a uma velocidade de 0,1 m/s escoa sobre as duas
FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS. Prof. MSc. Danilo Cândido
 FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS Prof. MSc. Danilo Cândido CONCEITOS DE GASES Um gás representa a forma mais simples da matéria, de baixa densidade e que ocupa o volume total de qualquer recipiente
FÍSICO-QUÍMICA GASES IDEAIS E GASES REAIS Prof. MSc. Danilo Cândido CONCEITOS DE GASES Um gás representa a forma mais simples da matéria, de baixa densidade e que ocupa o volume total de qualquer recipiente
ENGENHARIA FÍSICA. Fenômenos de Transporte A (Mecânica dos Fluidos)
 ENGENHARIA FÍSICA Fenômenos de Transporte A (Mecânica dos Fluidos) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br MECÂNICA DOS FLUIDOS ENGENHARIA FÍSICA AULA 5 CINEMÁTICA
ENGENHARIA FÍSICA Fenômenos de Transporte A (Mecânica dos Fluidos) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br MECÂNICA DOS FLUIDOS ENGENHARIA FÍSICA AULA 5 CINEMÁTICA
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
Exercícios e exemplos de sala de aula Parte 1
 PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
EXPERIÊNCIA 4 DETERMINAÇÃO DA MASSA ATÔMICA DO MAGNÉSIO
 CENTRO DE CIÊNCIAS TECNOLÓGICAS - CCT Departamento de Ciências Básicas e Sociais - DCBS Disciplina Química Experimental QEX Prof. Sivaldo Leite Correia EXPERIÊNCIA 4 DETERMINAÇÃO DA MASSA ATÔMICA DO MAGNÉSIO
CENTRO DE CIÊNCIAS TECNOLÓGICAS - CCT Departamento de Ciências Básicas e Sociais - DCBS Disciplina Química Experimental QEX Prof. Sivaldo Leite Correia EXPERIÊNCIA 4 DETERMINAÇÃO DA MASSA ATÔMICA DO MAGNÉSIO
LOQ Fenômenos de Transporte I. FT I 03 Tensão e viscosidade. Prof. Lucrécio Fábio dos Santos. Departamento de Engenharia Química LOQ/EEL
 LOQ 4083 - Fenômenos de Transporte I FT I 03 Tensão e viscosidade Prof. Lucrécio Fábio dos Santos Departamento de Engenharia Química LOQ/EEL Atenção: Estas notas destinam-se exclusivamente a servir como
LOQ 4083 - Fenômenos de Transporte I FT I 03 Tensão e viscosidade Prof. Lucrécio Fábio dos Santos Departamento de Engenharia Química LOQ/EEL Atenção: Estas notas destinam-se exclusivamente a servir como
SOLUÇÃO DA QUESTÃO: A equação da continuidade produz velocidade constante ao longo da tubulação: v 2 = v 1 = v.
 EAMB7 Mecânica dos Fluidos Intermediária Programa de Pós-Graduação em Engenharia Ambiental Departamento de Engenharia Ambiental, UFPR P, 8 Abr 8 Prof. Nelson Luís Dias NOME: GABARITO Assinatura: [ Água,
EAMB7 Mecânica dos Fluidos Intermediária Programa de Pós-Graduação em Engenharia Ambiental Departamento de Engenharia Ambiental, UFPR P, 8 Abr 8 Prof. Nelson Luís Dias NOME: GABARITO Assinatura: [ Água,
ENGENHARIA FÍSICA. Fenômenos de Transporte A (Mecânica dos Fluidos)
 ENGENHARIA FÍSICA Fenômenos de Transporte A (Mecânica dos Fluidos) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br MECÂNICA DOS FLUIDOS ENGENHARIA FÍSICA AULA 4 EQUAÇÃO MANOMÉTRICA
ENGENHARIA FÍSICA Fenômenos de Transporte A (Mecânica dos Fluidos) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br MECÂNICA DOS FLUIDOS ENGENHARIA FÍSICA AULA 4 EQUAÇÃO MANOMÉTRICA
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
FÍSICA BÁSICA II - LISTA 3 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância
Respostas a lápis ou com caneta de cor distinta à mencionada no item acima serão desconsideradas.
 Aluno: CPF: Matriculado no curso de Engenharia Data: 24/03/2011 Horário: Professor: Anibal Livramento da Silva Netto 1 a Avaliação de Física Teórica II Nas diversas questões desta avaliação, você deverá:
Aluno: CPF: Matriculado no curso de Engenharia Data: 24/03/2011 Horário: Professor: Anibal Livramento da Silva Netto 1 a Avaliação de Física Teórica II Nas diversas questões desta avaliação, você deverá:
META Estudar o comportamento de reações químicas que envolvem mais de uma etapa.
 EQUÇÕES CINÉTICS COMPOSTS Camilo ndrea ngelucci ula MET Estudar o comportamento de reações químicas que envolvem mais de uma etapa. OBJETIVOS o fi nal desta aula, o aluno deverá: compreender e determinar
EQUÇÕES CINÉTICS COMPOSTS Camilo ndrea ngelucci ula MET Estudar o comportamento de reações químicas que envolvem mais de uma etapa. OBJETIVOS o fi nal desta aula, o aluno deverá: compreender e determinar
RC1- A reação abaixo foi feta num reator batelada, obtendo-se os dados da tabela abaixo: 2 N 2 O 4 + O 2
 33 - Exercícios resolvidos -cinética - reação abaixo foi feta num reator batelada, obtendo-se os dados da tabela abaixo: N O 5 N O + O Ela pode ser de primeira ou segunda ordem alcule a energia de ativação
33 - Exercícios resolvidos -cinética - reação abaixo foi feta num reator batelada, obtendo-se os dados da tabela abaixo: N O 5 N O + O Ela pode ser de primeira ou segunda ordem alcule a energia de ativação
ENGENHARIA FÍSICA. Fenômenos de Transporte A (Mecânica dos Fluidos)
 ENGENHARIA FÍSICA Fenômenos de Transporte A (Mecânica dos Fluidos) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br MECÂNICA DOS FLUIDOS ENGENHARIA FÍSICA AULA 2...CONTINUAÇÃO...
ENGENHARIA FÍSICA Fenômenos de Transporte A (Mecânica dos Fluidos) Prof. Dr. Sérgio R. Montoro sergio.montoro@usp.br srmontoro@dequi.eel.usp.br MECÂNICA DOS FLUIDOS ENGENHARIA FÍSICA AULA 2...CONTINUAÇÃO...
Volume Parcial Molar
 Volume Parcial Molar 1. Introdução O volume molar é definido como o volume ocupado por 1 mol de uma substância pura. Por exemplo, o volume molar da água pura é 18 cm 3 /mol, conforme mostrado no cálculo
Volume Parcial Molar 1. Introdução O volume molar é definido como o volume ocupado por 1 mol de uma substância pura. Por exemplo, o volume molar da água pura é 18 cm 3 /mol, conforme mostrado no cálculo
Termodinâmica II - FMT 259
 Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 3 GABARITO (revisado em 22/04/0). Se as moléculas contidas em,0 g de água fossem distribuídas uniformemente sobre a superfície
Termodinâmica II - FMT 259 Diurno e Noturno, primeiro semestre de 2009 Lista 3 GABARITO (revisado em 22/04/0). Se as moléculas contidas em,0 g de água fossem distribuídas uniformemente sobre a superfície
304) Em um CSTR aberto para a atmosfera e com volume útil de 15 L ocorre a
 301) Um reator de mistura será projetado para conduzir a reação em fase líquida cujas ordens parciais coincidem com os respectivos coeficientes estequiométricos. A alimentação será feita a 9,8 L min -1
301) Um reator de mistura será projetado para conduzir a reação em fase líquida cujas ordens parciais coincidem com os respectivos coeficientes estequiométricos. A alimentação será feita a 9,8 L min -1
FENÔMENOS DE TRANSPORTE LISTA 02 DE EXERCÍCIOS PROF. MARCUS VINÍCIUS MARTINS FREITAS
 FENÔMENOS DE TRANSPORTE LISTA 02 DE EXERCÍCIOS PROF. MARCUS VINÍCIUS MARTINS FREITAS 1) Transformar as seguintes alturas de pressão para pressão em Pascais: a) 12 mca; b) 250 mmhg; c) 250 mmhg. 2. Transformar
FENÔMENOS DE TRANSPORTE LISTA 02 DE EXERCÍCIOS PROF. MARCUS VINÍCIUS MARTINS FREITAS 1) Transformar as seguintes alturas de pressão para pressão em Pascais: a) 12 mca; b) 250 mmhg; c) 250 mmhg. 2. Transformar
TÉCNICAS AVANÇADAS DE MODELAÇÃO E SIMULAÇÃO
 Universidade de Coimbra Faculdade de Ciência e Tecnologia Departamento de Engenharia Química TÉCNICAS AVANÇADAS DE MODELAÇÃO E SIMULAÇÃO PROFESSOR NUNO DE OLIVEIRA MODELAGEM DE UM SEPARADOR POR MEMBRANA
Universidade de Coimbra Faculdade de Ciência e Tecnologia Departamento de Engenharia Química TÉCNICAS AVANÇADAS DE MODELAÇÃO E SIMULAÇÃO PROFESSOR NUNO DE OLIVEIRA MODELAGEM DE UM SEPARADOR POR MEMBRANA
