ESTRUTURA CRISTALINA DE SILICATOS
|
|
|
- Eric Candal Lagos
- 6 Há anos
- Visualizações:
Transcrição
1 ESTRUTURA CRISTALINA DE SILICATOS Elementos em ordem de abundância na crosta: Oxigênio - O -2 1,30 A Silício Si +4 0,30 A NC = 4 Alumínio Al +3 0,47 A NC = 4 ou 6 A grande maioria dos outros cátions ocorre em coordenação octaédrica ou mais elevada
2 De cada 100 átomos na crosta terrestre, mais de 60 são de oxigênio, acima de 20, de silício e de 6 a 7 de alumínio. Ferro, cálcio, magnésio, sódio e potássio computam, cada um, dois átomos nessa crosta. Podemos assim imaginar a crosta: armação de íons de oxigênios ligados a íons de silício e alumínio. Os interstícios dessa estrutura estariam ocupados por íons de Mg, Fe, Ca, Na, K em estados de coordenação adequados a seus raios individuais. Mais de 90% da crosta é constituída por silicatos.
3 Estrutura Básica dos silicatos Arranjos atômicos de centenas de silicatos, que tem composições químicas complexas têm estruturas básicas relativamente simples e ordenada. Silício Elemento tetravalente Si +4 Tem grande afinidade com o oxigênio Ligações Si-O é 51% iônica e 49% covalente Formação de tetraedros de (SiO4) -4, tanto nas estruturas cristalinas quanto nos vidros. Relação de raios entre Si e O r Si = 0,29 r O Coordenação tetraédrica NC = 4 (4 átomos de O ficam arranjados ao redor de um átomo de silício)
4 FL= carga NC = 4 4 = 1 O 1Si O Si O 4 O -2-8 SiO 4-4 (SiO4) -4 tetraedro silício-oxigênio O Tetraedros de Sílica - (SiO 4 ) -4
5
6 Características da unidade fundamental dos silicatos Cada íon de oxigênio tem, portanto, a potencialidade de ligar-se com outro íon de silício e entrar em outro agrupamento tetraédrico, unindo, assim, os grupos tetraédricos através do oxigênio compartilhado Esta participação pode envolver um, dois, três ou todos os quatro íons de oxigênio no tetraedro, dando origem a uma diversidade de configurações estruturais.
7
8 Tipos de silicatos (subdivididos de acordo com o arranjo dos tetraedros) ORTOSSILICATOS Composto por um tetraedro, no qual nenhum oxigênio está compartilhado com outro Si. São tetraedros independentes ligados por outro cátion que não seja o silício. Razão O/Si = 4/1 = 4 1Si O -2-8 SiO 4-4 (SiO 4 ) -4 Neutralidade é satisfeita pela ligação dos oxigênios com cátions metálicos
9 Exemplos: minerais do tipo olivinas (forsterita Mg 2 SiO 4, faialita Fe 2 SiO 4, monticelita CaMgSiO 4 ) e os aluminosilicatos (cianita, andalusita, silimanita e mulita) Forsterita Mg 2 SiO 4 MgO NC=6 FL= 2/3 = 1/3 Oxigênio ligado a 3 magnésios e 1 silício
10 Al2SiO5 - Al2O3.SiO2
11 PIROSSILICATOS Composto por 2 tetraedros que compartilham um único átomo de oxigênio. Razão O/Si = 7/2 = 3,5 2 Si O Si 2 O 7-6 (Si 2 O 7 ) -6 (SiO 3,5 ) -3 Exemplo: melilita (Ca 2 MgSi 2 O 7 )
12 PIROXÊNIO OU METASSILICATOS Tetraedro compartilha 2 átomos de oxigênios Forma cadeias ou anéis Razão O/Si = 3/1 = 3 1 Si O -2-6 SiO 3-2 (SiO 3 ) -2 Exemplo: enstatita MgSiO 3 (cadeias de silicato); diopsídio MgCa(SiO 3 ), wolastonita CaSiO 3, Be 3 Al 2 Si 6 O 18 (esmeralda) Tetraedros compartilhando 2 oxigênios, formando anéis fechados. (Si 6 O 18 ) 12- (Si 3 O 9 ) 6- - Be 3 Al 2 Si 6 O 18 (6 tetraedros) - wolastonita CaSiO 3 (3 tetraedros)
13 diopsídio MgCa(SiO 3 )
14
15 Tetraedros compartilhando 2 oxigênios, formando anéis fechados. (Si 6 O 18 ) 12- (Si 3 O 9 ) 6- - Be 3 Al 2 Si 6 O 18 (6 tetraedros) - wolastonita CaSiO 3 (3 tetraedros) Os anéis (Si 6 O 18 ) estão dispostos na estrutura do berílio em folhas planas, ligadas fortemente pelos pequenos íons de Be 2+ e Al 3+. O Be 2+ está em coordenação 4 com o O 2-, e o Al 3+ está em coordenação 6. Os anéis de (Si 6 O 18 ) encontram-se dispostos uns sobre os outros de tal maneira que a região central forma orifícios ou canais, paralelos ao eixo c, onde íons OH -, F -, Li +, Cs +, Na + e moléculas de água podem se alojar.
16
17 ANFIBÓLIO Tetraedros de sílica compartilham igualmente 2 ou 3 átomos de oxigênio para formar uma camada dupla. Ligação de duas camadas de piroxênio com tetraedros alternados ligando as cadeias. Razão O/Si = (5,5)/2 = 2,75 2Si /2 O Si 2 O 5,5-3 (Si 2 O 5,5 ) 3- (Si 4 O 11 ) -6 Exemplo: asbestos (geralmente fratura fibrosa) (OH) 2 Ca 2 Mg 5 (Si 4 O 11 ) 2
18
19 Piroxênio Anfibólio
20 Qualquer estrutura de silicato mais complexa que o piroxênio precisa conter íons hidroxila para satisfazer as necessidades estruturais. FOLHAS DE SILICATO (DISSILICATOS OU FILOSSILICATOS) Tetraedros de sílica que compartilham 3 átomos de oxigênio para formar uma rede bidimensional contínua. Razão O/Si = 2,5/1 = 2,5 1Si ,5 O -2-5 SiO 2,5-1 (SiO 2,5 ) 1- (Si 2 O 5 ) 2- Exemplo: talco, micas, argilominerais (caulinita (OH) 4 Al 2 Si 2 O 5 )
21 QUARTZO Rede tridimensional composta de tetraedros de sílica que compartilham 4 átomos de oxigênio Razão O/Si = 2/1 = 2 1Si O -2-4 SiO 2 0 (SiO 2 ) Exemplo: quartzo, tridimita e cristobalita (formas polimórficas da sílica); feldspato
22 Cada uma das fases possui formas de alta e baixa temperatura transformações deslocativas. Envolve apenas pequenos deslocamentos de átomos, mudando o ângulo entre ligações Si-O-Si, mas sem rearranjos tetraédricos.
23 Estrutura da cristobalita Similar a da blenda de zinco, só que com átomos nas posições intersticiais. Compartilham todos os vértices. Estrutura da tridimita Estrutura monoclínica Estrutura do Quartzo Quartzo de alta hexagonal Quartzo de baixa trigonal Estrutura da cristobalita de alta
24
25 Substituição Isomórfica Estrutura é determinada pelo empacotamento dos ânions, e os cátions que associamse a cada grupo de ânions, dependem do seu tamanho comparado ao tamanho da abertura disponível no grupo de ânions. Em geral, pode ser afirmado que um íon pode ser substituído por outro se seu raio iônico diferir menos que 15% do íon a ser substituído Substituição isomórfica em minerais Minerais raramente se apresentam com compostos químicos simples, quase sempre, um ou mais íons da rede são substituídos em alguma proporção por outros. A substituição de íon por outro gera grandes variações na composição química e pode originar outros minerais
26 O íon substituto: - Deve ser comparável, em tamanho, ao íon original, caso contrário a coordenação será diferente. - A valência dos cátions isomórficos não influencia na habilidade de substituição, contudo, a neutralidade elétrica deve ser mantida: - Qualquer déficit de valência originado da substituição de um íon de menor valência deve ser compensado pela inclusão de íon adicionais ou pela mudança no estado de valência de algum íon já presente. Ex: Al 3+ e Si 4+ são comparáveis em tamanho Substituição do Si 4+ pelo Al 3+ em algumas posições na estrutura tridimensional da sílica gera um desbalanceamento elétrico na rede. Para o balanço elétrico deve ser introduzido um cátion, por exemplo, o Na +, que origina um feldspato. Si 4+ Na + Al 3+
27 FELDSPATOS O termo feldspato engloba uma série de silicatos de alumínio, contendo proporções variadas de potássio, sódio, cálcio e ocasionalmente bário. Reticulados cristalinos são similares em natureza à estrutura da cristobalita, com íons alcalinos e alcalinos terrosos localizados nos interstícios. Estrutura tridimensional de tetraedros de sílica, no qual alguns átomos de silício são substituídos por átomos de Al 3+, produzindo cargas negativas (solução sólida substitucional). Cargas são balanceadas pela presença de íons grandes nas posições intersticiais, dando origem a vários tipos de feldspatos. Tipos de feldspatos: - albita (NaAlSi 3 O 8 ) Na 2 O.Al 2 O 3.6SiO 2 - anortita (CaAl 2 Si 2 O 8 ) CaO. Al 2 O 3.SiO 2 - ortoclásio (KAlSi 3 O 8 ) K 2 O.Al 2 O 3.6SiO 2 - celsiana (BaAl 2 Si 2 O 8 ) - BaO. Al 2 O 3.SiO 2
28
29 Ortoclásio - empregado principalmente na manufatura de porcelana. O ortoclásio fundido também fornece a maior parte do brilho dos artigos de porcelana.
30 Estrutura dos argilominerais Argilominerais São constituídos por silicatos hidratados, podendo conter outros elementos como magnésio, cálcio, sódio, potássio, lítio e outros. São finamente divididos e usualmente aparecem na forma de placas. São compostos por uma ou mais camadas fundamentais Camada fundamental (Si 2 O 5 ) 2- (dissilicatos ou filossilicatos) Combinação de uma ou duas dessas camadas com uma camada composta por cátions coordenados octaedralmente. Se os cátions em camadas de coordenação octaedral têm a valência três, por exemplo, o Alumínio configuração similar a da gibsita Al(OH) 3
31
32 Gibsita Cátions em coordenação octaédrica Valência = 3 FL = 3/6 = ½ - cada alumínio está ligado a 6 OH- Cada OH- estará ligado a 2 Alumínios
33 Brucita Mg(OH) 2 ). Cátions (Magnésio) em coordenação octaédrica Valência dois FL = 2/6 = 1/3 - cada magnésio está ligado a 6 OH - Cada OH - estará ligado a 3 magnésios
34 Minerais em duas camadas Grupo da caulinita Fórmula geral: (OH) 2 Al 2 Si 2 O 5 - Al 2 O 3.2SiO 2.2H 2 O Constitui a maior porção dos vários tipos de argilominerais usados na indústria cerâmica. (caulim e argila plástica) Unidade fundamental 1 camada de (Si 2 O 5 ) -2 e 1 camada de gibsita Al(OH) 3 1 folha de tetraedro e 1 folha de octaedro
35 (Si 2 O 5 ) -2 com os íons oxigênios do ápice sendo satisfeitos por ligações com íons alumínio, e a coordenação octaédrica do alumínio sendo completada por íons hidroxila. Grupos hidroxilas numa folha estão em contato com oxigênios basais da próxima camada resulta em fracas ligações, o que causa uma excelente clivagem nas caulinitas. Pequenos cristais devido à falta de simetria na camada, sendo um lado tetraédrico e o outro octaédrico isso causa tensões tendendo a inclinar as folhas individuais de forma que a ligação fraca entre as camadas não possa agüentar. Não há ocorrência de substituição isomórfica
36
37 CAULINITA - (OH) 2 Al 2 Si 2 O 5 - Al 2 O 3.2SiO 2.2H 2 O
38
39
40
41
42
43
44 Talco - Mg3Si4O10.(OH)2
45 Minerais em três camadas Pirofilita Fórmula geral: (OH) 2 Al 2 (Si 2 O 5 ) 2 - Al 2 O 3.4SiO 2.H 2 O 2 camadas de (Si 2 O 5 ) -2 e 1 camada de gibsita Al(OH) 3 Clivagem ocorre entre as camadas, quebrando as ligações fracas. Ocorre em grande flocos devido ao arranjo simétrico das camadas nas folhas
46 Minerais 2:1 Pirofilita Al 2 (Si 2 O 5 ) 2 (OH) 2
47
48 Montmorilonita Fórmula geral: (OH) 2 (Al, Mg, Fe) 2 (Si 2 O 5 ) 2 Mesma estrutura da pirofilita com extensa substituição do Al por Mg e Fe em coordenação octaédrica. Pequeno tamanho de partícula Alta capacidade de troca de cátions Apresenta inchamento devido a adsorção de água entre as camadas O tipo e o número de íons adsorvidos afetam quimicamente a superfície das partículas.
49 (0.5Ca,Na) 0.7 (Al,Mg,Fe) 4 (Si,Al) 8 O 20 (OH) 4.nH 2 O Estrutura da montmorilonita. Os octaedros amarelos representam Mg 2+ substituindo Al 3+. Os cátions Ca 2+ e Na + (esferas lilás) encontram-se entre as folhas do tipo 2:1. Fonte:
50
51 Pequeno tamanho de partícula Ligação entre as camadas é fraca Quando colocados em água ou em ambientes úmidos, os cátions interlamelares se hidratam, entrando água entre as camadas, aumentando o espaçamento basal. Esse espaçamento varia com o tipo de cátion presente e com a quantidade de água disponível. A tendência à separação das camadas estruturais em meio aquoso pode ir até de partículas de espessura da própria camada. Argilas contendo esses argilominerais geralmente possuem ótimas propriedades plásticas e coloidais e apresentam grandes variações de propriedades físicas, dependendo dos cátions substitucionais (nas posições octaedrais) e dos cátions trocáveis. Possuem também alta retração de secagem
52 Micas Fórmula estrutural: KAl 2 (AlSi )(OH) 2 Na camada básica (Si 2 O 5 ) -2 (Si 4 O 10 ) 4-1 silício está sendo substituído por 1 alumínio (AlSi 3 O 10 ) 5-1 íon K + é adicionado para neutralizar as cargas Se Na + é adiconado mica paragonita Se Ca ++ é adionado Mica margarite substituições isomórficas do Si por Al nas posições tetraedrais Grande variação de composição química Diferem das montmorilonitas, pois os cátions de sódio e cálcio são ligados aos oxigênios basais da camada AlSi 3 O 10
53 Micas Mica muscovita KAl2(AlSi3010)(OH)2
54
55
56 Ilitas Fórmula estrutural (K,Na) x (Al,Mg,Fe) 2 (Al x Si 4-x O 10 ) (OH) 2 São consideradas intermediárias entre as estruturas das montmorilonitas e micas
57 Resumo Pirofilita, montomorilonita, mica e ilita apresentam a mesma estrutura básica (2:1) Na Pirofilita não ocorre nenhum tipo de substituição isomórfica Considerando a substituição na camada tetraedral: Al x Si 4-x tem-se: - Montmorilonitas x < 0,25 - Ilitas 0,25 < x < 0,75 - Micas x > 0,75
58 Relação entre propriedades e características estruturais Propriedades coloidais tais como plasticidade deriva do pequeno tamanho de partículas A ausência de partículas grandes pode ser atribuída a uma estrutura não simétrica (como a caulinita), com substituição isomórfica (como nas montmorilonitas). Substituição suficiente de Si por Al, como na mica, pode levar a uma ligação entre as camadas, as quais causam um aumento no tamanho de partículas e formam uma rede não expandida. Substituição em posições octaedrais aumentam a capacidade de troca de cátions, já que no balanceamento das cargas, os cátions estão fracamente ligados e, portanto são facilmente substituídos.
Estrutura de silicatos
 Estrutura de silicatos Tetraedros de SiO 2. ângulo de 109,2 o. O silício ocupa o centro do tetraedro e os oxigênios, os vértices do tetraedro Silicatos Átomos de silício e oxigênio Cadeias estruturais
Estrutura de silicatos Tetraedros de SiO 2. ângulo de 109,2 o. O silício ocupa o centro do tetraedro e os oxigênios, os vértices do tetraedro Silicatos Átomos de silício e oxigênio Cadeias estruturais
Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas
 Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas Prof. Dr. André Luiz Molisani Curso de Engenharia de Materiais e-mail: andre.molisani@fsa.br 2017 1 MATERIAL RECOMENDADO PARA ESTUDO: Capítulo
Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas Prof. Dr. André Luiz Molisani Curso de Engenharia de Materiais e-mail: andre.molisani@fsa.br 2017 1 MATERIAL RECOMENDADO PARA ESTUDO: Capítulo
Materiais Cerâmicos Silicatos. Conceitos Gerais
 Materiais Cerâmicos Silicatos Conceitos Gerais Processo Cerâmica com Argilas Massas Cerâmicas : São produzidas pela mistura de diversos componentes ( Materias Primas) Minerais no estado natural ou beneficiados
Materiais Cerâmicos Silicatos Conceitos Gerais Processo Cerâmica com Argilas Massas Cerâmicas : São produzidas pela mistura de diversos componentes ( Materias Primas) Minerais no estado natural ou beneficiados
Estruturas baseadas na HC Wurtzita ZnS
 Estruturas baseadas na HC Wurtzita ZnS Baseada num arranjo HC dos ânions com metade dos interstícios tetraedrais ocupados por cátions O número de coordenação de cada íon é 4 Se somente a metade das posições
Estruturas baseadas na HC Wurtzita ZnS Baseada num arranjo HC dos ânions com metade dos interstícios tetraedrais ocupados por cátions O número de coordenação de cada íon é 4 Se somente a metade das posições
Estrutur Es a trutur e Propriedades Pr dos materiais cerâmicos
 Estrutura e Propriedades dos materiais cerâmicos Fator de Empacotamento Atômico: FEA R a atoms unit cell FEA = 0,68 APF = Close-packed directions: length = 4R = 3 a Unit cell contains: 1 + 8 x 1/8 = 2
Estrutura e Propriedades dos materiais cerâmicos Fator de Empacotamento Atômico: FEA R a atoms unit cell FEA = 0,68 APF = Close-packed directions: length = 4R = 3 a Unit cell contains: 1 + 8 x 1/8 = 2
MINERALOGIA DOS SOLOS COMPOSIÇÃO MINERALÓGICA DOS SOLOS
 COMPOSIÇÃO MINERALÓGICA DOS SOLOS minerais resistentes ao intemperismo. Ex: quartzo minerais intemperizáveis em diferentes graus de alteração. Exs: feldspatos, micas minerais secundários originados do
COMPOSIÇÃO MINERALÓGICA DOS SOLOS minerais resistentes ao intemperismo. Ex: quartzo minerais intemperizáveis em diferentes graus de alteração. Exs: feldspatos, micas minerais secundários originados do
Estrutura macromolecular de silicatos naturais e aluminossilicatos
 3 Estrutura macromolecular de silicatos naturais e aluminossilicatos Este curso descreve os numerosos minerais naturais, e aponta as suas semelhanças com moléculas geopoliméricas (monômeros, dímeros, trímeros
3 Estrutura macromolecular de silicatos naturais e aluminossilicatos Este curso descreve os numerosos minerais naturais, e aponta as suas semelhanças com moléculas geopoliméricas (monômeros, dímeros, trímeros
Estrutura de cristais iônicos. Regras de Pauling
 Estrutura de cristais iônicos Regras de Pauling Estabilidade energética Por que os íons preferem ficar juntos, formando um cristal, do que moléculas isoladas? formar A Constante de Madelung é uma definição
Estrutura de cristais iônicos Regras de Pauling Estabilidade energética Por que os íons preferem ficar juntos, formando um cristal, do que moléculas isoladas? formar A Constante de Madelung é uma definição
GEOLOGIA. Professor: Adilson Soares Site:
 GEOLOGIA Professor: Adilson Soares E-mail: adilson.soares@unifesp.br Site: www.geologia.wiki.br Minerais e Rochas 1. Minerais e Rochas - conceito - propriedades dos minerais - tipos de rochas - ciclo das
GEOLOGIA Professor: Adilson Soares E-mail: adilson.soares@unifesp.br Site: www.geologia.wiki.br Minerais e Rochas 1. Minerais e Rochas - conceito - propriedades dos minerais - tipos de rochas - ciclo das
Revisão sobre Rochas e Minerais
 Revisão sobre Rochas e Minerais Quando conhecemos melhor as pedras, elas deixam de ser simples objetos inanimados e transformam-se em pequenos capítulos da história do planeta Terra e da nossa própria
Revisão sobre Rochas e Minerais Quando conhecemos melhor as pedras, elas deixam de ser simples objetos inanimados e transformam-se em pequenos capítulos da história do planeta Terra e da nossa própria
EPUSP Engenharia Ambiental. Mineralogia. PEF3304 Poluição do Solo
 EPUSP Engenharia Ambiental Mineralogia PEF3304 Poluição do Solo Solos são meios porosos criados na superfície terrestre por processos de intemperismo derivados de fenômenos biológicos, geológicos e hidrológicos.
EPUSP Engenharia Ambiental Mineralogia PEF3304 Poluição do Solo Solos são meios porosos criados na superfície terrestre por processos de intemperismo derivados de fenômenos biológicos, geológicos e hidrológicos.
Matérias-primas. Classificação geral: Cerâmicas Vidros Vitro-cerâmicos
 Matérias-primas Classificação geral: Cerâmicas Vidros Vitro-cerâmicos Matérias-primas : materiais particulados utilizados na formulação de peças cerâmicas. O processamento de cerâmicas, ao contrário de
Matérias-primas Classificação geral: Cerâmicas Vidros Vitro-cerâmicos Matérias-primas : materiais particulados utilizados na formulação de peças cerâmicas. O processamento de cerâmicas, ao contrário de
CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS
 CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO ESTABILIZAÇÃO DO AMETAL LIGAÇÃO IÔNICA
CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO ESTABILIZAÇÃO DO AMETAL LIGAÇÃO IÔNICA
GEOL Soluções sólidas. Adriana Alves
 GEOL 3056 Soluções sólidas Adriana Alves Variação composicional em minerals Ler Klein (2002) p.90-94 Minerais raramente são substâncias puras. A maioria exibe grande variação ccomposicional Variação se
GEOL 3056 Soluções sólidas Adriana Alves Variação composicional em minerals Ler Klein (2002) p.90-94 Minerais raramente são substâncias puras. A maioria exibe grande variação ccomposicional Variação se
Relação Rocha - Solo
 Relação Rocha - Solo ROCHA MINERAIS Primários (Litogênicos) Elementos Químicos INTEMPERISMO FÍSICO INTEMPERISMO QUÍMICO INTEMPERISMO QUÍMICO LIXIVIAÇÃO (excesso de água) Mineral Secundário (Pedogênico)
Relação Rocha - Solo ROCHA MINERAIS Primários (Litogênicos) Elementos Químicos INTEMPERISMO FÍSICO INTEMPERISMO QUÍMICO INTEMPERISMO QUÍMICO LIXIVIAÇÃO (excesso de água) Mineral Secundário (Pedogênico)
Compreendendo a Terra
 Frank Press Raymond Siever John Grotzinger Thomas H. Jordan Compreendendo a Terra 4a Edição Mineral: matéria prima da Terra Lecture Slides prepared by Peter Copeland Bill Dupré Copyright 2004 by W. H.
Frank Press Raymond Siever John Grotzinger Thomas H. Jordan Compreendendo a Terra 4a Edição Mineral: matéria prima da Terra Lecture Slides prepared by Peter Copeland Bill Dupré Copyright 2004 by W. H.
INTRODUÇÃO À GEOTECNIA (TEC00249)
 INTRODUÇÃO À GEOTECNIA (TEC00249) Minerais constituintes das rochas Prof. Manoel Isidro de Miranda Neto Eng. Civil, DSc A crosta terrestre: rochas e minerais Minerais São os materiais naturais, de origem
INTRODUÇÃO À GEOTECNIA (TEC00249) Minerais constituintes das rochas Prof. Manoel Isidro de Miranda Neto Eng. Civil, DSc A crosta terrestre: rochas e minerais Minerais São os materiais naturais, de origem
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I
 SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I
 SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS
 CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS GRANULOMETRIA O A CARACTERÍSTICAS FÍSICAS AMOSTRA DEFORMADA E INDEFORMADA COLETADA NO CAMPO DENSIDADE
CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS GRANULOMETRIA O A CARACTERÍSTICAS FÍSICAS AMOSTRA DEFORMADA E INDEFORMADA COLETADA NO CAMPO DENSIDADE
Ligações Químicas. No hidrônio, quantos pares de elétrons pertencem, no total, tanto ao hidrogênio quanto ao oxigênio? a) 1 b) 2 c) 3 d) 4 e) 6
 Aluno(a): Prof.: Éderson Ligações Químicas Questão 1) Abaixo temos as fórmulas de Lewis para átomos de cinco elementos químicos. Fórmulas eletrônicas de Lewis para alguns elementos Podemos afirmar que
Aluno(a): Prof.: Éderson Ligações Químicas Questão 1) Abaixo temos as fórmulas de Lewis para átomos de cinco elementos químicos. Fórmulas eletrônicas de Lewis para alguns elementos Podemos afirmar que
CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS
 CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS OS DIFERENTES NÍVEIS DE ORGANIZAÇÃO DOS SOLOS Exemplo de diferentes níveis de organização pedológica
CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS OS DIFERENTES NÍVEIS DE ORGANIZAÇÃO DOS SOLOS Exemplo de diferentes níveis de organização pedológica
Sólidos iônicos. Química Geral. Prof. Edson Nossol
 Sólidos iônicos Química Geral Prof. Edson Nossol Uberlândia, 07/10/2016 Sólido cristalino: possui ordem a longa distância: átomos, moléculas ou íons ocupam posições específicas Sólido não-cristalino: não
Sólidos iônicos Química Geral Prof. Edson Nossol Uberlândia, 07/10/2016 Sólido cristalino: possui ordem a longa distância: átomos, moléculas ou íons ocupam posições específicas Sólido não-cristalino: não
MINERAIS SECUNDÁRIOS
 MINERAIS SECUNDÁRIOS -Aula 27- Alexandre Paiva da Silva Minerais primários: diretamente da rocha Ex.: micas, feldspatos, quartzo, etc Minerais secundários: formados no solo a partir de outros minerais
MINERAIS SECUNDÁRIOS -Aula 27- Alexandre Paiva da Silva Minerais primários: diretamente da rocha Ex.: micas, feldspatos, quartzo, etc Minerais secundários: formados no solo a partir de outros minerais
ARGILOMINERAIS PROPRIEDADES E APLICAÇÕES
 Departamento de Engenharia Civil Pós-graduação ARGILOMINERAIS PROPRIEDADES E APLICAÇÕES Classificação Estrutural dos Argilominerais Introdução 1 Conceitos Geotécnicos Básicos 05/10/2011 Origem dos Solos
Departamento de Engenharia Civil Pós-graduação ARGILOMINERAIS PROPRIEDADES E APLICAÇÕES Classificação Estrutural dos Argilominerais Introdução 1 Conceitos Geotécnicos Básicos 05/10/2011 Origem dos Solos
A geologia é uma ciência que estuda a composição, estruturas e movimentos formadores da crosta terrestre. Esta subdivide-se em:
 Colégio Henrique Hennry Curso: Técnico de operações em Sistemas de petróleo Disciplina: Princípio de Geologia Introdução -1 A geologia é uma ciência que estuda a composição, estruturas e movimentos formadores
Colégio Henrique Hennry Curso: Técnico de operações em Sistemas de petróleo Disciplina: Princípio de Geologia Introdução -1 A geologia é uma ciência que estuda a composição, estruturas e movimentos formadores
ARRANJOS ATÔMICOS. Química Aplicada. Profº Vitor de Almeida Silva
 ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais
 Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais
 Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Matérias-primas naturais
 UNIVERSIDADE DE SÃO PAULO - USP ESCOLA DE ENGENHARIA DE LORENA EEL naturais Argilas 20/3/2018 Argilas Comparação entre as escalas principais de dimensões de partículas em sólidos Pérsio de Souza Santos
UNIVERSIDADE DE SÃO PAULO - USP ESCOLA DE ENGENHARIA DE LORENA EEL naturais Argilas 20/3/2018 Argilas Comparação entre as escalas principais de dimensões de partículas em sólidos Pérsio de Souza Santos
Materiais Cerâmicos Formulação. Conceitos Gerais
 Materiais Cerâmicos Formulação Conceitos Gerais Mulita - Síntese Objetivo : sintetizar mulita 3Al 2 O 3.2SiO 2 ou Al 6 Si 2 O 13 A mulita é uma fase cerâmica obtida pela reação entre alumina e sílica em
Materiais Cerâmicos Formulação Conceitos Gerais Mulita - Síntese Objetivo : sintetizar mulita 3Al 2 O 3.2SiO 2 ou Al 6 Si 2 O 13 A mulita é uma fase cerâmica obtida pela reação entre alumina e sílica em
CARGAS ELÉTRICAS DO SOLO. Atributos físicos e químicos do solo -Aula 12- Prof. Alexandre Paiva da Silva INTRODUÇÃO CARGAS ELÉTRICAS E FOTOSSÍNTESE:
 CARGAS ELÉTRICAS DO SOLO Atributos físicos e químicos do solo -Aula 12- Prof. Alexandre Paiva da Silva INTRODUÇÃO CARGAS ELÉTRICAS E FOTOSSÍNTESE: Vida na Terra Propriedade de uma dispersão coloidal Argilas
CARGAS ELÉTRICAS DO SOLO Atributos físicos e químicos do solo -Aula 12- Prof. Alexandre Paiva da Silva INTRODUÇÃO CARGAS ELÉTRICAS E FOTOSSÍNTESE: Vida na Terra Propriedade de uma dispersão coloidal Argilas
Ligações Químicas. Professor Haroldo
 Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
Ligações Químicas elementos químicos átomos moléculas
 Ligações Químicas Ligações Químicas Os diferentes elementos químicos combinam-se de várias maneiras formando uma grande variedade de substâncias, por meio das ligações químicas. Através das ligações químicas
Ligações Químicas Ligações Químicas Os diferentes elementos químicos combinam-se de várias maneiras formando uma grande variedade de substâncias, por meio das ligações químicas. Através das ligações químicas
Formação e estrutura dos principais minerais
 Formação e estrutura dos principais minerais Cada tipo de mineral, constitui uma espécie mineral. Ex: quarzto (SiO 2 ). Sempre que sua cristalização se der em condições geológicas ideais, a sua organização
Formação e estrutura dos principais minerais Cada tipo de mineral, constitui uma espécie mineral. Ex: quarzto (SiO 2 ). Sempre que sua cristalização se der em condições geológicas ideais, a sua organização
Capítulo 6 - LIGAÇÕES QUÍMICAS-resoluções
 Capítulo 6 - LIGAÇÕES QUÍMICAS-resoluções 1-C X e T devem ter a mesma carga com sinais contrários: +1 e -1, +2 e -2 ou +3 e -3. 2-B A) Fe 2 S 3 B) CsCl C) CaI 2 D) Al 2 3 E) Ba 3 N 2 Quanto maior a diagonal
Capítulo 6 - LIGAÇÕES QUÍMICAS-resoluções 1-C X e T devem ter a mesma carga com sinais contrários: +1 e -1, +2 e -2 ou +3 e -3. 2-B A) Fe 2 S 3 B) CsCl C) CaI 2 D) Al 2 3 E) Ba 3 N 2 Quanto maior a diagonal
Introdução a Engenharia e Ciência dos Materiais
 Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
Estrutura Cristalina dos Sólidos (Arranjos Atômicos)
 Estrutura Cristalina dos Sólidos (Arranjos Atômicos) INTRODUÇÃO As propriedades dos materiais dependem dos arranjos dos seus átomos. Esses arranjos podem ser classificados em: Estruturas moleculares: agrupamento
Estrutura Cristalina dos Sólidos (Arranjos Atômicos) INTRODUÇÃO As propriedades dos materiais dependem dos arranjos dos seus átomos. Esses arranjos podem ser classificados em: Estruturas moleculares: agrupamento
30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
 IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
Matérias-primas usadas no processamento de materiais cerâmicos
 usadas no processamento de materiais cerâmicos 6/3/2018 PROCESSAMENTO DE MATERIAIS CERÂMICOS naturais e sintéticas Fluxograma geral do processamento de cerâmicas Matérias - primas caracterizadas Cálculos
usadas no processamento de materiais cerâmicos 6/3/2018 PROCESSAMENTO DE MATERIAIS CERÂMICOS naturais e sintéticas Fluxograma geral do processamento de cerâmicas Matérias - primas caracterizadas Cálculos
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais. Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais
QUÍMICA. LIGAÇÕES QUÍMICAS Prof Francisco Sallas
 QUÍMICA LIGAÇÕES QUÍMICAS Prof Francisco Sallas chicosallas@hotmail.com Porque os átomos se ligam? A grande variedade de materiais que conhecemos, são formados pela combinação de átomos de elementos químicos.
QUÍMICA LIGAÇÕES QUÍMICAS Prof Francisco Sallas chicosallas@hotmail.com Porque os átomos se ligam? A grande variedade de materiais que conhecemos, são formados pela combinação de átomos de elementos químicos.
Ciências dos materiais- 232
 1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
Professora: Daniela Becker Mestranda: Jéssica de Aguiar
 Professora: Daniela Becker Mestranda: Jéssica de Aguiar JOINVILLE SC BRASIL 2016 Estruturas Cerâmicas São compostas por pelo menos dois elementos; Em geral são mais complexas do que a dos metais; Ex.:
Professora: Daniela Becker Mestranda: Jéssica de Aguiar JOINVILLE SC BRASIL 2016 Estruturas Cerâmicas São compostas por pelo menos dois elementos; Em geral são mais complexas do que a dos metais; Ex.:
Composição dos Solos
 Composição dos Solos Composição do Solo Fragmentos de rocha Minerais primários Minerais secundários: Argilo-minerias Silicatos não cristalinos Óid Óxidos e hidróxidos hidóid de ferro e alumínio íi Carbonatos
Composição dos Solos Composição do Solo Fragmentos de rocha Minerais primários Minerais secundários: Argilo-minerias Silicatos não cristalinos Óid Óxidos e hidróxidos hidóid de ferro e alumínio íi Carbonatos
... nas substâncias os átomos estão unidos uns aos outros? ... na água há um átomo de oxigênio e dois átomos de hidrogênio?
 Prof: Marcelo Vizeu Observe as substâncias presentes no nosso cotidiano H O H Na N N O O O Água oreto de sódio (sal de cozinha) Nitrogênio Ozônio Reflita: Porque...... nas substâncias os átomos estão
Prof: Marcelo Vizeu Observe as substâncias presentes no nosso cotidiano H O H Na N N O O O Água oreto de sódio (sal de cozinha) Nitrogênio Ozônio Reflita: Porque...... nas substâncias os átomos estão
Mineralogia. Oliveira, Francisco Sérgio Silva de. Mineralogia / Francisco Sérgio Silva de Oliveira. Varginha, slides : il.
 Mineralogia Oliveira, Francisco Sérgio Silva de. O48m Mineralogia / Francisco Sérgio Silva de Oliveira. Varginha, 2015. 16 slides : il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World Wide
Mineralogia Oliveira, Francisco Sérgio Silva de. O48m Mineralogia / Francisco Sérgio Silva de Oliveira. Varginha, 2015. 16 slides : il. Sistema requerido: Adobe Acrobat Reader Modo de Acesso: World Wide
contendo sulfetos, óxidos e gases Constituíntes do MAGMA O TiO 2 O 3 O Na 2 SiO 2 Al 2 FeO MgO CaO K 2 HCl HF N 2 O CO 2 CO SO 2 SO 3 S 2 H 2
 ROCHAS ÍGNEAS Aula de hoje: Conceito, gênese, ocorrências, propriedades macroscópicas e identificação das Rochas Ígneas de interesse no estudo de solos MAGMA material em estado de fusão, viscoso, pastoso,
ROCHAS ÍGNEAS Aula de hoje: Conceito, gênese, ocorrências, propriedades macroscópicas e identificação das Rochas Ígneas de interesse no estudo de solos MAGMA material em estado de fusão, viscoso, pastoso,
INTEMPERISMO QUÍMICO MUDANÇAS QUÍMICAS DE MINERAIS DA SUA FORMA MAIS INSTÁVEL PARA MAIS ESTÁVEL
 INTEMPERISMO QUÍMICO MUDANÇAS QUÍMICAS DE MINERAIS DA SUA FORMA MAIS INSTÁVEL PARA MAIS ESTÁVEL PERDA DE ELEMENTOS QUÍMICOS PRIMÁRIOS TRASFORMAÇÃO DE ELEMENTOS PRIMÁRIOS DA ROCHA EM SECUNDÁRIOS ALTERAÇÃO
INTEMPERISMO QUÍMICO MUDANÇAS QUÍMICAS DE MINERAIS DA SUA FORMA MAIS INSTÁVEL PARA MAIS ESTÁVEL PERDA DE ELEMENTOS QUÍMICOS PRIMÁRIOS TRASFORMAÇÃO DE ELEMENTOS PRIMÁRIOS DA ROCHA EM SECUNDÁRIOS ALTERAÇÃO
A4 Estrutura cristalina perfeição
 A4 Estrutura cristalina perfeição TEM Muitos dos materiais aplicados em engenharia têm estrutura cristalina: os átomos do material estão dispostos de modo regular e repetitivo Estrutura cristalina A célula
A4 Estrutura cristalina perfeição TEM Muitos dos materiais aplicados em engenharia têm estrutura cristalina: os átomos do material estão dispostos de modo regular e repetitivo Estrutura cristalina A célula
INTRODUÇÃO AOS MATERIAIS CERÂMICOS
 INTRODUÇÃO AOS MATERIAIS CERÂMICOS CAPÍTULO 2 - PROCESSOS DE FABRICAÇÃO PPGEM - EE - UFRGS 2. PROCESSOS DE FABRICAÇÃO 2.1 PROCESSAMENTO DE PÓS 2.2 CONFORMAÇÃO 2.3 SECAGEM 2.4 DENSIFICAÇÃO 2.5 ACABAMENTO
INTRODUÇÃO AOS MATERIAIS CERÂMICOS CAPÍTULO 2 - PROCESSOS DE FABRICAÇÃO PPGEM - EE - UFRGS 2. PROCESSOS DE FABRICAÇÃO 2.1 PROCESSAMENTO DE PÓS 2.2 CONFORMAÇÃO 2.3 SECAGEM 2.4 DENSIFICAÇÃO 2.5 ACABAMENTO
GMG 106 Cristalografia Fundamental. Polimorfos. Adriana Alves
 GMG 106 Cristalografia Fundamental Polimorfos Adriana Alves A partir das observações iniciais eu Pertita Plagioclásio zonado Estruturas minerais Da definição tem- se que minerais possuem arranjo atômico
GMG 106 Cristalografia Fundamental Polimorfos Adriana Alves A partir das observações iniciais eu Pertita Plagioclásio zonado Estruturas minerais Da definição tem- se que minerais possuem arranjo atômico
Estrutura de Sólidos Cristalinos. Profa. Dra Daniela Becker
 Estrutura de Sólidos Cristalinos Profa. Dra Daniela Becker Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
Estrutura de Sólidos Cristalinos Profa. Dra Daniela Becker Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
Aula 6: Estrutura Cristalina dos Metais
 Aula 6: Estrutura Cristalina dos Metais - Como a ligação metálica é não-direcional, não há restrições quanto ao número e posições dos vizinhos mais próximos. - A estrutura cristalina dos metais têm um
Aula 6: Estrutura Cristalina dos Metais - Como a ligação metálica é não-direcional, não há restrições quanto ao número e posições dos vizinhos mais próximos. - A estrutura cristalina dos metais têm um
12 GAB. 1 1 o DIA PASES 1 a ETAPA TRIÊNIO QUÍMICA QUESTÕES DE 21 A 30
 12 GAB. 1 1 o DIA PASES 1 a ETAPA TRIÊNIO 2005-2007 QUÍMICA QUESTÕES DE 21 A 30 21. A hemoglobina das células vermelhas do sangue contém o complexo de ferro com uma porfirina. Sabendo que um indivíduo
12 GAB. 1 1 o DIA PASES 1 a ETAPA TRIÊNIO 2005-2007 QUÍMICA QUESTÕES DE 21 A 30 21. A hemoglobina das células vermelhas do sangue contém o complexo de ferro com uma porfirina. Sabendo que um indivíduo
3. Origem das cargas elétricas no solo
 3. Origem das cargas elétricas no solo 3.1. Origem das cargas elétricas Há no solo, em geral, predominância de cargas negativas sobre positivas. Essa predominância, bastante significativa em solos de regiões
3. Origem das cargas elétricas no solo 3.1. Origem das cargas elétricas Há no solo, em geral, predominância de cargas negativas sobre positivas. Essa predominância, bastante significativa em solos de regiões
ESTRUTURA DOS SÓLIDOS CRISTALINOS. Mestranda: Marindia Decol
 ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 10 TURMA ANUAL
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 10 TURMA ANUAL 01. Item B I Correto. A energia para quebrar a ligação H F (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 10 TURMA ANUAL 01. Item B I Correto. A energia para quebrar a ligação H F (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando
Diferentes modelos de ligação química
 Ligação covalente Diferentes modelos de ligação química A grande diversidade de substâncias resulta da combinação de átomos dos elementos químicos através de diferentes modelos de ligação: covalente, iónica
Ligação covalente Diferentes modelos de ligação química A grande diversidade de substâncias resulta da combinação de átomos dos elementos químicos através de diferentes modelos de ligação: covalente, iónica
Lição 2 Rochas e Seus Minerais
 Quando conhecemos melhor as pedras, elas deixam de ser simples objetos inanimados e transformam se em pequenos capítulos da história do planeta Terra e da nossa própria história. (Fábio Ramos Dias de Andrade)
Quando conhecemos melhor as pedras, elas deixam de ser simples objetos inanimados e transformam se em pequenos capítulos da história do planeta Terra e da nossa própria história. (Fábio Ramos Dias de Andrade)
Ligações químicas e estrutura dos materiais
 Disciplina : - MFI Professores: Guilherme Ourique Verran - Dr. Eng. Metalúrgica Aula 02 Revisão de alguns conceitos fundamentais da Ciência dos Materiais Ligações químicas e estrutura dos materiais Conceitos
Disciplina : - MFI Professores: Guilherme Ourique Verran - Dr. Eng. Metalúrgica Aula 02 Revisão de alguns conceitos fundamentais da Ciência dos Materiais Ligações químicas e estrutura dos materiais Conceitos
Deep Sea Drilling Vessel (D/V) CHIKYU is the first riser equipped scientific drilling vessel built for science at the planning stage.
 Deep Sea Drilling Vessel (D/V) CHIKYU is the first riser equipped scientific drilling vessel built for science at the planning stage. It is capable of drilling up to 7,000m deep sea floor and aim to the
Deep Sea Drilling Vessel (D/V) CHIKYU is the first riser equipped scientific drilling vessel built for science at the planning stage. It is capable of drilling up to 7,000m deep sea floor and aim to the
Atividade extra. Questão 1 Cecierj Questão 2 Adaptado de UFRJ. Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Veja a seguir as distribuições eletrônicas para o magnésio e o oxigênio: Mg: K = 2 L = 8 M = 2 12 O: K = 2 L = 6 8 Explique como o composto MgO é formado e indique
Atividade extra Questão 1 Cecierj - 2013 Veja a seguir as distribuições eletrônicas para o magnésio e o oxigênio: Mg: K = 2 L = 8 M = 2 12 O: K = 2 L = 6 8 Explique como o composto MgO é formado e indique
INTEMPERISMO DE ROCHAS MINERALOGIA DE SOLOS
 INTEMPERISMO DE ROCHAS X MINERALOGIA DE SOLOS INTEMPERISMO DE ROCHAS 1-CONCEITO: conjunto de processos que ocorrem na superfície terrestre envolvendo ação de agentes atmosféricos, água, calor solar, gelo,vento,
INTEMPERISMO DE ROCHAS X MINERALOGIA DE SOLOS INTEMPERISMO DE ROCHAS 1-CONCEITO: conjunto de processos que ocorrem na superfície terrestre envolvendo ação de agentes atmosféricos, água, calor solar, gelo,vento,
Lição 4 Os Sólidos Ativos do Solo: Argila e Húmus
 Matéria inerte! Como se tal coisa pudesse existir. Bela é a vocação do mundo (...). Sob o microscópio eletrônico pode se perceber a intrincada harmonia das argilas (...) que são como a parede do estômago
Matéria inerte! Como se tal coisa pudesse existir. Bela é a vocação do mundo (...). Sob o microscópio eletrônico pode se perceber a intrincada harmonia das argilas (...) que são como a parede do estômago
Diferenças entre o C, Si e os demais elementos do grupo 14
 Diferenças entre o C, Si e os demais elementos do grupo 14 O carbono também difere dos demais elementos do grupo pela sua capacidade de formar cadeias (catenação). Isso porque as ligações C-C são fortes,
Diferenças entre o C, Si e os demais elementos do grupo 14 O carbono também difere dos demais elementos do grupo pela sua capacidade de formar cadeias (catenação). Isso porque as ligações C-C são fortes,
DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente
 FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
FOLHA DE QUESTÕES CURSO: ASS.: Engenharia de Produção DISCIPLINA: NOME: Química Geral DATA: Nº de ordem GRAU: PROVA: TURMA MATRÍCULA: Estudo Independente 5PRD31A 01) O grupo de átomos que é encontrado
CIÊNCIAS DA NATUREZA - QUÍMICA. Ligações Químicas
 CIÊNCIAS DA NATUREZA - QUÍMICA Prof. Adriana Strelow 1º Ano - 2016 Ligações Químicas Na natureza, dificilmente os átomos ficam sozinhos. Eles tendem a se unir uns aos outros para formarem novas substâncias.
CIÊNCIAS DA NATUREZA - QUÍMICA Prof. Adriana Strelow 1º Ano - 2016 Ligações Químicas Na natureza, dificilmente os átomos ficam sozinhos. Eles tendem a se unir uns aos outros para formarem novas substâncias.
ESTRUTURA DOS SÓLIDOS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais ESTRUTURA DOS SÓLIDOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º semestre de
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais ESTRUTURA DOS SÓLIDOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º semestre de
ORDEM. Periocidade. SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico de átomos, moléculas ou iões, formando uma estrutura cristalina regular
 Capítulo I ESTRUTURA CRISTALINA DE SÓLIDOS ORDEM curto alcance médio alcance longo alcance Periocidade unidimensional bidimensional tridimensional SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico
Capítulo I ESTRUTURA CRISTALINA DE SÓLIDOS ORDEM curto alcance médio alcance longo alcance Periocidade unidimensional bidimensional tridimensional SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico
Sólidos: Estudo de Estruturas Cristalinas
 UnB - Universidade de Brasília IQD - Instituto de Química Curso de Graduação Disciplina: Química Inorgânica 1 Experimental (Código 114073) Sólidos: Estudo de Estruturas Cristalinas A estrutura dos materiais
UnB - Universidade de Brasília IQD - Instituto de Química Curso de Graduação Disciplina: Química Inorgânica 1 Experimental (Código 114073) Sólidos: Estudo de Estruturas Cristalinas A estrutura dos materiais
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA INTENSIVA
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA INTENSIVA 01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA INTENSIVA 01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando
CONSOLIDAÇÃO DE MAGMAS
 CONSOLIDAÇÃO DE MAGMAS Prof. Ana Rita Rainho Condições de Texturas das rochas magmáticas Consoante as condições de arrefecimento do magma, o grau de desenvolvimento dos cristais é diferente. Fanerítica
CONSOLIDAÇÃO DE MAGMAS Prof. Ana Rita Rainho Condições de Texturas das rochas magmáticas Consoante as condições de arrefecimento do magma, o grau de desenvolvimento dos cristais é diferente. Fanerítica
PROF. DR. REGES HEINRICHS
 Universidade Estadual Paulista Campus de Dracena Curso Zootecnia Disciplina: Solos COLÓIDES DO SOLO PROF. DR. REGES HEINRICHS 2010 Introdução Colóides são partículas menores que 1 (um) micrômetro de diâmetro.
Universidade Estadual Paulista Campus de Dracena Curso Zootecnia Disciplina: Solos COLÓIDES DO SOLO PROF. DR. REGES HEINRICHS 2010 Introdução Colóides são partículas menores que 1 (um) micrômetro de diâmetro.
Como as rochas se transformam em solos?
 Como as rochas se transformam em solos? Na natureza existe uma tendência ao equilíbrio físico-químico entre as substâncias sólidas, líquidas e gasosas. A maior parte das rochas origina-se em grandes profundidades
Como as rochas se transformam em solos? Na natureza existe uma tendência ao equilíbrio físico-químico entre as substâncias sólidas, líquidas e gasosas. A maior parte das rochas origina-se em grandes profundidades
Resoluções TESTANDO SEUS CONHECIMENTOS. Capítulo 9 QUÍMICA. Ligações químicas. Agora é com você Pág. 58. Agora é com você Pág. 61
 Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 58 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 61 01 a) Por meio da distribuição eletrônica dos átomos que
Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 58 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 61 01 a) Por meio da distribuição eletrônica dos átomos que
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA FMJ
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA FMJ 03. Item C O equador da figura mostrada pode ser representado como abaixo. 01. Item B I Correto. A energia para quebrar a ligação H F (568 kj/mol) é
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA FMJ 03. Item C O equador da figura mostrada pode ser representado como abaixo. 01. Item B I Correto. A energia para quebrar a ligação H F (568 kj/mol) é
CAPÍTULO 2: MINERAIS 2.1. INTRODUÇÃO:
 CAPÍTULO 2: MINERAIS 2.1. INTRODUÇÃO: Apesar do surgimento da mineralogia como ciência ser um fato relativamente recente, pinturas que datam de 5.000 anos já mostravam os seres humanos negociando pedras
CAPÍTULO 2: MINERAIS 2.1. INTRODUÇÃO: Apesar do surgimento da mineralogia como ciência ser um fato relativamente recente, pinturas que datam de 5.000 anos já mostravam os seres humanos negociando pedras
PMT Fundamentos de Ciência e Engenharia dos Materiais 2º semestre de 2014
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais 2º semestre de 2014 ESTRUTURA DOS SÓLIDOS
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais 2º semestre de 2014 ESTRUTURA DOS SÓLIDOS
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS
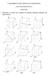 FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
Capítulo 9 TESTANDO SEUS CONHECIMENTOS QUÍMICA. Ligações químicas. Agora é com você Pág. 56. Agora é com você Pág. 59. Agora é com você Pág.
 Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 56 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 59 01 a) Por meio da distribuição eletrônica dos átomos que
Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 56 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 59 01 a) Por meio da distribuição eletrônica dos átomos que
Disciplina: Mineralogia e Tratamento de Minérios. Prof. Gustavo Baldi de Carvalho
 Disciplina: Mineralogia e Tratamento de Minérios Prof. Gustavo Baldi de Carvalho Indústrias: Plásticos Cerâmica Metalúrgica Amplamente utilizado nas indústrias de plásticos, tintas, papel e cosméticos,
Disciplina: Mineralogia e Tratamento de Minérios Prof. Gustavo Baldi de Carvalho Indústrias: Plásticos Cerâmica Metalúrgica Amplamente utilizado nas indústrias de plásticos, tintas, papel e cosméticos,
Materiais cerâmicos. Introdução. Princípios gerais. Estruturas cristalinas. J. D. Santos, FEUP
 Materiais cerâmicos Introdução. Princípios gerais. Estruturas cristalinas. J. D. Santos, FEUP jdsantos@fe.up.pt Ligação química Typical elements in Ceramics 2 Ligação química 3 Conceitos básicos Definição
Materiais cerâmicos Introdução. Princípios gerais. Estruturas cristalinas. J. D. Santos, FEUP jdsantos@fe.up.pt Ligação química Typical elements in Ceramics 2 Ligação química 3 Conceitos básicos Definição
Aula 7: Cristais 0,0,1 1/2,1/2,1/2 0,0,0 0,1/2,0 0,1,0 1/2,1/2,0 1,0,0. Aula 7 - Profa. Adélia
 Aula 7: Cristais Para poder descrever a estrutura cristalina é necessário escolher uma notação para posições, direções e planos As posições são definidas dentro de um cubo com lado unitário. 0,0,1 1/2,1/2,1/2
Aula 7: Cristais Para poder descrever a estrutura cristalina é necessário escolher uma notação para posições, direções e planos As posições são definidas dentro de um cubo com lado unitário. 0,0,1 1/2,1/2,1/2
05 - (UEL PR/1994) Localize na tabela periódica o elemento químico de número atômico 20 e escolha a(s)
 01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
AS LIGAÇÕES QUÍMICAS
 AS LIGAÇÕES QUÍMICAS O QUE SÃO AS LIGAÇÕES QUÍMICAS? São as ligações que se estabelecem entre a união de dois ou mais átomos. Existem três tipos de ligações químicas: A ligação covalente (partilha de elétrons)
AS LIGAÇÕES QUÍMICAS O QUE SÃO AS LIGAÇÕES QUÍMICAS? São as ligações que se estabelecem entre a união de dois ou mais átomos. Existem três tipos de ligações químicas: A ligação covalente (partilha de elétrons)
CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS
 CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS OS DIFERENTES NÍVEIS DE ORGANIZAÇÃO DOS SOLOS Exemplo de diferentes níveis de organização pedológica
CARACTERÍSTICAS FÍSICAS, QUÍMICAS E MINERALÓGICAS TÊM COMO OBJETIVO COMPLEMENTAR AS DESCRIÇÕES MORFOLÓGICAS OS DIFERENTES NÍVEIS DE ORGANIZAÇÃO DOS SOLOS Exemplo de diferentes níveis de organização pedológica
TP064 - CIÊNCIA DOS MATERIAIS PARA EP. FABIANO OSCAR DROZDA
 TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
Ligação iônica = transfere elétrons (um doa outro recebe) 1, 2, 3 e - c.v. 5, 6, 7 e - c.v. Doar e - Receber e - Íon+ Íon - Cl - : NaCl.
 LIGAÇÕES QUÍMICAS Os gases nobres aparecem isolados na natureza, ou seja, são estáveis na forma atômica. Isso ocorre em razão de possuírem 8 elétrons na última camada (exceção do hélio, que possui 2 elétrons
LIGAÇÕES QUÍMICAS Os gases nobres aparecem isolados na natureza, ou seja, são estáveis na forma atômica. Isso ocorre em razão de possuírem 8 elétrons na última camada (exceção do hélio, que possui 2 elétrons
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS
 GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2011-2 Visão Geral 1 2 3 4 5 6 Motivação Matéria Sólida Minerais Grupos de Minerais Identificação dos Minerais Origens: Minerais
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2011-2 Visão Geral 1 2 3 4 5 6 Motivação Matéria Sólida Minerais Grupos de Minerais Identificação dos Minerais Origens: Minerais
Gênese de minerais. Cristalização a partir de gases: bancos de enxôfre em vulcões. Ambientes de formação de minerais
 Gênese de minerais Ciclo de vida dos minerais Cristalização primária e sua história subseqüente Transições estruturais Mudanças na textura (crescimento dos grãos) Processos de exsolução Reações químicas
Gênese de minerais Ciclo de vida dos minerais Cristalização primária e sua história subseqüente Transições estruturais Mudanças na textura (crescimento dos grãos) Processos de exsolução Reações químicas
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS
 GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2012-1 Objetivos Compreender a diferença entre minerais e rochas Apresentar os conceitos químicos que embasam a compreensão do
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2012-1 Objetivos Compreender a diferença entre minerais e rochas Apresentar os conceitos químicos que embasam a compreensão do
estrutura atômica cristalino
 Aula 0b estrutura atômica cristalina ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone estrutura atômica cristalino 1 CRISTAL ESTRUTURA CRISTALINA Muitos
Aula 0b estrutura atômica cristalina ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone estrutura atômica cristalino 1 CRISTAL ESTRUTURA CRISTALINA Muitos
Grupo 1: Metais Alcalinos
 Metais Metais O caráter metálico refere-se às propriedades dos metais (brilhante ou lustroso, maleável e dúctil, os óxidos formam sólidos iônicos básicos e tendem a formar cátions em solução aquosa). O
Metais Metais O caráter metálico refere-se às propriedades dos metais (brilhante ou lustroso, maleável e dúctil, os óxidos formam sólidos iônicos básicos e tendem a formar cátions em solução aquosa). O
Necessária onde a sinterização no estado sólido não é possível (Si 3
 Líquido tem a função de cobrir as partículas dos pós e causar uma rápida densificação a temperaturas mais baixas que as necessárias para a sinterização no estado sólido Necessária onde a sinterização no
Líquido tem a função de cobrir as partículas dos pós e causar uma rápida densificação a temperaturas mais baixas que as necessárias para a sinterização no estado sólido Necessária onde a sinterização no
Formando Cerâmicas Tradicionais Queima. Prof. Ubirajara Pereira Rodrigues Filho
 Formando Cerâmicas Tradicionais Queima Prof. Ubirajara Pereira Rodrigues Filho Queima O tratamento térmico da argila moldada, chamado de queima, pode ser descrito como processo pelo qual os pós cerâmicos
Formando Cerâmicas Tradicionais Queima Prof. Ubirajara Pereira Rodrigues Filho Queima O tratamento térmico da argila moldada, chamado de queima, pode ser descrito como processo pelo qual os pós cerâmicos
Ligações Atômicas e Bandas de Energia. Livro Texto - Capítulo 2
 40 Ligações Atômicas e Bandas de Energia Livro Texto - Capítulo 2 Ligação Atômica 41 Porque estudar a estrutura atômica? As propriedades macroscópicas dos materiais dependem essencialmente do tipo de ligação
40 Ligações Atômicas e Bandas de Energia Livro Texto - Capítulo 2 Ligação Atômica 41 Porque estudar a estrutura atômica? As propriedades macroscópicas dos materiais dependem essencialmente do tipo de ligação
Estrutura Cristalina
 Estrutura Cristalina Para todos os tipos de sólidos (metálicos, iónicos, covalentes ou moleculares), a energia de ligação é máxima para uma distância de equílibrio específica r 0. Um sistema de átomos
Estrutura Cristalina Para todos os tipos de sólidos (metálicos, iónicos, covalentes ou moleculares), a energia de ligação é máxima para uma distância de equílibrio específica r 0. Um sistema de átomos
PERIODICIDADE. Química Geral Augusto Freitas
 PERIODICIDADE Química Geral Augusto Freitas 1 1 A organização da Tabela Periódica As colunas são denominadas Grupos ou Famílias As linhas são denominadas Períodos. 2 1 A organização da Tabela Periódica
PERIODICIDADE Química Geral Augusto Freitas 1 1 A organização da Tabela Periódica As colunas são denominadas Grupos ou Famílias As linhas são denominadas Períodos. 2 1 A organização da Tabela Periódica
