SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I
|
|
|
- Amanda Coradelli Tomé
- 5 Há anos
- Visualizações:
Transcrição
1 SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas
2 2 Ligação química
3 Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100 onde X A e X B são as eletronegatividades dos elementos A e B (A é o elemento mais eletronegativo) Percentual de caráter covalente será: (1 - % de caráter iônico)
4 Caráter iônico e covalente de um cerâmico
5 Caráter iônico e covalente de alguns cerâmicos
6 ESTRUTURA CRISTALINA Suposição: os átomos comportam-se como esferas rígidas Estrutura cristalina: rede de pontos equivalentes aos centros dos átomos (esferas) Número de Coordenação: número de primeiros vizinhos aos quais um determinado átomo está ligado.
7 Cerâmicas: são cristalinos Vidros: Amorfos
8 Sistemas cristalinos
9 Exemplo de estrutura cristalina de materiais metálicos: Cúbica de faces centradas Exemplos: Cr, -Fe, Mo
10 Estruturas hexagonal compacta e Cúbica de faces centradas
11
12 Empacotamento hexagonal compacto 2 átomos por célula unitária (0, 0, 0) (2/3, 1/3, 1/2)
13 Cúbica de faces centradas 4 átomos por célula unitária (0, 0, 0) (0, 1 /2, 1 /2) (1 /2, 0, 1 /2) (1 /2, 1 /2, 0)
14 Interstícios
15
16
17 Interstícios
18 Interstícios em estruturas compactas
19 O número de interstícios nas estruturas baseadas tanto no arranjo hexagonal como no cúbico de faces centradas é o mesmo: CFC: 8 tetraedrais 4 octaedrais HC: 12 tetraedrais 6 octaedrais
20 Estruturas de óxidos As estruturas de óxidos cerâmicos podem ser descritas como cátions localizados em interstícios (ou vazios) tetraedrais ou octaedrais, dentro de arranjos altamente empacotados de ânions, normalmente o oxigênio.
21 Regras de Pauling para formação de sólidos iônicos 1) Os cátions permanecem em contato direto com os ânions. Assim, a razão entre os raios do cátion e do ânion, R C /R A determina o número de coordenação. A estrutura mais estável é aquela que apresenta o maior estado de coordenação permitido.
22
23
24
25 2) A neutralidade elétrica deve ser mantida. Isso significa que a somatória das forças de ligação do ânion (em relação a todos os cátions aos quais está ligado) deve ser igual a valência do ânion. Se definirmos a força de ligação como sendo S = Vc / NC(cátion), essa regra estabelece que Va = S. NC(ânion) e portanto: V a / V c = n a / n c, onde n c e n a são os números de coordenação do cátion e do ânion, respectivamente.
26 Os poliedros de coordenação, que podem ser visualizados como tendo um cátion central, rodeado pelos ânions, comportam-se como unidades discretas.
27 3) Preferencialmente, os poliedros de coordenação unem-se entre si pelos vértices. As uniões feitas pelas faces e lados diminuem a estabilidade da estrutura devido ao aumento da repulsão eletrostática dos cátions centrais. Essa lei baseia-se no fato de que os cátions tendem a maximizar as suas distâncias a fim de se minimizar a repulsão eletrostática entre eles. Devemos observar que, na realidade, os íons não são esferas rígidas. A tendência para polarização (e desvio dos princípios de Pauling) aumenta se o cátion central ou os ânions periféricos são grandes.
28 4) A Regra 3 torna-se mais importante quando o NC é pequeno ou a valência do cátion é grande 5) Estruturas simples são sempre preferíveis à estruturas mais complexas.
29 A energia de ligação (que determina as principais propriedades dos sólidos) depende basicamente dos seguintes fatores: a valência do íon, a distância de equilíbrio, e o arranjo espacial dos átomos (estrutura atômica). Assim, é importante conhecer as classes mais comuns de estruturas atômicas de cerâmicas. Considere-se uma sub-rede de oxigênio em um óxido cerâmico cristalino. A seqüência de empilhamento dos ânions (oxigênio) é ABCABCABCA (no arranjo HCP, é ABABA). Muitos materiais cerâmicos podem ser encaixados nessa estrutura.
30
31 Estrutura cúbica simples Estrutura do cloreto de césio.aplicação das regras de Pauling R(Cl -1 )=0.181 nm R(Cs +1 )=0.167 nm
32 Compostos com estrutura do tipo cloreto de césio são raros pois a razão entre os raios é próxima de 1 e há um grande número de interstícios vazios. Além disso, para que a neutralidade elétrica seja mantida, os poliedros aniônicos devem compartilhar faces, o que é desfavorável do ponto de vista energético.
33 Estruturas cúbicas de faces centradas CFC 1) Estrutura do tipo Sal de Rocha NaCl Essa é a estrutura dos óxidos de Mg, Ca, Sr, Ba, Cd, Mn, Fe, Co, Ni. Ela pode ser visualizada como sendo 2 redes de cátions interpenetrantes, onde todos os sítios OCTAEDRAIS são preenchidos por ânions de oxigênio. Para esse arranjo, r c /r a = to Os materiais cerâmicos dessa família mais conhecidos são MgO e o CaO.
34 Sal de Rocha Como a relação entre os sítios octaedrais e o números de átomos é de 1:1, compostos desse tipo tem estequiomentria MX. Ex.: NiO R(Ni +2 )=0.069 nm R(O +2 )=0.140 nm
35
36
37 Compostos MX octaedrais preenchidos Todos interstícios Metade dos interstícios tetraedrais preenchidos Ex.: Calcule a densidade do MgO
38 Fluorita e Anti-fluorita Compostos cujas estruturas são baseadas em um empacotamento CFC com todos os interstícios tetraedrais preenchidos. Como o número de interstícios tetraedrais é o dobro do número de átomos, a estequiomentria é M 2 X. É o caso, por exemplo, do Li 2 O, Na 2 O e K 2 O. Cada tetraedro divide dois de seus oxigênios com o tetraedro vizinho.
39 Lembrando: o número de interstícios tetraedrais é o dobro do número de átomos no empacotamento CFC. Cada tetraedro divide dois de seus oxigênios com os tetraedros vizinhos.
40 O nome fluorita se dá graças ao mineral fluorita: CaF 2. Óxidos com essa estrutura, como ZrO 2, UO 2 e CeO 2 têm uma grande importância tecnológica devido à aplicações estruturais, elétricas e químicas. Ocorre em compostos binários onde o cátion é grande o suficiente para que haja coordenação octaedral (NC=8). A estrutura baseiase no empacotamento CFC de cátions com os ânions preenchendo todos os interstícios tetraedrais. Pode ser visualizada simplesmente revertendo-se as posições catiônicas e aniônicas da estrutura antifluorita.
41 Fluorita e Anti-fluorita
42 Ex: Li 2 O R(Li +1 )= nm R(O +2 )= nm Os íons de Li são um pouco maiores do que os previstos pela 1 a regra de Pauling, porém o número de sítios octaedrais é insuficiente para acomodar 8 átomos de lítio. Assim, é preferível a ocupação dos sítios tetraedrais.
43 Blenda Óxidos e sulfetos com cátions menores que apresentam coordenação tetraedral tendem a formar essa estrutura, assim como compostos covalentes. Ex.: ZnO, ZnS, BeO SiC, BN, GaAs Somente metade dos sítios tetraedrais estão preenchidos com os cátions bivalentes, para que seja satisfeita a estequiometria MX. Quatro ânions coordenam o cátion (F.L.=2/4). Cada ânion, por sua vez, é coordenado por 4 cátions. Os tetraedros de coordenação dividem somente vértices. Se todos os átomos da estrutura conhecida como blenda forem iguais, obtém-se a estrutura do diamante. Há 4 fórmulas MX por célula unitária.
44
45 Diamante
46 Estruturas baseadas no empacotamento hexagonal A estrutura da wurtzita baseia-se no empacotamento hexagonal compacto, com metade dos sítios tetraedrais ocupada pelos cátions. O número de coordenação de cada íon é 4. Ex.: ZnO ; apenas os interstícios tetraedrais com o ápice voltado para cima são preenchidos. A coordenação dos ânions ao redor dos cátions é 4 e vice-versa, semelhante à estrutura da blenda. Porém, a célula unitária é menor, contendo somente duas fórmulas MX por célula unitária. Ex.: AlN e -SiC
47
48
49 Coríndom Baseado na estequiometria de 2 cátions para 3 ânions, apresentada por esses compostos, os cátions que apresentam coordenação octaedral devem ocupar 2/3 dos interstícios disponíveis. O quociente R c /R A favorece coordenação octaedral. Ex: Al 2 O 3, Fe 2 O 3 e Cr 2 O 3 Verificar a validade da Segunda Regra de Pauling
50
51 Ilmenita e niobato de lítio Ilmenita Ex.: FeTiO 3 : estrutura semelhante à do corundum, porém o Al é substituído por Fe e Ti, em camadas alternadas. F.L.(Fe)=2/6 F.L.(Ti) =4/6 F.L.=2.(2/6)+2.(4/6)= 2
52
53 Niobato de lítio Para o LiNbO 3, cada plano apresenta 2/3 dos sítios octaedrais ocupados por um mesmo número de íons Li e Nb.
54
55 RUTILO Coordenação octaédrica, com os cátions ocupando somente metade dos sítios octaédricos disponíveis. Estrutura quasi-hcp: embora os cátions ocupem metade dos interstícios HCP, a célula unitária resultante é tetragonal. Observando a figura, é possível deduzir que esse arranjo resulta em propriedades de difusão anisotrópicas para alguns cátions. Alguns cátions pequenos são capazes de se difundir intersticialmente através dos sítios octaedrais não-ocupados e, dessa maneira, difundem-se mais rapidamente na direção a.
56
57 Outras estruturas Perovisquita
58 Ti (0, 0, 0); Ca (1/2, 1/2, 1/2); 3O (1/2, 0, 0), (0, 1/2, 0), (0, 0, 1/2) Ca (cuboctaedral) Ti 6-12-coordenado pelos O (octaedral) Força de ligação O: (4xCa + 2xTi) Octaedro de TiO 6 compartilha somente vértices CaO 12 cubooctaedro compartilha faces Exemplos: NaNbO 3, BaTiO 3, CaZrO, YAlO 3, KMgF 3 Muitos desses são ligeiramente assimétricos: ex.: BaTiO 3 é ferroeletrico
59
60
61 Ca 2+ é coordenado por 12 O 2- Ca-O tem f. l. = 2/12 = 1/6 Ti 4+ é coordenado por 6 O 2- Ti-O tem f. l. = 4/6 = 2/3 {Verde = Ca; Azul = Ti; Vermelho = O} O 2- tem valência total=2, satisfeita por {4xCa 2+ (1/6)}+{2xTi 4+ (2/3)}
62 Estrutura de supercondutores
63
64 YBa 2 Cu 3 O 7 - the 1:2:3 Supercondutor
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I
 SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
Estruturas baseadas na HC Wurtzita ZnS
 Estruturas baseadas na HC Wurtzita ZnS Baseada num arranjo HC dos ânions com metade dos interstícios tetraedrais ocupados por cátions O número de coordenação de cada íon é 4 Se somente a metade das posições
Estruturas baseadas na HC Wurtzita ZnS Baseada num arranjo HC dos ânions com metade dos interstícios tetraedrais ocupados por cátions O número de coordenação de cada íon é 4 Se somente a metade das posições
Estrutura de cristais iônicos. Regras de Pauling
 Estrutura de cristais iônicos Regras de Pauling Estabilidade energética Por que os íons preferem ficar juntos, formando um cristal, do que moléculas isoladas? formar A Constante de Madelung é uma definição
Estrutura de cristais iônicos Regras de Pauling Estabilidade energética Por que os íons preferem ficar juntos, formando um cristal, do que moléculas isoladas? formar A Constante de Madelung é uma definição
Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas
 Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas Prof. Dr. André Luiz Molisani Curso de Engenharia de Materiais e-mail: andre.molisani@fsa.br 2017 1 MATERIAL RECOMENDADO PARA ESTUDO: Capítulo
Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas Prof. Dr. André Luiz Molisani Curso de Engenharia de Materiais e-mail: andre.molisani@fsa.br 2017 1 MATERIAL RECOMENDADO PARA ESTUDO: Capítulo
Materiais Cerâmicos Estruturas Cristalinas. Conceitos Gerais
 Materiais Cerâmicos Estruturas Cristalinas Conceitos Gerais CHOCOLATE O chocolate, quando fica na geladeira costuma formar uma camada branca na superfície: O que você acha que pode ser? (a) Mofo? (b) Precipitados
Materiais Cerâmicos Estruturas Cristalinas Conceitos Gerais CHOCOLATE O chocolate, quando fica na geladeira costuma formar uma camada branca na superfície: O que você acha que pode ser? (a) Mofo? (b) Precipitados
Sólidos iônicos. Química Geral. Prof. Edson Nossol
 Sólidos iônicos Química Geral Prof. Edson Nossol Uberlândia, 07/10/2016 Sólido cristalino: possui ordem a longa distância: átomos, moléculas ou íons ocupam posições específicas Sólido não-cristalino: não
Sólidos iônicos Química Geral Prof. Edson Nossol Uberlândia, 07/10/2016 Sólido cristalino: possui ordem a longa distância: átomos, moléculas ou íons ocupam posições específicas Sólido não-cristalino: não
ESTRUTURA DOS SÓLIDOS CRISTALINOS. Mestranda: Marindia Decol
 ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
A4 Estrutura cristalina perfeição
 A4 Estrutura cristalina perfeição TEM Muitos dos materiais aplicados em engenharia têm estrutura cristalina: os átomos do material estão dispostos de modo regular e repetitivo Estrutura cristalina A célula
A4 Estrutura cristalina perfeição TEM Muitos dos materiais aplicados em engenharia têm estrutura cristalina: os átomos do material estão dispostos de modo regular e repetitivo Estrutura cristalina A célula
Física do Estado Sólido
 Física do Estado Sólido 2003-2004 Folha 3 - Estruturas cristalinas. Indique a rede subjacente aos desenhos da fig.. Encontre três conjuntos distintos de vectores fundamentais primitivos para cada um dos
Física do Estado Sólido 2003-2004 Folha 3 - Estruturas cristalinas. Indique a rede subjacente aos desenhos da fig.. Encontre três conjuntos distintos de vectores fundamentais primitivos para cada um dos
Estruturas Cristalinas Comuns em Cerâmicas
 Estruturas Cristalinas Comuns em Cerâmicas Prof. Dr. Ubirajara Pereira Rodrigues Filho Ligações Químicas em Cerâmicas Predominatemente Covalentes BN Predominantemente Iônicas BeO Geralmente, sólidos iônicos
Estruturas Cristalinas Comuns em Cerâmicas Prof. Dr. Ubirajara Pereira Rodrigues Filho Ligações Químicas em Cerâmicas Predominatemente Covalentes BN Predominantemente Iônicas BeO Geralmente, sólidos iônicos
Estrutur Es a trutur e Propriedades Pr dos materiais cerâmicos
 Estrutura e Propriedades dos materiais cerâmicos Fator de Empacotamento Atômico: FEA R a atoms unit cell FEA = 0,68 APF = Close-packed directions: length = 4R = 3 a Unit cell contains: 1 + 8 x 1/8 = 2
Estrutura e Propriedades dos materiais cerâmicos Fator de Empacotamento Atômico: FEA R a atoms unit cell FEA = 0,68 APF = Close-packed directions: length = 4R = 3 a Unit cell contains: 1 + 8 x 1/8 = 2
Estrutura Cristalina dos Sólidos (Arranjos Atômicos)
 Estrutura Cristalina dos Sólidos (Arranjos Atômicos) INTRODUÇÃO As propriedades dos materiais dependem dos arranjos dos seus átomos. Esses arranjos podem ser classificados em: Estruturas moleculares: agrupamento
Estrutura Cristalina dos Sólidos (Arranjos Atômicos) INTRODUÇÃO As propriedades dos materiais dependem dos arranjos dos seus átomos. Esses arranjos podem ser classificados em: Estruturas moleculares: agrupamento
Estrutura Cristalina
 Estrutura Cristalina Para todos os tipos de sólidos (metálicos, iónicos, covalentes ou moleculares), a energia de ligação é máxima para uma distância de equílibrio específica r 0. Um sistema de átomos
Estrutura Cristalina Para todos os tipos de sólidos (metálicos, iónicos, covalentes ou moleculares), a energia de ligação é máxima para uma distância de equílibrio específica r 0. Um sistema de átomos
Os materiais no estado sólido ocupam geralmente menos volume que no estado líquido (fundido).
 Instituto de Ciência e Tecnologia de Sorocaba Materiais e Reciclagem 3 Arranjo Atômico e Cristalografia Professor Sandro Donnini Mancini Sorocaba, Fevereiro de 2018. Os materiais no estado sólido ocupam
Instituto de Ciência e Tecnologia de Sorocaba Materiais e Reciclagem 3 Arranjo Atômico e Cristalografia Professor Sandro Donnini Mancini Sorocaba, Fevereiro de 2018. Os materiais no estado sólido ocupam
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais. Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais
Ciências dos materiais- 232
 1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
Professora: Daniela Becker Mestranda: Jéssica de Aguiar
 Professora: Daniela Becker Mestranda: Jéssica de Aguiar JOINVILLE SC BRASIL 2016 Estruturas Cerâmicas São compostas por pelo menos dois elementos; Em geral são mais complexas do que a dos metais; Ex.:
Professora: Daniela Becker Mestranda: Jéssica de Aguiar JOINVILLE SC BRASIL 2016 Estruturas Cerâmicas São compostas por pelo menos dois elementos; Em geral são mais complexas do que a dos metais; Ex.:
PROPRIEDADES DOS SÓLIDOS ESTRUTURA E TIPO DE LIGAÇÕES
 PROPRIEDADES DOS SÓLIDOS ESTRUTURA E TIPO DE LIGAÇÕES 1 REPRESENTAÇÃO Diferentes estados da matéria gás pouca ordem, movimentos rápidos. Sólido cristalino altamente ordenado líquido polar mais ordenado,
PROPRIEDADES DOS SÓLIDOS ESTRUTURA E TIPO DE LIGAÇÕES 1 REPRESENTAÇÃO Diferentes estados da matéria gás pouca ordem, movimentos rápidos. Sólido cristalino altamente ordenado líquido polar mais ordenado,
30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
 IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
Centro Universitário da Fundação Educacional de Barretos. Princípio de Ciências dos Materiais Prof.: Luciano H. de Almeida
 Centro Universitário da Fundação Educacional de Barretos Princípio de Ciências dos Materiais Prof.: Luciano H. de Almeida Porque estudar estrutura atômica? Ligação atômica e as propriedades dos materiais
Centro Universitário da Fundação Educacional de Barretos Princípio de Ciências dos Materiais Prof.: Luciano H. de Almeida Porque estudar estrutura atômica? Ligação atômica e as propriedades dos materiais
Propriedades dos sólidos metálicos. C. E. Housecroft, cap. 6
 C. E. Housecroft, cap. 6 O caráter metálico refere-se às propriedades dos metais (brilhante ou lustroso, maleável e dúctil, os óxidos formam sólidos iônicos básicos e tendem a formar cátions em solução
C. E. Housecroft, cap. 6 O caráter metálico refere-se às propriedades dos metais (brilhante ou lustroso, maleável e dúctil, os óxidos formam sólidos iônicos básicos e tendem a formar cátions em solução
Fotografia de vários cristais de fluorita CaF 2 3-0
 Arranjos Atômicos Fotografia de vários cristais de fluorita CaF 2 3-0 Conceito de Cristalinidade Cristalinidade corresponde a forma de organização da estrutura em um modelo ordenado e repetitivo de longo
Arranjos Atômicos Fotografia de vários cristais de fluorita CaF 2 3-0 Conceito de Cristalinidade Cristalinidade corresponde a forma de organização da estrutura em um modelo ordenado e repetitivo de longo
Ligações Químicas. Ligações iônicas Polarização e sólidos iônicos Ligação covalente Estrutura de Lewis Carga formal
 Ligações Químicas Ligações iônicas Polarização e sólidos iônicos Ligação covalente Estrutura de Lewis Carga formal Estrutura molecular As propriedades físicas dos elementos (como o raio, a energia de ionização
Ligações Químicas Ligações iônicas Polarização e sólidos iônicos Ligação covalente Estrutura de Lewis Carga formal Estrutura molecular As propriedades físicas dos elementos (como o raio, a energia de ionização
Estrutura de Sólidos Cristalinos. Profa. Dra Daniela Becker
 Estrutura de Sólidos Cristalinos Profa. Dra Daniela Becker Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
Estrutura de Sólidos Cristalinos Profa. Dra Daniela Becker Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03 CMA CIÊNCIA DOS MATERIAIS 2º Semestre de 2014 Prof.
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03 CMA CIÊNCIA DOS MATERIAIS 2º Semestre de 2014 Prof.
Ligação metálica corrente elétrica
 Ligações Metálicas Ligação metálica É o tipo de ligação que ocorre entre os átomos de metais. Quando muitos destes átomos estão juntos num cristal metálico, estes perdem seus elétrons da última camada.
Ligações Metálicas Ligação metálica É o tipo de ligação que ocorre entre os átomos de metais. Quando muitos destes átomos estão juntos num cristal metálico, estes perdem seus elétrons da última camada.
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2016 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2016 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
CAP.13 MATERIAIS CERÂMICOS
 CAP.13 MATERIAIS CERÂMICOS Smith cap 10 13. 1 13. 2 MATERIAIS CERÂMICOS São materiais inorgânicos não metálicos. Constituídos por elementos metálicos e nãometálicos, ligados quimicamente entre si. Ligações:
CAP.13 MATERIAIS CERÂMICOS Smith cap 10 13. 1 13. 2 MATERIAIS CERÂMICOS São materiais inorgânicos não metálicos. Constituídos por elementos metálicos e nãometálicos, ligados quimicamente entre si. Ligações:
Sólidos: Estudo de Estruturas Cristalinas
 UnB - Universidade de Brasília IQD - Instituto de Química Curso de Graduação Disciplina: Química Inorgânica 1 Experimental (Código 114073) Sólidos: Estudo de Estruturas Cristalinas A estrutura dos materiais
UnB - Universidade de Brasília IQD - Instituto de Química Curso de Graduação Disciplina: Química Inorgânica 1 Experimental (Código 114073) Sólidos: Estudo de Estruturas Cristalinas A estrutura dos materiais
Ciência dos materiais Aula 3. Profª Mª Patrícia Cristina Costa Ladeira
 Ciência dos materiais Aula 3 Profª Mª Patrícia Cristina Costa Ladeira patricia.ladeira@educadores.net.br patricia.ladeira@yahoo.com.br Recapitulando 2 Na Unidade 1 nós vimos: Aspectos históricos da Ciência
Ciência dos materiais Aula 3 Profª Mª Patrícia Cristina Costa Ladeira patricia.ladeira@educadores.net.br patricia.ladeira@yahoo.com.br Recapitulando 2 Na Unidade 1 nós vimos: Aspectos históricos da Ciência
ESTRUTURA CRISTALINA DOS MATERIAIS CERÂMICOS
 ESTRUTURA CRISTALINA DOS MATERIAIS CERÂMICOS PMT5783 Samuel M. Toffoli Antonio Carlos Vieira Coelho PMT EPUSP 2014 ESTRUTURA DOS MATERIAIS CERÂMICOS Referência Bibliográfica: Chiang, Y.-M.; Birnie, D.P.;
ESTRUTURA CRISTALINA DOS MATERIAIS CERÂMICOS PMT5783 Samuel M. Toffoli Antonio Carlos Vieira Coelho PMT EPUSP 2014 ESTRUTURA DOS MATERIAIS CERÂMICOS Referência Bibliográfica: Chiang, Y.-M.; Birnie, D.P.;
Física da Matéria Condensada
 Física da Matéria Condensada II Redes e estruturas cristalinas 1. Indique a rede subjacente aos desenhos das figuras 1 e 2. Encontre três conjuntos de vectores fundamentais primitivos para a fig. 1 e dois
Física da Matéria Condensada II Redes e estruturas cristalinas 1. Indique a rede subjacente aos desenhos das figuras 1 e 2. Encontre três conjuntos de vectores fundamentais primitivos para a fig. 1 e dois
Aula 6: Estrutura Cristalina dos Metais
 Aula 6: Estrutura Cristalina dos Metais - Como a ligação metálica é não-direcional, não há restrições quanto ao número e posições dos vizinhos mais próximos. - A estrutura cristalina dos metais têm um
Aula 6: Estrutura Cristalina dos Metais - Como a ligação metálica é não-direcional, não há restrições quanto ao número e posições dos vizinhos mais próximos. - A estrutura cristalina dos metais têm um
ORDEM. Periocidade. SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico de átomos, moléculas ou iões, formando uma estrutura cristalina regular
 Capítulo I ESTRUTURA CRISTALINA DE SÓLIDOS ORDEM curto alcance médio alcance longo alcance Periocidade unidimensional bidimensional tridimensional SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico
Capítulo I ESTRUTURA CRISTALINA DE SÓLIDOS ORDEM curto alcance médio alcance longo alcance Periocidade unidimensional bidimensional tridimensional SÓLIDO CRISTALINO OU CRISTAL agregado ordenado e periódico
ARRANJOS ATÔMICOS. Química Aplicada. Profº Vitor de Almeida Silva
 ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
Física dos Materiais FMT0502 ( )
 Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Estrutura de silicatos
 Estrutura de silicatos Tetraedros de SiO 2. ângulo de 109,2 o. O silício ocupa o centro do tetraedro e os oxigênios, os vértices do tetraedro Silicatos Átomos de silício e oxigênio Cadeias estruturais
Estrutura de silicatos Tetraedros de SiO 2. ângulo de 109,2 o. O silício ocupa o centro do tetraedro e os oxigênios, os vértices do tetraedro Silicatos Átomos de silício e oxigênio Cadeias estruturais
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS
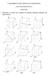 FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA - DQMC. Estrutura Interna. Prof Karine P.
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA - DQMC Estrutura Interna Prof Karine P. Naidek Estrutura Cristalina Os materiais sólidos podem ser classificados
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA - DQMC Estrutura Interna Prof Karine P. Naidek Estrutura Cristalina Os materiais sólidos podem ser classificados
Sólidos iônicos. Classificações de solidos iônicos pela razão radial razão radial = raio do íon menor dividido pelo raio do íon maior
 Sólidos iônicos Sólidos iônicos são construídos pela atração mútua de cátions a ânions. Sólidos reticulares consistem de átomos ligados aos seus vizinhos covalentemente através da extensão do sólido. Sólidos
Sólidos iônicos Sólidos iônicos são construídos pela atração mútua de cátions a ânions. Sólidos reticulares consistem de átomos ligados aos seus vizinhos covalentemente através da extensão do sólido. Sólidos
Informações estruturais de compostos iônicos. Arranjos entre os íons dos compostos iônicos.
 Arranjos entre os íons dos compostos iônicos. a Tendências gerais para os raios iônicos na tabela periódica: 1- Os raios iônicos aumentam para baixo em um grupo (coluna) na T.P. 2- Os raios dos íons de
Arranjos entre os íons dos compostos iônicos. a Tendências gerais para os raios iônicos na tabela periódica: 1- Os raios iônicos aumentam para baixo em um grupo (coluna) na T.P. 2- Os raios dos íons de
Ligações químicas e estrutura dos materiais
 Disciplina : - MFI Professores: Guilherme Ourique Verran - Dr. Eng. Metalúrgica Aula 02 Revisão de alguns conceitos fundamentais da Ciência dos Materiais Ligações químicas e estrutura dos materiais Conceitos
Disciplina : - MFI Professores: Guilherme Ourique Verran - Dr. Eng. Metalúrgica Aula 02 Revisão de alguns conceitos fundamentais da Ciência dos Materiais Ligações químicas e estrutura dos materiais Conceitos
Resoluções TESTANDO SEUS CONHECIMENTOS. Capítulo 9 QUÍMICA. Ligações químicas. Agora é com você Pág. 58. Agora é com você Pág. 61
 Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 58 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 61 01 a) Por meio da distribuição eletrônica dos átomos que
Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 58 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 61 01 a) Por meio da distribuição eletrônica dos átomos que
Introdução a Engenharia e Ciência dos Materiais
 Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
 Ligações Químicas Por que os átomos formam ligações químicas? Distância de equilíbrio Comprimento da ligação H-H r o = 74 pm distância internuclear Uma ligação química entre dois átomos é formada se
Ligações Químicas Por que os átomos formam ligações químicas? Distância de equilíbrio Comprimento da ligação H-H r o = 74 pm distância internuclear Uma ligação química entre dois átomos é formada se
LIGAÇÃO IÔNICA Resulta da atração eletrostática de íons com cargas opostas
 LIGAÇÃO IÔNICA Resulta da atração eletrostática de íons com cargas opostas NaCl(s) tem energia menor do que os átomos gasosos isolados Na(g) e Cl(g) 3 etapas hipotéticas: kj/mol 1) Na (g) Na + (g) + e
LIGAÇÃO IÔNICA Resulta da atração eletrostática de íons com cargas opostas NaCl(s) tem energia menor do que os átomos gasosos isolados Na(g) e Cl(g) 3 etapas hipotéticas: kj/mol 1) Na (g) Na + (g) + e
Defeitos em Cristais Iônicos. Prof Ubirajara Pereira Rodrigues Filho
 Defeitos em Cristais Iônicos Prof Ubirajara Pereira Rodrigues Filho Defeitos Os defeitos perturbam a ordem a longa distância da rede cristalina e afetam as propriedades dos compostos cristalinos que dependem
Defeitos em Cristais Iônicos Prof Ubirajara Pereira Rodrigues Filho Defeitos Os defeitos perturbam a ordem a longa distância da rede cristalina e afetam as propriedades dos compostos cristalinos que dependem
05 - (UEL PR/1994) Localize na tabela periódica o elemento químico de número atômico 20 e escolha a(s)
 01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
01 - (UEM PR/2012) Assinale o que for correto. (01) Dentro de uma família na tabela periódica, todos os elementos químicos têm temperatura de fusão aumentada com o aumento do número atômico. (02) Qualquer
PERIODICIDADE. Química Geral Augusto Freitas
 PERIODICIDADE Química Geral Augusto Freitas 1 1 A organização da Tabela Periódica As colunas são denominadas Grupos ou Famílias As linhas são denominadas Períodos. 2 1 A organização da Tabela Periódica
PERIODICIDADE Química Geral Augusto Freitas 1 1 A organização da Tabela Periódica As colunas são denominadas Grupos ou Famílias As linhas são denominadas Períodos. 2 1 A organização da Tabela Periódica
Ciência dos Materiais Estrutura Cristalina Difração de raios X. Professora: Maria Ismenia Sodero
 Ciência dos Materiais Estrutura Cristalina Difração de raios X Professora: Maria Ismenia Sodero maria.ismenia@usp.br Assuntos abordados Coordenação atômica Arranjo das estruturas sólidas: cristalinos ou
Ciência dos Materiais Estrutura Cristalina Difração de raios X Professora: Maria Ismenia Sodero maria.ismenia@usp.br Assuntos abordados Coordenação atômica Arranjo das estruturas sólidas: cristalinos ou
Sólidos. Prof. Fernando R. Xavier
 Sólidos Prof. Fernando R. Xavier UDESC 2015 Sólidos Sob um aspecto simples e prático, é dito sólido o estado da matéria onde seu volume e forma são bem definidos. Dentro de um sólido, os átomos ou moléculas
Sólidos Prof. Fernando R. Xavier UDESC 2015 Sólidos Sob um aspecto simples e prático, é dito sólido o estado da matéria onde seu volume e forma são bem definidos. Dentro de um sólido, os átomos ou moléculas
Capítulo 9 TESTANDO SEUS CONHECIMENTOS QUÍMICA. Ligações químicas. Agora é com você Pág. 56. Agora é com você Pág. 59. Agora é com você Pág.
 Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 56 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 59 01 a) Por meio da distribuição eletrônica dos átomos que
Resoluções Capítulo 9 Ligações químicas Agora é com você Pág. 56 01 X: 6s X + 5 Y = 4s 4p Y 1 + 1 1 [ X ][ Y ][ Y ] XY Agora é com você Pág. 59 01 a) Por meio da distribuição eletrônica dos átomos que
MATERIAIS CERÂMICOS E POLIMÉRICOS
 MATERIAIS CERÂMICOS E POLIMÉRICOS Curso: Engenharia Mecânica - Terceiro Semestre Letivo Período: Primeiro Semestre 2010 Carga Horária: 60 horas Docente: Prof. Dr. Wagner M. Pachekoski MATERIAIS CERÂMICOS:
MATERIAIS CERÂMICOS E POLIMÉRICOS Curso: Engenharia Mecânica - Terceiro Semestre Letivo Período: Primeiro Semestre 2010 Carga Horária: 60 horas Docente: Prof. Dr. Wagner M. Pachekoski MATERIAIS CERÂMICOS:
MATERIAIS CERÂMICOS. Curso: Engenharia de Produção / Engenharia Civil 1. ESTRUTURAS E PROPRIEDADES DE CERÂMICAS
 Curso: Engenharia de Produção / Engenharia Civil MATERIAIS CERÂMICOS 1. ESTRUTURAS E PROPRIEDADES DE CERÂMICAS Materiais cerâmicos são materiais inorgânicos e não-metálicos. A maioria dos materiais cerâmicos
Curso: Engenharia de Produção / Engenharia Civil MATERIAIS CERÂMICOS 1. ESTRUTURAS E PROPRIEDADES DE CERÂMICAS Materiais cerâmicos são materiais inorgânicos e não-metálicos. A maioria dos materiais cerâmicos
Materiais cerâmicos. Introdução. Princípios gerais. Estruturas cristalinas. J. D. Santos, FEUP
 Materiais cerâmicos Introdução. Princípios gerais. Estruturas cristalinas. J. D. Santos, FEUP jdsantos@fe.up.pt Ligação química Typical elements in Ceramics 2 Ligação química 3 Conceitos básicos Definição
Materiais cerâmicos Introdução. Princípios gerais. Estruturas cristalinas. J. D. Santos, FEUP jdsantos@fe.up.pt Ligação química Typical elements in Ceramics 2 Ligação química 3 Conceitos básicos Definição
Principais Tipos de Ligações Químicas. Iônicas Covalentes Metálicas
 Principais Tipos de Ligações Químicas Iônicas Covalentes Metálicas Principais Tipos de Ligações Químicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações de Lewis Numa
Principais Tipos de Ligações Químicas Iônicas Covalentes Metálicas Principais Tipos de Ligações Químicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações de Lewis Numa
TP064 - CIÊNCIA DOS MATERIAIS PARA EP. FABIANO OSCAR DROZDA
 TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
Ligações Químicas. Professor Haroldo
 Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
Cursos Profissionais-Física e Química 10º ano
 3.1.4. Parâmetros da ligação covalente A. O comprimento da ligação nas moléculas diatómicas Como já se referiu, quando os átomos se aproximam formando ligações dão origem a uma nova unidade estrutural-
3.1.4. Parâmetros da ligação covalente A. O comprimento da ligação nas moléculas diatómicas Como já se referiu, quando os átomos se aproximam formando ligações dão origem a uma nova unidade estrutural-
CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS
 CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO ESTABILIZAÇÃO DO AMETAL LIGAÇÃO IÔNICA
CONFIGURAÇÃO DOS GASES NOBRES ÁTOMOS ESTÁVEIS E ISOLADOS CONCEITO DE LIGAÇÃO IÔNICA UNIÃO ENTRE ÁTOMOS METÁLICOS E AMETÁLICOS OXIDAÇÃO ESTABILIZAÇÃO DO METAL REDUÇÃO ESTABILIZAÇÃO DO AMETAL LIGAÇÃO IÔNICA
Introdução aos Materiais Imperfeições em Sólidos Metais DEMEC TM229 Prof Adriano Scheid
 Introdução aos Materiais Imperfeições em Sólidos Metais DEMEC TM229 Prof Adriano Scheid Introdução Os sólidos contém inúmeras imperfeições nas estruturas cristalinas e muitas propriedades são alteradas
Introdução aos Materiais Imperfeições em Sólidos Metais DEMEC TM229 Prof Adriano Scheid Introdução Os sólidos contém inúmeras imperfeições nas estruturas cristalinas e muitas propriedades são alteradas
COMPOSTOS IÓNICOS A-B
 COMPOSTOS IÓNICOS AB B (baixa E i, logo baixa χ) B B A (alta E i, logo alta χ) 1s 1 Hidrogénio i Metalóides 1s 2 1s 2 Metais alcalinos Não metais 1s 2 2s 1 1s 2 2s 2 Metais alcalino terrosos Gases raros
COMPOSTOS IÓNICOS AB B (baixa E i, logo baixa χ) B B A (alta E i, logo alta χ) 1s 1 Hidrogénio i Metalóides 1s 2 1s 2 Metais alcalinos Não metais 1s 2 2s 1 1s 2 2s 2 Metais alcalino terrosos Gases raros
Click to edit Master title style
 Ligação iónica A ligação química em sólidos iónicos é frequentemente discutida em termos do modelo iónico de Goldshmidt: os iões são esferas carregadas, incompressíveis e não polarizáveis Pode ser usado
Ligação iónica A ligação química em sólidos iónicos é frequentemente discutida em termos do modelo iónico de Goldshmidt: os iões são esferas carregadas, incompressíveis e não polarizáveis Pode ser usado
Ligações Químicas. Ligações Químicas. Sólidos. Como os átomos se combinam e quais as forças que os mantêm unidos?
 Ligações Químicas Como os átomos se combinam e quais as forças que os mantêm unidos? Estudaremos as ligações entre os átomos com base em suas estruturas eletrônicas e periodicidade. Para ilustrar os diferentes
Ligações Químicas Como os átomos se combinam e quais as forças que os mantêm unidos? Estudaremos as ligações entre os átomos com base em suas estruturas eletrônicas e periodicidade. Para ilustrar os diferentes
Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais
 Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
FÍSICA DA MATÉRIA CONDENSADA 2009/10 Folha 1 I Redes e Estruturas Cristalinas
 FÍSICA DA MATÉRIA CONDENSADA 2009/10 Folha 1 I Redes e Estruturas Cristalinas 1 - Indicar a rede subjacente aos desenhos das figuras la) e lb). Encontrar três conjuntos de vectores fundamentais primitivos
FÍSICA DA MATÉRIA CONDENSADA 2009/10 Folha 1 I Redes e Estruturas Cristalinas 1 - Indicar a rede subjacente aos desenhos das figuras la) e lb). Encontrar três conjuntos de vectores fundamentais primitivos
Sólidos metálicos. Fe Hg
 Sólidos metálicos Fe Hg Quais são? Metalóides Não-metais Metais Sólidos metálicos partilha de e - s por muitos átomos iguais (muitos átomos e poucos electrões). Energias de ionização baixas. Propriedades
Sólidos metálicos Fe Hg Quais são? Metalóides Não-metais Metais Sólidos metálicos partilha de e - s por muitos átomos iguais (muitos átomos e poucos electrões). Energias de ionização baixas. Propriedades
Teoria das Bandas. Energia de Coesão e Propriedades. Grau de preenchimento da banda vs. Ordem de ligação
 Sumário 13 Metais 1 Teoria das Bandas. Energia de Coesão e Propriedades Hidrogénio metálico TOM/CLOA aplicada aos metais Energia de coesão vs. Energia de ligação Grau de preenchimento da banda vs. Ordem
Sumário 13 Metais 1 Teoria das Bandas. Energia de Coesão e Propriedades Hidrogénio metálico TOM/CLOA aplicada aos metais Energia de coesão vs. Energia de ligação Grau de preenchimento da banda vs. Ordem
Ligações Químicas elementos químicos átomos moléculas
 Ligações Químicas Ligações Químicas Os diferentes elementos químicos combinam-se de várias maneiras formando uma grande variedade de substâncias, por meio das ligações químicas. Através das ligações químicas
Ligações Químicas Ligações Químicas Os diferentes elementos químicos combinam-se de várias maneiras formando uma grande variedade de substâncias, por meio das ligações químicas. Através das ligações químicas
estrutura atômica cristalino
 Aula 0b estrutura atômica cristalina ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone estrutura atômica cristalino 1 CRISTAL ESTRUTURA CRISTALINA Muitos
Aula 0b estrutura atômica cristalina ZEA 1038 Ciência e Tecnologia dos Materiais Prof. João Adriano Rossignolo Profa. Eliria M.J.A. Pallone estrutura atômica cristalino 1 CRISTAL ESTRUTURA CRISTALINA Muitos
Ligação iônica = transfere elétrons (um doa outro recebe) 1, 2, 3 e - c.v. 5, 6, 7 e - c.v. Doar e - Receber e - Íon+ Íon - Cl - : NaCl.
 LIGAÇÕES QUÍMICAS Os gases nobres aparecem isolados na natureza, ou seja, são estáveis na forma atômica. Isso ocorre em razão de possuírem 8 elétrons na última camada (exceção do hélio, que possui 2 elétrons
LIGAÇÕES QUÍMICAS Os gases nobres aparecem isolados na natureza, ou seja, são estáveis na forma atômica. Isso ocorre em razão de possuírem 8 elétrons na última camada (exceção do hélio, que possui 2 elétrons
Regra do Octeto: (Lewis e Koosel)
 Ligações Químicas Regra do Octeto: (Lewis e Koosel) Um átomo estará estável quando sua última camada possuir 8 elétrons (ou 2, caso se trate da camada K). Os átomos não estáveis unem-se uns aos outros
Ligações Químicas Regra do Octeto: (Lewis e Koosel) Um átomo estará estável quando sua última camada possuir 8 elétrons (ou 2, caso se trate da camada K). Os átomos não estáveis unem-se uns aos outros
Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1. Estruturas dos sólidos cristalinos
 Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1 Estruturas dos sólidos cristalinos 1º semestre / 2016 Estruturas dos sólidos cristalinos
Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1 Estruturas dos sólidos cristalinos 1º semestre / 2016 Estruturas dos sólidos cristalinos
Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais
 Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Ligações Químicas Ligações Interatômicas: IÔNICA = metal + não-metal COVALENTE = não-metais METÁLICA = metais Ligação iônica Transferência de elétrons de um átomo para outro Íons de cargas opostas Forças
Temática: Teoria das ligações químicas e estrutura dos complexos e quelatos
 Aula: 14 Temática: Teoria das ligações químicas e estrutura dos complexos e quelatos Teoria das ligações químicas e estrutura dos complexos e quelatos. Verifica-se que a estrutura dos complexos e quelatos
Aula: 14 Temática: Teoria das ligações químicas e estrutura dos complexos e quelatos Teoria das ligações químicas e estrutura dos complexos e quelatos. Verifica-se que a estrutura dos complexos e quelatos
LIGAÇÕES QUÍMICAS. Prof. Marcel Piovezan. Curso Superior de Tecnologia em Processos Químicos
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES LIGAÇÕES QUÍMICAS Prof. Marcel Piovezan marcel.piovezan@ifsc.edu.br
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES LIGAÇÕES QUÍMICAS Prof. Marcel Piovezan marcel.piovezan@ifsc.edu.br
QUÍMICA, 9º Ano do Ensino Fundamental LIGAÇÕES QUÍMICAS. Ligações Químicas
 QUÍMICA, 9º Ano do Ensino Fundamental LIGAÇÕES QUÍMICAS Ligações Químicas Em que consiste a ligação entre dois átomos? Por que o diamante é duro e o sal não, se ambos são cristais? Eles possuem ligações
QUÍMICA, 9º Ano do Ensino Fundamental LIGAÇÕES QUÍMICAS Ligações Químicas Em que consiste a ligação entre dois átomos? Por que o diamante é duro e o sal não, se ambos são cristais? Eles possuem ligações
Ligações Químicas. No hidrônio, quantos pares de elétrons pertencem, no total, tanto ao hidrogênio quanto ao oxigênio? a) 1 b) 2 c) 3 d) 4 e) 6
 Aluno(a): Prof.: Éderson Ligações Químicas Questão 1) Abaixo temos as fórmulas de Lewis para átomos de cinco elementos químicos. Fórmulas eletrônicas de Lewis para alguns elementos Podemos afirmar que
Aluno(a): Prof.: Éderson Ligações Químicas Questão 1) Abaixo temos as fórmulas de Lewis para átomos de cinco elementos químicos. Fórmulas eletrônicas de Lewis para alguns elementos Podemos afirmar que
SOLIDOS METÁLICOS E SÓLIDOS IÔNICOS
 SOLIDOS METÁLICOS E SÓLIDOS IÔNICOS GASES e LÍQUIDOS: As moléculas têm movimentos contínuos e aleatórios e também giram e vibram, portanto não têm disposição organizada alonga distância. SÓLIDOS: As moléculas,
SOLIDOS METÁLICOS E SÓLIDOS IÔNICOS GASES e LÍQUIDOS: As moléculas têm movimentos contínuos e aleatórios e também giram e vibram, portanto não têm disposição organizada alonga distância. SÓLIDOS: As moléculas,
Ligações Químicas. Profª. Ms. Loraine Cristina do Valle Jacobs DAQBI.
 Ligações Químicas Profª. Ms. Loraine Cristina do Valle Jacobs lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs DAQBI LIGAÇÕES QUÍMICAS A partir do desenvolvimento da mecânica
Ligações Químicas Profª. Ms. Loraine Cristina do Valle Jacobs lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs DAQBI LIGAÇÕES QUÍMICAS A partir do desenvolvimento da mecânica
Tabela periódica e ligações química
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace Tabela periódica e ligações química Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Orbitais e números quânticos:
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace Tabela periódica e ligações química Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Orbitais e números quânticos:
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Propriedades da tabela periódica
 Propriedades da tabela periódica Química Geral Prof. Edson Nossol Uberlândia, 30/09/2016 calcogênioos halogênios Metais alcalinos Metais alcalinos terrosos Gases nobres Metais de transição Dimitris Mendeliev
Propriedades da tabela periódica Química Geral Prof. Edson Nossol Uberlândia, 30/09/2016 calcogênioos halogênios Metais alcalinos Metais alcalinos terrosos Gases nobres Metais de transição Dimitris Mendeliev
QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula /
 QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO QUÍMICA É A FORÇA QUE MANTÉM ÁTOMOS E/OU ÍONS UNIDOS NAS
QUI109 QUÍMICA GERAL (Ciências Biológicas) 7ª aula / 2016-2 Prof. Mauricio X. Coutrim (disponível em: http://professor.ufop.br/mcoutrim) LIGAÇÃO QUÍMICA É A FORÇA QUE MANTÉM ÁTOMOS E/OU ÍONS UNIDOS NAS
Sólidos metálicos. Fe Hg
 Sólidos metálicos Fe Hg Quais são? Metalóides Não-metais Metais Sólidos metálicos partilha de e - s por muitos átomos iguais (muitos átomos e poucos electrões). Energias de ionização baixas. Propriedades
Sólidos metálicos Fe Hg Quais são? Metalóides Não-metais Metais Sólidos metálicos partilha de e - s por muitos átomos iguais (muitos átomos e poucos electrões). Energias de ionização baixas. Propriedades
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2015 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2015 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
LISTA DE EXERCÍCIOS 6 1 (UNIDADE III INTRODUÇÃO À CIÊNCIA DOS MATERIAIS)
 UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CENTRO DE ENGENHARIAS DEPARTAMENTO DE ENGENHARIA E TECNOLOGIA DISCIPLINA: QUÍMICA APLICADA À ENGENHARIA PROFESSOR: FREDERICO RIBEIRO DO CARMO Estrutura cristalina
UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CENTRO DE ENGENHARIAS DEPARTAMENTO DE ENGENHARIA E TECNOLOGIA DISCIPLINA: QUÍMICA APLICADA À ENGENHARIA PROFESSOR: FREDERICO RIBEIRO DO CARMO Estrutura cristalina
ESTADO SÓLIDO. paginapessoal.utfpr.edu.br/lorainejacobs. Profª. Loraine Jacobs
 ESTADO SÓLIDO lorainejacobs@utfpr.edu.br paginapessoal.utfpr.edu.br/lorainejacobs Profª. Loraine Jacobs Estado Sólido Tradicionalmente, um sólido é definido como uma substância que mantém um volume e uma
ESTADO SÓLIDO lorainejacobs@utfpr.edu.br paginapessoal.utfpr.edu.br/lorainejacobs Profª. Loraine Jacobs Estado Sólido Tradicionalmente, um sólido é definido como uma substância que mantém um volume e uma
Ligação iônica Ligação covalente Ligação metálica
 Principais Tipos de Ligações Químicas Ligação iônica Ligação covalente Ligação metálica Iônicas Covalentes Metálicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações
Principais Tipos de Ligações Químicas Ligação iônica Ligação covalente Ligação metálica Iônicas Covalentes Metálicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações
5 Substituição catiônica em HA
 46 5 Substituição catiônica em HA Apresentaremos neste capítulo os resultados obtidos para as substituições de cádmio e estrôncio nos aglomerados de HA. Primeiramente foram feitos cálculos com a HA pura
46 5 Substituição catiônica em HA Apresentaremos neste capítulo os resultados obtidos para as substituições de cádmio e estrôncio nos aglomerados de HA. Primeiramente foram feitos cálculos com a HA pura
Física dos Materiais FMT0502 ( )
 Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Aulas Multimídias Santa Cecília. Profº Tiago Quick
 Aulas Multimídias Santa Cecília Profº Tiago Quick Ligações Químicas Conceitos Iniciais Prof. Tiago Quick Valência Chamamos de valência a quantidade de ligações químicas que um átomo pode fazer para atingir
Aulas Multimídias Santa Cecília Profº Tiago Quick Ligações Químicas Conceitos Iniciais Prof. Tiago Quick Valência Chamamos de valência a quantidade de ligações químicas que um átomo pode fazer para atingir
QUÍMICA A Ciência Central 9ª Edição Capítulo 8 Conceitos básicos de ligação química David P. White
 QUÍMICA A Ciência Central 9ª Edição Capítulo 8 Conceitos básicos de ligação química David P. White Ligações químicas, símbolos de Lewis e a regra do octeto Ligação química: é a força atrativa que mantém
QUÍMICA A Ciência Central 9ª Edição Capítulo 8 Conceitos básicos de ligação química David P. White Ligações químicas, símbolos de Lewis e a regra do octeto Ligação química: é a força atrativa que mantém
Diferenças entre o C, Si e os demais elementos do grupo 14
 Diferenças entre o C, Si e os demais elementos do grupo 14 O carbono também difere dos demais elementos do grupo pela sua capacidade de formar cadeias (catenação). Isso porque as ligações C-C são fortes,
Diferenças entre o C, Si e os demais elementos do grupo 14 O carbono também difere dos demais elementos do grupo pela sua capacidade de formar cadeias (catenação). Isso porque as ligações C-C são fortes,
Disciplina: Química Professor: Rubens Barreto. III Unidade
 Disciplina: Química Professor: Rubens Barreto III Unidade Ligações Químicas Ligações iônicas Tipos de Ligações Ligações covalentes Ligações metálicas Os gases nobres e a regra do octeto Todas as substâncias
Disciplina: Química Professor: Rubens Barreto III Unidade Ligações Químicas Ligações iônicas Tipos de Ligações Ligações covalentes Ligações metálicas Os gases nobres e a regra do octeto Todas as substâncias
Ideias e Conceitos Iniciais. CF086 - Introdução a Física do Estado Sólido 1
 Ideias e Conceitos Iniciais CF086 - Introdução a Física do Estado Sólido 1 Introdução O estudo de matéria condensada investiga propriedades de sólidos em geral. Tais propriedades emergem por causa do comportamento
Ideias e Conceitos Iniciais CF086 - Introdução a Física do Estado Sólido 1 Introdução O estudo de matéria condensada investiga propriedades de sólidos em geral. Tais propriedades emergem por causa do comportamento
PRINCÍPIOS DA ESTRUTURA EM SÓLIDOS. QFL-4010 Prof. Gianluca C. Azzellini
 PRINCÍPIOS DA ESTRUTURA EM SÓLIDOS Estrutura dos Sólidos Tipo Exemplo Unidades Natureza Estruturais da ligação Iônico NaCl, CaCl 2 Íons positivos Iônica - Atração e negativos Eletrostática forte Metálico
PRINCÍPIOS DA ESTRUTURA EM SÓLIDOS Estrutura dos Sólidos Tipo Exemplo Unidades Natureza Estruturais da ligação Iônico NaCl, CaCl 2 Íons positivos Iônica - Atração e negativos Eletrostática forte Metálico
UNIDADE 2 Ligações Químicas
 UNIDADE 2 Ligações Químicas 1. Utilizando os dados apresentados na tabela abaixo, estime a energia de ligação para o molibdênio (Mo). Dado: o ponto de fusão do Mo é 2617 o C. dica: faça um gráfico da energia
UNIDADE 2 Ligações Químicas 1. Utilizando os dados apresentados na tabela abaixo, estime a energia de ligação para o molibdênio (Mo). Dado: o ponto de fusão do Mo é 2617 o C. dica: faça um gráfico da energia
