ELÉCTRODOS MODIFICADOS POR POLIANILINA INCORPORANDO CENTROS CATALÍTICOS PARA A REDUÇÃO DO OXIGÉNIO MOLECULAR
|
|
|
- Lucas Gabriel Frade das Neves
- 8 Há anos
- Visualizações:
Transcrição
1 UNIVERSIDADE DE LISBOA FACULDADE DE CIÊNCIAS DEPARTAMENTO DE QUÍMICA E BIOQUÍMICA ELÉCTRODOS MODIFICADOS POR POLIANILINA INCORPORANDO CENTROS CATALÍTICOS PARA A REDUÇÃO DO OXIGÉNIO MOLECULAR Isabel Mecking Ornelas DISSERTAÇÃO MESTRADO EM QUÍMICA ESPECIALIZAÇÃO EM QUÍMICA 2013
2 2
3 UNIVERSIDADE DE LISBOA FACULDADE DE CIÊNCIAS DEPARTAMENTO DE QUÍMICA E BIOQUÍMICA ELÉCTRODOS MODIFICADOS POR POLIANILINA INCORPORANDO CENTROS CATALÍTICOS PARA A REDUÇÃO DO OXIGÉNIO MOLECULAR Isabel Mecking Ornelas DISSERTAÇÃO MESTRADO EM QUÍMICA ESPECIALIZAÇÃO EM QUÍMICA Tese orientada pelo Doutor Jorge Manuel Palma Correia e pela Doutora Ana Pimenta da Gama da Silveira Viana Semedo 2013
4 4
5 Agradecimentos Desejo agradecer a todos os que de alguma forma me ajudaram, incentivaram ou contribuíram para a realização deste trabalho, dentro e fora do laboratório. Ao meu orientador Doutor Jorge Correia pelo apoio constante, pela confiança e paciência, pelas encorajadoras discussões científicas, e pela perspectiva quando nada parecia querer funcionar. À minha co-orientadora Doutora Ana Viana pelos valiosos conselhos e opiniões, pela disponibilidade e por não deixar que perdesse o sentido de tempo. Obrigada também pela obtenção das imagens de microscopia de força atómica e pelas discussões e sugestões dadas para a sua análise. Ao Grupo de Electroquímica Interfacial pelo acolhimento e bom ambiente de trabalho. Um agradecimento especial às Anas Mourato e Melato, à Virgínia Ferreira e à Inês Almeida pela constante disponibilidade, paciência e toda a ajuda com material e equipamentos; a todos os colegas e ex-colegas que por lá passaram pelo companheirismo e suporte, especialmente aos meus colegas de mestrado e doutoramento. Ao CQB/DQB pelas condições disponibilizadas para a realização do trabalho experimental. À Fundação para a Ciência e a Tecnologia pelo financiamento concedido através do projecto PTDC/QUI-QUI/121857/2010. Por fim, um obrigada especial à minha família e aos meus amigos por todo o apoio e compreensão, pela motivação, pelos bons conselhos, pela paciência, por terem estado lá e por me terem aturado. i
6 ii
7 Resumo Neste trabalho pretendeu-se preparar novos materiais de cátodo baseados num polímero condutor, a polianilina (PAni), incorporando por co-deposição centros catalíticos contendo metais de transição (óxidos de manganês, ferroporfirina). Inicialmente estudaram-se eléctrodos modificados com filmes de polianilina crescidos por diferentes modos electroquímicos e condições operativas. A observação da superfície dos eléctrodos por microscopia de força atómica permitiu confirmar que os filmes obtidos possuíam morfologias e espessuras diferentes apesar de apresentarem electroactividades semelhantes. O acompanhamento do crescimento de um filme de polianilina por elipsometria in-situ permitiu estimar a sua espessura e os parâmetros ópticos ao longo da sua espessura em função do potencial eléctrico aplicado. Ensaios voltamétricos com Mn 2+ em solução ácida permitiram o estudo do seu comportamento electroquímico nesse meio. Modificaram-se eléctrodos com filmes de polianilina e óxidos de manganês por co-deposição potenciodinâmica; não foram detectadas diferenças no comportamento electroquímico destes materiais na presença e ausência de O2 quer em meio ácido quer em meio neutro. Incorporou-se uma porfirina aniónica de ferro, meso-tetra 4-sulfonatofenil ferro(iii)porfirina (FeTSPP), em filmes de polianilina durante a sua síntese potenciodinâmica. Estudos de microscopia de força atómica revelaram que a presença da porfirina altera profundamente a morfologia dos eléctrodos modificados. Os filmes contendo FeTSPP demonstraram bom desempenho para a catálise da redução de oxigénio em meio ácido, neutro e básico. Palavras chave: polianilina; electropolimerização; porfirina; electroredução do oxigénio molecular; elipsometria; microscopia de força atómica. iii
8 Abstract The purpose of this work was the preparation of new cathode materials based on a conducting polymer, polyaniline (PAni), with the incorporation of catalytic particles containing transition metals (manganese oxide, an iron-porphyrin) obtained through codeposition. PAni-modified electrodes were prepared under different electrochemical modes and conditions. Observation of the modified-electrode surfaces by atomic force microscopy confirmed that the studied films had different morphologies and thicknesses despite having similar electroactivities. In-situ ellipsometry permitted the study of a polyaniline film during its growth, allowing for the estimation of its thickness, as well as its optic parameters throughout its thickness as a function of applied electric potential. Cyclic voltammetry allowed the study of the electrochemical behavior of Mn 2+ in acidic solution. Electrodes were modified with films of polyaniline and manganese oxide through co-deposition. No significant catalytic activity toward oxygen reduction was detected in acidic or neutral solution. An anionic iron-porphyrin (Fe(III) meso-tetra (4-sulfonatophenyl) porphyrin, FeTSPP) was incorporated into polyaniline films by co-deposition. Atomic force microscopy images show dramatic changes in the modified electrode s morphology when the porphyrin was present during the polymerization process. PAni FeTSPP films revealed good performance toward O2 reduction in acidic, neutral and basic solutions. Keywords: polyaniline; electropolymerization; porphyrins; electroreduction of molecular oxygen; ellipsometry; atomic force microscopy iv
9 Índice 1. Introdução Células de Combustível Células de combustível de borohidreto directo Materiais de cátodo em DBFCs Polímeros condutores Polianilina Incorporação de centros catalíticos em polímeros condutores para catálise Polímeros condutores em cátodos para PEMFCs Experimental Electropolimerização da Anilina Electropolimerização potenciodinâmica da anilina Electropolimerização galvanostática da anilina Incorporação de centros catalíticos na matriz polimérica Co-deposição de PAni MnO Co-deposição de PAni FeTSPP Caracterização dos eléctrodos modificados Electroactividade Morfologia Propriedades ópticas e espessura dos filmes Actividade catalítica dos eléctrodos modificados para a reacção de redução do oxigénio Apresentação e Discussão dos Resultados Síntese e caracterização da matriz polimérica Preparação dos eléctrodos modificados Caracterização electroquímica Caracterização morfológica Determinação dos parâmetros ópticos e da espessura de um filme PAni 17/ Redução do oxigénio molecular PAni MnO Comportamento electroquímico do ião manganês em carbono vítreo Preparação dos eléctrodos modificados Redução do oxigénio molecular PAni FeTSPP Comportamento electroquímico de FeTSPP em carbono vítreo Preparação dos eléctrodos modificados Caracterização electroquímica Caracterização morfológica Redução do oxigénio molecular Conclusões Referências Bibliográficas v
10
11
12
13 Capitulo 1: 1. Introdução
14
15
16
17 1. Introdução 1.1. Células de Combustível Células de combustível (FCs, fuel cells) são dispositivos para a conversão de energia química em energia eléctrica. O princípio básico em que todos os tipos de FC se baseiam foi descoberto em 1839 por Christian Schönbein [1] e William Grove [2] e consiste na oxidação de um combustível, normalmente o hidrogénio, no ânodo e na redução de um agente oxidante, como por exemplo oxigénio molecular, no cátodo de uma célula galvânica. Os compartimentos anódico e catódico estão separados por um electrólito (geralmente um líquido, uma solução ou uma membrana) selectivo a uma espécie iónica (geralmente Na +, H + ou OH - ), forçando a passagem de uma corrente eléctrica contínua por um circuito externo. Um esquema da composição de uma FC moderna de H2 e O2 com uma membrana permeável a protões encontra-se na Figura 1.1. Após a sua descoberta, o seu funcionamento foi inicialmente estudado por William Grove, que construiu a primeira célula de combustível de H2 e O2 em [3] Figura 1.1 Esquema do funcionamento de uma célula de combustível de membrana polimérica de H2 e O2, adaptado de [4]. 3
18 1. Introdução Desde a sua descoberta, células de combustível têm vindo a ser desenvolvidas cada vez mais e têm-se obtido progressos no aumento da sua eficiência e na redução dos custos das próprias FCs e do hidrogénio (o combustível mais usado), permitindo a comercialização desta tecnologia em diversas áreas. [5] A gama de produtos já disponíveis comercialmente estende-se desde dispositivos pequenos e leves para aplicações portáteis, como no exemplo do carregador de baterias portátil PowerTrekk a, a FCs de grandes dimensões para aplicações estacionárias que exigem potências elevadas, como para a produção de energia eléctrica e aquecimento para alimentar um grupo de edifícios inteiros (como no caso do sistema PureCell System Model 400 (400 kw), da marca UTC Power, que fornece quase toda a energia usada pelo complexo de edifícios The Octagon no estado de Nova Iorque b ), passando pelos autocarros alimentados a células de combustível do projecto europeu CHIC c. Apesar do intenso estudo e de já estarem disponíveis comercialmente, as FCs ainda enfrentam desafios para que se possam tornar numa tecnologia de ponta e verdadeiramente rentáveis a nível comercial. A necessidade de se reduzir a razão custo/eficiência e de se melhorar o seu desempenho e a sua durabilidade [6], fazem desta tecnologia um tema actual e relevante para várias áreas da ciência. Para a electroquímica, os maiores desafios estão ligados ao desenvolvimento de catalisadores mais eficientes, selectivos e resistentes e de alternativas para o armazenamento de combustíveis (armazenamento de H2 eficientes e mais seguros, combustíveis alternativos como metanol, etanol ou borohidreto). A Figura 1.2 ilustra a distribuição de custos numa célula de combustível de membrana polimérica, PEMFC (polymer electrolyte membrane fuel cell) por componentes, mostrando a evolução destes desde 2007 e projectando objectivos para Como se pode observar, uma das prioridades para o Departamento de Energia dos EUA (DOE, Department of Energy) é a diminuição do custo associado aos catalisadores por mais de metade. a acedido em 03/2013. b acedido em 03/2013. c acedido em 03/
19 1. Introdução Figura 1.2 Custos de PEMFC por componentes actuais e projectados (para 5x10 5 unidades/ano) dados do DOE, retirado de [7] Células de combustível de borohidreto directo O borohidreto surgiu como alternativa ao hidrogénio em FCs em 1953 [8]. O BH4 - é um agente redutor bem conhecido, inócuo, estável ao ar e com capacidades volumétrica e gravimétrica de hidrogénio elevadas (superiores às de H2 líquido e de hidretos metálicos, respectivamente) [9], o que o tornam num combustível promissor para aplicações de pequeno e médio porte. Este reagente pode ser utilizado para armazenar hidrogénio em células de combustível de borohidreto indirecto (IBFCs, indirect borohydride fuel cells) ou directamente (em soluções alcalinas) no anólito de células de combustível de borohidreto directo (DBFCs, direct borohydride fuel cells), permitindo a obtenção de um potencial electroquímico mais elevado do que em FCs à base de H2 ou de metanol directo (DMFCs, direct methanol fuel cells). [9 11] Apesar de IBFCs já se encontrarem disponíveis comercialmente d ; as DBFCs ainda estão em fase de desenvolvimento. d acedido em 03/
20 1. Introdução equação 1.1: Reacções no ânodo: A oxidação do borohidreto é, idealmente, um processo de 8 electrões BH 4 8OH BO2 2 6H O 8e E = V vs. SHE (1.1) Na prática, a oxidação anódica do borohidreto é uma de três reacções concorrentes que ocorrem no ânodo: 1) Electro-oxidação de borohidreto; 2) Hidrólise de borohidreto; 3) Electro-oxidação de hidrogénio. A extensão de cada uma destas reacções é fortemente dependente do catalisador. A eficiência da célula é também influenciada pela concentração de borohidreto nos centros activos catalíticos, pela constituição do anólito (solução que flui pelo compartimento anódico) e pelas condições de funcionamento da célula, como a temperatura e a corrente. [9] Reacções no cátodo: Como comburente no cátodo podem ser usados O2 (puro ou do ar; meio alcalino) ou solução de H2O2 (alcalina ou ácida). As reacções de redução correspondentes são as seguintes [10] : O2: 2O2 4H2O 8e 8OH E = 0.4 V vs. SHE (1.2) H2O2, básico: 4HO 2 2 4H O 8e 12OH E = 0.87 V vs. SHE (1.3) H2O2, ácido: 4H2O2 8e 8H 8H2O E = 1.77 V vs. SHE (1.4) O H2O2 tem um potencial de redução padrão superior ao do O2, tendo assim uma eficiência máxima teórica mais elevada. [10] O peróxido de hidrogénio é ideal para aplicações anaeróbias, como para expedições ao fundo do mar ou missões extraterrestres. Em dispositivos para uso comum é mais rentável a utilização do O2 existente no ar, pois este fornece oxigénio suficiente para um bom funcionamento da DBFC e elimina a necessidade de armazenamento de comburente. 6
21 1. Introdução Geralmente, a redução catódica do agente oxidante é a reacção limitante em qualquer célula de combustível, incluindo DBFCs. [12 14] Este ponto será desenvolvido na secção (Materiais de cátodo em DBFCs). Electrólito: O electrólito em DBFCs é normalmente uma membrana polimérica, que pode ser permeável a catiões Na +, como a representada na Figura 1.3, ou permeável a OH -. Membranas catiónicas são geralmente usadas porque limitam mais eficientemente a passagem (crossover) de BH4 - para o cátodo, minimizando assim a diminuição de eficiência devido a esse fenómeno. [10] A temperatura de funcionamento das células de combustível de borohidreto directo é geralmente baixa, T 80 C. [15] Figura 1.3 Diagrama esquemático de uma DBFC, imagem retirada de [11] Materiais de cátodo em DBFCs Como já foi mencionado, células de combustível de borohidreto directo podem usar oxigénio ou peróxido de hidrogénio como comburente. Neste trabalho, o foco cairá sobre FCs alimentadas a O2. O catalisador catódico mais utilizado é a platina, que está muito bem estudada [11] e cujo valor da densidade de corrente de troca, i0, é dos mais 7
22 1. Introdução elevados. Contudo, este metal nobre apresenta desvantagens, não só a nível do seu custo (é um material raro e caro) mas também devido ao seu desempenho como catalisador. A redução do oxigénio em Pt é significativamente mais lenta (i A cm -2 a T = 25 C) [16] do que a oxidação do H2 (i A cm -2, T = 25 C) [16], sendo assim o passo limitante em todas as FCs de O2. Outro problema associado à platina é a sua boa actividade catalítica para a degradação (oxidação e hidrólise) de BH4 -[17], presente no compartimento catódico devido ao fenómeno de crossover, que pode ocorrer mesmo com membranas selectivas a Na + e que reduz a eficiência da célula. O esforço de investigação no desenvolvimento de electrocatalisadores catódicos que possam substituir a platina é justificado pelas razões acima referidas e tem como objectivo uma redução da razão custo/potência das FCs. Assim, o catalisador alternativo deve não só ser mais barato do que o metal nobre; esperase também que um material que catalise a electroredução do oxigénio por meio de um mecanismo reaccional diferente leve a melhorias nos parâmetros cinéticos (densidade de corrente de troca, i0, e coeficiente de simetria, α) aumentando a corrente e, assim, a eficiência da célula. Adicionalmente, pretende-se que o catalisador catódico seja insensível à presença de borohidreto, prevenindo assim um declínio no seu desempenho devido ao crossover destes aniões e/ou permitindo a construção de células sem membranas (diminuição de custos). Os materiais alternativos para catalisadores catódicos mais estudados podem ser divididos em três classes: metais (e ligas), óxidos metálicos e complexos metálicos orgânicos e inorgânicos. Metais como Au, Ag e Pd [17 19] demonstram boa actividade para ORR, mas também sofrem de pouca selectividade para a reacção, sendo afectados pela presença de borohidreto. Em contrapartida, têm-se destacado catalisadores catódicos à base de materiais não-nobres como óxidos de manganês [17,20,21] e perovskites [22], assim como macrociclos (especialmente porfirinas e ftalocianinas) de metais de transição, ou metais de transição em matrizes de polímeros condutores heterocíclicos [19,23 29]. Em regra, dentro da classe dos complexos metálicos, tem-se observado uma relação benéfica entre o desempenho do catalisador e a presença de ligações azoto-metal e carbono-azotometal. [30,31] Espera-se que o desenvolvimento de cátodos com estes materiais permita a construção e optimização de células de combustível mais eficientes e baratas. 8
23 1. Introdução 1.2. Polímeros condutores Polímeros electronicamente condutores (electronically conducting polymers, ECPs) são uma classe de materiais poliméricos orgânicos que conduzem carga eléctrica. A sua descoberta abriu caminho para o desenvolvimento de materiais condutores, semicondutores e de condutividade variável (Figura 1.4) e controlável, mais baratos e mais leves do que metais ou semicondutores inorgânicos. Apesar de haver relatos sobre a síntese de polímeros condutores muito antes (Letheby descreveu as características electrocrómicas de polianilina sintetizada por oxidação anódica em 1862 [32] ), esta classe de materiais só ganhou interesse na década de 70 do século passado devido ao trabalho de Alan J. Heeger, Alan G. MacDiarmid e Hideki Shirakawa [33,34], a quem foi atribuído o Prémio Nobel da Química em Figura 1.4 Gamas de condutividade de isoladores, semicondutores, condutores e ECPs; imagem retirada de [35]. Estruturalmente, um condutor orgânico tem que possuir um esqueleto suficientemente comprido constituído por ligações C-C simples e duplas conjugadas, criando um sistema de electrões deslocalizados ao longo da cadeia. Adicionalmente, é também necessária uma dopagem do material, a inserção de cargas electrões (dopagem tipo n) ou lacunas (a falta de um electrão; dopagem tipo p) cujo movimento 9
24 1. Introdução proporciona a condução eléctrica através do composto. Ao contrário dos semicondutores inorgânicos, a dopagem de um ECP não se deve à presença de impurezas elementares na estrutura cristalina, mas é gerada por redução (tipo n) ou oxidação (tipo p) do polímero. A alteração do estado redox de ECPs é reversível e pode ser obtida pela aplicação de um potencial eléctrico ou através de contacto com uma substância apropriada (e.g. agente oxidante ou redutor), permitindo um controle fácil e rápido da condutividade do material. Este processo é acompanhado por um fluxo de espécies iónicas (contra-iões, a espécie dopante ) de modo a manter a electroneutralidade. Este fenómeno de inserção ou expulsão de iões compensadores de carga é frequentemente acompanhado por fluxos de solvente (e eventualmente electrólito na forma de pares iónicos) que, conjuntamente com os efeitos coulombicos resultantes da alteração electrónica das cadeias poliméricas, pode conduzir ao aumento ou diminuição de volume do filme polimérico. [36 38] A perturbação da estrutura electrónica causada pela oxidação/redução do polímero leva à alteração dos níveis energéticos característicos do material e, consequentemente, a modificações de cor conforme o estado de oxidação do filme polimérico (efeito electrocrómico). [36 38] A condutividade dos ECPs é, tradicionalmente, interpretada através do modelo de polarões e bipolarões [39,40], originalmente desenvolvido para semicondutores inorgânicos. Quando um polímero conjugado é oxidado (ou reduzido), gera-se um ião (de spin S = 0) e um radical (S = ½), causando distorções estruturais locais. Estes defeitos (polarões) mantêm-se próximos um do outro ( 4 a 5 unidades monoméricas) e são estabilizados por efeitos de ressonância. Localmente, é criado um nível energético novo na zona entre as bandas de valência e de condução, ocupado por electrões desemparelhados. À medida que o processo de oxidação (ou redução) prossegue, formam-se mais polarões e este modelo prevê que, para dois polarões na mesma cadeia, é energeticamente mais favorável um acoplamento dos mesmos. O bipolarão assim formado tem spin nulo devido ao emparelhamento dos electrões e as duas cargas mantêm, aproximadamente, a mesma distância que o ião e o radical do polarão. A um nível elevado de dopagem, formam-se bandas de bipolarões, diminuindo o hiato óptico e aumentando a condutividade do material [41,42] (Figura 1.5). Cálculos teóricos prevêem 3 transições ópticas para o estado polarónico e duas para o bipolarónico. [43] Estas transições foram confirmadas por ensaios espectroscópicos. [39] 10
25 1. Introdução Bandas de condução Bandas de valência a b c d Figura 1.5 Evolução dos estados electrónicos (bandas) num polímero durante o processo de dopagem de acordo com o modelo do bipolarão: a) estado neutro, b) polarão, c) bipolarão, d) bandas bipolarónicas (elevado nível de dopagem); adaptado de [38]. Contudo, o modelo acima descrito considera cadeias de comprimento infinito e sem defeitos; Na prática, este modelo não é universalmente aplicável e há suporte experimental (estudos electroquímicos [44,45], de espectroscopia de ressonância de spin electrónico (electron spin resonance, ESR) [45], de condutividade [46] ) para uma interpretação alternativa baseada na teoria de orbitais moleculares, que descreve CPs como sistemas moleculares [47] e o processo de dopagem como uma sequência de reacções redox dependentes do potencial eléctrico que se podem sobrepor, resultando num patamar faradaico. [38] Dentro da classe de ECPs existe uma grande variedade estrutural e complexidade dos sistemas (por exemplo, é conhecido que as propriedades de cada polímero são fortemente influenciadas por parâmetros experimentais durante a sua síntese e dopagem). [36,38,48 55] Por essas razões, e apesar do estudo intenso nesta área desde a sua descoberta, há fenómenos cruciais cujos mecanismos ainda não estão completamente esclarecidos, como os dos processos de electropolimerização e de carga/descarga (dopagem/desdopagem), assim como as suas propriedades espectroscópicas e eléctricas. 11
26 1. Introdução À excepção do acetileno, que só pode ser polimerizado quimicamente, os polímeros condutores podem ser sintetizados por via química ou electroquímica, sendo que a segunda via é geralmente preferível por trazer várias vantagens: Controle sobre as condições de crescimento: a via electroquímica permite a formação de filmes em condições controladas de crescimento através da escolha do potencial eléctrico (por aplicação de um potencial constante modo potenciostático ou por varrimento numa determinada gama de potenciais eléctricos modo potenciodinâmico) ou da velocidade com que a polimerização ocorre (por aplicação de uma corrente constante modo galvanostático). A via química utiliza agentes oxidantes que polimerizam o monómero at once uma vez que são usados em excesso e não estequiometricamente. Modificação de eléctrodos: electroquimicamente são formados filmes à superfície de eléctrodos, permitindo um controle fácil do potencial eléctrico do polímero imediatamente após o seu crescimento. Quando um ECP é sintetizado por via química, o material é formado em forma de pós e tem que ser posteriormente depositado num eléctrodo. Controlo do grau de dopagem do polímero: através da via electroquímica, os filmes são obtidos logo no estado condutor (estado dopado) pois é pelo potencial eléctrico que se oxida o monómero e também o polímero (com inserção de contra-iões). Na abordagem química o agente oxidante oxida o monómero mas não o polímero que tem que ser dopado (química ou electroquimicamente) após a sua formação. Pureza do produto final: os filmes obtidos por electropolimerização consistem apenas em polímero e contra-iões (e solvente) enquanto o pó obtido por via química está fortemente contaminado pelo agente usado para a polimerização (normalmente Fe 3+ que é reduzido a Fe 2+ ) Flexibilidade na escolha das condições de polimerização: a via electroquímica permite escolher o poder oxidante que se pretende (através da selecção do potencial eléctrico) e assim adequar as condições para cada monómero qualquer que seja o seu potencial de oxidação. 12
27 1. Introdução Em regra, através da polimerização electroquímica, obtêm-se materiais com características (morfologia, condutividade, etc.) mais reprodutíveis e de melhor qualidade. De um modo geral, a síntese de um polímero condutor é um processo complexo que se dá em três fases [38] : (i) O primeiro passo consiste na oxidação e do monómero, originando num radical catião (RC). Esta espécie altamente reactiva pode reagir com outro RC (via RC-RC) ou com um monómero (M; via RC-M), originando um dímero. Segue-se a formação de oligómeros solúveis, preferencialmente através de passos de dimerização sucessivos [37,38,58,59], na camada de difusão do eléctrodo. (ii) A partir de um tamanho crítico, os oligómeros tornam-se insolúveis e dá-se a deposição destes à superfície do eléctrodo e a criação de núcleos a partir dos quais o crescimento das cadeias continua. (iii) Finalmente, a polimerização continua no estado sólido, envolvendo aumento do comprimento, ramificação e reticulação (crosslinking) das cadeias. O interesse em polímeros condutores para aplicações tecnológicas deve-se a várias propriedades exibidas por estes compostos e pela possibilidade de se criarem materiais com características específicas para a utilização pretendida (por variação das condições de síntese, copolimerização, integração de centros catalíticos na matriz polimérica, adição de grupos funcionais no monómero, etc.). Alguns exemplos de possíveis aplicações tecnológicas (e as propriedades dos ECPs que as permitem) incluem [36 38,60,61] : protecção contra corrosão (estabilidade química, possibilidade da sua deposição em topografias complexas, cobrindo superfícies irregulares na sua totalidade), uso em placas de circuitos impressos [62,63] (condutividade, possibilidade de serem depositados em padrões específicos numa superfície), em janelas inteligentes e dispositivos electroluminiscentes como ecrãs LED (light emitting diode) (propriedades electrocrómicas), electrocatálise e sensores químicos e bioquímicos (formação de filmes aderentes e porosos com propriedades físicas e químicas desejadas, incluindo a imobilização de centros catalíticos e Nota: apesar de polimerização redutiva também ser possível [56,57], a maior parte dos polímeros condutores é sintetizada por via oxidativa. 13
28 1. Introdução na sua matriz), em baterias recarregáveis (fácil transição entre estados redox diferentes, grande capacidade de acumulação de carga), em células de combustível (como electrocatalisadores), em dispositivos fotovoltaicos e na medicina como músculos artificiais (alteração reversível do seu volume por aplicação de um potencial eléctrico) Polianilina A polianilina (PAni) é um dos polímeros condutores mais bem estudados. A polimerização de PAni segue o mesmo esquema geral descrito para os polímeros condutores na secção anterior. Inicialmente dá-se a oxidação da anilina e formação de dímeros. Yang e Bard [64] mostraram que os dois produtos possíveis p aminodifenilamina (p-adpa, p-aminodiphenylamine, por ligação de cauda a cabeça ) e benzidina (por ligação de cauda a cauda ) são geradas nesta fase. As suas proporções são diferentes e dependem das condições experimentais, mas, em geral, p ADPA é o produto maioritário. A cadeia continua a crescer preferencialmente através de dimerizações sucessivas. [58,65,66] A Figura 1.6 ilustra a formação da espécie com quatro unidades monoméricas a partir de dois dímeros no seu estado oxidado (radicais). Figura 1.6 Dimerização de p-adpa; adaptado de [58]. Sob aplicação de potenciais suficientemente positivos são formados oligómeros radicais cuja solubilidade diminui com o aumento do seu tamanho tetrâmeros são menos solúveis no seu estado reduzido [58,67], octâmeros insolúveis. Estas espécies são depositadas à superfície do eléctrodo, criando núcleos a partir dos quais as cadeias de polianilina continuam a crescer. Pensa-se que a PAni é constituída por cadeias com 8 unidades 14
29 1. Introdução monoméricas ou mais e que estas também podem formar ramificações e produtos de adições na posição orto em certas condições (após períodos prolongados sob um potencial suficientemente anódico, ou em meio não ácido). [58,66,68] Morfologicamente, o crescimento de filmes de polianilina também pode ser dividido em 3 fases distintas, resultando em camadas com características diferentes. Estudos de elipsometria in-situ durante ensaios de polimerização potenciodinâmica e potenciostática de polianilina [69 71] revelaram que, numa fase inicial, a espessura da PAni no eléctrodo se mantém constante, apesar de haver um aumento de carga consumida com cada ciclo e de se observar um aumento de densidade do filme no seu estado reduzido. Os autores propõem que esta espessura corresponde à altura média dos núcleos de PAni depositados e que, durante esta fase, o polímero cresce lateralmente, de modo a cobrir a superfície do eléctrodo. Numa segunda etapa, observa-se um aumento da espessura do filme, acompanhado por um aumento de densidade e da quantidade de sítios no estado oxidado. Este crescimento mais facilitado é atribuído à actividade autocatalítica [55] da electropolimerização da anilina. Finalmente, após uma espessura crítica (dependente das condições de crescimento), observa-se um crescimento rápido de uma estrutura mais porosa, indicando uma mudança no mecanismo de crescimento, causando a formação de uma camada com uma estrutura diferente, menos densa e ordenada. Esta tendência também foi observada em ensaios de elipsometria efectuados ex-situ. [50] A estrutura da polianilina depende do seu estado de oxidação, como já foi referido, mas também do ph do meio. A Figura 1.7 ilustra os diferentes estados de oxidação e protonação da polianilina e indica as cores respectivas de cada estado. No seu estado mais reduzido, de leucoesmeraldina, a estrutura é do tipo benzenóide e o polímero é transparente ou amarelo claro; a pernigranilina, o estado mais oxidado, é azul-escuro ou violeta e apresenta uma estrutura quinóide; a estrutura da esmeraldina (verde) é mista. [36] A polianilina apenas apresenta boa condutividade quando em meio ácido (sal de esmeraldina). 15
30 -4 H+, -4 e- -4 H+, -4 e- -4 H+, -4 e- 1. Introdução Pernigranilina violeta Base de Esmeraldina azul Estado condutor Sal de Esmeraldina verde -4 HA Leucoesmeraldina amarelo Sal de Leucoesmeraldina amarelo -4 HA Figura 1.7 Fórmulas idealizadas da PAni nos seus diferentes estados de oxidação e protonação; adaptado de [36,42] Incorporação de centros catalíticos em polímeros condutores para catálise Devido a propriedades como o seu baixo peso específico, elevada área superficial (porosidade), condutividade e não-toxicidade [72], os ECPs representam uma classe de materiais com grande potencial para aplicações em (electro)catálise [37,73]. A polianilina é um dos CPs mais promissores e mais bem estudados [61,73 79] e, nesta secção, este polímero será particularmente considerado. Durante a conversão electrocatalítica de uma espécie em solução, há (pelo menos) três processos que têm que ser considerados [73] : 16
31 1. Introdução (i) a transferência electrónica heterogénea entre o eléctrodo e o polímero condutor e transporte de cargas dentro do próprio filme polimérico, que inclui transferência electrónica e o movimento das espécies iónicas (contra-iões) e solvente que a acompanham, assim como, eventualmente, mudanças conformacionais; (ii) difusão das espécies em solução até à zona de reacção onde se dá a conversão electrocatalítica, que pode ocorrer à superfície do filme ou no seu interior; (iii) transferência de carga entre a espécie em solução e o polímero condutor. Cada um destes processos é complexo, o que torna a interpretação de resultados experimentais difícil, apesar do desenvolvimento de modelos simplificados. [73] Os ECPs podem ser usados como catalisadores muitos possuem propriedades electrocatalíticas para diversas reacções mas também como suporte para centros catalíticos, que podem ser inseridos na sua matriz tridimensional por diversos métodos. A funcionalização de ECPs permite conferi-los com propriedades físicas e químicas específicas desejadas, em adição às propriedades electrónicas da cadeia conjugada do polímero. [36,38,73] Esta versatilidade faz com que esta classe de materiais seja interessante para várias aplicações. Polímeros condutores funcionalizados podem ser separados em duas grandes classes: (i) compósitos de ECPs e outros materiais e (ii) ECPs que contêm grupos funcionais na sua estrutura, covalentemente ligados a unidades monoméricas. No primeiro grupo, os compósitos mais comuns são os de ECPs e nanopartículas (NPs) metálicas. Existem vários métodos para a preparação destes materiais. Sih e Wolf [80] dividem as metodologias em dois grupos: a) sínteses em um só passo ( one-pot approach), em que o monómero ou o polímero age como redutor de iões metálicos e b) preparação prévia de NPs seguida de polimerização do polímero à volta das partículas ou de dispersão das NPs na matriz polimérica. Num artigo de revisão recente, Ciric- Marjanovic [61] resume os avanços na preparação e controlo das propriedades físicas e químicas de uma vasta gama de compósitos de PAni e metais (Au, Pt, Pd, Ag, Cu, Ni, Co, Fe, Ta, Zn, Mn, Zr, Ce), ligas metálicas e não metais (incluindo Si, S e materiais à base de carbono como nanotubos, nanodiamantes, grafeno, fulereno, etc.) e dá exemplos de 17
32 1. Introdução aplicações de cada tipo de compósito. Também têm sido estudados compósitos de ECPs com óxidos metálicos, complexos metálicos, biomoléculas, assim como materiais ternários combinando ECPs, metais e não-metais. [36,61,79,81,82] Outro método para a inserção de centros catalíticos na estrutura de ECPs consiste na adição de um grupo funcional a unidades monoméricas polimerizáveis. Deste modo, é possível distribuir as funcionalidades desejadas pela matriz tridimensional do polímero. Este processo pode ser realizado por duas vias: a primeira consiste na adição da funcionalidade pretendida no monómero e subsequente polimerização; a segunda na polimerização de monómeros contendo grupos reactivos, como esteres activos ou aminas protegidas, que podem ser modificados após a polimerização. [36] Polímeros condutores em cátodos para PEMFCs Ainda não há muitos estudos utilizando ECPs como material de cátodo para DBFCs, mas existem vários que avaliam o seu desempenho como catalisadores para a redução de oxigénio com o intuito de poderem ser usados em PEMFCs. Nesta secção serão descritos brevemente alguns cátodos à base de polímeros condutores (PAni e polipirrolo, PPy) que têm mostrado melhor desempenho para a redução do oxigénio. Num estudo com 5 dos ECPs mais comuns PAni, PPy, politiofeno (PTh), poli((3- metilo)tiofeno) (PMeT) e poli(3,4-etilenodioxitiofeno) (PEDOT), Khomenko et al. [83] demonstraram que todos os filmes estudados, com a excepção do PEDOT, possuíam actividade electrocatalítica para a redução do oxigénio molecular, sendo que os melhores resultados foram obtidos com os materiais contendo átomos de N na sua estrutura, PAni e PPy. A electroactividade destes polímeros pode ser melhorada através da incorporação de metais de transição na sua matriz. [31] Bashyam e Zelenay [30] imobilizaram cobalto numa matriz de PPy em carbono (C-PPy-Co). O compósito assim obtido demonstrou bom desempenho como cátodo numa célula de combustível de H2/O2 e estabilidade mesmo depois de 100 h de funcionamento. Martinez Millan et al. [84] estudaram filmes de PAni, PPy e PMeT em suporte de carbono com e sem cobalto (C-PAni-Co, C-PPy-Co, C-PMeT-Co e C- 18
33 1. Introdução PAni, C-PPy, C-PMeT, respectivamente) para avaliar a sua actividade para ORR e concluíram que C-PPy-Co, apresentando o melhor desempenho, é o melhor material para uma aplicação como cátodo de uma FC. Um compósito à base dos mesmos materiais foi testado por Qin et al. [29] como cátodo numa DBFC, obtendo bons resultados. Um bom desempenho também foi obtido por Cong et al. [85] com um compósito de C-PPy-Ox, em que Ox = Cu1.4Mn1.6O4. Os autores realizaram ensaios com aniões diferentes e concluíram que a actividade deste cátodo para a ORR depende do dopante. Num estudo teórico, Chen et al. [86] compararam catalisadores de PAni e Fe, Co ou Fe e Co. Os resultados indicam que os compósitos de PAni-CoFe são os mais activos para a redução de oxigénio e que o mecanismo ocorre através da formação de OOH (e não de H2O2) como intermediário Figura 1.8. Figura 1.8 Estrutura optimizada de PAni-CoFe durante a ORR; retirado de [86]. Experiências com um passo de tratamento térmico/pirólise de compósitos de polímeros condutores (PAni e PPy) e metais de transição têm demonstrado resultados melhores do que os seus precursores. [31,87 90] Em geral, compostos com C e N (centros CxN como os presentes em ECPs como PAni e PPy e em macrociclos heteroatómicos como porfirinas e ftalocianinas, assim como nos seus derivados pirolisados), com e sem metais de transição são os que têm demonstrado melhor actividade para ORR. Na prática há sempre uma mistura de estruturas diferentes num determinado material, pelo que ainda não se sabe bem qual é a melhor estrutura para a catálise. O mecanismo reaccional da redução do O2 nestes centros também ainda não está completamente esclarecido. Estas questões são 19
34 1. Introdução importantes para o desenvolvimento de catalisadores mais eficientes, que possam substituir os metais nobres. [31] Os 3 factores que afectam a efectividade cinética volumétrica de um catalisador são a frequência de turnover dos seus centros activos (a velocidade com que cada centro activo catalisa a reacção), o número de centros activos por unidade de volume de material (densidade de centros activos), e quantos centros estão activos durante a operação (utilização). Assim, para se melhorar o desempenho de um catalisador, em adição à procura de centros com melhor actividade, também se deve procurar desenvolver catalisadores com uma maior área superficial e com uma maior densidade de centros activos. [31] Este trabalho teve como objectivo o desenvolvimento e a caracterização de novos materiais de cátodo para células de combustível de borohidreto directo através da modificação de eléctrodos por co-deposição de polianilina e centros catalíticos contendo metais de transição. 20
35 Capitulo 2: 2. Experimental
36
37 2. Procedimento Experimental 2.1. Electropolimerização da Anilina Todos os reagentes foram utilizados na forma em que foram recebidos excepto a anilina, que foi previamente destilada sob pressão reduzida e armazenada a T 4 C sob atmosfera de azoto. A polianilina foi sintetizada por electropolimerização a partir de uma solução aquosa contendo anilina (Scharlau, p.a.) 0,1 M e ácido sulfúrico (BDH, 100%) ou ácido clorídrico (Sigma-Aldrich, 37%) 0,5 M. Entre cada ensaio poliu-se mecanicamente o eléctrodo de trabalho com alumina (Buehler) de granulometria 0,3 µm. Água millipore (milli-q, resistividade de 18,2 MΩ cm) foi utilizada para todas as soluções e lavagens. Utilizou-se uma célula electroquímica de teflon de um compartimento com um contra-eléctrodo de folha de platina e um eléctrodo de referência saturado de calomelanos (saturated calomel electrode, SCE). O eléctrodo de trabalho consistiu num disco de carbono vítreo (glassy carbon, GC) com uma área exposta de A = 0,567 cm 2 (diâmetro ϕ = 0,85 cm). Para os ensaios electroquímicos recorreu-se a um gerador de funções IMT Electrochemical Interface com um potenciostato DEA332 Digital Electrochemical Analyzer, ambos da marca Radiometer Copenhagen e com o software Voltamaster 2 ou a um potenciostato/galvanostato modelo 273A (EG&G Princeton Applied Research) em conjunto com o registador analógico Omnigraph 2000 (Houston Instrument) Electropolimerização potenciodinâmica da anilina Os filmes de polianilina foram sintetizados por aplicação de ciclos de potencial consecutivos entre -0,200 e +0,800 V vs. SCE durante os primeiros cinco ciclos, entre -0,200 e +0,750 V durante os três ciclos seguintes e entre -0,200 e +0,700 V após o oitavo ciclo. A diminuição do limite anódico foi efectuada de modo a evitar a sobreoxidação do filme polimérico, seguindo a metodologia empregue por Greef et al. [91]. 23
38 2. Procedimento Experimental Sintetizaram-se três filmes com electroactividades comparáveis mas com morfologias distintas variando as condições de crescimento: PAni 17/10: crescido a uma velocidade de varrimento ν = 10 mv s -1 durante 17 ciclos, usando ácido sulfúrico como electrólito; PAni 200/60: formado a partir de uma solução idêntica mas a uma velocidade de varrimento ν = 60 mv s -1 durante 200 ciclos; PAni 85/10 (HCl): crescida durante 85 ciclos a ν = 10 mv s -1 em solução de ácido clorídrico Electropolimerização galvanostática da anilina Foram electropolimerizados filmes através da aplicação de diferentes valores de correntes e durante diversos intervalos de tempo de modo a encontrar as condições ideais para a formação de um filme de polianilina com uma electroactividade semelhante à da PAni 17/10. Escolheram-se os seguintes parâmetros como os mais adequados: I = 50 µa (i = 88 µa cm -2 ) durante 7 minutos (420 s) Incorporação de centros catalíticos na matriz polimérica Foram incorporados centros catalíticos contendo metais no filme polimérico de modo a testar a sua actividade electrocatalítica para a reacção de redução do oxigénio (oxygen reduction reaction, ORR). As espécies estudadas foram óxidos de manganês e uma porfirina aniónica de ferro (meso-tetra 4-sulfonatofenil ferro(iii)porfirina, FeTSPP) Co-deposição de PAni MnO2 Para a incorporação de MnO2 na matriz polimérica durante o crescimento da PAni, utilizou-se uma solução contendo MnSO4 0,2 M (MnSO4 H2O, Panreac, p.a. ACS), H2SO4 0,5 M e anilina 0,1 M. 24
39 2. Procedimento Experimental O comportamento electroquímico de MnSO4 em H2SO4 0,5 M foi estudado num eléctrodo de GC por voltametria cíclica, variando-se a velocidade de varrimento e o limite anódico. Os filmes de PAni MnO2 foram crescidos potenciodinamicamente a uma velocidade de varrimento de ν = 10 mv s Co-deposição de PAni FeTSPP Para a incorporação de meso-tetra 4-sulfonatofenil ferro(iii)porfirina (FeTSPP, representada na Figura 2.1) na matriz polimérica durante o crescimento da PAni, utilizaram-se soluções do sal tetra sódico desta ferro-porfirina (Frontier Scientific) com 3 concentrações diferentes (0,2, 1 e 2 mm) contendo H2SO4 0,5 M e anilina 0,1 M. Figura 2.1 Estrutura de meso-tetra 4-sulfonatofenil ferro(iii)porfirina (FeTSPP) no seu estado desprotonado. O comportamento electroquímico de FeTSPP (1 mm) em H2SO4 0,5 M foi estudado num eléctrodo de GC por voltametria cíclica na gama de potenciais eléctricos de -0,5 E 1,5 V vs. SCE e a uma velocidade de varrimento de ν = 10 mv s -1, em solução arejada e desarejada. Todos os filmes de PAni FeTSPP foram electropolimerizados potenciodinamicamente nos intervalos de potencial já descritos para os filmes de polianilina (secção ) em soluções contendo FeTSPP, anilina 0,1 M e H2SO4 0,5 M. Estudou-se também um filme 25
40 2. Procedimento Experimental de PAni 4/10 com FeTSPP adsorvido. Para tal, cresceu-se um filme de PAni 4/10 que, após lavagem com água millipore, foi imerso em solução contendo FeTSPP 1 mm em H2SO4 0,5 M durante 40 min 2.3. Caracterização dos eléctrodos modificados Electroactividade À excepção dos filmes de PAni MnO2, todos os eléctrodos modificados foram caracterizados por voltametria cíclica em solução do electrólito suporte utilizado durante a sua síntese (H2SO4 ou HCl 0,5 M) na gama de potencial que permitia cobrir os diversos processos de eléctrodo relevantes para este estudo. A velocidade de varrimento empregue foi de ν = 20 mv s -1 para os filmes de PAni FeTSPP; os eléctrodos modificados por PAni MnO2 não foram sujeitos a esta caracterização voltamétrica para evitar a redução do MnO2 imobilizado na matriz polimérica Morfologia Neste trabalho utilizou-se a microscopia de força atómica para se avaliar a morfologia e espessura de alguns dos filmes estudados. A microscopia de força atómica (AFM, atomic force microscopy) é uma técnica da família das microscopias de ponta de prova (SPM, scanning probe microscopy). O funcionamento do microscópio de força atómica (AFM, atomic force microscope) baseia-se numa ponta afiada, geralmente feita de silício ou nitreto de silício, montada na extremidade de um cantilever ( alavanca ), cujo lado oposto (lado de cima ) é frequentemente revestido de um material reflector como ouro ou alumínio. [92] Esta alavanca está ligada a elementos piezo-eléctricos que controlam a posição tridimensional da ponta com grande precisão. À medida que a ponta vai varrendo uma superfície, as interacções entre estas provocam deflexões no cantilever, que vão sendo monitorizadas através de um laser que incide sobre o lado de cima do cantilever e reflectido para um fotodetector, geralmente composto por quatro fotodíodos. A partir da deflexão da consola podem-se calcular as interacções entre a ponta e a amostra. [92,93] Um esquema da montagem de um AFM está representado na Figura
41 2. Procedimento Experimental Figura 2.2 Esquema de montagem de um AFM; retirado de [92]. Um microscópio de força atómica pode funcionar em vários modos diferentes, que devem ser escolhidos consoante o tipo de amostra (dependendo da topografia, do material, etc.) e a informação que se pretende obter (topográfica, de fase, curvas de forçadistância, etc.). Os modos mais utilizados são os de contacto, não-contacto e contacto intermitente. A Figura 2.3 ilustra esquematicamente os regimes de força sob os quais estes modos operam. A distâncias grandes (superiores a, aproximadamente, nm [93,94] ), não se sentem forças entre a ponta e a superfície da amostra. À medida que a distância diminui, forças atractivas de van der Waals começam a puxar a ponta em direcção à superfície. Quando ponta e superfície se aproximam ainda mais uma da outra, interacções entre as camadas electrónicas das superfícies opostas resultam em forças repulsivas. O modo de contacto funciona sob regime de forças repulsivas, dominado por interacções entre as camadas electrónicas das superfícies da ponta/sonda e da amostra. O modo de não-contacto opera sob regime de forças atractivas, como as forças de van der Waals. No modo de contacto intermitente, ou tapping, a sonda oscila entre estas duas zonas, entrando e saindo de contacto com a superfície da amostra. 27
42 força 2. Procedimento Experimental contacto intermitente atractiva repulsiva contacto não contacto distância Figura 2.3 Diagrama ilustrando os regimes de força sob os quais cada um dos três modos mais comuns de funcionamento do AFM (modos de contacto, não-contacto e contacto intermitente) operam; adaptado de [92]. O modo de contacto foi o primeiro a ser desenvolvido e é geralmente utilizado para superfícies duras e pouco rugosas. Esta técnica pode ser usada em modo de força constante ou de força variável. No primeiro, a altura é alterada durante o varrimento da superfície da amostra de modo a manter a deflexão do cantilever e, assim, a força constate. A posição da sonda é monitorizada, obtendo-se assim informação topográfica sobre a amostra. Alternativamente, no modo de força variável, monitoriza-se a deflexão da sonda, que varia consoante a distância entre a ponta e a superfície da amostra. Este modo só pode ser usado com superfícies muito lisas, mas resulta em imagens topográficas com melhor resolução do que as obtidas em modo de força constante. Em amostras menos lisas, fricção entre ponta e protuberâncias podem danificar a ponta ou a própria amostra, levando a uma diminuição da resolução e a artefactos. Em modo de contacto intermitente, a sonda oscila a uma frequência próxima da sua frequência de ressonância. Quando a ponta se aproxima da amostra, interacções entre as superfícies opostas restringem a amplitude de oscilação. Para se obter informação topográfica, utiliza-se um mecanismo de feedback para se variar a altura da sonda de modo a manter-se constante a sua amplitude de oscilação. Sondas com flexibilidades e constantes de mola diferentes são utilizadas para amostras diferentes. As propriedades da superfície influenciam também a frequência de oscilação da sonda, resultando numa 28
43 2. Procedimento Experimental diferença entre a frequência imposta e a frequência real. Este fenómeno é utilizado para produzir imagens de fase simultaneamente com as imagens topográficas. Estas imagens podem dar informação qualitativa valiosa, contudo, a extracção de informação quantitativa é muito difícil porque a variação de fase é influenciada por vários factores experimentais, como adesão entre ponta e amostra, velocidade de varrimento, topografia e material da superfície, elasticidade da ponta e da superfície, etc. Em modo de não-contacto a sonda também oscila, mas com uma amplitude menor do que em modo de contacto intermitente. Quando a ponta se aproxima da amostra, interacções atractivas, de maior alcance, provocam alterações na frequência de oscilação da sonda, alterando a sua fase. Com a ajuda de um mecanismo de feedback, a distância entre a sonda e a superfície é ajustada de modo a não haver contacto. Este modo permite a obtenção de boas resoluções em superfícies imersas em solução, ou, se a amostra estiver ao ar, em superfícies altamente hidrofóbicas. Neste trabalho, a morfologia dos filmes foi acedida por microscopia de força atómica (AFM) através de um microscópio Nanoscope IIIa Multimode (DI Veeco) em modo tapping. Utilizaram-se pontas de silício com uma frequência de oscilação de ca. 300 khz. As imagens foram obtidas a uma velocidade de varrimento de ca. 1,5 Hz Propriedades ópticas e espessura dos filmes O crescimento de um filme de PAni 17/10 foi monitorizado através de elipsometria in-situ de modo a obterem-se os seus parâmetros ópticos e estrutura interna. A elipsometria é uma técnica espectroscópica (gama de infravermelho a ultravioleta) utilizada para obter as propriedades dieléctricas dos materiais em função da frequência. A elipsometria baseia-se na medição de alterações no estado de polarização de um feixe de luz monocromático e colimado após interacção com o material a ser estudado. Geralmente, e neste trabalho em particular, esta técnica é utilizada em modo de reflexão: a informação sobre as propriedades de uma superfície são obtidas através das diferenças no estado de polarização entre o feixe incidente, com propriedades bem definidas, e o 29
44 2. Procedimento Experimental feixe especularmente reflectido pelo material. A elipsometria é especialmente utilizada para estudar as propriedades dieléctricas de sólidos altamente absorsores e para a caracterização óptica de filmes finos. O vector do campo eléctrico de um feixe de luz que incida obliquamente numa superfície pode ser decomposto nas suas componentes paralela (p) e perpendicular (s, do alemão senkrecht) ao plano de incidência: E E p E. As componentes p e s da luz interagem de maneira diferente com o material sob análise, resultando numa alteração do estado de polarização da luz após reflecção. complexo, As propriedades ópticas de um material são descritas pelo seu índice de refracção nˆ n ik. A parte real do índice de refracção, n, está definida como a razão entre a velocidade da luz no vácuo, c, e a velocidade da luz num dado meio, v: s c n v parte imaginária, o coeficiente de extinção, k, está relacionado com o coeficiente de absorção, α, que pode ser medido por transmissão: k 4 A reflexão de luz obliquamente incidente numa interface entre dois meios anisotrópicos é controlada pelo ângulo de incidência e pelos índices de refracção complexos através das equações de Fresnel. Para a interface entre dois meios semiinfinitos como, por exemplo, a interface representada na Figura 2.4a, entre uma solução (meio a) e um eléctrodo (meio b), obtêm-se os seguintes coeficientes complexos para as componentes p e s do vector do campo eléctrico:.. A rˆ ab p nˆ nˆ a a cos b nˆ cos nˆ b b b cos a cos a e rˆ ab s nˆ nˆ b a cos b nˆ cos nˆ a a b cos a cos b (2.1) em que nˆ i é o índice de refracção complexo do meio i e i o ângulo de propagação do feixe de luz nesse meio (que é complexo para materiais absorsores), sendo os ângulos de propagação de dois meios adjacentes relacionados pela lei de Snell: nˆ a sin nˆ a b sin b (2.2) Na presença de uma terceira fase, c, com uma espessura finita, d, como o sistema representado na Figura 2.4b, o sistema passa a ser descrito pelas equações de Drude: 30
45 2. Procedimento Experimental rˆ acb p ac cb rˆ p rˆ p e 1 rˆ rˆ e ac p cb p i i e rˆ acb s rˆ 1 rˆ ac s ac rˆ s cb s cb rˆ s e i e i (2.3) em que 4π d ˆ n c cos c e nˆc ângulo de propagação dentro do filme. e c são o índice de refracção complexo do filme e o a) WE ambiente b) WE filme ambiente 1 ˆn sol 1 ˆn sol nˆ film, d film ˆn WE ˆn WE Figura 2.4 Representação esquemática de reflecção especular na interface entre uma solução electrolítica ( sol ) e um eléctrodo de trabalho (WE): a) na ausência e b) na presença de um filme fino ( film ) na superfície do WE. Experimentalmente, não é possível medir-se os coeficientes de reflexão de Fresnel das componentes p e s separadamente, mas sim a razão (complexa) entre os dois: rˆ p rˆ s (2.4) Os parâmetros elipsométricos são obtidos através dessa razão: tan e i (2.5) Sendo, assim, o ângulo azimutal, Ψ é definido como a tangente da razão entre as amplitudes dos coeficientes ( tan rˆ / ˆ p r s ) e desvio de fase, Δ, como a diferença entre as fases das componentes p e s. O par de valores registados pelo elipsómetro, Ψ,Δ, depende de vários parâmetros experimentais: dos índices de refracção de cada material, 31
46 2. Procedimento Experimental do ângulo de incidência, da(s) espessura(s) da(s) fase(s) finita(s) e do comprimento de onda da luz empregue.,, nˆ ( ), nˆ ( ), nˆ ( ),, d a b c a, (2.6) As características de um sistema (parâmetros ópticos de cada material, espessura de um filme absorsor) não podem ser obtidos analiticamente através dos parâmetros elipsométricos. Por essa razão, é necessária a utilização de programas de simulação em computador para se tratar e analisar os dados experimentais. Uma descrição mais detalhada sobre esta técnica (tipos de sistema mais estudados, estratégias para tratar os dados, formalismo matemático, etc.) encontra-se na literatura (vide referências [95 97] ). Neste trabalho utilizou-se um elipsómetro SE400 (Sentech) em modo PCSA, com um laser de He-Ne (comprimento de onda λ = 632,8 nm) a um ângulo de incidência de ϕ = 70. Os dados obtidos para os valores de potencial mais negativos (-0,200 E +0,050 V vs. SCE) foram tratados segundo um modelo de três camadas homogéneas por forma a se aceder às constantes dieléctricas e espessura dos filmes. Empregou-se uma célula electroquímica (esquematizada na Figura 2.5) de teflon com janelas em quartzo colocadas a um ângulo de 20 face à base da célula. O contra-eléctrodo consistiu numa rede de Pt e o eléctrodo de referência num SCE. O eléctrodo de trabalho foi o disco de GC descrito anteriormente. Contra-eléctrodo (rede de Pt) Janela (quartzo) ϕ = 20 C Compartimento do eléctrodo de referência Eléctrodo de trabalho (Ф = cm 2 ) Figura 2.5 Esquema da célula electroquímica utilizada para o ensaio de elipsometria insitu. 32
47 2. Procedimento Experimental 2.4. Actividade catalítica dos eléctrodos modificados para a reacção de redução do oxigénio A actividade electrocatalítica para a redução de oxigénio molecular (oxygen reduction reaction, ORR) de cada tipo de eléctrodo modificado foi avaliada em solução ácida (H2SO4 0,5 M, ph = 1). Adicionalmente, estudaram-se filmes seleccionados de PAni Fe-TSPP em soluções neutra (Na2SO4 0,5 M; ph = 6,4) e básica (Na2SO4 0,5 M + NaOH, ph = 10,4). O estudo foi efectuado por voltametria cíclica partindo do valor de potencial de circuito aberto e iniciando o varrimento no sentido catódico à velocidade de ν = 20 mv s - 1. Para remover O2 dissolvido na solução electrolítica, saturou-se a solução com N2 (Alphagaz, azoto BIP ( 99,9999%)); para reintroduzir O2, borbulhou-se ar na solução durante um período nunca inferior a 5 minutos. 33
48
49 Capitulo 3: 3. Apresentação e Discussão dos Resultados
50
51 3. Apresentação e Discussão dos Resultados 3.1. Síntese e caracterização da matriz polimérica As condições de crescimento da polianilina são determinantes para as propriedades estruturais, morfológicas, etc. destes filmes [36,37,42,50,52,53,69], controlando assim características como, por exemplo, a sua porosidade, espessura, a adesão do filme ao eléctrodo ou o tamanho e regularidade das cadeias poliméricas, que podem influenciar o desempenho dos centros catalíticos imobilizados na sua matriz. Por esse motivo, estudaram-se neste trabalho filmes de PAni sintetizados em diferentes modos e condições de crescimento por forma a se obterem eléctrodos modificados com electroactividades semelhantes mas morfologias distintas Preparação dos eléctrodos modificados Os voltamogramas cíclicos obtidos durante o crescimento potenciodinâmico da polianilina 17/10 em solução de ácido sulfúrico estão representados na Figura 3.1. No primeiro ciclo, durante o varrimento anódico, a corrente é aproximadamente nula até ao potencial E = +750 mv vs. SCE, ao qual o monómero começa a ser oxidado, resultando num aumento rápido da corrente. Quando o sentido do varrimento é invertido o processo de oxidação continua, observando-se o cruzamento das linhas voltamétricas durante os primeiros três ciclos de varrimento (vide Figura 3.1b). Este comportamento é normalmente observado durante a electropolimerização potenciodinâmica de ECPs e tradicionalmente tem sido atribuído a um processo de nucleação à superfície do eléctrodo, análogo ao que ocorre durante a electrodeposição de metais em eléctrodos de um material diferente, em que é necessária a aplicação de um sobrepotencial para que núcleos metálicos se formem à superfície do eléctrodo [98]. Contudo, alguns resultados experimentais parecem indiciar que esta característica nos voltamogramas cíclicos da electropolimerização de ECPs possa ser causada por outros processos por exemplo, em alguns casos, o cruzamento das linhas ocorre após o primeiro ciclo de crescimento, mesmo depois de o eléctrodo estar coberto de polímero. [99] Estas observações levaram ao estudo deste fenómeno e, recentemente, Heinze et al. [59] sugeriram que este efeito também poderá ser originado por uma reacção homogénea, em solução, entre o monómero no seu estado neutro, Mon, e um oligómero policatiónico, Olig n+, quando a oxidação do 37
52 i /(ma cm -2 ) 3. Apresentação e Discussão dos Resultados monómero é relativamente lenta e os potenciais redox das duas espécies estão próximos, sendo o potencial da oxidação do monómero o mais elevado. Assim, durante o primeiro varrimento anódico, formam-se espécies Olig n+, que reagem com Mon resultando em Olig (n-1)+ e Mon +. Por sua vez, o oligómero Olig (n-1)+ é re-oxidado no eléctrodo, gerando a corrente anódica observada enquanto o potencial for superior ao seu potencial de oxidação, que é inferior ao do monómero a) E vs SCE /mv i /(ma cm -2 ) b) E vs SCE /mv Figura 3.1 a) Voltamogramas cíclicos obtidos durante a síntese electroquímica do filme 17/10, e b) detalhe do primeiro ciclo; 17 ciclos, ν = 10 mv s -1 ; anilina 0,1 M, H2SO4 0,5 M. Na Figura 3.1 pode-se observar que o potencial de polimerização (valor de potencial a partir do qual se desenvolve a reacção correspondente à formação de novo material polimérico traduz-se num aumento abrupto de corrente eléctrica) se desloca sucessivamente para valores menos positivos, ocorrendo a E 750 mv no primeiro ciclo e a E 550 mv vs. SCE no 17º. Ao mesmo tempo, regista-se também um aumento da densidade de corrente no limite anódico a cada ciclo. Este efeito é atribuído a dois factores: à elevada actividade da polianilina, que catalisa o processo da sua própria formação [36,100] e, também, devido ao aumento da área superficial do eléctrodo, causado pela deposição de uma matriz porosa. Por causa desse aumento de corrente, o potencial do limite anódico de varrimento foi reduzido sistematicamente durante o crescimento do filme de modo a evitar uma sobreoxidação do mesmo. Durante o crescimento, o polímero vai sendo oxidado e reduzido a cada ciclo porque a conversão redox da polianilina ocorre a potenciais menores do que a oxidação 38
53 3. Apresentação e Discussão dos Resultados do monómero. Este comportamento é típico em polímeros condutores pois as cadeias oligoméricas e poliméricas, possuindo sistemas conjugados mais extensos, têm uma maior capacidade para estabilizar cargas, o que se reflecte num potencial de oxidação mais negativo [101]. O crescimento do filme polimérico é evidente pelo aumento de corrente nos picos correspondentes à oxidação e à redução da polianilina (Epa 150 mv, Epc 25 mv vs. SCE). O pico anódico a E 150 mv é atribuído à transição do estado reduzido de leucoesmeraldina (LE) ao estado parcialmente oxidado de esmeraldina (EM); o pico catódico a E 25 mv é atribuído à conversão inversa. [102,103] Na literatura encontram-se frequentemente picos de corrente na gama de potencial eléctrico entre 350 E 550 mv vs. SCE. A presença de respostas electroquímicas nesta gama de potenciais está associada a compostos quinóides na matriz polimérica, normalmente quinona/hidroquinona formadas durante a polimerização da anilina e incorporadas no filme durante o seu crescimento e/ou produtos de degradação da PAni, maioritariamente benzoquinona. [68,69] Na Figura 3.2 estão representados os voltamogramas obtidos durante o crescimento dos filmes PAni 200/60 e 85/10 (em HCl). Estes CVs apresentam as mesmas características descritas anteriormente sobre o filme PAni 17/10 (Figura 3.1): há, uma vez mais, um cruzamento das linhas dos varrimentos anódico e catódico nos ciclos iniciais de crescimento e um aumento da densidade de corrente perto do limite anódico de varrimento, confirmando a deposição de PAni à superfície do eléctrodo; o crescimento do filme verifica-se através do aumento da corrente dos picos redox característicos da PAni com cada ciclo. 39
54 i /(ma cm -2 ) i /(ma cm -2 ) 3. Apresentação e Discussão dos Resultados a) 200/ E vs SCE /mv b) 85/10 (HCl) E vs SCE /mv Figura 3.2 Crescimento dos filmes a) 200/60, ciclos 1, 5, 8, 15, 30, 40, 50, 60, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200; e b) 85/10 (HCl), ciclos 1, 5, 8, 15, 30, 45, 60, 75, 85. Comparando os voltamogramas dos filmes crescidos a ν = 10 mv s -1 em ácido sulfúrico (17/10, Figura 3.1a) e em ácido clorídrico (85/10, Figura 3.2b), pode-se verificar que a polianilina cresce muito mais lentamente em HCl. Esta diferença no crescimento da PAni nestes dois electrólitos é consistente com o reportado na literatura [69] e dever-se-á à formação de uma estrutura mais organizada no polímero sintetizado em ácido sulfúrico, conferindo ao material uma maior quantidade (e densidade) de centros redox e aumentando a condutividade do filme. Cresceram-se vários filmes pelo modo galvanostático, variando-se a corrente aplicada e o tempo de crescimento, de modo a optimizarem-se as condições para a formação de um eléctrodo modificado com a electroactividade pretendida. Observou-se que a aplicação de correntes mais elevadas durante o crescimento dá origem a filmes menos aderentes e com uma maior quantidade de produtos de degradação, evidentes pela presença de picos entre os potenciais 350 E 550 mv vs. SCE nos voltamogramas de caracterização. O melhor filme foi obtido através da aplicação de 50 µa (88 µa cm -2 ) durante 420 segundos (7 minutos). O cronopotenciograma do crescimento apresenta-se na Figura
55 E vs. SCE /mv 3. Apresentação e Discussão dos Resultados t /s Figura 3.3 Curva E-t obtida durante o crescimento galvanostático do filme Glv; condições de crescimento: I = 50 µa (88 µa cm -2 ), t = 420 s; anilina 0,1 M, H2SO4 0,5 M. Como se pode observar no cronopotenciograma, inicialmente há uma queda rápida no potencial (durante os primeiros 25 s, ΔE/Δt1 = -2,1 mv s -1 ) e, numa segunda fase, o declive diminui e mantém-se constante (ΔE/Δt2 = -0,1 mv s -1 ) até ao final do crescimento. Este comportamento está de acordo com o observado durante a polimerização potenciodinâmica da polianilina e com o comportamento reportado na literatura [59] : o potencial necessário para a oxidação do monómero é mais positivo durante a fase de inicial (nucleação) e desloca-se para valores mais negativos à medida que o filme cresce devido ao aumento da sua área superficial e à elevada capacidade de catalisar a sua própria formação Caracterização electroquímica Na Figura 3.4 encontram-se os voltamogramas de caracterização dos quatro tipos de filmes de polianilina estudados em solução do respectivo electrólito e na ausência de monómero. Os dados electroquímicos recolhidos com cada filme estão sumarizados na Tabela 3.1. Comparando os CVs, observa-se que apesar do filme 200/60 apresentar densidades de corrente ligeiramente mais elevadas do que os restantes, pode-se considerar que os quatro possuem electroactividades semelhantes. 41
56 i /(ma cm -2 ) 3. Apresentação e Discussão dos Resultados /10 200/60 85/10 (HCl) Glv E vs. SCE /mv Figura 3.4 Segundo ciclo de caracterização dos filmes de polianilina em solução de electrólito (0,5 M) usado durante o crescimento; ν = 50 mv s -1. Estudos de elipsometria [50,69] sugerem que quanto mais espesso for um filme, mais poroso este se torna. Assumindo que os quatro filmes tenham densidades semelhantes, os dados voltamétricos obtidos neste estudo aparentam seguir a essa tendência: quanto maiores as cargas registadas, mais próximo da unidade é a razão Qox/Qred. A razão entre a carga consumida durante a oxidação (Qox) e a carga recuperada durante a redução (Qred) pode ser considerada um indicador da porosidade de um eléctrodo modificado. Um valor de Qox/Qred > 1 reflecte uma redução incompleta do polímero e estará associado a um filme mais compacto, que dificulta a expulsão de aniões durante a descarga. A partir dos dados apresentados na Tabela 3.1, espera-se que o filme 200/60 seja o mais espesso e mais poroso (Qox = 6,59 mc cm -2, Qox/Qred = 1,01), o filme Glv o mais compacto (Qox = 3,76 mc cm -2, Qox/Qred = 1,12). Tabela 3.1 Dados electroquímicos dos voltamogramas de caracterização (2º ciclo) dos filmes de PAni apresentados na Figura 3.4. Ep a /mv vs. SCE ip a /ma cm -2 Ep c /mv vs. SCE ip c /ma cm -2 Qox /mc cm -2 Qred /mc cm -2 Q ox Q red 17/ , ,84 4,32-4,05 1,07 200/ , ,24 6,59-6,51 1,01 85/10(HCl) 180 1, ,88 4,96-4,70 1,06 Glv 182 1, ,67 3,76-3,35 1,12 42
57 3. Apresentação e Discussão dos Resultados Caracterização morfológica Morfologia Na Figura 3.5 estão representadas imagens topográficas tridimensionais de AFM dos filmes de polianilina estudados neste trabalho. Como se pode observar, os filmes têm topografias e rugosidades diferentes, sendo o filme 17/10 significativamente mais rugoso que os restantes, o filme 85/10 (HCl) o mais plano. a) 17/10 b) 200/ nm 0 nm 3 μm 150 nm 0 nm 3 μm 0 μm 0 μm c) 85/10 (HCl) d) Glv 150 nm 0 nm 200 nm 3 μm 0 nm 2 μm Figura 3.5 Imagens topográficas de AFM dos filmes de PAni a) 17/10, b) 200/60, c) 85/10 (HCl) e d) Glv. 0 μm 0 μm Na Figura 3.6 estão reproduzidas imagens de AFM de dimensões 1,5 x 1,5 μm 2 dos quatro filmes estudados nesta secção, representadas com a mesma escala de altura (0 z 150 nm). Estas micrografias revelam em detalhe as zonas mais planas de cada filme, realçando as diferenças nas suas morfologias e permitindo uma comparação dos grãos que constituem a matriz polimérica. Como se pode observar, os filmes de PAni são constituídos por formações globulares. As dimensões destes glóbulos variam entre os 43
58 3. Apresentação e Discussão dos Resultados filmes estudados, sendo ligeiramente maiores para os filmes 17/10 e 200/60 ( 70 ± 10 e 80 ± 20 nm de diâmetro, respectivamente) do que para os filmes 85/10 (HCl) e Glv ( 60 ± 10 e 50 ± 10 nm, respectivamente). No filme 17/10, os grãos menores agrupamse, formando aglomerados maiores e criando uma topografia com estrutura tipo cauliflower (couve-flor). A polianilina sintetizada na presença de HCl apresenta um alinhamento dos grãos. O filme galvanostático apresenta uma topografia mais rugosa mas mais regular que os filmes crescidos pelo modo potenciodinâmico. a) 17/10 b) 200/ nm c) 85/10 (HCl) d) Glv.. 0,5 μm.. 0 nm Figura 3.6 Imagens de AFM dos filmes de PAni a) 17/10, b) 200/60, c) 85/10 (HCl), d) Glv; escala: xy: 1,5 x 1,5 μm 2, z: 150 nm. Um dos parâmetros mais usados para avaliar a rugosidade de uma superfície é o seu desvio médio quadrático, Rq. [42,104] O valor de Rq depende de vários factores, incluindo a dimensão da amostra analisada e condições de aquisição de dados, como a forma e 44
Materiais / Materiais I
 Materiais / Materiais I Guia para o Trabalho Laboratorial n.º 4 CORROSÃO GALVÂNICA E PROTECÇÃO 1. Introdução A corrosão de um material corresponde à sua destruição ou deterioração por ataque químico em
Materiais / Materiais I Guia para o Trabalho Laboratorial n.º 4 CORROSÃO GALVÂNICA E PROTECÇÃO 1. Introdução A corrosão de um material corresponde à sua destruição ou deterioração por ataque químico em
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA
 PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
O Polarímetro na determinação de concentrações de soluções
 O Polarímetro na determinação de concentrações de soluções 1. O polarímetro Polarímetros são aparelhos que medem directamente a rotação de polarização, através da medição do ângulo de rotação de um analisador.
O Polarímetro na determinação de concentrações de soluções 1. O polarímetro Polarímetros são aparelhos que medem directamente a rotação de polarização, através da medição do ângulo de rotação de um analisador.
Análise de Circuitos com Díodos
 Teoria dos Circuitos e Fundamentos de Electrónica 1 Análise de Circuitos com Díodos Teresa Mendes de Almeida TeresaMAlmeida@ist.utl.pt DEEC Área Científica de Electrónica T.M.Almeida IST-DEEC- ACElectrónica
Teoria dos Circuitos e Fundamentos de Electrónica 1 Análise de Circuitos com Díodos Teresa Mendes de Almeida TeresaMAlmeida@ist.utl.pt DEEC Área Científica de Electrónica T.M.Almeida IST-DEEC- ACElectrónica
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia
 Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia Aluno: Julys Pablo Atayde Fernandes Células a Combustível:
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia Aluno: Julys Pablo Atayde Fernandes Células a Combustível:
Testando Nanotubos de Carbono : Sensores de Gás
 5 Testando Nanotubos de Carbono : Sensores de Gás Nos últimos anos a investigação da estrutura eletrônica de nanotubos de carbono têm atraído crescente interesse, e recentemente a síntese de nanotubos
5 Testando Nanotubos de Carbono : Sensores de Gás Nos últimos anos a investigação da estrutura eletrônica de nanotubos de carbono têm atraído crescente interesse, e recentemente a síntese de nanotubos
Medição da solubilidade de gases em líquidos iónicos com microbalança de cristais de quartzo
 Mestrado em Métodos Instrumentais e Controlo da Qualidade Analítica Medição da solubilidade de gases em líquidos iónicos com microbalança de cristais de quartzo Maria Jorge Pratas de Melo Pinto Orientador:
Mestrado em Métodos Instrumentais e Controlo da Qualidade Analítica Medição da solubilidade de gases em líquidos iónicos com microbalança de cristais de quartzo Maria Jorge Pratas de Melo Pinto Orientador:
Experiência 06 Resistores e Propriedades dos Semicondutores
 Universidade Federal de Santa Catarina Departamento de Engenharia Elétrica Laboratório de Materiais Elétricos EEL 7051 Professor Clóvis Antônio Petry Experiência 06 Resistores e Propriedades dos Semicondutores
Universidade Federal de Santa Catarina Departamento de Engenharia Elétrica Laboratório de Materiais Elétricos EEL 7051 Professor Clóvis Antônio Petry Experiência 06 Resistores e Propriedades dos Semicondutores
Detectores de incêndio Apollo
 Detector iónico de fumos Pág. 1 de 5 A parte sensível do detector consiste em duas câmaras uma câmara exterior aberta com uma câmara de referência semi-selada lá dentro. Montada dentro da câmara de referência,
Detector iónico de fumos Pág. 1 de 5 A parte sensível do detector consiste em duas câmaras uma câmara exterior aberta com uma câmara de referência semi-selada lá dentro. Montada dentro da câmara de referência,
Tutorial de Eletrônica Aplicações com 555 v2010.05
 Tutorial de Eletrônica Aplicações com 555 v2010.05 Linha de Equipamentos MEC Desenvolvidos por: Maxwell Bohr Instrumentação Eletrônica Ltda. Rua Porto Alegre, 212 Londrina PR Brasil http://www.maxwellbohr.com.br
Tutorial de Eletrônica Aplicações com 555 v2010.05 Linha de Equipamentos MEC Desenvolvidos por: Maxwell Bohr Instrumentação Eletrônica Ltda. Rua Porto Alegre, 212 Londrina PR Brasil http://www.maxwellbohr.com.br
ESTA PROVA É FORMADA POR 20 QUESTÕES EM 10 PÁGINAS. CONFIRA ANTES DE COMEÇAR E AVISE AO FISCAL SE NOTAR ALGUM ERRO.
 Nome: Assinatura: P2 de CTM 2012.2 Matrícula: Turma: ESTA PROVA É FORMADA POR 20 QUESTÕES EM 10 PÁGINAS. CONFIRA ANTES DE COMEÇAR E AVISE AO FISCAL SE NOTAR ALGUM ERRO. NÃO SERÃO ACEITAS RECLAMAÇÕES POSTERIORES..
Nome: Assinatura: P2 de CTM 2012.2 Matrícula: Turma: ESTA PROVA É FORMADA POR 20 QUESTÕES EM 10 PÁGINAS. CONFIRA ANTES DE COMEÇAR E AVISE AO FISCAL SE NOTAR ALGUM ERRO. NÃO SERÃO ACEITAS RECLAMAÇÕES POSTERIORES..
Estabilizada de. PdP. Autor: Luís Fernando Patsko Nível: Intermediário Criação: 22/02/2006 Última versão: 18/12/2006
 TUTORIAL Fonte Estabilizada de 5 Volts Autor: Luís Fernando Patsko Nível: Intermediário Criação: 22/02/2006 Última versão: 18/12/2006 PdP Pesquisa e Desenvolvimento de Produtos http://www.maxwellbohr.com.br
TUTORIAL Fonte Estabilizada de 5 Volts Autor: Luís Fernando Patsko Nível: Intermediário Criação: 22/02/2006 Última versão: 18/12/2006 PdP Pesquisa e Desenvolvimento de Produtos http://www.maxwellbohr.com.br
FICHA TÉCNICA Energia Solar Painéis Fotovoltaicos
 FICHA TÉCNICA Energia Solar Painéis Fotovoltaicos Nº Pág.s: 6 nº 04 20. Novembro. 2006 Painéis Fotovoltaicos 01 Uma das tecnologias renováveis mais promissoras e recentes de geração de energia eléctrica
FICHA TÉCNICA Energia Solar Painéis Fotovoltaicos Nº Pág.s: 6 nº 04 20. Novembro. 2006 Painéis Fotovoltaicos 01 Uma das tecnologias renováveis mais promissoras e recentes de geração de energia eléctrica
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
1 st Workshop fromthecreationproject in Research LinesofExcellence Covilhã, 18 de Novembro de 2013
 1 st Workshop fromthecreationproject in Research LinesofExcellence Covilhã, 18 de Novembro de 2013 Pedro Serra Sabrina Guia António Espírito Santo António Albuquerque 1 st Workshop fromthecreationproject
1 st Workshop fromthecreationproject in Research LinesofExcellence Covilhã, 18 de Novembro de 2013 Pedro Serra Sabrina Guia António Espírito Santo António Albuquerque 1 st Workshop fromthecreationproject
Corrosão e Protecção
 Corrosão e Protecção Capítulo 1.2 Fundamentos Docente: João Salvador Fernandes Lab. de Tecnologia lectroquímica Pavilhão de Minas, 2º Andar xt. 1964 Princípios de lectroquímica Quando se imerge uma placa
Corrosão e Protecção Capítulo 1.2 Fundamentos Docente: João Salvador Fernandes Lab. de Tecnologia lectroquímica Pavilhão de Minas, 2º Andar xt. 1964 Princípios de lectroquímica Quando se imerge uma placa
Helena Campos (Engenharia Química)
 Tipos de água Laboratorial e suas aplicações Helena Campos (Engenharia Química) 28 de Setembro de 2010 Principais contaminantes da água Particulas Suspensas: Sílica (SiO 2 ) Resíduos das tubagens Matéria
Tipos de água Laboratorial e suas aplicações Helena Campos (Engenharia Química) 28 de Setembro de 2010 Principais contaminantes da água Particulas Suspensas: Sílica (SiO 2 ) Resíduos das tubagens Matéria
CQ049 FQ IV Eletroquímica. www.quimica.ufpr.br/mvidotti. Terça/Quarta: 15:30 17:30
 CQ049 FQ IV Eletroquímica prof. Dr. Marcio Vidotti LEP Laboratório de Eletroquímica e Polímeros mvidotti@ufpr.br www.quimica.ufpr.br/mvidotti Terça/Quarta: 15:30 17:30 Espontaneidade de reações eletroquímicas
CQ049 FQ IV Eletroquímica prof. Dr. Marcio Vidotti LEP Laboratório de Eletroquímica e Polímeros mvidotti@ufpr.br www.quimica.ufpr.br/mvidotti Terça/Quarta: 15:30 17:30 Espontaneidade de reações eletroquímicas
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Informática
 Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Informática Francisco Erberto de Sousa 11111971 Saulo Bezerra Alves - 11111958 Relatório: Capacitor, Resistor, Diodo
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Informática Francisco Erberto de Sousa 11111971 Saulo Bezerra Alves - 11111958 Relatório: Capacitor, Resistor, Diodo
Disciplina de Didáctica da Química I
 Disciplina de Didáctica da Química I Texto de Apoio Concepções Alternativas em Equilíbrio Químico Autores: Susana Fonseca, João Paiva 3.2.3 Concepções alternativas em Equilíbrio Químico Tal como já foi
Disciplina de Didáctica da Química I Texto de Apoio Concepções Alternativas em Equilíbrio Químico Autores: Susana Fonseca, João Paiva 3.2.3 Concepções alternativas em Equilíbrio Químico Tal como já foi
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Como funciona um espectrofotómetro O espectrofotómetro é um aparelho
Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Como funciona um espectrofotómetro O espectrofotómetro é um aparelho
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
CONTEÚDOS OBJETIVOS PERÍODO
 ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
ENERGIA DO HIDROGÊNIO - Célula de Combustível Alcalina
 Universidade Federal do Pará Instituto de Tecnologia Programa de Pós Graduação em Engenharia Elétrica PPGEE0030 - INTRODUÇÃO ÀS ENERGIAS RENOVÁVEIS Docente: Professor Doutor João Tavares Pinho Discente:
Universidade Federal do Pará Instituto de Tecnologia Programa de Pós Graduação em Engenharia Elétrica PPGEE0030 - INTRODUÇÃO ÀS ENERGIAS RENOVÁVEIS Docente: Professor Doutor João Tavares Pinho Discente:
Corrosão Eletroquímica. Sumário 21 - Baterias e Corrosão. Definições e características Baterias primárias. Baterias secundárias
 Sumário 21 - Baterias e Corrosão Definições e características Baterias primárias Baterias de Leclanché (pilhas secas) Baterias Alcalinas Baterias de Lítio Baterias secundárias Baterias de chumbo Baterias
Sumário 21 - Baterias e Corrosão Definições e características Baterias primárias Baterias de Leclanché (pilhas secas) Baterias Alcalinas Baterias de Lítio Baterias secundárias Baterias de chumbo Baterias
DIODO SEMICONDUTOR. Conceitos Básicos. Prof. Marcelo Wendling Ago/2011
 DIODO SEMICONDUTOR Prof. Marcelo Wendling Ago/2011 Conceitos Básicos O diodo semicondutor é um componente que pode comportar-se como condutor ou isolante elétrico, dependendo da forma como a tensão é aplicada
DIODO SEMICONDUTOR Prof. Marcelo Wendling Ago/2011 Conceitos Básicos O diodo semicondutor é um componente que pode comportar-se como condutor ou isolante elétrico, dependendo da forma como a tensão é aplicada
Propriedades Físicas de alguns compostos
 Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
código 171608 AGRUPAMENTO DE ESCOLAS D. DOMINGOS JARDO Direção Regional de Educação de Lisboa
 código 7608 AGRUPAMENTO DE ESCOLAS D. DOMINGOS JARDO Direção Regional de Educação de Lisboa Ciclo: º Ano: 8º Disciplina: Físico-Química Conteúdos. Reações Químicas..Tipos de reações Investigando algumas
código 7608 AGRUPAMENTO DE ESCOLAS D. DOMINGOS JARDO Direção Regional de Educação de Lisboa Ciclo: º Ano: 8º Disciplina: Físico-Química Conteúdos. Reações Químicas..Tipos de reações Investigando algumas
Catalisadores. Substâncias que aumentam a velocidade de uma reacção sem serem consumidas
 Catalisadores Substâncias que aumentam a velocidade de uma reacção sem serem consumidas mecanismo: diminuição da barreira de energia de activação a adição de um catalisador não altera a posição de equilíbrio
Catalisadores Substâncias que aumentam a velocidade de uma reacção sem serem consumidas mecanismo: diminuição da barreira de energia de activação a adição de um catalisador não altera a posição de equilíbrio
Fenómenos Ondulatórios. Reflexão, refracção, difracção
 Fenómenos Ondulatórios Reflexão, refracção, difracção Natureza dualística da radiação electromagnética A radiação electromagnética é um fenómeno ondulatório envolvendo a propagação de um campo magnético
Fenómenos Ondulatórios Reflexão, refracção, difracção Natureza dualística da radiação electromagnética A radiação electromagnética é um fenómeno ondulatório envolvendo a propagação de um campo magnético
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B
 Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
Sistema Duplex. Vantagens e Aplicações. Luiza Abdala (luiza.abdala@vmetais.com.br) Engenheira Química - Desenvolvimento de Mercado
 Sistema Duplex Vantagens e Aplicações Luiza Abdala (luiza.abdala@vmetais.com.br) Engenheira Química - Desenvolvimento de Mercado METALURGIA Corrosão Tendência que os materiais têm de retornar ao seu estado
Sistema Duplex Vantagens e Aplicações Luiza Abdala (luiza.abdala@vmetais.com.br) Engenheira Química - Desenvolvimento de Mercado METALURGIA Corrosão Tendência que os materiais têm de retornar ao seu estado
ELETRODO OU SEMIPILHA:
 ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
LEI DE OHM. Professor João Luiz Cesarino Ferreira. Conceitos fundamentais
 LEI DE OHM Conceitos fundamentais Ao adquirir energia cinética suficiente, um elétron se transforma em um elétron livre e se desloca até colidir com um átomo. Com a colisão, ele perde parte ou toda energia
LEI DE OHM Conceitos fundamentais Ao adquirir energia cinética suficiente, um elétron se transforma em um elétron livre e se desloca até colidir com um átomo. Com a colisão, ele perde parte ou toda energia
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE
 -2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
1.3. Na figura 2 estão representados três excertos, de três situações distintas, de linhas de campo magnético. Seleccione a opção correcta.
 Escola Secundária Vitorino Nemésio Terceiro teste de avaliação de conhecimentos de Física e Química A Componente de Física 11º Ano de Escolaridade Turma C 13 de Fevereiro de 2008 Nome: Nº Classificação:
Escola Secundária Vitorino Nemésio Terceiro teste de avaliação de conhecimentos de Física e Química A Componente de Física 11º Ano de Escolaridade Turma C 13 de Fevereiro de 2008 Nome: Nº Classificação:
Os elementos de circuito que estudámos até agora foram elementos lineares. Ou seja, se duplicamos a ddp aos terminais de um
 O Díodo Os elementos de circuito que estudámos até agora foram elementos lineares. Ou seja, se duplicamos a ddp aos terminais de um componente, a intensidade da corrente eléctrica que o percorre também
O Díodo Os elementos de circuito que estudámos até agora foram elementos lineares. Ou seja, se duplicamos a ddp aos terminais de um componente, a intensidade da corrente eléctrica que o percorre também
www.e-lee.net Temática Circuitos Eléctricos Capítulo Teoria dos Circuitos COMPONENTES INTRODUÇÃO
 Temática Circuitos Eléctricos Capítulo Teoria dos Circuitos COMPONENTES INTRODUÇÃO Nesta secção, estuda-se o comportamento ideal de alguns dos dipolos que mais frequentemente se podem encontrar nos circuitos
Temática Circuitos Eléctricos Capítulo Teoria dos Circuitos COMPONENTES INTRODUÇÃO Nesta secção, estuda-se o comportamento ideal de alguns dos dipolos que mais frequentemente se podem encontrar nos circuitos
Compensação. de Factor de Potência
 Compensação de Factor de Potência oje em dia, praticamente todas as instalações eléctricas têm associadas aparelhos indutivos, nomeadamente, motores e transformadores. Este equipamentos necessitam de energia
Compensação de Factor de Potência oje em dia, praticamente todas as instalações eléctricas têm associadas aparelhos indutivos, nomeadamente, motores e transformadores. Este equipamentos necessitam de energia
ARTIGO TÉCNICO. Os objectivos do Projecto passam por:
 A metodologia do Projecto SMART MED PARKS ARTIGO TÉCNICO O Projecto SMART MED PARKS teve o seu início em Fevereiro de 2013, com o objetivo de facultar uma ferramenta analítica de confiança para apoiar
A metodologia do Projecto SMART MED PARKS ARTIGO TÉCNICO O Projecto SMART MED PARKS teve o seu início em Fevereiro de 2013, com o objetivo de facultar uma ferramenta analítica de confiança para apoiar
Diagrama de transição de Estados (DTE)
 Diagrama de transição de Estados (DTE) O DTE é uma ferramenta de modelação poderosa para descrever o comportamento do sistema dependente do tempo. A necessidade de uma ferramenta deste tipo surgiu das
Diagrama de transição de Estados (DTE) O DTE é uma ferramenta de modelação poderosa para descrever o comportamento do sistema dependente do tempo. A necessidade de uma ferramenta deste tipo surgiu das
Considerações Finais. Capítulo 8. 8.1- Principais conclusões
 Considerações Finais Capítulo 8 Capítulo 8 Considerações Finais 8.1- Principais conclusões Durante esta tese foram analisados diversos aspectos relativos à implementação, análise e optimização de sistema
Considerações Finais Capítulo 8 Capítulo 8 Considerações Finais 8.1- Principais conclusões Durante esta tese foram analisados diversos aspectos relativos à implementação, análise e optimização de sistema
Manual de funcionamento
 INSTITUTO SUPERIOR DE ENGENHARIA DE LISBOA ÁREA DEPARTAMENTAL DE ENGENHARIA DE ELECTRÓNICA E TELECOMUNICAÇÕES E DE COMPUTADORES Manual de funcionamento Setembro de 2012 Índice Índice Capítulo 1 - Medição
INSTITUTO SUPERIOR DE ENGENHARIA DE LISBOA ÁREA DEPARTAMENTAL DE ENGENHARIA DE ELECTRÓNICA E TELECOMUNICAÇÕES E DE COMPUTADORES Manual de funcionamento Setembro de 2012 Índice Índice Capítulo 1 - Medição
Universidade de Coimbra. Biosensores e Sinais Biomédicos (2007-2008)
 Universidade de Coimbra Biosensores e Sinais Biomédicos (2007-2008) Trabalho Prático N 1 ESTUDO DO COMPORTAMENTO DE SENSORES DE TEMPERATURA: Objectivo TERMOPARES E TERMÍSTORES Determinação da resposta
Universidade de Coimbra Biosensores e Sinais Biomédicos (2007-2008) Trabalho Prático N 1 ESTUDO DO COMPORTAMENTO DE SENSORES DE TEMPERATURA: Objectivo TERMOPARES E TERMÍSTORES Determinação da resposta
Capítulo 1: Eletricidade. Corrente continua: (CC ou, em inglês, DC - direct current), também chamada de
 Capítulo 1: Eletricidade É um fenômeno físico originado por cargas elétricas estáticas ou em movimento e por sua interação. Quando uma carga encontra-se em repouso, produz força sobre outras situadas em
Capítulo 1: Eletricidade É um fenômeno físico originado por cargas elétricas estáticas ou em movimento e por sua interação. Quando uma carga encontra-se em repouso, produz força sobre outras situadas em
Lista de Exercícios Espectrometria de Absorção Molecular ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS CITADOS ABAIXO.
 ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS CITADOS ABAIXO. 1 Um estudante dissolveu devidamente, 0,519 g de amostra e diluiu para 50,0 ml. Em seguida, tratou uma alíquota
ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS CITADOS ABAIXO. 1 Um estudante dissolveu devidamente, 0,519 g de amostra e diluiu para 50,0 ml. Em seguida, tratou uma alíquota
CAPÍTULO 1 MEDIÇÃO E O ERRO DE MEDIÇÃO
 CAPÍTULO 1 MEDIÇÃO E O ERRO DE MEDIÇÃO 1.1. Definições do Vocabulário Internacional de Metrologia (VIM) Metrologia: Ciência das medições [VIM 2.2]. Medição: Conjunto de operações que têm por objectivo
CAPÍTULO 1 MEDIÇÃO E O ERRO DE MEDIÇÃO 1.1. Definições do Vocabulário Internacional de Metrologia (VIM) Metrologia: Ciência das medições [VIM 2.2]. Medição: Conjunto de operações que têm por objectivo
 Termos Técnicos Ácidos Classe de substâncias que têm ph igual ou maior que 1 e menor que 7. Exemplo: sumo do limão. Átomos Todos os materiais são formados por pequenas partículas. Estas partículas chamam-se
Termos Técnicos Ácidos Classe de substâncias que têm ph igual ou maior que 1 e menor que 7. Exemplo: sumo do limão. Átomos Todos os materiais são formados por pequenas partículas. Estas partículas chamam-se
OBJETIVO Verificar as leis da Reflexão Verificar qualitativamente e quantitativamente a lei de Snell. Observar a dispersão da luz em um prisma.
 UNIVERSIDADE CATÓLICA DE BRASÍLIA CURSO DE FÍSICA LABORATÓRIO ÓPTICA REFLEXÃO E REFRAÇÃO OBJETIVO Verificar as leis da Reflexão Verificar qualitativamente e quantitativamente a lei de Snell. Observar a
UNIVERSIDADE CATÓLICA DE BRASÍLIA CURSO DE FÍSICA LABORATÓRIO ÓPTICA REFLEXÃO E REFRAÇÃO OBJETIVO Verificar as leis da Reflexão Verificar qualitativamente e quantitativamente a lei de Snell. Observar a
Exactidão da medição
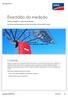 Exactidão da medição Valores energéticos e grau de rendimento dos inversores fotovoltaicos do tipo Sunny Boy e Sunny Mini Central Conteúdo Qualquer operador de um sistema fotovoltaico deseja estar o mais
Exactidão da medição Valores energéticos e grau de rendimento dos inversores fotovoltaicos do tipo Sunny Boy e Sunny Mini Central Conteúdo Qualquer operador de um sistema fotovoltaico deseja estar o mais
Caracterização temporal de circuitos: análise de transientes e regime permanente. Condições iniciais e finais e resolução de exercícios.
 Conteúdo programático: Elementos armazenadores de energia: capacitores e indutores. Revisão de características técnicas e relações V x I. Caracterização de regime permanente. Caracterização temporal de
Conteúdo programático: Elementos armazenadores de energia: capacitores e indutores. Revisão de características técnicas e relações V x I. Caracterização de regime permanente. Caracterização temporal de
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
ANEXO 14- PILHAS DE COMBUSTÍVEL
 ANEXO 14- PILHAS DE COMBUSTÍVEL 198 Conteúdo 1 Pilha de combustível... 199 1.1 O que é um elemento a combustível... 199 1.2 Princípio de funcionamento... 200 1.3 Tipos básicos de elementos a combustível...
ANEXO 14- PILHAS DE COMBUSTÍVEL 198 Conteúdo 1 Pilha de combustível... 199 1.1 O que é um elemento a combustível... 199 1.2 Princípio de funcionamento... 200 1.3 Tipos básicos de elementos a combustível...
Modelo Cascata ou Clássico
 Modelo Cascata ou Clássico INTRODUÇÃO O modelo clássico ou cascata, que também é conhecido por abordagem top-down, foi proposto por Royce em 1970. Até meados da década de 1980 foi o único modelo com aceitação
Modelo Cascata ou Clássico INTRODUÇÃO O modelo clássico ou cascata, que também é conhecido por abordagem top-down, foi proposto por Royce em 1970. Até meados da década de 1980 foi o único modelo com aceitação
UPS. Unidades de Alimentação Ininterrupta
 UPS Uma UPS é um dispositivo que, quando em funcionamento correcto, ajuda a garantir que a alimentação dos equipamentos que estão a ela ligados, não sejam perturbados, fornecendo energia, através de uma
UPS Uma UPS é um dispositivo que, quando em funcionamento correcto, ajuda a garantir que a alimentação dos equipamentos que estão a ela ligados, não sejam perturbados, fornecendo energia, através de uma
4 Segmentação. 4.1. Algoritmo proposto
 4 Segmentação Este capítulo apresenta primeiramente o algoritmo proposto para a segmentação do áudio em detalhes. Em seguida, são analisadas as inovações apresentadas. É importante mencionar que as mudanças
4 Segmentação Este capítulo apresenta primeiramente o algoritmo proposto para a segmentação do áudio em detalhes. Em seguida, são analisadas as inovações apresentadas. É importante mencionar que as mudanças
QUÍMICA Disciplina A Disciplina B Código Disciplina C/H Curso Disciplina C/H Código Curso Ano do Currículo 1ª período
 QUÍMICA Código Disciplina C/H Curso Disciplina C/H Código Curso Ano do Conclusão 74471 Química Estrutural 34 Química Química Inorgânica para Ciências Farmacêuticas OU 68 68977 Ciências Farmacêuticas 2008
QUÍMICA Código Disciplina C/H Curso Disciplina C/H Código Curso Ano do Conclusão 74471 Química Estrutural 34 Química Química Inorgânica para Ciências Farmacêuticas OU 68 68977 Ciências Farmacêuticas 2008
Energia, tecnologia e política climática: perspectivas mundiais para 2030 MENSAGENS-CHAVE
 Energia, tecnologia e política climática: perspectivas mundiais para 2030 MENSAGENS-CHAVE Cenário de referência O estudo WETO apresenta um cenário de referência que descreve a futura situação energética
Energia, tecnologia e política climática: perspectivas mundiais para 2030 MENSAGENS-CHAVE Cenário de referência O estudo WETO apresenta um cenário de referência que descreve a futura situação energética
Prof. Rogério Eletrônica Geral 1
 Prof. Rogério Eletrônica Geral 1 Apostila 2 Diodos 2 COMPONENTES SEMICONDUTORES 1-Diodos Um diodo semicondutor é uma estrutura P-N que, dentro de seus limites de tensão e de corrente, permite a passagem
Prof. Rogério Eletrônica Geral 1 Apostila 2 Diodos 2 COMPONENTES SEMICONDUTORES 1-Diodos Um diodo semicondutor é uma estrutura P-N que, dentro de seus limites de tensão e de corrente, permite a passagem
Escola Secundária Dr. Manuel Gomes de Almeida
 Escola Secundária Dr. Manuel Gomes de Almeida Ficha de trabalho de Biologia - 12º Ano Fermentação e actividade enzimática Nome: N º: Turma: Data: 1. A figura 1 representa um tipo de fermentação. Figura
Escola Secundária Dr. Manuel Gomes de Almeida Ficha de trabalho de Biologia - 12º Ano Fermentação e actividade enzimática Nome: N º: Turma: Data: 1. A figura 1 representa um tipo de fermentação. Figura
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007
 Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS
 TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
DIODOS. Professor João Luiz Cesarino Ferreira
 DIODOS A união de um cristal tipo p e um cristal tipo n, obtém-se uma junção pn, que é um dispositivo de estado sólido simples: o diodo semicondutor de junção. Figura 1 Devido a repulsão mútua os elétrons
DIODOS A união de um cristal tipo p e um cristal tipo n, obtém-se uma junção pn, que é um dispositivo de estado sólido simples: o diodo semicondutor de junção. Figura 1 Devido a repulsão mútua os elétrons
ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl]
![ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl] ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl]](/thumbs/26/8060460.jpg) TRABALHO 3 ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl] 1. OBJECTIVO Estudo da cinética da reacção de hidrólise ácida do composto Trans-[Co(en) 2 Cl 2 ]Cl. Determinação
TRABALHO 3 ESTUDO DA CINÉTICA DE HIDRÓLISE ÁCIDA DO COMPOSTO Trans-[(Co(en) 2 Cl 2 )Cl] 1. OBJECTIVO Estudo da cinética da reacção de hidrólise ácida do composto Trans-[Co(en) 2 Cl 2 ]Cl. Determinação
Departamento de Matemática - UEL - 2010. Ulysses Sodré. http://www.mat.uel.br/matessencial/ Arquivo: minimaxi.tex - Londrina-PR, 29 de Junho de 2010.
 Matemática Essencial Extremos de funções reais Departamento de Matemática - UEL - 2010 Conteúdo Ulysses Sodré http://www.mat.uel.br/matessencial/ Arquivo: minimaxi.tex - Londrina-PR, 29 de Junho de 2010.
Matemática Essencial Extremos de funções reais Departamento de Matemática - UEL - 2010 Conteúdo Ulysses Sodré http://www.mat.uel.br/matessencial/ Arquivo: minimaxi.tex - Londrina-PR, 29 de Junho de 2010.
DETERMINAÇÃO DA RESISTÊNCIA INTERNA DE UMA PILHA
 TLHO PÁTCO DETEMNÇÃO D ESSTÊNC NTEN DE UM PLH Objectivo Este trabalho compreende as seguintes partes: comparação entre as resistências internas de dois voltímetros, um analógico e um digital; medida da
TLHO PÁTCO DETEMNÇÃO D ESSTÊNC NTEN DE UM PLH Objectivo Este trabalho compreende as seguintes partes: comparação entre as resistências internas de dois voltímetros, um analógico e um digital; medida da
CAPACITORES. Vestibular1 A melhor ajuda ao vestibulando na Internet Acesse Agora! www.vestibular1.com.br
 CAPACITORES DEFINIÇÕES Quando as placas do capacitor estão carregadas com cargas iguais e de sinais diferentes, estabelece-se entre as placas uma diferença de potencial V que é proporcional à carga. Q
CAPACITORES DEFINIÇÕES Quando as placas do capacitor estão carregadas com cargas iguais e de sinais diferentes, estabelece-se entre as placas uma diferença de potencial V que é proporcional à carga. Q
Ligações Químicas Ligação Iônica Ligação Metálica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Separação de Misturas
 1. Introdução Separação de Misturas As misturas são comuns em nosso dia a dia. Como exemplo temos: as bebidas, os combustíveis, e a própria terra em que pisamos. Poucos materiais são encontrados puros.
1. Introdução Separação de Misturas As misturas são comuns em nosso dia a dia. Como exemplo temos: as bebidas, os combustíveis, e a própria terra em que pisamos. Poucos materiais são encontrados puros.
Armazenamento de energia
 Universidade do Vale do Rio dos Sinos UNISINOS Programa de Pós-Graduação em Engenharia Mecânica 3 º. trimestre, 2015 A energia solar é uma fonte de energia dependente do tempo. As necessidades de energia
Universidade do Vale do Rio dos Sinos UNISINOS Programa de Pós-Graduação em Engenharia Mecânica 3 º. trimestre, 2015 A energia solar é uma fonte de energia dependente do tempo. As necessidades de energia
RELAÇÃO DO TEMPO DE SINTERIZAÇÃO NA DENSIFICAÇÃO E CONDUTIVIDADE ELÉTRICA EM CÉLULAS À COMBUSTÍVEL. Prof. Dr. Ariston da Silva Melo Júnior
 RELAÇÃO DO TEMPO DE SINTERIZAÇÃO NA DENSIFICAÇÃO E CONDUTIVIDADE ELÉTRICA EM CÉLULAS À COMBUSTÍVEL Prof. Dr. Ariston da Silva Melo Júnior INTRODUÇÃO Célula à combustível é um material eletroquimico em
RELAÇÃO DO TEMPO DE SINTERIZAÇÃO NA DENSIFICAÇÃO E CONDUTIVIDADE ELÉTRICA EM CÉLULAS À COMBUSTÍVEL Prof. Dr. Ariston da Silva Melo Júnior INTRODUÇÃO Célula à combustível é um material eletroquimico em
Sensores Ultrasônicos
 Sensores Ultrasônicos Introdução A maioria dos transdutores de ultra-som utiliza materiais piezelétricos para converter energia elétrica em mecânica e vice-versa. Um transdutor de Ultra-som é basicamente
Sensores Ultrasônicos Introdução A maioria dos transdutores de ultra-som utiliza materiais piezelétricos para converter energia elétrica em mecânica e vice-versa. Um transdutor de Ultra-som é basicamente
CONHECIMENTOS ESPECÍFICOS TÉCNICO EM ELETRÔNICA
 CONHECIMENTOS ESPECÍFICOS TÉCNICO EM ELETRÔNICA 26. Com relação aos materiais semicondutores, utilizados na fabricação de componentes eletrônicos, analise as afirmativas abaixo. I. Os materiais semicondutores
CONHECIMENTOS ESPECÍFICOS TÉCNICO EM ELETRÔNICA 26. Com relação aos materiais semicondutores, utilizados na fabricação de componentes eletrônicos, analise as afirmativas abaixo. I. Os materiais semicondutores
Microfone e altifalante. Conversão de um sinal sonoro num sinal elétrico. sinal elétrico num sinal sonoro.
 Microfone e altifalante Conversão de um sinal sonoro num sinal elétrico. Conversão de um sinal elétrico num sinal sonoro. O funcionamento dos microfones e dos altifalantes baseia-se na: - acústica; - no
Microfone e altifalante Conversão de um sinal sonoro num sinal elétrico. Conversão de um sinal elétrico num sinal sonoro. O funcionamento dos microfones e dos altifalantes baseia-se na: - acústica; - no
DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA PERMEABILIDADE DAS MEMBRANAS CELULARES
 DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA FISIOLOGIA ANIMAL II AULA 4 PERMEABILIDADE DAS MEMBRANAS CELULARES CAETANA CARVALHO, PAULO SANTOS 2006 1 INTRODUÇÃO As
DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA FISIOLOGIA ANIMAL II AULA 4 PERMEABILIDADE DAS MEMBRANAS CELULARES CAETANA CARVALHO, PAULO SANTOS 2006 1 INTRODUÇÃO As
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X
 DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
Reações a altas temperaturas. Diagrama de Equilíbrio
 Reações a altas temperaturas Diagrama de Equilíbrio Propriedades de um corpo cerâmico Determinadas pelas propriedades de cada fase presente e pelo modo com que essas fases (incluindo a porosidade) estão
Reações a altas temperaturas Diagrama de Equilíbrio Propriedades de um corpo cerâmico Determinadas pelas propriedades de cada fase presente e pelo modo com que essas fases (incluindo a porosidade) estão
B) (até três pontos) Para os pares de espécies apresentados em i, ii e iii, tem-se, respectivamente, Al +, F - e Li.
 Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
Eficiência na Produção de Hidrogénio por Electrólise. Paulo S.D. Brito
 Bioenergia Portugal 2015 Portalegre, 28/05/2015 Eficiência na Produção de Hidrogénio por Electrólise Paulo S.D. Brito 28 de Maio 2015 Tópicos 1. Enquadramento 2. Armazenamento de energia 3. Eléctrodos
Bioenergia Portugal 2015 Portalegre, 28/05/2015 Eficiência na Produção de Hidrogénio por Electrólise Paulo S.D. Brito 28 de Maio 2015 Tópicos 1. Enquadramento 2. Armazenamento de energia 3. Eléctrodos
CIRCUITOS E SISTEMAS ELECTRÓNICOS
 INSTITUTO SUPERIOR DE CIÊNCIAS DO TRABALHO E DA EMPRESA Enunciado do 2º Trabalho de Laboratório CIRCUITOS E SISTEMAS ELECTRÓNICOS MODELAÇÃO E SIMULAÇÃO DE CIRCUITOS DE CONVERSÃO ANALÓGICO-DIGITAL E DIGITAL-ANALÓGICO
INSTITUTO SUPERIOR DE CIÊNCIAS DO TRABALHO E DA EMPRESA Enunciado do 2º Trabalho de Laboratório CIRCUITOS E SISTEMAS ELECTRÓNICOS MODELAÇÃO E SIMULAÇÃO DE CIRCUITOS DE CONVERSÃO ANALÓGICO-DIGITAL E DIGITAL-ANALÓGICO
Problemas de Termodinâmica e Estrutura da Matéria
 Problemas de Termodinâmica e Estrutura da Matéria 5 a série 5.1) O filamento de tungsténio de uma lâmpada incandescente está à temperatura de 800 C. Determine o comprimento de onda da radiação emitida
Problemas de Termodinâmica e Estrutura da Matéria 5 a série 5.1) O filamento de tungsténio de uma lâmpada incandescente está à temperatura de 800 C. Determine o comprimento de onda da radiação emitida
Fontes de Alimentação
 Fontes de Alimentação As fontes de alimentação servem para fornecer energia eléctrica, transformando a corrente alternada da rede pública em corrente contínua. Estabilizam a tensão, ou seja, mesmo que
Fontes de Alimentação As fontes de alimentação servem para fornecer energia eléctrica, transformando a corrente alternada da rede pública em corrente contínua. Estabilizam a tensão, ou seja, mesmo que
Estequiometria. Prof a. Dr a. Flaviana Tavares Vieira
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
ANÁLISE QUÍMICA INSTRUMENTAL
 ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
ANÁLISE QUÍMICA INSTRUMENTAL CROMATOGRAFIA 2 1 6 Ed. Cap. 10 268-294 6 Ed. Cap. 6 Pg.209-219 6 Ed. Cap. 28 Pg.756-829 6 Ed. Cap. 21 Pg.483-501 3 Separação Química Princípios de uma separação. Uma mistura
EXPERIMENTO N o 6 LENTES CONVERGENTES INTRODUÇÃO
 EXPERIMENTO N o 6 LENTES CONVERGENTES INTRODUÇÃO Ao incidir em uma lente convergente, um feixe paralelo de luz, depois de passar pela lente, é concentrado em um ponto denominado foco (representado por
EXPERIMENTO N o 6 LENTES CONVERGENTES INTRODUÇÃO Ao incidir em uma lente convergente, um feixe paralelo de luz, depois de passar pela lente, é concentrado em um ponto denominado foco (representado por
Qual o efeito da radiação solar na evaporação da água?
 16 Qual o efeito da radiação solar na evaporação da água? E16-1 o que necessitas coador holofote com uma potência de 500 w filtros de café frasco com água salgada (do mar ou de qualquer compartimento da
16 Qual o efeito da radiação solar na evaporação da água? E16-1 o que necessitas coador holofote com uma potência de 500 w filtros de café frasco com água salgada (do mar ou de qualquer compartimento da
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
Descobertas do electromagnetismo e a comunicação
 Descobertas do electromagnetismo e a comunicação Porque é importante comunicar? - Desde o «início dos tempos» que o progresso e o bem estar das sociedades depende da sua capacidade de comunicar e aceder
Descobertas do electromagnetismo e a comunicação Porque é importante comunicar? - Desde o «início dos tempos» que o progresso e o bem estar das sociedades depende da sua capacidade de comunicar e aceder
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA
 SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
Modos de Propagação. Tecnologia em Redes de Computadores 5º Período Disciplina: Sistemas e Redes Ópticas Prof. Maria de Fátima F.
 Modos de Propagação Tecnologia em Redes de Computadores 5º Período Disciplina: Sistemas e Redes Ópticas Prof. Maria de Fátima F. Bueno Marcílio 1 Modos de Propagação Antes de iniciarmos o estudo dos tipos
Modos de Propagação Tecnologia em Redes de Computadores 5º Período Disciplina: Sistemas e Redes Ópticas Prof. Maria de Fátima F. Bueno Marcílio 1 Modos de Propagação Antes de iniciarmos o estudo dos tipos
Espectometriade Fluorescência de Raios-X
 FRX Espectometriade Fluorescência de Raios-X Prof. Márcio Antônio Fiori Prof. Jacir Dal Magro FEG Conceito A espectrometria de fluorescência de raios-x é uma técnica não destrutiva que permite identificar
FRX Espectometriade Fluorescência de Raios-X Prof. Márcio Antônio Fiori Prof. Jacir Dal Magro FEG Conceito A espectrometria de fluorescência de raios-x é uma técnica não destrutiva que permite identificar
Transições de Fase de Substâncias Simples
 Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Ivan Guilhon Mitoso Rocha. As grandezas fundamentais que serão adotadas por nós daqui em frente:
 Rumo ao ITA Física Análise Dimensional Ivan Guilhon Mitoso Rocha A análise dimensional é um assunto básico que estuda as grandezas físicas em geral, com respeito a suas unidades de medida. Como as grandezas
Rumo ao ITA Física Análise Dimensional Ivan Guilhon Mitoso Rocha A análise dimensional é um assunto básico que estuda as grandezas físicas em geral, com respeito a suas unidades de medida. Como as grandezas
TIPOS DE termômetros. e termômetros ESPECIAIS. Pirômetros ópticos
 Pirômetros ópticos TIPOS DE termômetros e termômetros ESPECIAIS A ideia de construir um pirômetro óptico surgiu em meados do século XIX como consequência dos estudos da radiação dos sólidos aquecidos.
Pirômetros ópticos TIPOS DE termômetros e termômetros ESPECIAIS A ideia de construir um pirômetro óptico surgiu em meados do século XIX como consequência dos estudos da radiação dos sólidos aquecidos.
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09
 Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
ISO 9000:2000 Sistemas de Gestão da Qualidade Fundamentos e Vocabulário. As Normas da família ISO 9000. As Normas da família ISO 9000
 ISO 9000:2000 Sistemas de Gestão da Qualidade Fundamentos e Vocabulário Gestão da Qualidade 2005 1 As Normas da família ISO 9000 ISO 9000 descreve os fundamentos de sistemas de gestão da qualidade e especifica
ISO 9000:2000 Sistemas de Gestão da Qualidade Fundamentos e Vocabulário Gestão da Qualidade 2005 1 As Normas da família ISO 9000 ISO 9000 descreve os fundamentos de sistemas de gestão da qualidade e especifica
Hidrogênio x Hidrogênio Hidrogênio x Não metal Não metal x Não metal
 LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
ENSAIOS MECÂNICOS Permitem perceber como os materiais se comportam quando lhes são aplicados esforços
 ENSAIOS MECÂNICOS Permitem perceber como os materiais se comportam quando lhes são aplicados esforços Tipos Ensaios Destrutivos provocam a inutilização do material ensaiado Ensaios Não Destrutivos Ensaio
ENSAIOS MECÂNICOS Permitem perceber como os materiais se comportam quando lhes são aplicados esforços Tipos Ensaios Destrutivos provocam a inutilização do material ensaiado Ensaios Não Destrutivos Ensaio
