MODELO PROBABILÍSTICO DE AGREGADO PARA DENSIDADE DE MISTURAS AQUOSAS ORGÂNICAS
|
|
|
- Isabella Gorjão Van Der Vinne
- 6 Há anos
- Visualizações:
Transcrição
1 MODELO PROBABILÍSTICO DE AGREGADO PARA DENSIDADE DE MISTURAS AQUOSAS ORGÂNICAS Aluno: César Felipe Salomão Blanco Orientador: Maria Matos Colaborador: L.C. Scavarda do Carmo Resumo Neste trabalho foi desenvolvido um modelo para o cálculo da densidade das misturas orgânicas água-etanol, água-metanol, água-1-propanol, água-2-propanol, água-ácido acético, água-ácido fórmico e água-glicerina. O modelo assume que a interação do soluto com o solvente gera uma terceira espécie de molécula, o agregado. Este consta de uma ligação molecular binária soluto-solvente, com volume molecular menor que a soma dos volumes moleculares respectivos. A motivação para este estudo vem do fato de que o volume da mistura, para todas as concentrações, está sempre abaixo da relação linear volumeconcentração, esperada. Foram obtidos resultados muito promissores, claramente melhores que os obtidos com o modelo linear, apesar de o modelo de agregado conter ainda bastante espaço para futuras melhorias e adequações. Introdução Nossa intenção com a pesquisa é compreender melhor as interações que ocorrem nas misturas descritas acima. Alem disso, queremos testar o modelo de agregado para determinar se ele é, de fato, um modelo que aproxima o valor da densidade da mistura para várias concentrações de soluto. Após esse trabalho inicial poderíamos melhorar o modelo proposto, incluindo algumas correções, o que poderia trazer melhor descrição dos dados experimentais. Começaremos com um estudo do modelo linear, modelo este que não considera a interação soluto-solvente e depois estudaremos, descrevendo-o, o modelo de agregado. Faremos um ajuste de curvas visando à obtenção dos parâmetros do modelo de agregado e discutiremos em seguida possíveis melhorias e correções. O programa utilizado para o gerenciamento de dados e criação dos gráficos foi o Maple 10. Além deste foram utilizados em pequena escala o programa DrScheme, o editor de programas C SciTe e o compilador GCC. Os dados utilizados virão de tabelas experimentais [1] referentes às misturas acima mencionadas. Modelo linear Começaremos o trabalho analisando o modelo linear. Neste modelo consideraremos que não existe uma interação entre soluto-solvente, ou seja, tratamos a densidade da mistura como se estivéssemos tratando o soluto e o solvente individualmente. A densidade de qualquer substância é uma fração simples: m ρ = V Onde m representa a massa e V o volume. Podemos escrever essa relação em termos microscópicos se tomarmos as seguintes definições: M - massa normalizada do experimento (no nosso caso 1000g [1]); m s - massa molecular do soluto; m w - massa molecular do
2 solvente; v s - volume molecular do soluto; v w - volume molecular do solvente; a - concentração de soluto na mistura (varia de 0 até 1). 1 ρ = 1 1 αvs + (1 α ) vw m m s w Eliminando M e ajustando a fração: mm s w ρ = mwαvs + ms(1 α) vw Conhecendo os volumes e as massas moleculares das substâncias [1], ficamos com uma dependência em a que é nossa concentração de soluto. Podemos traçar o gráfico do modelo linear em contraste com o experimento para todas as substâncias: 1-PROPANOL
3 2-PROPANOL ETANOL
4 METANOL ÁCIDO ACÉTICO
5 ÁCIDO FÓRMICO GLICERINA Podemos notar que em todos os gráficos não há concordância do modelo linear com o experimento, sendo mais satisfatória na glicerina. Para melhor ilustrar o modelo linear traçamos o gráfico do inverso da densidade. Note que 1/? é uma função linear em a:
6 1 mwαvs + ms(1 α) vw = ρ mm 1 mwαvs + ms αvm w s ρ = w w mm s s 1 1 ( mv w s vm w s) = + α ρ m mm w w s A linearidade acima verificada reflete a hipótese do modelo linear de que a mistura não altera os volumes moleculares individuais. Traçamos, então, os gráficos do inverso da densidade para todas as misturas utilizando o modelo linear em comparação com o experimento: 1-PROPANOL
7 2-PROPANOL ETANOL
8 METANOL ÁCIDO ACÉTICO
9 ÁCIDO FÓRMICO GLICERINA Nesta última série de gráficos usamos escalas diferentes no eixo vertical, visando relacionar a discrepância teoria-experimento com a diferença entre as densidades de cada líquido da mistura binária. Note que em todos os gráficos a curva experimental segue por baixo da reta do modelo linear o que nos leva a acreditar que existe algum tipo de redução no
10 volume da mistura, base do nosso modelo de agregado proposto. Pode-se também notar uma maior discordância teoria-experimento na mistura água-ácido acético. Modelo de agregado Após notarmos o comportamento do volume da mistura em comparação ao modelo linear propomos um novo modelo que tem como suposição principal o fato de que existe uma interação entre as moléculas do soluto e do solvente e que essa interação gera uma nova molécula o agregado. Este agregado tem volume molecular menor do que a soma dos volumes moleculares do soluto e do solvente, sendo consistente com os dados experimentais. Iremos precisar de uma aproximação de quantos agregados existem na mistura para dada concentração de soluto, para tal criaremos duas funções P e Q. P representará a probabilidade de um soluto se ligar com um solvente formando um agregado e Q nos dirá quantos agregados efetivamente existem na mistura dada concentração do soluto. P é a fração do número de moléculas de solvente sobre o número total de moléculas na mistura, ou seja, é a probabilidade de um soluto encontrar um solvente na mistura. M (1 α) P m = (1 ) w M α M α + m m w s P = (1 α) m (1 α) w α + m m w s Q é o número de moléculas de soluto na mistura multiplicados pela probabilidade delas se ligarem P: Mα Q = P ms Essa grandeza representa o número de agregados formados. Com Q podemos construir a densidade no modelo de agregado, mas antes vamos introduzir um fator de redução f que irá variar de 0 até 1. Este fator se faz necessário já que não sabemos o volume molecular do agregado. A massa molecular do agregado, m a, é igual à soma das massas moleculares do soluto e do solvente e seu volume, v a, sofre redução de acordo com o fator f: ma = ms + mw v = f( v + v ) a s w Agora podemos escrever a densidade partindo da fórmula simples, de massa sobre volume: M ρ = M M [( α) Qv ] s + {[ (1 α)] Qv } w+ Qf( vw+ vs) m m s w
11 M ρ = M M Mα [( α) Qv ] s + {[ (1 α)] Qv } w+ Pf ( vw + vs) m m m s w s M ρ = M Mα M M α Mα [( α) Pv ] s + {[ (1 α)] Pv } w+ Pf( vw+ vs) m m m m m s s w s s 1 ρ = 1 α 1 α α [( α) Pv ] s+ {[ (1 α)] Pv } w + Pf ( vw + vs) m m m m m s s w s s A fórmula final independe de M, o que era esperado, pois o modelo não pode depender da massa da amostra escolhida para o experimento. Temos a densidade que depende de a, f e P, mas P depende diretamente de a, portanto, a densidade depende apenas de a e f. Faremos agora um ajuste de curvas para a obtenção do parâmetro f. A obtenção deste parâmetro é feita através um programa escrito no Maple 10 da seguinte forma: para cada ponto do experimento é feita a busca de um parâmetro f que ajuste o valor experimental ao valor teórico; de ponto a ponto o programa vai buscando os melhores fatores f; supomos que cada um desses pontos tem o mesmo peso para o ajuste final da curva. Tomamos então a soma de todos os f s encontrados e dividimos pelo número de pontos da curva experimental, tendo assim um fator f médio. Este procedimento de ajuste foi aplicado a todas as curvas e foram encontrados os seguintes f médios: água-etanol - f=0,938; água-metanol - 0,940; água-1-propanol - 0,970; água-2-propanol - 0,960; água-ácido acético - 0,938; água-ácido fórmico - 0,970; águaglicerina - 0,980. Com estes valores podemos traçar os gráficos do modelo de agregado em comparação com o experimento.
12 1-PROPANOL 2-PROPANOL
13 ETANOL METANOL
14 ÁCIDO ACÉTICO ÁCIDO FÓRMICO
15 GLICERINA Podemos notar que há uma concordância extremamente boa com o experimento, muito melhor do que o modelo linear. Note especialmente o resultado da comparação para o ácido acético, que apresentou maior discrepância para o modelo linear. Discrepância do modelo linear e propriedades macroscópicas das misturas A fim de compreender melhor os distintos comportamentos das misturas estudadas e as discrepâncias observadas em relação ao modelo linear fizemos uma análise para averiguar as propriedades macroscópicas de cada líquido, o objetivo é tentar correlacionar essas propriedades com algumas características das curvas experimentais de densidade como função da concentração. O resultado encontra-se na tabela a seguir.
16 ///////////////// a D1 D2 MM1/MM2 v1/v2 1-Propanol 30 Graus Propanol 30 Graus Ácido Acético 25 Graus Ácido Fórmico 20 Graus Etanol 25 Graus Glicerina 30 Graus Metanol 20 Graus Onde: a: concentração onde ocorre D1. D1 é o desvio máximo entre a densidade da mistura e a densidade do modelo linear. D2 é o desvio máximo entre a densidade da mistura e a densidade da água. MM1: massa molar do soluto, MM2: massa molar do solvente. v1: volume molecular do soluto, v2: volume molecular do solvente. Não foi encontrada uma correlação clara entre as propriedades dos líquidos (D2, MM1, MM2, v1, v2) e o comportamento das misturas (D1). Análise do modelo de agregado Numa tentativa de compreender melhor o papel do fator de redução volumétrica nas misturas líquidas estudadas foram feitos os gráficos da variação de f com a concentração, dado que, se o modelo de agregado for consistente, tal variação não deveria ser grande. Os gráficos a seguir mostram o comportamento de f como função da concentração para cada mistura.
17 1-PROPANOL 2-PROPANOL
18 ETANOL METANOL
19 ÁCIDO ACÉTICO ÁCIDO FÓRMICO
20 GLICERINA Podemos notar que f não se mantém constante em nenhum dos gráficos. Para o ácido fórmico esse fator se comporta de forma mais satisfatória, sem variações significativas. O interessante nesses gráficos é que podemos notar semelhanças entre alguns eles. Note que para os propanóis, o etanol e o metanol observa-se uma queda seguida de um pico, sendo que no metanol isso não fica tão claro quanto nos outros, mas existe. Os ácidos acético e fórmico se comportam de formas semelhantes e diferentemente dos álcoois, apesar do ácido acético apresentar um pico mais proeminente. Para a glicerina o fator f é sempre crescente. Com a análise acima podemos separar nossas misturas em três grupos, que são os álcoois, os ácidos e a glicerina. Isso pode estar nos dizendo que existe uma propriedade intrínseca de cada grupo a qual poderia explicar a forma na qual os agregados são formados. Acreditamos que esse resultado merece análise mais aprofundada a qual pretendemos realizar na etapa seguinte deste trabalho. Conclusão Neste trabalho desenvolvemos um modelo que leva em conta a interação solutosolvente de misturas líquidas binárias, o modelo de agregado molecular. Observou-se que o modelo se ajusta bastante bem às curvas de densidade de diferentes misturas líquidas, melhorando consideravelmente a descrição do comportamento dessas misturas em relação ao modelo linear. Um aspecto do modelo de agregado que deve ser considerado é o fato de termos usado uma probabilidade simples, desconsiderando a geometria das moléculas, por exemplo. O modelo permite, no entanto, o uso de outras funções de probabilidade. Outro aspecto do modelo de agregado é o fato de termos, por hipótese, suposto apenas agregados binários soluto-solvente, sem levar em consideração a existências de outros tipos de agregado como, por exemplo, agregados soluto-solvente-soluto ou outros.
21 Na segunda etapa da pesquisa serão analisados esses aspectos de modo a propor-se a direção a ser seguida visando possivelmente uma melhor compreensão sobre o comportamento microscópico das misturas. Referências 1 PERRY, R. H.; GREEN, D. W. Perry s Chemical Engineers Handbook. 7.ed. McGraw-Hill, p.
ESTUDO DA SOLUBILIDADE DO PARACETAMOL EM ALGUNS SOLVENTES UTILIZANDO O MODELO NRTL
 ESTUDO DA SOLUBILIDADE DO PARACETAMOL EM ALGUNS SOLVENTES UTILIZANDO O MODELO NRTL H. A. R. GOMES 1, A. B. N. BRITO 1 1 Universidade Federal do Espírito Santo, Centro Universitário Norte do Espírito Santo,
ESTUDO DA SOLUBILIDADE DO PARACETAMOL EM ALGUNS SOLVENTES UTILIZANDO O MODELO NRTL H. A. R. GOMES 1, A. B. N. BRITO 1 1 Universidade Federal do Espírito Santo, Centro Universitário Norte do Espírito Santo,
META Determinar o volume molar parcial de uma mistura binária de água/etanol pela medida de diferentes composições da mistura.
 QUANTIDADES PARCIAIS MOLARES META Determinar o volume molar parcial de uma mistura binária de água/etanol pela medida de diferentes composições da mistura. OBJETIVOS Ao final desta aula, o aluno deverá:
QUANTIDADES PARCIAIS MOLARES META Determinar o volume molar parcial de uma mistura binária de água/etanol pela medida de diferentes composições da mistura. OBJETIVOS Ao final desta aula, o aluno deverá:
Volume Parcial Molar
 Volume Parcial Molar 1. Introdução O volume molar é definido como o volume ocupado por 1 mol de uma substância pura. Por exemplo, o volume molar da água pura é 18 cm 3 /mol, conforme mostrado no cálculo
Volume Parcial Molar 1. Introdução O volume molar é definido como o volume ocupado por 1 mol de uma substância pura. Por exemplo, o volume molar da água pura é 18 cm 3 /mol, conforme mostrado no cálculo
GASES. https://www.youtube.com/watch?v=wtmmvs3uiv0. David P. White. QUÍMICA: A Ciência Central 9ª Edição Capítulo by Pearson Education
 GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
GASES PV nrt https://www.youtube.com/watch?v=wtmmvs3uiv0 David P. White QUÍMICA: A Ciência Central 9ª Edição volume, pressão e temperatura Um gás consiste em átomos (individualmente ou ligados formando
Óptica Física - Índice de Refração
 Óptica Física - Índice de Refração O desvio que a luz sofre quando passa de um meio para outro, depende da velocidade da luz nos dois meios. A grandeza física que relaciona as velocidades nos dois meios,
Óptica Física - Índice de Refração O desvio que a luz sofre quando passa de um meio para outro, depende da velocidade da luz nos dois meios. A grandeza física que relaciona as velocidades nos dois meios,
5ª LISTA - EXERCÍCIOS DE PROVAS Lei de Raoult
 Pg. 1/6 1 a Questão Metanol, CH 4 O, e etanol, C 2 H 6 O, são dois álcoois voláteis a 25 C. Ambos podem ser usados como solvente ou combustível e muitas vezes a mistura dos dois é empregada em processos
Pg. 1/6 1 a Questão Metanol, CH 4 O, e etanol, C 2 H 6 O, são dois álcoois voláteis a 25 C. Ambos podem ser usados como solvente ou combustível e muitas vezes a mistura dos dois é empregada em processos
Disciplina: Química A
 Disciplina: Química A EXTENSIVO E TERCEIRÃO PÁGINA: 6 EXERCÍCIO: 28.01 O álcool apresenta interações por ligações de hidrogênio, enquanto o hidrocarboneto interage por forças de dipolo induzido, dessa
Disciplina: Química A EXTENSIVO E TERCEIRÃO PÁGINA: 6 EXERCÍCIO: 28.01 O álcool apresenta interações por ligações de hidrogênio, enquanto o hidrocarboneto interage por forças de dipolo induzido, dessa
VERIFICAÇÃO DA ADEQUAÇÃO DO MODELO DE ANÁLISE DE VARIÂNCIA ANÁLISE DE RESÍDUOS
 VERIFICAÇÃO DA ADEQUAÇÃO DO MODELO DE ANÁLISE DE VARIÂNCIA ANÁLISE DE RESÍDUOS Conforme foi apresentado anteriormente, o modelo de análise de variância assume que as observações são independentes e normalmente
VERIFICAÇÃO DA ADEQUAÇÃO DO MODELO DE ANÁLISE DE VARIÂNCIA ANÁLISE DE RESÍDUOS Conforme foi apresentado anteriormente, o modelo de análise de variância assume que as observações são independentes e normalmente
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA
 Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
Aula 4: Gráficos lineares
 Aula 4: Gráficos lineares 1 Introdução Um gráfico é uma curva que mostra a relação entre duas variáveis medidas. Quando, em um fenômeno físico, duas grandezas estão relacionadas entre si o gráfico dá uma
Aula 4: Gráficos lineares 1 Introdução Um gráfico é uma curva que mostra a relação entre duas variáveis medidas. Quando, em um fenômeno físico, duas grandezas estão relacionadas entre si o gráfico dá uma
Escrita correta de resultados em notação
 Notas de Aula Laboratório de Física 1 e A Escrita correta de resultados em notação científica e confecção de gráficos 1 Prof. Alexandre A. C Cotta 1 Departamento de Física, Universidade Federal de Lavras,
Notas de Aula Laboratório de Física 1 e A Escrita correta de resultados em notação científica e confecção de gráficos 1 Prof. Alexandre A. C Cotta 1 Departamento de Física, Universidade Federal de Lavras,
MAE Introdução à Probabilidade e Estatística II Resolução Lista 5
 MAE 229 - Introdução à Probabilidade e Estatística II Resolução Lista 5 Professor: Pedro Morettin e Profa. Chang Chian Exercício 1 (a) De uma forma geral, o desvio padrão é usado para medir a dispersão
MAE 229 - Introdução à Probabilidade e Estatística II Resolução Lista 5 Professor: Pedro Morettin e Profa. Chang Chian Exercício 1 (a) De uma forma geral, o desvio padrão é usado para medir a dispersão
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Fases de Agregação da Matéria Sublimação (sólido em gás ou gás em sólido) Gás Evaporação (líquido em gás) Condensação (gás em líquido) Sólido
Físico-Química I. Profa. Dra. Carla Dalmolin. Misturas Simples. Termodinâmica das Misturas Propriedades das Soluções Atividade
 Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Termodinâmica das Misturas Propriedades das Soluções Atividade Misturas Simples Misturas de substâncias que não reagem Modelo simples para posteriormente
AULA 3. Tratamento Sistemático do Equilíbrio Químico
 AULA Tratamento Sistemático do Equilíbrio Químico Objetivos Escrever as equações químicas que descrevem as reações químicas. Escrever as expressões de constante de equilíbrio para as reações químicas.
AULA Tratamento Sistemático do Equilíbrio Químico Objetivos Escrever as equações químicas que descrevem as reações químicas. Escrever as expressões de constante de equilíbrio para as reações químicas.
ESTUDO E ANÁLISE DA MISTURA DE ÁGUA E ETANOL ATRAVÉS DE EQUAÇÕES DE ESTADO.
 ESTUDO E ANÁLISE DA MISTURA DE ÁGUA E ETANOL ATRAVÉS DE EQUAÇÕES DE ESTADO. S. F. VASCONCELOS 1, F. J. F. CHAVES 1, C. V. FERNANDES 1, N. SILVA 1, H. BISPO 1 1 Universidade Federal de Campina Grande, Unidade
ESTUDO E ANÁLISE DA MISTURA DE ÁGUA E ETANOL ATRAVÉS DE EQUAÇÕES DE ESTADO. S. F. VASCONCELOS 1, F. J. F. CHAVES 1, C. V. FERNANDES 1, N. SILVA 1, H. BISPO 1 1 Universidade Federal de Campina Grande, Unidade
BIK0102: ESTRUTURA DA MATÉRIA. Crédito: Sprace GASES. Professor Hugo B. Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace GASES Professor Hugo B. Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Pressão Atmosférica A pressão é a força atuando em um objeto por
Parte 1. Diagrama de fases ternário
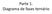 Parte 1. Diagrama de fases ternário Três componentes : água, citrato e poli(etileno glicol) 400 g/mol Observar passagem de sistema homogêneo para turvo cloud-point ou ponto de névoa em função da variação
Parte 1. Diagrama de fases ternário Três componentes : água, citrato e poli(etileno glicol) 400 g/mol Observar passagem de sistema homogêneo para turvo cloud-point ou ponto de névoa em função da variação
Físico-Química I. Profa. Dra. Carla Dalmolin. Diagrama de Fases. Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras
 Físico-Química I Profa. Dra. Carla Dalmolin Diagrama de Fases Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Sistemas Binários O equilíbrio de fases de sistemas com dois componentes
Físico-Química I Profa. Dra. Carla Dalmolin Diagrama de Fases Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Sistemas Binários O equilíbrio de fases de sistemas com dois componentes
PRÁTICA: LÍQUIDOS: DETERMINAÇÃO DA VISCOSIDADE
 PRÁTICA: LÍQUIDOS: DETERMINAÇÃO DA VISCOSIDADE 1. Introdução No estado líquido as moléculas estão mais próximas uma das outras e entre elas existem forças atrativas. Para um líquido fluir suas moléculas
PRÁTICA: LÍQUIDOS: DETERMINAÇÃO DA VISCOSIDADE 1. Introdução No estado líquido as moléculas estão mais próximas uma das outras e entre elas existem forças atrativas. Para um líquido fluir suas moléculas
QFL Instruções para elaboração dos relatórios 2013
 GERAL QFL 2453 - Instruções para elaboração dos relatórios 2013 Todos os relatórios devem apresentar: 1) Capa contendo os nomes dos alunos, número USP, a turma da qual fazem parte, título e número da experiência,
GERAL QFL 2453 - Instruções para elaboração dos relatórios 2013 Todos os relatórios devem apresentar: 1) Capa contendo os nomes dos alunos, número USP, a turma da qual fazem parte, título e número da experiência,
5. Resultados e Discussão
 47 5. Resultados e Discussão 5.1.1. Faixa de trabalho e Faixa linear de trabalho As curvas analíticas obtidas são apresentadas na Figura 14 e Figura 16. Baseado no coeficiente de determinação (R 2 ) encontrado,
47 5. Resultados e Discussão 5.1.1. Faixa de trabalho e Faixa linear de trabalho As curvas analíticas obtidas são apresentadas na Figura 14 e Figura 16. Baseado no coeficiente de determinação (R 2 ) encontrado,
Aula 9 PREPARO DE SOLUÇÕES. Maria de Lara Palmeira de Macedo Arguelho Beatriz. META Introduzir algumas técnicas básicas de preparo de soluções.
 Aula 9 PREPARO DE SOLUÇÕES META Introduzir algumas técnicas básicas de preparo de soluções. OBJETIVOS Ao fi nal desta aula, o aluno deverá: realizar os procedimentos de preparo de soluções do tipo sólido-líquido;
Aula 9 PREPARO DE SOLUÇÕES META Introduzir algumas técnicas básicas de preparo de soluções. OBJETIVOS Ao fi nal desta aula, o aluno deverá: realizar os procedimentos de preparo de soluções do tipo sólido-líquido;
ESTUDO COMPARATIVO DE MODELOS DE COEFICIENTES DE ATIVIDADE DA FASE LÍQUIDA PARA SEPARAÇÃO DA MISTURA ETANOL-ÁGUA
 ESTUDO COMPARATIVO DE MODELOS DE COEFICIENTES DE ATIVIDADE DA FASE LÍQUIDA PARA SEPARAÇÃO DA MISTURA ETANOL-ÁGUA A. APIO 1 e N. P. G. SALAU Universidade Federal de Santa Maria, Departamento de Engenharia
ESTUDO COMPARATIVO DE MODELOS DE COEFICIENTES DE ATIVIDADE DA FASE LÍQUIDA PARA SEPARAÇÃO DA MISTURA ETANOL-ÁGUA A. APIO 1 e N. P. G. SALAU Universidade Federal de Santa Maria, Departamento de Engenharia
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2. Propriedades Moleculares dos Gases
 CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
CURSO: ENGENHARIA CIVIL FÍSICA GERAL E EXPERIMENTAL II 2º Período Prof.a: Érica Muniz UNIDADE 2 Propriedades Moleculares dos Gases Estado Gasoso Dentre os três estados de agregação, apenas o estado gasosos
Luis Eduardo C. Aleotti. Química. Aula 61 - Propriedades Físicas dos Compostos Orgânicos
 Luis Eduardo C. Aleotti Química Aula 61 - Propriedades Físicas dos Compostos Orgânicos PROPRIEDADES FÍSICAS O que é? - Características da matéria, determinadas de forma experimental. - Não são alteradas,
Luis Eduardo C. Aleotti Química Aula 61 - Propriedades Físicas dos Compostos Orgânicos PROPRIEDADES FÍSICAS O que é? - Características da matéria, determinadas de forma experimental. - Não são alteradas,
DESAFIO EM QUÍMICA 24/09/16
 DESAFI EM QUÍMICA 24/09/16 Nome: Assinatura: Questão Valor Grau 1 a 2,0 2 a 2,0 3 a 2,0 4 a 2,0 5 a 2,0 Total 10,0 IMPRTANTE: 1) Explique e justifique a resolução de todas questões e derivações. As respostas
DESAFI EM QUÍMICA 24/09/16 Nome: Assinatura: Questão Valor Grau 1 a 2,0 2 a 2,0 3 a 2,0 4 a 2,0 5 a 2,0 Total 10,0 IMPRTANTE: 1) Explique e justifique a resolução de todas questões e derivações. As respostas
Estudo Físico-Químico dos Gases
 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer ainda um
CORRELAÇÃO E REGRESSÃO. Modelos Probabilísticos para a Computação Professora: Andréa Rocha. UNIVERSIDADE FEDERAL DA PARAÍBA Dezembro, 2011
 CORRELAÇÃO E REGRESSÃO CORRELAÇÃO E REGRESSÃO Modelos Probabilísticos para a Computação Professora: Andréa Rocha UNIVERSIDADE FEDERAL DA PARAÍBA Dezembro, 2011 CORRELAÇÃO Introdução Quando consideramos
CORRELAÇÃO E REGRESSÃO CORRELAÇÃO E REGRESSÃO Modelos Probabilísticos para a Computação Professora: Andréa Rocha UNIVERSIDADE FEDERAL DA PARAÍBA Dezembro, 2011 CORRELAÇÃO Introdução Quando consideramos
Propriedades Coligativas
 Propriedades Coligativas Propriedades Coligativas São propriedades que se somam pela presença de um ou mais solutos e dependem única e exclusivamente do número de partículas (moléculas ou íons) que estão
Propriedades Coligativas Propriedades Coligativas São propriedades que se somam pela presença de um ou mais solutos e dependem única e exclusivamente do número de partículas (moléculas ou íons) que estão
DIAGRAMA DE FASES. 4) (ITA) Considere as seguintes afirmações relativas aos sistemas descritos a seguir, sob
 DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
DIAGRAMA DE FASES 1) O gráfico abaixo apresenta a variação das pressões de vapor do sulfeto de carbono, metanol, etanol e água em função da temperatura. De acordo com o gráfico, assinale a afirmativa INCORRETA.
Objetivos. Escoamento de um fluido. O aluno deverá ser capaz de: Introduzir noções acerca do movimento dos fluidos.
 Introdução à hidrodinâmica MÓDULO 1 - AULA 3 Aula 3 Introdução à hidrodinâmica Objetivos O aluno deverá ser capaz de: Introduzir noções acerca do movimento dos fluidos. Estabelecer critérios para o estudo
Introdução à hidrodinâmica MÓDULO 1 - AULA 3 Aula 3 Introdução à hidrodinâmica Objetivos O aluno deverá ser capaz de: Introduzir noções acerca do movimento dos fluidos. Estabelecer critérios para o estudo
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA.
 ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
Com base nos dados acima, responda as questões propostas (cuidado com as unidades):
 Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Equilíbrio de Misturas Líquidas Binárias com o Sólido
 UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL INSTITUTO DE QUÍMICA DEPARTAMENTO DE FÍSICO-QUÍMICA QUI 03 313 FÍSICO-QUÍMICA II-A 4 a LISTA DE EXERCÍCIOS Equilíbrio de Misturas Líquidas Binárias com o Sólido
UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL INSTITUTO DE QUÍMICA DEPARTAMENTO DE FÍSICO-QUÍMICA QUI 03 313 FÍSICO-QUÍMICA II-A 4 a LISTA DE EXERCÍCIOS Equilíbrio de Misturas Líquidas Binárias com o Sólido
DISCIPLINA DE QUÍMICA
 DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
DISCIPLINA DE QUÍMICA OBJETIVOS: 1ª série Traduzir linguagens químicas em linguagens discursivas e linguagem discursiva em outras linguagens usadas em Química tais como gráficos, tabelas e relações matemáticas,
QUÍMICA Tipos de soluções Edson Mesquita
 QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
A eq. de Schrödinger em coordenadas esféricas
 A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
A eq. de Schrödinger em coordenadas esféricas A autofunção espacial, ψ, e a energia, E, são determinadas pela solução da equação independente do tempo: Separação de variáveis Solução do tipo: Que leva
Equilíbrio Químico. início x 2x 0 0
 Capítulo 7 Equilíbrio Químico. (ITA) Uma mistura gasosa é colocada a reagir dentro de um cilindro provido de um pistão móvel, sem atrito e sem massa, o qual é mantido à temperatura constante. As reações
Capítulo 7 Equilíbrio Químico. (ITA) Uma mistura gasosa é colocada a reagir dentro de um cilindro provido de um pistão móvel, sem atrito e sem massa, o qual é mantido à temperatura constante. As reações
Química Analítica I Tratamento dos dados analíticos Soluções analíticas
 Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Soluções Curva de solubilidade, concentrações e preparo de soluções Professor Rondinelle Gomes Pereira
 Soluções Definição: São misturas homogêneas, ou seja, mistura de dois ou mais componentes apresentando uma única fase contínua. As soluções são compostas por um ou mais soluto e um ou mais solvente. Soluto:
Soluções Definição: São misturas homogêneas, ou seja, mistura de dois ou mais componentes apresentando uma única fase contínua. As soluções são compostas por um ou mais soluto e um ou mais solvente. Soluto:
A teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
Aluno(a): COMENTADA. Série: 2 a Ensino Médio Turma: A / B / C / D / E Data: 17/08/2016
 QUÍMICA AVALIAÇÃO CLAUDI / SARA III UNIDADE Aluno(a): COMENTADA Série: 2 a Ensino Médio Turma: A / B / C / D / E Data: 17/08/2016 1. A prova é composta de 07 questões abertas e 03 questões objetivas. 2.
QUÍMICA AVALIAÇÃO CLAUDI / SARA III UNIDADE Aluno(a): COMENTADA Série: 2 a Ensino Médio Turma: A / B / C / D / E Data: 17/08/2016 1. A prova é composta de 07 questões abertas e 03 questões objetivas. 2.
Introdução. Uma mistura éconstituída por duas ou mais substâncias puras, sejam simples ou compostas MISTURA
 SOLUÇÕES Introdução MISTURA MISTURA HETEROGÊNEA Uma mistura éconstituída por duas ou mais substâncias puras, sejam simples ou compostas A mistura seráheterogênea quando apresentar duas ou mais fases perceptíveis.
SOLUÇÕES Introdução MISTURA MISTURA HETEROGÊNEA Uma mistura éconstituída por duas ou mais substâncias puras, sejam simples ou compostas A mistura seráheterogênea quando apresentar duas ou mais fases perceptíveis.
Modelos de Regressão Linear Simples - parte I
 Modelos de Regressão Linear Simples - parte I Erica Castilho Rodrigues 19 de Agosto de 2014 Introdução 3 Objetivos Ao final deste capítulo você deve ser capaz de: Usar modelos de regressão para construir
Modelos de Regressão Linear Simples - parte I Erica Castilho Rodrigues 19 de Agosto de 2014 Introdução 3 Objetivos Ao final deste capítulo você deve ser capaz de: Usar modelos de regressão para construir
Prática 10 Determinação da constante de equilíbrio entre íons Fe 3+ e SCN -
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC Disciplina: Química Geral Experimental QEX0002 Prática 10 Determinação da constante de equilíbrio
SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL
 ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL 1. CARACTERÍSTICAS GERAIS DA SOLUÇÃO IDEAL Para
ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES MAIS DE UM COMPONENTE VOLÁTIL A SOLUÇÃO DILUÍDA IDEAL 1. CARACTERÍSTICAS GERAIS DA SOLUÇÃO IDEAL Para
Condutividade Elétrica
 FQE1 Exp. 1 Condutividade Elétrica 1. Introdução A condução elétrica é um fenômeno de transporte em que a carga elétrica (elétrons ou íons) se move através do sistema. A condutividade elétrica, também
FQE1 Exp. 1 Condutividade Elétrica 1. Introdução A condução elétrica é um fenômeno de transporte em que a carga elétrica (elétrons ou íons) se move através do sistema. A condutividade elétrica, também
RECRISTALIZAÇÃO. Princípio: Dissolver a substância em um solvente a quente e deixar a solução esfriar lentamente. Cristalização versus Precipitação
 RECRISTALIZAÇÃO Método de purificação de substâncias sólidas Princípio: Dissolver a substância em um solvente a quente e deixar a solução esfriar lentamente. Cristalização versus Precipitação lento / seletivo
RECRISTALIZAÇÃO Método de purificação de substâncias sólidas Princípio: Dissolver a substância em um solvente a quente e deixar a solução esfriar lentamente. Cristalização versus Precipitação lento / seletivo
Medidas da radiação luminosa
 Medidas da radiação luminosa Curso de Introdução à Astronomia e Astrofísca Dr. Francisco Jablonski DAS/INPE chico@das.inpe.br O que medir? Vamos medir a quantidade de energia radiante produzida por fontes
Medidas da radiação luminosa Curso de Introdução à Astronomia e Astrofísca Dr. Francisco Jablonski DAS/INPE chico@das.inpe.br O que medir? Vamos medir a quantidade de energia radiante produzida por fontes
Física II Teoria Cinética dos Gases
 Física II Teoria Cinética dos Gases João Francisco Fuzile Rodrigues Garcia -- 8549323 Maiara Fernanda Moreno -- 8549344 Otávio Massola Sumi -- 8549452 Ex. 18.63 Explique, em termos do movimento molecular,
Física II Teoria Cinética dos Gases João Francisco Fuzile Rodrigues Garcia -- 8549323 Maiara Fernanda Moreno -- 8549344 Otávio Massola Sumi -- 8549452 Ex. 18.63 Explique, em termos do movimento molecular,
X Congresso Brasileiro de Engenharia Química Iniciação Científica
 Blucher Chemical Engineering Proceedings Dezembro de 24, Volume, Número X Congresso Brasileiro de Engenharia Química Iniciação Científica Influência da pesquisa em Engenharia Química no desenvolvimento
Blucher Chemical Engineering Proceedings Dezembro de 24, Volume, Número X Congresso Brasileiro de Engenharia Química Iniciação Científica Influência da pesquisa em Engenharia Química no desenvolvimento
4. Propriedades dos gases experimentos e modelo microscópico simples para a temperatura
 PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
PV T = nr, onde R é um número (a constante dos gases). Repare que esta é uma lei universal para qualquer gás em pressão e temperatura próxima da atmosférica: não aparece nenhuma dependência de características
PRÉ-REQUISITOS Ter estudado todo o conteúdo do primeiro principio da termodinâmica (Aula 4) e como se utilizar de um calorímetro (Aula 5).
 CALOR DE NEUTRALIZAÇÃO DE ÁCIDOS E BASES Aula 6 META Determinação da variação de entalpia na reação de neutralização de soluções aquosas de hidróxido de sódio e de ácido clorídrico e hidróxido de sódio
CALOR DE NEUTRALIZAÇÃO DE ÁCIDOS E BASES Aula 6 META Determinação da variação de entalpia na reação de neutralização de soluções aquosas de hidróxido de sódio e de ácido clorídrico e hidróxido de sódio
Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente.
 SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
P1 - PROVA DE QUÍMICA GERAL 09/04/11
 P1 - PROVA DE QUÍMICA GERAL 09/04/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) =
P1 - PROVA DE QUÍMICA GERAL 09/04/11 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Dados R = 0,0821 atm L mol -1 K -1 T (K) =
TÍTULO: ANÁLISE TITRIMÉTRICA (Volumétrica)
 Componente Curricular: Química dos Alimentos Prof. Barbosa e Prof. Daniel 4º Módulo de Química Procedimento de Prática Experimental Competências: Identificar as propriedades dos alimentos. Identificar
Componente Curricular: Química dos Alimentos Prof. Barbosa e Prof. Daniel 4º Módulo de Química Procedimento de Prática Experimental Competências: Identificar as propriedades dos alimentos. Identificar
DESTILAÇÃO Lei de Raoult
 DESTILAÇÃO Operação que consiste na separação de líquidos de suas eventuais misturas, por passagem de vapor e posterior condensação com retorno ao estado líquido, com auxílio de calor e/ou por redução
DESTILAÇÃO Operação que consiste na separação de líquidos de suas eventuais misturas, por passagem de vapor e posterior condensação com retorno ao estado líquido, com auxílio de calor e/ou por redução
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II
 INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO NORTE IFRN CAMPUS MOSSORÓ PROFESSOR: ALBINO DISCIPLINA: QUÍMICA II ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais
Modelos Lineares Generalizados - Modelos log-lineares para tabelas de contingência
 Modelos Lineares Generalizados - Modelos log-lineares para tabelas de contingência Erica Castilho Rodrigues 12 de Agosto Introdução 3 Vimos como usar Poisson para testar independência em uma Tabela 2x2.
Modelos Lineares Generalizados - Modelos log-lineares para tabelas de contingência Erica Castilho Rodrigues 12 de Agosto Introdução 3 Vimos como usar Poisson para testar independência em uma Tabela 2x2.
QUÍMICA MÓDULO 19 LEIS DA QUÍMICA. Professor Edson Cruz
 QUÍMICA Professor Edson Cruz MÓDULO 19 LEIS DA QUÍMICA INTRODUÇÃO Um exame apurado das propriedades físicas de um material (como densidade, ponto de fusão e ebulição) permite dizer se o material é uma
QUÍMICA Professor Edson Cruz MÓDULO 19 LEIS DA QUÍMICA INTRODUÇÃO Um exame apurado das propriedades físicas de um material (como densidade, ponto de fusão e ebulição) permite dizer se o material é uma
SOLUÇÕES - SOLUÇÃO IDEAL E AS PROPRIEDADES COLIGATIVAS
 ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES - SOLUÇÃO IDEAL E AS PROPRIEDADES COLIGATIVAS 1. TIPOS DE SOLUÇÕES Solução é uma mistura homogênea de
ESCOLA DE ENGENHARIA DE LORENA EEL/USP TERMODINÂMICA QUÍMICA PROF. ANTONIO CARLOS DA SILVA SOLUÇÕES - SOLUÇÃO IDEAL E AS PROPRIEDADES COLIGATIVAS 1. TIPOS DE SOLUÇÕES Solução é uma mistura homogênea de
APROXIMAÇÃO DE FUNÇÕES MÉTODO DOS MÍNIMOS QUADRADOS
 MÉTODO DOS MÍNIMOS QUADRADOS INTRODUÇÃO Frequentemente é possível estabelecer uma relação linear entre duas grandezas medidas experimentalmente. O método dos mínimos quadrados é uma maneira de se obter
MÉTODO DOS MÍNIMOS QUADRADOS INTRODUÇÃO Frequentemente é possível estabelecer uma relação linear entre duas grandezas medidas experimentalmente. O método dos mínimos quadrados é uma maneira de se obter
conhecida como molaridade é redefinida como concentração em quantidade de matéria. A quantidade de matéria do soluto (nsoluto anteriormente chamada nu
 SEGURANÇA E TÉCNICA DE LABORATÓRIO AULA 03: CONCENTRAÇÃO DE SOLUÇÕES TÓPICO 02: UNIDADES DE CONCENTRAÇÃO Uma solução é uma mistura homogênea de duas ou mais substancias. Uma destas substâncias é chamada
SEGURANÇA E TÉCNICA DE LABORATÓRIO AULA 03: CONCENTRAÇÃO DE SOLUÇÕES TÓPICO 02: UNIDADES DE CONCENTRAÇÃO Uma solução é uma mistura homogênea de duas ou mais substancias. Uma destas substâncias é chamada
Determinação espectrofotométrica do pka do indicador vermelho de metilo
 Determinação espectrofotométrica do pka do indicador vermelho de metilo Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 28 /05/99 Objectivos Nesta actividade experimental temos como objectivo a determinação
Determinação espectrofotométrica do pka do indicador vermelho de metilo Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 28 /05/99 Objectivos Nesta actividade experimental temos como objectivo a determinação
TEMPO DE QUEDA NA PRESSÃO ATMOSFÉRICA E NO VÁCUO
 TEMPO DE QUEDA NA PRESSÃO ATMOSFÉRICA E NO VÁCUO Aluno: Raphaël Antoine de Góes Bezerra Cambas Orientador: Sergio Leal Braga 1. Introdução Esse projeto foi montado com a idéia de mostrar a diferença do
TEMPO DE QUEDA NA PRESSÃO ATMOSFÉRICA E NO VÁCUO Aluno: Raphaël Antoine de Góes Bezerra Cambas Orientador: Sergio Leal Braga 1. Introdução Esse projeto foi montado com a idéia de mostrar a diferença do
sat 1 = 431 Pa e sat sat
 Modelos Baseados no Conceito de Composição Local 85 Exemplo 9. Para o sistema n-pentanol ()/n-hexano () as constantes da equação de Wilson são Λ = 0.0700 e Λ = 0.69. Admitindo que a fase vapor é ideal,
Modelos Baseados no Conceito de Composição Local 85 Exemplo 9. Para o sistema n-pentanol ()/n-hexano () as constantes da equação de Wilson são Λ = 0.0700 e Λ = 0.69. Admitindo que a fase vapor é ideal,
PRÁTICA 6: COLISÕES EM UMA DIMENSÃO
 PRÁTICA 6: COLISÕES EM UMA DIMENSÃO Nesta prática, estudaremos o fenômeno da colisão em uma dimensão, fazendo a aproximação de que o sistema é fechado (não há variação de massa) e isolado (não há forças
PRÁTICA 6: COLISÕES EM UMA DIMENSÃO Nesta prática, estudaremos o fenômeno da colisão em uma dimensão, fazendo a aproximação de que o sistema é fechado (não há variação de massa) e isolado (não há forças
FÍSICA E QUÍMICA A 10º ANO
 DEPARTAMENTO DE MATEMÁTICA E CIÊNCIAS EXPERIMENTAIS Planificação Anual FÍSICA E QUÍMICA A 10º ANO 2017 / 2018 1º Período - QUÍMICA Apresentação e divulgação de critérios 2 1. ELEMENTOS QUÍMICOS E SUA ORGANIZAÇÃO
DEPARTAMENTO DE MATEMÁTICA E CIÊNCIAS EXPERIMENTAIS Planificação Anual FÍSICA E QUÍMICA A 10º ANO 2017 / 2018 1º Período - QUÍMICA Apresentação e divulgação de critérios 2 1. ELEMENTOS QUÍMICOS E SUA ORGANIZAÇÃO
LEQ I Laboratórios em sentido lato
 LEQ I Laboratórios em sentido lato 2º. Ano (2º. Semestre) da Licenciatura Engenharia Henrique Matos (henrimatos@ist.utl.pt) Rosinda Ismael José Nuno Lopes Adriano Pacheco Estrutura Geral de LEQ I 1. Pesquisa
LEQ I Laboratórios em sentido lato 2º. Ano (2º. Semestre) da Licenciatura Engenharia Henrique Matos (henrimatos@ist.utl.pt) Rosinda Ismael José Nuno Lopes Adriano Pacheco Estrutura Geral de LEQ I 1. Pesquisa
Física. Resumo Eletromagnetismo
 Física Resumo Eletromagnetismo Cargas Elétricas Distribuição Contínua de Cargas 1. Linear Q = dq = λ dl 2. Superficial Q = dq = σ. da 3. Volumétrica Q = dq = ρ. dv Força Elétrica Duas formas de calcular:
Física Resumo Eletromagnetismo Cargas Elétricas Distribuição Contínua de Cargas 1. Linear Q = dq = λ dl 2. Superficial Q = dq = σ. da 3. Volumétrica Q = dq = ρ. dv Força Elétrica Duas formas de calcular:
Propriedades Coligativas
 Propriedades Coligativas Propriedades Coligativas São propriedades que se somam pela presença de um ou mais solutos e dependem única e exclusivamente do número de partículas (moléculas ou íons) que estão
Propriedades Coligativas Propriedades Coligativas São propriedades que se somam pela presença de um ou mais solutos e dependem única e exclusivamente do número de partículas (moléculas ou íons) que estão
Química. Xandão (Victor Pontes) Compostos Orgânicos
 Compostos Orgânicos Compostos Orgânicos 1. Três frascos não-rotulados encontram-se na prateleira de um laboratório. Um contém benzeno, outro, tetracloreto de carbono e o terceiro, metanol. Sabe-se que
Compostos Orgânicos Compostos Orgânicos 1. Três frascos não-rotulados encontram-se na prateleira de um laboratório. Um contém benzeno, outro, tetracloreto de carbono e o terceiro, metanol. Sabe-se que
Estudo Físico-Químico dos Gases
 19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
19/08/009 Estudo Físico-Químico dos Gases Prof. Alex Fabiano C. Campos Gás e Vapor Diagrama de Fase Gás Vapor Gás: fluido elástico que não pode ser condensado apenas por aumento de pressão, pois requer
QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO
 Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
Luis Eduardo C. Aleotti. Química. Aula 38 - Transformações Gasosas
 Luis Eduardo C. Aleotti Química Aula 38 - Transformações Gasosas TRANSFORMAÇÕES GASOSAS Gás e Vapor - Gás: Substância gasosa em temperatura ambiente. - Vapor: Estado gasoso de uma substância líquida ou
Luis Eduardo C. Aleotti Química Aula 38 - Transformações Gasosas TRANSFORMAÇÕES GASOSAS Gás e Vapor - Gás: Substância gasosa em temperatura ambiente. - Vapor: Estado gasoso de uma substância líquida ou
INTRODUÇÃO A MÉTODOS CROMATOGRÁFICOS
 INTRODUÇÃO A MÉTODOS CROMATOGRÁFICOS 1 Histórico da cromatografia moderna Mikhail Tsweett (1872-1919) Botânico russo: usou uma coluna empacotada contendo carbonato de cálcio como fase estacionária para
INTRODUÇÃO A MÉTODOS CROMATOGRÁFICOS 1 Histórico da cromatografia moderna Mikhail Tsweett (1872-1919) Botânico russo: usou uma coluna empacotada contendo carbonato de cálcio como fase estacionária para
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal.
 Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal. Equações de Estado Não é fácil trabalhar com as tabelas termodinâmicas. A dificuldade está associada ao volume delas e a possibilidade
Módulo V Equações de Estado, Fator de Compressibilidade e Modelo de Gás Ideal. Equações de Estado Não é fácil trabalhar com as tabelas termodinâmicas. A dificuldade está associada ao volume delas e a possibilidade
REVISÃO: CONDUTIVIDADE ELÉTRICA DE SOLUÇÕES AQUOSAS AULA 1 EXPRESSÕES DE CONCENTRAÇÃO PROF. ANA
 REVISÃO: CONDUTIVIDADE ELÉTRICA DE SOLUÇÕES AQUOSAS AULA 1 EXPRESSÕES DE CONCENTRAÇÃO DATA: 21/08/2015 PROF. ANA 1) SOLUÇÕES Soluções são misturas homogêneas de duas ou mais substâncias. - numa solução,
REVISÃO: CONDUTIVIDADE ELÉTRICA DE SOLUÇÕES AQUOSAS AULA 1 EXPRESSÕES DE CONCENTRAÇÃO DATA: 21/08/2015 PROF. ANA 1) SOLUÇÕES Soluções são misturas homogêneas de duas ou mais substâncias. - numa solução,
5 Resultados Experimentais
 5 Resultados Experimentais 5.1. Introdução Neste capítulo são apresentados os resultados medidos dos dois testes experimentais em escala real realizados para a comparação dos resultados teóricos. 5.2.
5 Resultados Experimentais 5.1. Introdução Neste capítulo são apresentados os resultados medidos dos dois testes experimentais em escala real realizados para a comparação dos resultados teóricos. 5.2.
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia. Aula Interlúdio molecular
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula Interlúdio molecular Energia Interna somatório de energias (cinética + potencial) Energia cinética relacionada
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula Interlúdio molecular Energia Interna somatório de energias (cinética + potencial) Energia cinética relacionada
RESOLUÇÃO DA LISTA COMPLEMENTAR INTERAÇÕES INTERMOLECULARES E SUA ASSOCIAÇÃO COM PROPRIEDADES FÍSICAS DAS SUBSTÂNCIAS
 RESOLUÇÃO DA LISTA COMPLEMENTAR INTERAÇÕES INTERMOLECULARES E SUA ASSOCIAÇÃO COM PROPRIEDADES FÍSICAS DAS SUBSTÂNCIAS 1 E Molécula A: apesar de essa molécula apresentar somente ligações polares (entre
RESOLUÇÃO DA LISTA COMPLEMENTAR INTERAÇÕES INTERMOLECULARES E SUA ASSOCIAÇÃO COM PROPRIEDADES FÍSICAS DAS SUBSTÂNCIAS 1 E Molécula A: apesar de essa molécula apresentar somente ligações polares (entre
Do ideal ao real II: propriedades de misturas e soluções
 7 Capítulo Capítulo Do ideal ao real II: propriedades de misturas e soluções For every complex problem there is an answer that is clear, simple, and wrong (Para cada problema complexo existe uma resposta
7 Capítulo Capítulo Do ideal ao real II: propriedades de misturas e soluções For every complex problem there is an answer that is clear, simple, and wrong (Para cada problema complexo existe uma resposta
PGF Física Atômica e Molecular
 PGF5109 - Física Atômica e Molecular Prof. Dr. Sylvio Canuto Carlos Bistafa, Cíntia C. Vequi-Suplicy, Rodrigo M. Gester Tarefa 5 Freqüência Vibracional e fatores de escala: Aprendendo a conviver com erros
PGF5109 - Física Atômica e Molecular Prof. Dr. Sylvio Canuto Carlos Bistafa, Cíntia C. Vequi-Suplicy, Rodrigo M. Gester Tarefa 5 Freqüência Vibracional e fatores de escala: Aprendendo a conviver com erros
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO.
 DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
DETERMINAÇÃO DE ALGUNS PARÂMETROS CINÉTICOS DA REAÇÃO DE DECOMPOSIÇÃO DO PERÓXIDO DE HIDROGÊNIO. Glauber Silva Godoi Aula 13 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros
Controle de Processos Aula: Principais váriaveis em controle de processos químicos
 107484 Controle de Processos Aula: Principais váriaveis em controle de processos químicos Prof. Eduardo Stockler Tognetti Departamento de Engenharia Elétrica Universidade de Brasília UnB 1 o Semestre 2015
107484 Controle de Processos Aula: Principais váriaveis em controle de processos químicos Prof. Eduardo Stockler Tognetti Departamento de Engenharia Elétrica Universidade de Brasília UnB 1 o Semestre 2015
Físico-Química I. Profa. Dra. Carla Dalmolin. Misturas Simples. Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras
 Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Misturas Simples Misturas de substâncias que não reagem Modelo simples para
Físico-Química I Profa. Dra. Carla Dalmolin Misturas Simples Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Misturas Simples Misturas de substâncias que não reagem Modelo simples para
Le rouge et le noir: probabilidades com cartas
 Le rouge et le noir: probabilidades com cartas Prof. Luiz T. F. Eleno 22 de fevereiro de 207 O baralho comum Vamos considerar um baralho comum no Ocidente, dito francês, que é aquele usado nos jogos de
Le rouge et le noir: probabilidades com cartas Prof. Luiz T. F. Eleno 22 de fevereiro de 207 O baralho comum Vamos considerar um baralho comum no Ocidente, dito francês, que é aquele usado nos jogos de
Olimpíada Mineira de Química 2016 Gabarito Oficial
 Olimpíada Mineira de Química 016 Gabarito Oficial Tabela de Respostas das Questões 1 a 0 Modalidade A 1 3 4 5 6 7 8 9 10 11 1 13 14 15 16 17 18 19 0 a b c d X X X X X X X X X X X X X X X X X X X X Tabela
Olimpíada Mineira de Química 016 Gabarito Oficial Tabela de Respostas das Questões 1 a 0 Modalidade A 1 3 4 5 6 7 8 9 10 11 1 13 14 15 16 17 18 19 0 a b c d X X X X X X X X X X X X X X X X X X X X Tabela
A variação de qualquer dimensão linear de um corpo com a temperatura se chama dilatação térmica.
 Dilatação Térmica de Sólidos Quando a temperatura de um corpo varia, ocorrem variações de comprimento em cada uma de suas dimensões, variações estas que dependem da forma do corpo e da substância de que
Dilatação Térmica de Sólidos Quando a temperatura de um corpo varia, ocorrem variações de comprimento em cada uma de suas dimensões, variações estas que dependem da forma do corpo e da substância de que
Equilíbrio Químico (2)
 Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Laboratório de Física I. Experiência 2 Determinação de densidades. 1 o semestre de 2017
 4310256 Laboratório de Física I Experiência 2 Determinação de densidades 1 o semestre de 2017 7 de março de 2017 2. Determinação de densidades Introdução Os estados da matéria podem, de forma simplificada,
4310256 Laboratório de Física I Experiência 2 Determinação de densidades 1 o semestre de 2017 7 de março de 2017 2. Determinação de densidades Introdução Os estados da matéria podem, de forma simplificada,
Campo Elétrico [N/C] Campo produzido por uma carga pontual
![Campo Elétrico [N/C] Campo produzido por uma carga pontual Campo Elétrico [N/C] Campo produzido por uma carga pontual](/thumbs/57/40344984.jpg) Campo Elétrico Ao tentar explicar, ou entender, a interação elétrica entre duas cargas elétricas, que se manifesta através da força elétrica de atração ou repulsão, foi criado o conceito de campo elétrico,
Campo Elétrico Ao tentar explicar, ou entender, a interação elétrica entre duas cargas elétricas, que se manifesta através da força elétrica de atração ou repulsão, foi criado o conceito de campo elétrico,
Ligações Químicas Interações Intermoleculares
 Ligações Químicas Interações Intermoleculares WWW.QUIMUSICANDO.ZZ.VC Prof. Jackson Alves Ligações intermoleculares O que mantém as moléculas unidas nos estados líquido e sólido? Que força faz a água, contrariando
Ligações Químicas Interações Intermoleculares WWW.QUIMUSICANDO.ZZ.VC Prof. Jackson Alves Ligações intermoleculares O que mantém as moléculas unidas nos estados líquido e sólido? Que força faz a água, contrariando
EXPERIÊNCIA 04: DETERMINAÇÃO DA DENSIDADE DE LÍQUIDOS E SÓLIDOS
 1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015.1 EXPERIÊNCIA 04: DETERMINAÇÃO DA DENSIDADE DE LÍQUIDOS E SÓLIDOS 1. Densidade Densidade (d) é uma grandeza expressa pela
1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015.1 EXPERIÊNCIA 04: DETERMINAÇÃO DA DENSIDADE DE LÍQUIDOS E SÓLIDOS 1. Densidade Densidade (d) é uma grandeza expressa pela
