CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
|
|
|
- Liliana Arantes Lencastre
- 7 Há anos
- Visualizações:
Transcrição
1 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias medidas de v 0 para a construção de um gráfico eterminação da inclinação (tangente) A análise gráfica leva a determinação de vários parâmetros cinéticos P U T F M A
2 P U T F M A Velocidade: período inicial Tempo Vo refere-se a quantidade de produto formado na unidade de tempo ensaio envolve a adição de todos os componentes, incluindo S e E Após a adição da E, a absorbância (Abs) é monitorada em função do tempo Abs vs tempo pode ser monitorada e a inclinação determinada Inclinação = Abs/unidade de tempo (min) Lembrar: A = cl (mudança [P]) [S] Tempo eterminação da velocidade inicial de uma reação catalisada por enzima a partir da inclinação instantânea em t = 0 no consumo de substrato ou formação do produto [P] Tempo Considerações Importantes: A enzima deve permanecer estável no curso de tempo de todas as medidas cinéticas As taxas iniciais são usadas como medidas de velocidades de reação A velocidade de reação não pode ser dependente da concentração de enzima Gráfico da conversão de S em P, na reação catalisada por uma enzima A produção de produto é linear com o tempo durante o tempo de intervalo usado
3 Constantes Cinéticas A concentração de substrato excede em muitas vezes a concentração de enzima, ou seja, a concentração de S é praticamente constante durante o ensaio K M k cat Uma única enzima é capaz de formar um produto Não existe produção considerável de produto na ausência de enzima Não existe cooperatividade. A ligação do substrato ao sítio de ligação na enzima não influencia a afinidade ou atividade de um sítio adjacente v 0 MEIAS S k cat /K M Nem substrato nem produto atuam como moduladores alostéricos ou alteram a velocidade de reação enzimática ½V max Constantes Cinéticas Constantes Cinéticas K M ÉaconstantedeMichaelis-Menten,queserefereàconcentração de substrato necessária para atingir a metade da V max na reação enzimática, em condições de saturação de S. K M representa a concentração de S na qual metade dos sítios ativos da enzima encontra-se saturado por moléculas de S, no estado estacionário. K M é uma constante de dissociação aparente e está relacionada com a afinidade da enzima pelo S, sendo o produto de todas as constantes de equilíbrio e dissociação até a etapa irreversível da reação. Quanto menor o valor de K M,maiorseráa afinidade da enzima pelo S. valor de K M varia consideravelmente de uma enzima para outra, e de uma enzima em particular, para S diferentes. Seu valor é expresso em concentração molar (e.g., M, mm, µm). k cat É uma constante de velocidade de primeira ordem que corresponde à etapa mais lenta da reação catalítica. valor de k cat é referido como o número de ciclos ou renovação (termo do inglês, turnover number), que corresponde ao número máximo de mols de S convertidos em P por mols de enzima por unidade de tempo (e.g., define o número de ciclos catalíticos que ocorre por unidade de tempo). Esta condição é encontrada somente quando a enzima está saturada pelo S. valordev max éexpressoemconcentraçãomolardesouppor unidade de tempo (e.g., M/min, µm/min), ao passo que k cat em tempo (e.g., min -1,s -1 ).
4 Constantes Cinéticas Parâmetros Cinéticos k cat /K M Essa razão define a eficiência catalítica de uma enzima e possui unidades de velocidade de segunda ordem. É bastante utilizada para avaliar a eficiência de diferentes enzimas, bem como para comparar o emprego de diferentes S para uma enzima em particular. A especificidade do S resulta preferencialmente de diferenças no estado de transição da reação catalisada em comparação as interações de ligação do estado fundamental. A razão k cat /K M reflete os efeitos de S nas duas constantes cinéticas e fornece um limite menor para a constante de velocidade de segunda-ordem e ligação do S. Medida ireta da eficiência da enzima na transformação do substrato K cat /K M : Eficácia na transformação do substrato ligado Eficiência na ligação do substrato V max v 0 K M UNIAES µm s -1 k cat /K M µm s -1 µm k cat s -1 µm -1 s -1 A velocidade de uma reação enzimática depende da concentração de enzima Podemos observar este efeito através de um gráfico das curvas de formação de P na presença de concentrações crescentes de enzima (onde a concentração de S é mantida constante) Formação de P em função de concentrações crescentes de enzima
5 Verifica-se que v o cresce linearmente com a concentração de enzima em condições padrões de reação. (no intervalo de [E] = 8 [E 1 ]) efeito da variação da concentração de S na velocidade de reação também é um fator importante a ser considerado no controle de reações enzimáticas. Podemos observar este efeito através de um gráfico das curvas de progresso de formação de P em função de concentrações crescentes de S, onde a concentração de enzima é mantida constante. Efeito da concentração de enzima na velocidade inicial de reação catalisada por enzima Avariaçãodev 0 em função da concentração de S é mostrada na Figura, cuja representação característica é de uma hipérbole. Cada medida de v 0 é determinada experimentalmente através das inclinações dos gráficos de concentração de P em função do tempo. Podem ser identificadas três regiões distintas na curva de progresso de reação. Na primeira região, em concentrações muito baixas de S ([S] < 0,01 K M ), a velocidade apresenta um perfil cinético de primeira ordem. Com o aumento na concentração de S, em uma região intermediária do gráfico, a velocidade apresenta uma dependência curvilínea em relação à concentração de S. Naterceiraregião do gráfico, observa-se a ocorrência de um patamar máximo caracterizado por altas concentrações de S, com perfil cinético de ordem zero, no qual v 0 é independente da concentração de S. Neste ponto, a enzima encontra-se saturada pelo S, e v 0 torna-se igual à velocidade máxima (V max ). Formação de P em função de concentrações crescentes de substrato Efeito da concentração de S na velocidade inicial de reação catalisada por enzima
6 Em 1913, Leonor Michaelis e Maud Menten demonstraram que as reações enzimáticas ocorrem em duas etapas. Na primeira etapa, ocorre a formação de um complexo E S, ao passo que, em uma segunda etapa, observa-se a dissociação deste complexo para a formação de P e a liberação da enzima livre. Este modelo assume que as reações cinéticas são conduzidas sob condições experimentais do chamado estado estacionário (do inglês, steady-state), que se refere ao intervalo de tempo no qual o complexo E S é mantido em um nível constante elevado. Em outras palavras, o equilíbrio entre enzima, S, e E S é estabelecido de forma muito rápida em relação à reação subsequente sofrida pela espécie de E S. Assim, ocomplexoe S estará em equilíbrio com a enzima e S, o que significa que k 1 >> k -1 e k 2. epresentação gráfica do equilíbrio rápido entre enzima, S, e E S, no estado estacionário (a corresponde ao período de indução e b a v o ). As análises cinéticas no estado estacionário permitem uma interpretação conveniente do curso de reações enzimáticas, sendo alcançada no laboratório em condições experimentais apropriadas, mantendo-se a concentração de S em grande excesso em relação à concentração de enzima ([S] >> [E 0 ]). esta forma, a enzima está presente em quantidades catalíticas e a variação da concentração de S (consumo) pode ser considerada desprezível. gráfico da figura anterior mostra que as inclinações das curvas de progresso de enzima e E S podem ser consideradas desprezíveis (com exceção de um breve período de indução da ordemdemilésimosdesegundo). A equação abaixo apresenta uma descrição quantitativa do esquema de Michaelis- Menten sob condições do estado estacionário, que pode ser caracterizada graficamente por uma curva de reação na forma de uma hipérbole. Isso indica que estas espécies podem ser consideradas constantes na unidade de tempo (sendo [S] >> [E] T,onde[E] T é a concentração total de enzima). Equação de Michaelis-Menten para a velocidade de reação catalisada por uma enzima.
7 Embora a interpretação deste gráfico seja relativamente simples, existem tratamentos matemáticos e gráficos que permitem a obtenção rápida dos parâmetros cinéticos. método tradicional baseia-se na representação linear da equação de Michaelis-Menten através de uma reta do tipo y = ax + b Velocidade (nm min -1 ) egião de ordem zero egião de primeira ordem eterminação experimental de K M e V max na cinética de Michaelis-Menten Gráfico da velocidade inicial versus concentração de substrato para uma reação catalisada por uma enzima. egiões de reação de primeira ordem e de ordem zero apresentam dependência linear e independência da concentração de substrato, respectivamente ecíproco da equação de Michaelis-Menten Este gráfico, chamado de Lineweaver-Burk ou de duplo-recíproco (i.e., uma representação gráfica dos recíprocos de v o e [S]), permite a determinação simples e direta de V max e K M, parametros que só poderiam ser estimados por aproximação a partir do gráfico de Michaelis-Menten. valor de k cat, por sua vez, pode ser obtido dividindo-se V max pela concentração de enzima empregada nos experimentos (k cat = V max /[E]). Este tratamento dá origem a um gráfico de 1/v o (em y) emfunçãode1/[s](emx) com uma reta de inclinação igual a K M /V max, que intercepta o eixo de ordenadas no ponto 1/V max e o eixo das abcissas no ponto -1/K M
8 Este gráfico, chamado de Lineweaver-Burk ou de duplorecíproco (i.e., uma representação gráfica dos recíprocos de v o e [S] de acordo com a equação anterior), permite a determinação simples e direta de V max e K M, parâmetros que só poderiam ser estimados por aproximação a partir do gráfico de Michaelis-Menten. valor de k cat, por sua vez, pode ser obtido dividindo-se V max pela concentração de enzima empregada nos experimentos. k cat = V max /[E T ]
Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13
 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
CQ110 : Princípios de FQ. Imagens de Rorschach
 Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 581-
 Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Catálise Enzimática. Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química.
 Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Aula 12: Enzimas Introdução e Cinética
 Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Cinética Química. Prof. Alex Fabiano C. Campos
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
 CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
Atividade a Distância 4 CINÉTICA
 Atividade a Distância 4 CINÉTICA Na parte 1 da Aula 3 vimos a definição de velocidade inicial e como deve ser medida. Agora, vamos ver como ela varia se mudarmos a concentração dos reagentes. Estamos acostumados
Atividade a Distância 4 CINÉTICA Na parte 1 da Aula 3 vimos a definição de velocidade inicial e como deve ser medida. Agora, vamos ver como ela varia se mudarmos a concentração dos reagentes. Estamos acostumados
São moléculas catalíticas protéicas (exceto algumas que são RNA) - Prefixo que designa a reação: lactato desidrogenase, catalase
 1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
Físico-química Farmácia 2014/02
 Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
QBQ 0102 Educação Física. Carlos Hotta. Enzimas 17/03/15
 QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
OBJETIVOS BIBLIOGRAFIA ENZIMAS E INIBIDORES ENZIMÁTICOS
 OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
Enzimas Alostéricas e com Múltiplos Sítios Ativos
 Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
Enzimas Alostéricas e com Múltiplos ítios Ativos A presença do substrato em um dos sítios influencia: - a ligação do substrato aos demais sítios vazios - a taxa de formação de produto nos sítios ocupados
A B A B. Espontaneidade vs. Velocidade de Reações. Enzimas como Catalisadores. Velocidade das reações depende da Energia de Ativação
 Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Cinética de reacções. enzimáticas mono-substrato
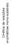 Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Engenharia Biomédica. Relatório Cinética da Enzima Invertase
 Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
[ A][ B] [ A] [ B] v {[A] }= Vmáx
![[ A][ B] [ A] [ B] v {[A] }= Vmáx [ A][ B] [ A] [ B] v {[A] }= Vmáx](/thumbs/75/72105322.jpg) Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Noções de Cinética Química
 QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
QB70C:// Química (Turmas S7/S72) Noções de Cinética Química Prof. Dr. Eduard Westphal (http://paginapessoal.utfpr.edu.br/eduardw) Capítulo 4 Atkins (5ed.) Cinética X Termodinâmica O G para a reação abaixo
PAG Química Cinética 1.
 1. 2. 3. errata: a reação é em mais de uma etapa, os gráficos devem apresentar pelo menos duas!! 4. 5. Explique se cada uma das alternativas abaixo é correta ou não, para reações químicas que ocorrem
1. 2. 3. errata: a reação é em mais de uma etapa, os gráficos devem apresentar pelo menos duas!! 4. 5. Explique se cada uma das alternativas abaixo é correta ou não, para reações químicas que ocorrem
Hidrólise da ureia pela urease
 Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Aula 2: Estrutura e Função de Proteínas
 Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Cinética Química. a temperatura na qual a reação ocorre e a presença de um catalisador.
 Cinética Química Cinética é o estudo da velocidade com a qual as reações químicas ocorrem. Existem quatro fatores importantes que afetam as velocidades das reações: o estado físico do reagente, as concentrações
Cinética Química Cinética é o estudo da velocidade com a qual as reações químicas ocorrem. Existem quatro fatores importantes que afetam as velocidades das reações: o estado físico do reagente, as concentrações
2 APLICAÇÕES INDUSTRIAIS Tabela 1: Enzimas aplicadas na indústria APLICAÇÃO ENZIMA
 CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias.
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Enzimas - Sítio catalítico
 Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015)
 Instituto de Ciências Biomédicas de Abel Salazar - ICBAS-UP Departamento de Química José Augusto Pereira Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015)
Instituto de Ciências Biomédicas de Abel Salazar - ICBAS-UP Departamento de Química José Augusto Pereira Introdução à cinética enzimática. Cinética da catálise pela invertase. Termodinâmica MIB (2015)
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae
 COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae Lauri Alves JUNIOR¹, André Luis Fachini de SOUZA², Vanessa Neves HÖPNER² ¹Acadêmico do curso
COMPARAÇÃO DE MÉTODOS DE LINEARIZAÇÃO DA EQUAÇÃO DE MICHAELIS-MENTEN DA INVERTASE DE Saccharomyces cerevisiae Lauri Alves JUNIOR¹, André Luis Fachini de SOUZA², Vanessa Neves HÖPNER² ¹Acadêmico do curso
Cinética Parte A. Introdução à Química II. Prof. Edson Nossol
 Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC
 IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
CINÉTICA QUÍMICA. Obs.: a variação da quantidade deverá ser sempre um valor positivo, então ela deverá ser em módulo. 1.
 CINÉTICA QUÍMICA 1. Introdução O Conhecimento e o estudo da velocidade das reações, além de ser muito importante em termos industriais, também está relacionado ao nosso dia-adia, verificamos que há algumas
CINÉTICA QUÍMICA 1. Introdução O Conhecimento e o estudo da velocidade das reações, além de ser muito importante em termos industriais, também está relacionado ao nosso dia-adia, verificamos que há algumas
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127. Cinética Química
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Cinética Tempo necessário
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Cinética Tempo necessário
é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições
 Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
TAREFA DA SEMANA DE 31 DE MARÇO A 04 DE ABRIL
 TAREFA DA SEMANA DE 31 DE MARÇO A 04 DE ABRIL QUÍMICA 3ª SÉRIE 1. (Udesc) Considere que um prego é fabricado apenas com o metal Fe. Se este prego entrar em contato com uma solução aquosa de HC, irá acontecer
TAREFA DA SEMANA DE 31 DE MARÇO A 04 DE ABRIL QUÍMICA 3ª SÉRIE 1. (Udesc) Considere que um prego é fabricado apenas com o metal Fe. Se este prego entrar em contato com uma solução aquosa de HC, irá acontecer
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA
 PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
Velocidade de reação. Química Geral. Prof. Edson Nossol
 Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
Velocidade de reação Química Geral Prof. Edson Nossol Uberlândia, 02/12/2016 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H - T S
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA.
 ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação
 Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
ENZIMAS. Universidade Agrícola Uppsala - Suécia Julho W.J.Melo
 ENZIMAS Universidade Agrícola Uppsala Suécia Julho 2003 Cinética Enzimática EFEITO DA CONCENTRAÇÃO DO SUBSTRATO!Como avaliar?!realizase experimento com as seguintes características: #A varios tubos de
ENZIMAS Universidade Agrícola Uppsala Suécia Julho 2003 Cinética Enzimática EFEITO DA CONCENTRAÇÃO DO SUBSTRATO!Como avaliar?!realizase experimento com as seguintes características: #A varios tubos de
Cinética Química. a b c p q r. As concentrações dos reagentes são funções do tempo:
 Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
4. Resultados e Discussão
 Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sítio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sítio ou centro ativo S + E
Gabarito. b) Quantos mols de sítios ativos existem em 1 mg de enzima? Assuma que cada subunidade possui um sítio ativo.
 Gabarito 4. A hidrólise de pirofosfato a ortofosfato é uma reação acoplada importante para deslocar o equilíbrio de reações biossintéticas, por exemplo a síntese de DNA. Esta reação de hidrólise é catalisada
Gabarito 4. A hidrólise de pirofosfato a ortofosfato é uma reação acoplada importante para deslocar o equilíbrio de reações biossintéticas, por exemplo a síntese de DNA. Esta reação de hidrólise é catalisada
Detecção de proteínas. Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas
 Detecção de proteínas Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas A detecção e quantificação de uma proteína através de espectrofotometria se baseia nas propriedades de
Detecção de proteínas Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas A detecção e quantificação de uma proteína através de espectrofotometria se baseia nas propriedades de
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade.
 MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
3.2.2 Métodos de relaxação Métodos de competição Métodos de elevada resolução temporal ORDENS E CONSTANTES DE
 ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008. Disciplina de BIOQUÍMICA I Curso de MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
CINÉTICA QUÍMICA. Prof. Gabriel P. Machado
 CINÉTICA QUÍMICA Prof. Gabriel P. Machado Conceito de velocidade média (v m ) em Química O conceito de velocidade é uma taxa de variação de algum determinado parâmetro por intervalo de tempo. Na Física,
CINÉTICA QUÍMICA Prof. Gabriel P. Machado Conceito de velocidade média (v m ) em Química O conceito de velocidade é uma taxa de variação de algum determinado parâmetro por intervalo de tempo. Na Física,
Aula de Bioquímica I. Tema: Cinética Enzimática. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Cinética Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Cinética Enzimática Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Cinética. Módulo I - Físico Química Avançada. Profa. Kisla P. F. Siqueira
 Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS. Enzimas. Prof. Me. Cássio Resende de Morais
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES
 CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES REAÇÃO GLOBAL: MOSTRA APENAS A MODIFICAÇÃO GLOBAL VELOCIDADE
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS MECANISMO: SEQUÊNCIA DETALHADA DE ETAPAS SIMPLES, ELEMENTARES REAÇÃO GLOBAL: MOSTRA APENAS A MODIFICAÇÃO GLOBAL VELOCIDADE
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS
 CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS A VELOCIDADE DE UMA REAÇÃO: É UMA MEDIDA DE QUÃO RÁPIDO UM REAGENTE É CONSUMIDO OU UM PRODUTO É FORMADO 1) Na reação de A +
CINÉTICA QUÍMICA É O ESTUDO DAS VELOCIDADES E MECANISMOS DAS REAÇÕES QUÍMICAS A VELOCIDADE DE UMA REAÇÃO: É UMA MEDIDA DE QUÃO RÁPIDO UM REAGENTE É CONSUMIDO OU UM PRODUTO É FORMADO 1) Na reação de A +
Copyright McGraw-Interamericana de España. Autorização necessária para reprodução ou utilização. Cinética Química
 Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
BCL 0307 Transformações Químicas
 BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
Capítulo by Pearson Education
 QUÍMICA A Ciência Central 9ª Edição Cinética química David P. White Fatores que afetam a velocidade de reações A cinética é o estudo da velocidade na qual as reações químicas ocorrem. Existem quatro fatores
QUÍMICA A Ciência Central 9ª Edição Cinética química David P. White Fatores que afetam a velocidade de reações A cinética é o estudo da velocidade na qual as reações químicas ocorrem. Existem quatro fatores
Avenida Lourival Alfredo, 176, Poeira, Marechal Deodoro, Alagoas, Brasil,
 5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
Experimento MRU Construindo Gráficos Propagação de Erros
 Universidade Federal de Lavras Departamento de Física Experimento MRU Construindo Gráficos Propagação de Erros Laboratório de Física A e I Objetivos e Materiais Objetivos: Estudar os conceitos básicos
Universidade Federal de Lavras Departamento de Física Experimento MRU Construindo Gráficos Propagação de Erros Laboratório de Física A e I Objetivos e Materiais Objetivos: Estudar os conceitos básicos
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
PQI 3221 Cinética Química e Processos Ambientais
 PQI 3221 inética Química e Processos Ambientais Aula 14 Balanços de massa em processos com reações químicas. inética química. Ordem de reação Prof. Antonio arlos S.. Teixeira entro de Engenharia de Sistemas
PQI 3221 inética Química e Processos Ambientais Aula 14 Balanços de massa em processos com reações químicas. inética química. Ordem de reação Prof. Antonio arlos S.. Teixeira entro de Engenharia de Sistemas
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
Aspectos práticos do estudo da cinética enzimática
 Aspectos práticos do estudo da cinética enzimática Tipos de ensaios de cinéticos Ensaios contínuos: o progresso da reacção é monitorizado continuamente, de forma automatizada Ensaios descontínuos: são
Aspectos práticos do estudo da cinética enzimática Tipos de ensaios de cinéticos Ensaios contínuos: o progresso da reacção é monitorizado continuamente, de forma automatizada Ensaios descontínuos: são
Cinética Química. Cinética Química...? É o estudo da velocidade das reações químicas e dos fatores que as influenciam.
 Cinética Química...? Universidade Federal de Campina Grande Centro de Ciência e Tecnologia groalimentar Profª Roberlucia Candeia Disciplina: Química geral É o estudo da velocidade das reações químicas
Cinética Química...? Universidade Federal de Campina Grande Centro de Ciência e Tecnologia groalimentar Profª Roberlucia Candeia Disciplina: Química geral É o estudo da velocidade das reações químicas
Físico-Química Experimental Exp. 10. Cinética Química
 Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Metabolismo e Endocrinologia
 Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Cinética Química. Mestrado integrado em Engenharia Biológica. Disciplina Química II, 2º semestre 2009/10. Professsora Ana Margarida Martins
 Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
Cinética enzimática. Cinética enzimática. Cinética enzimática 20/03/2012. Classificação sistemática das enzimas
 Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
QFL4420 FÍSICO- QUÍMICA II 2015
 QFL4420 FÍSICO- QUÍMICA II 2015 Química Ambiental e Licenciatura N 1 a lista de exercícios 1. O desproporcionamento de ácido bromoso 2 HBrO 2 HBrO HBrO 3 foi estudado a 293 K, tendo-se obtido as seguintes
QFL4420 FÍSICO- QUÍMICA II 2015 Química Ambiental e Licenciatura N 1 a lista de exercícios 1. O desproporcionamento de ácido bromoso 2 HBrO 2 HBrO HBrO 3 foi estudado a 293 K, tendo-se obtido as seguintes
a) Qual deverá ser o volume do PFR para converter 80% de A em fase líquida? Considerar alimentação a 44 L min -1 e C A0 = C B0 = 1 mol L -1
 501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
501) Um dado composto A se decompõe conforme a cinética enzimática de Michaelis-Menten,. Determine os parâmetros V máx e K M, considerando os dados experimentais a seguir. C A (kmol m -3 ) 0,1 0,01 0,005
Fabio Rodrigo da Costa Dias. 2. Velocidade média e instantânea das Reações Químicas
 Cinética Química Fabio Rodrigo da Costa Dias 1. Introdução Cinética química é a área da química responsável pelo estudo das velocidades das reações químicas, bem como dos fatores que influenciam nessas
Cinética Química Fabio Rodrigo da Costa Dias 1. Introdução Cinética química é a área da química responsável pelo estudo das velocidades das reações químicas, bem como dos fatores que influenciam nessas
2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados;
 CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
CINÉTICA QUÍMICA 1. Trata das velocidades das reações; 2. Aborda a rapidez com que os reagentes são consumidos e os produtos são formados; 3. A dependência da velocidade; 4. Estudo do mecanismo de reação.
Proteínas II. (Enzimas) Bioquímica Prof. Dr. Marcelo Soares
 Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Enzimas que ultrapassam o limite difusivo
 Enzimas que ultrapassam o limite difusio Em certas condições é possíel obserar eficiências catalíticas superiores ao limite difusional do substrato e enzima. 1 - Canalização de substratos: Enzima 1 Enzima
Enzimas que ultrapassam o limite difusio Em certas condições é possíel obserar eficiências catalíticas superiores ao limite difusional do substrato e enzima. 1 - Canalização de substratos: Enzima 1 Enzima
Cinética Química. R Δ[ R] vmédia. A fórmula acima calcula a velocidade média de desaparecimento de um reagente (
![Cinética Química. R Δ[ R] vmédia. A fórmula acima calcula a velocidade média de desaparecimento de um reagente ( Cinética Química. R Δ[ R] vmédia. A fórmula acima calcula a velocidade média de desaparecimento de um reagente (](/thumbs/72/67725684.jpg) Cinética Química André Silva Franco A cinética química estuda a velocidade das reações e todos os fatores envolvidos diretamente ou indiretamente na velocidade. m geral, mede-se a velocidade de uma reação
Cinética Química André Silva Franco A cinética química estuda a velocidade das reações e todos os fatores envolvidos diretamente ou indiretamente na velocidade. m geral, mede-se a velocidade de uma reação
Cinética Michaeliana [E] [A] é difícil de determinar em muitas situações, pelo que se. ) pode ser ajustada a uma. . É o valor máximo de
![Cinética Michaeliana [E] [A] é difícil de determinar em muitas situações, pelo que se. ) pode ser ajustada a uma. . É o valor máximo de Cinética Michaeliana [E] [A] é difícil de determinar em muitas situações, pelo que se. ) pode ser ajustada a uma. . É o valor máximo de](/thumbs/83/88787633.jpg) Cinética Michaeliana Diz-se que u enzia apresenta ua cinética Michaeliana sepre que a variação da velocidade inicial edida (v i ) pode ser ajustada a ua expressão da fora: v [E] 0 0 Cinética Michaeliana
Cinética Michaeliana Diz-se que u enzia apresenta ua cinética Michaeliana sepre que a variação da velocidade inicial edida (v i ) pode ser ajustada a ua expressão da fora: v [E] 0 0 Cinética Michaeliana
Inibidores Enzimáticos
 Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
Tabela 1: Aumento de velocidade de reação proporcionado por certas enzimas Enzima Velocidade da reação não catalisada
 Bioquímica Metabólica Noturno Prof. Roberto K. Salinas 2. Cinética enzimática Enzimas são catalisadores em sistemas biológicos. As características mais notáveis das enzimas são o seu poder catalítico e
Bioquímica Metabólica Noturno Prof. Roberto K. Salinas 2. Cinética enzimática Enzimas são catalisadores em sistemas biológicos. As características mais notáveis das enzimas são o seu poder catalítico e
ENZIMAS. Dra. Flávia Cristina Goulart. Bioquímica
 ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
Enzimas. Bianca Zingales IQ - USP
 Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
USO DE EQUAÇÕES LINEARES NA DETERMINAÇÃO DOS PARÂMETROS DE MICHAELIS-MENTEN
 Quim. Nova, Vol. 33, No. 7, 1607-1611, 2010 USO DE EQUAÇÕES LINEARES NA DETERMINAÇÃO DOS PARÂMETROS DE MICHAELIS-MENTEN Nakédia M. F. Carvalho, Bianca M. Pires, Octavio A. C. Antunes e Roberto B. Faria*
Quim. Nova, Vol. 33, No. 7, 1607-1611, 2010 USO DE EQUAÇÕES LINEARES NA DETERMINAÇÃO DOS PARÂMETROS DE MICHAELIS-MENTEN Nakédia M. F. Carvalho, Bianca M. Pires, Octavio A. C. Antunes e Roberto B. Faria*
Pi Principais i i Tópicos Abordados dd
 BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016
 CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
Enzimas e Actividade enzimática
 Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
QUÍMICA Cinética Química Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª.
 QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores
 Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Aula 4: Gráficos lineares
 Aula 4: Gráficos lineares 1 Introdução Um gráfico é uma curva que mostra a relação entre duas variáveis medidas. Quando, em um fenômeno físico, duas grandezas estão relacionadas entre si o gráfico dá uma
Aula 4: Gráficos lineares 1 Introdução Um gráfico é uma curva que mostra a relação entre duas variáveis medidas. Quando, em um fenômeno físico, duas grandezas estão relacionadas entre si o gráfico dá uma
