Atividade a Distância 4 CINÉTICA
|
|
|
- Denílson Correia Estrada
- 7 Há anos
- Visualizações:
Transcrição
1 Atividade a Distância 4 CINÉTICA Na parte 1 da Aula 3 vimos a definição de velocidade inicial e como deve ser medida. Agora, vamos ver como ela varia se mudarmos a concentração dos reagentes. Estamos acostumados a ver os gráficos de saturação de enzimas. Nas aulas para a graduação, o aluno já sabe que a enzima satura, mas não sabe exatamente o porquê. Então, para entender o que se passa, vamos fazer um exercício de raciocínio sobre a velocidade inicial das reações, sejam catalisadas ou não por enzimas. Tente esquecer a saturação, por enquanto... Na reação em que um substrato (S) forma um produto (P), o equilíbrio é representado por: k 1 S k 2 onde k 1 e k 2 são as constantes de velocidade da formação de produto e de resgente (substrato), respectivamente. No início da reação, bem antes de chegar ao equilíbrio, apenas a etapa 1 ocorre e podemos determinar a velocidade inicial da reação (V 0 ), através da equação: P V 0 = k 1.[S] (eq. 1) Essa é uma equação de reta, semelhante àquela que já vimos, do tipo y = A + Bx. Na eq. 1, V 0 é a variável dependente (y), a concentração de substrato é a variável independente (x) e k 1 é a inclinação da reta (B). Nesse caso, A = 0, ou seja, sempre que x = 0, y = 0. Vamos traduzir? O que quero dizer é que, no caso de não existir substrato na reação (x = 0), a reação não existe (V 0 = 0)! Tem sentido, não? Além disso, a equação diz que V 0 é proporcional à [S]. Isso quer dizer que V 0 aumenta sempre que [S] aumenta. Vamos fazer uma simulação dessa situação. Estamos trabalhando em uma temperatura constante, então k 1 é constante. Considere k 1 = 0,1 s -1. Calcule V 0 para diferentes concentrações de substrato: [S] (mol) V 0 (mol/s)* *Obs: a unidade que representa a velocidade pode ser escrita como mol/s ou mol.s -1. Qual seria o melhor gráfico para representar essa situação acima? V0 (mol/s) (A) [Substrato] (mol) V0 (mol/s) (B) [Substrato] (mol) V0 (mol/s) (C) [Substrato] (mol)
2 A maioria de vocês escolheu o gráfico correto (B). A situação que usamos foi aquela da reação espontânea, S P, onde consideramos apenas a primeira etapa, ou seja, a formação de P. Essa reação não chegou ao equilíbrio e, portanto, só a etapa 1 está ocorrendo. Essa etapa tem k 1 = 0,1 s -1 e se calcularmos V 0 para diferentes concentrações de substrato usando a eq. 1, teremos: [S] (mol) V 0 (mol/s)* 1 0,1 2 0,2 4 0,4 8 0,8 10 1,0 Essa equação, V 0 = k 1.[S], diz que V 0 é proporcional à concentração inicial de reagente (S). Isso quer dizer que na ausência de S, V 0 = 0. Mas também quer dizer que V 0 aumenta sempre que a concentração de S aumenta e que esse aumento é linear. Ou seja, se usarmos uma concentração infinita de S, V 0 tenderá ao infinito também! Mas, o que você acha que deve acontecer num sistema em que temos enzimas? Num primeiro momento, sei que vem aquela idéia da saturação, e ela existe sim, mas gostaria que vocês entendessem de onde vem essa saturação. Quero dizer: vocês já sabem o que é a saturação do ponto de vista estrutural, mas talvez não saibam do ponto de vista cinético. Bom, antes de continuarmos, vamos ver alguns conceitos de cinética química: Para uma decomposição unimolecular, temos: A P e V 0 = k.[a] (eq. 1b) Com dois reagentes, ou seja, uma decomposição bimolecular, temos: A + B P e V 0 = k.[a].[b] (eq. 2) Então, vamos para outra representação de um esquema cinético, agora com a participação de uma enzima (E): S + E k 1 k 2 P + E DICA: Não há formação de complexo enzimasubstrato (ES) e a enzima não é consumida na reação ([E] = constante). Se a velocidade dessa reação for medida com diferentes concentrações de S, pode-se determinar V 0 a partir da equação 2. Nesse caso, manteremos a concentração de enzima constante (10 µg/ml) e vamos variando a concentração de substrato da mesma forma que na questão anterior. Podemos considerar a mesma constante de velocidade (k 1 = 0,1 s -1 ). Qual a equação de velocidade nesse caso? Lembrem-se [S] (mol) V 0 (???/???) Qual seria o melhor gráfico para representar essa situação acima? Um linear, como aqueles mostrados em A e B, ou um com saturação, como mostrado em C? Observação: Indique o TIPO de gráfico (linear ou não). Quando temos uma reação bimolecular, do tipo: A + B P, a velocidade é calculada pela eq. 2. Porém, há casos em que a concentração de um dos reagentes é constante (porque é um catalisador ou porque está em grande excesso em relação ao outro reagente). Com isso, a concentração de tal reagente deve ser considerada constante e, portanto, será agregada à constante de velocidade. Complicado? Talvez, mas podemos pensar em etapas... Vamos considerar que na reação A + B P a concentração de B é muitíssimo maior que a
3 concentração de A. Nesse caso, podemos dizer que B praticamente não é consumido na reação, o que podemos considerar como sendo constante no tempo de reação em que estamos medindo V 0. Que tal colocar isso em números? Considere uma situação em que iniciamos a reação com [A] = 0,01 mol/l e [B] = 10 mol/l, sendo que ao final da reação há um consumo de apenas 0,0005 mol/l de cada reagente. Dessa forma, chegamos ao final da reação com [A] = 0,0095 mol/l, o que corresponde a um consumo de 5% de A. Nesse mesmo tempo de reação, teríamos [B] = 9,9995 mol/l, ou seja, um gasto de 0,005% de B. Comparativamente, podemos considerar que a concentração de B ficou constante. Nesse caso, a eq. 2 deve ser reescrita: V 0 = k 1 [A] constante Lembrando que k 1 é constante, teremos, então: V 0 = constante constante [A] PARA QUEM AINDA NÃO SE CONFORMA: Lembro que estamos trabalhando um caso cinético hipotético, pois quero que compreendam a saturação que nunca aconteceria se as enzimas atuassem como meros catalisadores químicos! A atividade enzimática pode ser expressa em: - Unidade Internacional (U): uma U representa a quantidade de enzima que catalisa 1 µmol de susbtrato por minuto, a 25 C (o ph deve ser indicado em cada caso): 1 µmol/min. - Atividade específica: esta leva em conta a quantidade de enzima no meio de reação e é dada por nmol de substrato por minuto, por mg de enzima (µmol/min.mg). - Atividade molecular: mmol/min.mmol E. ou seja, V 0 = k 1.[A] eq. 3 sendo k 1 uma nova constante! Portanto, variação de V 0 em função de [A] é LINEAR, como no caso descrito pela eq. 1. Como comentei acima, outra situação onde isso acontece é com o uso de catalisadores. Ou seja, B pode não ser um reagente, mas um catalisador que é prontamente devolvido ao meio de reação, mantendo sua concentração praticamente constante. Com isso, teremos o mesmo raciocínio anterior. Ou seja, para o caso descrito, de uma enzima E hipotética que é mantida constante e/ou prontamente devolvida para a reação, teremos a mesma situação: V 0 = k 1 [S] constante ou V 0 = k 1 [S], e o comportamento é linear, como descrito acima. Muito simples! Vamos para o próximo desafio??? Neste novo esquema cinético, forma-se o complexo Enzima/Substrato (ES): E + S k1 k2 Para a formação de P, precisamos que ocorram as etapas 1 (k 1 ) e 3 (k 3 ), correto? Mas quando uma reação ocorre em etapas, como a descrita acima, a velocidade é determinada pela etapa mais lenta. Agora, respondam: E S k3 k4 E + P Qual é a equação de velocidade inicial dessa reação se a etapa lenta for a 1?
4 Nesse caso, ocorre saturação ou V 0 aumenta linearmente com [S]? Para responder isso, é preciso definir quais são os reagentes dessa reação, pois estes são os que definem a velocidade inicial! Lembrem-se que V 0 = k.[reagente] inicial. Como a maioria percebeu, se a etapa 1 é a mais lenta, os substratos da reação são E e S, e o produto, ES. A equação de velocidade inicial é: V 0 = k 1.[E].[S] (eq. 2b) Nesse caso hipotético, o produto ES se desfaz rapidamente, tanto pela etapa 2 (volta) como pela etapa 3 (formação de produto), "devolvendo" a enzima para o meio. Com isso, a concentração de E se mantém praticamente constante. Mais uma vez, podemos definir k 1 ', que é igual a k 1.[E]. situação descrita, em termos de equação de velocidade inicial de reação. Como já vimos, a etapa lenta é a que define a velocidade de uma reação. Neste caso em que a etapa lenta é a 3; o reagente é o complexo enzima-substrato e a equação é descrita por: V 0 = k 3.[ES] A concentração de enzimas é constante e, portanto, a velocidade da reação aumenta com [S] até que todas as enzimas estejam na forma de ES. Com isso, finalmente vemos a tão esperada saturação! Dessa forma, mesmo que a concentração de S seja infinita, V 0 atinge um valor que depende da concentração inicial de enzimas, pois isso também define a concentração de ES, não só a [S]. Então, V 0 = k 1 '.[S] (eq. 3b) A eq. 3b diz que a velocidade INICIAL depende apenas da concentração inicial de S. Se fizermos um gráfico de V 0 em função da concentração de S, o mesmo será LINEAR. O desafio final para entendermos o tratamento cinético das reações catalisadas por enzimas. Considerando o mesmo esquema cinético anterior, sendo que, agora, a etapa limitante é aquela com constante de velocidade k 3. E + S k1 k2 E S k3 k4 E + P Nesse caso, como fica a dependência de V 0 com a concentração de [S]? Ao aumentarmos [S] na reação, vamos atingir uma saturação ou teremos, mais uma vez, um gráfico linear? Esse é o caso que descreve as enzimas Michaelianas, ou seja, as enzimas que tem o comportamento descrito por Michaelis- Menten. Logo a seguir vamos entrar nesse formalismo. Por enquanto, vamos analisar a Esse raciocínio que desenvolvemos até o momento foi crucial para a compreensão do mecanismo de catálise enzimática. Victor Henri (1902) postulou a existência de um complexo intermediário enzima-substrato para explicar o mecanismo de ação das enzimas. Em 1913, Leonor Michaelis e Maud Leonora Menten confirmaram essa hipótese e descreveram um modelo matemático para a cinética enzimática. MODELO CINÉTICO DE MICHAELIS- MENTEN A reação catalisada por uma enzima, ao atingir o equilíbrio, pode ser representada pelo esquema cinético apresentado nos dois últimos desafios, onde vemos a formação do complexo ES. Se considerarmos a condição de equilíbrio, a velocidade da reação (V), ou seja, de formação do produto, seria: V = k 3 [ES] k 4 [E].[P] (eq. 4)
5 Porém, no estado inicial, quando a concentração de P é muito pequena, estamos longe de atingir o equilíbrio e podemos simplificar a reação: E + S Isso quer dizer que no estado inicial da reação não ocorre a etapa 4, e a velocidade de reação, neste caso, será V 0 = k 3.[ES]. Na análise cinética da reação catalisada por uma enzima, devemos considerar o ESTADO ESTACIONÁRIO que é aquele em que, apesar de estarem mudando as concentrações de reagentes (diminuindo) e de produtos (aumentando), não há variação na concentração dos intermediários da reação. No caso descrito pelo esquema cinético acima, o intermediário da reação é o complexo ES e no estado estacionário: ou... k 1 [E].[S] = (k 2 + k 3 )[ES] (eq. 5) Essa equação pode ser rearranjada, agrupando as constantes de velocidade: [E][S] (k 2 + k 3 )/k 1 = [ES] (eq. 6) Para simplificar a equação 6, foi definida a constante de Michaelis-Menten (K m ): Km = k1 k2 E S (k 2 + k 3 ) k 1 k3 V FORMAÇÃO =V DECOMPOSIÇÃO DE ES DE ES Analise a equação 7, e responda: E + P (eq. 7) ATENÇÃO: Antes de ver a questão, chamamos a atenção para que, na resposta, deve usar eq. 7 sem modificação. Ou seja, considere apenas a forma como K m foi definida (uma relação entre constantes de velocidade e que, portanto, descrevem etapas da reação global) SEM FAZER SUBSTITUIÇÕES POR CONCENTRAÇÕES (de S, E, ES e/ou P). - Qual o significado de Km? Para ver se compreendeu, raciocine dessa forma: o que significa um valor alto de K m? E um valor baixo de K m? Em primeiro lugar, essa é uma relação entre constantes de velocidade, então K m tem que ser constante! Por isso pedimos que não substituíssem por concentrações, pois teríamos um valor de K m para cada condição utilizada. Na equação 7, temos duas constantes de velocidade para dissociação de ES (k2 e k3) divididas pela constante de velocidade para a associação, que gera ES. Ou seja, duas constantes de velocidade de reação de decomposição, divididas pela constante de velocidade de formação. Essa relação está mostrando o quanto o complexo prefere estar na forma de ES ou não. O que quero dizer é que K m define a afinidade da enzima pelo substrato. Afinidade alta significa que a formação do complexo ES (k1) prevalece sobre sua dissociação (k2 e/ou k3). Respondendo a parte B, um valor alto de K m descreve uma situação em que a enzima tem baixa afinidade pelo substrato e um valor baixo de K m, o oposto, mostra que a enzima tem uma alta afinidade pelo substrato. Dando continuidade, substituímos a eq. 7 na eq. 6: [E][S] Km = [ES] (eq. 8) Considerando-se que toda a enzima no meio de reação está na sua forma livre (E) ou na forma de complexo (ES), podemos dizer que: [E] TOTAL = [E] + [ES] ou... [E] = [E] TOTAL [ES] (eq. 9)
6 Na eq. 8, [E] pode ser substituída pela expressão da eq. 9: [ES] = ([E] TOTAL - [ES]).[S] Km Que pode ser rearranjada: [ES] = [E] TOTAL.[S] [S] + Km eq. 10 eq. 10b Assim definida a [ES], podemos substituí-la na equação de velocidade inicial da reação que é V 0 = k 3.[ES] (questão 4), chegando a uma nova equação: A equação 11 mostra como a velocidade inicial está relacionada à concentração de enzimas e de substratos no meio de reação. Reparem que a equação diz que, V 0 depende não só das concentrações de enzimas e de substratos no meio de reação, pois devemos levar em conta a afinidade entre eles, ou seja, o K m! Agora, respondam: em que situação teremos V 0 = k 3 [E] TOTAL? (usando a eq. 11) V 0 = k 3 [E] TOTAL.[S] [S] + Km (eq. 11) ESTA ATIVIDADE SERÁ COMPLETADA À MEDIDA QUE VOCÊS CONCLUIREM AS PERGUNTAS QUE FOREM SURGINDO. NO FINAL, SERÁ UMA AULA COMPLETA. É proibida a reprodução de parte ou do todo desta publicação sem a permissão formal de seus autores. Laboratório de Biocalorimetria Instituto de Bioquímica Médica UFRJ Apoio:
CQ110 : Princípios de FQ. Imagens de Rorschach
 Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Imagens de Rorschach 1 Leis de velocidade Velocidade de uma reação química: Variação de reagentes / produtos em função do tempo: a A+ b B produtos v = k [A] x [B] y Lei de velocidade k: constante de velocidade
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
Introdução aos Conceitos de Velocidade Máxima e de Atividade Específica de Enzimas
 RBEBBM -01/2001 Introdução aos Conceitos de Velocidade Máxima e de Atividade Específica de Enzimas (Introducing the Concepts of Maximal Velocity and Specific Activity of Enzymes) Autores:M. Lucia Bianconi
RBEBBM -01/2001 Introdução aos Conceitos de Velocidade Máxima e de Atividade Específica de Enzimas (Introducing the Concepts of Maximal Velocity and Specific Activity of Enzymes) Autores:M. Lucia Bianconi
CINÉTICA QUÍMICA. Prof. Gabriel P. Machado
 CINÉTICA QUÍMICA Prof. Gabriel P. Machado Conceito de velocidade média (v m ) em Química O conceito de velocidade é uma taxa de variação de algum determinado parâmetro por intervalo de tempo. Na Física,
CINÉTICA QUÍMICA Prof. Gabriel P. Machado Conceito de velocidade média (v m ) em Química O conceito de velocidade é uma taxa de variação de algum determinado parâmetro por intervalo de tempo. Na Física,
Avenida Lourival Alfredo, 176, Poeira, Marechal Deodoro, Alagoas, Brasil,
 5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
5 CINÉTICA QUÍMICA 1 Introdução A química é, por sua própria natureza, preocupada com a mudança. As reações químicas convertem substâncias com propriedades bem-definidas em outros materiais com propriedades
Cinética de reacções. enzimáticas mono-substrato
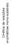 Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Cinética de reacções enzimáticas mono-substrato Curva de progresso de reacção enzimática mono-substrato [P] Concentração relativa Tempo = e kt d d [P] v = = = k e dt dt kt Atenuação da velocidade de reacção
Química Geral e Inorgânica. QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin. Cinética Química
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Cinética Química Cinética Química É a área da química que está preocupada com a velocidade das reações químicas.
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Cinética Química Cinética Química É a área da química que está preocupada com a velocidade das reações químicas.
C n i é n t é i t c i a
 Cinética Velocidade Média A velocidade média de consumo de um reagente ou de formação de um produto é calculada em função da variação da quantidade de reagentes e produtos pela variação do tempo. Vm =
Cinética Velocidade Média A velocidade média de consumo de um reagente ou de formação de um produto é calculada em função da variação da quantidade de reagentes e produtos pela variação do tempo. Vm =
Cinética Química. a b c p q r. As concentrações dos reagentes são funções do tempo:
 Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
Cinética Química A cinética química estuda a evolução das reacções químicas no tempo a b c p q r A+ B+ C+... P+ Q+ R+... Concentrações: [A],[B],[C],... Coeficientes estequiométricos: a,b,c,... Constantes
PAG Química Cinética 1.
 1. 2. 3. errata: a reação é em mais de uma etapa, os gráficos devem apresentar pelo menos duas!! 4. 5. Explique se cada uma das alternativas abaixo é correta ou não, para reações químicas que ocorrem
1. 2. 3. errata: a reação é em mais de uma etapa, os gráficos devem apresentar pelo menos duas!! 4. 5. Explique se cada uma das alternativas abaixo é correta ou não, para reações químicas que ocorrem
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética Química. Prof. Alex Fabiano C. Campos. Rapidez Média das Reações
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Catálise Enzimática. Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química.
 Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Avaliação Quantitativa das Preparações Enzimáticas
 Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
Avaliação Quantitativa das Preparações Enzimáticas Como diferenciar enzimas? Quando não podemos determinar a concentração de uma enzima devemos diferenciar as enzimas por sua atividade (moléculas não podem
META Compreender os conceitos relacionado a lei de arrhenius e seus modelos matematicos. Compreender as aplicações catálise e seus fundamentos.
 ATIVIDADS SOBR LI D ARHHNIUS CATÁLIS Aula 7 MTA Compreender os conceitos relacionado a lei de arrhenius e seus modelos matematicos. Compreender as aplicações catálise e seus fundamentos. OBJTIVOS Ao fi
ATIVIDADS SOBR LI D ARHHNIUS CATÁLIS Aula 7 MTA Compreender os conceitos relacionado a lei de arrhenius e seus modelos matematicos. Compreender as aplicações catálise e seus fundamentos. OBJTIVOS Ao fi
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA
 PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
PROVA ESCRITA DE CONHECIMENTOS EM QUÍMICA INFORMAÇÕES IMPORTANTES: - IDENTIFIQUE TODAS AS FOLHAS DESTA PROVA COM SEU NÚMERO DE INSCRIÇÃO. Obs.: EM HIPÓTESE NENHUMA USE SEU NOME NAS FOLHAS COMO IDENTIFICAÇÃO.
Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
 CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
São moléculas catalíticas protéicas (exceto algumas que são RNA) - Prefixo que designa a reação: lactato desidrogenase, catalase
 1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
BCL 0307 Transformações Químicas
 BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 09 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Concentrações, velocidades
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Cinética Química. Prof. Alex Fabiano C. Campos
 Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Cinética Química Prof. Alex Fabiano C. Campos Rapidez Média das Reações A cinética é o estudo da rapidez com a qual as reações químicas ocorrem. A rapidez de uma reação pode ser determinada pela variação
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Físico-Química Experimental Exp. 10. Cinética Química
 Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
Cinética Química 1. Introdução Cinética química é o estudo da progressão das reações químicas, o que determina suas velocidades e como controlá-las. Ao estudar a termodinâmica de uma reação, leva-se em
CINÉTICA QUÍMICA VELOCIDADE DE UMA REAÇÃO. Giseli Menegat e Maira Gazzi Manfro
 CINÉTICA QUÍMICA VELOCIDADE DE UMA REAÇÃO Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br VELOCIDADE MÉDIA DAS REAÇÕES O conceito de velocidade abordado
CINÉTICA QUÍMICA VELOCIDADE DE UMA REAÇÃO Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br VELOCIDADE MÉDIA DAS REAÇÕES O conceito de velocidade abordado
Aula 12: Enzimas Introdução e Cinética
 Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Cinética Química Lei de Velocidade Integrada Mostra a variação das concentrações
Aula 3 REAÇÕES ELEMENTARES. META Estudar as reações elementares e suas peculiaridades
 REAÇÕES ELEMENTARES Camilo Andrea Angelucci Aula META Estudar as reações elementares e suas peculiaridades OBJETIVOS Ao fi nal desta aula, o aluno deverá: reações Elementares molecularidade de uma reação
REAÇÕES ELEMENTARES Camilo Andrea Angelucci Aula META Estudar as reações elementares e suas peculiaridades OBJETIVOS Ao fi nal desta aula, o aluno deverá: reações Elementares molecularidade de uma reação
BCL 0307 Transformações Químicas
 BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 08 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Cinética química
BCL 0307 Transformações Químicas Prof. Dr. André Sarto Polo Bloco B S. 1014 ou L202 andre.polo@ufabc.edu.br Aula 08 http://pesquisa.ufabc.edu.br/pologroup/transformacoes_quimicas.html Cinética química
QBQ 0316 Bioquímica Experimental. Carlos Hotta. Análise de dados (P1 e P2)
 QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
TEORIA DO ESTADO ESTACIONÁRIO E SIMULAÇÃO COMPUTACIONAL.
 EXERCÍCIOS SOBRE: TEORIA DA COLISÃO, TEORIA DO ESTADO ESTACIONÁRIO E SIMULAÇÃO COMPUTACIONAL. Glauber Silva Godoi META Desenvolver no aluno a capacidade de extrair os parâmetros cinéticos de uma reação
EXERCÍCIOS SOBRE: TEORIA DA COLISÃO, TEORIA DO ESTADO ESTACIONÁRIO E SIMULAÇÃO COMPUTACIONAL. Glauber Silva Godoi META Desenvolver no aluno a capacidade de extrair os parâmetros cinéticos de uma reação
2 APLICAÇÕES INDUSTRIAIS Tabela 1: Enzimas aplicadas na indústria APLICAÇÃO ENZIMA
 CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
CINÉTICA ENZIMÁTICA INTRODUÇÃO O conhecimento das propriedades cinéticas das enzimas é importante para compreender as transformações que ocorrem no interior das células que participam dos processos fermentativos
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação
 Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Aula: 28 Temática: Efeito da Temperatura na Velocidade de Reação Em grande parte das reações, as constantes de velocidade aumentam com o aumento da temperatura. Vamos analisar esta dependência. A teoria
Cinética Química. a temperatura na qual a reação ocorre e a presença de um catalisador.
 Cinética Química Cinética é o estudo da velocidade com a qual as reações químicas ocorrem. Existem quatro fatores importantes que afetam as velocidades das reações: o estado físico do reagente, as concentrações
Cinética Química Cinética é o estudo da velocidade com a qual as reações químicas ocorrem. Existem quatro fatores importantes que afetam as velocidades das reações: o estado físico do reagente, as concentrações
QUÍMICA Cinética Química Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª.
 QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
QUÍMICA Cinética Química Concentração, Pressão, Temperatura e Catalisador - Parte 4 Prof ª. Giselle Blois CONCENTRAÇÃO DOS REAGENTES: O aumento da concentração dos reagentes acarreta em um aumento da velocidade
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Cinética Tempo necessário
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Cinética Tempo necessário
Físico-química Farmácia 2014/02
 Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Físico-química Farmácia 2014/02 1 Decomposição Química Cinética de decomposição Lei de velocidade Ordem de reação Tempo de meia vida e prazo de validade Fatores que influenciam a estabilidade Equação de
Concentração dos reagentes Quanto maior a concentração dos reagentes, maior a velocidade da reação.
 Setor 3306 Aula 20 Lei da velocidade das reações Complemento. As reações químicas podem ocorrer nas mais diferentes velocidades. Existem reações tão lentas que levam milhares de anos para ocorrer, como
Setor 3306 Aula 20 Lei da velocidade das reações Complemento. As reações químicas podem ocorrer nas mais diferentes velocidades. Existem reações tão lentas que levam milhares de anos para ocorrer, como
Copyright McGraw-Interamericana de España. Autorização necessária para reprodução ou utilização. Cinética Química
 Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
Capítulo 3 Cinética Química Velocidade de Uma Reacção Lei de Velocidades Relação Entre a Concentração de Reagente e o Tempo Energia de Activação e Dependência das Constantes de Velocidade com a Temperatura
AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: CONCENTRAÇÃO DE REAGENTES E TEMPERATURA DE REAÇÃO.
 AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: CONCENTRAÇÃO DE REAGENTES E TEMPERATURA DE REAÇÃO. Aula 11 Glauber Silva Godoi META Desenvolver no aluno a capacidade de avaliar
AVALIAÇÃO DOS FATORES QUE INFLUENCIAM A VELOCIDADE DAS REAÇÕES QUÍMICAS: CONCENTRAÇÃO DE REAGENTES E TEMPERATURA DE REAÇÃO. Aula 11 Glauber Silva Godoi META Desenvolver no aluno a capacidade de avaliar
ocorridas na concentração dos participantes das reações em função do tempo:
 CINÉTICA QUÍMICA Fala Gás Nobre! Preparado para reagir? Então vamos para mais um resumo de química! Você já parou pra pensar, que a velocidade com que as reações químicas acontecem, podem estar relacionadas
CINÉTICA QUÍMICA Fala Gás Nobre! Preparado para reagir? Então vamos para mais um resumo de química! Você já parou pra pensar, que a velocidade com que as reações químicas acontecem, podem estar relacionadas
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA.
 ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
ESTUDO DA CINÉTICA DA HIDRÓLISE ÁCIDA DO ACETATO DE ETILA. Glauber Silva Godoi Aula 14 META Desenvolver no aluno a capacidade de extrair informações quanto aos parâmetros cinéticos de uma reação a partir
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Reações de Segunda Ordem Exercício 05: Entre os possíveis destinos do NO 2 na química
Química Geral e Experimental II: Cinética Química. Prof. Fabrício Ronil Sensato
 Química Geral e Experimental II: Cinética Química Prof. Fabrício Ronil Sensato Resolução comentada de exercícios selecionados. Versão v2_2005 2 1) Para a reação em fase gasosa N 2 + 3H 2 2NH 3, 2) A decomposição,
Química Geral e Experimental II: Cinética Química Prof. Fabrício Ronil Sensato Resolução comentada de exercícios selecionados. Versão v2_2005 2 1) Para a reação em fase gasosa N 2 + 3H 2 2NH 3, 2) A decomposição,
3.2.2 Métodos de relaxação Métodos de competição Métodos de elevada resolução temporal ORDENS E CONSTANTES DE
 ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
ÍNDICE Prefácio... 3 1. INTRODUÇÃO... 7 1.1. Dificuldades iniciais no desenvolvimento da Cinética Química no séc. XX... 8 1.2. A Cinética Química actual... 12 2. LEIS DE VELOCIDADE DE REACÇÃO... 27 2.1.
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade.
 MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
MECANISMOS a descrição microscópica da reação; são propostos com base na lei de velocidade. 1 Mecanismo: como os reagentes são convertidos em produtos, no nível molecular. LEI DE VELOCIDADE ----> MECANISMO
CINÉTICA QUÍMICA. Profa. Loraine Jacobs DAQBI.
 CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica Estado
CINÉTICA QUÍMICA Profa. Loraine Jacobs DAQBI lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Estudo da velocidade das reações químicas. REAGENTES PRODUTOS Termodinâmica Estado
GOVERNO DO ESTADO DE MATO GROSSO DO SUL SECRETARIA DE ESTADO DE EDUCAÇÃO
 Conteúdo 14 Cinética Química CINÉTICA QUÍMICA É à parte da química que estuda a maior ou menor rapidez com que uma reação química ocorre e os fatores que a influenciam. Este estudo é importante para o
Conteúdo 14 Cinética Química CINÉTICA QUÍMICA É à parte da química que estuda a maior ou menor rapidez com que uma reação química ocorre e os fatores que a influenciam. Este estudo é importante para o
Enzimas e Actividade enzimática
 Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Cinética Química. c) A opção (C) está correta. B 3+ e B 4+ não aparecem na reação global, portanto, são intermediários da reação.
 Capítulo 6 Cinética Química 1. (ITA) Considere o seguinte mecanismo de reação genérica: A 4+ + B 2+ A 3+ + B 3+ (etapa lenta) A 4+ + B 3+ A 3+ + B 4+ (etapa rápida) C + + B 4+ C 3+ + B 2+ (etapa rápida)
Capítulo 6 Cinética Química 1. (ITA) Considere o seguinte mecanismo de reação genérica: A 4+ + B 2+ A 3+ + B 3+ (etapa lenta) A 4+ + B 3+ A 3+ + B 4+ (etapa rápida) C + + B 4+ C 3+ + B 2+ (etapa rápida)
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias.
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
META Estudar o comportamento de reações químicas que envolvem mais de uma etapa.
 EQUÇÕES CINÉTICS COMPOSTS Camilo ndrea ngelucci ula MET Estudar o comportamento de reações químicas que envolvem mais de uma etapa. OBJETIVOS o fi nal desta aula, o aluno deverá: compreender e determinar
EQUÇÕES CINÉTICS COMPOSTS Camilo ndrea ngelucci ula MET Estudar o comportamento de reações químicas que envolvem mais de uma etapa. OBJETIVOS o fi nal desta aula, o aluno deverá: compreender e determinar
Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13
 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Cinética. Módulo I - Físico Química Avançada. Profa. Kisla P. F. Siqueira
 Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
Cinética Módulo I - Físico Química vançada Profa. Introdução Estudo das velocidades das reações químicas; Velocidade em função das concentrações das espécies presentes; Leis de velocidade: equações diferenciais;
QUÍMICA 3 - APOSTILA 3. Prof. Msc João Neto
 QUÍMICA 3 - APOSTILA 3 Prof. Msc João Neto CINÉTICA QUÍMICA parte da Química que estuda a velocidade ou rapidez das reações. Prof. Msc João Neto Produtos (Formados) A + B AB Reagentes (Consumidos) Prof.
QUÍMICA 3 - APOSTILA 3 Prof. Msc João Neto CINÉTICA QUÍMICA parte da Química que estuda a velocidade ou rapidez das reações. Prof. Msc João Neto Produtos (Formados) A + B AB Reagentes (Consumidos) Prof.
Suponhamos que tenha sido realizado um. estudo que avalia dois novos veículos do mercado: o Copa e o Duna. As pesquisas levantaram os seguintes dados:
 A U A UL LA Acelera Brasil! Suponhamos que tenha sido realizado um estudo que avalia dois novos veículos do mercado: o Copa e o Duna. As pesquisas levantaram os seguintes dados: VEÍCULO Velocidade máxima
A U A UL LA Acelera Brasil! Suponhamos que tenha sido realizado um estudo que avalia dois novos veículos do mercado: o Copa e o Duna. As pesquisas levantaram os seguintes dados: VEÍCULO Velocidade máxima
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016
 CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
CINÉTICA QUÍMICA TUTOR: LUIZ EDUARDO NOCHI DISCIPLINA: QUÍMICA (FÍSICO QUÍMICA) CURSO ALCANCE (TURMA A E B ) DATA: 17/09/2016 O QUE É CINÉTICA QUÍMICA? É a área da química que estuda a velocidade das reações
[ A][ B] [ A] [ B] v {[A] }= Vmáx
![[ A][ B] [ A] [ B] v {[A] }= Vmáx [ A][ B] [ A] [ B] v {[A] }= Vmáx](/thumbs/75/72105322.jpg) Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Capítulo by Pearson Education
 QUÍMICA A Ciência Central 9ª Edição Cinética química David P. White Fatores que afetam a velocidade de reações A cinética é o estudo da velocidade na qual as reações químicas ocorrem. Existem quatro fatores
QUÍMICA A Ciência Central 9ª Edição Cinética química David P. White Fatores que afetam a velocidade de reações A cinética é o estudo da velocidade na qual as reações químicas ocorrem. Existem quatro fatores
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 581-
 Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
MARATONA PISM III 2016 PROFESSOR: ALEXANDRE FIDELIS BLACK LICENCIADO E BACHAREL EM QUÍMICA -UFJF
 MARATONA PISM III 2016 PROFESSOR: ALEXANDRE FIDELIS BLACK LICENCIADO E BACHAREL EM QUÍMICA -UFJF Parte da química que estuda a rapidez das reações Este estudo é importante para o nosso dia-a-dia, pois
MARATONA PISM III 2016 PROFESSOR: ALEXANDRE FIDELIS BLACK LICENCIADO E BACHAREL EM QUÍMICA -UFJF Parte da química que estuda a rapidez das reações Este estudo é importante para o nosso dia-a-dia, pois
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127. Cinética Química
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO UFRJ INSTITUTO DE QUÍMICA IQG127 Cinética Química Prof. Antonio Guerra Departamento de Química Geral e Inorgânica - DQI Cinética Química Definição e Objetivo Estudar
Fabio Rodrigo da Costa Dias. 2. Velocidade média e instantânea das Reações Químicas
 Cinética Química Fabio Rodrigo da Costa Dias 1. Introdução Cinética química é a área da química responsável pelo estudo das velocidades das reações químicas, bem como dos fatores que influenciam nessas
Cinética Química Fabio Rodrigo da Costa Dias 1. Introdução Cinética química é a área da química responsável pelo estudo das velocidades das reações químicas, bem como dos fatores que influenciam nessas
QUÍMICA GERAL EXPERIMENTAL 2º SEMESTRE DE 2016 EXPERIMENTO VIRTUAL DE CINÉTICA QUÍMICA
 QUÍMICA GERAL EXPERIMENTAL 2º SEMESTRE DE 2016 EXPERIMENTO VIRTUAL DE CINÉTICA QUÍMICA Acesse a página da Internet http://salvadorhurtado.wikispaces.com/file/view/cinequim.swf e siga as orientações para
QUÍMICA GERAL EXPERIMENTAL 2º SEMESTRE DE 2016 EXPERIMENTO VIRTUAL DE CINÉTICA QUÍMICA Acesse a página da Internet http://salvadorhurtado.wikispaces.com/file/view/cinequim.swf e siga as orientações para
Cinética Química. Mestrado integrado em Engenharia Biológica. Disciplina Química II, 2º semestre 2009/10. Professsora Ana Margarida Martins
 Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
Cinética Química Mestrado integrado em Engenharia Biológica Disciplina Química II, 2º semestre 2009/10 Professsora Ana Margarida Martins Usamos atermodinâmica para saber se uma reacção é favorecida no
FUP - Faculdade UnB Planaltina Disciplina: Energia e Dinâmica das Transformações Químicas Professor: Alex Fabiano C. Campos
 FUP - Faculdade UnB Planaltina Disciplina: Energia e Dinâmica das Transformações Químicas Professor: Alex Fabiano C. Campos 1. Conceitue colisão efetiva, colisão não-efetiva, energia de ativação e complexo
FUP - Faculdade UnB Planaltina Disciplina: Energia e Dinâmica das Transformações Químicas Professor: Alex Fabiano C. Campos 1. Conceitue colisão efetiva, colisão não-efetiva, energia de ativação e complexo
PROVA PARA INGRESSO NO MESTRADO. Programa de Pós Graduação em Química 09/12/2016 NOME
 PROVA PARA INGRESSO NO MESTRADO Programa de Pós Graduação em Química 09/12/2016 NOME Instruções para a prova: Coloque seu nome nesta folha antes de continuar; Marcar com um X, no quadro abaixo, as questões
PROVA PARA INGRESSO NO MESTRADO Programa de Pós Graduação em Química 09/12/2016 NOME Instruções para a prova: Coloque seu nome nesta folha antes de continuar; Marcar com um X, no quadro abaixo, as questões
Velocidade inicial (mol L -1 s -1 ) 1 0,0250 0,0250 6,80 x ,0250 0,0500 1,37 x ,0500 0,0500 2,72 x 10-4.
 P3 - PROVA DE QUÍMICA GERAL - 31/05/14 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Dados gerais: G = - n F E G = G o + RT Q ΔE RT ΔE nf Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0
P3 - PROVA DE QUÍMICA GERAL - 31/05/14 Nome: Nº de Matrícula: GABARITO Turma: Assinatura: Dados gerais: G = - n F E G = G o + RT Q ΔE RT ΔE nf Questão Valor Grau Revisão 1 a,5 a,5 3 a,5 4 a,5 Total 10,0
Cinética Química. Cinética Química: Velocidade média, instantânea e inicial. Lei cinética. Fatores que influenciam a velocidade.
 Cinética Química IV Cinética Química: Velocidade média, instantânea e inicial. Lei cinética. Fatores que influenciam a velocidade. Mecanismos reacionais. Catálise. Cinética Química Cinética Química é a
Cinética Química IV Cinética Química: Velocidade média, instantânea e inicial. Lei cinética. Fatores que influenciam a velocidade. Mecanismos reacionais. Catálise. Cinética Química Cinética Química é a
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS
 BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
BIOENGENHARIA I PROF. MARCELO HENRIQUE ENGENHARIA DE ALIMENTOS Introdução à Cinética das reações químicas O termo cinética está relacionado a movimento quando se pensa nele a partir de seu conceito físico.
Polimerização Passo-a-Passo ou por Condensação
 Reacção entre grupos funcionais; duas moléculas com grupos funcionais que reagem entre si, formando como produto uma molécula mais longa. 05-11-2006 Maria da Conceição Paiva 1 05-11-2006 Maria da Conceição
Reacção entre grupos funcionais; duas moléculas com grupos funcionais que reagem entre si, formando como produto uma molécula mais longa. 05-11-2006 Maria da Conceição Paiva 1 05-11-2006 Maria da Conceição
Modelos de Regressão Linear Simples parte I
 Modelos de Regressão Linear Simples parte I Erica Castilho Rodrigues 27 de Setembro de 2017 1 2 Objetivos Ao final deste capítulo você deve ser capaz de: Usar modelos de regressão para construir modelos
Modelos de Regressão Linear Simples parte I Erica Castilho Rodrigues 27 de Setembro de 2017 1 2 Objetivos Ao final deste capítulo você deve ser capaz de: Usar modelos de regressão para construir modelos
Cinética Química 17/04/17. V m h. Prof. Xuxu. Velocidade das reações químicas. Velocidade das reações químicas. Velocidade Média. Hora da saída: 11:45
 Seja Bem-indo a Goiânia elocidade Média Cinética Química Hora da saída: 11:45 Δd 40km m 40 km Δt 1h h Distância Hidrolândia: 40 km Seja Bem-indo a Hidrolândia Prof. Xuxu Hora da chegada: 12:45 elocidade
Seja Bem-indo a Goiânia elocidade Média Cinética Química Hora da saída: 11:45 Δd 40km m 40 km Δt 1h h Distância Hidrolândia: 40 km Seja Bem-indo a Hidrolândia Prof. Xuxu Hora da chegada: 12:45 elocidade
Biomatemática - Prof. Marcos Vinícius Carneiro Vital (ICBS UFAL) - Material disponível no endereço
 Universidade Federal de Alagoas Instituto de Ciências e Biológicas e da Saúde BIOB-3 Biomatemática Prof. Marcos Vinícius Carneiro Vital 1. Uma função linear especial. 1.1. Absorção de potássio. - Para
Universidade Federal de Alagoas Instituto de Ciências e Biológicas e da Saúde BIOB-3 Biomatemática Prof. Marcos Vinícius Carneiro Vital 1. Uma função linear especial. 1.1. Absorção de potássio. - Para
Gabarito. b) Quantos mols de sítios ativos existem em 1 mg de enzima? Assuma que cada subunidade possui um sítio ativo.
 Gabarito 4. A hidrólise de pirofosfato a ortofosfato é uma reação acoplada importante para deslocar o equilíbrio de reações biossintéticas, por exemplo a síntese de DNA. Esta reação de hidrólise é catalisada
Gabarito 4. A hidrólise de pirofosfato a ortofosfato é uma reação acoplada importante para deslocar o equilíbrio de reações biossintéticas, por exemplo a síntese de DNA. Esta reação de hidrólise é catalisada
A B A B. Espontaneidade vs. Velocidade de Reações. Enzimas como Catalisadores. Velocidade das reações depende da Energia de Ativação
 Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
Enzimas como atalisadores A B Espontaneidade vs. Velocidade de Reações A B Reações espontâneas liberam energia - exergônicas Diamante Grafite Glicose + 0 2 2 Reações exergônicas precisam ultrapassar barreira
Cinética Parte A. Introdução à Química II. Prof. Edson Nossol
 Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
Cinética Parte A Introdução à Química II Prof. Edson Nossol Uberlândia, 03/11/2017 Cinética química Estuda as velocidades das reações e os fatores que a influencia tempo Termodinâmica x cinética G = H
Modelos de Regressão Linear Simples - parte I
 Modelos de Regressão Linear Simples - parte I Erica Castilho Rodrigues 19 de Agosto de 2014 Introdução 3 Objetivos Ao final deste capítulo você deve ser capaz de: Usar modelos de regressão para construir
Modelos de Regressão Linear Simples - parte I Erica Castilho Rodrigues 19 de Agosto de 2014 Introdução 3 Objetivos Ao final deste capítulo você deve ser capaz de: Usar modelos de regressão para construir
Equilíbrio Químico (2)
 Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Química Geral e Experimental II Equilíbrio químico Resolução comentada de exercícios selecionados versão equilíbrio_v1_2005 Prof. Fabricio R.
 Química Geral e Experimental II Equilíbrio químico comentada de exercícios selecionados versão equilíbrio_v1_2005 Prof. Fabricio R. Sensato 1) A constante de equilíbrio K c da reação: H 2 (g) + Cl 2 (g)
Química Geral e Experimental II Equilíbrio químico comentada de exercícios selecionados versão equilíbrio_v1_2005 Prof. Fabricio R. Sensato 1) A constante de equilíbrio K c da reação: H 2 (g) + Cl 2 (g)
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC
 IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
IMPLEMENTAÇÃO EM LINGUAGUEM PYTHON DE MÉTODOS DE ESTIMAÇÃO E COMPAPARAÇÃO DE PARÂMETROS CINÉTICOS APLICADO A HIDRÓLISE CATALISADA POR ALDC A. S. PEREIRA 1, J. B. M. NETO 1, C. M. G. FARIAS 1 e L. R. B.
Pi Principais i i Tópicos Abordados dd
 BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
BC0307 Transfo ormaçõe es Químicas Pi Principais i i Tópicos Abordados dd Combustíveis: Termodinâmica vs. Cinética; Por que uma reação ocorre e quanto rápida ela é; Leis de velocidade, ordem de reação
OBJETIVOS BIBLIOGRAFIA ENZIMAS E INIBIDORES ENZIMÁTICOS
 OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
OBJETIVOS Enzimas: Funções, Nomenclatura e Propriedades Fundamentos da Cinética Enzimática Cinética Enzimática: Michaelis-Menten Ensaios Cinéticos: Padronização e Validação Parâmetros Cinéticos: vo, KM,
Com base nos dados acima, responda as questões propostas (cuidado com as unidades):
 Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Curso: Farmácia Atenção, dois dos exercícios da lista entrarão na P1. Concentrações: 01. Em uma rápida pesquisa pela internet é possível achar diversas receitas relacionadas à preparação de alguns cosméticos
Quí. Monitor: Marcos Melo
 Professor: Xandão Monitor: Marcos Melo Específicas: Cinética Química 27 nov EXERCÍCIOS DE AULA 1. A água oxigenada H 2O 2 (aq) se decompõe, produzindo água e gás oxigênio, de acordo com a equação: H 2O
Professor: Xandão Monitor: Marcos Melo Específicas: Cinética Química 27 nov EXERCÍCIOS DE AULA 1. A água oxigenada H 2O 2 (aq) se decompõe, produzindo água e gás oxigênio, de acordo com a equação: H 2O
cas AULA 5 es Quími rmaçõ o sfo Tr C0307
 BC0307 Transfo ormaçõe es Químicas AULA 5 - Combustíveis (Termodinâmica x Cinética); - Por que uma reação ocorre? - Qual a velocidade d da reação? - Cinética: leis de velocidade, ordem de reação e sua
BC0307 Transfo ormaçõe es Químicas AULA 5 - Combustíveis (Termodinâmica x Cinética); - Por que uma reação ocorre? - Qual a velocidade d da reação? - Cinética: leis de velocidade, ordem de reação e sua
QUÍMICA Cinética Química Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador - Parte 1 Prof ª.
 QUÍMICA Cinética Química Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador - Parte 1 Prof ª. Giselle Blois Concentração, Pressão, Temperatura e Catalisador As
QUÍMICA Cinética Química Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador - Parte 1 Prof ª. Giselle Blois Concentração, Pressão, Temperatura e Catalisador As
1 Calcule a velocidade média de desaparecimento de A (bolinhas vermelhas) durante o intervalo de tempo de 20 a 40 s. Reação: A B
 Físico-Química Prof. José Ginaldo Silva Jr. Lista de Exercícios de Cinética Química 1 Calcule a velocidade média de desaparecimento de A (bolinhas vermelhas) durante o intervalo de tempo de 20 a 40 s.
Físico-Química Prof. José Ginaldo Silva Jr. Lista de Exercícios de Cinética Química 1 Calcule a velocidade média de desaparecimento de A (bolinhas vermelhas) durante o intervalo de tempo de 20 a 40 s.
EXPERIÊNCIA 8 CINÉTICA E VELOCIDADES DAS REAÇÕES QUÍMICAS
 1. OBJETIVOS EXPERIÊNCIA 8 CINÉTICA E VELOCIDADES DAS REAÇÕES QUÍMICAS No final desta experiência, esperase que o aluno seja capaz de determinar a variação da velocidade de uma reação em função da variação
1. OBJETIVOS EXPERIÊNCIA 8 CINÉTICA E VELOCIDADES DAS REAÇÕES QUÍMICAS No final desta experiência, esperase que o aluno seja capaz de determinar a variação da velocidade de uma reação em função da variação
Aula 14 Cinética Química
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 14 Cinética Química Dr. Tiago P. Camargo Velocidades de reação... 85 % das espécies dependem da luz solar Apenas
Universidade Tecnológica Federal do Paraná Departamento Acadêmico de Química e Biologia Aula 14 Cinética Química Dr. Tiago P. Camargo Velocidades de reação... 85 % das espécies dependem da luz solar Apenas
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
4. Resultados e Discussão
 Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
Absorbância 4. Resultados e Discussão 4.1. Obtenção da curva de calibração A obtenção da curva de calibração, absorbância vs. concentração de Paraquat, é necessária para a análise química do pesticida.
EQUILÍBRIO QUÍMICO 1. Giseli Menegat e Maira Gazzi Manfro
 E daí mocinha, qual conteúdo vem agora? EQUILÍBRIO QUÍMICO! EQUILÍBRIO QUÍMICO 1 Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br ALGUNS CONCEITOS IMPORTANTES
E daí mocinha, qual conteúdo vem agora? EQUILÍBRIO QUÍMICO! EQUILÍBRIO QUÍMICO 1 Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br ALGUNS CONCEITOS IMPORTANTES
P4 - PROVA DE QUÍMICA GERAL 30/06/12
 P4 - POVA DE QUÍMICA GEAL 30/06/ Nome: Nº de Matrícula: GABAITO Turma: Assinatura: Questão Valor Grau evisão a,5 a,5 3 a,5 4 a,5 Total 0,0 Constantes e equações: 73,5 K = 0 C = 0,08 atm L mol - K - = 8,345
P4 - POVA DE QUÍMICA GEAL 30/06/ Nome: Nº de Matrícula: GABAITO Turma: Assinatura: Questão Valor Grau evisão a,5 a,5 3 a,5 4 a,5 Total 0,0 Constantes e equações: 73,5 K = 0 C = 0,08 atm L mol - K - = 8,345
PQI-2321 Tópicos de Química para Engenharia Ambiental I
 PQI-2321 Tópicos de Química para Engenharia Ambiental I Aula 20 Prof. Moisés Teles moises.teles@usp.br Departamento de Engenharia Química da Escola Politécnica da UP Motivação: Microorganismos e Engenharia
PQI-2321 Tópicos de Química para Engenharia Ambiental I Aula 20 Prof. Moisés Teles moises.teles@usp.br Departamento de Engenharia Química da Escola Politécnica da UP Motivação: Microorganismos e Engenharia
é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições
 Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Cinética Química Cinética química é o estudo da velocidade das reações, de como a velocidade varia em função das diferentes condições Fatores que afetam a velocidade da reação: Concentração dos reagentes.
Experiência 9 Transferência de Calor
 Roteiro de Física Experimental II 39 Experiência 9 Transferência de Calor OBJETIVO O objetivo desta aula é estudar os processos de transferência de calor entre dois corpos, na situação em que nenhum deles
Roteiro de Física Experimental II 39 Experiência 9 Transferência de Calor OBJETIVO O objetivo desta aula é estudar os processos de transferência de calor entre dois corpos, na situação em que nenhum deles
